ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] В данной заявке заявляется приоритет по предварительной заявке на патент США № 61/948421, поданной 5 марта 2014 г., и предварительной заявке на патент США № 62/114313, поданной 10 февраля 2015 г., которые включены в данный документ в полном объеме для любых целей посредством ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение относится к композициям на основе сиалированных гликопротеинов и способам их применения при лечении различных патологических состояний и расстройств.
ОПИСАНИЕ ТЕКСТОВОГО ФАЙЛА, ПОДАННОГО В ЭЛЕКТРОННОМ ВИДЕ
[0003] Содержание текстового файла, поданного в электронном виде, включено в данный документ в полном объеме посредством ссылки: Копия Перечня последовательностей в формате, пригодном для чтения на компьютере (имя файла: ULPI_020_02WO_SeqList_ST25.txt, дата создания: 2 марта 2015 г., размер файла: 9 килобайт).
УРОВЕНЬ ТЕХНИКИ
[0004] В последние годы значительно возросло количество имеющихся в продаже терапевтических белков, и большинство этих белков являются гликопротеинами. Присутствие сиаловой кислоты в гликопротеине может благоприятно влиять на абсорбцию, время полужизни в сыворотке и клиренс из сыворотки, а также физические, химические и иммуногенные свойства соответствующего гликопротеина. Следовательно, в определенных случаях может быть желательно увеличить содержание сиаловой кислоты в гликопротеине, предназначенном для фармакологического применения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] Настоящее изобретение частично основано на том открытии, что для рекомбинантного гликопротеина, полученного из клеток млекопитающих с использованием бессывороточной/безбелковой среды, улучшено сиалирование рекомбинантного гликопротеина, например, без уменьшения содержания М6Ф в рекомбинантном гликопротеине.
[0006] В некоторых вариантах реализации настоящего изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,05 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,1 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,5 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,7 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 1 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 1,5 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 2 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 5 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 10 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин с содержанием сиаловой кислоты более 20 моль/моль рекомбинантного гликопротеина.
[0007] В некоторых вариантах реализации настоящего изобретения предложена композиция, содержащая рекомбинантный гликопротеин, причем по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% остатков галактозы рекомбинантного гликопротеина сиалированы.
[0008] В некоторых вариантах реализации настоящего изобретения предложена композиция, содержащая рекомбинантный гликопротеин, причем рекомбинантный гликопротеин представляет собой β-глюкуронидазу человека и имеет степень сиалирования, которая составляет по меньшей мере 0,7 моль/моль рекомбинантного гликопротеина.
[0009] В некоторых других вариантах реализации настоящего изобретения предложена композиция, содержащая рекомбинантный гликопротеин, причем рекомбинантный гликопротеин представляет собой β-глюкуронидазу человека и имеет степень сиалирования, которая составляет по меньшей мере 0,7 моль/моль рекомбинантного гликопротеина, и высокий уровень маннозо-6-фосфатных (М6Ф) фрагментов.
[0010] В одном варианте реализации настоящего изобретения предложена композиция, содержащая рекомбинантный гликопротеин, причем рекомбинантный гликопротеин представляет собой β-глюкуронидазу человека и имеет степень сиалирования, которая составляет по меньшей мере 0,7 моль/моль рекомбинантного гликопротеина, и высокий уровень маннозо-6-фосфатных (М6Ф) фрагментов, который составляет по меньшей мере 10 мол. % от общего количества гликана рекомбинантного гликопротеина.
[0011] В другом варианте реализации настоящего изобретения предложена композиция, содержащая рекомбинантный гликопротеин, причем рекомбинантный гликопротеин представляет собой β-глюкуронидазу человека и имеет степень сиалирования, которая составляет по меньшей мере 0,7 моль/моль рекомбинантного гликопротеина, и высокий уровень маннозо-6-фосфатных (М6Ф) фрагментов, например, K поглощения находится на уровне 60%, 70%, 80%, 90% или максимальном, как, например, от примерно 1 нМ до примерно 3 нМ, при определении с использованием фибробластных клеток человека (МПС 7).
[0012] Еще в одном варианте реализации изобретения предложена композиция, содержащая рекомбинантный гликопротеин, причем рекомбинантный гликопротеин представляет собой β-глюкуронидазу человека и имеет степень сиалирования, которая составляет по меньшей мере 0,7 моль/моль рекомбинантного гликопротеина, и высокий уровень маннозо-6-фосфатных (М6Ф) фрагментов, например, полумаксимальное поглощение фибробластными клетками человека, как, например, концентрации, при которых поглощение гликопротеина (например, β-глюкуронидазы человека) достигает 50% от максимального значения, составляет не более чем примерно 1 нМ, 2 нМ, 3 нМ, 4 нМ или 5 нМ.
[0013] В некоторых вариантах реализации настоящего изобретения предложен препарат совокупности рекомбинантных гликопротеинов, причем по меньшей мере 50 процентов совокупности сиалировано. В некоторых вариантах реализации настоящего изобретения предложен препарат совокупности рекомбинантных гликопротеинов, причем по меньшей мере 60 процентов совокупности сиалировано. В некоторых вариантах реализации настоящего изобретения предложен препарат совокупности рекомбинантных гликопротеинов, причем по меньшей мере 70 процентов совокупности сиалировано. В некоторых вариантах реализации настоящего изобретения предложен препарат совокупности рекомбинантных гликопротеинов, причем по меньшей мере 80 процентов совокупности сиалировано. В некоторых вариантах реализации настоящего изобретения предложен препарат совокупности рекомбинантных гликопротеинов, причем по меньшей мере 90 процентов совокупности сиалировано.
[0014] Также предложен способ получения композиции/препарата согласно настоящему изобретению. В некоторых вариантах реализации изобретения способ включает экспрессию рекомбинантного гликопротеина в культуре клеток в бессывороточной или безбелковой среде. В некоторых вариантах реализации изобретения для выращивания клеток можно использовать безбелковую среду с химически определенным составом. В некоторых вариантах реализации изобретения среда не содержит эффективное количество сахара, выбранного из галактозы, фруктозы, N-ацетилманнозамина, маннозы и их комбинаций. Например, эффективное количество сахара составляет более чем 0,01 мМ, 0,05 мМ или 0,1 мМ.
[0015] В некоторых вариантах реализации изобретения культура клеток содержит клетки млекопитающих. Типовые клетки млекопитающих включают, но не ограничиваются ими, клетки яичников китайского хомячка (CHO), HeLa, VERO, BHK, Cos, MDCK, 293, 3T3, клетки миеломы (например, NSO, NSI) или WI38. В конкретном варианте реализации изобретения клетки млекопитающих представляют собой клетки яичников китайского хомячка (CHO).
[0016] В некоторых других вариантах реализации изобретения культура клеток содержит клетки растений. Типовые клетки растений включают, но не ограничиваются ими, клетки моркови или культуру на основании клеток любого другого растения, например, разработанную для получения рекомбинантного белка.
[0017] Дополнительно предложен способ лечения лизосомной болезни накопления (ЛБН), включающий введение индивиду, нуждающемуся в таком лечении, терапевтически эффективного количества композиции/препарата, как описано в данном документе. В типовом варианте реализации изобретения композиция/препарат содержит рекомбинантную β-глюкуронидазу человека. В дополнительном типовом варианте реализации изобретения ЛБН представляет собой мукополисахаридоз 7 типа (т.е. МПС 7, МПС VII или синдром Слая). В некоторых вариантах реализации изобретения рекомбинантные β-глюкуронидазы человека, предложенные в данном документе, имеют повышенное содержание сиаловой кислоты и являются особенно эффективными при лечении ЛБН, например МПС 7.
[0018] В некоторых вариантах реализации настоящего изобретения предложен способ лечения лизосомной болезни накопления (ЛБН) у субъекта, включающий введение композиции/препарата в соответствии со схемой лечения, как описано в данном документе, причем такое введение приводит к статистически значимому терапевтическому эффекту при лечении ЛБН. В типовом варианте реализации изобретения композиция/препарат содержит рекомбинантную β-глюкуронидазу человека. В дополнительном типовом варианте реализации изобретения ЛБН представляет собой МПС 7.
ОПРЕДЕЛЕНИЯ
[0019] При использовании в данном документе термин «эффективный» (например, «эффективное количество») означает достаточный для получения желаемого, ожидаемого или предполагаемого результата. Эффективное количество может представлять собой терапевтически эффективное количество. «Терапевтически эффективное количество» относится к такому количеству активного ингредиента, которое, при введении субъекту, является достаточным для осуществления лечения конкретного заболевания или патологического состояния. «Терапевтически эффективное количество» будет зависеть, например, от заболевания или патологического состояния, тяжести заболевания или патологического состояния и возраста, массы и т.д. субъекта, подвергаемого лечению.
[0020] Как правило, в некоторых вариантах реализации изобретения «лечение» любого патологического состояния, заболевания или расстройства относится к ослаблению патологического состояния, заболевания или расстройства (т.е. прекращению или ослаблению развития заболевания или по меньшей мере одного из его клинических симптомов). В некоторых вариантах реализации изобретения «лечение» относится к улучшению по меньшей мере одного физического параметра, которое может быть незаметно для субъекта. В некоторых вариантах реализации изобретения «лечение» относится к ингибированию патологического состояния, заболевания или расстройства либо физически (например, стабилизация явного симптома), либо физиологически (например, стабилизация физического параметра), либо одновременно физически и физиологически. В некоторых вариантах реализации изобретения «лечение» относится к задержке появления патологического состояния, заболевания или расстройства.
[0021] В соответствии с устоявшимся правилом в патентном законе единственное число относится к «одному или более» при использовании в данной заявке, в том числе в формуле изобретения. Термин «или» в формуле изобретения используется для обозначения «и/или», если явно не указано, что он относится только к альтернативным вариантам, или альтернативные варианты взаимно исключают друг друга. В частности, предполагается, что любое перечисление элементов с использованием термина «или» означает, что любой из этих перечисленных элементов также можно исключить из соответствующего варианта реализации изобретения.
[0022] Повсюду в данной заявке термин «примерно» используется для указания того, что значение включает стандартное отклонение ошибки устройства или способа, применяемого для установления значения.
[0023] Гликопротеин, при использовании в данном документе, представляет собой белок, который модифицирован присоединением одного или более углеводов, в особенности присоединением одного или более остатков сахаров.
[0024] При использовании в данном документе «GUS» относится к β-глюкуронидазе, типовому гликопротеину в соответствии с настоящим изобретением.
[0025] Сиалирование, при использовании в данном документе, представляет собой присоединение остатка сиаловой кислоты к белку, который может являться гликопротеином. Термин «сиаловая кислота», при использовании в данном документе, охватывает группу сахаров, содержащих 9 или более атомов углерода, включая карбоксильную группу. Общая структура, охватывающая все известные природные формы сиаловой кислоты, представлена ниже.

[0026] Группы R1 в различных положениях одной молекулы могут быть одинаковыми или различными. R1 может представлять собой водород или ацетил, лактил, метил, сульфат, фосфат, ангидро, сиаловую кислоту, фукозную, глюкозную или галактозную группу. R2 может представлять собой N-ацетильную, N-гликолильную, амино, гидроксильную, N-гликолил-O-ацетильную или N-гликолил-O-метильную группу. R3 представляет предшествующий остаток сахара в олигосахариде, к которому присоединена сиаловая кислота в гликопротеине. R3 может представлять собой галактозу (присоединенную по положению 3, 4 или 5), N-ацетилгалактозу (присоединенную по положению 6), N-ацетилглюкозу (присоединенную по положению 4 или 6), сиаловую кислоту (присоединенную по положению 8 или 9) или 5-N-гликолилнейраминовую кислоту. Essentials of Glycobiology, Ch. 15, Varki et al., eds., Cold Spring Harbor Laboratory Press, New York (1999). В природе обнаружено более 40 форм сиаловой кислоты. Essentials of Glycobiology, Ch. 15, Varki et al., eds., Cold Spring Harbor Laboratory Press, New York (1999). Распространенной формой сиаловой кислоты является N-ацетилнейраминовая кислота (НАНК), в которой R1 представляет собой водород во всех положениях, а R2 представляет собой N-ацетильную группу.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0027] Фиг. 1 представляет собой график, на котором сравнивается фармакокинетика рекомбинантных β-глюкуронидаз человека, GUS CR01 и GUS партии 43/44 у крыс после двухстадийной инфузии. Данные показывают, что инфузия CR01 с большей степенью сиалирования приводит к менее быстрому клиренсу и более высокой средней концентрации в течение инфузии, что увеличивает общее воздействие фермента, возможно, усиливая проникновение в ткани, которые сложнее лечить.
[0028] Фиг. 2 представляет собой график, показывающий только фазу постинфузионного клиренса GUS CR01 в сравнении с GUS партии 43/44, которую использовали для расчета значений t1/2. Этих различий в скорости клиренса достаточно, чтобы обеспечить более высокие уровни ферментов в сыворотке, что показано на фиг. 1.
[0029] Фиг. 3 представляет собой серию графиков, показывающих уровни GUS в тканях, для исследования фармакокинетики GUS CR01 в сравнении с GUS партии 43/44. Показано, что увеличивается доставка и поглощение тканью β-глюкуронидаз человека, так как для всех тканей общее поглощение сиалированных β-глюкуронидаз человека (CR01) выше, чем фермента с более низкой степенью сиалирования (43-44). После вычитания эндогенной активности глюкуронидазы эффективная доставка терапевтических β-глюкуронидаз человека увеличивается от 2 до практически 10 раз - необыкновенный и неожиданный результат.
[0030] Фиг. 4 представляет собой график, показывающий результаты измерения уровней гликозаминогликана (ГАГ) в моче в течение 36 недель у трех субъектов, которых лечили рекомбинантной β-глюкуронидазой человека (rhGUS). У субъектов, которых лечили rhGUS, наблюдалось быстрое и непрерывное зависимое от дозы снижение уровней ГАГ в моче.
[0031] Фиг. 5 иллюстрирует среднее снижение уровней гликозаминогликана (ГАГ) в моче в конце каждого интервала введения лекарственного средства в течение 36-недельного исследования с участием трех субъектов, которых лечили rhGUS. Доза 4 мг/кг QOW приводила к наибольшему снижению уровней ГАГ в моче.
[0032] Фиг. 6 представляет собой график, показывающий результаты измерения уровней гликозаминогликана (ГАГ) в сыворотке в течение 36 недель у трех субъектов, которых лечили rhGUS. Каждый субъект продемонстрировал снижение уровней ГАГ в сыворотке по меньшей мере на 25% в конце 36-недельного курса лечения.
[0033] Фиг. 7 представляет собой график, показывающий результаты измерения размера печени субъектов, которых лечили rhGUS. После 36-недельного курса лечения наблюдалось значительно меньшее увеличение печени.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0034] Настоящее изобретение частично основано на том открытии, что для рекомбинантного гликопротеина, полученного из клеток млекопитающих с использованием бессывороточной/безбелковой среды, улучшено сиалирование рекомбинантного гликопротеина и дополнительно повышены уровни маннозо-6-фосфатных фрагментов в рекомбинантном гликопротеине.
Композиции на основе сиалированных гликопротеинов
[0035] Композиции, описанные в данном документе, содержат один или более гликопротеинов, которые имеют высокое или повышенное содержание сиаловой кислоты.
[0036] Сиаловые кислоты представляют ряд аминосахаров с 9 атомами углерода, включающий более 50 членов, полученных из N-ацетилнейраминовой кислоты. Хотя сиаловая кислота является только одним компонентом из нескольких моносахаридов, строящих гликаны гликопротеинов, она оказывает сильное влияние на свойства и стабильность любых терапевтических гликопротеинов по нескольким причинам: (I) концевые остатки галактозы являются одним из важных факторов, определяющих время полужизни гликопротеинов в сыворотке крови. Время полужизни в сыворотке регулируется экспрессией азиалогликопротеиновых рецепторов печени. Эти рецепторы связывают несиалированные гликопротеины, а связанные азиалогликопротеины удаляются из сыворотки посредством эндоцитоза. Поэтому экспрессия концевой сиаловой кислоты на остатках галактозы предотвращает деградацию гликопротеинов в сыворотке; (II) сиаловые кислоты имеют важное значение для маскирования антигенных детерминант или эпитопов. Известно, что рецепторы иммунной системы (рецепторы T- и B-клеток) часто предпочитают несиалированные структуры. Следовательно, возможность возникновения антител против терапевтических гликопротеинов коррелирует со степенью их сиалирования; (III) отрицательно заряженные сиаловые кислоты влияют на характерные для белков параметры, такие как термическая стабильность, устойчивость к протеолитическому распаду или растворимость (Bork et al., Increasing the Sialylation of Therapeutic Glycoproteins: The potential of the Sialic Acid Biosynthetic Pathway, Journal of Pharmaceutical Sciences, Vol. 98, No. 10, October 2009).
[0037] В одном аспекте изобретения предложены композиции, содержащие рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,05 моль/моль, 0,1 моль/моль, 0,5 моль/моль, 0,7 моль/моль, 1 моль/моль, 1,5 моль/моль, 2 моль/моль, 5 моль/моль, 10 моль/моль или 20 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения предложены композиции, содержащие рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,5 моль/моль рекомбинантного гликопротеина. В дополнительных вариантах реализации изобретения предложены композиции, содержащие рекомбинантный гликопротеин с содержанием сиаловой кислоты более 0,7 моль/моль рекомбинантного гликопротеина. В некоторых дополнительных вариантах реализации изобретения предложены композиции, содержащие рекомбинантный гликопротеин с содержанием сиаловой кислоты более 1 моль/моль рекомбинантного гликопротеина.
[0038] В некоторых вариантах реализации изобретения рекомбинантный гликопротеин представляет собой рекомбинантную форму β-глюкуронидазы человека, фермента, отвечающего за катализ гидролиза с отщеплением остатков β-D-глюкуроновой кислоты с невосстанавливающего конца мукополисахаридов. В некоторых вариантах реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет более чем 0,1 моль/моль, 0,5 моль/моль, 0,7 моль/моль, 1 моль/моль, 1,5 моль/моль, 2 моль/моль или 5 моль/моль rhGUS. В одном типовом варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет более чем 0,7 моль/моль rhGUS. В другом типовом варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет более чем 1,0 моль/моль rhGUS. Еще в одном типовом варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет примерно 1,2 моль/моль rhGUS.
[0039] В некоторых вариантах реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет от примерно 0,5 моль/моль до примерно 2,0 моль/моль rhGUS. В одном варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет от примерно 0,6 моль/моль до примерно 1,5 моль/моль rhGUS. В другом варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет от примерно 0,7 моль/моль до примерно 1,4 моль/моль rhGUS. В типовом варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет от примерно 0,8 моль/моль до примерно 1,3 моль/моль rhGUS. В другом типовом варианте реализации изобретения содержание сиаловой кислоты в рекомбинантной β-глюкуронидазе человека (rhGUS) составляет от примерно 1,0 моль/моль до примерно 1,2 моль/моль rhGUS.
[0040] В некоторых вариантах реализации изобретения композиция по настоящему изобретению содержит рекомбинантный гликопротеин, в котором по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% участков, пригодных для связывания с сиаловой кислотой, сиалированы. Как правило, участком, пригодным для связывания с сиаловой кислотой или сиалирования, является галактоза. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин, причем по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% остатков галактозы рекомбинантного гликопротеина сиалированы. В некоторых вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин, причем по меньшей мере 50% остатков галактозы рекомбинантного гликопротеина сиалированы. В дополнительных вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин, причем по меньшей мере 60% остатков галактозы рекомбинантного гликопротеина сиалированы. В некоторых дополнительных вариантах реализации изобретения композиция содержит рекомбинантный гликопротеин, причем по меньшей мере 70% остатков галактозы рекомбинантного гликопротеина сиалированы.
[0041] В некоторых вариантах реализации изобретения рекомбинантный гликопротеин представляет собой рекомбинантную β-глюкуронидазу человека (rhGUS). В некоторых вариантах реализации изобретения по меньшей мере 40%, 50%, 60%, 70% или 80% остатков галактозы рекомбинантной β-глюкуронидазы человека (rhGUS) сиалированы. В одном типовом варианте реализации изобретения по меньшей мере 50% остатков галактозы rhGUS сиалированы. В другом типовом варианте реализации изобретения по меньшей мере 60% остатков галактозы rhGUS сиалированы. Еще в одном типовом варианте реализации изобретения по меньшей мере 70% остатков галактозы rhGUS сиалированы. Еще в одном типовом варианте реализации изобретения примерно 70%, 71%, 72%, 73%, 74% или примерно 75% остатков галактозы rhGUS сиалированы.
[0042] В некоторых вариантах реализации изобретения от по меньшей мере примерно 40% до по меньшей мере примерно 90% остатков галактозы рекомбинантной β-глюкуронидазы человека (rhGUS) сиалированы. В одном варианте реализации изобретения от по меньшей мере примерно 50% до по меньшей мере примерно 80% остатков галактозы рекомбинантной β-глюкуронидазы человека (rhGUS) сиалированы. В другом варианте реализации изобретения от по меньшей мере примерно 60% до по меньшей мере примерно 80% остатков галактозы рекомбинантной β-глюкуронидазы человека (rhGUS) сиалированы. В типовом варианте реализации изобретения от по меньшей мере примерно 65% до по меньшей мере примерно 75% остатков галактозы рекомбинантной β-глюкуронидазы человека (rhGUS) сиалированы.
[0043] В другом аспекте изобретения предложены композиции, содержащие рекомбинантный гликопротеин с высоким содержанием сиаловой кислоты, а также высоким уровнем маннозо-6-фосфатных (М6Ф) фрагментов. При использовании в данном документе, фрагменты М6Ф включают любой маннозо-6-фосфат, способный связываться с М6Ф-рецепторами или распознаваться ими, включая, без какого-либо ограничения, монофосфорилированный и бифосфорилированный маннозо-6-фосфат. В одном варианте реализации изобретения фрагменты М6Ф включают любой М6Ф, связывающийся с катион-независимым М6Ф-рецептором (CI-MPR). В другом варианте реализации изобретения фрагменты М6Ф включают любой М6Ф, связывающийся с катион-зависимым М6Ф-рецептором (CD-MRP). Еще в одном варианте реализации изобретения фрагменты М6Ф включают любой бифосфорилированный М6Ф.
[0044] Согласно настоящему изобретению высокий уровень маннозо-6-фосфатных фрагментов может включать любой уровень фрагментов М6Ф, который специалист в данной области техники считает высоким, например, измеренный с использованием любого подходящего способа, известного или позже разработанного специалистом в данной области техники. В одном варианте реализации изобретения высокий уровень фрагментов М6Ф рекомбинантного гликопротеина включает уровни фрагментов М6Ф, составляющие по меньшей мере 10 мол. %, 11 мол. %, 12 мол. %, 13 мол. %, 14 мол. % или 15 мол. % от общего количества гликана рекомбинантного гликопротеина. Например рекомбинантный гликопротеин может иметь высокий уровень М6Ф, что определено по процентному отношению площади пика М6Ф к общей площади пика гликана, например по меньшей мере 10%, 11%, 12%, 13%, 14% или 15%. В некоторых вариантах реализации изобретения рекомбинантный гликопротеин представляет собой рекомбинантную β-глюкуронидазу человека (rhGUS) и содержит фрагменты М6Ф на уровне, составляющем по меньшей мере 10 мол. %, 11 мол. %, 12 мол. %, 13 мол. %, 14 мол. % или 15 мол. % от общего количества гликана rhGUS. В типовом варианте реализации изобретения rhGUS содержит фрагменты М6Ф на уровне от примерно 13% до примерно 15%.
[0045] В другом варианте реализации изобретения высокий уровень фрагментов М6Ф рекомбинантного гликопротеина включает высокий уровень поглощения рекомбинантного гликопротеина клетками человека, например, высокое сродство к поглощению фибробластными клетками человека. Например, рекомбинантный гликопротеин может характеризоваться М6Ф-зависимой константой (К) поглощения, составляющей не более 1 нМ, 1,1 нМ, 1,2 нМ, 1,3 нМ, 1,4 нМ, 1,5 нМ, 1,6 нМ, 1,7 нМ, 1,8 нМ, 1,9 нМ, 2 нМ, 2,1 нМ, 2,2 нМ, 2,3 нМ, 2,4 нМ, 2,5 нМ, 2,6 нМ, 2,7 нМ, 2,8 нМ, 2,9 нМ, 3 нМ, 4 нМ или 5 нМ, любыми пригодными клетками человека, например фибробластными клетками человека. В некоторых вариантах реализации изобретения рекомбинантный гликопротеин представляет собой рекомбинантную β-глюкуронидазу человека (rhGUS) и характеризуется М6Ф-зависимой К поглощения, составляющей менее 5 нМ, менее 4 нМ, менее 3 нМ или менее 2 нМ. В типовом варианте реализации изобретения rhGUS характеризуется М6Ф-зависимой K поглощения, составляющей от примерно 1,2 нМ до примерно 1,8 нМ.
[0046] Еще в одном варианте реализации изобретения высокий уровень фрагментов М6Ф в рекомбинантном гликопротеине включает более низкие концентрации, необходимые для достижения максимального поглощения рекомбинантного гликопротеина клетками человека, например более низкие полумаксимальные концентрации. Например, для рекомбинантного гликопротеина может достигаться максимальное поглощение клетками человека, например фибробластными клетками, при концентрациях менее 10 нМ, 9 нМ, 8 нМ, 7 нМ, 6 нМ, 5 нМ, 4 нМ, 3 нМ, 2 нМ или 1 нМ. В некоторых вариантах реализации изобретения рекомбинантный гликопротеин представляет собой рекомбинантную β-глюкуронидазу человека (rhGUS), для которой максимальное поглощение клетками человека, например фибробластными клетками, может достигаться при концентрациях менее 5 нМ, менее 4 нМ, менее 3 нМ или менее 2 нМ. В типовом варианте реализации изобретения максимальное поглощение клетками человека, например фибробластными клетками, для rhGUS может достигаться при концентрациях от примерно 1,2 нМ до примерно 1,8 нМ.
[0047] Еще в одном варианте реализации изобретения высокий уровень фрагментов М6Ф в рекомбинантном гликопротеине включает один или более уровней фрагментов М6Ф, соответствующих уровням фрагментов М6Ф, связанным с природной степенью сиалирования рекомбинантного гликопротеина, например степенью сиалирования рекомбинантного гликопротеина до применения какого-либо способа повышения, такого как использование способов, описанных в настоящей заявке.
[0048] Согласно настоящему изобретению в некоторых вариантах реализации изобретения рекомбинантный гликопротеин, например рекомбинантная β-глюкуронидаза человека или любой другой лизосомальный фермент, имеет степень сиалирования по меньшей мере 1 моль/моль и высокий уровень фрагментов М6Ф, который составляет по меньшей мере 10 мол. %, 11 мол. %, 12 мол. %, 13 мол. %, 14 мол. % или 15 мол. % от общего количества гликана рекомбинантного гликопротеина. В одном варианте реализации изобретения рекомбинантный гликопротеин, например рекомбинантная β-глюкуронидаза человека или любой другой лизосомальный фермент, имеет степень сиалирования по меньшей мере 1 моль/моль и высокий уровень фрагментов М6Ф с поглощением клетками человека, например фибробластными клетками человека, составляющим по меньшей мере 1 нМ, 1,1 нМ, 1,2 нМ, 1,3 нМ, 1,4 нМ, 1,5 нМ, 1,6 нМ, 1,7 нМ, 1,8 нМ, 1,9 нМ или 2 нМ. В другом варианте реализации изобретения рекомбинантный гликопротеин, например рекомбинантная β-глюкуронидаза человека или любой другой лизосомальный фермент, имеет степень сиалирования по меньшей мере 1 моль/моль и высокий уровень фрагментов М6Ф с максимальным поглощением клетками человека, например фибробластными клетками человека, которое составляет менее 10 нМ, 9 нМ, 8 нМ, 7 нМ, 6 нМ, 5 нМ, 4 нМ, 3 нМ, 2 нМ или 1 нМ рекомбинантного гликопротеина.
[0049] Еще в одном аспекте изобретения предложена композиция, содержащая совокупность рекомбинантных гликопротеинов, причем по меньшей мере 50%, 60%, 70%, 80% или 90% совокупности сиалировано. В одном варианте реализации изобретения по меньшей мере 50%, 60%, 70%, 80% или 90% совокупности представляет собой рекомбинантный гликопротеин согласно настоящему изобретению, например, применительно к степени сиалирования и уровню М6Ф.
[0050] Рекомбинантным гликопротеином, предложенным в настоящем изобретении, может быть любой гликопротеин. Типовые рекомбинантные гликопротеины включают такие, которые содержат последовательность аминокислот, идентичную или в значительной степени подобную всему или части одного из следующих белков: лиганда Flt3 (как описано в WO 94/28391), лиганда CD40 (как описано в патенте США № 6087329), эритропоэтина, тромбопоэтина, кальцитонина, лептина, IL-2, ангиопоэтина-2 (как описано в Maisonpierre et al. (1997), Science 277(5322):55-60, включенной в данный документ посредством ссылки), лиганда Fas, лиганда для рецептора-активатора NF-каппа B (RANKL, как описано в WO 01/36637), лиганда, вызывающего апоптоз, из семейства факторов некроза опухолей (ФНО) (TRAIL, как описано в WO 97/01633), тимусного стромального лимфопоэтина, гранулоцитарного колониестимулирующего фактора, гранулоцитарно-моноцитарного колониестимулирующего фактора (ГМКСФ, как описано в патенте Австралии № 588819), фактора роста тучных клеток, фактора роста стволовых клеток (описанного, например, в патенте США № 6204363, включенном в данный документ посредством ссылки), эпидермального фактора роста, фактора роста кератиноцитов, фактора роста и развития мегакариоцитов, RANTES, гормона роста, инсулина, инсулинотропина, инсулиноподобных факторов роста, паратиреоидного гормона, интерферонов, включая α-интерфероны, γ-интерфероны или консенсус-интерфероны (такие как описанные в патентах США № 4695623 и 4897471, оба включены в данный документ посредством ссылки), фактора роста нервов, нейротрофического фактора головного мозга, синаптотагмин-подобных белков (SLP 1-5), нейротрофина-3, глюкагона, интерлейкинов 1-18, колониестимулирующих факторов, лимфотоксина-β, фактора некроза опухолей (ФНО), фактора ингибирования лейкемии, онкостатина-M и различных лигандов для молекул поверхности клеток ELK и Hek (таких как лиганды для eph-родственных киназ или LERKS). Описания белков, которые можно получить согласно способам данного изобретения, могут быть найдены, например, в Human Cytokines: Handbook for Basic and Clinical Research, Vol. II (Aggarwal and Gutterman, eds. Blackwell Sciences, Cambridge, Mass., 1998); Growth Factors: A Practical Approach (McKay and Leigh, eds., Oxford University Press Inc., New York, 1993); и The Cytokine Handbook (A. W. Thompson, ed., Academic Press, San Diego, Calif., 1991), которые включены в данный документ посредством ссылки.
[0051] Рекомбинантные гликопротеины по настоящему изобретению могут включать любой лизосомальный фермент, в особенности любой фермент, пригодный для заместительной ферментной терапии (ЗФТ). Примеры таких ферментов включают, без какого-либо ограничения, кислую альфа-глюкозидазу, кислую бета-глюкозидазу или глюкоцереброзидазу, альфа-галактозидазу A, кислую бета-галактозидазу, бета-гексозаминидазу A, бета-гексозаминидазу B, кислую сфингомиелиназу, галактоцереброзидазу, кислую церамидазу, арилсульфатазу, альфа-L-идуронидазу, идуронат-2-сульфатазу, гепаран-N-сульфатазу, альфа-N-ацетилглюкозаминидазу, ацетил-КоА, альфа-глюкозамидин-N-ацетилтрансферазу, N-ацетилглюкозамин-6-сульфатсульфатазу, N-ацетилгалактозамин-6-сульфатсульфатазу, кислую бета-галактозидазу, арилсульфатазу B, кислую альфа-маннозидазу, кислую бета-маннозидазу, кислую альфа-L-фукозидазу, сиалидазу и альфа-N-ацетилгалактозаминидазу.
[0052] В некоторых типовых вариантах реализации изобретения рекомбинантный гликопротеин по настоящему изобретению представляет собой рекомбинантную β-глюкуронидазу человека (rhGUS). β-глюкуронидаза человека представляет собой гликопротеин, который содержит до 16 олигосахаридов на молекулу, в том числе различные цепи, которые могут содержать большое количество маннозы, могут быть сложных и гибридных типов.
[0053] Также в данном документе описаны изолированные или очищенные полипептиды гликопротеинов. Например, в данном документе описаны изолированные или очищенные полипептиды rhGUS. Описанные изолированные или очищенные полипептиды rhGUS можно использовать в одной или более композициях или способах, представленных в данном документе.
[0054] Полипептиды rhGUS могут содержать пептидную последовательность rhGUS, а также ее фрагменты, ее природные варианты и ее неприродные варианты. Последовательность rhGUS представлена в SEQ ID №: 1. В данном документе описаны изолированные или очищенные полипептиды, которые состоят из SEQ ID №: 1. В данном документе также описаны изолированные или очищенные полипептиды, которые содержат SEQ ID №: 1, а также ее фрагменты. Фрагменты могут содержать по меньшей мере примерно 10, 20, 50, 100, 200, 300, 400, или 500, или более заменимых аминокислот. Также в данном документе описаны изолированные или очищенные полинуклеотиды, которые состоят из или содержат полинуклеотидную последовательность, которая способна кодировать аминокислотную последовательность SEQ ID №: 1.
[0055] В некоторых вариантах реализации изобретения содержание сиаловой кислоты в полипептиде rhGUS составляет более чем 0,1 моль/моль, 0,5 моль/моль, 0,7 моль/моль, 1 моль/моль, 1,5 моль/моль, 2 моль/моль или 5 моль/моль полипептида rhGUS. В некоторых вариантах реализации изобретения содержание сиаловой кислоты в полипептиде rhGUS составляет от примерно 0,5 моль/моль до примерно 2,0 моль/моль полипептида rhGUS. В одном варианте реализации изобретения содержание сиаловой кислоты в полипептиде rhGUS составляет от примерно 0,6 моль/моль до примерно 1,5 моль/моль полипептида rhGUS. В другом варианте реализации изобретения содержание сиаловой кислоты в полипептиде rhGUS составляет от примерно 0,7 моль/моль до примерно 1,4 моль/моль полипептида rhGUS. В типовом варианте реализации изобретения содержание сиаловой кислоты в полипептиде rhGUS составляет от примерно 0,8 моль/моль до примерно 1,3 моль/моль полипептида rhGUS. В другом типовом варианте реализации изобретения содержание сиаловой кислоты в rhGUS составляет от примерно 1,0 моль/моль до примерно 1,2 моль/моль полипептида rhGUS.
[0056] В дополнительных вариантах реализации изобретения по меньшей мере 40%, 50%, 60%, 70% или 80% остатков галактозы полипептида rhGUS сиалированы. В типовом варианте реализации изобретения от по меньшей мере примерно 65% до по меньшей мере примерно 75% остатков галактозы полипептида rhGUS сиалированы.
[0057] Как описано в данном документе, гликопротеины по данному изобретению могут быть получены рекомбинантно. Полинуклеотид, кодирующий рекомбинантный гликопротеин по данному изобретению, может быть включен в рекомбинантный экспрессионный вектор. В типовом варианте реализации изобретения рекомбинантный гликопротеин представляет собой rhGUS. Следовательно, заявка также относится к рекомбинантному экспрессионному вектору, содержащему полинуклеотид, кодирующий rhGUS. В одном варианте реализации изобретения белок rhGUS, полученный при помощи рекомбинантного экспрессионного вектора, состоит из или содержит SEQ ID №: 1.
[0058] Как известно в данной области техники, рекомбинантные векторы могут быть экспрессированы в пригодной клетке-хозяине с использованием способов, хорошо известных в данной области техники. Следовательно, заявка также относится к клетке-хозяину, содержащей полинуклеотид, кодирующий rhGUS. В одном варианте реализации изобретения белок rhGUS, полученный при помощи клетки-хозяина, состоит из или содержит SEQ ID №: 1. Пригодные клетки-хозяева для экспрессии белка rhGUS по настоящему изобретению могут включать любую клеточную линию, которая может гликозилировать белки, предпочтительно клеточную линию млекопитающих, которая создана методами генной инженерии для экспрессии белка. Например, можно использовать клетки яичников китайского хомячка (CHO), HeLa, VERO, BHK, Cos, MDCK, 293, 3T3, клетки миеломы (например, NSO, NSI) или WI38. В типовом варианте реализации изобретения клетки, используемые для получения рекомбинантного гликопротеина, представляют собой клетки яичников китайского хомячка (CHO).
[0059] Еще в одном аспекте изобретения предложен состав, содержащий один или более гликопротеинов, которые характеризуются высоким или повышенным содержанием сиаловой кислоты. Составы, как правило, включают жидкие формы (растворы), такие как, без ограничения, ресуспендированные лиофилизаты, и твердые формы, такие как, без ограничения, лиофилизованные формы, гели, микроинкапсулированные частицы и пасты. Составы в соответствии с некоторыми вариантами реализации настоящего изобретения могут представлять собой комбинации жидких составов, лиофилизатов и жидких растворов, полученных из ресуспендированных лиофилизатов, используемые совместно с гелем, частицами или пастами.
[0060] В некоторых вариантах реализации изобретения состав представляет собой раствор, содержащий водную буферную систему и рекомбинантный гликопротеин. Буферная система может содержать фосфат натрия (Na-Pi), гистидин, аргинин, глицилглицин, винную кислоту, яблочную кислоту, молочную кислоту, аспарагиновую кислоту, янтарную кислоту или их любую комбинацию. В типовом варианте реализации изобретения буферная система содержит Na-Pi и гистидин. В другом варианте реализации изобретения буферная система содержит Na-Pi, гистидин и аргинин.
[0061] В некоторых вариантах реализации изобретения буферная система дополнительно содержит один или более других ингредиентов, таких как, без ограничения, хлорид натрия (NaCl), полиоксиэтилен (твин 20), хлорид калия и сорбит (например, D-сорбит). В типовом варианте реализации изобретения буферная система содержит Na-Pi, гистидин, NaCl и твин 20.
[0062] В данной области техники хорошо известно, что стабильность белков может зависеть от pH и/или ионной силы состава. Согласно некоторым вариантам реализации настоящего изобретения pH состава составляет от примерно 9,0 до примерно 5,0, например от примерно 7,5 до примерно 6,0. В некоторых вариантах реализации изобретения pH составляет примерно 9,0, примерно 8,0, примерно 7,5, примерно 7,0, примерно 6,5, примерно 6,0, примерно 5,5 или примерно 5,0. В настоящем изобретении впервые обнаружено, что более низкое значение pH состава повышает стабильность рекомбинантного гликопротеина. Например, Таблица 6 в примере 2 демонстрирует повышение стабильности, которая определена по процентному содержанию тетрамеров, при изменении pH от 7,5 до 6,0.
Способы получения
[0063] Еще в одном аспекте настоящего изобретения предложен способ увеличения степени сиалирования гликопротеина и дополнительно уровня М6Ф гликопротеина, полученного с использованием культуры клеток в бессывороточной или безбелковой среде.
[0064] Как правило, питательные среды можно разделить на несколько подгрупп в зависимости от уровня определенности состава среды. Например, питательная среда может представлять собой: 1) среду, содержащую сыворотку (обычно 10-20% фетальной бычьей сыворотки (ФБС)); 2) среду со сниженным содержанием сыворотки (обычно 1-5% ФБС); 3) бессывороточную среду (синоним среды с определенным составом); 4) безбелковую среду (не содержит белки, но содержит неидентифицированные пептиды из растительных гидролизатов); 5) среду с химически определенным составом (содержит только рекомбинантные белки и/или гормоны); 6) безбелковую среду с химически определенным составом (содержит только низкомолекулярные составляющие, но может содержать синтетические пептиды/гормоны); и 7) безбелковую среду с химически определенным составом, не содержащую пептидов (содержит только низкомолекулярные составляющие).
[0065] В некоторых вариантах реализации настоящего изобретения можно использовать среду со сниженным содержанием сыворотки, чтобы вырастить клетки для экспрессии гликопротеинов. В некоторых вариантах реализации настоящего изобретения можно использовать бессывороточную среду, чтобы вырастить клетки для экспрессии гликопротеинов. В некоторых вариантах реализации изобретения можно использовать безбелковую среду, чтобы вырастить клетки для экспрессии гликопротеинов. В некоторых вариантах реализации изобретения можно использовать среду с химически определенным составом, чтобы вырастить клетки для экспрессии гликопротеинов. В некоторых вариантах реализации изобретения для выращивания клеток можно использовать безбелковую среду с химически определенным составом, как продемонстрировано в примере 1. Дополнительно в некоторых других вариантах реализации изобретения можно использовать безбелковую не содержащую пептидов среду с химически определенным составом, чтобы вырастить клетки для экспрессии гликопротеинов.
[0066] В данной области техники хорошо известно, что бессывороточная среда может содержать неидентифицированные продукты животного происхождения, такие как сывороточный альбумин (выделенный из крови), гидролизаты, факторы роста, гормоны, белки-носители и факторы прикрепления. Эти неидентифицированные продукты животного происхождения могут содержать сложные нежелательные примеси, такие как липиды, связанные с альбумином. В отличие от этого, в среде с химически определенным составом все компоненты идентифицированы, а их концентрации точно известны. В некоторых вариантах реализации изобретения среда с химически определенным составом полностью свободна от компонентов животного происхождения. В некоторых вариантах реализации изобретения среда с химически определенным составом не содержит ФБС, бычий сывороточный альбумин (БСА), человеческий сывороточный альбумин (ЧСА) или их комбинации. Для того, чтобы достичь этого, в среду с химически определенным составом обычно добавляют рекомбинантные варианты альбумина и факторов роста, обычно полученные из риса или E. coli, или синтетические химические вещества, такие как полимер поливиниловый спирт, который может воспроизводить некоторые функции БСА/ЧСА.
[0067] В некоторых вариантах реализации изобретения безбелковая среда, описанная в данном документе, не содержит какие-либо белки или компоненты биологического происхождения. Отсутствие белков в среде устраняет риск загрязнения переносимыми с кровью или другими патогенами или нечеловеческими белками. Кроме того, такие безбелковые среды обычно полностью определены в отношении наименования и количества всех ингредиентов, что может обеспечить отличную однородность продукта, превосходные характеристики контроля качества продукта и лучшую стабильность продукта, чем в средах, содержащих белки.
[0068] В некоторых вариантах реализации изобретения среда, используемая в данном документе, не содержит эффективное количество сахара, выбранного из галактозы, фруктозы, N-ацетилманнозамина, маннозы и их комбинаций. Например, эффективное количество сахара составляет более чем 0,01 мМ, 0,05 мМ или 0,1 мМ.
[0069] В некоторых вариантах реализации настоящего изобретения предложен способ культивирования клеток млекопитающих, включающий выращивание культуры клеток млекопитающего, чтобы получить белок, например гликопротеин, в бессывороточной или безбелковой среде. Пригодные клетки для практического осуществления настоящего изобретения включают любую клеточную линию, которая может гликозилировать белки, предпочтительно клеточную линию млекопитающих, которая создана методами генной инженерии для экспрессии белка. В некоторых вариантах реализации изобретения клетки представляют собой гомогенные клеточные линии. В данной области техники известно большое количество пригодных клеточных линий. Например, можно использовать клетки яичников китайского хомячка (CHO), HeLa, VERO, BHK, Cos, MDCK, 293, 3T3, клетки миеломы (например, NSO, NSI) или WI38. В типовом варианте реализации изобретения клетки, используемые для получения рекомбинантного гликопротеина, представляют собой клетки яичников китайского хомячка (CHO).
[0070] Согласно некоторым вариантам реализации настоящего изобретения особенно эффективными являются клетки CHO, которые широко используются для получения рекомбинантных белков, например цитокинов, факторов свертывания крови и антител (Brasel et al. (1996), Blood 88: 2004-2012; Kaufman et al. (1988), J. Biol Chem 263:6352-6362; McKinnon et al. (1991), J Mol Endocrinol 6: 231-239; Wood et al. (1990), J. Immunol 145: 3011-3016). Пригодной является мутантная клеточная линия, дефицитная по дигидрофолатредуктазе (ДГФР) (Urlaub et al. (1980), Proc. Natl. Acad. Sci. USA 77:4216-4220), такая как DXB11 или DG-44, потому что эффективная система экспрессии селектируемых и амплифицированных генов ДГФР позволяет получить высокие уровни экспрессии рекомбинантного белка в этих клетках (Kaufman (1990), Meth. Enzymol. 185: 527-566). Кроме того, эти клетки просты в обращении в виде адгезивных или суспензионных культур и демонстрируют относительно хорошую генетическую стабильность. Клетки CHO и рекомбинантные белки, которые в них экспрессируются, широко изучены и утверждены регуляторными органами для применения при производстве лекарственных препаратов.
[0071] В некоторых вариантах реализации изобретения клетки выращивают при помощи метода периодических культур с подпиткой. Метод периодических культур с подпиткой определяют как технику, в которой одно или более питательных веществ (субстратов) добавляют к питательной среде для усиления роста и достижения высокой плотности клеток в биореакторе. Как правило, добавление питательных веществ контролируемым образом оказывает благоприятное влияние на скорость роста и производительность процесса. В некоторых вариантах реализации изобретения в биореакторе можно получить концентрацию клеток выше 106 клеток/мл, 107 клеток/мл, 2x107 клеток/мл, 5x107 клеток/мл или 108 клеток/мл. В некоторых вариантах реализации изобретения биореакторы, используемые в методе периодических культур с подпиткой, имеют объем по меньшей мере 10 л, 20 л, 50 л, 80 л, 100 л, 250 л, 500 л или 1000 л. Клетки можно выращивать или в суспензионных, или в адгезивных культурах. В типовом варианте реализации изобретения клетки выращивают в суспензии. Предпочтительными являются клетки млекопитающих, а в конкретном типовом варианте реализации изобретения клетки млекопитающих представляют собой клетки яичников китайского хомячка.
Терапевтическое воздействие
[0072] Еще в одном аспекте изобретения предложены способы лечения патологического состояния или расстройства, включающие введение индивиду, нуждающемуся в таком лечении, терапевтически эффективного количества композиции/препарата, как описано в данном документе.
[0073] Композиции/препараты, описанные в данном документе, можно использовать отдельно или вместе с любыми терапевтическими агентами/композициями для различных целей, как, например, в способах лечения, описанных в данном документе. В связи с этим композиции/препараты могут быть фармацевтически приемлемыми.
[0074] В некоторых вариантах реализации изобретения патологическое состояние или расстройство, требующее лечения, связано с ферментной недостаточностью. Ферментные недостаточности в отделах клетки, таких как аппарат Гольджи, эндоплазматический ретикулум и лизосома, приводят к большому количеству разнообразных заболеваний человека. Например, лизилгидроксилаза, фермент, обычно находящийся в полости эндоплазматического ретикулума, необходима для правильного процессинга коллагена; отсутствие фермента приводит к синдрому Элерса-Данлоса VI типа, серьезному расстройству соединительной ткани. GnT II, обычно находящийся в аппарате Гольджи, необходим для нормального гликозилирования белков; отсутствие GnT II приводит к дефектам развития мозга.
[0075] В типовом варианте реализации изобретения патологическое состояние или расстройство, связанное с ферментной недостаточностью, представляет собой лизосомную болезнь накопления (ЛБН). Более сорока лизосомных болезней накопления (ЛБН) обусловлены, прямо или косвенно, отсутствием одного или более белков в лизосоме. ЛБН возникают в результате нарушения метаболизма различных субстратов, в том числе гликосфинголипидов, гликогена, мукополисахаридов и гликопротеинов. Метаболизм субстратов обычно происходит в лизосоме, а процесс постадийно регулируется различными деструктивными ферментами. Поэтому недостаток активности любого фермента может нарушать весь процесс и приводить к накоплению конкретных субстратов. Ниже перечислен ряд лизосомных болезней накопления и соответствующие дефектные ферменты:
болезнь Помпе: кислая альфа-глюкозидаза
болезнь Гоше: кислая бета-глюкозидаза или глюкоцереброзидаза
болезнь Фабри: альфа-галактозидаза A
GMI-ганглиозидоз: кислая бета-галактозидаза
болезнь Тея-Сакса: бета-гексозаминидаза A
болезнь Сандхоффа: бета-гексозаминидаза B
болезнь Ниманна-Пика: кислая сфингомиелиназа
болезнь Краббе: галактоцереброзидаза
болезнь Фарбера: кислая церамидаза
метахроматическая лейкодистрофия: арилсульфатаза A
болезнь Гурлера-Шейе: альфа-L-идуронидаза
болезнь Хантера: идуронат-2-сульфатаза
болезнь Санфилиппо типа A: гепаран-N-сульфатаза
болезнь Санфилиппо типа B: альфа-N-ацетилглюкозаминидаза
болезнь Санфилиппо типа C: ацетил-КоA: альфа-глюкозамидин-N-ацетилтрансфераза
болезнь Санфилиппо типа D: N-ацетилглюкозамин-6-сульфатсульфатаза
болезнь Моркио типа A: N-ацетилгалактозамин-6-сульфатсульфатаза
болезнь Моркио типа B: кислая бета-галактозидаза
болезнь Марото-Лами: арилсульфатаза B
болезнь Слая: бета-глюкуронидаза
альфа-маннозидоз: кислая альфа-маннозидаза
бета-маннозидоз: кислая бета-маннозидаза
фукозидоз: кислая альфа-L-фукозидаза
сиалидоз: сиалидаза
болезнь Шиндлера-Канзаки: альфа-N-ацетилгалактозаминидаза
[0076] В некоторых типовых вариантах реализации настоящего изобретения предложен способ лечения ЛБН, включающий введение индивиду, нуждающемуся в таком лечении, терапевтически эффективного количества композиции/препарата, как описано в данном документе. В одном типовом варианте реализации изобретения композиция/препарат содержит рекомбинантную β-глюкуронидазу человека. В другом типовом варианте реализации изобретения ЛБН представляет собой мукополисахаридоз 7 типа (т.е. МПС 7, МПС VII или синдром Слая), расстройство, возникающее в результате дефицита β-глюкуронидазы. В некоторых вариантах реализации изобретения рекомбинантная β-глюкуронидаза человека имеет повышенное содержание сиаловой кислоты и особенно эффективна при лечении ЛБН, например МПС 7.
[0077] В некоторых вариантах реализации настоящего изобретения предложен способ лечения патологического состояния или расстройства у субъекта, включающий введение композиции/препарата в соответствии со схемой лечения, как описано в данном документе, причем такое введение приводит к статистически значимому терапевтическому эффекту при лечении патологического состояния или расстройства. В некоторых вариантах реализации изобретения субъект представляет собой человека. В некоторых вариантах реализации изобретения композиция/препарат содержит рекомбинантный гликопротеин, который имеет повышенное содержание сиаловой кислоты. В типовом варианте реализации изобретения рекомбинантный гликопротеин имеет степень сиалирования по меньшей мере 0,7 моль/моль рекомбинантного гликопротеина. В другом типовом варианте реализации изобретения рекомбинантный гликопротеин имеет степень сиалирования по меньшей мере 1 моль/моль рекомбинантного гликопротеина. В некоторых вариантах реализации изобретения патологическое состояние или расстройство связано с ферментной недостаточностью. В типовом варианте реализации изобретения патологическое состояние или расстройство, связанное с ферментной недостаточностью, представляет собой лизосомную болезнь накопления (ЛБН).
[0078] Следовательно, в настоящем изобретении предложен способ лечения лизосомной болезни накопления (ЛБН) у субъекта, включающий введение композиции/препарата, как описано в данном документе, причем введение приводит к статистически значимому терапевтическому эффекту при лечении ЛБН. В типовом варианте реализации изобретения композиция/препарат содержит рекомбинантную β-глюкуронидазу человека, которая имеет повышенное содержание сиаловой кислоты. В дополнительном типовом варианте реализации изобретения ЛБН представляет собой мукополисахаридоз 7 типа (т.е. МПС 7, МПС VII или синдром Слая).
[0079] Согласно настоящему изобретению лечение ЛБН включает любую форму лечения ЛБН, например ослабление любого симптома ЛБН, уменьшение тяжести любого симптома ЛБН, сокращение продолжительности одного или более симптомов ЛБН, лечение или ингибирование любого фактора или состояния, связанного с ЛБН, или уменьшение клинических критериев либо определение степени или состояния ЛБН.
[0080] Согласно настоящему изобретению рекомбинантную β-глюкуронидазу человека по настоящему изобретению вводят в соответствии со схемой лечения ЛБН. В одном варианте реализации изобретения ЛБН представляет собой МПС 7. Такая схема лечения включает разовую дозировку, дозировку в сутки, в каждые две недели, а также количество доз в цикл лечения, или их комбинации.
[0081] Как правило, рекомбинантную β-глюкуронидазу человека (rhGUS) по настоящему изобретению можно вводить в дозе от примерно 0,1 мг до 20 мг, от 0,2 мг до 15 мг, от 0,5 до 12 мг, от 1 мг до 10 мг, от 1,5 мг до 8 мг, от 2 мг до 6 мг на кг. В некоторых вариантах реализации изобретения rhGUS вводят в дозе примерно 0,1 мг, 0,2 мг, 0,5 мг, 1 мг, 2 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг или примерно 12 мг на кг. В типовом варианте реализации изобретения rhGUS вводят в дозе примерно 4 мг на кг. Дозу можно регулировать в соответствии с состоянием каждого пациента, а также другими лекарственными препаратами, которые принимает пациент.
[0082] В некоторых вариантах реализации изобретения такую дозу вводят 1 раз в час, 1 раз в день, 1 раз в неделю (т.е. QW), 1 раз в две недели (т.е. QOW) или 1 раз в месяц.
[0083] В некоторых вариантах реализации изобретения rhGUS вводят каждый час, приблизительно каждые 1-24 часа, 1-20 часов, 1-16 часов, 1-12 часов, 1-8 часов, 1-6 часов, 1-4 часа, 1-2 часа или каждый час. В некоторых вариантах реализации изобретения rhGUS вводят приблизительно каждые 2, 3, 4, 5 или 6 часов или вводят приблизительно каждые 10 минут, 15 минут, 30 минут, 45 минут или 60 минут.
[0084] В некоторых вариантах реализации изобретения rhGUS можно вводить путем непрерывной инфузии. В некоторых вариантах реализации изобретения rhGUS можно вводить пациенту в течение периодов лечения, которые составляют по меньшей мере примерно 2, 4, 6, 10, 12 часов или дольше, что в некоторых вариантах реализации изобретения может повышать эффективность. В некоторых вариантах реализации изобретения rhGUS вводят путем непрерывной инфузии в течение 1-24 часов, 1-20 часов, 1-16 часов, 1-12 часов, 1-10 часов, 1-8 часов, 1-6 часов, 1-4 часов, 1-2 часов. В некоторых вариантах реализации изобретения rhGUS вводят путем непрерывной инфузии в течение примерно 10 минут, 15 минут, 30 минут, 45 минут или 60 минут. В некоторых вариантах реализации изобретения rhGUS вводят путем непрерывной инфузии в течение примерно 1 часа, 2 часов, 3 часов, 4 часов, 5 часов, 6 часов, 7 часов, 8 часов, 10 часов, 12 часов, 24 часов или более. В типовом варианте реализации изобретения rhGUS вводят путем непрерывной инфузии в течение 4 часов. В некоторых вариантах реализации изобретения периоды непрерывной инфузии отделены периодами, в которые инфузию не выполняют (т.е. периоды, в которые не вводят rhGUS). Инфузию можно проводить любым пригодным способом, например, при помощи мини-насоса.
[0085] В некоторых вариантах реализации изобретения rhGUS вводят приблизительно каждые 1-30 дней, каждые 1-25 дней, каждые 1-20 дней, каждые 1-14 дней, каждые 1-10 дней, каждые 1-5 дней или каждый день.
[0086] В некоторых вариантах реализации изобретения rhGUS вводят в течение примерно 1-12 недель, примерно 1-24 недель, примерно 1-36 недель, примерно 1-48 недель, примерно 1-60 недель или примерно 1-72 недель. В некоторых вариантах реализации изобретения rhGUS вводят в течение примерно 1 месяца, 4 месяцев, 8 месяцев, 12 месяцев, 16 месяцев, 20 месяцев или более. В некоторых вариантах реализации изобретения rhGUS вводят в течение примерно 1 года, 2 лет, 5 лет, 10 лет или более. В некоторых вариантах реализации изобретения rhGUS вводят непрерывно (т.е. долговременное применение).
[0087] rhGUS может находиться в лиофилизированной форме, которую ресуспендируют стерильным (например, водным) разбавителем перед введением. rhGUS можно вводить любым эффективным путем, в том числе при помощи подкожной инъекции, внутримышечной инъекции, внутривенной инъекции или инфузии или перорально. В некоторых типовых вариантах реализации изобретения rhGUS вводят при помощи внутривенной инфузии. Как правило, назначенную дозу rhGUS можно вводить в виде одной дозы (например, инъекции) или можно растянуть на 24 часа или менее, например при помощи непрерывной инфузии или повторяющихся инъекций субдоз или тому подобного, или как подробно описано в данном документе. В одном варианте реализации изобретения назначенную дозу rhGUS можно вводить в виде одной инъекции или в виде многократных инъекций.
[0088] В одном варианте реализации изобретения для уменьшения тяжести ЛБН пациенту вводят rhGUS приблизительно раз в две недели (т.е. QOW) в дозе между примерно 0,5 и 12 мг (например, примерно 1, 2, 4, 8 или 12 мг) на кг. В типовом варианте реализации изобретения пациенту вводят rhGUS приблизительно раз в две недели в дозе примерно 4 мг на кг. В некоторых вариантах реализации изобретения курс лечения может длиться 12, 24, 36, 48 или 60 недель или непрерывно (т.е. долговременное применение).
[0089] Согласно настоящему изобретению rhGUS, используемую в способах настоящего изобретения, можно применять или отдельно, или в комбинации со стандартом лечения ЛБН, или как часть схемы лечения, включающей стандарт лечения ЛБН. В некоторых вариантах реализации изобретения пациентам можно вводить антигистаминное средство в профилактических целях до каждой инфузии rhGUS. В дополнительных вариантах реализации изобретения пациенту можно вводить жаропонижающее средство (например, ибупрофен или ацетаминофен) до каждой инфузии rhGUS.
[0090] Согласно некоторым вариантам реализации настоящего изобретения введение rhGUS обеспечивает статистически значимый терапевтический эффект. В одном варианте реализации изобретения статистически значимый терапевтический эффект определяют на основании одного или более стандартов или критериев, установленных одним или более регуляторными органами в США, например FDA, или других странах. В другом варианте реализации изобретения статистически значимый терапевтический эффект определяют на основании результатов, полученных из плана и/или процедуры клинического исследования, утвержденных регуляторными органами.
[0091] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании рандомизированного плацебо-контролируемого одностороннего перекрестного клинического исследования с замаскированным началом. В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании данных из схемы клинического исследования, в котором субъектов случайным образом распределяли в одну из 4 групп, при этом каждая группа представляет определенную последовательность лечения в различные моменты времени, заранее заданные слепым методом. В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании данных, полученных от группы больных из по меньшей мере 4, 6, 8, 10 или 12 субъектов. В типовом варианте реализации изобретения статистически значимый терапевтический эффект определяют на основании данных, полученных от группы больных из 12 субъектов.
[0092] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании исследования, включающего 12 субъектов, случайным образом распределенных в соотношении 1:1:1:1 в одну из четырех групп с различными последовательностями лечения, чтобы начать лечение или при помощи 4 мг/кг rhGUS раз в две недели (т.е. QOW), или при помощи плацебо, а затем перейти к 4 мг/кг rhGUS QOW в различные заранее заданные моменты времени. В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании исследования субъектов, которым вводили или 4 мг/кг rhGUS, или плацебо QOW в течение 48 недель.
[0093] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании исследования, в котором rhGUS вводят QOW при помощи медленной внутривенной инфузии в течение приблизительно 4 часов. В некоторых вариантах реализации изобретения пациентам вводят антигистаминное средство (например, цетризин или лоратадин) в профилактических целях до каждой инфузии rhGUS.
[0094] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют, измеряя уровни гликозаминогликана (ГАГ) в моче в качестве первичной конечной точки. Обширные исследования расстройств МПС, проведенные в течение последних 20 лет, дают значимую и релевантную научную информацию, которая позволяет считать уровни ГАГ в моче биомаркером, с достаточным основанием предсказывающим клиническую пользу. Патогенез заболевания и механизм действия rhGUS при МПС 7 хорошо известны, а данные для других подобных расстройств МПС со сравнимыми заместительными ферментными терапиями (ЗФТ) подтвердили, что ГАГ в моче является прямым патофизиологическим и легко измеряемым маркером патогенеза заболевания МПС, и ГАГ в моче является обоснованным показателем эффекта лечения и клинической пользы при расстройствах МПС. В типовом варианте реализации изобретения статистически значимый терапевтический эффект определяют на основании определения уровней ГАГ в моче в клиническом исследовании, включающем 12 субъектов, которым вводили 4 мг/кг rhGUS или плацебо QOW в течение 48 недель.
[0095] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют, измеряя вторичные критерии эффективности (т.е. вторичные конечные точки), такие как многодоменный показатель респондентов и оценка индивидуализированной клинической реакции.
[0096] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют с использованием многодоменного показателя респондентов, который объединяет независимые многодоменные анализы, для обеспечения возможности определения более широкого базиса для эффективности без сложностей при попытках сконструировать пригодные комбинированные конечные точки. В некоторых вариантах реализации изобретения многодоменный показатель респондентов дает оценку эффективности rhGUS по всему широкому спектру клинических характеристик, обычно наблюдаемых у пациентов с МПС 7.
[0097] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют, оценивая индивидуализированную клиническую реакцию (ICR). Она является мерой отклика каждого субъекта на лечение, которое выбрано на основании обоснованности измерения результата по отношению к опасениям, о которых сообщил субъект/родитель/лицо, осуществляющее уход, способности субъекта верно осуществить оценку клинического результата и степени ухудшения состояния для этого индивида. Использование ICR делает возможной оценку клинической пользы rhGUS путем оценки изменения предварительно заданного индивидуализированного клинического результата, который считают наиболее важным для каждого субъекта, а затем определения суммарного показателя отклика для испытуемой группы. В некоторых вариантах реализации изобретения вторичные критерии эффективности (т.е. вторичные конечные точки) могут включать оценку лечения субъектов по признакам и симптомам МПС 7, которые в наибольшей степени мешают повседневной жизни субъекта (т.е. оценка клинических проблем). В некоторых вариантах реализации изобретения оценка может включать определение функции легких, определение дистанции безболевой ходьбы, определение объема движения при сгибании руки в плечевом суставе и определение функции мелкой моторики.
[0098] В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании данных со значением альфа, которое меньше или равно примерно 0,05, 0,04, 0,03, 0,02 или 0,01. В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании данных с доверительным интервалом, который больше или равен 95%, 96%, 97%, 98% или 99%. В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют на основании данных со значением p, которое меньше или равно примерно 0,05, 0,04, 0,03, 0,02 или 0,01. В некоторых вариантах реализации изобретения статистически значимый терапевтический эффект определяют в случае утверждения III фазы клинического исследования композиций и способов, предложенных в настоящем изобретении, например, управлением FDA в США.
[0099] Как правило, статистический анализ может включать любой пригодный метод, разрешенный регуляторным органом, например FDA, в США, или Китае, или любой другой стране. В некоторых вариантах реализации изобретения статистический анализ включает нестратифицированный анализ, логарифмический ранговый критерий, например метод Kaplan-Meier, Jacobson-Truax, Gulliken-Lord-Novick, Edwards-Nunnally, Hageman-Arrindel и иерархическое линейное моделирование (HLM), а также регрессионный анализ Кокса.
[00100] В некоторых вариантах реализации изобретения для предсказания отклика на терапию и/или определения эффективности лечения можно использовать биомаркеры лизосомного накопления. В некоторых вариантах реализации изобретения можно измерить уровни гликозаминогликана (ГАГ) в моче, а снижение уровней ГАГ в моче использовать как показатель положительного отклика на терапию. В некоторых вариантах реализации изобретения повышенные уровни биомаркера ГАГ в моче, которые затем снижаются при введении rhGUS, предсказывают отклик на терапию. В некоторых вариантах реализации изобретения эту информацию можно применять при назначении схемы лечения (как описано в данном документе) лизосомной болезни накопления (например, МПС 7) с использованием rhGUS. В связи с этим в настоящем изобретении предложены способы назначения схемы лечения, которая включает установление уменьшения уровня биомаркера ЛБН в биологическом образце от субъекта, которого лечили при помощи rhGUS, и назначение схемы лечения при помощи rhGUS на основании снижения уровня одного или более биомаркеров ЛБН в биологическом образце. В некоторых вариантах реализации изобретения биомаркер ЛБН представляет собой ГАГ в моче. В некоторых вариантах реализации изобретения сниженный или уменьшенный уровень ГАГ в моче является показателем отклика на терапию и/или эффективности лечения при помощи rhGUS. В некоторых вариантах реализации изобретения снижение уровня ГАГ в моче до заранее заданного стандартного уровня является показателем лучшего прогноза лечения при помощи rhGUS.
ПРИМЕРЫ
Пример 1: Получение и количественное определение общего содержания сиаловой кислоты
[00101] Рекомбинантная β-глюкуронидаза человека (rhGUS), полученная в соответствии с настоящим изобретением, была обозначена GUS CR01. Рекомбинантный белок получен из клеток яичников китайского хомячка (CHO), которые разработаны так, чтобы экспрессировать и секретировать фермент в питательную среду с использованием биореактора для культивирования.
[00102] Предыдущие партии β-глюкуронидазы (обозначенные как партия GUS 43/44) получены с использованием той же клеточной линии при помощи процесса, в котором клетки выращивают присоединенными к микроносителям в условиях непрерывной перфузии. Клетки, как правило, растут в среде для выращивания, содержащей фетальную бычью сыворотку (FBS). Потом FBS вымывают и заменяют средой, содержащей гидролизаты, а кондиционированную среду собирают в условиях перфузии.
[00103] В отличие от ранее описанных способов GUS CR01 получали в системе для культивирования, в которой клетки выращивали в суспензии с использованием метода периодических культур с подпиткой. Другим отличием является то, что GUS CR01 культивировали только в безбелковой среде с химически определенным составом, а не в содержащей сыворотку среде, используемой ранее.
[00104] Способ количественного определения общего содержания сиаловой кислоты в GUS разработан отделом контроля качества компании Rentschler Biotechnologie (RB) для исследования высвобождения из лекарственной субстанции GUS. В этом способе остатки сиаловой кислоты высвобождаются из гликановых структур rhGUS при кислотном гидролизе. Высвобожденную сиаловую кислоту затем метят OPD (O-фенилендиамином дигидрохлоридом) и анализируют при помощи обращенно-фазовой ВЭЖХ (ОФ-ВЭЖХ). На данный момент в компании RB на общее содержание сиаловой кислоты проанализированы партия rhGUS 43/44 и шесть партий rhGUS, полученных в компании RB. Эти результаты (Таблица 1) согласуются с результатами, полученными GlycoSolutions.
Таблица 1. Результаты определения общего содержания сиаловой кислоты в GUS
ранее
Пример 2: Фармакокинетика у самцов крыс линии Спрег-Доули
[00105] В этом примере рекомбинантные β-глюкуронидазы, полученные в соответствии с настоящим изобретением, сравнивали с полученными в соответствии со способами, ранее описанными в данной области техники. Целью этого исследования было оценить фармакокинетику и распределение в тканях рекомбинантных β-глюкуронидаз человека при внутривенном введении путем одной двухчасовой инфузии самцам крыс линии Спрег-Доули. Скорость инфузии составляла 1/3 от общего объема в первый час, а затем 2/3 от общего объема во второй час. Этот режим дозирования разработан, чтобы смоделировать режим дозирования, который будут использовать для пациентов.
Вещества и методики
Тестируемые образцы и инфузии
[00106] В этом исследовании использовали три тестируемых образца: 0,9% раствор хлорида натрия в качестве контрольного образца, не содержащего ферменты, GUS CR01 и GUS партии 43/44. Полное описание тестируемых образцов можно найти в Таблице 2.
Таблица 2. Тестируемые образцы
Тестируемый образец № 1
Название: 0,9% раствор хлорида натрия для инъекций, фармакопея США (физиологический раствор)
Поставщик: Baxter Healthcare (Марион, Северная Каролина)
Физические свойства: прозрачная жидкость
Идентификатор/номер партии C883827
Показатель стерильности: стерильный
Условия хранения: при комнатной температуре
Срок годности: 04/2014
Тестируемый образец № 2
Название: GUS CR01
Поставщик: Ultragenyx Pharmaceutical Inc. (Новато, Калифорния)
Количество: ~32,5 мл
Концентрация: 2,0 мг/мл
Активность GUS, единицы/мл 10,75 мЕдиниц/мл
Удельная активность, единицы/мг 5,35 мЕдиниц/мг
Физические свойства: прозрачная жидкость
Идентификатор/номер партии CR01
Условия хранения: 2-8°C
Срок годности: не указан
Тестируемый образец № 3
Название: GUS, партия 43/44
Поставщик: Ultragenyx Pharmaceutical Inc. (Новато, Калифорния)
Количество: ~25 мл
Концентрация: 2,5 мг/мл* (2,18 мг/мл)
Активность GUS, единицы/мл 11,4 мЕдиниц/мл
Удельная активность, единицы/мг 5,23 мЕдиниц/мг
Физические свойства: прозрачная жидкость
Идентификатор/номер партии 43/44
Условия хранения: -60 - -80°C
Срок годности: не указан
[00107] Тестируемые образцы вводили самцам крыс линии Спрег-Доули в дозе ~2 мг/кг массы тела при помощи одной инфузии, состоящей из двух одночасовых фаз. В течение первого часа проводили вливание одной трети дозы, а в течение второго часа - вливание двух третей дозы (Таблица 3).
Таблица 3. Номера групп крыс, доза и скорости инфузии

* Дозу GUS партии 43/44 изначально рассчитывали на основании содержания белка, определенного при помощи анализа с использованием БХК, которое составляло 2,5 мг/мл. Если концентрацию белка рассчитывали на основании поглощения или ОП 280 и коэффициента ослабления 2,12, фактическая доза составляла 84,8% x 2 = 1,7 мг/кг.
[00108] Образцы крови забирали у каждой крысы перед лечением, а затем через определенные интервалы в течение фаз медленной инфузии, быстрой инфузии и после инфузии в соответствии с планом, представленным в Таблице 4. Крови давали свернуться, сыворотку отделяли и хранили замороженной при -80°C до перемещения на сухой лед для анализа.
Таблица 4. План проведения инфузий и забора крови
Активность GUS в сыворотке
[00109] Активность β-глюкуронидазы определяли следующим образом. 25 мкл сыворотки, разбавленной от 1:4 до 1:300 0,1 М ацетатом натрия с pH 4,8 и 1 мг/мл кристаллического БСА смешивали с 50 мкл 10 мМ субстрата 4-метилумбеллиферил-β-D-глюкуронида в 0,1 М ацетате натрия, pH 4,8, 1 мг/мл кристаллического БСА. Все растворы предварительно нагревали до 37°C, перемешивали, а затем инкубировали при 37°C в течение 30 минут. Реакции останавливали добавлением 200 мкл карбоната глицина, pH 10,5, и анализировали с использованием планшет-ридера Molecular Devices M2e при длинах волн возбуждения/эмиссии 366/446 нм. Активность выражали следующим образом: 1 единица = 1 нмоль образовавшегося 4-метилумбеллиферона/мл/ч при 37°C.
Активность GUS в тканях
[00110] Ткани отбирали при аутопсии и помещали в криопробирки, резко замороженные в жидком азоте, и хранили при -80°C до перемещения на сухой лед для анализа. Распределение активности GUS в тканях оценивали следующим образом. Все или часть образцов тканей размораживали и объединяли с 10-20 объемами 25 мМ Трис, 140 мМ NaCl, 1 мМ фенилметилсульфонилфторида, pH 7,2. Гомогенаты тканей готовили с использованием гомогенизатора Kinematica Polytron в течение 30 секунд на льду; полученные гомогенаты однократно замораживали/размораживали (при -80°C), а затем в течение 20 секунд обрабатывали ультразвуком, охлаждая на льду. 25 мкл каждого гомогената анализировали на содержание β-глюкуронидазы с использованием 4-метилумбеллиферил-β-D-глюкуронида, как описано выше. Концентрацию белка в гомогенатах определяли при помощи метода с бицинхониновой кислотой. Уровни β-глюкуронидазы в тканях выражали в нмоль гидролизованного 4-метилумбеллиферона/ч/мг белка.
Результаты и обсуждение
Фармакокинетика GUS CR01 в сравнении с GUS партии 43/44 в плазме
[00111] Фиг. 1 иллюстрирует активность β-глюкуронидазы в сыворотке крыс из каждой группы, в которой проводили инфузию, в течение стадии медленной инфузии, стадии быстрой инфузии и постинфузионной стадии. Кривая для группы 1, в которой проводили инфузию только физиологического раствора, указывает на низкий эндогенный уровень β-глюкуронидазы крыс, которая присутствует в сыворотке этих крыс. Эндогенный уровень вычитали из значений на двух других графиках, полученных для крыс, которым проводили инфузию фермента.
[00112] Графики для GUS CR01 и GUS партии 43/44 иллюстрируют изменяющееся во времени увеличение активности ферментов, которая достигает уровня стационарного состояния к концу периода медленной инфузии, затем снова увеличивается одновременно с началом периода быстрой инфузии. Однако уровень GUS CR01 в сыворотке в 2 раза выше в конце периода медленной инфузии и в 3 раза выше в конце периода быстрой инфузии по сравнению с уровнем GUS партии 43/44. На фиг. 1 также можно увидеть, что наблюдается быстрый клиренс обоих ферментов из сыворотки после прекращения инфузий, что характерно для лизосомальных ферментов в целом.
[00113] На фиг. 2 приведен постинфузионный клиренс для обоих ферментов, из которого были рассчитаны величины t1/2. GUS партии 43/44 выводится из кровотока со значением t1/2 1-й фазы, которое составляет 4,50 минуты. В отличие от этого GUS CR01 выводится немного медленнее, t1/2 составляет 5,30 минуты. Исходные данные о клиренсе анализировали при помощи различных методов, чтобы пересчитать величины t1/2 (фиг. 4 A и B). Значения Cmax (14800 для GUS CR01 в сравнении с 4300 для GUS партии 43/44) и AUC-t (18700 в сравнении с 5580) также демонстрируют 3-кратное увеличение для GUS (Таблица 5). Значение t1/2 рассчитывали совсем другим путем, если учитывали только вторую фазу. Значение t1/2 2-й фазы составляет 1,1 ч для GUS CR01 и 0,967 ч для GUS партии 43/44 (Таблица 5).
Таблица 5.

Распределение в тканях GUS CR01 по сравнению с GUS партии 43/44
[00114] В дополнение к клиренсу двух ферментов оценивали распределение GUS CR01 в тканях печени, селезенки, сердца, почки, мозга и легкого по сравнению с распределением GUS партии 43/44. Экстракты, приготовленные из каждой из этих тканей, анализировали на содержание β-глюкуронидазы и белка, как описано в методиках. Результаты анализов выражали в виде единиц активности β-глюкуронидазы / мг белка ткани. Обобщенные результаты этих анализов можно увидеть на фиг. 4. На каждом из графиков этой фигуры общие уровни фермента, включающие эндогенную β-глюкуронидазу крыс, показаны слева. На правой части каждого графика из общего уровня фермента вычли средний эндогенный уровень фермента. Средний эндогенный уровень β-глюкуронидазы для каждой ткани рассчитывали с использованием значений от всех пяти крыс из группы 1, в которой проводили инфузию физиологического раствора.
[00115] В каждой ткани уровень GUS у крыс, которым проводили инфузию или GUS CR01, или GUS партии 43/44, выше, чем у крыс, которым проводили инфузию физиологического раствора. После вычитания эндогенных уровней GUS становится понятно, что у крыс, которым проводили инфузию GUS CR01, наблюдаются уровни GUS по меньшей мере в два раза выше, чем у крыс, которым проводили инфузию GUS партии 43/44.
[00116] Исследование планировали, чтобы оценить фармакокинетику β-глюкуронидазы и характеристики распределения в тканях GUS CR01 и GUS партии 43/44. В настоящем исследовании было установлено, что GUS CR01 выводится из кровотока со значением t1/2 1-й фазы, которое составляет 5,30 минуты, по сравнению с меньшим значением t1/2 для GUS партии 43/44, которое составляет 4,50 минуты. Значение t1/2 второй фазы также немного выше для GUS CR01.
[00117] Более значительные различия между 2 ферментами были обнаружены для Cmax, AUC-t и распределения в тканях. Максимальная концентрация (Cmax) (активность) β-глюкуронидазы в сыворотке в конце двухчасового периода инфузии для GUS CR01 составляла 14829 единиц/мл, что в 4,2 раза больше, чем концентрация 3537 единиц/мл, полученная для GUS партии 43/44. Увеличение Cmax можно объяснить накоплением медленнее выводящегося фермента, что приводит к более высоким концентрациям в крови в течение периода инфузии. Величина AUC-t также была намного выше (более чем в 3 раза) для GUS CR01 в сравнении с GUS партии 43/44, что представлено на фиг. 1.
[00118] Последнее, но не менее важное наше наблюдение заключалось в том, что во всех исследуемых тканях уровни GUS CR01 были в два или более раз выше, чем уровни GUS партии 43/44. Известно, что характеристики клиренса лизосомального фермента из кровотока влияют на распределение в тканях. Вероятно, увеличение t1/2 GUS CR01 в кровотоке увеличит эффективность распределения фермента по выбранным тканям. Более важно то, что изменения распределения в тканях, по-видимому, очень хорошо коррелируют с изменениями Cmax и AUC-t. Как можно увидеть на фиг. 3, величины ошибок достаточно большие, что отражает широкий интервал значений, полученных для отдельных крыс из каждой исследуемой группы. Трехкратное повторение анализа на β-глюкуронидазу в некоторых тканях подтвердило исходные значения, что позволяет нам считать, что для этих крыс действительно наблюдается широкий интервал значений.
[00119] Ранее анализ GUS CR01 показал, что хотя уровень маннозо-6-фосфата и многие другие свойства очень похожи для двух ферментов, содержание сиаловой кислоты в GUS CR01 в 28 раз выше, чем содержание в GUS партии 43/44 (1,1 моль/моль мономера GUS в сравнении с 0,04 моль/моль мономера GUS). См. Таблицу 6.
Таблица 6. Характеристики GUS CR01 и GUS партии 43/44
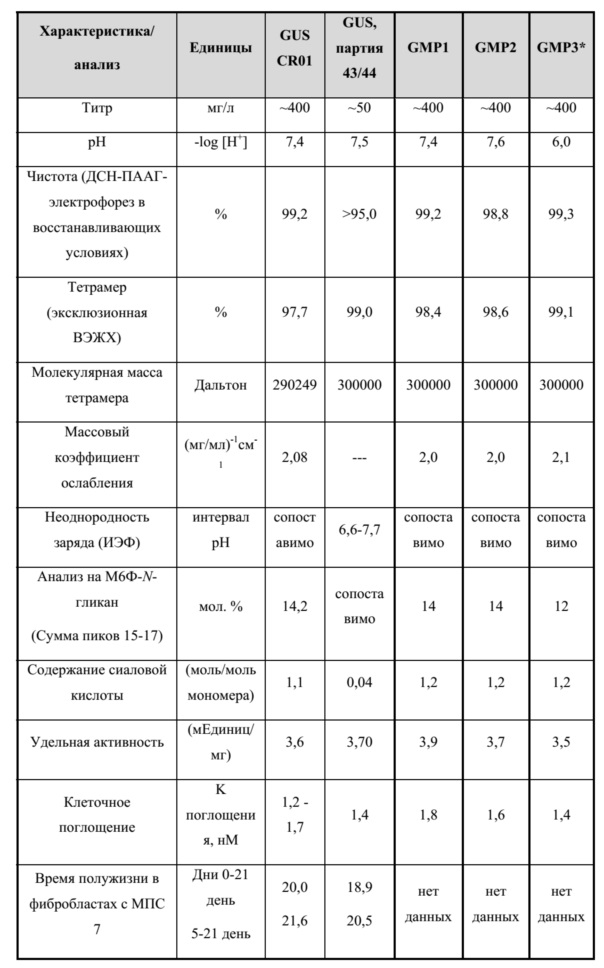
* Анализ моносахаридов показал, что 71% остатков галактозы в GMP3 GUS сиалированы.
[00120] После объединения данных становится совершенно очевидно, что лучшее распределение в тканях GUS CR01, продемонстрированное в данном документе, обусловлено увеличением содержания сиаловой кислоты, так как хорошо известно, что сиаловая кислота замедляет клиренс гликопротеинов из кровотока маннозными рецепторами, расположенными в эндотелиальных клетках на внутренних стенках кровеносных сосудов. Комбинация высоких уровней сиаловой кислоты и фрагментов маннозо-6-фосфата с высоким сродством является оптимальной для уменьшения поглощения тканями посредством других углеводных рецепторов за счет высокого содержания сиаловой кислоты, что обеспечивает более высокие концентрации в кровотоке, и следовательно, достижение превосходного поглощения целевыми тканями вследствие высокого сродства маннозо-6-фосфата.
Пример 3: Лечение МПС VII с использованием заместительной ферментной терапии
[00121] Цель этого примера - продемонстрировать, что заместительная ферментная терапия для мукополисахаридоза VII типа (т.е. МПС VII; синдром Слая) с использованием рекомбинантно полученной β-глюкуронидазы человека (rhGUS) уменьшает лизосомальное накопление в 36-недельном клиническом исследовании.
[00122] В этом примере трем субъектам, у которых диагностирован МПС VII, вводили rhGUS с повышенным содержанием сиаловой кислоты. Введение доз выполняли согласно следующему расписанию в течение 36 недель:
недели 1-12: 2 мг/кг раз в две недели;
недели 13-20: 1 мг/кг раз в две недели;
недели 21-28: 4 мг/кг раз в две недели; и
недели 29-36: 2 мг/кг раз в две недели.
[00123] В течение 36-недельного курса лечения оценивали безопасность и эффективность rhGUS. Оказалось, что соединение rhGUS является безопасным и хорошо переносимым. Важно, что вплоть до 36 недели не наблюдалось серьезных побочных эффектов, реакций на лекарственное средство или реакций гиперчувствительности, связанных с инфузией, у кого-либо из трех субъектов.
[00124] Для определения эффективности вначале оценивали уровни гликозаминогликанов (ГАГ) в моче и сыворотке крови, так как лизосомальное накопление ГАГ является характерной особенностью дефицита GUS. У субъектов, которых лечили с использованием rhGUS, наблюдалось быстрое и непрерывное зависимое от дозы снижение уровня гликозаминогликана (ГАГ) в моче. См. фиг. 4. Среднее снижение уровня ГАГ в моче в конце каждого интервала введения лекарственного средства показано на фиг. 5; видно, что доза 4 мг/кг приводила к наибольшему снижению уровней ГАГ в моче.
[00125] Также у всех трех субъектов, которых лечили rhGUS, наблюдалось постепенное снижение уровня гликозаминогликана (ГАГ) в сыворотке. Характерно, что каждый субъект продемонстрировал снижение уровней ГАГ в сыворотке по меньшей мере на 25% в конце 36-недельного курса лечения. См. фиг. 6.
[00126] В заключение, у субъектов, которых лечили rhGUS, оценивали размер печени, так как у пациентов, страдающих от МПС VII, часто наблюдается увеличение размера печени. После 36-недельного курса лечения наблюдалось значительно меньшее увеличение печени. См. фиг. 7.
[00127] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же самое значение, которое понятно специалисту в области техники, к которой относится настоящая заявка. В данном документе описаны типичные способы и материалы, хотя для практического осуществления или апробации настоящего изобретения можно использовать любые способы и материалы, подобные или эквивалентные описанным в данном документе.
[00128] Хотя изобретение описано по отношению к конкретным вариантам реализации, понятно, что оно допускает дополнительные изменения, и предполагается, что данная заявка распространяется на любое применение или любые разновидности, адаптации изобретения, в целом следующие принципам изобретения и включающие такие отступления от настоящего описания, которые находятся в пределах известной или общепринятой практики в области техники, к которой принадлежит изобретение, и которые могут быть применены к существенным признакам, изложенным выше в данном документе, и которые следуют из прилагаемой формулы изобретения.
[00129] Описания, в том числе формула изобретения, фигуры и/или чертежи, всех без исключения патентов, патентных заявок и публикаций, цитируемых в данном документе, включены в данный документ в полном объеме посредством ссылки. В случае любого противоречия между цитируемым источником и данным описанием изобретения руководствоваться следует данным описанием. При описании вариантов реализации настоящей заявки для ясности применяют специальную терминологию. Однако предполагается, что изобретение не ограничено конкретной выбранной терминологией. Ничего в данном описании не следует рассматривать как ограничивающее объем настоящего изобретения. Все представленные примеры являются типичными и неограничивающими. Описанные выше варианты реализации могут быть модифицированы или изменены в пределах сущности изобретения, что понятно специалистам в данной области техники с учетом вышеизложенного.








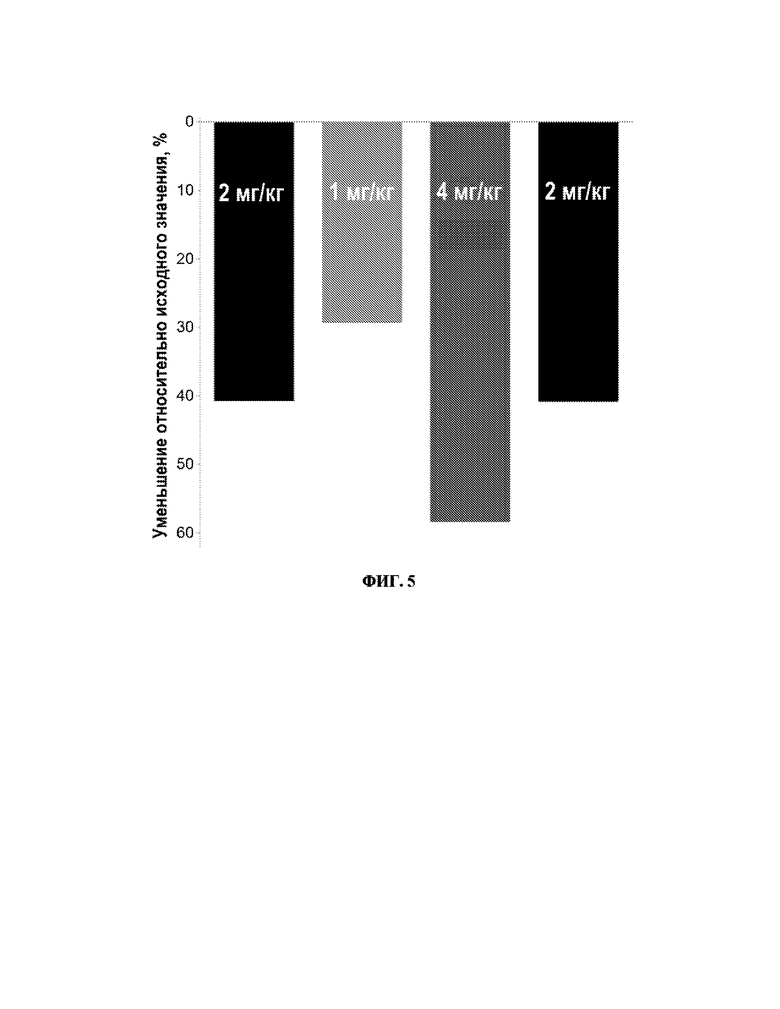
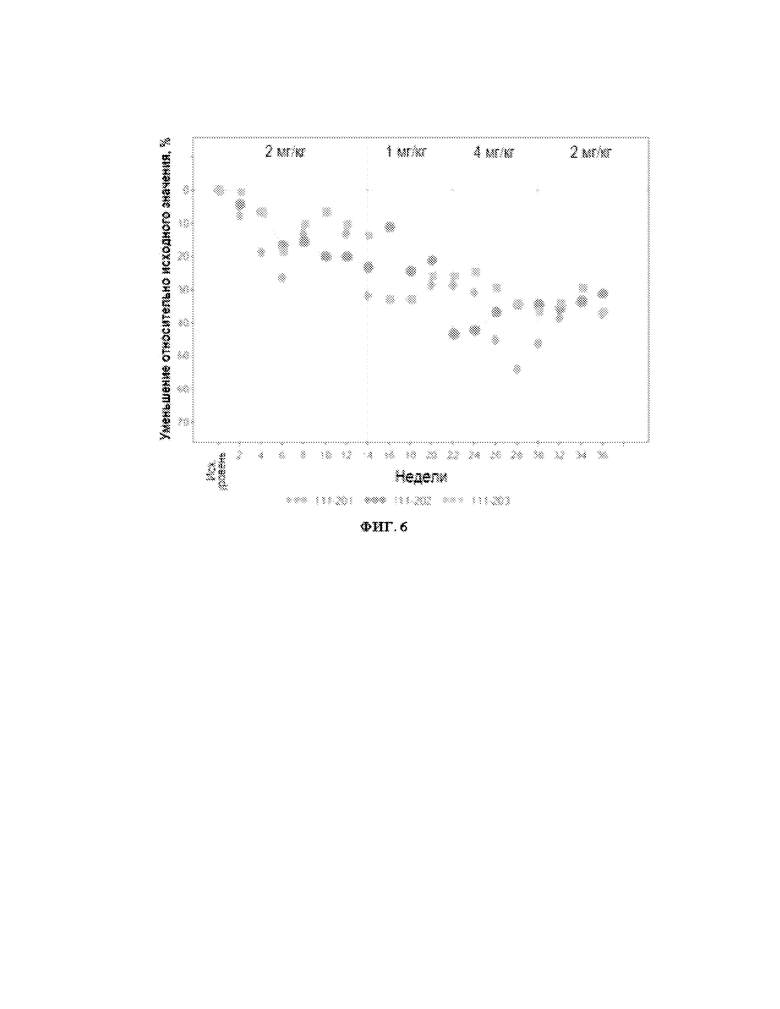

Изобретение относится к области медицины. Предложена композиция для лечения лизосомной болезни накопления, содержащая рекомбинантный гликопротеин, представляющий собой β-глюкуронидазу человека и имеющий степень сиалирования примерно 1,1 моль/моль. Изобретение обеспечивает увеличение содержания сиаловой кислоты в гликопротеине, предназначенном для фармакологического применения. 8 з.п. ф-лы, 7 ил., 6 табл., 3 пр.
1. Композиция для лечения лизосомной болезни накопления, содержащая рекомбинантный гликопротеин, причем рекомбинантный гликопротеин представляет собой β-глюкуронидазу человека и имеет степень сиалирования, которая составляет примерно 1,1 моль/моль рекомбинантного гликопротеина.
2. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет уровень маннозо-6-фосфатных (М6Ф) фрагментов, который составляет по меньшей мере 10 мол. % от общего количества гликана рекомбинантного гликопротеина.
3. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет уровень фрагментов М6Ф, который составляет по меньшей мере 12 мол. % от общего количества гликана рекомбинантного гликопротеина.
4. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет степень сиалирования, которая составляет примерно 1,1 моль/моль, и уровень фрагментов М6Ф, который составляет по меньшей мере 10 мол. % от общего количества гликана рекомбинантного гликопротеина.
5. Композиция по п. 1, отличающаяся тем, что рекомбинантная β-глюкуронидаза человека содержит SEQ ID №: 1.
6. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет М6Ф-зависимую константу (К) поглощения, составляющую менее 5 нМ.
7. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет М6Ф-зависимую константу (К) поглощения, составляющую менее 3 нМ.
8. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет М6Ф-зависимую константу (К) поглощения, составляющую менее 2 нМ.
9. Композиция по п. 1, отличающаяся тем, что рекомбинантный гликопротеин имеет М6Ф-зависимую константу (К) поглощения, составляющую от 1,2 до 1,8 нМ.
| VOGLER C | |||
| et al | |||
| Overcoming the blood-brain barrier with high-dose enzyme replacement therapy in murine mucopolysaccharidosis VII | |||
| Proc Natl Acad Sci USA | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| LEE K | |||
| et al | |||
| A biochemical and pharmacological comparison of enzyme replacement therapies for the glycolipid storage disorder Fabry disease | |||
| Glycobiology | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Пульверизатор | 1929 |
|
SU17622A1 |
Авторы
Даты
2019-05-24—Публикация
2015-03-05—Подача