Область изобретения
Настоящее изобретение относится к физико-химическому способу производства лекарственных грибов и произведенным грибам.
Уровень техники
Обычно грибы культивируют в мешках или контейнерах на различных материалах, таких как целлюлоза, песок, глина, в соответствии с различными способами и качеством конечного продукта. В соответствии с настоящим изобретением, предпочтительно используют полипропиленовые контейнеры, главным образом бутылки, расположенные на полках в технологических теплицах, при регулируемых в соответствии с необходимостью естественном или искусственном освещении, влажности и температуре. Такой способ описан в Rodriguez-Estrada and Royse (2005) in the cultivation (при культивации Pleurotus eryngii).
Краткое описание изобретения
Одной целью настоящего изобретения является создать способ культивации, оптимальный по выходу и качеству, и особенно подходящий для стандартизации и физико-химического развития в грибах активных компонентов, отчасти уже присутствующих и/или введенных в качестве прекурсоров, таким образом, чтобы количество таких компонентов являлось достаточным для лечения или предотвращения неопластических/дегенеративных заболеваний, начиная от уровня ранее научно доказанной эффективности.
Другой целью настоящего изобретения является получение определенного субстрата для культивации каждого вида грибов, выбранного в соответствии с его способностью противодействовать упомянутым заболеваниям, и его адаптивности к культивации согласно упомянутому способу Rodriguez-Estrada и Royse.
Еще одной целью настоящего изобретения является выбор разновидностей грибов, модифицированных для использования в качестве лекарственных грибов, т.е. выбранных на основании их научно доказанной активности при лечении или предотвращении неопластических/дегенеративных заболеваний. Этот способ представляет собой реализацию такой активности в плане стандартизации активных компонентов, эффективных в оказании желаемого лечебного действия.
С целью достижения указанных целей, в настоящем изобретении предложен физико-химический способ производства обогащенных грибов, модифицированных для выработки биологически активных веществ и получаемых в технологических теплицах на контейнерах, содержащих дозированное количество субстрата, включающий стадии выделения и предпосевного развития мицелия, созревания субстрата, посева мицелия желаемого вида грибов, инкубации с развитием грибного примордия в условиях, контролируемых и управляемых механизмами и процессорами, способными регулировать температуру, влажность и облучение, развития карпофоров, их сбор и обработка пульсирующим светом для стимуляции производства витамина D2. Физическую обработку электромагнитными полями (ЭМП) использовали на всех стадиях до сбора для содействия внедрению микроэлементов в карпофор через мицелий, а также использовали химическую обработку путем добавления в субстрат яичного порошка, и после посева мицелия - неорганических микроэлементов. Таком образом получают лекарственные грибы, обладающие терапевтическими и профилактическими свойствами, в общем смысле способствующие здоровью и способные рассматриваться как функциональные пищевые продукты, возможно относящиеся к новой пищевой категории и способные вызвать физиологический ответ организма, направленный против хронических дегенеративных заболеваний, в частности онкологических заболеваний.
В частности, физическая обработка способствует увеличению количества карпофоров, увеличению сухой массы и влажности, уменьшению времени производства, и помимо этого, оптимальному преобразованию неорганических микроэлементов в органические вещества; далее, физическая обработка позволяет улучшить метаболизм субстрата и конечное качество грибов. Преимущественным образом физическая обработка проводится согласно определенной последовательности и состоит в воздействии ЭМП с величиной индукции 15-25 мТл в течение 10-20 минут в день начиная со стадии выделения и предпосевного развития мицелия, и на всех стадиях до развития грибного примордия, и далее проводится воздействие ЭМП с величиной индукции 100 мТл в течение 2-3 минут в день до сбора урожая. Было показано (Jamil, 2011), что такая последовательная обработка с низкой интенсивностью EMF в течение долгих периодов времени полезна на ранних стадиях до образования примордия, тогда как более интенсивное ЭПМ необходимо для вертикального развития карпофоров в течение коротких периодов времени. Такая обработка в некоторых случаях даже позволяет сократить время производства вдвое, увеличивая количество сборов.
Яичный порошок добавляют в субстрат в массовом отношении в количестве от 2 до 3% от сухой массы субстрата в контейнере, таким образом, чтобы капрофор выработал биологически активное количество эрготионеина. Эрготионеин стимулирует клеточную детоксикацию и антиоксидантно-воспалительный механизм.
Неорганические микроэлементы включают комплекс, выбираемый из группы, включающей соли селена, германия, цинка и меди, которые добавляют в массовом отношении от 1 до 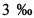 от сухой массы субстрата в контейнере. Неорганические микроэлементы важны для антиоксидантных, антидегеренативных и противоопухолевых свойств, так как они являются компонентами многих ферментно-витаминных комплексов и стимулируют активность иммунной системы против опухолей и других хронических дегенеративных заболеваний.
от сухой массы субстрата в контейнере. Неорганические микроэлементы важны для антиоксидантных, антидегеренативных и противоопухолевых свойств, так как они являются компонентами многих ферментно-витаминных комплексов и стимулируют активность иммунной системы против опухолей и других хронических дегенеративных заболеваний.
Пульсирующий свет стимулирует производство витамина D2; частота пульсации и продолжительность обработки может меняться в зависимости от вида грибов, с целью достижения количества 2000 ME витамина D2 на одну порцию в день свежих или высушенных грибов, что соответствует антидегенеративной и антинеопластический дозе, согласно сообщениям ряда авторов.
Настоящее изобретение также представляет контейнер для производства грибов, обогащенных биологически активными веществами, в форме продолговатой цилиндрической бутылки, изготовленной из пластического материала, и снабженной верхним горлышком с крышкой и дном с нижним горлышком с крышкой, при этом бутылка снабжена парой закрываемых патрубков для прохождения жидкости.
Упомянутые патрубки расположены вблизи как дна, так и горлышка, и повернуты в сторону дна и горлышка относительно продольной оси бутылки.
Разновидности грибов выбирают на основании как ранее продемонстрированной способности противодействовать неопластическим и дегенеративным заболеваниям, так и адаптивности к способу культивации, используемому в способе по настоящему изобретению, из группы, включающей следующие двадцать разновидностей: Pleurotus eryngii, Pleurotus ostreatus, Lentinus edodes "Shiitake", Flammulina velutipes, conical Morchella Parsons, Auricularia auricula-judae (L.:Fr.) Schroeter, Auricularia polytricha (Mont.) Sacc., Tremella fuciformis Berk. Brand, Agrocybe aegerita, Pholiota nameko, Hypsizygus tessulatus (Bull.) Singer, Hypsizygus ulmarius, Grifola frondosa "Maitake", Agaricus brasiliensis, Agaricus blazei Murrill, Ganoderma lucidum, Coriolus versicolor, Phellinus linteus, Hericium erinaceus, Poria cocos.
Кроме того, настоящее изобретение представляет способ применения грибов, обогащенных активными веществами и стандартизированных, в качестве пищи (новый пищевой продукт), как в свежем, так и в сушеном виде, в целом или измельченном виде, с целью предотвращения и лечения неопластических дегенеративных заболеваний, так как в дополнение к пищевой ценности они обладают функциональной активностью и терапевтическими свойствами. Эти грибы отличаются от обычных разновидностей латинским суффиксом officinalis (сокращенно off.), который добавляется к научному латинскому названию этих разновидностей.
На практике, одновременно с физической обработкой ЕМП различной интенсивности, некоторые минеральные вещества и неорганические микроэлементы, растворенные в воде, поступают в бутылку, в которой находится минимальное количество компоста в качестве твердого субстрата, предоставляя азот и углерод, с добавкой яичного порошка, в качестве источника цистеина, являющегося прекурсором конечного продукта эрготионеина. Твердый субстрат также содержит соли германия (растворимые германаты), селена (селенит натрия), цинка (гидроксид цинка), и меди (гидроксид меди) в концентрации 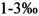 , которые вводятся в структуру гриба. Твердый субстрат, после посева в него мицелия, автоматически увлажняется водой. В компосте обычно присутствуют побочные продукты производства муки, отруби, солома, размолотые зерна, карбонат кальция и т.д., каждый из которых обладает таким соотношением углерода и азота (C/N), которое является оптимальным для культивации грибов. С добавлением яичного порошка содержание азота в компосте составляет от 1,8 до 2%. Сразу после сбора гриб подвергают облучению пульсирующим светом ксеноновой лампы для содействия производству эргокальциферола (витамина D2). Грибы, полученные таким образом, частично поступают в продажу в своей обычной форме, т.е. свежими, высушенными или лиофилизированными, и частично используются для приготовления пищевых добавок.
, которые вводятся в структуру гриба. Твердый субстрат, после посева в него мицелия, автоматически увлажняется водой. В компосте обычно присутствуют побочные продукты производства муки, отруби, солома, размолотые зерна, карбонат кальция и т.д., каждый из которых обладает таким соотношением углерода и азота (C/N), которое является оптимальным для культивации грибов. С добавлением яичного порошка содержание азота в компосте составляет от 1,8 до 2%. Сразу после сбора гриб подвергают облучению пульсирующим светом ксеноновой лампы для содействия производству эргокальциферола (витамина D2). Грибы, полученные таким образом, частично поступают в продажу в своей обычной форме, т.е. свежими, высушенными или лиофилизированными, и частично используются для приготовления пищевых добавок.
Конечные вещества, в качестве цели способа по настоящему изобретению, производят с помощью физических агентов, электромагнитных полей и пульсирующего света в случае витамина D2, или химических агентов, которыми могут быть органические прекурсоры, например аминокислота цистеин в случае эрготионеина, или минеральные неорганические прекурсоры (металлы и редкоземельные элементы), которые должны быть превращены в органические вещества посредством ферментативной каталитической активации, в форме коллоидных микроэлементов. Эти вещества были выбраны на основе тщательного анализа литературы как наиболее активные в грибах для предотвращения и лечения, в частности, неопластических и дегенеративных заболеваний в целом, и уже присутствуют в минимальных количествах в рассматриваемых грибах, из чего возникла идея их производства из прекурсоров и/или повышения концентрации последних до соответствующих уровней, характеризуемых терапевтическим действием при сохранении полной пищевой безопасности.
Эрготионеин - это аминокислота, обладающая существенной эффективностью в качестве антиоксиданта. Он производится исключительно в грибах путем декарбоксилирования гистидина с образованием цистеина, и его способность действовать в качестве антиоксиданта обусловлена наличием сульфгидрильной группы, которая быстро истощается при окислении из-за уникальности таутомерной структуры с периодом полужизни продолжительностью в один месяц, которая быстро переходит из окисленной в восстановленную форму не-ферментативным образом. В результате антиоксидантные свойства (цитопротекция) сохраняются до одного месяца, в отличие от других натуральных антиоксидантов, действующих до нескольких дней; прежде всего, особенно митохондриальная ДНК, в частности из клеток с низким или нулевым репликативным индексом, таких как нервные клетки, защищается от окислительного стресса и последующего повреждения. Эрготионеин обеспечивает цитопротекцию и стабильность клетки, особенно у клеток с одинаковым временем полужизни, таких как красные кровяные клетки, в которых он часто обнаруживается, а также в отношении нарушений, против которых он был предложен в качестве лекарства Hartmen et al., 1988; эрготионеин предохраняет другие антиоксиданты в организме, такие как глютатион, так он окисляется вместо них; он не метаболизируется ни в одной из тканей организма млекопитающих, однако у человека был обнаружены специфические внутриклеточные транспортеры. Присутствие и действие серы в SH группах придает эрготионеину, в дополнение к антиоксидантным свойствам, также противовоспалительные свойства, и трофическое и очищающее воздействие на соединительную ткань и ткани печени, с одновременной стимуляцией иммунной системы. Эрготионеин действует на уровне предотвращения вялотекущих хронических воспалений, которые сегодня считаются наиболее важной причиной возникновения дегенеративных (нейродегенеративных) и неопластических заболеваний. У него нет рекомендованной дневной дозы. Эрготионеин содержится во всех грибах, особенно в боровиках, и его содержание можно повысить добавлением к почве яичного порошка в количестве 1-3% от количества сухого растительного субстрата.
Действие и свойства добавок для почвы указаны ниже.
Антиоксидантные свойства: Se, эрготионеин, Ge
Локальные цитотоксические свойства: Ge
Антиоксидантные и противовоспалительные свойства: эрготионеин
Иммуностимуляторы: эрготионеин, Se, Ge, Z, Cu
Антипролиферативные / Про-дифференцирующие свойства: витамин D2
Цитопротекторные свойства: эрготионеин
Антианемические свойства: Cu
Антикахексионные свойства: Zn
Противоопухолевые свойства в отношении органов дыхательных путей: Ge
Поддержка тироидной функции: Se
Предотвращение опухолеобразования: Se, витамин D2, Zn
Антинейродегенеративные свойства: эрготионеин
Антибактериальные / антивирусные свойства: Cu
Кожные заболевания: эрготионеин, Se, Zn, витамин D2
Все дегенеративные заболевания начинаются с клеточной оксидации, когда она не контролируется различными антиоксидантными системами организма. Антиоксиданты, содержащиеся в пище, даже будучи принятыми в количестве, достаточном для запуска этих систем, например системы глютатиона, не могут противостоять этому процессу из-за их малого времени полужизни, составляющего от нескольких часов до нескольких дней, что часто недостаточно для восстановления нарушенной ферментативной системы, в частности в сильно нагруженных и интоксицированных органах, таких как страдающие хроническими заболеваниями. Есть только одно природное вещество в грибах, действие которого длится более 30 дней и которое окисляется вместо других клеточных антиоксидантных систем, защищая их. Этим веществом является эрготионеин, типичная аминокислота, содержащаяся в грибах.
Это вещество является самым лучшим из существующих природных антиоксидантов, так как оно доступно, производится из яичного порошка, и работает как начальная, первичная защитная система по улучшению работы клеточной структуры (INPUT), на которой основано действие всех других антиоксидантов и противовоспалительных веществ, особенно неорганических микроэлементов. Действие эрготионеина включает не только специфическое воздействие индивидуальных неорганических микроэлементов на соответствующие органы и функции, но также способствует общим физиологическим функциям организма с акцентом на иммунный ответ. Основа, закладываемая эрготионеином и неорганическими микроэлементами, подкрепляется витамином D2, который вводится с помощью пульсирующего света. Пульсирующий свет действует в дневной дозировке 2000 ME на неопластические /дегенеративные заболевания благодаря его клеточным антипролиферативным и продифференцирующим свойствам на конечный продукт (OUTPUT), оптимизируя жизненный цикл путем стабилизации ДНК. Также нельзя забывать, что производство эргостерола (стерольное ядро которого образует основу структуры витамина D2) также стимулируется пульсирующим светом, и эргостерол, согласно литературным источникам, также проявляет противоопухолевые свойства.
Таким образом, из лекарственных, или officinalis грибов согласно настоящему изобретению можно получить уникальный пищевой продукт, способный от начала до конца противодействовать неопластической трансформации и клеточной дегенерации благодаря его антиоксидантным, противовоспалительным, антипролиферативным/продифференцирующим стабилизирующим клеточную ДНК и иммуномодулирующим свойствам. Этот пищевой продукт реализовывает ранее известные противоопухолевые/антидегенеративные свойства ряда разновидностей грибов по настоящему изобретению, каковые возможности в значительной мере обеспечиваются полисахаридами (альфа и бета-глюкан) и гликопротеинами грибной клеточной структуры.
Способ включает метаболическое действие грибов, культивированных на субстратах, обогащенных яичным порошком, с целью преобразования прекурсора аминокислоты цистеина в грибную аминокислоту эрготионеин для стимуляции у человека механизма клеточной детоксикации, и антиоксидантного и противовоспалительного механизмов.
Способ включает трансформацию в грибах неорганических микроэлементов (Se, Ge, Cu, Zn), содержащихся в субстрате в форме солей, в органические соединения, с целью улучшения антиоксидантных, антидегенеративных и противоопухолевых свойств грибов, так как микроэлементы являются частью многих ферментно-витаминных комплексов и стимулируют работу иммунной системы против раковых заболеваний и других хронических дегенеративных заболеваний.
Подробное описание изобретения
В настоящем изобретении идентифицируется категория пищевых продуктов, обладающих противоопухолевыми и антидегенеративными свойствами, как на уровне предотвращения, так и в качестве пищевой добавки для людей, находящихся в зоне риска заболевания по наследственным или генетическим причинам, или уже страдающих от болезни, или рискующих заболеть повторно.
Эти пищевые продукты являются искусственно культивированными грибами, которые уже известны как обладающие некоторыми лечебными свойствами при неопластических и дегенеративных заболеваниях, а также стимулирующие иммунную систему. Эти грибы становятся функциональными, т.е. усиливают свои противоопухолевые свойства и лекарственные возможности, благодаря типичной способности грибов к биосинтезу новых соединений из прекурсоров или преобразованию минералов, металлов, редкоземельных элементов, добавленных в субстрат для роста, в органические соединения, что делает их биодоступными. Благодаря стандартизации и применяемой технологии, эти грибы подвергаются модификации, в результате которой улучаются их лекарственные свойства в качестве пищевого продукта, и они могут называться лекарственными или officinalis. Фактически, по аналогии с фармакопеей лекарственных растений, эти грибы проходят трансформацию в "почти медикамент" не в фармацевтической лаборатории, где выделяют активное вещество, а в технологической теплице в соответствии с физиологией их роста. Эта трансформация не изменяет природу исходного продукта, то есть гриба, но расширяет эффективность применения идентифицированной популяции, приводя к продукту, который является стандартизированным, биоактивным, безопасным и эффективным, а также полезным и питательным. Именно по этой причине лекарственные грибы являются пищевым продуктом, наиболее близким к концепции так называемых «нутрицевтиков», т.е. пищевых продуктов или их экстрактов, в которых польза от пищевой ценности комбинирована с лечебной пользой фармацевтического продукта. Можно сказать, что грибы становятся лекарственными в отношении определенных нутрицевтических свойств, происходящих от их биосинтетических способностей, усиливающих потенциальные возможности разновидности, с помощью контролируемых условий культивации; таким образом, лекарственные грибы могут считаться новым пищевым продуктом, пищевым продуктом с функциональной пищевой ценностью, усиливающей физиологические функции и возможности организма в борьбе против неопластических/дегенеративных заболеваний.
Культивацию можно осуществлять по модулярному принципу, так как она проводится в индивидуальных контейнерах, таких как бутылки, расположенные в высокотехнологичных теплицах, которые могут представлять собой приспособленные для этой цели грузовые контейнеры, оборудованные автоматической системой кондиционирования воздуха, которая управляется программным обеспечением для гарантии успешного производственного процесса.
Процесс производства, основанный на таких инструментах, как описанные ниже бутылки, а также на технологиях автоматизации, управляемых программным обеспечением, позволяют производить различные грибы со стандартизацией и наблюдением за измененными активными веществами.
Грибы не только пригодны в качестве пищевой добавки для этой категории пациентов, но они также легко усваиваются благодаря интеграции витаминов С и Е, и в случае критически больных пациентов, их можно принимать в качестве добавки в форме экстракта в капсулах или порошке, что многократно усиливает их терапевтический потенциал.
В частности, настоящее изобретение описывает компоненты, используемые для приготовления компоста, такие как: пшеничная солома, в чистом виде или в смеси с остатками от обработки дерева, обрезками веток, отрубями, опилками и т.д.; в компост важно добавлять карбонат кальция в количестве от 3 до 5% с целью поддержки оптимального значения рН для культивации растений. Мицелий, выращиваемый обычно на злаковых зернах, нуждается в отверстии в твердом субстрате для посева. В противоположность этому, при культивации на жидкой среде, мицелий можно вводить в компост с помощью шприца или инжектора. Во вторую очередь, в компост внутри контейнера можно добавлять смесь микроэлементов и солей, для обеспечения поддержки оптимального значения рН, что позволяет существенно упростить описываемый способ. Вначале вводится определенное количество минеральных микроэлементов, которое постепенно абсорбируется из мицелия в ходе роста в полипропиленовых бутылках, в соответствии с настоящим изобретением, тем самым сразу позволяя избежать проблем с изменением рН субстрата из-за полива, изменяющего почву. Некоторые соли, в улучшенном варианте данного способа, могут добавляться вместе с поливом. Что касается субстрата, который отличается в зависимости от разновидности грибов, то в качестве наиболее подходящего может быть выбран вариант описанный Tan et al., 2005, например состоящий из 72-73% опилок, 23-25% отрубей, 1% гипса, 1% суперфосфата кальция, с добавлением почвенных добавок в соответствии с настоящим изобретением. В любом случае, длинные компоненты должны быть измельчены до размера 2-3 см и затем перемешаны, и храниться при влажности 70% в специальном оборудовании, известном как кормораздатчик. Готовый субстрат подвергают обработке известными способами с нагреванием в автоклаве при температуре 110-120 С° в течение 1-2 часов или в печи при атмосферном давлении в течение нескольких часов в зависимости от достигнутой температуры, например 98 С°, и объема мешков.
Что касается производственного контейнера, он представляет собой бутылку из полипропилена, предпочтительно объемом 1 литр, с коротким горлом и широким отверстием, для развития грибов.
В отношении двадцати разновидностей грибов, ранее известных как обладающие научно доказанными антинеопластическими/антидегенеративными свойствами, была доказана их эффективность для применения согласно способу по настоящему изобретению: Pleurotus eryngii, Pleurotus ostreatus, Lentinus edodes "Shiitake", Flammulina velutipes, Morchella conica Parsons, Auricularia auricula-judae (L.:Fr.) Schroeter, Auricularia polytricha (Mont.) Sacc, Tremella fuciformis Berk. Brand, Agrocybe aegerita, Pholiota nameko, Hypsizygus tessulatus (Bull.) Singer, Hypsizygus ulmarius, Grifola frondosa "Maitake", Agaricus brasiliensis, Agaricus blazei Murrill, Ganoderma lucidum, Coriolus versicolor, Phellinus linteus, Hericium erinaceus, Poria cocos.
Pleurotus eryngii off.
Этому грибу будет уделено особое внимание, так как способ культивации в полипропиленовых контейнерах в теплицах начался с P. eryngii (Rodriguez-Estrada и Royse, 2005). Вид Pleurotus, далее обозначенный сокращением Р., который включает съедобные обычно культивируемые грибы с приятными органолептическими свойствами, имеет представляющие большой интерес питательные и функциональные качества. В частности, Pleurotus eryngii характеризуется высоким содержанием углеводов, белков и пищевых волокон, в дополнение к низкому содержанию липидов. Присутствуют все существенные аминокислоты с преимуществом глютамата, аспартата и аргинина, и лимитирующей кислотой является лейцин. Растворимые сахара, такие как галактоза, сорбитол и мальтоза, присутствуют в ограниченных количествах. Содержание натрия является особенно низким. По сообщениям в литературе, содержится существенное количество витаминов (С, А, В2, B1, D, и ниацина). Как у всех съедобных грибов, высокое содержание пищевых волокон и стеролов вместе с низким содержанием жиров, натрия и калорий, делает Pleurotus eryngii стратегическим пищевым продуктом для предотвращения сердечно-сосудистых заболеваний. Подтверждены свойства по снижению холестерина и уровня глюкозы в крови. Высокое содержание и разнообразие пищевых волокон может способствовать кишечному эубиозу. Белки этого гриба обладают хорошей биологической ценностью и более высоким содержанием белка (1,21 г /100 г массы свежего гриба) чем у P. ostreatus, Lentinus edodes и Flammulina velutipes. Минеральный состав показывает хорошее среднее содержание: особенно высокую концентрацию имеет цинк (89,3 мкг/г), медь (22 мкг/г), железо (29,3 мкг/г), натрий (240 мкг/г) (Rodriguez Estrada а.е., 2007) и т.д. Однако, практически отсутствует витамин D2, так же как и селен, но это возможно исправить с помощью способа по настоящему изобретению. Фактически, в природе абсорбция ионов металла у грибов меняется в зависимости от вида и экосистемы, в которой происходит развитие, в частности от кислотности и содержания органики в почве (Gast С.J., 1988). Как будет показано далее, мицелий штаммов различного происхождения способен к абсорбции жидкой синтетической среды, обогащенной несколькими неорганическими источниками селена (Na2SeO3, Na2SeO4 или SeO2) в различных концентрациях (Baeza А., 2000, 2002, Stajic М., 2006) и к накоплению, более чем любой другой гриб из проверенных, повышенных концентраций свинца в базидиоме (НН Dogan, 2006). Это позволяет P. eryngii служить не только прекрасным пищевым источником микроэлементов, но и эффективным индикатором загрязнения окружающей среды. Что касается фармакологических свойств, способность к снижению уровня холестерина обусловлена содержанием мевинолина (ловастатина), ингибитора гидроксиметилглутарил-кофермента А (HMG-CoA) редуктазы, содержащегося в хорошем количестве от 120,9 мг до 150 мг на килограмм сухой массы плодового тела (Chen SY, 2012). Работа Mizutani от 2008 г. является одним из исследований с целью оценки снижения постпрандиальной гипертриглицеридемии у двух групп пациентов из Японии (29 человек), получавших жирную пищу (40 г), при этом одна из двух групп получала P. eryngii; не говоря уже об эффекте снижения уровня глюкозы в крови (De Silva DD, 2012; Chen J., 2009; Kim JI, 2010). Волокна в форме полисахаридов (бета-глюканы), как растворимые, так и нерастворимые, такие как пре- и пробиотики, влияют на эубиоз кишечной микрофлоры (Synytsya А., 2009; Cheung PCK, 1998; Manzi Р., 2000) и также важны для иммунного ответа. Третичная спиральная конформация бета (1-3) глюканов считается важной для их иммуностимулирующей активности (Maeda YY, 1988), в особенности направленной против онкологических заболеваний. Например, производные плеурана, бета-глюкана, выделяемого из различных разновидностей Pleurotus, демонстрируют иммуномодуляторные и противоопухолевые свойства (Karacsonyi S., 1994; Paulik S., 1996; Rop О., 2009). Высокоразветвленные бета-глюканы из Pleurotus tuber-regium и их серосодержащие производные демонстрируют значительную противоопухолевую активность in vivo и in vitro (Tao Y., 2006). Некоторые альфа-глюканы, выделенные из мицелия гриба P. ostreatus, ингибируют пролиферацию клеток рака кишечника путем индукции апоптоза (Lavi I., 2006). Хлороформенный экстракт P. eryngii демонстрирует ингибиторный эффект на топомеразу ДНК млекопитающих; будучи очищен и идентифицирован как Убихинон-9, он способен ингибировать, индуцируя апоптоз, лейкемические клетки U937, но не нормальные фибробласты (Bae JS, 2009). Что касается противовоспалительных свойств, экстракт P. eryngii демонстрирует способность существенно подавлять дегрануляцию и высвобождение гистамина из лаброцитов, а также высвобождение и синтез IL-4, который является цитокином, способным индуцировать синтез IgE и развитие лаброцитов и активных сигнальных белков при аллергическом ответе, действуя на сигнальный механизм, работающий при посредничестве факторов транскрипции NFAT, NF-kB, API и рецептора FceRI (Nabeshima Y., 2005; Han EH, 2011; Jedinak A., 2011). Экстракт P. Eryngii успешно использовали при лечении экспериментального атопического дерматита на животной модели, вызванного динитрохлорбензолом (DNCB): ингибиторное действие на контактную аллергию по всей видимости осуществляется модуляцией Th1/Th2 ответа и уменьшением воспалительного инфильтрата в местах кожного поражения (Choi JH, 2013). В 2001, Wang et al. описали вещество с молекулярной массой 11,5 кДа которое назвали плеурерин, с протеазной активностью, способное оказывать ингибиторное действие на синтез белка, а также на обратную транскриптазу вируса ВИЧ-1. Те же авторы выделили пептид с противогрибковой активностью с молекулярной массой 10 кДа, названный ими эрингин, и термостабильную рибонуклеазу с молекулярной массой 10 кДа, обладающую противовирусной, иммуномодулирующей и антинеопластической активностью (Wang Н., 2001, 2004.). P. eryngii может играть важную роль в костном метаболизме: соединение, выделенное из базидиомы P. eryngii увеличивает щелочную фосфатазную активность остеобластов с повышенной генной экспрессией и секрецией остеопротегерина, и уменьшение ресорбционных областей костей (Kim SW, 2006). Ngai и Ng (2006) также выделили из базидиомы гемолизин под названием эрингеолизин, мономерный, с массой 17 кДа, обладающий цитотоксичностью в отношении клеток лейкемии и антибактериальной активностью против Bacillus spp, без противогрибкового эффекта (Ngai PHK, 2006). В заключение, антивирусный потенциал P. eryngii приписывается антителу xb68Ab (Fu М., 2003). Таким образом, действие Pleurotus eryngii является мощным и разнообразным, в спектре от диабета до гиперхолестеринемии, на сердечно-сосудистую систему и на метаболизм, но что самое интересное, это иммуномодуляторная и антивирусно-антинеопластическая активность, которая может быть усилена в отношении лекарственных грибов по способу в соответствии с настоящим изобретением, в частности активность в отношении стимуляции апоптоза клеток лейкемии и аденокарциномы кишечника.
Способ производства лекарственных грибов, в частности, применяется к Pleurotus eryngii. Продукт, получаемый согласно способу по настоящему изобретению, будет обозначаться как Pleurotus eryngii officinalis, сокращенно off. Особенное внимание уделяется субстрату, немного другому чем для других представителей Pleurotus, так как он созревает и стерилизуется отдельно, состоит из соломы и древесных отходов с добавлением опилок и смешивается в подходящих смесителях с карбонатом кальция с добавкой 5-10% муки из жмыха семян хлопчатника с целью стимуляции мицелия (Uppadhyay, 1991). Значение рН необходимо поддерживать между 4,5 и 6. Бутылка должна быть полной наполовину, в отличие от обычных 2/3, и немедленно после посева мицелия на субстрат вносятся добавки (Se, Ge, Cu, Zn в равных частях в количестве 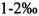 от сухой массы субстрата и при воздействии ЭМП малой мощности с величиной индукции 10-20 мТл в течение 10 минут в день), в течение первых двадцати дней температуру поддерживают на уровне 18 С° и затем повышают до 23 С° в последующие пятнадцать дней. Вовремя инкубации поддерживается относительная влажность от 60 до 70% и концентрация СО2 не более 3000 миллионных долей (ppm). В конце из каждой бутылки механически удаляется верхняя, самая старая часть субстрата, приблизительно 1-2 см. С целью поддержания надлежащего уровня увлажнения поверхности субстрата и благоприятствования образованию примордия, бутылку можно накрыть или перевернуть. Во время инкубации, мицелий постепенно распространяется по субстрату до тех пор, пока не проникнет в него глубоко, в форме милдью, которая обычно белого цвета.
от сухой массы субстрата и при воздействии ЭМП малой мощности с величиной индукции 10-20 мТл в течение 10 минут в день), в течение первых двадцати дней температуру поддерживают на уровне 18 С° и затем повышают до 23 С° в последующие пятнадцать дней. Вовремя инкубации поддерживается относительная влажность от 60 до 70% и концентрация СО2 не более 3000 миллионных долей (ppm). В конце из каждой бутылки механически удаляется верхняя, самая старая часть субстрата, приблизительно 1-2 см. С целью поддержания надлежащего уровня увлажнения поверхности субстрата и благоприятствования образованию примордия, бутылку можно накрыть или перевернуть. Во время инкубации, мицелий постепенно распространяется по субстрату до тех пор, пока не проникнет в него глубоко, в форме милдью, которая обычно белого цвета.
Затем после 35-го дня инкубации Pleurotus eryngii (в случае Pleurotus eryngii off. время инкубации уменьшается на 1/3 благодаря ЭМП), бутылки переносят в культивационные комнаты, где, после заполнения почвой до обычных 2/3 бутылки, их оставляют на 7-10 дней при температуре 14-15 С° и относительной влажности 80-90% при концентрации СО2 менее 2000 ppm и освещенности 50-200 люкс. Когда примордий начинает дифференцировать на поверхности субстрата, бутылки выравнивают и устанавливают следующие параметры окружающей среды: температура 16-18 С°, относительная влажность 75-90%, менее 1000 ppm СО2 и освещенность 50-500 люкс, и при ЭМП высокой интенсивности (100 мТл) в течение 5 минут в день. Через приблизительно 10-13 дней карпофоры готовы к сбору (в случае Pleurotus eryngii off. это время уменьшается на 1/3 благодаря ЭМП), после чего их подвергают продолжительной обработке пульсирующим светом для получения 2000 МЕ/день в свежей порции. Производство выражается в однократном сбором грибов. Биологическая производительность, являющаяся массовым отношением между свежими грибами и сухим субстратом, составляет более 70%. Трансформация P. eryngii в лечебные грибы имеет целью улучшение изначально существенных противоопухолевых и антиоксидантных свойств путем повышения содержания витамина D2 и селена, которых не хватает в исходных грибах, в частности с целью предотвращения заболеваний. Принимая во внимание хроническую дегенеративную природу других заболеваний, для которых он показан, а также особенно благоприятные вкусовые качества и питательность P. eryngii off. в качестве съедобного гриба, его можно рекомендовать для ежедневного приема для всех людей, особенно пожилых, и страдающих от хронических дегенеративных заболеваний, и особенно для уже заболевших, и тех, кто находится в зоне риска заболевания онкологическими заболеваниями повторно, или по врожденным или наследственным причинам.
Pleurotus ostreatus off.
Pleurotus ostreatus off является базидиомицетом, больше всего выращиваемым в мире, и почти самым популярным благодаря его вкусу и текстуре. Исследование показало, что многие другие типы грибов вида Pleurotus обладают более или менее схожим действием, даже если способность к росту в других внешних условиях и на других типах субстратов которая продемонстрирована на Pleurotus ostreatus (Р. о.) для понимания метаболизма, делает его грибом вида Pleurotus, обладающим наибольшим потенциалом для благотворных изменений согласно способу производства лекарственных грибов. С точки зрения питательной ценности, Р.о. содержит (относительно сухой массы): белки 10-30%, витамин С 30-144 мг/100 г, ниацин 109 мг/100 г, фолиевая кислота 65 мг/100 г, высокое содержание калия 306 мг/100 г. В частности, используют холестерин-понижающее действие Pleurotus ostreatus, проявляющееся благодаря молекуле со схожим с ловастатином действием (Gunde-Cimerman et al. 1993-1995). Так же, как и Pleurotus eryngii, Pleurotus ostreatus обладает способностью стимулировать иммунную систему и существенной противоопухолевой активностью. Было обнаружено, что благодаря белку и полисахариду, Pleurotus ostreatus может ингибировать развитие саркомы 180, индуктора мышиного рака, и может противодействовать раку простаты у человека (Zhuang et al., 1993; Zhang et al. 1994; Gu and Sivam, 2006). Исследования проводились на лабораторных животных на линиях опухолевых клеток, при этом нет информации о клинических исследованиях на людях. Таким образом, действие Pleurotus ostreatus off. на опухоли является общим действием на иммунную систему, и в частности может оказываться на рак простаты.
Способ культивации Pleurotus ostreatus off. намного проще, чем ранее упомянутого Pleurotus eryngii, с некоторыми предосторожностями: температура во время инкубации должна поддерживаться близко к 30 С° и понижаться до 25 С° через 35 дней, так как этот гриб хорошо растет даже при низких температурах. Во время производства влажность субстрата должна поддерживаться на уровне приблизительно 70-75% с влажностью воздуха приблизительно 95-98%, при оптимальной температуре для карпофоров 14-16 С°. Производство происходит в несколько периодов или сборов (2-3), отделенных один от другого промежутками в 10-20 дней, и заканчивается через 60 дней; в ходе производства в бутылке происходит только один сбор, но он быстрее благодаря ЭМП. Матрица субстрата должна быть богата целлюлозой и лигнином, а бедный субстрат имеет C/N соотношение равное 500. Можно использовать все элементы, упомянутые выше (мелко рубленная солома, опилки, отруби, и т.д.), но вещества, такие как нитрат аммония (2-3%), жмых соевых бобов (10%) и мука из люцерны (10%), с содержанием азота от 0,8 до 1,5% из яичного порошка, для этого вида грибов необходимо добавлять особым образом. С целью получения необходимого значения рН, 5-10% карбоната кальция смешивают с массой субстрата с оптимальным для культивации значением рН от 6 до 6,5. В соответствии с настоящим изобретением, субстрат обогащают 2-3% яичного порошка одновременно с облучением ЭМП малой мощности. Соли вводят в бутылку через 2-3 дня после посева мицелия и начала инкубации и, из-за низкой специфичности абсорбции отдельных микроэлементов, минеральные добавки вводят в количестве 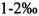 от сухой массы с эквивалентным содержанием каждого (Se, Ge, Cu, Zn) в 25%. Процесс производства проходит по стандартной процедуре (за исключением добавления почвы, как в случае Pleurotus eryngii), включая облучение ЭМП большой мощности и пульсирующим светом после сбора.
от сухой массы с эквивалентным содержанием каждого (Se, Ge, Cu, Zn) в 25%. Процесс производства проходит по стандартной процедуре (за исключением добавления почвы, как в случае Pleurotus eryngii), включая облучение ЭМП большой мощности и пульсирующим светом после сбора.
Благодаря высокому содержанию в грибе витамина С, трансформация в лекарственный гриб позволяет использовать антиоксидантный и иммуностимулирующий синергетический эффект благодаря микроэлементам, что расширяет его применение в случае многих дегенеративных заболеваний, как было ранее сказано в отношении Pleurotus eryngii. Еще один эффект заключается в том, что при соответствующей дозировке нет необходимости в дополнительном приеме витамина С (что делает гриб еще более эффективным против опухолей, на уровне фито-грибного комплекса). Также Pleurotus ostreatus обладает обычной усвояемостью и приятным вкусом, что делает возможным употребление этого гриба в пищу в больших количествах всеми людьми и в любое время.
Lentinus edodes off.
Lentinus edodes (шиитаке) является грибом, шире всего применяемым в медицине при лечении онкологических пациентов. Полисахарид лентинан является наиболее известным и применяется даже в фармацевтической форме в числе соединений с активностью модуляции биологического ответа (BRM). Этот глюкан является одним из компонентов грибной стенки и извлекается с высоким выходом из карпофоров, или из мицелия. Лентинан является высокомолекулярным полисахаридом, состоящим из мономеров глюкозы, соединенных вместе Beta-1,3 гликозидными связями, с наличием латерального разветвления В 1,6 каждые 5 линейных остатков (Aoki, 1984). Лентинан экстрагируют горячей водой (90-95 С°) в течение 12 часов и затем очищают. Лентинан обладает способностью восстанавливать или повышать возможности иммунной системы пациента, отвечать на пролиферацию, вызванную лимфокинами и цитокинами, дифференциацию и созревание таких лимфоцитов как В, Т и NK против вирусных патогенов и опухолей (Chihara, 1990). Водные экстракты L. edodes способны противодействовать пролиферации клеток саркомы 180 in vitro и in vivo (Chihara et al. 1969, Wasser and Weiss 1999 и т.д.). Suga et al. (1984) продемонстрировали способность лентинана предотвращать онкогенез и ингибировать образование метастазов (Suga et al., 1989). Прием лентинана также вызывает высвобождение клетками хозяина активных соединений, таких как фактор васкулярной дилатации (VDHF), интерлейкин 3 (IL-3), вместе с другими IL, и стимулирующий фактор клеточного роста (CSF). Эти молекулы могут взаимодействовать с лимфоцитами и другими клетками для стимуляции воспалительного и иммунного ответа (Maeda et al., 1984). Mizuno et al. в 1995 продемонстрировал in vivo связь с T, В и NK лимфоцитами. Макрофаги, активированные лентинаном, производят небольшие количества простагландинов IL-10 и IL-6, и CD4 Т лимфоциты усиливают производство IFN фактора и ослабляют IL-4. Далее макрофаги стимулируют производство оксида азота (NO). Пероральное введение лентинана in vivo вызывает у лабораторных мышей сильную противоопухолевую активность из-за повышения уровня различных лимфокинов (Yap and Ng, 2003). Другие исследования показали, что лентинан не только пригоден для лечения раковых опухолей, ассоциированных с обычным лечением (СНТ), но также защищает хромосомы от повреждений, вызываемых химиотерапией (Hasegawa et al., 1989) или микотоксинами (Ricordy et al., 2004). Также из карпофоров был выделен другой полисахарид, L-II, D-глюкопираноза, который стимулирует иммунную систему схожим с лентинаном образом (Zheng et al., 2005). Водной экстракцией из почвенного мицелия были получены смеси полисахаридов, называемые LEM, обладающие противоопухолевыми, иммуностимулирующими и антивирусными свойствами (Wasser and Weiss, 1999). Один из компонентов LEM, называемый ЕР-3, обладающий структурой, схожей с лигнином (одна молекула из группы, идентифицированная в грибе), способен ингибировать in vitro репликацию многих вирусов, включая ВИЧ (Jones, 1995). В мицелии также идентифицировали антиоксидантные соединения, такие как тиопролин, аминокислота-деактиватор нитритных радикалов, образующих нитрозамины, и другие экстракты, ингибирующие афлатоксины и микотоксины, участвующие в развитии некоторых форм опухолей (Fanelli et al., 2000, Ricelli et al., 2002, Reverberi et al., 2005). L. edodes содержит значительное количество эргостерола и витамина D2 и аминокислоты эритаденина, усиливающей метаболизм холестерина путем конверсии липопротеинов низкой плотности (LDL) в липопротеины высокой плотности (HDL). В популярной медицине предлагается прием маленькой чашки в день отжатого экстракта в холодной воде, полученного в течение ночи (10 свежих карпофоров или 10 г высушенных карпофоров в 600 г воды). Ввиду изначально сильного иммуностимулирующего действия благодаря содержанию лентинана, лечебная форма Lentinus edodes off. будет обладать еще более выраженным эффектом стимуляции иммунной системы. Таким образом, рекомендуется его применение в качестве иммуноадъюванта при химиотерапии, что уже практикуется в Японии, и/или при активной фазе злокачественных опухолей и неоплазии, затрагивающей иммунную систему, такой как лимфомы и лейкемии.
Состав шиитаке, по сравнению с P. Eryngii, характеризуется пониженным содержанием сухого вещества, средним содержанием белка, и низким содержанием других элементов, являющихся частью сухого вещества. Главные аминокислоты, такие как глютаминовая кислота, аспарагиновая кислота, аланин, лейцин и серии, находятся в белковой фракции. В усредненном составе, содержание сухого вещества составляет 7,66%, белка 21,73%, жиров 1,66%, волокон 6,12%, минералов 7,41%; содержание хитина мало (5,84%) но выше чем в P. ostreatus (4,86%) и P. eryngii (4,77%). Повышено содержание, в мг/кг сухого вещества (DM), меди (40,7), железа (40,6) и марганца (19,50), тогда как содержание калия, фосфора и алюминия понижено. Содержание витамина А (31,10 мкг/кг DM) эквивалентно его среднему содержанию в грибах, тогда как содержание витаминов B1, В2 и В6 является умеренным, что характерно для всех лесных грибов. Наблюдается хорошее содержание витамина С (94 мкг/кг DM), а также витаминов D2 и D3 (соответственно 90,5 и 200,5 мкг/кг DM) (Lelley and Vetter 2005).
В отношении производства, необходимо отметить следующие особенности:
1) Подготовка субстрата: используют свежие древесные опилки в смеси с остатками обработки злаков, кукурузы и др. Например, Stamets в 2000 описывает следующую формулу (древесные опилки твердых пород 52%, стружка 25%, рисовые или пшеничные отруби 20%, CaSO4 3%, влажность 60%), но опилки необходимо ферментировать при периодическом увлажнении и перемешивании, с контролем температуры, в течение нескольких месяцев для получения однородной массы и удаления летучих соединений, вредных для мицелия (Oei, 2003): затем в кормораздатчик необходимо добавить другие соединения при контролируемой влажности и значении рН (от 4,5 до 6). В конченой фазе перед помещением в бутылки субстрат необходимо смешать с яичным порошком (2-3%), уплотнить, измельчить, и простерилизовать в автоклаве на подходящих барабанах при температуре 121 С° в течение 2-3 часов (Choi 2005).
2) Посев, длится 2-4 недели: должен проводиться мицелием (2-3% от влажной массы субстрата), выращенным в основном на опилках, вводимым с помощью специального инжектора в верхнюю часть бутылки в полностью асептических условиях, при этом горлышко бутылки нужно оставить открытым. В этой фазе введение добавочных почвенных микроэлементов также должно производиться в равных количествах (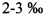 от сухой массы субстрата).
от сухой массы субстрата).
3) Инкубация, которая делится на четыре фазы:
a) Колонизация субстрата: мицелий внедряется в компост, температура которого поддерживается на уровне 25 С°, при слабом освещении или в темноте, и высокой влажности внутри бутылок (90-95%).
b) Формирование плектенхимы, продолжающееся 2-4 недели: мицелий, выросший с повышением СО2 организуется в подобий плотной белой ткани.
c) Формирование гломерулы, вызванной повышением уровня СО2 и температуры: мицелий образует маленькие кластеры гифы.
d) Бурое окрашивание, а именно дальнейшее утолщение пленки с приобретением плотной консистенции и красновато-коричневого цвета: уровень СО2 понижается и образуется примордий. Две последние фазы длятся 2-4 недели.
4) Примордий и развитие базидиомы. Для появления примордия необходимо изменение внешних условий. Температура нужно понизить ниже 20 С° и высокую относительную влажность (85-95%) необходимо поддерживать пониженной с помощью подходящей вентиляции. Уровень СО2 должен быть ниже 1000 ppm, также необходима освещенность в 500-2000 люкс (370-420 нм). Через 5-7 дней температуру необходимо повысить выше 20 С°, а уровень влажности установить между 60 и 80%. В период от 7 до 14 дня, грибы в первую очередь растут в высоту, после чего их шляпки темнеют и увеличиваются. Производительность колеблется от 15 до 35% от влажной массы субстрата (Oei, 2003) и с применением бутылок можно достичь двух сборов. Этот способ с использованием пластиковых бутылок применяется в Китае с 80-х годов (Fan et al. 2005). Процесс можно ускорить вдвое при условии тщательного отбора разновидности шиитаке и внимательной установке влажности, вентиляции и температуры в пределах альтернативных значений (15-20 С°), что позволяет сократить производственный цикл до приблизительно 3 месяцев; конечно, при условии использования при культивации автоматического оборудования и кондиционирования воздуха. Применение ЭМП (низкой интенсивности до образования примордия и затем высокой интенсивности) может дополнительно сократить продолжительность производственного цикла.
Lentinus edodes можно подвергнуть обработке согласно способу по настоящему изобретению и тем самым получить Lentinus edodes off. Последний намного более активен благодаря эрготионеину и минеральным добавкам, которых недостает в Lentinus edodes. Пациент может принимать его циклично в течение двух недель каждый месяц и затем заменить его другими грибами для интенсивной иммуностимуляции, которая не должна превышать пределы физиологических возможностей организма.
Flammulina velutipes off.
Интерес, возникший в Японии к свойствам грибов, который привел к интенсивному развитию потребления и применения в этой стране грибов в качестве функциональной пищи, в частности для предотвращения и лечения онкологических заболеваний, возник именно благодаря Flammulina velutipes (F.v.). Фактически было доказано, что в провинции Нагано в 70-х годах среди фермеров, производивших и употреблявших именно эти грибы, происходило меньше случаев заболевания раком желудка, чем у остального населения страны. Необходимо напомнить, что в это время (в 70-х годах) Япония являлась страной с наибольшим числом случаев заболевания раком желудка в мире. Ввиду серьезной эпидемиологической ситуации, органы здравоохранения Японии начали стимулировать потребление грибов, и последующее научное исследование выявило содержание в этих грибах полисахарида, названного "Flammulina velutipes полисахарид» (FVP), обладающего доказанным эффектом против саркомы 180 у мышей (Jiang et al., 1999), и в течение чуть более двадцати лет количество случаев заболевания раком желудка среди населения Японии снизилось до уровня показателей других индустриальных стран. Были также обнаружены другие иммуномодуляторные эффекты полисахаридов и белков, выделенных из F. velutipes (She et al., 1998, Wang Y.T. et al., 2004; Liao et al. 2006). В ходе других исследований в мицелии этих грибов были идентифицировано присутствие различных белков, способных ингибировать функцию рибосом, тем самым блокируя белковый синтез (Ng and Wang, 2004), предотвращать активность ангиотензина (Kim et al., 2002), ингибировать аллергические реакции на пищу у лабораторных мышей (Heish et al., 2003).
Этот гриб широко употребляют в пищу на Дальнем Востоке как в свежем виде, так и в качестве нутрицевтика, при этом на Западе его свойства неизвестны и в пищу его не употребляют, вероятно из-за малой плотности тела и маслянистой шляпки. Питательность гриба различается и сильно зависит от использованного для культивации субстрата, что делает F. velutipes одним из грибов с наиболее неожиданными результатами добавления в субстрат различных добавок; однако, содержание белков в необработанном грибе составляет от 17 до 31%, жиров от 1,9 до 5,8%, волокон 3,7%, минералов 7,4%.
Полисахариды F.v. являются компонентами, стимулирующими иммунитет, и их противоопухолевая активность была доказана; после трансформации в лечебную форму гриб можно использовать против любых солидных опухолей и в частности против рака желудка.
В отношении субстрата предпочтительным является использование грубых опилок от лиственных деревьев (дуба и бука), так как это повышает мягкость субстрата (80%) с последующей ферментацией, попеременно увлажняя и высушивая его в течение 4-5 недель. В опилки добавляют 20% рисовых отрубей и 1-3% СаСО3. Влажность регулируют в диапазоне 58-60% со значением рН равным 5-6 (Oei, 2003).
Можно выделить следующие фазы:
1) Упаковка и стерилизация. После тщательного смешивания субстрата с яичным порошком, который всегда добавляют в количестве 2-3% от сухого веса, субстрат помещают в полипропиленовые бутылки объемом 1000 мл с коротким и широким горлом. Затем бутылки закрывают крышками, снабженными фильтрами для газообмена, и отправляют на стерилизацию в автоклаве при температуре 121 С° в течение 1-2 часов.
2) Инокуляция и инкубация. Когда температура субстрата достигает 20 С°, его инокулируют мицелием, выращенным на опилках, с помощью известного приспособления, в количестве от 2 до 3% от его веса. Через день, согласно способу по настоящему изобретению, вносят минеральные добавки в той же пропорции (25% × 4) в количестве 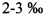 от сухой массы субстрата. Микроэлементы вводят в большем количестве для получения более значительного иммуностимулирующего эффекта, в комбинации с противоопухолевым полисахаридом. Применение ЭМП начинается в обычном режиме. Затем бутылки помещают на полки в обстановке пониженной освещенности при температуре 20-25 С°. Инкубационный период считается законченным, когда субстрат почти полностью покрывается мицелием, обычно через 20-30 дней (или меньше, при использовании ЭМП).
от сухой массы субстрата. Микроэлементы вводят в большем количестве для получения более значительного иммуностимулирующего эффекта, в комбинации с противоопухолевым полисахаридом. Применение ЭМП начинается в обычном режиме. Затем бутылки помещают на полки в обстановке пониженной освещенности при температуре 20-25 С°. Инкубационный период считается законченным, когда субстрат почти полностью покрывается мицелием, обычно через 20-30 дней (или меньше, при использовании ЭМП).
3) Производство. После инкубации бутылки помещают в производственную среду с контролируемой температурой, вентиляцией и влажностью. Здесь их открывают и удаляют верхнюю часть субстрата, где присутствует инокулят, для способствования компактному и равномерному образованию примордия. Температуру снижают до 10-12 С°, влажность до 80-85%, в отсутствии света и в атмосфере с высоким содержанием СО2 (2000-4000 ppm). В этих условиях через 10-14 дней примордий дифференцирует, и температуру снижают до 3-5 С° на период продолжительностью 5-7 дней для дальнейшего роста. После того, как размер стебля достигает приблизительно 2 см, температуру увеличивают до значения 5-8 С°, содержание СО2 поддерживают высоким, влажность на уровне 60-75%, при очень тусклом свете приблизительно 20-50 люкс. Когда карпофоры выступают над краем бутылки на 2-3 см, на бутылку надевают муфту в форме рукава. Муфта благоприятствует удлинению стеблей, их вертикальному положению, и накоплению СО2. Когда карпофоры достигают длины 13-14 см, они готовы к сбору, и затем обрабатываются пульсирующим светом. Обычно происходит два сбора общим количеством 160-220 г на бутылку (Oei, 2003). Так как F.v. является зимним грибом, параметры (температуру, влажность и содержание СО2) можно менять в сторону еще более низкой температуры (10-16 С°), высокой влажности (90-95%) и пониженного СО2 (0,2-0,4%), что делает возможным первый сбор уже через 5-8 дней.
Принимая во внимание невысокую плотность тела у F.v. с низким содержанием модификаторов биологического ответа (BRM) и микроэлементов, возможно что минеральные добавки в высокой концентрации, вместе с увеличением содержания витамина D, особенно повысят активность F.v. off., и будет возможно получить лекарственный гриб с важными и благоприятными свойствами. F.v. является легкоусвояемым грибом и его лекарственная форма допускает легкую абсорбцию BRM и микроэлементов, что позволяет использовать F.v. в качестве основного гриба для некоторых онкологических пациентов, так как его можно принимать ежедневно.
Morchella tapered off. (Parsons)
Morchella является аскомицетом, поэтому на первой стадии необходимо дополнительно сформировать склероций, представляющий собой вегетативную прорастающую форму. Будучи аскомицетом, Morchella развивается внутренне, во время первой фазы накопления питательных веществ (симбиотическая фаза) для образования проростков (склероция), на обычном субстрате из 70-80% растительных опилок, 20% рисовых, пшеничных или овсяных отрубей, и 2% СаСО3 для регулировки рН до значения 5,8-6,2. В субстрат необходимо добавить 2-3% яичного порошка. Аскомицеты немедленно засевают на этот субстрат; через 18-21 дней, склероций извлекают, промывают и помещают в бутылки с тонким слоем торфа поверх субстрата на 50% в присутствии минеральных добавок в обычных пропорциях (25% × 4) в количестве 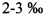 от сухой массы субстрата. В то же самое время начинают обработку ЭМП. Через 12-36 часов мицелий (сапрофитовая фаза) распространяется по бутылке. С этого момента начинается развитие гриба за счет склероция, он растет в высоту по направлению к источнику света, в подходящих условиях влажности и температуры, и развитие карпофора занимает 20-30 дней (вдвое меньше при условии применения ЭМП). Так как Morchella является аскомицетом, возможно что процедура обработки пульсирующим светом не приведет к желаемому результату в отношении витамина D2. Этот гриб является не самым простым для культивации, но при этом вкусным грибом со следующим содержанием компонентов: 20% белков, 4,8% жиров, 8,7% волокон, 64,4% углеводов.
от сухой массы субстрата. В то же самое время начинают обработку ЭМП. Через 12-36 часов мицелий (сапрофитовая фаза) распространяется по бутылке. С этого момента начинается развитие гриба за счет склероция, он растет в высоту по направлению к источнику света, в подходящих условиях влажности и температуры, и развитие карпофора занимает 20-30 дней (вдвое меньше при условии применения ЭМП). Так как Morchella является аскомицетом, возможно что процедура обработки пульсирующим светом не приведет к желаемому результату в отношении витамина D2. Этот гриб является не самым простым для культивации, но при этом вкусным грибом со следующим содержанием компонентов: 20% белков, 4,8% жиров, 8,7% волокон, 64,4% углеводов.
Спиртовые экстракты жидких культур мицелия Morchella esculenta продемонстрировали противовоспалительное, противоопухолевое и иммуностимулирующее действие (Nitha et al., 2006). В частности, эти грибы обладают способностью снижать избыток мочевой кислоты (противоподагрическое действие). Лекарственная форма может обладать активностью, упомянутой выше, в частности противовоспалительной; по этой причине яичный порошок добавляют в большем количестве.
Так как Morchella является грибом с низким содержанием микроэлементов и эргостерола, возможно что данная процедура приведет к появлению противоопухолевых свойств, в дополнение к уже имеющимся значительным противовоспалительным и урикозурическим свойствам. Morchella считается очень вкусным и легкоусвояемым грибом, и сохранит эти качества также и в лекарственной форме.
Auricularia auricula-judae off. (L.:Fr.) Schroeter
Auricularia polytricha off. (Mont) Sacc.
Культивация Auricularia началось на Востоке в 500-600 до нашей эры, где его ценили как за кулинарные, так и за терапевтические качества. Содержание питательных веществ следующее: 8-10% белков; 0,8-1,2% жиров; 4-7% минералов; 84-87% углеводов; 9-14% волокон. Следует отметить высокое содержание углеводов. Эти две разновидности грибов в сущности аналогичны по их культивации и свойствам.
Субстраты обычно содержат семена хлопчатника, зерновые, отруби или древесину лиственных деревьев; в целом, предпочтительны представители семейства Fagaceae.
Субстраты можно компостировать на несколько дней или использовать сразу после приготовления.
В обоих случаях их помещают в устойчивые к нагреванию полипропиленовые бутылки и стерилизуют в течение 60 минут при температуре 121 С°.
Состав компостированного субстрата следующий: опилки (78%), отруби (20%), СаСО3 (1%), сахароза (1%). Компоненты перемешивают, увлажняют и придают им форму копны, которую накрывают пластиковым листом и дважды перемешивают с интервалом в два дня.
Состав компостированного субстрата следующий: отходы семян хлопчатника (93%), пшеничные отруби (5%), сахароза (1%), СаСО3 (1%).
И в тот, и в другой добавляют яичный порошок (2-3% от сухой массы); также добавляют воду до влажности 60%, после чего субстрат помещают в термостойкий контейнер.
После остывания субстрата его инокулируют мицелием и инкубируют при температуре 25 С°±2 С° в течение 28-30 дней: после этого вводят минеральные добавки в равных частях (25% × 4) в количестве 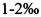 . Вскоре после этого применяют ЭМП низкой и высокой интенсивности.
. Вскоре после этого применяют ЭМП низкой и высокой интенсивности.
Более раннее образование примордия происходит при облучении во время инкубации светом более 500 люкс.
Auricularia является грибом, который подходит для трансформации в лечебный, за исключением образования витамина D, которое происходит очень слабо.
Он обладает антикоагулянтными свойствами, при этом полисахаридная фракция оказывает гипогликемический эффект на диабетических мышей (Yuan, 1998). Многие противоопухолевые свойства, продемонстрированные в отношении саркомы 180 (Kio, 1991) и карциномы Эрлиха (Ying, 1987), считаются обусловленными высоким содержанием полисахаридов. Из-за малого количества производимого витамина D необходимо, чтобы реализация противоопухолевых свойств проходила через иммунную стимуляцию с увеличенным количеством минеральных добавок и яичного порошка. Лекарственная форма, получаемая таким образом, сохраняет приятные вкусовые качества и показания к употреблению в пищу.
Tremella fuciformis off.
Tremella fuciformis является прекрасным съедобным грибом, который можно употреблять как в свежем, так и в высушенном виде, принимая дважды в день по 15 г (Hobbs, 2000). Этот гриб, помимо содержания многих витаминов и минералов, богат медью, потому что обладает способностью накапливать медь, извлеченную из субстрата для роста. Содержание питательных веществ в сухом веществе гриба составляет 4,6% белка, 0,2% жиров, 1,4% волокон и 0,4% минералов. В традиционной китайской медицине, возможно по этой причине, его используют для лечения геморроя и кровотечений всех типов; в Европе - против абсцессов, абдоминальных болей, сердечных заболеваний и заболеваний иммунной системы. Благодаря значительному содержанию аденозина, Tremella fuciformis используют при васкулярном тромбозе и в целом при лечении сердечно-сосудистых заболеваний, а также для снижения уровня липидов, в качестве антикоагулянта и средства против агрегации тромбоцитов. Описан антидиабетический эффект у лабораторных мышей (Yuan et al., 1998; Takeujchi et al., 2004). Также описаны противоопухолевые свойства (Misaki et al., 1981; Ukai et al. 1983) благодаря стимуляции лейкоцитов и сильному антагонистическому антиоксидантному действию на свободные радикалы посредством активации фермента супероксиддисмутаза (SOD) (Cu-Zn) в тканях печени и мозга. Этот гриб пригоден для применения при таких онкологических заболеваниях благодаря начальной концентрации меди (Cu) и цинка (Zn), внесенных в качестве добавок, с последующим добавлением к субстрату медь-содержащих минералов, благодаря чему возможна поддержка высокого уровня активации SOD, добавляющая антиоксидантные свойства и стимулирующая сопротивление иммунной системы онкологическим заболеваниям.
В природе Tremella fuciformis произрастает как сапрофит на многих деревьях твердых пород, особенно в регионах с тропическим и субтропическим климатом; его культивация не особенно распространена, однако встречается применение в кулинарных и лечебных целях.
Tremella fuciformis можно выращивать и на натуральных бревнах, однако очень распространена культивация на синтетической почве, инокулированой смешанной культурой, в состав которой также входит аскомицет Hypoxylon archeri, который часто ассоциируется в природе с разлагающейся древесиной. В состав субстрата входят растительные опилки (78%), рисовые отруби (20%) и СаСО3 (2%) для поддержания значения рН в интервале значений от 5,8 до 6,2, с добавлением яичного порошка (2-3% от сухой массы субстрата).
Hypoxylon archeri усиливает способность Т. fuciformis усваивать из субстрата питательные вещества, таким образом это положительно влияет на выход продукта. Субстрат с внесенными в него добавками помещают в бутылки с открытым верхним отверстием, накрытым газопроницаемой тканью. Субстрат стерилизуют, охлажают и инокулируют смешанной культурой, а также минеральными добавками в количестве 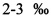 от сухой массы субстрата в бутылке, с соотношением микроэлементов, составленным в пользу Zn и Cu, которые составляют 70% от всех минеральных добавок. Если необходимо, бутылкам обеспечивают вентиляцию посредством открытия нижнего отверстия. Воздействие ЭМП применяют в количестве согласно способу по настоящему изобретению.
от сухой массы субстрата в бутылке, с соотношением микроэлементов, составленным в пользу Zn и Cu, которые составляют 70% от всех минеральных добавок. Если необходимо, бутылкам обеспечивают вентиляцию посредством открытия нижнего отверстия. Воздействие ЭМП применяют в количестве согласно способу по настоящему изобретению.
Через приблизительно 30 дней вегетативного роста при оптимальной температуре 25-28 С° и высокой влажности (85-95%), субстрату создают условия, благоприятные для развития примордия. Эти условия заключаются в пониженной температуре и влажности, и увеличенном поступлении воздуха и света (температура 20-25 С°, влажность 80-85%). Грибы собирают через 35-40 дней после инокуляции, когда они дорастают до диаметра 10-15. С применением ЭМП время сокращается приблизительно на 1/3. Пульсирующий свет не вызывает заметного увеличения содержания витамина D2 для этого типа гриба (аскомицет).
У необработанных грибов свежие карпофоры обладают очень высоким содержанием воды (92-94%), и низким содержанием витаминов и минеральных элементов (Chang and Hayes, 1978). В случае лекарственного гриба ситуация противоположная - хотя содержание воды остается высоким, грибы обогащены внесенными микроэлементами, особенно ионами Zn и Cu для влияния на иммунную систему.
Лекарственные свойства этого гриба обусловлены высоким содержанием полисахаридов, в частности гетерокислотного полисахарида под названием глюкуроноксиломаннан. Этот полисахарид проявляет иммуномодуляторную и противоопухолевую активность: клинические исследования показали, что этот гриб эффективен для контроля лейкопении во время химиотерапии и радиационной терапии (Smith, Rowan and Sullivan, 2002). В частности, стимулируется производство интерлейкинов (Ukai et al., 1972, Misaki and Kakatura 1995). Известный трофический эффект в отношении кожи, из-за которого Tremella fuciformis издавна используют в дальневосточной медицине, возникает благодаря защите васкулярных эндотелиальных клеток от радиации, а также стимуляции эматогенеза, при этом и то, и другое используют во время химиотерапии и радиационной терапии (Stamets 2000). Лекарственная форма стимулирует уже имеющийся эффект влияния на иммунную систему, работающий при посредничестве лейкоцитов и интерлейкинов посредством эрготионеин-микроэлементного комплекса (Zn+Cu).
Agrocybe aegerita off.
Agrocybe aegerita является одним из самых популярных грибов благодаря своему вкусу, и самым выращиваемым грибом в мире. Обычно он известен как опенок, и относится к сапрофитным грибам. Этот гриб содержит в своем составе значительное количество витаминов, в частности витамин D, и микроэлементов.
Очень простая методика культивации практически аналогична таковой для ранее упомянутого Pleurotus, и включает стерилизацию субстрата в полипропиленовых бутылках в автоклаве при температуре 121 С° в течение 2 часов.
Субстрат такой же, как для Pleurotus, содержащий 70-80% пшеничной соломы, 10% пшеничных отрубей, 2% СаСО3, 2% нитрата аммония, 8-10% люцерновой муки; в эту смесь добавляют яичный порошок в количестве 2-3% от сухой массы субстрата.
После стерилизации бутылки населяют мицелием, выращенным на зерновках зерновых культур, и на следующий день добавляют минеральные добавки в количестве 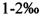 и в сбалансированной пропорции 25% × 4 микроэлемента. Затем субстрат подвергают действию ЭМП в соответствии со способом по настоящему изобретению и инкубируют в темноте, в вентилируемой среде, при температуре 25 С° в течение 3 недель. Важно соблюдать относительную влажность 70%.
и в сбалансированной пропорции 25% × 4 микроэлемента. Затем субстрат подвергают действию ЭМП в соответствии со способом по настоящему изобретению и инкубируют в темноте, в вентилируемой среде, при температуре 25 С° в течение 3 недель. Важно соблюдать относительную влажность 70%.
В начале четверной недели, для плодоношения температуру понижают до 13-18 С° при 90-95% влажности воздуха, при этом уровень СО2 должен быть менее 1500 ppm и необходимо соблюдать 12-часовой световой цикл с освещенностью 500-1000 люкс. Через приблизительно 30-35 дней после инокуляции появляется примордий, который будет готов к сбору через несколько дней. Время цикла сокращается на 50% при использовании ЭМП. С изначально хорошим содержанием витамина D2, процесс обогащения с применением пульсирующего света позволяет достичь желаемого содержания 2000 ME на свежую порцию в день.
До недавнего времени A. aegerita считался грибом с незначительными лекарственными свойствами, но последние исследования показали присутствие в нем лектина тереина. Пектины представляют собой класс белков, способных к связыванию карбоксильных доменов гликопротеинов, принимающих участие в механизме иммунного ответа, а также в распознавании групп крови и удалении токсичных гликопротеинов из кровотока; A. aegerita обладает противоопухолевыми и антивирусными свойствами, продемонстрированными в отношении растительных вирусов, называемых AAL (Zhao et al., 2003, Yang et al. 2005). Противоопухолевое действие обусловлено стимуляцией иммунной системы хозяина и в частности стимуляцией факторов некроза опухоли (TNF) и интерлейкина-1 бета (Wang et al., 2004, Yang et al., 2005). Обогащение, достигаемое в лекарственных грибах, обеспечивает эффект в отношении всех опухолей посредством усиления иммунного ответа, являющегося результатом действия антипролиферативного витамина D, при сохранении хорошей усвояемости и вкуса гриба, что делает его одним из тех лекарственных грибов, которые можно длительно употреблять любым пациентам.
Pholiota nameko off.
Pholiota nameko off. является грибом прекрасного качества, относящимся к семейству Strophariacee, высоко ценимым на Дальнем Востоке, но неизвестным на Западе, где к нему не возникло интереса, возможно по причине его вязкости. Этот гриб употребляют в пищу в свежем или консервированном виде.
Это очень интересный по составу гриб. Фактически, сухая субстанция содержит 20,8% белка, 4,2% жиров, 66,7% углеводов, 8,3% минералов и 6,3% волокон. Содержание витаминов, выраженное в миллиграммах на 100 г сухого вещества, впечатляет: тиамин (18,8), рибофлавин (14,6) и ниацин (72,9). Основными минеральными элементами являются кальций, калий и железо (Stamets 2000). Богатство и полнота указанных компонентов, особенно серосодержащих аминокислот, делает этот гриб одним из тех, для которых улучшение состава может иметь наиболее неожиданный и привлекательный эффект, особенно введение эрготионеина.
Техника культивации аналогична таковой для Flammulina velutipes. Одним из наиболее широко используемых субстратов является содержащий опилки и стружки (52% и 25% соответственно) подходящих деревьев, пшеничные или рисовые отруби (20%) и сульфат кальция (3%), с влажностью на уровне 70%, перемешанный и с добавлением яичного порошка со значительным изменением в сравнении с предыдущими грибами. Яичный порошок используют в количестве 4-5% от сухой массы субстрата. Это делается с целью преобразования Pholiota патеко в гриб с наиболее выдающимися лекарственными свойствами, особенно включая способность к детоксикации, а также противовоспалительные и антиоксидантные свойства благодаря эрготионеину, который усиливает антиинфекционные качества исходного гриба. После помещения в бутылки, согласно настоящему изобретению, и стерилизации субстрата, производится посев мицелия, выращенного на пшеничной зерновке, и днем позже вносятся минеральные добавки в количестве 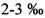 с равным соотношением компонентов (25% × 4). Затем, после применения ЭМП согласно способу по настоящему изобретению, инкубация продолжается в темноте в течение приблизительно 2-3 недель при температуре 25-28 С°. На стадии роста бутылки открывают, поддерживая высокую относительную влажность (98%) и понижая температуру до 10-15 С° для осенних сортов, и до 18-22 С° для весенних сортов, при интенсивности освещения 300-1000 люкс (Demas, 1989). Приблизительно через неделю появляется примордий, и через несколько дней он готов к сбору, при этом указанные сроки сокращаются в случае применения ЭМП. Второй сбор возможен при выскребании горлышка, возможном внесении частично пористой мембраны, переворачивания бутылки после удаления нижней пробки, и использования второго отвода для поливки. В таком случае возможно получение продукта в количестве 30% от массы субстрата.
с равным соотношением компонентов (25% × 4). Затем, после применения ЭМП согласно способу по настоящему изобретению, инкубация продолжается в темноте в течение приблизительно 2-3 недель при температуре 25-28 С°. На стадии роста бутылки открывают, поддерживая высокую относительную влажность (98%) и понижая температуру до 10-15 С° для осенних сортов, и до 18-22 С° для весенних сортов, при интенсивности освещения 300-1000 люкс (Demas, 1989). Приблизительно через неделю появляется примордий, и через несколько дней он готов к сбору, при этом указанные сроки сокращаются в случае применения ЭМП. Второй сбор возможен при выскребании горлышка, возможном внесении частично пористой мембраны, переворачивания бутылки после удаления нижней пробки, и использования второго отвода для поливки. В таком случае возможно получение продукта в количестве 30% от массы субстрата.
Некоторые авторы (Bianco Colletto, 1981) сообщают об антибиотических свойствах в отношении Bacillus subtilis и других бактерий. Stamets в 2000 г. показал, что некоторые китайские авторы получили данные об антибиотическом эффекте в отношении бактерий штамма Staphylococcus и о противоопухолевой активности в отношении саркомы 180 у мышей.
При трансформации в лекарственный гриб, как уже указывалось, благодаря эрготионеину добавляются противовоспалительные, антиоксидантные и детоксикационные свойства, с возможными показаниями против онкологических заболеваний, вызванных воздействием окружающей среды или производственным химическим воздействием с сопутствующей интоксикацией и дегенерацией печени, в также против некоторых онкологических заболеваний мочевого пузыря, печени и носоглотки.
Hypsizygus tessulatus off. (Bull.) Singer Hypsizygus ulmarius off. (Bull.) Redhead
Это группа хорошо известных грибов, ценимых на Дальнем Востоке, в частности выращиваемых в Японии, очень похожих по способу культивации на вид Pleurotus. Они принадлежат к семейству Tricholomatacee. Эти грибы обладают схожими характеристиками, что также относится к культивации, и употребляются в пищу в свежем или сушеном виде, или в форме порошка. Подробная информация по составу отсутствует.
В Японии эти грибы культивируют в полипропиленовых бутылках. Субстрат по своему составу схож с другими составами для древесных грибов: 52% опилок, 25% стружки, 20% пшеничных отрубей, 3% СаСО3. Смесь увлажняют до уровня 63/65% и смешивают с 2-3% яичного порошка.
Согласно настоящему изобретению, бутылки наполняют механическим способом. Субстрат спрессован, и в дне бутылки находится отверстие, в которое засевают мицелий. На следующий день в то же отверстие, но выше, помещают минеральные добавки в количестве 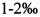 с равным соотношением четырех микроэлементов; сразу после этого субстрат подвергают действию ЭМП. Инкубация Н. tessulatus проходит в темном помещении при температуре 20-25 С° в течение приблизительно 30-45 дней. После этого бутылки открывают и способствуют образованию примордия путем соскребания поверхности субстрата, понижении температуры до 10-15 С°, при относительно высокой относительной влажности (98-100%), при концентрации СО2 менее 0,1% и освещенности 500-1000 люкс, в течение приблизительно 7-12 дней. После этого температуру повышают до 13-18 С°, относительную влажность немного снижают, а концентрацию СО2 повышают до 0,2-0,4%. Как и в случае Flammulina v., с целью способствовать развитию длинных стеблей, на горлышки бутылок надевают манжет размером 7-8 см. Производство проходит с двумя сборами в количестве
с равным соотношением четырех микроэлементов; сразу после этого субстрат подвергают действию ЭМП. Инкубация Н. tessulatus проходит в темном помещении при температуре 20-25 С° в течение приблизительно 30-45 дней. После этого бутылки открывают и способствуют образованию примордия путем соскребания поверхности субстрата, понижении температуры до 10-15 С°, при относительно высокой относительной влажности (98-100%), при концентрации СО2 менее 0,1% и освещенности 500-1000 люкс, в течение приблизительно 7-12 дней. После этого температуру повышают до 13-18 С°, относительную влажность немного снижают, а концентрацию СО2 повышают до 0,2-0,4%. Как и в случае Flammulina v., с целью способствовать развитию длинных стеблей, на горлышки бутылок надевают манжет размером 7-8 см. Производство проходит с двумя сборами в количестве 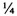 от массы субстрата (Stamets 2000) и может быть ускорено при применении ЭМП. При культивации Н. ulmarius, если не использовать воротник, происходит преимущественное образование шляпки. Это образование обычно обратно пропорционально длине стеблей, что приводит к образованию более коротких, приземистых и мясистых стеблей с более широкими шляпками. Таким образом, органолептические свойства Н. ulmarius становятся лучше, и здоровые экземпляры остаются по существу неизменными.
от массы субстрата (Stamets 2000) и может быть ускорено при применении ЭМП. При культивации Н. ulmarius, если не использовать воротник, происходит преимущественное образование шляпки. Это образование обычно обратно пропорционально длине стеблей, что приводит к образованию более коротких, приземистых и мясистых стеблей с более широкими шляпками. Таким образом, органолептические свойства Н. ulmarius становятся лучше, и здоровые экземпляры остаются по существу неизменными.
Эта разновидность относится к виду Pleurotus, которые имеют некоторые общие свойства (см. P. ostreatus). Stamets (2000) обнародовал японские исследования, касающиеся сильных противоопухолевых свойств этих грибов. В некоторых исследованиях сообщается о технологии гибридизации между Hypsizygus и Laetiporus sulphureus для производства медикаментов против тромбоза (Okamura et al., 2000).
В отношении противоопухолевой терапевтической стратегии применения лекарственных грибов, можно сделать ссылку на сказанное в отношении P. ostreatus.
В частности, целью является придание грибу антиоксидантных, противовоспалительных и детоксикационных свойств благодаря эрготионеину, производимому в хорошем количестве.
Grifola frondosa off. "Maitake"
Этот гриб является самым важным съедобным и наиболее хорошо исследованным грибом в отношении его лекарственного действия на онкологические заболевания. Он является важным и широко распространенным в мире грибом благодаря своим органолептическим качествам, которые стоят на первом месте перед лекарственными, хотя последние также важны. Способы культивации, разработанные в Японии в конце 80-х годов, наряду с результатами исследований, проведенных в мире в отношении его противоопухолевых качеств и соответствующей пользы, внесли свой вклад в быстрое завоевание этим грибом успеха на мировых рынках в качестве как пищевого продукта, так и нутрицевтика.
Grifola frondosa off. "Maitake" имеет уникальные свойства состава, такие как содержание влаги (80%), которое ниже чем у большинства других грибов (90%). Содержание белка очень высоко, почти 27% сухого вещества, а углеводов - около 50%. Содержание витаминов в процентах от массы сухого вещества составляет 1,5 мг витамина В1, 1,6 мг витамина В2, 54 мг ниацина, 63 мг витамина С и 410 ME витамина D (что достигает рекомендованной дневной дозы согласно ВОЗ). Содержание минералов и металлов составляет: магний 67 мг %, железо 0,5 мг %, кальций 11 мг % и фосфор 425 мг % (Stamets and Chilton, 1983).
Технология культивации включает стерилизацию субстрата в полипропиленовых бутылках. Состав используемого субстрата соответствует таковому для древесных грибов: опилки 52%, стружка 25%, пшеничные отруби 20%, карбонат или сульфат кальция 3%. Влажность повышают до 60-65%, а значение рН до 5,5-6,5. Яичный порошок добавляют в количестве 2-3% от сухой массы смеси. Более крупные элементы, такие как щепки, необходимы для поддержания мягкости и аэрации смеси. Субстрат, находящийся в бутылках, после стерилизации в автоклаве засевают мицелием, выращенным на пшеничных или пшенных зернах. На следующий день в бутылку на относительно большом расстоянии от мицелия вносят минеральные добавки (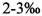 от сухой массы субстрата, в тех же пропорциях). Сразу после этого применяют обработку ЭМП в обычном режиме. Инкубация и появление примордия происходит в закрытых контейнерах в темных или слабоосвещенных помещениях, при температуре 20-25 С° в присутствии в бутылке СО2 с высокой концентрацией (20000-40000 ppm). Через приблизительно 30-40 дней мицелий колонизирует весь субстрат, на поверхности появляется желтоватый экссудат и утолщение мицелия, и еще через 10-12 дней появляется примордий в форме маленьких сероватых образований 2,5-6 см в диаметре. Контейнер оставляют закрытым еще 2-3 дня, потом открывают верх бутылки, понижают температуру до 16-18 С°, относительную влажность поддерживают в пределах 80-95%, освещенность на уровне 200-500 люкс, уровень СО2 не более 0,1%. Через 18-25 дней карпофоры готовы к сбору (это время может быть меньше при использовании ЭМП). Количество продукта составляет 1/4 массы субстрата. Обработка пульсирующим светом немедленно приводит к ожидаемому результату (2000 ME на порцию свежих грибов в день), при условии достаточного количества в необработанных грибах.
от сухой массы субстрата, в тех же пропорциях). Сразу после этого применяют обработку ЭМП в обычном режиме. Инкубация и появление примордия происходит в закрытых контейнерах в темных или слабоосвещенных помещениях, при температуре 20-25 С° в присутствии в бутылке СО2 с высокой концентрацией (20000-40000 ppm). Через приблизительно 30-40 дней мицелий колонизирует весь субстрат, на поверхности появляется желтоватый экссудат и утолщение мицелия, и еще через 10-12 дней появляется примордий в форме маленьких сероватых образований 2,5-6 см в диаметре. Контейнер оставляют закрытым еще 2-3 дня, потом открывают верх бутылки, понижают температуру до 16-18 С°, относительную влажность поддерживают в пределах 80-95%, освещенность на уровне 200-500 люкс, уровень СО2 не более 0,1%. Через 18-25 дней карпофоры готовы к сбору (это время может быть меньше при использовании ЭМП). Количество продукта составляет 1/4 массы субстрата. Обработка пульсирующим светом немедленно приводит к ожидаемому результату (2000 ME на порцию свежих грибов в день), при условии достаточного количества в необработанных грибах.
Grifola frondosa является одним из наиболее хорошо исследованных грибов в отношении его лекарственных свойств. Из него производят вещества с противоопухолевым, антивирусным, антибактериальным, противогрибковым, иммуностимуляторным, гепатопротекторным, антидиабетическим и противогипертоническим эффектом (Wasser and Weiss, 1999; Hobbs, 2000; Maywell, 2001). Было показано, что экстракты G. frondosa в отношении некоторых свободных радикалов демонстрируют прямой антиоксидантный эффект (Май, 2004), который связан с содержанием фенола в мицелии. Однако, наиболее изученными соединениями являются бета глюканы (бета 1-3 и бета глюкан 1-6), которые в избытке содержатся в мицелии и плодовом теле (Hobbs, 2000; Reshetnikof et al. 2001). Есть четкие данные о том, что условия культивации и качество субстрата очень сильно влияют на количество и состав полисахаридов (Ohno et al., 1985, 1986 Mizuno and Zhuang, 1995). В целом, лучший терапевтический эффект достигается у экстрактов плодового тела, в котором содержится больше бета-гликанов, чем в мицелии (Minato et al., 2001, Reshetnikof et al. 2001). Модификации субстрата в соответствии с настоящим изобретением, имеющие целью повысить содержание минералов, микроэлементов, аминокислот, витамина D (эрготионеина) и белков, могут влиять на количество и качество бета-глюканов в продукте, достигая мощного действия бета-глюканов в качестве фракции Maitake D и MD, присутствующих в очищенных активных экстрактах против опухолей, начиная с приема ежедневной дозы лекарственных грибов. Среди прочего, Grifola frondosa является одним из наиболее хорошо усвояемых и гипоаллергенных грибов на рынке. Его можно употреблять свежим, высушенным, или законсервированным в масле.
К настоящему времени охарактеризовано 29 различных фракций экстрактов плодовых тел G. frondosa, и 28 из них признаны BRM-активными (Mizuno et al., 1986, Zhuang et al., 1994). Выделенные бета глюканы отличаются по составу и структуре полисахаридной цепи; некоторые являются гликопротеинами, другие лишены белкового компонента, но все они в той или иной степени подвержены влиянию условий экстракции и применяемым технологическим процедурам. По этой причине грибы in toto употребляемые в качестве пищи, являются лучшей формой приема таких BRM. Однако, нельзя не упомянуть фракцию D (главная цепь с бета-связями 1-3 и бета-разветвлением 1-6), которая in vitro демонстрирует противоопухолевый эффект против саркомы 180 у мышей и против рака простаты (Mizuno et al., 1986; Kurashige et al., 1997; Konno et al., 2002) и прямой цитотоксический эффект на клетки рака простаты, в дополнение к раннему стимулирующему эффекту на NK лимфоциты и более продолжительный ингибиторный эффект по причине высвобождения факторов IL-12 из макрофагов (Kodama et al., 2002, 2004), ответственных за уничтожение клеток опухоли. Недавно была выделена другая более чистая фракция D, т.е. MD фракция, при введении животным она оказывает более сильный противоопухолевый эффект, чем фракция D (Maywell, 2001). Пероральный прием MD фракции привел к хорошим результатам регрессии опухолей (Kodama et al., 2002) в исследовании в Японии, в котором участвовали 160 человек, страдающих раком легких, груди и печени в поздних стадиях (III-IV); наблюдалась существенная регрессия опухолей и/или улучшение симптомов в 50-80% случаев рака груди и рака легких, тогда как другие исследования показали, что почти в 80% случаев улучшилось общее состояние; наблюдалось облегчение последствий химиотерапии (СНТ), и в той же степени (83%) наблюдалось улучшение болевых симптомов. Также исследовали применение Grifola frondosa для предотвращения метастазирования опухолей. Клетки гепатокарциномы ММ-164 вводили трем группам мышей: первая группа получала с пищей 20% порошка G. frondosa, вторая группа получала фракцию D в количестве 1 мг/кг и контрольная группа получала обычную пищу. Через 30 дней измерили количество метастазов в печени; метастазирование в печени было ингибировано на 91,3% в случае приема фракции D, и на 81,3% в случае приема порошка грибов. Следует отметить прекрасный результат в случае порошка грибов, содержащего намного меньше фракции D, что позволило предположить, что ежедневный прием с пищей этих грибов может снизить риск метастазирования на 80-90%. Заметный эффект иммунной стимуляции был описан для полисахарид-гликопротеинового экстракта (гетерогликан, связанный с белками) grifolano МТ-2 (1-3 бета глюкан с разветвлением 1-6) который активирует NK и Т лимфоциты и способствует высвобождению интерлейкина-1 и супероксид аниона макрофагами (Adachi et al., 1987; Zhuang et al., 1993). Другой вариант, D-Grifolan, изучали на клеточной линии гормонально независимого рака простаты (Fullerton et al., 2000). В течение 24 часов была достигнута почти полная смерть неопластических клеток (более 95%) при дозе 500 мг/мл D-Gryphon. Ассоциация с витамином С (200 мг/мл) позволила значительно уменьшить количество D-Grifon (30-60 мг/мл), с сохранением такой же эффективности. По этой причине в сочетании с грибом рекомендуется прием витамина С, потому что он действует синергетически, способствуя апоптозу клеток опухоли из-за повреждений от окислительного стресса.
Такое про-апоптическое действие, которое относится ко всем лекарственным грибам в области онкологии, в частности к лекарственным грибам по данному изобретению, соединяет иммуностимуляторное действие бета-глюканов с антиоксидантным действием витамина С.Упомянутое действие осуществляется также при посредничестве ингибирования глиоксалазы I, фермента жизненно важной детоксикации клетки. Блокировка этого фермента приводит к накоплению метилглиоксаля, который оказывает цитотоксический эффект в частности на опухолевые клетки, которые обычно используют путь анаэробного гликолиза для производства энергии. Конечным эффектом при этом является блокировка клеточного метаболизма и гибель неопластических клеток, которые с биохимической точки зрения являются более хрупкими, чем нормальные клетки, которые фактически не затрагиваются этой метаболической блокировкой. Дозировка витамина С совершенно сравнима с указанной Linus Pauling и по этой причине является полностью включенной в способ получения лекарственных грибов. Рекомендуется ежедневный прием добавки витамина С из натуральных источников (шиповника, и т.д.) в количестве от 300 мг до 3 г в зависимости от степени тяжести неопластического заболевания.
Другое соединение, N-ацетилгалактозамин-лектин (GFL), демонстрирует цитотоксичность по отношению к клеткам HeLa (опухолевая линия клеток шейки матки человека, используемая для in vitro исследований), возможно благодаря взаимодействию между лектином и карбоксильными доменами рецепторов опухолевых клеток (Kawagishi, 1995).
В 1998 в США, Управление по контролю за продуктами и лекарствами (FDA) авторизовало вторую стадию исследований потенциала D фракции при лечении рака груди и простаты. В ходе этих исследований было показано, что противоопухолевый эффект возникает благодаря разным типам действия: защита здоровых клеток, замедление или ингибирование роста опухолевых клеток, и ингибирование образования метастазов (Maywell, 2001).
Как было указано ранее, эффект от изменения G. frondosa officinalis вероятно ведет к противоопухолевой активности, аналогичной таковой у фракций D и MD, путем стимуляции апоптоза в случае наиболее распространенных видов рака, таких как рак кишечника, легких, печени и груди, и в частности таких гормонально зависимых, как происходящие из желез, таких как аденокарциномы груди, простаты и шейки матки.
Agaricus brasiliensis off.
Agaricus blazei Murrill off.
До 2001 было два гриба: A. blazei Murrill, в честь W.A. Murrill, который открыл его во Флориде в 1945 году, и другой blazei (Heinemann). Затем в 2005 в Бразилии в штате Sao Paulo были найдены другие схожие разновидности, но таксономисты решили, что это другой вид, A. brasiliensis. Возможно, многие исследования лекарственных свойств относятся к обоим видам, так как разновидности из разных регионов культивировались индифферентно. Под названием AbM (Agaricus blazei Murrill), этот гриб является одним из самых известных лекарственных грибов, изучаемых и применяемых при лечении онкологических пациентов, и по этой причине известней среди лекарственных грибов.
A. brasiliensis содержит в своем составе высокий процент белка, 37-48% от сухой массы, что является самым высоким показателем среди культивируемых грибов, 40% углеводородов, 3% жиров и приблизительно 7% минералов, из которых 2,5% калия, 1% фосфора, и 0,1% магния. Он содержит высокий процент витаминов В и D группы и несколько существенных элементов, включая железо, марганец, цинк и медь (Amazonas, 2005). Этот гриб продают свежим, высушенным, а также в виде порошка или экстракта.
Этот гриб, аналогично шампиньону, вместе с которым они принадлежат к одному семейству, нуждается в субстрате для выращивания, уже частично деградированном другими микроорганизмами. По этой причине элементы субстрата необходимо подвергать ферментации и пастеризации. Простым субстратом (Stamets, 2000) является навоз скота, произведенный не более недели назад. Тем не менее, рекомендуется использовать следующий субстрат: остатки от культивации сахарного тростника (45%) или солома разного типа (44%), соевые отруби (25%), мочевина (1%), сульфат аммония (1%), фосфат (0.5%), гипс (3%) и карбонат кальция (3%). Яичный порошок необходимо добавлять в субстрат в разном количестве от 3% до 5% от сухой массы субстрата. Начальная фаза ферментации такая же, как в случае A. bisporus. Оптимальное содержание азота в субстрате должно быть высоким, влажность смеси необходимо поддерживать на уровне 75%, рН на щелочном уровне (9-9,5), соотношение C/N равным 30/1, содержание азота в сухом субстрате приблизительно 2%. На первой стадии ферментации при соблюдении корректных условий влажности, температуры и количества кислорода, процесс дезинтеграции и трансформации субстрата начинается благодаря мезофильным микроорганизмам, утилизирующим углеводы из субстрата при повышенной температуре и выборе популяции термофильных микроорганизмов, размножающихся оптимальным образом при температуре выше 45 С°; при этом температура во внутренних частях субстрата может достигать 75-80 С°. По этой причине его необходимо полностью перемешать три раза с перерывом в три дня. Ферментация заканчивается через 9 дней, затем субстрат необходимо пастеризовать в течение дня при температуре 60-66 С°, и затем два дня выдержать при температуре 49-52 С°. Когда температура падает ниже 35 С°, субстрат помещают в открытые аэрируемые бутылки и проводят посев, аккуратно заполняя бутылки на 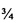 субстрата. Температуру поддерживают на уровне 25-30 С°, при влажности 80-85%, небольшой вентиляции и обработке ЭМП. В этих условиях колонизация проходит за 15-20 дней. Когда мицелий заселяет почти весь субстрат, в бутылку необходимо добавить слой толщиной 3-5 см из торфа с добавлением 10% гипса после очистки, вместе с микроэлементами в количестве
субстрата. Температуру поддерживают на уровне 25-30 С°, при влажности 80-85%, небольшой вентиляции и обработке ЭМП. В этих условиях колонизация проходит за 15-20 дней. Когда мицелий заселяет почти весь субстрат, в бутылку необходимо добавить слой толщиной 3-5 см из торфа с добавлением 10% гипса после очистки, вместе с микроэлементами в количестве 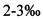 от массы субстрата в обычных пропорциях. Для начала плодоношения с дифференциацией примордия необходимо понизить температуру ниже 25 С°, снизить концентрацию СО2 с помощью вентиляции до 400-800 ppm, поддерживать относительную влажность на уровне приблизительно 85-90% и уменьшить освещенность (100-200 люкс). Через 20-25 дней для начала развития карпофоров температуру повышают до 24-27 С°, применяют интенсивное облучение ЭМП и собирают первый урожай через 4-8 дней. Возможно собрать два или три урожая. Развитию способствует переворачивание бутылки. В целом, количество получаемой продукции составляет 10% от массы субстрата, при этом время может быть сокращено при применении ЭМП.
от массы субстрата в обычных пропорциях. Для начала плодоношения с дифференциацией примордия необходимо понизить температуру ниже 25 С°, снизить концентрацию СО2 с помощью вентиляции до 400-800 ppm, поддерживать относительную влажность на уровне приблизительно 85-90% и уменьшить освещенность (100-200 люкс). Через 20-25 дней для начала развития карпофоров температуру повышают до 24-27 С°, применяют интенсивное облучение ЭМП и собирают первый урожай через 4-8 дней. Возможно собрать два или три урожая. Развитию способствует переворачивание бутылки. В целом, количество получаемой продукции составляет 10% от массы субстрата, при этом время может быть сокращено при применении ЭМП.
В литературе широко описаны противоопухолевые, иммуностимулирующие, антибактериальные и гепатопротекторные лекарственные свойства этого гриба, а также защита ДНК от окисления и антиокислительные свойства в целом (Ker et al., 2005; Zhong et al., 2005; Benardshaw et al., 2005, 2006: Bellini et al., 2006; Grinde et al., 2006; Jin et al., 2006). Эти свойства в большинстве обусловлены бета 1-3 глюканом с бета 1-6 разветвлением, при этом количество глюкана превышает его содержание в любых других лекарственных грибах, так как оно достигает 14% от общего содержания полисахаридов в этом грибе (Stamets, 2000). Противоопухолевая активность экстракта A. blazei обусловлена как непрямым действием, включающим стимуляцию иммунного ответа пациента, так и ингибированием ангиогенеза, что препятствует образованию метастазов (Kimura et al., 2004; Kobayashi et al., 2005; Zhang et al., 2006). Более того, экстракт вызывает апоптоз опухолевых клеток, но не здоровых клеток (Jin et al., 2006). Экстракт A. blazei стимулирует активность NK клеток (о лимфоцитов) и стимулирует производство интерферона гамма, приводя таким образом к более эффективному уничтожению опухолевых клеток в организме (Benardshaw et al., 2005, Zhong et al., 2006). Ответ клеток хозяина в присутствии экстракта A. blazei происходит при посредничестве клеточных рецепторов толл-подобного типа (Kassai et al., 2004). В AbM содержатся многие цитотоксические карциностатические полисахариды, выделенные из мицелия, плодового тела и спор, с разными названиями (АВ-Р, ATOM, AB-FP). Среди прочего они обладают способностью способствовать активности белка р38 MAPK (митоген-активируемая протеинкиназа) по подавлению клеточной линии HRA рака яичников и вызыванию апоптозных процессов, таких как транслокация про-апоптического белка Вах из цитозоля в митохондрию с высвобождением цитохрома С и активацией каспазы 9. Многие из этих биохимических механизмов включают взаимодействие между антиген представляющими клетками (АРС), NK клетками и цитотоксическими Т лимфоцитами с производством гамма интерферона (цитотоксического и антипролиферативного), и специфическими интерлейкинами, такими как IL-12, ответственными за клеточную активацию. Но AbM обладает антинеопластическим действием не только благодаря полисахаридам, но и липидам, и аминокислотам (белкам). Фактически, AbM содержит 3,6% липидов, из которых 73,2% являются фосфолипидами с антинеопластическим эффектом (Wasser and Weiss, 1999) и содержит значительное количество тирозиназы, т.е. фермента, катализирующего трансформацию аминокислоты тирозина в допамин, что позволяет организму производить значительное количество убихинона, или кофермента Q. Эта молекула является существенной для транспорта электронов на митохондриальном уровне, для потребления кислорода и производства энергии. Проводилось исследование антиангиогенной активности эргостерола в AbM, которая ингибирует неоваскуляризацию, стимулированную клетками легочной карциномы Льюиса (LLC) у мышей через кожный контакт и внутрибрюшинную инъекцию, при повышенных дозах: эргостерол продемонстрировал ингибирование неоваскуляризации в дозозависмом режиме (Takaku et al., 2001). Действие на иммунную систему полисахаридов AbM, выражающееся в системном противоопухолевом цитотоксическом эффекте, прекрасно сочетается с действием липидов, которые оказывают прямое и специфическое противоопухолевое воздействие на клеточном уровне, и также с действием убихинона, повышающем реактивность клеток, снабжение тканей кислородом и стимулирующим очищение от токсинов. Согласно научной литературе, антинеопластическое действие продемонстрировано особенно в отношение солидных опухолей, опухолей, относящихся к асцитам (асциты яичников и печени), и опухолей, вызываемых химическими канцерогенами. О терапевтическом успехе сообщалось у пациентов, страдающих лейкемией и лимфомами, особенно не-Ходжкинскими лимфомами.
Понятно, что обогащение лекарственного гриба согласно настоящему изобретению такими веществами, как аминокислоты и липиды (эргостерол), которые уже присутствуют в грибе, может только усилить синергию с бета-глюканами, главным образом присутствующими в этом грибе, с тем последствием, что он является нутрицевтиком в форме пищевого продукта.
Для полноты картины следует напомнить, что в мицелии содержится канцерогенный продукт агаритин, являющийся гидразидом, и в более концентрированной форме в его ближайшем родственнике A. bisporus. Необходимо подчеркнуть, что агаритин находится в мицелии, однако биохимический комплекс в плодовом теле, благодаря хорошо известному антиканцерогенному эффекту этого гриба, эффективно ему противодействует. Однако этот факт, вместе с сообщениями о гепатотоксическом эффекте от японских докторов (Mukai et al., 2006), необходимо принимать во внимание для предосторожности перед проведением дальнейших клинических и эпидемиологических исследований, в особенности в отношении пациентов с повреждением печени.
Другие грибы
Существуют другие грибы, часто несъедобные, с медицинскими свойствами, которые можно использовать при лечении онкологических заболеваний, такие как Inonotus obliquus, Fomes fomentarius, Cordyceps sinensis, Androdia camphorata, и др. Об этих грибах в настоящее время недостаточно информации касательно способов их культивации, используемых разновидностей, а также возможности и пользы добавок при трансформации в лечебную форму согласно настоящему изобретению. В ожидании их включения, наряду с другими и на основании научных доказательств, в список лекарственных грибов, необходимо отметить три несъедобных гриба, являющихся ключевыми среди медицинских грибов при лечении онкологических заболеваний: Ganoderma lucidum, Coriolus versicolor, Phellinus linteus.
Так как они лишены приятных вкусовых качеств и считаются несъедобными согласно правилам многих стран, эти грибы можно употреблять только в форме настоек или отваров свежих или сушеных грибов, убедившись в удалении самого гриба из жидкости перед ее употреблением.
Ganoderma lucidum off.
Рейши, как в Японии называют Ganoderma lucidum, среди грибов, называемых «китайскими», возможно является самым широко известным и употребляемым в пищу грибом в мире из-за его медицинских качеств. Фактически, вопреки его консистенции «жесткой кожи» и, вследствие этого, несъедобности, он находится среди наиболее употребляемых в пищу грибов (и не только в виде настойки), потому что его ежедневный прием обеспечивает "долгую жизнь и хорошее здоровье", как считается уже 3000 лет правления китайских императоров.
Ganoderma lucidum содержит: минеральные соли (железо, цинк, медь, марганец, калий, магний, кальций, и особенно германий), витамин В (фолиевую кислоту), семнадцать аминокислот, включая незаменимые, полисахариды, стеролы, вещества с антигистаминной активностью (аденозин, тритерпены, люциденовая кислота, ганодеровая кислота, и др.).
Автоматизированные способы культивации этого гриба разработаны недавно и не в промышленном масштабе. Компоненты субстрата включают растительные опилки и стружки (88%), пшеничные отруби (10%), сахарозу (1%) и карбонат кальция (1%) (Chiu et al., 2000). После тщательного перемешивания и добавления 1-2% яичного порошка, субстрат оставляют ферментироваться в форме копны на 4-7 дней, несколько раз в день переворачивая его, после чего его расфасовывают в бутылки согласно способу по настоящему изобретению, и стерилизуют в автоклаве при 121 С° в течение приблизительно двух часов. Бутылки открывают в потоке стерильного воздуха и засевают мицелий, выращенный на пшенице, внося минеральные добавки в количестве 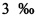 от массы сухого субстрата, при этом половину минеральных добавок составляют соли германия, и помещают на инкубацию при средней температуре 25 С° в темноту на 30 дней. ЕМП применяют в обычном циклическом режиме. Влажность окружающей среды поддерживают на высоком уровне (85-95%); температуру сначала снижают (18-24 С°), затем повышают до 25-28 С° на две последние недели плодоношения; необходима освещенность на уровне 750-1500 люкс в течение 12 часов в день. После первого сбора можно получить второй сбор, если перевернуть бутылку и открыть отверстие внизу, с общим количеством карпофора в размере 90 г из бутылки, содержащей 700 г субстрата. Применение ЭМП сокращает время процесса на 1/3 и способствует аккумуляции Ge.
от массы сухого субстрата, при этом половину минеральных добавок составляют соли германия, и помещают на инкубацию при средней температуре 25 С° в темноту на 30 дней. ЕМП применяют в обычном циклическом режиме. Влажность окружающей среды поддерживают на высоком уровне (85-95%); температуру сначала снижают (18-24 С°), затем повышают до 25-28 С° на две последние недели плодоношения; необходима освещенность на уровне 750-1500 люкс в течение 12 часов в день. После первого сбора можно получить второй сбор, если перевернуть бутылку и открыть отверстие внизу, с общим количеством карпофора в размере 90 г из бутылки, содержащей 700 г субстрата. Применение ЭМП сокращает время процесса на 1/3 и способствует аккумуляции Ge.
Ganoderma lucidum является одним из грибов, наиболее широко официально изученных в отношении их медицинских свойств, с более чем тысячью публикаций. Была выделена комплексная группа полисахаридов с иммуностимуляторными свойствами, среди них бета-глюканы, гетеро бета-глюканы и хитин-ксило-глюканы; исследования на лабораторных животных показали противоопухолевый и антиметастатический эффекты полисахаридов этого гриба (Silva, 2004; Lu et al., 2004; Fan, 2005; Wang et al., 1997). Действие этих соединений на некоторые клеточные линии человеческих опухолей вероятно связаны со стимуляцией макрофагов и Т лимфоцитов с последующим производством различных цитокинов, таких как IL-1 и IL-6. Некоторые гликопротеины стимулируют производство клеток селезенки, ответственных за созревание лимфоцитов, и производство цитокинов (Hsu et al., 2004). В литературе также сообщается об антиоксидантных свойствах экстракта G. lucidum (Jones and Jenardhanan, 2000), выражающихся в ингибировании липидного перокисления в некоторых биологических системах и в защите от острой кардиотоксичности, вызываемой этанолом (Wong et al., 2004; Sun et al., 2004). Этот мощный антиоксидантный эффект, отмеченный в многочисленных исследованиях, продемонстрировавших защитное действие против бронхита и герпеса, про-апоптический и противовоспалительный эффекты, вместе с гепатопротекторными, иммуномодуляторными и антидиабетическими свойствами (Gao et al., 2003, Hsu et al., 2004; Liu et al., 2004; Hong et al., 2004; Fan et al., 2005; Kim et al., 2005; Myojin et al., 2005; Li et al., 2005), проявляются благодаря присутствию некоторого количества германия, который является самым мощным из имеющихся в природе антиоксидантов; согласно настоящему изобретению, его количество увеличивается при внесении добавок.
Среди прочего, при присутствии германия с его интенсивным антиоксидантным действием только у двух онкологических патологий установлена роль окислительного стресса и при которых применялся G. lucidum: носоглоточная карцинома и хроническая миелогенная лейкемия.
Фактически G. lucidum officinal содержит большое количество органического германия; поэтому добавки можно модифицировать относительно стандарта, увеличивая количество неорганического германия до 50%. Антиоксидантная активность германия, водорастворимого неметалла, связана с длительной антиоксидантной активностью эрготионеина. В результате Ge становится намного более активным и эффективным также в форме рекомендуемого приема, травяного чая на горячей воде, наиболее подходящего для действия растворенного микроэлемента с тропизмом, усиливающимся при всех онкологических заболеваниях респираторной и желудочно-кишечной системы.
Coriolus versicolor off. super и extra
Среди грибов медицинского применения, этот гриб является наиболее интенсивно исследованным в отношении ряда его свойств и противоопухолевых эффектов, вызываемых веществами, выделенными из карпофоров и мицелия. Этот базидиомицет принадлежит к классу грибов, разлагающих лигнин. Из этого свойства происходят многие антинеопластические эффекты С. versicolor. Лигнин является полимерным материалом, укрепляющим стенки растительных клеток, и работающим как каркас для целлюлозных микроволокон. Лигнин является одним из самых прочных материалов в природе, комбинируя устойчивость к атмосферным условиям и ультрафиолетовой радиации с эластичностью и пластичностью. Грибные лакказы, в частности из С. versicolor (Crisante, University of Tuscia, 2013), являются единственными, которые могут разложить лигнин сначала на мономерные соединения, лигнаны, которые в соответствующих концентрациях в живых системах могут действовать как вторичные метаболиты, или формировать базовые компоненты полисахаридов, белков или липидов, являющихся частью того же самого гриба. Мономеры лигнина (две единицы 2-фенилпропана), происходящие из грибного катаболизма, являются энантиомерно чистыми, потому что производятся путем стереохимически контролируемого присоединения, и поэтому активными, но большая часть пищевых лигнанов происходит из льняных семян, содержащих преимущественно секоизоларицирезинол (более 3,7 г/кг сухой массы). Это относится в частности к грибам С. versicolor и P. ostreatus. Известны недавние исследования роли льняных семян против рака груди. Возможно лакказам помогает высокая температура субстрата в ходе ферментативного процесса, и некоторые другие ферменты. Процессы окислительной деградации лигнина, которые происходят под действием лакказ при более низких температурах, осуществляются при посредничестве класса химических молекул, называемых медиаторами, которые аллостерически являются посредниками в реакциях между ферментом, молекулярным субстратом, и кислородом, для поддержки реакции при низком окислительно-восстановительном потенциале лакказ. Систему О2 / лакказы / медиатор (Crisante, 2013) использовали для окисления бензильных фрагментов катехинов, получая соединения с хемопревентивной и противоопухолевой активностью, такие как таксифолин, и прекурсоры проантоцианидинов. В ходе деградационного ферментативного процесса в субстрате, а также в ходе процесса инкубации и развития мицелия с помощью лакказ, производятся такие вторичные метаболиты, обладающие биологической активностью (ВАМ), как лигнаны и проантоцианидины, уже оказывающие противоопухолевое действие. И затем базовые молекулы, компоненты полисахаридов, наиболее известные противоопухолевые агенты С.Versicolor, такие как PSK (полисахарид -K, крестин) и PSP (полисахарид-пептид).
Таким образом, способом повышения содержания лигнанов, проантоцианидинов, PSP и PSK является увеличение содержания лакказ, что достигается добавлением в субстрат меди. Вероятно, в природе содержание этого активного вещества находится во взаимосвязи с количеством меди в почве. Если ферментация происходит при высокой температуре и низком содержании кислорода, будет получено более высокое содержание лигнанов и проантоцианидинов в мицелии, и затем в плодовом теле (С.versicolor off. Super). Если ферментация преждевременно останавливается при понижении температуры и проветривании смеси, результатом является быстрое плодоношение и более высокое содержание в карпофоре PSP и PSK (С.versicolor off. Extra).
Оптимальный субстрат для выращивания содержит опилки и стружку различных лесных деревьев с составом смеси, аналогичным таковому в случае Lentinus edodes. Субстрат увлажняют до значения 65-70%, добавляют яичный порошок в количестве 2-3% от сухой массы субстрата. Субстрат оставляют на несколько дней для ферментации, затем помещают в бутылки в соответствии с настоящим изобретением, и стерилизуют в автоклаве. Посев проводят с использованием мицелия, выращенного на опилках и стружках, к которым необходимо добавить такую же минеральную добавку в количестве 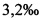 от сухой массы, содержащую 80% медьсодержащих минеральных веществ. Инкубацию проводят при температуре приблизительно 25 С° в течение приблизительно трех недель. После этого бутылки открывают с верхней стороны для улучшения развития базидиомы. Условия, необходимые на разных стадиях роста грибов, включают температуру 18-25 С°, высокую влажность, хорошее проветривание (уровень СО2: 500-1000 ppm) и освещение 500-2000 люкс. Бутылки также подвергают действию ЭМП. От появления примордия до созревания проходит приблизительно 40-50 дней (20-30 дней с MCF и инкорпорацией Cu до 100%). После сбора облучение позволяет получить существенное количество витамина D2. В течение нескольких месяцев может быть два или три сбора с производством в количестве 10-20% от массы сухого субстрата в бутылке.
от сухой массы, содержащую 80% медьсодержащих минеральных веществ. Инкубацию проводят при температуре приблизительно 25 С° в течение приблизительно трех недель. После этого бутылки открывают с верхней стороны для улучшения развития базидиомы. Условия, необходимые на разных стадиях роста грибов, включают температуру 18-25 С°, высокую влажность, хорошее проветривание (уровень СО2: 500-1000 ppm) и освещение 500-2000 люкс. Бутылки также подвергают действию ЭМП. От появления примордия до созревания проходит приблизительно 40-50 дней (20-30 дней с MCF и инкорпорацией Cu до 100%). После сбора облучение позволяет получить существенное количество витамина D2. В течение нескольких месяцев может быть два или три сбора с производством в количестве 10-20% от массы сухого субстрата в бутылке.
PSK выделили в Японии в 60-х годах. Он состоит из 68% полисахарида и 32% белка. Молекулярная масса составляет 94-100 кДа. Этот полисахарид состоит из мономеров D-глюкопиранозы, связанных в основной цепи бета 1-4 связями и бета 1-3 связями в боковых цепях. Последние, в свою очередь, имеют другие боковые разветвления, связанные бета 1-6 связями, связывающие полисахарид с белковой частью молекулы О-N гликозидными связями. В этом полисахариде основным сахаром является глюкоза, но есть и другие. Белковая часть богата аминокислотами, такими как аспарагиновая кислота и глютаминовая кислота (Kidd, 2000). PSK составляет по массе приблизительно 1/3 от всех полисахаридов, выделяемых из мицелия. Результаты исследований in vitro и на лабораторных животных показали эффективность PSK при лечении определенных опухолей: аденосаркомы, фибросаркомы, мастоцитомы, плазмацитомы, меланомы, саркомы, карциномы груди, легких и кишечника (Tsukagoshi et al., 1984).
PSP выделили в Китае в 80-х годах, он имеет молекулярную массу 100 кДа. Он структурно близок к PSK и отличается от него тем, что связи в главной цепи являются преимущественно бета 1-3, перемежающимися с некоторыми альфа 1-4; также в данном случае основным сахаром является D-глюкоза. Результаты экспериментов на животных показали, что PSP стимулирует пролиферацию Т-клеток и производство интерферона гамма и интерлейкина 2 (Ng, 1998). Было продемонстрировано, что PSP является нетоксичным соединением с иммуностимуляторной активностью, улучшающим как качество жизни онкологических пациентов, так и их выживаемость (Jong and Yang 1999). Также он облегчает побочные эффекты и предотвращает подавление иммунной системы у пациентов, проходящих диагностический терапевтический маточный кюретаж (RDT) и химиотерапию (СНТ) (Ng, 1998). В отношении PSP было доказано прямое воздействие на некоторые типы опухолей, таких как опухоли желудка и дыхательной системы, усиленное его способностью вызывать апоптоз клеток опухоли, но не нормальных клеток (Dong et al., 1996; Jong and yang, 1999; Heish et al., 2002; Chow et al., 2003; Tsang et al., 2003; Yang et al., 2005). Однако, не все виды опухолей поддаются лечению (Dong, 1997). PSP также обладает антиметастатическими свойствами при ингибировании неоангиогенеза (Но et al., 2004).
Как PSK, так и PSP хорошо абсорбируются и переносятся при пероральном приеме, и благодаря исключительной переносимости, могут употребляться в количестве до 20 г сушеного карпофора в день в виде чая, и до 5 г в день в виде капсул.
Двойной эффект, увеличение лигнанов или увеличение полисахаридов, достигаемый при добавлении в субстрат меди и регулировании ферментации, обеспечивает содержание фермента лакказы на ранней или поздней стадии. Этим определяются конечные свойства гриба, отличающиеся концентрацией лигнанов или полисахаридов PSP-PSK, соответственно получают два типа грибов Coriolus versicolor officinalis, т.е. super и extra, которые можно применять при различных карциномах с большим или меньшим ослаблением иммунной системы, а также на разных стадиях одного и того же онкологического заболевания, с более или менее прямым цитотоксическим действием или неоангиогенезным/метастатическим ингибированием.
Phellinus linteus off.
Гриб Phellinus linteus (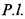 ), в английском варианте «Meshima», является базидиомицетом, принадлежащим к семейству полипоровых. Этот гриб широко применяется в народной медицине на Дальнем Востоке, особенно для лечения желудочно-кишечных заболеваний и диабета. Его фармакологическая активность обусловлена содержанием полисахаридов различного состава, с проявлением антиоксидантных, антидиабетических и противоопухолевых свойств. Фактически,
), в английском варианте «Meshima», является базидиомицетом, принадлежащим к семейству полипоровых. Этот гриб широко применяется в народной медицине на Дальнем Востоке, особенно для лечения желудочно-кишечных заболеваний и диабета. Его фармакологическая активность обусловлена содержанием полисахаридов различного состава, с проявлением антиоксидантных, антидиабетических и противоопухолевых свойств. Фактически, 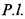 является одним из наиболее важных и изученных среди противоопухолевых грибов, в отношении его иммуномодулирующих способностей, начиная с исследования Sliva et al., опубликованного в British Journal of Cancer в 2008, по изучению ингибиторного эффекта (при посредничестве АКТ) на рост, ангиогенез и инвазивность клеток рака груди. Но еще в 1969 году Chihara et al. удалось показать, что полисахаридные экстракты
является одним из наиболее важных и изученных среди противоопухолевых грибов, в отношении его иммуномодулирующих способностей, начиная с исследования Sliva et al., опубликованного в British Journal of Cancer в 2008, по изучению ингибиторного эффекта (при посредничестве АКТ) на рост, ангиогенез и инвазивность клеток рака груди. Но еще в 1969 году Chihara et al. удалось показать, что полисахаридные экстракты 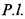 подавляют рост опухолей in vivo; позднее было показано, что фураны демонстрируют активность против меланомы мышиных клеток и человеческой легочной аденокарциномы. Kim et al. в 2006 году продемонстрировали, что полисахаридный комплекс, экстрагированный из
подавляют рост опухолей in vivo; позднее было показано, что фураны демонстрируют активность против меланомы мышиных клеток и человеческой легочной аденокарциномы. Kim et al. в 2006 году продемонстрировали, что полисахаридный комплекс, экстрагированный из 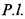 , значительно увеличивает пролиферацию В лимфоцитов, производство цитокинов и оксида азота макрофагами, и особенно цитолиз клеток YAC-1 лимфомы in vitro. После этого в других исследованиях было продемонстрирована стимуляция NK лимфоцитов грибом
, значительно увеличивает пролиферацию В лимфоцитов, производство цитокинов и оксида азота макрофагами, и особенно цитолиз клеток YAC-1 лимфомы in vitro. После этого в других исследованиях было продемонстрирована стимуляция NK лимфоцитов грибом 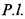 NK лимфоциты известных своей способностью лизировать клетки разных типов опухолей путем экзоцитоза гранул, содержащих перфорин, и вызывать лизис клеток посредством "перфорации" клеточной мембраны. Кроме того, NK лимфоциты отвечают за раннее и позднее ингибиторное влияние на рост опухоли путем регулирования абсолютного количества NK лимфоцитов, как на выживание пациента с ингибированием прогрессирования заболевания, так и в ответ на СНТ, в частности при раке поджелудочной железы (Davis et al., 2012). Это воздействие
NK лимфоциты известных своей способностью лизировать клетки разных типов опухолей путем экзоцитоза гранул, содержащих перфорин, и вызывать лизис клеток посредством "перфорации" клеточной мембраны. Кроме того, NK лимфоциты отвечают за раннее и позднее ингибиторное влияние на рост опухоли путем регулирования абсолютного количества NK лимфоцитов, как на выживание пациента с ингибированием прогрессирования заболевания, так и в ответ на СНТ, в частности при раке поджелудочной железы (Davis et al., 2012). Это воздействие 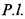 на иммуномодуляцию особенно затрагивает активность NK клеток. Иммуномодуляторные способности
на иммуномодуляцию особенно затрагивает активность NK клеток. Иммуномодуляторные способности 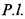 были клинически подтверждены в 2013 (Chang et al.) на аденокарциноме поджелудочной железы, при этом коммерческий полисахаридный комплекс, экстрагированный из
были клинически подтверждены в 2013 (Chang et al.) на аденокарциноме поджелудочной железы, при этом коммерческий полисахаридный комплекс, экстрагированный из 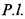 (Aclang) использовали для ретроспективного исследования в дополнение к СНТ на 103 пациентах после хирургической резекции протоковой аденокарциномы поджелудочной железы, с существенным влиянием на рецидивы в плане увеличения продолжительности периодов ремиссии почти в три раза у пациентов, получавших CHT+Aclang, в сравнении с пациентами, не получавшими
(Aclang) использовали для ретроспективного исследования в дополнение к СНТ на 103 пациентах после хирургической резекции протоковой аденокарциномы поджелудочной железы, с существенным влиянием на рецидивы в плане увеличения продолжительности периодов ремиссии почти в три раза у пациентов, получавших CHT+Aclang, в сравнении с пациентами, не получавшими 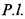 . Эти результаты в отношении рака поджелудочной железы, вместе с таковыми в отношении рака кишечника (Song et al., 2011, Li et al. 2011), рака груди (Lu et al. 2009, Sliva et al., 2008), и карциномы легких (Guo et al., 2007), делают
. Эти результаты в отношении рака поджелудочной железы, вместе с таковыми в отношении рака кишечника (Song et al., 2011, Li et al. 2011), рака груди (Lu et al. 2009, Sliva et al., 2008), и карциномы легких (Guo et al., 2007), делают 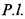 одним их самых активных грибов против онкологических заболеваний благодаря иммуноопосредствованному действию, смещающему баланс Th1-Th2 в сторону Th2, с прямой цитотоксической активацией NK лимфоцитами с эффектом подавления роста клеток опухоли, снижения рецидивов, стимуляции и подкрепления СНТ с уменьшенными побочными эффектами и болями, а также для предотвращения рака. Иммуномодуляторное действие
одним их самых активных грибов против онкологических заболеваний благодаря иммуноопосредствованному действию, смещающему баланс Th1-Th2 в сторону Th2, с прямой цитотоксической активацией NK лимфоцитами с эффектом подавления роста клеток опухоли, снижения рецидивов, стимуляции и подкрепления СНТ с уменьшенными побочными эффектами и болями, а также для предотвращения рака. Иммуномодуляторное действие  , также наблюдается при других заболеваниях, таких как аллергии и пищевая непереносимость, синдром дырявого кишечника и артрит, при которых также действуют большие количества хитина, содержащегося в
, также наблюдается при других заболеваниях, таких как аллергии и пищевая непереносимость, синдром дырявого кишечника и артрит, при которых также действуют большие количества хитина, содержащегося в  Хитин является неперевариваемым полисахаридом, действующим отчасти как строительный раствор, заделывающий повреждения в стенках желудка, и отчасти как регулятор бактерий, действуя на лимфатические узлы и на местный иммунный баланс.
Хитин является неперевариваемым полисахаридом, действующим отчасти как строительный раствор, заделывающий повреждения в стенках желудка, и отчасти как регулятор бактерий, действуя на лимфатические узлы и на местный иммунный баланс.
Среди минеральных компонентов  помимо меди также содержит германий (разновидности rimosus и gilvus, Chenghom 2010) и представляет собой среднее между Coriolus versicolor и Ganoderma lucidum.
помимо меди также содержит германий (разновидности rimosus и gilvus, Chenghom 2010) и представляет собой среднее между Coriolus versicolor и Ganoderma lucidum.
Это также подтверждается техникой культивации лекарственной формы, буквально такой же, как описанная для Coriolus versicolor с некоторыми изменениями для Ganoderma lucidum, и с существенной разницей в концентрации минеральных добавок (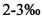 от сухой массы субстрата) относительно двух компонентов (Ge and Cu), составляющих 70% of минерального вещества. Лекарственные свойства согласно настоящему изобретению усиливают физиологическое действие компонентов
от сухой массы субстрата) относительно двух компонентов (Ge and Cu), составляющих 70% of минерального вещества. Лекарственные свойства согласно настоящему изобретению усиливают физиологическое действие компонентов 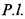 , обеспечивая хорошую абсорбцию главным образом в форме травяного чая, благодаря экстракции минералов и полисахаридов в горячую воду, в дополнение к оптимальному и приятному способу приема онкологическими пациентами.
, обеспечивая хорошую абсорбцию главным образом в форме травяного чая, благодаря экстракции минералов и полисахаридов в горячую воду, в дополнение к оптимальному и приятному способу приема онкологическими пациентами.
Другие съедобные грибы Hericium erinaceus off.
Этот гриб является редким съедобным паразитирующим грибом, предпочитающим живые дубовые деревья. Плодовое тело напоминает голову обезьяны, поэтому он известен в Азии под соответствующим названием. 100 г гриба содержит 31,7 г белков, 4 г жиров, 9,8 г минералов, 17,6 г углеводов, 30 г волокон, 1,2 мг натрия, 1,2 мг фосфора, 20,3 мг железа, 1,3 мг кальция, 4,46 мг калия, 123 мг магния, 5,3 мг тиамина, 3,9 мг рибофлавина, 240 ME эргокальциферола, 18,3 мг ниацина, 381 мг эргостерола и следовые количества цинка, германия и селена. Гриб содержит бета-глюканы и различные полисахариды (гериценоны, и др.) с эффектом в отношении эзофагиального и желудочного рака (Ying, 1987) и фактор стимуляции роста нервов (эринацин) (NGF) (Kawagishi 1991-94), потенциально полезный при деменции. Водные экстракты полисахаридов полезны при заболеваниях желудочно-кишечного тракта, таких как гастрит, язвы, язвенный колит и др. Действие полисахаридных экстрактов на эзофагиальный и желудочный рак является иммуноопосредствованным.
Культивация лекарственной формы аналогична таковой для Lentinus edodes (шиитаке): фаза роста мицелия на субстрате, содержащем добавки яичного порошка (2-3% от сухой массы субстрата), длящаяся от 10 до 14 дней при температуре от 21 до 24 С° и относительной влажности 95-100%, и концентрации СО2 от 5000 до 40000 ppm. Вначале применяют ЭМП с низкой интенсивностью. Приблизительно на седьмой день в контейнер добавляют соли в количестве 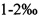 с преобладанием (70%) германия и селена, остаток равномерно содержит Zn и Cu. Целью этой добавки является усиление антиоксидантных свойств лекарственной формы. Образование примордия происходит за 3-5 дней (1-2 для с ЭМП); вентиляцию усиливают, температуру снижают до 10-15 С°, а концентрацию СО2 ДО 500-700 ppm, при освещенности 500-1000 люкс. Развитие карпофоров при облучении ЭМП высокой интенсивности происходит за короткое время (4-5 дней) если поднять температуру до 18-24 С° и поддерживать другие параметры стабильными. Можно получить еще 1-2 сбора.
с преобладанием (70%) германия и селена, остаток равномерно содержит Zn и Cu. Целью этой добавки является усиление антиоксидантных свойств лекарственной формы. Образование примордия происходит за 3-5 дней (1-2 для с ЭМП); вентиляцию усиливают, температуру снижают до 10-15 С°, а концентрацию СО2 ДО 500-700 ppm, при освещенности 500-1000 люкс. Развитие карпофоров при облучении ЭМП высокой интенсивности происходит за короткое время (4-5 дней) если поднять температуру до 18-24 С° и поддерживать другие параметры стабильными. Можно получить еще 1-2 сбора.
При уже существенном содержании эргостерола и витамина D2 в свежем грибе, увеличение этого содержания при помощи пульсирующего света происходит экспоненциально и легко может достичь 2000 ME на порцию в день. Этот гриб обладает хорошим балансом между органолептическими свойствами в качестве пищевого продукта и привнесенными, но не чрезмерными свойствами лекарственного гриба. Этим подтверждается возможность получения гриба, действительно эффективного в отношении онкологических заболеваний, в особенности желудочно-кишечного рака; этот гриб можно принимать в пишу в качестве ежедневного продукта в разной форме, он также является питательным.
Poria cocos off.
Этот гриб является аскомицетом, растущим на корнях хвойных деревьев, его склероций (считающийся трюфелем) является предметом упорных поисков и с удовольствием употребляется в пищу в Африке и Южной Азии. На Востоке его применяют в народной медицине тысячи лет в качестве седативного средства и диуретика. Из этого гриба были выделены полисахариды и тритерпены, обладающие иммуномодуляторными и противоопухолевыми свойствами. Наряду с растениями и травами, его часто применяют при лечении гепатита. Растворимые гетерополисахариды, выделенные из Poria cocos продемонстрировали противоопухолевые свойства в отношении клеточных линий желудочной карциномы и саркомы 180. Некоторые ВАМ, выделенные из склеротия (эргостерол пероксид, тумулозовая кислота, пачимовая кислота и др.) и тритерпеновые соединения показали значительный ингибиторный эффект на клеточные линии колоректального рака и рака желудка in vitro.
Культивация и лекарственное преобразование являются модификацией первой фазы (формирования склероция), ранее описанной для Morchella conica.
Полный потенциал в отношении неопластических /дегенеративных заболеваний неизвестен, но лекарственная форма имеет общие иммуномодуляторные и противоопухолевые свойства. Его можно принимать в пищу так же, как другие корнеплоды; можно также использовать как соус для пасты, таким же образом как трюфели, благодаря похожему аромату.
Грибы, полученные описанным способом, и обработанные с повышением концентрации и стандартизацией веществ, биологически активных при лечении и предотвращении онкологических/дегенеративных заболеваний, добавляют терапевтическую функциональную активность к своей основной уже существующей пищевой ценности. Суффикс "officinalis" можно добавлять к латинскому научному названию разновидностей этих грибов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГРИБНОЕ ПИВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2608497C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ, И СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2418062C1 |
| ПРЕПАРАТ С ПОЛИФУНКЦИОНАЛЬНОЙ МЕДИКО-БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ, ВЛИЯЮЩИЙ НА ТКАНЕВОЙ ОБМЕН, НА ОСНОВЕ ШТАММА ГРИБА Pleurotus ostreatus ВКПМ F-819 | 2012 |
|
RU2487930C1 |
| Штамм соматических структур макроскопического гриба вешенки обыкновенной РLеURотUS оSтRеатUS продуцент плодовых тел съедобного гриба | 1990 |
|
SU1755736A1 |
| Способ получения кормового продукта | 2021 |
|
RU2790269C2 |
| ПРЕПАРАТ НА ОСНОВЕ ГРИБА PLEUROTUS 1137, ВЛИЯЮЩИЙ НА МУЖСКУЮ РЕПРОДУКТИВНУЮ ФУНКЦИЮ | 2010 |
|
RU2422151C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНО-БЕЛКОВОГО КОРМА ИЗ ДРЕВЕСНОЙ ЗЕЛЕНИ | 1995 |
|
RU2088106C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВОГО КОРМА ИЗ ДРЕВЕСНЫХ ОТХОДОВ | 1995 |
|
RU2092073C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОВИРУСНОГО СРЕДСТВА И ПРОТИВОВИРУСНОЕ СРЕДСТВО | 2012 |
|
RU2522880C2 |
| Применение препарата "Экстракт мицелия вешенки "РЕВИТАЦЕЛ" на основе штамма гриба Pleurotus ostreatus ВКПМ F-819, влияющего на мужскую репродуктивную функцию | 2016 |
|
RU2634384C1 |
Изобретение относится к производству грибов, обогащенных биологически активными веществами. Физико-химический способ производства грибов предусматривает культивирование грибов в предварительно наполненных субстратом контейнерах в окружающей среде технологической теплицы. При этом проводят следующие стадии: изоляция и развитие мицелия желаемой разновидности гриба до посева, созревание субстрата, посев мицелия, инкубация мицелия с развитием грибного примордия в контролируемых условиях с помощью аппаратов и процессоров, приспособленных для регулировки температуры, влажности и облучения, развитие карпофоров, сбор карпофоров и обработка карпофоров пульсирующим светом для стимуляции производства витамина D2. Причем применяют физическое воздействие путем обработки упомянутой окружающей среды электромагнитным полем, осуществляемое на всех стадиях до сбора карпофоров, а также химическую обработку путем добавления в субстрат яичного порошка, а после посева мицелия – неорганических микроэлементов. Изобретение позволяет получить обогащенные биологически активными веществами грибы, обладающие терапевтическими возможностями, в частности, в области онкологии и в целом в области противодействия клеточной дегенерации при различных заболеваниях. 5 з.п. ф-лы.
1. Физико-химический способ производства грибов, обогащенных биологически активными веществами, при котором упомянутые грибы культивируют в предварительно наполненных субстратом контейнерах в окружающей среде технологической теплицы, включающий следующие стадии:
- изоляция и развитие мицелия желаемой разновидности гриба до его посева,
- созревание субстрата,
- посев мицелия,
- инкубация мицелия с развитием грибного примордия в контролируемых условиях с помощью аппаратов и процессоров, приспособленных для регулировки температуры, влажности и облучения,
- развитие карпофоров,
- сбор карпофоров,
- обработка карпофоров пульсирующим светом для стимуляции производства витамина D2,
физическое воздействие путем обработки упомянутой окружающей среды электромагнитным полем, осуществляемой на всех стадиях, предшествующих сбору карпофоров, с целью улучшения метаболической активности субстрата путем содействия ферментному производству активных метаболитов и производству органических соединений из неорганических микроэлементов для улучшения качества и количества грибов, а также
характеризующийся тем, что проводят химическую обработку с добавлением в субстрат яичного порошка и, после посева мицелия, неорганических микроэлементов, в результате чего получают лекарственные грибы, обладающие терапевтическими возможностями, в частности, в области онкологии и в целом в отношении дегенерации клеток при различных заболеваниях.
2. Способ по п. 1, в котором упомянутая обработка электромагнитными полями (ЭМП) характеризуется значением индукции 15-25 мТл в течение промежутка времени продолжительностью 10-20 мин в день начиная со стадии изоляции и формирования мицелия перед посевом и на всех стадиях до формирования грибного примордия, затем ЭМП со значением индукции 100 мТл в течение промежутка времени продолжительностью 2-3 минуты в день до стадии сбора карпофоров для соответствующего сокращения времени производства, в частности, во время инкубации и формирования карпофоров из грибного примордия.
3. Способ по п. 1, в котором яичный порошок добавляют в субстрат в массовом отношении в количестве от 2 до 5% от сухой массы субстрата в контейнере, чтобы карпофор производил эрготионеин в биологически активном количестве.
4. Способ по п. 1, в котором упомянутые неорганические микроэлементы включают комплекс солей селена, германия, цинка и меди.
5. Способ по п. 4, в котором упомянутые соли добавляют в массовом отношении в количестве от 1 до 3 % от сухой массы субстрата в контейнере.
6. Способ по п. 1, в котором грибные разновидности выбирают из группы, состоящей из: Pleurotus eryngii, Pleurotus ostreatus, Lentinus edodes "Shiitake", Flammulina velutipes, Morchella conica Parsons, Auricularia auricula-judae (L.:Fr.) Schroeter, Auricularia polytricha (Mont.) Sacc., Tremella fuciformis Berk. Brand, Agrocybe aegerita, Pholiota nameko, Hypsizygus tessulatus (Bull.) Singer, Hypsizygus ulmarius, Grifola frondosa "Maitake", Agaricus brasiliensis, Agaricus blazei Murrill, Ganoderma lucidum, Coriolus versicolor, Phellinus linteus, Hericium erinaceus, Poria cocos.
| US 20090269441 A1, 29.10.2009 | |||
| WO 2008150129 A3, 26.02.2009 | |||
| CN 103449858 A, 18.12.2013 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЖИДКОГО МИЦЕЛИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ В ОБОГАЩЕНИИ БЕЛКОМ КОРМОВ ДЛЯ ЖИВОТНЫХ | 2011 |
|
RU2498558C2 |
| СПОСОБ ВЫРАЩИВАНИЯ МИЦЕЛИЯ Ganoderma lucidum | 2010 |
|
RU2446206C1 |
| Аппарат для сортирования звонкой монеты калиброванием по диаметру | 1929 |
|
SU16930A1 |
| СПОСОБ ВЫРАЩИВАНИЯ РАСТЕНИЙ, ГРИБОВ И МОРСКИХ СЪЕДОБНЫХ ВОДОРОСЛЕЙ | 1993 |
|
RU2090053C1 |
Авторы
Даты
2019-05-29—Публикация
2016-09-30—Подача