Изобретение относится к области медицины, где может найти применение в медицинской практике для профилактики и лечения ишемических нарушений мозгового кровообращения, транзиторных ишемических атак и может быть использовано для создания отечественного лекарственного средства для терапии ишемического инсульта.
Известно соединение 3-(2-метоксиэтил)-5-пропан-2-ил-2,6-диметил-4-(3-нитрофенил)-1,4-дигидропиридина 3,5-дикарбоксилат под названием нимодипин, проявляющее церебропротекторное и нейротрофическое действие при ишемических нарушениях мозгового кровообращения в клинической практике (Gelmers H.J. The effects of nimodipine on the clinical course of patients with acute ischemic stroke // Acta Neurol. Scand. - 1984. - Vol. 69, No. 4. - P. 232-239) и нейропротекторное действие в эксперименте на животных (Bielenberg G.W., Beck Т., Sauer D., Burniol M., Krieglstein J. Effect of cerebroprotective agents on cerebral blood flow and on postischemic energy metabolism in the rat brain // J. Cereb. Blood. Flow. Metab. - 1987. - Vol. 7. - P. 480-488).
Недостатками известного решения являются высокая токсичность, невысокая продолжительность терапевтического действия и большой спектр вызываемых им побочных эффектов, среди которых наиболее часто наблюдаются сердечные аритмии, снижение артериального давления, брадикардия, диспепсические расстройства.
Известны производные 2-диэтиламино-21, 61-диметилфенилацетамида с антиаритмической активностью. Новые производные представляют собой новые соли лидокаина: L-аргинат, L-глутаминат, N-ацетил-L-глутаминат, 2-аминопропионат, аминоацетат, сукцинат, N-ацетилцистеинат и β-фенил-α-аминопропионат, более эффективные и безопасные по сравнению с гидрохлоридом лидокаина (RU 2223263, МПК С07С 237/04, С07С 229/06, С07С 229/24, опубл. 10.02.2004).
Недостатками является отсутствие церебропротекторного действия при ишемическом и дистрофическом поражении головного мозга, слабо выраженные антигипоксические свойства.
Технический результат заключается в создании производного 2,6-диметилфенилацетамида - 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноат, которое обладает высокой церебропротекторной активностью, позволяет снизить острую токсичность и увеличить продолжительность фармакологического действия при ишемическом нарушении мозгового кровообращения.
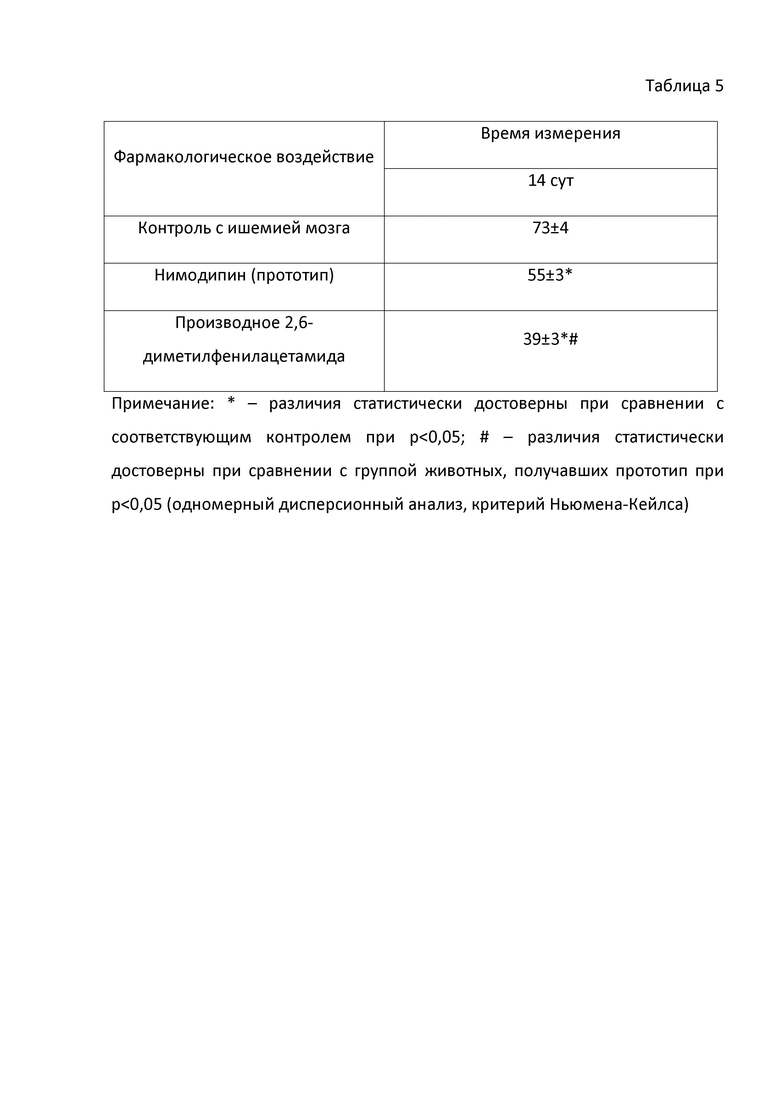
Сущность изобретения заключается в том, в способе получения производного 2,6-диметилфенилацетамида, к 20 г очищенного 2-диэтиламино-N-(2,6-диметилфенил) ацетамида приливают 200 мл воды очищенной и добавляют 14,33 г N-ацетил-2-аминоэтансульфоновой кислоты, смесь перемешивают на водяной бане при 55-60°C в течение 30-40 мин, полученный раствор фильтруют, воду отгоняют. Остаток сушат до постоянного веса и просеивают. Получают 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноат общей формулы (1):
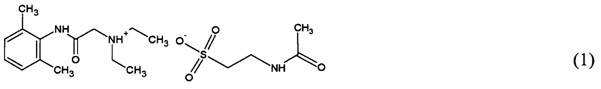
обладающего церебропротекторной активностью.
Способ получения производного 2,6-диметилфенилацетамида общей формулы (1) заключается в следующем.
Пример 1. Способ получения производного 2,6-диметилфенилацетамида общей формулы (1)
В реактор вместимостью 2 л, снабженный мешалкой, обратным холодильником и термометром, загружают 20 г очищенного 2-диэтиламино-N-(2,6-диметилфенил) ацетамида, приливают 200 мл воды очищенной и добавляют 14,33 г N-ацетил-2-аминоэтансульфоновой кислоты. Включают мешалку, массу нагревают на водяной бане до температуры 55-60°C и перемешивают при указанной температуре в течение 30-40 мин. Водный раствор субстанции общей формулы (1) фильтруют через фильтр Шота №4. Маточный раствор после фильтрации передают в аппарат для отгонки воды. Отгонку воды проводят в аппарате при температуре 30-35°C и вакууме 30-40 мм рт.ст. После завершения отгонки воды остаток кристаллизуется. Его переносят в вакуум-сушильный шкаф и сушат в вакууме 30-40 мм рт.ст. при температуре 30-35°C до постоянного веса. Высушенный остаток просеивают в сухом помещении через сито №32 (размер отверстий 200 мкм). Получают 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноат, белый или почти белый кристаллический порошок без запаха, гигроскопичный.
Выход 30,5 г (89,4%).
В литературе не описаны фармацевтические композиции, готовые лекарственные формы, содержащие производное 2,6-диметилфенилацетамида общей формулы (1).
Исследования фармакологической активности производного 2,6-диметилфенилацетамида общей формулы (1) представлены в нижеследующих примерах.
Пример 2. Острая токсичность производного 2,6-диметилфенилацетамида общей формулы (1) и прототипа
Острая токсичность производного 2,6-диметилфенилацетамида общей формулы (1) изучена в опытах на белых беспородных мышах (40 особей обоего пола весом 19-22 г, полученных из питомника филиала «Столбовая» ФГБУН НЦБМТ ФМБА России) при внутривенном введении растворов производного 2,6-диметилфенилацетамида общей формулы (1) и прототипа в объеме 0,4-0,6 мл в возрастающих концентрациях.
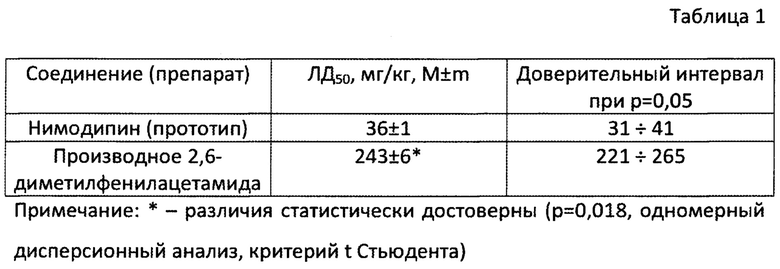
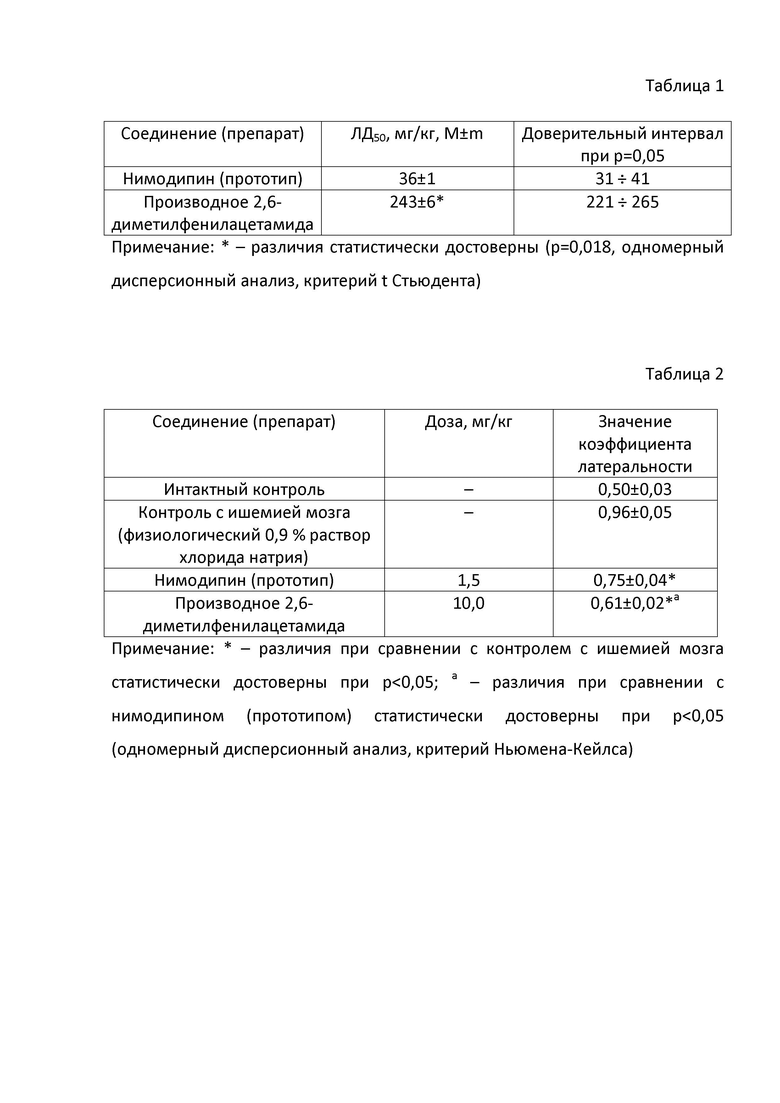
Показатель ЛД50 рассчитывали методом Личфилда-Уилкоксона (Е.В. Арзамасцев, И.В. Березовская, О.В. Верстакова и др. Методические рекомендации по изучению общетоксического действия лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Ч. 1. - М.: Гриф и К, 2012. - С. 25-35; Гуськова Т.А. Токсикология лекарственных средств. - М.: Издательский дом «Русский врач». - 2003. - С. 20-24.). Результаты исследования производного 2,6-диметилфенилацетамида общей формулы (1), а также прототипа нимодипина, представлены в табл. 1.
Из предлагаемых в табл. 1 данных хорошо видно, что заявленное соединение более, чем в шесть раз менее токсично, нежели прототип нимодипин при внутривенном введении. Причем, производное 2,6-диметилфенилацетамида общей формулы (1) относится к классу 3 (умеренно токсичные вещества) классификации токсичности химических веществ в соответствии с ГОСТ 12.1.007-76 (Березовская И.В. Классификация химических веществ по параметрам острой токсичности при парентеральных способах введения // Хим.-фарм. журнал. - 2003. - Т. 37, №3. - С. 32-34).
Пример 3. Церебропротекторная активность производного 2,6-диметилфенилацетамида общей формулы (1) на модели интралюминальной окклюзии / реперфузии средней мозговой артерии у крыс
Церебропротекторная активность производного 2,6-диметилфенилацетамида общей формулы (1) изучена в опытах на белых нелинейных крысах (64 особей-самцов весом 350-400 г, полученных из питомника филиала «Андреевка» ФГБУН НЦБМТ ФМБА России) при внутривенном введении водных растворов производного 2,6-диметилфенилацетамида общей формулы (1) и нимодипина (прототип) в объеме 0,8-1,0 мл в возрастающих дозах.
Фокальную ишемию головного мозга воспроизводили путем интралюминальной окклюзии средней мозговой артерии слева с ее последующей реперфузией (Longa E.Z., Weinstein P.R., Carlson S., Cummins R. Reversible middle cerebral artery occlusion without craniectomy in rats // Stroke; a journal of cerebral circulation. - 1989. - Vol. 20, No. 1. - P. 84-91).
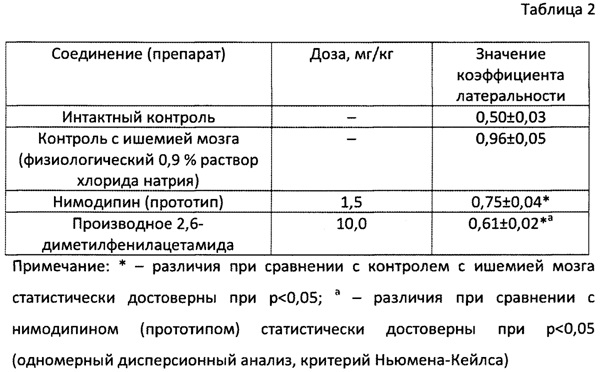
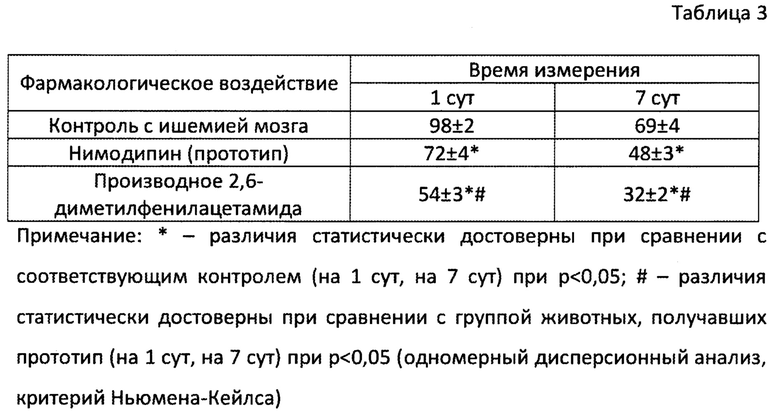
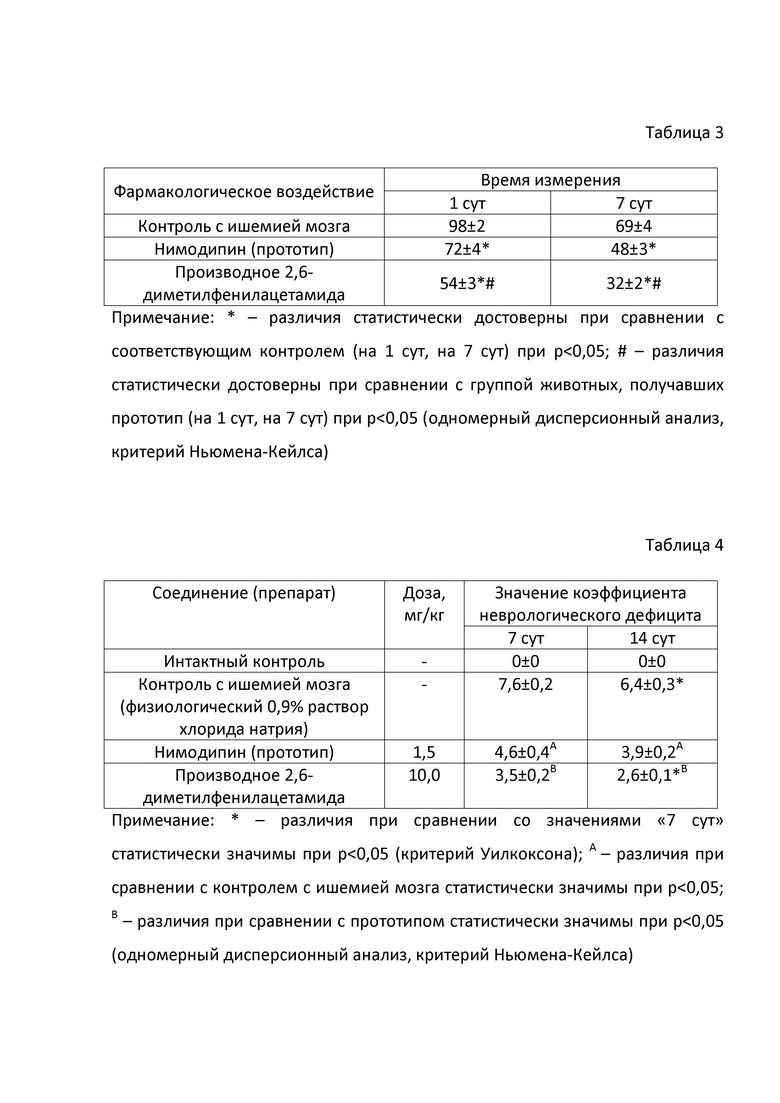
Результаты исследования церебропротекторного действия производного 2,6-диметилфенилацетамида общей формулы (1) на модели интралюминальной окклюзии / реперфузии средней мозговой артерии представлены в табл. 2, 3. Из представленных в табл. 2 данных хорошо видно, что внутривенное введении производного 2,6-диметилфенилацетамида общей формулы (1) в дозе 10 мг/кг за 5-10 мин до воспроизведения ишемии мозга приводит к формированию более мягкого сенсомоторного дефицита, измеряемого на 7 сут опыта, чем внутривенное введение прототипа в сравнимой дозе, что может свидетельствовать о более высокой активности производного 2,6-диметилфенилацетамида общей формулы (1) при ишемически-реперфузионном синдроме. При проведении морфологического исследования головного мозга крыс на 7 и 14 сут (по 50% животных из каждой серии), перенесших окклюзию средней мозговой артерии с ее последующей реперфузией, установлено (табл. 3), что внутривенное введение производного 2,6-диметилфенилацетамида общей формулы (1) сопровождается снижением объема поражения тканей мозга при сравнении с прототипом. Наименьший размер некроза установлен при профилактическом введении производного 2,6-диметилфенилацетамида общей формулы (1) как на 7, так и на 14 сут.
Таким образом, в отличие от прототипа, производное 2,6-диметилфенилацетамида общей формулы (1) отличается большей силой церебропротекторного действия при обратимой окклюзии средней мозговой артерии у крыс с ее последующей реперфузией.
Пример 4. Церебропротекторная активность производного 2,6-диметилфенилацетамида общей формулы (1) на модели необратимой перевязки средней мозговой артерии у крыс
Экспериментальная модель воспроизводилась у наркотизированных уретаном (380-420 мг/кг внутрибрюшинно) половозрелых нелинейных крыс-самцов весом 350-400 г (24 особи), полученных из питомника филиала «Андреевка» ФГБУН НЦБМТ ФМБА России. Изучение церебропротекторной активности производного 2,6-диметилфенилацетамида общей формулы (1) и нимодипина (прототип) у животных проводили по методу Bederson и соавт. (Bederson J., Pitts L., Tsuji M. et al. Rat middle cerebral artery occlusion: evaluation of the model and development of a neurological examination // Stroke. - 1986. - Vol. 17. - P. 472-476).
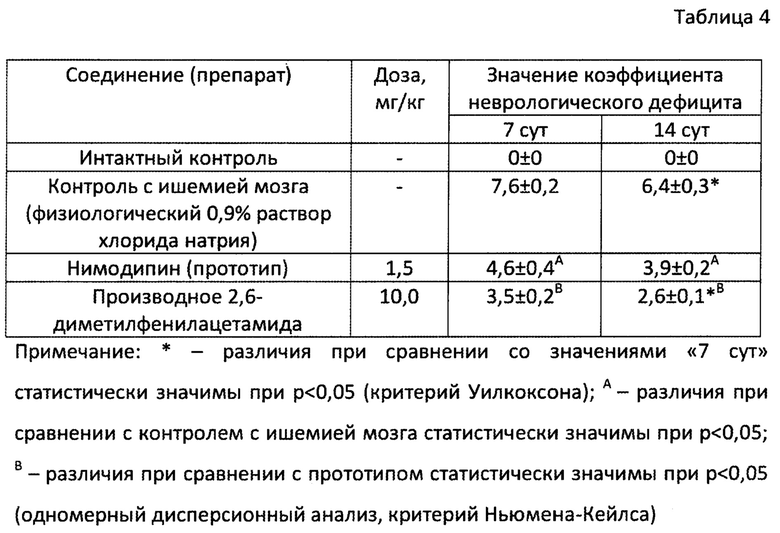
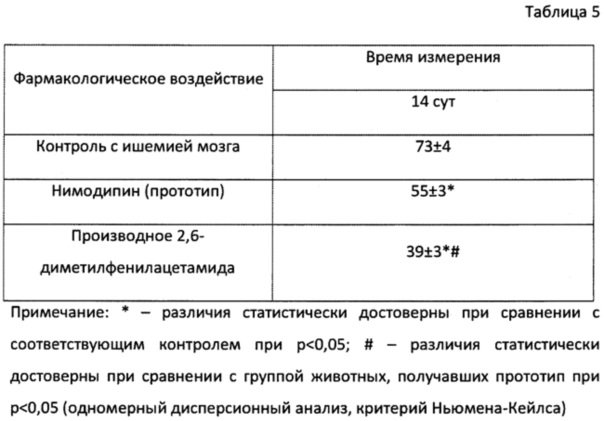
Результаты исследования церебропротекторной активности приведены в табл. 4 и 5.
Как видно в табл. 4, внутривенное введение производного 2,6-диметилфенилацетамида общей формулы (1) в профилактическом режиме приводит к формированию более мягкого неврологического дефицита, что может свидетельствовать о более легком поражении головного мозга при перевязке мозговой артерии. При этом, следует обратить внимание, что в отличие от прототипа, на фоне введения производного 2,6-диметилфенилацетамида общей формулы (1) отмечалась положительная динамика симптомов к 14-м суткам наблюдения, по сравнению с 7 сут опыта.
При оценке глубины и объема поражение ипсилатерального полушария головного мозга крысы при ишемическом процессе были получены следующие результаты (табл. 5). Необратимая перевязка средней мозговой артерии приводила к поражению трех четвертей ткани полушария головного мозга. Внутривенное введение производного 2,6-диметилфенилацетамида общей формулы (1) в профилактическом режиме сокращало объем мозгового некроза, при этом производное 2,6-диметилфенилацетамида общей формулы (1) было более эффективным, чем прототип (нимодипин).
Таким образом, по силе и длительности церебропротекторного эффекта на модели необратимой перевязки средней мозговой артерии производное 2,6-диметилфенилацетамида общей формулы (1) превосходит прототип.
Исследования проведены в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР №755 от 12.08.1987 г.), Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., Приказ Министерства здравоохранения Российской Федерации от 01.04.2016 г. №199н «Об утверждении правил надлежащей лабораторной практики», ГОСТ 33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами» (введен в действие 01.07.2016 г.) и одобрены Локальным этическим комитетом.
По сравнению с известным решением применение производного 2,6-диметилфенилацетамида - 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноата общей формулы (1) позволяет снизить острую токсичность, увеличить силу и продолжительность церебропротекторного эффекта при интралюминальной окклюзии средней мозговой артерии с ее последующей реперфузией и при ишемии головного мозга, вызванной необратимой перевязкой мозговой артерии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фармацевтическая композиция, обладающая антиаритмической активностью различной этиологии | 2021 |
|
RU2783944C1 |
| СПОСОБ ЗАЩИТЫ ГОЛОВНОГО МОЗГА В РЕКОНСТРУКТИВНОЙ ХИРУРГИИ СОННЫХ АРТЕРИЙ | 2004 |
|
RU2279878C2 |
| НЕЙРОПРОТЕКТОРНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ СВОЙСТВАМИ АНТИОКСИДАНТА И ДОНАТОРА ОКСИДА АЗОТА | 2016 |
|
RU2680526C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ ПОРАЖЕНИЙ МОЗГА | 2004 |
|
RU2288714C2 |
| ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2213562C2 |
| N-(ацетилсалицилоил)пиразол, обладающий церебропротекторным действием при недостаточности мозгового кровообращения | 2016 |
|
RU2632005C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦЕРЕБРОПРОТЕКТОРНЫМ, ЭНДОТЕЛИОПОЗИТИВНЫМ И АНТИТРОМБОТИЧЕСКИМ ДЕЙСТВИЕМ | 2015 |
|
RU2594254C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОИНСУЛЬТНЫМ ДЕЙСТВИЕМ | 2020 |
|
RU2737731C1 |
| ЦЕРЕБРОПРОТЕКТОР МЕТАБОЛИЧЕСКОГО ДЕЙСТВИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2761549C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОЛОНГИРОВАННОЙ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2538674C2 |
Изобретение относится к области фармацевтической химии. Предложен новый способ получения нового производного 2,6-диметилфенилацетамида - 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноата. Согласно способу по изобретению к 20 г очищенного 2-диэтиламино-N-(2,6-диметилфенил)ацетамида приливают 200 мл воды очищенной и добавляют 14,33 г N-ацетил-2-аминоэтансульфоновой кислоты, смесь перемешивают на водяной бане при 55-60°С в течение 30-40 мин, полученный раствор фильтруют, воду отгоняют. Остаток сушат до постоянного веса и просеивают. Получают 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноат общей формулы (1), обладающий церебропротекторной активностью. 5 табл., 4 пр.
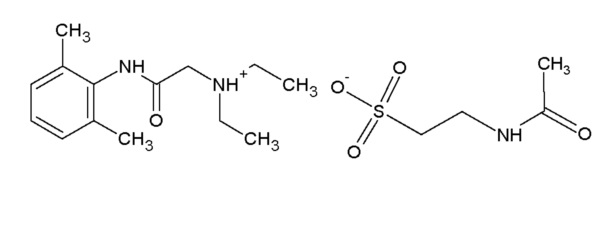
(1)
Способ получения производного 2,6-диметилфенилацетамида, обладающего церебропротекторной активностью, заключающийся в том, что к 20 г очищенного 2-диэтиламино-N-(2,6-диметилфенил) ацетамида приливают 200 мл воды очищенной и добавляют 14,33 г N-ацетил-2-аминоэтансульфоновой кислоты, смесь перемешивают на водяной бане при 55-60°С в течение 30-40 мин, полученный раствор фильтруют, воду отгоняют, остаток сушат до постоянного веса и просеивают, после чего получают 2-(диэтиламино)-N-(2,6-диметилфенил) ацетамида 2-ацетаминоэтансульфоноат общей формулы (1)
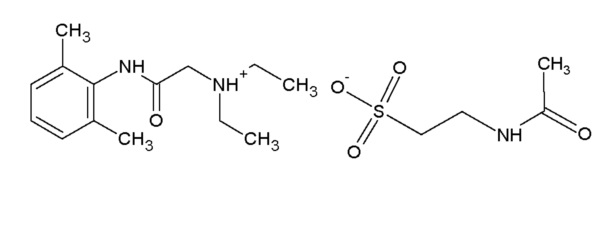
(1)
| ПРОИЗВОДНЫЕ 2-ДИЭТИЛАМИНО-2',6'-ДИМЕТИЛФЕНИЛАЦЕТАМИДА, ПРОЯВЛЯЮЩИЕ АНТИАРИТМИЧЕСКУЮ АКТИВНОСТЬ | 2002 |
|
RU2223263C1 |
| Л.Н.Сернов и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОЛОНГИРОВАННОЙ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2538674C2 |
| Е.В.Семелева и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2019-06-04—Публикация
2018-05-21—Подача