Область техники, к которой относится изобретение
Настоящее изобретение относится к новым производным 5-хлорбензо[d]оксазол-2(3H)-она, обладающим фармакологической активностью, способам их получения, содержащим их фармацевтическим композициям и их применению при лечении различных расстройств.
Предпосылки создания изобретения
Кинуренин-монооксигеназа (KMO) представляет собой флавин-аденин-динуклеотид (FAD), зависимый от монооксигеназы, расположенной на внешней митохондриальной мембране. KMO известна как катализатор окисления L-кинуренина (KYN) в 3-гидроксикинуренин (3HK) в части основного пути катаболизма триптофана. 3HK затем преобразуется в 3-гидроксиантраниловую кислоту и 2,3-пиридиндикарбоновую кислоту, кинурениназу (KYNU) и 3-гидроксиантранилат-3,4-диоксигеназу (3-HAAO).
КМО сильно экспрессируется в эндотелиальных клетках и моноцитах тканей, включая печень, плаценту, почки [Alberati-Giani, FEBS Lett. 410:407-412(1997)], и на более низком уровне, в микроглии и макрофагах в головном мозге.
Увеличенные уровни 3HK и 2,3-пиридиндикарбоновой кислоты и сниженные уровни кинуреновой кислоты (KYNA), которая образуется альтернативным путем из кинуренина, вовлечены в целый ряд заболеваний, включая болезнь Хантингтона, болезнь Паркинсона, болезнь Альцгеймера, боковой амиотрофический склероз (ALS) [Amaral, Outeiro et Al. Journal of Molecular medicine 2013: 91(6): 705-713] и острый панкреатит [Mole, McFerran et al. British Journal of Surgery 2008: 95: 855-867]. В ЦНС 3-HK и 2,3-пиридиндикарбоновая кислота, как было показано, являются нейротоксическими, и KYNA обладает нейропротекторными эффектами. Поэтому можно ожидать, что ингибирование окислительной активности KMO приведет к снижению уровня 3-HK и 2,3-пиридиндикарбоновой кислоты и повышению уровня KYNA, и потенциально сможет оказать пользу при этих заболеваниях.
Существует большой объем доказательств того, что метаболизм триптофана также изменяется в условиях острой травмы. Например, увеличение уровней кинуренина связаны с развитием сепсиса после травмы [Pellegrin, 2005, Logters, 2009], в то время как повышение как уровня кинуренина, так и 3-HK коррелирует с развитием функциональной недостаточности при остром панкреатите [Mole, McFerran et al. British Journal of Surgery 2008: 95: 855-867]. Такая разрегуляция метаболизма триптофана частично объясняется индукцией индоламина 2,3-диоксигеназы (IDO, фермент, который преобразует триптофан в N-формилкинуренин)), как часть воспалительного каскада, но развитие физиологической дисфункции органа появляется в зависимости от хода течения метаболитов [Mole, McFerran et al. British Journal of Surgery 2008: 95: 855-867].
Острый панкреатит (AP) является результатом локальной травмы органа, обусловленной рядом факторов, таких как желчные камни или избыточное потребление алкоголя. Возникающая боль в животе является крайне тяжелой, и пациенты будут в любом случае обращаться в отделение неотложной помощи сразу после начала обострения, с увеличением уровня сыворотки амилазы, используемой в качестве диагностического средства. В большинстве случаев эта болезнь является самоизлечивающейся, и боль устраняется в течение 24-36 часов. Однако у оставшихся 20-30% пациентов происходят системные воспалительные реакции, что приводит к быстрому прогрессированию множественной физиологической недостаточности (MOD). Это приводит к длительному пребыванию в отделении интенсивной терапии (в среднем 17 дней), с коэффициентом смертности около 30%. Несмотря на высокую неблагоприятность и серьезность заболевания, отсутствует эффективное доступное лечение со стандартной текущей медицинской помощью, будучи исключительно благоприятной.
В SU1143745 описаны способы получения производных 3-(3-бензоксазолонил)пропановой кислоты. В JP54098330 описано взаимодействие производных бензоксазолпропионовой кислоты с тионилхлоридом при производстве бактерицидного производного трициклического оксазолхинолина или тиазолхинолина для применения в сельском хозяйстве и садоводстве. Onkol et al, (J. Faculty of Pharmacy of Gazi University (202), 19(1), 15-24) описали производные (2-оксобензазолин-3-ил)алкановых кислот и тестирование этих соединений на антиноцицептивную активность. Kalcheva V et al (Godishnik na Sofiiskiya Universitet Sv. Kliment Okhridski, Khimicheski Fakultet (1972), Volume Date 1969-1970, 64, 33-42) описали цианоэтилирование бензоксазолтиона, бензоксазолон и некоторые производные бензоксазолона.
В WO2013016488, WO2011091153, WO2010017132, WO2010017179, WO2010011302, WO2008022286 и WO2008022281 описаны ингибиторы KMO для нацеливания против нейродегенеративных расстройств или заболеваний; в EP1475385, EP1424333 описаны ингибиторы KMO для нацеливания против дегенеративных и воспалительных состояний. По-прежнему существует потребность в эффективных ингибиторах КМО, которые подходят для внутривенного введения при применении в лечении острого панкреатита и других состояний, связанных с синдромом системного воспалительного ответа (SIRS).
В настоящее время обнаружен структурно новый класс соединений, который предоставляет ингибиторы KMO, которые могут быть полезны при лечении острого панкреатита и острых состояний, связанных с синдромом системного воспалительного ответа (SIRS).
Сущность изобретения
Поэтому, в первом аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения в качестве лекарственного средства:
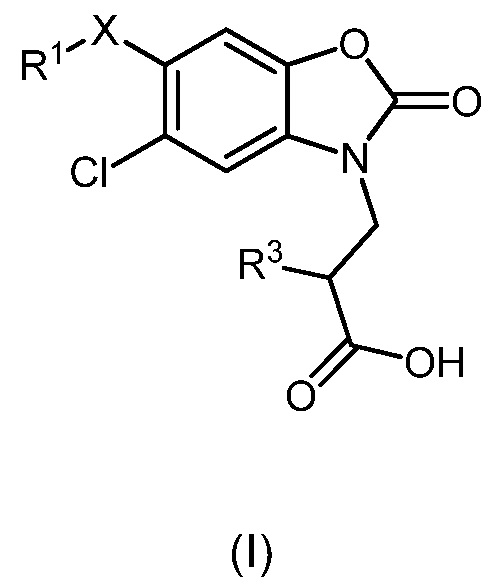 ,
,
где
X представляет собой связь, и R1 представляет собой -H, -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен галогеном, метилом, этилом или O;
m равен 1 или 2;
n равен 0 или 1;
R2 представляет собой -H, -метил или -этил; и
R3 представляет собой водород или метил.
Термин ʺалкилʺ, как использовано в данном описании, означает алкильную группу с прямой или разветвленной цепью во всех изомерных формах. Термин ʺC1-4алкилʺ означает алкильную группу, содержащую по меньшей мере 1 и, в большинстве случаев, 4 атома углерода. Примеры таких C1-4алкильных групп включают метил, этил, пропил, изопропил, н-бутил, изобутил, втор-бутил и трет-бутил.
Термин ʺгалогенʺ, как использовано в данном описании, означает, например, атом фтора (F), хлора (Cl), брома (Br) или йода (I), и термин ʺгалогенʺ означает, например, фтор (-F), хлор (-Cl), бром(-Br) или йод(-I).
Термин ʺгетероарилʺ, как использовано в данном описании, означает 5- или 6-членное ненасыщенное кольцо, которое содержит один или более гетероатомов. Когда термин ʺгетероарилʺ представляет 5-членную группу, он содержит гетероатом, выбранный из O, N или S и может необязательно дополнительно содержать 1-3 атома азота. Когда термин ʺгетероарилʺ представляет 6-членную группу, он содержит от 1 до 3 атомов азота. Примеры таких 5- или 6-членных гетероарильных колец включают, но, не ограничиваясь ими, пирролил, триазолил, тиадиазолил, тетразолил, имидазолил, пиразолил, изотиазолил, тиазолил, изоксазолил, оксазолил, оксадиазолил, фуразанил, фуранил, тиенил, пиридил, пиримидинил, пиразинил, пиридазинил и триазинил.
Термин ʺциклоалкилʺ, как использовано в данном описании, означает карбоциклическое кольцо, содержащее атомы углерода. Термин ʺC3-4циклоалкилʺ означает карбоциклическое кольцо, содержащее 3 или 4 атома углерода, например, циклопропил или циклобутил.
В дополнительных аспектах настоящее изобретение предоставляет соединение формулы (I) или его соль и фармацевтическую композицию, содержащую соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
Подробное описание изобретения
Как обсуждено выше, в первом аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения в качестве лекарственного средства:
 ,
,
где
X представляет собой связь, и R1 представляет собой -H, -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен галогеном, метилом, этилом или O;
m равен 1 или 2;
n равен 0 или 1;
R2 представляет собой -H, -метил или -этил; и
R3 представляет собой водород или метил.
В дополнительном аспекте настоящее изобретение предоставляет соединение формулы (I') или его фармацевтически приемлемую соль для применения в качестве лекарственного средства:
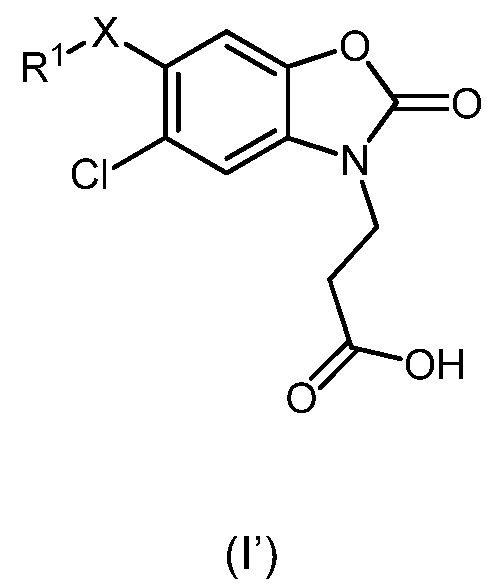 ,
,
где
X представляет собой связь, и R1 представляет собой -H, -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен метилом или O;
m равен 1 или 2;
n равен 0 или 1; и
R2 представляет собой -H или -метил.
Соединения формулы (I) или их фармацевтически приемлемые соли являются ингибиторами активности KMO и поэтому предполагаются в качестве потенциального применения при лечении расстройств или состояний, опосредованных KMO.
Такие состояния или расстройства включают острый панкреатит, другие состояния, связанные с синдромом системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, острой тяжелой печеночной энцефалопатией или острой печеночной недостаточностью.
Дополнительные состояния или расстройства включают гиперпролиферативные заболевания доброкачественного или злокачественного характера, при которых клетки различных тканей и органов проявляют аномальную картину роста, распространения, миграции, сигнализации, старения и смерти. Как правило, гиперпролиферативное заболевание относится к заболеваниям и расстройствам, связанным с неконтролируемой пролиферацией клеток, включая, но, не ограничиваясь ими, неконтролируемый рост клеток органа и ткани в результате раковых и доброкачественных опухолей. Гиперпролиферативные расстройства, связанные с эндотелиальными клетками, могут привести к болезненному ангиогенезу, такому как, ангиомы, эндометриоз, ожирение, возрастная макулярная дегенерация сетчатки и различные ретинопатии, а также пролиферации EC и гладких мышечных клеток, которые вызывают рестеноз, как следствие стентирования при лечении атеросклероза. Гиперпролиферативные расстройства с участием фибробластов (т.е. фиброгенез) включают, но, не ограничиваясь ими, расстройства избыточного рубцевания (т.е. фиброз), такие как возрастная макулярная дегенерация сетчатки, сердечное ремоделирование и недостаточность, связанные с инфарктом миокарда, избыточное ранозаживление, такое как обычно происходит вследствие травмы или операции, при келоидных и фиброзных опухолях и стентировании.
Кроме того, такие состояния или расстройства включают отторжение трансплантата (суппрессия Т-клеток) и реакция «трансплантат против хозяина», хроническая болезнь почек, системные воспалительные расстройства, воспалительные расстройства мозга, включая малярию и африканский трипаносомоз, удар и пневмококковый инфекционный менингит.
Кроме того, такие состояния или расстройства включают цирроз печени, хронический панкреатит, фиброз печени, фиброз и ишемически-реперфузионное повреждение легких.
Кроме того, такие состояния или расстройства дополнительно включают, например, нейродегенеративные заболевания, психиатрические или неврологические заболевания или расстройства, болезнь Крейцфильда-Якоба, индуцированную травмой нейродегенерацию, неврологический синдром высокого давления, дистонию, оливопонтоцеребральную атрофию, рассеянный склероз, эпилепсию, последствия инсульта, церебральную ишемию, ишемические расстройства, включая инсульт (фокальная ишемия), гипоксию, мульти-инфарктную деменцию, последствия травмы или повреждения головного мозга, повреждения спинного мозга, деменцию, такую как старческое слабоумие, индуцированную СПИД-ом энцефалопатию, другие инфекции, связанные с энцефалопатией, вирусный или бактериальный менингит, инфекционные заболевания, вызванные вирусами, бактериями и другими паразитами (например, вирусная инфекция общей центральной нервной системы (ЦНС), бактериальные или паразитарные инфекции, например, полиомиелит, болезнь Лайма (инфекции Borrelia burgdorferi)), септический шок и малярию, рак, рак с церебральной локализацией, печеночную энцефалопатию, системную волчанку, обезболивание и сидром отмены опиатов, пищевое поведение, психиатрические расстройства, такие как бессонница, депрессия, шизофрения, серьезный дефицит в рабочей памяти, серьезный дефицит в долгосрочной памяти, снижение в познании, серьезный дефицит внимания, серьезный дефицит в исполнительном функционировании, медлительность в обработке информации, медлительность в нейронной активности, тревога, генерализованные тревожные расстройства, паническая тревога, обсессивно-компульсивные расстройства, социальная фобия, тревожность, посттравматические стрессовые расстройства, острая стрессовая реакция, реакция настраивания, тревожное расстройство, вызванное разлукой, снятие тревожности алкоголем, депрессивные расстройства, расстройства развивающегося или стареющего головного мозга, диабет или его развитие, синдром Туретта, синдром ломки X-хромосомы, расстройства спектра аутизма, расстройства, вызванные серьезными и широко распространенными нарушениями чувства мышления, речи и способности относиться к другим, расстройства настроения, психологические расстройства, характеризуемые аномалиями эмоционального состояния, такие как, но без ограничений, биполярное расстройство, однополярная депрессия, основная депрессия, эндогенная депрессия, инволюционная депрессия, реакционная депрессия, психотическая депрессия, депрессия, вызванная сопутствующими медицинскими состояниями, депрессивные расстройства, циклотимические расстройства, дистимические расстройства, поведенческие расстройства из-за основного медицинского состояния, поведенческие расстройства неуточненного характера и индуцированные веществом поведенческие расстройства.
Кроме того, такие состояния или расстройства также включают, например, острый панкреатит, острый некротический панкреатит, СПИД (болезнь), анальгезию, асептический менингит, заболевание головного мозга, например синдром Жиля де ла Туретта, синдром Аспергера, синдром Ретта, повсеместное развитие расстройств, заболевание головного мозга, связанное со старением и развитием болезни головного мозга, синдром эмоционального выгорания, отравление монооксидом углерода, инфаркт миокарда или сердечную недостаточность и геморрагический шок (глобальная ишемия головного мозга), образование катаракты и старение глаз, заболевания центральной нервной системы, цереброваскулярные заболевания, синдром хронической усталости, хронический стресс, когнитивные расстройства, судорожные расстройства, такие как эпилепсия с большими и малыми судорожными припадками и частично комплексная эпилепсия, сахарный диабет, болезни нервной системы (например, дискинезия, расстройства движения, вызванные L-DOPA, наркотическая зависимость, боль и катаракта), лекарственную зависимость, отмену препарата, расстройства питания, синдром Гийена Барра и другие невропатии, печеночную энцефалопатию, иммунные заболевания, иммунные расстройства и терапевтическое лечение, направленное на изменение биологических реакций (например, введение интерферонов или интерлейкинов), воспалительные расстройства центральной и/или периферической нервной системы, телесные повреждения (травма, множественные травмы), умственные и поведенческие расстройства, метаболические заболевания, болезненные боли или расстройство, выбранное из группы воспалительной боли, невропатической боли или мигрени, аллодинию, гипералгезийную боль, фантомные боли, невропатические боли, связанные с диабетической невропатией, некоторой полиорганной недостаточностью, боязнью утопления, некрозом, новообразованиями головного мозга, неопластическими расстройствами, включая лимфомы и другие злокачественные расстройства крови, болезни нервной системы (неврологический синдром высокого давления, инфекция), никотиновую зависимость и другие расстройства привыкания, включая зависимость от алкоголизма, конопли, бензодиазепина, барбитуратов, морфина и кокаина, изменение аппетита, расстройства сна, изменения в модели сна, упадок сил, усталость, низкую самооценку, самоупреки неуместной вины, частые мысли о смерти или самоубийстве, планы или попытки совершения самоубийства, чувство безнадежности и бесполезности, психомоторное возбуждение или замедление, уменьшение возможности для мышления, концентрации или решительности без приема нейропротекторного препарата, боль, посттравматическое стрессовое расстройство, сепсис, болезнь позвоночника, спиноцеребеллярную атаксию, атопическую системную волчанку, травматические повреждения головного и спинного мозга, и синдромы тремора и различные расстройства движения (дискинезия), плохой баланс, брадидикенизию, ригидность, тремор, изменения в речи, потерю выражения лица, мелкий неразборчивый почерк, трудности при глотании, слюни, деменцию, путаницу, страх, сексуальные дисфункции, нарушения функций речи, нарушения в принятии решений, насильственные проявления, агрессивность, галлюцинации, апатию, нарушения в абстрактном мышлении.
Кроме того, такие состояния или расстройства также включают, например, сердечно-сосудистые заболевания, которые относятся к заболеваниям и расстройствам сердца и системы кровообращения. Эти заболевания часто связаны с дислипопротеинемией или дислипидемией. Сердечно-сосудистые заболевания включают, но, не ограничиваясь ими, кардиомегалию, атеросклероз, инфаркт миокарда и застойную сердечную недостаточность, ишемическую болезнь сердца, гипертензию и гипотонию.
В частности, такие состояния или расстройства включают такие состояния или расстройства, при которых повышенные уровни триптофана метаболитов коррелирует с тяжестью заболевания и плохим прогнозом, включая шок, травмы у пациентов с множественной полиорганной недостаточностью, тяжелым острым панкреатитом и хронической болезнью почек (Logters, T.T., et al. (2009) Shock 32: 29-34, Dabrowski et al (2014) Inflammation 37: 223-234, Changsirivathanathamrong et al (2011) Critical Care Medicine 39: 2678-2683, Mole, D.J., et al.(2008) Br J Surg 95: 855-867, Zhao (2013) Renal Failure 35: 648-653, Pawlak, K. et al (2009) Blood Coagulation and Fibrinolysis 20: 590-594, Kabayashi, T. et al (2014) Biochemical and Biophysical Research Communications 445: 412-416).
Соответственно, во втором аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль, где X и R1 являются такими, как определено выше для формулы (I), для применения при лечении любого из указанных выше состояний или расстройств, и в частности, острого панкреатита.
Настоящее изобретение, кроме того, предоставляет соединение формулы (I) или его фармацевтически приемлемую соль, где X и R1 являются такими, как определено выше для формулы (I), для применения при профилактике любого из указанных выше состояний или расстройств, и в частности, острого панкреатита.
Настоящее изобретение, кроме того, предоставляет способ лечения указанных выше состояний или расстройств, особенно острого панкреатита, у млекопитающих, включая людей, включающий введение страдающему пациенту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где X и R1 являются такими, как определено выше для формулы (I).
Настоящее изобретение также предоставляет применение соединения формулы (I) или его фармацевтически приемлемой соли, где X и R1 являются такими, как определено выше для формулы (I), при изготовлении лекарственного средства для применения при лечении указанных выше состояний или расстройств, и особенно, острого панкреатита.
В третьем аспекте настоящее изобретение предоставляет соединение формулы (I) или его соль:
 ,
,
где
X представляет собой связь, и R1 представляет собой -H, -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен галогеном, метилом, этилом или O;
m равен 1 или 2;
n равен 0 или 1;
R2 представляет собой -H, -метил или -этил; и
R3 представляет собой водород или -метил,
при условии, что соединением формулы (I) или его солью не является 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота или 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановая кислота.
В дополнительном аспекте настоящее изобретение предоставляет соединение формулы (IA) или его соль:
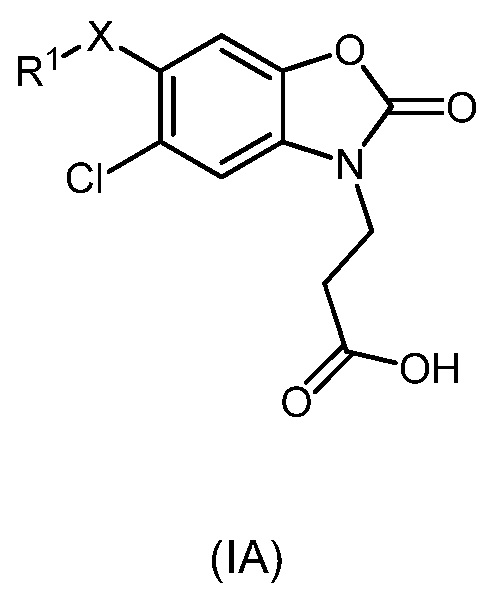 ,
,
где
X представляет собой связь, и R1 представляет собой -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен метилом или O;
m равен 1 или 2;
n равен 0 или 1; и
R2 представляет собой -H или -метил.
В одном из вариантов осуществления предоставлено соединение формулы (I) или его соль:
 ,
,
где
X представляет собой связь, и R1 представляет собой -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен галогеном, метилом, этилом или O;
m равен 1 или 2;
n равен 0 или 1;
R2 представляет собой -H, -метил или -этил; и
R3 представляет собой водород или -метил.
В одном из вариантов осуществления соединения формулы (I), X представляет собой связь, и R1 представляет собой -H, -галоген или -CN.
В конкретном варианте осуществления X представляет собой связь, и R1 представляет собой -H, -Cl, -F, -Br или -CN.
В альтернативном варианте осуществления X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил.
В конкретном варианте осуществления X представляет собой -CH2-, и R1 представляет собой -H, -CH3 или -CH(CH3)2.
В более конкретном варианте осуществления X представляет собой -CH2-, и R1 представляет собой -H.
В альтернативном варианте осуществления X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен галогеном, метилом или O.
В альтернативном варианте осуществления X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен метилом или O.
В более конкретном варианте осуществления X представляет собой -O-, и R1 представляет собой -CHR2CH2OMe, -(CH2)nC3-4циклоалкил или -(CH2)nоксетан.
В более конкретном варианте осуществления X представляет собой -O-, и R1 представляет собой -CHR2гетероарил.
В более конкретном варианте осуществления X представляет собой -O-, и R1 представляет собой -CHR2пиридил.
В более конкретном варианте осуществления X представляет собой -O-, и R1 представляет собой -CHR2-пирид-2-ил.
В одном из вариантов осуществления R2 представляет собой водород.
В альтернативном варианте осуществления R2 представляет собой -метил.
В альтернативном варианте осуществления R2 представляет собой этил.
В одном из вариантов осуществления R3 представляет собой водород. В альтернативном варианте осуществления R3 представляет собой метил.
В альтернативном варианте осуществления X представляет собой -O-, и R1 представляет собой 1-пирид-2-илэтил, метил, этил, изобутил, циклопропилметил, циклобутилметил, бензил, 2-метоксиэтил, пропил, 3,3,3-трифторпропил, пирид-2-илметил, изопропил, циклобутил, циклопропил, 2,2,2-трифторэтил, оксетан-3-ил, оксетан-3-илметил, 1-метоксипропан-2-ил, 6-метилпиридин-3-ил, 2-метилпиридин-4-илметил, пирид-2-илметил-N-оксид, 1-метил-1H-имидазол-2-илметил, 2-метилпиридин-3-илметил, пиримидин-2-илметил, 2-метилоксазол-5-илметил, 5-метилоксазол-2-илметил, 1H-имидазол-2-илметил, пиридазин-3-илметил, 1-(2-метилоксазол-5-ил)этил, 1-(5-фторпиридин-2-ил)этил, 1-(5-метилпиридин-2-ил)этил, 5-фторпропиридин-2-илметил, 5-хлорпиридин-2-илметил, 1-(5-хлорпиридин-2-ил)этил, 5-метилпиридин-2-илметил, 1-(6-метилпиридин-2-ил)этил, 1-(пиридин-2-ил)пропил, 1-(4-метилпиридин-2-ил)этил, 1-(пиридазин-3-ил)этил, 6-метилпиридазин-3-илметил, 1-(6-метилпиридазин-3-ил)этил, 1-(5-метилпиридин-2-ил)пропил, 1-(5-метилпиридин-2-ил)этил, 1-(4-метилпиридин-2-ил)этил, 1-(пиридазин-3-ил)этил, 6-метилпиридазин-3-илметил, 1-(6-метилпиридазин-3-ил)этил, 1-пиримидин-2-илэтил или 1-оксазол-2-илэтил.
В альтернативном варианте осуществления X представляет собой -O-, и R1 представляет собой 1-пирид-2-илэтил, метил, этил, изобутил, циклопропилметил, циклобутилметил, бензил, 2-метоксиэтил, пропил, 3,3,3-трифторпропил, пирид-2-илметил, изопропил, циклобутил, циклопропил, 2,2,2-трифторэтил, оксетан-3-ил, оксетан-3-илметил, 1-метоксипропан-2-ил, 6-метилпиридин-3-ил, 2-метилпиридин-4-илметил, пирид-2-илметил-N-оксид, 1-метил-1H-имидазол-2-илметил, 2-метилпиридин-3-илметил, пиримидин-2-илметил, 2-метилоксазол-5-илметил, 5-метилоксазол-2-илметил, 1H-имидазол-2-илметил или пиридазин-3-илметил.
В еще более конкретном варианте осуществления X представляет собой -O-, R1 представляет собой -CHR2-пирид-2-ил, и R2 представляет собой -метил.
В еще более конкретном варианте осуществления X представляет собой -O-, R1 представляет собой -CHR2-пирид-2-ил, R2 представляет собой -метил, и R3 представляет собой водород.
Все свойства и варианты осуществления соединений формулы (I) применимы для соединений формулы (IA) при внесении соответствующих изменений. Здесь и далее по тексту, все ссылки на соединения формулы (I) включают соединения формулы (IA).
Все свойства и варианты осуществления соединений формулы (I) применимы для соединений формулы (IA) и (I') при внесении соответствующих изменений. Здесь и далее по тексту, все ссылки на соединения формулы (I) включают соединения формулы (IA) и (I').
Пролекарства соединений формулы (I) включены в объем настоящего изобретения. В одном из вариантов осуществления соединения формулы (I) или их соли не являются пролекарствами.
Как использовано в данном описании, термин ʺпролекарствоʺ означает соединение, которое преобразуется в организме, например гидролизом в крови, в активную форму, которая обладает медицинскими эффектами. Фармацевтически приемлемые пролекарства описаны T. Higuchi and V. Stella, в Prodrugs as Novel Delivery Systems, Vol. 14 of the A.C.S. Symposium Series, и Edward B. Roche, ed., в Bioreversible Carriers in Drug Design, American Pharmaceutical Association and Pergamon Press, 1987, и D. Fleishner, S. Ramon and ч. Barba в ʺImproved oral drug delivery: solubility limitations overcome by the use of Prodrugsʺ, Advanced Drug Delivery Reviews (1996) 19(2) 115-130. Пролекарства представляют собой любые ковалентно связанные носители, которые высвобождают соединение формулы (I) in vivo, когда такое пролекарство вводится пациенту. Пролекарства, как правило, получают в ходе модификаций функциональных групп, таким образом, что модификация расщепляется in vivo, приводя к образованию первичного соединения. Пролекарства могут включать, например, соединения настоящего изобретения, в которых карбоксильная группа связана с любой группой, которые при введении пациенту, расщепляются с образованием карбоксильной группы. Таким образом, репрезентативные примеры пролекарств включают (но, не ограничиваясь ими) фосфонатные, карбаматные, ацетатные, формиатные и бензоатные производные карбоновой кислоты функциональной группы соединений формулы (I).
Соединения формулы (I) или их соли включают соединения примеров 1-61 и их соли.
В одном из вариантов осуществления соединения формулы (I) или их соли выбраны из группы, состоящей из:
3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5,6-дихлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-фтор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-метокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циано-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклопропилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклобутилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-(бензилокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(2-метоксиэтокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-пропоксибензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(3,3,3-трифторпропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиридин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(2,2,2-трифторэтокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((1-метоксипропан-2-ил)окси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-4-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-(((3-(2-карбоксиэтил)-5-хлор-2-оксо-2,3-дигидробензо[d]оксазол-6-ил)окси)метил)пиридин-1-оксида;
3-(5-хлор-6-((1-метил-1H-имидазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиримидин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилоксазол-5-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилоксазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-((1H-имидазол-2-ил)метокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
3-(5-хлор-2-оксо-6-(пиридазин-3-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(1-(2-метилоксазол-5-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты (рацемической);
(R)-3-(5-хлор-6-(1-(5-фторпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-фторпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-хлорпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-хлорпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)пропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(4-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридазин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)пропокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиримидин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты (неизвестный индивидуальный энантиомер);
(S)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
(R)-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
и их солей.
В дополнительном варианте осуществления соединения формулы (I) или их соли выбраны из группы, состоящей из:
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5,6-дихлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-фтор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-метокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циано-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклопропилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклобутилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-(бензилокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(2-метоксиэтокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-пропоксибензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(3,3,3-трифторпропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиридин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(2,2,2-трифторэтокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((1-метоксипропан-2-ил)окси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-4-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-(((3-(2-карбоксиэтил)-5-хлор-2-оксо-2,3-дигидробензо[d]оксазол-6-ил)окси)метил)пиридин-1-оксида;
3-(5-хлор-6-((1-метил-1H-имидазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиримидин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилоксазол-5-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилоксазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-((1H-имидазол-2-ил)метокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
3-(5-хлор-2-оксо-6-(пиридазин-3-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(1-(2-метилоксазол-5-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты (рацемическая);
(R)-3-(5-хлор-6-(1-(5-фторпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-фторпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-хлорпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-хлорпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)пропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(4-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридазин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)пропокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиримидин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
(R)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
и их солей.
В одном из вариантов осуществления соединения формулы (I) или их соли выбраны из группы, состоящей из:
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5,6-дихлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-фтор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-метокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циано-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклопропилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклобутилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-(бензилокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(2-метоксиэтокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-пропоксибензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(3,3,3-трифторпропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиридин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(2,2,2-трифторэтокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((1-метоксипропан-2-ил)окси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-4-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-(((3-(2-карбоксиэтил)-5-хлор-2-оксо-2,3-дигидробензо[d]оксазол-6-ил)окси)метил)пиридин-1-оксида;
3-(5-хлор-6-((1-метил-1H-имидазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиримидин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилоксазол-5-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилоксазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-((1H-имидазол-2-ил)метокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
3-(5-хлор-2-оксо-6-(пиридазин-3-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
и их солей.
В дополнительном варианте осуществления соединения формулы (I) или их соли выбраны из группы, состоящей из:
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(1-(2-метилоксазол-5-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты (рацемическая);
(R)-3-(5-хлор-6-(1-(5-фторпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-фторпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-хлорпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-хлорпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)пропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(4-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридазин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)пропокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиримидин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты (неизвестный индивидуальный энантиомер);
(R)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
(S)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
и их солей.
Соединения формулы (I) способны образовывать аддитивные соли оснований. Такие соли могут быть образованы путем взаимодействия с соответствующим основанием, необязательно в подходящем растворителе, таком как органический растворитель, с получением соли, которая может быть выделена кристаллизацией и фильтрованием.
Благодаря их возможному применению в медицине, следует принимать во внимание, что для применения солей соединений формулы (I) в медицине, они должны быть фармацевтически приемлемыми. Подходящие фармацевтически приемлемые соли будут очевидны специалистам в данной области и включают такие, которые описаны Berge, в J. Pharm. Sci., 1977, 66, 1-19. Фармацевтически приемлемые соли оснований включают, но, не ограничиваясь ими, соли аммония, соли щелочных металлов, таких как натрий и калий, соли щелочноземельных металлов, таких как кальций и магний, и соли с органическими основаниями, включая соли первичных, вторичных и третичных аминов, таких как трет-бутиламин, циклогексиламин, диметиламин, триметиламин, диэтилтриамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол (TRIS) и N-метил-D-глюкамин.
В дополнительном варианте осуществления соединения формулы (I) или их соли выбраны из группы, состоящей из:
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
3-(5,6-дихлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-фтор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-метокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циано-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-этокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-этил-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-изобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-(циклопропилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-(циклобутилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(6-(бензилокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-(2-метоксиэтокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-пропоксибензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-(3,3,3-трифторпропокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-(пиридин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-изопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-циклобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-циклопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-(2,2,2-трифторэтокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-(оксетан-3-илокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-изобутил-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-(оксетан-3-илметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((1-метоксипропан-2-ил)окси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((6-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((2-метилпиридин-4-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-(((3-(2-карбоксиэтил)-5-хлор-2-оксо-2,3-дигидробензо[d]оксазол-6-ил)окси)метил)пиридин-1-оксида;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((1-метил-1H-имидазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((2-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-(пиримидин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((2-метилоксазол-5-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((5-метилоксазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
3-(6-((1H-имидазол-2-ил)метокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-(пиридазин-3-илметокси)бензо[d]оксазол-3(2H)-ил)пропаноата.
В дополнительном варианте осуществления соединения формулы (I) или их соли выбраны из группы, состоящей из:
гидрохлорида (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в соединении с серной кислотой (1:1);
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в соединении с метансульфоновой кислотой (1:1);
N-бензил-2-фенилэтанамин (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
N1,N2-дибензилэтан-1,2-диамин (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
(2R,3R,4S,5R)-3,4,5,6-тетрагидрокси-2-(метиламино)гексаналь (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в соединении с (S)-2-амино-5-гуанидинпентановой кислотой (1:1);
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в соединении с (S)-2,6-диаминогексановой кислотой (1:1);
натрий (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в соединении с 4-метилбензолсульфоновой кислотой (1:1);
N1-(2-аминоэтил)этан-1,2-диамин (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-(1-(2-метилоксазол-5-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата (рацемический);
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-6-(1-(5-фторпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((5-фторпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((5-хлорпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-6-(1-(5-хлорпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-6-(1-(5-хлорпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-6-((5-метилпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-6-(1-(6-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)пропокси)бензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)пропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-6-(1-(4-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридазин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)пропокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
2-амино-2-(гидроксиметил)пропан-1,3-диол 3-(5-хлор-2-оксо-6-(1-(пиримидин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата (неизвестный индивидуальный энантиомер);
2-амино-2-(гидроксиметил)пропан-1,3-диол (S)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата и
2-амино-2-(гидроксиметил)пропан-1,3-диол (R)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата.
В одном из вариантов осуществления соединением формулы (I) или его солью является:
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота или ее соль.
В конкретном варианте осуществления соединением формулы (I) или его солью является:
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота или ее соль фармацевтически приемлемая соль.
В более конкретном варианте осуществления соединением формулы (I) или его солью является:
2-амино-2-(гидроксиметил)-1,3-пропандиольная соль 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты.
В альтернативном варианте осуществления соединением формулы (I) или его солью является: 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота.
В альтернативном варианте осуществления соединением формулы (I) или его солью является 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота или ее соль.
В одном из вариантов осуществления соединением формулы (I) или его солью является (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота или ее соль.
В одном из вариантов осуществления соединением формулы (I) или его солью является (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота или ее соль.
В конкретном варианте осуществления соединением формулы (I) или его солью является 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота или ее фармацевтически приемлемая соль.
В конкретном варианте осуществления соединением формулы (I) или его солью является (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота или ее фармацевтически приемлемая соль.
В конкретном варианте осуществления соединением формулы (I) или его солью является (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота или ее фармацевтически приемлемая соль.
В более конкретном варианте осуществления соединением формулы (I) или его солью является 2-амино-2-(гидроксиметил)-1,3-пропандиольная соль 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты.
В более конкретном варианте осуществления соединением формулы (I) или его солью является 2-амино-2-(гидроксиметил)-1,3-пропандиольная соль (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты.
В альтернативном варианте осуществления соединением формулы (I) или его солью является 2-амино-2-(гидроксиметил)-1,3-пропандиольная соль (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты.
В объем настоящего изобретения включены все возможные стехиометрические и нестехиометрические формы солей соединений формулы (I).
Некоторые соединения формулы (I) или их соли могут существовать в форме сольватов. Как использовано в данном описании, термин ʺсольватʺ означает комплекс переменной стехиометрии, образованный растворенным компонентом (в настоящем изобретении соединение формулы (I) или его соль) и растворителем. Такие растворители для целей настоящего изобретения не должны вмешиваться в биологическую активность данного растворенного компонента. Примеры подходящих растворителей включают воду, метанол, этанол и уксусную кислоту. Если используемым растворителем является вода, данный сольват может быть назван гидратом.
Некоторые соединения формулы (I) способны существовать в стереоизомерных формах. Следует понимать, что настоящее изобретение включает все геометрические и оптические изомеры этих соединений и их смеси, включая рацематы. Различные стереоизомерные формы могут быть отделены один от другого способами, известными в данной области техники (например, разделением хиральной ВЭЖХ) или любой данный изомер может быть получен стереоспецифическим или асимметрическим синтезом. Настоящее изобретение также предоставляет любую из таутомерных форм и их смеси.
Настоящее изобретение также включает изотопно-меченные соединения и соли, которые идентичны соединениям формулы (I) или их солям, но по причине того, что один или более атомов заменены атомом, имеющим атомную массу или численную массу, отличную от атомной или численной массы, обычно встречающейся в природе. Примерами изотопов, которые могут быть включены в соединения формулы (I) или их соли являются изотопы водорода, углерода, азота, фтора, такие как 3H, 11C, 14C и 18F. Такие изотопно-меченные соединения формулы (I) или их соли полезны в распространенных анализах лекарственных средств и/или субстратов тканей. Например, изотопы 11C и 18F особенно полезны в ПЭТ (позитронно-эмиссионная томография). ПЭТ является полезным в томографии головного мозга. Изотопно-меченные соединения формулы (I) и их соли, как правило, могут быть получены путем осуществления методик, описанных ниже, заменой немеченного изотопом реагента легкодоступным изотопно-меченным реагентом. В одном из вариантов осуществления соединения формулы (I) или их соли являются немеченными изотопом.
Для того чтобы применять соединения формулы (I) в терапии, их обычно формулируют в фармацевтическую композицию в соответствии со стандартной фармацевтической практикой.
В дополнительном аспекте настоящее изобретение предоставляет фармацевтическую композицию, которая содержит a) соединение формулы (I) или его фармацевтически приемлемую соль; и b) один или более фармацевтически приемлемых эксципиентов.
В одном из вариантов осуществления соединением формулы (I) или его фармацевтически приемлемой солью является 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота или ее фармацевтически приемлемые соли.
В дополнительном аспекте настоящее изобретение предоставляет фармацевтическую композицию, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или эксципиент.
В дополнительном аспекте настоящее изобретение предоставляет способ получения фармацевтической композиции, включающий смешивание соединения формулы (I) или его фармацевтически приемлемой соли и фармацевтически приемлемого носителя или эксципиента.
Фармацевтическая композиция настоящего изобретения, которая может быть получена смешением, соответственно при температуре окружающей среды и атмосферном давлении, обычно адаптируется для перорального, парентерального или ректального введения и, таким образом, может быть в форме таблеток, капсул, жидких препаратов для перорального введения, порошков, гранул, таблеток для рассасывания, восстанавливаемых порошков, инъекционных растворов или растворов для инфузии, или суспензий, или суппозиториев.
В одном из вариантов осуществления инъекционные растворы или растворы для инфузии, или восстанавливаемые порошки являются предпочтительными.
В альтернативном варианте осуществления композиция, адаптированная для перорального введения, является предпочтительной.
Таблетки и капсулы для перорального введения могут быть в единичной дозированной форме и могут содержать общепринятые эксципиенты, такие как связующие агенты (например, предварительно желатинизированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактозу, микрокристаллическую целлюлозу или гидрофосфат кальция); лубриканты для таблеток (например, стеарат магния, тальк или диоксид кремния); дезинтегранты (например, картофельный крахмал или натрийгликолятный крахмал); и приемлемые смачивающие агенты (например, лаурилсульфат натрия). Таблетки могут быть покрыты согласно методам, хорошо известным в нормальной фармацевтической практике.
Жидкие препараты для перорального введения могут быть в форме, например, водной или масляной суспензии, растворов, эмульсий, сиропов или эликсиров, или могут быть в форме сухого продукта для восстановления в воде или другом подходящем базовом растворе перед применением. Такие жидкие препараты могут содержать общепринятые добавки, такие как суспендирующие агенты (например, сорбитовый сироп, производные целлюлозы или гидрогенизированные пищевые жиры), эмульгирующие агенты (например, лецитин или аравийская камедь), безводные базовые растворы (которые могут включать пищевые масла, например, миндальное масло, маслянистые сложные эфиры, этиловый спирт или фракционированные растительные масла), консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота) и, если требуется, общепринятые ароматизаторы или красители, буферные соли и подсластители при необходимости. Препараты для перорального введения могут быть соответствующим образом сформулированы, с получением препарата с контролируемым высвобождением активного соединения.
Для парентерального введения, жидкие единичные дозированные формы получают с использованием соединения настоящего изобретения или его фармацевтически приемлемой соли и стерильного базового раствора. Составы для инъекций могут быть представлены в единичной дозированной форме, например в ампулах или в мультидозах, при использовании соединения настоящего изобретения или его фармацевтически приемлемой соли и стерильного базового раствора, необязательно с добавлением консерванта. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масле или водном растворителе, и могут содержать формулирующие агенты, такие как суспендируюшие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может быть в форме порошка для восстановления в подходящем базовом растворе, например стерильной не пирогенной воде, перед применением. Данное соединение, независимо от базового раствора и используемой концентрации, может быть или суспендировано или разведено в базовом растворе. При получении растворов для инъекций данное соединение может быть растворено и простерилизовано фильтрованием перед заполнением в подходящий флакон или ампулу и загерметизировано. Предпочтительно, адъюванты, такие как местный анестетик, консерванты и буферирующие агенты растворяют в данном базовом растворе. Для повышения стабильности, данная композиция может быть заморожена после заполнения флакона, и вода удалена в вакууме. Парентеральные суспензии получают по существу аналогичным образом, за исключением того, что данное соединение суспендируют в базовом растворе вместо растворения, и стерилизация не может быть достигнута путем фильтрования. Данное соединение может быть стерилизовано под воздействием этиленоксида перед суспендированием в стерильном базовом растворе. Предпочтительно, поверхностно-активное вещество или смачивающий агент включают в данную композицию для облегчения равномерного распределения данного соединения.
Лосьоны могут быть сформулированы с водной или масляной основой и, как правило, будут содержать также один или более эмульгирующих агентов, стабилизирующих агентов, диспергирующих агентов, суспендирующих агентов, сгущающих агентов или красителей. Капли могут быть сформулированы с водной или неводной основой, также содержащие один или более диспергирующих агентов, стабилизирующих агентов, солюбилизирующих агентов или суспендирующие агентов. Они также могут содержать консервант.
Соединения настоящего изобретения также могут быть сформулированы в ректальные композиции, такие как суппозитории или удерживающие клизмы, например, содержащие обычные суппозиторные основы, такие как масло какао или другие глицериды.
Соединения настоящего изобретения также могут быть сформулированы в виде депо препаратов. Такие составы длительного действующие могут вводиться имплантацией (например, подкожно или внутримышечно) или внутримышечной инъекцией. Таким образом, например, соединения настоящего изобретения могут быть сформулированы с подходящими полимерными или гидрофобными веществами (например, такими как эмульсия в приемлемом масле) или ионообменными смолами, или в виде умеренно растворимых производных, например, умеренно растворимая соль.
Для интраназального введения, соединения настоящего изобретения могут быть сформулированы в виде растворов для введения через устройство, подходящее для дозированных или однократных доз, или, альтернативно, в виде порошка с подходящим носителем для введения с использованием подходящего устройства для доставки. Таким образом, соединения формулы (I) могут быть сформулированы для перорального, буккального, парентерального, местного (включая офтальмологическое и назальное), депо или ректального введения или в форме, подходящей для введения ингаляцией или инсуффляцией (либо через рот или нос).
Соединения настоящего изобретения могут быть сформулированы для местного введения в форме мазей, кремов, гелей, лосьонов, вагинальных суппозиториев, аэрозолей или капель (например, глазных, ушных или капель в нос). Мази и кремы, например, могут быть сформулированы с водной или масляной основой при добавлении подходящих сгущающих и/или гелирующих агентов. Мази для введения в глаза могут быть изготовлены в стерильном виде с использованием стерильных компонентов.
Данная композиция может содержать от 0,1% до 99% по массе, предпочтительно от 10 до 60% по массе активного вещества в зависимости от способа введения. Доза данного соединения, используемая при лечении перечисленных выше расстройств, будет варьироваться обычным путем в зависимости от серьезности данного расстройства, массы пациента и других аналогичных факторов. Однако, в качестве общей рекомендации, подходящие единичные дозы могут составлять 0,05-5000 мг, 1,0-500 мг или 1,0-200 мг, и такие единичные дозы могут вводиться более чем один раз в день, например, два или три раза в день. Такая терапия может быть продлена на несколько недель, месяцев или лет.
Поэтому соединения формулы (I) и их фармацевтически приемлемые соли предназначены для применения в лечении состояний или расстройств, которые опосредованы KMO. В частности, соединения формулы (I) и их фармацевтически приемлемые соли полезны при лечении острого панкреатита, хронической болезни почек, других состояний, связанных с синдромом системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, острой тяжелой печеночной энцефалопатией или острой печеночной недостаточностью.
В одном из вариантов осуществления соединения формулы (I) и их фармацевтически приемлемые соли полезны при лечении острого панкреатита, других состояний, связанных с синдромом системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, острой тяжелой печеночной энцефалопатией или острой печеночной недостаточностью.
Следует понимать, что "лечение", как использовано в данном описании, включает профилактику, а также облегчение установленных симптомов, признаков и особенностей заболевания.
В дополнительном аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения в терапии.
Настоящее изобретение, кроме того, предоставляет способ лечения состояний или расстройств у млекопитающих, включая людей, которые могут быть опосредованы KMO, включающий введение страдающему пациенту терапевтически безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
Настоящее изобретение, кроме того, предоставляет способ лечения острого панкреатита, других состояний, связанных с синдромом системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, острой тяжелой печеночной энцефалопатией или острой печеночной недостаточностью, включающий введение страдающему пациенту терапевтически безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
Настоящее изобретение, кроме того, предоставляет способ лечения острого панкреатита, включающий введение страдающему пациенту терапевтически безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
Настоящее изобретение, кроме того, предоставляет способ лечения хронической болезни почек, включающий введение страдающему пациенту терапевтически безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет применение соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для применения при лечении состояний или расстройств, опосредованных KMO.
В другом аспекте настоящее изобретение предоставляет применение соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для применения в лечении острого панкреатита, других состояний, связанных с синдром системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, тяжелой острой печеночной энцефалопатией или острой печеночной недостаточностью.
В другом аспекте настоящее изобретение предоставляет применение соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для применения при лечении острого панкреатита.
В другом аспекте настоящее изобретение предоставляет применение соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для применения при лечении хронической болезни почек.
В другом аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения при лечении состояний или расстройств, опосредованных KMO.
В другом аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения при лечении острого панкреатита, других состояний, связанных с синдромом системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, тяжелой острой печеночной энцефалопатией или острой печеночной недостаточностью.
В другом аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения при лечении острого панкреатита.
В другом аспекте настоящее изобретение предоставляет соединение формулы (I) или его фармацевтически приемлемую соль для применения при лечении хронической болезни почек.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию для применения при лечении острого панкреатита, хронической болезни почек, других состояний, связанных с синдром системного воспалительного ответа (SIRS), болезнью Хантингтона, болезнью Альцгеймера, спиноцеребеллярной атаксией, болезнью Паркинсона, комплексом СПИД-деменции, амиотрофическим боковым склерозом (ALS), депрессией, шизофренией, сепсисом, кардиогенным шоком, тяжелой травмой, острым повреждением легких, острым респираторным дистресс-синдромом, острым холециститом, тяжелыми ожогами, пневмонией, обширными хирургическими вмешательствами, ишемией кишечника, острой тяжелой болезнью печени, тяжелой острой печеночной энцефалопатией или острой печеночной недостаточностью, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов.
Соединения формулы (I), где X представляет собой связь или -CH2-, может быть синтезировано по существу согласно реакционной схеме 1.
Схема реакций 1

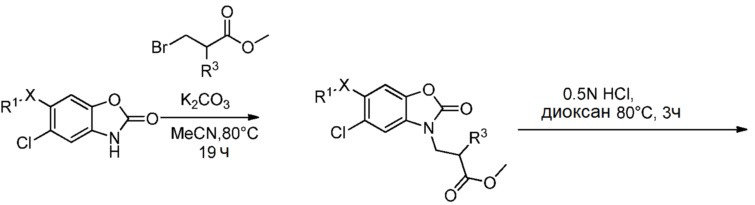
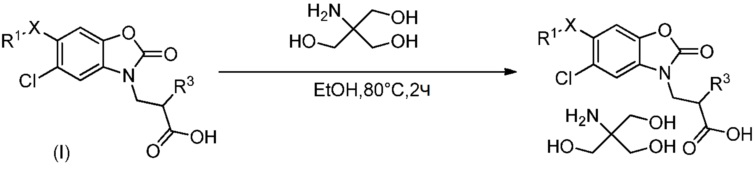
Соединения формулы (I), где X представляет собой -O-, может быть синтезировано по существу согласно реакционной схеме 2.
Схема реакций 2


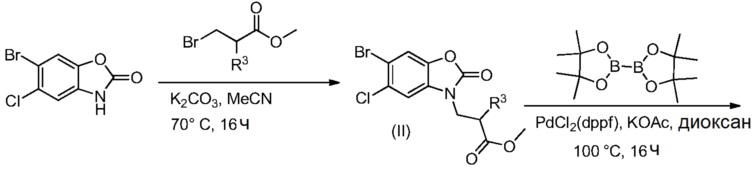

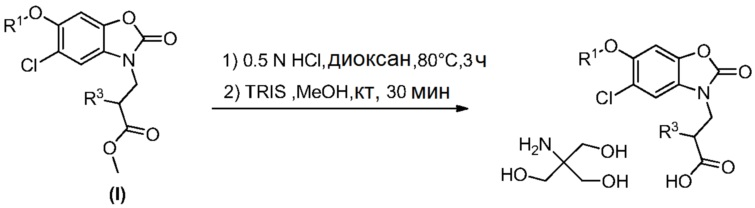
Метил 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноат (II) может быть использован для синтеза соединения формулы (I), где X представляет собой связь или -CH2-.
Специалисту в данной области техники будет очевидно, что может быть необходима защита определенных реакционноспособных фторсодержащих заместителей в ходе некоторых из указанных выше синтезов. Могут быть использованы технологии стандартной защиты и удаления защиты, описанные в Greene T.W. Protective groups in organic synthesis, New York, Wiley (1981). Например, первичные амины могут быть защищены в виде фталимидных, трифторацетильных, бензильных, трет-бутилоксикарбонильных, бензилоксикарбонильных или тритильных производных. Группы карбоновой кислоты могут быть защищены в виде сложных эфиров. Группы альдегидов или кетонов могут быть защищены в виде ацеталей, кеталей, тиоацеталей или тиокеталей. Удаление защиты с таких групп осуществляют с использованием общепринятых методик, хорошо известных в данной области техники. Например, защитные группы, такие как трет-бутилоксикарбонил, можно удалить при использовании кислоты, такой как хлористоводородная или трифторуксусная кислота, в подходящем растворителе, таком как дихлорметан, простой диэтиловый эфир, 1,4-диоксан, изопропанол или их смеси.
Некоторые соединения формулы (I) также являются коммерчески доступными, включая 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановую кислоту.
Примеры
Следующие примеры иллюстрируют настоящее изобретение. Эти примеры не предназначены для ограничения объема настоящего изобретения, но скорее для того, чтобы рекомендовать специалистам в данной области методики получения и применения данных соединений, композиций и способов настоящего изобретения. Хотя описаны конкретные варианты осуществления настоящего изобретения, специалисту в данной области будет очевидно, что возможны различные изменения и модификации, не отходя от существа и объема настоящего изобретения.
Все публикации, включая, но, не ограничиваясь ими, патенты и патентные заявки, на которые ссылаются в данном описании, включены посредством ссылки, как если бы каждая индивидуальная публикация была конкретно и индивидуально включена в данное описание в виде ссылки во всей ее полноте.
Следующие примеры промежуточных соединений и примеры иллюстрируют получение соединений настоящего изобретения.
Аббревиатуры
DCM - дихлорметан
DEAD - диэтилазодикарбоксилат
ДМСО - диметилсульфоксид
ч - час(ы)
ЖХМС - жидкостная хроматография-масс-спектрометрия
MeCN - ацетонитрил
мин - минуты
ЯМР - ядерно-магнитный резонанс
RT/Rt: - время удерживания
ТГФ - тетрагидрофуран
TFA - трифторуксусная кислота
TRIS - 2-амино-2-(гидроксиметил)-1,3-пропандиол
Условия ЖХМС
ЖХМС метод A/B/C
Agilent 1200-6110.
Уровень сигнала: сигнал A: 214 нм, сигнал B: 254 нм;
Температура колонки: 40°C.
Колонка: HALO C18 4,6*50 мм, 2,7 мкМ.
1,00 мин: A: 5,0% B: 95,0%
2,00 мин: A: 5,0% B: 95,0%
2,01 мин: A: 95,0% B: 5,0%
2,50 мин: A: 95,0% B: 5,0%
1,00 мин: A: 5,0% B: 95,0%
2,00 мин: A: 5,0% B: 95,0%
2,01 мин: A: 95,0% B: 5,0%
2,50 мин: A: 95,0% B: 5,0%
1,00 мин: A: 5,0% B: 95,0%
2,00 мин: A: 5,0% B: 95,0%
2,01 мин: A: 95,0% B: 5,0%
2,50 мин: A: 95,0% B: 5,0%
ЖХМС метод D/E
Аналитическую ВЭЖХ проводили на X-Terra MS C18 колонке (3,5 мкм 30×4,6 мМ id), элюируя 0,01M ацетатом аммония в воде (растворитель A) и 100% ацетонитрилом (растворитель B), с использованием следующего градиента элюирования 0-4 минуты: 5-100% B, 4-5 минуты 100% B, при скорости потока 1,4 мл/минута при 40°C.
Масс-спектр (МС) снимали на масс-спектрометре Waters ZQ с использованием положительной ионизации с электрораспылением [ES+ дает MH+ молекулярные ионы] или отрицательной ионизации с электрораспылением [ES- дает (M-H)- молекулярные ионы]. Конусное напряжение: 20 В (метод D) или 40 В (метод E).
ЖХМС метод F/G
Подвижная фаза: A: 0,1% муравьиная кислота в воде
B: 0,1% муравьиная кислота в MeCN
Время (мин)/%B: 0/3, 0,4/3, 3,2/98, 3,8/98, 4,2/3, 4,5/3
Температура колонки: 35°C
Скорость потока: 0,6 мл/мин
Подвижная фаза: A: 5 мм бикарбонат аммония в воде (pH~10); B: MeCN
Время (мин)/%B: 0/5, 0,5/5, 1/15, 3,3/98, 5,2/98, 5,5/5, 6/5
Температура колонки: 35°C
Скорость потока: 1,3 мл/мин
Промежуточное соединение 1: 4-Хлор-5-метил-2-нитрофенол
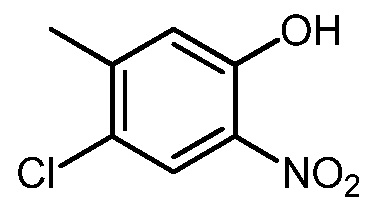
4-Хлор-3-метилфенол (500 г, 3,51 моль) растворяли в уксусной кислоте (2,5 л) при 10°C, затем по каплям добавляли азотную кислоту (70%, 410 г, 4,56 моль) и выдерживали при температуре <30°C. После завершения добавления, полученную смесь перемешивали при температуре от 20 до 30°C в течение 1 ч. После завершения реакции, реакционную смесь фильтровали, твердое вещество тщательно промывали уксусной кислотой (200 мл) и водой (500 мл), твердое вещество собирали и сушили на воздухе, с получением 4-хлор-5-метил-2-нитрофенола в виде желтого твердого вещества (308 г, 47%).
1H ЯМР (300 МГц, CDCl3) δ 10,43 (с, 1H), 8,09 (с, 1H), 7,05 (с, 1H), 2,43 (с, 3H).
Промежуточное соединение 2: 2-Амино-4-хлор-5-метилфенол
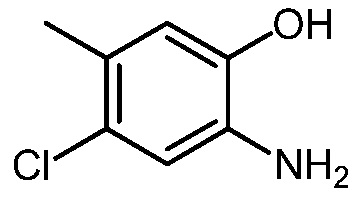
4-Хлор-5-метил-2-нитрофенол (промежуточное соединение 1, 150 г, 0,802 моль), трихлорид железа (15 г, 10% масс), активированный уголь (15 г, 10% масс) в метаноле (600 мл) и реакционную смесь нагревали до 80°C. По каплям добавляли гидразингидрат (80%, 502 г, 8,02 моль), и реакционную смесь перемешивали при 80°C в течение 15 ч. Реакционную смесь фильтровали, фильтраты собирали, растворитель удаляли, и остаток растворяли в этилацетате (300 мл). Этилацетатный раствор промывали водой (200 мл), затем насыщенным раствором соли (200 мл ×3) и сушили над сульфатом натрия. Растворитель удаляли, с получением 2-амино-4-хлор-5-метилфенола в виде фиолетового твердого вещества (100 г, 79%).
ЖХМС (A): Rt 1,32 мин, MH+ 158/160.
Промежуточное соединение 3: 5-Хлор-6-метилбензо[d]оксазол-2(3H)-он
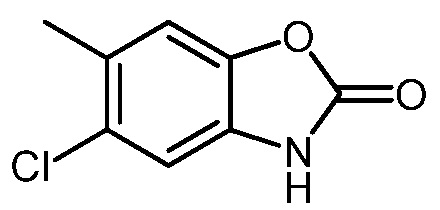
Смесь 2-амино-4-хлор-5-метилфенола (промежуточное соединение 2, 100 г, 0,637 моль), N,N'-карбонилдиимидазола (155 г, 0,955 моль) в ТГФ (500 мл) перемешивали при 66°C в течение 1 ч, растворитель удаляли, и остаток разбавляли водой (1 л). Твердое вещество отделяли фильтрованием, растворяли в этилацетате (500 мл) и сушили над сульфатом натрия. Полученную смесь фильтровали, и растворитель из фильтрата выпаривали при пониженном давлении, с получением 5-хлор-6-метилбензо[d]оксазол-2(3H)-она в виде желтого твердого вещества (100 г, 86%).
1H ЯМР (300 МГц, d6-ДМСО) δ 11,73 (шир.с, 1H), 7,35 (с, 1H), 7,16 (с, 1H), 2,34 (с, 3H).
Промежуточное соединение 4: 4-Хлор-1-метокси-2-нитробензол
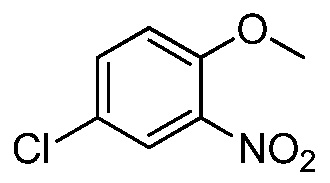
Гидроксид натрия (44,16 г, 1,104 моль) растворяли в метаноле (500 мл), и метанольный раствор добавляли к 1,4-дихлор-2-нитробензолу (100 г, 0,521 моль) в метаноле при 70°C. После добавления, реакционную смесь перемешивали при 70°C в течение 2 ч, затем охлаждали и выливали в воду (3 л). Твердое вещество отделяли фильтрованием и промывали водой (2 л), с получением 4-хлор-1-метокси-2-нитробензола в виде бледно-желтого твердого вещества (93 г, 95%).
1H ЯМР (300 МГц, CDCl3) δ 7,83 (д, J=2,4 Гц, 1H), 7,50 (дд, J=8,7 Гц, J=2,4 Гц, 1H), 7,03 (д, J=8,7 Гц, 1H), 3,95 (с, 3H).
Промежуточное соединение 5: 5-Хлор-2-метоксианилин
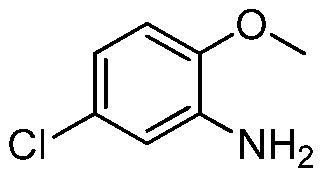
Гидразингидрат (80%, 186 г, 2,975 моль) по каплям добавляли к кипящей с обратным холодильником смеси 4-хлор-1-метокси-2-нитробензола (промежуточное соединение 4, 93 г, 0,496 моль), трихлорида железа (9,3 г, 10% масс) и активированного угля (9,3 г, 10% масс) в метаноле (1 л). После добавления, реакционную смесь перемешивали при кипячении с обратным холодильником в течение 16 ч, реакционную смесь фильтровали и растворитель выпаривали из фильтрата в вакууме. Остаток промывали петролейным эфиром (2 л), с получением 5-хлор-2-метоксианилина в виде белого твердого вещества (76,7 г, 98%).
1H ЯМР (300 МГц, CDCl3) δ 6,67-6,65 (м, 3H), 3,83 (шир.с, 2H), 3,81 (с, 3H).
Промежуточное соединение 6: 4-Бром-5-хлор-2-метоксианилин
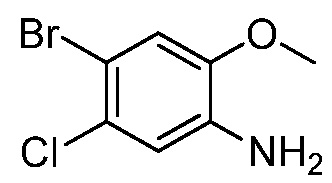
Смесь 5-хлор-2-метоксианилина (промежуточное соединение 5, 76,7 г, 0,487 моль) в ацетонитриле (500 мл) при 0°C обрабатывали N-бромсукцинимидом (86,7 г, 0,487 моль) путем добавления порциями около 2 ч. После добавления, растворитель удаляли, и остаток очищали колоночной хроматографией (диоксид кремния: 200-300 меш, 200 г), элюируя смесью петролейный эфир/этилацетат от 20:1 до 4:1), с получением 4-бром-5-хлор-2-метоксианилина в виде светло-желтого твердого вещества (40,2 г, 35%).
ЖХМС (A): Rt 1,63 мин, MH+ 236/238.
1H ЯМР (300 МГц, CDCl3) δ 6,93 (с, 1H), 6,78 (с, 1H), 3,83 (с, 3H).
Промежуточное соединение 7: 2-Амино-5-бром-4-хлорфенол
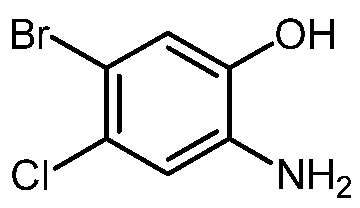
4-Бром-5-хлор-2-метоксианилин (промежуточное соединение 6, 10g, 42,3 ммоль) в DCM (200 мл) охлаждали до 0°C. Трибромид бора (21,2 г, 84,6 ммоль) по каплям добавляли около 30 мин, реакционную смесь перемешивали при 0°C в течение 1 час и затем при комнатной температуре в течение 14 ч. Реакционную смесь выливали в ледяную воду, добавляли гидрокарбонат натрия для доведения до pH>7, и водный слой экстрагировали этилацетатом (300 мл ×3). Органическую фазу сушили над сульфатом магния, и растворитель удаляли в вакууме, с получением 2-амино-5-бром-4-хлорфенола в виде красного твердого вещества (8,4 г, 89%, используемого без дополнительной очистки на следующей стадии).
ЖХМС (A): Rt 1,46 мин, MH+ 222/224.
Промежуточное соединение 8: 6-Бром-5-хлорбензо[d]оксазол-2(3H)-он
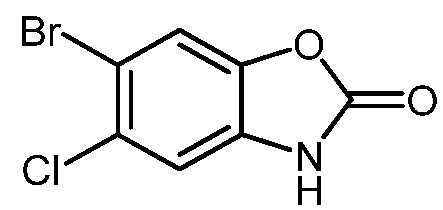
Смесь 2-амино-5-бром-4-хлорфенола (промежуточное соединение 7, 8,4 г, 37,8 ммоль), N,N-карбонилдиимидазола (12,2 г, 75,6 ммоль) в ТГФ (250 мл) нагревали при 80°C в течение ч. Растворитель удаляли в вакууме, и остаток очищали колоночной хроматографией (диоксид кремния: 200-400 меш, 100 г), элюируя смесью петролейный эфир/этилацетат от 9:1 до 5:1), с получением 6-бром-5-хлорбензо[d]оксазол-2(3H)-она в виде оранжевого твердого вещества (7,7 г, 82%).
ЖХМС (A): Rt 1,49 мин, MH+ 248/250.
Промежуточное соединение 9: Метил 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноат
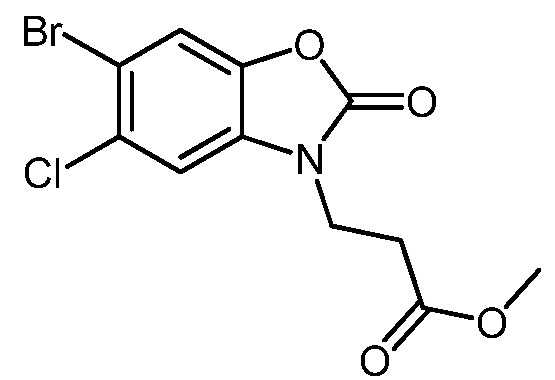
Смесь 6-бром-5-хлорбензо[d]оксазол-2(3H)-она (промежуточное соединение 8, 7,7 г, 31 ммоль), метил 3-бромпропаноата (6,2 г, 37 ммоль), карбоната калия (8,5 г, 62 ммоль) в ацетонитриле (200 мл) перемешивали при 70°C в течение 16 ч, растворитель выпаривали в вакууме, остаток очищали колоночной хроматографией (диоксид кремния: 200-400 меш, 50 г), элюируя смесью петролейный эфир/этилацетат 4:1, с получением метил 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата в виде оранжевого твердого вещества (6,2 г, 62%).
ЖХМС (A): Rt 1,66 мин, MH+=334/336.
Промежуточное соединение 10: Метил 3-(5-хлор-2-оксо-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензо[d]оксазол-3(2H)-ил)пропаноат
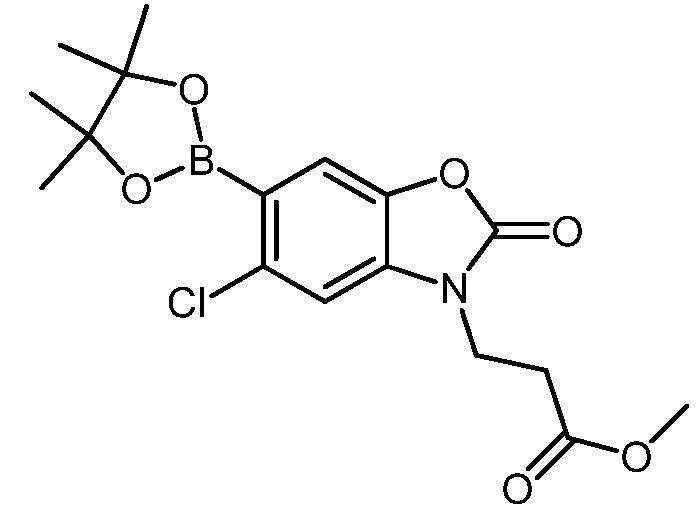
Смесь метил 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата (промежуточное соединение 9, 5,2 г, 15,56 ммоль), бис(пинаколато)диборона (11,8 г, 46,7 ммоль), [1,1'-бис(дифенилфосфоно)ферроцен]дихлорпалладия (II) (568 мг, 0,778 ммоль), ацетата калия (3 г, 31,12 ммоль) в 1, 4-диоксане (500 мл) перемешивали при 100°C в течение 16 час в атмосфере азота. Растворитель выпаривали в вакууме, и остаток очищали колоночной хроматографией (диоксид кремния: 200-300 меш, 80 г), элюируя смесью петролейный эфир/этилацетат=9:1, затем 8:1), с получением метил 3-(5-хлор-2-оксо-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензо[d]оксазол-3(2H)-ил)пропаноата в виде желтого масла (5,2 г, 87%).
ЖХМС (A): Rt 1,73 мин, MH+ 382/384.
Промежуточное соединение 11: Метил 3-(5-хлор-6-гидрокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноат
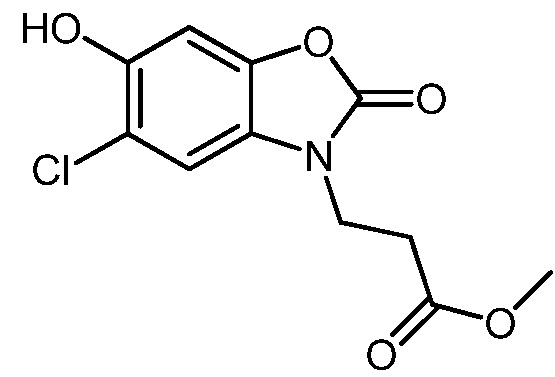
Смесь метил 3-(5-хлор-2-оксо-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензо[d]оксазол-3(2H)-ил)пропаноата (промежуточное соединение 10, 5,2 г, 13,6 ммоль) в пероксиде водорода (30%, 12 мл), уксусной кислоты (10 мл) и ТГФ (100 мл) перемешивали при комнатной температуре в течение 16 ч. Добавляли воду, полученную смесь экстрагировали этилацетатом (100 мл ×3), органическую фазу сушили над сульфатом магния, и растворитель выпаривали в вакууме. Остаток очищали колоночной хроматографией (диоксид кремния: 200-300 меш, 50 г), элюируя смесью петролейный эфир/этилацетат=9:1, 8:1, 6:1, 4:1), с получением метил 3-(5-хлор-6-гидрокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата в виде желтого твердого вещества (2,5 г, 68%).
ЖХМС (A): Rt 1,32 мин, MH+ 272.
Промежуточное соединение 12: Метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноат
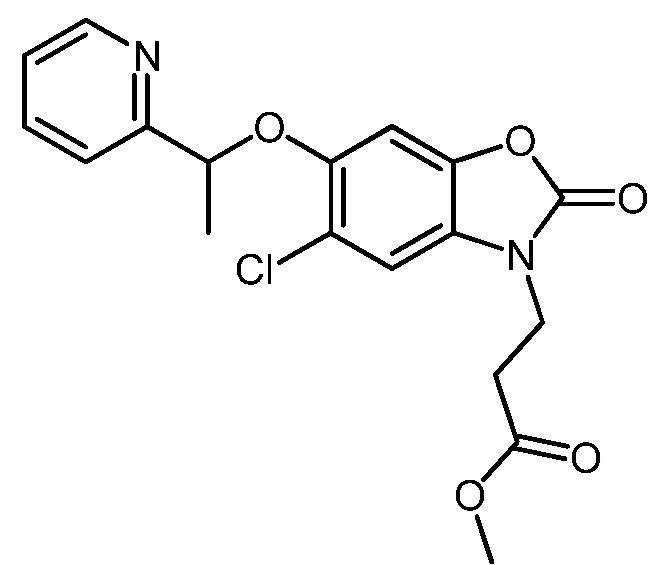
1-(Пиридин-2-ил)этанол (71 мг, 0,57 ммоль), диэтилазодикарбоксилат (84 мг, 0,48 ммоль) и трифенилфосфин (126 мг, 0,48 ммоль) добавляли в метил 3-(5-хлор-6-гидрокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноат (промежуточное соединение 11, 0,13 г, 0,48 ммоль) в толуоле (10 мл), и реакционную смесь перемешивали при комнатной температуре в течение 2 дней. Реакционную смесь выливали в воду (15 мл), водный слой экстрагировали этилацетатом (10 мл ×3), органические слои объединяли и сушили над сульфатом натрия, и частично очищали колоночной хроматографией [диоксид кремния: 200-300 меш, 10 г], элюируя смесью петролейный эфир/этилацетат=4:1], с получением метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата в виде белого твердого вещества (270 мг, неочищенный).
ЖХМС (A): Rt 1,57 мин, MH+ 377.
Промежуточное соединение 13: (R)-Метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноат
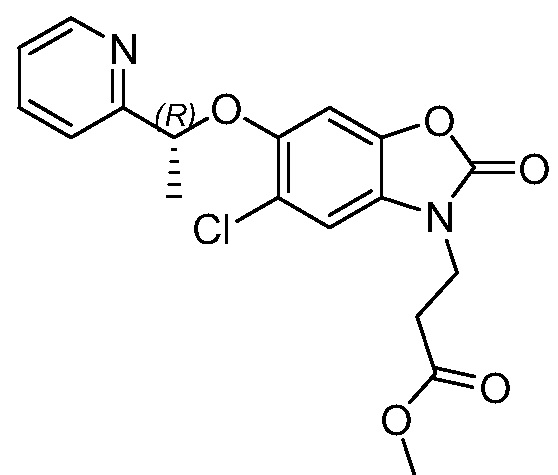
К метил 3-(5-хлор-6-гидрокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноату (промежуточное соединение 11, 133 мг, 0,49 ммоль) в толуоле (10 мл) добавляли (S)-1-(пиридин-2-ил)этанол (60 мг, 0,49 ммоль), трифенилфосфин (93 мг, 0,74 ммоль), диэтилазодикарбоксилат (129 мг, 0,74 ммоль), и полученную реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Растворитель удаляли, и остаток очищали колоночной хроматографией (диоксид кремния: 200-300 меш, 5 г), элюируя смесью петролейный эфир/этилацетат 5:1, с получением (R)-метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата в виде бесцветного масла (170 мг, 90%).
ЖХМС (A): Rt 1,40 мин, MH+=377/379.
Промежуточное соединение 14: (S)-метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноат
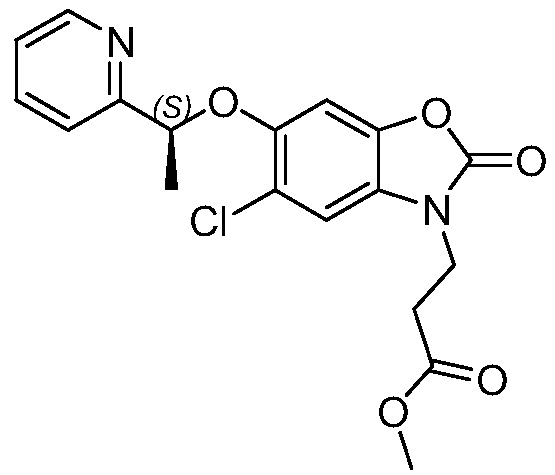
К метил 3-(5-хлор-6-гидрокси-2-оксобензо[d]оксазол-3(2H)-ил)пропаноату (промежуточное соединение 11, 133 мг, 0,49 ммоль) в толуоле (10 мл) добавляли (R)-1-(пиридин-2-ил)этанол (60 мг, 0,49 ммоль), трифенилфосфин (193 мг, 0,74 ммоль), диэтилазодикарбоксилат (129 мг, 0,74 ммоль), полученную реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Растворитель удаляли, и остаток очищали колоночной хроматографией (диоксид кремния: 200-300 меш, 5 г), элюируя смесью петролейный эфир/этилацетат 5:1), с получением (S)-метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата в виде бесцветного масла (160 мг, 86%).
ЖХМС (A): Rt 1,60 мин, MH+=377/379.
Пример 1: 3-(5-Хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота
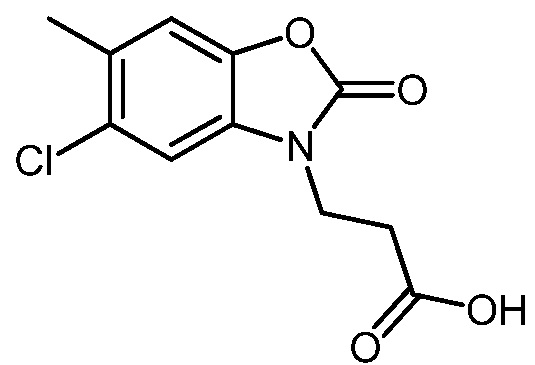
5-Хлор-6-метилбензо[d]оксазол-2(3H)-он (промежуточное соединение 3, 150 г, 0,82 моль), 3-бромпропановую кислоту (251 г, 1,64 моль), карбонат калия (226 г, 1,64 моль) смешивали в ацетонитриле (2 л), и полученную реакционную смесь перемешивали при 80°C в течение 18 ч. Реакционную смесь охлаждали до температуры окружающей среды и фильтровали. Твердое вещество собирали, подкисляли до pH 4~5 хлористоводородной кислотой (3Н) и экстрагировали этилацетатом (300 мл ×5). Объединенные органические фазы сушили над сульфатом натрия, фильтровали, фильтрат собирали, и растворитель выпаривали, с получением 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде желтого твердого вещества (220 г). Использовали без дополнительной очистки.
1H ЯМР (300 МГц, d6-ДМСО) δ 12,43 (шир.с, 1H), 7,51 (с, 1H), 7,36 (с, 1H), 4,00 (т, J=6 Гц, 2H), 2,70 (т, J=6 Гц, 2H), 2,33 (с, 3H).
Пример 1 (альтернативное получение): 3-(5-Хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота
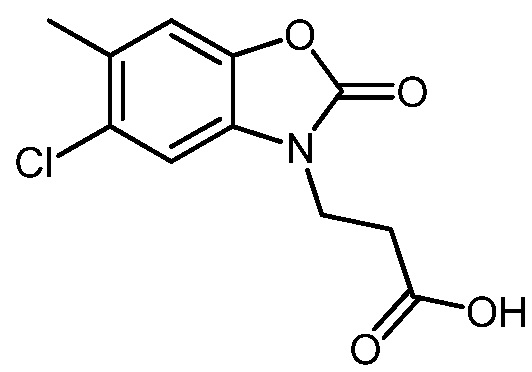
Смесь 5-хлор-6-метилбензо[d]оксазол-2(3H)-она (250 мг, 1,362 ммоль, коммерчески доступный), карбоната калия (565 мг, 4,09 ммоль) и 3-бромпропановой кислоты (417 мг, 2,72 ммоль) в ацетонитриле (10 мл) нагревали до 90°C и перемешивали в течение 2 ч. Полученную смесь охлаждали и фильтровали; выделенный белый порошок промывали ацетонитрилом, суспендировали в воде и подкисляли до pH 2 хлористоводородной кислотой (1Н). Полученное в результате твердое вещество затем растирали с горячим ацетонитрилом, фильтровали и сушили, с получением 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде белого порошка (225 мг, 64,6%).
ЖХМС (E): Rt 2,29 мин, [M-H]- 254/256
Пример 1a (Образование трис-соли): 2-Амино-2-(гидроксиметил)-1,3-пропандиольная соль 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты
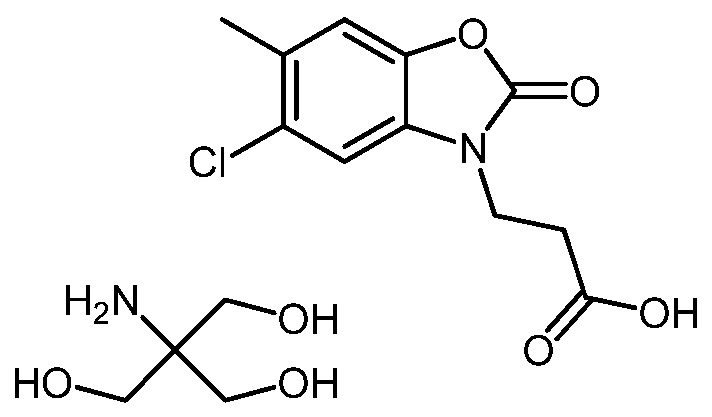
Смесь 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты (пример 1, 220 г, 0,863 моль), 2-амино-2-(гидроксиметил)пропан-1,3-диола (104,5 г, 0,863 моль) в этаноле (4 л) перемешивали при 80°C в течение 2 ч, реакционную смесь фильтровали, фильтрат собирали и охлаждали до температуры окружающей среды. Полученную смесь фильтровали, полученное твердое вещество промывали этанолом (200 мл) и сушили на воздухе, с получением 2-амино-2-(гидроксиметил)-1,3-пропандиольной соли 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде не совсем белого твердого вещества (150 г, 46%).
ЖХМС (A): Rt 1,41 мин, MH+ 256/258.
1H ЯМР (300 МГц, CD3OD) δ 7,37 (с, 1H), 7,16 (с, 1H), 4,05 (т, J=6 Гц, 2H), 3,64 (с, 6H), 2,59 (т, J=6 Гц, 2H), 2,37 (с, 3H).
Пример 2: 2-Амино-2-(гидроксиметил)-1, 3-пропандиольная соль 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты

Метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноат (промежуточное соединение 12, 270 мг) в хлористоводородной кислоте (0,5Н, 5 мл) добавляли к 1,4-диоксану (5 мл), и реакционную смесь перемешивали при 80°C в течение часа. Растворитель удаляли, остаток очищали препаративной ВЭЖХ [элюент: MeCN-вода (0,1% TFA), градиент: 60-90% MeCN], с получением 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде желтого масла (30 мг, 0,08 ммоль). Добавляли метанол (2 мл) и 2-амино-2-(гидроксиметил)-1,3-пропандиол (10 мг, 0,08 ммоль), и полученную реакционную смесь перемешивали при комнатной температуре в течение 30 минут. Полученную смесь концентрировали, с получением 2-амино-2-(гидроксиметил)-1,3-пропандиольной соли 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде желтого масла (40 мг, 17%).
ЖХМС (A): Rt 1,36 мин, MH+ 363.
1H ЯМР (300 МГц, CD3OD) δ 8,52 (д, J=6 Гц, 1H), 7,82 (т, J=6 Гц, 1H), 7,57 (д, J=9 Гц, 1H), 7,41 (с, 1H), 7,35-7,31 (м, 1H), 6,91 (с, 1H), 5,44 (дд, J=12, 6 Гц, 2H), 4,02 (т, J=6 Гц, 2H), 3,66 (с, 6H), 2,62 (т, J=6 Гц, 2H), 1,69 (д, J=6 Гц, 3H).
Пример 3: (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота
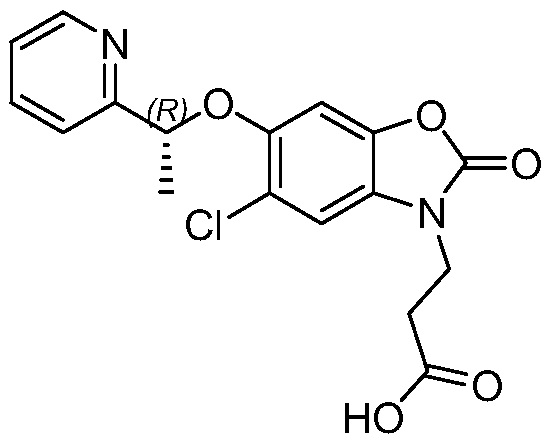
Хлористоводородную кислоту (0,5Н, 4 мл) добавляли к раствору (R)-метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноата (промежуточное соединение 13, 170 мг) в 1,4-диоксане (4 мл), и полученную реакционную смесь перемешивали при 80°C в течение 16 ч. Растворитель удаляли, и остаток очищали препаративной ВЭЖХ (ацетонитрил/вода (0,1% TFA) 20:80-70:30). Растворитель удаляли, и остаток дополнительно очищали сверхкритической жидкостной хроматографией (гексан/этанол 1:1, 0,2% TFA), с получением (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде желтого масла (30 мг, 18%).
ЖХМС (A): Rt 1,37 мин, MH+=363/365.
Пример 3a (Образование трис-соли): 2-Амино-2-(гидроксиметил)-1,3-пропандиольная соль (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты
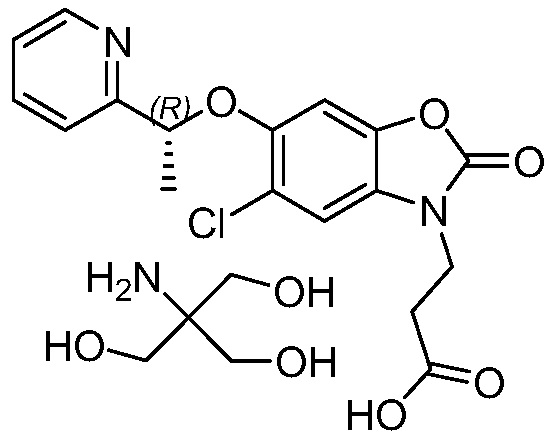
2-Амино-2-(гидроксиметил)пропан-1,3-диол (10 мг, 0,08 моль) добавляли к (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоте (пример 3 (свободная кислота), 30 мг, 0,08 ммоль) в метаноле (2 мл), полученную реакционную смесь перемешивали при температуре окружающей среды в течение 30 минут, и растворитель удаляли в вакууме, с получением 2-амино-2-(гидроксиметил)-1,3-пропандиольной соли (R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде желтого масла (40 мг, 100%).
ЖХМС (A): Rt 1,38 мин, MH+=363/365.
1H ЯМР (300 МГц, CD3OD) δ 8,51 (д, J=3 Гц, 1H), 7,82 (тд, J=9, 3 Гц, 1H), 7,57 (д, J=9 Гц, 1H), 7,42 (с, 1H), 7,34-7,33 (м, 1H), 6,91 (с, 1H), 5,43 (кв, J=6 Гц, 1H), 4,02 (т, J=6 Гц, 2H), 3,66 (с, 6H), 2,59 (т, J=6 Гц, 2H), 1,69 (д, J=6 Гц, 3H).
Хиральная ВЭЖХ: 214 нм (100,0%), 254 нм (100,0%).
Пример 4: (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановая кислота
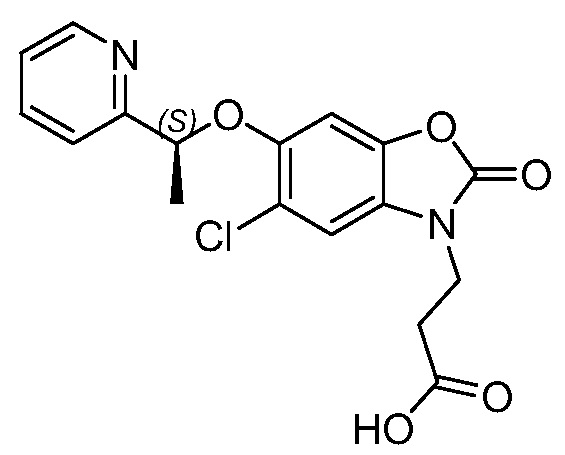
Хлористоводородную кислоту (0,5Н, 4 мл) добавляли к (S)-метил 3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропаноату (промежуточное соединение 14, 160 мг) в 1,4-диоксане (4 мл), и полученную реакционную смесь перемешивали при 80°C в течение 16 ч. Растворитель удаляли, остаток очищали препаративной ВЭЖХ (ацетонитрил/вода (0,1% TFA) 20:80-70:30). Растворитель удаляли, и остаток дополнительно очищали сверхкритической жидкостной хроматографией (гексан/этанол 1:1, 0,2% TFA), с получением (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты (23 мг, 5%).
ЖХМС (A): Rt 1,37 мин, MH+=363/365.
Хиральная ВЭЖХ: 214 нм (100,0%), 254 нм (100,0%).
Гидроксид натрия (44,16 г, 1,104 моль) растворяли в метаноле (500 мл), и полученные метанольные растворы добавляли к 1,4-дихлор-2-нитробензолу (100 г, 0,521 моль) в метаноле при 70°C. После добавления, реакционную смесь перемешивали при 70°C в течение 2 ч, затем охлаждали и выливали в воду (3 л). Твердое вещество отделяли фильтрованием и промывали водой (2 л), с получением 4-хлор-1-метокси-2-нитробензола в виде бледно-желтого твердого вещества (93 г, 95%).
Пример 4a (Образование трис-соли): 2-амино-2-(гидроксиметил)-1,3-пропандиольная соль (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты
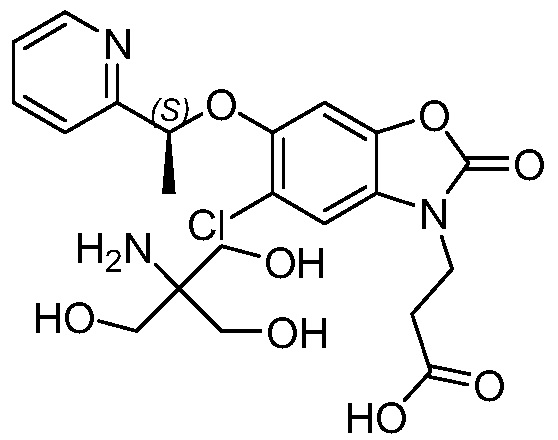
2-Амино-2-(гидроксиметил)пропан-1,3-диол (8 мг, 0,063 моль) добавляли к (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоте (пример 4 (свободная кислота), 23 мг, 0,063 ммоль) в метаноле (2 мл), и полученную реакционную смесь перемешивали при комнатной температуре в течение 30 мин. Растворитель удаляли, и остаток очищали препаративной ВЭЖХ (ацетонитрил/вода (0,1% TFA) 20:80-70:30). После удаления растворителя, добавляли метанол (2 мл) и 2-амино-2-(гидроксиметил)пропан-1,3-диол (3 мг, 0,024 ммоль), полученную реакционную смесь перемешивали при комнатной температуре в течение 30 мин. Удаление растворителя давало 2-амино-2-(гидроксиметил)-1,3-пропандиольную соль (S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты в виде коричневого твердого вещества (10 мг, 13%).
ЖХМС (A): Rt 1,37 мин, MH+=363/365.
1H ЯМР (300 МГц, CD3OD) δ 8,51 (д, J=3 Гц, 1H), 7,82 (тд J=9, 3 Гц, 1H), 7,57 (д, J=9 Гц, 1H), 7,42 (с, 1H), 7,34-7,33 (м, 1H), 6,91 (с, 1H), 5,43 (кв, J=6 Гц, 1H), 4,02 (т, J=6 Гц, 2H), 3,66 (с, 6H), 2,59 (т, J=6 Гц, 2H), 1,69 (д, J=6 Гц, 3H).
Хиральная ВЭЖХ: 214 нм (100,0%), 254 нм (100,0%).
1H ЯМР (300 МГц, CDCl3) δ 7,83 (д, J=2,4 Гц, 1H), 7,50 (дд, J=8,7 Гц, J=2,4 Гц, 1H), 7,03 (д, J=8,7 Гц, 1H), 3,95 (с, 3H).
Соединения примеров 5, 6, 8, 9, 11 и 25 получали методикой, по существу соответствующей схеме 1, или с использованием метил 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата (II). Соединения примеров 7, 10, 12-24 и 26-37 получали методикой, по существу аналогичной примеру 2, согласно схеме 2.
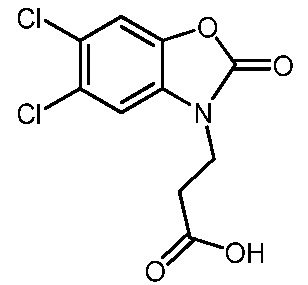
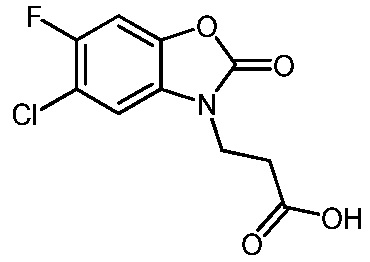

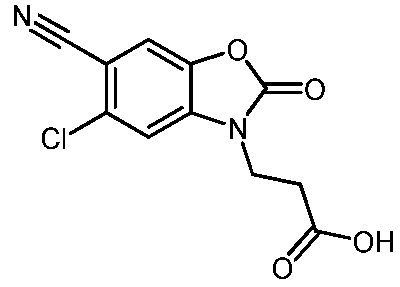
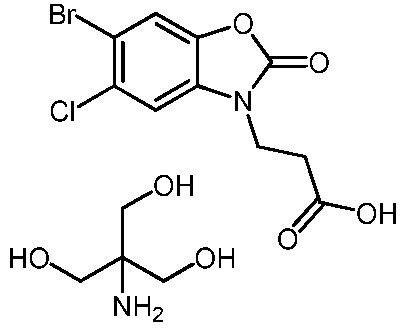
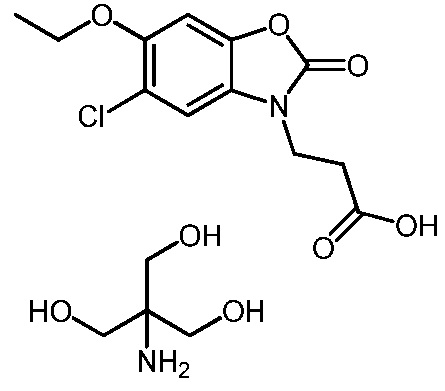
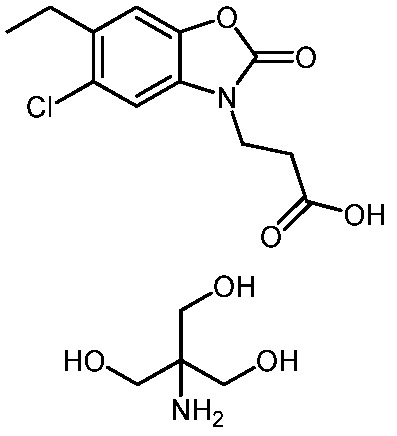
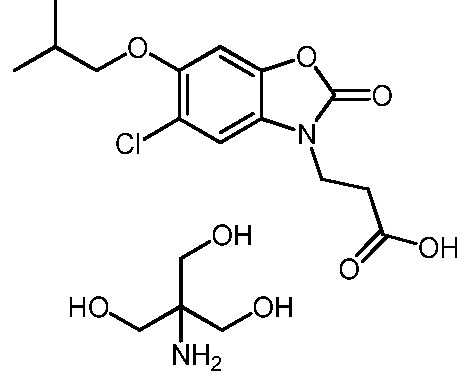
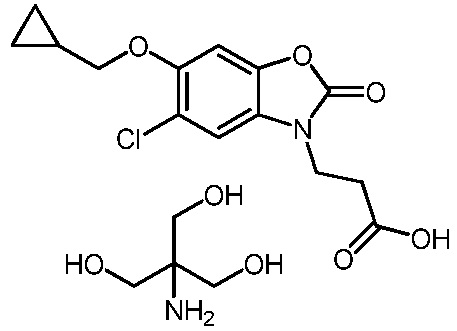
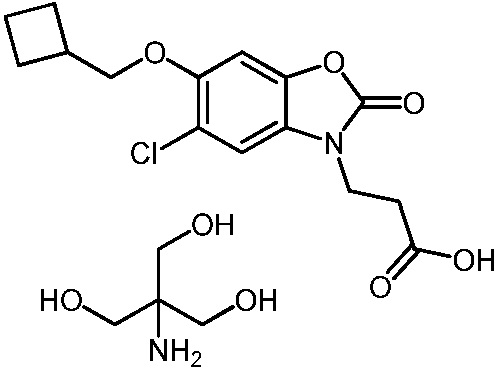
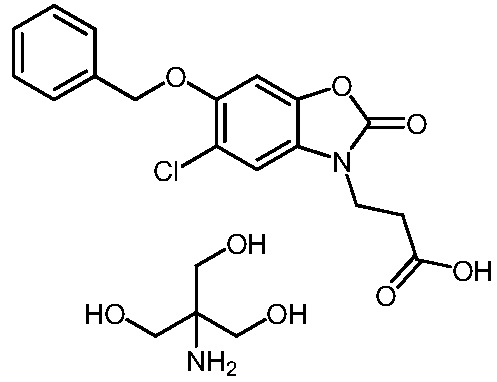
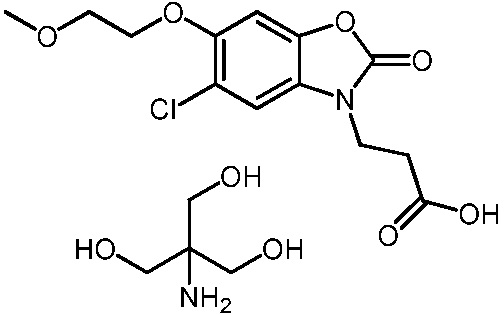

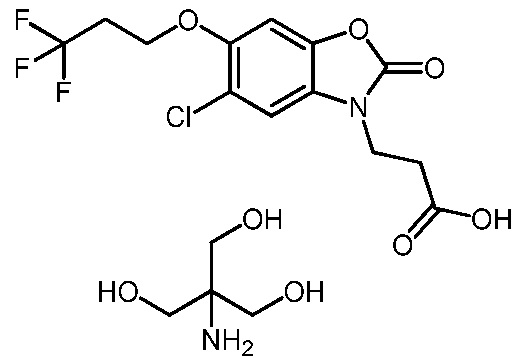
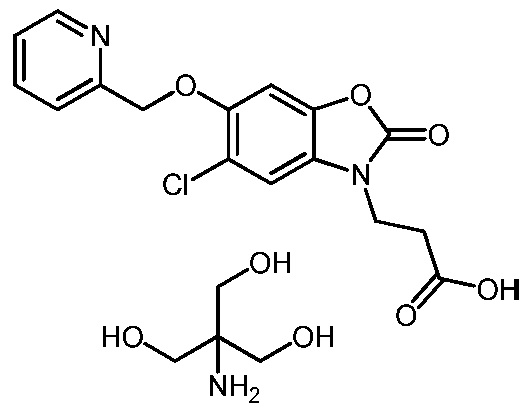
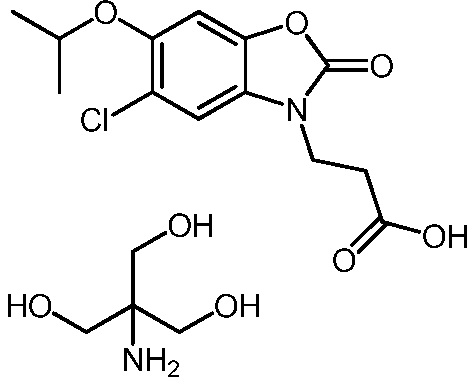
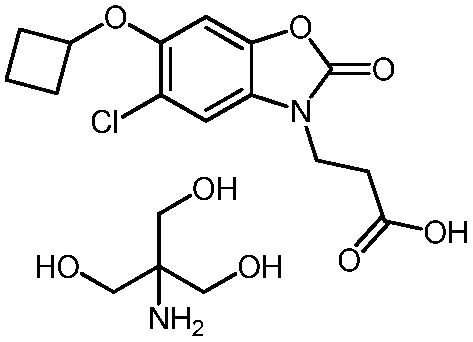
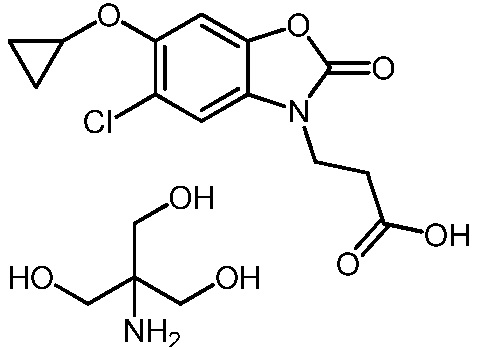
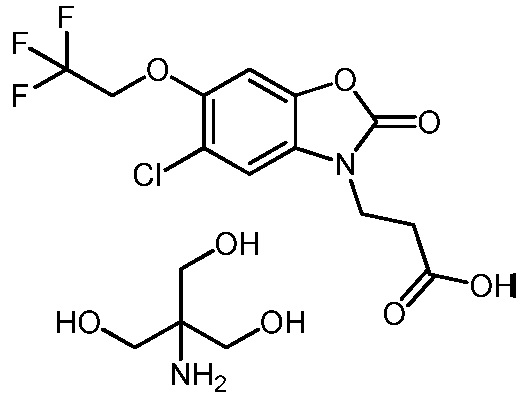
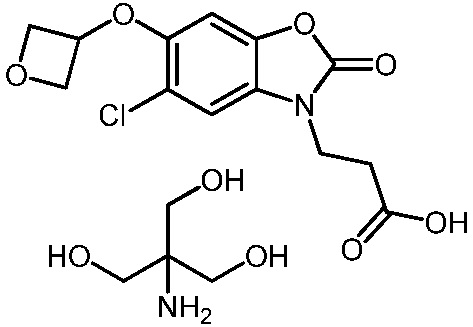
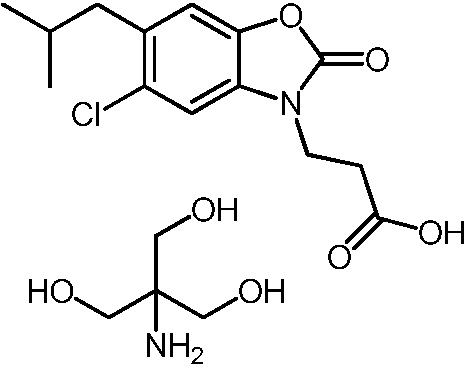
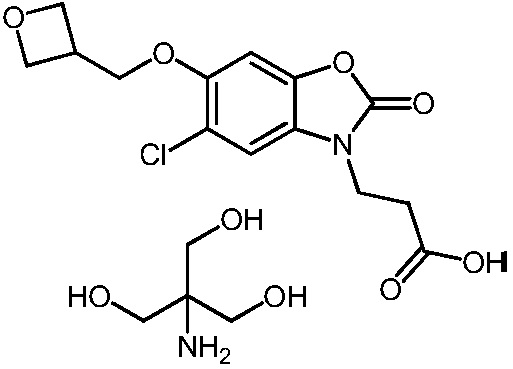

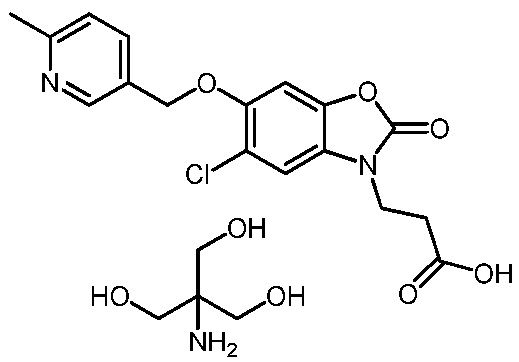
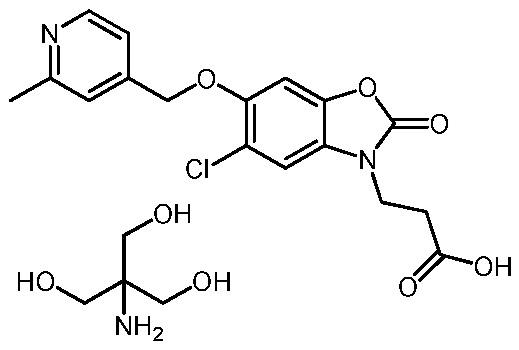
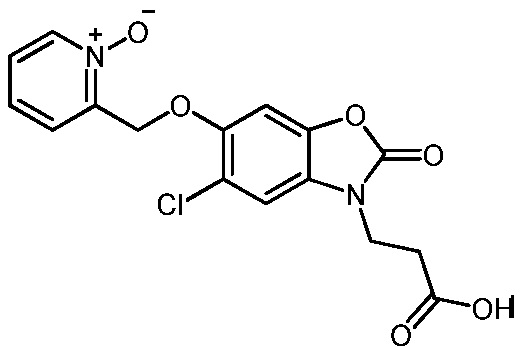
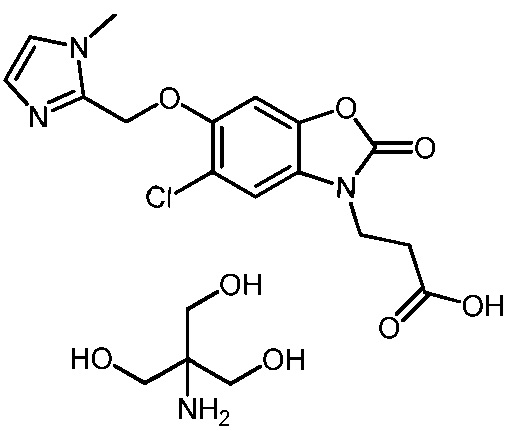
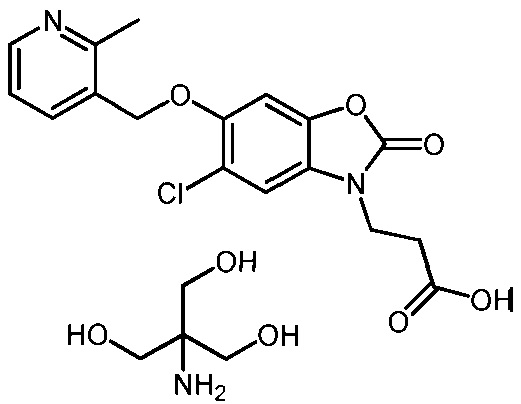

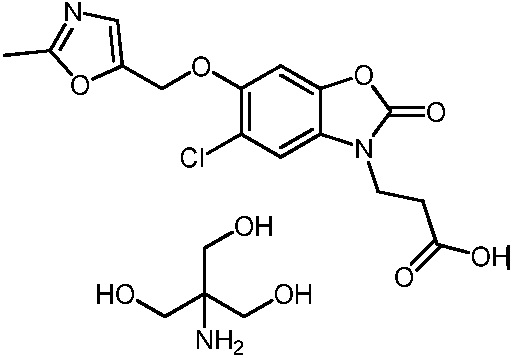
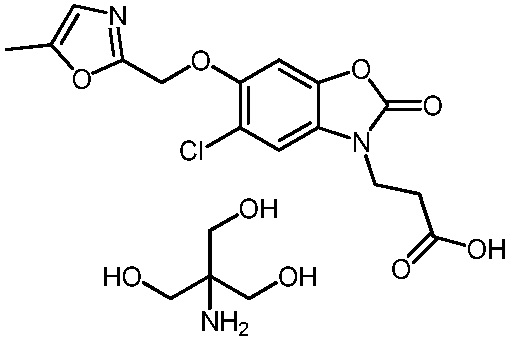
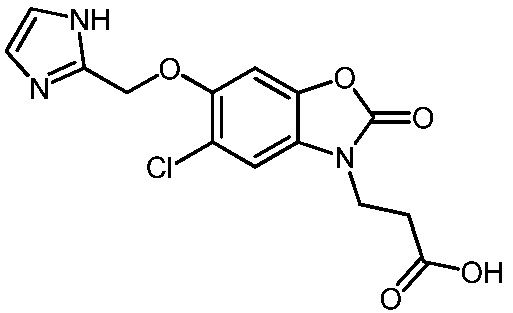
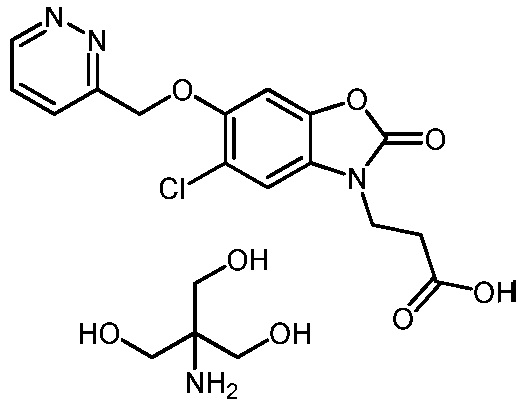
Соединения примеров 3b-3l и 38-61 получали по методике, по существу соответствующей схеме 1, или с использованием метил 3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропаноата (II).
(мин)
Метод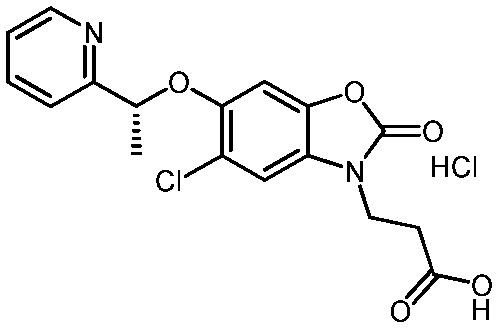
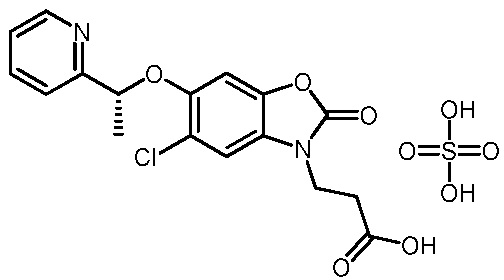
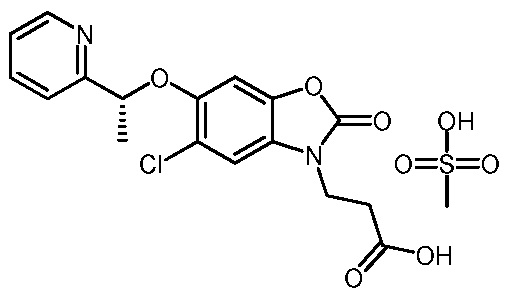
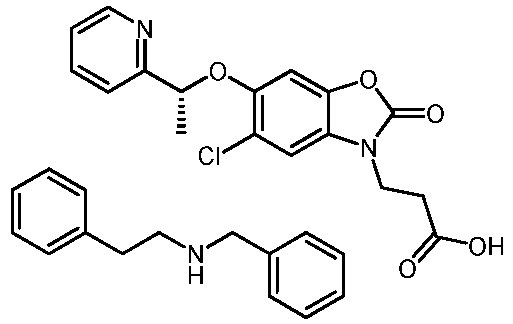
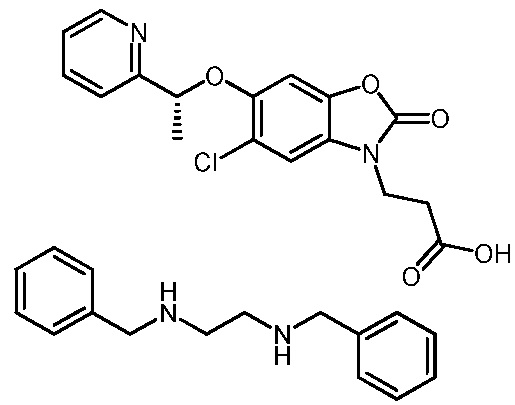
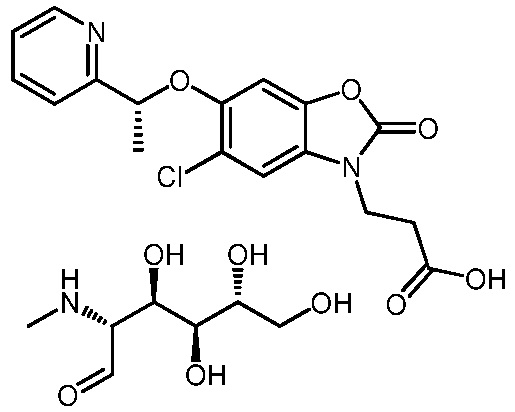
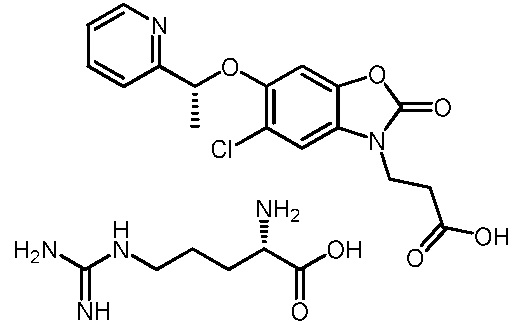
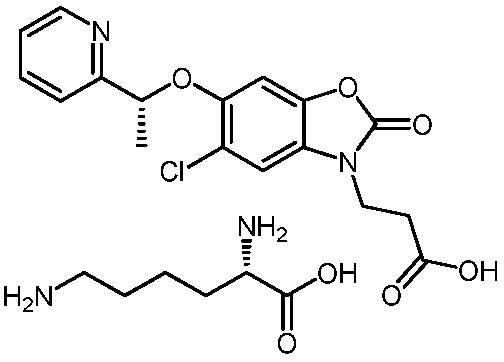
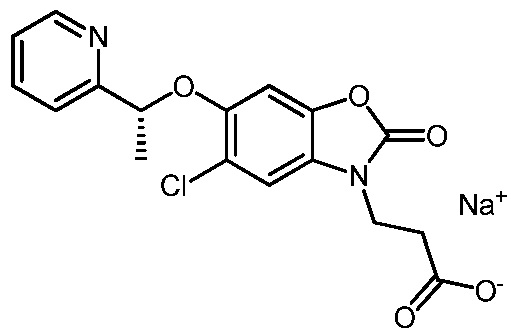
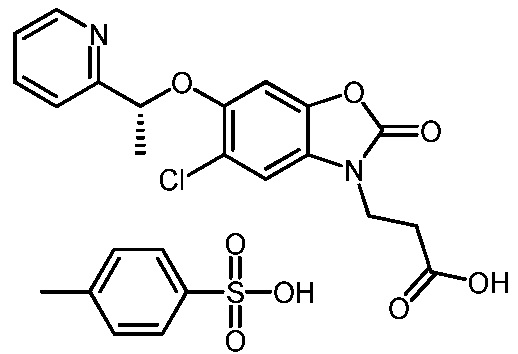
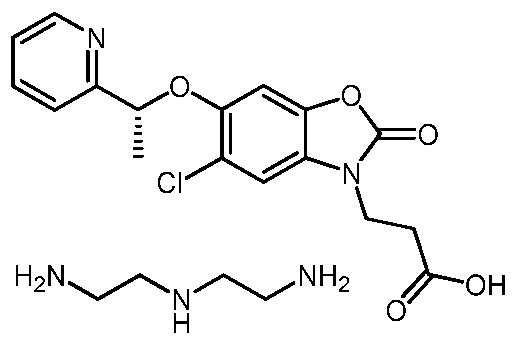
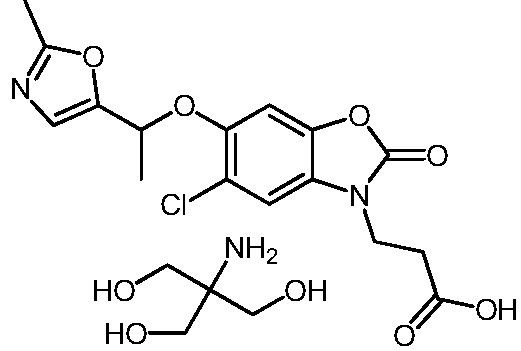
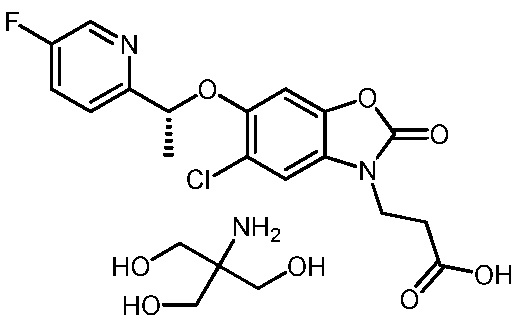
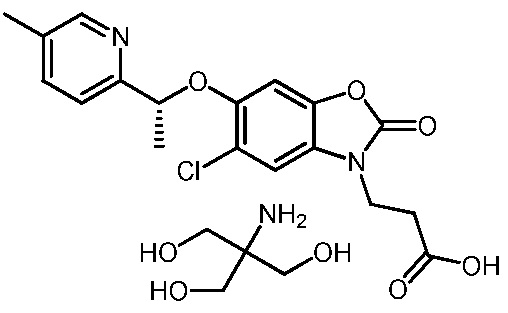
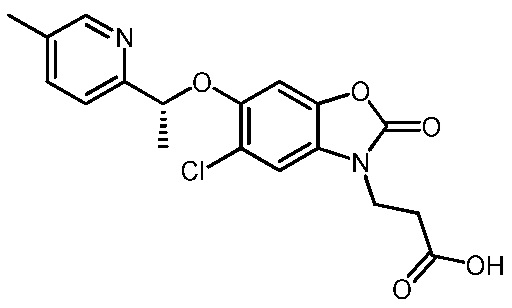
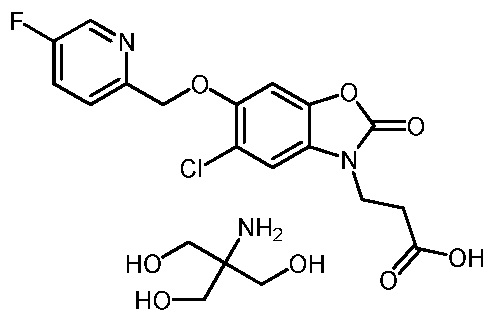
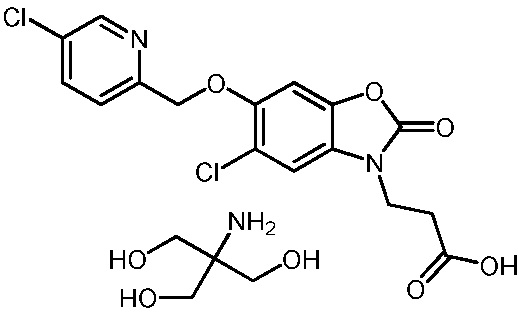

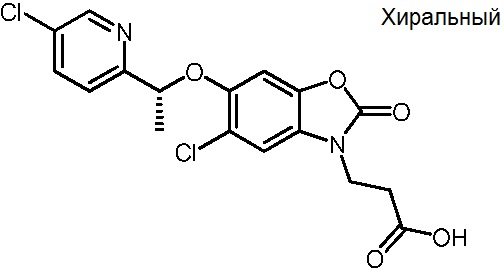
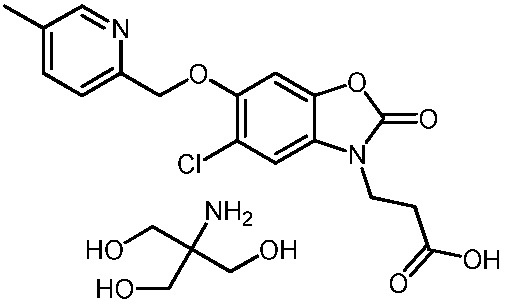
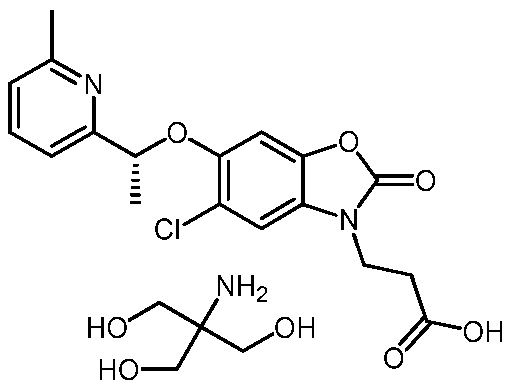
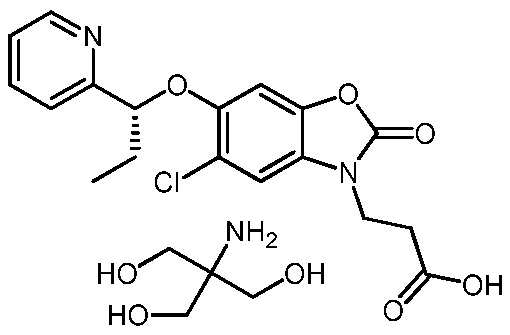


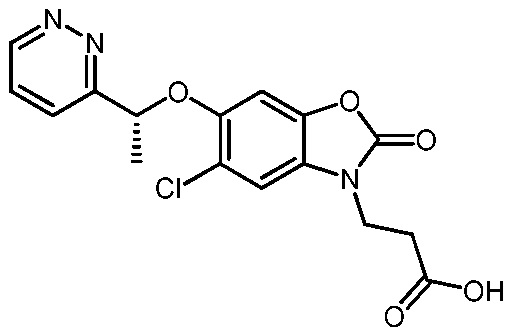
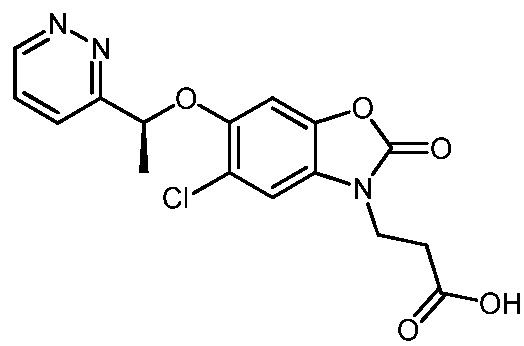
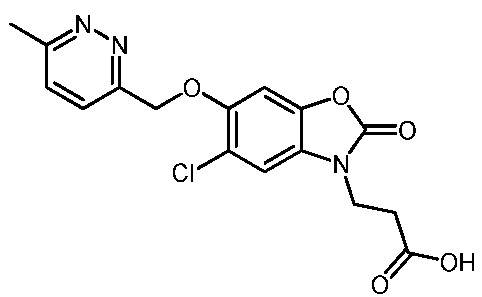
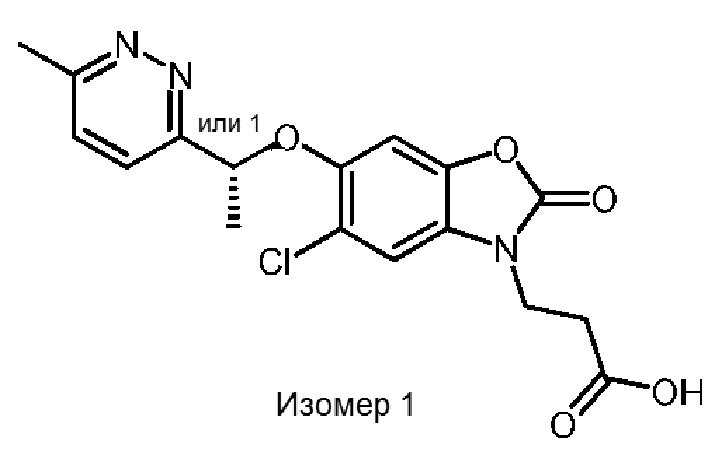
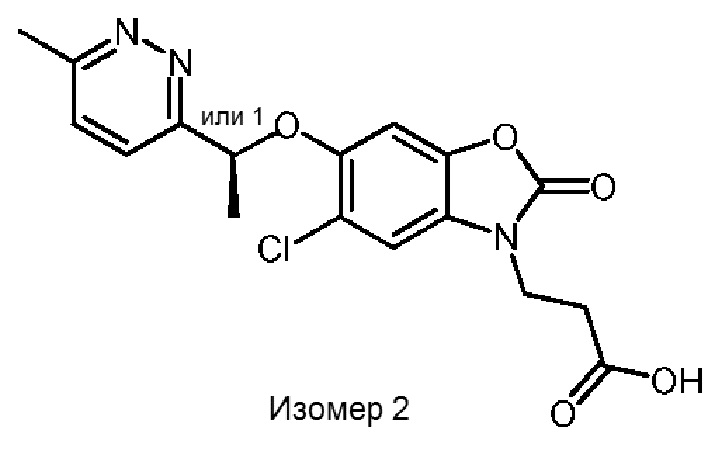
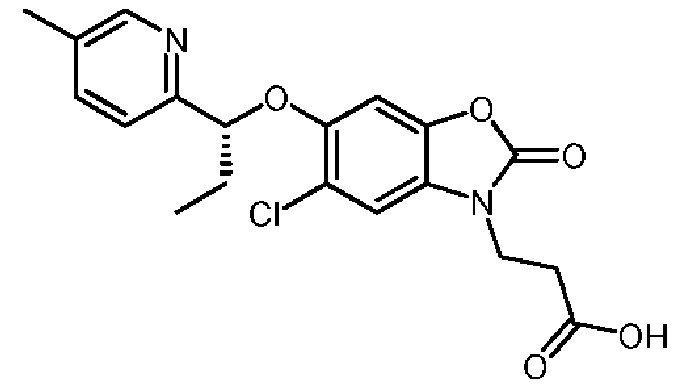
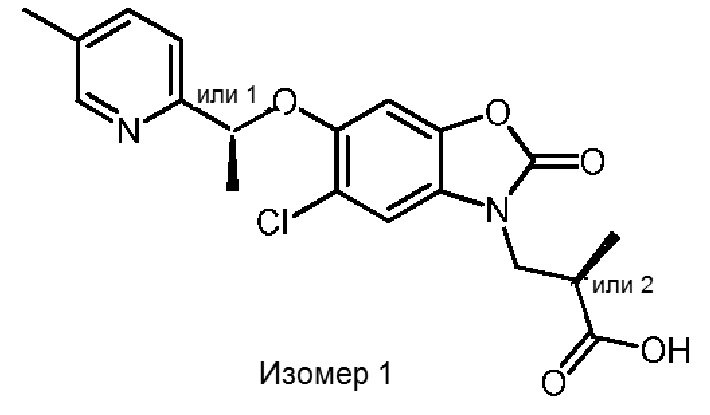
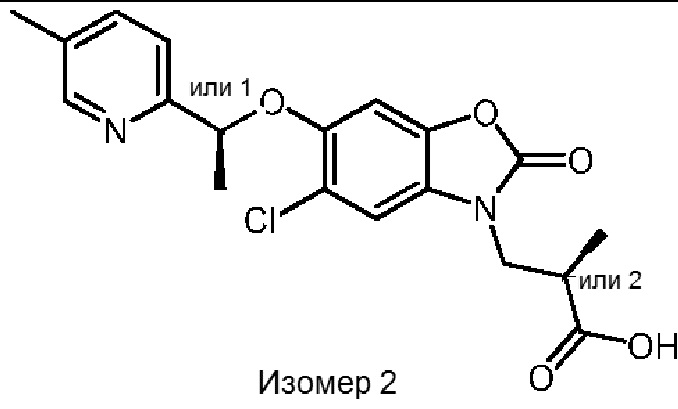
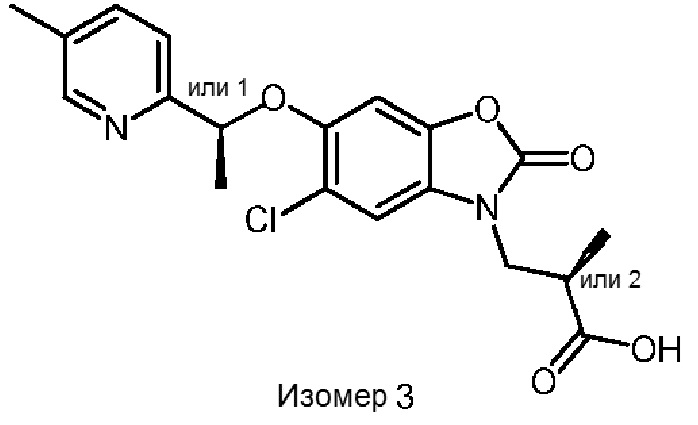
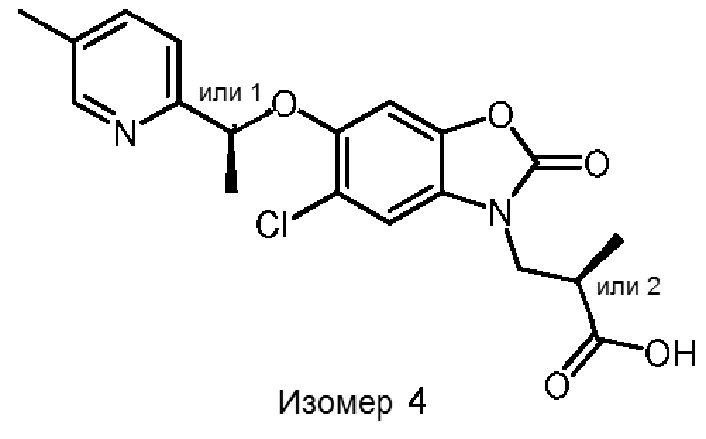
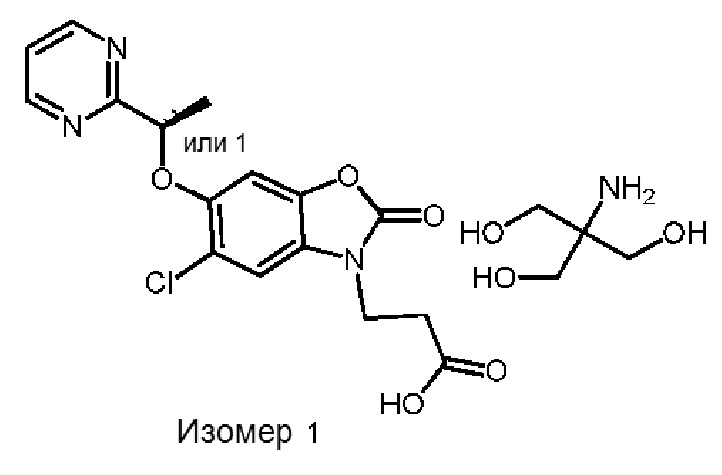
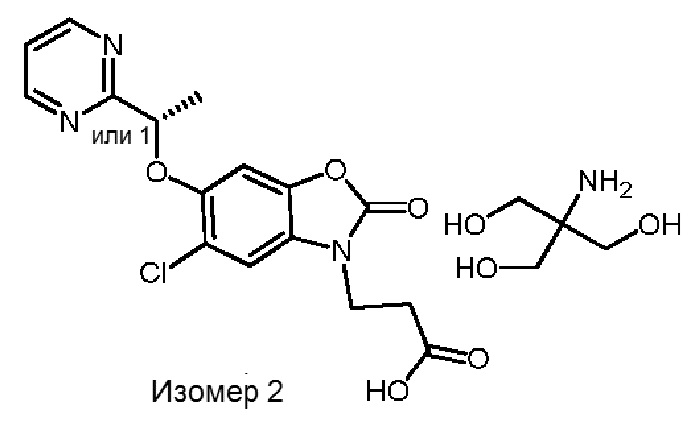
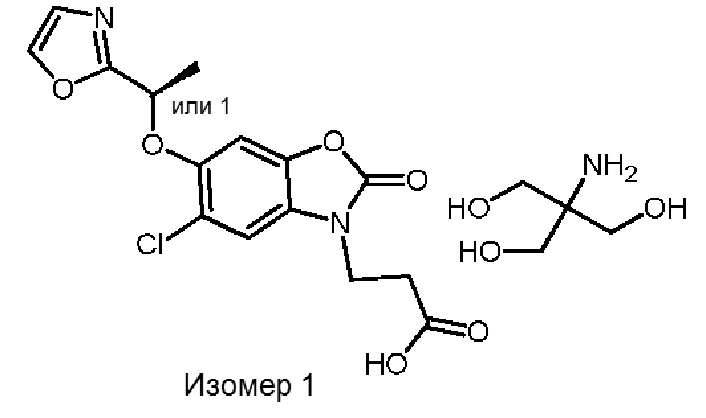
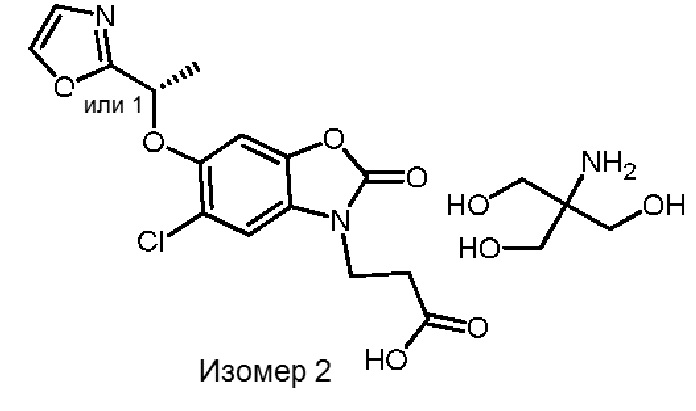
Потенциальная возможность и эффективность соединений настоящего изобретения для ингибирования KMO может быть определена скоростным МС анализом, осуществляемым на клонированных ферментах человека, как описано в данном описании. Соединения формулы (I) продемонстрировали ингибирующую активность в отношении КМО фермента, с использованием функционального скоростного МС анализа, как описано в данном описании.
Протокол скоростного МС анализа KMO
Материалы и методики
Материалы
L-Кинуренин (Kyn), 3-гидрокси-DL-кинуренин (3-HK), гидрат тетранатриевой соли восстановленного β-никотинамидадениндинуклеотид-2'-фосфата (NADPH), 4-(2-гидроксиэтил)пиперазин-1-этансульфоновую кислоту (Hepes), DL-дитиотреитол (DTT), этилендиаминтетрауксусную кислоту (EDTA), CHAPS и трифторуксусную кислоту (TFA) приобретали у фирмы Sigma-Aldrich Ltd. (Gillingham, Dorset, UK). Ацетонитрил и муравьиная кислота со степенью чистоты для ВЭЖХ были поставлены фирмой Fisher Scientific (Loughborough, UK).
Клонирование и экспрессия KMO человека
Полную длину KMO человека амплифицировали посредством PCR из pcDNA5/FRT/V5-His-TOPO/hKMO (вектор, поставляемый Эдинбургским университетом) и клонировали в pGEX6P-1 (GE Healthcare) с помощью BamH1 и Sal1 сайтов рестрикции. ДНК, кодирующую метку N-терминальной глутатион-S-трансферазы (GST), с последующим предварительным расщеплением сайта расщепления протеазы, и полную длину KMO амплифицировали посредством PCR от pGEX6P-1-КМО и клонировали в pFastbac1 (Invitrogen) с помощью Xbal и EcoR1 сайтов рестрикции.
pFastbac1 GST-КМО трансформировали в геном бакуловируса с использованием BAC-BAC технологии (Invitrogen), и получали бакмид ДНК и трансфицировали в клетки Spodoptera frugiperda (Sf9) с использованием Cellfectin II (Invitrogen). Экспрессию белка желаемой молекулярной массы (ММ 82634) прослеживали Вестерн-блот анализом с использованием конъюгата анти-GST-пероксидазы.
Получение мембран из клеток Sf9, экспрессирующих GST-KMO человека
Исходный вирус P1 генерировали из одного клона и использовали для инфицирования 3× 1,5 л культур клеток Sf9 в 3 л колбах Эрленмейера и Фернбаха. Клетки Sf9 выращивали в среде Hyclone SFX (Thermo Scientific) до около 3×106 клеток/мл и инфицировали по разносторонней номинальной инфекции 3. Клетки собирали спустя 48 часов и разрушали смешиванием в 50 мМ Hepes, pH 7,4, 1 мМ EDTA буфере, содержащем ингибиторы протеазы. Использовали низкую скорость вращения (400 g) для удаления клеточного дебриза, а затем высокую скорость вращения (75000 g) для пеллетирования мембран. Полученные мембраны очищали в сахарозе с прерывистой градиентной плотностью путем ресуспендирования в 10% (масс./об.) сахарозе и расслоением около 40% (масс./об.) сахарозы, оба в указанном выше буфере. Полученное центрифугировали при 150000 g, и очищенные мембраны отбирали с поверхности раздела, собирали центрифугированием при 100000 g, ресуспендировали в буфере, и аликвоты хранили при -80°C. Активность KMO обнаруживалась только при взаимодействии с мембранной фракцией, и отсутствие активности KMO детектировалось в полученных мембранах из неинфицированных клеток Sf9. Получали партию 104 мг очищенных мембран Sf9 KMO (как определено анализом Пирса BCA белка с использованием бычьего сывороточного альбумина в качестве стандарта) и подтверждали в анализе RF МС.
Анализ высокопроизводительной масс-спектрометрии RapidFire
Получали 11 точек 3-кратных серийных разведений тестируемых соединений в ДМСО, и 100 нл этих растворов распределяли в 384-луночные V-образные полипропиленовые планшеты (Greiner Bio-one, Стоунхаус, Великобритания) с использованием акустического распределителя Echo 555 (Labcyte, Саннивейл, CA). Это давало конечную концентрацию для анализа в диапазоне от 100 мкМ до 1,7 нм в конечном объеме 10 мкл для анализа (см. ниже). 100 нл ДМСО распределяли в колонках 6 и 18 для высокого и низкого контроля, соответственно, с предварительной инактивацией фермента в колонке 18 путем подачи 30 мкл 0,5% (об./об.) TFA.
Условия анализа KMO человека при использовании выделенных мембран KMO представляли собой 50 мМ Hepes, pH 7,5, 2 мМ DTT, 1 мМ EDTA, 100 мкМ CHAPS, 200 мкМ NADPH, 10 мкМ кинуренин и 8 мкг/мл KMO-мембран в общем реакционном объеме 10 мкл.
Анализ проводили сначала распределением 5 мкл 2× раствора фермента (16 мкг/мл KMO-мембран в 50 мМ Hepes, pH 7,5, 2 мМ DTT, 2 мМ EDTA, 200 мкМ CHAPS) в планшеты, содержащие 100 нл соединений, и инкубированием в течение 10 минут при температуре окружающей среды. Реакции инициировали добавлением 5 мкл 2× раствора субстрата (400 мкМ NADPH, 20 мкМ кинуренин в 50 мМ Hepes, pH 7,5, 2 мМ DTT) и инкубировали в течение 2 час при комнатной температуре перед гашением реакции добавлением 30 мкл 0,5% (об./об.) TFA. Планшеты центрифугировали при 2500 об./мин. в течение 10 минут перед анализом. Все дополнения осуществляли с использованием дозатора Multidrop Combi dispenser (Thermo Fisher Scientific).
Гашеные планшеты для анализа переносили в систему высокопроизводительный интегрированный автоматический пробоотборник RapidFire200/твердофазное экстрагирование (SPE) (Agilent Technologies, Wakefield, MA). Образцы отсасывали с помощью аспиратора из каждой лунки в течение 500 мс, и 10 мкл непосредственно загружали в RapidFire картридж с микрошкалой SPE C18 (тип C), который промывали в течение 3 сек водой со степенью чистоты для ВЭЖХ, содержащей 0,1% (об./об.) муравьиной кислоты, для удаления неорганических компонентов. Аналиты затем элюировали в масс-спектрометр в 3-х секундный цикл элюирования с использованием смеси 80% (об./об.) ацетонитрил/вода, содержащая 0,1% (об./об.) муравьиной кислоты, и картридж затем уравновешивали промывкой водой, содержащей 0,1% (об./об.) муравьиной кислоты в течение 500 мс. Это давало общий временной цикл 7 сек, включая анализ 384-луночных планшетов примерно в 45 мин.
Как Kyn, так и 3-HK детектировали с использованием Sciex API4000 тройного квадрупольного масс-спектрометра (приобретенный у Biosystems, Concord, Ontario, Canada), оборудованного интерфейсом с электрораспылением и работающего в положительном ионном режиме. Мониторинг нескольких реакции (MRM) использовали для детекции как Kyn, так и 3-HK с использованием Q1/Q3 переходов при m/z 209,4-192,0 и m/z 225,3-208,2, соответственно. Данный спектрометр использовали при ESI напряжении 5500 В и температуре источника 600°C, с продолжительностью времени 50 мс для каждого перехода.
Данные анализов
Отдельные MRM переходы сохраняли в виде текстовых файлов, и извлеченные ионные хроматограммы интегрировали и обрабатывали с использованием программного обеспечения максимальной интеграции RapidFire® (версия 3.6).
Использованные данные интегрированной площади пиков для 3-HK анализировали в ActivityBase (ID Bisiness Solutions Ltd, Surrey, Великобритания). Кривые доза-ответ строили по уравнению (1):
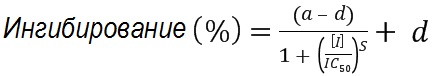 (1),
(1),
где a обозначает не ингибируемый ответ, d обозначает полностью ингибированный ответ, [I] обозначает концентрацию данного ингибитора, IC50 обозначает [I], которая дает 0,5×(a-d), и S обозначает угловой коэффициент Хилла.
Иллюстративные соединения настоящего изобретения имеют срединные значения pIC50>6,1 в приведенном выше анализе МС Rapidfire. Соединение примера 1 имеет срединные значения pIC50=7,9 в приведенном выше анализе МС Rapidfire. Соединение примера 2 имеет срединные значения pIC50=8,4 в приведенном выше анализе МС Rapidfire.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 3-(6-ХЛОР-3-ОКСО-3,4-ДИГИДРО-(2H)-1,4-БЕНЗОКСАЗИН-4-ИЛ)ПРОПИОНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ KMO | 2016 |
|
RU2746001C2 |
| НОВЫЕ ТИЕНОПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2605403C2 |
| ПРОИЗВОДНЫЕ 3-ОКСО-1-ЦИКЛОБУТЕНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2296753C2 |
| АРОМАТИЧЕСКИЕ ПРОИЗВОДНЫЕ 6,7-ДИЗАМЕЩЕННЫХ 3-ХИНОЛИНКАРБОКСАМИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ИХ ПРИМЕНЕНИЕ ДЛЯ ИЗГОТОВЛЕНИЯ ЛЕКАРСТВА | 2002 |
|
RU2281940C2 |
| АГОНИСТЫ GPR40 | 2011 |
|
RU2627703C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2016 |
|
RU2760554C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ПУТИ JAK | 2011 |
|
RU2672100C2 |
| ПРОИЗВОДНЫЕ АРИЛАМИДОВ В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2011 |
|
RU2535671C1 |
| НОВЫЕ ГИДРОКСИКИСЛОТНЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2016 |
|
RU2745430C1 |
| БОРСОДЕРЖАЩИЕ ИНГИБИТОРЫ PDE4 | 2019 |
|
RU2793936C2 |
Изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, где X представляет собой связь, и R1 представляет собой -галоген или -CN; или X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил, выбранный из пиридина, имидазола, пиримидина, пиридазина или оксазола, может быть дополнительно замещен галогеном, метилом, этилом или O; m равен 1 или 2; n равен 0 или 1; R2 представляет собой -H, -метил или -этил; и R3 представляет собой водород, при условии, что соединением формулы (I) или его фармацевтически приемлемой солью не является 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота или 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановая кислота. Также изобретение относится к конкретным соединениям, приведенным в формуле изобретения. Соединения по изобретению предназначены для применения при лечении состояний или расстройств, опосредованных KMO. 10 н. и 8 з.п. ф-лы, 1 табл., 77 пр.
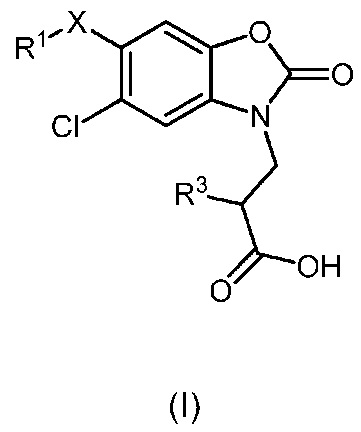
1. Соединение формулы (I) или его фармацевтически приемлемая соль:
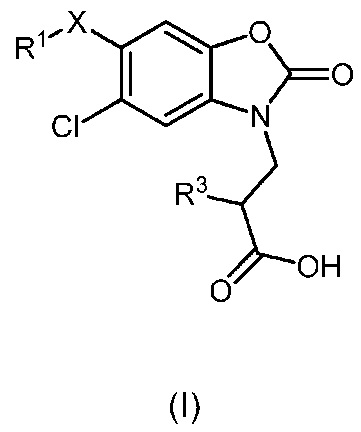 ,
,
где
X представляет собой связь, и R1 представляет собой -галоген или -CN; или
X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил; или
X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил, выбранный из пиридина, имидазола, пиримидина, пиридазина или оксазола, может быть дополнительно замещен галогеном, метилом, этилом или O;
m равен 1 или 2;
n равен 0 или 1;
R2 представляет собой -H, -метил или -этил; и
R3 представляет собой водород,
при условии, что соединением формулы (I) или его фармацевтически приемлемой солью не является 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановая кислота или 3-(5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановая кислота.
2. Соединение формулы (I) по п.1, где X представляет собой -CH2-, и R1 представляет собой -H или -C1-3алкил.
3. Соединение формулы (I) по п.1, где X представляет собой -CH2-, и R1 представляет собой -H.
4. Соединение формулы (I) по п.1, где X представляет собой -O-, и R1 представляет собой -C1-4алкил, -(CH2)mCF3, -CHR2CH2OMe, -(CH2)nC3-4циклоалкил, -(CH2)nоксетан, -бензил или -CHR2гетероарил; где гетероарил может быть дополнительно замещен метилом или O.
5. Соединение формулы (I) по п.1, где X представляет собой -O-, и R1 представляет собой -CHR2гетероарил.
6. Соединение формулы (I) или его фармацевтически приемлемая соль, которое является соединением, выбранным из группы, состоящей из:
3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5,6-дихлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-фтор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-метокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циано-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-бром-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-этил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклопропилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(циклобутилметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-(бензилокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(2-метоксиэтокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-пропоксибензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(3,3,3-трифторпропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиридин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклобутокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-циклопропокси-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(2,2,2-трифторэтокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-изобутил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(оксетан-3-илметокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((1-метоксипропан-2-ил)окси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-4-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
2-(((3-(2-карбоксиэтил)-5-хлор-2-оксо-2,3-дигидробензо[d]оксазол-6-ил)окси)метил)пиридин-1-оксида;
3-(5-хлор-6-((1-метил-1H-имидазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилпиридин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-2-оксо-6-(пиримидин-2-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((2-метилоксазол-5-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилоксазол-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(6-((1H-имидазол-2-ил)метокси)-5-хлор-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
3-(5-хлор-2-оксо-6-(пиридазин-3-илметокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-(1-(2-метилоксазол-5-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты (рацемическая);
(R)-3-(5-хлор-6-(1-(5-фторпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-фторпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-хлорпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-хлорпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((5-метилпиридин-2-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридин-2-ил)пропокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(4-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-2-оксо-6-(1-(пиридазин-3-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты;
3-(5-хлор-6-((6-метилпиридазин-3-ил)метокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(6-метилпиридазин-3-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)пропокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(S)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
(R)-3-(5-хлор-6-(1-(5-метилпиридин-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)-2-метилпропановой кислоты;
3-(5-хлор-2-оксо-6-(1-(пиримидин-2-ил)этокси)бензо[d]оксазол-3(2H)-ил)пропановой кислоты (индивидуальный энантиомер);
(S)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты и
(R)-3-(5-хлор-6-(1-(оксазол-2-ил)этокси)-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты,
или их фармацевтически приемлемой соли.
7. Соединение формулы (I), которое представляет собой 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановую кислоту формулы:
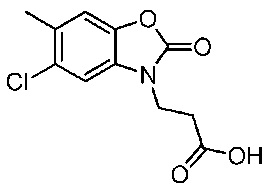
или ее фармацевтически приемлемую соль.
8. Соединение формулы (I) или его фармацевтически приемлемая соль, которое представляет собой 2-амино-2-(гидроксиметил)-1,3-пропандиольную соль 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановой кислоты формулы:

9. Соединение формулы (I) или его фармацевтически приемлемая соль по любому из пп.1, 6, 7 или 8 для применения в терапии при лечении состояний или расстройств, опосредованных KMO.
10. Соединение формулы (I) или его фармацевтически приемлемая соль по любому из пп.1, 6, 7 или 8 для применения при лечении состояний или расстройств, опосредованных KMO.
11. Соединение формулы (I) или его фармацевтически приемлемая соль по любому из пп.1, 6, 7 или 8 для применения при лечении острого панкреатита.
12. Применение соединения формулы (I) или его фармацевтически приемлемой соли по любому из пп.1-8 при изготовлении лекарственного средства для лечения состояний или расстройств, опосредованных KMO.
13. Применение соединения формулы (I) или его фармацевтически приемлемой соли по любому из пп.1-8 при изготовлении лекарственного средства для лечения острого панкреатита.
14. Способ лечения состояний или расстройств, опосредованных KMO, включающий введение хозяину, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли по любому из пп.1-8.
15. Способ лечения острого панкреатита, включающий введение хозяину, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли по любому из пп.1-8.
16. Фармацевтическая композиция для лечения состояний или расстройств, опосредованных KMO, содержащая a) эффективное количество соединения по любому из пп.1-8 или его фармацевтически приемлемой соли и b) один или более фармацевтически приемлемых эксципиентов.
17. Фармацевтическая композиция по п.16, содержащая 3-(5-хлор-6-метил-2-оксобензо[d]оксазол-3(2H)-ил)пропановую кислоту или ее фармацевтически приемлемую соль.
18. Фармацевтическая композиция для применения при лечении острого панкреатита, содержащая соединение формулы (I) или его фармацевтически приемлемую соль по любому из пп.1-8 и один или более фармацевтически приемлемых эксципиентов.
| Способ получения производных 3-(3-бензоксазолонил)пропановой кислоты | 1983 |
|
SU1143745A1 |
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| US 4370340 A, 25.01.1983. | |||
Авторы
Даты
2019-07-01—Публикация
2014-12-17—Подача