ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к системе планирования дозы для терапевтического лечения пораженной ткани органа и, в частности, изобретение относится к системе планирования дозы для лечения в области онкологии.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Лечение опухолей у онкологических пациентов можно выполнять с использованием нескольких способов от минимально инвазивных способов, например, брахитерапии, до хирургических способов, в ходе которых удаляют весь орган, содержащий опухоль. Менее инвазивные способы фокальной терапии набирают популярность благодаря усовершенствованиям в области ранней диагностики и скрининга, и потенциально меньших побочных эффектов.
Рабочий процесс от диагностики до лечения рака состоит из нескольких этапов. Биопсию обычно выполняют в течение этапа диагностики, чтобы оценить тип опухоли и предоставить балльную оценку (в дальнейшем, индекс) распространения рака. Биопсию обычно берут в нескольких местах и вычисляют общий индекс. Для вывода упомянутого общего индекса применяют несколько способов:
1. число миллиметров злокачественного образования на один биоптат;
2. суммарное число миллиметров злокачественного образования по всем биоптатам;
3. процентное содержание злокачественного образования на один биоптат;
4. суммарное процентное содержание злокачественного образования во всем образце;
5. число положительных биоптатов;
6. доля положительных биоптатов (число положительных биоптатов и суммарное число биоптатов).
Патент США 7831293B2 описывает способ обозначения границы биологической мишени для лечения. Данный документ описывает способ, по которому в месте биопсии оставляют определимый маркер. Данный маркер используют для корреляции гистопатологических данных с функциональной визуализацией. Поскольку набор данных, используемых для создания плана лечения опухоли, может различать и дифференцировать конкретную патологию и прогрессирование опухоли или агрессивность разных областей целевой ткани, то план лечения можно использовать для направления терапии на разные области ткани отдельного биологического целевого объема с разными интенсивностями. Патологически задаваемые точки опухоли коррелируют с функциональным исследованием (например, МР-спектроскопией (магнитно-резонансной спектроскопической визуализацией), ОФЭКТ (однофотонной эмиссионной КТ), ПЭТ (позитронной эмиссионной томографией) или оптической биопсией) таким образом, что полученные положительные результаты на функциональном изображении могут служить известным маркером для участков поражения. Если функциональное исследование может обнаруживать данные зоны прежде скрытых очагов опухоли, то другие зоны, показывающие активность на функциональном исследовании, можно рассматривать как представляющие дополнительные скрытые очаги опухоли и поэтому использовать для обозначения границы биологического целевого объема для лечения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Целью изобретения является усовершенствование планирования лечения. Данная цель достигается с помощью системы планирования дозы для терапевтического лечения пораженной ткани интересующего органа, содержащей:
- модуль создания биопсийной карты, выполненный с возможностью приема биопсийной информации об интересующем органе, касающейся мест биопсии и тканевых характеристик ткани, обнаруженной в местах биопсии, при этом модуль создания биопсийной карты дополнительно выполнен с возможностью создания пространственно-аннотированной биопсийной карты для органа посредством привязки пространственной информации о местах биопсии к тканевым характеристикам ткани, обнаруженной в соответствующих местах биопсии, и
- модуль вычисления вероятностной карты, выполненный с возможностью создания вероятностной карты опухоли посредством вычисления вероятности опухоли для мест в органе, из которых не отбирали биопсию, путем использования опухолевых и/или тканевых характеристик из мест биопсии, и
- модуль планирования дозы, выполненный с возможностью создания дозового плана на основе вероятностной карты опухоли, причем ограничивающие условия планирования являются такими, что для зоны со средней повышенной вероятностью опухоли планируется повышенная плановая доза, и для зоны со средней пониженной вероятностью опухоли планируется пониженная плановая доза.
В настоящее время, в лучевой терапии существуют две важных проблемы. Первая состоит в том, что точное оконтуривание опухолевой ткани может быть сложной задачей. Существует множество различий между оконтуриваниями, выполненными разными наблюдателями на основе медицинских изображений. Кроме того, определение правильной дозы может быть сложной задачей. Предлагалось изменять дозу в пределах опухоли с учетом агрессивности опухоли, чтобы повысить вероятность контроля опухоли и ослабить побочные эффекты. Однако, данный способ, так называемого, окрашивания опухоли цифрами основан на (функциональной) визуализации (например, методами ПЭТ, диффузионно-взвешенной МРТ, МРТ с динамическим контрастированием) ткани. Авторы настоящего изобретения обнаружили, что упомянутые методы визуализации обеспечивают только косвенные показатели вероятности опухоли и агрессивности опухоли. Поэтому, при непосредственном использовании результатов биопсии для вычисления вероятностной карты опухоли, которая, в свою очередь, представляет собой входные данные для модуля планирования дозы, план лечения можно улучшить. Вероятностная карта опухоли может быть картой, представляющей пространственное распределение расчетных вероятностей присутствия опухоли. Данная карта может также представлять пространственное распределение по расчетным плотностям опухолевых клеток или уровням агрессивности (например, индекс Глиссона в случае рака простаты).
В соответствии с вариантами осуществления изобретения, система планирования дозы дополнительно содержит биопсийную систему с контролем по изображениям, выполненную с возможностью взятия биопсии из предварительно заданных мест в органе и дополнительно выполненную с возможностью представления по меньшей мере пространственной информации о местах биопсии в модуль создания биопсийной карты. Данный вариант осуществления выгоден потому, что он может способствовать усовершенствованию рабочего процесса лечения опухоли. Нацеленные биопсии могут выполняться и основываться на гистопатологическим анализе биопсий, возможно непосредственное создание биопсийной карты, которую затем можно использовать для вычисления вероятностной карты и дозового плана. Затем данный план можно непосредственно применять для лечения. Контроль по изображениям можно обеспечивать, например, посредством ультразвуковой или магнитно-резонансной визуализации.
В соответствии с дополнительным вариантом осуществления изобретения, биопсийная система с контролем по изображениям содержит, так называемую, фотонную иглу. Автоматический анализ спектра, получаемый посредством фотонной иглы, будет дополнительно ускорять диагностику для процесса лечения.
В соответствии с дополнительным вариантом осуществления изобретения, биопсийная система с контролем по изображениям содержит модуль совмещения, выполненный с возможностью совмещения изображения органа, полученного ультразвуковой системой, с изображением органа, полученного второй системой медицинской визуализации, при этом места биопсии определяются по меньшей мере частично на основании изображения, полученного второй системой медицинской визуализации. Данный вариант осуществления выгоден потому, что, хотя ультразвук может быть очень удобен для контроля по изображениям, в некоторых ситуациях типа, например, рака простаты, ультразвук может и не подходить как средство визуализации для определения мест, содержащих подозрительную ткань. В данных ситуациях места подозрительной ткани можно определять на основании изображений, полученных другим средством визуализации, например, МРТ, ПЭТ, ОФЭКТ, КТ (с контрастированием). После совмещения подозрительные места, найденные посредством изображений, полученных второй системой медицинской визуализации, можно перевести в координатную систему ультразвукового средства.
Система планирования дозы может быть выполнена с возможностью создания дозового плана для чего-то одного из радиотерапии, протонной терапии, криотерапии, радиочастотной абляции, лазерной абляции или лечения высокоинтенсивным сфокусированным ультразвуком.
Приведенные и другие аспекты изобретения будут очевидны из последующего описания вариантов осуществления.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фигура 1 - система планирования дозы в соответствии с изобретением,
Фигура 2 - пример вероятностной карты опухоли, и
Фигура 3 - дозовый план, соответствующий вероятностной карте опухоли, показанной на фигуре 2.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
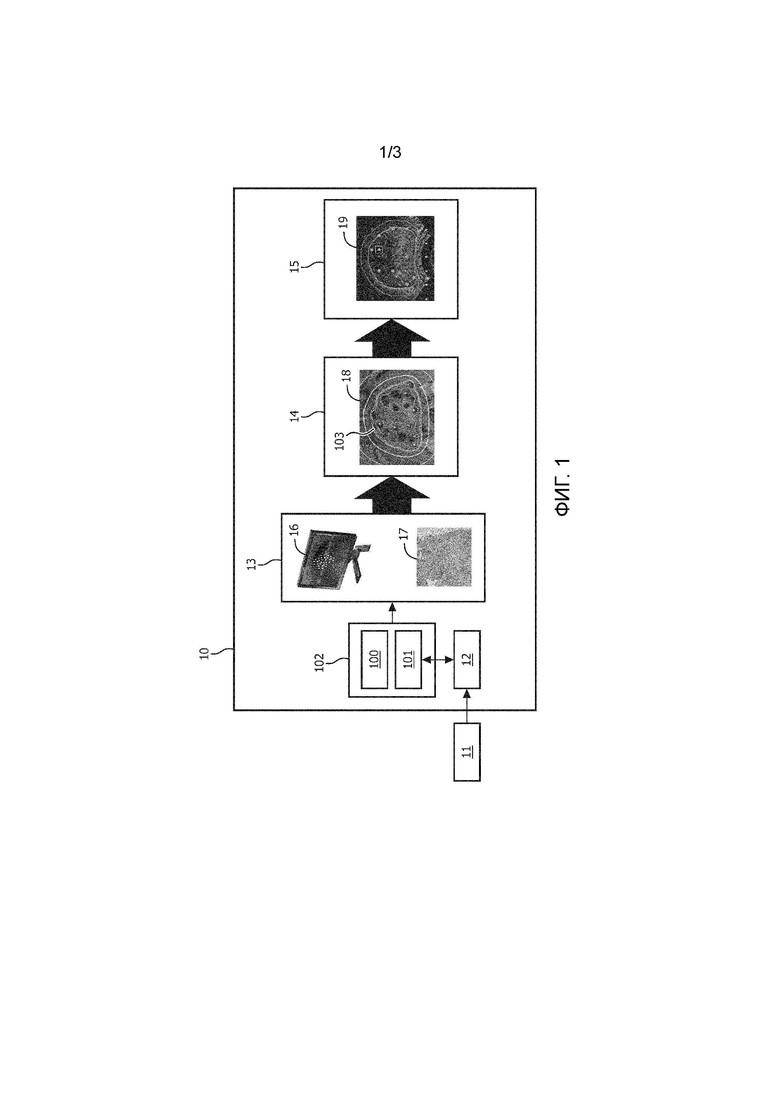
Фигура 1 изображает систему планирования дозы 10 в соответствии с изобретением. Система планирования дозы 10 содержит модуль 13 создания биопсийной карты, модуль 14 вычисления вероятностной карты и модуль 15 планирования дозы. Рабочий процесс планирования дозы с использованием изобретения может начинаться с получения 11 изображений интересующего органа, по которым можно идентифицировать подозрительные места в органе. Возможна также идентификация неподозрительных мест. Упомянутые изображения могут быть, например, магнитно-резонансными (МР) изображениями. МР изображения могут представляться в модуль 12 совмещения. В течение процедуры биопсии, биопсийная система 102 с контролем по изображениям может получать ультразвуковые изображения для навигации биопсии посредством ультразвуковой системы 101. По меньшей мере одно из ультразвуковых изображений представляется в модуль 12 совмещения. Затем модуль совмещения совмещает ультразвуковое изображение с МР изображением таким образом, что идентифицированные подозрительные и неподозрительные места органа могут быть переведены в координатную систему визуализации ультразвуковой системы 101. Затем оператор системы может направлять фотонную иглу 100 в идентифицированные места для выполнения гистопатологического анализа на ткани 17.
В качестве альтернативы, биопсию можно отбирать и пересылать в патологический отдел для анализа. Анализ ткани дает, в результате, тканевые характеристики типа плотности опухолевых клеток, процентного содержания опухолевых клеток, агрессивность опухоли и т.п. Тканевые характеристики, найденные из биопсийной ткани 17 из мест 16 биопсии, представляются в модуль 13 создания биопсийной карты, который создает биопсийную карту посредством привязки мест биопсии к соответствующим тканевым характеристикам.
Биопсийная карта служит входными данными для модуля 14 вычисления вероятностной карты, который использует ее для вычисления вероятностной карты 18 опухоли. В данном случае линия 103 окружает зону, в которой вероятность опухоли превышает некоторый порог. Модуль 14 вычисления вероятностной карты может быть выполнен с возможностью создания вероятностной карты 18 опухоли на основе интерполяции или модели формы опухоли. Интерполяция может быть выгодной, поскольку данный способ не требует предварительного знания формы опухоли.
Модель формы опухоли может использовать доступную статистическую информацию о распространении опухоли по отношению к, например, плотности опухолевых клеток, агрессивности опухоли, мутаций ДНК, уровней экспрессии ДНК, уровней белка, обнаруженных в биопсийном материале. Модели формы опухоли известны, например, из публикации Shen et al., Optimized prostate biopsy via a statistical atlas of cancer spatial distribution, Medical Image Analysis 8 (2004) 139-150. В данном способе упомянутые авторы экспериментально создали облако глобальной вероятности для нахождения положительного результата биопсии и его использования для оптимального расположения иглы. В данном случае, основным пунктом применения для настоящего изобретения является распределение вероятности, которое можно использовать для моделирования вероятностной карты опухоли.
Другими примерами литературы, описывающей распределения опухолей, которые можно использовать как исходную информацию для формирования вероятностной карты опухоли, являются публикации Menze et al., Image-based modeling of tumour growth in patients with glioma, Optimal control in image processing, Springer, Heidelberg/Germany, 2011. hal-00825866, и Gevertz et al., Simulating tumour growth in confined heterogeneous environments, Phys. Biol. 5 (2008) 036010. Кроме того, можно собрать дополнительные данные по вероятности присутствия опухоли в некотором месте, при наличии положительной или отрицательной биопсийной пробы в другом месте.
Фигура 2 представляет пример вероятностной карты опухоли. Фигура 2 содержит ультразвуковое изображение простаты 204. Места, в которых биопсия взята, но опухоль не обнаружена, обозначены знаком «-» 202. Места, в которых биопсия взята, и в которых опухоль обнаружена в биопсийной пробе, обозначены знаком «+» 203. Вероятность опухоли снижается от положений 203 к линии 204, которая является изолинией, указывающей на некоторое значение вероятности опухоли, например, 95%.
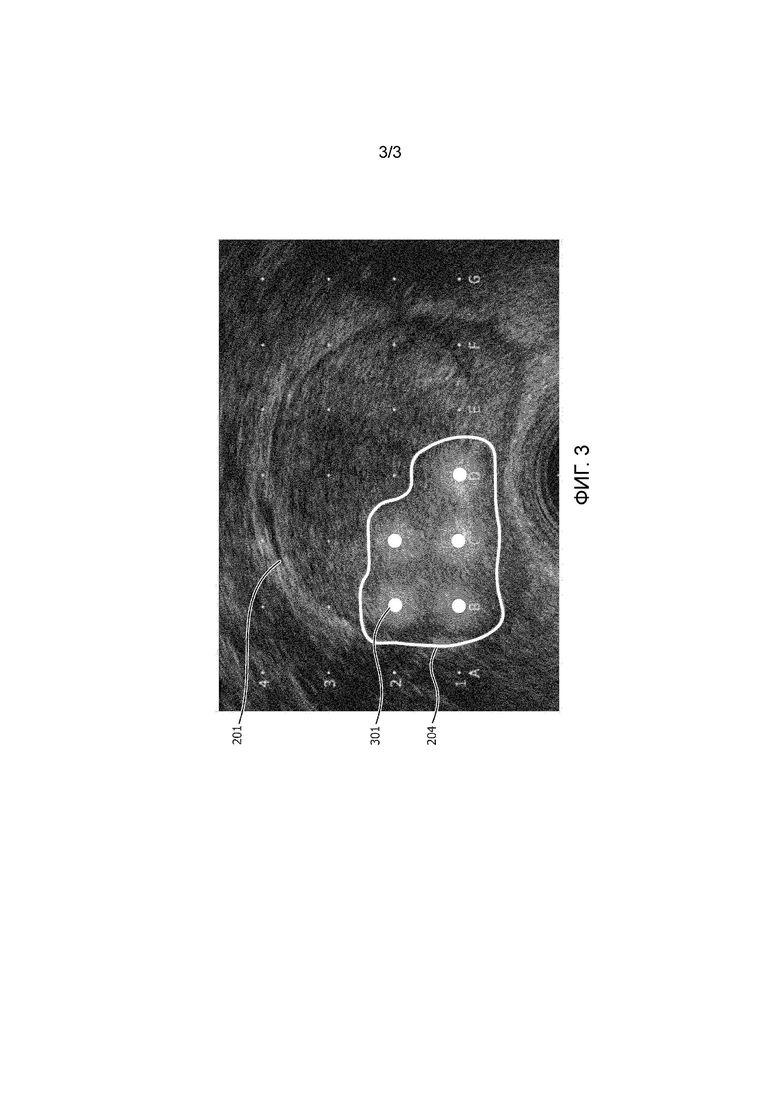
Вероятностная карта опухоли представляется в модуль 15 планирования дозы, который создает дозовый план 19 на основании вероятностной карты опухоли. Фигура 3 представляет дозовый план, соответствующий вероятностной карте опухоли, показанной на фигуре 2. Зону, окруженную изолинией 204, считают общим объемом опухоли (GTV), и планируют лечение как таковое.
В качестве альтернативы, модуль планирования дозы может, например, создавать дозовый план на основании вероятностной карты опухоли при посредстве радиобиологических моделей. Данные модели обычно учитывают плотность опухолевых клеток, но могут также учитывать агрессивность опухоли или уровень гипоксии, который влияет на, по меньшей мере, радиотерапевтический результат и может определяться по, например, уровням HIF-1 (индуцируемого при гипоксии фактора 1). Данные значения можно получать из биопсийных проб и использовать в вероятностной карте опухоли. Дозу облучения можно также определять на основе интерполяции. В качестве альтернативы, можно также выбрать вариант применения увеличенной дозы к области с высокой (например > 95%) вероятностью опухоли и применения стандартной дозы к областям с вероятностью опухоли от низкой до средней (например, 5-95%). Модуль планирования дозы может быть также выполнен с возможностью использования условий ограничения дозы для подверженного риску органа, расположенного вблизи органа, подлежащего лечению. Однако, возможны другие примеры, и изобретение не ограничено раскрытыми примерами.
Хотя изобретение подробно изложено и иллюстрировано на чертежах и в вышеприведенном описании, упомянутые иллюстрации и описание следует считать наглядными или примерными, а не ограничительными; изобретение не ограничено раскрытыми вариантами осуществления и может применяться для планирования дозы в области лечения заболеваний.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА КОНТРОЛЯ ИЗОБРАЖЕНИЙ | 2016 |
|
RU2703688C2 |
| СПОСОБ ПЛАНИРОВАНИЯ ВЫСОКОДОЗНОЙ ВНУТРИТКАНЕВОЙ ЛУЧЕВОЙ ТЕРАПИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2576875C1 |
| СПОСОБ ОТБОРА ПАЦИЕНТОВ ДЛЯ УЛЬТРАЗВУКОВОЙ ГЕМИАБЛЯЦИИ ЛОКАЛИЗОВАННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2017 |
|
RU2676599C1 |
| ВЕРОЯТНОСТЬ ПОВРЕЖДЕНИЯ ЗДОРОВЫХ ТКАНЕЙ, АДАПТИРОВАННАЯ С УЧЕТОМ МАРКЕРОВ | 2010 |
|
RU2564077C2 |
| Способ проведения пункционной биопсии | 2016 |
|
RU2634040C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ БИОХИМИЧЕСКОГО РЕЦИДИВА У БОЛЬНЫХ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПОСЛЕ ГОРМОНОЛУЧЕВОЙ ТЕРАПИИ | 2015 |
|
RU2605838C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2020 |
|
RU2747591C1 |
| Способ трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха и устройство для его осуществления | 2019 |
|
RU2722655C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ МОРФОЛОГИЧЕСКОЙ ВЕРИФИКАЦИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2022 |
|
RU2793842C1 |
| СПОСОБ ДИАГНОСТИКИ СТАДИИ ИНВАЗИИ РАКА МОЧЕВОГО ПУЗЫРЯ | 2007 |
|
RU2332168C1 |

Изобретение относится к медицине, а именно к системе планирования дозы для терапевтического лечения пораженной ткани органа. Предложена система, содержащая: модуль создания биопсийной карты, выполненный с возможностью приема биопсийной информации об интересующем органе, касающейся мест биопсии и тканевых характеристик ткани, обнаруженной в местах биопсии, при этом модуль создания биопсийной карты дополнительно выполнен с возможностью создания пространственно-аннотированной биопсийной карты для органа посредством привязки пространственной информации о местах биопсии к тканевым характеристикам ткани, обнаруженной в соответствующих местах биопсии, и модуль вычисления вероятностной карты, выполненный с возможностью создания вероятностной карты опухоли посредством вычисления вероятности опухоли для мест в органе, из которых не отбирали биопсию, путем использования опухолевых и/или тканевых характеристик из мест биопсии, и модуль планирования дозы, выполненный с возможностью создания дозового плана на основе вероятностной карты опухоли, причем ограничивающие условия планирования являются такими, что для зоны со средней повышенной вероятностью опухоли планируется повышенная плановая доза, а для зоны со средней пониженной вероятностью опухоли планируется пониженная плановая доза. Изобретение обеспечивает усовершенствование планирования лечения. 9 з.п. ф-лы, 3 ил.
1. Система планирования дозы для терапевтического лечения пораженной ткани интересующего органа, содержащая:
- модуль создания биопсийной карты, выполненный с возможностью приема биопсийной информации об интересующем органе, касающейся мест биопсии и тканевых характеристик ткани, обнаруженной в местах биопсии, при этом модуль создания биопсийной карты дополнительно выполнен с возможностью создания пространственно-аннотированной биопсийной карты для органа посредством привязки пространственной информации о местах биопсии к тканевым характеристикам ткани, обнаруженной в соответствующих местах биопсии, и
- модуль вычисления вероятностной карты, выполненный с возможностью создания вероятностной карты опухоли посредством вычисления вероятности опухоли для мест в органе, из которых не отбирали биопсию, путем использования опухолевых и/или тканевых характеристик из мест биопсии, и
- модуль планирования дозы, выполненный с возможностью создания дозового плана на основе вероятностной карты опухоли, причем ограничивающие условия планирования являются такими, что для зоны со средней повышенной вероятностью опухоли планируется повышенная плановая доза, а для зоны со средней пониженной вероятностью опухоли планируется пониженная плановая доза.
2. Система планирования дозы по п. 1, в которой вероятностная карта опухоли является пространственным распределением чего-то одного из расчетных вероятностей присутствия опухоли, расчетных плотностей опухолевых клеток или уровня агрессивности опухоли.
3. Система планирования дозы по п. 1 или 2, дополнительно содержащая биопсийную систему с контролем по изображениям, выполненную с возможностью взятия биопсии из предварительно заданных мест в органе и дополнительно выполненную с возможностью представления по меньшей мере пространственной информации о местах биопсии в модуль создания биопсийной карты.
4. Система планирования дозы по п. 3, в которой биопсийная система с контролем по изображениям содержит фотонную иглу, при этом фотонная игла выполнена с возможностью представления биопсийной информации, касающейся мест биопсии и тканевых характеристик ткани, обнаруженных в местах биопсии, в модуль создания биопсийной карты для интересующего органа.
5. Система планирования дозы по п. 3 или 4, в которой биопсийная система с контролем по изображениям содержит ультразвуковую систему для контроля по изображениям в течение биопсии.
6. Система планирования дозы по п. 5, содержащая модуль совмещения, выполненный с возможностью совмещения изображения органа, полученного ультразвуковой системой, с предыдущим изображением органа, полученным вторым средством визуализации, при этом места биопсии по меньшей мере частично определяются на основании предыдущего изображения.
7. Система планирования дозы по одному из предыдущих пунктов, выполненная с возможностью создания дозового плана для по меньшей мере одного из группы видов лечения, содержащей брахитерапию, протонную терапию, криотерапию, радиочастотную абляцию, лазерную абляцию и лечение высокоинтенсивным сфокусированным ультразвуком.
8. Система планирования дозы по любому из предыдущих пунктов, в которой модуль вычисления вероятностной карты выполнен с возможностью создания вероятностной карты опухоли на основе интерполяции опухолевых и/или тканевых характеристик между местами биопсии или на основе модели формы опухоли, использующей опухолевые и/или тканевые характеристики в качестве входных данных.
9. Система планирования дозы по любому из предыдущих пунктов, в которой опухолевые характеристики являются по меньшей мере одной группой характеристик, содержащей плотность клеток, размер опухоли в биопсийной пробе, процентное содержание опухоли на одну биопсийную пробу или показатель, относящийся к агрессивности опухоли.
10. Система планирования дозы по любому из предыдущих пунктов, в которой модуль планирования дозы дополнительно выполнен с возможностью использования условий ограничения дозы для подверженного риску органа, расположенного вблизи органа, подлежащего лечению.
| US 2003135115 A1, 17.07.2003 | |||
| US 5398690 A, 21.03.1995 | |||
| WO 2016198626 A1, 15.12.2016 | |||
| Johannes G Korporaal et al, The use of probability maps to deal with the uncertainties in prostate cancer delineation, Feb 2010,Radiotherapy and Oncology 94(2):168-72. |
Авторы
Даты
2019-07-01—Публикация
2016-06-10—Подача