Родственные заявки
[0001] По настоящей заявке испрашивается преимущество и приоритет предварительной заявки США № 61/907980, зарегистрированной 22 ноября 2013 года, содержание которой полностью включено в настоящее описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Предлагаемые варианты осуществления в некоторых аспектах основаны на демонстрации в настоящем описании роли гастрина в регуляции старения системы кишечник-яичник и эффектов направленного действия гастрина для улучшения состояния опосредованного гастрином остеопороза. Предложены способы, композиции и средства, содержащие антагонисты гастрина, для лечения, стабилизации, улучшения состояния и профилактики заболеваний и состояний костей.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0003] Остеопороз, характеризующийся потерей костной массы и высоким риском переломов, представляет собой одно из широко распространенных заболеваний особенно в пожилом возрасте и по оценкам затрагивает приблизительно 100 миллионов человек по всему миру. Несмотря на то, что частота возникновения перелома кости у пожилых людей, как правило, повышается, терапевтические стратегии являются ограниченными. В настоящее время антирезорбтивные средства (например, бисфосфонаты, деносумаб, гормональная терапия) являются наиболее широко используемыми видами лечения остеопороза. Эти средства предназначены замедлять ремоделирование костной ткани и увеличивать плотность костной ткани. Однако они были связаны со значительными побочными эффектами, включая остеонекроз челюсти, атипичные переломы, фибрилляцию предсердий и повышенный риск инсульта или злокачественной опухоли. Анаболические средства можно использовать для образования новой кости у пациентов с остеопорозом. Однако поиски анаболических факторов, которые повышают костную массу и регулируют баланс между опосредованным остеобластами формированием костей и ожирением костного мозга, вызывали затруднения. Кроме того, единственное коммерчески доступное анаболическое средство (терипаратид) является не только очень дорогостоящим и вызывающим затруднения при введении, но также связано с побочными эффектами, включая пониженное артериальное давление, тошноту, боль, слабость и депрессию. Кроме того, было выявлено, что использование терипаратида у крыс вызывает рост злокачественных опухолей (остеогенной карциномы). Как правило, терапевтические стратегии для остеопороза являются ограниченными, и разработка новых терапевтических подходов, которые стимулируют образование костей, является одним из приоритетов.
[0004] Хотя недостаточность яичников и деминерализация костей являются общепризнанными ключевыми элементами при остеопорозе, точная этиология остается до кона неизвестной. Лучшее понимание этиологии остеопороза и связанных с костями заболеваний или состояний может приводить к альтернативным способам и композициям для лечения остеопороза и других заболеваний и состояний костей.
[0005] Существует необходимость в способах и композиции для лечения остеопороза и других заболеваний и состояний костей. Настоящее изобретение преодолевает указанные выше проблемы и обеспечивает новое средство для лечения, стабилизации, и/или профилактики прогрессирования заболевания или состояния костей посредством регуляции эффектов гастрина.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] Настоящее изобретение относится к способам, применениям, соединениям и композициям для лечения, например, стабилизации и/или профилактики, например, профилактики прогрессирования заболевания или нарушения костей путем введения средства нуждающемуся в этом индивидууму. В некоторых вариантах осуществления заболевание или нарушение костей характеризуют остеопорозом. В других вариантах осуществления средство, вводимое нуждающемуся в этом индивидууму, направленно воздействует, например, ингибирует или оказывает антагонистическое действие на гастрин и/или рецепторы гастрина, такое как антагонисты гастрина или гастринового рецептора. По одному из вариантов осуществления вводимое средство направленно воздействует на рецептор CCK2.
[0007] Предоставленные варианты осуществления в некоторых аспектах относятся к демонстрации в настоящем описании того, что гормон гастрин прямо или опосредованно регулирует образование костей, таким образом, способствуя потере костной массы с последующей патофизиологией костей, соответствующей остеопоротическим изменениям (см. фигура 57). Предоставленные варианты осуществления относятся в некоторых аспектах к демонстрации в настоящем описании того, что блокада таких эффектов гастрина, например, с использованием антагониста гастрина, который направленно воздействует на рецептор CCK2, оказывает положительное действие на моделях остеопороза на животных и, таким образом, является пригодной для лечения, профилактики и улучшения состояния остеопороза и других заболеваний и состояний костей.
[0008] Таким образом, некоторые варианты осуществления относятся к способам, соединениям, композициям и видам применения антагонистов гастрина, например, средств, которые антагонизируют активность гастрина, при заболеваниях и состояниях костей, таких как заболевания и состояния, которые клинически, патологически или радиологически характеризуют как остеопороз. В некоторых аспектах способы и виды использования включают лечение, улучшение состояния и/или профилактику заболеваний и состояний, включая заболевания и состояния. Некоторые аспекты относятся к способам и композициям для лечения, улучшения состояния заболевания/состояний костей, например, таких, которые характеризуют как остеопороз, с использованием средств, направленно воздействующих на гастрин и/или рецепторы гастрина, например, антагонисты гастрина, например, у i) людей пожилого возраста (мужчин или женщин), например, у престарелых пациентов; ii) женщин со сниженной овариальной функцией или с ее недостаточностью, iii) индивидуумов с гипергастринемией, включая индивидуумов с естественной гипергастринемией (например, неопластической или связанной с атрофией слизистой желудка) и/или гипергастринемией, возникающей вследствие применения фармакотерапии, подавляющей кислоту, (например, классов средств, включая любые ингибиторы протонной помпы или любые короткодействующие или долго действующие антагонисты двух типов гистаминовых рецепторов) и/или iv) индивидуумов с резекцией желудка. В некоторых вариантах осуществления лечение, улучшение состояния и/или профилактику проводят с использованием направленно воздействующего на гастрин средства, например, антагониста гастрина, такого как направленно воздействующего на гастрин или направленно воздействующего на рецептор гастрина средства, например, антагониста гастрина или гастринового рецептора, например, средства, которое направленно воздействует на рецептор CCK2.
[0009] Некоторые варианты осуществления относятся к способам, видам использования и средствам для лечения или профилактики заболевания или состояния костей у индивидуума путем введения индивидууму направленно воздействующего на гастрин или рецептор гастрина средства, таким образом, проводя лечение или профилактику заболевания или состояния или его прогрессирования. В некоторых аспектах направленное на гастрин или рецептор гастрина средство представляет собой антагонист гастрина или антагонист гастринового рецептора, такой как селективный антагонист гастринового рецептора, такой как селективный антагонист рецептора CCK2, например, антагонист, который не антагонизирует другие рецепторы или другие рецепторы гастрина. Примером селективного антагониста рецептора CCK2 является YF476.
[0010] В некоторых аспектах заболевание или состояние костей представляет собой заболевание или состояние, которое характеризуют как остеопороз, например, заболевание или состояние, которое характеризовали как остеопороз клинически, патологически или радиологически. В некоторых аспектах индивидуум представляет собой индивидуума женского пола со сниженной овариальной функцией или недостаточностью яичников. В других аспектах индивидуум: (a) представляет собой индивидуума женского пола со сниженной овариальной функцией или недостаточностью яичников и (b) страдает гипергастринемией. В некоторых аспектах индивидуум: (a) представляет собой индивидуума женского пола со сниженной овариальной функцией или недостаточностью яичников, (b) страдает гипергастринемией, (c) переносил резекцию желудка. В некоторых аспектах индивидуум страдает естественной гипергастринемией, такой как гипергастринемия, которая представляет собой неопластическую гипергастринемию или гипергастринемию, связанную с фармакотерапией, подавляющей кислоту, такой как введение ингибитора протонной помпы или антагонист гистаминовых рецепторов 2 типа. В некоторых аспектах способ дополнительно включает введение индивидууму ингибитора протонной помпы или антагониста гистаминовых рецепторов 2 типа, одновременно или последовательно в любом порядке с направленно воздействующим на гастрин или рецептор гастрина средством. В некоторых аспектах способ дополнительно включает проведение другого лечения остеопороза одновременно или последовательно в любом порядке по отношению к средству.
[0011] В некоторых вариантах осуществления способ лечения заболевания или состояния костей, связанного с гипергастринемией, у нуждающегося в этом индивидуума включает введение индивидууму по меньшей мере одной дозы терапевтически эффективного количества направленно воздействующего на рецептор гастрина средства, таким образом проводя лечение заболевания или состояния костей, связанного с гипергастринемией.
[0012] В других вариантах осуществления способы дополнительно включают введение доз направленно воздействующего на рецептор гастрина средства внутривенно.
[0013] В дополнительных вариантах осуществления способы дополнительно включают введение доз направленно воздействующего на рецептор гастрина средства перорально.
[0014] В некоторых вариантах осуществления способы дополнительно включают заболевание или состояние, характеризуемое как остеопороз.
[0015] В других вариантах осуществления способы дополнительно включают введение селективного антагониста рецептора CCK2.
[0016] В дополнительных вариантах осуществления способы дополнительно включают введение селективного антагониста рецептора CCK2 YF476.
[0017] В некоторых вариантах осуществления способы дополнительно включают индивидуума, который представляет собой индивидуума женского пола ос сниженной овариальной функцией или недостаточностью яичников. В других вариантах осуществления способы дополнительно включают индивидуума, который представляет собой: (a) индивидуума женского пола со сниженной овариальной функцией или недостаточностью яичников и (b) страдает гипергастринемией. В некоторых вариантах осуществления способы дополнительно включают индивидуума, который: (a) представляет собой индивидуума женского пола ос сниженной овариальной функцией или недостаточностью яичников, (b) страдает гипергастринемией, (c) переносил резекцию желудка.
[0018] В еще одном варианте осуществления гипергастринемия представляет собой неопластическую гипергастринемию или гипергастринемию, связанную с фармакотерапией, подавляющей кислоту.
[0019] В других вариантах осуществления способы дополнительно включают введение селективного направленно воздействующего на рецептор гастрина средства с терапевтически эффективным количеством ингибитора протонной помпы (PPI) или антагониста гистаминовых рецепторов 2 типа (H2R) одновременно или последовательно в любом порядке.
[0020] В еще одном варианте осуществления способы дополнительно включают, где PPI представляет собой омепразол, и антагонист H2R представляет собой локстидин.
[0021] В других вариантах осуществления способы дополнительно включают введение терапевтически эффективного количества направленно воздействующего на рецептор гастрина средства при 0,2-14 мкг/кг массы тела индивидуума.
[0022] В дополнительных вариантах осуществления терапевтически эффективное количество направленно воздействующего на рецептор гастрина средства составляет 10-25 наномоль.
[0023] В некоторых вариантах осуществления направленно воздействующее на рецептор гастрина средство вводят индивидууму посредством подкожной инъекции.
[0024] В дополнительных вариантах осуществления направленно воздействующее на рецептор гастрина средство вводят индивидууму посредством внутривенной инъекции.
[0025] В некоторых вариантах осуществления направленно воздействующее на рецептор гастрина средство вводят индивидууму перорально в виде суточной дозы в таблетках в дозах 20-100 мг.
[0026] Также предложены средства и композиции, например, фармацевтические композиции, и наборы для применения в предоставленных способах, такие как средства и композиции, содержащие направленно воздействующие на гастрин и на рецептор гастрина средства, например, антагонисты, и наборы, содержащие те же компоненты с инструкциями по введению таким индивидуумам.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0027] Фигура 1 представляет собой диаграмму, демонстрирующую соединения, регулирующие ремоделирование костной ткани. Овариальная функция (и секреция эстрогена) положительно связана с поддержанием костной ткани. Предполагают, что витамин D дополняет это, но, несмотря на то, что низкий уровень витамина D ассоциирован с остеопорозом, это может являться сопутствующий симптом, т.к. мутации рецептора витамина D не связаны с повышенным риском переломов. Продуцируемый паращитовидной железой PTH отрицательно регулирует физиологию костей, где эффект усиливается низкими уровнями кальция. Эстроген антагонизирует отрицательный эффект PTH. Роль гормонов желудочно-кишечного тракта еще до конца не ясна, но известно, что удаление желудка усиливает остеопороз. Полагают, что это отражает потерю кислоты и получаемое в результате снижение усвоение кальция.
[0028] Фигура 2 представляет собой иллюстрацию, демонстрирующую физиологические и структурные параметры и праметры прочности костей. Для оценки динамики и остеопоротических переломов костей на различных моделях на животных использовали компьютерную микротомографию (MicroCT) и сгибание костей, а также накопление осмия и ПЦР. MicroCT оценивали плотность и объем губчатых и трубчатых костей. Можно проводить измерения радиуса и окружности трубчатой кости. Можно проводить вычисления плотности соединительной ткани, показатель структурной организации (SMI), а также жесткости (все параметры структуры) кости. Полярный момент инерции (pMOI), а также перелом и рабочие нагрузки определяют исходную прочность кости. По накоплению осмия определяют изменения адипогенных фенотипов, тогда как ПЦР можно оценивать активацию транскриптов, участвующих в активации костной ткани.
[0029] Фигура 3 представляет собой серию графиков (3A-3D), демонстрирующих, что G-клетки действуют как сенсоры кальция. Стимулируемое CaCl2 (4 мМ) приток кальция (сдвиг FITC: >чем в 5 раз вправо - измеряемый с использованием проточной цитометрии), которое не наблюдалось при отсутствии CaCl2 (3A). CaCl2 зависящим от дозы образом стимулировал высвобождение гастрина (EC50=4,1 мМ, в 8 раз), и ингибировали предварительной инкубацией (10 минут) с антагонистом кальциевых каналов, нифедипином (1 мкМ) (3B). Эта опосредованная кальцием секреция гастрина не являлась связанной с продукцией цАМФ (3C), и ее невозможно было ингибировать ингибитором PKA H-89 (10 мкМ) или ингибитором MAPK PD98059 (0,1 мкМ), которые связаны с опосредованной цАМФ/MAPK секрецией гастрина (3D). В противоположность этому, вортманнин (1 нМ), ингибитор путей передачи сигнала PI3K существенно ингибировал опосредованное CaCl2 высвобождение гастрина. Эти результаты демонстрируют, что секреция гастрина является связанной с регулируемым кальциевыми каналами кальций-чувствительный механизм, который трансдуцировался через пути передачи сигнала PI3K. Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с нестимулированными клетками, WORT: вортманнин.
[0030] Фигура 4 представляет собой серию графиков (4A-4D), демонстрирующих стимуляцию PTH функции G-клеток. PTH стимулировал высвобождение гастрина в ~8 раз больше с ожидаемой EC50=60 нМ (4A), эффект, который можно было ингибировать предварительной инкубацией с ингибитором PKA, H-89 (10 мкМ) в течение 10 минут (4B). PTH также зависящим от дозы образом стимулировал продукцию цАМФ (E50=4 нМ, 250%) (4C), ответ, который получали посредством H-89 (предварительная инкубация: 10 минут - 10 мкМ) (4D). Эти результаты демонстрируют, что секреция гастрина сопряжена с опосредованной рецептором PTH активацией PKA и передачей сигналов цАМФ. Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с нестимулированными клетками или в сравнении с одним PTH.
[0031] Фигура 5 представляет собой два графика (5A-5B), демонстрирующих, что кальцитонин ингибирует функцию G-клеток. Кальцитонин ингибировал высвобождение гастрина с ожидаемой IC50=1,9 нМ (~20%, 5A), эффект, который получали предварительной инкубацией с ингибитором PKA, H-89 (10 мкМ). Кальцитонин зависящим от дозы образом ингибировал продукцию цАМФ (I50=3,8 нМ, 20%) (5B). Эти результаты демонстрируют, что секреция гастрина сопряжена с опосредованным рецептором кальцитонина ингибированием PKA передачи сигналов цАМФ. Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с нестимулированными, #p<0,05 в сравнении с опосредованным кальцитонином ингибированием.
[0032] Фигура 6 представляет собой серию графиков (6A-6C), демонстрирующих ингибирование эстрогеном функции G-клеток. G-клетки экспрессируют транскрипты ESRα (6A), и 17β-эстрадиол ингибирует синтез цАМФ (IC50=1,1×10-12M, -15%) и высвобождение гастрина (IC50=4,6×10-12M, ~20%) (6B). Кроме того, предварительная инкубация с таким агонистом ESRα ингибировала фосфорилирование MAPK (75%, 6C). Эти результаты выявляют, что секреция гастрина ингибируется опосредованным эстрогеновым α-рецептором ингибированием продукции PKA/цАМФ и передачи сигнала MAPK. Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с одним 17β-эстрадиолом (1 нМ).
[0033] Фигура 7 представляет собой модель регуляции G-клеток. Просветные средства, включая поступающий с пищей кальций, непосредственно или опосредованно индуцируют фосфорилирование ERK путем активации аденилатциклазы (AC) посредством связывания с Gα, что приводит к секреции гастрина. PTH через сопряженный с G-белком рецептор PTH1 также стимулирует высвобождение гастрина этим путем. Фосфорилирование ERK может положительно влиять на приток Ca2+, который непосредственно увеличивается в зависимости от рациона. Кальциевые каналы L-типа аналогично регулируют секрецию через активацию PKC. Ингибиторы секреции гастрина включают кальцитонин (через ингибирование цАМФ) и эстрогены, которые активируют ERα с ингибированием цАМФ и пути MAPK. AC: аденилатциклаза; GAS: гастрин; PDK: фосфоинозитид-зависимая киназа; PKA: протеинкиназа A; пунктирные линии отражают ингибирование, сплошные линии - стимуляцию.
[0034] Фигура 8 представляет собой два графика (8A-8B), демонстрирующих стимуляцию гастрином секреции PTH человека. Рецепторы гастрина (CCK2) и гистамина (H1) экспрессируются в in главными клетками PTH, выделенными из клинических хирургических резекций (8A). Эти клетки экспрессируют высокие уровни (в 3 раза выше) PTH (5A). Стимулируемый гастрином синтез PTH (EC50=10-9M, 40%) и высвобождение (EC50=4,2×10-10M, 50%) (8B). Эти результаты демонстрируют, что синтез и секреция PTH сопряжены с опосредованной рецептором гастрина (CCK2) активацией. Среднее значение±SEM (n=4 эксперимента).
[0035] Фигура 9 представляет собой серию графиков (9A-9D), демонстрирующих, что гастрин стимулирует функцию C-клеток щитовидной железы (MTC-SK). Стимулируемая гастрином продукция цАМФ (EC50=6,7×10-13M, ~5-кратная) предотвращалась селективным антагонистом рецептора CCK2, YF476 (9A). YF476 отдельно не оказывал достоверный эффект. Стимулирующее гастрином действие в отношении цАМФ можно было ингибировать предварительной инкубацией с ингибитором PKA, H-89 (10 мкМ) (9B). На секрецию кальцитонина зависящим от дозы образом оказывал влияние гастрин, эффект, обратимый YF476 (9C). Гастрин (0,1 нМ) стимулировал (~3-кратно) транскрипцию гена кальцитонина, эффект, обратимый предварительной инкубацией с H-89 (10мкМ) (9D). H-89 не ингибировал экспрессию рецептора CCK2 (9D). Эти результаты выявляли, что синтез и высвобождение кальцитонина регулируется опосредованной рецептором гастрина (CCK2) активацией PKA и передачей сигналов цАМФ. Среднее значение±SEM (n=4 эксперимента). #p<0,05 в сравнении с нестимулированными, *p<0,05 в сравнении с одним гастрином (0,1 нМ).
[0036] Фигура 10 представляет собой иллюстрацию (10A), микрофотографию (10B) и серию графиков (10C-10F), демонстрирующую эффект гастрина на синтез и секрецию PTH и MTC-SK - модельная система совместного культивирования. Клетки PTH человека, выделяемые из хирургических образцов, культивировали совместно с линией клеток MTC-SK. Диаграмма, на которой подробно представлены места расположения клеток и участок расположения мишени представлены на 10A, тогда как на микрофотографиях продемонстрирован рост каждого из этих типов клеток (10B). Добавление гастрина к системе совместного культивирования значительно стимулировало транскрипцию (~75%, 10C) и секрецию (~60%, 10D) PTH. Эти эффекты моно было предотвращать предварительной инкубацией (10 минут) с избирательным антагонистом рецептора CCK2, YF476 (10 нМ). В противоположность этому, гастрин ингибировал как транскрипцию (до основного уровня - 10E), так и высвобождение кальцитонина (~70% - 10F). Эти результаты выявляют, что основной эффект гастрина в модельной системе заключается в стимуляции PTH и ингибировании кальцитонина. Последний эффект являются противоположным стимулирующему действию гастрина в экспериментах одной культуры (одни клетки MTC-SK). CON=контроль, GAS=гастрин (10-10M), G+INH=гастрин+YF476 (10-11M). PET=полиэфирная мембрана (0,4 мм). Среднее значение±SEM, n=3. *p<0,05 в сравнении с контролем (нестимулируемые), **p<0,05 в сравнении с гастрином (10-10M).
[0037] Фигура 11 представляет собой график (11A) и серию микрофотографий (11B-11H), демонстрирующих экспрессию рецептора CCK2 в выделенных получаемых из кости клетках и в кости. Уровни транскриптов рецептора CCK2 идентифицировали в остеобластах свода черепа (OB), линия клеток hFOB (hFOB) и в получаемых из костного мозга мезенхимальных стволовых клетках человека (BMMSC) (11A). С использованием иммуногистохимии идентифицировали специфическое иммуноокрашивание в эпифизарной пластинке (EP), а также в клетках костного мозга (стрелки) (11B, 11C - увеличение 100×). Клетки, вовлеченные в эндохондральное окостенение, экспрессируют рецепторы (11D, E, F), как экспрессируют остеобласты (11F). Подтверждали наличие положительных по CCK2R остеобластов, выстилающих внутреннюю надкостницу (11G), а также в срастающейся кости (11H). Авторы интерпретируют эти результаты как указание на то, что CCK2R экспрессируется на хондроцитах, остеобластах и мезенхимальных клетках костного мозга, и CCK2R участвует в регуляции окостенение и срастании костей. Направленное воздействие на рецептор, вероятно, регулирует эти явления. Иммуноокрашивание CCK2R=коричневые клетки (DAB), контрастное окрашивание=гематоксилин. 11D-H: увеличение=400×.
[0038] Фигура 12 представляет собой фотографию (12A), анализ последовательности (12B) и фотографию (12C), демонстрирующую экспрессию гастрина/CCK2 в образцах костного мозга человека. Стандартной ПЦР идентифицировали полосу ~320 пар оснований (стрелка) в выделенном костном мозге трубчатой кости - образцы, получаемые в результате ампутации при атеросклерозе, индуцированном ишемией конечности (нет признаков остеомиелита) (12A). Анализом последовательности (BioEdit) идентифицировали 92% гомологию с каноническим геном CCK2 (12B). Вестерн-блоттингом подтверждали экспрессию CCK2 в 10 исследуемых образцах (стрелка - 50 кДа) (12C).
[0039] Фигура 13 представляет собой группу графиков (13A и 13B), демонстрирующих эффект гастрина и направленное действие CCK2 на пролиферацию клеток костного происхождения. Гастрин зависящим от дозы образом стимулировал поглощение BrdU во всех типах клеток с EC50=1-2×10-11M (13A). Это не предотвращали селективным антагонистом рецептора CCK2, YF476, который, по-видимому, увеличивал пролиферацию, в частности в BMMSC (13B). Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с нестимулированными, #p<0,05 в сравнении с гастрином (0,1 нМ).
[0040] Фигура 14 представляет собой группу графиков (14A и 14B), демонстрирующих эффект гастрина и направленное действие CCK2 на минерализацию клеток костного происхождения. Гастрин зависящим от дозы образом ингибировал минерализация костей (измеряемую с использованием Ostemalge) во всех типах клеток при IC50=3,2×10-11-1,3×10-10 M (14A). Это не предотвращали селективным антагонистом рецептора CCK2, YF476, который повышал минерализацию, в частности в остеобластах свода черепа (14B). Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с нестимулированными, #p<0,05 в сравнении с гастрином (0,1 нМ).
[0041] Фигура 15 представляет собой группу графиков, демонстрирующих эффект гастрина и направленное действие CCK2 на экспрессию генов клеток костного происхождения. Гастрин (1 нМ) ингибировал экспрессию гена дифференцировки остеобластов, щелочную фосфатазу (ALKP) во всех типах клеток (верхний ряд). Это предотвращали селективным антагонистом рецептора CCK2, YF476 (1 нМ). Гастрин также ингибировал M-CSH и RANKL в остеобластах, которые нормализовал YF476 (нижний ряд). Среднее значение±SEM (n=4 эксперимента). *p<0,05 в сравнении с нестимулированными, #p<0,05 в сравнении с гастрином (1 нМ).
[0042] На фигуре 16 продемонстрированы эффекты краткосрочной и хронической гипергастринемии на уровни циркулирующего гормона на моделях на Mastomys. Уровни гастрина значительно повышались на 8 (в ~2 раза) и 16 неделях (в ~3,5 раза) лечения. Уровень эстрогена (эстрадиола) снижался (~50%) у животных с краткосрочной и длительной гипергастринемией. PTH значительно повышался на 8 неделе (~75%), но значительно снижался на 16 неделе (в ~3 раза). Эти результаты демонстрируют, что краткосрочная гипергастринемия на модели in vivo ингибирует высвобождение эстрогена с взаимной активацией секреции PTH. Длительная гипергастринемия также связана со снижением уровня эстрадиола, но это не приводит к повышенному уровню PTH. Механизм последнего до конца не ясен, но может отражать подавление рецептора CCK2 или ответов его сигнальной системы в железе PTH, подвергаемой длительной стимуляции гастрином. Среднее значение±SEM, *p<0,05 в сравнении с контрольными животными. #p<0,05 в сравнении обрабатываемыми животными на 8 неделе. CON=контрольные животные, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0043] Фигура 17 представляет собой пару графиков (17A и 17B) и фотографии (17C), демонстрирующие экспрессию связанных с системой кальция рецепторов, PTH1R, ERα и CaSR в желудке на моделях на Mastomys. Результаты ПЦР и вестерн-блоттинга слизистой желудка от нормальных (n=4) по сравнению с животными, которых обрабатывали локстидином в течение 8 (n=4) и 16 (n=5) недель соответственно. В своде краткосрочная (8 недель) и длительная (16 недель) гипергастринемия значительно повышали уровень HDC, но снижали экспрессию PTH1R и ERα соответственно (17A). В антральном отделе гипергастринемия была связана со значительными повышениями уровней транскриптов гастрина, а также повышениями уровней экспрессии PTH1R, ERα и CaSR (17B). Эти эффекты являлись более выраженными при длительной гипергастринемии. Эффекты РНК воспроизводились на уровне белков (вестерн-блоттинг - 17C). В частности, экспрессия PTH1R являлась пониженной в своде (F), но повышалась в антральном отделе (A) - верхняя панель. Экспрессия ERα в антральном отделе являлась повышенной на 16 неделе (центральная панель), как и CaSR (нижняя панель). Эти результаты демонстрируют, что свод и антральный отдел реагируют на краткосрочную и длительную гипергастринемию различными синтезом и видами экспрессии рецепторов, связанных с системой кальций:кость. В частности, функциональные рецепторы подавляются в синтезирующей гистамин части желудка (своде), но активируются в секретирующем гастрин (антральном) отделе желудка. В некоторых аспектах это отражает сенсибилизацию антрального отдела и чувствительных к кальцию G-клеток. Среднее значение±SEM, *p<0,05 в сравнении с контрольными (необрабатываемыми) животными. CON=контрольные животные, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
44] На фигуре 18 продемонстрирована экспрессия рецептора CCK2 в паращитовидной железе и щитовидной железе. Иммуноокрашивание на рецептор CCK2 выявляло, что большая часть клеток паращитовидной железы в паращитовидной железы являются положительными в отношении CCK2 (различные красители отражают мембраносвязанную экспрессию [стрелки] и клеточные ядра] 18A). В щитовидной железе можно идентифицировать отдельные C-клетки, которые окрашиваются антителами против CCK2 (окрашивание отражает мембраносвязанную экспрессию [стрелки] - 18B, 18C (две нижние стрелки)). В противоположность этому инфильтрирующие иммунные клетки в щитовидной железе Mastomys являются отрицательными в отношении CCK2 (три верхние стрелки, только синие ядра) (18C). Эти результаты демонстрируют мембранную экспрессию рецептора CCK2 в PTH и клетках щитовидной железы. Это соответствует результатам in vitro, демонстрирующим эффекты гастрина на клетки, выделяемые из этих структур. Краситель для ядра=DAPI, другой краситель=меченный FITC CCK2. Антитело от Abeam (ab14439, кролика поликлональное, разведение 1:100).
[0045] На фигуре 19 представлены изменения губчатой кости на модели краткосрочной и хронической гипергастринемии на животных, измеряемые с использованием компьютерной микротомографии (microCT). Объем костной ткани (19A) и отношение объема костной ткани к объему губчатой котной ткани (19B) являлись пониженными как у животных с краткосрочной гипергастринемией, так и у животных с длительной гипергастринемией, но это являлось более выраженным у животных, которых обрабатывали в краткосрочном периоде (50% в сравнении с 30%). Две величины плотности, кажущейся плотности (19C) и плотности ткани (19D) являлись существенно сниженными в обеих группах гастрина (~100%). Плотность соединительной ткани (измерение числа трабекул в единице объема) являлась существенно сниженной (~60%) в группе длительной гипергастринемии (19E). Краткосрочный гастрин являлся вязанным с преобразованием кости из более пластинчатой структуры (SMI близкий к 0) в более балкообразную структуру (SMI более >1) (19F). Это не являлось настолько выраженным у животных с длительной гипергастринемией. Эти результаты демонстрируют, что гастрин существенно изменяет фенотип кости на модели на Mastomys. Изменения соответствуют "остеопорозному" фенотипу. BV=объем костной ткани, TV=объем губчатого вещества, плот. соед. тк.=плотность соединительной ткани, SMI=показатель структурной модели (параметры геометрии балки:пластины). Среднее значение±SEM, *p<0,05 в сравнении с контрольными животными. CON=контрольные животные, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0046] Фигура 20 представляет собой серию фотографий, демонстрирующих окрашивание на основе осмия на активацию жировой ткани кости. Адипоциты поглощают осмий, и их легко идентифицировать в кости. У контрольных животных (правая бедренная кость, n=5, верхняя панель) преимущественно демонстрировали накопление осмия в большеберцовом эпифизе. У животных с краткосрочной гипергастринемией также демонстрировали накопление осмия в эпифизе, но также отмечали существенное поглощение в метафизе (n=5, нижняя панель). Эти результаты соответствуют активации гастрином жировой ткани и "стареющему" фенотипу.
[0047] Фигура 21 представляет собой серию микрофотографий, демонстрирующих окрашенные толуидиновым синим, TRAP бедренные кости от контрольных, обрабатываемых в течение 8 недель и 16 недель локстидином Mastomys, демонстрирующих характер минерализации костей и полости резорбции. В одном из аспектов изменения у обрабатываемых локстидином животных отражают снижение минерализации костей и повышенную резорбцию - признаки, соответствующие остеопорозным фенотипам. BM=минерализация костей, RC=полость резорбции.
[0048] Фигура 22 представляет собой серию графиков (22A-22C), демонстрирующих сравнение между microCT и разрушением костей на моделях Mastomys. Бедренные кости подвергали нагрузке на разрушение (сгибание в четырех точках) с использованием сервогидравлической испытательной машины (Instron модель 8874). Отмечали значимую корреляцию (R2=0,86, p<0,01) между прочностью кости и нагрузкой перелома (22A), демонстрирующую, что для повышенной прочности костей требуется большая нагрузка перелома. Авторы оценивали взаимосвязь между измерениями сгибания кости и microCT по отношению к плотности губчатого и трубчатого веществ. Эти данные выявляли, что плотность губчатого вещества обратно коррелировала (R2=-0,54) с силой, необходимой для перелома кости (22B), тогда как повышенная плотность трубчатого вещества соотносилась с более высокими нагрузками переломов (R2=0,71, 22C). Эти результаты демонстрируют, что механическая сила, необходимая для перелома кости соотносится со структурой и плотностью костей, и что комбинация этих двух подходов предоставляет физиологически релевантную информацию в этой модели. N=7 животных, uCT=microCT.
[0049] Фигура 23 представляет собой таблицу, в которой обобщены опосредуемые гастрином изменения на модели на Mastomys. По сравнению с контролем (необрабатываемыми животными с нормогастринемией) краткосрочная обработка локстидином повышала уровень циркулирующего гастрина и PTH, но понижала уровень эстрадиола. Это соотносилось со сниженной плотностью костей и остеопорозным фенотипом. В желудке экспрессия PTH1R повышалась, при этом экспрессия ERα снижалась. Не детектировали изменений кальцийчувствительного рецептора (CaSR). По сравнению с контролем длительная обработка локстидином повышала уровень циркулирующего гастрина, но снижала уровень PTH, а также эстрадиола. Это соотносилось со сниженной плотностью костей и остеопорозным фенотипом. В желудке экспрессия PTH1R, ERα и CaSR повышалась в соответствии с активацией метаболического фенотипа на основе кальция. 8 недель=обработка локстидином в течение 8 недель, 16 недель=обработка локстидином в течение 16 недель, п. костей=измерения плотности костей, Osteo=остеопорозный фенотип.
[0050] Фигура 24 представляет собой таблицу, демонстрирующую обзор опосредованных гастрином изменений фенотипа кости на модели на Mastomys. По сравнению с контролем (необрабатываемыми животными с нормогастринемией) у животных с краткосрочной обработкой выявляли повышенный уровень циркулирующего гастрина и PTH, но пониженный уровень эстрадиола. Это соотносилось со сниженной плотностью костей и остеопорозным фенотипом (включая слабую кость с низкой прочностью на скручивание). У животных, получавших длительную обработку, не отмечали повышенный уровень циркулирующего гастрина, но уровни PTH и эстрадиол являлись пониженными. Это соотносилось со сниженной плотностью костей и остеопорозным фенотипом, который характеризовался слабой, но прочной костью. pMOI=полярный момент инерции, PTH=паратиреоидный гормон.
[0051] Фигура 25 представляет собой график, демонстрирующий эффекты овариэктомии на опосредованные краткосрочной и хронической гипергастринемией уровни циркулирующего PTH на модели на Mastomys. Овариэктомия повышала уровни PTH на ~100%. Краткосрочная гипергастринемия аналогично повышала уровни PTH. Уровень PTH повышался (на 300% выше контроля) у животных с OVX/обработкой в течение 8 недель. Длительная обработка гастрином значительно снижала уровни на ~60%. Овариэктомия предотвращала это, нормализуя уровни PTH. Эти результаты подтверждают опосредованную овариэктомией активацию высвобождения PTH (согласующуюся со снижением эстрогена), и что это усиливается краткосрочной гипергастринемией на модели in vivo. Длительная гипергастринемия, по-видимому, снижает высвобождение PTH, эффект, который также наблюдают у животных после овариэктомии. Механизм может отражать подавление рецептора CCK2 или ответов его сигнальной системы в железе PTH, подвергаемой длительной стимуляции гастрином. Такой эффект преобладает над снижением эстрогена, что указывает на то, что гастрин может играть роль в функционировании железы PTH. Среднее значение±SEM, *p<0,05 в сравнении с контрольными животными, #p<0,05 в сравнении с одной OVX. CON =контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0052] Фигура 26 представляет собой серию графиков (26A-26D), демонстрирующих экспрессию связанных с нейроэндокринной системой транскриптов в желудке на моделях овариэктомии на Mastomys с нормо- и гипергастринемией. Результаты ПЦР слизистой желудка от нормальных животных (n=11) по сравнению с Mastomys после овариэктомии (OVX; n=8) (верх) и между животными с OVX и краткосрочной (n=4) и длительной (n=4) гипергастринемией-OVX (низ). Овариэктомия значительно повышала экспрессию CgA (в 4 раза) и HDC (в ~6 раз) (26A) в слизистой желудка. Ни краткосрочная, ни длительная гипергастринемия не оказывала какой-либо дополнительных эффект на опосредованный OVX синтез CgA (в 2,8-4,2 раза по сравнению с в 4,3 раза) (26B). Краткосрочная гипергастринемия повышала экспрессию гастрина (в ~40 раз - 26C) и HDC (в ~40 раз - 26D). Длительная гипергастринемия повышала гастрин, а также HDC, но эффект являлся более выраженным для экспрессии HDC, получаемого из ECL-клеток (в ~45 раз- 26D). Эти результаты подтверждают, что эстроген регулирует транскрипцию HDC ECL-клеток (и таким образом синтез гистамина), и что синтез гастрина аналогично регулируется эстрогеном. Циркулирующий гастрин дополнительно повышает экспрессию. Среднее значение±SEM, *p<0,05 в сравнении с не подвергаемыми овариэктомии животными. #p<0,05 в сравнении OVX. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0053] Фигура 27 представляет собой график, демонстрирующий экспрессию связанных с системой кальция рецепторов PTH1R, ERα и CaSR в желудке на модели овариэктомии на Mastomys с нормогастринемией. Результаты ПЦР слизистая желудка от нормальных Mastomys по сравнению с Mastomys после овариэктомии (OVX). Овариэктомия повышала экспрессию андрогенного рецептора (в ~6 раз), а также оба эстрогеных рецептора (ESR1 и ESR2, оба в ~4 раза) в слизистой желудка. CaSR и PTH1R также являлись повышенными в результате снижения уровня эстрогена (в 5 и 4 раза соответственно). Эти результаты подтверждают, что снижение уровня эстрогена связано с усилением экспрессии транскриптов, связанных с чувствительной к кальцию системой, и системой паращитовидной железа:яичник. Циркулирующий гастрин дополнительно повышает экспрессию. Среднее значение±SEM, *p<0,05 в сравнении с животными, не подвергавшимися овариэктомии. CON=контрольные животные с ложной операцией (n=11), OVX=овариэктомия (n=8). AR=андрогенный рецептор, ESR=эстрогенный рецептор, CaSR=кальцийчувствительный рецептор, PTH1R=рецептор 1 типа паращитовидной железы.
[0054] Фигура 28 представляет собой серию графиков (28A-E), демонстрирующих экспрессию связанных с системой кальция рецепторов PTH1R, AR, ERα и CaSR в желудке на модели овариэктомии на Mastomys с гипергастринемией. Результаты ПЦР слизистой желудка от животных с OVX и краткосрочной (n=4) и длительной (n=4) гипергастринемией с OVX. Индуцированные овариэктомией повышения андрогенных рецепторов нормализовалист у животных с краткосрочной и длительной гипергастринемией, где эффект являлся более выраженным у животных с краткосрочной гипергастринемией (28A). Аналогичный результат отмечали для обоих эстрогеновых рецепторов (28B, C). CaSR (28D) и PTH1R (28E) значительно снижались в результате гипергастринемии. Эти результаты выявляют, что экспрессия рецепторов, связанных с системой кальций:кость, которая является повышенной в результате овариэктомии в слизистой желудка, "нормализовалась" как краткосрочной, так и длительной гипергастринемией. Это отражает физиологическую попытку регулировать или перекалибровать чувствительность к кальцию в среде с высоким уровнем гастрина. Среднее значение±SEM, *p<0,05 в сравнении с животными после овариэктомии, #p<0,05 в сравнении с животными с краткосрочной гипергастринемией. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия. AR=андрогенный рецептор, ESR=эстрогенный рецептор, CaSR=кальцийчувствительный рецептор, PTH1R=рецептор 1 типа паращитовидной железы.
[0055] Фигура 29 представляет собой серию снимков экрана (29A-H), демонстрирующий характеристики компьютерной микротомографии (microCT) губчатой и трубчатой кости. Для губчатой кости от животных после овариэктомии демонстрировали значительное уменьшение (29B) по сравнению с контрольной костью (29A). Краткосрочная (29C) и длительная (29D) гипергастринемия нивелировали это - эффекты являлись более выраженными у животных с длительной гипергастринемией. В трубчатой кости овариэктомия была ассоциирована с изображениями губчатой и трубчатой кости от нормальных животных, животных после овариэктомии (OVX) и животных после OVX, обрабатываемых локстидином в течение 8 и 16 недель, соответственно. После OVX отмечают остеопороз, в частности в губчатом веществе бедренной кости. В некоторых аспектах это может усиливаться в результате повышений уровней гастрина. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0056] Фигура 30 представляет собой серию графиков (30A-D), демонстрирующих измерения MicroCT в губчатой и трубчатой кости на моделях овариэктомии на Mastomys с нормо- и гипергастринемией. Плотность губчатой кости значительно снижалась в результате овариэктомии (~50%) по сравнению с нормальными животными (30A). Это усиливалось длительной гипергастринемией (85%). Объем губчатого вещества также значительно снижался в результате овариэктомии (~50%) (30B). Это усиливалось длительной гипергастринемией (~70%). Плотность трубчатой кости не снижалась в результате овариэктомии, но являлась значительно ниже у животных с длительной гипергастринемией (~5%, 30C). Объем трубчатого вещества значительно снижался в результате овариэктомии (~30%) (30D). Это усиливалось краткосрочной гипергастринемией (~30%). Эти результаты демонстрируют, что гастрин усиливает остеопороз на модели овариэктомии и приводит к характеристикам microCT, соответствующим остеопорозному фенотипу. Эффекты длительной гипергастринемии в основном отражаются в изменениях в губчатом веществе. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0057] Фигура 31 представляет собой серию графиков (31A-D), демонстрирующих измерения MicroCT внутрикостных и надкостных размеров в трубчатой кости на моделях овариэктомии на Mastomys с нормо- и гипергастринемией. Внутрикостный радиус значительно уменьшался в результате овариэктомии (~20%) по сравнению с нормальными животными (31A). Это существенно усиливалось при краткосрочной гипергастринемии (30%). Внутрикостная окружность также значительно уменьшалась в результате овариэктомии (~18%) (31B). Это существенно усиливалось при краткосрочной гипергастринемии (~27%). Аналогично, надкостный радиус уменьшался у животных после овариэктомии (~20%, 31C), эффект значительно усиливался краткосрочной гипергастринемией (~30%). Надкостная окружность также уменьшалась в результате овариэктомии (~20%), эффект усиливался краткосрочной гипергастринемией (~30%) (31D). Эти результаты демонстрируют, что гастрин увеличивает размеры трубчатых костей, эффекты преимущественно усиливаются краткосрочной гипергастринемией. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0058] Фигура 32 представляет собой пару микрофотографий, демонстрирующих окрашенные толуидиновым синим, TRAP бедренные кости от Mastomys после овариэктомии, идентифицирующие характер минерализации костей и полости резорбции, а также число и положение остеокластов. Окрашивание TRAP указано красными клетками; остеокласты представляет собой окрашенные красным многоядерные клетки (желтая стрелка). Левая панель (увеличение 100×), правая панель (увеличение 400×). RC=полость резорбции.
[0059] Фигура 33 представляет собой серию графиков (33A-D), демонстрирующих результаты сгибания в 4 точках посредством Instron бедренных костей на моделях овариэктомии на Mastomys с нормо- и гипергастринемией. В результате овариэктомии повышалась жесткость (~15%), эффект, который значительно усиливался длительной гипергастринемией (33A). Краткосрочная гипергастринемия была ассоциирована со снижением жесткости до нормальных уровней. Предельная нагрузка для перелома кости являлась значительно ниже у животных после овариэктомии (~20% ~ 33B). Гипергастринемия не изменяла этой ситуации, но для животных с длительной гипергастринемией требовалась большая нагрузка для перелома кости по сравнению с животными с краткосрочной гипергастринемией. Нагрузка перелома аналогичным образом снижалась у животных после овариэктомии (~25%) и не изменялась под действием гастрина (33C). Однако для животных с длительной гипергастринемией не требовалась более высокая нагрузка для перелома по сравнению с животными с краткосрочной гипергастринемией. Полная работа, необходимая для перелома кости, увеличивалась у животных после овариэктомии (~20%) (33D). При этом длительная гипергастринемия не оказывала влияния на работу, для костей от животных с краткосрочной гипергастринемией требовалась на -50% меньше работы для перелома. Эти результаты демонстрируют, что на прочность костей после овариэктомии краткосрочное действие гастрина (приводящее к слабым костям) и длительное действие гастрина (делающее кости крепче) оказывает дифференциальное влияние. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0060] Фигура 34 представляет собой серию графиков (34A-E), демонстрирующих общую прочность кости на моделях овариэктомия на Mastomys с нормо- и гипергастринемией. Полярный момент инерции (pMOI) значительно понижался у животных после овариэктомии (25%, 34A). Эта величина перелом при нагрузке при скручивании в частности усиливалась краткосрочной гипергастринемией (~50%). pMOI значимо коррелировал с жесткостью (R2=0,23 - 34B), предельной нагрузкой (R2=0,33 - 34C) и нагрузкой перелома (R2=0,3 - 34D). Полная работа не коррелировала с pMOI (34E). Эти результаты подтверждают, что прочность на скручивание костей после овариэктомии снижается, и что краткосрочное действие гастрина конкретно увеличивает этот параметр. Общая корреляция с жесткостью и максимальными/нагрузками перелома является отражением эффектов овариэктомии на Mastomys. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия.
[0061] Фигура 35 представляет собой серию графиков (35A-I), демонстрирующих экспрессию связанных с ремоделированием костной ткани транскриптов в костном мозге, получаемом из трубчатой кости, на модели овариэктомии на Mastomys с нормогастринемией. Результаты ПЦР клеток костного мозга от нормальных по сравнению с Mastomys после (OVX) овариэктомии. Овариэктомия значительно понижала экспрессию ALOX5 (35A - воспаление: ~20%) и RUNX2 (29B - дифференцировка остеобластов: ~100% - 35B), но не TCF4 (35C - участвующем в опосредованном TGFβ образовании костей), IGF-1 (35D - образование костей), PTGS2 (35E - воспаление) или RANKL (35F - остеопороз). Отмечали увеличения CXCL12 (35G - активация остеобластов: ~20%), PPARg (35H - дифференцировка адипоцитов: ~60%) и HIF-1a (35I - опосредованное гипоксией повреждение костей: ~250%). Эти результаты подтверждают, что снижение эстрогена связано с активацией получаемых из костного мозга транскриптов, связанных с ремоделирование и остеопорозом. Среднее значение±SEM, *p<0,05 в сравнении с животными, не подвергавшимися овариэктомии. CON=контрольные животные с ложной операцией (n=11), OVX=овариэктомия (n=8).
[0062] Фигура 36 представляет собой таблицу, демонстрирующую обзор опосредованных гастрином изменений костного фенотипа на модели на Mastomys после овариэктомии. По сравнению с одной овариэктомией (животные с нормогастринемией с пониженным эстрогеном, повышенным PTH и остеопоротическими переломами, например, с жесткими, слабыми костями) для животных с краткосрочной гипергастринемией демонстрировали сниженные характеристики трубчатых костей, что было ассоциировано с более слабой костью с более низкой прочностью на скручивание. Такой фенотип являлся более выраженным, чем при одной овариэктомии. У животных с длительной гипергастринемией (с нормальным уровнем PTH) отмечали повреждение губчатой кости, приводящее к заметно жесткой кости. Такой фенотип являлся более выраженным, чем при одной овариэктомии. pMOI=полярный момент инерции, PTH=паратиреоидный гормон.
[0063] Фигура 37 представляет собой серию графиков, демонстрирующих эффекты нокаута по гастрину, нокаута по гистидиндекарбоксилазе или двойного нокаута на уровни циркулирующих гормонов на моделях на мышах после овариэктомии. Уровни эстрогена значительно снижались у всех животных ~50% в результате овариэктомии. Овариэктомия не влияла на уровни гастрина, но у животных с KO по HDC экспрессировались в ~3 раза повышенные уровни по сравнению с животными с KO по гастрину или двойным KO. PTH значительно снижался (~80%) у животных с KO по гастрину. В противоположность этому уровни повышались после овариэктомии как у животных с KO по HDC, так и у животных с двойным KO (~100%). Эти результаты демонстрируют, что снижение эстрогена не активирует высвобождение PTH у животных с KO по гастрину. Это дает основания предполагать, что гастрин модифицирует функцию эстрогена в паращитовидной железе. Среднее значение±SEM, *p<0,05 в сравнении с животными, не подвергавшимися овариэктомии. G=KO по гастрину, GH=двойной KO по гастрину/HDC, H=KO ПО HDC, KO=нокаут, N=без овариэктомии, O=овариэктомия.
[0064] Фигура 38 представляет собой серию графиков, демонстрирующих экспрессию рецепторов нейроэндокринной системы и кальцийчувствительных рецепторов в желудке на моделях нокаута на мышах после овариэктомии. В своде желудка комбинация KO по гастрину и овариэктомия значительно повышала CCK2 (чувствительность к гастрину ECL-клеток: в ~3 раза выше) и HDC (синтез гистамина ECL: в ~20 раза выше). В противоположность этому, не отмечали изменений в своде мышей с KO по HDC после овариэктомии. В антральном отделе CaSR значительно снижался у животных с KO по гастрину после овариэктомии (~60%), при этом CaSR (~60%), а также сама экспрессия гастрина (~70%) снижалась в антральном отделе мышей с KO по HDC после овариэктомии. В одном из аспектов это отражает то, что овариэктомия и снижение эстрогена в значительной степени активирует ECL-клетку и снижает кальцийчувствительные ответы G-клеток у животных с KO по гастрину. У животных с KO по HDC эффекты овариэктомии являются ограниченными антральным отделом. Среднее значение±SEM, *p<0,05 в сравнении животные, не подвергавшиеся овариэктомии. G=KO по гастрину, H=KO по HDC, KO=нокаут, N=без овариэктомии, O=овариэктомия.
[0065] Фигура 39 представляет собой серию графиков (39A-F), демонстрирующих измерения MicroCT в измерениях в трубчатом и губчатом веществах на моделях на мышах после овариэктомии. У животных с KO по гастрину внутрикостный радиус (39A) и окружность (39B) значительно уменьшались (~30%) после овариэктомии. Это отражает то, что сочетание снижения эстрогена и отсутствие гастрина повышало толщину трубчатой кости. Снижение гастрина в этих обстоятельствах не оказывает отрицательного влияния на костную ткань. У животных с KO по HDC овариэктомия значительно снижала объем трубчатой костной ткани (~25% - 39C), но приводили к костной ткани с более высокой прочностью на скручивание (39D). Это определяет, что снижение гистамина усугубляет эффекты эстрогена на костную ткань. Двойной KO был ассоциирован с уменьшением объема в губчатой (~50% - 39E) и трубчатой костной ткани (~15% - 39F), но это не переходило в существенную слабость костной ткани. Это выявляет, что, несмотря на то, что наблюдают некоторые изменения костного фенотипа, сочетание снижения гастрина и гистамина значительно не изменяет биологию костной ткани. G=KO по гастрину, GH=двойной KO по гастрину/HDC, H=KO по HDC, N=без овариэктомии, O=овариэктомия.
[0066] Фигура 40 представляет собой серию графиков (40A-D), демонстрирующих экспрессию связанных с ремоделированием костной ткани транскриптов в получаемом из трубчатой ткани костном мозге на моделях овариэктомии на мышах с нокаутом. Результаты ПЦР клеток костного мозга от мышей, не подвергавшихся овариэктомии, по сравнению с мышами после овариэктомии. Овариэктомия значительно повышала экспрессию ALOX5 (40A - воспаление: ~100%), CXCL12 (40B - активация остеобластов: ~70%), HIF-1a (40C - опосредованное гипоксией повреждение костей: в ~5 раз) и IGF-1 (40D - образование костей: ~100%) только у животных с KO по гастрину. Эти результаты позволяют предположить, что сочетание снижения эстрогена и гастрина ассоциировано с усилением экспрессии получаемых из костного мозга транскриптов, связанных с ремоделированием. Значения нормализовали на животных, не подвергавшихся овариэктомии. Среднее значение±SEM, *p<0,05 в сравнении с животными, не подвергавшимися овариэктомии. G=KO по гастрину, GH=Двойной KO по гастрину/HDC, H=KO по HDC, N=без овариэктомии, O=овариэктомия.
[0067] Фигура 41 представляет собой таблицу, демонстрирующую обзор изменений костного фенотипа на моделях нокаута на мышах после овариэктомии. У животного с нокаутом по гастрину после овариэктомии демонстрировали увеличение внутрикостных характеристик и относительно нормальный костный фенотип, несмотря на "проостеопенический" гормональный фон (снижение эстрогена, повышенный PTH). Для мыши с KO по HDC демонстрировали сниженный объем трубчатой ткани, но костная ткань являлась прочнее. Для двойного нокаута также демонстрировали некоторые изменения характеристик губчатого и трубчатого вещества - которые не приводили к измененной прочности костной ткани. Комбинированное снижение (как гастрина, так и гистамина), несмотря на овариальную функцию и повышенный PTH, не приводило к аномальному костному фенотипу. Снижение гастрина, по-видимому, является защитным для костного фенотипа. GAS=гастрин, pMOI=полярный момент инерции, PTH=паратиреоидный гормон.
[0068] Фигура 42 представляет собой серию графиков, демонстрирующих измерения MicroCT в губчатой кости у контрольных, подвергнутых овариэктомии мышей и мышей CD-1, подвергнутых овариэктомии, обрабатываемых антагонистом гастрина. Отношение BV/TV, плотность соединительной ткани (Conn-Dens), число трабекул (TB.N), поверхность и плотность костной ткани значительно снижались в результате овариэктомии. Показатель структурной организации (SMI), толщина губчатого вещества (Tb.Th) и пространство губчатого вещества (Tb.Sp) являлись повышенными. Обработка антагонистом гастрина предотвращала большую часть этих эффектов за исключением толщины и пространства губчатого вещества. Эти результаты демонстрируют, что селективное блокирование гастринового рецептора улучшает состояние остеопороза на модели овариэктомии и приводит к характеристикам microCT, соответствующим нормальному фенотипу. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0069] Фигура 43 представляет собой серию графиков, демонстрирующих измерения MicroCT в трубчатой костной ткани у контрольных, подвергнутых овариэктомии мышей и мышей CD-1, подвергнутых овариэктомии, обрабатываемых антагонистом гастрина. Плотность трубчатого вещества и поверхность (BS) костной ткани значительно снижались в результате овариэктомии. Толщина трубчатого вещества (Ct.TH) увеличивалась. Обработка антагонистом гастрина предотвращала эффекты на плотность, но не изменяла толщину. Эти результаты демонстрируют, что селективное ингибирование гастринового рецептора предотвращает снижение плотности трубчатого вещества на модели овариэктомии. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0070] Фигура 44 представляет собой серию графиков, демонстрирующих общую прочность костной ткани у контрольных, необрабатываемых и обрабатываемых антагонистом гастрина мышей. Овариэктомия значительно снижала прочность костной ткани, включая жесткость, выходную жесткость, максимальную (max) нагрузку и нагрузку перелома для разрушения и увеличенную полную работу, необходимую для того, чтобы сломать кость. Обработка антагонистом гастрина предотвращала эти эффекты за исключением нагрузки. Эти результаты подтверждают, что прочность костей после овариэктомии снижается, и что направленное воздействие на рецептор гастрина улучшает опосредованный снижением эстрогена эффект. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0071] Фигура 45 представляет собой серию микрофотографий, демонстрирующих окрашивание толуидиновым синим, TRAP бедренных костей от контрольных и мышей CD-1 после овариэктомии, обрабатываемых антагонистом гастрина (OVX+GA) или носителем (OVX). На характер минерализации костей (BM: пониженная), полости резорбции (RC: увеличенные) и остеокласты (окрашенные многоядерные клетки (два стрелки): повешенные количество) оказывало влияние OVX. Эти эффекты предотвращали обработкой лекарственным средством. В одном из аспектов это означает, что направленное воздействие на рецепторы CCK2 нормализует морфологию костной ткани, несмотря на низкие уровни эстрогена.
[0072] Фигура 46 представляет собой серию графиков, демонстрирующих эффекты обработки антагонистом гастрина на уровни циркулирующих гормонов на модели на мышах после овариэктомии. Эстроген значительно снижался, тогда как PTH и гастрин повышались в результате овариэктомии. Обработка антагонистом гастрина не оказывала эффекта на PTH, но нормализовала уровни гастрина. Овариэктомия повышала все три маркера костной ткани, PINP, CTX1 и остеокальцин. Антагонист гастрина ингибировал каждый из этих эффектов. Авторы интерпретируют эти результаты таким образом, чтобы отобразить то, что маркеры активности костной ткани, вызываемые овариэктомией, нормализуются направленным воздействием на рецептор гастрина. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0073] Фигура 47 представляет собой серию графиков, демонстрирующих измерения MicroCT в губчатой кости у контрольных, подвергнутых овариэктомии крыс и крыс CD, подвергнутых овариэктоми, обрабатываемых антагонистом гастрина. Отношение BV/TV, число трабекул (TB.N), толщина губчатого вещества (Tb.Th), поверхность и плотность костной ткани значительно снижались в результате овариэктомии. Показатель структурной организации (SMI) и пространство губчатого вещества (Tb.Sp) увеличивались. Обработка антагонистом гастрина предотвращала большую часть этих эффектов за исключением SMI. Эти результаты демонстрируют, что селективное ингибирование гастринового рецептора улучает состояние остеопороза на модели овариэктомии и приводит к характеристикам microCT, соответствующим нормальному фенотипу у крыс CD. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0074] Фигура 48 представляет собой серию графиков, демонстрирующих измерения MicroCT в трубчатой кости у контрольных, подвергнутых овариэктомии крыс и крыс CD, подвергнутых овариэктомии, обрабатываемых антагонистом гастрина. Плотность трубчатого вещества и поверхность (BS) костной ткани, и полярный момент инерции (pMOI) значительно снижались в результате овариэктомии. Обработка антагонистом гастрина предотвращала эффекты в отношении плотности и была ассоциирована с повышенным отношением BV/TV, а также толщиной трубчатого вещества (Ct.TH). Эти результаты демонстрируют, что селективное ингибирование рецептор гастрина предотвращало снижение плотности трубчатой кости на модели овариэктомии. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0075] Фигура 49 представляет собой серию графиков, демонстрирующих общую прочность костной ткани у контрольных, необрабатываемых и обрабатываемых антагонистом гастрина крыс. Овариэктомия значительно снижала прочность костной ткани, включая жесткость, выходную жесткость, а также нагрузку перелома для разрушения. Обработка антагонистом гастрина предотвращала эти эффекты. Эти результаты подтверждают, что прочность костей после овариэктомии снижается, и что направленное воздействие на рецептор гастрина улучшало эти опосредованные эстрогеном эффекты. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0076] Фигура 50 представляет собой серию микрофотографий, демонстрирующих окрашивание толуидиновым синим, TRAP бедренных костей от контрольных крыс и крыс CD после овариэктомии, обрабатываемых антагонистом гастрина (OVX+GA) или носителем (OVX). На характер минерализации костей (переменно снижающейся), полости резорбции (RC) (увеличенные) и остеокласты (окрашенные многоядерные клетки (две стрелки): увеличенное количество) оказывала влияние OVX. Эти эффекты предотвращали обработкой лекарственным средством. В одном из аспектов это отражает то, что направленное воздействие на рецепторы CCK2 нормализует морфологию костной ткани, несмотря на низкие уровни эстрогена.
[0077] Фигура 51 представляет собой серию микрофотографий, демонстрирующих эффекты обработки антагонистом гастрина на уровни циркулирующих гормонов на модели на крысах после овариэктомии. Эстроген значительно снижался, тогда как гастрин повышался в результате овариэктомии. Обработка антагонистом гастрина не оказывала достоверного эффекта. Овариэктомия повышала PINP и остеокальцин. Антагонист гастрина ингибировал эти эффекты. В одном из аспектов эти результаты демонстрируют, что маркеры активности костной ткани, вызываемые овариэктомией, нормализуются направленным воздействием на рецептор гастрина. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0078] Фигура 52 представляет собой серию графиков, демонстрирующих измерения MicroCT в губчатой кости у контрольных, подвергнутых овариэктомии и подвергнутых овариэктомии Mastomys, обрабатываемых антагонистом гастрина. Отношение BV/TV, число трабекул (TB.N), плотность и поверхность костной ткани значительно снижались в результате овариэктомии, при этом показатель структурной организации (SMI) и пространство губчатого вещества (Tb.Sp) увеличивались. Обработка антагонистом гастрина предотвращала эти эффекты и была ассоциирована с увеличением толщины губчатого вещества (Tb.Th). Эти результаты демонстрируют, что селективное ингибирование рецептор гастрина улучшает состояние остеопороза на модели овариэктомии и приводит к характеристикам microCT, соответствующим нормальному фенотипу у Mastomys. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0079] Фигура 53 представляет собой группу графиков, демонстрирующих измерения MicroCT в трубчатой кости у контрольных, подвергнутых овариэктомии и подвергнутых овариэктомии Mastomys, обрабатываемых антагонистом гастрина. Ни в одной из измеряемых категорий овариэктомия не оказывала влияние, или обработка антагонистом гастрина не вызывала изменений. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM.
[0080] Фигура 54 представляет собой группу графиков, демонстрирующих общую прочность костной ткани у контрольных, необрабатываемых и обрабатываемых антагонистом гастрина Mastomys. Овариэктомия значительно снижала прочность костной ткани, включая жесткость, выходную жесткость, а также максимальную нагрузку и нагрузку перелома для разрушения. Увеличивалась полная работа. Обработка антагонистом гастрина предотвращала эти эффекты. Эти результаты подтверждают, что прочность костей после овариэктомии снижалась, и что направленное воздействие на рецептор гастрина улучшало эти опосредованные эстрогеном эффекты. CON=контрольные животные, OVX=животные после овариэктомии, 8 недель=краткосрочная гипергастринемия, 16 недель=длительная гипергастринемия. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0081] Фигура 55 представляет собой набор микрофотографий, демонстрирующих окрашивание толуидиновым синим, TRAP бедренных костей от контрольных и подвергнутых овариэктомии Mastomys, обрабатываемых антагонистом гастрина (OVX+GA) или носителем (OVX). На характер минерализации костей (BM: сниженной), полости резорбции (RC: увеличенные) и остеокласты (окрашенные многоядерные клетки (две стрелки): увеличенное количество) оказывало влияние OVX. Эти эффекты предотвращали обработкой лекарственным средством. Авторы интерпретируют эти результаты таким образом, чтобы отобразить, что направленное воздействие на рецепторы CCK2 нормализует морфологию костной ткани, несмотря на низкие уровни эстрогена и конститутивную активацию гастринового рецептора.
[0082] Фигура 56 представляет собой группу графиков, демонстрирующих эффекты обработки антагонистом гастрина на уровни циркулирующих гормонов на модели Mastomys после овариэктомии. Эстроген значительно снижался, тогда как PTH и гастрин повышались в результате овариэктомии. Обработка антагонистом гастрина предотвращала эффекты на PTH и гастрин. Овариэктомия значительно повышала PINP, CTX-1 и остеокальцин. Антагонист гастрина ингибировал эти эффекты. Авторы интерпретируют эти результаты таким образом, чтобы отражать то, что маркеры активности костной ткани, вызываемые овариэктомией, нормализуются направленным воздействием на рецептор гастрина. CON=контрольные животные, OVX=животные после овариэктомии, OVX+GA=обрабатываемые антагонистом гастрина животные после овариэктомии. Среднее значение±SEM. *p<0,05 в сравнении с CON, **p<0,05 в сравнении с одной OVX.
[0083] На фигуре 57 представлена интегральная модель регуляции ремоделирования костной ткани на основании результатов, демонстрируемых в настоящем описании. В настоящем описании продемонстрировано, что эффекты овариальной функции (и секреции эстрогена) и секреция PTH паращитовидной железой представлены в настоящем описании модулируются секретирующей гастрин G-клеткой антрального отдела. В качестве основной кальций-чувствительной клетки в желудке и связующим звеном сигнальной системы PTH и эстрогена в желудке, гастрин через свой отрицательный эффект на ремоделирование костной ткани (активация остеокластов) является главным соединением, регулирующим костный фенотип. Эти роли могут быть модифицированы кальцитонином и щитовидной железой и усилены высвобождением гистамина ECL-клетками. Темно-серые линии=стимулирующее, светло-серые линии=ингибирующее действие.
[0084] Фигура 58 представляет собой диаграмму, демонстрирующую распределение мишеней гастринового/CCK2 рецептора в организме. Рецептор экспрессируется в щитовидной железе (включая паращитовидные железы), в желудке, а также в костной ткани. В щитовидной железе CCK2 экспрессируется на секретирующих кальцитонин C-клетках, а также на секретирующих PTH клетках в паращитовидной железе. В кишечнике CCK2 экспрессируется в секретирующих гистамин ECL-клетках, тогда как в костной ткани экспрессия рецептора может быть представлена на многих клетках, включая остеобласты и клетки-предшественники остеобластов. Направленное воздействие на рецептор гастрина/CCK2 конкретными антагонистами ингибирует заболевания костей, например, остеопороз непосредственно (кость) или опосредованно через систему желудок и щитовидная железа/паращитовидная железа. PTH=паращитовидная железа.
ПОДРОБНОЕ ОПИСАНИЕ
[0085] По одному из вариантов осуществления настоящее изобретение относится к новому способу лечения, стабилизации и/или профилактики прогрессирования заболевания или состояния костей. Этот новый способ основан на открытии того, что гормон гастрин непосредственно или опосредованно регулирует образование костей, таким образом, способствуя остеопорозу с последующей патофизиологией костной ткани, соответствующей остеопорозным изменениям (см. фигуру 57).
[0086] По одному из аспектов настоящего изобретения выявлено, что блокада таких эффектов гастрина с использованием антагониста гастрина, который направленно воздействует на рецептор CCK2, оказывает положительное действие на моделях на животных, страдающих заболеванием или состоянием костей, которое характеризуется остеопорозом.
[0087] Таким образом, настоящая заявка относится к использованию направленно воздействующих на гастрин средств, таких как антагонисты гастрина, или средств, которые антагонизируют активность гастрина, для лечения заболеваний или состояний костей (см. фигуру 58).
A. Определения
[0088] Как используют в настоящем описании, термин "состояние" в основном относится к заболеванию, событию или изменению состояния здоровья.
[0089] Как используют в настоящем описании, термин "заболевание или состояние костей" относится к заболеванию или состоянию, ассоциированному с аномалией костной ткани, которое можно лечить увеличением костной массы и/или роста кости. Например, заболевание или состояние костей может включать: первичный остеопороз; вторичный остеопороз; несовершенный остеогенез; остеодистрофию; остеопению; болезнь Педжета; остеолитические поражения, вызываемые костным метастазом, лучевой терапией или химиотерапией; периодонтальное заболевание; альвеолярный остеопороз; остеопороз вследствие иммобилизации или недостаточности половых гормонов; остеопороз вследствие метастатической злокачественной опухоли; потерю костной и хрящевой ткани, вызванную воспалительным заболеванием; остеоартрит; потерю костной ткани при остеотомии; детская идиопатическая потеря костной ткани; искривление позвоночника и переломы костей. Заболевание или состояние костей может представлять собой заболевание или состояние костей, связанное с гипергастринемией. Заболевание или состояние костей также может проявляться у индивидуумов при конкретных обстоятельствах, таких как описано в абзаце ниже.
[0090] Как используют в настоящем описании, термин "индивидуум" относится к млекопитающему, предпочтительно человеку. Например, такой индивидуум может включать индивидуумов, которые представляют собой i) лиц пожилого возраста (мужского или женского пола); ii) женщин со сниженной овариальной функцией или ее недостаточностью, iii) любых индивидуумов с гипергастринемией - естественной (неопластической или связанной с атрофией слизистой желудка) или iv) в следствие использования подавляющей кислоту фармакотерапии (классов средств, включая все ингибиторы протонной помпы или антагонистов двух рецепторов гистамина короткого или длительного действия), или v) индивидуумов с резекцией желудка. Во всех таких случаях заболевание или состояние костей можно улучшать у таких индивидуумов посредством использования класса средства, направленно воздействующего на гастрин. Например, класс средства, направленно воздействующего на гастрин, представляет собой антагонист гастрина, направленно воздействующий на рецептор CCK2.
[0091] Как используют в настоящем описании, термин "направленно воздействующее на гастрин средство" означает антагонист гастрина, такой как направленно воздействующее на гастрин или направленно воздействующее на рецептор гастрина средство, а также антагонист гастрина или гастринового рецептора, например, средство, которое направленно воздействуй на рецептор CCK2.
[0092] Как используют в настоящем описании термин "терапевтически эффективное количество" означает количество направленно воздействующего на гастрин средства, как описано в настоящей заявке, которое обеспечивает цель лечения, улучшения эффектов или профилактики заболевания или состояния костей, или улучшает состояние тяжести заболевания или состояния и частоты возникновения. Улучшение состояния тяжести заболевания или состояния костей включает купирование заболевания или состояния, а также замедление прогрессирования заболевания или состояния.
[0093] Как используют в настоящем описании, термин "лечить" или "лечение" означает уменьшение, взывание остановки или отдаления наступления, или снижения прогрессирования, развития, начала или тяжести заболевания или состояния или одного или более симптомов, связанных с заболеванием или нарушением, или состоянием, описываемым в настоящем описании, или улучшение состояния существующих неконтролируемых или нежелательных симптомов, профилактику дополнительных симптомов или улучшение состояния или профилактику исходных метаболических причин симптомов. Таким образом, термины означают, что благоприятный результат обеспечивали индивидууму с заболеванием или симптомом, или с возможностью развития такого заболевания или симптома. Ответ получают, когда индивидуум испытывает частичное или полное облегчение или уменьшение одного или более признаков или симптомов заболевания, состояния или болезни, такое как, но, не ограничиваясь ими, купирование или профилактика остеопороза, купирование или профилактику потери костной массы, купирование или профилактику перелома кости или его риска, увеличение или профилактика снижения плотности костной ткани, увеличение ремоделирования кости, уменьшение резорбции костной ткани и/или регенерации костной ткани.
[0094] Следует понимать, что использование термина "приблизительно" в настоящем описании по отношению к перечисляемому числовому значению включает перечисляемое числовое значение и числовые значения в пределах плюс или минус десять процент от перечисляемого значения.
[0095] Следует понимать, что использование термина "между" в настоящем описании при обозначении диапазона числовых значений включает числовые значения в каждой конечной точке диапазона. Например, последовательность нуклеиновой кислоты длиной в диапазоне от 10 пар оснований до 20 пар оснований включает последовательности нуклеиновой кислоты длиной 10 пар оснований и последовательность нуклеиновой кислоты длиной 20 пар оснований.
B. Роль G-клеток и гастрина в чувствительности к кальцию и заболевании костей
[0096] Остеопороз, характеризующийся потерей костной ткани и высоким риском переломов, представляет собой одно из наиболее распространенных заболеваний, особенно в пожилом возрасте, и по оценкам затрагивает приблизительно 100 миллионов человек во всем мире. Несмотря на то, что недостаточность яичников и деминерализация костей являются общепризнанными ключевыми элементами при этом заболевании, точная этиология остается до конца неизвестной. Касательно фигуры 1, продемонстрированы известные гормональные и минеральные соединения, регулирующие ремоделирование костной ткани.
[0097] В обычных обстоятельствах ремоделирование костной ткани происходит как физиологические или механические реакции для поддержания прочности и минерального гомеостаза (в частности кальция). Они включают взаимосвязанные явления образования и резорбции вследствие активности остеобластов и остеокластов. Как правило, это включает четыре этап, включающих активацию предшественников остеокластов, активную резорбцию, снижение резорбции и образование новой костной ткани. Первые два этапы занимают 2-4 недели, последний этап занимает 4-6 месяцев до завершения.
[0098] Ремоделирование костной ткани повышается у женщины в перименопаузе и сразу после менопаузы, а затем замедляется при дальнейшем старении, но продолжается с большей скоростью, чем у женщины в перименопаузе. Также полагают, что ремоделирование костной ткани повышается у стареющих мужчин.
[0099] Касательно фигуры 2, трубчатая кость является плотной и твердой и окружает пространство костного мозга. Она содержит внешнюю надкостную поверхность и внутреннюю внутрикостную поверхность. Как правило, она является менее метаболически активной по сравнению с губчатой костью. Активность периостальной поверхности является важной для аппозиционного роста и срастания перелома. Внутрикостная поверхность обладает более высокой ремоделирующей активностью, чем надкостная поверхность, что, вероятно, является результатом большего биомеханическое растяжение или большего воздействия каскада сигнальных реакций от прилежащего компартмента костного мозга.
[0100] Увеличенное ремоделирование трубчатого вещества вызывает увеличение пористости трубчатого вещества и снижение массы трубчатой кости. Резорбция костной ткани, как правило, превышает образование костной ткани на внутрикостной поверхности, тогда как образование костной ткани, как правило, превышает резорбцию костной ткани на надкостной поверхности.
[0101] Губчатая кость состоит из сотоподобной сети губчатых пластин и балок, чередуемых в компартменте костного мозга. Она является более метаболически активной, чем трубчатая кость. Оборот в этом типе костей является наиболее важным для минерального метаболизма и поддержания механической прочности.
[0102] Биология ремоделирования костной ткани является сложной и включает диапазон активирующих факторов, например, PTH, эстроген, факторы роста и воспалительные цитокины, а также потребление с пищей, например, кальция и витамина D. Это привело к разработке широкого спектра видов терапии, которые в настоящее время являются доступными для ведения. Они включают гормонозаместительную терапию, бисфосфонаты, диеты с высоким содержанием кальция и витамина D, использование статинов, фактора роста фибробластов-1 или самого паратиреоидного гормона (PTH).
[0103] PTH считается основным регулирующим соединением костного метаболизма, т.к. он усиливает высвобождение Ca2+ из костного резервуара через процесс резорбции. Однако эффект PTH является опосредованным, т.к. остеокласты не содержат рецептор PTH. Вместо этого PTH связывается с остеобластами и приводит к экспрессии RANKL. RANKL активирует клетки-предшественники остеокластов через рецептор RANK, со сливанием с образованием новых остеокластов, которые обеспечивают резорбцию кости.
[0104] Доказательство, подвергающее роль PTH при остеопорозе, получили из нескольких исследований, описывающих что значения PTH являются выше у лиц пожилого возраста, чем у молодых людей. Был предложен ряд факторов, которые способствуют более высоким значениям PTH, включая сниженную функцию почек, менее эффективное всасывание в кишечнике кальция (Ca2+), возможно, вследствие утраты мотивации есть, устойчивости к кальцемической активности PTH, большего преобладания недостатка витамина D и, более конкретно, при повышенном pH в желудке, отмечаемом в пожилом возрасте.
[0105] Последний отражает утрату париетальной клеточной массы (атрофию слизистой оболочки) с сопутствующими повышениями pH в желудке, а также повышенной секреции гастрина нейроэндокринной G-клеткой антрального отдела.
[0106] Связанные с возрастом изменения целостности и функции слизистой желудка считают основной проблемой жалоб пожилых людей в области гастроэнтерологии, а также они обуславливают повышенную чувствительность к лекарственным средствам, кровотечение и неспособность всасывать Ca2+ и железо на соответствующем уровне.
[0107] Полагают, что система Ca2+/PTH/витамин D поддерживает системный гомеостаз Ca2+ путем координации функций паращитовидной железы, почки, котной ткани и желудочно-кишечного тракта с повышением уровня Ca2+ в сыворотке без сопутствующего повышения уровней фосфора в сыворотке. Такая система преимущественно предназначена защищать от гипокальциемии посредством мобилизации Ca2+ из скелета, сохранения Ca2+ почками и повышения желудочно-кишечного всасывания Ca2+.
[0108] В ответ на снижение концентрации Ca2+ в сыворотке кальцийчувствительный рецептор (CaSR) в паращитовидной железе увеличивает секрецию PTH, тогда как CasR в почке снижает экскрецию Ca2+ почками. Однако чувствительность к кальцию не ограничена паращитовидными железами, и CaSR содержится в различных других типах клеток, включая продуцирующую гастрин G-клетку в антральном отделе. Эта нейроэндокринная клетка, с учетом ее расположения в желудке, уникальным образом локализована, чтобы воспринимать и реагировать на поступление с пищей Ca2+.
[0109] CaSR детектируют изменения концентрации внеклеточного Ca2+ и инициируют адаптивные гормональные ответы и реакции ионного транспорта для поддержания системного гомеостаза кальция. В настоящее время считают, что паращитовидная железа, C-клетки щитовидной железы и почка обеспечивают физиологически релевантные участки экспрессии CaSR. В основном, низкий уровень (<1 мМ) циркулирующего внеклеточного Ca2+ является основным факторов, вызывающим секрецию PTH клетками паращитовидной железы. При более высоких концентрациях Ca2+ ингибирует синтез и секрецию PTH через фосфорилирование и последующую инактивацию CaSR.
[0110] CaSR также идентифицировали в парафолликулярных C-клетках овец и в линии клеток медуллярной карциномы щитовидной железы (MTC), TT. Последние обеспечивают секрецию Ca2+ с кальцитонином.
[0111] Хотя CaSR идентифицировали в остеобластах и остеокластах, физиологическая роль в чувствительности к Ca2+ остается неясной, т.к. они экспрессируются на очень низких уровнях в этих клетках. В отличие от костных клеток, физиологически релевантный CaSR идентифицировали в желудке. Недавно клонировали и секвенировали CaSR из G-клеток антрального отдела человека, и он функционирует при концентрациях Ca2+ >2 мМ.
[0112] В следующих ниже подразделах (1-8) приведен краткий обзор и обсуждение исследований, демонстрируемых в настоящем описании в примерах. Эти подразделы приведены для дополнительной иллюстрации примеров и не предназначены ограничивать результаты и заключения, содержащиеся в них.
1. Исследования выделенных G-клеток
[0113] В настоящем описании продемонстрирована физиологическая роль G-клеток в качестве сенсоров Ca2+ (см. пример 1, фигуру 3). В основном, кальций, усваиваемый во время приема пищи (1-10 мМ), стимулирует высвобождение гастрина. Механически внеклеточный Ca2+ захватывается CaSR желудка, который активирует высвобождение гастрина через кальций-индуцируемые пути. Результаты, демонстрируемые в настоящем описании, дополнительно идентифицируют G-клетку как основную нейроэндокринную клетку гомеостаза кальция в кишечнике/паращитовидной железе.
[0114] Проводили исследования для подтверждения наличия рецептора PTH на G-клетке и опосредованного PTH высвобождения гастрина после активации цАМФ (см. фигуру 4). Эти исследования подтверждаются другими исследованиями. Например, инфузия PTH (40 единиц/20 минут) повышала уровни гастрина в антральном отделе и смешанной венозной крови без индукции системной гиперкальциемии у свиней под анестезией. Кроме того, нативный бычий PTH и синтетический PTH 1-34 человека (0,02-4 Ед/мин) вызывал быстрое (в течение 10-30 минут) и выраженное (приблизительно в 10 раз) увеличение высвобождение гастрина у молодых свиней под анестезией.
[0115] Также проводили исследования на выделенных клетках гастрина для демонстрации того, что 17β-эстрадиол (агонист ESRα) ингибировал высвобождение гастрина (см. фигуру 6). Не выявляли негеномные направленные эффекты эстрогена в других типах клеток, таких как ткань молочной железы. Эти эффекты, опосредованный ERα сигнальный каскад MAPK, также можно демонстрировать в G-клетке, где эстроген является эффективным ингибитором секреции гастрина.
[0116] Эта информация указывает на то, что изменение эстрогенной среды в соответствии с состоянием менопаузы сильно изменяет/стимулирует функцию G-клеток (сигнальный каскад и секрецию). Это соответствует предшествующим сообщениям на стареющих крысах существования среды, которая включает повышенную функцию G-клеток и высокий PTH. Такое сочетание является общепризнанным по отношению к развитию остеопороза.
[0117] Дополнительные исследования in vitro идентифицировали, что секрецию гастрина может модулироваться продукцией гистамина и серотонина в кишечнике. Предположение о роли гистамина в модуляции костной системы связано с неоднозначной информацией. Высвобождение избытка гистамина при мастоцитозе и аллергических заболеваниях может приводить к развитию остеопороза. В противоположность этому, гистамин может повышать резорбцию кости как непосредственно через предшественники остеокластов и остеокласты, так и опосредованно путем повышения экспрессии RANKL (активирующий остеокласты рецептор) в остеобластах. Кроме того, в исследованиях in vivo антагонисты рецепторов H1 и H2 могут оказывать защитное действие на костную ткань, хотя это сопоставимо не воспроизводится на всех экспериментальных моделях. Однако гистамин регулирует высвобождение гастрина ex vivo, а также in vitro.
[0118] Роль серотонина в метаболизме костной ткани полностью до конца не ясна. Инъекция серотонина повышает минеральную плотность костной ткани у крыс через опосредованную серотонином пролиферацию остеобластов (эти клетки экспрессируют рецепторы 5-HT2). На модели на животных серотонин, по-видимому, ингибирует образование костей зависимым от Lrp5 образом. Lrp5 ограничивает продукцию серотонина через ингибирование фермента, ограничивающего скорость синтеза серотонина, триптофангидроксилазы 1 (Tph1). Однако в клинических исследованиях мутации LRP5 не ассоциированы с изменением циркулирующего серотонина, и у пациентов выявляют высокую костную массу. Ингибиторы обратного захвата серотонина (SSRI) были ассоциированы с пролиферацией остеобластов, но у женщин среднего возраста использование SSRI не было ассоциировано с увеличенной скоростью остеопороза. Кроме того, высокий уровень циркулирующего серотонина при карциноидном синдроме не был ассоциирован с клинически значимой более низкой плотностью костной ткани, худшей структуры костной ткани или более низким уровнем маркеров образование костной ткани. Любой эффект серотонина может альтернативно осуществляться через G-клетку; высвобождение гастрина стимулируется рецепторами 5-HT3. Таким образом, амин может модулировать образование костной ткани через действие на G-клетке.
[0119] При совокупной оценке данные и наблюдения, приведенные в настоящем описании, например, существование люминального кальцийчувствительного рецептора, селективная экспрессия рецепторов для функциональной регуляции паращитовидной железы и щитовидной железы, а также витамина D и экспрессии аминергических рецепторов (положительно регулируемых гистамином и серотонином) определяет G-клетку как основную нейроэндокринную клетку в системе кишечник/паращитовидная железа гомеостаза кальция.
2. Исследования мишеней гастрина (in vitro)
[0120] В исследованиях, продемонстрированные в настоящем описании, исследуют, какие клетки могут являться возможными мишенями гастрина. Кроме того, в этих исследованиях анализируют, может ли продуцирующая гастрин клетка регулировать систему гомеостаза кальция через высвобождение гастрина (см. пример 2).
[0121] Наличие рецепторов CCK2 в главных клетках PTH до конца не установлено, но это предполагали в ряде физиологических исследований. В выделенных клетках паращитовидной железы крупного рогатого скота гастрин в высоких концентрациях (>1 мкМ) повышал накопление цАМФ (40-60% в ~50% экспериментов) необходимое условие для высвобождения PTH.
[0122] Модели на птицах также поддерживали это наблюдение. Индукция гипергастринемии (с использованием ингибитора протонной помпы (PPI), омепразола (400 мкМ/кг/сутки) в течение 5 недель) у кур приводила к уменьшению размера PTH железы, а также к транскрипции PTH. Эти эффекты воспроизводили инъекцией гастрина (непрерывной 5 нмоль/кг/час в течение 3 недель).
[0123] Исследования, описываемые в настоящем описании, демонстрируют экспрессию гастрина/рецепторов CCK2 на выделенных главных клетках PTH человека (из хирургических образцов, получаемых от человека), и что гастрин оказывает стимулирующее действие на синтез и высвобождение PTH человека (см. фигуру 8). Таким образом, в настоящем описании демонстрируют, что клетки паращитовидной железы являются мишенями гастрина. Вследствие того, что PTH стимулирует высвобождение гастрина (см. фигуру 4), активация секреции паращитовидной железы (PTH) свидетельствует о петле стимуляции с прямой связью (от G-клетка до PTH). В исследованиях, представленных в настоящем описании, также идентифицировали экспрессия стимулирующего рецептора гистамина H1.
[0124] Экспрессию стимулирующего рецептора гистамина H1 также идентифицировали на G-клетках. Гистамин является известным активирующим фактором продукции цАМФ и секреции PTH в нормальной и гиперплазированной PTH железах. C-клетки и получаемые из C-клеток опухоли (медуллярные карциномы щитовидной железы) экспрессируют рецепторы гастрина/CCK2. Кроме того, гастрин индуцирует продукцию цАМФ и высвобождение кальцитонина в срезах щитовидной железы человека.
3. Идентификация функциональных мишеней гастрина в кости
[0125] Для оценки прямых эффектов гастрина на самой кость оценивали содержание рецепторов гастрина на костных клетках, и оказывал ли гастрин эффект на получаемые из кости клетки (см. пример 3).
[0126] Эффекты гастрина анализировали на трех различных моделях: 1) остеобласты свода черепа мыши; 2) линии остеобластных клеток зародыша человека, hFOB 1.19; 3) получаемых из костного мозга мезенхимальных стволовых клетках человека (BMMSC). Остеобласты свода черепа представляют собой известные модели для исследования функции остеобластов, включая пролиферацию, минерализацию и клеточную сигнализацию. hFOB представляет собой линию трансфицированных большим T-антигеном SV40 клеток человека, используемую в качестве модели для исследования нормальной дифференцировки остеобластов человека, физиологии остеобластов и эффектов гормонов, фактора роста и других цитокинов на функцию и дифференцировку остеобластов. BMMSC представляют собой полипотентные стромальные клетки костного мозга, которые могут дифференцироваться в различные типы клеток, необходимых для регенерации ткани, включая остеобласты и хондроциты, и, по-видимому, играют патологическую роль при связанном с возрастом остеоартрите.
[0127] Результаты, демонстрируемые в настоящем описании, показывают, что гастрин может активировать/регулировать многие типы клеток в кости. Вследствие того, что циркулирующая кровь, содержащая гастрин, проходит через костный мозг, изменения уровней циркулирующего гастрина являются биологически значимыми для любой клетки костного происхождения, которая экспрессирует рецептор CCK2.
[0128] Вследствие того, что гастрин представляет собой известный фактор регуляции пролиферации, также исследовали эффект гастрина на пролиферацию (поглощение BrdU) на трех различных клеточных моделях. Результаты, демонстрируемые в настоящем описании, выявляют, в частности, что, гастрин стимулирует пролиферацию остеобластов и BMMSC, которую не предотвращает селективный антагонист гастрина (GA). Результаты дополнительно указывают на то, что гастрин вызывает дифференцировку остеобластов с утратой минерализации. Антагонист GA не снижает пролиферацию, но сохраняет остео-фенотип. В демонстрируемых в настоящем описании результатах показано, что гастрин непосредственно влияет на функцию костной клетки на двух уровнях: для остеобластов и получаемых из костного мозга стволовых клеток и т.д. эффект проявляется в пластинке роста путем регуляции поведения хондроцитов.
4. Исследования гастрина: эффекты ингибиторов протонной помпы на функцию G-клеток
[0129] Секреция гастрина представляет собой динамическую физиологическую реакцию, которая регулируется двумя аспектами старения, которые ассоциированы с остеопорозом - старением и атрофией слизистой желудка - которая ассоциирована с повышенным pH в желудке в течение длительного времени вследствие утраты секретирующих кислоту париетальных клеток. Устойчивые повышения pH в желудке, которые приводят к повышенным уровням циркулирующего гастрина, также связаны с длительными использованием PPI или антагонистов рецептора H2. Эти средства, как правило, используют для лечения симптомов желудочной диспепсии или гастроэзофагеального рефлюкса, которые являются значимыми, в частности в стареющей женской популяции.
[0130] Кислая желудочная среда (низкий pH в желудке) также является важной для облегчения продукции ионизированного кальция, который оптимально всасывается ЖК трактом.
[0131] Документально подтверждено, что у людей гастрэктомия (недостаток кислоты) и пернициозная анемия (утрата париетальных клеток, достигающая высшей точки при состоянии низкой кислотности) ассоциированы с повышенным риском остеопении и перелома. Гастрэктомия, как правило, включает резекцию секретирующих кислоту клеток при существенном уменьшении желудочной кислоты, пернициозная анемия ассоциирована с утратой париетальных клеток (продуцирующих кислоту), повышенным pH в желудке (>4), но желудок сохраняет функциональные нейроэндокринные клетки в своде (ECL-клетки) и антральном отделе (продуцирующие гастрин клетки).
[0132] Повышенный pH в желудке и повышенные уровни гастрина также возникают при стареющем желудке, а также при длительном использовании PPI. PPI вовлечены в увеличение резорбции кости и риска перелома. В настоящем описании продемонстрированы роли ингибирования кислоты (повышенного pH в желудке) на функцию G-клеток и секрецию гастрина (см. пример 4). Результаты наряду с другими показаниями демонстрируют, что повышенный pH в желудке значительно влияет на функцию G-клеток. В частности, нарушается Ca2+-чувствительное действие и реакция на физиологическую регуляцию G-клеток.
5. Эффекты блокады кислоты на динамику костной ткани: модель гипергастринемия на Mastomys
[0133] Появление эффективных подавляющих кислоту лекарственных средств, таких как PPI, коренным образом изменили ведение связанных с кислотой заболеваний. Многие миллионы индивидуумов используют эти лекарственные средства непрерывно или в течение длительного периода времени.
[0134] Хорошо известно, что существенная гипохлоргидрия (высокий pH в желудке), в частности среди популяции пожилых людей, которые также обладают пониженным клиренсом PPI и характеризуются более высоким уровнем распространения инфекции Helicobacter pylori, приводит к нарушению всасывания кальция. Это подтверждается рядом исследований, которые продемонстрировали, что терапия PPI снижает всасывание нерастворимого кальция, а также плотность костей. Таким образом, существенный повышенный риск перелома бедра связан с длительной терапией PPI, в частности у тех, кто принимает в течение длительного времени PPI в высоких дозах.
[0135] Принимая во внимание указанные выше проблемы с PPI, результаты, демонстрируемые в настоящем описании, исследуют эффект подавление кислоты на желудок, циркулирующие гормоны, паращитовидные железы, а также физиологию костей на модели на Mastomys (см. пример 5). Результаты наряду с другими показаниями подтверждают, что гипергастринемия, индуцируемая подавляющими кислоту лекарственными средствами, ассоциирована с изменениями, которые являются аналогичными морфологическим проявлениям, идентифицируемым при остеопорозе.
6. Эффекты блокады кислоты на динамику костной ткани у Mastomys после овариэктомии
[0136] Овариэктомия проводили на модели на Mastomys для получения фенотипа "постменопаузного" фенотип для исследования костей. Поскольку в настоящем описании было показано, что снижение эстрогена регулирует G-клетки, оценивали конкретную роль снижения эстрогена на фенотип костной ткани (см. пример 6). Результаты наряду с другими показаниями подтверждают, что уровни циркулирующего гастрина усиливают опосредованные снижением эстрогена изменения костей.
7. Эффекты на нейроэндокринную функцию желудка и динамику костной ткани: модели нокаута гена на мышах (с овариэктомией и без нее)
[0137] У крыс гастрэктомия (удаление всего желудка, включая G-клетки антрального отдела и секретирующие гистамин ECL-клетки свода) или использование PPI, например, омепразола, приводит к нарушению всасывания фосфата кальция и сниженной минеральной плотности костной ткани и остеопении. Дополнительное наблюдение заключается в том, что инфузия гастрина-17 индуцирует гипокальциемию у крыс.
[0138] У экспериментальных животных частичная и полная гастрэктомия и ваготомия желудка (трункальная/избирательная и т.д.) (что изменяет секрецию нейроэндокринных клеток) оказывает влияние на гомеостаз внеклеточных минералов и приводит к остеопении в качестве позднего последствия.
[0139] Механизмы, лежащие в основе остеопении после ваготомии или после гастрэктомии, не известны. Предположительно они отражают прямые эффекты гастрина на систему PTH/Ca2+ или на функцию костей или непрямой эффект, например, посредством гистамина. Следует отметить наблюдение, что ипсилатеральная ваготомия является терапевтической для легочная гипертрофической остеопатии (HPOA), связанной с раком легких. Аналогично, ваготомия, вызванная инвазивными апикальными неопластическими поражениями легкого (синдром Панкоста), связана с ипсилатеральными изменениями костей в руке.
[0140] Гистамин секретируется аргентаффинной-подобной клеткой (ECL) свода желудка и является основным регулирующим фактором секреции кислоты, т.к. его секреция преимущественно вызывается циркулирующим гастрином. ECL-клетка кислотопродуцирующей (свода желудка) слизистой оболочки представляет собой "закрытую" эндокринную клетку, локализованную - т.е. она не имеет доступа к просвету желудка, и, таким образом, не реагирует непосредственно на поступающий с пищей кальций.
[0141] Секретируемые продукты ECL-клетки включают гистамин, хромогранин A и панкреастатин, и кальций-связывающий белок, кальбиндин. ECL-клетки экспрессируют рецепторы гастрина и гистамина и функционируют главным образом для преобразования сигнала гастрина (посредством секреции гистамина) для регуляции опосредуемой смежными париетальными клетками (HCL) секреции кислоты.
[0142] Было продемонстрировано, что сам по себе гистамин оказывает независимое влияние на функцию костных клеток. Однако исследования являются недостоверными относительно того, оказывает ли гистамин защитное или остеопеническое действие. Отмечалось, что избыток высвобождения гистамина при мастоцитозе и аллергических заболеваниях является связанным с развитием остеопороза. Это дает основание предполагать, что гистамин играет отрицательную роль в ремоделировании костной ткани. Дополнительное подтверждение этого предположения обеспечивает наблюдение, что хирургическая резекция продуцирующей кислоту части желудка (кислотопродуцирующей/слизистой оболочки свода), которая содержит ECL-клетки, снижает костную массу у крысы. Эти наблюдения дополнительно подтверждают исследованиями in vitro. Таким образом, в остеобластных клетках MC3T3-E1 (E1), которые экспрессируют рецепторы гистамина H1-3, гистамин повышает экспрессию транскрипта RANKL и продукцию белка. Эти эффекты ингибируются антагонистом рецепторов H1. В совместных культурах с клетками костного мозга (клетки MC3T3-E1 (E1), получаемые из свода черепа мыши), гистамин стимулировал остеокластогенез в присутствии витамина D3. Этот эффект блокируют предварительной инкубацией с нейтрализующим антителом против ODF/RANKL. С использованием подхода микропанели для исследования дифференцировки гематопоэтических клеток-предшественников костного мозга в резорбирующие костную ткань остеокласты отмечали, что RANKL стимулирует 70 генов-мишеней, включая рецептор H1. Исследования с антагонистом рецептора H2, фамотидином, на крысах после овариэктомии демонстрировали ингибирование потери костной массы позвоночника в результате снижения активности остеокластов. Эти эффекты являлись краткосрочными и проходили за 6 месяцев. Обобщение этих данных указывает на то, что гистамин играет активную роль в регуляции резорбции кости. Это наблюдение подтверждается данными случая на основе большого регистра: контрольное исследование, демонстрирующее, что длительное использование антагониста рецепторов гистамина H1 снижало риск перелома кости.
[0143] В ECL-клетках критический фермент, ответственный за регуляцию секреции гистамина, представляет собой гистидиндекарбоксилазу (HDC). Мыши с нулевой HDC характеризовались полным отсутствием синтеза гистамина, а также сниженной базальной секрецией желудочной кислоты и устойчивостью к гастрину. У таких животных выявляют значительно увеличенную толщину бедренной кости и толщину грудных позвонков, связанных с повышенным содержанием минеральных веществ в костной ткани и сниженной резорбции кости. Снижалось как количество остеокластов, так же и их активность. Когда мышей с нулевой HDC подвергают овариэктомии, остеопороз трубчатых и губчатых костей снижается на 50%, что указывает на то, что дефицит гистамина защищает скелет от индуцируемого эстрогеном остеопороза. Таким образом, заключение сводится к тому, что гистамин действует, увеличивая опосредованное эстрогеном ремоделирование костной ткани.
[0144] Хотя вполне возможно считать, что ECL-клетка продуцирует альтернативный остеотропный амин или пептид, такой гормон не был идентифицирован. Таким образом, по-видимому, вероятно, что роль гистамина заключается в то, что он является связывающим фактором между гастрином, ECL-клеткой и патофизиологией костной ткани, т.к. синтез и секреция этого амина настолько неразрывно связана с гастрином.
[0145] Исследования в настоящем описании демонстрируют взаимосвязь гистамина и гастрина при опосредовании метаболизма костной ткани (целостности) с использованием моделей нокаута по гастрину и гистамину (см. пример 7).
[0146] Исследовали направленное воздействие на рецептор гастрина/CCK2 на фармакологической уровне при заболеваниях, включающих рак поджелудочной железы, нейроэндокринные опухоли желудка и пептическую язву. Генез последней связан со стимулирующей кислоту функцией ECL-клеток через синтез и высвобождение гистамина и концепцией, что подавление секреции гистамина блокадой рецепторов гастрина снижает секрецию кислоты. Один из таких антагонистов представляет собой YF476, антагонист гастринового/CCK2 рецептора на основе 1,4-бензодиазепин-2-она, родственный исходному аналогу L365.260. Для YF476 демонстрировали эффективность в отношении синтеза и высвобождение гистамина ECL-клетками in vitro и in vivo. вследствие того, что секреция гистамина активируется опосредованной гастрином стимуляцией рецептора CCK2, отдельное физиологическое событие на основе эффектов секреции кислоты включает способность антагониста рецептора CCK2 не только блокировать связанные с высвобождением гистамина эффекты на костную ткань, но любые прямые эффекты гастрина на саму костную ткань.
8. Контрольно-проверочное исследование: эффекты антагониста гастрина на опосредованный овариэктомией костный фенотип на трех моделях на грызунах
[0147] В исследованиях, описываемых в настоящем описании, оценивали эффекты антагониста гастрина, YF476, на опосредованные OVX снижения плотности костной массы/изменения костной массы на трех моделях на грызунах с акцентом на исследования прочности костей, морфологии и циркулирующих биомаркеров (см. пример 8).
C. Лечение заболевание или состояния костей с использование направленно воздействующих на гастрин средств
[0148] Исследования, предоставленные в настоящем описании, демонстрируют наряду с другими показаниями наличие рецепторов CCK2 к костной ткани и эффективность направленно воздействующих гастрин средств для лечения заболевания костей. Предложены способы и композиции для использования таких направленно воздействующих на гастрин средств для лечения и профилактики заболеваний или состояний костей, включая заболевания или состояния, характеризуемые как остеопороз.
[0149] В некоторых вариантах осуществления подходящие направленно воздействующие на гастрин средства включают, но не ограничиваются ими, регулирующие гастрин средства, включая: гастриносвобождающий пептид (GRP) (бомбезин), соматостатин и аналоги соматостатина, включая октреотид (OCTR) и RC-160. В других вариантах осуществления подходящие направленно воздействующие на гастрин средства включают антагонист рецепторов CCK2, включают нетазепид (YF476) и другие агонисты гастринового/CCK2 рецептора на основе 1,4-бензодиазепин-2-он-бастина. В некоторых вариантах осуществления направленно воздействующее на гастрин средство выбрано из агонистов рецептора CCK2: Z-360, L-740093, YM022, RP73870, JB93182, AG041R, проглумида (и аналогов), JNJ-2607109 (и производных), CI-988, PD-135158, L-365260, LY-288513, L-364718, GW-5823, лорглумида, CR 2194 (спироглумида), PD-149164, PD-135666, CI-1015, RP-69758, TP-680, PD-140548 и итриглумида (и производных).
[0150] Направленно воздействующее на гастрин средство можно вводить индивидууму любыми подкожными способами введения. В некоторых вариантах осуществления направленно воздействующее на гастрин средство вводят посредством неглубокой внутримышечной инъекции. В других вариантах осуществления направленно воздействующее на гастрин средство вводят внутривенно или перорально.
Примеры
[0151] Следующие ниже примеры приведены, чтобы лучше иллюстрировать описываемое в заявке изобретение, и их не следует интерпретировать как ограничивающие объем изобретения. В тех случаях, когда указывают конкретные вещества, они приведены только для целей иллюстрации и не предназначены ограничивать изобретение. Специалист в данной области может разрабатывать эквивалентные способы или реагенты без проведения изобретательской деятельности, и не выходя за рамки объема изобретения.
Пример 1: Исследования выделенных G-клеток
[0152] Со ссылкой на фигуру 3, проводили исследования, демонстрирующие физиологическую роль G-клетки в качестве сенсора Ca2+. Повышение концентрации внешнего Ca2+ стимулировало высвобождение гастрина выделенными G-клетками посредством механизмов, включающих путь PKC и приток Ca2+ через дигидропиридинчувствительные кальциевые каналы. EC50 составляла 4,1 мМ, и это происходило преимущественно PKC-регулируемым путем. Эти результаты соответствуют G-клетке, функционирующей как сенсор поступающего с пищей (люминального) кальция.
[0153] Кроме того, на G-клетке идентифицировали наличие рецептора PTH. Со ссылкой на фигуру 4, после активации цАМФ демонстрировали опосредованное PTH высвобождение гастрина. PTH в значительной степени стимулировал высвобождение гастрина (EC50=60 нМ) путем активации PKA и продукции внутриклеточной цАМФ, демонстрируя, что рецептор PTH G-клетках является функциональным, и что PTH может регулировать секрецию гастрина такой люминальной кальцийчувствительной клеткой антрального отдела.
[0154] В G-клетках также идентифицировали рецептор кальцитонина. Со ссылкой на фигуру 5, показано, что кальцитонин (из C-клеток щитовидной железы) в отличие от PTH ингибировал высвобождение гастрина путем ингибирования продукции цАМФ.
[0155] Это демонстрирует, что G-клетку, как и другие мишени PTH/кальцитонина (например, остеобласты), могут стимулировать (PTH) или ингибировать (кальцитонин) клетки нейроэндокринной системы, которые не содержатся в желудке.
[0156] Эти наблюдения подтверждают, что известные соединения, регулирующие гомеостаз кальция (через детекцию уровней Ca2+ в плазме -PTH/клетки щитовидной железы) могут непосредственно влияет на люминальную кальцийчувствительную клетку желудка - продуцирующую гастрин G-клетку - и модифицирует ее профиль секреции.
[0157] Оценивали эффект овариального гормона эстрогена на функцию G-клеток. Со ссылкой на фигуру 6, оценивали присутствие транскрипта эстрогенового рецептора (ESRα) на продуцирующую гастрин клетку с использованием ПЦР в режиме реального времени. Дополнительно демонстрировали в выделенных продуцирующих гастрин клетках, что 17-эстрадиол (агонист ESRα) ингибировал высвобождение гастрина (IC50=4,6×10-12M), продукцию цАМФ (IC50=1,1×10-12M) и активность MAPK (фигура 6).
[0158] Эта информация указывает на то, что изменение эстрогенной среды, соответствующее состоянию менопаузы, сильно изменяет/стимулирует функцию G-клеток (сигнальный каскад и секрецию). Это соответствует предшествующим сообщениям о существовании среды, которая включает повышенную функцию G-клеток и высокий PTH у стареющих крыс. Такое сочетание является общепринятым в отношении развития остеопороза.
[0159] Со ссылкой на таблицу 1, сравнение транскриптов с выделенными препаратами нейроэндокринных EC- и ECL-клеток демонстрирует, что G-клетка является единственной клеткой, которая может являться чувствительной к люминальному кальцию, т.к. она является единственной нейроэндокринной клеткой, которая экспрессирует CaSR, но не кальбиндин. Со ссылкой на фигуру 7, это свидетельствует о том, что секреция гастрина G-клеткой может непосредственно регулироваться PTH, секретируемым главными клетками паращитовидной железы, кальцитонином из C-клеток щитовидной железы и эстрогеном из овариальных клеток.
Сравнение наличия связанных с метаболизмом кальция транскриптов и нейроэндокринных рецепторов в G-клетках, EC-клетках и ECL-клетках, как измеряют анализом транскриптома (микропанели U133A)
CaSR: кальцийчувствительный рецептор; ESRα=эстроген-альфа; H3= подтип 3 гистамина; 5-HT3: подтип 3 серотонина; PTH: паращитовидная железа
[0160] Результаты определяют G-клетку как основную нейроэндокринную клетку в системе гомеостаза кальция кишечник/паращитовидная железа.
Пример 2: Исследования мишеней гастрина (in vitro)
[0161] Оценивали типы клеток как возможные мишени гастрина. Оценивали регуляцию продуцирующей гастрин клеткой системы гомеостаза кальция путем высвобождения гастрина.
[0162] Демонстрировали экспрессию гастриновых/рецепторов CCK2 на выделенных главных клетках PTH человека (из хирургических образцов человека). Со ссылкой на фигуру 8, дополнительно демонстрировали, что гастрин оказывает стимулирующее действие на синтез и высвобождение PTH человека. Эти результаты указывают на то, что клетки паращитовидной железы являются мишенью гастрина. Вследствие того, что PTH стимулирует высвобождение гастрина (см. фигуру 4), активация секреции паращитовидной железы (PTH) указывает на петлю стимуляции с прямой связью (G-клетка к PTH). На этих клетках также идентифицировали экспрессию стимулирующего рецептора гистамина H1.
[0163] Со ссылкой на фигуру 9, гастрин стимулировал высвобождение цАМФ, а также кальцитонина высокодифференцированной линией клеток MTC человека, MTC-SK, эффекты, которые предотвращали селективным антагонистом CCK2, YF476 (IC50=8,6×10-13M). Эти результаты указывают на то, что C-клетки щитовидной железы представляют собой мишень гастрина. Вследствие того, что кальцитонин ингибирует высвобождение гастрина (см. фигуру 5), активация C-клеток обеспечивает ингибирующую петлю с обратной связью.
[0164] Для оценки общей ответной реакции (стимулирующей или ингибирующей) системы щитовидная железа/паращитовидная железа на гастрин оценивали эффекты гастрина на совместно культивируемые системы паращитовидная железа/MTC-SK. Оценивали, являлся ли гастрин стимулирующим фактором резорбции кости (через повышенный синтез и высвобождение PTH) или ингибитором этого процесса через высвобождение кальцитонина.
[0165] Со ссылкой на фигуру 10, стимуляция рецептора CCK2 (экспрессируемого в C-клетках паращитовидной железы и щитовидной железы) приводила к значительному повышению транскрипции и секреции PTH культивируемыми клетками PTH. В противоположность этому, гастрин приводил к значительному ингибированию синтеза и высвобождения кальцитонина. Эти эффекты предотвращали предварительной инкубацией с селективным антагонистом CCK2, YF476.
[0166] Эти результаты указывают на то, что стимуляцию гастрином C-клеток щитовидной железы предотвращает PTH, высвобождающийся клетками паращитовидной железы. Это служит доказательством того, что в этой модельной системе совместного культивирования эффекты гастрина преимущественно представляет собой опосредованный PTH эффект. У здоровых добровольцев эффект инфузии гастрина сводится к повышению секреции PTH, а не кальцитонина (значительно более низкий уровень высвобождения). Это позволяет предположить, что любой эффект in vivo гастрина на щитовидную железу преимущественно связан с паращитовидными железами и высвобождением PTH.
[0167] Эти результаты подтверждают, что высвобождение гормона в кишечнике (желудке) люминальной чувствительной клеткой (G-клетка) непосредственно регулирует секрецию кальцитонина C-клеткой паращитовидной железы и опосредованно C-клеткой щитовидной железы.
Пример 3: Идентификация функциональных мишеней гастрина в костной ткани
[0168] Для оценки прямых эффектов гастрина на саму костную ткань оценивали, наличие рецепторов гастрина на костные клетки, и оказывал ли гастрин эффект на клетки костного происхождения. Для идентификации экспрессии рецептора в костной ткани использовали техники QPCR, вестерн-блоттинга и иммуногистохимии. В дальнейшем анализировали эффекты гастрина на трех различных моделях: 1) остеобласты свода черепа мыши; 2) линии остеобластных клеток зародыша человека, hFOB 1.19; 3) получаемые из костного мозга мезенхимальные стволовые клетки человека (BMMSC).
[0169] Рецептор CCK2. С использованием количественной ПЦР в режиме реального времени идентифицировали экспрессию рецептора CCK2 в остеобластах свода черепа, линии клеток hFOB и BMMSC человека (фигура 11A). Экспрессию идентифицировали на всех моделях со значениями CQ в диапазоне 31,2-34. Иммуногистохимией (IHC) идентифицировали рецепторы гастрина в костях мыши - специфическое иммуноокрашивание идентифицировали в хондроцитах в пластинке роста. Некоторую экспрессию идентифицировали в остеобластах, а также в клетках, которые выстилают внутреннюю надкостницу (фигура 11B-C). Также проводили стандартную ПЦР и вестерн-блоттинг на костном мозге трубчатой кости человека - образцах, получаемых из 10 костных мозгов (собираемых после ампутации вследствие атеросклероза, индуцированного ишемией конечности (без признаков остеомиелита). ПЦР идентифицировали полосу с размером, соответствующим рецептору CCK2 (фигура 12A). Проводили его секвенирование (по Сенгеру) и идентифицировали, что он обладает 92% гомологией с CCK2R (фигура 12B). Вестерн-блоттингом подтверждали экспрессию белка рецептора CCK2 во всех образцах от человека (фигура 12C).
[0170] Вывод. Мишень гастрина можно было идентифицировать в остеобластных клетках свода черепа мыши, в линиях клеток hFOB и BMMSC, а также в кости, включая пластинку роста (хондроциты), и в костном мозге человека (сбор образов во внутрикостной области), что указывает на то, что гастрин может активировать/регулировать многие типы клеток в кости. Вследствие того, что циркулирующая кровь, содержащая гастрин, проходит через костный мозг, изменения уровней циркулирующего гастрина являются биологически значимыми для любой клетки костного происхождения, которая экспрессирует рецептор CCK2.
[0171] Эффекты гастрина in vitro. Гастрин является известным регулирующим пролиферацию соединением, таким образом, сначала исследовали эффект гастрина на пролиферацию (поглощение BrdU) на трех различных клеточных моделях. Гастрин стимулировал пролиферацию во всех трех типах клеток с EC50 1-2×10-11M (фигура 13A) и максимальным эффектом ~50% (1 нМ). Такие стимулирующие действия на пролиферацию не ингибировались предварительной инкубацией с селективным антагонистом гастрина YF476 (фигура 13B). Это соединение, по-видимому, усиливало пролиферацию в клетках BMMSC. Для оценки биологической роли активации гастрином остеобластов и BMMSC проводили исследования для оценки, приводили ли эти опосредованные гастрином эффекты к минерализации костей. Измеряли связывание флуоресцентного Osteomalge с гидроксиапатитным участком минерализованных узелков. Гастрин ингибировал минерализацию костей во всех трех типах клеток с IC50 3,2×10-11-1,3×10-10M (фигура 14A) и максимальным ингибирующим эффектом ~30-50% (1 нМ). Это ингибирующее действие на минерализацию ингибировали предварительной инкубацией с селективным антагонистом гастрина, YF476 (фигура 14B). Это соединение, по-видимому, специфически увеличивает минерализацию в остеобластных клетках свод черепа мышей.
[0172] Вывод. Гастрин стимулирует пролиферацию остеобласта и BMMSC, что не предотвращается антагонистом гастрина. Опосредованная гастрином пролиферация связана со снижением минерализации, что указывает на реверсию фенотипа остеобласта. GA предотвращал это ингибирующее действие гастрина. Эти результаты указывают на то, что гастрин вызывает дифференцировку остеобластов со снижением минерализации. Антагонист не снижает пролиферацию, но поддерживает остео-фенотип. Этот эффект являлся наиболее заметным в остеобластах свода черепа.
[0173] Для дополнительной оценки биологической роли активации гастрина проводили исследования для оценки, повышали ли эти опосредованные гастрином эффекты экспрессию морфогенетического белка кости 2 (BMP2 - участвующего в дифференцировке остеобластов), RANKL (активирующего остеокласты рецептора, экспрессируемого на остеобластоах) и макрофагального колониестимулирующего фактора (M-CSF - участвующего в регуляции клеток-предшественников костного мозга и активирующего фактора активности остеокластов).
[0174] В культурах клеток свода черепа мыши гастрин (1 нМ) полностью ингибировал экспрессию гена MSCF-1, также ингибировал транскрипцию RANKL (в 0,8 раз) и ALKP (фигура 15). В hFOB гастрин также ингибировал эти транскрипты. Предварительная инкубация с YF476 предотвращала и нормализовала эти эффекты. Ни один из этих генов не идентифицировали в BMMSC, но отмечали эффекты гастрина на ALKP, при этом BMP2 не идентифицировали в каком-либо типе клеток. Это определяет, что эффекты гастрина являются катаболическими, и их ингибирование YF476 приводит к нормализации функции остеобластов, а также вызывает анаболический фенотип.
[0175] Эти данные указывают на то, что гастрин регулирует не только пролиферацию и дифференцировку остеобластов, а также участвует в регуляции клеток-предшественники. Кроме того, гастрин приводит к пролиферации BMMSC. Соединение YF предотвращало фенотипические эффекты без ингибирования пролиферации. Таким образом, гастрин непосредственно влияет на функцию костной клетки на двух уровнях: эффект на остеобласты и получаемые из костного мозга стволовые клетки и т.д. реализуется на пластинке роста через регуляцию поведения хондроцитов.
Пример 4: Исследования гастрина: эффекты ингибиторов протонной помпы на функцию G-клетки
[0176] Вследствие того, что PPI вовлечены в увеличение резорбции кости и риска перелома, оценивали роль ингибирования кислоты (повышенный pH в желудке) на функцию G-клеток и секрецию гастрина. G-клетки выделяли из слизистой оболочки антрального отдела мышей (Mastomys - Praomys natalensis), которых обрабатывали необратимым антагонистом рецептора H2 - локстидином 1 мг/л - в питьевой воде с получением устойчивой гипергастринемии. Этих животных всесторонне исследовали в качестве модели патофизиологии желудочной кислоты, связанной с длительным фармакологическим ингибированием секреции кислоты (патобиология состояния низкой кислотности).
[0177] У Mastomys (6-9 месяцев), которых обрабатывали в течение 30 суток с необратимым подавлением желудочной кислоты, демонстрировали повышенные уровни гастрина в плазме (104±23 пг/мл в сравнении с 28±13 пг/мл у необрабатываемых животных, p<0,05). Это является отражением снижения высвобождения гастрина, ингибируемого низким pH (с последующими повышенными уровнями pH в желудке). Таким образом, такая обработка приводит к модели ахлоргидрии и гипергастринемии на животных.
[0178] Содержание гастрина, уровней транскриптов гастрина, а также базального высвобождения гастрина значимо повышалось (p<0,05) в G-клетках, выделяемых из ахлоргидрических (высокий pH в желудках - G-клетки с низким воздействием кислотой) по сравнению с G-клетками, выделяемыми у необратываемых животных (таблица 2).
Краткое описание различий между нормальным pH в желудке и повышенным pH в желудке (пониженная кислотность) в выделенных G-клетка грызунов
GRP=гастриносвобождающий пептид, OCTR=октреотид
[0179] Со ссылкой на таблицу 2, повышенный pH в желудке (состояния низкой кислотности) стимулирует содержание (> в 2 раза), транскрипцию (> в 4 раза) и секрецию (> в 8 раз) гастрина G-клетками. Физиологический ответ этих клеток на стимулирующие лиганды, например, GRP и кальций, снижается - EC50 повышается. Аналогично, эти клетки являются менее чувствительными к ингибиторам, например, октреотиду (OCTR), IC50 повышается в ~5 раз.
[0180] Соединения, регулирующие высвобождение гастрина, GRP (бомбезин) и соматостатин (OCTR) проявляли увеличенную (GRP: EC50: 1,1 пМ в сравнении с 1 нМ соответственно) и сниженную эффективность (аналог соматостатина, октреотид: от 28 пМ до 140 пМ) соответственно (таблица 2). Кроме того, "гипергастринемические" G-клетки являлись на ~100% менее чувствительными в отношении детекции кальция (EC50=10 мМ в сравнении с 4 мМ в нормогастринемических клетках).
[0181] Эти данные демонстрируют, что увеличение среды (pH) в желудке in vivo существенно влияет на функцию G-клеток. Повышение pH в желудке (как происходит у пожилых индивидуумов или пациентов на PPI) специфически изменяет чувствительность к распознаванию Ca2 G-клеток и реакцию на физиологическую регуляцию. Это демонстрирует, что длительное ингибирование функции париетальных клеток и снижение секреции кислоты значительно изменяет реакцию антральных G-клеток на люминальную среду.
[0182] Это наблюдение имеет клиническую значимость, т.к. в условиях высокого люминального pH продуцируется больше гастрина. Гипергастринемия является важной, т.к. гастрин стимулирует высвобождение PTH и оказывает непосредственный эффект на костные клетки (см. фигуры 8, 10, 11).
Пример 5: Эффекты блокады кислоты на динамику костной ткани
Модель гипергастринемии на Mastomys
[0183] На модели на Mastomys анализировали эффекты подавления кислоты на желудок, циркулирующие гормоны, паращитовидные железы, а также на физиологию костей.
[0184] Очень мало известно о биологии костей этих животных. В одном из исследований идентифицировали дегенерацию межпозвоночных дисков у большинства животных (~80%) в возрасте >9 месяцев и серьезные остеоартритические изменения в диартродиальных суставах (локти, колени).
[0185] Среди лабораторных грызунов Mastomys за исключением одной линии инбредных мышей (STR/1N), по-видимому, являются наиболее восприимчивыми к остеоартриту.
[0186] Животных (самок) в возрасте 4-6 месяцев обрабатывали локстидином в течение 60 или 120 суток. Соответствующие по возрасту и полу необрабатываемые животные представляли собой контрольную группу.
[0187] Циркулирующие гормоны. Анализ гормонов (ELISA) подтверждал изменения гастрина/PTH и эстрадиола в зависимости от блокады рецепторов H2. В частности, краткосрочное повышение секреции гастрина (8 недель обработки локстидином) было связано с повышенной секрецией PTH и ингибированием эстрадиола/эстрогена (фигура 16). Длительная (16 недель), хроническая гипергастринемия была связана с ингибированием PTH и эстрадиола.
[0188] Желудок. Демонстрировали активацию гистамина ECL (гистидиндекарбоксилаза-HDC) (фигура 17A) и гастрина G-клеток (на уровне иРНК) во время гипергастринемии (фигура 17B). Это соотносилось с активацией PTH1R (на уровнях иРНК и белка) и избирательными снижениями ERα в желудке (на уровнях иРНК и белка) во время краткосрочной гипергастринемии; затем это повышалось на 16 неделе и было связано с активацией CaSR (на уровнях иРНК и белка) во время гипергастринемии (фигура 17A-C).
[0189] Паращитовидная железа. С использованием иммуногистохимии демонстрировали экспрессию рецептора CCK2 в паращитовидной железе и щитовидной железе Mastomys (фигура 18). Результаты выявляли, что клетки паращитовидной железы, а также C-клетки щитовидной железы экспрессируют рецептор гастрина. Рецептор CCK2 в паращитовидных железах обеспечивают основу для системы G-клетка:PTH, таким образом гастрин может регулировать секрецию паращитовидной железой (например, PTH).
[0190] Морфология и динамика костной ткани. Использовали оценку micro CT для разработки морфометрических анализов костной ткани (фигура 19) бедренных костей грызунов у животных с гипергастринемией. Анализы демонстрировали более низкие объемы костной ткани и сниженную плотность, и сопротивление растяжению. Эти данные демонстрируют, что повышенные уровни гастрина стимулировали резорбцию костей.
[0191] По показателю структурной организации (SMI) определяли сдвиг отношения пластины/балки, что демонстрирует изменение геометрии бедренной кости. Таким образом, гастрин повышал SMI, что указывает на изменение костного фенотипа путем ремоделирования в сторону более балкообразной структуры. Последняя ассоциирована с более слабыми и более жесткими костями и ломкостью костей, отмечаемой у женщин с остеопорозом.
[0192] В отличие от нормальных Mastomys животные с хронической гипергастринемией обладали остеоартритическим фенотипом со следующими ниже признаками: утолщение эпифизарной пластинки, хрупкость костей (аномальная восстановление костей вследствие увеличенного образования адипоцитов) и идентификация аномальных иммуногенных признаков.
[0193] Из бедренных костей выделяли костный мозг и оценивали на остеокластогенез. Остеокласты и остеобласты можно было культивировать при аномально раннем периоде времени по сравнению с клетками, выделяемыми у мышей после овариэктомии. Это свидетельствует об активации этих двух популяций клеток на модели гипергастринемии. Это соответствует активации индуцируемого рецептором CCK2 события.
[0194] По сравнению с мышами после овариэктомии у Mastomys с гипергастринемией демонстрируют усиленное морфологическое ремоделирование костной ткани. Наличие аномального фенотипа костного мозга дополнительно подтверждали идентификацией на основе количественно ПЦР пути активации у животных с гипергастринемией. Это включало снижение экспрессии ALOX5 и PTGS2 (воспаление), снижение экспрессии PPARy (активация адипоцитов) и повышение экспрессии TNFSR11 (RANKL) (активность остеоцитов). Результаты ПЦР соответствовали в частности активации деятельности остеоцитов с наблюдаемыми макроскопическими изменениями костного мозга (эпифизарный рост, ломкость костей).
[0195] Для дополнительной оценки фенотипа костного мозга и оценки, активировалась ли жировая ткань кости (величина метаболизма и целостности костной ткани), использовали протокол окрашивания на основе осмия у контрольных животных, совпадающих по возрасту-полу, и у животных с краткосрочной гипергастринемией. Отмечали значительное увеличение поглощения у обрабатываемых животных (фигура 20). Это соответствует "старой" кости/остеопорозному фенотипу.
[0196] Эти результаты подтверждают, что краткосрочная гипергастринемия ассоциирована с изменениями костей, которые являются аналогичными морфологическим проявлениям, идентифицируемым при остеопорозе.
[0197] В дальнейшем анализировали гистоморфометрия костей. Эти исследования идентифицировали пониженную минерализацию костей с увеличенными полостями резорбции, а также существенно сниженные количества (p<0,05) TRAP-положительных остеокластов (15±6 p<0,05 и 16±4,5 p<0,05, в сравнении с 9±3 в контролях) у Mastomys с обработкой в течение 8 недель и 16 недель. Также отмечали признаки остеоидных швов и остеомаляции (фигура 21).
[0198] Наконец, анализировали прочность костей у Mastomys с использованием устройства Instron. Бедренные кости подвергали нагрузке для перелома при сгибании в четырех точках. Тесты проводили со скоростью отклонения 0,05 мм/сек с использованием сервогидравлической испытательной машины (Instron модель 8874, Instron Corp., Norwood, MA, USA).
[0199] Наконец, анализировали прочность костей у Mastomys с использованием устройства Instron. Бедренные кости подвергали нагрузке для перелома при сгибании в четырех точках. T Тесты проводили со скоростью отклонения 0,05 мм/сек с использованием сервогидравлической испытательной машины (Instron модель 8874, Instron Corp., Norwood, MA, USA).
[0200] Жесткость находилась в диапазоне от 158-173 Н/мм. Предельная нагрузка, необходимая для перелома кости, находилась в диапазоне 32,8-45,7 Н/мм. Эти значение сильно коррелировали друг с другом (фигура 17A, R2=0,86, p<0,003, линейный регрессионный анализ).
[0201] Сравнения плотности костей (micro CT) и силы перелома идентифицировали корреляции для губчатой (R2=0,54, 22B) и трубчатой (R2=0,71, 22C) костей.
[0202] Таким образом, измерения прочности кости с использованием устройства Instron обеспечивают дополнительную информацию, указывающую на развитие аномального и связанного с хрупкими костями фенотипа во время гипергастринемии. Эти механические характеристики подтверждают доказательство биологической основы вызываемого гастрином "остеопорозного" фенотипа на модели гипергастринемии.
[0203] Вывод (фигура 23, 24). Краткосрочная гипергастринемия (8 недель) вызывает наглядные и измеряемые изменения остеопорозного типа в бедренной кости. В антральном отделе желудка краткосрочная гипергастринемия была ассоциирована с активной G-клеткой (транскриптом), повышенной экспрессией PTH1R и сниженной восприимчивость к эстрогену (ERα/β и AR) без изменения экспрессии CaSR. Наблюдения анализа костей являются аналогичными наблюдениям, выявляемым в состоянии постменопаузы человека.
[0204] Удлинение гипергастринемии до 16 недель (хроническая модель) приводило к измеряемым остеопорозным изменениям в бедренной кости и было ассоциировано с повышенной экспрессией антральных CaSR и ERα, а также PTH1R (фигура 17).
[0205] Сочетание повышенного уровня циркулирующего гастрина и повышенной экспрессии PTH1R на G-клетках являлось надежным признаком, связанным с остеопорозным фенотипом.
[0206] Эти результаты указывают на то, что Mastomys с гипергастринемией являются подходящей моделью для оценки эффектов гастрина на патофизиологию костной ткани, и для них демонстрируют значительные проостеопорозные эффекты гипергастринемии на костную ткань.
Пример 6: Эффекта блокады кислоты на динамику костной ткани у Mastomys после овариэктомии
[0207] Овариэктомия представляет собой стандартный способ получения "постменопаузного" фенотипа для исследований костной ткани. Вследствие того, что эстроген оказывает регулирующее действие на G-клетки (см. фигуру 6), затем оценивали конкретную роль снижения эстрогена в отношении костного фенотипа у необрабатываемых животных, у животных после овариэктомии, а также у животных после овариэктомии с краткосрочной (8 недель) и длительной (16 недель) гипергастринемией. Двустороннюю овариэктомию (OVX) и перевязку маточных труб проводили с использованием заднего доступа у Mastomys. Животных исследовали после 8 недель.
[0208] Циркулирующие гормоны. Через 8 недель эстроген снижался в результате овариэктомии. Однако PTH в сыворотке повышался в ~2 раза (фигура 25).
[0209] Желудок. Овариэктомия была связана со значительным повышением транскрипции хромогранина A (CgA) и HDC, но экспрессия гастрина не изменялась (фигура 26). Это демонстрирует, что один из эффектов эстрогена в желудке заключается в подавлении синтеза гистамина ECL-клетками.
[0210] Овариэктомия повышала транскрипцию андрогенных (в 6 раз) и эстрогенных рецепторов (ESRα/β: в 4-7 раз) слизистой желудка, а также CaSR (в 5 раз) и PTH1R (в 4 раза) (фигура 27). Таким образом, удаление эстрогена приводило к детектируемым изменениям рецепторов клеток желудка, участвующих в восприятии и реакции на поступающий с пищей кальций, т.е. системы CaSR и паращитовидной железы (PTH1R).
[0211] Модель краткосрочной гипергастринемии/OVX. Краткосрочная гипергастринемия на модели овариэктомии повышала циркулирующий PTH (фигура 25). В желудке транскрипты гастрина и HDC повышались в результате комбинации подавления кислоты (8 недель локстидина) и OVX (фигура 26B-D). Повышенную экспрессию рецепторов, а именно AR/ESRα/β, CaSR и PTH1R, которая возникает после OVX (т.е. фигура 27) не идентифицировали у животных с гипергастринемией. Уровни являлись пониженными и больше не отличались от контроля (фигура 28). Это указывает на то, что фармакологическое подавление секреции кислоты (с повышением pH в желудке и гастрина) нормализует экспрессию рецепторов в желудке, участвующих в чувствительности к кальцию, даже когда удаляли эстроген.
[0212] Модель длительной гипергастринемии/OVX. Гипергастринемия в течение 16 недель была ассоциирована с нормализацией уровней PTH в плазме (фигура 30). HDC в желудке повышался (фигура 26). Уровни AR/ESRα, CaSR и PTH1R у обрабатываемых в течение 16 недель животных не отличались от контроля (фигура 28). Экспрессия рецепторов в желудке вовлечена в чувствительность к кальцию на длительной модели, т.к. на краткосрочной модели он являлись нормальными во время удаления эстрогена.
[0213] Морфология и динамика костной ткани на модели OVX и модели OVX с гипергастринемией
[0214] Анализ Micro CT. Трабекулярная топографи представлена на фигуре 29. Измерения костей идентифицировали, что после овариэктомии плотность и объем снижались ~50%. Это соответствует предшествующим сообщениям на моделях овариэктомии на грызунах (фигура 30A, C). Опосредованные гастрином снижения являлись наиболее значимыми (p<0,005) у животных с длительной гипергастринемией (80-85% снижения). У последних животных также выявляли снижения (~5%, p<0,05) плотности трубчатой ткани (фигура 30B). Объем трубчатой кости уменьшался у всех животных OVX (~15%), но наиболее существенно (p<0,005, ~30%) у животных с краткосрочной гипергастринемией (фигура 30D).
[0215] Дополнительные измерения трубчатой кости идентифицировали значительные уменьшения внутренней надкостницы и надкостницы. OVX уменьшала радиус (20%) и окружность (18%) (фигура 31A-D). Наиболее значительные уменьшения идентифицировали у животных с краткосрочной гипергастринемией (радиус: 25-30%; окружность 27%). Они являлись меньше по сравнению с уменьшениями, измеряемыми во время одной OVX (p<0,02). Измерения у животных с длительной гипергастринемией не отличались от измерений при одной OVX.
[0216] Эти результаты выявляют, что повышенные уровни циркулирующего гастрина усиливали опосредованные снижением эстрогена изменения костной ткани. Наиболее значимые эффекты краткосрочной гипергастринемии наблюдали на уровне трубчатой кости и внутренней надкостницы/андкостницы, при этом эффекты длительной гипергастринемии преобладали в губчатой кости, определяя роль последнего также в регуляции метаболизма и прочности костной ткани. Для оценки последней проводили исследования испытания на прочность.
[0217] Гистоморфометрия костной ткани. Овариэктомия была ассоциирована со сниженной минерализацией костей с увеличенными полостями резорбции, а также значительно повышенными (p<0,05) количествами TRAP-положительных остеокластов (26,8±11 в сравнении с 9±3 в контролях, p<0,05) (фигура 32).
[0218] Тестирование механической прочности кости. Анализ сгибания в четырех точках бедренной кости идентифицировал увеличение жесткости у животных с OVX (фигура 33A). OVX также снижала максимальную нагрузку и нагрузку перелома (фигура 33B, C). Это указывает на то, что снижение эстроген само по себе снижает прочность костной ткани (эффект на трубчатую структуру), при этом повышая ее жесткость (эффект на губчатую структуру относился к изменениям балки/пластинки). Краткосрочная гипергастринемия снижала количество работы, необходимой для перелома кости (фигура 33D). Эти параметры отражают эффект, указывающий на слабую, поврежденную трубчатую кость (фигура 30-31). Получаемая в результате OVX прочность костей восстанавливалась в результате краткосрочной гипергастринемии, что подтверждает, что эти эффекты гастрина ограничены фазами активации и резорбции ремоделирования костной ткани. Длительная гипергастринемия восстанавливала нагрузку и работу, необходимую для перелома кости. Однако у этих животные повышалась жесткость костей, что согласуется с изменениями губчатой структуры (фигура 30). Это соответствует фенотипу ремоделирование костной ткани, который включает фазы восстановления и формирования образования костной ткани, но является аномальным тем, что костная ткань является жесткой и, таким образом, слабой.
[0219] Оценка механической прочности. pMOI (полярный момент инерции) представляет собой показатель общей прочности (и жесткости) кости и является пропорциональным разрушающей нагрузке (при кручении). Он увеличивается при аномальном срастании. Этот параметр оценивали для обеспечения дополнительного показателя прочности кости, т.к. он конкретно представляет собой показатель слабости кости. OVX снижал pMOI, который дополнительно значительно снижался в результате краткосрочной гипергастринемии (фигура 34A). Это подтверждает, что овариэктомия ослабляет кости, и демонстрирует, что повышение гастрина усугубляет слабость костной ткани. Длительная гипергастринемия была ассоциирована с пониженным pMOI (по сравнению с контролями), но не отличалась от одной OVX. Это соответствует данным сгибания в 4 точках (см. выше) и включает эффекты гастрина во время краткосрочного (аномальная активация и ремоделирование) и длительного (аномальное восстановление и образование костной ткани) воздействия.
[0220] Анализ ПЦР в реальном времени костного мозга. OVX оказывала существенное влияние на экспрессию пяти генов, ассоциированных с ремоделированием костной ткани (два снижались и три повышались). В частности, получаемые из костного мозга трубчатой кости ALOX5 (воспаление) и RUNX2 (дифференцировка остеобластов) значительно снижались (фигура 35). Экспрессия CXCL12, PPARγ и HIF-1α повышалась. CXCL12 ассоциирован с опосредованной PTH активацией остеобластов, PPARγ с дифференцировкой адипоцитов (защитный механизм костной ткани) и HIF-1α с опосредованным гипоксией повреждением костей (снижает экспрессию RUNX2, связанного с активацией периостеальных костных клеток-предшественников). Это соответствует ингибированию дифференцировки остеобластов и активации остеокластов.
[0221] Ни краткосрочная (8 недель), ни длительная (16 недель) гипергастринемия значительно не изменяли (не усиливали или не ингибировали) опосредованные OVX изменения экспрессии генов в ремоделировании костной ткани. Однако гастрин существенно снижал PTGS2 (или индуцибельный COX2). Это является реакцией на повреждение кости и соответствует биологическому ответу, связанному с защитой.
[0222] Вывод (фигура 36). Связанные с овариэктомией аномалии костей (губчатых и трубчатых) на модели на Mastomys были ассоциированы с изменениями физиологии костной ткани (ингибированием функции остеобластов) и экспрессии гена на уровне клетки костного мозга из кортикального вещества кости. Это соотносилось с повышением нейроэндокринных маркеров слизистой желудка, включая HDC, и чувствительности к кальцию/ответов PTH1R.
[0223] Краткосрочная гипергастринемия после овариэктомия дополнительно ослабляла кость с аналогичными изменениями костных фенотипов (сниженными плотности и объемы губчатой и трубчатой структур) и профилей экспрессии генов костного мозга (например, активации HIF-1α), как одна овариэктомия. Повышенная транскрипция гастрина являлась наиболее значимым изменением в желудке при нормализации экспрессии CaSR/PTH1R.
[0224] Длительная гипергастринемия приводила к слабой и очень жесткой кости. Аналогичные изменения отмечали в фенотипах (сниженные плотности и объемы губчатой и трубчатой структур), а также в экспрессии генов костного мозга (активация HIF-1α) для одной овариэктомии. Наиболее значимым изменением в желудке являлась активация HDC при нормализации экспрессии CaSR/PTH1R.
[0225] В целом, утрата костной массы/аномалии ассоциированы с изменениями активации клеток костного мозга и изменениями транскрипции нейроэндокринных клеток слизистой желудка.
Пример 7: Эффекты на нейроэндокринную функцию желудка и динамику костной ткани: модели нокаута генов на мышах - с овариэктомией и без нее
[0226] Исследования с использованием моделей нокаута гастрина и гистамина демонстрировали взаимосвязь между гистамином и гастрином в опосредовании метаболизма костной ткани (целостности) и оценивали роль гастрина и гистамина на различных видах модели на Mastomys. В этих исследованиях оценивали эффекты опосредованной гастрином секреции гистамина на биологию костной ткани (а также наблюдения авторов, что G-клетки регулируются эстрогеном). Использовали три комбинации нокаута: мыши с нокаутом по HDC, а также с нокаутом по гастрину и животные с нокаут двойной комбинации (HDC/GAS).
[0227] Циркулирующие гормоны. a) Эстрадиол снижался (80-90%) до одинакового уровня (~2 пг/мл) на всех три моделях KO после овариэктомии (фигура 37). b) Гастрин являлся низким у всех мышей с KO по гастрину и у мышей с двойным KO (10-20 пг/мл); у животных с KO по HDC уровни гастрина являлись в 5× выше, чем у животных с KO по GAS или KO по GAS/HDC. Эти уровни не затрагивались овариэктомией и являлись аналогичными Mastomys с нормогастринемией.
[0228] Уровни PTH являлись аналогичными во всех трех моделях KO (фигура 37), но являлись на -50% Mastomys с нормогастринемией. Овариэктомия повышала уровни PTH у животных с KO по HDC и по HDC/GAS, что согласуется с утратой ингибирующего действия эстрогена на секрецию паращитовидной железы. Это дает основание предполагать, что отсутствие гистамина не оказывает влияние на секрецию паращитовидной железы. В противоположность этому PTH снижался после овариэктомии у животных с KO по GAS. У Mastomys гипергастринемии в течение 8 недель повышала высвобождение PTH, и эксперименты in vitro подтверждали опосредованное гастрином высвобождение PTH. Это позволяет предположить, что гастрин является необходимым для физиологического высвобождения PTH. Комбинация снижения эстрогена и гастрина приводит к паращитовидной железе с "низкой" секрецией PTH. Вследствие того, что PTH связан с активацией остеокласта через RANK-остеобласт (резорбцию кости)102, отсутствие гастрина в этих условиях можно расценивать как "защитное".
[0229] Желудок. У животных с KO по гастрину OVX значительно усиливала экспрессию рецептора CCK2 в своде (в 3 раза) (фигура 38) и повышала HDC в 10 раз, что указывает на то, что эстроген оказывает ингибирующее действие на ECL-клетку. В антральной G-клетке OVX снижала экспрессию CaSR на 60%, что указывает на то, что чувствительность G-клетки к кальцию регулируется эстрогеном. У животных с KO по HDC OVX снижало экспрессию большей части генов-мишеней, включая CaSR, PTH1R и CCK2 по сравнению с контролем (без овариэктомии). Экспрессия гастрина также значительно понижалась. У животных с двойным KO овариэктомия повышала экспрессию CCK2. Эти данные указывают на то, что эстроген регулирует экспрессию транскриптов, участвующих в чувствительности кальция и, таким образом, метаболизме кальция. В частности, ECL- и G-клетка желудка являются эстроген-чувствительными особенно в отношении физиология кальция.
Морфология и динамика костной ткани
[0230] Micro CT костной ткани. У мышей с KO по гастрину овариэктомия не оказывала достоверного эффекта на плотность и объем бедренной кости, но увеличивала толщину внутренней надкостницы и надкостницы (фигура 39A). Это являлось прямо противоположно эффектам, отмечаемым при краткосрочной и длительной гипергастринемии (сниженные плотность и объем губчатых и трубчатых костей, а также внутрикостных и надкостных параметров - см. фигуру 24). Это приводило к кости, которая не являлась жесткой и ослабленной по сравнению с костями без овариэктомия. Это демонстрирует, что отсутствие гастрина (при низкой эстрогенной среде) являлось защитным и может отражать низкие уровни циркулирующего PTH у этих животных.
[0231] Мыши с KO по HDC. Овариэктомия у мышей с KO по HDC не оказывала достоверного эффекта на плотность и объем бедренной кости или на толщину внутренней надкостницы/надкостницы. Однако кость являлась жесткой, для нее требовалась более высокая нагрузка для перелома, и для нее демонстрировали увеличенный pMOI (p<0,03) по сравнению с костями без овариэктомии (фигура 39B). Таким образом, исследования авторов изобретения подтверждают более ранние исследования99, что комбинация снижения эстрогена и гистамина увеличивает прочность костей.
[0232] Мыши с KO по Gas/HDC. Овариэктомия у мышей с двойным KO по гастрину/HDC не оказывала достоверного эффекта на плотность бедренной кости, но объемы губчатой и трубчатой костей уменьшались (p<0,03) (фигура 39C). Не отмечали изменений толщины внутренней надкостницы/надкостницы. Это приводило к кости, которая не являлась ослабленной по сравнению с костями без овариэктомии.
[0233] Количественная ПЦР костного мозга. Овариэктомия у животных с KO по гастрину была ассоциирована с повышением экспрессии двух генов ALOX5 и CXCL12 (фигура 40A-B). Они участвуют в синтезе лейкотриена и воспалении, и активации остеобластов через PTH соответственно. На модели на Mastomys овариэктомия снижала экспрессию ALOX5, но повышала экспрессию CXCL12, эффекты на которые не оказывала значительного влияния гипергастринемия. Овариэктомия у животных с KO по HDC и HDC/GAS не оказывала достоверного эффекта, что указывает на то, что гистамин не играет роли в регуляции этих двух генов.
[0234] ПЦР костного мозга также идентифицировали, что овариэктомия у животных с KO по гастрину была ассоциирована с повышением экспрессии HIF-1α и IGF1 (фигура 40C-D). Они участвуют, как ранее отмечают, в регуляции остеопрогениторных клеток и поддерживают костную массу соответственно.
[0235] Вывод (фигура 41). Снижение гастрина (при низкой эстрогенной среде) на модели на мышах изменяло физиологию костной ткани, но не являлось вязанным со значимым отличием прочности кости. В противоположность этому, овариэктомия с краткосрочной или длительной гипергастринемией (на модели на Mastomys) приводила к существенно более слабой кости. Таким образом, гастрин, по-видимому, оказывает неблагоприятный и "незащитный" эффект на костный мозг. Отдельно KO по HDC (при низкой эстрогенной среде) было ассоциировано со значительно более сильной (и жесткой) костью, что позволяет предполагать, что гистамин, так же как и гастрин, могут играть регулирующую роль в физиологии костной ткани. Удаление гистамина (посредством KO по HDC) предотвращало этот эффект и, таким образом, согласовалось с утверждением, что гастрин и гистамин совместно являются ключевыми регулирующими факторами физиологии костной ткани.
[0236] Сочетание снижения гастрина и HDC (например, снижении гистамина) в низкой эстрогенной среде не являлось связанным с существенно более слабой костью, и динамика костной ткани не отличалась от нормальной. Это позволяет предположить, что гистамин (так же как и гастрин) могут активировать "остеопорозно"-подобный фенотип костей. Таким образом, снижение (удаление) гистамина (посредством KO по HDC) предотвращало проостеопорозный эффект, индуцируемый снижением эстрогенов.
Пример 8: Контрольно-проверочные исследования: эффекты антагониста гастрина на опосредованный овариэктомией костный фенотип на трех моделях на грызунах
[0237] Эффекты антагониста гастрина YF476 на опосредованное OVX снижение плотности кости/изменения кости на трех моделях на грызунах оценивали, уделяя особое внимание исследованиям прочности, морфологии кости и циркулирующим биомаркерам. Анализировали две модели "нормальной" OVX: a) мышь (линия: CD-1 [швейцарская линия] - Charles River) и b) крыса (линия: CD IGS [линия Sprague Dawley] - Charles River), а также модель на Mastomys (эндогенно активируемые сигнальные каскады гастринового/CCK2 рецептора).
[0238] Животных, которых подвергали хирургической операции (OVX) в возрасте 2 месяцев, оставляли восстанавливаться, а затем подвергали пероральному ингибированию кислоты, также антагонисту гастрина (GA), YF476 (однократная инъекция). Мышей и крыс подвергали PPI, омепразолу, при этом Mastomys подвергали действию антагониста рецептора H2, локстидина. Введение GA представляло собой однократную подкожную инъекцию в начале ингибирования кислоты. В точки зрения фармакокинетики эта доза лежит в диапазоне 15-20 нмоль в течение периода 8 недель. Подробное описание касательно дозирования приведено в таблице 3.
Дозирование в контрольно-проверочных исследованиях
[0239] Три группы включали для каждой модели на животных: a) группа A=обрабатываемые плацебо/физиологическим раствором (без OVX/контроли); b) группа B=OVX+ингибирующая кислоту терапия (OVX) и c) группа C=обрабатываемые GA животные после овариэктомии (OVX+GA). По завершению исследования (2 месяца) авторы оценивали, восстанавливал ли GA опосредованные OVX изменения параметров костей (microCT, прочности и гистоморфометрии костей, а также циркулирующих маркеров).
[0240] Модель 1: OVX мышей. В начале обработки GA возраст животных составлял 89 суток (3,0 месяца), и в конце исследования их возраст составлял 146 суток (4,8 месяцев). Анализ данных губчатой кости идентифицировал, что овариэктомия значительно снижала BV/TV (0,05±0,02 в сравнении 0,18±0,04, p<0,05) и плотность (37±5 в сравнении 173±18, p<0,05) и повышала SMI (1,8±1,2 в сравнении 1,1±0,4, p<0,05) и пространство губчатого вещества (0,6±0,18 в сравнении 0,28±0,05, p<0,05) (таблица 4, фигура 42). Обработка антагонистом гастрина предотвращала эти опосредованные овариэктомией изменения костей за исключением толщины и пространства губчатого вещества, которые оставались повышенными. Это соотносилось со значительным повышением плотности губчатой кости(70,7±19, p<0,05 в сравнении OVX).
Результаты губчатых костей на модели 1
[0241] Анализ параметров трубчатой кости идентифицировал, что овариэктомия значительно уменьшала поверхность кости (11,6±0,9 в сравнении 13,4±1,4, p<0,05), повышала толщину трубчатой структуры (0,2±0,01 в сравнении 0,15±0,01, p<0,05) и была связана со снижением (989±26 в сравнении 1153±39, p<0,05) плотности трубчатой кости (таблица 5, фигура 43). Обработка антагонистом предотвращала опосредованное OVX уменьшение плотности (1025±37, p<0,05 в сравнении с OVX).
Данные по трубчатым костям на модели 1
[0242] Измерения прочности кости с использованием устройства подтверждали пригодность антагониста гастрина для восстановления опосредованного OVX костного фенотипа. Овариэктомия значительно снижала (p<0,05) прочность костей (жесткость [246±29 в сравнении с 294±34], выходная жесткость [221±28 в сравнении с 271±33], нагрузка перелома для разрушения [37±6 в сравнении с 56±7]) и увеличивала полную работу, необходимую для перелома кости [28,3±9,7 в сравнении с 20,4±2,3, p<0,05]. Обработка антагонистом гастрина нормализовала эти опосредованные овариэктомией изменений костной ткани за исключением нагрузки перелома [43±6], которая являлась повышенной, но оставалась ниже, чем в контролях (таблица 6, фигура 44).
Данные прочности костей
[0243] Гистоморфометрией идентифицировали пониженную минерализацию костей с увеличенными полостями резорбции, а также значительно повышенное (p<0,05) число TRAP-положительных остеокластов (29±5 в сравнении с 16±3, p<0,05) у мышей с OVX. Обработка антагонистом предотвращала эти явления (фигура 45).
[0244] Овариэктомия значительно (p<0,05) снижала циркулирующий эстроген (1,9±0,9 пг/мл в сравнении с 5,1±1,9) и была ассоциирована с повышением PTH (123±74 пг/мл в сравнении с 51±32) и гастрина (3200±263 пг/мл в сравнении с 2437±787). Обработка антагонистом предотвращала опосредуемое овариэктомией повышение гастрина, но не PTH (таблица 7, фигура 46). Циркулирующие биомаркеры кости также изменялись в результате OVX. В частности, PINP повышался (0,19±0,01 нг/мл в сравнении с 0,1±0,006, p<0,05), как и повышался CTx-1 (0,60±0,14 нг/мл в сравнении 0,29±0,13, p<0,05) и остеокальцин (6,7±2,3 нг/мл в сравнении с 4,1±1,2, p<0,05). Обработка антагонистом ослабляла каждое из этих трех опосредуемых овариэктомией изменений.
Уровни циркулирующих в крови маркеров в каждой из трех групп
[0245] Вывод (Модель 1). Однократная инъекция антагонистов гастрина являлась связанной с предотвращением опосредованных овариэктомией изменений костей (анализируемых на 8 неделе) на модели на мышах. Эти эффекты происходили несмотря на низкие уровни циркулирующего эстрогена и высокие уровни PTH, и были проиллюстрирован нормализацией гистоморфометрических параметров (минерализация, число остеокластов) и экспрессией циркулирующих биомаркеров костной ткани, соответствующей анаболическим эффектам.
[0246] Модель 2: модель OVX на крысах. В начале обработки GA возраст животных составлял 98 суток (3,2 месяца), и при завершении исследования их возраст составлял 163 суток (5,4 месяца). Анализ данных губчатой кости идентифицировал, что овариэктомия значительно снижала BV/TV (0,15±0,03 в сравнении с 0,27±0,07, p<0,05) и плотность (159±26 в сравнении с 287±71, p<0,05). Пространство губчатого вещества (0,58±0,1 в сравнении с 0,44±0,19, p<0,05), а также SMI (1,5±0,2 в сравнении с 0,6±0,4, p<0,05) также увеличивались (таблица 8, фигура 47). Обработка антагонистом гастрина предотвращала эти опосредуемые овариэктомией изменения костей за исключением SMI (1,3±0,17), который оставался повышенным. Это соотносилось с существенным увеличением плотности губчатой кости (204±27, p<0,05 в сравнении с OVX).
Результаты данных губчатой кости из модели 2
[0247] Анализ параметров трубчатых костей идентифицировал, что овариэктомия значительно уменьшала поверхность кости (42,7±2,5 в сравнении с 49,9±3, p<0,05), увеличивала толщину трубчатой структуры (0,66±0,03 в сравнении с 0,61±0,07, p<0,05) и являлась связанной с уменьшением (1067±22 в сравнении с 1144±17, p<0,05) плотности трубчатой структуры (таблица 9, фигура 48). Обработка антагонистом предотвращала опосредуемое OVX уменьшение плотности (1098±24, p<0,05 в сравнении с OVX).
Результаты данных трубчатой кости из модели 2
(обрабатываемые GA)
[0248] Измерения прочности костей с использованием устройства подтверждали пригодность антагониста гастрин для предотвращения опосредуемого OVX костного фенотипа. Овариэктомия значительно снижала (p<0,05) прочность костей (жесткость [495±43 в сравнении с 578±48], выходную жесткость [445±39 в сравнении с 526±66] и нагрузку перелома для разрушения [265±29 в сравнении с 300±17]). Обработка антагонистом гастрина нормализовала эти опосредуемые овариэктомией изменения костей (таблица 10, фигура 49).
Данные прочности костей
[0249] Гистоморфометрией идентифицировали измененную минерализацию костей с увеличенными полостями резорбции, а также существенно увеличенным (p<0,05) числом TRAP-положительных остеокластов (11±3 в сравнении с 2±2, p<0,05) у крыс OVX. Обработка антагонистом предотвращала эти явления (фигура 50).
[0250] Овариэктомия значительно (p<0,05) снижала циркулирующий эстроген (2,1±0,3 пг/мл в сравнении с 5,3±2,5) и была ассоциирована с увеличением гастрина (3200±789 пг/мл в сравнении с 954±406). Обработка антагонистом не оказывала достоверного эффекта на эстроген или гастрин (таблица 11, фигура 51). Циркулирующие биомаркеры костной ткани также изменялись в результате OVX. В частности, PINP (0,57±0,18 нг/мл в сравнении с 0,35±0,06, p<0,05), и остеокальцин повышался (1,35±0,9 нг/мл в сравнении с 0,43±0,07, p<0,05). Обработка антагонистом ослабляла каждое из этих опосредуемых овариэктомией изменений.
Уровни циркулирующих в крови маркеров в каждой из трех групп
[0251] Вывод (модель 2). Однократная инъекция антагонистов гастрина была ассоциирована с восстанавливаемыми опосредуемыми овариэктомией изменениями костной ткани (анализировали на 8 неделе) на модели на крысах. Эти эффекты происходили, несмотря на низкий уровни циркулирующего эстрогена и высокие уровни гастрина, и были проиллюстрированы нормализацией гистоморфометрических параметров (минерализация, число остеокластов) и экспрессией циркулирующих биомаркеров костной ткани, соответствующей анаболическому эффекту.
[0252] Модель 3: модель OVX на Mastomys. В начале обработки GA возраст животных составлял животные 121 сутки (4,0 месяца) и при завершении исследования 180 суток (6,0 месяцев). Овариэктомия значительно снижала отношение BV/TV (0,06±0,03 в сравнении с 0,14±0,05, p<0,05), число трабекул (1,4±0,3 в сравнении с 2,0±0,6, p<0,05) и поверхность кости (8,5±3,7 в сравнении с 18,5±2,3, p<0,05) и повышала SMI (1,1±0,3 в сравнении с 0,74±0,21, p<0,05), а также пространство губчатое вещество (0,82±0,15 в сравнении с 0,57±0,17, p<0,05) (таблица 12, фигура 52). Это соотносилось со значительным снижением плотности губчатой кости (60,6±37 в сравнении с 157±51, p<0,05). Обработка антагонистом гастрина предотвращала эти опосредуемые овариэктомией изменения костей, нормализуя плотность губчатой кости (187±66). Лекарственное средство также было ассоциировано с увеличением числа трабекул (2,4±0,6, p<0,05 в сравнении с контролем) и толщины (0,08±0,01, p<0,05 в сравнении с контролем).
Результаты данных губчатой кости из модели 3
[0253] Оценкой параметров трубчатых костей идентифицировали, что овариэктомия не изменяла значительно какие-либо параметры трубчатой кости (таблица 13, фигура 53). Обработка антагонистом гастрина не оказывала эффекта у животных после овариэктомии.
Результаты данных трубчатой кости из модели 3
[0254] Измерения прочности кости с использованием устройства Instron подтверждали пригодность антагониста гастрина для предотвращения опосредуемого OVX костного фенотипа. Овариэктомия значительно снижала (p<0,05) прочность кости (жесткость [138±7 в сравнении с 332±65], выходная жесткость [125±6 в сравнении с 299±59], нагрузка перелома до разрушения [38±4 в сравнении с 56±13]) и увеличивала полную работу, необходимую для разлома кости [51±7,7 в сравнении с 34±11,6, p<0,05]. Обработка антагонистом гастрина нормализовала эти опосредуемые овариэктомией изменения костной ткани (таблица 14, фигура 54).
Данные прочность кости
[0255] Гистоморфометрией идентифицировали пониженную минерализацию костей с увеличенными полостями резорбции, а также значительно сниженное (p<0,05) число TRAP-положительных остеокластов (27±11 в сравнении с 9±3, p<0,05) у Mastomys с OVX. Обработка антагонистом предотвращала эти явления (фигура 55).
[0256] Овариэктомия значительно (p<0,05) снижала циркулирующий эстроген (1,9±0,6 пг/мл в сравнении с 8,9±2,1) и была ассоциирована с повышением PTH (523±308 пг/мл в сравнении с 290±71) и гастрина (7265±3198 пг/мл в сравнении в 3705±2015). Обработка антагонистом предотвращала опосредуемое овариэктомией повышение гастрина (2704±430) и PTH (150±37) (таблица 15, фигура 56). Циркулирующие биомаркеры костной ткани также изменялись в результате OVX. В частности, PINP повышался (0,16±0,03 нг/мл в сравнении с 0,13±0,01, p<0,05), как повышался CTx-1 (0,24±0,17 нг/мл в сравнении с 0,03±0,03, p<0,05), при этом повышался остеокальцин (1,6±1,1 нг/мл в сравнении с 0,4±0,16, p<0,05). Обработка антагонистом ослабляла каждое из этих трех опосредуемых овариэктомией изменений
Уровни циркулирующих в крови маркеров в каждой из трех групп
[0257] Вывод (модель 3). Однократная инъекция антагониста гастрина была ассоциирована с предотвращением опосредуемых овариэктомией изменений костной ткани (анализируемых на 8 неделе) на модели на Mastomys. Эти эффекты происходили, несмотря на низкий циркулирующий эстроген, и были проиллюстрированы нормализацией гистоморфометрических параметров (минерализация, число остеокластов) и экспрессией циркулирующих биомаркеров костной ткани, соответствующей анаболическим эффектам.
[0258] Вывод (модели 1, 2 и 3). Однократная инъекция антагонистов гастрина (10-20 мк/мг массы тела) предотвращала опосредуемый овариэктомией остеопороз и восстанавливала прочность, нормализующуюся или с тенденций к нормализации, в трех из 3 моделей. Это происходило, несмотря на низкие уровни циркулирующего эстрогена и высокого PTH и было ассоциировано с модификацией сигнального каскада прокостной массы.
[0259] На всем протяжении этой заявки приведены ссылки на содержание данных различные веб-сайтов, публикации, патентные заявки и патенты. (На веб-сайты приводят ссылки по их адресам унифицированного указателя ресурса или URL во Всемирной сети Интернет.) Описания каждой из такой ссылок, таким образом, полностью включены в настоящее описание посредством ссылки.
[0260] Настоящее изобретение не должно быть ограничено в объеме вариантами осуществления, описываемыми в настоящем описании, которые предназначены в качестве отдельных иллюстраций индивидуальных аспектов изобретения, и любой, который является функционально эквивалентным, входит в объем изобретения. Различные модификации моделей и способов по изобретению в дополнение к тем, которые описывают в настоящем описании, станут понятны специалистам в данной области из указанных выше описания и указаний, и аналогичным образом предназначены входить в объем изобретения. Такие модификации или другие варианты осуществления можно осуществлять на практике, не выходя за замки истинного объема и сущности изобретения.
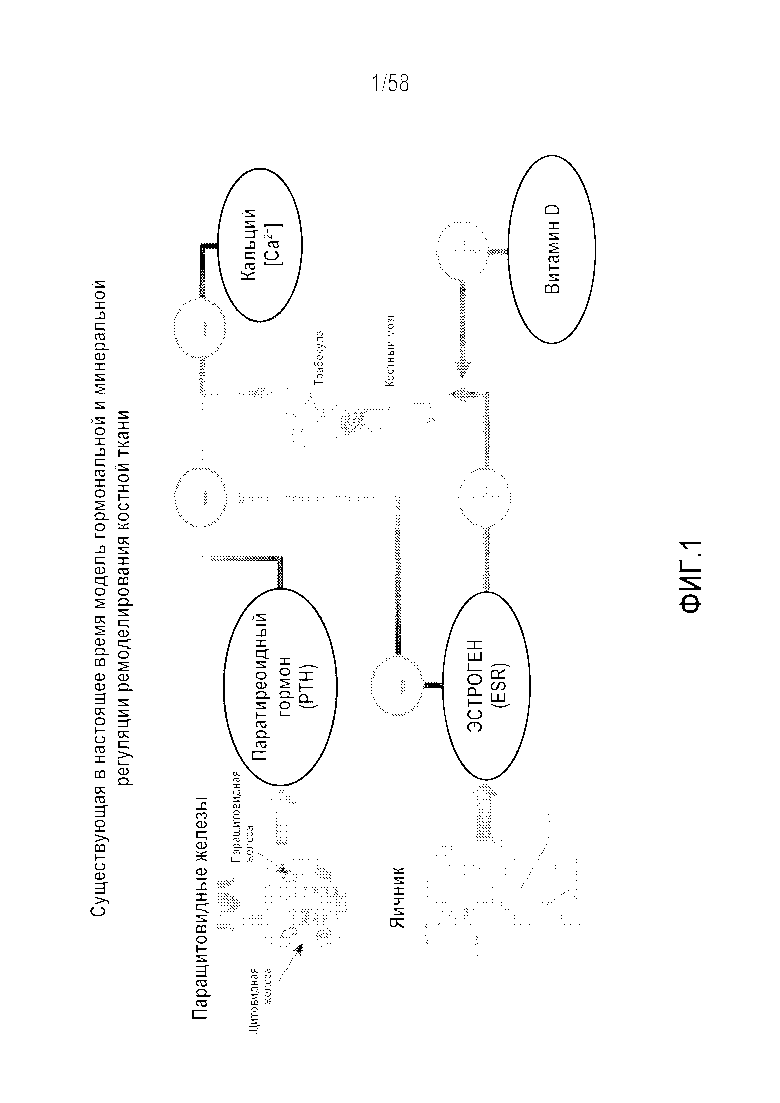
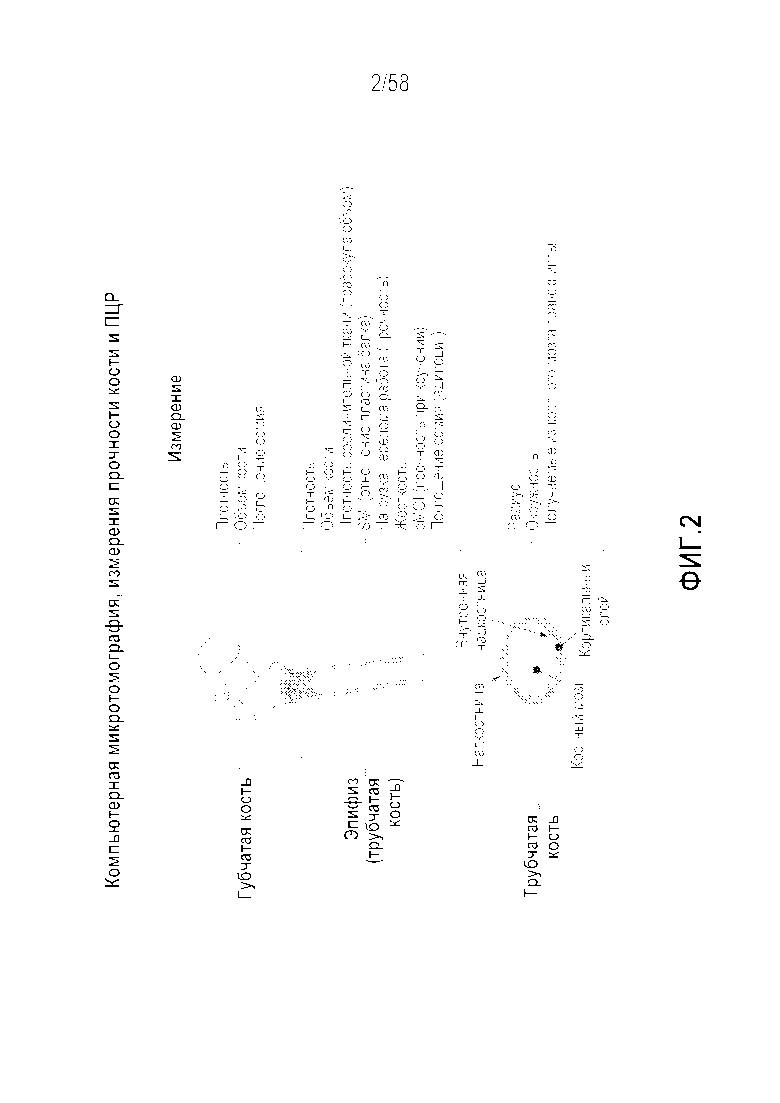




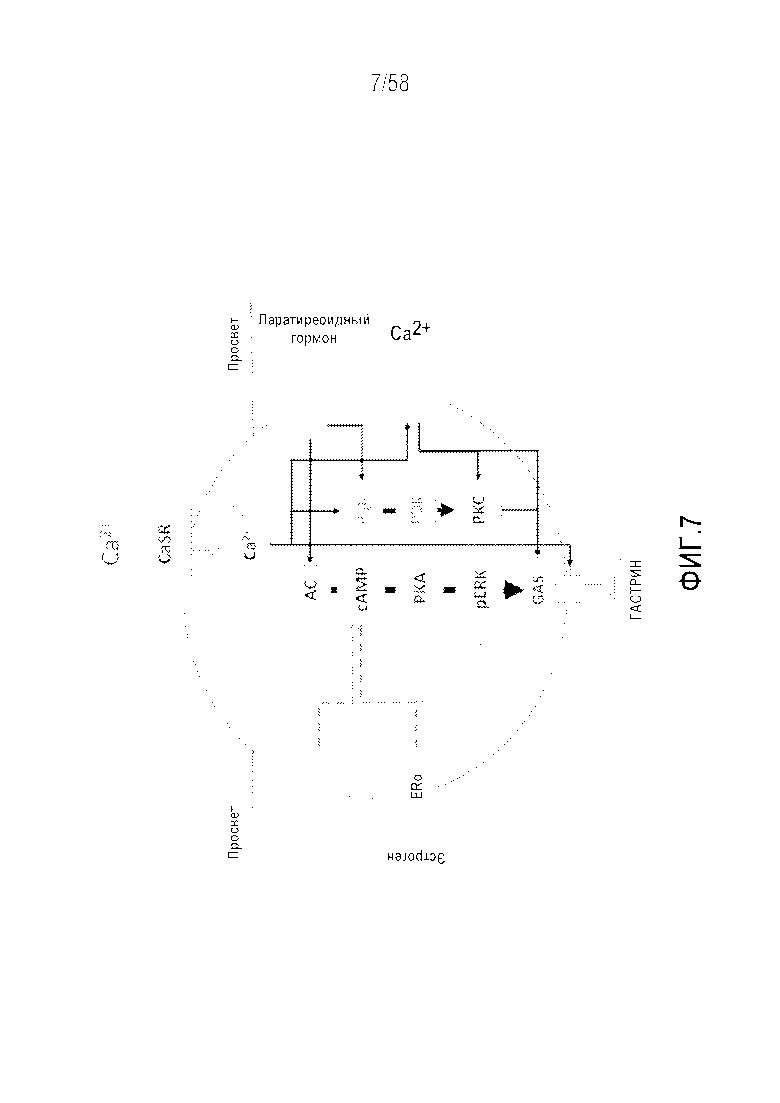
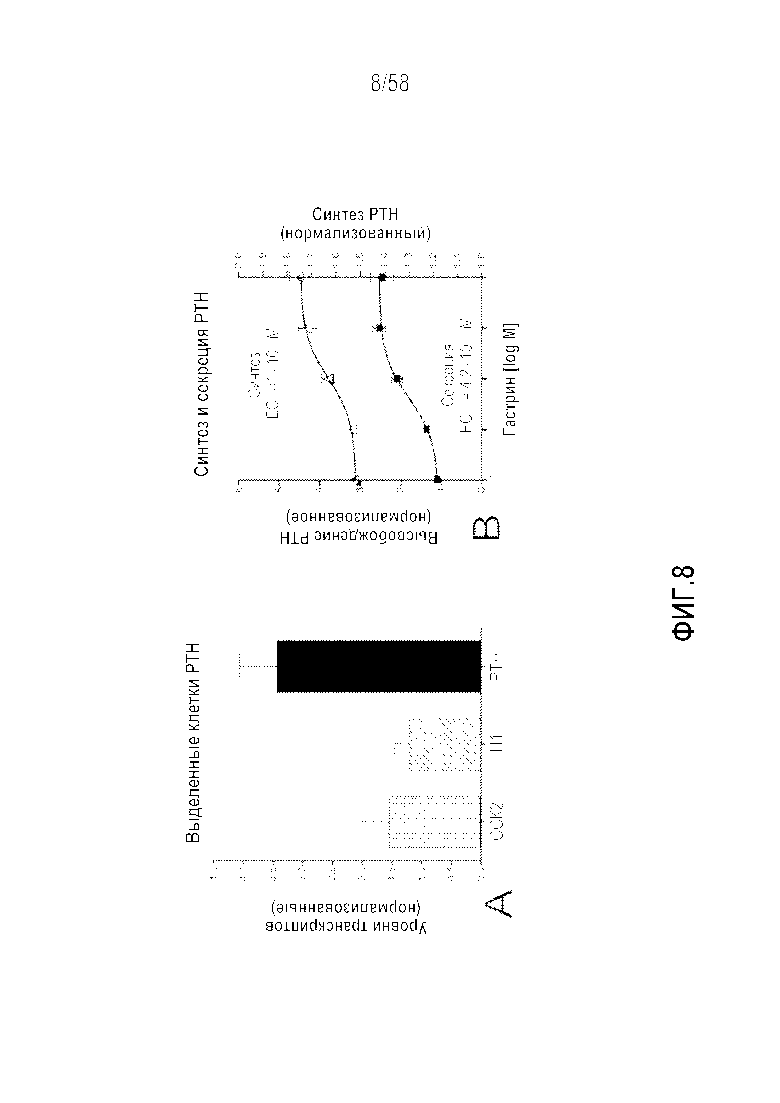
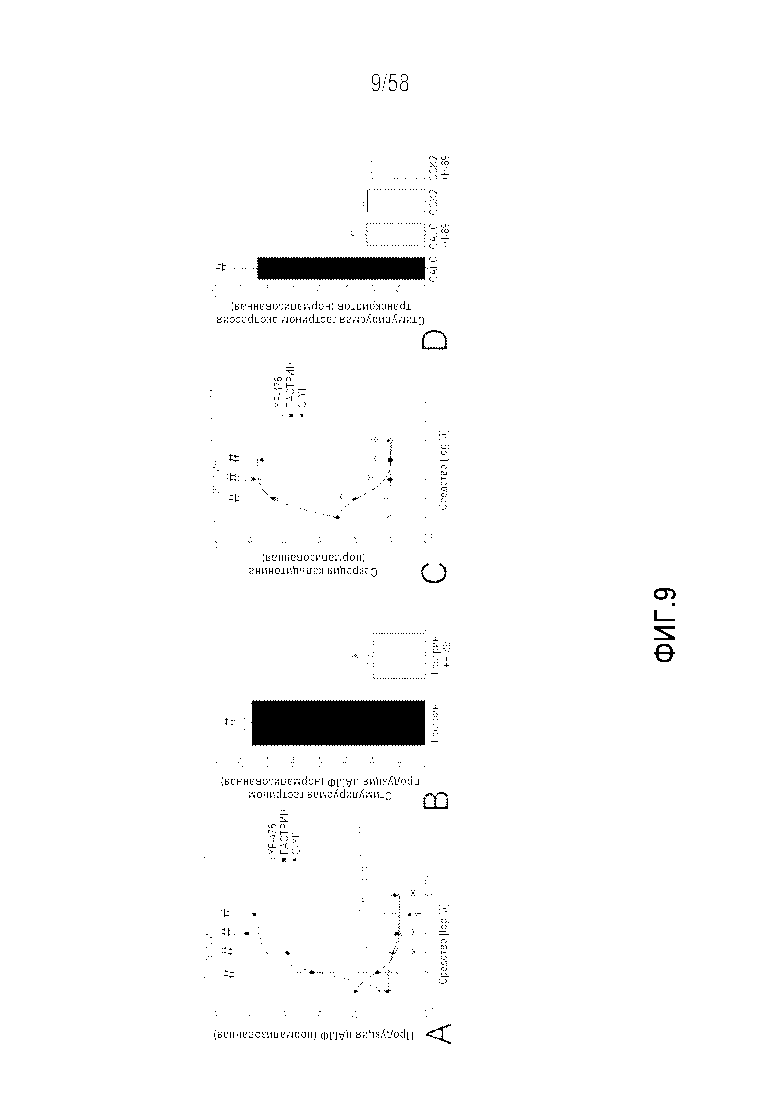






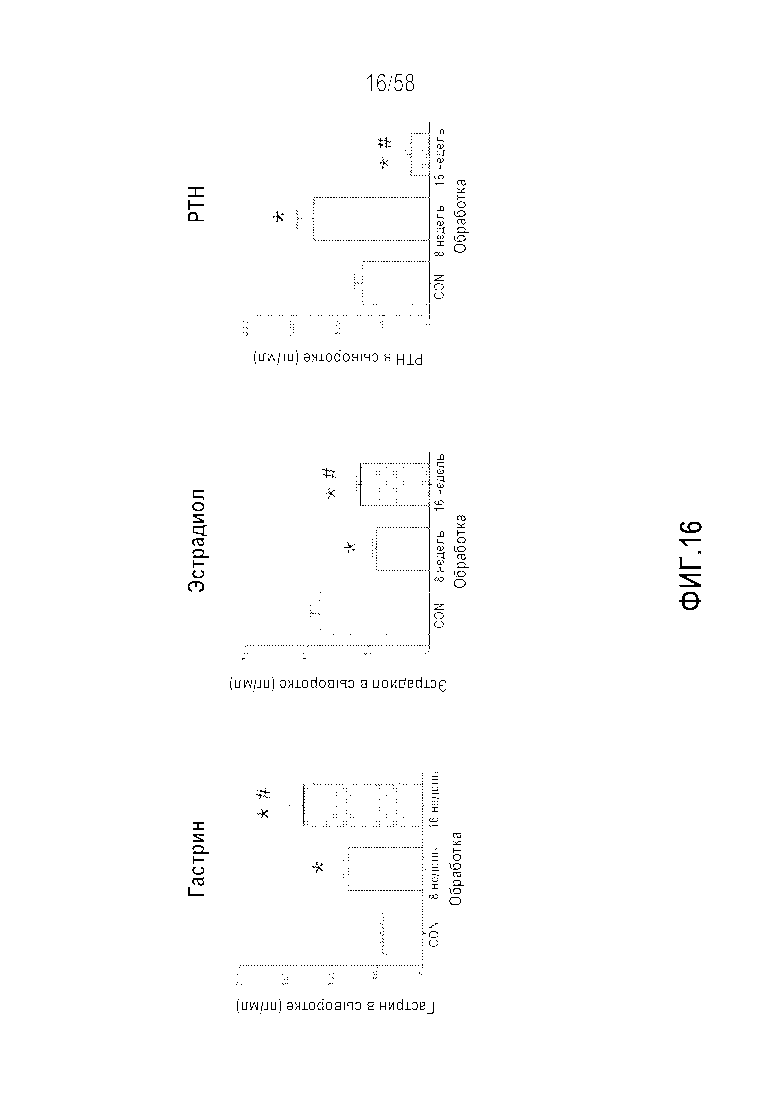
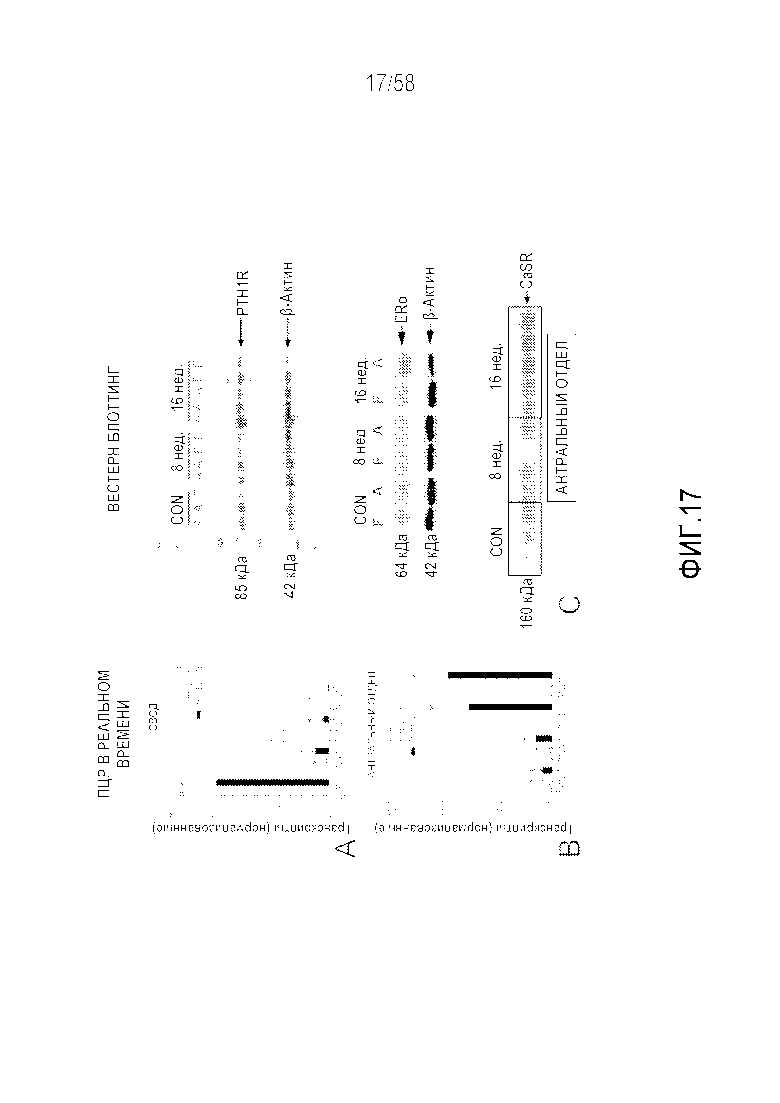

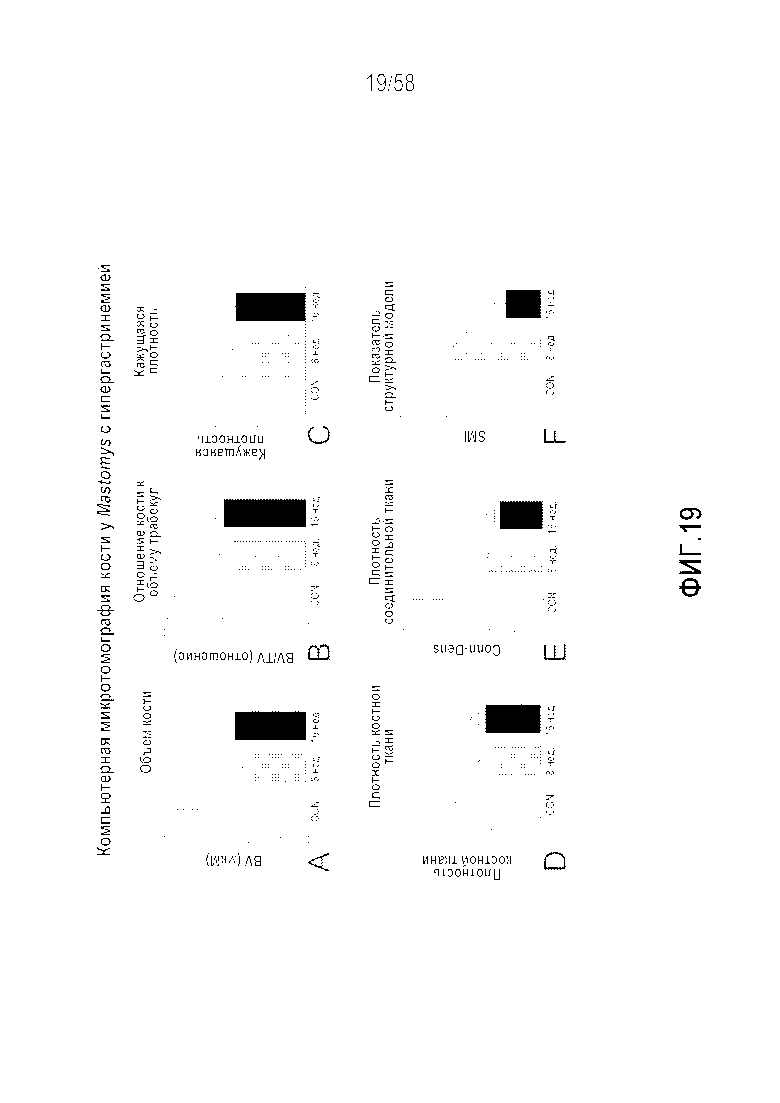





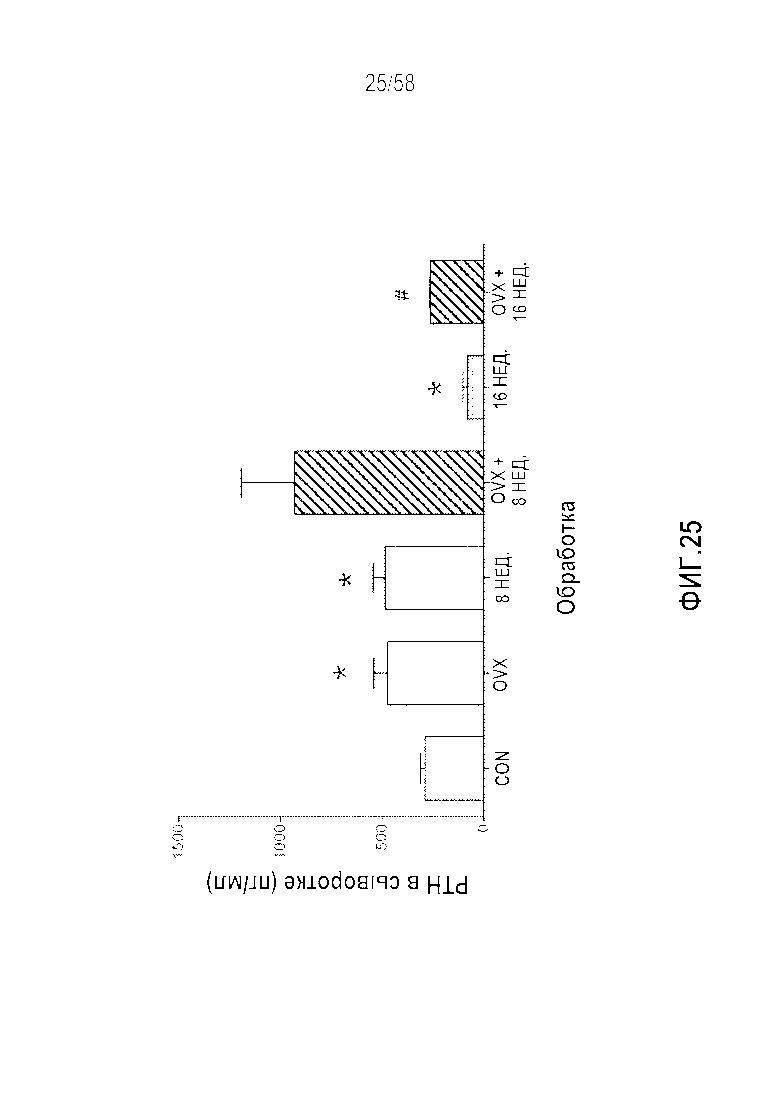
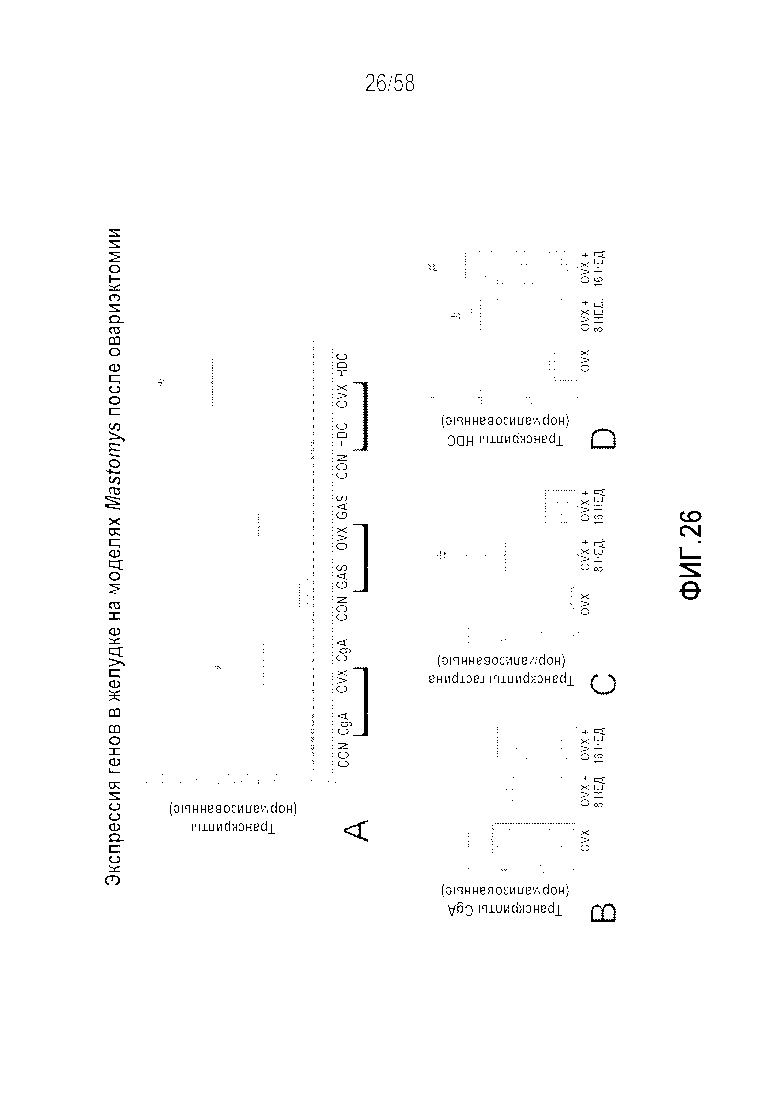
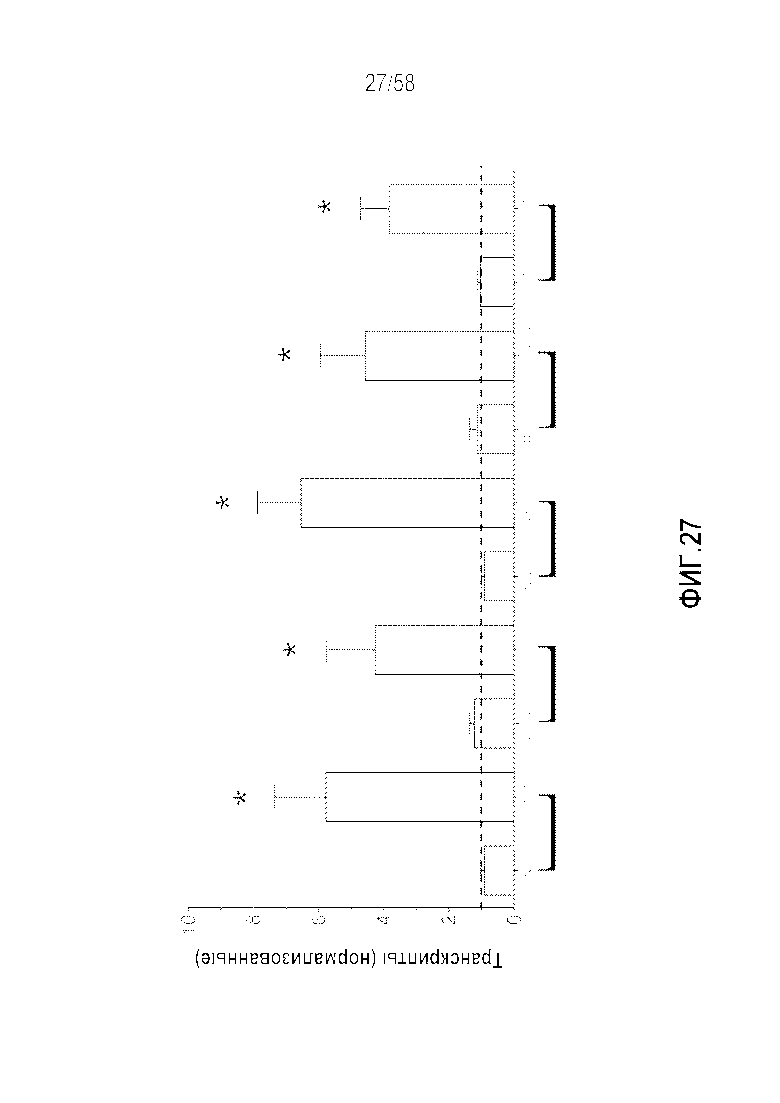
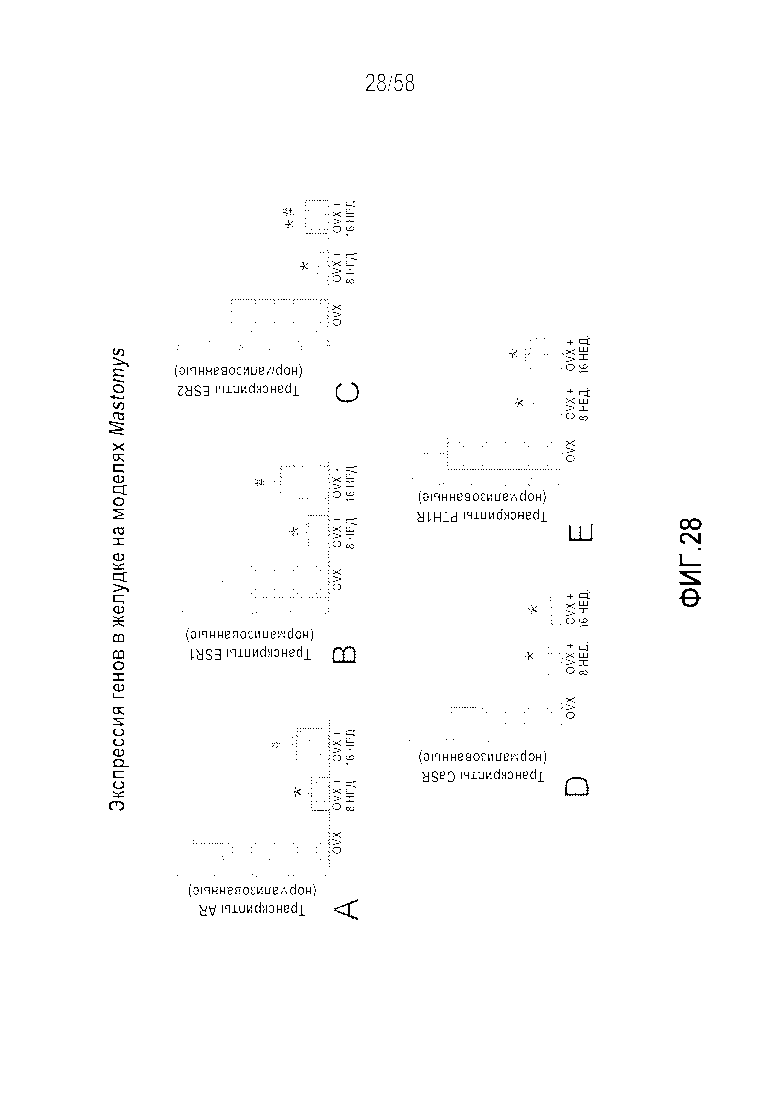



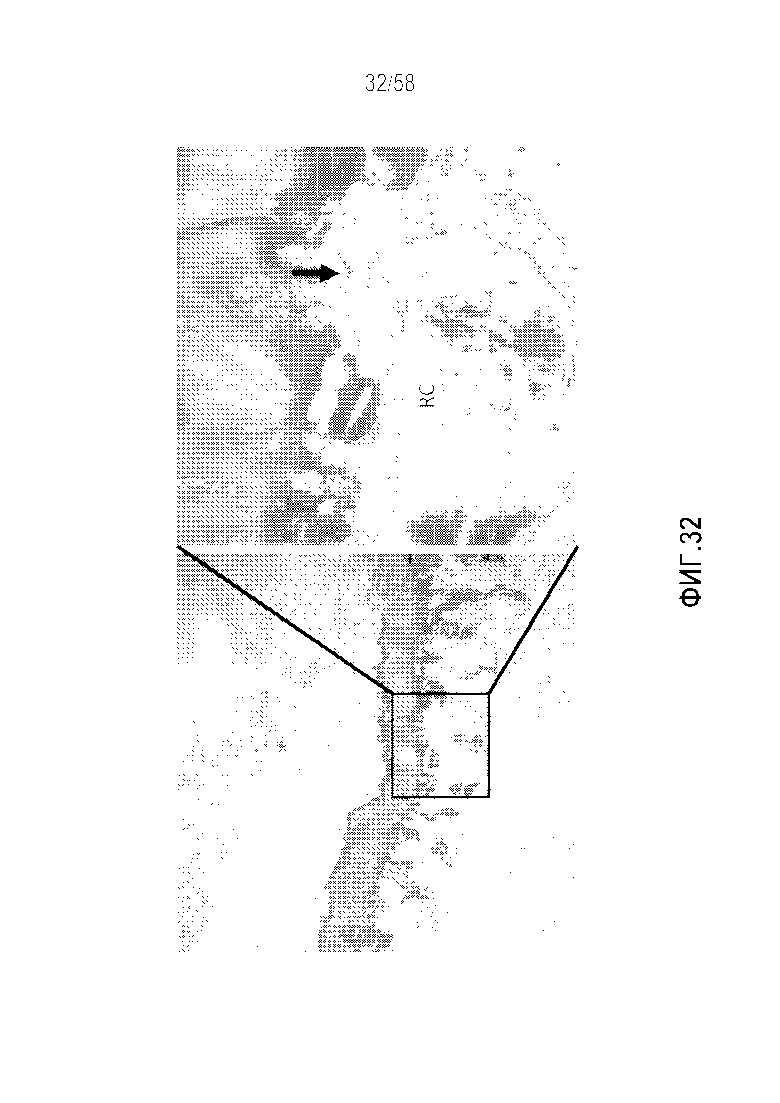



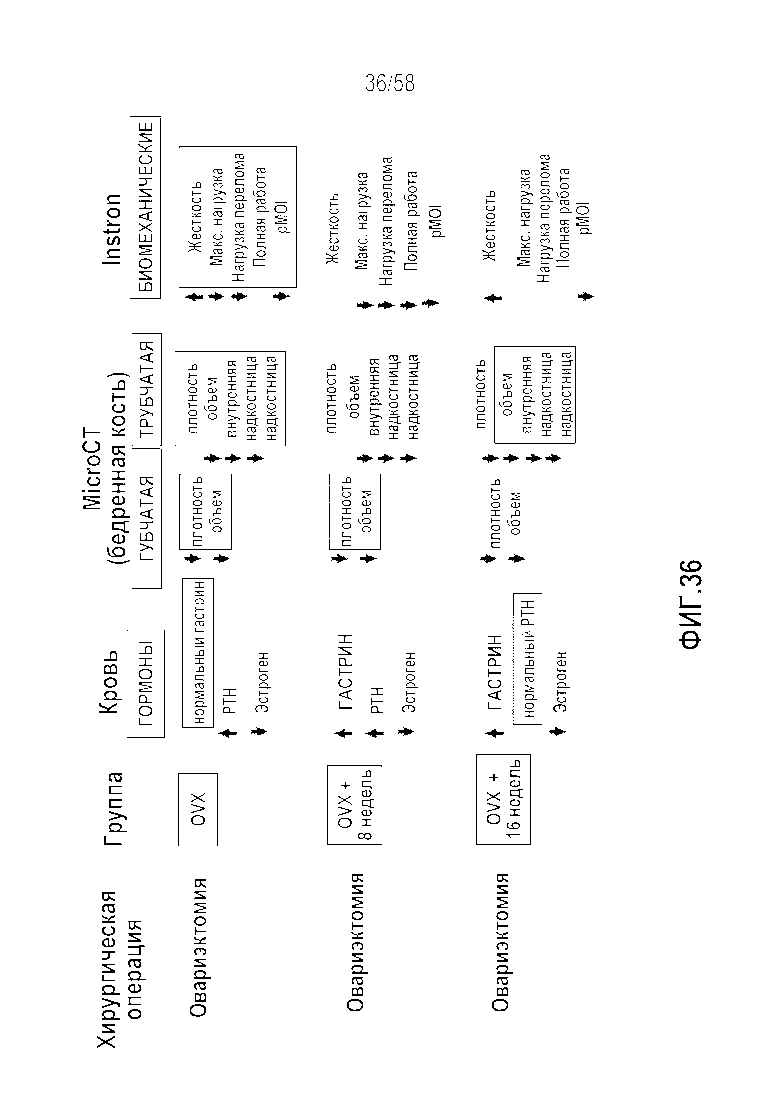
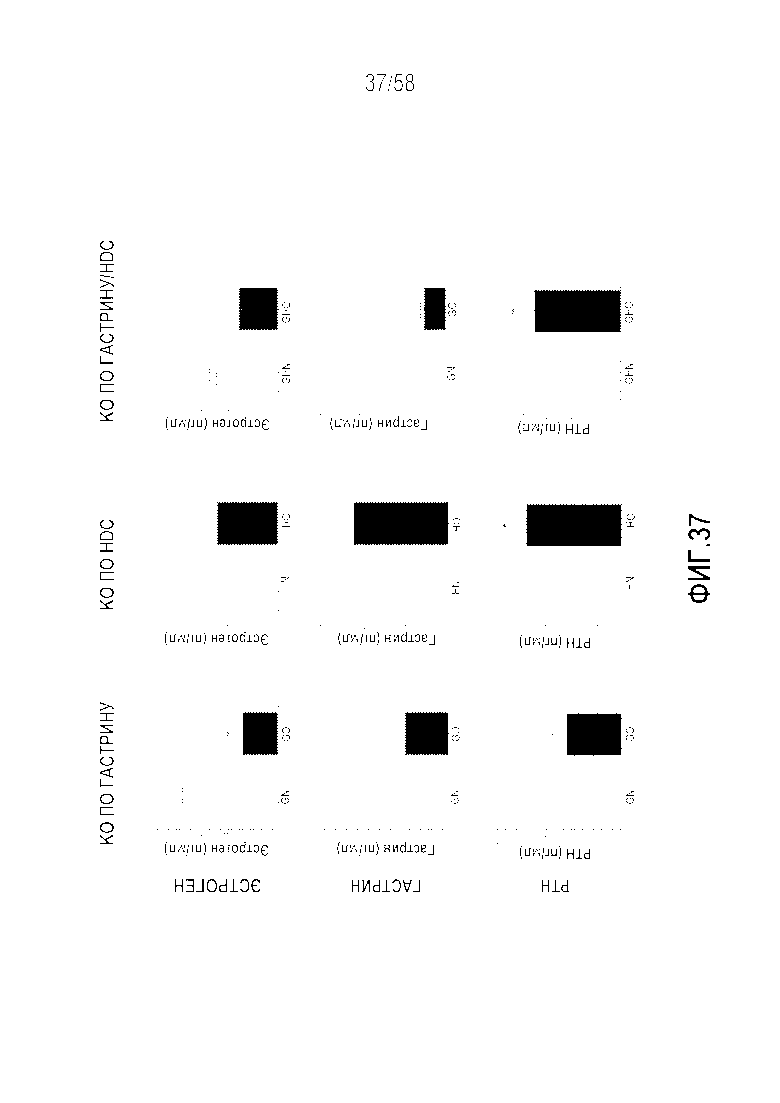
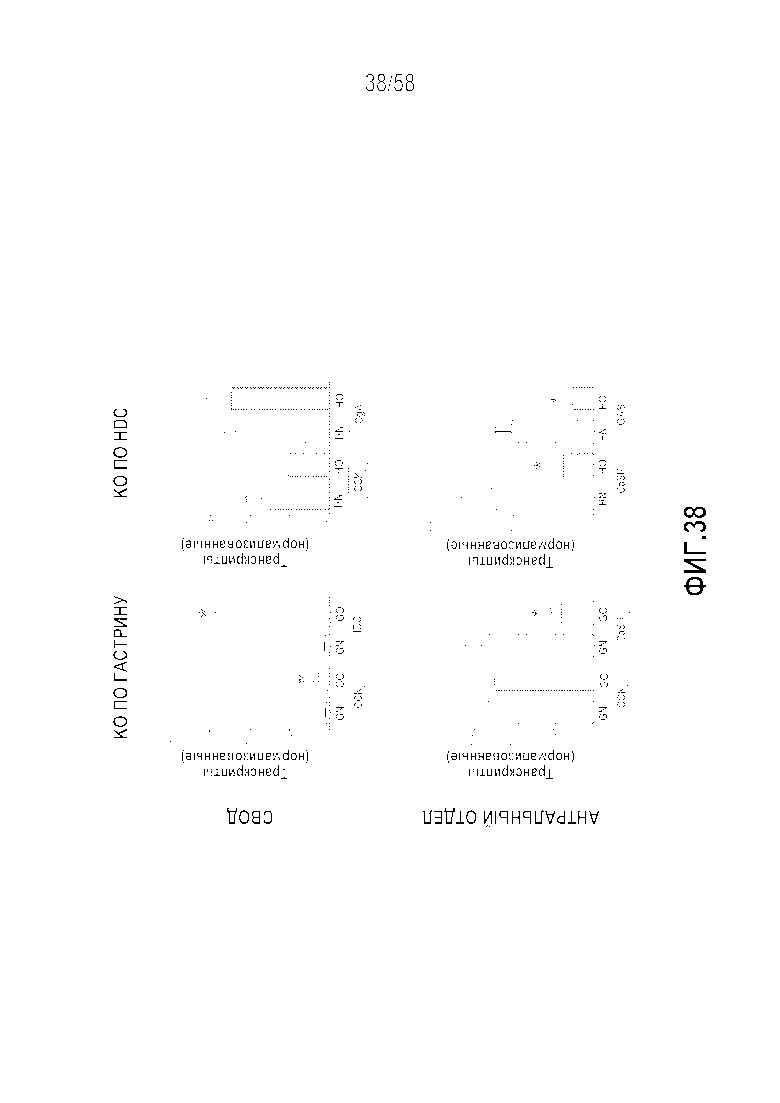
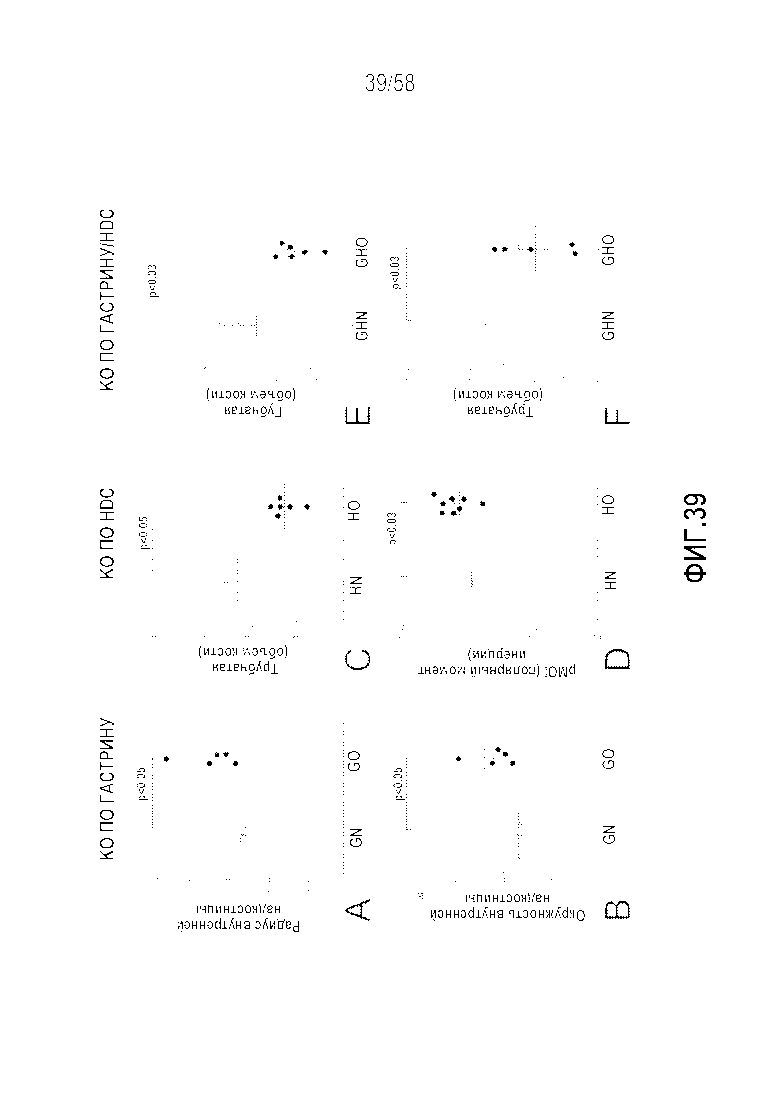

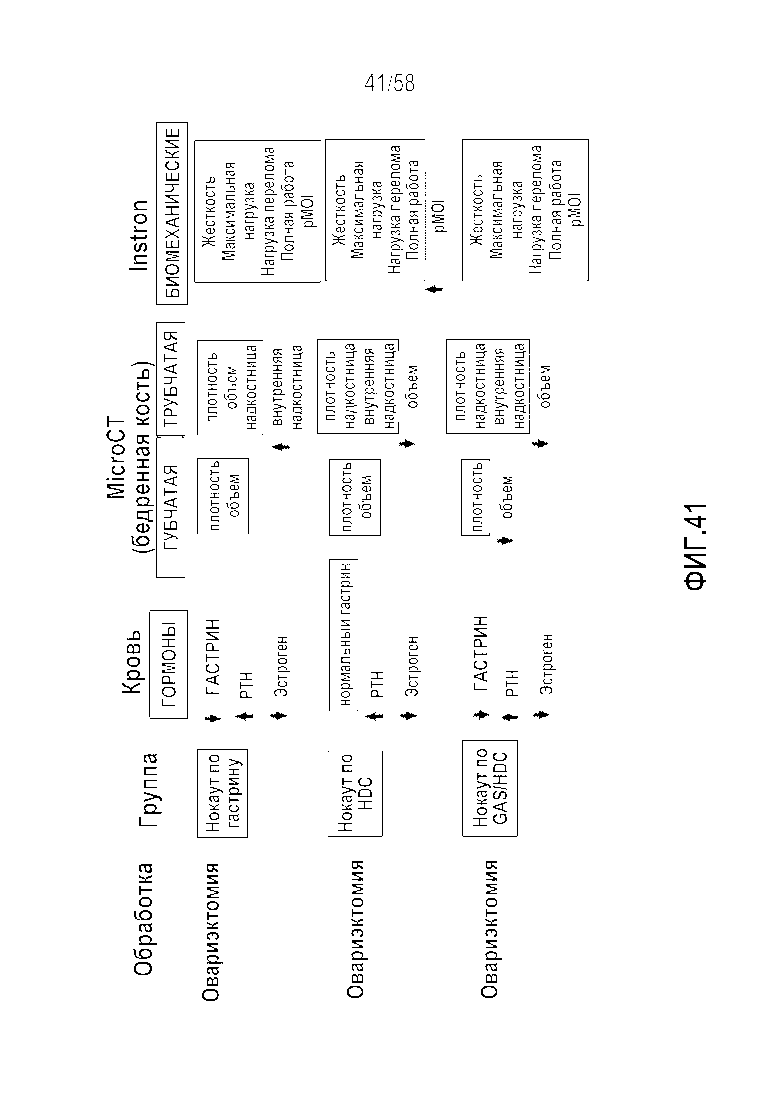

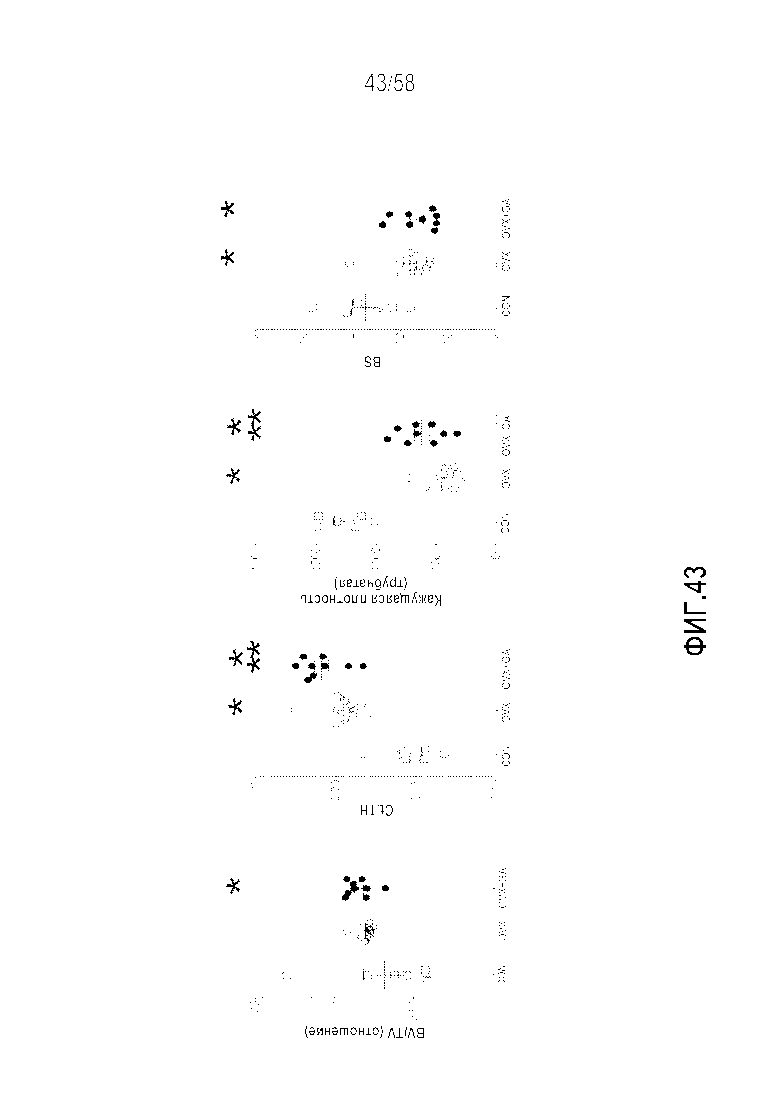


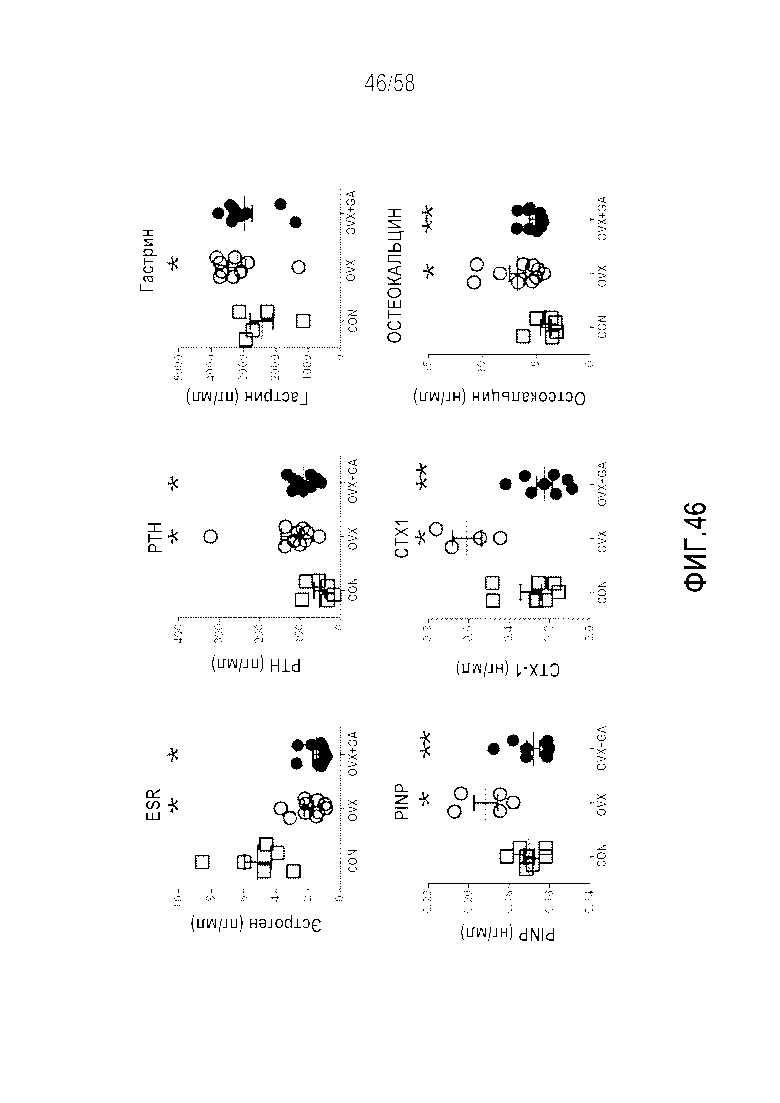
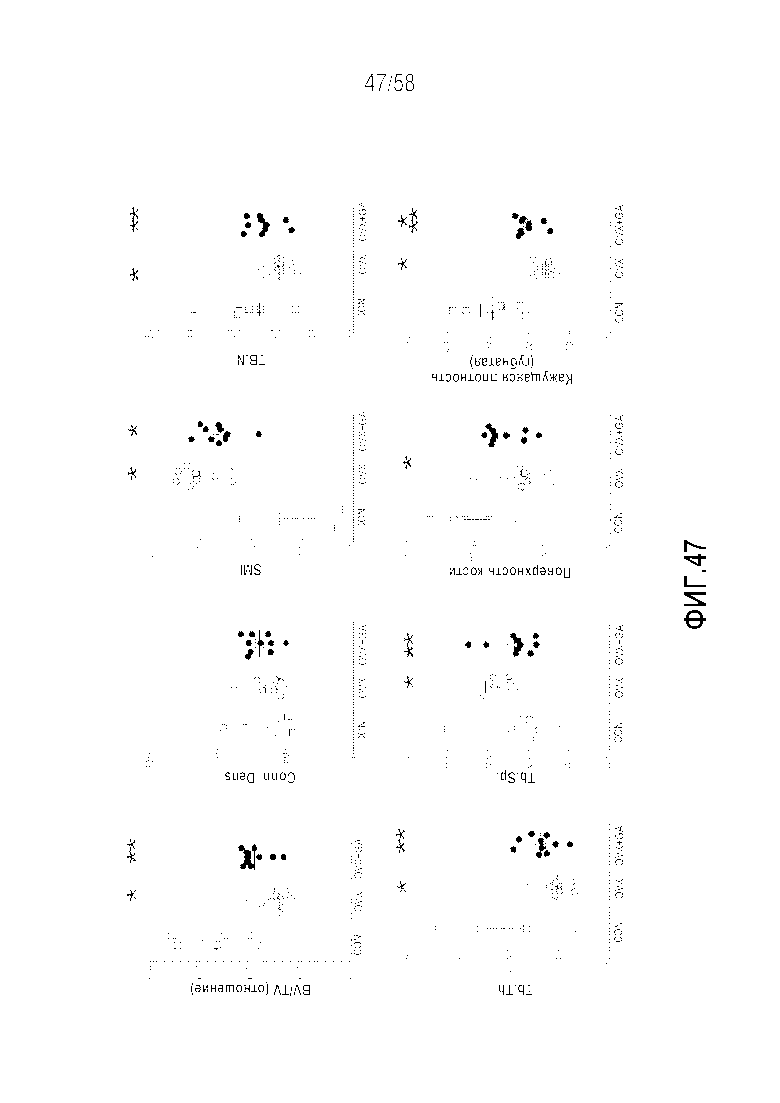
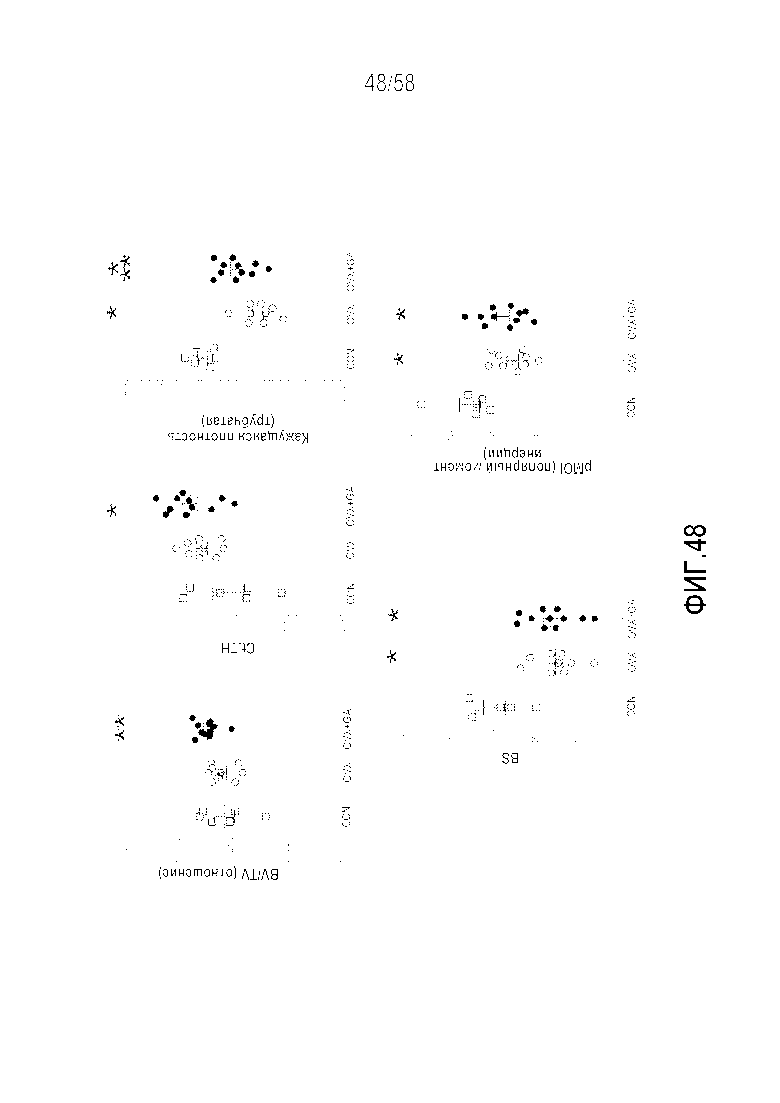




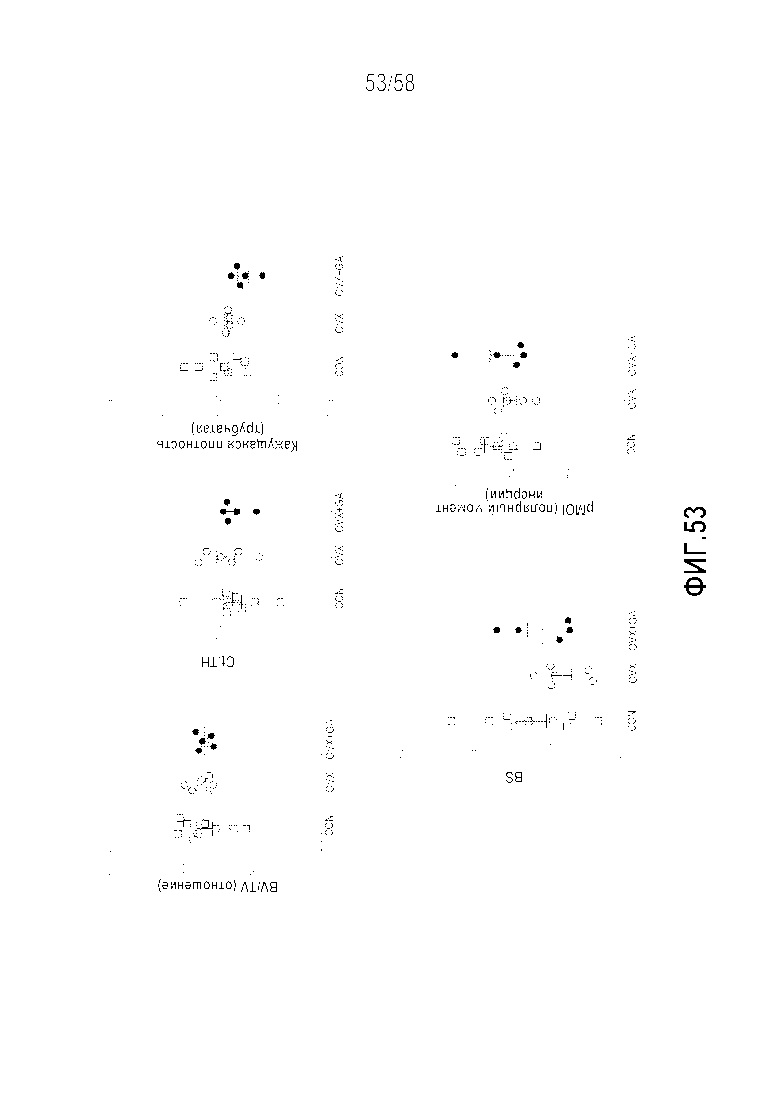
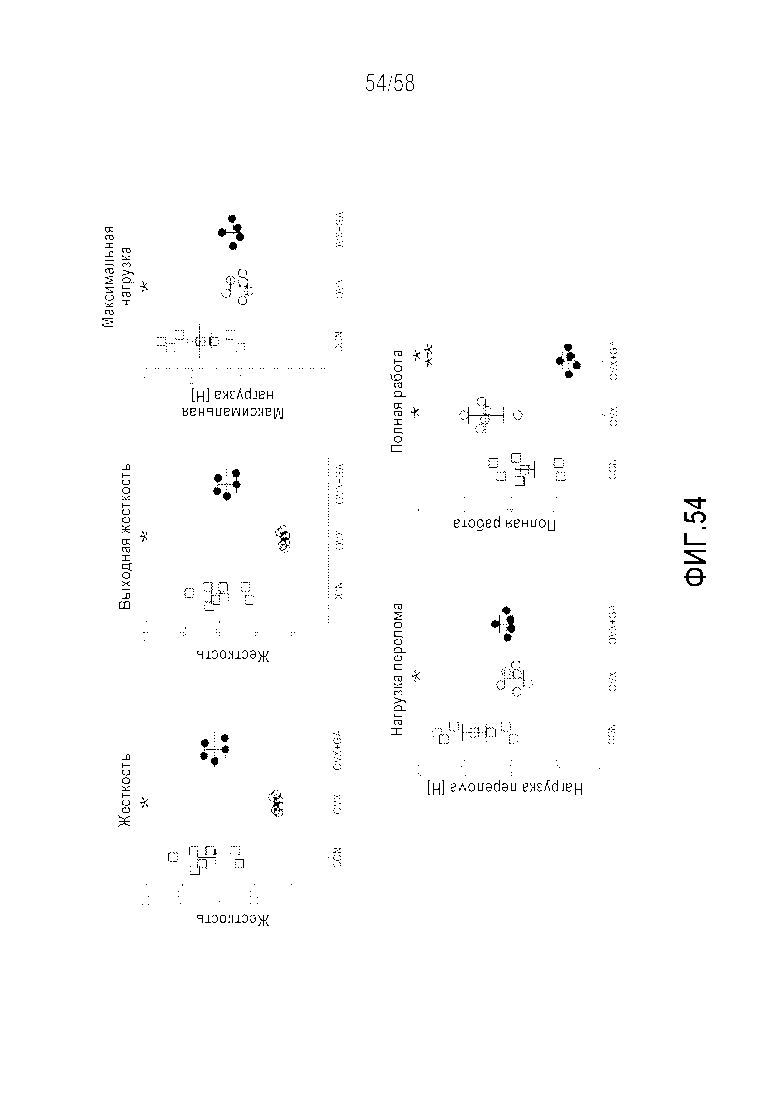
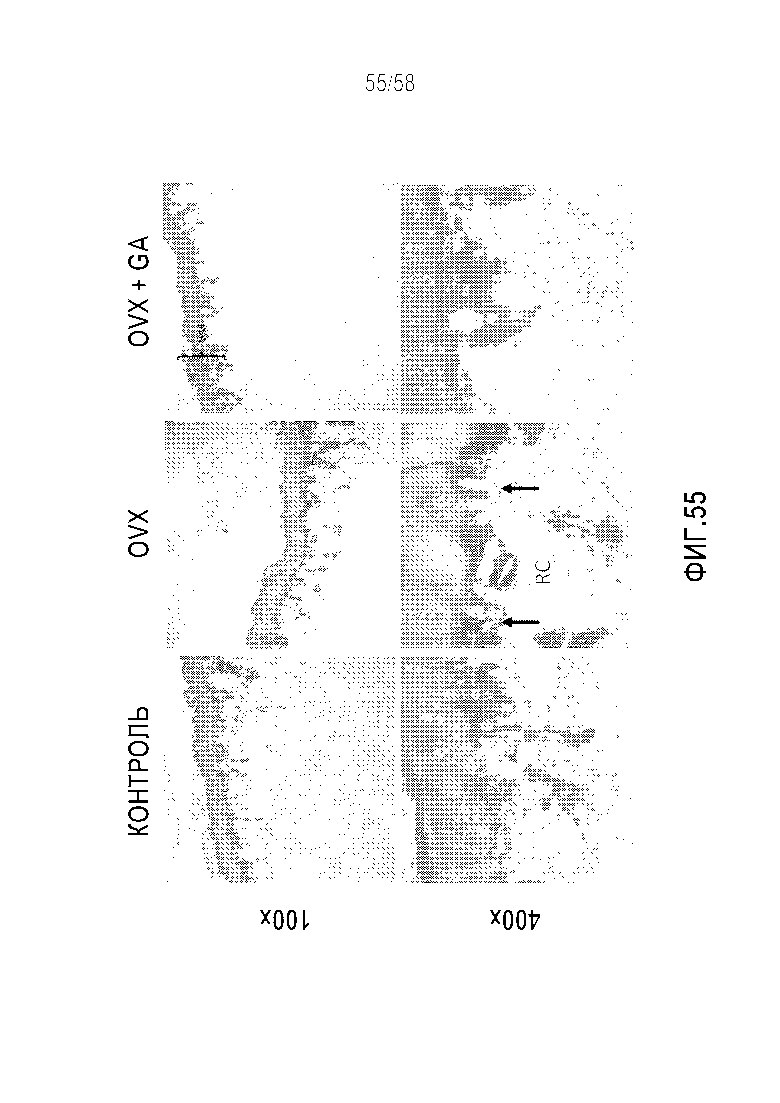

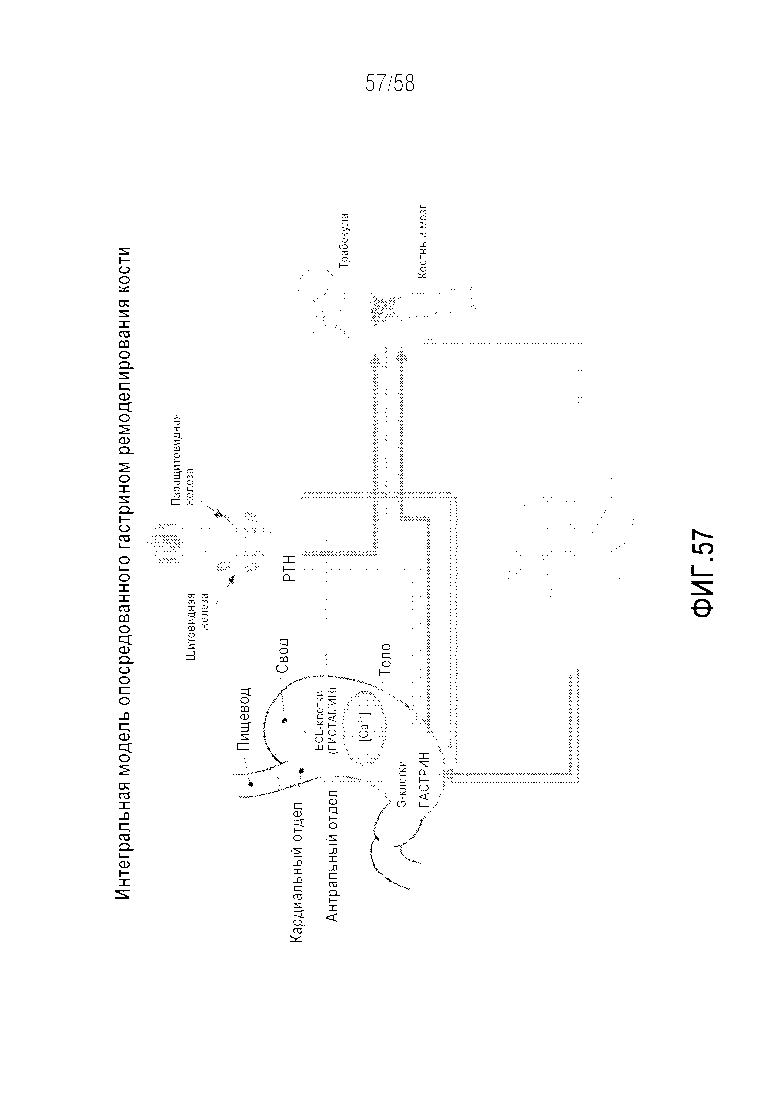

Настоящее изобретение относится к медицине, а именно к терапии, и касается лечения остеопороза, связанного с гипергастринемией. Для этого вводят эффективное количество YF476. Это обеспечивает повышение плотности костной ткани и, соответственно, прочности костей за счет селективного ингибирования рецепторов ССК2. 11 з.п. ф-лы, 58 ил., 15 табл., 8 пр.
1. Способ лечения остеопороза, связанного с гипергастринемией, у нуждающегося в этом индивидуума, включающий введение индивидууму по меньшей мере одной дозы терапевтически эффективного количества YF476, таким образом проводя лечение остеопороза.
2. Способ по п. 1, где YF476 вводят в течение периода времени лечения до разрешения остеопороза.
3. Способ по п. 1, где индивидуум представляет собой женщину со сниженной овариальной функцией или недостаточностью яичников.
4. Способ по п. 1, где индивидуум: (a) представляет собой женщину со сниженной овариальной функцией или недостаточностью яичников и (b) страдает гипергастринемией.
5. Способ по п. 1, дополнительно включающий введение YF476 с терапевтически эффективным количеством ингибитора протонной помпы (PPI) или антагониста рецепторов гистамина 2 (H2R) одномоментно или последовательно в любом порядке.
6. Способ по п. 1, где терапевтически эффективное количество YF476 представляет собой 10-25 наномоль.
7. Способ по п. 4, где гипергастринемия представляет собой неопластическую гипергастринемию или гипергастринемию, связанную с фармакотерапией, подавляющей кислоту.
8. Способ по п. 1, где терапевтически эффективное количество YF476 составляет 0,2-14 мкг/кг массы тела индивидуума.
9. Способ по п. 1, где YF476 вводят индивидууму в однократной дозе посредством подкожной инъекции.
10. Способ по п. 1, где YF476 вводят индивидууму посредством внутривенной инъекции.
11. Способ по п. 1, где YF476 вводят индивидууму перорально в дозе в диапазоне 20-100 мг.
12. Способ по п. 5, где PPI или антагонист H2R вводят перорально индивидууму.
| WO 2005007107 A2, 27.01.2005 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОСТЕОПОРОЗА У ЖЕНЩИН В ПЕРИОД МЕНОПАУЗЫ | 2007 |
|
RU2379043C2 |
| SCHINKE T | |||
| et al | |||
| "Impaired gastric acidification negatively affects calcium homeostasis and bone mass" | |||
| Nature Medicine, 2009, vol.15, no.6, pp.674-682 | |||
| BOYCE M | |||
| et al | |||
| Электрический аппарат для охраны касс, основанный на действии катодного реле | 1922 |
|
SU476A1 |
| Aliment Pharmacol Ther | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2019-07-03—Публикация
2014-11-21—Подача