Область техники, к которой относится изобретение
Настоящее изобретение относится к применению софорикозида для получения лекарственных средств для предотвращения и/или лечения дегенерации суставного хряща и остеоартрита у женщин после менопаузы.
Уровень техники
Остеоартрит (ОА) представляет собой наиболее распространенный тип остеоартроза у людей среднего и пожилого возраста. На наступление и развитие заболевания воздействуют многие факторы, такие как возраст, гормоны, окружающая среда и генетические факторы. Основными патологическими проявлениями заболевания являются дефекты хряща в синовиальном соединении. Заболеваемость среди женщин после менопаузы выше, чем у мужчин. У женщин с низким уровнем эстрогена риск остеоартрита повышен (Sower MR, McConnell D, Jahhausch M et al., Estradiol and its metabolites and their association with knee osteoarthritis Arthritis Theum. 2006, 8; 54(8): 2481-7). Это предполагает, что эстроген играет роль в патогенезе остеоартрита. Эстроген действует путем связывания с рецепторами эстрогена (ER) в суставах, которые экспрессируются в хряще и в субхондральной кости. Активность, конформация и уровень экспрессии ER в суставах являются важными факторами в патогенезе остеоартрита.
Рецепторы эстрогена представляют собой ядерные рецепторы, которые относятся к семейству рецепторов стероидных гормонов. Они локализованы в цитоплазме и ядре и обычно функционируют по способу, сходному со способом действия зависимого от лиганда фактора транскрипции. Они прямо взаимодействуют с гомологичной последовательностью ДНК путем связывания с районом промотора гена-мишени или взаимодействует с другими факторами транскрипции путем белок-белкового взаимодействия. Дополнительно, из-за наличия быстрого ответа отдельных клеточных систем на эстроген недавно высказано предположение о его негеномном действии.
ER включает два подтипа, а именно рецептор эстрогена-α и рецептор эстрогена-β. Ген рецептора эстрогена-α находится на хромосоме 6q25-27, содержащей 8 экзонов размером 140 kb (тысяч оснований). Ген рецептора эстрогена-β находится на хромосоме 6q22-24, содержащей 8 экзонов размером примерно 40 kb.
Половые гормоны играют важную роль в поддержании массы костной ткани у человека. Связанное с возрастом и операциями снижение половых гормонов может привести к потере костной массы, приводящей к остеопорозному перелому кости. У пожилых женщин после менопаузы часто обнаруживается остеопороз, который с трудом поддается лечению. В современном обществе при старении популяции количество пожилых женщин возрастает. Среди женщин с увеличенной потерей костной массы (или даже с остеопорозом) при пониженном уровне эстрогена в кровотоке высок риск перелома кости, что приводит к повышенной смертности в результате остеопороза, перелому костей и различным осложнениям.
Ранее Ham и соавторы описали модель с применением овариэктомированных макак яванских. 180 Пар обезьян делили на три группы, где одна группа представляла собой модельную группу и две другие группы получали эстрогенозаместительную терапию (ERT) и полученный из сои фитоэстроген (SPE). Через три года в модельной группе наблюдается больше дефектов хряща и остеоцитов по сравнению с группой, получавшей эстрогенозаместительную терапию, указывает на возможность облегчения остеоартрита с помощью продолжительной эстрогенозаместительной терапии. В суставном хряще определяли уровни белка, связывающего инсулиноподобный ростовой фактор (IGFBR)-2, IGFBR-3, коллагена и протеогликана, и обнаружили, что уровни IGFBR-3 в группе, получавшей эстрогенозаместительную терапию, выше, чем в модельной группе, и результаты других измерений в группе, получавшей терапию, не проявляли статистически достоверных отличий от модельной группы.
Измеряли индексы оборота костной ткани для района субхондральной кости (SC) и метафиза (ЕМС) проксимального конца большой берцовой кости. Обнаружено, что индексы для обоих районов были наивысшими в модельной группе, и таковые индексы в группе, получавшей выделенный из сои фитоэстроген, были на следующем месте, а индексы в группе, получавшей эстрогенозаместительную терапию, были наименьшими. В модельной группе степень окостенения SC района была выше, чем ЕМС района. Объем трабекулярной кости выше в группе, получавшей выделенный из сои фитоэстроген, чем в модельной группе, что указывает на возможность понижения риска остеоартрита путем уменьшения остеогенеза в SC районе в результате применения продолжительной эстрогенозаместительной терапии. Недавно та же группа исследователей путем измерения (числа?) остеоцитов в районе проксимального сустава большой берцовой кости показала, что продолжительная эстрогенозаместительная терапия не может непрерывно уменьшать образование остеоцитов на границе раздела хряща и кости и около большеберцовых суставов (Olson EJ, Lindgren BR, Carlson CS et al., Effects of long-term estrogen replacement therapy on the prevalence and area of periartricular tibial osteophytes in surgically postmenopausal cynomolgus monkeys. Bone, 2007). Из эпидемиологических данных можно видеть, что патогенез ОА связан с биомеханическим изменением костей, происходящими в результате уменьшения костной массы у женщин после менопаузы. Совсем недавно Jacobsen и соавторы провели измерение плотности кости и бедренной суставной щели у отобранных 3913 пациентов с остеоатритом (1470 мужчин и 2443 женщин) и обнаружили, что суставная щель мало изменяется за время жизни мужчин, но она значительно сужается после 45 лет у женщин, что в значительной степени коррелирует с уменьшением костной массы (р<0,0001) (Jacobsen S, Jensen TW, Bach-Mortensen P et al., Low bone mineral density is associated with reduced hip joint space width in women: results from Copenhagen Osteoarthritis Study. Menopause, 2007).
Многие исследования постулируют, что эстрогены оказывают действие на хондроциты in vivo и in vitro, что коррелирует с уровнем экспрессии рецепторов эстрогена. Телопепдид коллагена типа II (СТХ-II) является специфическим катаболитом коллагена типа II in vivo. Поскольку большая часть коллагена типа II in vivo наличествует в хряще, CTX-II в крови и моче может применяться в качестве маркера, специфичного для катаболизма хряща. По сообщениям, это индикатор применяют во многих исследования. Andersen и соавторы измеряли уровни CTX-II в образцах мочи, полученных от крыс через 2, 4, 6, 8 недель после овариэктомии, относительно уровня до овариэктомии. Обнаружено, что хрящ караболизируется наиболее быстро через 2 недели и более медленно после этого. Катаболизм хряща ингибируется ERT и модулятором рецептора эстрогена (SERM) через 2 недели. Катаболизм хряща через 4 недели, в основном, коррелирует с дегенерацией коленного суставного хряща через 8 недель (Hoegh-Andersen P, Tanko LB, Andersen TL et al., Ovariectomized rats as a model of postmenopausal osteoarthritis: validation and application Arthritis Res Ther. 2004, 6(2), R169-80, 2004).
Недавно Oestergard и соавторы определили уровни CTX-II в крови, оценили морфологические изменения суставов через 9 недель и определили внутрисуставные уровни CTX-II с помощью иммуногистохимиии у 46 крыс SD, которые были сгруппированы в 4 группы, а именно модельная группа с овариэктомией, группа, получавшая раннюю ERT, группа, получавшая ERT с запозданием, и группа после ложной операции. Результаты показали, что ERT может ослаблять дегенерацию суставного хряща, в группе, получавшей ERT с запозданием, эффект был слабее, чем в случае более раннего вмешательства, CTX-II определяли внутрисуставно, и они были совместно локализованы в дефектах хряща (Oestergaard S, Sondergaard ВС, Hoegh-Andersen P, et al.. Effects of ovariectomy and estrogen therapy "on type II collagen degradation and structural integrity of articular cartilage in rats: implications of the time of initiation, Arthritis Rheum. Aug. 2006; 54(8):2441-51). Показано, что уровень экспрессии ER в суставном хряще уменьшается после овариэктомии (см., например, Oshima Y, Matsuda К, Yoshida A, et al.. Localization of Estrogen Receptors alpha and beta in the Articular Surface of the Rat Femur. Acta Histochem Cvtochem. Feb. 27, 2007; 40(1):27-34; and Dai G, Li J, Liu X, et al., The relationship of the expression of estrogen receptor in chondrocyte and osteoarthritis induced by bilateral ovariectomy in guinea pig, J. Huazhong Univ Sci Technolog Med Sci. 2005; 25(6):683-6). Показано, что экспрессия матрикеных металлопротеиназ (ММР) увеличивается в шейке матки после менопаузы, и поэтому экспрессия тканевого ингибитора (TIMP) подавляется. ММР важен для разрушения коллагена суставного хряща. Lee и соавторы обнаружили, что 17β-E2 может ингибировать экспрессию мРНК ММР-1 в хондроцитах и улучшать гомеостаз между ММР и TIMP (Richette P, Dumontier MF, Francois M, et al., Dual effects of 17-beta-oestradiol on interleukin 1 beta-induced proteoglycan degradation in chondrocytes, Ann Rheum Pis. Feb. 2004; 63(2):191-9), Поэтому повышенный катаболизм коллагена типа II и разрушение хрящевого матрикса являются результатом пониженного уровня эстрогена, пониженной экспрессии ER и повышенной экспрессии ММР.
Эти эксперименты на животных позволяют считать, что флуктуации уровня эстрогена могут быть одной из причин остеоартрита среди женщин после менопаузы. Раннее введение эстрогена функционирует как ингибирование наступления ОА путем уменьшения уровня ER в хряще. Поздняя ERT ингибирует наступление остеоартрита и ослабляет развитие остеоартрита путем регуляции метаболизма субхондральной кости.
Эстроген оказывает воздействие на суставный хрящ по зависимому от дозы способу, что исследовано, в основном, в опытах in vitro. Многие считают, что низкие дозы эстрогена могут ингибировать разрушение хрящевого матрикса, индуцированное воспалительными цитокинами, а высокие дозы эстрогена могут способствовать дегенерации хряща. IL1-β представлен как про-воспалительный фактор при патогенезе остеоартрита. Richette и соавторы путем культивации суставных хондроцитов кролика показали, что низкая концентрация 17-β-эстрадиола (Е2) (0,1 нмоль/л) ингибирует разрушение протеогликана, индуцированное интерлейкином (IL) 1β, а высокая концентрация (10 нмоль/л) усиливает его действие (Lee YJ, Lee ЕВ, Kwon YE, et al., Effect of estrogen on the expression of matrix metalloproteinase (MMP)-l, MMP-3, and MMP-13 and tissue inhibitor ofmetalloprotemase-1 in osteoarthritis chondrocytes Rheumatol Int. 2003 Nov; 23(6):282-8. April 9, 2003).
Рецепторы, узнающие последовательности ДНК, сходные с таковой для рецептора эстрогена, и лиганды которых не идентифицированы, известны как рецепторы, родственные рецепторам эстрогена, относящиеся к группе так называемых ядерных рецепторов-«сирот». Они представляют собой ERR-α, ERR-β и ERR-γ (известные также как NR3B1, NR3B2 и NR3B3, соответственно, согласно номенклатуре ядерных рецепторов от 1999). Экспрессия этих рецепторов ускоряется эстрогеном в отдельных тканях. Обнаружено, что ERR-α может функционировать при регуляции передачи сигнала эстрогена и взаимодействовать с ER. Bonnelye et al. обнаружили экспрессию ERR-α в суставных хондроцитах взрослых крыс с помощью иммуногистохимии, повышенную экспрессию SOX-9 и ускоренное развитие хряща, индуцированное повышенной экспрессией ERR-α в культуре хондроцитов, и подавление образования хряща, индуцированное ингибированием экспрессии ERR-α. Эти данные указывают на то, что ERR-α играет роль в образовании хряща и поддержании гомеостаза хряща (Bonnelye E, Zimgibi RA, Jurdic P, et al., The orphan nuclear estrogen receptor-related receptor-alpha regulates cartilage formation in vitro: implication ofSox9 Endocrinology March 2007, 148(3):1195-205).
В итоге эстроген и его рецептор оказывают воздействие на патогенез и развитие остеоартрита. Рецептор эстрогена экспрессируется в суставном хряще и субхондральной кости. Активность белка и конформация эстрогена могут влиять на суставный хрящ и субхондральную кость. Генетический полиморфизм связан с патогенезом остеоартрита. К настоящему моменту в ряде исследований показано, что модулятор рецептора эстрогена может функционировать как эстрогенозаместительная терапия и эстроген может ускорять экспрессию своего рецептора, указывая на то, что действие эстрогена на остеоартрит опосредуется рецептором эстрогена. Заболеваемость остеоартритом повышена среди женщин после менопаузы, и эпидемиологическое свидетельство действия эстрогенозаместительной терапии не является достаточным. Механизм действия эстрогена и его рецептора на остеоартрит неясен, и его необходимо дополнительно иллюстрировать.с помощью более перспективных эпидемиологических наблюдений, а также с помощью дополнительных опытов in vivo и in vitro.
Дополнительно, прием эстрогена также связан со многими побочными эффектами, и самым серьезным побочным эффектом является повышенный риск развития рака груди и рака эндометрия.
Поэтому в данной области техники есть потребность в поиске лекарственного средства для лечения остеоартрита без повышения риска развития рака груди и рака эндометрия.
Генистеин представляет собой изофлавоновое соединение, присутствующее у растений. У различных растений оно присутствует в форме агликона или гликозида. В форме гликозида сахарид, образующий гликозидную связь с кислородом, может быть моносахаридом, таким как глюкоза или неогесперидоза, и глюкозилапиозидом. Сахаридная цепь может представлять собой одну цепочку в положении 7 или 4′ или две цепочки в положениях 7 и 4'. Или углерод-гликозидная связь может находиться в положении 8 или 6, 8. Генистеин-4′-O-глюкопиранозид, известный также как софорикозид, генистеин-7-О-глюкопиранозид или генистин являются наиболее распространенной формой гликозидов.
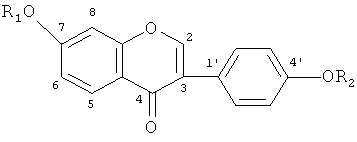
Генистин представляет собой один из активных ингредиентов соевых бобов, относящийся к изофлавонам. Согласно сообщениям 1953 г., он обнаруживается в остатке (жмыхе) соевых бобов, применяемом для кормления крупного рогатого скота. Эстрогеноподобная активность, присущая генистину, приводит к повышению веса тела крупного рогатого скота.
В последние годы дополнительно обнаружено, что этот изофлавон, присутствующий в соевых бобах, может применяться для уменьшения риска рака груди среди женщин после менопаузы и ингибирует рост опухоли мочевого пузыря и раннее развитие рака простаты у крыс. Недавно показано, что экстракт соевых бобов, содержащий генистин, можно применять не только в качестве эстрогеноподобного агента, а также для ингибирования интестинального поглощения глюкозы, что могло бы в этой связи применяться при диабете, и в качестве защитного агента против перекисного окисления липидов, индуцированного глюкозой. Дополнительно, бедренно-метафизарные ткани, полученные от пожилых самок крыс, тестируют in vitro. Результаты демонстрируют, что генистин или генистеин значительно повышают содержание щелочной фосфатазы, ДНК и кальция в бедренно-метафизарных тканях, указывая на то, что эти соединения воздействуют на синтез кости. Одновременно генистин можно применять для предотвращения потери костной массы у овариэктомированных крыс.
Софорикозид получают из плодов растения Sophora japonica L. семейства Leguminosae. Его применение распространено в китайской традиционной медицине. Софорикозид обнаружен также в стеблях Piptanthus nepalensis и листьях Schinus latifolius семейства Anacariaceae. Софорикозид обладает противовоспалительным действием, он может ингибировать пролиферативную фазу воспалительного процесса и уменьшать действие глутамат-пируваттрансаминазы. Недавно показано, что он ингибирует отек, индуцированный ирландским мхом, и отек уха, вызванный кротоновым маслом, а также является ингибитором интерлейкина-5.
Японская патентная заявка JP 11-116487 раскрывает только применение софорикозида для лечения диабета и т.п.
Китайский патент CNO 1113 081.4 раскрывает только применение софорикозида для лечения остеопороза у женщин после менопаузы.
Раскрытие изобретения
Одним объектом настоящего изобретения является предоставление применения софорикозида для получения лекарственного средства для предотвращения и/или лечения дегенерации суставного хряща, конкретно, у женщин после менопаузы, не обладающего побочными эффектами на грудь или матку человека.
Другим объектом настоящего изобретения является применение софорикозида для получения лекарственного средства для предотвращения и/или лечения остеоартрита, конкретно, у женщин после менопаузы, не обладающего побочными эффектами на грудь или матку человека.
Поэтому настоящее изобретение относится к применению софорикозида следующей формулы для получения лекарственного средства для предотвращения и/или лечения дегенерации суставного хряща у женщин после менопаузы:
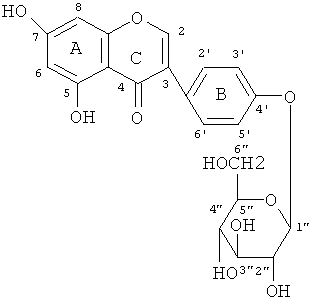
3-[4-(β-D-глюкопиранозил)-бензил]5,7-дигидро-4Н-1-бензопиран-4-он(4′,5,7-тригидроксилизофлавон-4′-D-глюкозид).
В другом аспекте настоящее изобретение относится к применению софорикозида следующей формулы для получения лекарственного средства для предотвращения и/или лечения остеоартрита у женщин после менопаузы:

3-[4-(β-D-глюкопиранозил)-бензил]5,7-дигидро-4Н-1-бензопиран-4-он(4′,5,7-тригидроксилизофлавон-4′-D-глюкозид).
В дополнительном аспекте настоящее изобретение относится к способу предотвращения и/или лечения дегенерации суставного хряща у женщин после менопаузы, включающему введение субъекту, который в этом нуждается, терапевтически эффективного количества софорикозида следующей формулы:

3-[4-(β-D-глюкопиранозил)-бензил]5,7-дигидро-4Н-1-бензопиран-4-он(4′,5,7-тригидроксилизофлавон-4′-D-глюкозид).
В другом дополнительном аспекте настоящее изобретение относится к способу предотвращения и/или лечения остеоартрита у женщин после менопаузы, включающему введение субъекту, который в этом нуждается, терапевтически эффективного количества софорикозида следующей формулы:

3-[4-β-D-глюкопиранозил)-бензил]5,7-дигидро-4Н-1-бензопиран-4-он(4′,5,7-тригидроксилизофлавон-4′-D-глюкозид).
Предпочтительно, софорикозид экстрагируют из Sophora subprograms, например Glycine max или Sophora japonica, особенно Sophora japonica.
В области фармацевтической техники хорошо известно получение многих общепринятых лекарственных форм, таких как капсулы, таблетки для орального введения и т.п., в которые можно включать софорикозид с помощью общепринятых подходов.
Краткое описание фигур
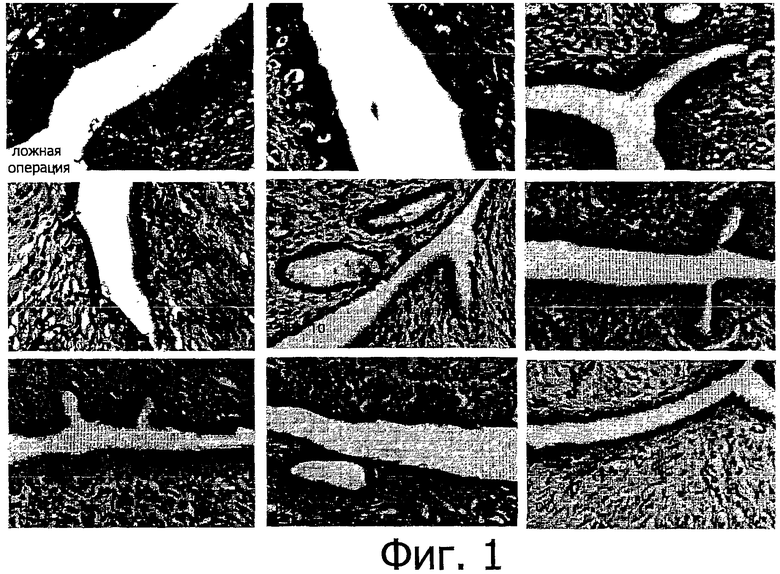
Фигура 1 представляет собой микрограф (микрофотографию) среза матки, окрашенного НЕ, согласно примеру 3 (объектив 40X).
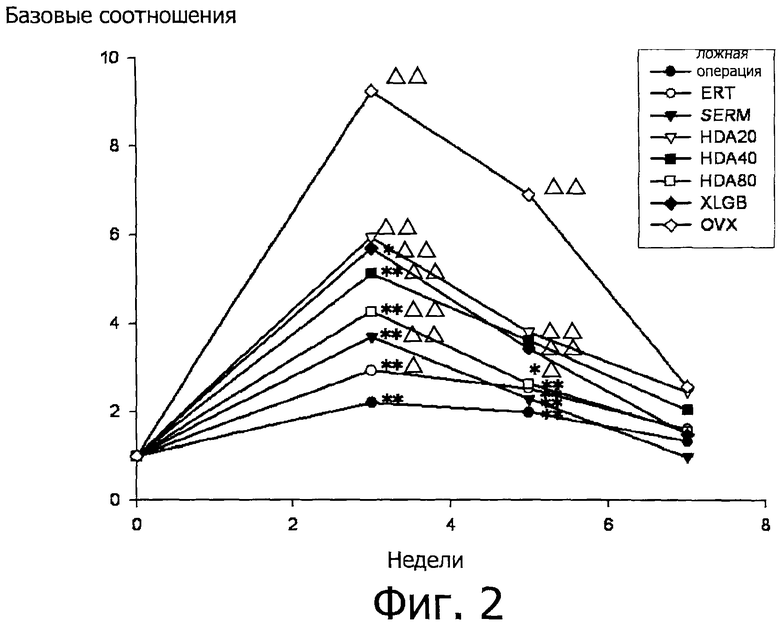
Фигура 2 представляет собой график базовых соотношений СТХ-II в группах в согласно примеру 4.
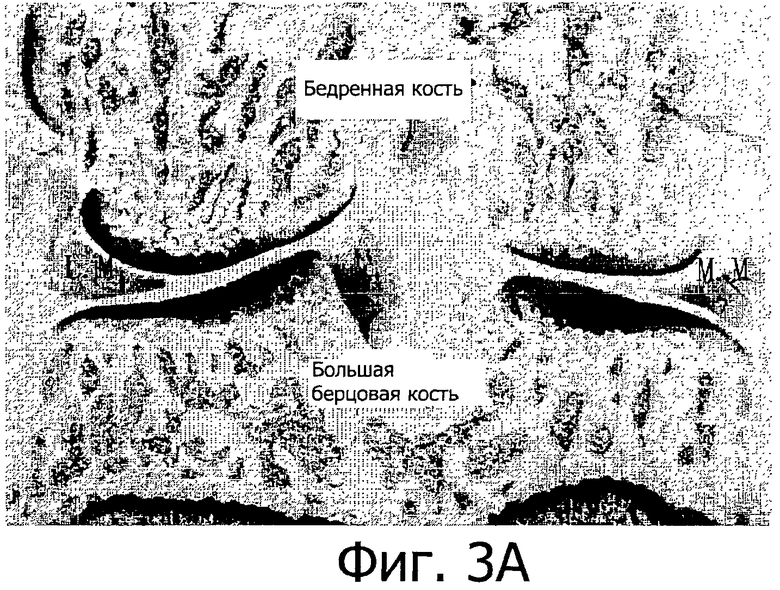
Фигура 3 представляет собой микрограф срезов целого сустава при патологии, окрашенных толуидиновым синим (объектив 1X), показывающих бедренную кость, большую берцовую кость и медиальный и латеральный мениски.
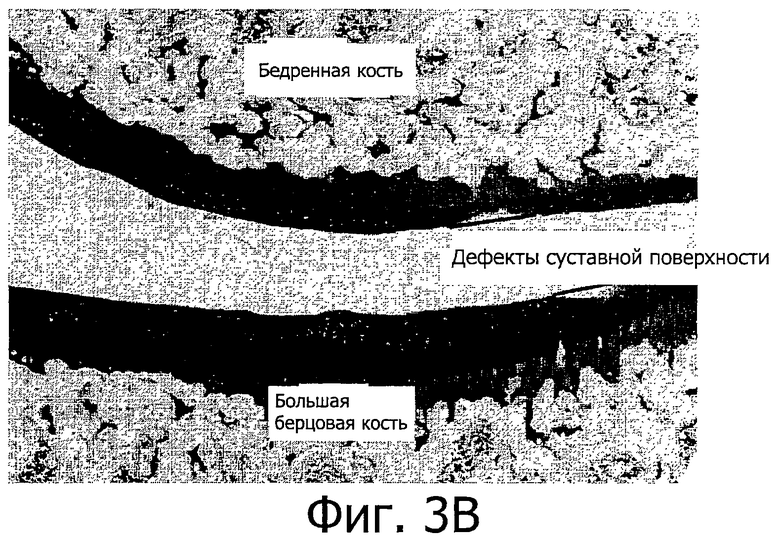
Фигура 3А представляет собой микрограф срезов суставной поверхности при патологии, окрашенных толуидиновым синим, показывающих бедренную кость, большую берцовую кость и дефекты суставной поверхности.
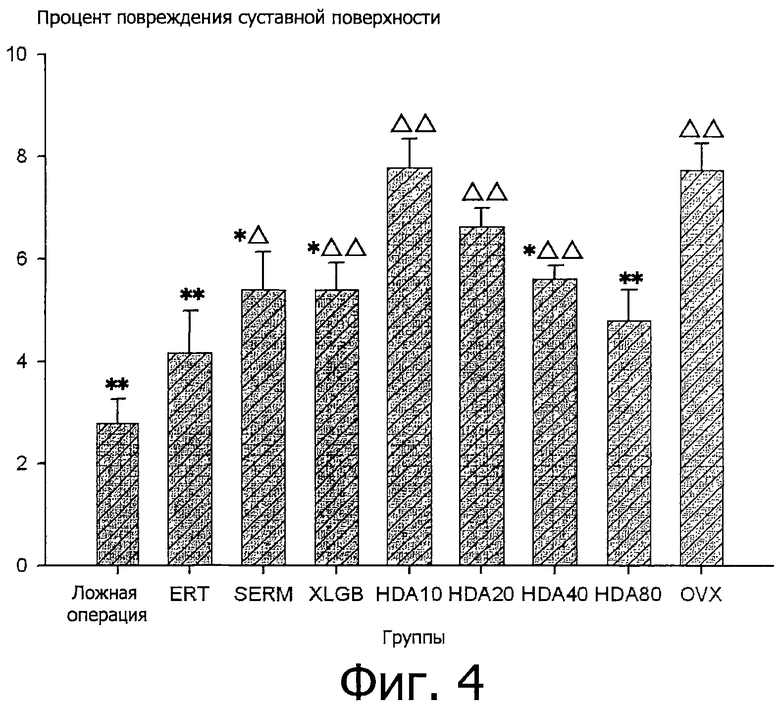
Фигура 4 представляет собой гистограмму профиля повреждения в группах согласно примеру 5 в соответствии с таблицей 3.
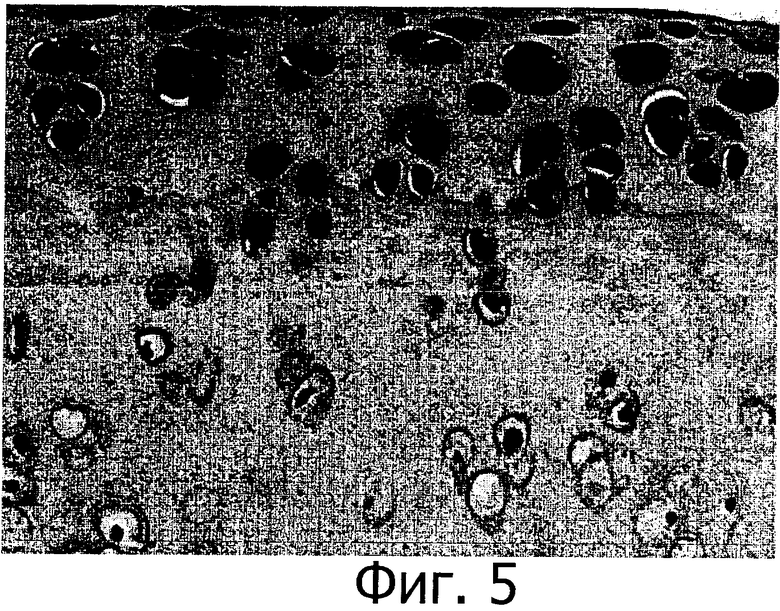
Фигура 5 представляет собой микрограф нормального суставного хряща, окрашенного с помощью иммуногистохимии для выявления ER-α (объектив 40X); ER-α экспрессируется в поверхностном слое, в среднем слое и в слое тучных клеток нормального суставного хряща.
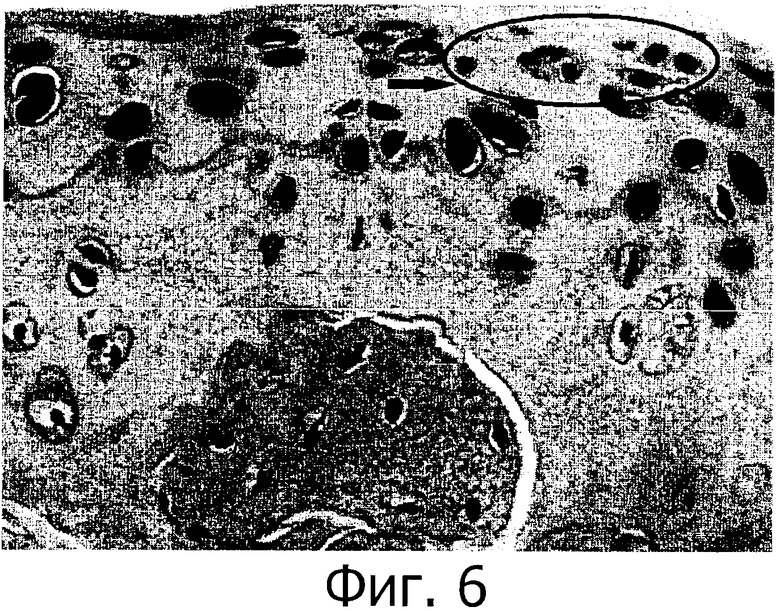
Фигура 6 представляет собой микрограф больного суставного хряща, окрашенного с помощью иммуногистохимии для выявления ER-α (объектив 40Х), где ER-α не экспрессируется в хондроцитах в области разрушения суставной поверхности.
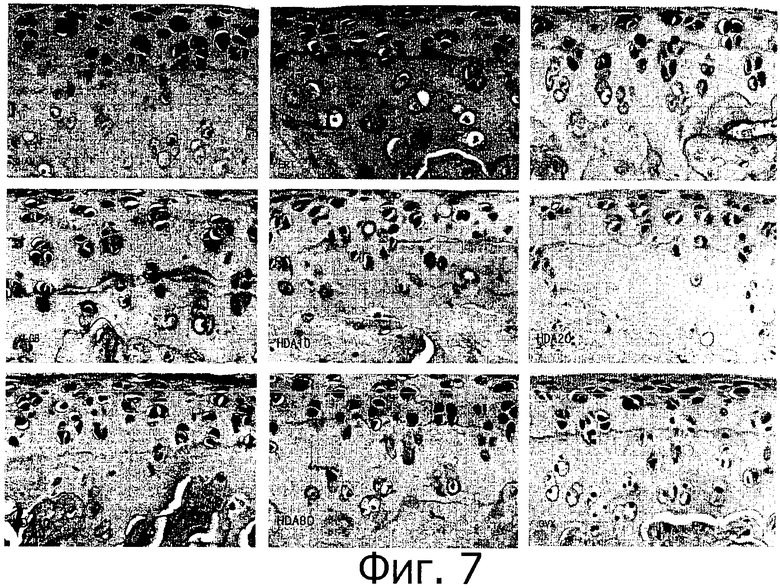
Фигура 7 представляет собой микрограф образцов суставного хряща согласно примеру 6, окрашенных с помощью иммуногистохимии для выявления ЕР-α (объектив 40Х).
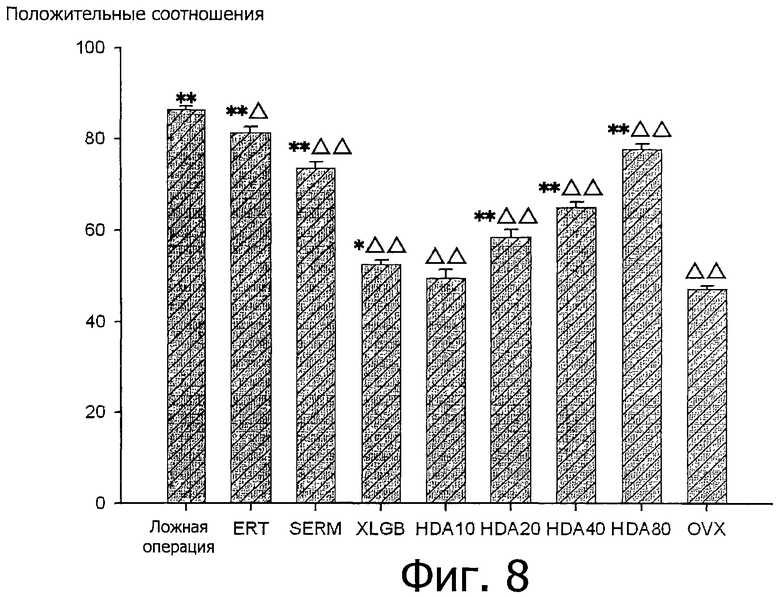
Фигура 8 представляет собой гистограмму положительных соотношений экспрессии ER-α в суставных хондроцитах указанных групп в соответствии с таблицей 4.
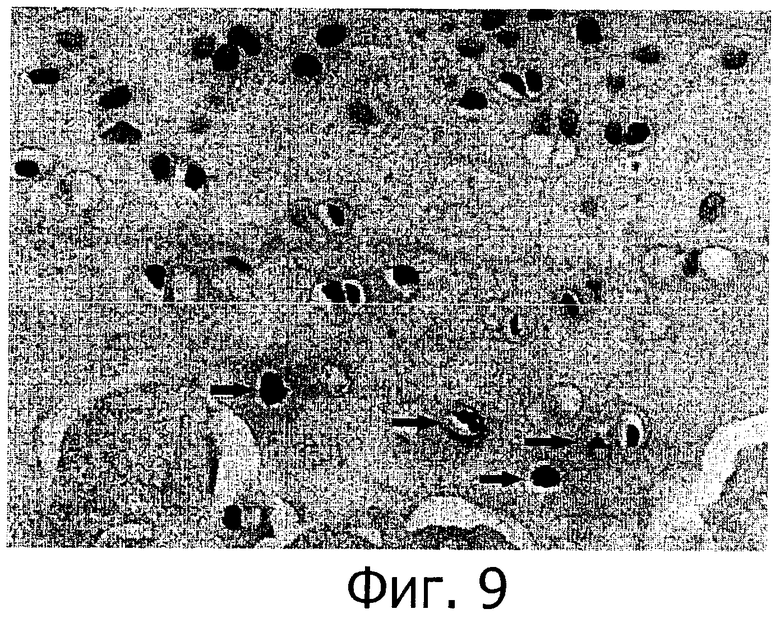
Фигура 9 представляет собой микрограф нормального суставного хряща, окрашенного по способу TUNEL (объектив 40X), где небольшое число клеток в состоянии апоптоза распределено по минерализованному слою хондроцитов и слою гипертрофированных хондроцитов, где клетки в состоянии апоптоза отмечены стрелками.
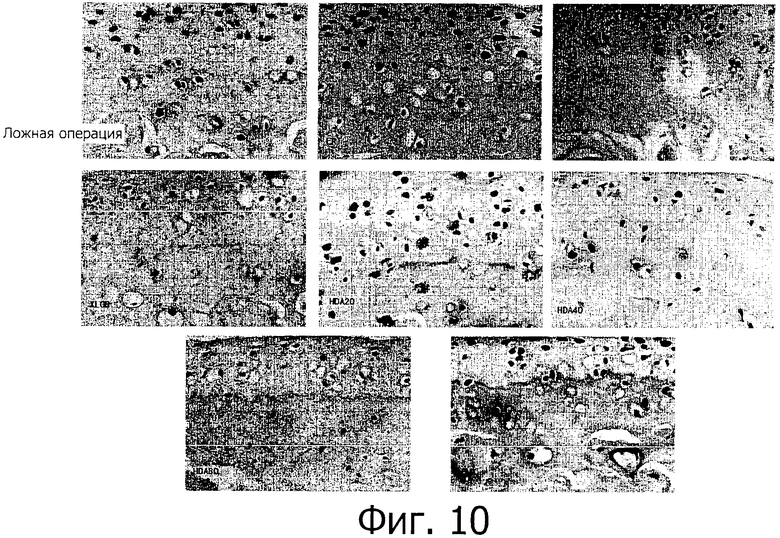
Фигура 10 представляет собой микрограф образцов суставного хряща, окрашенного по способу TUNEL, для указанных групп (объектив 40Х).
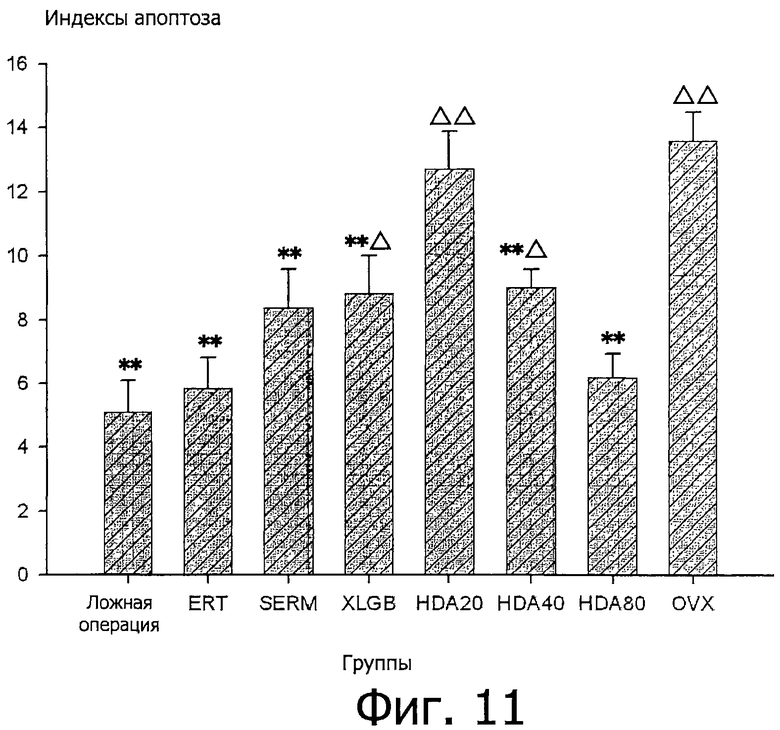
Фигура 11 представляет собой гистограмму индекса апоптоза в образцах суставного хряща в группах согласно примеру 7 в соответствии с таблицей 5.
Осуществление изобретения
Примеры
Пример 1. Образование групп и постановка моделей
66 самок крыс SD в возрасте 6 месяцев рандомизуют с образованием модельной группы (после овариэктомии, OVX), группы после ложной операции и следующих групп вмешательства, получавших: ERT, избирательный модулятор рецептора (SERM), Xialingubao, 10 мг софорикозида (HDA10), 20 мг софорикозида (HDA20), 40 мг софорикозида (HDA40) и 80 мг софорикозида (HDA80).
1. Способ моделирования
Группа OVX и группы вмешательства. Крысам дают анестезию путем внутривенной инъекции 1% пентобарбитала натрия в объеме 5 мл/кг. После наступления анестезии крыс помещают лицом вниз и удаляют шерсть в районе третьего поясничного позвонка ниже реберной дуги. Кожу обрабатывают бромидом бензалкония и надсекают примерно на 1 см. Подкожные ткани и связки надсекают и мышцы разделяют без рассечения. Брюшину осторожно вскрывают. Белый жир осторожно приподнимают с помощью тканевого пинцета, введенного в брюшную полость через разрез. Жир осторожно отворачивают, чтобы открыть квинкунциальный яичник, на который затем накладывают лигатуру с помощью стерильной шелковой нити 1. Яичник отделяют путем разрезания яйцевода глазными ножницами. После остановки кровотечения путем сдавливания жировой слой возвращают на место в брюшной полости. Далее делают разрез на противоположной стороне и проводят те же операции с целью иссечения яичника с противоположной стороны. На брюшину, фасцию, подкожные ткани и кожу по очереди накладывают швы. Разрезы подвергают санитарной обработке.
Группа с ложной операцией: яичники открывают с помощью таких же процедур, но не удаляют. После иссечения такого же количества жира на разрезы накладывают швы.
2. Условия разведения/содержания животных и вмешательства
Крыс содержат в чистой SPF камере для животных в центре экспериментальных животных Шанхайского института биологических наук, CAS, с температурой, поддерживаемой на уровне 24°С, влажностью, поддерживаемой на уровне 40-60%, и суточным ритмом 12 час/12 час. Крысам дают нормальный корм и очищенную воду ad libitum.
Носитель представляет собой 1% карбоксиметилцеллюлозу натрия (CMC-Na). Группе после ложной операции и группе OVX вводят носитель путем принудительного кормления.
Группам вмешательства вводят следующие составы с активным агентом, растворенным в носителе:
Группа ERT: прогинова ((Progynova), таблетка, содержащая валерат эстрадиола, производства Schering S.A., France, Batch no. 072A-2) 0,8 мг/кг/день;
Группа SERM: эвиза ((Evisa), таблетка, содержащая гидрохлорид ралоксифена, производства Lilly S.A., Spain, batch no. A208711) 3 мг/кг/день;
Группа XLGB: капсула ксианлингубао (Xianlingubao) (Guizhou Tongjitang Pharma Co Ltd., batch no. 060361) 270 мг/кг/день;
Группа HDA10: софорикозид (Shanghai Golden Wood Biological Technology Co., Ltd., batch no 04292004) 10 мг/кг/день;
Группа HDA20: софорикозид (Shanghai Golden Wood Biological Technology Co., Ltd., batch no 04292004) 20 мг/кг/день;
Группа HDA40: софорикозид (Shanghai Golden Wood Biological Technology Co., Ltd., batch no 04292004) 40 мг/кг/день;
Группа HDA80: софорикозид (Shanghai Golden Wood Biological Technology Co., Ltd., batch no 04292004) 80 мг/кг/день.
3. Получение животных образцов
Образцы мочи (1~1,5 мл) собирают в пробирки эппендорф от крыс до начала моделирования и на 3, 5 и 7 неделю с применением метаболических клеток и хранят при -20°С.
Крыс забивают путем цервикального смещения через 11 недель. Матку удаляют, взвешивают и фиксируют в 4% параформальдегиде (PFA). Целые суставы правых колен удаляют и фиксируют в 4% PFA.
Пример 2. Вес тела крыс и сырой вес матки до и после обработки
Крыс взвешивают и затем забивают. Матки удаляют из тел крыс и определяют их сырой вес.
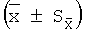
Проведен статистический анализ отклонения (дисперсионный анализ). Дисперсия сырого веса внутренних органов в группе после ложной операции высокая, вероятно, из-за разных стадий менструального цикла. Во всех группах вес тела до обработки не имеет статистического отличия от такового после обработки. Сырой вес маток, полученных от овариэктомированных животных, статистически достоверно отличается от веса таковых, полученных от животных после ложной операции (р<0,01), что указывает на успешную овариэктомию. Сырой вес маток, полученных в группе после ложной операции и в группе ERT, статистически достоверно отличается от веса полученных в модельной группе (р<0,01), а таковые, полученные в других группах вмешательства, не проявляют статистического отличия от полученных в группе OVX (р>0,05), что предполагает стимулирующее действие эстрогена на матку и отсутствие стимулирующего действия на матку в других группах.
Пример 3. Срезы препарата матки
1. Погружение. Матки крыс, полученные согласно примеру 1, фиксируют в 4% параформальдегиде в течение 24 час, дегидратируют в 75% этаноле в течение ночи, в 85% этаноле в течение 45 мин, в 95% этаноле в течение 45 мин 2 раза и в 100% этаноле в течение 45 мин 2 раза, помещают в ксилол на 15 мин 2 раза для просветления; помещают в термостат при 65°С, пропитывают воском в течение 3 час и погружают в парафин.
2. Получение срезов. Срезы маточные люминальные коронарные (uterine luminal coronal) крыс получают с помощью парафинового микротома (Leica Model RM2235) при толщине 5 мкм. Срезы помещают в теплую воду при 30°С и располагают на предметных стеклах, предварительно обработанных полилизином. Стекла переносят в термостат при 65°С на 3 часа и хранят в условиях окружающей среды до применения.
3. Окраска матки с помощью НЕ
1) Удаление воска из срезов. Срезы помещают в термостат при 65°С на 3 часа, затем погружают в ксилол на 10 мин 3 раза, в 100% этанол на 10 мин 2 раза, в 95% этанол на 10 мин 2 раза, в 85% этанол на 10 мин, в 75% этанол на 10 мин и в дважды дистиллированную воду;
2) Окраска: срезы окрашивают с помощью гематоксилина в течение 4 мин, затем синят путем промывки водой в течение 10 мин и окрашивают раствором эозина А в течение 4 мин и раствором эозина А в течение 2 мин;
3) Дегидратирование: растворы дегидратируют в 95% этаноле в течение 10 мин 2 раза и в 100% этаноле в течение 10 мин 2 раза;
4) Просветление: срезы погружают в ксилол на 10 мин 2 раза;
5) Монтируют на подложке из нейтральной смолы.
На фигуре 1 показаны профили окрашивания гематоксилином срезов матки указанных групп, полученные с помощью микроскопии при увеличении 40Х. В верхнем ряду на фигуре 1 показаны, слева направо, первая - группа контроля, за ней следуют группа ERT, группа SERM; во втором ряду слева направо первая - группа XLGB, затем группа HDA10 и далее группа HDA20; в третьем ряду слева направо показаны первая - группа HDA40, за ней группа HDA80 и далее группа OVX. Эндометрий в группе после ложной операции утолщен и выглядит чешуйчатым. Эндометрий в группе OVX тонкий и выглядит плоским. Эндометрий в группе ERT толще, чем в группе OVX, и в других группах он выглядит похожим на таковой в группе OVX.
Пример 4. Определение содержания CTX-II
1. Концентрацию CTX-II в образцах мочи, полученных согласно примеру 1, определяют с помощью набора Urine Pre-Clinical (PC) Cartilaps ELISA и конкурентного анализа с применением связанного с ферментом иммуносорбента (ELISA). Концентрацию креатина (называемого здесь и далее «Креа») в образцах мочи определяют с помощью многофункционального биохимического анализатора (Beckman coulter DXC800). Содержание CTX-II корректируют по следующей формуле:
скорректированное CTX-II (мг/моль)=CTX-II (мкг/л)/Креа (ммоль/л).
2. Принцип действия ELISA
ELISA применяет ковалентное связывание молекул фермента с антителом или анти-антителом, которое не оказывает действия на иммунологические свойства антитела или биологическую активность фермента. Меченное ферментом антитело может специфично связывать антиген или антитело, адсорбированное на твердой подложке. После добавления раствора субстрата его донирующая водород группа может быть превращена из бесцветной восстановленной формы в окрашенную окисленную форму под действием фермента, и вследствие этого появляется окраска. Таким образом, изменение цвета субстрата можно применять для индикации иммунологической реакции, и интенсивность окраски пропорциональна количеству антитела или антигена в образце. Колориметрическую реакцию можно количественно оценить с помощью устройства для считывания микропланшетов ELISA, так чтобы сочетать чувствительность ферментативной реакции со специфичностью реакции антиген/антитело, что делает ELISA специфичным и чувствительным подходом.
3. Определение CTX-II (мкг/л)
1) Образцы мочи, полученные согласно примеру 1, размораживают путем выдерживания при комнатной температуре в течение 30 мин. Аликвоты 200 мкл применяют для определения Креа. В аликвоты 10 мкл каждого образца добавляют стандартный раствор А и смесь разводят 1:4;
2) Получение стандартов: стандарты с концентрациями 0 мкг/л, 1,56 мкг/л, 3,13 мкг/л, 6,25 мкг/л, 12,5 мкг/л, 25 мкг/л, 50 мкг/л и 100 мкг/л получают согласно следующей таблице:
3) 100 мкл биотинилированного антигена добавляют в каждую лунку 96-луночного планшета, покрытого стрептавидином, и планшет запечатывают с помощью устройства для запечатывания планшетов и инкубируют при комнатной температуре в течение 30 мин;
4) Раствор для промывки разводят 1:5 деионизованной водой;
5) Планшет промывают 5 раз;
6) Стандарты, образцы и образцы для контроля качества (10 мкл каждый) добавляют в лунки и затем добавляют по 150 мкл первичного антитела. Планшет запечатывают с помощью устройства для запечатывания планшетов и инкубируют при 4°С в течение 21±3 час;
7) Планшет промывают 5 раз;
8) В каждую лунку добавляют по 100 мкл антител, конъюгированных с пероксидазой из хрена. Планшет запечатывают и инкубируют при комнатной температуре в течение 60 мин;
9) Планшет промывают 5 раз;
10) Добавляют 100 мкл тетраметилбензидина (ТМВ) и планшет инкубируют в темноте 15 мин для развития окраски субстрата;
11) В каждую лунку добавляют 10 мкл раствора для остановки реакции;
12) Оптическую плотность (OD) определяют с помощью устройства для считывания микропланшетов (Molecular Devices corporation, BD03315) при 450 нм и 650 нм и таким образом получают 4-параметрическую кривую регрессии для определения концентрации в каждом образце.
4. Определение Креа в образцах мочи (ммоль/л): концентрацию Креа определяют с применением многофункционального биохимического анализатора (Beckman coulter DXC800) в лабораторном отделении Шанхайского госпиталя Руйжин.
Базовые соотношения CTX-II рассчитывают по вышеприведенной формуле, и результаты показаны на фигуре 2, где ** отмечает р<0,01 vs модельной группы в тот же момент времени и * отмечает р<0,05 vs модельной группы в тот же момент времени.
Соотношения концентраций CTX-II в группе овариэктомированных относительно базовых представлены на фигуре 2, где проведен статистический дисперсионный анализ полученных данных. Результаты. показывают, что в группе OVX уровень CTX-II в моче значительно повышен (р<0,01) и Co1II активно метаболизируется в суставном хряще, но метаболизм Co1II постепенно возвращается к базовому уровню в течение 7 недель. В группе после ложной операции CTX-II в моче в основном стабилен во время эксперименты (р<0,05), и метаболизм Co1II в суставном хряще также стабилен. Эстрогенозаместительная терапия, селективный модулятор рецептора эстрогена и HDA80 существенно подавляют метаболический пик CTX-II вскоре после овариэктомии (р<0,01). Ксианлингубао (традиционное китайское лекарство) и HDA40 также оказывают такое действие, но в более слабой степени (р<0,05). Эстрогенозаместительная терапия, селективный модулятор рецептора эстрогена с эстрогеноподобным эффектом, HAD и китайская традиционная медицина играют роль в предотвращении и облегчении вышеописанного патологического процесса.
Пример 5. Повреждения суставной поверхности
1. Срезы коленного сустава крыс при патологии
А) Погружение:
1) Коленные суставы крыс фиксируют в 4% PFA в течение 48 час;
2) Образцы деминерализуют в 15% этилендиаминтетрауксусной кислоте (ЭДТА) в течение 15 дней;
3) Образцы дегидратируют в 75% этаноле в течение ночи;
4) Образцы дегидратируют в 85% этаноле в течение 45 мин;
5) Образцы дегидратируют в 95% этаноле в течение 45 мин 2 раза;
6) Образцы дегидратируют в 100% этаноле в течение 45 мин 2 раза;
7) Образцы просветляют в ксилоле 20 мин 2 раза;
8) Образцы пропитывают воском в течение 3 час в термостате при 65°С и
9) Образцы погружают в парафин.
В) Получение срезов
Коронарные срезы получают с помощью парафинового микротома (Leica Model RM2235) при толщине 5 мкм, применяя медиальный коллатеральный лигамент в качестве маркера. Срезы переносят в теплую воду при 30°С и помещают на предметные стекла, предварительно обработанные полилизином. Стекла переносят в термостат при 65°С на 3 часа и хранят в условиях окружающей среды до применения.
2. Окрашивание Ammonia Toluene Blue и измерение дефектов суставной поверхности
А) Окрашивание Ammonia Toluene Blue:
1) Освобождение срезов от воска: срезы помещают в термостат при 65°С на 3 часа и затем погружают в ксилол на 10 мин 3 раза, в 100% этанол на 10 мин 2 раза, в 95% этанол на 10 мин 2 раза, в 85% этанол на 10 мин, в 75% этанол на 10 мин и в дважды дистиллированную воду;
2) Окрашивание: срезы окрашивают в 1% Ammonia Toluene Blue в течение 5 мин и промывают водой 10 мин;
3) Дегидратирование: срезы дегидратируют в ацетоне I в течение 10 мин и в ацетоне II в течение 10 мин;
4) Просветление: срезы погружают в ксилол I на 10 мин и в ксилол II на 10 мин;
5) Срезы закрепляют на нейтральной смоле.
В) Анализ изображений повреждений сустава
Длину повреждений в четырех несущих вес поверхностях суставного хряща медиального и латерального бедренных мыщелков и медиального и латерального большеберцовых плато измеряют с помощью системы для анализа микроскопических изображений Axioplan 2 (многофункциональный автоматический флуоресцентный микроскоп Axioplan 2, система анализа изображений KS400, Ver. 3.0, цифровая камера AxioCam с разрешением 4900×3090) с участием двух независимых специалистов в области получения и анализа изображений (фигура 3A и 3В). Результаты усредняют. Рассчитывают процент повреждения для каждой из четырех хрящевых поверхностей. В итоге общий процент повреждения коленного сустава рассчитывают как:
(Процент повреждения каждой части суставной поверхности)=(длина повреждения)/(общая длина несущей вес тела суставной поверхности)×100%
(Процент повреждения суставной поверхности коленного сустава)=(общая длина повреждения)/(общая длина суставной поверхности)×100%
Профили дегенерации каждой части коленного сустава или целого коленного сустава крыс в каждой группе показаны в нижеприведенной таблице 3 и на фигуре 4. Для данных проводят статистический дисперсионный анализ. Результаты показывают, что различия профилей дегенерации суставного хряща между группой OVX и группой после ложной операции являются статистически значимыми (р<0,01), что указывает на усугубление дегенерации хряща после овариэктомии. Дегенерация суставного хряща, возникающая в результате овариэктомии, ослабляется в результате вмешательства, отличного от HDA10 и HDA20, причем ERT и HDA80 значительно более эффективны в сравнении с OVX (р<0,01), но не в сравнении с ложной операцией (р>0,05). XLGB, SERM и HDA80 эффективны, но не способны полностью обратить дегенерацию. Эти эффекты статистически отличаются от таковых после OVX (р<0,05), но не от таковых после ложной операции (р<0,05).
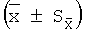
Пример 6. Окрашивание рецептора эстрогена суставных хондроцитов и расчет процента положительных клеток
1. Окрашивание рецептора эстрогена суставных хондроцитов:
1) Освобождение срезов от воска: срезы помещают в термостат при 65°С на 3 часа и затем погружают в ксилол на 5 мин 2 раза, в 100% этанол на 5 мин 2 раза, в 95% этанол на 5 мин 2 раза, в 85% этанол на 5 мин, в 75% этанол на 5 мин и в дважды дистиллированную воду на 5 мин 2 раза и в PBS на 5 мин 3 раза;
2) Удаление эндогенных пероксидаз: срезы обрабатывают 3% раствором H2O2-метанол в течение 10 мин и промывают PBS в течение 5 мин 3 раза;
3) Блокирование антигена: срезы обрабатывают 0,3% бычьим сывороточным альбумином (БСА) в течение 30 мин;
4) Первичные антитела: к каждому срезу добавляют 55 мкл антител против ER-α (Santa Cruz Biotechnology, Inc sc+542) (1:50). Срезы инкубируют при 4°С в течение ночи и затем промывают PBS в течение 5 мин 3 раза;
5) Вторичные антитела: после добавления биотинилированного вторичного антитела (1:200) срезы инкубируют при 37°С в течение 30 мин и затем промывают PBS в течение 5 мин 3 раза;
6) Добавление SABC (комплекса стрептавидин-биотин): после добавления SABC (1:300) срезы инкубируют при 37°С в течение 30 мин и затем промывают PBS в течение 5 мин 3 раза;
7) Визуализация: к каждому срезу добавляют 75 мкл 3,3′-диаминобензидина (DAB). После инкубации в течение 3-6 мин срезы изучают с помощью микроскопа;
8) Дополнительное окрашивание: срезы промывают проточной водой в течение 3 мин и затем окрашивают гематоксилином в течение 10 сек, затем промывают проточной водой 10 мин, погружают в 95% этанол на 10 мин 2 раза, погружают в 100% этанол на 10 мин 2 раза, помещают в ксилол на 10 мин 2 раза и под конец закрепляют на нейтральной смоле.
2. Анализ изображений и расчет процента положительных клеток.
Медиальный и латеральный бедренные мыщелки и медиальное и латеральное плато большой берцовой кости наблюдают с помощью системы для анализа микроскопических изображений Axioplan 2 (см выше) с участием двух независимых специалистов в области получения и анализа изображений, где процент клеток, экспрессирующих ER-α, рассчитывают в двух независимых полях для каждого района и средний процент рассматривают как процент положительных клеток в каждом указанном районе. Средний процент для четырех районов рассматривают как общий процент положительных клеток для указанного коленного сустава и средний процент, полученный двумя специалистами, рассматривают как окончательный экспериментальный результат.
(Процент положительных клеток)=(число положительных хондроцитов в поле)/(общее число хондроцитов в поле)×100%
Профили экспрессии ER-α для каждой группы крыс показаны на фигуре 7, где в группе после ложной операции ER-α экспрессируется во всех слоях суставного хряща; положительные по ER-α клетки в верхнем слое суставного хряща в группе OVX, группе HDA10 и группе HDA20 представлены значительно меньше, чем в нормальном суставном хряще; положительных по ER-a клеток в суставном хряще группы ERT и HDA80 больше, чем у OVX группы, и примерно столько же, как в нормальном суставном хряще; экспрессия ER-α повышена в группе SERM и в группе XLGB по сравнению с группой OVX.
Положительные соотношения экспрессии ER-α и различия среди указанных групп показаны в таблице 4 и на фигуре 8. Эти результаты предполагают, что в нормальном суставном хряще (группа после ложной операции) ER-α экспрессируется в поверхностном слое, среднем слое и в слое тучных клеток (фигура 5). ER-α не экспрессируется в поверхностном слое суставного хряща в районах повреждения. Экспрессия ER-α значительно уменьшена в суставном хряще овариэктомированных крыс (р<0,01). Экспрессия ER-α повышена у овариэктомированных крыс, получавших эстроген, SERM и HDA в дозе выше 10 мг, и ее трудно обратить к нормальному уровню (р<0,05 для группы ERT по сравнению с группой после ложной операции, р<0,05 для других групп по сравнению с группой после ложной операции). Результат для группы XLGB статистически отличается от такового в группе OVX (р<0,05), и действие ERT значительно улучшено по сравнению с другими группами (р<0,01).
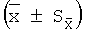
Пример 7. Наблюдение профилей апоптоза хондроцитов
1. Принцип способа TUNEL, применяемого для диагностики апоптоза
Когда клетка претерпевает апоптоз, хромосомная ДНК фрагментируется постепенно и в несколько этапов. Хромосомная ДНК вначале расщепляется на большие фрагменты размером 50-300 килобаз с помощью эндогенных нуклеаз. Затем примерно 30% хромосомной ДНК беспорядочно расщепляется в межнуклеосомальных районах с помощью Са2+- и Mg2+-зависимых эндонуклеаз с образованием мультимеров размером 180-200 пар оснований нуклеосомальной ДНК. Свободные 3′-концы, образуемые в результате разрыва двухцепочечной ДНК или разрыва одноцепочечной ДНК, можно метить путем добавления производного, образуемого из дезоксирибонуклеотида и флуоресцеина, пероксидазы, щелочной фосфатазы с помощью терминальной дезоксинуклеотидилтрансферазы. Клетку в состоянии апоптоза можно детектировать соответственно. Такие способы в основном представляют собой присоединение метки к открытым концам, опосредованное терминальными дезоксинуклеотидилтрансферазами.
2. Окраска по способу TUNEL
1) Удаление из срезов воска: срезы помещают в термостат при 65°С на 3 часа и затем погружают в ксилол на 5 мин 2 раза, в 100% этанол на 10 мин 2 раза, в 95% этанол на 5 мин 2 раза, в 85% этанол на 5 мин, в 75% этанол на 5 мин и в PBS на 5 мин 2 раза;
2) Предварительная обработка: каждый срез инкубируют с 60 мкл свежеприготовленной протеазы К (20 мкг/мл) в камере с увлажнением при 37°С в течение 20 мин, затем промывают PBS в течение 2 мин 2 раза;
3) Удаление эндогенных пероксидаз: срезы обрабатывают 3% раствором H2O2-метанол в течение 5 мин и промывают PBS в течение 5 мин 3 раза;
4) Уравновешивание: каждый срез промывают 75 мкл раствора для уравновешивания в течение 10 сек и декантируют, оставшуюся воду отсасывают;
5) Добавление TdT фермента: к каждому срезу немедленно добавляют 55 мкл рабочего раствора, причем положительный контроль оставляют без обработки, и срезы помещают в камеру с увлажнением при 37°С на 1 час;
6) Остановка реакции: срезы осторожно покачивают в растворе для остановки реакции в течение 15 мин и промывают PBS в течение 3 мин 3 раза и осторожно декантируют;
7) Визуализация: каждый срез инкубируют с 65 мкл антидигоксин-пероксидазы в камере с увлажнением при комнатной температуре в течение 30 мин и промывают PBS в течение 2 мин 4 раза. После инкубации с достаточным количеством субстрата пероксидазы (75 мкл) в течение 3~6 мин каждый срез визуализуют с помощью микроскопии;
8) Дополнительное окрашивание: срезы промывают проточной водой в течение 3 мин и далее окрашивают гематоксилином в течение 10 сек, затем промывают проточной водой в течение 10 мин, погружают в 95% этанол на 10 мин 2 раза, погружают в 100% этанол на 10 мин 2 раза, помещают в ксилол на 10 мин 2 раза и под конец закрепляют на нейтральной смоле.
3. Анализ изображений и расчет индекса апоптоза.
Медиальный и латеральный бедренные мыщелки и медиальное и латеральное большеберцовые плато коленного сустава исследуют с помощью системы для анализа микроскопических изображений Axioplan 2 (см. выше) с участием двух независимых специалистов в области получения и анализа изображений, причем индекс апоптоза рассчитывают в двух независимых полях для каждого района и средний индекс рассматривают как индекс апоптоза в каждом указанном районе. Средний индекс для четырех районов рассматривают как общий индекс апоптоза для указанного коленного сустава и средний индекс, полученный двумя специалистами, рассматривают как окончательный экспериментальный результат.
(Индекс апоптоза)=(число положительных клеток в поле)/(общее число хондроцитов в поле)×100%
Фигура 10 представляет собой микрограф образцов суставного хряща, окрашенных по TUNEL, в указанных группах (объектив 40х), где большое количество клеток в состоянии апоптоза обнаруживается во всех слоях суставного хряща в группе OVX и оно повышено в поверхностном слое и в среднем слое. Минорное количество клеток в состоянии апоптоза в основном детектируется в минерализованном слое сустава в группе после ложной операции. Количество клеток в состоянии апоптоза в суставном хряще группы ERT и группы HDA8Q меньше, чем в группе OVX, и близко к таковому в нормальном суставном хряще. Количество клеток в состоянии апоптоза в других группах меньше, чем в группе HDA20, чем в группе OVX. Эти результаты предполагают, что небольшое количество клеток в состоянии апоптоза существует в минерализованном слое нормального суставного хряща крыс и количество клеток в состоянии апоптоза среди суставных хондроцитов возрастает у овариэктомированных крыс (группа OVX) (р<0,01). Хондроциты в состоянии апоптоза детектируются во внешнем слое, включая поверхностный слой и средний слой суставного хряща (см., например, фигуру 10). Вмешательство, отличное от HDA10, приводит к статистически значимому уменьшению числа хондроцитов в состоянии апоптоза по сравнению с группой OVX (р<0,05). Эффекты, наблюдаемые в группе XLGB и в группе HDA40, слабее по сравнению с группой после ложной операции (р<0,05).
Индексы апоптоза хондроцитов в коленных суставах крыс представлены в следующей таблице 5 и на фигуре 11.
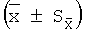
Настоящее изобретение относится к области фармацевтики и медицины и касается применения софорикозида для получения лекарственного средства для предотвращения и/или лечения дегенерации суставного хряща или остеоартрита у женщин после менопаузы, обладающего высокой эффективностью и не имеющего побочных эффектов. 2 н. и 4 з.п. ф-лы, 11 ил., 5 табл., 7 пр.
1. Применение софорикозида следующей формулы для получения лекарственного средства для предотвращения и/или лечения дегенерации суставного хряща у женщин после менопаузы:

3-[4-(β-D-глюкопиранозил)-бензил]5,7-дигидро-4Н-1-бензопиран-4-он(4′,5,7-тригидроксилизофлавон-4′-D-глюкозид).
2. Применение по п.1, при котором софорикозид получают из Sophora subprograms.
3. Применение по п.1, при котором софорикозид получают из Glycine max или Sophora japonica.
4. Применение софорикозида следующей формулы для получения лекарственного средства для предотвращения и/или лечения остеоартрита у женщин после менопаузы:

3-[4-(β-D-глюкопиранозил)-бензил]5,7-дигидро-4Н-1-бензопиран-4-он(4′,5,7-тригидроксилизофлавон-4′-D-глюкозид).
5. Применение по п.4, при котором софорикозид получают из Sophora subprograms.
6. Применение по п.4, при котором софорикозид получают из Glycine max или Sophora japonica.
| KR 1020010037308 A, 07.05.2001 | |||
| WO 2008010663 A1, 24.01.2008 | |||
| US 20060182825 A1, 17.08.2006 | |||
| US 20050239721 A1, 23.06.2005. |
Авторы
Даты
2012-06-27—Публикация
2009-08-06—Подача