Изобретение относится к биомедицине и может быть использовано для изучения механизмов действия на опухолевые клетки эндоканнабиноидов, эндованилоидов и других биоактивных липидов.
Биоактивные липиды, относящиеся к семейству эндоканнабиноидов и эндованилоидов, - анандамид, дофаминамиды жирных кислот, а также растительный ванилоид капсаицин - обладают разнонаправленным действием, зависящим от состояния мишени: они способны подавлять некоторые клетки иммунной системы (Sancho R, Macho A, de La Vega L, Calzado MA, Fiebich BL, Appendino G, Munoz E. Immunosuppressive activity of endovanilloids: N-arachidonoyl-dopamine inhibits activation of the NF-kappa B, NFAT, and activator protein 1 signaling pathways. // J Immunol. 2004 Feb 15; 172(4):2341-514), обладают нейропротекторными и антиоксидантными свойствами (Bobrov MY, Lizhin AA, Andrianova EL, Gretskaya NM, Frumkina LE, Khaspekov LG, Bezuglov VV. Antioxidant and neuroprotective properties of N-arachidonoyldopamine. // Neurosci Lett. 2008 Jan 24; 431(1):6-11) в отношении нормальных клеток в стрессовых условиях, но при этом подавляют пролиферацию культур трансформированных клеток, по крайней мере, ряда линий глиом, нейробластом, сарком, лимфом и лейкемий (AkimovMG, Bezuglov VV, DopaminesA New Life for the Old Dopamine. // Dopamine: Functions, Regulation and Health Effects. Nova Publishers, NY, 2012). Особый интерес в качестве потенциальных противораковых агентов данным веществам придает их способность ингибировать рост раковых стволовых клеток (Visnyei K, Onodera Н, Damoiseaux R, Saigusa K, Petrosyan S, De Vries D, Ferrari D, Saxe J, Panosyan EH, Masterman-Smith M, Mottahedeh J, Bradley KA, Huang J, Sabatti C, Nakano I, Kornblum HI. A molecular screening approach to identify and characterize inhibitors of glioblastoma stem cells. // Mol Cancer Ther. 2011 Oct; 10(10): 1818-28). При этом данные вещества обладают низкой токсичностью для организма в целом: после ежедневного введения N-докозагексаеноилдофамина мышам в концентрации 10 мг/кг в течение 21 дня, а также после однократного введения этого вещества в дозе 1000 мг/кг животные оставались здоровыми (Shashoua VE, Hesse GW. N-docosahexaenoyl, 3 hydroxytyramine: a dopaminergic compound that penetrates the blood-brain barrier and suppresses appetite. // Life Sci. 1996; 58(16): 1347-57).
При этом разработка лекарственных препаратов на основе данных соединений существенно затруднена скудностью данных о механизме их действия, что затрудняет оптимизацию их структуры с целью увеличения токсичности и селективности, и о том, возможно ли возникновение лекарственной устойчивости к ним у опухолевых клеток.
Известныклеточные линии, устойчивые к цисплатину (Barr MP, Gray SG, Hoffmann AC, Hilger RA, Thomale J, O'Flaherty JD, Fennell DA, Richard D, O'Leary JJ, O'Byrne KJ. Generation and characterisation of cisplatin-resistant non-small cell lung cancer cell lines displaying a stem-like signature. // PLoS One. 2013; 8(1): e54193. doi: 10.1371 / journal. pone. 0054193). Данные клеточные линии характеризуются повышенным содержанием опухолевых стволовых клеток и метастатическими свойствами, однако, их механизм устойчивости связан не с метаболизмом липидов, а с системой контроля целостности ДНК.
Известны клеточные линии, устойчивые к пеметрекседу, гемцитабину и винорелбину (Hudson AL, Weir С, Moon Е, Harvie R, Klebe S, Clarke SJ, Pavlakis N, Howell VM. Establishing a panel of chemo-resistant mesothelioma models for investigating chemo-resistance and identifying new treatments for mesothelioma. Sci Rep. 2014 Aug 21; 4: 6152). Недостатком данных линий является то, что основой их механизма устойчивости является экспрессия транспортеров группы семейства ABC.
Известны клеточные линии, устойчивые к метатрексату и к N-(фосфонацетил)-L-аспартату (Cillo С, Dick JE, Ling V, Hill RP. Generation of drug-resistant variants in metastatic В16 mouse melanoma cell lines. Cancer Res. 1987 May 15; 47(10): 2604-8). Недостатком данных линий является их нестабильность и высокая гетерогенность.
Известналиния глиобластомы человека U251, устойчивая к действию противоракового алкилирующего агента темозоломида (Temozolomide) (Qiang Pan, Xue-jun Yang, Hua-min Wang, Xue-tao Dong, Wei Wang, Yu LI, Jing-min LI. Chemoresistance to Temozolomide in Human Glioma Cell Line U251 is Associated with Increased Activity of O6-methylguanineDNA Methyltransferase and Can be Overcome by Metronomic Temozolomide Regimen. // Cell Biochem Biophys 2012. 62: 185-191). Недостатком данной линии является изменение экспрессии фермента O6-метилгуанин-ДНК метилтрансферазы, не имеющего отношения к метаболизму и функциям биоактивных липидов в качестве ключевого результата, и отсутствие данных о чувствительности линии к другим химиотерапевтическим агентам.
Известен наиболее близкий аналог данного изобретения - клеточная линия глиомы С6, устойчивая к цитотоксическому действию тетрагидроканнабинола (Lorente М, Carracedo A, Torres S, Natali F, Egia A, 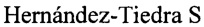 , Salazar M,
, Salazar M,  ,
,  , Velasco G. Amphiregulin is a factor for resistance of glioma cells to cannabinoid-induced apoptosis. Glia. 2009 Oct; 57(13): 1374-85). Основным недостатком данных клеточных линий является их селекция с помощью экзогенного вещества тетрагидроканнабинола, которое является ксенобиотиком и, следовательно, может не задействовать по крайней мере часть метаболических путей, которые могут участвовать в регуляции сигнала эндогенных липидов.
, Velasco G. Amphiregulin is a factor for resistance of glioma cells to cannabinoid-induced apoptosis. Glia. 2009 Oct; 57(13): 1374-85). Основным недостатком данных клеточных линий является их селекция с помощью экзогенного вещества тетрагидроканнабинола, которое является ксенобиотиком и, следовательно, может не задействовать по крайней мере часть метаболических путей, которые могут участвовать в регуляции сигнала эндогенных липидов.
Клеточные линии с повышенной устойчивостью к действию ацилдофаминов ранее не были описаны.
Задачей изобретения является получение клеточной линии с повышенной устойчивостью к цитотоксическому действию эндованилоидов, пригодной для изучения механизмов действия эндоканнабиноидов, эндованилоидов и других липидов на опухолевые клетки и механизмов резистентности опухолевых клеток к цитотоксическому действию биоактивных липидов.
Поставленная задача решается за счет клеточной линии крысиной глиомы С6-DDA на основе линии крысиной глиомы С6, характеризующейся повышенной устойчивостью к ацилдофаминам.
Технический результат заявленной клеточной линии крысиной глиомы С6-DDA заключается в возрастании LC50 для ацилдофаминов и их аналогов в 2 и более раза без изменения LC50 для даунорубицина. Устойчивость сохраняется на протяжении как минимум трех месяцев непрерывного культивирования.
Перечисленные свойства делаю тклеточную линию крысиной глиомы С6-DDA пригодной для изучения механизма действия и цитотоксических свойств в отношении опухолевых клеток различных биоактивных липидов, в первую очередь групп эндованилоидов и эндоканнабиноидов.
Клеточная линия крысиной глиомы C6-DDA депонирована во Всероссийской коллекции промышленных микроорганизмов, регистрационный номер Н-173.
Получение клеточной линии. Исходным материалом для получения устойчивой линии является линия крысиной глиомы С6, полученная из Российской коллекции клеточных культур (РККК) при Институте Цитологии РАН (Санкт-Петербург, Россия). Исходную линию культивируют в среде DMEM с добавлением 10% FBS (эмбриональная телячья сыворотка) как адгезионную культуру при 37°С с 5% содержанием СО2. Пересев осуществляют 0.25% раствором трипсина каждые 2-3 дня с кратностью рассева 1:10 или 5×105 клеток на флакон с поверхностью 25 см2. Клеточная линия крысиной глиомы C6-DDA получена путем ступенчатого отбора устойчивых клеток возрастающими концентрациями N-докозагексаеноилдофамина до достижения концентрации 48 мкМ.
Культуральные свойства. Клеточную линию крысиной глиомы C6-DDA культивируют в монослойных культурах в среде DMEM с 10% сыворотки эмбрионов коров. Для диспергирования клеточного монослоя при пересевах используют смесь 0,25% раствора трипсина и 0,02% раствора Версена в соотношении 1:1,5 при комнатной температуре. Урожай клетоксфлаконаплощадью 25 см2 составляетоколо 5 млнклеток. Для криоконсервирования при температуре -196°С применяют смесь, состоящую 70% питательной среды DMEM, 20% сыворотки эмбрионов коров и 10% диметилсульфоксида, приконцентрацииклеток 1-2×106 вмл. Жизнеспособность клеток по тестувитального окрашивания трипановым синим после хранения в жидком азоте составляет 70-80%. Клетки восстанавливают исходные ростовые и морфологические свойства в течение одного пассажа.
Морфологические признаки. При посеве клетки крысиной глиомы C6-DDA равномерно распределяются по поверхности субстрата. Клетки однородные эпителиоподобные, крупные, полигональной формы с длинными с многочисленными короткими цитоплазматическими отростками или веретенообразной формы с 2-4 длинными отростками и небольшим телом. По мере уплотнения монослоя отростки укорачиваются, и форма клеток приближается к овальной. Ядра крупные, овальные.
Чувствительность к цитотоксическому действию N-ацилдофаминов, даунорубицина и метатрексата. Клетки линии крысиной глиомы С6-DDA обладают устойчивостью к набору эндованилоидов семейства N-ацилдофаминовс увеличением полулетальной дозы по сравнению с исходной линией клеток в 2 и более раз (таблица 1). Метатрексат в отношении линии крысиной глиомы С6-DDA проявляет токсичность с LC50=100 мкМ, в то время как для исходной линии крысиной глиомы С6 он не обладает токсичностью вплоть до концентрации 200 мкМ. Даунорубицин обладает средней токсичностью для линиикрысиной глиомы C6-DDA (LC50=55 мкМ), которая не отличается от исходной линии крысиной глиомы С6. Выработанная устойчивость сохраняется при непрерывном культивировании на протяжении трех месяцев.
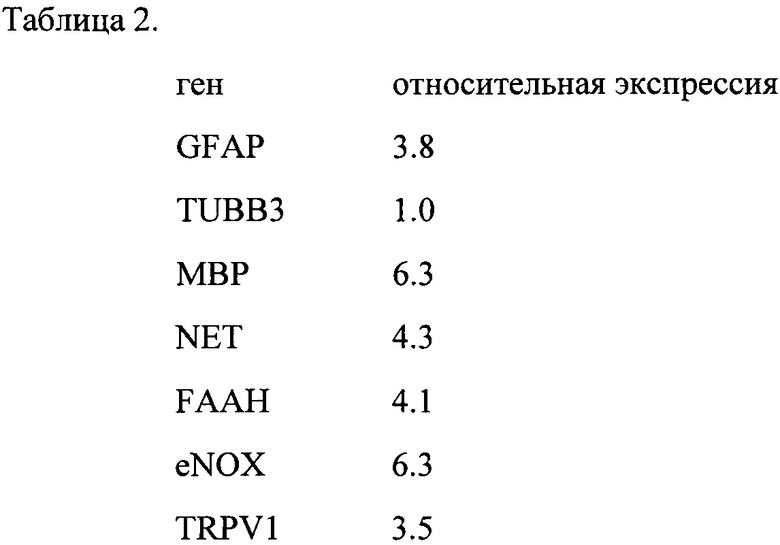
Экспрессия маркеров дифференцировки. В полученной линии крысиной глиомы C6-DDA по сравнению с исходной линией крысиной глиомы С6 наблюдается экспрессия маркеров астроцитарной дифференцировки SOX2, усиление экспрессии GFАР, а также маркера нейрональной дифференцировки Tubb3; гидролазы амидов жирных кислот FAAH, усилена экспрессия норадреналинового транспортера NET и оксидоредуктазы плазмалеммы ecto-NOX.
Контроль клеточной линии крысиной глиомы C6-DDA на посторонние контаминанты. При исследовании клеточной линии крысиной глиомы C6-DDA на стерильность (наличие бактерий, грибов) методом световой микроскопии после культивирования в среде без антибиотиков и антимикотиков получены отрицательные результаты.
Изобретение иллюстрируют следующие графические материалы:
Таблица 1. Значения полулетальных концентраций ацилдофаминов и их производных для исходного и устойчивых вариантов линии крысиной глиомы С6, мкМ. Среднее±стандартное отклонение.
Таблица 2. Относительная экспрессия мРНК маркерных генов и генов каннабиноидно-ванилоидной системы в культуре клеток крысиной глиомы С6-DDA по сравнению с исходной линией крысиной глиомы С6
Изобретение иллюстрируют следующие примеры:
Пример 1. Оценка цитотоксического действия биоактивных липидов.
Предварительно оценивают цитотоксичность N-докозагексаеноилдофамина для клеточной линии. Для этого клетки высеивают в ростовой среде в ростовой среде DMEM с 10% FBS и 2 мМ L-глутамина с плотностью 105/см2. Через 24 часа культивирования к клеткам добавляютисследуемые вещества в виде раствора DMSO в ростовой среде с финальной концентрацией DMSO 0.5%, с заменой культуральной среды на новую. Клетки инкубируют с исследуемыми веществами 24 часа. В качестве положительного контроля используютклетки, к которым добавляютростовую среду с финальной концентрацией DMSO 0.5%. Жизнеспособность клеток определяют с помощью МТТ теста с заменой среды с веществами на раствор МТТ в растворе Хэнкса.
Пример 2. Отбор устойчивой клеточной линии.
Предварительно оценивают цитотоксичность N-докозагексаеноилдофамина для клеточной линии. Для этого клетки высеивают в ростовой среде в ростовой среде DMEM с 10% FBS и 2 мМ L-глутамина с плотностью 105/см2. Через 24 часа культивирования к клеткам добавляютисследуемые вещества в виде раствора DMSO в ростовой среде с финальной концентрацией DMSO 0.5%, с заменой культуральной среды на новую. Клетки инкубируют с исследуемыми веществами 24 часа. В качестве положительного контроля используютклетки, к которым добавляю тростовую среду с финальной концентрацией DMSO 0.5%. Жизнеспособность клеток определяют с помощью МТТ теста с заменой среды с веществами на раствор МТТ в растворе Хэнкса.
Выбирают начальную концентрацию N-докозагексаеноилдофамина таким образом, чтобы при ее добавлении погибало 80% популяции клеток.
Монослой выращивают в ростовой среде DMEM с 10% FBS в неселекционных условиях и 2 мМ L-глутамина. По достижении 95% конфлюэнтности средузаменяют на новую с добавлением N-докозагексаеноилдофамина в виде раствора в ДМСО (финальная концентрация 0.5%), инкубируют 24 часа и заменяют среду на неселективную. Далее действуют циклически. Выжившие клетки выращивают до достижения монослоя, разделяют на две части и вновь доращивают до монослоя. После этого к одной части клеток вновь добавляют N-докозагексаеноилдофамин в концентрации на 2 мкМ выше предыдущего шага. Если после этого есть выжившие клетки, их вновь выращивают и делают новый шаг селекции. Если выживших нет, используют вторую часть культуры и меньшее приращение концентрации. Если погибших нет, повторяют добавление вещества с большей концентрацией. Селекцию проводят до достижения отбирающей концентрации 48 мкМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФЛУОРЕСЦИРУЮЩАЯ КЛЕТОЧНАЯ ЛИНИЯ ГЛИОМЫ И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2018 |
|
RU2699754C1 |
| ПРОИЗВОДНЫЕ 5-АМИНО-3-(2-АМИНОПРОПИЛ)-[1,2,4]ТИАДИАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2536824C1 |
| Производные нестероидных противовоспалительных средств | 2018 |
|
RU2732297C2 |
| ОПУХОЛЕВАЯ ВАКЦИНА, СОДЕРЖАЩАЯ АЛЛОГЕННЫЕ ИЛИ КСЕНОГЕННЫЕ ОПУХОЛЕВЫЕ КЛЕТКИ | 2007 |
|
RU2456997C2 |
| ЛИНИЯ КЛЕТОК PIGAS, СОДЕРЖАЩАЯ СТАБИЛЬНО ИНТЕГРИРОВАННЫЙ В ГЕНОМ САЙТ СВЯЗЫВАНИЯ ТРАНСКРИПЦИОННОГО ФАКТОРА STAT-1 | 2015 |
|
RU2619643C1 |
| БИНАРНАЯ ИММУНОЛИПОСОМАЛЬНАЯ НАНОСИСТЕМА АДРЕСНОЙ ДОСТАВКИ К КОННЕКСИН-43 ПОЛОЖИТЕЛЬНЫМ ОПУХОЛЕВЫМ КЛЕТКАМ | 2009 |
|
RU2422154C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2714932C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО НА ОСНОВЕ ИММУНОЛИПОСОМАЛЬНОЙ БИОЛОГИЧЕСКОЙ КОНСТРУКЦИИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ВЕКТОРНОЙ ДОСТАВКИ В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ ПРИ ОПУХОЛЕВОМ ПРОЦЕССЕ | 2007 |
|
RU2336901C1 |
| АУТОЛОГИЧНАЯ ВАКЦИНА ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2008 |
|
RU2392946C2 |
| ПРОТИВОРАКОВОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО В ФОРМЕ CAPE-НАГРУЖЕННЫХ МИКРОВЕЗИКУЛ НАПРАВЛЕННОГО ДЕЙСТВИЯ И СПОСОБ ЕГО РАЗРАБОТКИ | 2018 |
|
RU2785400C2 |
Изобретение относится к области биотехнологии, а именно к клеточной линии крысиной глиомы С6-DDA. Клеточная линия крысиной глиомы C6-DDA является устойчивой к цитотоксическому действию N-ацилдофаминов как тест-культура для изучения механизмов действия биоактивных липидов, получена на основе линии крысиной глиомы С6 и характеризуется невосприимчивостью к цитотоксическому действию дофаминамидов природных полиненасыщенных жирных кислот вплоть до концентрации 40 мкМ, наличием длинных или многочисленных коротких отростков и повышенной экспрессией маркеров астроцитарной дифференцировки GFAP, SOX2, гидролазы амидов жирных кислот FAAH, норадреналинового транспортера NET и оксидоредуктазы ecto-NOX, депонирована во Всероссийской коллекции промышленных микроорганизмов, регистрационный номер Н-173. 2 табл., 2 пр.
Клеточная линия крысиной глиомы C6-DDA, устойчивая к цитотоксическому действию N-ацилдофаминов как тест-культура для изучения механизмов действия биоактивных липидов, получена на основе линии крысиной глиомы С6 и характеризуется невосприимчивостью к цитотоксическому действию дофаминамидов природных полиненасыщенных жирных кислот вплоть до концентрации 40 мкМ, наличием длинных или многочисленных коротких отростков и повышенной экспрессией маркеров астроцитарной дифференцировки GFAP, SOX2, гидролазы амидов жирных кислот FAAH, норадреналинового транспортера NET и оксидоредуктазы ecto-NOX, депонирована во Всероссийской коллекции промышленных микроорганизмов, регистрационный номер Н-173.
| RU 2016149792 A, 22.06.2018 | |||
| БРЮХОВЕЧКИЙ И.С | |||
| "Гемопоэтические стволовые клетки с индуцированным апоптозом эффективно подавляют рост клеток глиомы in vitro, но запускают новый механизм образования опухолевых стволовых клеток", Гены & Клетки | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
Авторы
Даты
2019-07-17—Публикация
2017-11-20—Подача