Изобретение относится к области синтеза физиологически активных соединений и может найти применение при изготовлении фармакологических препаратов для лечения онкологических заболеваний.
Злокачественные новообразования устойчиво занимают второе место в структуре заболеваемости и смертности человека. Значительные усилия и средства направляются во всем мире на разработку новых подходов к терапии новообразований и поиск эффективных лекарственных средств. Однако проблема создания адекватного фармакологического инструментария для борьбы с онкологическими заболеваниями далека от своего решения. Ежегодно выходящие на рынок препараты для терапии данного заболевания оказываются либо чересчур специфичными для какого-то одного типа рака, и только на определенной стадии, либо слишком токсичными для организма пациента в целом. При этом разработке высокоэффективных препаратов препятствует высокая гетерогенность раковых структур и обилие мутаций в тех частях клетки, которые могли бы быть потенциальными мишенями терапии.
Существует два принципиально различных подхода к поиску новых противораковых агентов: синтез соединений, направленных на определенную мишень в раковых клетках, способных подавить их рост, и поиск новых цитостатических и цитотоксических агентов среди библиотек органических соединений. При втором подходе механизм антиракового действия вещества чаще всего исследуется после доказательства его эффективности в клинических исследованиях. Учитывая гетерогенность раковых клеток, новые соединения должны быть мультифункциональными, что позволит воздействовать на различные мишени, которые могут быть по-разному доступны в различных раковых клетках.
Производные тиадиазолов обладают сильной ароматичностью циклической системы, что приводит к их высокой стабильности in vitro. У этих соединений, как правило, отсутствует токсичность для высших позвоночных, включая человека. Присоединение к тиадиазольному ядру различных функциональных групп, способных реагировать с различными рецепторами, позволяет получить физиологически активные соединения с превосходными фармакологическими свойствами. Эти вещества проявляют фунгицидную, противобактерицидную, инсектицидную, гербицидную, противовоспалительную, нейростимулирующую и антиконвульсивную активность [N. Siddiqui, P. Ahuja, W. Ahsan, S.N. Pandeya, M.S. Alam // «Thiadiazoles: Progress Report on Biological Activities» Journal of Chemical and Pharmaceutical Research 2009, 1(1): 19-30]. Некоторые производные 1,2,4-тиадиазола могут быть основой препаратов для борьбы с болезнью Альцгеймера, заболеваниями сердечно-сосудистой системы [Gupta A., Mishra P., Pandeya S.N. et al. // Eur. J. Med. Chem. 2009. V.44. P.1100-1105]. Эти соединения обладают способностью связываться с рядом G-белоксопряженных рецепторов (опиодных, дофаминовых, аденозиновых) и могут выступать как противовоспалительные агенты [A. Castro, Т. Castano, A. Encinas. W. Porcal, С. Gil. Bioorg. Med. Chem. 2006, 14, 1644].
Авторам настоящего изобретения удалось обнаружить новые, ранее неизвестные физиологически активные свойства для производных 5-амино-3-(2-аминопропил)-[1,2,4]тиадиазола, а именно - высокую противораковую активность.
Изобретение направлено на решение задачи расширения арсенала средств, которые могут быть использованы в качестве новых и эффективных лекарств для лечения онкологических заболеваний.
Поставленная задача решается применением производных 5-амино-3-(2-аминопропил)-[1,2,4]тиадиазола общей формулы:
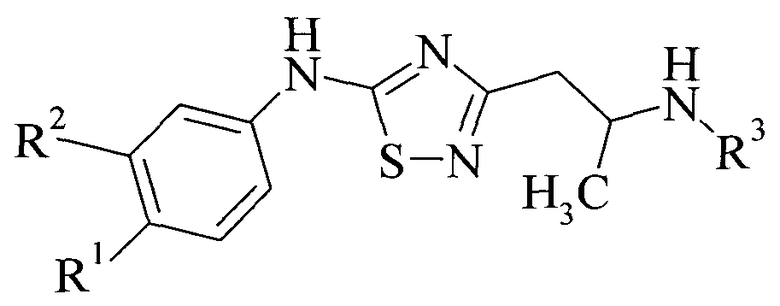 , где
, где
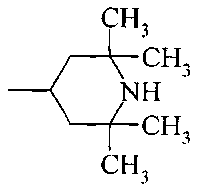
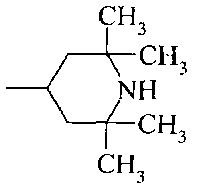
R1, R2 могут быть одинаковыми или различными и независимо означают водород, галоген, алкил;
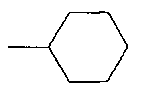
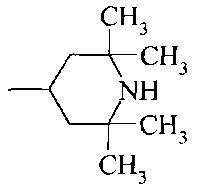
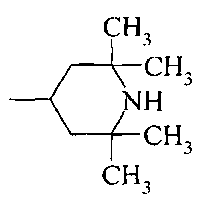
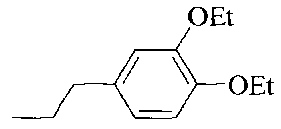
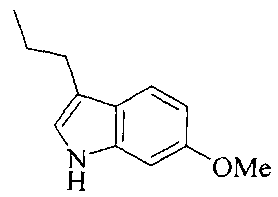
R3 означает алкил, аралкил, гетероаралкил, циклоалкил;
в виде оснований или фармакологически приемлемых солей.
Термин "галоген" означает хлор, фтор, бром или йод.
Термин "алкил" означает незамещенную или замещенную алкильную группу с прямой или разветвленной цепью, содержащую от 1 до 12 атомов углерода. Заместителями в алкильной группе могут быть галогены, гидрокси- и алкоксигруппы (например, метокси, этокси и аналогичные), циано, нитро, тригалогенметильные (например, трифторметил и аналогичные), необязательно замещенные аминогруппы (например, амино, диметиламино, ацетиламино, N-пиперидино, N-морфолино и аналогичные), ацильные группы (например, формил, ацетил, бензоил и аналогичные), карбоксамидные (например, N,N-диэтилкарбоксамидная и аналогичные), карбоксигруппы, карбалкоксигруппы и аналогичные.
Термин "аралкил" означает алкильную группу с концевым необязательно замещенным арильным заместителем.
Термин "гетероаралкил" означает гетероарил, к которому присоединена алкильная группа, охарактеризованная выше. Примеры подходящих заместителей включают необязательно замещенные этилиндол-3-ил, пропил-3-имидазол-1-ил.
Термин "циклоалкил" означает насыщенную необязательно замещенную циклическую группу с 3-8 кольцевыми атомами углерода, необязательно включающую гетероатомы N и О в количестве от 1 до 2 (например, циклопропил, циклогексил, пиперазинил, морфолинил).
Синтез указанных соединений описан ранее [Прошин А.Н., Бачурин С.О. Патент РФ №2449997, "5-Амино-3-(2-аминопропил)-[1,2,4]тиадиазолы", от 10.05.2012; Прошин А.Н., Серков И.В., Бачурин С.О. "Новые бинарные соединения на основе 1,2,4-тиадиазола" ДАН, 2012, 446, №1, с.48-50; Proshin A.N.; Serkov I.V.; Bachurm S.O., "5-Amino-[1,2,4]thiadiazole derivatives", WO 2012050484, Pub. 19.04.2012, EP 2628734, Pub 21.08.2013].
Способность изученных соединений оказывать цитотоксическое действие подтверждена на культурах раковых клеток крысиной глиомы С6 и человеческой остеосаркомы HOS. Во всех экспериментах указанные соединения проявляли умеренную или сильную цитостатическую активность и вызывали гибель раковых клеток в концентрациях от 2 до 100 мкМ.
Таким образом, применение производных 5-амино-3-(2-аминопропил)-[1,2,4] тиадиазола решает задачу расширения номенклатуры веществ, обладающих способностью ингибировать раковые клетки, т.к. ранее противораковые свойства этих соединений не были известны.
Методика эксперимента
1. Культивирование клеток
Клетки глиомы С6 крысы (клеточный банк Российской коллекции клеточных культур. Институт цитологии РАН, СПб) культивировали при температуре 37°C в атмосфере 5% CO2 в среде DMEM (ПанЭко, Россия), содержавшей 10% телячьей эмбриональной сыворотки (РАА Laboratories, США), 2 мМ глутамина, 25 мМ HEPES [6], 100 ед./мл пенициллина, 0.1 мг/мл стрептомицина и 0.25 мкг/мл амфотерицина В (ПанЭко, Россия).
Клетки человеческой остеосаркомы HOS (клеточный банк Российской коллекции клеточных культур. Институт цитологии РАН, СПб) культивировали при температуре 37°C в атмосфере 5% CO2 в среде Игла MEM с солями Эрла (ПанЭко, Россия), содержавшей 10% телячьей эмбриональной сыворотки (РАА Laboratories, США), 2 мМ аланилглутамина, 1 мМ пирувата натрия, набор заменимых аминокислот для среды MEM (ПанЭко, Россия), 100 ед./мл пенициллина, 0.1 мг/мл стрептамицина и 0.25 мкг/мл амфотерицина В (ПанЭко, Россия).
Прикрепленные клетки снимали с помощью 0.25% раствора трипсина в 0.53 мМ ЭДТА с солями Хэнкса (ПанЭко, Россия). Подсчет клеток выполняли с помощью камеры Горяева.
2. Определение ингибирующей активности веществ
Для анализа цитотоксичности исследуемых веществ культуры клеток рассеивали в 96-луночные планшеты в количестве 1.25×104 клеток/см2 и растили в течение трех дней до плотности 105 клеток/см2 (половина максимальной плотности клеток). Серийные разведения испытуемых веществ в диапазоне 0.1-100 мкМ (финальная концентрация после добавления к клеткам) готовили в ДМСО и растворяли в среде культивирования, после чего добавляли к культуре клеток (три повтора для каждой концентрации) и инкубировали 18 часов. Время инкубации выбирали, исходя из критерия наибольших различий между веществами. Финальная концентрация ДМСО составила 0.5%. К контролю добавляли только ДМСО в финальной концентрации 0.5%. Отдельно был поставлен контроль без ДМСО (нет различий с контролем с 0.5% ДМСО). Для оценки жизнеспособности клеток под действием исследуемых веществ использовали МТТ-тест (оценка восстановления красителя МТТ митохондриями живых клеток) [Mosmann Т. (1983) J. Immunol. Methods, 65, 55-63.]. После удаления среды с исследуемыми веществами клетки инкубировали 1.5 ч с 0.5 мг/мл раствором МТТ (ПанЭко, Россия) в растворе Хэнкса (ПанЭко, Россия). После этого раствор удаляли, растворяли клетки в ДМСО и оценивали количество восстановленного красителя фотометрически при длинах волн 574 и 620 нм с помощью аппарата Эфос 9505 (МЗ Сапфир, Россия). Дополнительно перед проведением МТТ-теста состояние клеток оценивали микроскопически. Каждый эксперимент повторяли три раза. Кривые для вычисления LD50 строили с помощью программы GraphPad Prism 5.0, в ней же проводили дисперсионный анализ данных с применением теста Тьюкея (Tukey). Достоверными считали отличия с p<0.05.
Ниже приведены результаты определения цитотоксической активности производных 5-амино-3-(2-аминопропил)-[1,2,4]тиадиазола и их солей на клетках глиомы С6 крысы (табл.1) и на клетках остеосаркомы человека HOS (табл.2), которые иллюстрируют, но не исчерпывают данное изобретение.
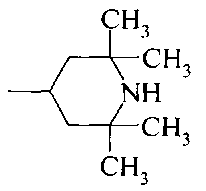
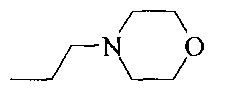
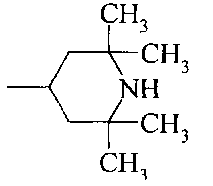



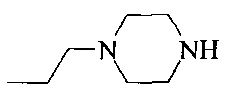

Как видно из этой таблицы, большинство соединений проявляет активность при концентрациях от 2 до 20 мкМ.
На данной линии клеток активность соединений находилась в пределах 13-50 мкМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| Новые лекарственные средства с цитотоксической активностью на основе производных азолоазинов для химиотерапии рака молочной железы | 2022 |
|
RU2814965C2 |
| Радиопротекторное, радиомитигаторное и радиосенсибилизирующее средство на основе натриевой соли аминодигидрофталазиндиона натрия (лекарственного препарата Тамерон) и других солей щелочных и щелочноземельных металлов аминодигидрофталазиндиона | 2022 |
|
RU2804886C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2714932C1 |
| 4-(2,4-ДИМЕТОКСИФЕНИЛ)-2-(2-ГИДРОКСИФЕНИЛ)-5,6-ДИГИДРО-4Н-БЕНЗО[H]ХРОМЕН-3-КАРБОНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2707972C1 |
| Средство, обладающее цитотоксической активностью в отношении культуры клеток глиомы U87MG | 2024 |
|
RU2839886C1 |
| СПОСОБ И КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКОВОГО ЗАБОЛЕВАНИЯ, ТОЗИЛАТ И ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ N-(4-ХЛОР-3-(ТРИФТОРМЕТИЛ)ФЕНИЛ)-N'-(4-(2-(N-МЕТИЛКАРБАМОИЛ)-4-ПИРИДИЛОКСИ)ФЕНИЛ)МОЧЕВИНЫ | 2002 |
|
RU2316326C2 |
| ОНКОГЕННОЕ RAS-СПЕЦИФИЧНОЕ ЦИТОТОКСИЧЕСКОЕ СОЕДИНЕНИЕ И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2448703C2 |
| ДЕЗОКСИПРОИЗВОДНЫЕ ЦИТИДИНА ИЛИ УРИДИНА ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ РАКА | 2020 |
|
RU2797489C2 |
| 2-(1,1-Диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополон, обладающий цитотоксической активностью по отношению к культуре клеток рака кожи А431 и рака легкого Н1299 | 2023 |
|
RU2810581C1 |
| Фармацевтическая композиция, проявляющая цитотоксичность в отношении клеток карциномы толстой кишки человека | 2020 |
|
RU2747147C1 |
Изобретение относится к применению в качестве цитостатических средств для борьбы с онкологическим процессом производных 5-амино-3-(2-аминопропил)-[1,2,4]тиадиазола общей формулы (I) в виде оснований или фармакологически приемлемых солей. В формуле (I) R1, R2 могут быть одинаковыми или различными и независимо означают водород, галоген, алкил, R3 означает алкил, аралкил, гетероаралкил, циклоалкил. 2 табл.
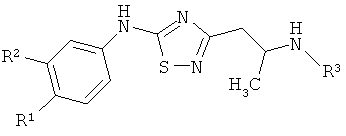 (I)
(I)
Применение в качестве цитостатических средств для борьбы с онкологическим процессом производных 5-амино-3-(2-аминопропил)-[1,2,4]тиадиазола общей формулы:
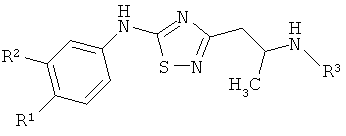 ,
,
где R1, R2 могут быть одинаковыми или различными и независимо означают водород, галоген, алкил;
R3 означает алкил, аралкил, гетероаралкил, циклоалкил;
в виде оснований или фармакологически приемлемых солей.
| 5-АМИНО-3-(2-АМИНОПРОПИЛ)-[1,2,4]ТИАДИАЗОЛЫ | 2011 |
|
RU2449997C1 |
| ПРОИЗВОДНЫЕ 2-АМИНО-1,3,4-ТИАДИАЗОЛА, ПРОЯВЛЯЮЩИЕ АНТИМЕТАСТАТИЧЕСКУЮ АКТИВНОСТЬ | 1995 |
|
RU2114109C1 |
| PROSHIN A | |||
| N., Novel binary compounds derived from 1,2,4-thiadiazole, Doklady Chemistry, 2012, 446(1), pp.171-173 | |||
| SERKOV I | |||
| V., Novel hybrid compounds based on amino derivatives of 1,2,4-thiadiazole and docosahexaenoic acid, Doklady Chemistry, 2012, 447(1), pp.238-240 | |||
Авторы
Даты
2014-12-27—Публикация
2013-12-03—Подача