Настоящее изобретение относится к области медицины, в частности, к области химико-фармацевтической промышленности и описывает пептиды, полученные из эзрина, в частности пептид, содержащий аминокислотную последовательность согласно общей формуле (I) X1EKKRRETVERE Х2Х3, где каждый X представляет собой остаток неполярной аминокислоты. Применение пептидов в качестве иммуностимулирующих агентов, а более конкретно, для применения в лечении и предотвращении противовирусных, антибактериальных и противогрибковых инфекций, и лечении заболеваний желудочно-кишечного тракта, в частности, язвенных расстройств желудочно-кишечного тракта. Настоящее изобретение также относится к фармацевтическим композициям, содержащим пептиды. Кроме того, изобретение относится к способам лечения инфекции и язвенных заболеваний желудочно-кишечного тракта, включающим введение пептидов пациентам, нуждающимся в этом.
Белок эзрин, также известный как цитовиллин или виллин-2, представляет собой белок, который кодируется у человека геном EZR. Пептиды, полученные из белка эзрина, обладающие биологической активностью, хорошо известны. Наиболее близкий аналог к пептиду согласно настоящему изобретению представляет собой фармацевтический тетрадекапептид NH2_Thr-Glu-Lys-Lys-Arg-Arg-Glu-Thr-Val-Glu-Arg-Glu-Lys-Glu_COOH, содержащий 14 аминокислотных остатков, который известен как пептид НЕР-1 или пептид эзрина человека один (последовательность ID No. 2: TEKKRRETVEREKE) и который разработали для лечения ВИЧ-инфекции [R.D. Holms, AIDS prophylactics. PCT/GB95/001285, 02.06.95, WO 95/33768] и, кроме того, для лечения широкого спектра бактериальных, грибковых и вирусных инфекций.
Лиофилизированный фармацевтический продукт GEPON® (номер регистрационного удостоверения: Р N000015/01-010911), содержащий примерно 96% пептида НЕР-1, широко используют для медицинских целей в Российской Федерации (Kladova, О.V., Kharlamova, F.S., Shcherbakova, А.А., Legkova, T.P., Feldfix, L.I., Znamenskaya, A.A., Ovchinnikova, G.S., Uchaikin, V.F. The first experience of Hepon intranasal application in children with respiratory infections. // Pediatrics, 2002, No. 2, pp. 86-88), (Polyakova Т.О., Magomedov, M.M., Artemyev, M.E., Surikov, E.V., Palchun, V.T. A new approach in the treatment of chronic diseases of the pharynx // Attending Doctor, 2002, No. 4, pp. 64-65), (Novokshonov, A.A., Uchaikin, V.F., Sokolova, N.V., Tikhonova, O.N., Portnykh, О. Yu. Biocenosis-protecting therapy of intestinal infections in children. // Russian Medical Journal, special supplement "Diseases of the Digestive System", 2004, volume 6, No. 1), (Parfenov, A.I. The activator of the local immunity Hepon in the complex treatment of dysbiotic disorders of the intestine. // Experimental and Clinical Gastroenterology, 2003, №3, pp. 66-69), (Tishchenko, A.I. A new approach in the treatment of recurrent urogenital candidiasis. // Attending Doctor, 2002, No. 3, pp. 46-47), (Telunts, A.V. Treatment of candidiasis in infants. // Questions of Gynecology, Obstetrics, and Perinatology, 2004, vol. 3, No. 4, pp. 89-90), (Ataullakhanov, R.I., Holms, R.D., Katlinsky, A.V., Pichugin A.V., Papuashvili, M.N., Shishkova, N.M. Treatment with Hepon immunomodulator increases the efficacy of the immune control of opportunistic infections in HIV-infected patients. // Allergy, Asthma, and Clinical Immunology, 2002, No. 10, pp. 3-11), (Cherednichenko, T.V., Uchaikin, V.F., Chaplygina, G.V., Kurbanova, G.M. A new efficient treatment of viral hepatitis. // Attending Doctor, 2003, No. 3, pp. 82-83), (Gorbarets, I.P., Voronkova, N.V., lopatina, T.V, Ivanovskaya, V.N., Braginsky, D.M., Blokhina, N.P., Malyshev, N.A. The combined use of Hepon drug product and recombinant interferon-alpha in the patients with chronic hepatitis С increases the efficiency of antiviral treatment and reduces side effects of the therapy // Hepatology, 2003, No. 4, pp. 23-28), (Lazebnik, L.В., Zvenigorodskaya, L.A., Firsakova, V.Yu., Pichugin, A.V., Ataullakhanov, R.I. The application of Hepon immunomodulator in the treatment of erosive ulcerous lesions of gastroduodenal zone. // Experimental and Clinical Gastroenterology, 2003, No. 3, pp. 17-20), (Malakhova, N.S., Pichugin, A.V., Khalif I.L., Ataullakhanov, R.I. The application of Hepon immunomodulator for the treatment of nonspecific ulcerative colitis // Farmateka, 2005, No. 6 [101], pp. 105-108), Dudchenko, M.A., Lysenko, B.F., Chelishvili, A.L., Katlinsky, A.V., Ataullakhanov, R.R. Complex treatment of trophic ulcers. // Attending Doctor, 2002, No. 10, pp. 72-75), (Bardychev, M.S. Treatment of local radiation injuries with the activator of local immunity. // Russian Medical Journal, 2003, volume 11, No. 11 (183), pp. 646-647), Salamov G., R. Holms, W. Bessler, R. Ataullakhanov. Treatment of hepatitis С virus infection with human ezrin peptide one (HEP1) in HIV infected patients // Arzneimittel-Forschung (Drug Research) 2007; 57(7): 497-504].
НЕР-1 обладает биологической активностью против вируса гепатита С и может применяться для лечения пациентов с гепатитом С [R.D. Holms, R.I. Ataullakhanov. HCV combination therapy. PCT/GB2004/000330, 27.01.2004, WO 2004067024 А2].
НЕР-1 обладает противоязвенной биологической активностью и может быть использован для лечения язвенных заболеваний желудочно-кишечного тракта [R.D. Holms, I. Ataullakhanov. The use of peptides in anti-ulcer therapy. PCT/GB2006/004390, 23.11.2006, WO/2007/060440].
Авторы настоящего изобретения разработали новый пептид, который получили синтетически и который обладает высокой иммуностимулирующей активностью. Как показали биологические исследования, указанный пептид согласно настоящему изобретению, как описано, и содержащие указанный пептид фармацевтические композиции обладают высокой иммуностимулирующей активностью, превышающей активность пептида НЕР-1, который является основным компонентом лекарственного продукта GEPON®.
Согласно первому аспекту настоящего изобретения, предложен пептид, содержащий аминокислотную последовательность согласно общей формуле (I) X1EKKRRETVEREX2X3, где каждый из X1, Х2 и Х3 представляет собой остаток неполярной аминокислоты (SEQ ID NO: 5).
Остатки неполярных аминокислот могут быть независимо выбраны из группы, состоящей из глицина, аланина, валина, лейцина, метионина, изолейцина, пролина, фенилаланина и триптофана, и/или их комбинациий.
В некоторых вариантах реализации X1, Х2 и/или Х3 могут быть независимо выбраны из неполярных аминокислот, имеющих небольшие R-группы, в частности глицина, аланина и/или валина и/или их комбинаций. Таким образом, согласно некоторым вариантам реализации настоящего изобретения каждый из X1, Х2 и Х3 является независимо выбранным из группы, состоящей из глицина, аланина и валина.
В некоторых вариантах реализации X1, Х2 и/или Х3 все могут быть одной и той же аминокислотой. В предпочтительном варианте реализации по меньшей мере один из X1, Х2 и Х3 представляет собой глицин. В более предпочтительном варианте реализации по меньшей мере 2 из X1, Х2 и Х3 представляют собой глицин. В наиболее предпочтительном варианте реализации каждый из X1, Х2 и Х3 представляет собой глицин. В одном из вариантов реализации пептид содержит аминокислотную последовательность согласно общей формуле (I) X1 EKKRRETVERE Х2Х3, где каждый из X1, Х2 и Х3 является неполярным, и, кроме того, где по меньшей мере один, или по меньшей мере два, из X1, Х2 и Х3 являются глицином. В предпочтительном варианте реализации пептид имеет последовательность GEKKRRETVEREGG.
В настоящем описании, применяются однобуквенные коды для обозначения различных аминокислот. Используя трехбуквенные или однобуквенные коды, аминокислоты могут также быть упомянуты следующим образом: глицин (G или Gly), аланин (А или Ala), валин (V или Val), лейцин (L или Leu), изолейцин (I или Ile), пролин (Р или Pro), фенилаланин (F или Phe), тирозин (Y или Tyr), триптофан (W или Trp), лизин (К или Lys), аргинин (R или Arg), гистидин (Н или His), аспарагиновая кислота (D или Asp), глутаминовая кислота (Е или Glu), аспарагин (N или Asn), глутамин (Q или Gln), цистеин (С или Cys), метионин (М или Met), серии (S или Ser) и треонин (Т или Thr). В случае, когда остаток может представлять собой аспарагиновую кислоту или аспарагин, могут использоваться обозначения Asx или В. В случае, когда остаток может представлять собой глутаминовую кислоту или глутамин, могут использоваться обозначения Glx или Z. Ссылки на аспарагиновую кислоту включают аспартат, и на глутаминовую кислоту включают глютамат, если контекст не указывает на иное.
Термин пептид может включать композиции, содержащие аминокислотные последовательности, раскрытые в настоящем описании. Например, пептиды могут быть модифицированы (например, на С или N концах) для обеспечения их защиты от разрушения или увеличения их биологической доступности и/или биологической совместимости, если специалист сочтет это надлежащим или необходимым. Следует отметить, что характеристики, относящиеся к "пептиду согласно настоящему изобретению" в равной степени применимы к аминокислотной последовательности, указанной в общих формулах.
Пептид согласно настоящему изобретению может быть любой длины в случае, если аминокислотная последовательность содержит общую формулу (I) X1EKKRRETVEREX2X3, где каждый X представляет собой остаток неполярной аминокислоты, как описано в настоящем описании.
В некоторых вариантах реализации, пептид содержит от 14 до 25 остатков в длину, например, от 14 до 20 остатков в длину, или от 14 до 18 остатков в длину и содержит аминокислотную последовательность согласно общей формуле (I) (или его далее определенных вариантов реализации). В некоторых вариантах реализации, пептид содержит 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 остатков в длину и содержит аминокислотную последовательность согласно общей формуле (I) (или его далее определенных вариантов реализации). В других вариантах реализации, пептид содержит от 14 до 25 остатков в длину, например, от 14 до 20 остатков в длину, или от 14 до 18 остатков в длину и содержит последовательность, соответствующую SEQ ID No: 1 (GEKKRRETVEREGG). В некоторых вариантах реализации, пептид содержит 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 остатков в длину и содержит последовательность, соответствующую SEQ ID No: 1 (GEKKRRETVEREGG). В одном из вариантов реализации, пептид содержит между 14 и 18 остатков в длину и содержит аминокислотную последовательность согласно общей формуле (I) X1 EKKRRETVERE Х2Х3, где каждый из X1, Х2 и Х3 является неполярным, и, кроме того, где по меньшей мере два из X1, Х2 и Х3 являются глицином. В предпочтительных вариантах реализации, пептид согласно настоящему изобретению содержит по меньшей мере 14 аминокислот в длину и содержит SEQ ID No: 1 (GEKKRRETVEREGG).
Предпочтительно, пептид согласно настоящему изобретению содержит 14 аминокислотных остатков в длину. В наиболее предпочтительном варианте реализации согласно настоящему изобретению, пептид имеет последовательность NH2_Gly-Glu-Lys-Lys-Arg-Arg-Glu-Thr-Val-Glu-Arg-Glu-Gly-Gly_COOH (последовательность ID No.1: GEKKRRETVEREGG) (в настоящем описании упоминается как HP-V2).
Целью настоящего изобретения является расширение диапазона пептидных соединений, обладающих улучшенной иммуностимулирующей активностью. Более того, задачей настоящего изобретения является получение фармацевтической композиции с наивысшей иммуностимулирующей активностью и широким спектром действия на основе заявленного пептида и известных пептидов эзрина. В целом, пептиды согласно настоящему изобретению имеют более высокий иммуностимулирующий профиль и/или более высокую противовирусную активность по сравнению с пептидами, содержащими или состоящими из SEQ ID NO: 2. Иммуностимуляция и противовирусная активность могут быть измерены любым способом, известным специалисту в данной области. Например, иммунологическая активность пептида может быть оценена по воздействию на синтез мРНК цитокина в клетках J-96 (например, интерферона альфа (IFN-α), интерлейкина 1 бета (IL-1β) и интерлейкина шесть (IL-6)). Противовирусная активность поддается измерению по цитотоксическому воздействию на вирус энцефаломиокардита (ЕСМ) и/или по половине максимально ингибирующей концентрации (IC50) для пептида в процессе ингибирования репликации вируса ЕМС. Другие методы будут очевидны для специалиста в данной области.
Желаемая цель может быть достигнута при помощи предлагаемого нового пептида, содержащего последовательность согласно формуле (I), и его производных как описано в настоящем описании, и более конкретно последовательность, соответствующую SEQ ID No. 1: GEKKRRETVEREGG. Данные пептиды согласно настоящему изобретению получают синтетическим способом, и они обладают высокой иммуностимулирующей активностью. Поиск пептидных последовательностей в базе данных по адресу http://research.bioinformatics.udel.edu/peptidematch/index.jsp и поиск белковых последовательностей в базе данных по адресу http://www.uniprot.org/blast/ подтвердил новизну пептида (HP-V2), содержащего 14 аминокислотных остатков (последовательность ID No. 1: GEKKRRETVEREGG).
Как показали биологические исследования, пептид согласно настоящему изобретению и его фармацевтические композиции обладают высокой иммуностимулирующей активностью, превышающую активность пептида НЕР-1, который является основным компонентом лекарственного продукта GEPON®.
Известный пептид эзрина НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE), и два меньших пептида: пептид HP 1-5 согласно формуле NH2_Thr-Glu-Lys-Lys-Arg_COOH (последовательность ID No. 3: TEKKR), далее обозначаемый как НР1-5, и пептид НР6-14 согласно формуле NH2_Arg-Glu-Thr-Val-Glu-Arg-Glu-Lys-Glu_COOH (последовательность ID No. 4: RETVEREKE) далее обозначаемый как НР6-14, применяли для приготовления фармацевтических композиций с пептидом согласно настоящему изобретению. Последние два пептида представляют собой продукты расщепления пептида НЕР1 (последовательность ID No. 2: TEKKRRETVEREKE) и имеют последовательности, которые идентичны описанным ранее [R.D. Holms. Regulatory/unfolding peptides of ezrin. PCT/GB00/03566, 15.09.2000, WO 01/025275]. Пептид HP1-5 и пептид HP6-14 представляют собой два спутниковых пептида, которые были обнаружены в лекарственном продукте GEPON® в качестве примесей.
В некоторых вариантах реализации, пептид согласно настоящему изобретению может быть объединен с НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE) или с пептидом HP 1-5 согласно формуле NH2_Thr-Glu-Lys-Lys-Arg_COOH (последовательность ID No. 3: TEKKR), далее обозначаемый как HP1-5, или с пептидом НР6-14 согласно формуле NH2_Arg-Glu-Thr-Val-Glu-Arg-Glu-Lys-Glu_COOH (последовательность ID No. 4: RETVEREKE), далее обозначаемый как НР6-14.
Пептиды согласно настоящему изобретению и комбинации пептидов, описанные в настоящем описании, могут быть подходящими для применения в медицине, например, для применения для лечения и предотвращения вирусных, бактериальных и грибковых инфекций, а также для лечения язвенных заболеваний слизистых оболочек и мягких тканей.
Согласно второму аспекту настоящего изобретения, предложен пептид согласно настоящему изобретению (такой как пептид согласно общей формуле (I), в частности пептид, содержащий аминокислотную последовательность, соответствующую SEQ ID No: 1), для применения в медицине. Конкретные медицинские применения включают лечение или предотвращение инфекции. Инфекция может являться вирусной, бактериальной или грибковой инфекцией. Другие варианты реализации настоящего изобретения включают лечение или предотвращение изъязвления слизистых оболочек кишечника, таких как язв желудка, толстой кишки, двенадцатиперстной кишки или тонкой кишки, а также лечение или предотвращение воспалительных заболеваний кишечника, в том числе заболеваний и/или расстройств, связанных с язвами желудка, толстой кишки, двенадцатиперстной кишки или тонкой кишки и синдромом раздраженного кишечника (IBS). Пептиды согласно настоящему изобретению также предложены для применения для лечения или предотвращения неспецифического язвенного колита и болезни Крона. В предпочтительных вариантах реализации, пептиды согласно настоящему изобретению предложены для применения для лечения или предотвращении воспалений и/или изъявлений нижней части кишечника.
Также предложен пептид согласно настоящему изобретению (такой как пептид согласно общей формуле (I), в частности пептид, содержащий аминокислотную последовательность, соответствующую SEQ ID No: 1), для применения в стимулировании иммунного ответа у субъекта. В некоторых вариантах реализации настоящего изобретения, пептиды могут применяться для стимулирования выработки эндогенного интерферона у субъекта. Пептиды могут быть также применены для стимулирования активации MAPK/ERK сигнального пути.
В некоторых вариантах реализации настоящего изобретения, пептид согласно настоящему изобретению может быть объединен с пептидом НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE), или с пептидом HP1-5 согласно формуле NH2_Thr-Glu-Lys-Lys-Arg COOH (последовательность ID No. 3: TEKKR), далее обозначаемый как HP 1-5, или с пептидом НР6-14 согласно формуле NH2_Arg-Glu-Thr-Val-Glu-Arg-Glu-Lys-Glu_COOH (последовательность ID No. 4: RETVEREKE), далее обозначаемый как НР6-14. Например, пептид согласно общей формуле (I), в частности пептид, содержащий аминокислотную последовательность соответствующую SEQ ID No: 1, может быть объединен с одним или несколькими соответствующим SEQ ID No: 2, 3 или 4. Такие комбинации являются подходящими для применения в медицинских аспектах согласно настоящему изобретению, включая лечение и предотвращение инфекции. Инфекция может являться вирусной, бактериальной или грибковой инфекцией. Комбинации пептидов также являются подходящими для применения для лечения или предотвращении изъязвления слизистых оболочек кишечника, таких как язв желудка, толстой кишки, двенадцатиперстной кишки или тонкой кишки, а также для лечения или предотвращении воспалительных заболеваний кишечника, в том числе заболеваний и/или расстройств, связанных с язвами желудка, толстой кишки, двенадцатиперстной кишки или тонкой кишки и синдромом раздраженного кишечника (IBS). Пептиды согласно настоящему изобретения также предложены для применения для лечения или предотвращения язвенного колита и болезни Крона. В предпочтительных вариантах реализации, комбинации пептидов согласно настоящему изобретению предложены для применения для лечения или предотвращения воспаления и/или изъявления нижней части кишечника.
Дополнительно, варианты реализации настоящего изобретения распространяются на способы лечения или предотвращения инфекций, язв желудка, толстой кишки, двенадцатиперстной кишки или тонкой кишки, заболеваний и/или расстройств, связанных с язвами желудка, толстой кишки, двенадцатиперстной кишки или тонкой кишки, синдромом раздраженного кишечника (IBS), неспецифическим язвенным колитом и болезнью Крона, включающим введение пептида согласно настоящему изобретению (такого как пептида согласно общей формулы (I), в частности пептида, содержащего аминокислотную последовательность соответствующую SEQ ID No: 1) пациенту, нуждающемуся в этом. Инфекция может являться вирусной, бактериальной или грибковой инфекцией. Пептиды согласно настоящему изобретению вводят в терапевтически эффективном количестве и могут быть введены с одним или несколькими другими активными фармацевтическими соединениями. В частности, пептиды согласно настоящему изобретению могут быть введены в комбинации с одним или несколькими из пептидов соответствующим SEQ ID No: 2, 3 и/или 4.
Таким образом, также предложена комбинация пептида согласно настоящему изобретению (такой как пептид согласно общей формуле (I), в частности, пептид, содержащий аминокислотную последовательность, соответствующую SEQ ID No: 1) и пептида, содержащего аминокислотную последовательность соответствующую SEQ ID No: 2, 3, или 4, для применения в медицине. Такие медицинские применения включают лечение или предотвращение инфекций (таких как вирусных, бактериальных или грибковых инфекций), изъязвления слизистых оболочек кишечника (например, язв желудка, язв толстой кишки, язв двенадцатиперстной кишки и язв тонкой кишки), или воспалительных заболеваний кишечника или болезни или расстройства, связанного с воспалительным заболеванием кишечника (например, IBS, неспецифическим язвенным колитом или болезнью Крона). В предпочтительных вариантах реализации, пептиды согласно настоящему изобретению предложены для применения для лечения или предотвращения воспаления и/или изъявления нижней части кишечника. Такие медицинские применения также включают стимуляцию иммунного ответа у субъекта.
В предпочтительных вариантах реализации, когда пептиды согласно настоящему изобретению применяют в комбинации с НЕР-1, HP 1-5 или НР6-14, дополнительный пептид состоит из аминокислотной последовательности, соответствующей SEQ ID No: 2, 3, или 4.
Также предложен способ стимуляции иммунного ответа у субъекта, включающий введение терапевтически эффективного количества пептида согласно настоящему изобретению (такой как пептид согласно общей формуле (I), в частности, пептид, содержащий аминокислотную последовательность, соответствующую SEQ ID No: 1) пациенту, нуждающемуся в этом.
Согласно третьему аспекту настоящего изобретения, предложена фармацевтическая композиция, содержащая пептид согласно настоящему изобретению и фармацевтически приемлемый носитель или наполнитель. В некоторых вариантах реализации согласно настоящему изобретению, фармацевтическая композиция может дополнительно содержать дополнительное фармацевтически активное соединение. В частности, фармацевтическая композиция может дополнительно содержать НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE), HP 1-5 (последовательность ID No. 3: TEKKR), или HP6-14 (последовательность ID No. 4: RETVEREKE).
Соответственно, в одном из вариантов реализации, настоящее изобретение обеспечивает фармацевтическую композицию, содержащую пептид, содержащий между 14 и 18 остатков в длину, пептид, содержащий аминокислотную последовательность, имеющую последовательность X1 EKKRRETVERE Х2Х3, где каждый из X1, Х2 и Х3 является неполярным, и, кроме того, где по меньшей мере два из X1, Х2 и Х3 являются глицином, и фармацевтически приемлемый носитель или наполнитель.
Фармацевтические композиции согласно настоящему изобретению могут содержать другие фармацевтически активные вещества, такие как противовирусные, антибактериальные, противогрибковые, обезболивающие и/или противовоспалительные вещества. Фармацевтическая композиция может быть получена с использованием любого удобного адъюванта и/или его физиологически приемлемых разжижителей.
Наполнители, носители, консерванты и стабилизаторы, которые обычно применяют специалисты в области доставки лекарственного средства, могут применяться в качестве приемлемого носителя или наполнителя для приготовления предлагаемых фармацевтических композиций. Для инъекций, преимущественно используют дистиллированную воду или физиологический раствор.
Фармацевтическая композиция может быть приспособлена для введения любым подходящим способом, например, пероральным (в том числе через щеку или подъязычно), ректальным, назальным, местным (в том числе через щеку, подъязычно или через кожу), вагинальным или парентеральным (включая подкожный, внутримышечный, внутривенный или внутрикожный) способом. Такие композиции могут быть получены любым способом, известным в области фармации, например, путем смешивания активного ингредиента с носителем(ями) или вспомогательным веществом(ами) в стерильных условиях. В конкретных вариантах реализации, фармацевтическая композиция согласно настоящему изобретению, содержащая пептиды согласно настоящему изобретению, представлена в виде таблетки для перорального введения, такой как таблетка глюкозы. В некоторых вариантах реализации, таблетка является растворимой.
Фармацевтические композиции, приспособленные для перорального введения, могут быть представлены в виде отдельных единиц, таких как капсул или таблеток; в виде порошков или гранул; в виде растворов, сиропов или суспензий (в водных или неводных жидкостях, или в качестве пищевых пен или взбитой массы, или в виде эмульсий). В предпочтительных вариантах реализации, фармацевтическая композиция согласно настоящему изобретению, содержащая пептиды согласно настоящему изобретению, представлена в виде таблетки для перорального введения, такой как таблетка глюкозы. В некоторых вариантах реализации, таблетка является растворимой.
В некоторых вариантах реализации настоящего изобретения, пептиды представлены в виде лиофилизированного порошка или гранул.
Подходящие вспомогательные вещества для таблеток или твердых желатиновых капсул включают в себя лактозу, кукурузный крахмал или его производные, стеариновую кислоту или ее соли. Подходящие вспомогательные вещества для применения с мягкими желатиновыми капсулами включают в себя, например, растительные масла, воски, жиры, полутвердые или жидкие полиолы и т.д.
Для приготовления растворов и сиропов, вспомогательные вещества, подходящие для применения, включают в себя, например, воду, полиолы и сахара. Для приготовления суспензий масла (например, растительное масло) могут применяться для получения суспензий типа "масло в воде" или "вода в масле".
Фармацевтические композиции, приспособленные для введения через кожу, могут быть представлены в виде отдельных пластырей, предназначенных для того, чтобы оставаться в тесном контакте с эпидермисом реципиента в течение длительного периода времени. Например, активный ингредиент может быть доставлен из пластыря путем ионофореза, как описано в Pharmaceutical Research, 3 (6), стр. 318 (1986).
Фармацевтические композиции, приспособленные для местного введения, могут быть приготовлены в виде мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел. Для инфекции глаза или других внешних тканей, например рта и кожи, композиции подходящим образом применяют в качестве мази для местного применения или крема. При приготовлении в виде мази, активный ингредиент может быть использован либо с парафиновой, либо с водорастворимой мазевой основой. В качестве альтернативы, активный ингредиент может быть приготовлен в виде крема с основой для крема по типу "масло в воде" или "вода в масле". Фармацевтические композиции, приспособленные для местного введения в глаз, включают глазные капли, в которых активный ингредиент растворен или суспендирован в подходящем носителе, особенно в водном растворителе. Фармацевтические композиции, приспособленные для местного введения в рот, включают леденцы, пастилки и жидкости для полоскания рта.
Фармацевтические композиции, приспособленные для ректального введения, могут быть представлены в виде суппозиториев или клизм.
Фармацевтические композиции, адаптированные для назального введения, в которых носитель представляет собой твердое вещество, включают крупный порошок, имеющий размер частиц, например, в диапазоне от 20 до 500 мкм. Подходящие композиции, в которых носитель представляет собой жидкость, для введения в виде назального спрея или в виде назальных капель, включают водные или масляные растворы активного ингредиента.
Фармацевтические композиции, приспособленные для введения путем ингаляции, включают мелкодисперсные пудры или аэрозоли, которые могут быть образованы посредством различных типов дозированных под повышенным давлением аэрозолей, распылителей или инсуффляторов.
Фармацевтические композиции, приспособленные для вагинального введения, могут быть представлены в виде вагинальных суппозиториев, тампонов, кремов, гелей, паст, пен или составов для распыления.
Фармацевтические композиции, приспособленные для парентерального введения включают водный и неводный стерильный инъекционный раствор, который может содержать антиоксиданты, буферы, бактериостатические агенты и растворенные вещества, которые делают состав по существу изотоническим крови предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты и загустители. Вспомогательные вещества, которые могут применяться в инъекционных растворах, включают, например, воду, спирты, полиолы, глицерин и растительные масла. Композиции могут быть представлены в упаковках на один прием или для многократного приема, например в запаянных ампулах и флаконах, и могут храниться в высушенном сублимацией (лиофилизированном) состоянии, требующем только добавления вводимой стерильной жидкости, например, воды для инъекций, непосредственно перед использованием. Приготовленные по индивидуальному рецепту растворы и суспензии для инъекций могут быть приготовлены из стерильных порошков, гранул и таблеток.
Фармацевтические композиции могут содержать консерванты, повышающие растворимость агенты, стабилизирующие агенты, увлажняющие агенты, эмульгаторы, подсластители, красители, отдушки, соли (вещества согласно настоящему изобретению сами по себе могут быть представлены в виде фармацевтически приемлемой соли), буферы, покрывающие агенты или антиоксиданты. Они также могут содержать терапевтически активные агенты в дополнение к веществу согласно настоящему изобретению.
Дозировка фармацевтических композиций согласно настоящему изобретению может варьироваться в широких пределах, зависящих от заболевания или расстройства, подлежащего лечению, возраста и состояния индивидуума, подлежащего лечению, и т.д., и в конечном итоге врач будет определять подходящие дозировки для применения.
Такие композиции могут быть приготовлены для человека или для ветеринарной медицины. Настоящую заявку следует толковать как применяющуюся в равной степени как для человека, так и животных, если контекст явно не подразумевает иное.
Согласно одному варианту реализации, настоящее изобретение обеспечивает фармацевтическую композицию в виде таблетки для перорального введения, в частности таблетки глюкозы, содержащей пептид, содержащий от 14 до 18 остатков в длину, пептид, содержащий аминокислотную последовательность, имеющую последовательность X1 EKKRRETVERE Х2Х3, где каждый из X1, Х2 и Х3 является неполярными, и, кроме того, где по меньшей мере два из X1, Х2 и Х3 являются глицином, и фармацевтически приемлемый носитель или наполнитель. В более предпочтительном варианте реализации, пептид имеет последовательность GEKKRRETVEREGG.
Изобретение включает способы получения подходящих фармацевтических композиций, а также применение пептида согласно настоящему изобретению в получении лекарственного средства для применения в медицине, для применения в любом из видов применений, указанных в настоящем описании.
Согласно другому аспекту настоящего изобретения, предложена последовательность нуклеиновой кислоты, кодирующая пептид согласно настоящему изобретению, в частности пептид согласно общей формуле I, такой как пептид, содержащий аминокислотную последовательность, соответствующую SEQ ID No: 1 или SEQ ID No: 5.
Нуклеиновая кислота может представлять собой ДНК, кДНК или РНК, такую как мРНК, полученную путем клонирования или путем химического синтеза. ДНК может быть одноцепочечной или двухцепочечной. Одноцепочечная ДНК может являться кодирующей смысловой нитью или может являться некодирующей или антисмысловой нитью.
Согласно еще одному дополнительному аспекту настоящего изобретения предложен вектор, содержащий нуклеиновую кислоту согласно настоящему изобретению. Согласно еще одному дополнительному аспекту настоящего изобретения предложена клетка-хозяин, содержащая вектор согласно настоящему изобретению. Способы производства или получения таких нуклеиновых кислот, векторов и клеток-хозяев также включены в настоящее изобретение и известны в данной области техники.
Пептид по настоящему изобретению может быть синтезирован при помощи синтетической пептидной химии, например, пептид согласно настоящему изобретению может быть синтезирован при помощи жидкофазного синтеза (Combinatorial Chemistry: A Practical Approach, ed. Hicham Fenniri, Oxford University Press (2000)) с использованием стандартной процедуры или при помощи твердофазного синтеза, например, синтеза "Fmoc" или "Bmoc", (Fmoc Solid Phase Peptide Synthesis: A Practical Approach (Practical Approach S.), ed.s W. Chan &, Peter White, Oxford University Press (2000)) Когда используется твердофазный синтез, то используется твердая фаза, такая как полистирольная смола или полиамидная смола или ПЭГ (полиэтиленгликольная) гибридная полистирольная смола или смола на основе ПЭГ (полиэтиленгликоля). Различные защитные группы используются в процессе синтеза, например, N-концевые защитные группы, трет-бутилоксикарбонильные (t-Boc) или 9-фторфенилметилоксикарбонильные (Fmoc) защитные группы. Кроме того, могут быть использованы бензилоксикарбонильные (Z) группы или аллилоксикарбонильные (Alloc) защитные группы, или удаляемые светом (литографические) защитные группы, или может быть использован метод защиты боковых групп. Пептидные продукты очищают при помощи ВЭЖХ разделения или любым другим способом очистки. Структура пептида подтверждена при помощи аминокислотного анализа, масс-спектрометрии, а также данными высокоэффективной жидкостной хроматографии.
В некоторых случаях, фрагменты могут быть синтезированы с использованием твердотельных методов, и далее в сочетании друг с другом в растворе. Пептиды могут быть синтезированы от стороны карбонильной группы до стороны аминогруппы в аминокислотной цепи в указанном способе, хотя пептиды синтезируются в обратном направлении в клетках. В таких способах, аминозащищенная аминокислота связана с шариком субстрата (т.е. шариком смолы), образуя ковалентную связь между карбонильной группой и смолой. С аминогруппы затем снимают защиту и подвергают взаимодействию с карбонильной группой следующей аминозащищенной аминокислоты. Цикл повторяют так часто, как это требуется для того, чтобы сформировать желаемую пептидную цепь. Синтезированный пептид затем отщепляют от шарика в конце процедуры. Защитные группы для аминогрупп в основном используемые в указанном синтезе пептидов представляют собой 9-фторфенилметилоксикарбонильную группу ("Fmoc") и трет-бутилоксикарбонил ("Вос"). Группу Fmoc удаляют с амино-конца с основанием, в то время как Boc группу удаляют с кислотой.
Пептид НЕР-1, пептид HP1-5 и пептид НР6-14, используемые в настоящем изобретении для приготовления фармацевтических композиций, были приготовлены при помощи способа жидкофазного синтеза лицензированным изготовителем ООО "Иммафарма" (Москва).
Согласно другому аспекту настоящего изобретения, предложен способ получения пептидов согласно настоящему изобретению, в частности пептидов согласно общей формуле 1, таких как пептиды, содержащие аминокислотную последовательность соответствующую SEQ ID No: 1 или SEQ ID No: 5. Способ может включать синтез пептидов при помощи жидкофазного синтеза или твердофазного синтеза.
Согласно одному варианту реализации настоящего изобретения, предложен пептид, состоящий из 14 аминокислот в длину, где аминокислотная последовательность представляет собой GEKKRRETVEREGG. Пептид является подходящим для применения в медицине, в частности в лечении изъязвления и/или воспаления нижней части кишечника. Пептид может быть представлен в виде таблетки для перорального введения, в частности таблетки глюкозы.
Предпочтительные признаки для второго и последующих аспектов указанного изобретения являются такими же, как для первого аспекта с соответствующими изменениями.
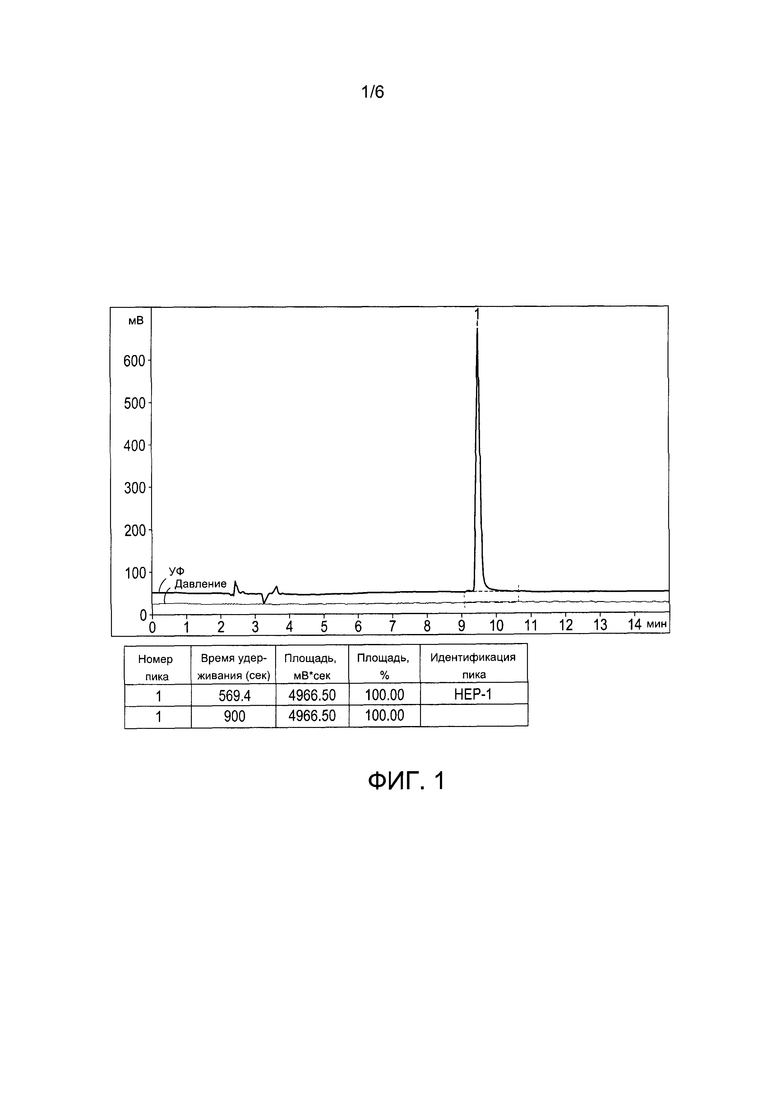
Настоящее изобретение далее будет описано путем ссылки на следующие примеры, которые присутствуют только для справочных целей и не должны быть истолкованы как ограничивающие изобретение. В примерах ссылки сделаны на ряд чертежей, на которых: Фигура 1. Высокоэффективная жидкостная хроматография пептида НЕР-1. Колонка Luna С18 (2), 4,6×250 мм, частицы 5,0 мкм. Подвижная фаза: А - вода, 5% ацетонитрила (ACN), 0,1% ТФУ; В - 0,1% ТФУ; программа 5-25% ACN в течение 20 мин. Скорость потока: 1 мл/мин. Х-ось: время, Y-ось: поглощение УФ (мВ, верхняя линия, с пиками), давление (нижняя, горизонтальная линия).
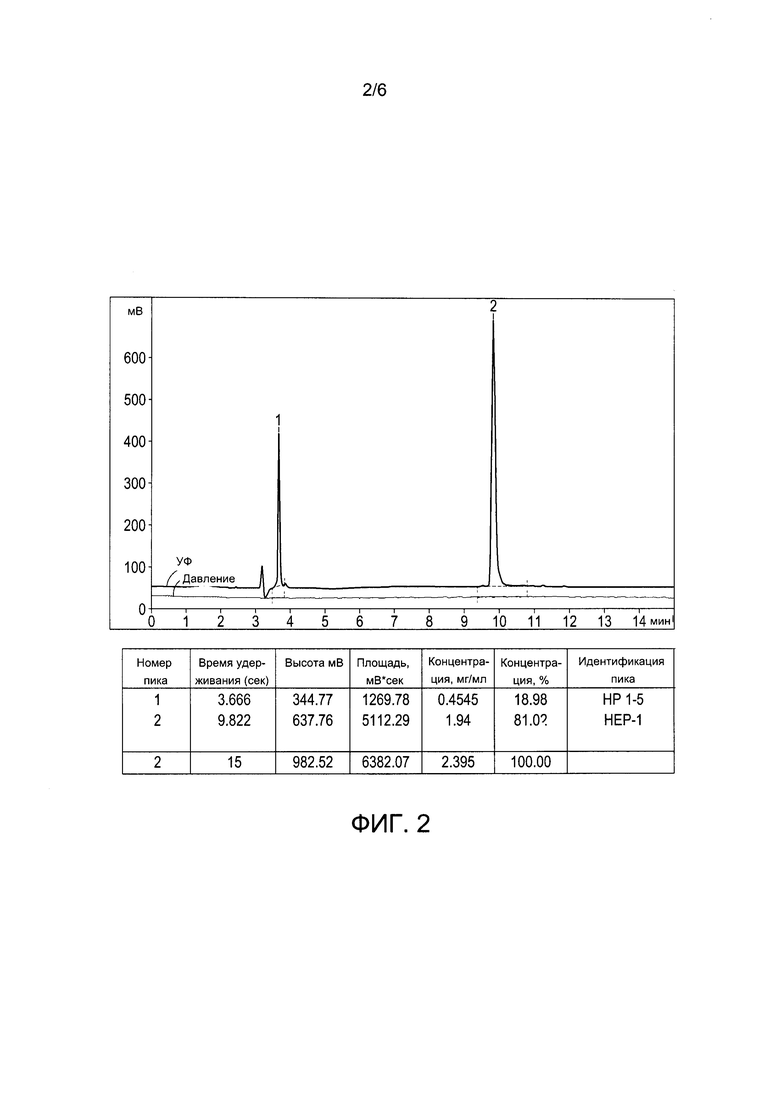
Фигура 2. Высокоэффективная жидкостная хроматография смеси пептида НЕР-1 и пептида HP 1-5. Колонка Luna С18 (2), 4,6×250 мм., частицы 5,0 мкм. Подвижная фаза: А - вода, 5% ACN, 0,1% ТФУ; В - 0,1% ТФУ; программа 5-25% ACN в течение 20 мин. Скорость потока: 1 мл/мин. Х-ось: время, Y-ось: поглощение УФ (мВ, верхняя линия, с пиками), давление (нижняя, горизонтальная линия).
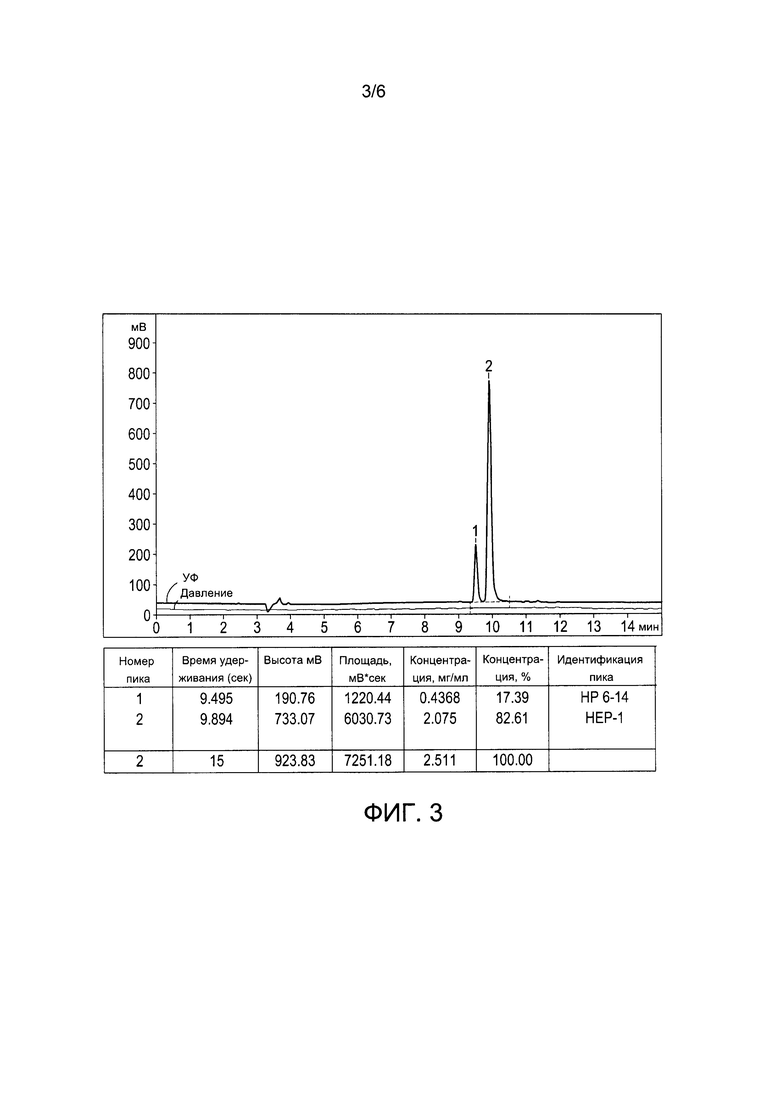
Фигура 3. Высокоэффективная жидкостная хроматография смеси пептида НЕР-1 пептида и пептида HP6-14. Колонка Luna С18 (2), 4,6×250 мм, частицы 5,0 мкм. Подвижная фаза: А - вода, 5% ACN, 0,1% ТФУ; В - 0,1% ТФУ; программа 5-25% ACN в течение 20 мин. Скорость потока: 1 мл/мин. Х-ось: время, Y-ось: поглощение УФ (мВ, верхняя линия, с пиками), давление (нижняя, горизонтальная линия).
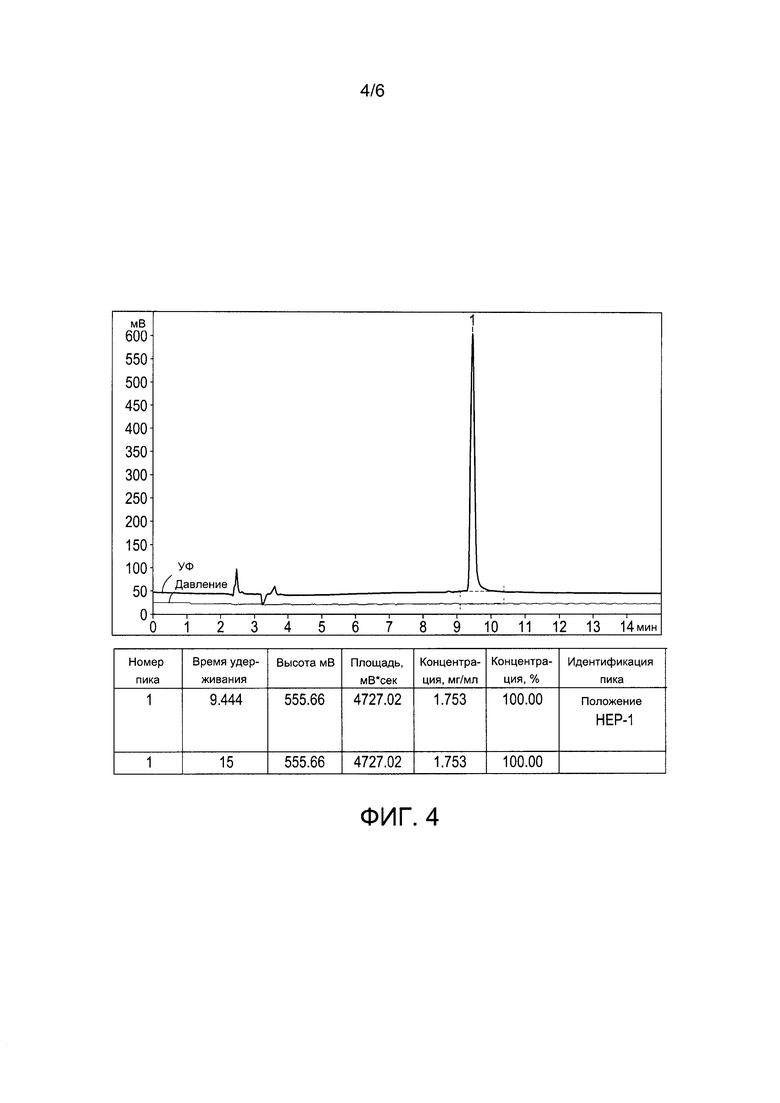
Фигура 4. Высокоэффективная жидкостная хроматография смеси пептида НЕР-1 и пептида HP-V2. Колонка Luna С18 (2), 4,6×250 мм, частицы 5,0 мкм. Подвижная фаза: А - вода, 5% ACN, 0,1% ТФУ; В - 0,1% ТФУ; программа 5-25% ACN в течение 20 мин. Скорость потока: 1 мл/мин. Х-ось: время, Y-ось: поглощение УФ (мВ, верхняя линия, с пиками), давление (нижняя, горизонтальная линия).
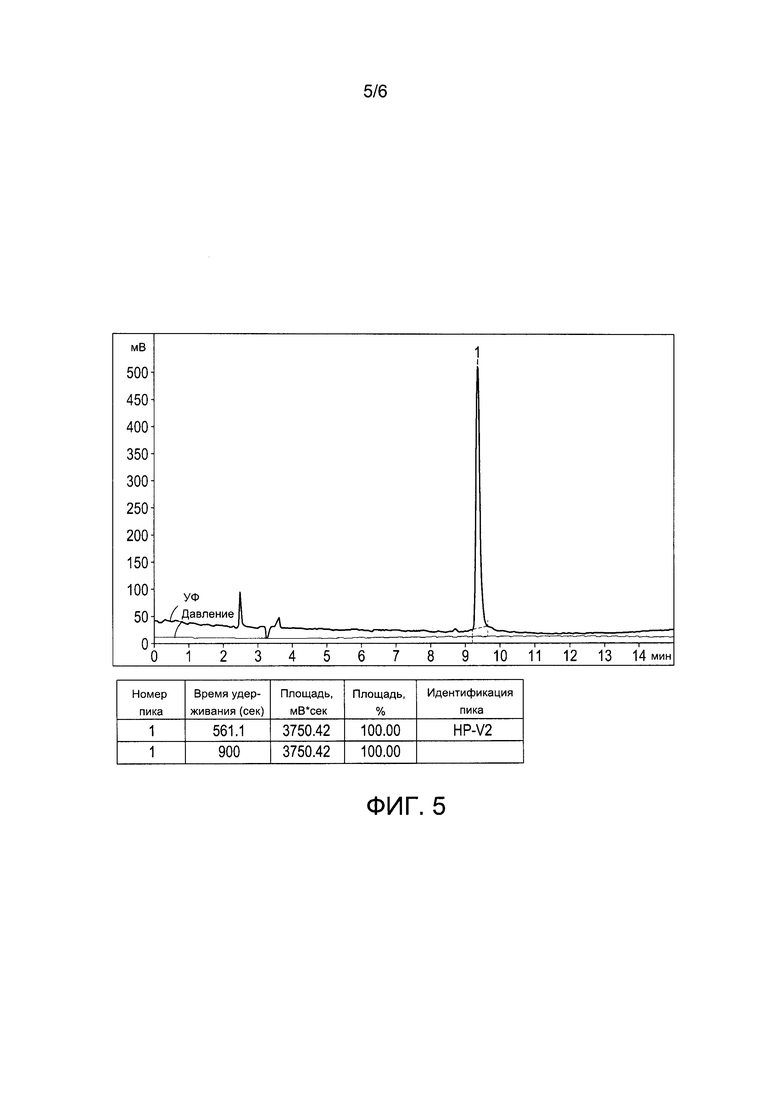
Фигура 5. Высокоэффективная жидкостная хроматография смеси пептида HP-V2. Колонка Luna С18 (2), 4,6×250 мм, частицы 5,0 мкм. Подвижная фаза: А - вода, 5% ACN, 0,1% ТФУ; В - 0,1% ТФУ; программа 5-25% ACN в течение 20 мин. Скорость потока: 1 мл/мин. Х-ось: время, Y-ось: поглощение УФ (мВ, верхняя линия, с пиками), давление (нижняя, горизонтальная линия).
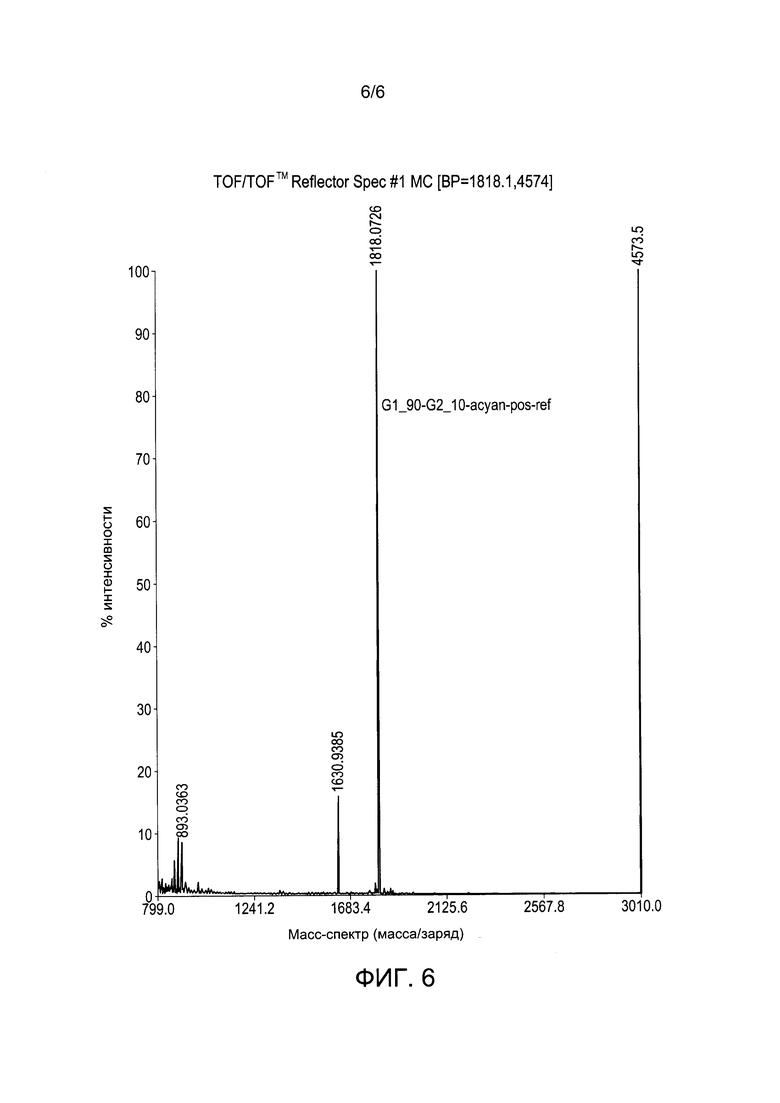
Рисунок 6. МАЛДИ ТОФ/ТОФ-спектр (MALDI TOF/TOF-spectrum) смеси пептида НЕР-1 и пептида HP-V2.
Примеры
Метод высокоэффективной жидкостной хроматографии использовали для точной оценки концентрации каждого компонента в процессе приготовления фармацевтических композиций. Результаты исследования показали, что было невозможно отличить пептид HP-V2, содержащий одинаковое количество аминокислот с пептидом НЕР-1, в условиях высокоэффективной жидкостной хроматографии (ВЭЖХ), и указанный факт не позволяет оценить количественное содержание композиций, основанных на HP-V2 и НЕР-1 (пример 4; фиг. 1, фиг. 4, фиг. 5). В тоже время количественное содержание композиций заявленного пептида HP-V2 и спутниковых пептидов HP 1-5 и НР6-14 может быть легко рассчитано на основе хроматограмм как следствие их хорошего разделения (примеры 2, 3; фиг. 2, фиг. 3).
Однако времяпролетная (TOF) МАЛДИ (MALDI) масс-спектрометрия четко обнаруживает каждый пептид в смеси из двух пептидов, включающих 14 аминокислотных остатков, в частности, в смеси из пептида HP-V2 (последовательность ID No: 1: GEKKRRETVEREGG), который определен как HP-V2, и пептида НЕР-1 (последовательность ID No: 2: TEKKRRETVEREKE), который определен как НЕР-1 (пример 5; фиг. 6).
Пример 1. Получение пептида HP-V2
Синтез пептида HP-V2 проводили твердофазным способом с применением алкоксибензильного полимера. Присоединения проводили с применением способа, основанного на использовании либо: 1) тетрафторбората O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (TBTU); или 2) 1-гидроксибензотриазола (НОВТ) и N,N'-диизопропилкарбодиимида (DIPC). Прикрепление последовательных Fmoc-защищенных аминокислотных остатков проводили однократно, за исключением случаев, когда не вступившие в реакцию аминогруппы находили на растущем пептидил-полимере после реакции конденсации. Контроль за содержанием не вступившей в реакцию аминогруппы в пептидил-полимере проводили посредством нингидринового теста. Трифторуксусную кислоту с добавлением тиоанизола, фенола, этандитиола, триизопропилсилана и воды применяли для разделения пептида и полимерного носителя и для окончательной разблокировки. Структура и однородность целевого продукта была подтверждена при помощи аминокислотного анализа, масс-спектрометрии, а также данных высокоэффективной жидкостной хроматографии.
Следующие фармацевтические композиции на основе предложенного пептида HP-V2 (последовательность ID No. 1: GEKKRRETVEREGG), а также их смеси со следующими пептидами были получены:
НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE);
HP1-5 (последовательность ID No. 3: TEKKR);
HP6-14 (последовательность ID No. 4: RETVEREKE).
Фармацевтические композиции:
Фармацевтическая композиция, содержащая эффективное количество пептида согласно последовательности ID No: 1: GEKKRRETVEREGG, и фармацевтически приемлемый носитель или наполнитель - остальные.
Фармацевтическая композиция, содержащая эффективное количество пептида согласно последовательности ID No: 1: GEKKRRETVEREGG, пептид согласно последовательности ID No: 2: TEKKRRETVEREKE, и фармацевтически приемлемый носитель или наполнитель - остальные.
Фармацевтическая композиция, содержащая эффективное количество пептида согласно последовательности ID No: 1: GEKKRRETVEREGG, пептид согласно последовательности ID No: 3: TEKKR, и фармацевтически приемлемый носитель или наполнитель - остальные.
Фармацевтическая композиция, содержащая эффективное количество пептида согласно последовательности ID No: 1: GEKKRRETVEREGG, пептид согласно последовательности ID No: 4: RETVEREKE, и фармацевтически приемлемый носитель или наполнитель.
Конкретные смеси, содержащие пептиды HP-V2 и Нер-1, НР1-5, НР6-14, которые применяли для получения фармацевтических композиций, предложены в примере 6.
Пептид HP-V2 или его смеси с вышеприведенными пептидами в количестве от 0,01 мг до 1000 мг растворяют в стерилизованной воде объемом от 1 мл до 10 мл. Лекарственные формы могут быть получены на основе приготовленного раствора и могут быть применены перорально, анально или вагинально, или интраназально в виде капель, или в виде спрея для ингаляции.
Пептид HP-V2 или комбинацию пептидов в количестве от 0,01 мг до 1000 мг помещают в таблетку или капсулу, или суппозитории, или гель, или в состав мази в сочетании с подходящими наполнителями, носителями, консервантами и стабилизаторами, которые обычно используются специалистами в области доставки лекарственных средств.
Пептид HP-V2 или комбинация пептидов в указанных выше фармацевтических композициях, может применяться для приготовления лекарственных форм, которые могут быть применены перорально, анально или вагинально, или которые могут быть применены локально. Стерильный раствор, содержащий от 0,01 мг до 1000 мг пептида HP-V2 или комбинацию пептидов, растворенных в воде для инъекций объемом от 1 мл до 10 мл или любом физиологическом солевом растворе, вводят в виде инъекций подкожным, внутримышечным или внутривенным способом.
Пример 2. Разделение пептидов НЕР-1 и HP 1-5 при помощи ВЭЖХ
Высокоэффективную жидкостную хроматографию (ВЭЖХ) применяли для разделения пептидов, основанную на их времени удерживания. Маточные растворы пептидов НЕР-1 и HP 1-5 получали посредством их солюбилизации в деионизированной воде при концентрации в 1 -2 мг/мл с последующим стерилизующим фильтрованием через фильтры Millipore с размером пор 0,2 мкм. Композицию, содержащую 80% пептида НЕР-1 и 20% пептида HP 1-5, получали путем смешивания соответствующих маточных растворов в соответствующих объемах.
ВЭЖХ проводили на колонке Luna С18 (2) размером 4,6×250 мм, заполненной частицами размером 5 мкм. Подвижная фаза была подготовлена программой смешивания фаз А и В, где А содержала воду, 5% ацетонитрила (ACN), 0,1% ТФУ, и В содержала 0,1% ТФУ. Программируемый градиент от 5 до 25% (ACN) сформировали в течение 20 минут. Объем пробы составил 20 мкл; скорость потока составила 1 мл/мин. Пики регистрировали автоматически по их поглощению УФ излучения в разное время удерживания.
Фиг. 1 иллюстрирует пик ВЭЖХ пептида НЕР-1 с характерным временем удерживания от 9 до 1 минуты. Фиг. 2 иллюстрирует четкое разделение двух пиков, НЕР-1 (RT=9,822 мин) и HP 1-5 (RT=3,666 мин) при помощи ВЭЖХ.
Пример 3. Разделение пептидов НЕР-1 и НР6-14 при помощи ВЭЖХ
Маточные растворы пептидов НЕР-1 и НР6-14 и их смесей были получены согласно описанию примера 2. Анализ пептидов и их смесей при помощи ВЭЖХ проводили на колонке Luna С18 (2) размером 4,6×250 мм, заполненной частицами размером 5 мкм, согласно описанию примера 1.
В использованных условиях ВЭЖХ, смесь пептидов НЕР-1 и НР6-14 была четко разделена на 2 пика (фиг. 3), один из которых обладал временем удерживания, которое было характерно для пептида НР6-14 (RT=9,495 мин), а другой обладал временем удерживания, которое было характерно для пептида НЕР-1 (RT=9,894 мин).
Пример 4. Анализ смеси пептидов НЕР-1 и HP-V2 при помощи ВЭЖХ
Маточные растворы пептидов НЕР-1 и HP-V2 пептидов, а также их смеси получили согласно описанию примера 2. Анализ методом ВЭЖХ пептидов и смесей проводили на колонке Luna С18 (2) размером 4,6×250 мм., заполненной частицами размером 5 мкм, согласно описанию примера 2.
В использованных условиях ВЭЖХ, смесь пептидов НЕР-1 и HP-V2 элюировали из колонки в виде одного пика (фиг. 4) со временем удерживания, которое было характерно для пептида HEP-1. Анализ методом ВЭЖХ чистого раствора пептида HP-V2 показал (фиг. 5), что время удерживания указанного пептида, в самом деле, было аналогичным времени удерживания пептида НЕР-1. Это означает, что невозможно отличить пептиды HP-V2 и НЕР-1 в указанных условиях ВЭЖХ.
Пример 5. Масс-спектрометрия смеси пептидов НЕР-1 и HP-V2
Маточные растворы пептидов НЕР-1 и HP-V2 пептидов, а также их смесей, получали согласно описанию примера 2. MALDITOF спектры переупорядочивали на Bruker Ultraflex TOF/TOF масс-спектрометре с использованием 2,5-диоксибензойной кислоты в качестве матрицы.
Масс-спектр смеси пептидов НЕР-1 и HP-V2 (фигура 6) явно обнаруживает два пептида с их молекулярными ионами 1818,0726 (MW) для НЕР-1 и 1630,9385 (MW) для HP-V2.
Введение в примеры 6-8
Следующие примеры 6-8 демонстрируют биологическую активность всех используемых пептидов и их смесей. Данные пептиды индуцируют выработку интерферона и обеспечивают защиту различных типов клеток человека от гибели, вызываемой инфекцией вируса цитопатического энцефаломиокардита в дозе составляющей 100 ЦПД50/мл в культурах клеток in vitro.
Пептид (HP-V2) (последовательность ID No. 1: GEKKRRETVEREGG), содержащий 14 аминокислотных остатков, и его композиции с пептидом НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE), или с пептидом HP1-5 (последовательность ID No. 3: TEKKR), или с пептидом НР6-14 (последовательность ID No. 4: RETVEREKE) исследовали на их способность индуцировать антивирусный ответ с выработкой интерферона I типа в культурах различных клеток. Авторы настоящего изобретения использовали традиционную методологию тестирования противовирусной (интерферон-индуцирующей) активности соединений в культуре in vitro, которая широко используется для скрининга иммуностимулирующих, противовирусных лекарственных средств и индукторов интерферона.
В указанной методологии in vitro, авторы настоящего изобретения предварительно обработали различные типы клеток исследуемыми пептидами, после чего клетки инфицировали дозой составляющей 100 ЛД50 вируса энцефаломиокардита. Через 24 часа после заражения оценивали цитопатический эффект вируса чтобы оценить защитную активность тестируемого соединения, если последний имеет возможность привести клетки к состоянию, устойчивому к вирусу, который является смертельным для клеток.
Как хорошо известно, в подавляющем большинстве случаев такая защитная активность соединений основывается на индукции интерферонов (термин «интерферон» означает соединение, которое продуцируется клеткой и предотвращает репликацию вируса). Представлялось возможным оценить противовирусную (интерферон-индуцирующую) активность указанных соединений с использованием различных концентраций указанных пептидов и их композиций in vitro.
Чем ниже концентрация, которая защищает 50% клеток от гибели от инфекционной дозы составляющей 100 ЛД50 вируса энцефаломиокардита, тем выше противовирусная (интерферон-индуцирующая) активность исследуемого соединения.
Пептид (HP-V2) (последовательность ID No. 1: GEKKRRETVEREGG), содержащий 14 аминокислотных остатков, и его комбинации с пептидом НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE), или с пептидом HP 1-5 (последовательность ID No. 3: TEKKR), или с пептидом НР6-14 (последовательность ID No. 4: RETVEREKE) исследовали в отношении иммуностимулирующей (противовирусной, интерферон-индуцирующей) активности.
Пример 6. Исследование противовирусной (интерферон-индуцирующей) активности пептидов в культуре линии клеток гепатомы человека
Линию клеток гепатомы человека PLC/PRF/5 (Alexander) получили из Научно-Исследовательского Института Вирусологии имени Ивановского (Москва). Полную среду для культивирования клеток готовили на основе минимальной эссенциальной среды Игла (MEM Eagle medium) дополненной 10% фетальной телячьей сыворотки (FCS), L-глутамином (300 мкг/мл), и пенициллином (100 ед/мл).
Были протестированы следующие пептиды:
НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE);
HP1-5 (последовательность ID No. 3: TEKKR);
HP6-14 (последовательность ID No. 4: RETVEREKE);
HP-V2 (последовательность ID No. 1: GEKKRRETVEREGG);
Смеси пептидов:
MXHP1-5+HEP-1 - смесь из 90% пептида НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE) и из 10% пептида HP 1-5 (последовательность ID No. 3: TEKKR); МХНР6-14+НЕР-1 - смесь из 90% пептида НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE) и из 10% пептида НР6-14 (последовательность ID No. 4: RETVEREKE);
MXHP-V2+HP1-5 - смесь из 90% пептида HP-V2 (последовательность ID No. 1: GEKKRRETVEREGG) и из 10% пептида HP 1-5 (последовательность ID No. 3: TEKKR); MXHP-V2+HP6-14 - смесь из 90% пептида HP-V2 (последовательность ID No. 1: GEKKRRETVEREGG) и из 10% пептида НР6-14 (последовательность ID No. 4: RETVEREKE).
MXHP-V2+HEP-1 - смесь из 95% пептида HP-V2 (последовательность ID No. 1: GEKKRRETVEREGG) и из 5% пептида НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE).
Пептиды растворяли в дистиллированной воде, после чего стерилизовали пропусканием через фильтры с размером пор 0,2 мкм, чтобы получить маточный раствор, составляющий 1-2 мг/мл. В начальный день, клетки высевали в лунки 96-луночного планшета в полной культуральной среде с плотностью клеток составляющей 200 тысяч клеток в 1 мл. В первый день, серийные разведения каждого испытуемого образца (24 серийных разведений с шагом 2) получили в триплетах в лунках 96-луночного планшета. На третий день, все культуры инфицировали дозой, соответствующей 100 ЦПД50/мл вируса энцефаломиокардита штамма "Колумбия SK-Col-SK". Наконец, на четвертый день, цитопатический эффект вируса оценивали с использованием инвертированного микроскопа Leitz в присутствии различных концентраций исследуемого пептида или в культурах без пептида (контроль).
Противовирусный эффект лекарственного средства оценивали на основе его минимальной концентрации, защищающей 50% клеток от гибели, вызванной вирусом энцефаломиокардита в дозе составляющей 100 ЦПД50/мл. Титр интерферона (ед/мл) рассчитывали как значение, обратное к максимальному разведению лекарственного средства, которое обеспечивало защиту 50% клеток от гибели, вызванной вирусом энцефаломиокардита в дозе составляющей 100 ЦПД50/мл.
Полученные данные представлены в таблице 1. Очевидно, что все испытанные пептиды и их комбинации предотвращают репликацию вируса энцефаломиокардита в клетках гепатомы человека. Пептиды обеспечивали защиту клетки гепатомы от цитопатического эффекта вируса путем индукции выработки интерферона. Эффективность пептидов и их композиций была иной. Самый высокий уровень противовирусной (интерферон-индуцирующей) активности зарегистрировали с пептидом HP-V2 и его композицией с пептидом HP1-5.

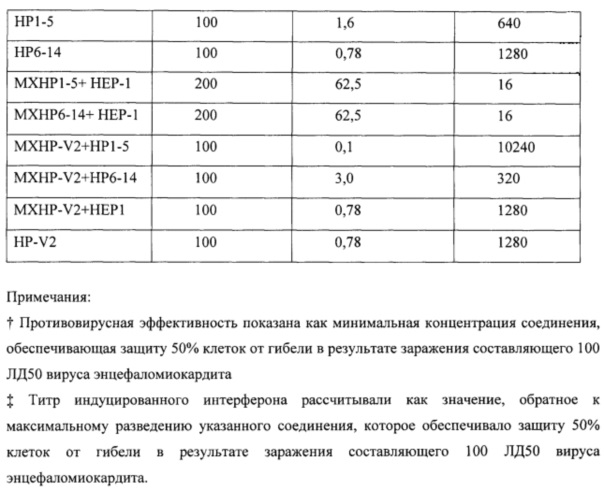
Пример 7. Исследование противовирусной (интерферон-индуцирующей) активности пептидов в культуре линии клеток цервикальной карциномы человека
Линию клеток цервикальной карциномы человека HELA получили из Научно-Исследовательского Института Вирусологии имени Ивановского (Москва). Полная среда для культивирования клеток, пептидов и их композиций, а также способ оценки их противовирусной (интерферон-индуцирующей) активности являлись аналогичными согласно описанию примера 5.
Полученные данные представлены в таблице 2. Очевидно, что все исследуемые пептиды и их композиции предотвращают развитие вирусной инфекции энцефаломиокардита в клетках цервикальной карциномы человека. Пептиды обеспечивали защиту клеток цервикальной карциномы от цитопатического эффекта вируса путем индукции выработки интерферона. Пептиды и их композиции обладали различной активностью. Максимальную противовирусную (интерферон-индуцирующую) активность определили при использовании пептида HP1-5 (последовательность ID No. 3: TEKKR) и пептида HP6-14 (последовательность ID No. 4: RETVEREKE), а также их комбинаций с пептидом.
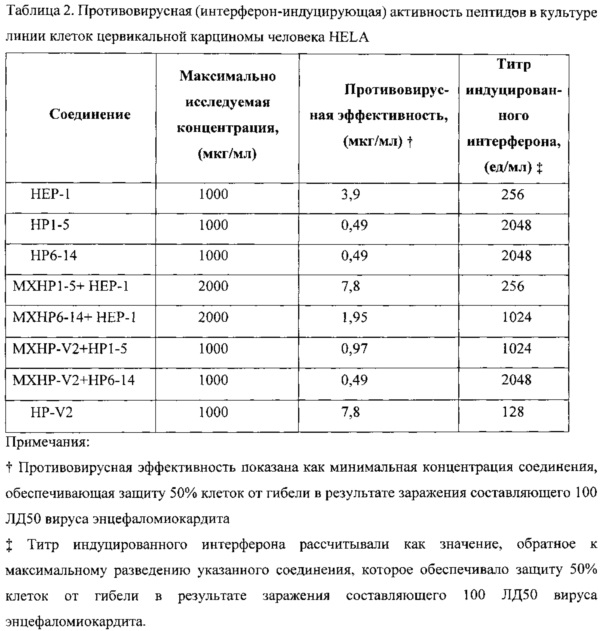
Пример 8. Исследование противовирусной (интерферон-индуцирующей) активности пептидов в культуре линии эпителиальных клеток сердца человека Girardi
Культуру линии эпителиальных клеток сердца человека Girardi получили из Научно-Исследовательского Института Вирусологии имени Ивановского (Москва). Полная среда для культивирования клеток, пептидов и их композиций, а также способ оценки их противовирусной (интерферон-индуцирующей) активности являлись аналогичными согласно описанию примера 5.
Полученные результаты представлены в таблице 3. Из представленных данных видно, что все исследуемые пептиды и композиции предотвращают развитие вирусной инфекции энцефаломиокардита в клетках линии эпителиальных клеток сердца человека Girardi. Исследуемые пептиды и их композиции являлись высокоэффективными в индуцировании выработки интерферонов и в обеспечении защиты линии эпителиальных клеток сердца человека Girardi от цитопатического эффекта вируса. Максимальную противовирусную (интерферон-индуцирующую) активность обнаружили при использовании комбинаций пептида НЕР-1 (последовательность ID No. 2: TEKKRRETVEREKE) с пептидом HP 1-5 (последовательность ID No. 3: TEKKR) и пептидом НР6-14 (последовательность ID No. 4: RETVEREKE), а также комбинации пептида HP-V2 (последовательность ID No. 1: GEKKRRETVEREGG) с пептидом HP 1-5 (SEQ ID No. 3: TEKKR) и с пептидом HEP1 (последовательность ID No. 2: TEKKRRETVEREKE).
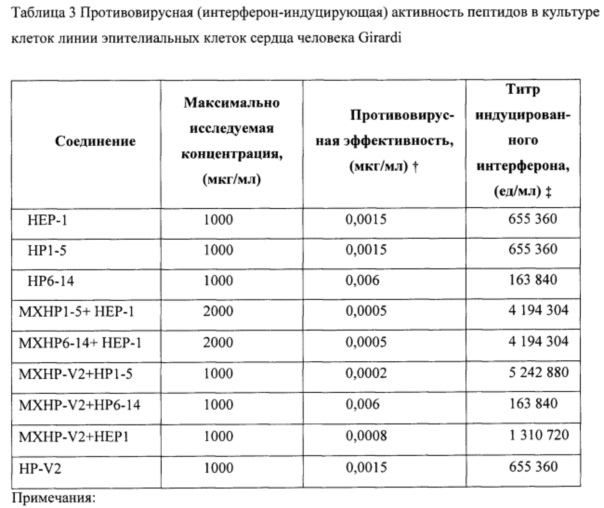

Как показывают предложенные примеры с описанием биологических испытаний и таблицы, предлагаемый новый пептид HP-V2 обладает высокой иммуностимулирующей активностью, которая является идентичной (таблица 3) или которая в 4 раза выше (таблица 1) при сравнении с активностью известного пептида НЕР-1. Кроме того, фармацевтические композиции с наивысшей иммуностимулирующей активностью и с широким спектром действия (таблицы 1-3), которые в несколько раз выше, чем у известного пептида НЕР-1 и его композиций, были получены на основе заявляемого пептида HP-V2 и известных пептидов эзрина.
Пример 9: Исследование для демонстрации влияния на молекулярный механизм в восстановлении тканей и пролиферации клеток
Следующее исследование свидетельствует о том, что пептид согласно настоящему изобретению (HP-V2) участвует в молекулярном механизме восстановления тканей и пролиферации клеток. Известно, что соединения, которые влияют на молекулярный механизм пролиферации клеток, например регуляцию экспрессии трансформирующего фактора роста бета (TGFP), связан с восстановлением кишечника ((Monteleone et al., "Mongersen, an Oral SMAD7 Antisense Oligonucleotide, and Crohn's Disease", New England Journal of Medicine, 372:1104-1113). В дополнение, Akita et al., "Basic Fibroblast Growth Factor in Scarless Wound Healing", Adv. Wound Care, 2013, 2(2):44-49 обсуждает преимущества и роль основного фактора роста фибробластов (bFGF) в безшрамном заживлении раны в клиническом применении и основном механизме. bFGF представляет собой гликопротеин, который широко применяют в лечении ран и язв. bFGF легко применим к любому типу раны и приводит к лучшему результату по цвету, текстуре и твердости. Chen et al., "NGF Accelerates Cutaneous Wound Healing by Promoting the Migration of Dermal Fibroblasts via the PI3K/Akt-Racl-JNK and ERK Pathways", BioMed Research International, Volume 2014, Article ID 547187) показал, что фактор роста нервов (NGF) значительно ускорил заживление кожных эксцизионных ран у крыс и миграция фибробластов, индуцированная NGF, может способствовать этому процессу заживления. Также было показано, что активации всех путей PBK/Akt, Racl, JNK и ERK была вовлечена в регуляцию NGF-индуцированной миграции фибробластов. Кроме того, Raffetto et al., "Mitogen-activated protein kinase pathway regulates cell proliferation in venous ulcer fibroblasts", Vase. Endovascular Surg., 2006, 40(1):59-66 показал, что путь МАРК ERK является важным для пролиферации клеток в венозной язвой фибробластов.
Следовательно, пептиды согласно настоящему изобретению являются подходящими для предотвращения и лечения воспаления и изъявления нижней части кишечника.
Показано, что пептид GEKKRRETVEREGG (SEQ ID No: 1) индуцирует активацию фибробластов, которые являются основным типом клеток, ответственным за регенерацию тканей, а также заживление ран и язв. Указанный пример демонстрирует непосредственное активирующее влияние пептида GEKKRRETVEREGG (SEQ ID No: 1) на фибробласты мыши, обнаруживая быстрый признак активации внутри клеток на уровне сигнального пути MAPK-ERK.
Пептид GEKKRRETVEREGG (SEQ ID No: 1) получали согласно описанию примера 1, фибробласты мышей BALB/c приобретали в Американской коллекции типовых культур и культивировали в полной среде, состоящей из минимальной эссенциальной среды Игла (DMEM) с высокой концентрацией глюкозы с добавлением 10% фетальной телячьей сыворотки, 1 мМ пируват натрия, 1:50 MEM заменимых аминокислот, 2 мМ L-глутамина, 10 мкг/мл гентамицина и 50 мкМ β-меркаптоэтанола. Клетки выращивали в чашке для культивирования диаметром 10 см. при 5% CO2 и 37°С. Клеточные пассажи сделали при 50-60% заселенности. Для отделения клеток, применяли 0,05% трипсин/ЭДТА с последующим центрифугированием (470×г, 15 мин) в 10-кратном объеме промывочной среды, содержащей 10% FCS для инактивации трипсина. Супернатант отбрасывали и клеточный осадок суспендировали в полной культуральной среде объемом 10 мл, после чего число клеток подсчитывали с использованием гемоцитометра до применения клеток в экспериментах.
Фибробласты культивировали в 8-луночных культуральных планшетах, исследуемый пептид или раствор цитокина TGF-β1 (положительный контроль), или эквивалентный объем культуралыгой среды (отрицательный контроль) добавляли в соответствующий трипликат культур. Клетки инкубировали в присутствии пептида GEKKRRETVEREGG SEQ ID No: 1 (10 мкг/мл), или трансформирующего фактора роста бета 1 (TGF-β1) или без какого-либо соединения-эффектора в течение 1 или 6 часов при 5% CO2 и 37°С. В указанные моменты времени, клетки собирали, дважды промывали с БСА и лизировали с использованием буфера для экстракции клеток в присутствии ингибиторов протеазы в течение 30 мин. при 4°С. Экстракты очищали путем центрифугирования (14000×г, 10 мин., 4°С). Концентрацию белка измеряли с использованием реагента для анализа белка (Pierce, 23225). Соответствующие разведения экстрактов (10 мкг. белка на дорожку) затем фракционировали при помощи 8% ДСН-ПААГ-электрофореза и далее переносили на PVDF-мембрану (Amersham) для иммунного блоттинга. Целевые белки обнаружили с помощью антител, специфичных к фосфо-р44/42 митоген-активируемой протеинкиназе (МАРК) (Cell Signaling, 4370) и глицеральдегид-3-фосфатдегидрогеназе (GAPDH) (Abeam ab8245). Белковые полосы визуализировали и далее измеряли их интенсивности, используя программное обеспечение ImageJ. Данные представили через значение (количество пикселей на полосу) внеклеточно регулируемой киназы 1 (ERK1), внеклеточно регулируемой киназы 2 (ERK2) или фосфо-ERK1 и фосфо-ERK2 нормированных до значения, соответствующего GAPDH-полосам. Средние значения + среднеквадратичное отклонение рассчитали с использованием данных по 3-м независимым измерениям.
Результаты экспериментов исследователей показывают, что оба пептида GEKKRRETVEREGG (SEQ ID No: 1) и положительный контроль TGF-β1 индуцируют быструю активацию MAPK/ERK сигнального пути в фибробластах. Через 1 час после инокуляции указанных соединений-эффекторов концентрацию фосфорилированной ERK1 (44 кД) и ERK2 (42 кД) увеличили приблизительно в 3-5 раза. Таким образом, через 1 час после активации фибробластов с GEKKRRETVEREGG (SEQ ID No: 1) пептидом (10 мкг/мл) или TGF-β1 (5 нг/мл), нормированные значения фосфо-ERK1 составили 0,4+0,02 (р<0,01) и 0,5+0,02 (р<0,01), соответственно, в сравнении с 0,1+0,002 в отрицательном контроле, и значения фосфо-EPK2 составили 1,3+0,05 (р<0,01) и 1,9+0,1 (р<0,01) в сравнении с 0,4+0,01 в отрицательном контроле. Позже, через 6 часов после активации, значения фосфо-ERK1 в фибробластах, активированных пептидом GEKKRRETVEREGG (SEQ ID No: 1) или TGF-β1 составили 0,1+0,006 (р>0,1) и 0,3+0,02 (p<0,05), соответственно, в то время как 0,1+0,01 в культурах отрицательного контроля. Значения фосфо-ERK2 в момент времени 6 часов составили 0,1+0,01 (р>0,1), 0,35+0,02 (р<0,01) и 0,1+0,007 в пептиде, TGF-β1 и неактивированных культурах соответственно.
Вышеприведенное исследование показало, что активность HP-V2 аналогична активности TGF-β1 (положительный контроль), и, следовательно перспективна для применения для предотвращения и лечения воспаления и изъязвления нижней части кишечника.





Группа изобретений относится к медицине и касается пептида, подходящего для индукции интерферона, содержащего аминокислотную последовательность согласно общей формуле (I) X1EKKRRETVEREX2X3 (SEQ ID No: 5), причем каждый из X1, X2 и X3 представляет собой остаток неполярной аминокислоты. Группа изобретений также касается фармацевтической композиции, подходящей для индукции интерферона, содержащей указанный пептид; способа стимуляции иммунного ответа у субъекта, нуждающегося в этом, включающего введение субъекту терапевтически эффективного количества указанного пептида; способа лечения и/или предотвращения заболевания, требующего лечения иммуностимулирующим агентом, включающего введение субъекту терапевтически эффективного количества указанного пептида. Группа изобретений обеспечивает индукцию интерферона. 4 н. и 21 з.п. ф-лы, 6 ил., 3 табл., 9 пр.
1. Пептид, подходящий для индукции интерферона, содержащий аминокислотную последовательность согласно общей формуле (I)
X1EKKRRETVEREX2X3 (SEQ ID No: 5),
причем каждый из X1, X2 и X3 представляет собой остаток неполярной аминокислоты.
2. Пептид по п. 1, отличающийся тем, что неполярная аминокислота независимо выбрана из группы, состоящей из глицина, аланина, валина, лейцина, метионина, изолейцина, пролина, фенилаланина, триптофана и/или их комбинаций.
3. Пептид по п. 1, отличающийся тем, что X1, X2 и/или X3 представляет собой глицин.
4. Пептид по п. 3, отличающийся тем, что указанная аминокислотная последовательность представляет собой GEKKRRETVEREGG (SEQ ID Nо: 1).
5. Фармацевтическая композиция, подходящая для индукции интерферона, содержащая эффективное количество пептида по любому из пп. 1-4, и фармацевтически приемлемый носитель или наполнитель.
6. Фармацевтическая композиция по п. 5, дополнительно содержащая эффективное количество пептида согласно SEQ ID Nо: 2 (TEKKRRETVEREKE).
7. Фармацевтическая композиция по п. 5, дополнительно содержащая эффективное количество пептида согласно SEQ ID Nо: 3 (TEKKR).
8. Фармацевтическая композиция по п. 5, дополнительно содержащая эффективное количество пептида согласно SEQ ID Nо: 4 (RETVEREKE).
9. Пептид по любому из пп. 1-4 для применения в стимуляции иммунного ответа у субъекта.
10. Фармацевтическая композиция по любому из пп. 5-8 для применения в стимуляции иммунного ответа у субъекта.
11. Пептид по любому из пп. 1-4 для применения для лечения или предотвращения вирусной, бактериальной или грибковой инфекции.
12. Фармацевтическая композиция по любому из пп. 5-8, для применения для лечения или предотвращения вирусной, бактериальной или грибковой инфекции.
13. Пептид по любому из пп. 1-4 для применения для лечения или предотвращения изъязвления слизистых оболочек кишечника.
14. Фармацевтическая композиция по любому из пп. 5-8, для применения для лечения или предотвращения изъязвления слизистых оболочек кишечника.
15. Пептид для применения по п. 13, отличающийся тем, что изъязвление слизистых оболочек кишечника представляет собой язву желудка, язву толстой кишки, язву двенадцатиперстной кишки, или язву тонкой кишки.
16. Фармацевтическая композиция для применения по п. 14, отличающаяся тем, что изъязвление слизистых оболочек кишечника представляет собой язву желудка, язву толстой кишки, язву двенадцатиперстной кишки, или язву тонкой кишки.
17. Пептид по любому из пп. 1-4 для применения для лечения или предотвращения воспалительного заболевания кишечника, или заболевания, или расстройства, связанного с воспалительным заболеванием кишечника.
18. Фармацевтическая композиция по любому из пп. 5-8 для применения для лечения или предотвращения воспалительного заболевания кишечника, или заболевания, или расстройства, связанного с воспалительным заболеванием кишечника.
19. Пептид для применения по п. 17, отличающийся тем, что заболевание или расстройство, связанное с воспалительным заболеванием кишечника, выбрано из группы, состоящей из синдрома раздраженного кишечника (IBS), неспецифического язвенного колита и болезни Крона.
20. Фармацевтическая композиция для применения по п. 18, отличающаяся тем, что заболевание или расстройство, связанное с воспалительным заболеванием кишечника, выбрано из группы, состоящей из синдрома раздраженного кишечника (IBS), неспецифического язвенного колита и болезни Крона.
21. Способ стимуляции иммунного ответа у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества пептида по любому из пп. 1-4 или фармацевтической композиции по любому из пп. 5-8.
22. Способ лечения и/или предотвращения заболевания, требующего лечения
иммуностимулирующим агентом, включающий введение субъекту терапевтически эффективного количества пептида по любому из пп. 1-4 или фармацевтической композиции по любому из пп. 5-8.
23. Способ лечения или предотвращения заболевания по п. 22, отличающийся тем, что указанное заболевание представляет собой вирусную, бактериальную или грибковую инфекцию, изъязвление слизистых оболочек кишечника, или воспалительное заболевание кишечника, или заболевание, или расстройство, связанное с воспалительным заболеванием кишечника.
24. Способ по п. 23, отличающийся тем, что изъязвление слизистой оболочки кишечника представляет собой язву желудка, язву толстой кишки, язву двенадцатиперстной кишки, или язву тонкой кишки.
25. Способ по п. 23, отличающийся тем, что заболевание или расстройство, связанное с воспалительным заболеванием кишечника, выбрано из группы, состоящей из синдрома раздраженного кишечника (IBS), неспецифического язвенного колита и болезни Крона.
| SALAMOV G | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| BUKONG TN | |||
| et al | |||
| A Novel Human Radixin Peptide Inhibits Hepatitis C Virus Infection at the Level of Cell Entry.Int J Pept Res Ther | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| WO 2004067024 A2, 12.08.2004 | |||
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ СПИДА, ИЛИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ, ИЛИ СВЯЗАННЫХ С НИМИ НАРУШЕНИЙ | 1995 |
|
RU2127599C1 |
Авторы
Даты
2019-07-18—Публикация
2016-06-01—Подача