Изобретение относится к области фармации и касается способа получения средства из растительного сырья, обладающего адаптогенной активностью.
В последнее десятилетие вследствие возрастающего эколого-социального прессинга отмечается существенное снижение общей сопротивляемости, связанное с депрессией адаптационно- компенсаторных механизмов. В этих условиях особую значимость приобретают профилактические мероприятия, направленные на повышение неспецифической резистентности организма. Одним из методов достижения этого состояния является применение фармакологических средств, обладающих адаптогенной активностью и повышающих сопротивляемость к широкому спектру стрессогенных факторов. Наиболее перспективным направлением является разработка новых препаратов на основе сырья природного происхождения, растущий интерес к которым отмечается во всем мире.
Связано это с тем, что препараты, получаемые из сырья растительного и животного происхождения, продуктов моря и пчеловодства, обладают рядом преимуществ по сравнению с синтетическими средствами: содержат широкий спектр биологически активных веществ; обладают несколькими видами фармакологической активности; характеризуются плавным нарастанием фармакологического эффекта. Кроме того, препараты природного происхождения отличаются низкой токсичностью и отсутствием побочных реакций при длительном приеме [3].
Перспективным направлением поиска и разработки новых адаптогенных препаратов природного происхождения является исследование средств неспецифического действия из арсенала тибетской медицины, рекомендуемых для ослабленных, а также лиц преклонного возрастав качестве общеукрепляющих, «дающих долголетие и здоровье» [11,12].
На основе рецептурной прописи «пять корней» [11] разработан сухой экстракт из корневищ купены душистой (Polygonatum odoratum (Mill) Druce), корней горичника Морисона (Peucedanum morisonii Bess.), корней пиона уклоняющегося (Paeonia anomala L.), корней спаржи лекарственной (Asparagus officinalis L.), плодов якорцев стелющихся (Tribulus terrestris L.), условно названный «Пентафитон».
Компоненты данного средства содержат широкий набор биологически активных веществ, относящихся к различным классам химических соединений: стероиды (диосцин, даукостерин, диосгенин, стигмастерин), флавоноиды (рутин, астрагалин, кверцетин, кемпферол, изорамнетин и их гликозиды), фенолкарбоновые кислоты (кофейная, салициловая, галловая, бензойная), алкалоиды (гармол, гармалин), фенолы (пеонол, пеонолид) и др. [7, 8, 9].
Фармакологическая активность данных видов известна, так извлечения пиона уклоняющегося проявляют антиоксидантную и иммуномоделирующую активность; якорцев стелющихся - андрогенную и иммуностимулирующую; горичник Морисона - антибактериальную; спаржа лекарственная - антиоксидантную и иммуномодулирующую; купены душистой - кардиотоническую [7, 8, 9].
Таким образом, по данным народной и научной медицины препараты из пиона, горичника, якорцев, спаржи и купены обладают выраженным антиоксидантным и иммуномодулирующим действием, что указывает на целесообразность применения данной композиции в качестве адаптогенного средства.
Целью изобретения является повышение адаптогенной активности средства за счет более высокого содержания действующих веществ (стероидов, флавоноидов, алкалоидов, оксикоричных кислот, фенолов).
Для достижения указанной цели растительный материал (сырье) - корневища купены душистой (200 г), корни горичника Морисона (200 г), корни пиона уклоняющегося (200 г), корни спаржи лекарственной (200 г), плоды якорцев стелющихся (200 г) экстрагируют 50% этиловым спиртом в соотношении сырье : экстрагент, равном 1:(14-16) (с учетом коэффициента водопоглощения), при температуре 60°С и постоянном перемешивании. Процесс повторяют трижды. Время экстракции при 1-ом и 2-ом контактах фаз - 60 мин, при 3-ем контакте фаз - 30 мин. Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°С в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 270.0 г готового продукта, что составляет 27.0±0.5% от массы воздушно-сухого сырья.
Предложенный способ позволяет получить конечный продукт, сухой экстракт (под условным названием «Пентафитон»), представляющий собой мелкодисперсный порошок коричневого цвета с приятным запахом и сладковатым вкусом, с содержанием влаги - не более 5%.
Способ иллюстрируется нижеследующими примерами.
Пример 1
Для достижения указанной цели растительный материал (сырье) -корневища купены душистой (200 г), корни горичника Морисона (200 г), корни пиона уклоняющегося (200 г), корни спаржи лекарственной (200 г), плоды якорцев стелющихся (200 г) измельчают на мельнице до размера частиц диаметром 1 мм (сито №10 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 14 л 50% этилового спирта в соотношении сырье-экстрагент равном 1:14 с учетом коэффициента водопоглощения сырья. Экстрагируют при температуре 60°С и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще две экстракции в течение 60 и 30 мин, подавая каждый раз в экстрактор 50% спирт в количестве равном объему слитого извлечения (1-ый слив - 10.85 л, 2-ой слив - 9.80 л, 3-ий слив - 9.60 л). Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°С в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 270.3 г готового продукта, что составляет 27.06% от массы воздушно-сухого сырья. Экстракт сухой «Пентафитон» представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и сладковатым вкусом; комкуется, содержание влаги - 4.05%.
Острая токсичность экстракта сухого «Пентафитон» определялась на белых беспородных мышах-самцах с исходной массой 20.0±1.0 г при внутрибрюшинном и внутрижелудочном введениях растворенного в воде экстракта. Каждую дозу экстракта «Пентафитон» испытывали на 10 животных. Наблюдение за животными вели в течение 14 дней. Регистрировали наблюдаемые признаки интоксикации, проводили вскрытие и осмотр погибших животных. Результаты исследований показали, что при внутрибрюшинном введении больших доз экстракта сухого «Пентафитон» белым мышам наблюдаются признаки интоксикации, выражающиеся в замедлении ориентировочной реакции, резких движениях, появлением тонических, а затем тонико-клонических судорог. Животные погибали при явлениях сердечно-сосудистой недостаточности преимущественно в течение суток от введения экстракта сухого «Пентафитон». LD50 по Керберу при внутрибрюшинном введении экстракта сухого «Пентафитон» 1960±60.76 мг/кг. При внутрижелудочном введении данного средства в максимально возможной дозе, гибель животных не регистрировалась, и не наблюдалось явных признаков интоксикации. Эти данные позволяют отнести испытуемый экстракт сухой «Пентафитон» к группе малотоксичных веществ по классификации Сидорова [10].
В дальнейшем было исследовано влияние экстракта сухого «Пентафитон» на основные фазы воспалительного процесса.
Влияние экстракта сухого «Пентафитон» на физическую выносливость и устойчивость к гипоксии.
Исследования проведены на 55 белых крысах линии Вистар обоего пола с исходной массой 160-180 г, содержащихся на стандартном рационе вивария.
Для определения общей физической выносливости использовали общепринятую методику плавания с грузом 5% от массы тела [5]. Водный раствор «Пентафитона» вводили внутрижелудочно в объеме 1.0 мл/100 г, содержащим 0.5; 1.0; 3.0% раствора «Пентафитона» однократно за 1 час до тестирования, а также многократно в течение 7 дней в объеме 1.0 мл/100 г, содержащим 3.0 мл водного настоя 1 раз в день до приема пищи. Животным контрольной группы внутрижелудочно вводили аналогичный объем дистиллированной воды. В качестве препарата сравнения использовали деалколизированный раствор экстракта элеутероккока жидкого в объеме 1 мл/ 100 г. Оценивали продолжительность плавания животных до полного утомления, критерием которого служило 10-секундное погружение в воду. Полученные данные приведены в таблице 1.
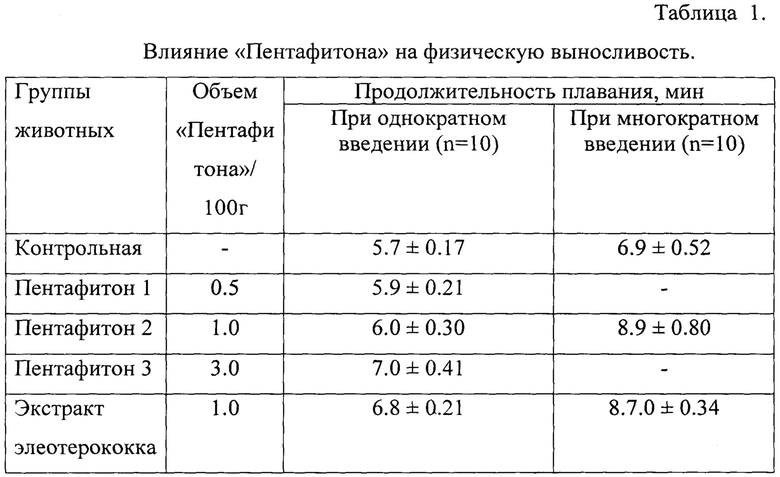
Как следует, из данных. Приведенных в таблице 1, однократное введение «Пентафитона» в объеме 0.5 и 1.0 мл/ кг не оказывало существенного влияния на продолжительность плавания животных, тогда как при использовании его в объеме 3.0 мл/ кг отмечалось повышение общей физической выносливости на 20% по сравнению с данными животных контрольной группы. Исходя из этого, в дальнейших экспериментах, в качестве эксперементально-терапевтического был использован объем «Пентафитона», соответствующий 3.0 мл/кг.
Семидневное превентивное введение «Пентафитона» в объеме 3.0 мл/кг сопровождалось более существенным повышением общей физической выносливости, о чем свидетельствует увеличение продолжительности плавания животных опытной группы в среднем на 30% по сравнению с показателями контрольной группы.
Таким образом, полученные данные свидетельствуют, что «Пентафитон» оказывает стимулирующее действие на общую физическую выносливость, характеризующуюся преобладанием аэробных процессов энергообеспечения тканей. Установлено, что наиболее выраженной актопротективной активностью испытуемое средство обладает при введении в объеме 3.0 мл/ кг, содержащей 3.0 мл водного настоя; эффективность повышается при многократном введении. Пример 2
Для достижения указанной цели растительный материал (сырье) -корневища купены душистой (200 г), корни горичника Морисона (200 г), корни пиона уклоняющегося (200 г), корни спаржи лекарственной (200 г), плоды якорцев стелющихся (200 г) измельчают на мельнице до размера частиц диаметром 1 мм (сито №10 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 15 л 50% этилового спирта в соотношении сырье-экстрагент равном 1:15 с учетом коэффициента водопоглощения сырья. Экстрагируют при температуре 60°С и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще две экстракции в течение 60 и 30 мин, подавая каждый раз в экстрактор 50% спирт в количестве равном объему слитого извлечения (1-ый слив - 11.05 л, 2-ой слив - 9.85 л, 3-ий слив - 9.65 л). Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°С в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 270.8 г готового продукта, что составляет 27.10% от массы воздушно-сухого сырья. Экстракт сухой «Пентафитон» представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и сладковатым вкусом; комкуется, содержание влаги -4.05%.
Исследования проведены на 55 белых крысах линии Вистар обоего пола с исходной массой 160-180 г, содержащихся на стандартном рационе вивария.
Для определения скоростной физической выносливости использовали общепринятую методику бега животных на 10-дорожечном третбане пр и скорости движения полотна 40 м/мин [5]. острую гипобарическую гипоксию воспроизводили в борокамере при отмосферном давлении 198.8 мм ртутного столба, парциальном давлении кислорода 50 мм ртутного столба, что соответствует «подьему» животных на высоту 1000 м над уровнем моря. Для воспроизведения гистотоксической гипоксии животным внутрибрюшиннон однократно вводили натрия нитропруссид в дозе 20 мг/кг [4]. Устойчивость к гипоксии оценивали по продолжительности жизни животных.
Водный раствор «Пентафитона» вводили внутрижелудочно в объеме 1.0 мл/100 г, содержащим 3.0% раствора «Пентафитона» однократно за 1 час до тестирования, а также многократно в течение 7 дней в объеме 1.0 мл/100 г, содержащим 3.0 мл водного настоя 1 раз в день до приема пищи. Животным контольной группы внутрижелудочно вводили аналогичный объем дистиллированной воды. В качестве препарата сравнения использовали деалколизированный раствор экстракта элеутероккока жидкого в объеме 1 мл/100 г. Полученные данные приведены в таблице 2.
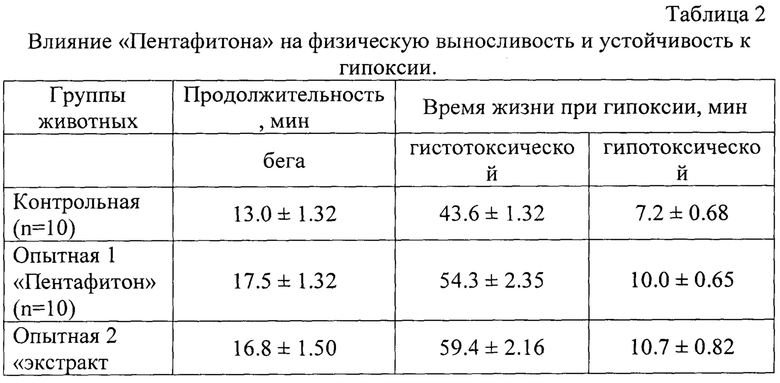

Как следует из таблицы, превентивно-курсовое введение «Пентафитона» сопровождается увеличением продолжительности бега на 26% по сравнению с данными животных контрольной группы. Установлено, что профилактическое введение «Пентафитона» увеличивало время жизни крыс при гистотоксической и гипобарической гипоксии на 20 и 38% соответственно, по отношению к контролю. При этом актопротективная и антигипоксическая активность «Пентафитона была аналогичной таковой у препарата сравнения «экстракта элеутероккока».
Пример 3
Для достижения указанной цели растительный материал (сырье) -корневища купены душистой (200 г), корни горичника Морисона (200 г), корни пиона уклоняющегося (200 г), корни спаржи лекарственной (200 г), плоды якорцев стелющихся (200 г) измельчают на мельнице до размера частиц диаметром 1 мм (сито №10 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 16 л 50% этилового спирта в соотношении сырье-экстрагент равном 1:16 с учетом коэффициента водопоглощения сырья. Экстрагируют при температуре 60°С и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще две экстракции в течение 60 и 30 мин, подавая каждый раз в экстрактор 50% спирт в количестве равном объему слитого извлечения (1-ый слив - 11.55 л, 2-ой слив - 10.05 л, 3-ий слив - 9.86 л). Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°С в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 270.9 г готового продукта, что составляет 27.05% от массы воздушно-сухого сырья. Экстракт сухой «Пентафитон» представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и сладковатым вкусом; комкуется, содержание влаги -4.05%.
Исследования проведены на 55 белых крысах линии Вистар обоего пола с исходной массой 160-180 г, содержащихся на стандартном рационе вивария. Иммобиллизационный стресс воспроизводили общепринятым методом путем фиксации животных на спине в течение 20 ч. Для воспроизведения эмоционального стесса, животных иммобилизировали в пластиковых пеналах и погружали в воду (23 С) по мечевидный отросток грудины на 2 часа [6]. Статистическую обработку результатов проводили с использованием U-критерия Манна-Уитни.
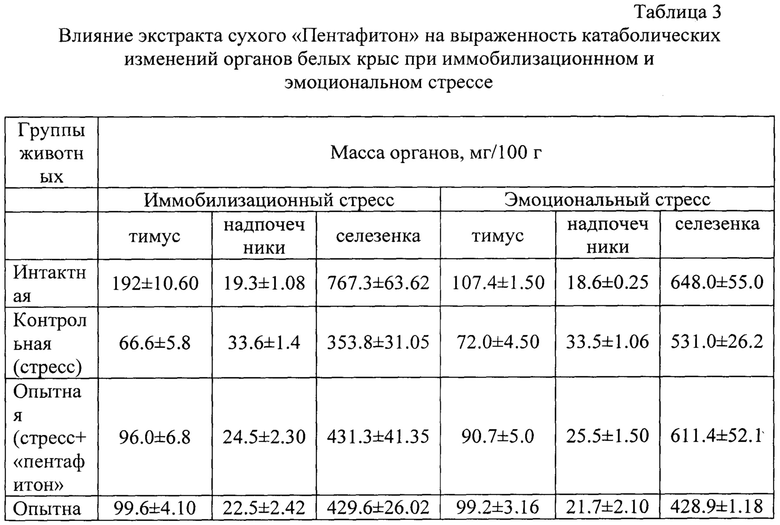

Как видно из таблицы 3, в результате иммобилизационного и эмоционального стресса у животных развивается комплекс дистрофических изменений внутренних органов, характерных для стесс-реакции: инволюция лимфоидных органов, гипертрофия надпочечников, появление деструктивных поражений слизистой оболочки желудка. Более выраженные изменения внутренних органов отмечены при иммобилизационном стрессе, что очевидно связано с более длительным стрессорным воздействием. Профилактическое введение растительного средства «Пентафитон» в объеме 3.0 мл/ 100 г, оказало выраженное антистрессорное действие, о чем свидетельствует уменьшение относительной массы надпочечников крыс опытной группы при иммобилизационном и эмоциональном стрессе в среднем на 27.9%; увеличении относительной массы тимуса - на 30% и селезенки - на 18% по сравнению с аналогичными показателями животных контрольной группы. Антистессорная активность испытуемого средства была сопоставима с таковой у препарата сравнения - экстракта элеутероккока.
Таким образом, исследование адаптогенной активности растительного средства «Пентафитон» показало, что его превентивное введение в объеме 3.0 мл/100 г сопровождается повышением сопротивляемости организма животных к действию экстремальных факторов различной природы: интенсивных физических нагрузок (общих и скоростных); гипобарической и тканевой гипоксии; иммобилизационного и эмоционального стресса. Можно полагать, что в основе адаптационной перестройки организма, развивающейся под влиянием испытуемого средства, лежит ряд функциональных и метаболических изменений, происходящих на различных уровнях биологической организации и обеспечиваемых широким спектром биологически активных веществ, входящих в его состав, таких как тритерпеновые и стероидные сапонины, флавоноиды, полисахариды, органические кислоты. Можно полагать, что указанные биологически активные вещества стимулируют эрготропные и трофотропные процессы в клетках и тем самым формируют состояние неспецифически повышенной сопротивляемости организма к действию экстремальных факторов различной природы. В частности, при интенсивных физических нагрузках, реализация актопротективного эффекта испытуемого средства связана с оптимизацией энергетического обмена в клетках, обеспечивающего активацию ресинтеза АТФ и уменьшении метаболического анида, являющегося, как известно главным лимитирующим фактором физической работоспособности. Показано, что активация ресинтеза АТФ под влиянием «Пентафитона» обеспечивается как повышением кислородтранспортной функции крови, так и оптимизацией лимитирующих звеньев энергетического обмена в клетках, что подтверждается полученными данными о выраженной антигипоксической активности «Пентафитона» при кислороддефицитных состояниях различного генеза.
Таким образом, полученные данные свидетельствуют, что растительное" средство «Пентафитон» обладает широким спектром адаптогенной активности, что аргументирует перспективность его дальнейшего исследования и внедрения в клиническую практику в качестве средства, предназначенного для повышения неспецифической сопротивляемости организма, предупреждения утомления при физических и психических нагрузках, а также для повышения работоспособности.
На основании качественного фитохимического анализа [1, 2, 13] в полученном сухом экстракте установлено наличие следующих биологически активных веществ.
1. Стероиды
Проба проводилась хроматограф ическим методом на бумаге в системе изооктан - уксусная кислота - хлороформ (100:1:4), проявление проводили реактивом Санье - 1% спиртовый раствор ванилина - с последующей обработкой хроматограммы смесью уксусного ангидрида с кислотой серной (9:12:1). Пятна окрашивались в желтый цвет, величина Rf диосгенина составляла 0,63.
2. Органические кислоты. Методом ТСХ на пластинках «Silufol UV254», в системе 96% этанол - концентрированный раствор аммиака -вода (60:10:3) - на хроматограмме должно быть не менее четырех пятен коричневого цвета, соответствующих винной, лимонной, яблочной и щавелевой кислотам.
3. Фенолкарбоновые кислоты. Двумерная восходящая хроматография на бумаге марки FN-12 в системах растворителей:
- н-Бутанол - уксусная кислота - вода (4:1:2);
- 15% уксусная кислота.
При просмотре хроматограммы в УФ-свете, после обработки парами аммиака, идентифицированы со стандартными образцами:
- кофейная кислота - Rf=0.80 (А), 0.42 (Б);
- феруловая - Rf=0.67 (А), 0.70 (Б).
4. Флавоноиды. При использовании пластинок «Сорбфил ПТСХ-АФ-А-УФ» (система растворителей хлороформ - метанол - вода, 26:14:3) на хроматограмме обнаруживается пятна рутина (Rf около 0.6), изорамнетина (Rf около 0.7), кемпферола (Rf около 0.8), а также, астрагалина.
Количественное определение
Исследование проводили методом ВЭЖХ на хроматографе Agilent 1290 со спектрофотометрическим детектором и масс-спектрометрическим (6460) 151 детекторами. Условия хроматографирования: колонка: ZorbaxXDB-C18 (Agilent, США) размером 150×4.6 мм, диаметр частиц сорбента 5 мкм; предколонка: Security Guard C18 (4,3 мм; Phenomenex, США); температура колонки: 25°C; объем вводимой пробы: 20 мкл; скорость подвижной фазы: 1 мл/мин; подвижная фаза в градиентном режиме: А - деионизированная вода, подкисленная трифторуксусной кислотой до (рН 3.0); В - ацетонитрил. Условия УФ детектирования: длина волны 205 нм при ширине спектральной полосы 4 нм. Условия масс-спектрометрического детектирования: режим выбранных ионов - m/z 869.5 (М-Н)+; давление небулайзера - 70 пси; скорость газа-осушителя - 12 л/мин; его температура - 350°С. В качестве стандарта использован диосцин, время удерживания которого составляет 21,0 мин. Для разработки методики количественного определения был построен график линейной зависимости.

Исследование показало, что экстракт «Пентофитон» при доверительной вероятности 95% содержит 12.7% стероидных сапонинов в пересчете на диосцин. Ошибка единичного определения не превышает 5%, результаты эксперимента можно считать удовлетворительными.
Таким образом, разработанная методика позволяет количественно оценивать содержание стероидных сапонинов в пересчете на диосцин в экстракте сухом «Пентафитон» и проводить стандартизацию экстракта по данному показателю.
Количественная оценка проводилась по выходу экстрактивных веществ [1, 2] и суммы стероидных сапонинов. Метрологические характеристики представлены в табл. 5.
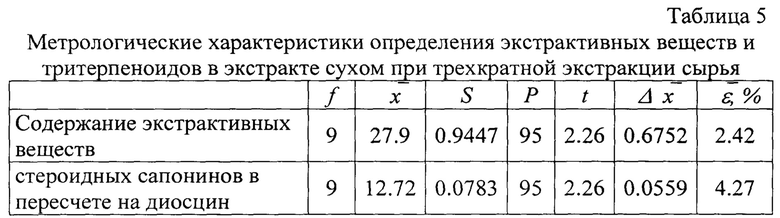
Предложенный способ получения достаточно прост, не требует сложной схемы очистки, позволяет получать продукт постоянного состава. Технология может быть внедрена на предприятиях, выпускающих лекарственные препараты.
Для выявления оптимальных технологических режимов нами были изучены основные факторы, влияющие на процесс экстрагирования растительного сырья: природа экстрагента, его соотношение с сырьем, температурный режим, степень измельчения сырья, продолжительность и количество экстракций.
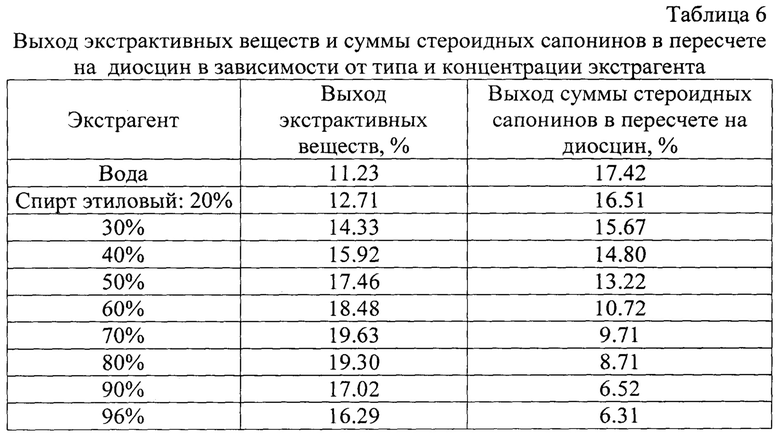
В качестве экстрагентов были использованы вода и этиловый спирт различных концентраций (20, 30, 40, 50, 60, 70, 80, 90, 96%).
Как видно из табл. 6, оптимальным экстрагентом является 50% этиловый спирт, так как позволяет добиться максимального выхода суммы тритерпеноидов с учетом выхода экстрактивных веществ.
Оптимальную степень измельчения определяли для экстракта сухого в целом. Количественную оценку проводили по выходу экстрактивных веществ и суммы стероидных сапонинов в пересчете на диосцин. На основании полученных данных (табл. 7) и с учетом того, что слишком мелкое измельчение растительного материала ведет к загрязнению извлечения труднофильтруемыми высокомолекулярными соединениями, измельчение сырья следует проводить совместно до размера частиц 1 мм.

В связи с тем, что в исходном растительном сырье содержатся термолабильные вещества, изучение влияния температуры на процесс экстракции проводили в интервале температур от 20 до 60°С.Данные представлены в табл. 8, оптимальная температура экстракции - 60±5°С.

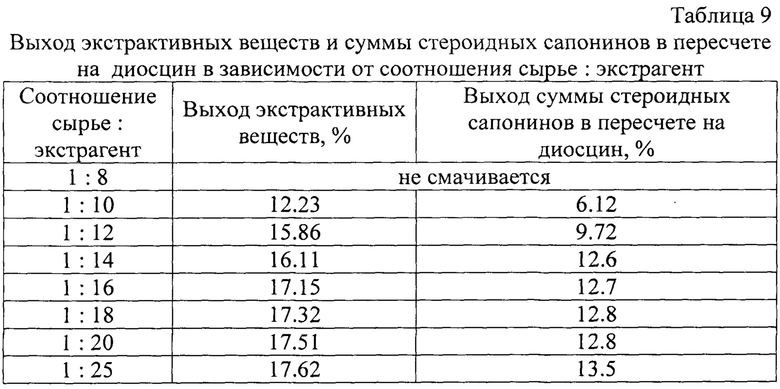
При изучении влияния соотношения сырье: экстрагент на процесс экстракции установлено (табл. 9), что с увеличением количества экстрагента возрастает выход экстрактивных веществ и суммы стероидных сапонинов в пересчете на диосцин, но рост этот для соотношений 1:16 и выше незначителен, поэтому для предотвращения дополнительного расхода экстрагента выбрано соотношение равное 1:(14-16) (с учетом коэффициента водопоглощения).
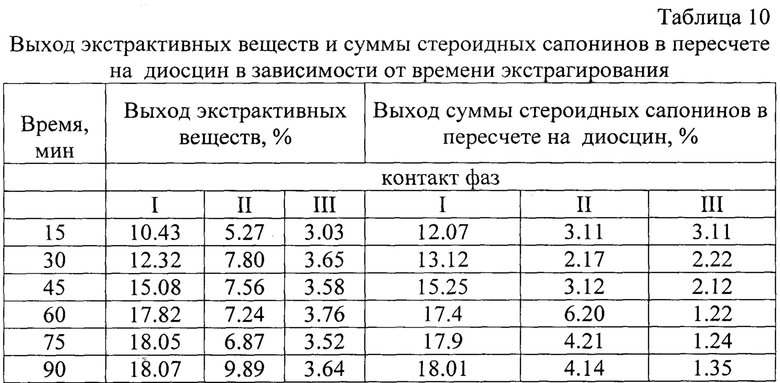
Для определения продолжительности и необходимого количества экстракций установлено время достижения равновесных концентраций экстрактивных веществ и тритерпеноидов в системе сырье: экстрагент в ходе трехкратной экстракции. Для этого проводили экстракцию измельченного сырья 50% этиловым спиртом в соотношении 1:14 на водяной бане при температуре 60°С и постоянном перемешивании в колбе с обратным холодильником. Извлечения, полученные через определенные промежутки времени (15, 30, 45, 60, 75, 90 мин) в процессе трех экстракций, анализировали на содержание экстрактивных веществ и тритерпеноидов. Установлено, что равновесные концентрации устанавливаются при 1-ом и 2-ом контактах фаз через 60 мин, при 3-ем контакте фаз через 30 мин (табл. 10). Трехкратная экстракция обеспечивает достаточно полное истощение сырья - извлекается до 96% действующих веществ.
Предлагаемый способ позволяет получить препарат постоянного состава с более высокой адаптогенной за счет более высокого содержания действующих веществ (тритерпеноидов, флавоноидов, алкалоидов, оксикоричных кислот, дубильных веществ, антоцианов, полисахаридов).
Посчитать экономическую эффективность предлагаемого способа в настоящее время не представляется возможным, однако вышеуказанные преимущества в сочетании с простой схемой получения способствуют рациональному использованию лекарственного растительного сырья и открывают перспективу внедрения данного способа в фармацевтическую промышленность.
Источники информации
1. Государственная Фармакопея СССР. Вып. 1. Общие методы анализа /МЗ СССР. - 11-е изд., доп. - М.: Медицина, 1987. - 336 с.
2. Государственная Фармакопея СССР: Вып. 2. Общие методы анализа. Лекарственное растительное сырье /МЗ СССР. - 11-е изд., доп. - М.: Медицина, 1989. - 400 с.
3. Машковский М.Д. Лекарственные средства. - М., 2008. - 1200 с.
4. Методические рекомендации по экспериментальному изучению препаратов, предлагаемых для клинического изучения в качестве антигипоксических средств. - М., 1990. - 57 с.)
5. Определение безопасности и эффективности биологически активных добавок к пище. Методологические указания. - М.,1999. - 87 с.
6. Перцов С.С.Язвенные поражения желудка у крыс Август и Вистар при остром и эмоциональном стрессе //Бюл.эксп.биол. и медицины. - 1995. - №11. - С. 469-473].
7. Растительные ресурсы России: Дикорастущие цветковые растения, их компонентный состав и биологическая активность. В 6 т. Т.1. Семейства Magnoliaceae - Julandaceae, Ulmaceae, Moraceae, Cannabaceae, Urticaceae. / сост. Беленовская Л.М., Лесиовская E.E., Бобылева Н.С. - СПб., М, 2008. - 421 с.
8. Растительные ресурсы России: Дикорастущие цветковые растения, их компонентный состав и биологическая активность. В 6 т. Т.3. Семейства Fabaceae-Apiaceae. / сост. Л.М. Беленовская, Е.Е. Лесиовская, Н.С. Бобылева - СПб., М, 2010. - 601 с.
9. Растительные ресурсы России: Дикорастущие цветковые растения, их компонентный состав и биологическая активность. В 6 т. Т.6. Семейства Butomaceae-Typhaceae) / сост. Беленовская Л.М., Лесиовская Е.Е., Бобылева Н.С. - СПб., М, 2014. - 391 с.
10. Сидоров К.К. О классификации токсичности ядов при парентеральных способах ведения //Токсикология новых промышленных химических веществ. - М. - 1973. - Вып. 13. - С. 47-51.
11. Сумати Праждня. Большой рецептурник Агинского дацана. Ксилограф Агинского дацана. - Нач. ХХ в. - 151 л. Рукопись, перевод Дашиева Д.Б.
12. «Чжуд-ши»:Канон тибетской медицины. Пер. с тибетского Д.Б. Дашиева. - М.: «Восточная литература», 2001. - 766 с.
13. Химический анализ лекарственных растений. Учебное пособие для фарм. ВУЗов. / Под ред. проф. Н.И. Гринкевич. - М., 1983. - 176 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2716161C1 |
| Композиция фиточая, содержащая панты | 2020 |
|
RU2746625C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2695335C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО СТРЕССПРОТЕКТИВНОЙ И АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2582282C1 |
| Способ получения средства, обладающего антигипоксической активностью | 2017 |
|
RU2669365C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ПИЩЕВАЯ ДОБАВКА | 2011 |
|
RU2449600C1 |
| СЕДАТИВНОЕ СРЕДСТВО | 2005 |
|
RU2295955C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2331432C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2372934C1 |
| Способ получения средства, обладающего стресспротективной, антигипоксической и анксиолитической активностью | 2019 |
|
RU2705582C1 |
Изобретение относится к химико-фармацевтической промышленности, а именно к способу получения средства, обладающего адаптогенной активностью. Способ получения лекарственного средства, обладающего адаптогенной активностью, представляет собой сухой экстракт, полученный из следующего растительного сырья в соотношении: корневищ купены душистой 20 г, корней горичника Морисона 20 г, корней пиона уклоняющегося 20 г, корней спаржи лекарственной 20 г, плодов якорцев стелющихся 20 г, которые измельчают до размера частиц диаметром 1 мм и экстрагируют 50% этиловым спиртом в соотношении сырье : экстрагент, равном 1 : (14-16), при температуре 60°С и постоянном перемешивании, процесс повторяют трижды и объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием, после чего очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°С в течение 8 ч и измельчают на мельнице пропеллерного типа. Вышеописанный способ позволяет получить средство с повышенным выходом действующих веществ, в том числе флавоноидов, которое обладает выраженными адаптогенными свойствами. 10 табл., 1 пр.
Способ получения лекарственного средства, обладающего адаптогенной активностью, представляющего собой сухой экстракт, полученный из следующего растительного сырья в соотношении: корневищ купены душистой 20 г, корней горичника Морисона 20 г, корней пиона уклоняющегося 20 г, корней спаржи лекарственной 20 г, плодов якорцев стелющихся 20 г, которые измельчают до размера частиц диаметром 1 мм и экстрагируют 50% этиловым спиртом в соотношении сырье : экстрагент, равном 1 : (14-16), при температуре 60°С и постоянном перемешивании, процесс повторяют трижды и объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием, после чего очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°С в течение 8 ч и измельчают на мельнице пропеллерного типа.
| СПОСОБ ПОЛУЧЕНИЯ СУММЫ ЭКСТРАКТИВНЫХ ВЕЩЕСТВ, ОБЛАДАЮЩИХ АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2076727C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2187317C2 |
| КОМПОЗИЦИЯ ИНГРЕДИЕНТОВ "АДАПТОВИТ", ОБЛАДАЮЩАЯ АНТИГИПОКСАНТНЫМ ДЕЙСТВИЕМ | 1997 |
|
RU2114628C1 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АДАПТОГЕННЫМ, ГЕПАТОПРОТЕКТОРНЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2011 |
|
RU2473358C1 |
Авторы
Даты
2019-07-23—Публикация
2018-03-05—Подача