Настоящее изобретение относится к интегрированному способу переработки и применения каждой части растения гваюлы серебристой (Parthenium argentatum), включая остаточные части, для цели производства не только натурального каучука, но также соединений, которые могут использоваться в энергетической отрасли и в производстве химических веществ, таких как, например, биобутадиен или бутандиолы, а также в биоочистке.
В настоящей патентной заявке все технологические условия, которые упоминаются в тексте, должны рассматриваться в качестве предпочтительных условий, даже если это не заявляется определенным образом.
Для целей настоящих разъяснений термин «включать» или «содержать» также заключает в себе термин «состоять из» или «состоять, в основном, из».
Для целей настоящих разъяснений, если не заявляются другие условия, определенные интервалы всегда включают предельные значения.
Гваюла представляет собой кустарниковое растение, характерное для полупустынных регионов на юго-западе США и в северной Мексике. Это растение аккумулирует натуральный каучук в форме латекса, главным образом, в коре (ветвей и ствола). Кроме того, вышеупомянутое растение также производит смолы, состоящие, главным образом, из терпеновых соединений, которые распределяются в наибольшей степени в древесной фракции. После экстракции каучука и смолы лигноцеллюлозная фракция может использоваться в качестве источника подвергающихся ферментации сахаров, в то время как листья используются в качестве источника эфирных масел и восков.
Эффективность экстракции каучука снижается, если листья присутствуют в течение процесса экстракции, потому что в результате этого образуется тонкодисперсный материал в течение последующих стадий измельчения. Этот тонкодисперсный материал проявляет тенденцию к закупориванию фильтрация систем, снижает устойчивость разбавленных дисперсий каучука (латекса) и, в конечном счете, увеличивает вплоть до 20% содержание металлов и зольность (непригодный для использования остаток после сжигания растения).
В патенте США № 2434412, в котором описан способ, используемый в экспериментальном проекте в городе Салтильн (штат Коауила, Мексика), показано, что степень извлечения каучука снижается на 10 пунктов, когда листья не удаляются с растений.
В заявке на патент США № 2012/0063969 описано использование механического воздушного оборудования для разделения (сепараторной системы 14/16-18), которая отделяет листья, цветки и мелкие ветви, которые составляют вплоть до приблизительно 30-35% массы растения. Эта фракция листьев цветков направляется в секцию последующей переработки для дальнейших приложений, которые не описываются в патентной заявке.
В настоящее время листья направляются на сжигание или распределяются в качестве почвенных добавок.
Листья содержат значительную фракцию эфирных масел, которые могут количественно экстрагироваться.
В своей статье Scora et al. (R. W. Scora, J. Kumamoto, J. Agric. Food Chem., 1979 г., с. 27) описывают, что пинен и лимонен представляют собой наиболее часто встречающиеся компоненты во фракции эфирных масел, и что вышеупомянутые компоненты встречаются чаще в растениях вида Parthenium argentatum, чем в растениях других видов рода Parthenium.
Используя способ дистилляции с паром в атмосфере CO2, авторы получили масло, содержащее от 60% до 80% монотерпенов, приблизительный состав которых представляет собой следующий: от 17 до 24% α-пинена, от 10 до 20% β-пинена, от 6 до 9% сабинена, от 6 до 9% лимонена, от 9 до 13% терпинолена и 6% борнилацетата.
Пинен представляет собой важное основное соединение для химического синтеза соединений, пригодных для использования в парфюмерной отрасли. Лимонен в чистом виде производится в количестве, составляющем приблизительно 30000 тонн в год (A. D. Karl, Swift, «Каталитические превращения основных терпеновых исходных веществ», Topics in Catalysis, 2004 г., т. 27, с. 1-4).
В настоящее время натуральные терпеновые смолы синтезируются посредством полимеризации α- и β-пинена, получаемых путем дистилляции скипидарного масла, производимого путем дистилляции с паром сосновой/лиственничной смолы).
Кроме того, пинен может использоваться для получения синтетических связующих веществ. Например, в международной патентной заявке № WO 2008/147439, европейской патентной заявке № 2152511, патентной заявке США № 2008/300526 и японской патентной заявке № 2010529227 описано (приклеивающееся к влажной коже) связующее вещество, которое составляют гваюловый каучук и повышающее клейкость вещество на основе гваюловой или политерпеновой смолы, содержащей поли-α- или β-пинен. Смола обеспечивает связующие свойства по отношению к влажной коже и в воде, в то время как каучуковый компонент придает сцепление связующему веществу.
Листья покрывает тонкий слой воска, который представляет собой незначительный компонент сухой массы листьев (приблизительно от 1 до 3%). Гваюловый воск имеет свойства, аналогичные свойствам карнаубского воска. Воск можно извлекать, используя органический растворитель (например, гексан), и очищать посредством последующей экстракции спиртом (например, метанолом).
В своей статье J. Marvah et al. (J. Marvah, Wood Chem. & Techn., 1994 г., т. 14, с. 563) описывает экстракцию листьев с помощью циклогексана в качестве растворителя и последующую очистку посредством экстракции метанолом, за которой следует кристаллизация из CHCl3 с выходом, составляющим приблизительно 2% по отношению к массе сухих листьев.
Натуральный гваюловый каучук присутствует, главным образом, в коре и в древесной ткани растения как водная суспензия, тонко диспергированная в клетках растения (латекс).
Экстракция и получение латекса и каучука подробно описываются в литературе. В патентной заявке США № 2006/149015, патентной заявке США № 7923039, международной патентной заявке № WO 2007/081376, международной патентной заявке № WO 2007/081376, европейском патенте № 1969036, европейском патенте № 1969036 и патентной заявке США № 2012/0063969 описаны устройство и технологические стадии сбора урожая, экстракции, концентрирования и исследования гваюлового латекса. Возможность использования багассы в других процессах, таких как экстракция смолы, а также описывается использование лигнина, целлюлозы и гемицеллюлозы. В конечном счете, описаны все материалы, получаемые из гваюлы, которые не представляют собой латекс, такие как смола, лигнин, связующие вещества, пестициды, противогрибковые вещества, этанол, скошенный материал для мульчирования, органические добавки для почвы, топливо, гранулы, строительные материалы и изоляционные материалы. В патенте США № 7259231, патентной заявке США № 2006/106183, международной патентной заявке № WO 2007/046859, патентной заявке США № 2011/021743, патентной заявке США № 2008/015336, европейском патенте № 1948715, европейском патенте № 1948715, европейском патенте № 1948715 описаны способы экстракции, разделения, фракционирования и очистки растительных биополимеров (гваюловой смолы и каучука) посредством экстракции сверхкритическим растворителем (например, сверхкритическим CO2, который представляет собой хороший растворитель для смолы, но не для каучука), а также использование полярных и/или неполярных вспомогательных растворителей для улучшения селективной экстракции смолы или каучука. В перечисленных выше патентах описаны разнообразные приложения, которые представлены ниже:
i) одновременная экстракция смолы и каучука сверхкритическим CO2 и неполярным вспомогательным растворителем (таким как, например, гексан, 1-гексен или циклогексан) и последующее фракционирование сверхкритическим CO2;
ii) селективная экстракция смолы сверхкритическим CO2 и полярным вспомогательным растворителем (таким как, например, H2O, ацетон или этанол) и последующая экстракция каучука неполярным растворителем.
В этих патентных заявках предусматривается необязательная стадия предварительной обработки растения, такая как, например, удаление листьев; стадия разделения; стадия фракционирования и стадия очистки, но когда растение разделяется на соответствующие компоненты (ветви, листья, смолы и каучук), разработана только экстракции смолы, и описан соответствующий процесс экстракции.
В патенте США № 7790036, патентной заявке США № 2009/099327, международной патентной заявке № WO 2009/051606, европейском патенте № 2205661, европейском патенте № 2205661 описаны способы быстрой экстракции биополимеров, таких как каучук, их растений, таких как гваюла, с использованием растворителя, называемого термином «разбавленный гексан». «Разбавленный гексан» определяется как двухкомпонентная система растворителей, в которой вспомогательный растворитель CO2 используется для увеличения объема и уменьшения плотности гексана. Хотя эти способы используются как для смол, так и для каучука, они оставляют нетронутой лигноцеллюлозную багассу, и отсутствуют какие-либо сведения о ее использовании.
Латекс используется для изготовления промышленных изделий посредством пленочного покрытия (таких как, например, перчатки) или компонентов для специализированных приложений в биомедицинской области (таких как, например, катетеры, специализированные протезы, как описано, например, в патенте США № 8431667 и международной патентной заявке № WO 2009/078883, которые заявляют изготовление изделий на основе тонкой эластичной пленки, толщина которой составляет менее чем 0,04 мм), из натурального каучука, получаемого из гваюлового латекса.
В европейском патенте № 2183303, международной патентной заявке № WO 2009/025675, патентной заявке США № 2009/054595, японской патентной заявке № 2010/536987 и европейском патенте № 2183303 описан способ изготовления изделий из гваюлового каучука, имеющих аналогичные или улучшенные физические свойства по сравнению с каучуком из бразильской гевеи (Hevea brasiliensis).
В международной патентной заявке № WO 2007/081376 заявлен способ экстракции каучука и смолы, в котором используется растворитель (ацетон), способный количественно экстрагировать компоненты смолы. В этом документе описан способ экстракции биополимеров, например, натурального каучука, из растений, не представляющих собой гевею, в частности, из гваюлы.
Одновременная экстракция смолы и каучука подробно описывается в литературе. В международной патентной заявке № WO 2013/134430 описан способ одновременной экстракции смолы и каучука с помощью смеси растворителей, содержащей, например, ацетон и гексан. Смесь после экстракции содержит от 10 до 50% растительного материала, от 50 до 90% смеси, содержащей два растворителя (гексан и ацетон или циклогексан и ацетон в количестве от 10 до 35%), от 0,5 до 10% воды из растения. Полярные растворители, используемые в международной патентной заявке № WO 2013/134430, представляют собой C1-C8-спирты, простые и сложные C2-C8-эфиры, циклические простые C4-C8-эфиры, C3-C8-кетоны и их сочетания. В международной патентной заявке № WO 2013/192217 описаны некоторые виды предварительной обработки биомассы, которые доводят до максимума экстракцию каучука и смолы из растения, в то время как в патенте США № 7790036 описано применение разбавленного гексана (т. е. смешанного с соответствующим растворителем) в качестве растворителя для экстракции, который оказывается более эффективным, чем сверхкритический CO2 или смесь CO2 и гексана в качестве вспомогательного растворителя.
Условия экстракции смолы и каучука были подробно исследованы в двух статьях, которые цитируются ниже:
- M. E. Salvucci et al., Industrial Crops and Products, 2009 г., т. 30, с. 9-16 и
- K. Cornish et al., Industrial Crops and Products, 2013 г., т. 41, с. 158-164.
В этих статьях описан способ количественного определения разнообразных фракций смолы и каучука, в котором осуществляется «Ускоренная экстракция растворителем» (ASE). Полярный растворитель, такой как ацетон или ацетонитрил, используется для экстракции смолы, в то время как неполярный растворитель (циклогексан) используется для экстракции каучука.
Во всех цитируемых документах описаны способы оптимизации условий для хранения, экстракции и очистки каучука и/или смолы из растения, независимо от условий, необходимых для достижения полного использования остаточной лигноцеллюлозной фракции, которая, тем не менее, составляет от 40 до 50% массы багассы. После экстракции и удаления растворителя смола может использоваться во многих прикладных областях (как показывают номера 9, 10 и 11 на фиг. 1). В связи с этим Nakajama («Будущее развитие гваюлы», F. S. Nakayama, Industrial Crops and Products, 2005 г., т. 22, с. 3-13) составил исчерпывающий список многочисленных возможных приложений гваюловой смолы в ходе исследований и экспериментов в масштабе лаборатории и опытного производства. Помимо прочего, сесквитерпеновый компонент смол (включая аргентатин A и B) может заменять синтетические соединения за счет своего пестицидного или фунгицидного действия (как показывает номер 10 на фиг. 1). Например, для борьбы с паразитическими нематодами оказывается возможным использование смолы, которая заменяет метилбромид, опасное химическое вещество, которое было запрещено в качестве противопаразитического вещества вследствие своей токсичности. Аргентатин A (один из основных компонентов гваюловой смолы) оказался ингибитором ацетилхолиназы с соответствующими противомикробными свойствами.
Фракция экстрагированной смолы может использоваться для нанесения на древесный материал, где, как было подтверждено экспериментально, он повышает сопротивление материала по отношению к микробиологическому и атмосферному воздействию. Nakayama (F. S. Nakayama et al., Industrial Crops and Products, 2001 г., т. 14, с. 105-111) обнаружил, что гваюловая смола, используемая для консервации изделий, изготовленных из древесины, проявляет такую же эффективность, как традиционные синтетические соединения (как показывает номер 9 на фиг. 1). Чтобы использовать смолу, которая присутствует в древесине растения, и в результате этого избежать стадии экстракции стадия, существует возможность использования древесного материала, получаемого непосредственно из растения и при этом содержащего фракцию смолы, в композиционных материалах, содержащих полиэтилен, или в других древесных материалах для изготовления композиционных материалов в таких приложениях, где требуется повышенное сопротивление к нападению термитов и/или сопротивление по отношению к грибам или другим микроорганизмам. В патентной заявке США № 2009/0099309 и международной патентной заявке № WO 2009/051605 описан способ получения термопластического многокомпонентного полимера гваюловой смолы посредством реакции смолы, в которой содержится приблизительно 20% низкомолекулярного каучука (LMR), с ненасыщенным мономером, в качестве которого выбирается, например, стирол, простой виниловый эфир, изопрен, метакриловая и акриловая кислоты и соответствующие амиды и сложные эфиры, в органическом растворителе, таком как, например, толуол. Сополимеризация повышает прочность когезии, прозрачность, а также термическую и окислительную устойчивость смолы, и в результате этого становится возможным термоплавкое приложение.
В международной патентной заявке № WO 2008/147439, европейском патенте № 2152511 и патентной заявке США № 2008/300526 описаны прикрепляющиеся к влажной коже связующие материалы, которые составляют гваюловый каучук и повышающее клейкость вещество, основу которого представляет собой гваюловая смола или политерпен (поли-α- или β-пинен). Эта смола обеспечивает связующие свойства на влажной коже и в воде, в то время как каучук придает сцепление со связующим веществом.
В документах предшествующего уровня техники описана возможность модификации компонентов гваюловой смолы посредством химических реакций для цели ее использования в качестве повышающего клейкость вещества или в качестве компонента для композиционных материалов. Например, в патентной заявке США № 1985/4542191 описана обработка, в которой используется формальдегид, фенолформальдегид или карбамидоформальдегид. Способы получения вышеупомянутых веществ включают следующие стадии: обработка формальдегидом; обработка фенолформальдегидом; обработка карбамидоформальдегидом; обработка кислотами и обработка сульфидами, а также их сочетания.
Разрушение и осахаривание лигноцеллюлозной гваюловой биомассы было всесторонне исследовано, о чем четко свидетельствует анализ документов предшествующего уровня техники. Известно, что гваюловая багасса может использоваться в качестве источника сахаров после соответствующей разрушающей обработки и последующей реакции гидролиза. Например, в своей работе Srinivasan et al. (N. Srinivasan, Bioresource Technology, 2010 г., т. 101, с. 9785-9791) исследовали осахаривание гваюловой багассы посредством взрывной обработки сверхкритическим CO2 при высоком давлении (взрыв сверхкритического CO2). После экстракция латекса и смолы багасса подвергается взрывной обработке при повышенной температуре, составляющей вплоть до 200°C, и повышенном давлении, составляющем вплоть до 4000 фунтов на квадратный дюйм (27,6 МПа). Лигноцеллюлозный остаток затем подвергается ферментативной обработке для цели завершения гидролиза целлюлозы. Суммарный выход мономерных сахаров (C5 и C6) в процессе гидролиза составлял 86% по отношению к суммарному количеству первоначально присутствующих восстанавливающих сахаров. Однако те же авторы в последующей работе сообщают результаты оптимизационной обработки условий и параметров (N. Srinivasan et al., Biomass and Bioenergy, 2012 г., т. 47, с. 451-458) с использованием такой же технологии взрыв сверхкритического CO2) и делают вывод о том, что в наилучших условиях получается суммарный выход мономеров в процессе гидролиза, составляющий 57% по отношению к первоначальному количеству сахаров. Способ осахаривания, описанный в этих статьях, предусматривает использование повышенных температур и давлений и, таким образом, не является предпочтительным. Кроме того, суммарный выход в процессе гидролиза, после оптимизации, не превышает 57% в технологических условиях повышенной температуры и давления.
Кроме того, известно, что Chundawat (S. P. S. Chundawat et al., Industrial Crops and Products, 2012 г., т. 37, с. 486-492) наблюдали, что осахаривание гваюловой багассы может осуществляться с использованием технологии разрушения волокон аммиаком (AFEX) в качестве технологии предварительной обработки биомассы. Были исследованы разнообразные формы багассы, в том числе непереработанные и получаемые после экстракции смолы. Наилучшие результаты были получены в случае багассы, из которой была удалена смола, и которая обеспечивала в процессе гидролиза суммарный выход мономерных C5- и C6-сахаров, составляющий 44% по отношению к количеству первоначально присутствующих сахаров. Получаемые в результате сахара в любом случае оказываются подвергающимися ферментации под действием дрожжей с образованием этанола. В этой технологии предварительной обработки используется аммиак при высоком давлении, который должен рециркулировать, чтобы процесс становился устойчивым. Кроме того, данная технология включает осахаривание багассы с выходами, составляющими не более чем 44%. Кроме того, как отмечается в статье, гидролиз целлюлозы из багассы, получаемой после последовательной экстракции каучука (основной водой) и смолы (полярным растворителем), оказывается менее эффективным, чем в случае целлюлозы из цельного растения, которое не подвергается обработке каким-либо способом. Если осуществляется его очистка в достаточной степени, лигнин может использоваться в качестве источника химических соединений после соответствующих реакций деполимеризации и/или получения производных. В качестве альтернативы, он используется как компонент универсального наполнителя в полимерных материалах таких как, например, пластмассы и каучуки, для улучшения соответствующих механических и физико-химических свойств. Например, он может использоваться в композициях эпоксидных смол и фенолформальдегидных смол. В случае шинных каучуков лигнин действует в качестве армирующего компонента вместо технического углерода; по сравнению с последним, лигнин имеет менее высокую плотность, является неэлектропроводным, имеет более светлый цвет и способен заменять технический углерод, часто улучшая механические и физико-химические свойства композиции.
В патенте DE 10057910-A1 описано получение лигнина, который подвергается дериватизации (химической модификации) под действием нуклеофильных соединений, образуя сложные эфиры, простые эфиры или полуацетали. Такой лигнин может использоваться в качестве добавки или в качестве наполнителя для изготовления полимерных продуктов, таких как, например, полистирол, повышая соответствующую способность биоразложения. Barzegari et al. описывают использование лигнина в качестве наполнителя в полистироле и сополимерах этилена, стирола и бутилена (M. R. Barzegari et al., Polymer Composites, 2012 г., т. 33, с. 353-361). Были исследованы реологические и механические свойства смесей, содержащих лигнин в повышенных количествах, составляющих вплоть до 80%. Согласно наблюдениям, модуль упругости увеличивается в зависимости от количества лигнина, присутствующего в композиционном материале. Pucciariello et al. описывают физические свойства некоторых смесей лигнина с синтетическими полимерами (R. Pucciariello et al., Polymer, 2004 г., т. 45, с. 4159-4169. Лигнин, источником которого является злаковая солома, предварительно обработанная посредством парового взрыва, смешивали с полиэтиленом разнообразной плотности и полистиролом. Оказывается возможной обработка смесей с использованием традиционных технологий, применяемых в случае термопластических полимеров. В смесях, содержащих лигнин, модуль упругости незначительно увеличивается, в то время как напряжение и сопротивление растяжению уменьшаются. Кроме того, лигнин действует в качестве стабилизатора по отношению к разрушению, вызываемому ультрафиолетовым излучением.
Возможность использования лигнина в качестве источника органических соединений, биотоплива и водорода проанализировали Azadi et al. (P. Azadi et al., Renewable and Sustainable Energy Reviews, 2013 г., т. 21, с. 506-523). Разнообразные технологии могут использоваться в промышленном масштабе для деполимеризации лигнина и получения органических соединений (ароматических соединений, включая фенол) или для превращения лигнина в синтетический газ, который может использоваться для производства жидкого топлива или промежуточных и органических соединений, включая превращение биомассы в бензол, толуол и ксилол (BTX). Например, применения лигнина (несульфонированного, аналогичного лигнину, который описывается в настоящем изобретении) может включать такие области, как битумы, цементные добавки, активированный уголь, углеродные волокна, фенольные смолы, а также продовольственный сектор, например, производство синтетического ванилина. Эти типы приложений в разнообразных отраслях промышленности представляет документ «Химические вещества с высшей добавленной стоимостью из биомассы - результаты отбора потенциальных кандидатов из лигнина, произведенного в процессе биологической переработки», т. II, Тихоокеанская северо-западная национальная лаборатория (PNNL) -16983, 2007 г., и включают использование лигнина в качестве углеродных волокон, в качестве добавки для полимеров и пластмасс, в качестве компонента в синтезе смол, связующих материалов и клеев.
Таким образом, существует потребность в разработке интегрированного способа, позволяющего использовать все компоненты растения гваюлы. С другой стороны, документы предшествующего уровня техники, описывают только разделение и использование индивидуальных компонентов растения гваюлы с использованием способов, которые часто оказываются независимыми друг от друга.
Таким образом, заявитель разработал интегрированный способ, который делает возможным использование каждой отдельной части растения гваюлы.
В частности, заявитель обнаружил, что твердый остаток, который получается после процессов экстракции восков и эфирных масел может предпочтительно использоваться, чтобы получать смолы, лигнин и подвергающиеся ферментации сахара.
Подвергающиеся ферментации сахара могут производиться из гемицеллюлозы и целлюлозы и могут после этого использоваться для производства химических веществ, таких как биобутадиен или бутандиолы, микробные масла и биотоплива (через липиды или триглицериды).
Это объясняется тем, что целлюлоза и гемицеллюлоза могут быть сделаны более легкодоступными посредством применения соответствующих технологий разрушения биомассы, которые, например, вызывают нарушение взаимодействия между целлюлозой и лигнином. Таким образом, гемицеллюлоза и целлюлоза могут легче разлагаться с использованием соответствующих технологий гидролиза для получения простых сахаров (осахаривание), которые использоваться в качестве источника питания для вызывающих ферментацию микроорганизмов.
Хотя в литературе присутствуют некоторые примеры разрушения и осахаривания биомассы, получаемой из растения гваюлы, использование этой остаточной фракции до настоящего времени не было подробно исследовано.
Первая задача настоящего изобретения, таким образом, заключается в том, чтобы предложить интегрированный способ, который перерабатывает и использует каждую отдельную часть биомассы, которая производится из растения гваюлы, и из которой производятся разнообразные продукты, которые могут использоваться в качестве источников энергии и в качестве химических веществ, таких как биобутадиен, например, в процессе получения топлива, энергии и химикатов из биомассы.
Следующая задача настоящего изобретения заключается в том, чтобы предложить интегрированный способ, в котором стадии разрушения и осахаривания делают возможным более эффективное производство подвергающихся ферментации сахаров в отношении количества и качества, другими словами при пониженном содержании примесей по сравнению с другими технологиями, уже известными и используемыми в документах предшествующего уровня техники.
Для этой цели заявитель разработал интегрированный способ переработки и применения каждой части растения гваюлы серебристой (Parthenium argentatum), который включает последовательные стадии в таком порядке:
- отделение ствола и ветвей (3) от листьев (2) вышеупомянутого растения посредством механической обработки (1);
- обработка листьев (100), в которой производятся воски и эфирные масла (102), а также фракция (101), в которой содержатся целлюлоза, гемицеллюлоза (углеводы) и, в меньшей степени, соли, органические соединения и лигнин;
- экстракция (200) из ствола и ветвей жидкой фазы (4), в результате которой образуется первый твердый древесный остаток (5), называемый термином «багасса» в настоящем документе;
- обработка вышеупомянутого первого твердого древесного остатка (5), в результате которой производятся сахара, смола, каучук и лигнин.
Интегрированный способ, который предлагается в настоящей патентной заявке, имеет преимущество эффективного и удобного использования всего растения гваюлы, которое обычно используется только селективно для производства натурального каучука или смолы.
Использование всех компонентов гваюлы делает возможным также производство, помимо натурального каучука, соединений, которые являются пригодными для использования в разнообразных отраслях промышленности, таких как энергетическая, пищевая, фармацевтическая или лесная промышленность (как показывают номера 9, 10 и 11 на фиг. 1), и, в более общем случае, в производстве химических веществ. Эти вещества включают, например, мономеры, пригодные для использования в синтезе полимеров и синтетических каучуков, такие как бутадиен. Интегрированный способ, который предлагает настоящее изобретение, допускает использование всех фракций, которые могут быть получены из растения гваюлы, включая любые остаточные фракции, причем особо следует отметить производство подвергающихся ферментации сахаров, получаемых из лигноцеллюлозной фракции.
Следующие цели и преимущества настоящего изобретения становятся более очевидными из следующего описания и прилагаемых чертежей, которые представлены исключительно в качестве неограничительного примера.
Фиг. 1 описывает интегрированный способ, в котором осахаривание осуществляется перед стадией экстракции смолы, согласно предпочтительному варианту осуществления настоящего изобретения.
Фиг. 2 описывает интегрированный способ, в котором стадия экстракции смолы осуществляется перед осахариванием, согласно предпочтительному варианту осуществления настоящего изобретения.
Фиг. 3 описывает обработку листьев растения гваюлы согласно предпочтительному варианту осуществления настоящего изобретения.
Фиг. 4 описывает обработку ствола и ветвей растения гваюлы для экстракции латекса согласно предпочтительному варианту осуществления настоящего изобретения.
Фиг. 5 описывает обработку ствола и ветвей растения гваюлы для экстракции каучука согласно предпочтительному варианту осуществления настоящего изобретения.
Фиг. 6 описывает экстракцию смолы из первого твердого древесного остатка согласно предпочтительному варианту осуществления.
Фиг. 7 описывает стадию осахаривания предпочтительному варианту осуществления.
Эти чертежи будут подробно описаны ниже.
Подробное описание
Как показывают фиг. 1-7, настоящее изобретение, соответственно, предлагает интегрированный способ переработки и применения каждой части растения гваюлы серебристой (Parthenium argentatum), который включает последовательные стадии в таком порядке:
- отделение ствола и ветвей (3) от листьев (2) вышеупомянутого растения посредством механической обработки (1);
- обработка листьев (100), в которой производятся воски и эфирные масла (102), а также фракция (101), в которой содержатся целлюлоза, гемицеллюлоза (углеводы) и, в меньшей степени, соли, органические соединения и лигнин;
- экстракция (200) из ствола и ветвей жидкой фазы (4), в результате которой образуется первый твердый древесный остаток (5), называемый термином «багасса» в настоящем документе;
- обработка вышеупомянутого первого твердого древесного остатка (5), в результате которой производятся сахара, смола, каучук и лигнин.
Согласно предпочтительному варианту осуществления настоящего изобретения, обработка ствола и ветвей (3) представляет собой экстракцию основной водой, в процессе которой образуются водная эмульсия (4) и первый твердый древесный остаток (5), в котором содержатся лигнин, целлюлоза, гемицеллюлоза, смола и остаточный каучук. Концентрированный латекс (203 или 13 на фиг. 1 и 2) экстрагируется из вышеупомянутой водной эмульсии. Натуральный каучук (204 или 14 на фиг. 1 и 2) может быть получен из концентрированного латекса (203 или 13 на фиг. 1 и 2) посредством дополнительной стадия коагуляции. Согласно предпочтительному варианту осуществления настоящего изобретения, ствол и ветви (3), с другой стороны, обрабатываются посредством экстракции неполярным органическим растворителем, в качестве которого предпочтительно выбираются неразветвленные, разветвленные и циклические алканы, содержащие от 5 до 12 атомов углерода и называемые термином «C5-C12-алканы», предпочтительно содержащие от 6 до 8 атомов углерода и называемые термином «C6-C8- алканы», предпочтительнее содержащие 5, 6, 7 и 8 атомов углерода; более предпочтительные алканы представляют собой соединения, в качестве которых выбираются н-пентан, н-гексан, н-гептан, н-октан и циклогексан, а также их смеси, и образуются органический раствор (211) и первый твердый древесный остаток (5), в котором содержатся гемицеллюлоза, целлюлоза и лигнин. Натуральный каучук (212 или 14 на фиг. 1 и 2) экстрагируется из вышеупомянутого органического раствора, предпочтительно посредством осаждения полярным растворителем, таким как, например, ацетон, этилацетат или их смеси, причем данный каучук может после этого также повторно диспергироваться в воде, образуя латекс (216 или 13 на фиг. 1 и 2).
Согласно предпочтительному варианту осуществления, способ, описанный и заявленный в настоящей патентной заявке, включает последовательные стадии в таком порядке:
- отделение ствола и ветвей (3) от листьев (2) вышеупомянутого растения посредством механической обработки (1)
- обработка листьев (100), в которой производятся воски и эфирные масла (102), и твердая фракция (101), в которой содержатся целлюлоза, гемицеллюлоза (углеводы) и, в меньшей степени, соли, органические соединения и лигнин;
- экстракция (200) из ствола и ветвей жидкой фазы (4) и в результате которой образуется первый твердый древесный остаток (5), называемый термином «багасса» в настоящем документе;
- экстракция смолы и каучука (300) из вышеупомянутого первого твердого древесного остатка (5), в результате которого образуются пятый твердый древесный остаток (19), содержащий лигнин, гемицеллюлозу и целлюлозу;
- гидролиз (400) вышеупомянутого пятого твердого остатка (19), в котором образуются сахара, содержащие 5 атомов углерода (8), и шестого твердого древесного остатка (20), содержащего лигнин и целлюлозу;
- гидролиз вышеупомянутого шестого твердого остатка (20) для превращения целлюлозы в сахара, содержащие 6 атомов углерода и называемые термином «C6» в настоящем документе, в результате которого образуются конечный твердый остаток (18) содержащий лигнин и остаточная целлюлоза в количестве, составляющем менее чем 20%.
Для целей настоящего описания и прилагаемой формулы изобретения, выражение «сахара, содержащие 5 атомов углерода» рассматривается таким образом, что им обозначается сахар пентоза или проще пентоза, которая представляет собой моносахаридный углевод, содержащий пять атомов углерода и имеющий химическую формулу C5H10O5. Для целей настоящего описания и прилагаемой формулы изобретения, выражение «сахара, содержащие 6 атомов углерода» рассматривается таким образом, что им обозначается сахар гексоза или проще гексоза, которая представляет собой моносахаридный углевод, содержащий шесть атомов углерода и имеющий химическую формулу C5H12O6..
Как показывает фиг. 2, первый твердый древесный остаток (5) обрабатывается посредством экстракции органическим неполярным растворителем (300), в качестве которого предпочтительно выбираются неразветвленные, разветвленные и циклические алканы, содержащие от 5 до 12 атомов углерода и называемые термином «C5-C12-алканы», предпочтительно имеющий от 6 до 8 атомов углерода и называемые термином «C6-C8 алканы», предпочтительнее содержащие 5, 6, 7 и 8 атомов углерода, более предпочтительные алканы представляют собой соединения, в качестве которых выбираются н-пентан, н-гексан, н-гептан, н-октан и циклогексан и их смеси, для отделения смолы и каучука (7), и в результате этого образуется пятый твердый древесный остаток (19), содержащий лигнин, гемицеллюлозу и целлюлозу. Вышеупомянутый пятый твердый остаток (19) после этого подвергается осахариванию (400) на двух стадиях. На первой стадии осуществляется кислотный гидролиз (404), чтобы превращать гемицеллюлозу в сахара, содержащие 5 атомов углерода и называемые термином «C5» в настоящем документе, и в результате этого образуется шестой твердый древесный остаток (20), содержащий лигнин и целлюлозу.
Кислотный гидролиз осуществляется фосфоновой кислотой, представляющей собой органическую кислоту, имеющую общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом.
Алкильная группа может предпочтительно содержать от 1 до 6 атомов углерода, предпочтительнее от 1 до 3 атомов углерода.
В качестве алкильной группы предпочтительно выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Ароматическая группа предпочтительно выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленная или разветвленная алкил, содержащий от 1 до 3 атомов углерода, предпочтительно R' представляет собой метил.
Группа, содержащая гетероатом, предпочтительно выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно -CH3OH-PO(OH)2 (дифосфонатная) группа.
Более предпочтительными являются алкилфосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, которая может содержать от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода; предпочтительнее в качестве R выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Более предпочтительными являются фосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует группа, содержащая гетероатом, выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно CH2-PO(OH)2 (дифосфонатная) группа.
Среди фосфоновых кислот те, которые являются предпочтительными, представляют собой соединения, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует -CH3OH-PO(OH)2 (дифосфонатная) группа или этидроновая кислота (известная как 1-гидроксиэтан-1,1-дифосфоновая кислота), или в которой в качестве R присутствует метильная группа или метанфосфорная кислота (метилфосфоновая кислота).
Значение pH в течение кислотного гидролиза предпочтительно составляет от 0,6 до 1,6, предпочтительно от 0,8 до 1,3, предпочтительнее от 0,9 до 1.
Кислотный гидролиз предпочтительно осуществляется при температуре в интервале, который составляет от 120°C до 160°C, предпочтительнее от 130°C до 150°C, еще предпочтительнее при 140°C.
После этого вышеупомянутый шестой твердый остаток (20) подвергается последующему гидролизу, в качестве которого выбирается ферментативный, химический или термохимический гидролиз (402), для превращения целлюлозы в сахара, содержащие 6 атомов углерода и называемые термином «C6» в настоящем документе, и результате этого образуются твердый остаток (18), содержащий лигнин и остаточную целлюлозу в количестве, составляющем менее чем 20%. Согласно предпочтительному варианту осуществления, способ, описанный и заявленный в настоящей патентной заявке, включает последовательные стадии в таком порядке:
- отделение ствола и ветвей (3) от листьев (2) вышеупомянутого растения посредством механической обработки (1);
- обработка листьев (100), в которой производятся воски и эфирные масла (102), и твердая фракция (101), в которой содержатся целлюлоза, гемицеллюлоза (углеводы) и, в меньшей степени, соли, органические соединения и лигнин;
- экстракция (200) из ствола и ветвей жидкой фазы (4), в результате которой образуется первый твердый древесный остаток (5), называемый термином «багасса» в настоящем документе;
- обработка первого твердого древесного остатка (5), в котором образуются сахара, содержащие 5 атомов углерода (8) и в результате этого образуется второй твердый остаток (15);
- обработка вышеупомянутого второго твердого остатка (15), в которой образуются сахара, содержащие 6 атомов углерода (16), и третий твердый остаток (17) (400),
- экстракция смолы и каучука (7) (300) из вышеупомянутого третьего твердого остатка (17) и образование четвертого древесного остатка (18), состоящего, главным образом, из лигнина.
Согласно вышеупомянутому предпочтительному варианту осуществления, который представлен на фиг. 1, первый твердый древесный остаток (5) обрабатывается способом двухстадийного осахаривания.
На первой стадии осуществляется кислотный гидролиз (404), чтобы превращать гемицеллюлозу в сахара, содержащие 5 атомов углерода, C5, образуя второй твердый остаток (15), содержащий лигнин, целлюлозу, каучук и смолы.
Кислотный гидролиз осуществляется фосфоновой кислотой, представляющей собой органическую кислоту, имеющую общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом.
Алкильная группа может предпочтительно содержать от 1 до 6 атомов углерода, предпочтительнее от 1 до 3 атомов углерода.
В качестве алкильной группы предпочтительно выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Ароматическая группа предпочтительно выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, предпочтительно R' представляет собой метил.
Группа, содержащая гетероатом, предпочтительно выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно -CH3OH-PO(OH)2 (дифосфонатная) группа.
Более предпочтительными являются алкилфосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, которая может содержать от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода; предпочтительнее в качестве R выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил.
Более предпочтительными являются фосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует группа, содержащая гетероатом, выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно CH2-PO(OH) 2 (дифосфонатная) группа.
Среди фосфоновых кислот те, которые являются предпочтительными, представляют собой соединения, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует -CH3OH-PO(OH)2 (дифосфонатная) группа или этидроновая кислота (известная как 1-гидроксиэтан-1,1-дифосфоновая кислота), или в которой в качестве R присутствует метильная группа или метанфосфорная кислота (метилфосфоновая кислота).
Значение pH в течение кислотного гидролиза предпочтительно составляет от 0,6 до 1,6, предпочтительно от 0,8 до 1,3, предпочтительнее от 0,9 до 1.
Кислотный гидролиз предпочтительно осуществляется при температуре в интервале, который составляет от 120°C до 160°C, предпочтительнее от 130°C до 150°C, еще предпочтительнее при 140°C.
После этого вышеупомянутый второй твердый остаток (15) обрабатывается предпочтительно посредством гидролиза, в качестве которого выбирается ферментативный, химический или термохимический гидролиз (402), для превращения целлюлозы в C6-сахара, содержащие 6 атомов углерода, и в результате этого образуются третий твердый остаток (17) включающий лигнин, смола, остаточный каучук, и остаточная целлюлоза в количестве, составляющем менее чем 20%.
Третий твердый остаток (17) затем подвергается экстракции органическим растворителем (300), в качестве которого выбираются ацетон, спирты, этилацетат и их смеси, чтобы отделить смолу и остаточный каучук (7) от четвертого твердого остатка (18), содержащего лигнин и целлюлозу в количестве, составляющем менее чем 20%.
Эта конкретная и предпочтительная последовательность операций, включая осахаривание (400), предшествующее экстракции смолы (300), обеспечивает преимущество экстракции смолы посредством единственной стадии экстракции с использованием органического растворителя. При использовании обратной последовательности, в которой сначала осуществляется экстракция смолы (300), после которой осуществляется осахаривание (400), оказываются необходимыми две последующие экстракции органическим растворителем, если смола должна быть извлечена количественно.
В результате выделения C5- и C6-сахаров перед экстракцией смолы повышаются степень превращения и выход подвергающихся ферментации мономерных сахаров по сравнению со случаем осуществления обратной последовательности. Таблица 1 представляет значения выхода и степени превращения, полученные в отношении некоторых примеров.
Полисахаридный, гемицеллюлозный и целлюлозный компоненты могут подвергаться гидролизу, образуя соответствующие простые мономерные компоненты, такие как, например, глюкоза (C6), получаемая из целлюлозы, и смесь C5-сахаров в пропорции, составляющей вплоть до 80%, таких как, например, ксилоза и арабиноза, получаемые из гемицеллюлозы.
Мономерные сахара, получаемые таким способом, могут предпочтительно использоваться в качестве источника углерода в процессах ферментации для производства спиртов, таких как, например, этанол и бутанол, диолы, такие как, например, 1,3-пропандиол, 1,3-бутандиол, 1,4-бутандиол или 2,3-бутандиол, и другие химические вещества, получаемые посредством ферментации.
После соответствующей реакции дегидратация диолы могут использоваться для производства бутадиена, который является пригодным для использования в качестве мономера для синтеза биополибутадиена. В качестве альтернативы, такие сахара могут использоваться для ферментативного синтеза липидов, триглицеридов с высоким содержанием ненасыщенных кислот (например, олеиновой кислоты) или других промежуточных веществ и продуктов.
Вышеупомянутые спирты, диолы, липиды или другие промежуточные вещества или продукты могут предпочтительно использоваться в химической промышленности или в изготовлении автомобильного топлива.
После кислотного гидролиза багасса содержит гваюлин A и B, гидролизованный с образованием партениола, гидроксибензойной кислоты и коричной кислоты. Партениол можно затем выделять, осуществляя селективное осаждение спиртами, например, метанолом, без направления на последующий гидролиз гваюлинов. Партениол представляет собой соединение, которое проявляет активность по отношению к термитам, а также представляет собой важное основное соединение для синтеза парфюмерных продуктов или продуктов для уничтожения насекомых-вредителей.
Как показывает фиг. 6, согласно предпочтительному варианту осуществления настоящего изобретения, первый твердый древесный остаток (5) подвергается предварительной обработке посредством кислотного гидролиза (404), который превращает гемицеллюлозу в C5-сахара (8), и образуется второй твердый остаток (15), содержащий целлюлозу, смолу, остаточный каучук и лигнин.
Кислотный гидролиз осуществляется под действием фосфоновой кислоты, представляющей собой органическую кислоту, имеющую общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом.
Алкильная группа может предпочтительно содержать от 1 до 6 атомов углерода, предпочтительнее от 1 до 3 атомов углерода.
В качестве алкильной группы предпочтительно выбирается метил, этил, 1-пропил, 2-стве пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Ароматическая группа предпочтительно выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, предпочтительно R' представляет собой метил.
Группа, содержащая гетероатом, предпочтительно выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно -CH3OH-PO(OH)2 (дифосфонатная) группа.
Более предпочтительными являются алкилфосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, которая может содержать от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода; предпочтительнее в качестве R выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил.
Более предпочтительными являются фосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует группа, содержащая гетероатом, выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно CH2-PO(OH)2 (дифосфонатная) группа.
Среди фосфоновых кислот те, которые являются предпочтительными, представляют собой соединения, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует -CH3OH-PO(OH)2 (дифосфонатная) группа или этидроновая кислота (известная как 1-гидроксиэтан-1,1-дифосфоновая кислота), или в которой в качестве R присутствует метильная группа или метанфосфорная кислота (метилфосфоновая кислота).
Значение pH в течение кислотного гидролиза предпочтительно составляет от 0,6 до 1,6, предпочтительно от 0,8 до 1,3, предпочтительнее от 0,9 до 1.
Кислотный гидролиз предпочтительно осуществляется при температуре в интервале, который составляет от 120°C до 160°C, предпочтительнее от 130°C до 150°C, еще предпочтительнее при 140°C. Вышеупомянутый второй твердый остаток (15) после этого подвергается экстракции неполярным органическим растворителем, в качестве которого предпочтительно выбираются неразветвленные, разветвленные и циклические алканы, содержащие от 5 до 12 атомов углерода и называемые термином «C5-C12-алканы», предпочтительно содержание от 6 до 8 атомов углерода и называемые термином «C6-C8-алканы», предпочтительнее содержащие 5, 6, 7 и 8 атомов углерода; более предпочтительные алканы представляют собой соединения, в качестве которых выбираются н-пентан, н-гексан, н-гептан, н-октан и циклогексан и их смеси, и при этом образуются органический раствор (305) и первый твердый древесный остаток, содержащий гемицеллюлозу, целлюлозу и лигнин (306). Органический раствор экстрагируется полярным органическим растворителем (307), в качестве которого предпочтительно выбираются ацетон, спирты, этилацетат и их смеси, для отделения посредством осаждения каучука (310) от смол, которые остаются в растворе (312), в то время как твердая фракция подвергается процессам, в качестве которых предпочтительно выбираются ферментативный гидролиз или химический или термохимический гидролиз, (311), и получается твердый древесный остаток, содержащий, по меньшей мере, 80% лигнина (308) и C6-сахаров из целлюлозы (309).
Целое растение гваюла разрезают у шейки ствола и механически очищают от листьев (1) таким образом, чтобы отделить ствол и ветви (3) от листьев (2).
В совокупности листья составляют от 30 до 50% сухой массы целого растения. Листья отделяют от растения перед стадией экстракции латекса, потому что содержание в них каучука составляет от лишь 0,5% до 1,7 мас.% по отношению к полной массе растения и составляет менее чем 20% всего каучука. Следовательно, обработка посредством экстракции каучука сосредоточена исключительно на древесной части ветвей и ствола, в которой содержится более 80% каучука.
Рассмотрим следующее описание фиг. 1 и 4.
Листья (2) можно обрабатывать (100), чтобы получать воски и эфирные масла (102), предпочтительно способом, выбранным из экстракции растворителем, или посредством паровой экстракции, или посредством экстракции сверхкритическим CO2.
Когда воски и эфирные масла отделяются от листьев, остается твердая фракция (101), в которой содержатся целлюлоза, гемицеллюлоза, а также, в меньшей степени, лигнин, соли и органические соединения.
Согласно предпочтительному варианту осуществления, твердая фракция (101) обрабатывается посредством осахаривания (400).
Способ осахаривание (400), который уже был описан в настоящем документе, на двух последующих стадиях приводит к образованию сахаров, содержащих 5 атомов углерода (C5) (8) и 6 атомов углерода (C6) (16). Первая стадия предпочтительно осуществляется посредством кислотного гидролиза (404) органической кислотой, выбранной из фосфоновых кислот, имеющих общую формулу R-PO(OH)2 (I), или из алкилсульфоновых кислот, имеющих общую формулу R1-SO3H (II).
Согласно настоящее изобретение, в качестве R выбирается неразветвленная или разветвленная алкильная группа, ароматическая группа или группа, содержащая гетероатом.
Согласно настоящее изобретение, в качестве R1 выбирается неразветвленная или разветвленная алкильная группа, содержащая от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода.
Алкильная группа R может предпочтительно содержать от 1 до 6 атомов углерода, предпочтительнее от 1 до 3 атомов углерода.
Когда R представляет собой алкильную группу, в качестве вышеупомянутой группы предпочтительно выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Когда R представляет собой ароматическую группу, вышеупомянутая группа предпочтительно выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, предпочтительно R' представляет собой метил.
Когда R представляет собой группу, содержащую гетероатом, вышеупомянутая группа предпочтительно выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно -CH2-PO(OH)2 (дифосфонатная) группа. В качестве алкильной группы R1 предпочтительно выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Более предпочтительными являются алкилфосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, которая может содержать от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода; предпочтительнее в качестве R выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Более предпочтительными являются фосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует группа, содержащая гетероатом, выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно CH3-PO(OH)2 (дифосфонатная) группа.
Среди фосфоновых кислот те, которые являются предпочтительными, представляют собой соединения, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует -CH3OH-PO(OH)2 (дифосфонатная) группа или этидроновая кислота (известная как 1-гидроксиэтан-1,1-дифосфоновая кислота), или в которой в качестве R присутствует метильная группа или метанфосфорная кислота (метилфосфоновая кислота). Среди алкилсульфоновых кислот предпочтительной является метансульфоновая кислота (CH3-SO3H). Значение pH в течение кислотного гидролиза предпочтительно составляет от 0,6 до 1,6, предпочтительно от 0,8 до 1,3, предпочтительнее от 0,9 до 1.
Кислотный гидролиз предпочтительно осуществляется при температуре в интервале, который составляет от 120°C до 160°C, предпочтительнее от 130°C до 150°C, еще предпочтительнее при 140°C.
После кислотного гидролиза получаются C5-сахара (8) и второй твердый остаток (15, 20).
Вторая стадия представляет собой гидролиз, в качестве которого предпочтительно выбирается ферментативный гидролиз или химический или термохимический гидролиз (402), и образуются C6-сахара (16) и твердый остаток (17 или 18), который содержит только лигнин или лигнин вместе с каучуком и смолой.
Как C5-сахара, так и C6-сахара могу использоваться для производства химических веществ, микробных масел и биотоплива (12) посредством ферментации (403).
Листья содержат вплоть до 7-8 мас.% смолистых веществ с высоким содержанием эфирных масел, которые составляют более 75% всех эфирных масел, присутствующих в растении. Помимо содержания каучука и смола, листья имеют состав, аналогичный составу остальной части растения, который дополняют в небольших количествах (составляющих приблизительно 1% свежей массы) эфирные масла, содержащие, главным образом, терпены (сесквитерпены) и воски. Эфирные масла и воски представляют собой продукты, имеющие высокую добавленную стоимость, которые используются, главным образом, в производстве фармацевтических продуктов и соединений для душистых и парфюмерных изделий (103). Эфирные масла могут использоваться в пищевой промышленности (как ароматизирующие вещества или добавки) или в области косметики, а также в производстве парфюмерных изделий, которые составляют наибольший рынок в количественном отношении.
Еще одно применение эфирных масел представляет собой производство специальных связующих веществ (повышающих клейкость веществ). В этом случае компоненты масел вступают в реакцию гомополимеризации, производя натуральное связующее вещество, или реагируют с другими компонентами, такими как фенол или стирол, производя в процессе в сополимеризации синтетические связующие вещества.
Предпочтительный способ получения восков и эфирных масел представляет собой дистилляция с паром собранных листьев, пока они еще находятся в свежем состоянии. В случае термически чувствительных масел предпочтительно используется экстракция растворителем, представляющим собой натуральные жиры или сверхкритический CO2. Хотя содержание эфирного масла в листьях гваюлы составляет приблизительно 1% по отношению к свежей массе, это количество находится на таком же уровне или даже превышает уровни, обнаруживаемые для многих растений, из которых эфирные масла экстрагируются и используются для производства товарных продуктов.
Как эфирные масла, так и смолы, которые присутствуют в листьях, имеют свойства, которые часто оказываются вредными или раздражающими, когда эти вещества используются в изготовлении кормов для животных, как ясно свидетельствуют следующие статьи:
- I. T. Hernandez, Tech. Pecuaria Mexico, 1976 г., т. 31, с. 89; и
- T. F. Banigan, A. J. Verbiscar, C. W. Weber, «Состав листьев, семян и древесины гваюлы», J. Agric. Food Chem., 1982 г., т. 30, с. 427-481.
Эти статьи описывают, что листья гваюлы являются приемлемыми в качестве компонента кормов для животных только в том случае, если удаляется смола. По этой причине смола должна быть экстрагирована перед изготовлением пищевых композиций.
Известно, что смолы могут экстрагироваться с использованием органических растворителей (например, циклогексана) и посредством более селективных технологий, предпочтительно таких как паровая экстракция или экстракция сверхкритическим CO2.
Листья гваюлы могут также эффективно использоваться в качестве добавок для сельскохозяйственной почвы, поскольку они производят микробицидное или регулирующее рост бактерий действие, как ясно свидетельствуют следующие статьи:
- J. D. Bultman, R. K. Gilbertson, J. Adaskaveg, T. L. Amburgey, S. V. Parikh, C. A. Bailey, «Эффективность гваюловой смолы в качестве пестицида», Bioresour. Technol., 1991 г., т. 35, с. 1997-2001; и
- F. S. Nakayama, S. H. Vinyard, P. Chow, D. S. Bajwa, J. A. Youngquist, J. H. Muehl, A. M. Krzysik, «Гваюла в качестве консерванта для древесины», Ind. Crops Prod., 2001 г., т. 14, с. 105-111.
Эти статьи описывают, что некоторые терпеновые компоненты смолы проявляют эффективное противогрибковое действие.
С другой стороны, G. T. Maatooq и J. J. Hoffmann в своей статье «Фунгистатические сесквитерпениоды из растений рода Parthenium», Phytochemistry, 1996 г., т. 43, с. 67-69, заявляют, что именно сесквитерпеновые компоненты несут ответственность за фунгицидную активность. Среди альтернативных источников натурального каучука гваюла представляет особый интерес вследствие низкого содержания в ней белков, потенциально аллергических веществ, которые, с другой стороны, присутствуют в значительно большем количестве в натуральном каучуке, экстрагированном из деревьев бразильской гевеи (Hevea brasiliensis). По этой причине, полученный из гевеи каучук проявляет высокую способность аллергических реакций, когда он используется в производстве продуктов, которые применяются посредством контакта с кожей.
Хотя экстракция латекса из лигноцеллюлозного компонента представляет собой основную цель выращивания и производства гваюловой биомассы, если должны быть достигнуты высокий уровень эффективности и приемлемая экономическая отдача в отношении всей производственной цепи, оказываются также необходимыми использование и последующая утилизация полисахаридной фракции, включающей гемицеллюлозу, целлюлозу и инулин, а также другие компоненты растения, такие как смолы, эфирные масла, воски и лигнин.
Предпочтительный способ применения гваюлового латекса и каучука представлен на фиг. 4 (способ получения латекса) и на фиг. 5 (способ получения каучука). Как показывает фиг. 4, после измельчения в мельнице ствол и ветви (3) подвергаются экстракции основным водным раствором (200-A), и в результате этого отделяется водная эмульсия (201), которую стабилизируют соответствующие поверхностно-активные вещества, от первого твердого древесного остатка или багассы (5) физическими методами, предпочтительно посредством прессования. Получаемая багасса (5) содержит лигнин, целлюлозу, гемицеллюлозу, остаточный каучук и смолу и может обрабатываться посредством осахаривания на двух стадиях (400), в котором осуществляется кислотный гидролиз фосфоновой кислотой, представляющей собой органическую кислоту, имеющую общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом. Алкильная группа может предпочтительно содержать от 1 до 6 атомов углерода, предпочтительнее от 1 до 3 атомов углерода.
В качестве алкильной группы предпочтительно выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Ароматическая группа предпочтительно выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, предпочтительно R' представляет собой метил.
Группа, содержащая гетероатом, предпочтительно выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно -CH3OH-PO(OH)2 (дифосфонатная) группа.
Более предпочтительными являются алкилфосфоновые кислоты, имеющие общую формулу R-P-O(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, которая может содержать от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода; предпочтительнее в качестве R выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Более предпочтительными являются фосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует группа, содержащая гетероатом, выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно CH2-PO(OH)2 (дифосфонатная) группа.
Среди фосфоновых кислот те, которые являются предпочтительными, представляют собой соединения, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует -CH3OH-PO(OH)2 (дифосфонатная) группа или этидроновая кислота (известная как 1-гидроксиэтан-1,1-дифосфоновая кислота), или в которой в качестве R присутствует метильная группа или метанфосфорная кислота (метилфосфоновая кислота).
Значение pH в течение кислотного гидролиза предпочтительно составляет от 0,6 до 1,6, предпочтительно от 0,8 до 1,3, предпочтительнее от 0,9 до 1.
Кислотный гидролиз предпочтительно осуществляется при температуре в интервале, который составляет от 120°C до 160°C, предпочтительнее от 130°C до 150°C, еще предпочтительнее при 140°C.
Концентрированный латекс (203) получается из водной эмульсии (201) посредством обработки путем концентрирования (200-F), обычно путем центрифугирования, в котором остается остаточная вода (205). После концентрирования латекс может уже использоваться в качестве натурального каучука. Натуральный каучук (204 и 14 на фиг. 1) может также быть получен из вышеупомянутого концентрированного латекса в процессе последующей коагуляции, которая осуществляется путем добавления коагулянтов, такие как, например, органические кислоты (лимонная кислота или уксусная кислота) или неорганические кислоты (серная кислота) (200-B).
Как концентрированный латекс, так и коагулированный натуральный каучук может использоваться в производстве изделий и продуктов. Коагулированный каучук может предпочтительно использоваться в секторе шинного производства.
Остаточная вода от переработки (205) имеет высокое содержание органических веществ и, после необязательной нейтрализации, может необязательно использоваться для производства биогаза (206) посредством анаэробной ферментации, или она может повторно использоваться на стадии экстракции основной водой.
Как показывает фиг. 5, оказывается возможным производство натурального каучука из ветвей и ствола без экстракции латекса.
Ветви и стволы после измельчения в мельнице, экстрагируются (200-C) неполярным органическим растворителем, в качестве которого предпочтительно выбираются гексан, циклогексан и их смеси, и образуются первый органический раствор (211) и первый твердый древесный остаток (5), который содержит лигнин, целлюлозу и гемицеллюлозу, и в нем практически отсутствуют остаточные смолы и каучук. Данный первый твердый остаток может после этого обрабатываться посредством осахаривания на двух стадиях (400), причем кислотный гидролиз осуществляется фосфоновой кислотой, представляющей собой органическую кислоту, имеющую общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом.
Алкильная группа может предпочтительно содержать от 1 до 6 атомов углерода, предпочтительнее от 1 до 3 атомов углерода.
В качестве алкильной группы предпочтительно выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил. Ароматическая группа предпочтительно выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, предпочтительно R' представляет собой метил.
Группа, содержащая гетероатом, предпочтительно выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно -CH3OH-PO(OH)2 (дифосфонатная) группа.
Более предпочтительными являются алкилфосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, которая может содержать от 1 до 6 атомов углерода, предпочтительно от 1 до 3 атомов углерода; предпочтительнее в качестве R выбирается метил, этил, 1-пропил, 2-пропил, н-бутил, втор-бутил, трет-бутил, изобутил, пентил, 1-метилбутил, 1-этилпропил, 2-метилбутил, 1,2-диметилпропил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил или 2,3-диметилбутил.
Более предпочтительными являются фосфоновые кислоты, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует группа, содержащая гетероатом, выбирается из групп, в которых содержится кислород (O), предпочтительно -OH-группа или карбонильная группа; или содержится азот (N), предпочтительно -NH2-группа или N-замещенная -NH2-группа; или содержится фосфор (P), предпочтительно CH2-PO(OH)2 (дифосфонатная) группа.
Среди фосфоновых кислот те, которые являются предпочтительными, представляют собой соединения, имеющие общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует -CH3OH-PO(OH)2 (дифосфонатная) группа или этидроновая кислота (известная как 1-гидроксиэтан-1,1-дифосфоновая кислота), или в которой в качестве R присутствует метильная группа или метанфосфорная кислота (метилфосфоновая кислота).
Значение pH в течение кислотного гидролиза предпочтительно составляет от 0,6 до 1,6, предпочтительно от 0,8 до 1,3, предпочтительнее от 0,9 до 1.
Кислотный гидролиз предпочтительно осуществляется при температуре в интервале, который составляет от 120°C до 160°C, предпочтительнее от 130°C до 150°C, еще предпочтительнее при 140°C.
Натуральный каучук (212) осаждается посредством добавления полярного растворителя (200-D), в качестве которого предпочтительно выбираются ацетон, спирты, предпочтительно включая этанол, сложные эфиры, предпочтительно включая этилацетат, или их смесь, в первую органическую фазу (211), и образуется вторая органическая фаза (213), из которой могут быть выделены смолы (215), предпочтительно посредством удаления растворителя.
Натуральный каучук (212) может повторно суспендироваться в воде в форме тонкой эмульсии для восстановления латекса (213) посредством соответствующих технологий для диспергирования и стабилизации эмульсий (200-E).
Латекс и каучук могут затем использоваться для производства продуктов и изделий на основе натурального каучука.
Фиг. 6 описывает предпочтительный способ применения смола согласно настоящей патентной заявке.
Первый твердый древесный остаток (5) предварительно обрабатывается посредством осахаривания (400) на двух стадиях, согласно способу, описанному в различных разделах текста настоящей патентной заявки (здесь он не представлен в целях краткости), чтобы гемицеллюлоза превращалась в C5-сахара (8), образуя второй твердый остаток (15), содержащий целлюлозу, смолу, остаточный каучук и лигнин.
Вышеупомянутый второй твердый остаток после этого подвергается экстракции неполярным органическим растворителем (303), предпочтительно выбранным из гексана, циклогексана и их смесей (305), и получается твердая фракция, содержащая целлюлозу и лигнин (306). Органический раствор экстрагируется полярным органическим растворителем, в качестве которого предпочтительно выбираются ацетон и спирты, причем среди них этанол является предпочтительным, или сложные эфиры, причем среди них этилацетат является предпочтительным, или соответствующая смесь (307), чтобы отделить каучук (310) и смолу (312). Твердая фракция подвергается обработке, в качестве которой выбирается ферментативный гидролиз или химический или термохимический гидролиз (311), и получаются C6-сахара из целлюлозы (309) и твердый древесный остаток включающий, по меньшей мере, 80% лигнина (308).
Фиг. 7 описывает предпочтительный способ применения багассы для изготовления подвергающихся ферментации сахаров.
Гваюловая багасса представляет собой биомассу, которую составляют целлюлоза, гемицеллюлоза, лигнин, остаточный каучук и смола. Вышеупомянутая биомасса представляет собой сложную структуру, в которой содержатся полимерные компоненты трех основных типов, а именно целлюлоза, гемицеллюлоза и лигнин, которые вступают в сильные взаимодействия друг с другом.
Взаимодействие между этими полимерами должно быть прекращено, таким образом, что, когда гидролизуется менее устойчивый полимер, а именно гемицеллюлоза, имеющая более высокую кристалличность и устойчивость целлюлоза также может легко подвергаться воздействию специфических ферментов для достижения полного гидролиза.
Для цели оптимизации степени превращения гемицеллюлозы и целлюлозы багассы в сахара, пригодные для использования в производстве продуктов, используемых в качестве источников энергии или химических веществ, как известно, вышеупомянутая багасса подвергается начальной обработка, предварительной обработке или разрушению. Вышеупомянутая предварительная обработка делает возможным ослабление связей между лигнином и целлюлозой, делая последнюю более склонной к последующему гидролизу, например, под действием ферментов, и одновременно делает возможным гидролиз гемицеллюлозы, которая разрушается легче, чем целлюлоза, образуя простые сахара, содержащие 5 атомов углерода.
После этого простые C5-сахара могут подвергаться процессам ферментации (403).
Могут использоваться разнообразные типы предварительной обработки багассы, в качестве которых предпочтительно выбираются химическая предварительная обработка кислотами или основаниями; физико-химическая предварительная обработка, выбранная из обработки при высоком давлении и температуре, измельчения, микроволновой или ультразвуковой обработки; или биологическая предварительная обработка, такая как, например, разрушение выбранными микроорганизмами.
Способ, который традиционно используется для вышеупомянутой цели, представляет собой кислотный гидролиз, который может осуществляться в присутствии разбавленных или концентрированных кислот. Однако способы предварительной обработки кислотами, которые описаны в документах предшествующего уровня техники, могут проявлять некоторые недостатки. Например, осуществление кислотного гидролиза при чрезмерно высоких температурах может приводить к образованию продуктов побочных реакций, включая дегидратацию сахаров и частичную деполимеризацию лигнина, таких как, например, фурфураль (F), гидроксиметилфурфураль (HMF) или фенольные соединения, которые действуют как ингибиторы роста микроорганизмов, традиционно используемых в последующих процессах ферментации сахаров, вызывая существенное снижение эффективности и производительности вышеупомянутых способов.
Если, с другой стороны, кислотный гидролиз осуществляется при чрезмерно низких температурах, может быть достигнуто недостаточное разложение багассы, причем такое разложение является необходимым для высвобождения целлюлозных волокон из покрывающей из сетки, содержащей гемицеллюлозу и лигнин, таким образом, чтобы волокна могли предпочтительно участвовать на последующей стадии ферментативного гидролиза. Это объясняется тем, что целлюлозные волокна, сплетенные с гемицеллюлозой и лигнином, не являются легкодоступными для ферментов (например, целлюлазы), которые традиционно используются в ферментативном гидролизе. Кроме того, кислоты, которые обычно используются для этой цели и описываются в литературе, такие как серная или хлористоводородная кислота, не всегда обеспечивают желательные результаты, в частности, в отношении высоких общих выходов мономерных сахаров и снижения уровня образования нежелательных побочных продуктов (F и HMF или других продуктов, которые ингибируют ферментацию).
Чтобы преодолеть основные недостатки предшествующего уровня техники, заявитель, соответственно, решил подвергать багассу (5) осахариванию на двух стадиях, как всесторонне описано и заявлено в настоящей патентной заявке (404 и 402).
В частности, первая стадия представляет собой кислотный гидролиз (404), как всесторонне описано и заявлено в настоящей патентной заявке, который превращает гемицеллюлозу в C5-сахара и образует второй твердый древесный остаток, содержащий целлюлозу, лигнин, смолы и каучук.
Вышеупомянутый твердый остаток после этого подвергается последующему гидролизу (402), в качестве которого может выбираться ферментативный гидролиз или химический или термохимический гидролиз, и образуются C6-сахара (16) и твердый остаток (17, 18), который преимущественно содержит лигнин, или лигнин, остаточный каучук и смолу, а также целлюлозу в количестве, составляющем не более чем 20%.
Вышеупомянутый твердый остаток может после этого использоваться для экстракции остаточной смолы и каучука, как описано в настоящей патентной заявке, или для производства лигнина, как уже было всесторонне описано и заявлено в настоящей патентной заявке. C5-сахара и C6-сахара могут соответствующим образом использоваться для ферментации под действием микроорганизмов (403), способных производить химические вещества, микробные масла или биотоплива (12).
Таким образом, согласно наблюдениям, экстракция смолы является количественной не только после осуществления предварительной обработки багассы разбавленными кислотами, но также после последующего гидролиза ферментами.
Таким образом, заявитель предложил интегрированный способ производства сахаров из биомассы, которым могут обеспечиваться:
- повышенная степень превращения гемицеллюлозного компонента (более 95%) и, следовательно,
- высокий выход сахаров, содержащих от 5 до 6 атомов углерода, в частности сахаров, содержащих 5 атомов углерода, таких как ксилоза или арабиноза (т. е. выход сахаров, содержащих от 5 до 6 атомов углерода составляет более чем или равняется 95%, причем вышеупомянутый выход вычисляется по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе), и
- небольшое количество побочных продуктов, представляющих собой, например, фурфураль (F) и гидроксиметилфурфураль (HMF), составляющее менее чем или равное 3% (по отношению к полной массе сахаров).
Ниже представлены некоторые иллюстративные неограничительные примеры настоящего изобретения, чтобы способствовать пониманию настоящего изобретения и его осуществлению.
Пример 1 - экстракция и выход эфирных масел
В паровой экстрактор вводили 100 г листьев гваюлы (50% H2O). Дистилляцию осуществляли в течение 4 часов и собирали 1000 см3 H2O. На поверхности водной фазы выделяли 1,1 г масла, которое анализировали методом газовой хроматографии и масс-спектрометрии, определяя следующие основные компоненты: борнеол, эвдесмол и спатуленол. Таким образом, борнеол получали гидролизом борнилацетата, одного из основных компонентов фракции.
Сравнительный пример 1 - экстракция смолы из непереработанной багассы
В однолитровую колбу вводили 100 г багассы (50% H2O) и 500 см3 ацетона. Смесь перемешивали при 45°C в течение 2 часов, фильтровали и осуществляли промывание ацетоном. Ацетоновый раствор концентрировали. Получали 2,9 г вязкого остатка, соответствующего 5,8 мас.% по отношению к сухой биомассе. Остаток багассы подвергали еще одной экстракции ацетоном в идентичных условиях (500 мл ацетона, перемешивание в течение 2 часов при 45°C). После промывания свежим растворителем и фильтрации твердого остатка ацетоновый раствор концентрировали посредством удаления растворителя при пониженном давлении. Получали 0,8 г смолы. Количество смолы, экстрагированной на двух стадиях, соответствовало 7,4 мас.% по отношению к сухой исходной багассе.
Пример 3 - экстракция смолы из багассы, обработанный разбавленными кислотами
В однолитровую колбу вводили 100 г влажной багассы, полученной в результате обработки разбавленными кислотами (301) (пример 5). Согласно наблюдениям, компонент, состоящий из гемицеллюлозы (приблизительно 18 мас.%), полностью гидролизовался. Остаток сохранял остаточное содержание смол и каучука (не экстрагированного в форме латекса). Образец, содержащий 50% H2O, суспендировали в 500 см3 ацетона. Смесь перемешивали в течение 2 часов при 45°C, фильтровали и осуществляли промывание свежим растворителем. Ацетоновый раствор концентрировали. Получали 3,1 г, что соответствовало 6,2% по отношению к сухой багассе без гемицеллюлозы.
Вышеупомянутое количество по отношению к непереработанной багассе перед гидролизом кислотами соответствует суммарному количеству смолы, присутствующей в багассе (7,5%).
Пример 4 - экстракция активных ингредиентов из багассы, обработанной разбавленными кислотами
Смолу, экстрагировали в примере 3, анализировали методом газовой хроматографии. Наблюдали, что часть сложноэфирных групп гваюлинов (от 50 до 80% в зависимости от условий обработки разбавленными кислотами) гидролизовалась, образуя спиртовой терпеновый компонент (партениол), а также коричную кислоту (для гваюлина A) и метоксибензойную кислоту (для гваюлина B) (схема 1).
Схема 1


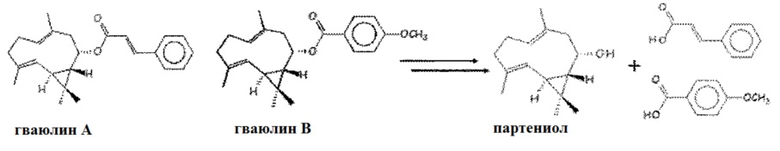
Партениол можно было затем легко экстрагировать и очищать, используя известные способы (например, посредством экстракции холодным спиртом).
Пример 5 - гидролиз метанфосфоновой кислотой
В открытый в атмосферу однолитровый автоклав Büchi модели 3E вводили 25 г предварительно измельченной гваюловой багассы с диаметром частиц мельче 2 мм. Затем вводили 500 г водного раствора метанфосфоновой кислоты CH3-P(O)(OH)2 при pH 1,1. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (600 об/мин) в течение 45-минутного периода до достижения температуры, составляющей 140°C, при этом получали вторую реакционную смесь, включающую первую твердую фазу, содержащую лигнин и целлюлозу, и первую водную фазу, содержащую сахара, произведенные из гемицеллюлозы. Когда автоклав выдерживали для охлаждения до комнатной температуры (23°C), вышеупомянутые фазы отделяли посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 40,3 мас.% целлюлозы, 18,7 мас.% гемицеллюлозы и 30,4 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли.
Первую водную фазу анализировали, как описано выше, и при этом получали следующие результаты:
выход: 99,1% (по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе);
степень разложения C6: 0,0%;
степень разложения C5: 0,9%
содержание C5: 83,1%.
Пример 6 - гидролиз этидроновой кислотой
В открытый в атмосферу однолитровый автоклав Büchi модели 3E вводили 25 г предварительно измельченной гваюловой багассы с диаметром частиц мельче 2 мм. Затем вводили 500 г водного раствора этидроновой кислоты, т. е. 1-гидроксиэтан-1,1-дифосфорной кислоты CH3-CH(OH)[P(O)(OH)2], при pH 1,1. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (600 об/мин) в течение 45-минутного периода до достижения температуры, составляющей 140°C, при этом получали вторую реакционную смесь, включающую первую твердую фазу, содержащую лигнин и целлюлозу, и первую водную фазу, содержащую сахара, произведенные из гемицеллюлозы. Когда автоклав выдерживали для охлаждения до комнатной температуры (23°C), вышеупомянутые фазы отделяли посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 40,3 мас.% целлюлозы, 18,7 мас.% гемицеллюлозы и 30,4 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли.
Первую водную фазу анализировали, как описано выше, и при этом получали следующие результаты:
выход: 98,2% (по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе);
степень разложения C6: 0,0%;
степень разложения C5: 1,1%;
содержание C5: 84,3%.
Сравнительный пример 2 - гидролиз фосфорной кислотой
В открытый в атмосферу однолитровый автоклав Büchi модели 3E вводили 25 г предварительно измельченной багассы гваюлы серебристой (Parthenium argentatum) с диаметром частиц мельче 2 мм. Затем вводили 500 г водного раствора фосфорной кислоты H3POH4 при pH 1,1. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (600 об/мин) в течение 45-минутного периода до достижения температуры, составляющей 140°C, при этом получали вторую реакционную смесь, включающую первую твердую фазу, содержащую лигнин и целлюлозу, и первую водную фазу, содержащую сахара, произведенные из гемицеллюлозы. Когда автоклав выдерживали для охлаждения до комнатной температуры (23°C), вышеупомянутые фазы отделяли посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 40,3 мас.% целлюлозы, 18,7 мас.% гемицеллюлозы и 30,4 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли.
Первую водную фазу анализировали, как описано выше, и при этом получали следующие результаты:
выход: 87% (по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе);
степень разложения C6: 3,3%;
степень разложения C5: 9,7%;
содержание C5: 71,1%.
Из примеров 5 и 6 и сравнительного примера 2 ясно, что при работе в идентичных условиях выходы сахаров, содержащих от 5 до 6 атомов углерода, оказались ниже, а количества побочных продуктов, представляющих собой фурфураль (F) и гидроксиметилфурфураль (HMF), оказались выше, когда использовалась фосфорная кислота (сравнительный пример 2), по сравнению с примерами 5 и 6, в котором были использованы алкилфосфоновые кислоты в соответствии с настоящим изобретением.
Пример 7 - гидролиз листьев метансульфоновой кислотой
В открытый в атмосферу однолитровый автоклав Büchi модели 3E вводили 25 г лиственной фракции 101, получаемой после экстракции эфирных масел и восков и имеющей влагосодержание 50%. Затем вводили 500 г водного раствора метансульфоновой кислоты (CH3-SO3H) при pH 1,1. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (600 об/мин) в течение 45-минутного периода до достижения температуры, составляющей 140°C, при этом получали вторую реакционную смесь, включающую первую твердую фазу, содержащую лигнин и целлюлозу, и первую водную фазу, содержащую сахара, произведенные из гемицеллюлозы. Когда автоклав выдерживали для охлаждения до комнатной температуры (23°C), вышеупомянутые фазы отделяли посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 30 мас.% целлюлозы, 30 мас.% гемицеллюлозы и 4 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли.
Первую водную фазу анализировали, как описано выше, и при этом получали следующие результаты:
выход: 98,8% (по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе);
степень разложения C6: 0,0%;
степень разложения C5: 1,6%;
содержание C5: 60%.
Пример 8 - гидролиз листьев метанфосфоновой кислотой
В открытый в атмосферу однолитровый автоклав Büchi модели 3E вводили 10 г лиственной фракции 101, получаемой после экстракция эфирных масел и восков и имеющей влагосодержание 50%. Затем вводили 500 г водного раствора метанфосфоновой кислоты при pH 1,1. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (600 об/мин) в течение 45-минутного периода до достижения температуры, составляющей 140°C, при этом получали вторую реакционную смесь, включающую первую твердую фазу, содержащую лигнин и целлюлозу, и первую водную фазу, содержащую сахара, произведенные из гемицеллюлозы. Когда автоклав выдерживали для охлаждения до комнатной температуры (23°C), вышеупомянутые фазы отделяли посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 30 мас.% целлюлозы, 30 мас.% гемицеллюлозы и 4 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли.
Первую водную фазу анализировали, как описано выше, и при этом получали следующие результаты:
выход: 97% (по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе);
степень разложения C6: 0,0%;
степень разложения C5: 1,4%;
содержание C5: 65%.
Таблица 1
Гваюловая багасса. Выходы для гидролиза гемицеллюлозы (гидролиз разбавленными кислотами), целлюлозы (гидролиз ферментами) и суммарная степень превращения в подвергающиеся ферментации сахара по отношению к присутствующим углеводам
Пример 10 - ферментативный гидролиз остатка, предварительно обработанного кислотой
В закрытый смесительный реактор непрерывного действия вводили 10 г остатка гваюлы серебристой (Parthenium argentatum), полученного в примере 5 и имеющем содержание воды 50%, после гидролиза гемицеллюлозы метанфосфоновой кислотой вместе с 450 г воды. Добавляли смесь ферментов (Novozyme, DK), соответствующую концентрации 20 мг на 1 г целлюлозы, присутствующей в образце. Смесь содержала, главным образом, целлюлазу, но также присутствовали гемицеллюлаза и β-глюкозидаза. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (300 об/мин) при 50°C в течение 60 часов. После вышеупомянутого периода оставшуюся твердую фазу отделяли от надосадочной жидкости посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 49 мас.% целлюлозы, 1,0 мас.% гемицеллюлозы и 36,9 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Получали 1,7 г глюкозы, соответствующей выходу при гидролизе целлюлозы, составляющему 75%. Учитывая степень превращения гемицеллюлозы, полученную в примере 5, суммарная степень превращения в мономерные сахара по отношению к суммарному количеству присутствующих сахаров составляла 83%.
Сравнительный пример 3 - ферментативный гидролиз непереработанной багассы без предварительной обработки кислотой
В закрытый смесительный реактор непрерывного действия вводили 10 г непереработанной багассы гваюлы серебристой (Parthenium argentatum) после экстракция латекса, имеющей содержание воды 50%, вместе с 450 г воды. Добавляли смесь ферментов (Novozyme, DK), соответствующую концентрации 30 мг на 1 г целлюлозы, присутствующей в образце. Смесь содержала, главным образом, целлюлазу, но также присутствовали гемицеллюлаза и β-глюкозидаза. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (300 об/мин) при 50°C в течение 60 часов. После вышеупомянутого периода оставшуюся твердую фазу отделяли от надосадочной жидкости посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 40 мас.% целлюлозы, 18,7% гемицеллюлозы и 30,4% лигнина. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли. Получали 0,02 г ксилозы, соответствующей выходу при гидролизе гемицеллюлозы, составляющему 4%, и 0,19 г глюкозы, соответствующей выходу при гидролизе целлюлозы, составляющему 10%. Таким образом, суммарный выход углеводов при гидролизе составлял 8% по отношению к суммарному количеству присутствующих мономерных сахаров.
Пример 10 и сравнительный пример 3 показывают, что биомасса должна быть предварительно обработана кислотами для достижения высокой степени превращения в подвергающиеся ферментации сахара.
Пример 11 - экстракция смолы из багассы, обработанной разбавленными кислотами и ферментами
В однолитровую колбу вводили 100 г влажной багассы, полученной в результате обработки разбавленными кислотами (404) и ферментами (402) (пример 10). Согласно наблюдениям, компонент гемицеллюлозы, составляющий приблизительно 18 мас.%, полностью гидролизовался, в то время как целлюлоза гидролизовалась на 75%. Полученный лигноцеллюлозный остаток сохранял остаточное содержание смол и каучука, не экстрагированного в форме латекса. Образец, содержащий 50% H2O, суспендировали in 500 см3 ацетона. Смесь перемешивали в течение 2 часов при 45°C, фильтровали и осуществляли промывание свежим растворителем. Ацетоновый раствор концентрировали. Получали 5,9 г, что соответствовало 11,8% по отношению к сухому остатку без гемицеллюлозы и (частично) без целлюлозы. Вышеупомянутое количество по отношению к непереработанной багассе перед гидролизом кислотами соответствует суммарному количеству смолы, присутствующей в исходной багассе (7,5%).
Сравнительный пример 4 - ферментативный гидролиз остатка, предварительно обработанного кислотой и обессмоленного
В закрытый смесительный реактор непрерывного действия вводили 10 г остатка гваюлы, полученного в примере 3 и имеющем содержание воды 50%, после гидролиза гемицеллюлозы метанфосфоновой кислоты и после экстракции смолы (302) вместе с 450 г воды. Добавляли смесь ферментов (Novozyme, DK) соответствующую концентрации 20 мг на 1 г целлюлозы, присутствующей в образце. Смесь содержала, главным образом, целлюлазу, но также присутствовали гемицеллюлаза и β-глюкозидаза. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (300 об/мин) при 50°C в течение 60 часов. После вышеупомянутого периода оставшуюся твердую фазу отделяли от надосадочной жидкости посредством фильтрации. Исходная биомасса имела следующий состав: 53 мас.% целлюлозы, 0,2 мас.% гемицеллюлозы и 40 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Получали 1,3 г глюкозы, соответствующей выходу при гидролизе целлюлозы, составляющему 55%. Учитывая степень превращения гемицеллюлозы, полученную в примере 5, суммарная степень превращения в мономерные сахара по отношению к суммарному количеству присутствующих сахаров составляла 69%.
Сравнительный пример 5 - ферментативный гидролиз обессмоленного остатка, предварительно обработанного кислотой
В закрытый смесительный реактор непрерывного действия вводили 10 г остатка гваюлы, полученного в сравнительном примере 6 и имеющего содержание воды 50%, после экстракции смолы и последующего гидролиза гемицеллюлозы метанфосфоновой кислотой, вместе с 450 г воды. Добавляли смесь ферментов (Novozyme, DK), соответствующую концентрации 30 мг на 1 г целлюлозы, присутствующей в образце. Смесь содержала, главным образом, целлюлазу, но также присутствовали гемицеллюлаза и β-глюкозидаза. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (300 об/мин) при 50°C в течение 60 часов. После вышеупомянутого периода оставшуюся твердую фазу отделяли от надосадочной жидкости посредством фильтрации. Исходная биомасса имела следующий состав: 51 мас.% целлюлозы, 3 мас.% гемицеллюлозы и 38 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Получали 1,2 г глюкозы, соответствующей выходу при гидролизе целлюлозы, составляющему 50%. Учитывая степень превращения гемицеллюлозы (85%), полученную в примере 5, суммарная степень превращения в мономерные сахара по отношению к суммарному количеству присутствующих сахаров составляла 61%.
Сравнительные примеры 4 и 5 показывают, что когда изменяется последовательность «гидролиз углеводов/экстракция смолы», степень превращения углеводов значительно снижается, как представлено в таблице 1. Изменение данной последовательности включает осуществление стадии экстракции смолы перед конечным ферментативным гидролизом целлюлозы, как до, так и после гидролиза гемицеллюлозы разбавленными кислотами. С другой стороны, следует отметить, что когда оказывается желательным предоставление приоритета извлечению смолы посредством осуществления экстракции смолы перед конечным гидролизом ферментами, для извлечения смолы требуется половина количества растворителя, если обработка кислотой уже была осуществлена (пример 3).
Сравнительный пример 6 - гидролиз обессмоленного остатка метансульфоновой кислотой
В открытый в атмосферу однолитровый автоклав Büchi модели 3E вводили 25 г остатка гваюловой багассы, обработанного в сравнительном примере 1 (после экстракции смолы). Затем вводили 500 г водного раствора метанфосфоновой кислоты CH3-P(O)(OH)2 при pH 1,1. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (600 об/мин) в течение 45-минутного периода до достижения температуры, составляющей 140°C, при этом получали вторую реакционную смесь, включающую первую твердую фазу, содержащую лигнин и целлюлозу, и первую водную фазу, содержащую сахара, произведенные из гемицеллюлозы. Когда автоклав выдерживали для охлаждения до комнатной температуры (23°C), вышеупомянутые фазы отделяли посредством фильтрации. Биомасса имела следующий состав: 43 мас.% целлюлозы, 20 мас.% гемицеллюлозы и 32 мас.% лигнина. Было обнаружено, что остаток составляли органические кислоты, белковые и небелковые азотистые вещества, липиды и минеральные соли.
Первую водную фазу анализировали, как описано выше, и при этом получали следующие результаты:
выход: 85% (по отношению к суммарному количеству гемицеллюлозы, присутствующей в исходной биомассе);
степень разложения C6: 0,0%;
степень разложения C5: 01,1%;
содержание C5: 75,1%.
Сравнительный пример 6 представляет собой изготовление остатка, используемого в ферментативном гидролизе в сравнительном примере 5. Вместе с примером 5 он определяет изготовление обессмоленных и необессмоленных остатков, используемых в сравнительном примере 4 и в сравнительном примере 5.
Пример 12 - листья. Ферментативный гидролиз остатка, предварительно обработанного метансульфоновой кислотой
В закрытый смесительный реактор непрерывного действия вводили 10 г твердого остатка листьев гваюлы, полученного в примере 8 и имеющего содержание воды 50%, после гидролиза гемицеллюлозы метансульфоновой кислотой вместе с 450 г воды. Добавляли смесь ферментов (Novozyme, DK), соответствующую концентрации 40 мг на 1 г целлюлозы, присутствующей в образце. Смесь содержала, главным образом, целлюлазу, но также присутствовали гемицеллюлаза и β-глюкозидаза. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (300 об/мин) при 50°C в течение 60 часов. После вышеупомянутого периода оставшуюся твердую фазу отделяли от надосадочной жидкости посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 43 мас.% целлюлозы, 1,0 мас.% гемицеллюлозы и 5,6 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Получали 1,4 г глюкозы, соответствующей выходу при гидролизе целлюлозы, составляющему 72%. Учитывая степень превращения гемицеллюлозы, полученную в примере 8, суммарная степень превращения в мономерные сахара по отношению к суммарному количеству присутствующих сахаров составляла 85%.
Пример 13 - листья. Ферментативный гидролиз остатка, предварительно обработанного метанфосфоновой кислотой
В закрытый смесительный реактор непрерывного действия вводили 10 г твердого остатка листьев гваюлы, полученного в примере 9 и имеющего содержание воды 50%, после гидролиза гемицеллюлозы метанфосфоновой кислотой вместе с 450 г воды. Добавляли смесь ферментов (Novozyme, DK), соответствующую концентрации 40 мг на 1 г целлюлозы, присутствующей в образце. Смесь содержала, главным образом, целлюлазу, но также присутствовали гемицеллюлаза и β-глюкозидаза. Первую реакционную смесь, получаемую таким способом, интенсивно перемешивали (300 об/мин) при 50°C в течение 60 часов. После вышеупомянутого периода оставшуюся твердую фазу отделяли от надосадочной жидкости посредством фильтрации. Исходная биомасса имела следующий состав, определенный, как описано выше: 43 мас.% целлюлозы, 1,0 мас.% гемицеллюлозы и 5,6 мас.% лигнина, по отношению к суммарной массе исходной биомассы. Получали 1,5 г глюкозы, соответствующей выходу при гидролизе целлюлозы, составляющему 74%. Учитывая степень превращения гемицеллюлозы, полученную в примере 9, суммарная степень превращения в мономерные сахара по отношению к суммарному количеству присутствующих сахаров составляла 86%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА САХАРОВ ИЗ БИОМАССЫ, ПОЛУЧЕННОЙ ИЗ РАСТЕНИЙ ГВАЮЛА | 2018 |
|
RU2772346C2 |
| СПОСОБ ПОЛУЧЕНИЯ САХАРОВ ИЗ БИОМАССЫ, ПОЛУЧЕННОЙ ИЗ РАСТЕНИЙ ГВАЙЮЛЫ | 2019 |
|
RU2793789C2 |
| СПОСОБ ЭКСТРАГИРОВАНИЯ СМОЛЫ И КАУЧУКА ИЗ ГВАЮЛОВЫХ РАСТЕНИЙ | 2016 |
|
RU2709876C1 |
| СПОСОБ ЭКСТРАКЦИИ ЛАТЕКСА, СМОЛЫ И КАУЧУКА ИЗ ГВАЮЛОВЫХ РАСТЕНИЙ | 2016 |
|
RU2731382C2 |
| Способ получения сахаров из биомассы | 2014 |
|
RU2670927C1 |
| ЗАМКНУТЫЙ СПОСОБ ПОЛУЧЕНИЯ ФУРФУРОЛА ИЗ БИОМАСС | 2015 |
|
RU2713659C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОСАХАРИДОВ ИЛИ ЭТАНОЛА ВМЕСТЕ С СУЛЬФИНИРОВАННЫМ ЛИГНИНОМ ИЗ ЛИГНОЦЕЛЛЮЛОЗНОЙ БИОМАССЫ | 2009 |
|
RU2525163C2 |
| Способ выделения изопреновых компонентов гваюлы | 2016 |
|
RU2704821C2 |
| СПОСОБЫ ОБРАБОТКИ ЛИГНОЦЕЛЛЮЛОЗНЫХ МАТЕРИАЛОВ | 2013 |
|
RU2634700C2 |
| ПОЛУЧЕНИЕ МОНОМЕРОВ ИЗ ЛИГНИНА В ПРОЦЕССЕ ДЕПОЛИМЕРИЗАЦИИ СОДЕРЖАЩЕЙ ЛИГНОЦЕЛЛЮЛОЗУ КОМПОЗИЦИИ | 2017 |
|
RU2739567C2 |
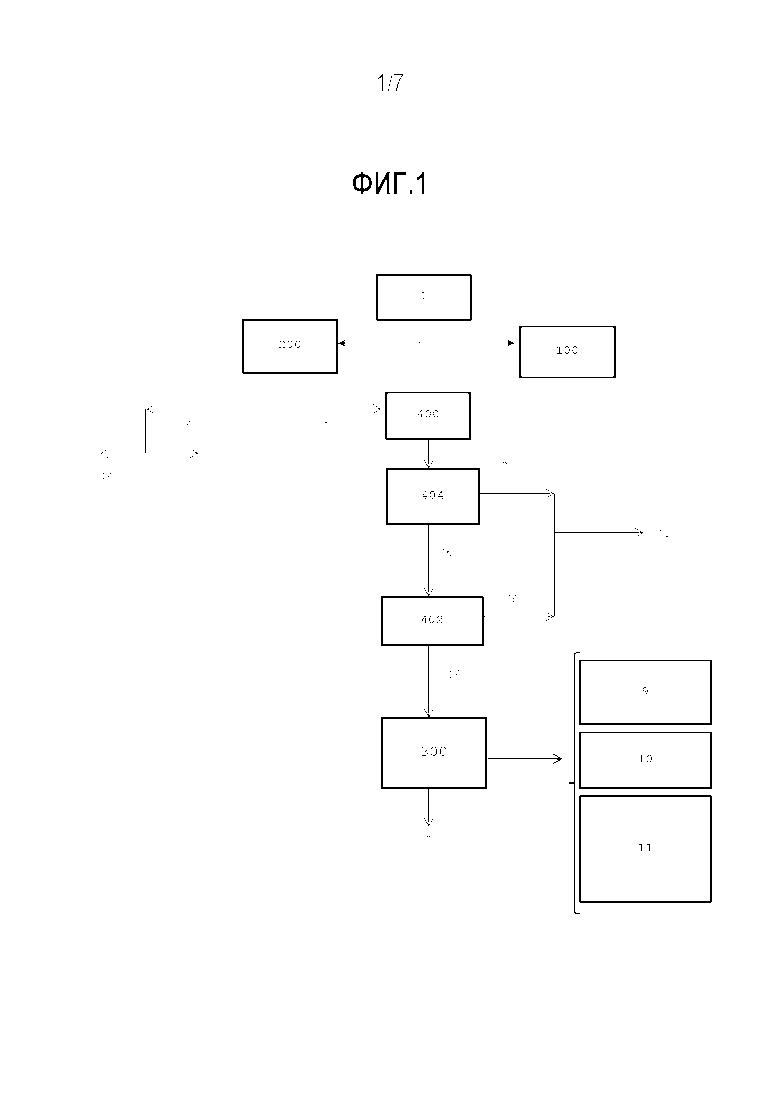
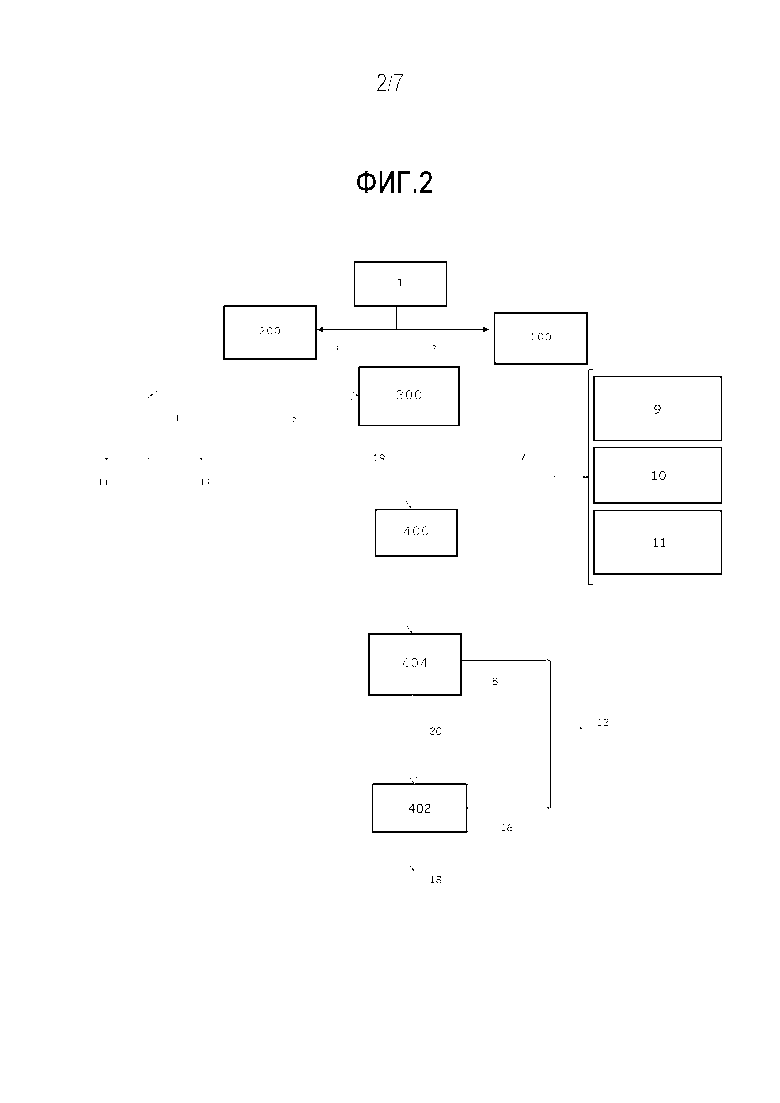
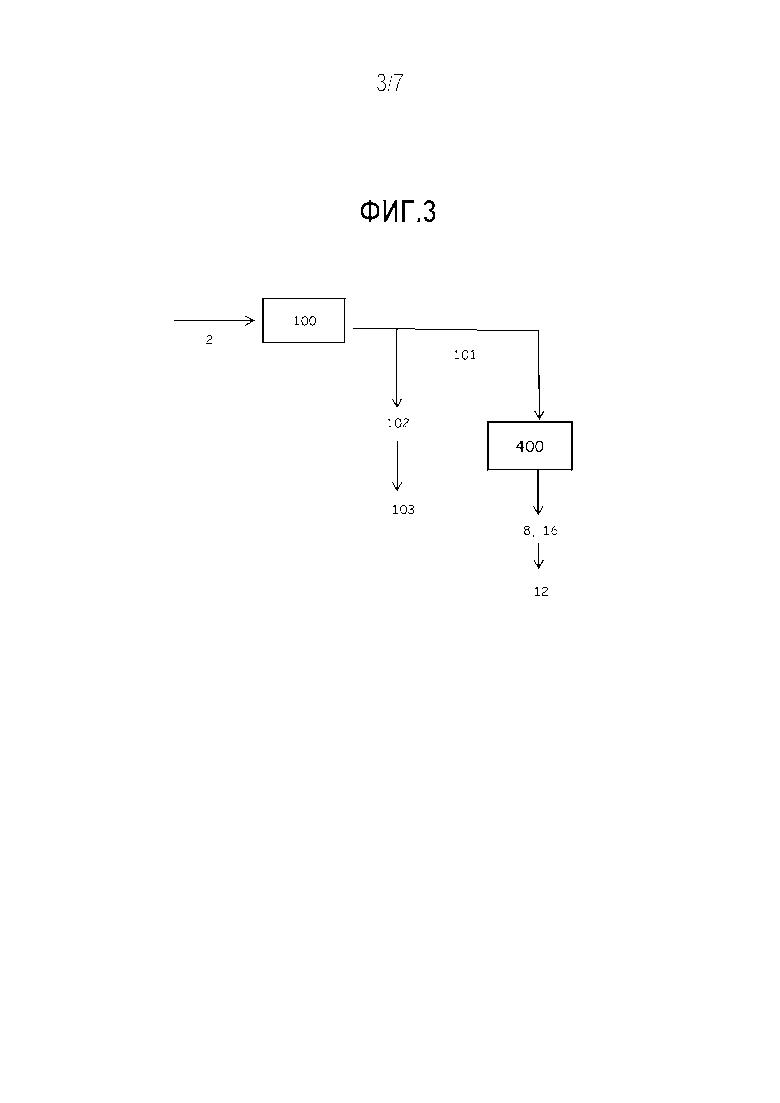
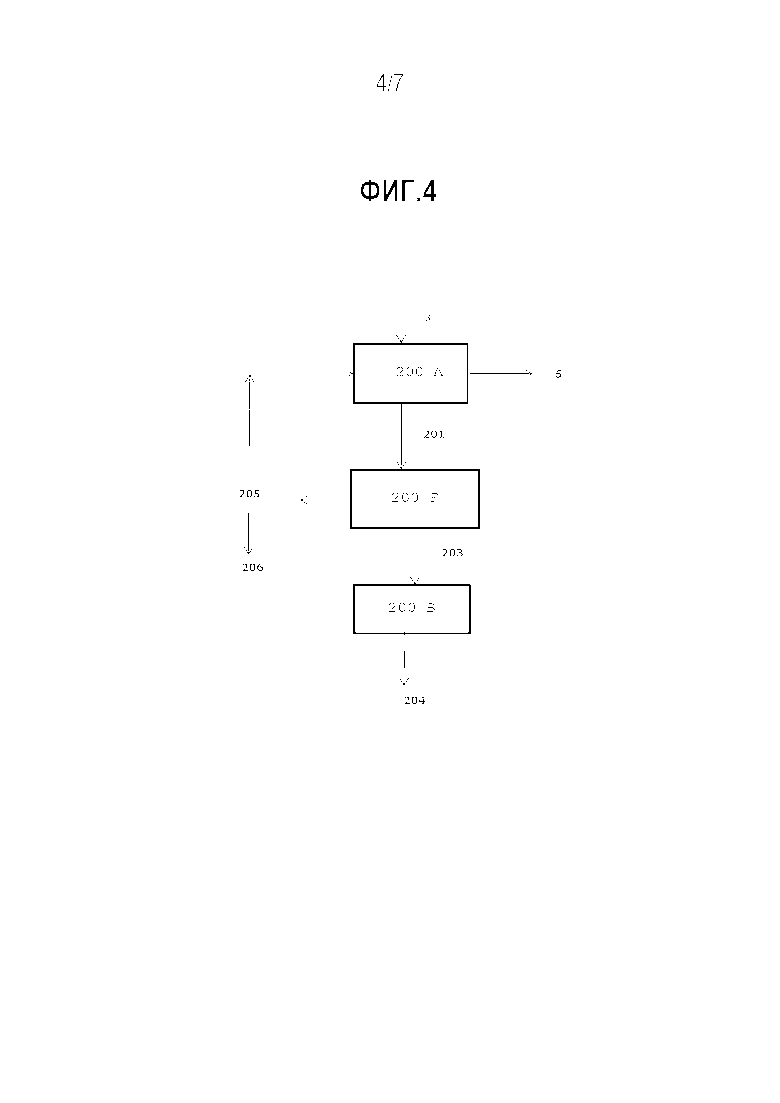
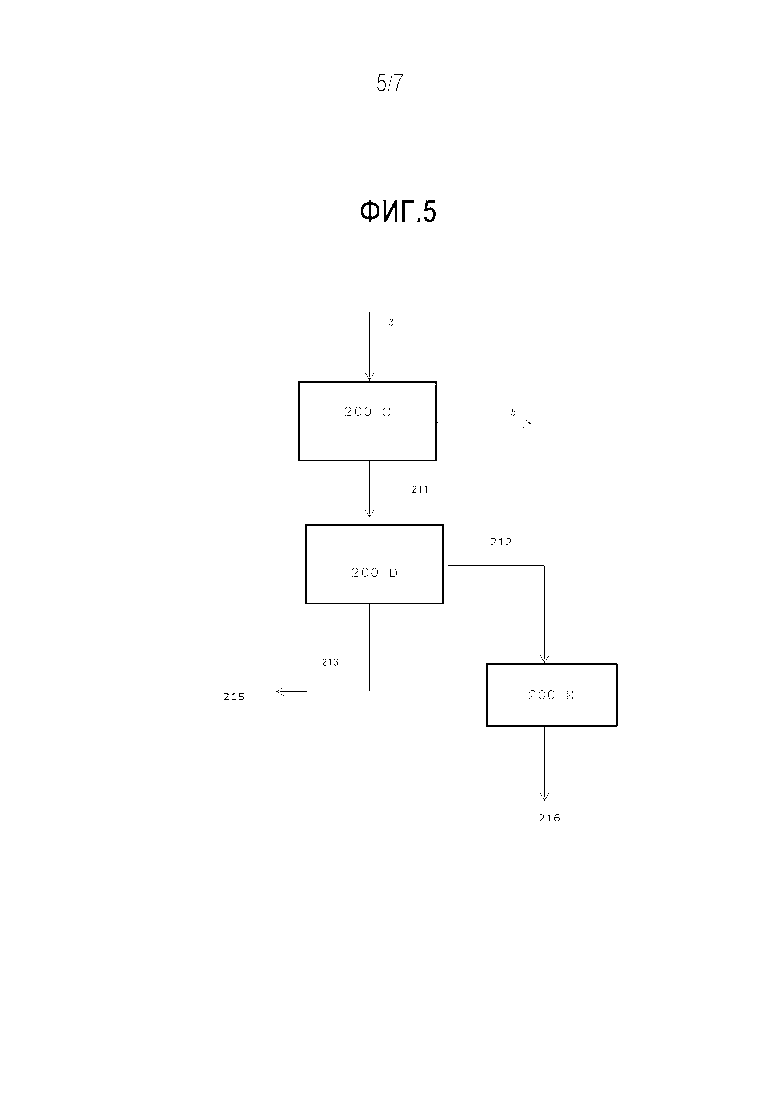
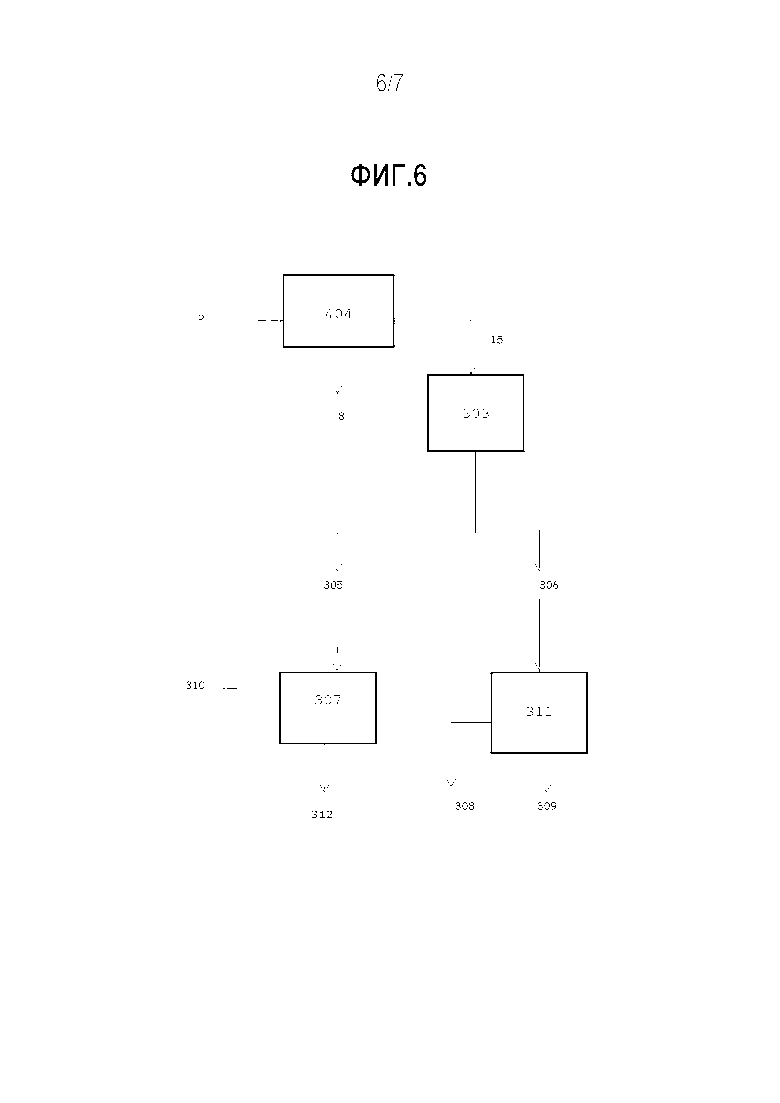
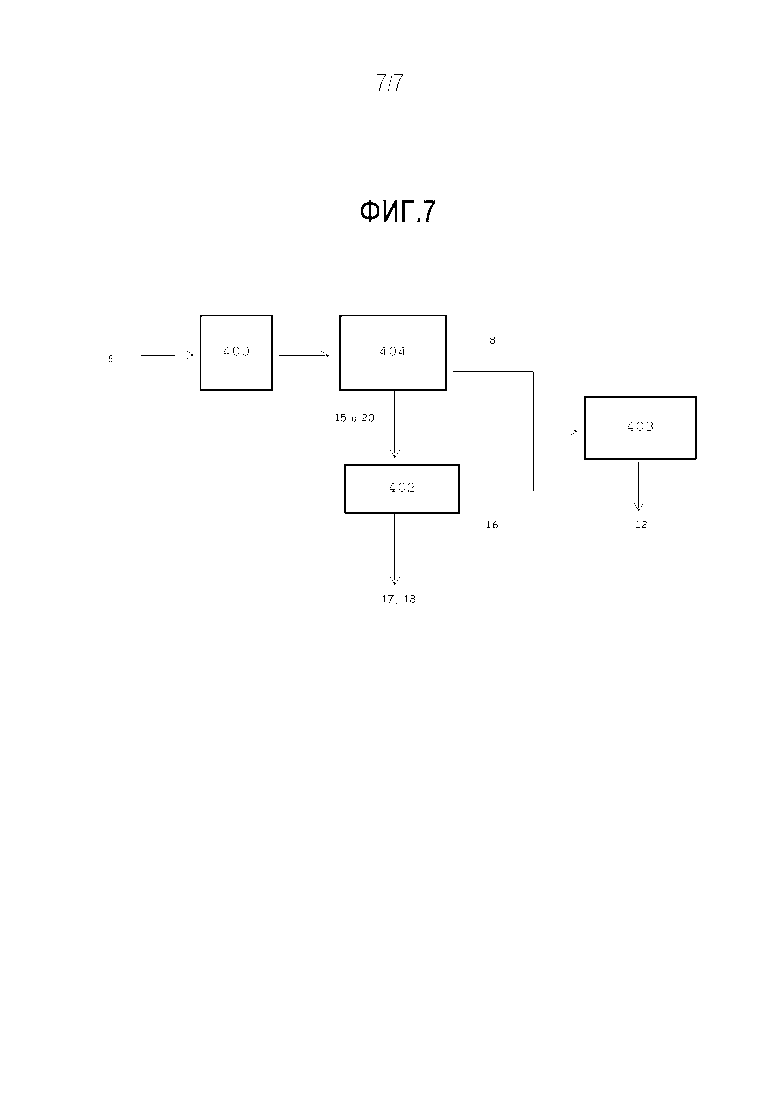
Изобретение относится к интегрированному способу переработки и применения каждой части растения гваюлы серебристой (Parthenium argentatum), включая остаточные части, для цели производства не только натурального каучука, но также соединений, которые могут использоваться в энергетической отрасли и в производстве химических веществ. Способ включает следующие стадии в таком порядке: отделение ствола и ветвей от листьев вышеупомянутого растения посредством механической обработки; обработка листьев, в которой производятся воски и эфирные масла, а также фракция, в которой содержатся целлюлоза, гемицеллюлоза (углеводы) и, в меньшей степени, соли, органические соединения и лигнин; экстракция из ствола и ветвей жидкой фазы; обработка вышеупомянутого первого твердого древесного остатка, в результате которой производятся сахара, смола, каучук и лигнин. В результате экстракции образуется первый твердый древесный остаток, называемый термином «багасса». Изобретение позволяет использовать все компоненты растения гваюлы и далее после процесса экстракции получать воски и эфирные масла, которые используются для получения смолы и лигнина. 30 з.п. ф-лы, 7 ил.
1. Интегрированный способ переработки и применения каждой части растения гваюлы серебристой (Parthenium argentatum) который включает следующие стадии в таком порядке:
- отделение ствола и ветвей (3) от листьев (2) вышеупомянутого растения посредством механической обработки (1);
- обработка листьев (100), в которой производятся воски и эфирные масла (102), а также фракция (101), в которой содержатся целлюлоза, гемицеллюлоза (углеводы) и, в меньшей степени, соли, органические соединения и лигнин;
- экстракция (200) из ствола и ветвей жидкой фазы (4), в результате которой образуется первый твердый древесный остаток (5), называемый термином «багасса» в настоящем документе;
- обработка вышеупомянутого первого твердого древесного остатка (5), в результате которой производятся сахара, смола, каучук и лигнин.
2. Способ по п.1, в котором ствол и ветви (3) обрабатывают посредством экстракции основной водой и образуются водная эмульсия (4) и первый твердый древесный остаток (5), в котором содержатся лигнин, целлюлоза, гемицеллюлоза и остаточный каучук.
3. Способ по п.2, в котором концентрированный латекс (203) экстрагируют из вышеупомянутой водной эмульсии и на последующей стадии коагуляция натуральный каучук (204) отделяют от концентрированного латекса.
4. Способ по п.1, в котором ствол и ветви обрабатывают посредством экстракции неполярным органическим растворителем и образуются органический раствор (211) и первый твердый древесный остаток (5), в котором содержатся гемицеллюлоза, целлюлоза и лигнин.
5. Способ по п.4, в котором натуральный каучук (212) экстрагируют из вышеупомянутого органического раствора, причем данный натуральный каучук после этого диспергируется в воде и образуется латекс (216).
6. Способ по п.1, в котором первый твердый остаток обрабатывают согласно следующим стадиям в таком порядке:
- экстракция смолы и каучука (300) из вышеупомянутого первого твердого древесного остатка (5), в результате которого образуются пятый твердый древесный остаток (19), содержащий лигнин, гемицеллюлозу и целлюлозу;
- гидролиз (400) вышеупомянутого пятого твердого остатка (19), в котором образуются сахара, содержащие 5 атомов углерода (8), и шестой твердый древесный остаток (20), содержащий лигнин и целлюлозу;
- гидролиз вышеупомянутого шестого твердого остатка (20) для превращения целлюлозы в сахара, содержащие 6 атомов углерода и называемые термином «C6» в настоящем документе, в результате которого образуются конечный твердый остаток (18), содержащий лигнин, и остаточная целлюлоза в количестве, составляющем менее чем 20%.
7. Способ по п.6, в котором первый твердый древесный остаток (5) обрабатывают посредством экстракции неполярным органическим растворителем (300) для отделения смолы и каучука (7), и в результате этого образуется пятый твердый древесный остаток (19), содержащий лигнин, гемицеллюлозу и целлюлозу.
8. Способ по пп. 6 и 7, в котором пятый твердый остаток (19) подвергают кислотному гидролизу (404) для превращения гемицеллюлозы в сахара, содержащие 5 атомов углерода и называемые термином «C5» в настоящем тексте, в результате которого образуется шестой твердый древесный остаток (20), содержащий лигнин и целлюлозу.
9. Способ по п.8, в котором кислотный гидролиз осуществляется фосфоновой кислотой, имеющей общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом.
10. Способ по п.9, в котором R представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода, или R выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, или R представляет собой группу, содержащую гетероатом и выбранную из групп, содержащих кислород (O), или содержащих азот (N), или содержащих фосфор (P).
11. Способ по п.9, в котором R выбран из метильной, этильной или CH3OH-PO(OH)2-группы.
12. Способ по любому из пп. 8-11, в котором pH в течение кислотного гидролиза составляет от 0,6 до 1,6.
13. Способ по п.6, в котором последующий гидролиз выбирают из ферментативного, химического или термохимического гидролиза.
14. Способ по п.1, в котором первый твердый остаток обрабатывают согласно следующим стадиям в таком порядке:
- обработка первого твердого древесного остатка (5), в которой образуются сахара, содержащие 5 атомов углерода (8), и в результате этого образуется второй твердый остаток (15),
- обработка вышеупомянутого второго твердого остатка (15), в которой образуются сахара, содержащие 6 атомов углерода (16), и третий твердый остаток (17) (400),
- экстракция смолы и каучука (7) (300) из вышеупомянутого третьего твердого остатка (17) и образование четвертого древесного остатка (18), состоящего, главным образом, из лигнина.
15. Способ по п.14, в котором третий твердый древесный остаток (17) обрабатывают посредством экстракции растворителем, представляющим собой органический неполярный (300) растворитель, для отделения смолы и каучука (7), и в результате этого образуется пятый твердый древесный остаток (19), содержащий лигнин, гемицеллюлозу и целлюлозу.
16. Способ по п.14, в котором первый твердый остаток (5) подвергают кислотному гидролизу (404) для превращения гемицеллюлозы в сахара, содержащие 5 атомов углерода, в результате которого образуются второй твердый древесный остаток (15), содержащий лигнин и целлюлозу.
17. Способ по п.16, в котором кислотный гидролиз осуществляется фосфоновой кислотой, имеющей общую формулу R-PO(OH)2 (I), в которой в качестве R присутствует неразветвленная или разветвленная алкильная группа, или ароматическая группа, или группа, содержащая гетероатом.
18. Способ по п.17, в котором R представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода, или R выбирается из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, или R представляет собой группу, содержащую гетероатом и выбранную из групп, содержащих кислород (O), или содержащих азот (N), или содержащих фосфор (P).
19. Способ по п.18, в котором R выбран из метильной, этильной или CH3OH-PO(OH)2-группы.
20. Способ по любому из пп. 16-19, в котором pH в течение кислотного гидролиза составляет от 0,6 до 1,6.
21. Способ по п.16, в котором последующий гидролиз выбирают из ферментативного, химического или термохимического гидролиза.
22. Способ по п.1, в котором:
- листья (2) подвергают обработке (100) для получения восков и эфирных масел (102), образуется твердая фракция (101), в которой содержатся целлюлоза, гемицеллюлоза и, в меньшей степени, лигнин, соли и органические соединения;
- вышеупомянутую твердую фракцию (101) подвергают кислотному гидролизу для превращения гемицеллюлозы в мономерные сахара, содержащие 5 атомов углерода (8), C5, и образуется промежуточный продукт, содержащий целлюлозу,
- вышеупомянутый промежуточный продукт затем подвергают последующему гидролизу для превращения целлюлозы (402) в сахара, содержащие 6 атомов углерода (16), C6.
23. Способ по п.22, в котором кислотный гидролиз осуществляется органической кислотой, выбранной из фосфоновых кислот, имеющих общую формулу R-PO(OH)2 (I), или алкилсульфоновых кислот, имеющих общую формулу R1-SO3H (II), в которой R выбран из неразветвленной или разветвленной алкильной группы, ароматической группы или группы, содержащей гетероатом, и R1 выбран из неразветвленной или разветвленной алкильной группы, содержащей от 1 до 6 атомов углерода.
24. Способ по п.23, в котором R представляет собой алкильную группу, содержащую от 1 до 6 атомов углерода, или R выбран из соединений, имеющих формулу R'-C6H5 или R'-C10H8, где R' представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, или R представляет собой группу, содержащую гетероатом и выбранную из групп, содержащих кислород (O), или содержащих азот (N), или содержащих фосфор (P).
25. Способ по п.24, в котором R выбран из метильной, этильной или CH3OH-PO(OH)2-группы.
26. Способ по п.23, в котором R1 представляет собой метил.
27. Способ по п.22, в котором C5-сахара и C6-сахара используют для получения химических веществ, микробных масел или биотоплива (12) посредством ферментации (403).
28. Способ по п.27, в котором получаемые химические вещества представляют собой бутандиолы или биобутадиен.
29. Способ по любому из пп. 22-28, в котором pH в течение кислотного гидролиза составляет от 0,6 до 1,6.
30. Способ по п.22, в котором воски и эфирные масла отделяют способом, выбранным из экстракции растворителем, или паровой экстракции, или экстракции сверхкритическим CO2.
31. Способ по п.22, в котором последующий гидролиз осуществляется способом, выбранным из ферментативного, химического или термохимического гидролиза.
| US 7259231 B2, 21.08.2007 | |||
| Способ получения 8-трихлорметил-кофеина и 7-хлорметил-8-трихлорметил-кофеина | 1941 |
|
SU66308A1 |
| WO 2013192182 A1, 27.12.2013 | |||
| НИТРИЛЬНЫЕ КАУЧУКИ | 2008 |
|
RU2479591C2 |
| US 7923039 B2, 12.04.2011 | |||
| US 4804741 A, 14.02.1989 | |||
| US 4526959 A, 02.07.1985 | |||
| ФИЗИОТЕРАПЕВТИЧЕСКИЙ ЛАЗЕРНЫЙ УДАРНО-ВОЛНОВОЙ СПОСОБ ЛЕЧЕНИЯ ЖИВОГО ОРГАНИЗМА ОТ ОПУХОЛЕВЫХ И ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2268675C2 |
| WO 2013134429 A1, 12.09.2013. | |||
Авторы
Даты
2019-08-01—Публикация
2015-10-21—Подача