Настоящее изобретение относится к индолин-2-он и 1,3-дигидро-пирроло[3,2-с]пиридин-2-оновым производным общей формулы
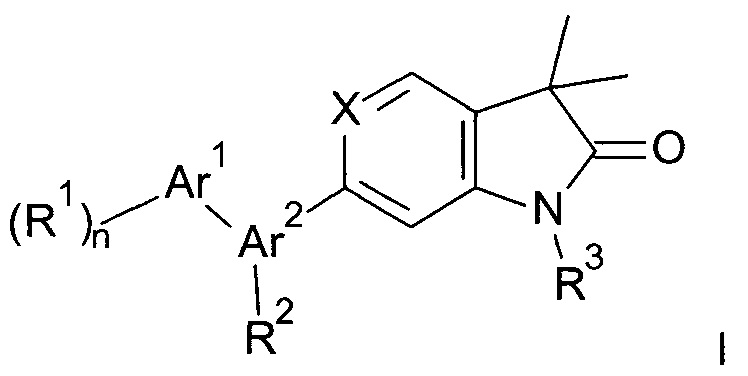
где
Аr1 представляет собой фенил, пиридинил или пиримидинил;
Аr2 представляет собой 5- или 6-членную гетероарильную группу, содержащую 2 или 3 гетероатома, выбранных из N, О или S;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R2 представляет собой водород или низший алкил;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
X представляет собой СН или N;
n представляет собой 1 или 2;
а также их фармацевтически приемлемым солям, рацемической смеси или соответствующего ей энантиомера и/или оптического изомера и/или стереоизомера, для лечения некоторых расстройств центральной нервной системы (ЦНС), которые представляют собой позитивные (психоз) и негативные симптомы шизофрении, злоупотребление лекарственными средствами, алкогольную и лекарственную зависимость, обсессивно-компульсивные расстройства, когнитивное нарушение, биполярные расстройства, расстройства настроения, глубокую депрессию, терапевтически резистентную депрессию, тревожные расстройства, болезнь Альцгеймера, аутизм, болезнь Паркинсона, хроническую боль, пограничное расстройство личности, нарушения сна, синдром хронической усталости, тугоподвижность, противовоспалительные эффекты при артрите и нарушения равновесия.
WO 9106545 описывает сходные структуры, содержащие фенил-замещенные имидазоловые группы в качестве Аr2 для предотвращения агрегации эритроцитов и тромбоцитов. ЕР 2108641 и WO 2008046083 раскрывают очень широкий объем аналогичных соединений, которые являются ингибиторами р38 азот активированной протеинкиназы для лечения воспалительных заболеваний и доброкачественной гиперплазии простаты, соответственно.
В настоящее время обнаружено, что соединения формулы I могут применяться для лечения заболеваний ЦНС. Показано, что описанные соединения обращают индуцированную L-687,414 ((3R,4R)-3-амино-1-гидрокси-4-метил-пирролидин-2-он, антагонист глицинового сайта NMDA) гиперлокомоции, поведенческой фармакодинамической мышиной модели для предсказания эффективности в отношении шизофрении, описанной D. Alberati et al. в Pharmacology, Biochemistry and Behavior, 97 (2010), 185-191. Авторы описали, что гиперлокомоция, индуцированная под действием L-687414, ингибировалась рядом известных антипсихотических лекарственных средств. Соединения формулы I демонстрируют заметную активность в этой модели. Эти данные предсказывают наличие антипсихотической активности у соединений по настоящему изобретению, что делает их полезными для лечения позитивных (психоз) и негативных симптомов шизофрении, злоупотребления лекарственными средствами, алкогольной и лекарственной зависимости, обсессивно-компульсивных расстройств, когнитивного нарушения, биполярных расстройств, расстройства настроения, глубокой депрессии, терапевтически резистентной депрессии, тревожных расстройств, болезни Альцгеймера, аутизма, болезни Паркинсона, хронической боли, пограничного расстройства личности, нарушений сна, синдрома хронической усталости, тугоподвижности, противовоспалительных эффектов при артрите и нарушений равновесия.
Эти результаты показаны в Таблице 1.
Помимо устранения симптомов L-687414-индуцированной гиперлокомоции в эксперименте, описанном выше, некоторые соединения по настоящему изобретению были протестированы в SmartCube®, автоматизированной системе, в которой поведение обработанных соединениями мышей в ответ на стимуляции фиксируют с помощью цифровой видеотехники и анализируют, используя компьютерные алгоритмы (Roberds et al., Frontiers in Neuroscience, 2011, Vol. 5, Art. 103, 1-4). Таким образом, нейрофармакологические эффекты тестируемого соединения могут быть предсказаны на основании сходства с основными классами соединений, такими как антипсихотические средства, анксиолитики и антидепрессанты. В примерах 35, 47, 62 и 93 продемонстрировано сходство с атипичными антипсихотическими средствами. Результаты показаны в Таблице 2.
Шизофрения представляет собой комплексную группу психических расстройств, обычно появляющихся в позднем подростковом возрасте или в раннем взрослом возрасте с распространенностью по всему миру, составляющей приблизительно 1% взрослого населения, которая имеет огромный социальный и экономический эффект. Критерии Ассоциации европейских психиатров (International classification of diseases (ICD) - Международная классификация болезней) и Американской ассоциации психиатров (Diagnostic and Statistical Manual of Mental Disorders (DSM) - Руководство по диагностике и статистике психических расстройств) в отношении диагностики шизофрении требуют наличия двух или более характерных симптомов: бредовых расстройств, галлюцинаций, дезорганизованной речи, глубоко дезорганизованного или кататонического стиля поведения (позитивных симптомов) или негативных симптомов (алогии, аффективной тупости, отсутствии мотивации, ангедонии). Как группа, люди с шизофренией имеют функциональные нарушения, начало проявления которых может быть обнаружено в детском возрасте, которые могут продолжаться на протяжении всей взрослой жизни и делать большинство пациентов неспособными поддерживать нормальную трудовую деятельность или иным образом выполнять нормальную социальную функцию. Кроме того, они имеют сокращенную продолжительность жизни по сравнению с населением в целом и страдают от повышения заболеваемости целым рядом других нейропсихиатрических синдромов, включая злоупотребление лекарственными средствами, обсессивно-компульсивные симптомы и патологические непроизвольные движения, до проведения лечения антипсихотическими средствами. Шизофрения также ассоциирована с целым рядом когнитивных нарушений, биполярных расстройств, глубокой депрессией и тревожными расстройствами, тяжесть которых ограничивает жизнедеятельность пациентов, даже когда психотические симптомы находятся под удовлетворительным контролем. Первичное лечение шизофрении заключается в применении антипсихотических средств. Антипсихотические средства, например, рисперидон, оланзапин, однако, не существенно ослабляет негативные симптомы и когнитивную дисфункцию.
Антипсихотические лекарственные средства продемонстрировали клиническую эффективность в отношении лечения приведенных ниже заболеваний:
Фибромиалгии, которая представляет собой синдром, характеризующийся хронической генерализованной болью, ассоциированной с разными соматическими симптомами, такими как нарушения сна, усталость, тугоподвижность, нарушения равновесия, гиперчувствительность к физическим и психологическим внешним стимулам, депрессия и тревога (CNS Drugs, 2012, 26(2): 135-53);
Шизоаффективных расстройств: которые включают психотические и аффективные симптомы, это расстройство попадает в спектр между биполярными расстройствами (с депрессивными и маниакальными эпизодами, алкогольной и лекарственной зависимостью, злоупотреблением лекарственными средствами) и шизофренией. J. Clin. Psychiatry, 2010, 71, Suppl. 2, 14-9; Pediatr. Drugs, 2011, 13 (5), 291-302;
Глубокой депрессии: BMC Psychiatry, 2011, 11, 86;
Терапевтически резистентной депрессии: Journal of Psychopharmacology, 0(0), 1-16;
Тревоги: European Neuropsychopharmacology, 2011, 21, 429-449;
Биполярных расстройств: Encephale, International J. of Neuropsychopharmacology, 2011, 14, 1029-1049; International J. of Neuropsychopharmacology, 2012, pages 1-12; J. of Neuropsychopharmacology, 2011, 0(0), 1-15;
Расстройств настроения: J. Psychopharmacol. 2012, Jan 11 CNS Drugs, 2010, Feb. 24(2), 131-61;
Аутизма: Current opinion in pediatrics, 2011, 23: 621-627; J. Clin. Psychiatry, 2011, 72(9), 1270-1276;
Болезни Альцгеймера: J. Clin. Psychiatry, 2012, 73(1), 121-128;
Болезни Паркинсона: Movement Disorders, Vol. 26, No. 6, 2011;
Синдрома хронической усталости: European Neuropsychopharmacology, 2011, 21, 282-286;
Пограничного расстройства личности: J. Clin. Psychiatry, 2011, 72 (10), 1363-1365; J. Clin. Psychiatry, 2011, 72 (10), 1353-1362;
Противовоспалительных эффектов при артрите: European J. Of Pharmacology, 678, 2012, 55-60.
Объектами настоящего изобретения являются соединения формулы I для применения при лечении заболеваний ЦНС, связанных с позитивными (психоз) и негативными симптомами шизофрении, злоупотреблением лекарственными средствами, алкогольной и лекарственной зависимостью, обсессивно-компульсивными расстройствами, когнитивным нарушением, биполярными расстройствами, расстройствами настроения, глубокой депрессией, терапевтически резистентной депрессией, тревожными расстройствами, болезнью Альцгеймера, аутизмом, болезнью Паркинсона, хронической болью, пограничным расстройством личности, нарушениями сна, синдромом хронической усталости, тугоподвижностью, противовоспалительными эффектами при артрите и нарушениями равновесия. Другими объектами настоящего изобретения являются новые соединения, лекарственные средства, содержащие такие новые соединения, а также способы получения соединений формулы I, комбинации соединений формулы I с зарегистрированными для продажи антипсихотическими средствами, антидепрессантами, анксиолитиками или стабилизаторами настроения и способы лечения расстройств ЦНС, упомянутых выше.
Соединения формулы I для применения при лечении вышеуказанных заболеваний ЦНС являются следующими:
1-циклопропил-6-(5-(4-фторфенил)-1Н-имидазол-2-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(5-фенил-1Н-имидазол-2-ил)индолин-2-он
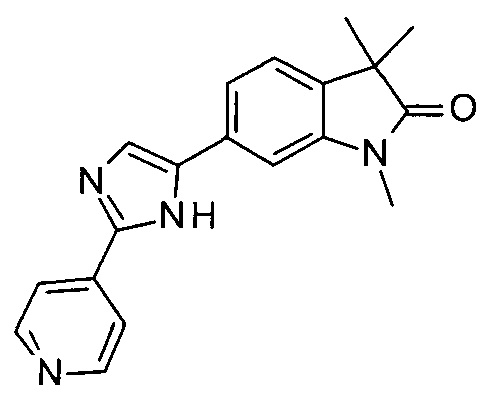
1,3,3-триметил-6-(2-(пиридин-4-ил)-1Н-имидазол-5-ил)индолин-2-он
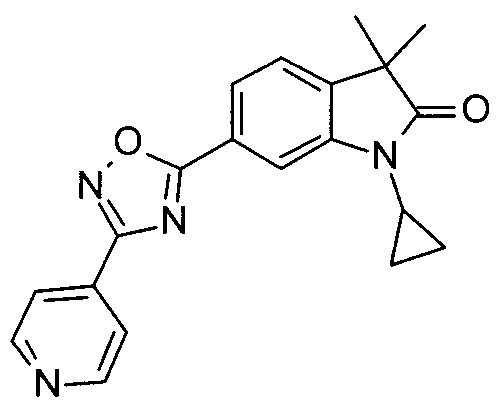
1-циклопропил-3,3-диметил-6-(3-(пиридин-4-ил)-1,2,4-оксадиазол-5-ил)индолин-2-он
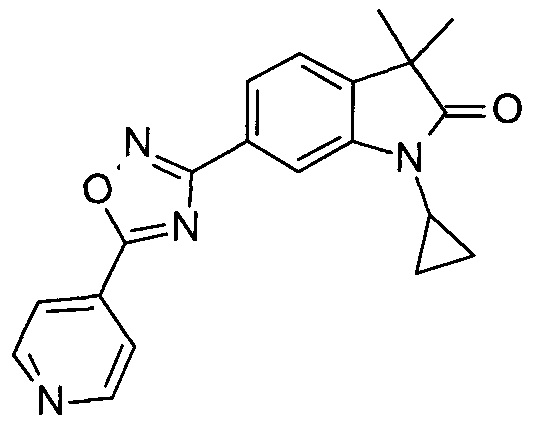
1-циклопропил-3,3-диметил-6-(5-(пиридин-4-ил)-1,2,4-оксадиазол-3-ил)индолин-2-он
3,3-диметил-1-оксетан-3-ил-6-(3-пиридин-4-ил-[1,2,4]оксадиазол-5-ил)-1,3-дигидро-индол-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-4-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-4-ил)оксазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)-1-(оксетан-3-ил)индолин-2-он
3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)-1-(оксетан-3-ил)индолин-2-он
3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
1-(2-Гидроксиэтил)-3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(3-пиридин-4-ил-изоксазол-5-ил)-1,3-дигидро-индол-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-4-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-пиразол-4-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
3,3-диметил-6-(5-(2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1-(оксетан-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-пиразол-4-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(5-(пиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-1,2,3-триазол-1-ил)индолин-2-он
3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(2-(3-метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(5-(пиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
1-этил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
6-[1-(2-фторпиридин-4-ил)имидазол-4-ил]-1,3,3-триметилиндол-2-он
1,3,3-триметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)-1-(оксетан-3-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолт-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(2-метил-1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-2-метил-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
1,3,3-триметил-6-(5-(6-метилпиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(1-метил-5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)пиримидин-4-ил)индолин-2-он
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-3-(2-метилпиридин-4-ил)-1Н-пиразол-5-ил)индолин-2-он
3,3-диметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)-1-(оксетан-3-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-2-метил-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-[2-(2-метил-пиридин-4-ил)-оксазол-5-ил]-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
6-(1-(5-фтор-2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
6-(2-(5-фтор-2-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он
3,3-диметил-6-[5-(2-метил-пиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-1-оксетан-3-ил-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
6-(1-(2-фтор-5-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
6-(2-(2-фтор-5-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он
6-(5-(5-фтор-2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1,3,3-триметилиндолин-2-он
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-5-ил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(6-метил-3-пиридил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метил-4-пиридил)индолин-2-он
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(2-метил-4-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(2-метилпиридин-4-ил)-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1-(1-метил-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1-(1-метил-1Н-пиразол-3-ил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метилпиримидин-5-ил)индолин-2-он
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-6-[1-(2-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-6-[1-(3-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
6-[4-(5-фтор-2-метил-4-пиридил)имидазол-1-ил]-1,3,3-триметил-индолин-2-он
1,3,3-триметил-6-[5-(3-метил-4-пиридил)изоксазол-3-ил]индолин-2-он
1,3,3-триметил-6-[4-(3-метил-4-пиридил)имидазол-1-ил]индолин-2-он
1,3,3-триметил-6-[4-(2-метил-4-пиридил)имидазол-1-ил]индолин-2-он
6-[4-(2-фтор-4-пиридил)имидазол-1-ил]-1,3,3-триметил-индолин-2-он
1-(3-циклопропилсульфонилпропил)-6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-1-(2-гидроксиэтил)-3,3-диметил-индолин-2-он
1-(3-циклопропилсульфонилпропил)-6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он или
6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он.
Одним объектом настоящего изобретения являются новые соединения общей формулы
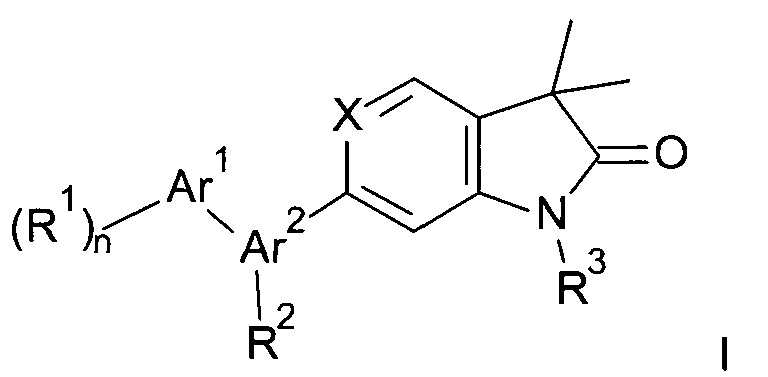
где
Аr1 представляет собой фенил, пиридинил или пиримидинил;
Аr2 представляет собой 5- или 6-членную гетероарильную группу, содержащую 2 или 3 гетероатома, выбранных из N, О или S;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R2 представляет собой водород или низший алкил;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
X представляет собой СН или N;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемические смеси, или соответствующие энантиомеры и/или оптические изомеры и/или стереоизомеры, за исключением, что Аr2 не является 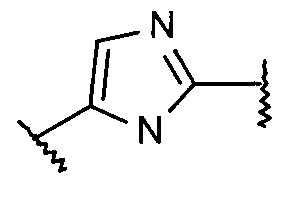 ,
, 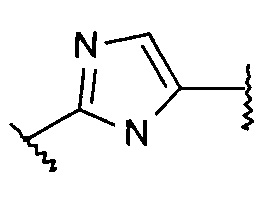 , например, следующие соединения:
, например, следующие соединения:
1-циклопропил-3,3-диметил-6-(3-(пиридин-4-ил)-1,2,4-оксадиазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(пиридин-4-ил)-1,2,4-оксадиазол-3-ил)индолин-2-он
3,3-диметил-1-оксетан-3-ил-6-(3-пиридин-4-ил-[1,2,4]оксадиазол-5-ил)-1,3-дигидро-индол-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-4-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-4-ил)оксазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)-1-(оксетан-3-ил)индолин-2-он
3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)-1-(оксетан-3-ил)индолин-2-он
3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
1-(2-Гидроксиэтил)-3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(3-пиридин-4-ил-изоксазол-5-ил)-1,3-дигидро-индол-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-4-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-пиразол-4-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1 -циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
3,3-диметил-6-(5-(2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1-(оксетан-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-пиразол-4-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(5-(пиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-1,2,3-триазол-1-ил)индолин-2-он
3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(2-(3-метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(5-(пиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
1-этил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
6-[1-(2-фторпиридин-4-ил)имидазол-4-ил]-1,3,3-триметилиндол-2-он
1,3,3-триметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(6-метил пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)-1-(оксетан-3-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(2-метил-1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-2-метил-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
1,3,3-триметил-6-(5-(6-метилпиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(1-метил-5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)пиримидин-4-ил)индолин-2-он
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)индолин-2-он
1,3,3-триметил-6-(4-метил-3-(2-метилпиридин-4-ил)-1Н-пиразол-5-ил)индолин-2-он
3,3-диметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)-1-(оксетан-3-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-2-метил-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-[2-(2-метил-пиридин-4-ил)-оксазол-5-ил]-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
6-(1-(5-фтор-2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
6-(2-(5-фтор-2-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он
3,3-диметил-6-[5-(2-метил-пиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-1-оксетан-3-ил-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
6-(1-(2-фтор-5-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
6-(2-(2-фтор-5-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он
6-(5-(5-фтор-2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1,3,3-триметилиндолин-2-он
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-5-ил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(6-метил-3-пиридил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метил-4-пиридил)индолин-2-он
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(2-метил-4-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(2-метилпиридин-4-ил)-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1-(1-метил-1Н-имидазол-4-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1-(1-метил-1Н-пиразол-3-ил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метилпиримидин-5-ил)индолин-2-он
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-6-[1-(2-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-6-[1-(3-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
3,3-диметил-6-(1-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
6-[4-(5-фтор-2-метил-4-пиридил)имидазол-1-ил]-1,3,3-триметил-индолин-2-он
1,3,3-триметил-6-[5-(3-метил-4-пиридил)изоксазол-3-ил]индолин-2-он
1,3,3-триметил-6-[4-(3-метил-4-пиридил)имидазол-1-ил]индолин-2-он
1,3,3-триметил-6-[4-(2-метил-4-пиридил)имидазол-1-ил]индолин-2-он
6-[4-(2-фтор-4-пиридил)имидазол-1-ил]-1,3,3-триметил-индолин-2-он
1-(3-циклопропилсульфонилпропил)-6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-1-(2-гидроксиэтил)-3,3-диметил-индолин-2-он
1-(3-циклопропилсульфонилпропил)-6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он или
6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ic
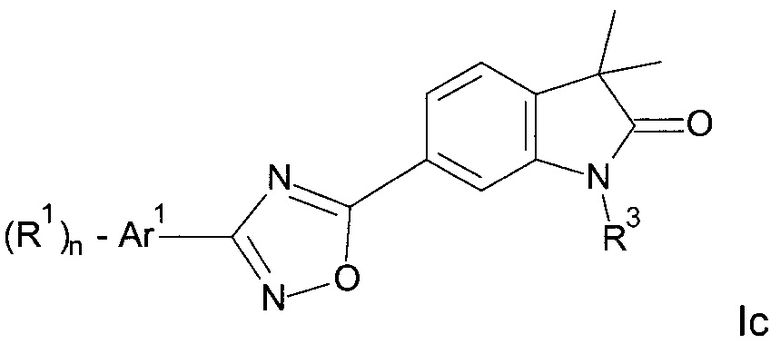
где
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер. Одним дополнительным объектом настоящего изобретения являются соединения формулы Id
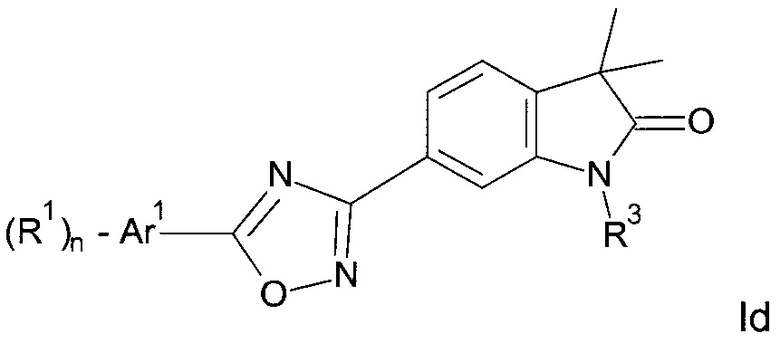
где
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Iе
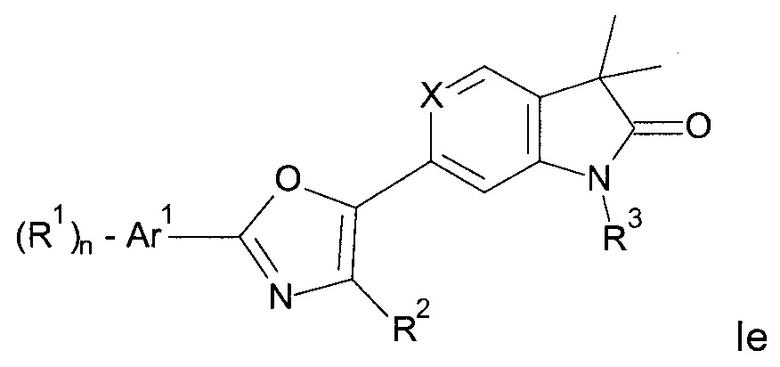
где
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R2 представляет собой водород или низший алкил;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы If
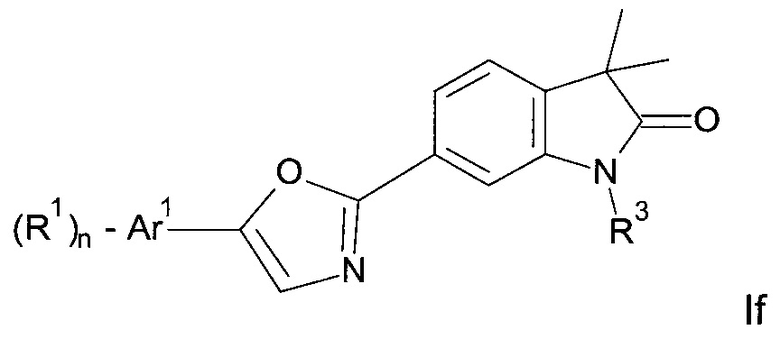
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ig
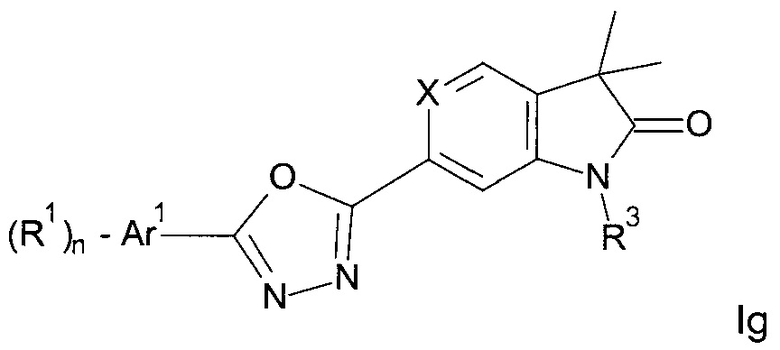
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ih
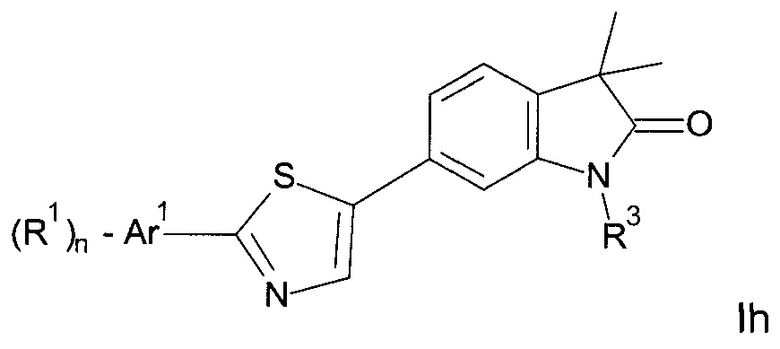
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ik
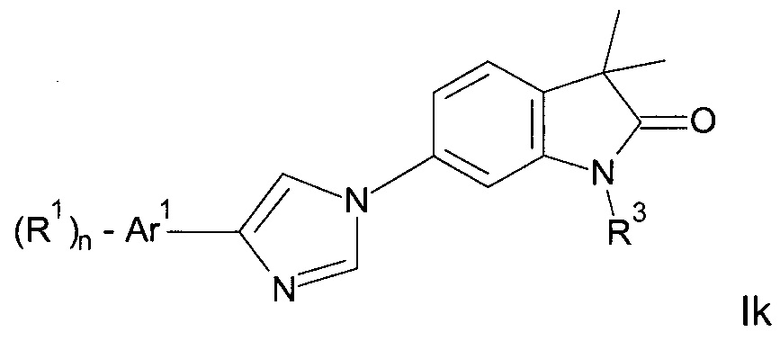
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ii
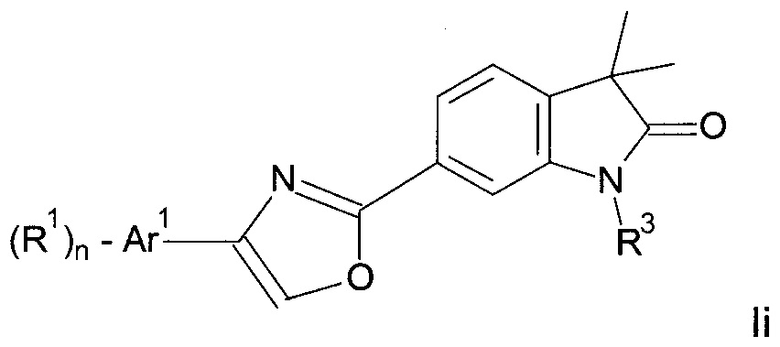
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы II
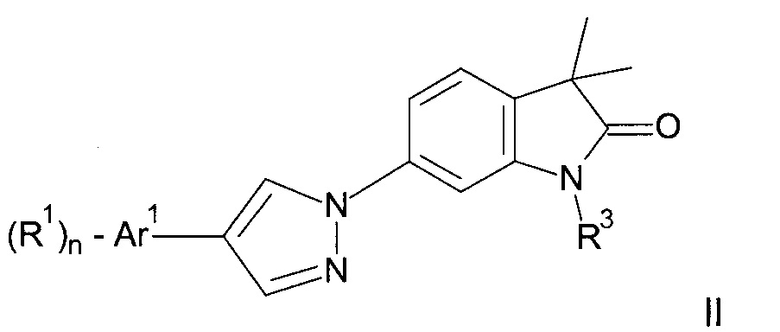
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R2 представляет собой водород или низший алкил;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Im
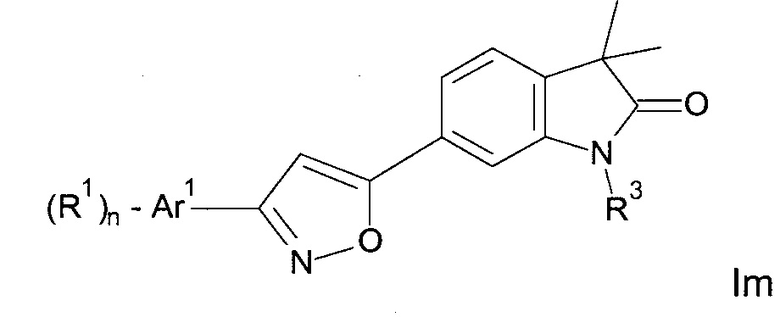 или
или
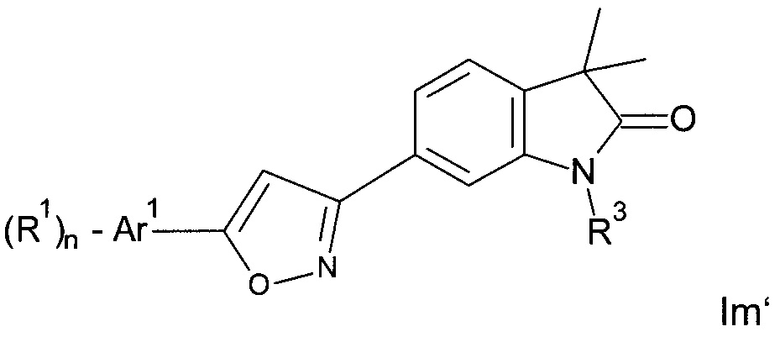
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы In
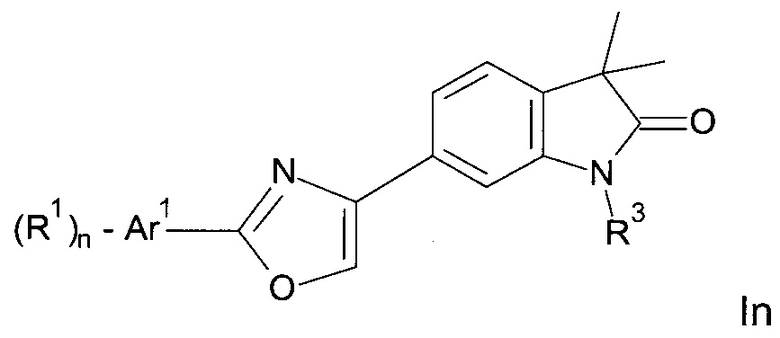
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Io
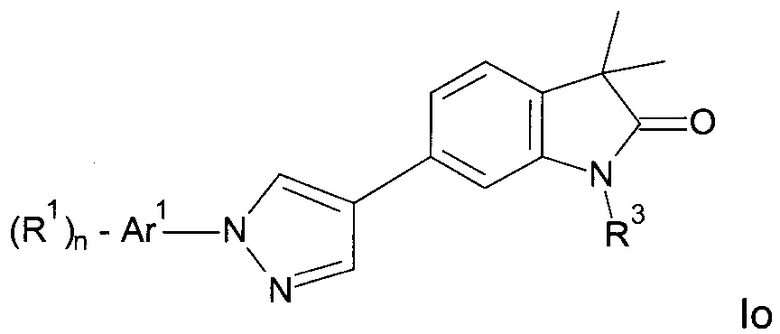
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ip
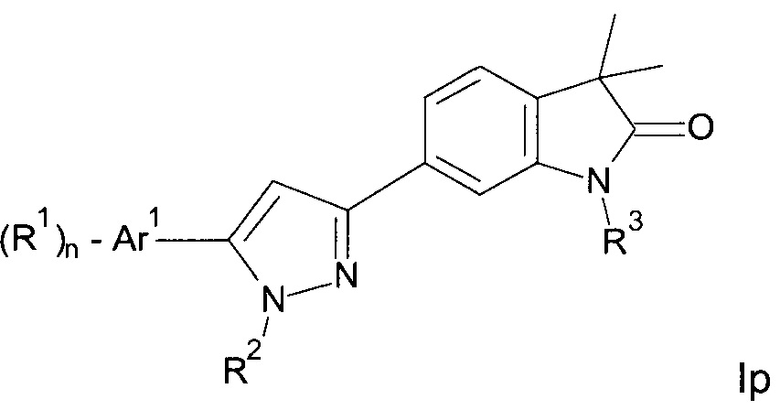
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R2 представляет собой водород или низший алкил;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Iq
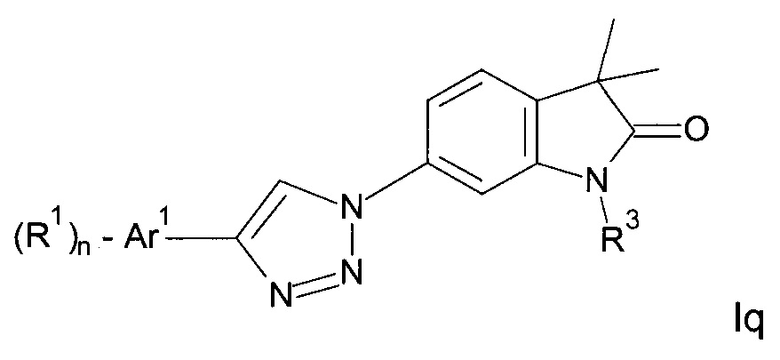
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Ir
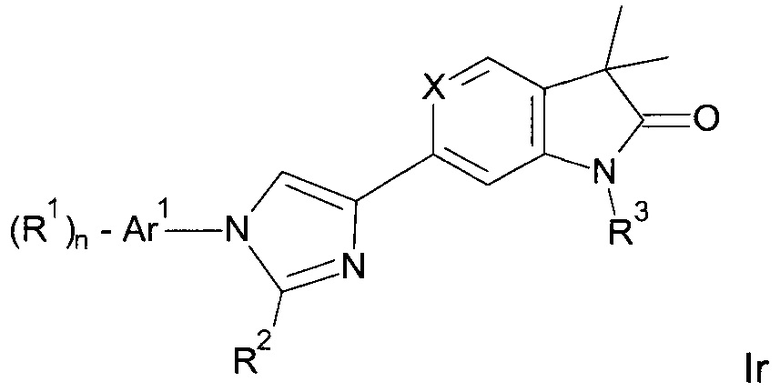
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R2 представляет собой водород или низший алкил;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Одним дополнительным объектом настоящего изобретения являются соединения формулы Is
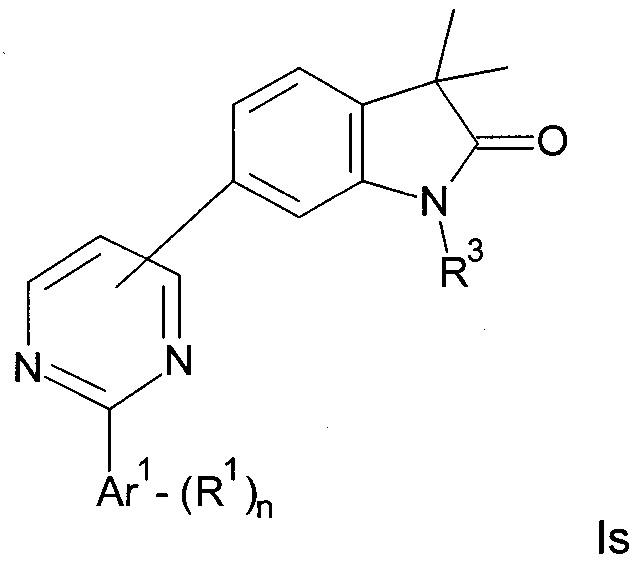
Аr1 представляет собой фенил, пиридинил или пиримидинил;
R1 представляет собой водород, низший алкил, галоген или низший алкокси;
R3 представляет собой водород, низший алкил, низший алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены низшим алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
n представляет собой 1 или 2;
а также их фармацевтически приемлемые соли, рацемическая смесь или их соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Настоящим изобретением охватываются соответствующие пролекарства соединений формулы I.
Широко известным антипсихотическим лекарственным средством для лечения шизофрении является оланзапин. Оланзапин (зипрекса) принадлежит классу лекарственных средств, известных как атипичные антипсихотические средства. Другие представители этого класса включают, например клозапин (клозарил), рисперидон (риспердал), арипипразол (абилифай) и зипрасидон (геодон).
Оланзапин одобрен к применению для лечения психотических расстройств, долгосрочного лечения биполярных расстройств и в комбинации с флуоксетином для лечения депрессивных эпизодов, ассоциированных с биполярными расстройствами, и для лечения терапевтически резистентной депрессии.
Соединения по настоящему изобретению могут быть объединены с антипсихотическими лекарственными средствами, такими как оланзапин (зипрекса), клозапин (клозарил), рисперидон (риспердал), арипипразол (абилифай), амисульприд (солиан), азенапин (сафрис), блонансерин (лоназен), клотиапин (энтумин), илоперидон (фанапт), луразидон (латуда), мосапрамин (кремин), палиперидон (инвега), пероспирон (люллан), кветиапин (сероквель), ремоксиприд (роксиам), сертиндол (сердолект), сульпирид (сулпирид, эглонил), зипрасидон (геодон, зелдокс), зотепин (ниполепт), галоперидол (галдол, серенас), дроперидол (дролептан), хпорпромазин (торазин, ларгактил), флуфеназин (проликсин), перфеназин (трилафон), прохпорперазин (компазин), тиоридазин (мелларил, меллерил), трифлуоперазин (стелазин), трифлупромазин (весприн), левомепромазин (нозинан), прометазин (фенерган), пимозид (орал) и циамемазин (терциан).
Одним из предпочтительных воплощений изобретения является комбинация, где зарегистрированное для продажи антипсихотическое лекарственное средство представляет собой оланзапин (зипрекса), клозапин (клозарил), рисперидон (риспердал), арипипразол (абилифай) или зипрасидон.
Кроме того, соединения по настоящему изобретению могут быть объединены с антидепрессантами, такими как селективные ингибиторы обратного захвата серотонина [циталопрам (целекса), эсциталопрам (лексапро, ципралекс), пароксетин (паксил, сероксат), флуоксетин (прозак), флувоксамин (лувокс), сертралин (золофт, люстрал)], ингибиторы обратного захвата серотонина-норэпинефрина [дулоксетин (симбалта), милнаципран (иксел, савелла), венлафаксин (эффексор), дезвенлафаксин (пристик), трамадол (трамал, ультрам), сибутрамин (меридиа, редуктил)], антагонисты и ингибиторы обратного захвата серотонина [этоперидон (аксиомин (axiomin), этонин (etonin)), лубазодон (УМ-992, УМ-35995), нефазодон (серзон, нефадар), тразодон (дезирел)], ингибиторы обратного захвата норэпинефрина [ребоксетин (эдронакс), вилоксазин (вивалан), атомоксетин (страттера)], ингибиторы обратного захвата норэпинефрина-дофамина [бупропион (велбутрин, зибан), дексметилфенидат (фокалин), метилфенидат (риталин, концерта)], норэпинефрин-дофамин- рилизинг-агенты [амфетамин (аддерал), декстроамфетамин (декседрин), декстрометамфетамин (дезоксин), лиздексамфетамин (виванс (vyvanse))], трициклические антидепрессанты [амитриптилин (элавил (elavil), эндеп (endep)), кломипрамин (анафранил), дезипрамин (норпрамин, пертофран), досулепин [дотиепин] (протиаден), доксепин (адапин, синекван), имипрамин (тофранил), лофепрамин (фепрапакс (feprapax), гаманил, ломонт (lomont)), нортриптилин (памелор), протриптилин (вивактил), тримипрамин (сурмонтил)], тетрациклические антидепрессанты [амоксапин (азендин), мапротилин (лудиомил), миансерин (больвидон, норвал, толвон), миртазапин (ремерон)], ингибиторы моноаминоксидазы [изокарбоксазид (марплан), моклобемид (аурорикс, манерикс), фенелзин (нардил), селегилин [L-депренил] (элдеприл, зелапар, емсам), транилципромин (парнат), пирлиндол (пиразидол)], агонисты рецепторов 5-НТ1А [буспирон (буспар), тандоспирон (седиель (sediel)), вилазодон (виибрид)], антагонисты рецепторов 5-НТ2 [агомелатин (вальдоксан), нефазодон (нефадар, серзон)], селективные усилители обратного захвата серотонина (тианептин).
Предпочтительным воплощением данного изобретения является комбинация, где зарегистрированное для продажи антидепрессивное лекарственное средство представляет собой циталопрам (целекса), эсциталопрам (лексапро, ципралекс), пароксетин (паксил, сероксат), флуоксетин (прозак), сертралин (золофт, люстрал), дулоксетин (симбалта), милнаципран (иксель, савелла), венлафаксин (эффексор) или миртазапин (ремерон).
Кроме того, соединения могут быть объединены с анксиолитиками, такими как алпразолам (хелекс, ксанакс, ксанор, онакс (опах), алпрокс, рестил, тафил, паксил, бретазенил, бромазепам (лектопам (lectopam), лексотанил, лексотан, бромам (bromam)), бротизолам (лендормин, дормекс, синтонал (sintonal), ноктилан (noctilan)), хлордиазепоксид (либриум, ризолид (risolid), элениум), цинолазепам (геродорм), клоназепам (ривотрил, клонопин, икторивил, пакспам, клоразепат (транксен, транксилиум), клотиазепам (вератран (veratran), клозан (clozan), ризе (rize)), клоксазолам (сепазон (sepazon), олкадил (olcadil)), делоразепам (дадумир (dadumir)), диазепам (антенекс, апаурин, апзепам, апозепам, гексалид, паке, стесолид, стедон, валиум, вивал, валаксона (valaxona)), эстазолам (просом), этизолам (этилаам (etilaam), пасаден (pasaden), депас (depas)), флунитразепам (рохипнол, флусканд, флунипам, ронал, рогидорм (rohydorm)), флуразепам (далмадорм, далман), флутопразепам (рестас (restas)), галазепам (паксипам), кетазолам (анксон), лопразолам (дормонокт), лоразепам (ативан, теместа, тавор, лорабенз), лорметазепам (лорамет, ноктамид, проноктан), медазепам (нобриум), мидазолам (дормикум, версед, гипновель, дормонид), ниметазепам (еримин (erimin)), нитразепам (могадон, алодорм, пасисин (pacisyn), думолид, нитразадон), нордазепам (мадар, стилни (stilny)), оксазепам (сереста, серакс, серенид, серепакс, собрил (sobril), оксабенз, оксапакс), феназепам, пиназепам (домар), празепам (лисанксиа (lysanxia), центракс), премазепам, квазепам (дорал), темазепам (ресторил, нормисон, эугипнос, темаз, тенокс), тетразепам (миоластан), триазолам (гальцион, риламир (rilamir)), клобазам (фризиум, урбанол (urbanol)), эсзопиклон (лунеста), залеплон (соната, старнок (starnoc)), золпидем (амбиен, нитамел, стилнокт, стилнокс, золдем, золнод), зопиклон (имован, рован (rhovane), ксимован (ximovan); зилез (zileze); зимоклон; зимован; зопитан (zopitan); зоркпон), прегабалин (лирика) и габапентин (фанатрекс, габарон, грализ, нейронтин, нупентин (nupentin)).
Одним из предпочтительных воплощений изобретения является комбинация, где зарегистрированным для продажи анксиолитическим лекарственным средством является алпразолам (хелекс, ксанакс, ксанор, онакс, алпрокс, рестил, тафил, паксал), хпордиазепоксид (либриум, ризолид, элениум), клоназепам (ривотрил, клонопин, икторивил, паксам), диазепам (антенекс, апаурин, апзепам, апозепам, гексалид, паке, стесолид, стедон, валиум, вивал, валаксона), эстазолам (просом), эсзопиклон (лунеста), залеплон (соната, старнок), золпидем (амбиен, нитамел, стилнокт, стилнокс, золдем, золнод), прегабалин (лирика) или габапентин (фанатрекс, габарон, грализ, нейронтин, нупентин).
Другим объектом изобретения является комбинация со стабилизаторами настроения, такими как карбамазепин (тегретол), ламотриджин (ламиктал), литий (эскалит, питан, литобид) и вальпроевая кислота (депакот).
Кроме того, данные соединения могут быть объединены с соединениями с прокогнитивным действием, такими какдонепезил (арисепт), галантамин (разадин), ривастигмин (экселон) и мемантин (наменда).
Предпочтительными показаниями, при которых используют соединения по настоящему изобретению, являются психотические заболевания типа шизофрении.
Как здесь используется, термин ''низший алкил'' означает группу с насыщенной прямой или разветвленной цепью, содержащую от 1 до 7 атомов углерода, например, метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет-бутил и тому подобное. Предпочтительными алкильными группами являются группы из 1-4 атомов углерода.
Как здесь используется, термин ''низший алкокси'' означает группу, где алкильный остаток является таким, как определено выше, и который присоединен через атом кислорода.
Как здесь используется, термин ''низший алкил, замещенный гидрокси'' означает группу, где алкильный остаток является таким, как определено выше, где по меньшей мере один атом водорода заменен на гидроксигруппу.
Термин ''циклоалкил'' означает алкильное кольцо с 3-6 кольцевыми атомами углерода.
Термин ''галоген'' означает атом хлора, йода, фтора и брома.
Термин ''5 или 6 членная гетероарильная группа, содержащая 2 или 3 гетероатома, выбранных из N, О или S'' означает ароматическое кольцо, например, следующие группы:
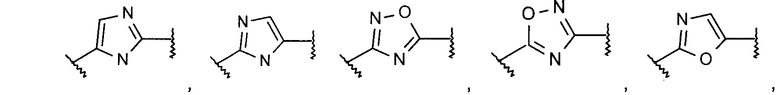
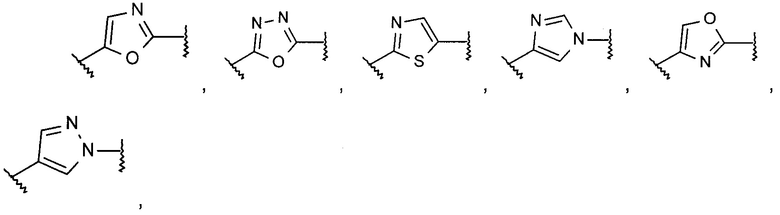
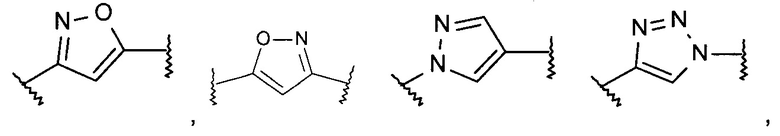
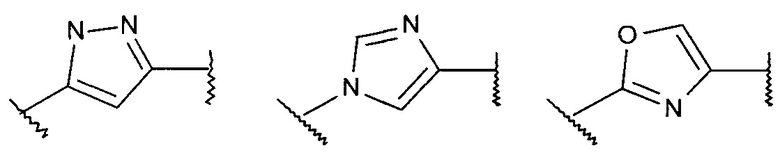 или
или 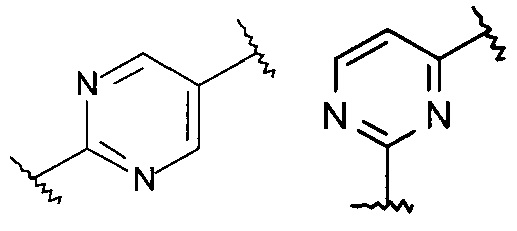
Термин ''фармацевтически приемлемые кислотно-аддитивные соли'' охватывает соли с неорганическими и органическими кислотами, такими как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п.
Соединения по настоящему изобретению формулы I и их фармацевтически приемлемые соли могут быть получены способами, известными в данной области техники, например, способами, описанными ниже, которые содержат
а) взаимодействие соединения формулы
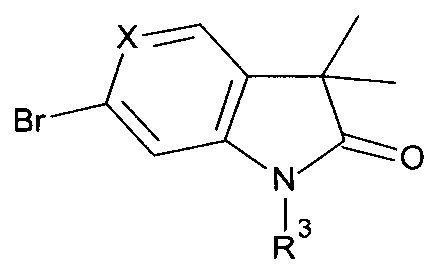
с соединением формулы
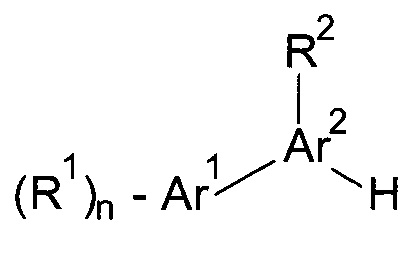
С получением соединения формулы
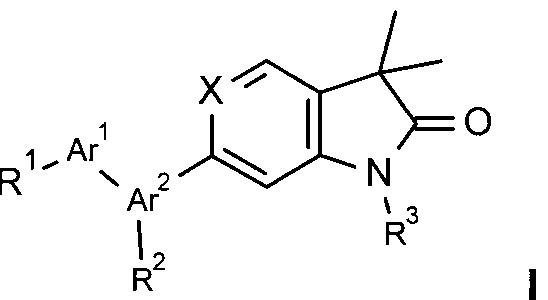
Где заместители обладают значениями, как описано выше, и,
если необходимо, конвертирование полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли; или
b) взаимодействие соединения формулы
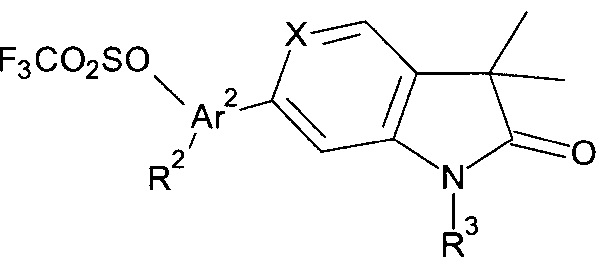
с соединением формулы
(R1)n-Ar1-В(ОН)2
С получением соединения формулы
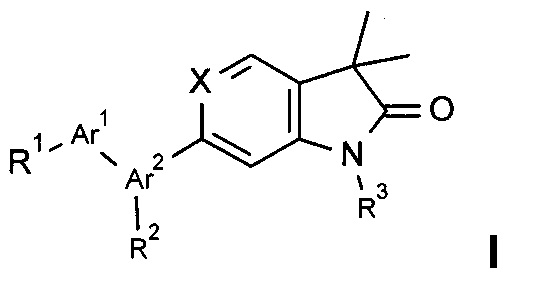
Где заместители обладают значениями, как описано выше, и,
если необходимо, конвертирование полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли;
с) взаимодействие соединения формулы
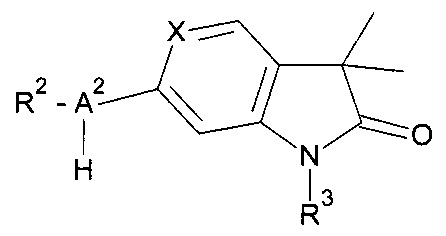
с соединением формулы
(R1)n-Ar1-Br
С получением соединения формулы

Где заместители обладают значениями, как описано выше, и,
если необходимо, конвертирование полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли;
Получение соединений формулы I настоящего изобретения может быть осуществлено путем последовательного или конвергентного синтезов. Пути синтеза соединений по изобретению показаны на приведенных далее схемах. Знания, необходимые для проведения данной реакции и очистки полученных продуктов, известны специалистам в данной области техники. Заместители и индексы, использованные в следующем далее описании способов, имеют значение, приведенное в данном описании ранее, если не указано иное.
Более подробно, соединения формулы I могут быть получены приведенными ниже способами, способами, приведенными в разделе Примеры, или аналогичными способами. Соответствующие реакционные условия для отдельных стадий реакций известны специалисту в данной области техники. Последовательность реакций не ограничивается последовательностью, показанной на схемах, однако в зависимости от исходных веществ и соответствующей им реакционной способности последовательность стадий реакций можно менять по своему усмотрению. Исходные вещества либо имеются в продаже, либо могут быть получены способами, аналогичными способам, приведенным ниже, способами, описанными в разделе Примеры, или способами, известными в данной области техники.
Для R3 = метил, соединения общей формулы 2 (X=СН) (Схема 1) могут, например, быть получены посредством триметилирования 6-гало-оксиндолов 1 (X=СН) с помощью Me-LG, где LG представляет собой уходящую группу, такую как йодид, бромид, хлорид, тозилат в присутствии основания, такого как гидрид натрия, и где Y представляет собой галоген, например, бромид.
Схема 1
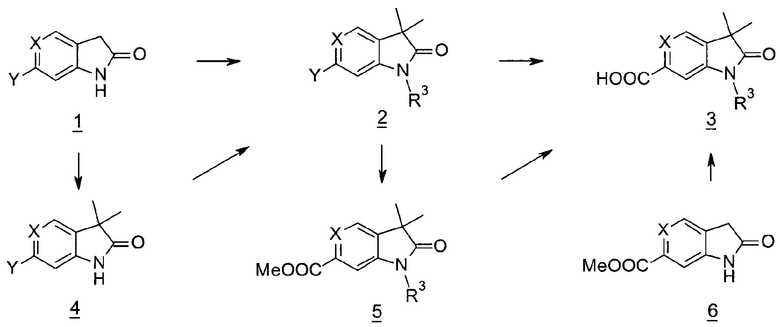
Для R3 ≠ метил, соединения общей формулы 2 (X=СН) (Схема 1) могут, например, быть получены посредством диметилирования 6-гало-оксиндолов 1 (X=СН) с Me-LG (LG представляет собой уходящую группу, такую как йодид, бромид, хлорид, тозилат) в присутствии основания, такого как трет-бутоксид калия и в присутствии медь(I)бромид-диметилсульфидного комплекса с получением диалкилированного продукта 4 (X=СН). Соединения общей формулы 2 (X=СН, N) могут быть получены посредством алкилирования соединений общей формулы 4 (X=СН, N) с R3-LG в присутствии основания, такого как гидрид натрия или карбонат цезия или посредством бороновых кислот R3-B(OH)2 или эфиров R3-B(OR’)2 (например, R3-4,4,5,5-тетраметил-[1,3,2]диоксаборолан) в услвоиях металлического катализа (например, катализа палладием(0) или медью(II)) в присутствии основания, такого как, например, натрия бис(триметилсилил)амид или карбонат натрия.
Соединения формулы 5 (X=СН, N) (Схема 1) могут быть получены из соединений общей формулы 2 (X=СН, N) посредством карбонилирования с помощью монооксида углерода в метаноле и в присутствии ферроцен-палладиевого катализатора. Гидролиз метиловых эфиров 5 (X=СН) с использованием, например, гиидроксида натрия, дает кислоты 3 (X=СН). Альтернативно, для R3 = метил, кислота 3 (X=СН) может быть получена посредством взаимодействия метилового эфира 6 с избытком Me-LG в присутствии избытка основания, такого как гидрид натрия в ТГФ с последующим гидролизом промежуточного эфира с использованием гидроксида натрия. Для R3=Н, кислота 3 (X=СН) может быть получены посредством взаимодействия метилового эфира 6 с 2 эквивалентами Me-LG в присутствии 2 эквивалентов основания, например, гидрида натрия, в ДМФ С последующим гидролизом эфирной группы с использованием, например, гидроксида натрия.
Схема 2
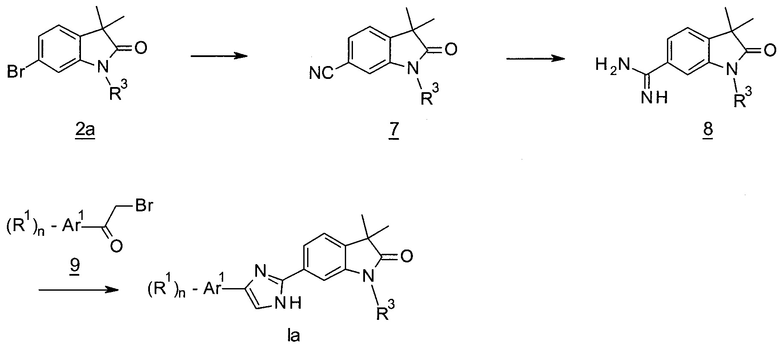
Имидазолы формулы Iа (Схема 2) могут быть получены посредством замещения бромидов 2а с помощью цианидов, например, цианида цинка, в присутствии палладиевого катализатора, с получением нитрилов 7. Добавление LiHMDS к нитрилам 7 с последующим кислотным гидролизом дает амидины 8, которые могут быть циклизованы с α-бромметилкетонами 9 в присутствии основания с получением имидазолов Iа.
Схема 3
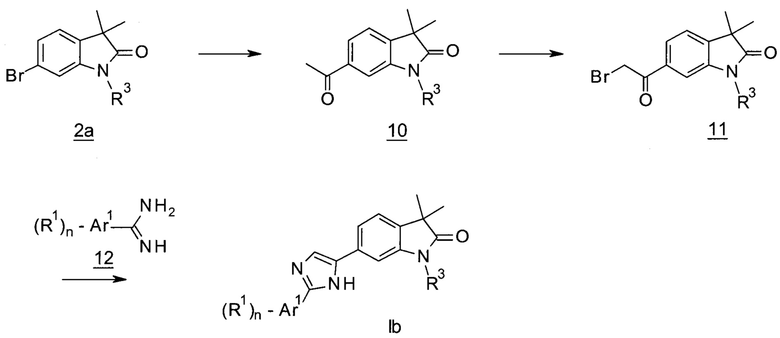
Имидазолы формулы Ib (Схема 3) могут быть получены с использованием в качестве исходного вещества бромидов 2а, которые могут взаимодействовать с N-бутилвиниловым эфиром в присутствии палладиевого катализатора с получением метилкетонов 10. Бромирование соединений 10 с помощью, например, тетра-N-бутиламмония трибромида с последующей конденсацией образовавшихся α-галометилкетонов 11 с амидинами 12 дает имидазолы Ib.
Схема 4
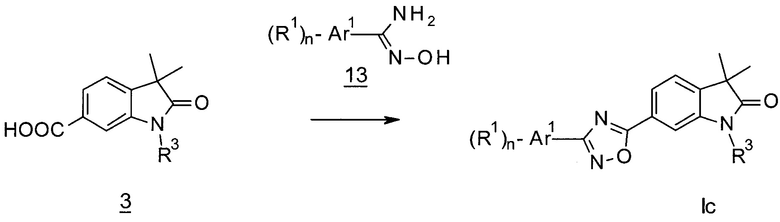
1,2,4-Оксадиазолы формулы Ic (Схема 4) могут быть получены посредством конденсации кислот 3 (X=СН) с N-гидроксиамидинами 13, например, в присутствии карбонилдиимидазола.
Схема 5
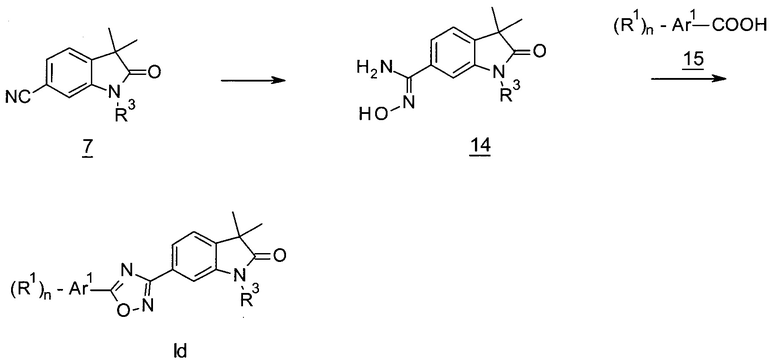
1,2,4-Оксадиазолы формулы Id (Схема 5) могут быть получены посредством взаимодействия нитрилов 7 с гидроксиламином с последующей конденсацией образовавшихся N-гидроксиамидинов 14 с кислотами 15, например, в присутствии карбонилдиимидазола.
Схема 6
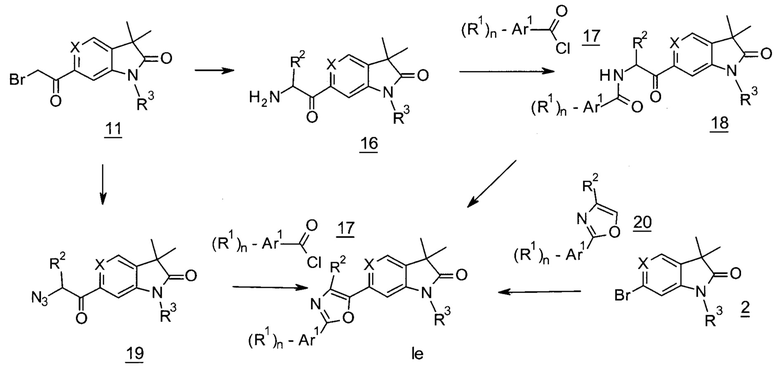
Оксазолы формулы Ie (X=СН) (Схема 6) могут быть получены посредством взаимодействия бромидов 11 с гексаметилентетрамином с получением аминометилкетонов 16, которые могут быть ацилированы с использованием хлорангидридов 17 с получением амидов 18. Циклизация 18 с (метоксикарбонилсульфамоил)триэтиламмония гидроксидом дает оксазолы Ie (X=СН). Альтернативно, оксазолы формулы Ie (X=СН) могут быть получены посредством замещения бромидов 11 с помощью азида натрия с последующим взаимодействием азида 19 с хлорангидридами 17 в присутствии трифенилфосфина. В третьем способе, бромид 2 (X=СН, R3=Н) может быть сначала защищен с помощью п-метоксибензилхлорида с получением 2 (X=СН, R3=РМВ), которое может быть связано с оксазолами 20 в присутствии трифенилфосфина, ферроцен-палладиевых катализаторов и карбоната серебра с последующей депротекцией с использованием ТФУ с получением оксазолов формулы Ie (X=СН). В четвертом способе, бромид 2 (X=N, R3 = циклопропил) может взаимодействовать с оксазолами 20 в присутствии палладиевого катализатора, например, диацетата палладия и фосфинового лиганда, например, 2-(дициклогексилфосфино)бифенила, и карбоната цезия с получением оксазолов Ie (X=N).
Схема 7
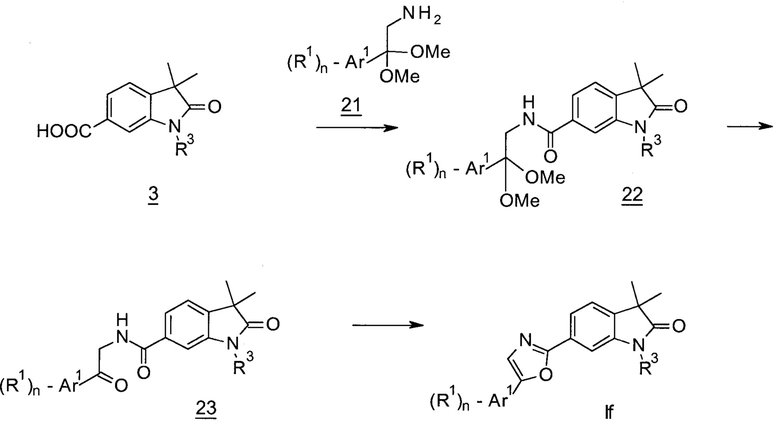
Оксазолы формулы If (Схема 7) могут быть получены с использованием в качестве исходного вещества кислот 3 (X=СН), которые могут быть активированы до промежуточных хлорангидридов с использованием тионилхлорида с последующим связыванием с амином 21 с получением амидацеталей 22. Депротекция ацетальной группы с использованием соляной кислоты и последующая циклизация образовавшихся кетонов 23 в присутствии (метоксикарбонилсульфамоил)триэтиламмония гидроксида дает оксазолы формулы If.
Схема 8
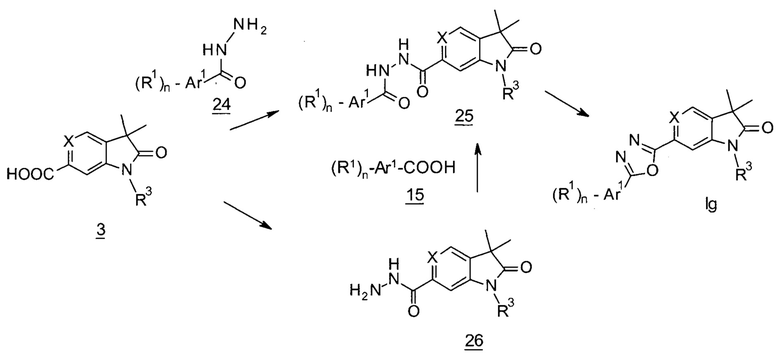
Оксадиазолы формулы Ig (X=СН) (Схема 8) могут быть получены с использованием в качестве исходного вещества кислот 3 (X=СН), которые могут взаимодействовать с гидразидами 24 в присутствии EDCI и 1Н-бензо[d][1,2,3]триазол-1-ола, приводя к ацетилгидразидам 25 (X=СН). Альтернативно, кислоты 3 (X=N) могут быть активированы до промежуточных хлорангидридов с использованием тионилхлорида с последующим взаимодействием с гидразином с получением гидразидов 26 (X=N), которые могут быть связаны с кислотами 15 с получением ацетилгидразидов 25 (X=N). Циклизация 25 с использованием п-толуолсульфонилхлорида приводит к оксадиазолам формулы Ig.
Схема 9
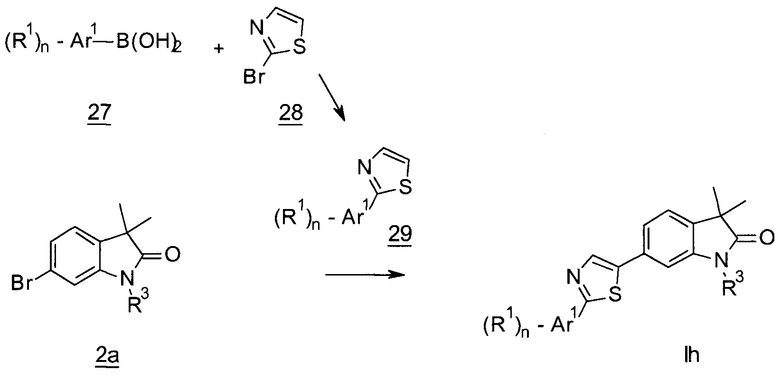
Тиазолы формулы In (Схема 9) могут быть получены посредством связывания бромидов 2а с замещенными тиазолами 29, в присутствии трифенилфосфина, ферроцен-палладиевых катализаторов и карбоната серебра. Замещенные тиазолы 29 могут быть получены связыванием по Сузуки бороновой кислоты 27 с бромтиазолом 28 в присутствии палладиевого катализатора, например, тетракис(трифенилфосфин)палладия(0).
Схема 10
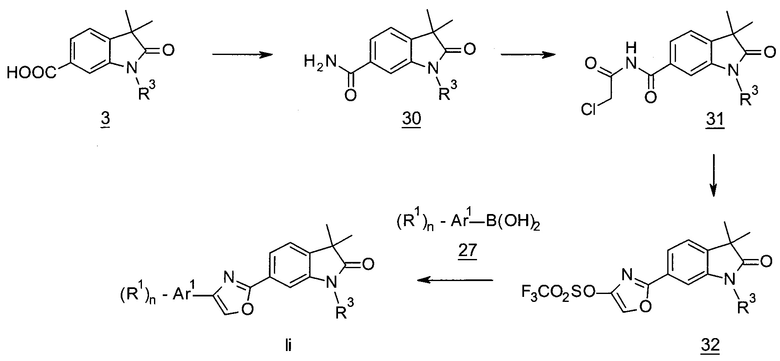
Оксазолы формулы Ii (Схема 10) могут быть получены превращением кислот 3 (X=СН) в образованные in situ хлорангидриды с последующим взаимодействием с аммонием с получением амидов 30, которые могут взаимодействовать с хлорацетилхлоридом с получением хлорметилкетонов 31. Превращение в оксазолтрифлаты 32 может быть проведено с помощью основания, например гидрида натрия с последующим взаимодействием с трифторметансульфоновым ангидридом в присутствии основания, например, триэтиламина. Связывание по Сузуки соединения 32 с бороновыми кислотами 27 в присутствии палладиевого катализатора, например, бис(трифенилфосфин)палладий(II)хлорида дает оксазолы формулы Ii.
Схема 11
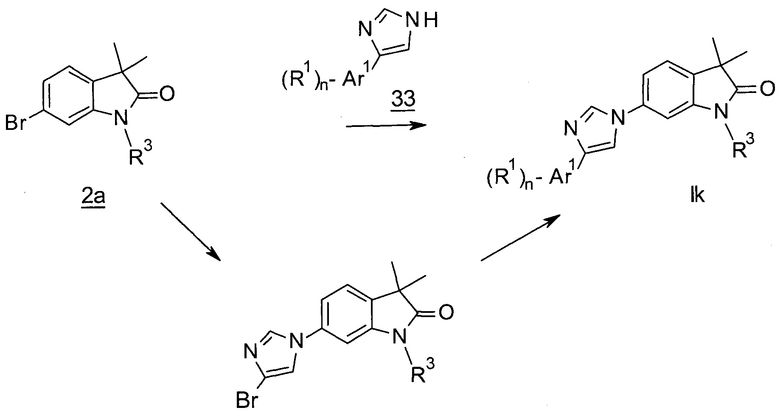
Имидазолы формулы Ik (Схема 11) могут быть получены связыванием бромидов 2а с замещенными имидазолами 33 в присутствии катализатора, например, хлорида меди(I) и 2-ацетилциклогексанона в N-метилпирролидоне. Замещенные имидазолы 33 известны и могут быть получены, например, в соответствии с Ganellin et al., J. Med. Chem. 38, 3342, 1995. Альтернативно, взаимодействие может быть проведено с получением 4-бромимидазола, который затем может быть арилирован с помощью соответствующих Аr1-бороновых кислот или эфиров Аr1-бороновоых кислот в присутствии основания, такого как карбонат калия или NaOtBu и катализатора, такого как PdCl2(PPh3)2 или палладацикл Brettphos с получением соединений формулы Ik.
Схема 12
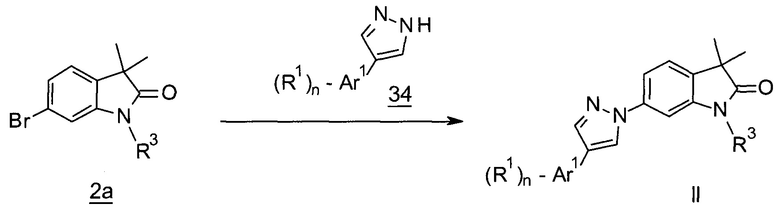
Пиразолы формулы Il (Схема 12) могут быть получены посредством связывания бромидов 2а с замещенными пиразолами 34 в присутствии катализатора, например хлорида меди(I) и L-пролина в ДМСО. Замещенные пиразолы 34 известны и могут быть получены, например, в соответствии с Bauer et al., J. Med. Chem. 11, 981, 1968.
Схема 13
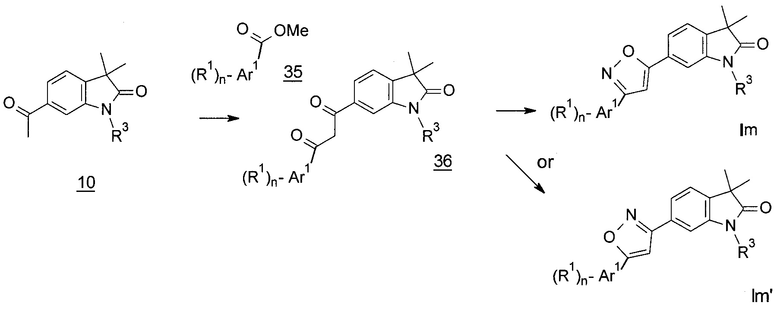
Изоксазолы формулы Im (Схема 13) могут быть получены посредством взаимодействия метилкетонов 10 с эфирами 35 в присутствии основания, например, гидрида натрия с получением дикетонов 36, которые могут быть циклизованы с гидроксиламином с получением изоксазолов Im и/или Im’.
Схема 14
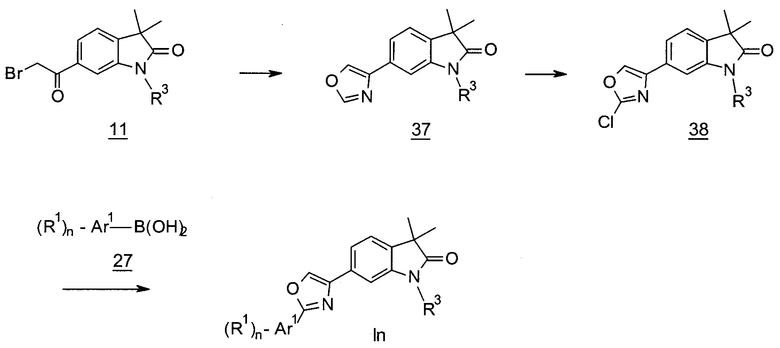
Оксазолы формулы In (Схема 14) могут быть получены посредством циклизации бромметилкетонов 11 с помощью гидроксиламина с получением оксазолов 37, которые могут быть хлорированы с использованием гексахлорэтана и основания, например, LiHMDS, с получением хлоро-оксазолов 38. Сочетание по Сузуки соединений 38 с бороновыми кислотами 27 в присутствии палладиевого катализатора, например, бис(трифенилфосфин)палладий(II)дихлорида дает оксазолы In.
Схема 15
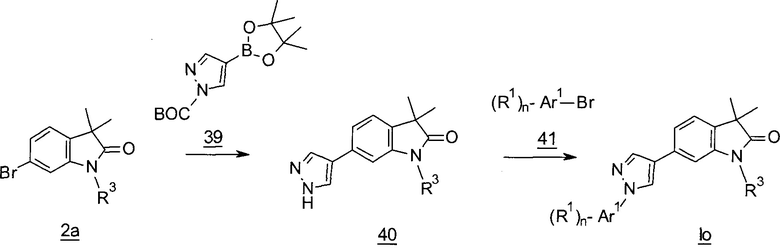
Пиразолы формулы Io (Схема 15) могут быть получены сочетанием по Сузуки бромидов 2а с бороновым эфиром 39 в присутствии палладиевого катализатора, например, [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия(II) с получением пиразолов 40, которые могут быть алкилированы с помощью бромидов 41 в присутствии йодида меди(I) и L-пролина в ДМСО с получением пиразолов формулы Iо.
Схема 16
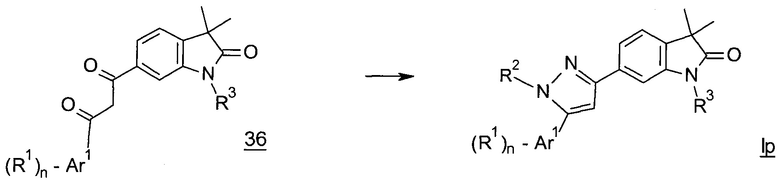
Имидазолы формулы Ip (Схема 16) могут быть получены из дикетонов 36 и гидразина в присутствии основания, например, DIPEA с получением имидазолов формулы Ip.
Схема 17
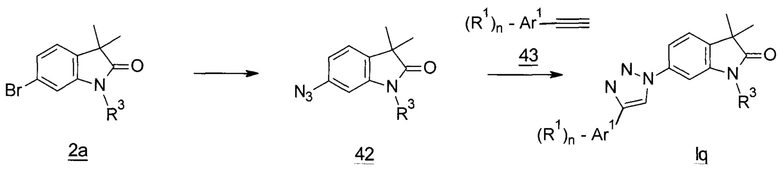
Триазолы формулы Iq (Схема 17) могут быть получены из бромидов 2а и азида, например, азида натрия, в присутствии натриевой соли аскорбиновой кислоты и транс-(1R,2R)-N,N'-бисметил-1,2-циклогександиамина с получением азидов 42. Циклизация соединений 42 может быть достигнута с помощью ацетиленов 43 в присутствии натриевой соли аскорбиновой кислоты и сульфата меди(II) в воде с получением триазолов формулы Iq.
Схема 18
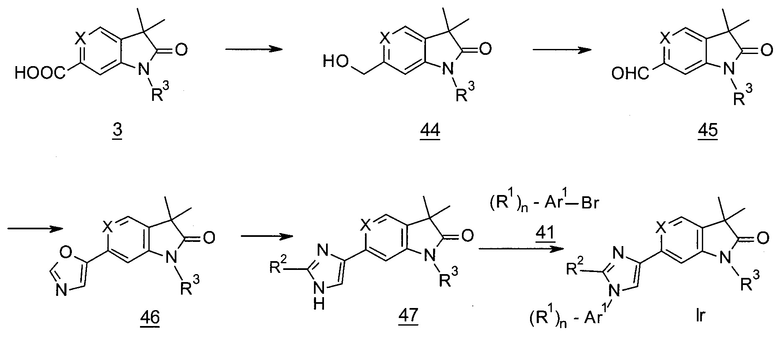
Имидазолы формулы Ir (Схема 18) могут быть получены из кислот 3 (X=СН) посредством восстановления с помощью, например, боран-тетрагидрофуранового комплекса с получением спиртов 44, которые могут быть окислены с помощью, например, диоксида марганца до альдегидов 45. Циклизация соединений 45 с помощью тозилметилизоцианида дает оксазолы 46, которые могут быть превращены в имидазолы 47 в присутствии формамида. Связывание соединений 47 с бромидами 41 в присутствии хлорида меди(I) и 2-ацетилциклогексанона в ДМСО дает имидазолы формулы Ir. Альтернативно, соединения формулы 47 могут взаимодействовать с 2- или 4-фторпиридинами или 2-хлорпиримидинами в присутствии карбоната цезия также с получением соединений формулы Ir.
Схема 19
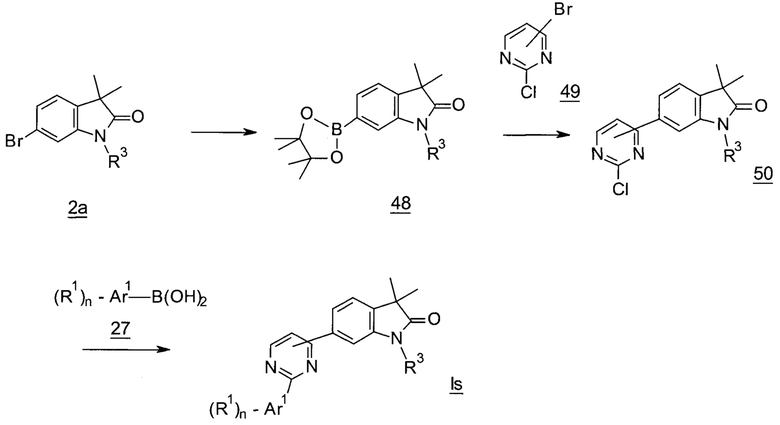
Пиримидины формулы Is (Схема 19) могут быть получены из бромидов 2а посредством взаимодействия с бис(пинаколато)дибором и палладиевым катализатором, например [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладием(II), с получением бороновых эфиров 48, которые могут быть связаны с 4-бромо-2-хлорпиримидином или 5-бромо-2-хлорпиримидином в присутствии [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия(II) с получением хлорпиримидинов 50. Связывание по Сузуки соединений 50 с бороновыми кислотами 27 в присутствии [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия(II) дает пиримидины формулы Is
Схема 20
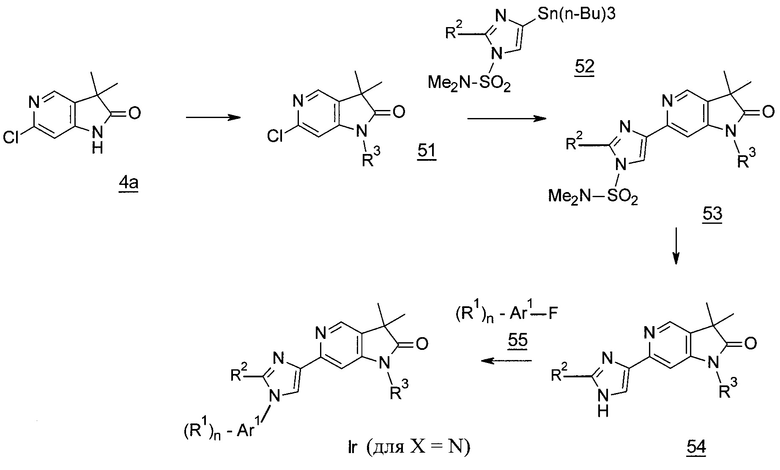
Имидазолы формулы Ir (Схема 20) могут быть получены из известного хлорпиридина 4а (Woolford et al., WO 2012143726), который может быть алкилирован с помощью бороновой кислоты, например, циклопропилбороновой кислоты, в присутствии ацетата меди(II) и основания, например, натрия бис(триметилсилил)амида, с получением алкилированных хлоро-пирролопиридинов 51, которые могут быть связаны с N,N-диметил-4-(трибутилстаннил)-1Н-имидазол-1-сульфонамидом (полученным в соответствии с Altenbach et al., J. Med. Chem. 51, 6571, 2008) и палладиевым катализатором, например тетракис(трифенилфосфин)палладий(0), с получением сульфонамидов 53. Отщепление сульфонамидной группы в соединении 53 может быть выполнено с помощью кислоты, например, водного раствора соляной кислоты, с получением имидазолов 54, которые могут быть связаны с ароматическим фторидом 55 и основанием, например, карбонатом цезия, с получением имидазолов формулы Ir.
Схема 21
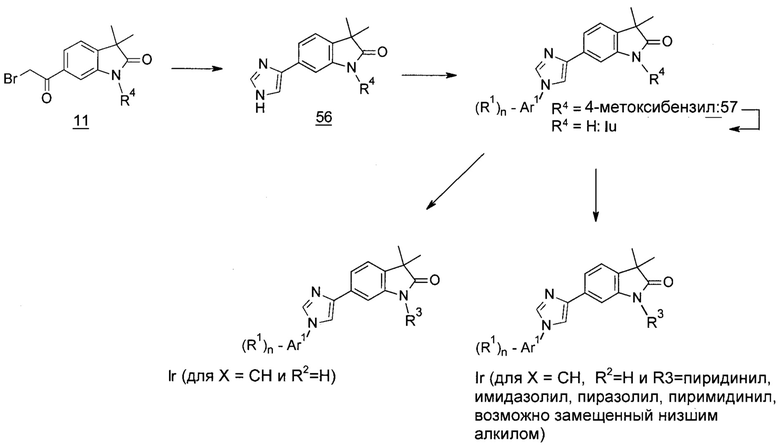
Альтернативно Схеме 18, соединения формулы 56 могут быть сразу получены из соединений формулы 11 посредством обработки формамидом. Это может дать соединения формулы 57 и Iu посредством способов, изображенных на Схеме 18. Соединения формулы 57 могут быть преобразованы в соединения формулы Iu посредством обработки с помощью ТФУ (Схема 21). Соединения формулы Iu могут быть трансформированы в соединения формулы Ir посредством взаимодействия с соответствующими гетероарилбромидами в присутствии основания, такого как карбонат кали, источника меди(I), такого как CuI, и подходящего лиганда, такого как N,N'-диметилэтилен-1,2-диамин.
Соединения формулы Ir могут быть получены посредством обработки соединений формулы Iu подходящим алкилирующим агентом в присутствии основания, такого как карбонат цезия.
Экспериментальная часть
Следующие примеры представлены для иллюстрации настоящего изобретения. Они не должны рассматриваться как ограничивающие объем изобретения, но скорее как представляющие его.
Аббревиатуры: DIPEA, диизопропилэтиламин; DMAP диметиламинопиридин; ДМФ, диметилформамид; ДМСО, диметилсульфоксид; EtOAc, этилацетат; HATU, O-(7-азабензотриазол-1-ил)-N,N,N,N'-тетраметилурония гексафторфосфат; LiHMDMS, лития гексаметилдисилазид; МеОН, метанол; РМВ, п-метоксибензил; TBAF, тетрабутиламмония фторид; ТВМЕ, трет-бутилметиловый эфир; ТФУ, трифторуксусная кислота; ТГФ, тетрагидрофуран.
Общие условия: хроматография на силикагеле проводилась либо с использованием картриджей, заполненных силикагелем (колонки ISOLUTE®, флеш-колонки TELOSTM), или силика-NН2 геля (флеш-колонки TELOSTM NH2) на ISCO Combi Flash Companion, или стеклянных колонок на силикагеле 60 (32-60 меш, 60 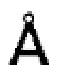 ). MS: масс-спектр (MS) измерялся с помощью метода положительного и негативного ионораспыления на оборудовании Perkin-Elmer SCIEX API 300.
). MS: масс-спектр (MS) измерялся с помощью метода положительного и негативного ионораспыления на оборудовании Perkin-Elmer SCIEX API 300.
Пример 1
1-циклопропил-6-(5-(4-фторфенил)-1Н-имидазол-2-ил)-3,3-диметилиндолин-2-он
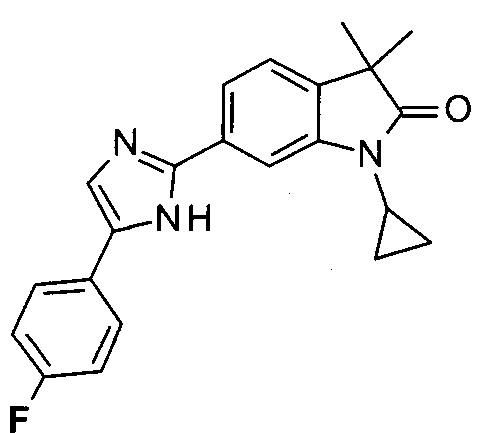
a) 6-бромо-3,3-диметил-индолин-2-он
К суспензии трет-бутилата калия (12.8 г) в безводном ТГФ (80 мл) добавили по порциям при 0°С 6-бромоиндолин-2-он (5.0 г) с последующим комплексом бромида меди(I) с диметилсульфидом (470 мг). Mel (6.82 г) добавили по каплям в течение 45 мин, поддерживая внутреннюю температуру ниже 8°С, смесь нагрели до 22°С и перемешивание продолжили в течение 16 часов. Смесь погасили при 0°С с помощью насыщенного водного раствора хлорида аммония и разбавили ТВМЕ и водой. Органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, EtOAc/н-гептан, 1:1) с получением соединения, указанного в заголовке (5.17 г), в виде коричневого осадка (5.17 г, 91%). MS ESI (m/z): 240.4/242.4 [(М+Н)+].
b) 6-бромо-1-циклопропил-3,3-диметилиндолин-2-он
К черной суспензии 6-бромо-3,3-диметилиндолин-2-она (7.0 г), циклопропилбороновой кислоты (5.01 г), DMAP (10.7 г) и ацетата меди(II) (5.56 г) в толуоле (400 мл) добавили раствор бис(триметилсилил)амида натрия в ТГФ (2 М, 15.3 мл) при барботировании смеси сухим воздухом, с последующим нагреванием до 95°С в течение 7 ч. Смесь разделили между водной HCl (2 М) и ТВМЕ, органический слой промыли водной HCI (2 М), высушили, выпарили и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 20% EtOAc в n-гептане) с получением соединения, указанного в заголовке (7.1 г, 87%), в виде красного осадка. MS (ESI, m/z): 280.4/282.4 [(М+Н)+].
c) 1-ииклопропил-3,3-диметил-2-оксоиндолин-6-карбонитрил
Суспензию 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она (2.0 г) в ДМФ (36 мл) продули аргоном, обработали дицианоцинком (1.04 г) и тетракис(трифенилфосфин)палладием(0) (825 мг) и перемешивание продолжили при 85°С в течение 16 ч.
Смесь эвапорировали, остаток разделили между водным карбонатом натрия (1 М) и EtOAc, органический слой промыли водным карбонатом натрия (1 М), высушили, выпарили и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 40% ЕtOAс в n-гептане) с получением соединения, указанного в заголовке (1.61 г, колич.), в виде светло-желтого осадка. MS (ESI, m/z): 227.5 [(М+Н)+].
d) 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксимидамид
В коричневый раствор лития бис(триметилсилил)амида в ТГФ (1 М, 8.2 m) и безводного диэтилового эфира (17 мл) добавили при 0°С за 3 порции 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбонитрил (900 мг) и перемешивание продолжили при 22°С в течение 21 ч. Смесь охладили до 0°С, обработали соляной кислотой (6 М, 4.0 мл) и перемешивание продолжили при 0°С в течение 40 мин и при 22°С в течение 5 ч. Смесь разделили между водой и диэтиловым эфиром, рН водного слоя довели до 14 с использованием твердого NaOH и экстрагировали дихлорметаном. Органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (537 мг, 56%), в виде серо-белого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 244.5 [(М+Н)+].
e) 1-циклопропил-6-(5-(4-фторфенил)-1Н-имидазол-2-ил)-3,3-диметилиндолин-2-он (Пример 1)
Смесь 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксимидамида (130 мг) и 2-бромо-1-(4-фторфенил)этанона (151 мг) в водном растворе гидрокарбоната натрия (1 М, 1.9 мл) и ТГФ (120 мл) нагревали до температуры кипения в течение 16 ч. Смесь эвапорировали, остаток разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 15% МеОН в дихлорметане), который затем подвергли второй хроматографии (Si-NH2, градиент, 0% до 70% EtOAc в n-гептане) с получением соединения, указанного в заголовке (121 мг, 63%), в виде белой пены. MS (ESI, m/z): 362.6 [(М+Н)+].
Пример 2
1,3,3-триметил-6-(5-фенил-1Н-имидазол-2-ил)индолин-2-он
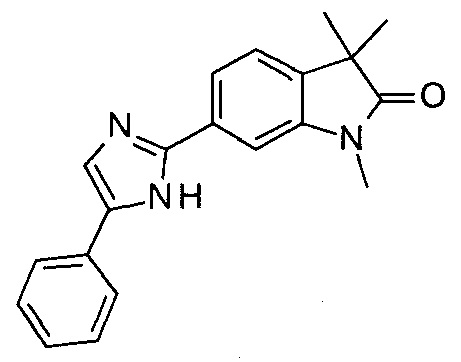
a) 6-бромо-1,3,3-триметилиндолин-2-он
В атмосфере аргона NaH (60% на минеральном масле, 7.32 г) суспендировали в безводном ТГФ (45 мл). Суспензию 6-бромоиндолин-2-она (10.0 г) в безводном ТГФ (108 мл) добавили по порциям в течение 10 мин, сохраняя температуру ниже 27°С. Реакционную смесь нагрели до 25°С, Mel (11.4 мл) добавили по каплям в течение 1 ч, при этом внутренняя температура осторожно поддерживалась между 24 и 27°С и перемешивание продолжили в течение 18 ч. Насыщенный водный раствор NH4Cl (20 мл) осторожно добавили при 10-15°С, смесь разбавили EtOAc и водным насыщенным раствором NaHCO3, органический слой промыли насыщенным водным раствором, высушили и эвапорировали. Остаток очистили с помощью флеш-хроматографии (силикагель, градиент, от 0% до 30% EtOAc в n-гептане) с получением соединения, указанного в заголовке (10.1 г, 84%) в виде светло-красного осадка. MS (ESI, m/z): 254.1/256.2 [(М+Н)+].
b) 1,3,3-триметил-6-(5-фенил-1Н-имидазол-2-ил)индолин-2-он (Пример 2)
6-бромо-1,3,3-триметилиндолин-2-он конвертировали по аналогии с примером 1с-е с использованием бромо-1-(фенил)этанона на стадии е с получением соединения, указанного в заголовке, в виде белого осадка. MS (ESI, m/z): 318.1 [(М+Н)+].
Пример 3
1,3,3-триметил-6-(2-(пиридин-4-ил)-1Н-имидазол-5-ил)индолин-2-он
a) 6-ацетил-1,3,3-триметилиндолин-2-он
Смесь 6-бромо-1,3,3-триметилиндолин-2-она (1.0 г) из примера 2а, 1,3-бис(дифенилфосфино)пропана (418 мг), ацетата палладия(II) (88 мг), N-бутилвинилового эфира (1.63 г) и карбоната калия (653 мг) в ДМФ (14 мл) и воде (1.4 мл) продули аргоном в течение 5 мин и нагревали в микроволновой печи при 120°С в течение 1 ч. Смесь обработали при 22°С водной соляной кислотой (2 н, 7.5 мл) и перемешивание продолжили в течение 3 ч. Смесь разделили между насыщенным водным гидрокарбонатом аммония и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в n-гептане) с получением соединения, указанного в заголовке (660 мг, 77%), в виде светло-желтого осадка. MS (ESI, m/z): 218.5 [(М+Н)+].
b) 6-(2-Бромоацетил)-1,3,3-триметилиндолин-2-он
К раствору 6-ацетил-1,3,3-триметилиндолин-2-она (660 мг) в ТГФ (20 мл) и МеОН (12 мл) добавили раствор тетра-н-бутиламмония трибромида (1.49 г) в ТГФ (7 мл) и перемешивание продолжили при 45°С в течение 17 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили дважды с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в n-гептане) с получением соединения, указанного в заголовке (646 мг, 72%), в виде светло-коричневой жидкости. MS (ESI, m/z): 296.3/298.3 [(М+Н)+].
с) 1,3,3-триметил-6-(2-(пиридин-4-ил)-1Н-имидазол-5-ил)индолин-2-он (Пример 3)
Смесь гидрохлорида изоникотинимидамида (511 мг) в водном растворе гидрокарбоната натрия (1 М, 4.3 мл) и ТГФ (225 мл) перемешивали при 22°С в течение 20 мин. Раствор 6-(2-бромоацетил)-1,3,3-триметилиндолин-2-она (320 мг) в ТГФ (16 мл) добавили и нагревали до температуры кипения в течение 22 ч. Смесь эвапорировали, остаток разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили дважды с помощью флеш-хроматографии (силикагель, градиент, 0% до 15% МеОН в дихлорметане, содержащем 1% NH3), с получением соединения, указанного в заголовке (168 мг, 48%), в виде светло-желтой пены. MS (ESI, m/z): 319.5 [(М+Н)+].
Пример 4
1-циклопропил-3,3-диметил-6-(3-(пиридин-4-ил)-1,2,4-оксадиазол-5-ил)индолин-2-он
a) Метил 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксилат
К раствору 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b (3.0 г), триэтиламин (2.18 г) в EtOAc (40 мл) и МеОН (40 мл) добавили 1,1'-бис(дифенилфосфино)ферроцен-палладий(II)дихлорид дихлорметановый аддукт (0.87 г) и смесь карбонилировали при 50 бар давления СО при 100°С в течение 48 ч. Смесь эвапорировали, и остаток очистили с помощью флеш-хроматографии (силикагель, EtOAc/н-гептан, 1:1) с получением соединения, указанного в заголовке (2.79 г, 91%), в виде черного осадка. MS (ESI, m/z): 260.5 [(М+Н)+].
b) 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоновая кислота
Смесь метил 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксилата (3.6 г) в МеОН (56 мл) и водном гидроксиде натрия (1 М, 56 мл) перемешивали при 22°С в течение 5 ч. Смесь разделили между водой и ТВМЕ, рН водного слоя довели до 1 с использованием водной соляной кислоты (25%), водный слой экстрагировали дихлорметаном, органический слой высушили и эвапорировали с получением соединения, указанного в заголовке (3.33 г, 98%), в виде светло-желтого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 246.5 [(М+Н)+].
c) 1-циклопропил-3,3-диметил-6-(3-(пиридин-4-ил)-1,2,4-оксадиазол-5-ил)индолин-2-он (Пример 4)
Раствор 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоновой кислоты (140 мг) и карбонилдиимидазола (111 мг) в безводном ТГФ (6 мл) нагревали до температуры кипения в течение 2 ч. 4-пиридиламидоксим (94 мг) добавили и перемешивание продолжили при кипении с обратным холодильником в течение 1.5 ч. Смесь эвапорировали, остаток растворили в уксусной кислоте (6 мл) и нагревали до температуры кипения в течение 1.5 ч и перемешивание продолжили при 22°С в течение 16 ч. Смесь эвапорировали, остаток разделили между водным карбонатом натрия (1 М) и дихлорметаном, органический слой промыли водным карбонатом натрия (1 М), высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в дихлорметане) с получением соединения, указанного в заголовке (189 мг, 96%), в виде белого осадка. MS (ESI, m/z): 347.5 [(М+Н)+].
Пример 5
1-циклопропил-3,3-диметил-6-(5-(пиридин-4-ил)-1,2,4-оксадиазол-3-ил)индолин-2-он
a) 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбонитрил
Суспензию 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b (2.0 г) в ДМФ (36 мл) продули аргоном, обработали дицианоцинком (1.04 г) и тетракис(трифенилфосфин)палладием(0) (825 мг) и перемешивание продолжили при 85°С в течение 16 ч.
Смесь эвапорировали, остаток разделили между водным карбонатом натрия (1 М) и EtOAc, органический слой промыли водным карбонатом натрия (1 М), высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 40% EtOAc в н-гептане) с получением соединения, указанного в заголовке (1.61 г, колич.), в виде светло-желтого осадка. MS (ESI, m/z): 227.5 [(М+Н)+].
b) (Z)-1-циклопропил-N'-гидрокси-3,3-диметил-2-оксоиндолин-6-карбоксимидамид
Смесь 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбонитрила (170 мг), гидрохлорида гидроксиламина (132 мг) и DIPEA (248 мг) в этаноле (1.5 мл) нагревали до 70°С в течение 4 ч и эвапорировали. Остаток разделили между водным карбонатом натрия (1 М) и EtOAc, органический слой промыли водным карбонатом натрия (1 М), высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (240 мг, са. 80% pure, 99%), в виде светло-зеленой пены, которую использовали без дополнительной очистки. MS (ESI, m/z): 260.5 [(М+Н)+].
с) 1-циклопропил-3,3-диметил-6-(5-(пиридин-4-ил)-1,2,4-оксадиазол-3-ил)индолин-2-он (Пример 5)
Раствор изоникотиновой кислоты (91 мг) и карбонилдиимидазола (130 мг) в безводном ТГФ (7.4 мл) нагревали до температуры кипения в течение 1.5 ч, (Z)-1-циклопропил-N'-гидрокси-3,3-диметил-2-оксоиндолин-6-карбоксимидамид (240 мг, 80% чистоты) добавили и нагревание продолжили в течение 1.5 ч. Смесь эвапорировали, остаток растворили в уксусной кислоте (7.4 мл) и нагревали до температуры кипения в течение 1 ч. Смесь эвапорировали, остаток разделили между водным карбонатом натрия (1 М) и EtOAc, органический слой промыли водным карбонатом натрия (1 М), высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 5% МеОН в дихлорметане) с получением соединения, указанного в заголовке (171 мг, 67%), в виде светло-желтого осадка. MS (ESI, m/z): 347.5 [(М+Н)+].
Пример 6
3,3-диметил-1-оксетан-3-ил-6-(3-пиридин-4-ил-[1,2,4]оксадиазол-5-ил)-1,3-дигидро-индол-2-он
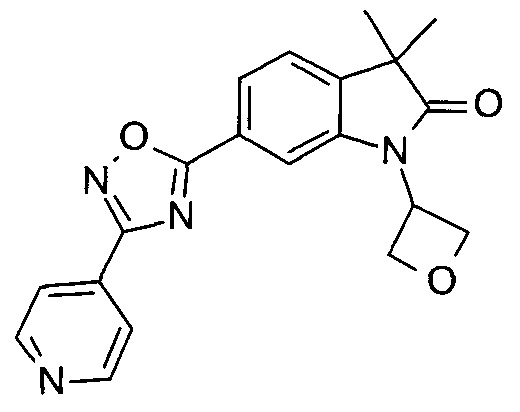
a) 6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он
Смесь 6-бромо-3,3-диметилиндолин-2-она из примера 1а (500 мг), 3-бромооксетана (594 мг) и карбоната цезия (1.36 г) в ДМФ (17 мл) продули аргоном в течение 5 мин и нагревали до 60°С в течение 18 ч. Смесь разделили между водной HCl (1 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в н-гептане) с получением соединения, указанного в заголовке (550 мг, 80%), в виде оранжевого воскообразного осадка. MS (ESI, m/z): 296.3/298.3 [(М+Н)+].
b) Метил 3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбоксилат
6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он конвертировали по аналогии с примером 4а с получением соединения, указанного в заголовке (97%), в виде вязкого коричневого масла. MS (ESI, m/z): 276.5 [(М+Н)+].
c) 3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбоновая кислота
Метил 3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбоксилат конвертировали по аналогии с примером 4b с получением соединения, указанного в заголовке (93%), в виде серо-белого осадка. MS (ESI, m/z): 262.5 [(М+Н)+].
d) 3,3-диметил-1-оксетан-3-ил-6-(3-пиридин-4-ил-[1,2,4]оксадиазол-5-ил)-1,3-дигидро-индол-2-он (Пример 6)
3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбоновую кислоту конвертировали по аналогии с примером 4с с получением соединения, указанного в заголовке (52%), в виде белого осадка. MS (ESI, m/z): 363.5 [(М+Н)+].
Пример 7
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
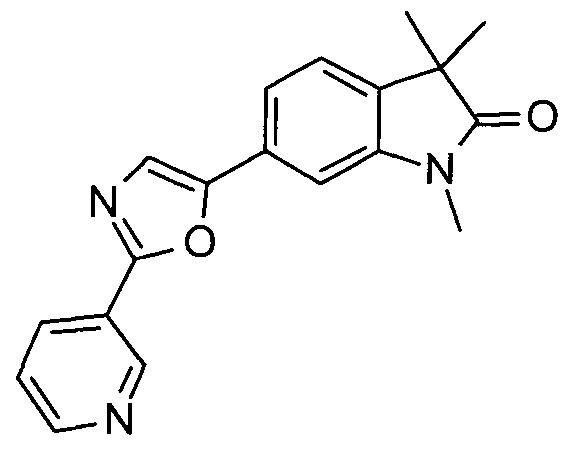
a) 2-оксо-2-(1,3,3-триметил-2-оксоиндолин-6-ил)этанаминия хлорид
Суспензию 6-(2-бромоацетил)-1,3,3-триметилиндолин-2-она из примера 3b (400 мг) и гексаметилентетрамина (189 мг) в толуоле (10 мл) нагревали до 40°С в течение 3 ч. Смесь отфильтровали и остаток промыли толуолом и диэтиловым эфиром. Осадок растворили в EtOH (10 мл) и соляной кислоте (25%, 3 мл), перемешивали при 22°С в течение 2 ч и эвапорировали с получением неочищенного соединения, указанного в заголовке (475 мг, колич.), в виде желтого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 233.5 [(М+Н)+].
b) N-(2-oкco-2-(1,3,3-триметил-2-оксоиндолин-6-ил)этил)никотинамид
К раствору гидрохлорида никотиноилхлорида (237 мг) и 2-оксо-2-(1,3,3-триметил-2-оксоиндолин-6-ил)этанаминия хлорида (470 мг) в дихлорметане (4 мл) добавили при 0°С DIPEA (740 мг) и перемешивание продолжили при 22°С в течение 2 ч. Смесь разделили между водой и EtOAc, органический слой высушили и эвапорировали с получением соединения, указанного в заголовке (333 мг, 77%), в виде светло-коричневой пены, которую использовали без дополнительной очистки. MS (ESI, m/z): 338.5 [(М+Н)+].
с) 1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он (Пример 7)
Смесь N-(2-оксо-2-(1,3,3-триметил-2-оксоиндолин-6-ил)этил)никотинамида (330 мг) и (метоксикарбонилсульфамоил)триэтиламмония гидроксида (699 мг) в ТГФ (8 мл) нагревали в микроволновой печи при 100°С в течение 20 мин. Раствор эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (140 мг, 55%), в виде светло-коричневой пены. MS (ESI, m/z): 320.5 [(М+Н)+].
Пример 8
1-циклопропил-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
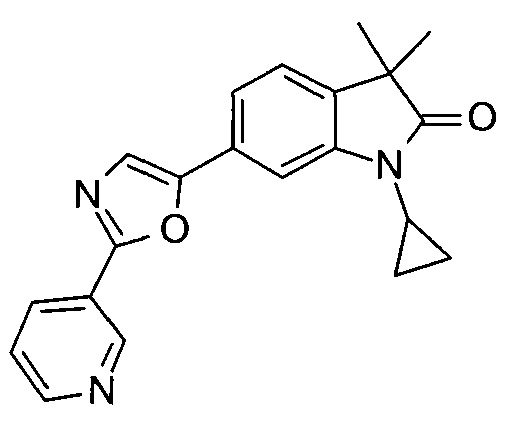
6-бромо-1-циклопропил-3,3-диметил индол ин-2-он из примера 1b конвертировали по аналогии с примером 3а-b в 6-(2-бромоацетил)-1-циклопропил-3,3-диметил-индолин-2-он, который конвертировали по аналогии с примером 7а-с с получением соединения, указанного в заголовке, в виде светло-желтого осадка. MS (ESI, m/z): 346.5 [(М+Н)+].
Пример 9
1-циклопропил-3,3-диметил-6-(5-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
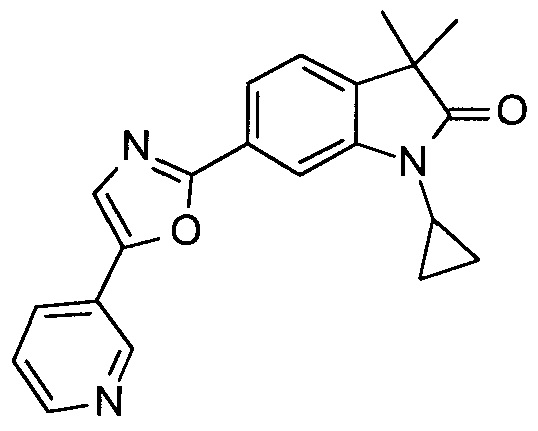
а) 1-ииклопропил-N-(2,2-диметокси-2-(пиридин-3-ил)этил)-3,3-диметил-2-оксоиндолин-6-карбоксамид
Раствор 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоновой кислоты (150 мг) из примера 4b, тионилхлорида (109 мг) и ДМФ (9 мг) в толуоле (2 мл) нагревали до 110°С в течение 3 ч. Смесь эвапорировали, остаток разбавили дихлорметаном (2 мл), обработали при 22°С 2,2-диметокси-2-(пиридин-3-ил)этанамина дигидрохлоридом (203 мг, полученный в соответствии с Bouchet et al., WO 2000002875), с последующим добавлением DIPEA (592 мг) и перемешивание продолжили в течение 22°С. Реакционную смесь разделили между водным карбонатом натрия и дихлорметаном, органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (260 мг, колич.) в виде вязкого масла, которое использовали без дополнительной очистки. MS (ESI, m/z): 410.6 [(М+Н)+].
b) 1-циклопропил-3,3-диметил-2-оксо-N-(2-оксо-2-(пиридин-3-ил)этил)индолин-6-карбоксамид
Раствор 1-циклопропил-N-(2,2-диметокси-2-(пиридин-3-ил)этил)-3,3-диметил-2-оксоиндолин-6-карбоксамида (260 мг) в соляной кислоте (37%, 5 мл) перемешивали при 22°С в течение 2 ч. Смесь разделили между водным раствором карбоната натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 7% МеОН в дихлорметане) с получением соединения, указанного в заголовке (110 мг, 48%), в виде белой пены. MS (ESI, m/z): 364.6 [(М+Н)+].
c) 1-циклопропил-3,3-диметил-6-(5-(пиридин-3-ил)оксазол-2-ил)индолин-2-он (Пример 9)
Смесь 1-циклопропил-3,3-диметил-2-оксо-N-(2-оксо-2-(пиридин-3-ил)этил)индолин-6-карбоксамида (110 мг) и (метоксикарбонилсульфамоил)триэтиламмония гидроксида (216 мг) в ТГФ (3 мл) нагревали в микроволновой печи при 100°С в течение 20 мин. Раствор эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (55 мг, 53%), в виде светло-желтого осадка. MS (ESI, m/z): 346.5 [(М+H)+].
Пример 10
1-циклопропил-3,3-диметил-6-(2-(пиридин-4-ил)оксазол-5-ил)индолин-2-он
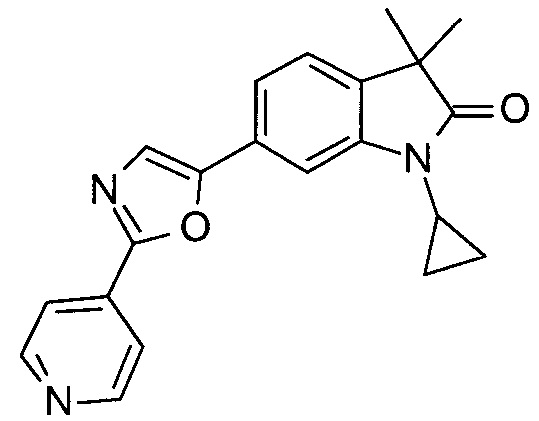
Пример 10 получили по аналогии с примером 8 с использованием пиридин-4-карбонилхлорида с получением соединения, указанного в заголовке, в виде желтого вязкого масла. MS (ESI, m/z): 346.5 [(М+Н)+].
Пример 11
3,3-диметил-1-(оксетан-3-ил)-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
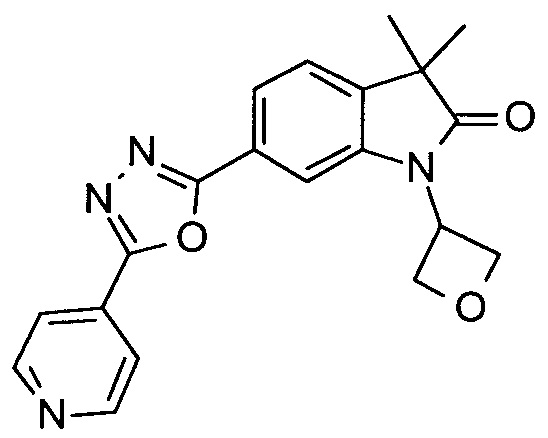
a) N'-Изоникотиноил-3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбогидразид
К раствору 3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбоновой кислоты (170 мг) из примера 6 с, 1Н-бензо[d][1,2,3]триазол-1-ола (141 мг), N1-((этилимино)метилен)-N3,N3-диметилпропан-1,3-диамина гидрохлорида (200 мг) и триэтиламина (165 мг) в дихлорметане (10 мл) добавили изоникотиногидразид (125 мг) и перемешивание продолжили при 22°С в течение 19 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 15% МеОН в дихлорметане с 1% NH3) с получением соединения, указанного в заголовке (150 мг, 59%), в виде белого осадка. MS (ESI, m/z): 381.5 [(М+Н)+].
b) 3,3-диметил-1-(оксетан-3-ил)-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он (Пример 11)
К раствору N'-изоникотиноил-3,3-диметил-1-(оксетан-3-ил)-2-оксоиндолин-6-карбогидразида (150 мг) и п-толуолсульфонилхлорида (142 мг) в ацетонитриле (6 мл) добавили триэтиламин (150 мг) и перемешивание продолжили при 22°С в течение 4 ч. Смесь разделили между водным раствором гидрокарбоната натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (141 мг, 97%), в виде белого осадка. MS (ESI, m/z): 363.5 [(М+Н)+].
Пример 12
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
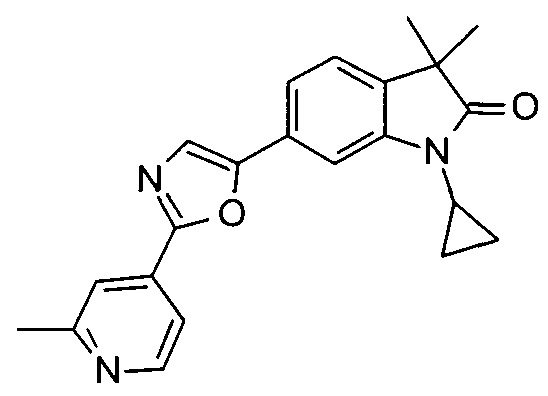
Пример 12 получили по аналогии с примером 10 с использованием 2-метилпиридин-4-карбонилхлорида с получением соединения, указанного в заголовке, в виде в виде светло-желтой пены. MS (ESI, m/z): 360.5 [(М+Н)+].
Пример 13
1,3,3-триметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
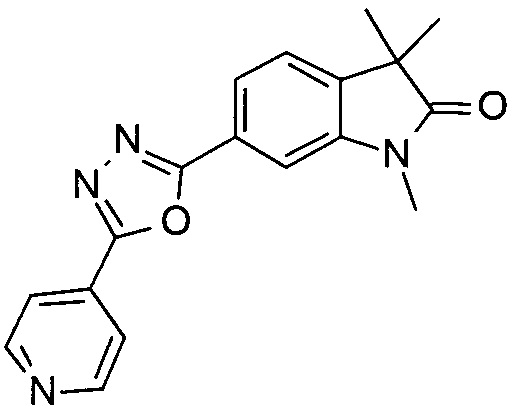
а) 1,3,3-триметил-2-оксоиндолин-6-карбоновая кислота
К суспензии NaH (12.6 г) в ТГФ (260 мл) добавили при 22°С метил 2-оксоиндолин-6-карбоксилат (15.0 г) в течение 30 мин, после чего добавили Mel (44.5 г) с использованием шприцевой помпы в течение 80 мин, поддерживая температуру между 24-28°С и перемешивание продолжили в течение 2.5 ч. Раствор NaOH (6.3 г) в воде (20 мл) добавили и перемешивание продолжили в течение 1 ч. Смесь разделили между водой и ТВМЕ, рН водного слоя довели до 1, суспензию отфильтровали и остаток высушили с получением соединения, указанного в заголовке (16.0 г, 93%), в виде коричневого осадка.
b) N'-Изоникотиноил-1,3,3-триметил-2-оксоиндолин-6-карбогидразид
1,3,3-триметил-2-оксоиндолин-6-карбоновую кислоту конвертировали по аналогии с примером 11а с получением соединения, указанного в заголовке (93%), в виде светло-желтой пены. MS (ESI, m/z): 339.5 [(М+Н)+].
c) 1,3,3-триметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он (Пример 13)
N'-Изоникотиноил-1,3,3-триметил-2-оксоиндолин-6-карбогидразид конвертировали по аналогии с примером 11b с получением соединения, указанного в заголовке (84%), в виде серо-белого осадка. MS (ESI, m/z): 321.5 [(М+Н)+].
Пример 14
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он
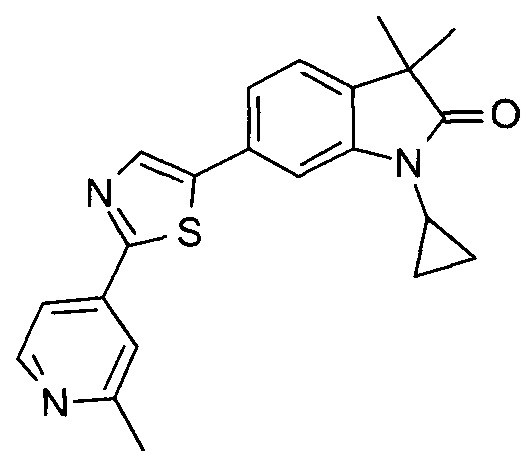
a) 2-(2-Метилпиридин-4-ил)тиазол
Аргон барботировали через смесь 2-метилпиридин-4-илбороновой кислоты (614 мг), 2-бромтиазола (736 мг) и водного карбоната натрия (2 М, 4.5 мл) в диоксане (8 мл), после чего добавили тетракис(трифенилфосфин)палладий(0) (259 мг) и смесь нагревали до 90°С в течение 16 ч. Реакционную смесь отфильтровали через дикалит, фильтрат разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 30% до 50% EtOAc в н-гептане) с получением соединения, указанного в заголовке (325 мг, 41%), в виде светло-коричневого осадка. MS (ESI, m/z): 177.5 [(М+Н)+].
b) 1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он (Пример 14)
Смесь 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она (220 мг), 2-(2-метилпиридин-4-ил)тиазола (152 мг), трифенилфосфина (21 мг), 1,1'-бис(дифенилфосфино)ферроцен-палладий(II)дихлорид дихлорметанового аддукта (32 мг), и карбоната серебра (433 мг), в воде (5 мл) нагревали до 90°С в течение 4 д. Реакционную смесь отфильтровали через дикалит, фильтрат разделили между солевым раствором и дихлорметаном, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 40% до 60% EtOAc в н-гептане). Фракцию, содержащую соединение, эвапорировали, остаток разделили между водной соляной кислотой и EtOAc, рН водного слоя довели до 9 с использованием водного гидроксида натрия и водный слой экстрагировали дихлорметаном. Органический слой высушили и эвапорировали с получением соединения, указанного в заголовке (126 мг, 43%), в виде желтого вязкого масла. MS (ESI, m/z): 376.6 [(М+Н)+].
Пример 15
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
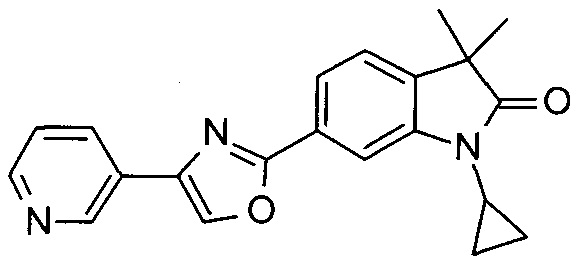
a) 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксамид
К суспензии 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоновой кислоты (1.2 г) из примера 4b в толуоле (11 мл) добавили тионилхлорид (698 мг) и ДМФ (36 мг) и перемешивание продолжили при температуре кипения в течение 2 ч. Смесь эвапорировали, остаток растворили в дихлорметане (27 мл), добавили водный аммоний (25%, 18 мл) и смесь интенсивно перемешивали при 22°С в течение 2 дней. Смесь разделили между водным карбонатом натрия (1 М) и дихлорметаном, органический слой высушили и эвапорировали с получением соединения, указанного в заголовке (1.17 г, 98%), в виде белого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 245.5 [(М+Н)+].
b) N-(2-Хлорацетил)-1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксамид
Суспензию 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксамида (1.17 г) и хлорацетилхлорида (2.76 г) нагревали до 110°С в течение 1 ч. Смесь очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (1.18 г, 77%), в виде белого осадка. MS (ESI, m/z): 321.5 [(М+Н)+].
c) 2-(1-циклопропил-3,3-диметил-2-оксоиндолин-6-ил)оксазол-4-ила трифторметансульфонат
К суспензии гидрида натрия (174 мг) в 1,4-диоксане (30 мл) добавили при 22°С раствор N-(2-хлорацетил)-1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоксамида (1.16 г) в 1,4-диоксане (30 мл) и перемешивание продолжили при температуре кипения в течение 0.5 ч и при 22°С в течение 1 ч. Смесь отфильтровали, фильтрат эвапорировали и остаток растворили в дихлорметане (15 мл). К раствору добавили при -78°С триэтиламин (732 мг) с последующим трифторметансульфоновым ангидридом (1.53 г) и перемешивание продолжили при 22°С в течение 30 мин. Раствор разделили между насыщенным гидрокарбонатом натрия и дихлорметаном, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (600 мг, 40%), в виде белого осадка. MS (ESI, m/z): 417.5 [(М+Н)+].
d) 1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он (Пример 15)
Смесь 2-(1-циклопропил-3,3-диметил-2-оксоиндолин-6-ил)оксазол-4-ила трифторметансульфоната (200 мг), пиридин-3-илбороновой кислоты (65 мг) и водного карбоната натрия (1 М, 0.7 мл) в 1,4-диоксане (7 мл) дегазировали аргоном, бис(трифенилфосфин)палладий(II)хлорид (17 мг) добавили и смесь нагревали в микроволновой печи до 150°С в течение 20 мин. Раствор отфильтровали через дикалит, фильтрат эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с последующей препаративной ВЭЖХ очисткой (RP-18, градиент, ацетонитрил/вода) с получением соединения, указанного в заголовке (98 мг, 54%), в виде белого осадка. MS (ESI, m/z): 346.6 [(М+Н)+].
Пример 16
1-циклопропил-3,3-диметил-6-(4-(пиридин-4-ил)оксазол-2-ил)индолин-2-он
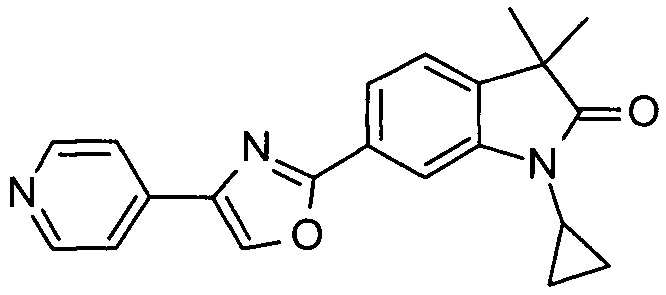
Пример 16 получили по аналогии с примером 15 с использованием пиридин-4-илбороновой кислоты с получением соединения, указанного в заголовке, в виде белого осадка. MS (ESI, m/z): 346.5 [(М+Н)+].
Пример 17
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
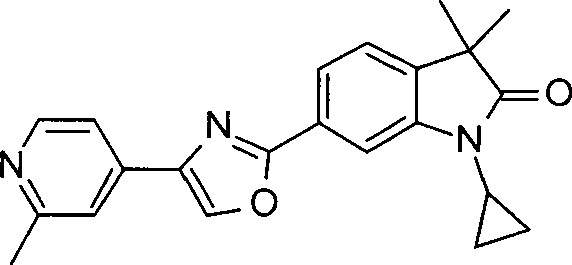
Пример 17 получили по аналогии с примером 15 с использованием 2-метилпиридин-4-илбороновой кислоты с получением соединения, указанного в заголовке, в виде белого осадка. MS (ESI, m/z): 360.6 [(М+Н)+].
Пример 18
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)тиазол-5-ил)индолин-2-он
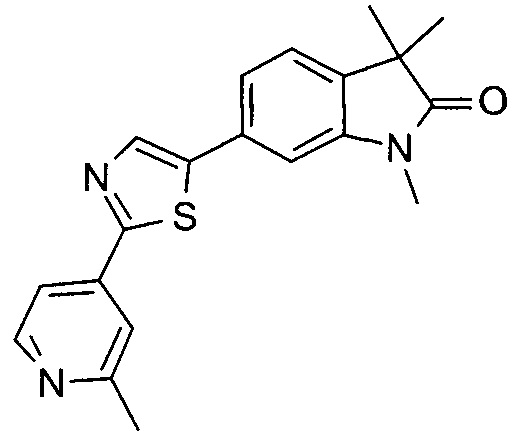
Пример 18 получили по аналогии с примером 14 с использованием в качестве исходного вещества 6-бромо-1,3,3-триметилиндолин-2-она из примера 2а с получением соединения, указанного в заголовке, в виде желтой пены. MS (ESI, m/z): 350.5 [(М+Н)+].
Пример 19
1-циклопропил-3,3-диметил-6-(5-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
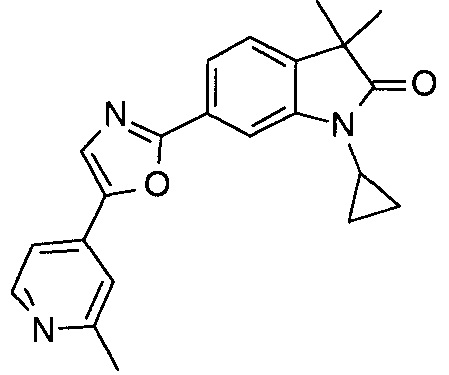
Пример 19 получили по аналогии с примером 9 с использованием 2,2-диметокси-2-(2-метилпиридин-4-ил)этанамина с получением соединения, указанного в заголовке, в виде светло-желтого осадка. MS (ESI, m/z): 360.6 [(М+Н)+].
Пример 20
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
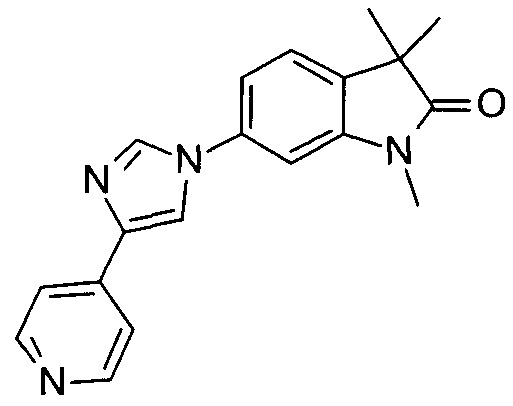
Суспензию 6-бромо-1,3,3-триметилиндолин-2-она из примера 2а (110 мг), 4-(1Н-имидазол-4-ил)пиридина гидрохлорид (79 мг, полученный в соответствии с Ganellin et al., J. Med. Chem. 38, 3342, 1995), карбоната калия (188 мг) и 2-ацетилциклогексанона (30 мг) в N-метилпирролидоне (1.0 мл) продули аргоном в течение 5 мин, затем добавили хлорид меди(I) (9 мг) и смесь нагревали при 130°С в течение 36 ч. Смесь разделили между насыщенным гидрокарбонатом натрия и ЕtOАс, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 15% МеОН в дихлорметане). Фракцию, содержащую соединение, эвапорировали и остаток тритурировали с диэтиловым эфиром и высушили с получением соединения, указанного в заголовке (100 мг, 73%), в виде серо-белого осадка. MS (ESI, m/z): 319.2 [(М+Н)+].
Пример 21
1,3,3-триметил-6-(4-(пиридин-3-ил)оксазол-2-ил)индолин-2-он
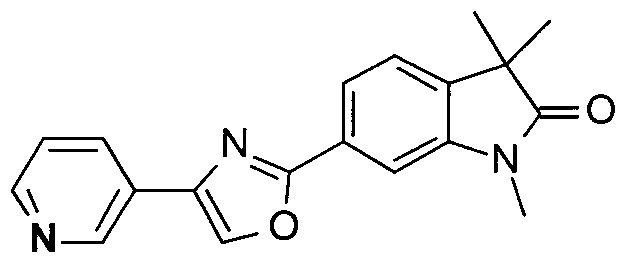
Пример 21 получили по аналогии с примером 15 с использованием в качестве исходного вещества 1,3,3-триметил-2-оксоиндолин-6-карбоновой кислоты из примера 13а с получением соединения, указанного в заголовке, в виде белого осадка. MS (ESI, m/z): 320.6 [(М+Н)+].
Пример 22
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
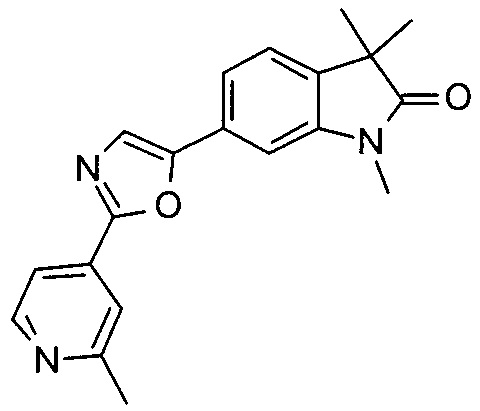
a) 2-(2-Метилпиридин-4-ил)оксазол
К раствору оксазола (201 мг) в ТГФ (3 мл) добавили при -78°С BuLi (1.6 М в гексане, 2.2 мл), с последующим добавлением хлорида цинка (2 М в 2-метилтетрагидрофуране, 2.9 мл) и перемешивание продолжили при 22°С в течение 30 мин. 4-бромо-2-метилпиридин (0.50 г) и тетракис(трифенилфосфин)палладий(0) (336 мг) добавили и перемешивание продолжили при 60°С в течение 5 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 40% до 60% EtOAc в н-гептане) с получением соединения, указанного в заголовке (295 мг, 63%) в виде желтого осадка. MS (ESI, m/z): 161.5 [(М+Н)+].
b) 1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он (Пример 22)
6-бромо-1,3,3-триметилиндолин-2-он из примера 2а взаимодействовал с 2-(2-метилпиридин-4-ил)оксазолом по аналогии с примером 14b с получением соединения, указанного в заголовке, в виде серо-белой пены. MS (ESI, m/z): 334.5 [(М+Н)+].
Пример 23
3,3-диметил-1-(оксетан-3-ил)-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
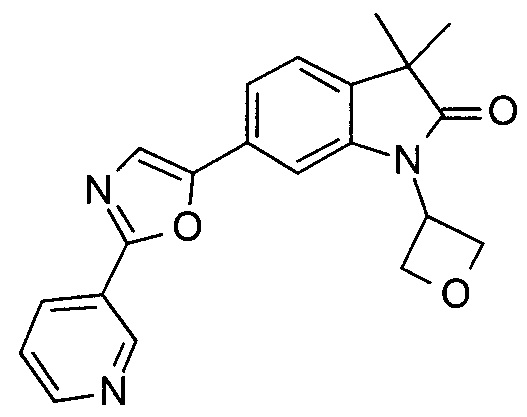
a) 2-(Пиридин-3-ил)оксазол
Оксазол связали с 3-бромопиридином по аналогии с примером 22а с получением соединения, указанного в заголовке (53%), в виде светло-желтого осадка. MS (ESI, m/z): 147.2 [(М+Н)+].
b) 3,3-диметил-1-(оксетан-3-ил)-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он (Пример 23)
6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он из примера 6а взаимодействовал с 2-(пиридин-3-ил)оксазолом по аналогии с примером 14b с получением соединения, указанного в заголовке (31%), в виде белой пены. MS (ESI, m/z): 362.6 [(М+Н)+].
Пример 24
3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)-1-(оксетан-3-ил)индолин-2-он
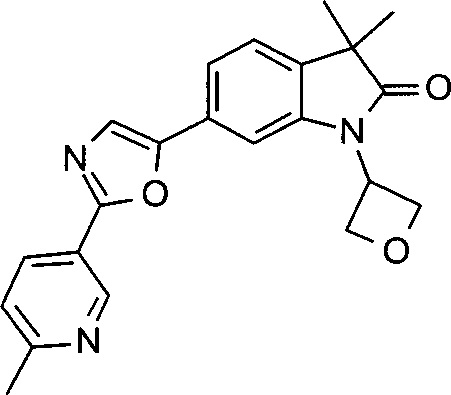
a) 2-(6-Метилпиридин-3-ил)оксазол
Оксазол связали с 5-бромо-2-метилпиридином по аналогии с примером 22а с получением соединения, указанного в заголовке (59%), в виде светло-желтого осадка. MS (ESI, m/z): 161.5 [(М+Н)+].
b) 3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)-1-(оксетан-3-ил)индолин-2-он (Пример 24)
6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он из примера 6а взаимодействовал с 2-(6-метилпиридин-3-ил)оксазолом по аналогии с примером 14b с получением соединения, указанного в заголовке (24%), в виде белого осадка. MS (ESI, m/z): 376.5 [(М+Н)+].
Пример 25
3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
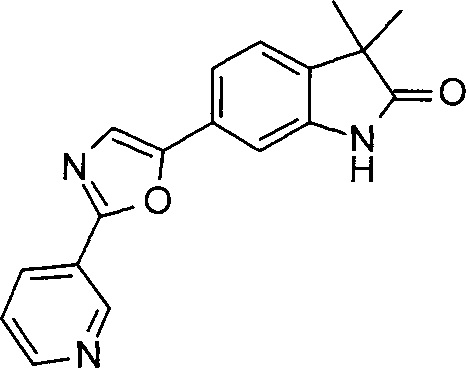
a) 6-бромо-1-(4-метоксибензил)-3,3-диметилиндолин-2-он
Смесь 6-бромо-3,3-диметилиндолин-2-она из примера 1а (250 мг) в ДМФ (8 мл) продули аргоном. 1-(Бромометил)-4-метоксибензол (209 мг) и карбонат цезия (679 мг) добавили и перемешивание продолжили при 80°С в течение 1 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в н-гептане) с получением соединения, указанного в заголовке (340 мг, 91%), в виде красной жидкости. MS (ESI, m/z): 360.0/362.5 [(М+Н)+].
b) 1-(4-Метоксибензил)-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
6-бромо-1-(4-метоксибензил)-3,3-диметилиндолин-2-он взаимодействовал с 2-(пиридин-3-ил)оксазолом из примера 23а по аналогии с примером 14b с получением соединения, указанного в заголовке (58%), в виде желтого осадка. MS (ESI, m/z): 426.7 [(М+Н)+].
c) 3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он (Пример 25)
Раствор 1-(4-метоксибензил)-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-она (112 мг) в ТФУ (1 мл) нагрели до 110°С в течение 2 дней. Смесь разделили между водным карбонатом натрия (2 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 50% до 80% EtOAc в н-гептане). Фракцию, содержащую соединение, эвапорировали, остаток разделили между водной соляной кислотой и EtOAc, рН водного слоя довели до 9 с использованием водного гидроксида натрия, и водный слой экстрагировали дихлорметаном. Органический слой высушили и эвапорировали с получением соединения, указанного в заголовке (42 мг, 52%), в виде серо-белого осадка. MS (ESI, m/z): 306.5 [(М+Н)+].
Пример 26
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)-1-(оксетан-3-и л)индол и н-2-он
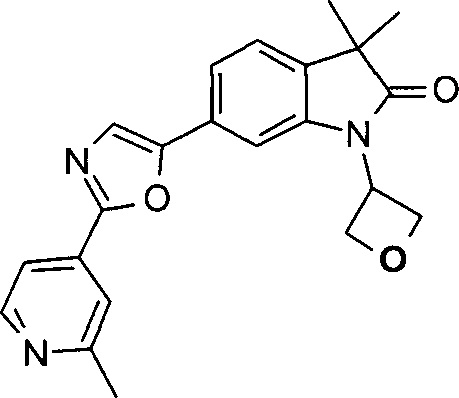
6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он из примера 6а взаимодействовал с 2-(2-метилпиридин-4-ил)оксазолом из примера 22а по аналогии с примером 14b с получением соединения, указанного в заголовке (30%), в виде желтой пены. MS (ESI, m/z): 376.6 [(М+Н)+].
Пример 27
3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
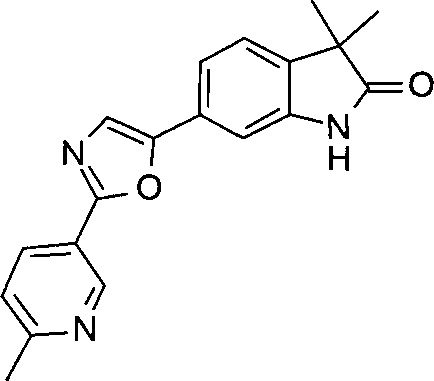
Пример 27 получили по аналогии с примером 25 с использованием 2-(6-метилпиридин-3-ил)оксазола из Примера 24а с получением соединения, указанного в заголовке, в виде коричневого осадка. MS (ESI, m/z): 320.6 [(М+Н)+].
Пример 28
1-(2-Гидроксиэтил)-3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
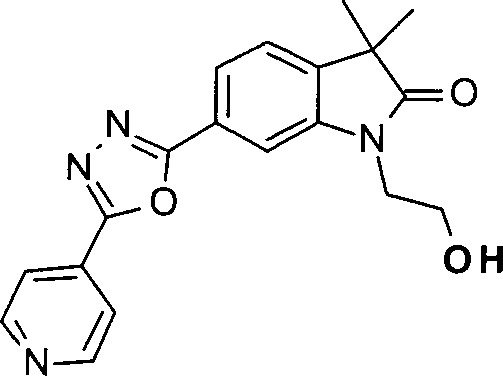
a) 3,3-диметил-2-оксоиндолин-6-карбоновая кислота
К раствору метил 2-оксоиндолин-6-карбоксилата (17.6 г) в ДМФ (260 мл) добавили Mel (26.1 г) с последующим NaH (3.68 г), поддерживая температуру при 22°С. Через 30 мин вторую порцию NaH (1.84 г) добавили с последующей через 1 ч третьей порцией (1.84 г) и перемешивание продолжили при 22°С в течение 16 ч. Воду (7 мл) с последующим гидроксидом натрия (34.5 г) добавили и перемешивание продолжили при 45°С в течение 1 ч и при 22°С в течение 16 ч. Смесь разделили между ТВМЕ и водой, рН водного слоя довели до 3 с использованием водной соляной кислоты (25%) и экстрагировали дихлорметаном. Органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (17.9 г, 95%), в виде красного осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 204.2 [(М-Н)-].
b) 3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
3,3-диметил-2-оксоиндолин-6-карбоновую кислоту конвертировали в соединение, указанное в заголовке (36%), по аналогии с примером 11а-b, и получили в виде оранжевого осадка. MS (ESI, m/z): 307.6 [(М+Н)+].
c) 1-(2-(Трет-бутилдиметилсилилокси)этил)-3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
Смесь 3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-она (171 мг) в ДМФ (2.5 мл) продули аргоном, затем обработали (2-бромэтокси)(трет-бутил)диметилсиланом (267 мг) и карбонатом цезия (364 мг) и перемешивание продолжили при 80°С в течение 16 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 20% MeOH/NH4OH в дихлорметане) с получением загрязненного соединения, указанного в заголовке (307 мг), в виде коричневого осадка, который затем использовали без дополнительной очистки. MS (ESI, m/z): 465.7 [(М+Н)+].
d) 1-(2-Гидроксиэтил)-3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он (Пример 28)
К раствору 1-(2-(трет-бутилдиметилсилилокси)этил)-3,3-диметил-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-она (307 мг) в ТГФ (13 мл) добавили при 0°С TBAF (136 мг) и перемешивание продолжили при 0°С в течение 10 мин и при 22°С в течение 3 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 20% MeOH/NH4OH в дихлорметане) с получением соединения, указанного в заголовке (137 мг, 75%), в виде светло-желтого осадка. MS (ESI, m/z): 351.6 [(М+Н)+].
Пример 29
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
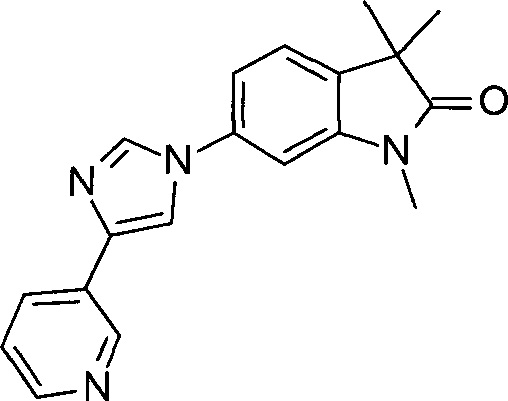
Пример 29 получили по аналогии с примером 20 с использованием 3-(1Н-имидазол-4-ил)пиридина (полученный в соответствии с Denton et al., J. Med. Chem., 48, 224, 2005) с получением соединения, указанного в заголовке (38%), в виде светло-желтого осадка. MS (ESI, m/z): 319.6 [(М+Н)+].
Пример 30
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
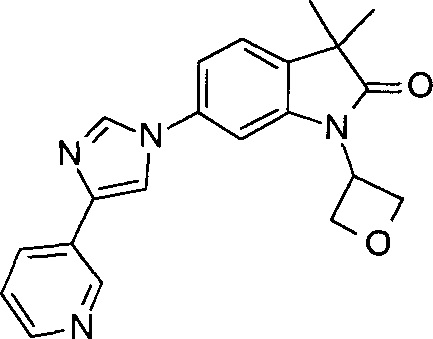
Пример 30 получили по аналогии с примером 20 с использованием 6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-она из примера 6а и 3-(1Н-имидазол-4-ил)пиридина (полученный в соответствии с Denton et al., J. Med. Chem., 48, 224, 2005) с получением соединения, указанного в заголовке (36%), в виде белого осадка. MS (ESI, m/z): 361.6 [(М+Н)+].
Пример 31
1,3,3-триметил-6-(4-метил-2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
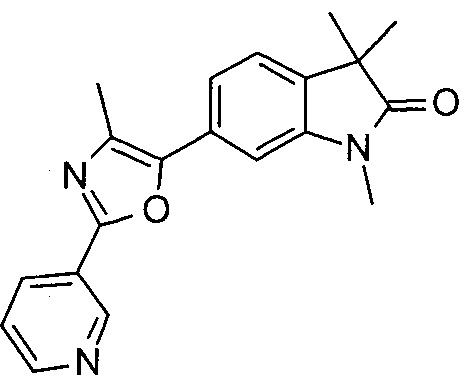
6-бромо-1,3,3-триметилиндолин-2-он из примера 2а взаимодействовал с 4-метил-2-(пиридин-3-ил)оксазолом (полученный в соответствии с Dondoni et al., Synthesis (8), 693-6, 1987) по аналогии с примером 14b с получением соединения, указанного в заголовке (57%), в виде белого осадка. MS (ESI, m/z): 334.6 [(М+Н)+].
Пример 32
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
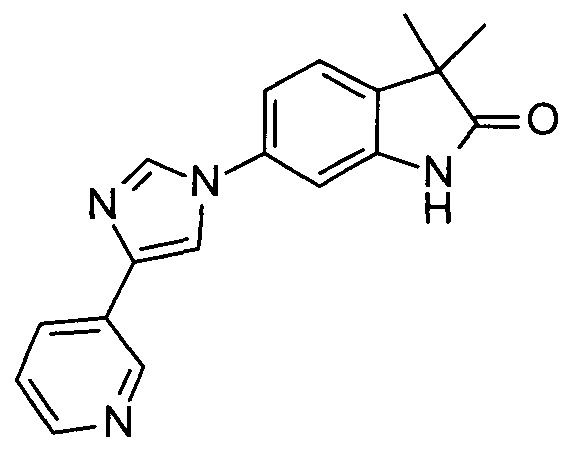
Пример 32 получили по аналогии с примером 20 с использованием 6-бромо-3,3-диметил-индолин-2-она из примера 1а и 3-(1Н-имидазол-4-ил)пиридина (полученный в соответствии с Denton et al., J. Med. Chem., 48, 224, 2005) с получением соединения, указанного в заголовке (22%), в виде белого осадка. MS (ESI, m/z): 305.5 [(М+Н)+].
Пример 33
1-циклопропил-3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
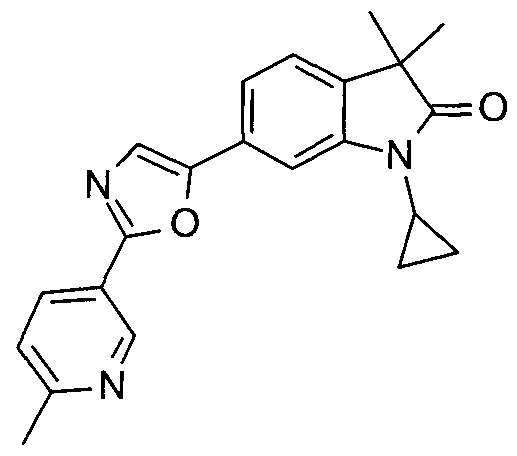
Пример 33 получили по аналогии с примером 27 с использованием 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b с получением соединения, указанного в заголовке, в виде белой пены. MS (ESI, m/z): 360.6 [(М+Н)+].
Пример 34
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
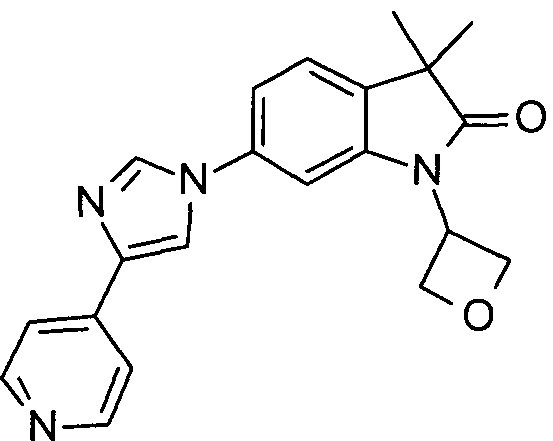
Пример 34 получили по аналогии с примером 20 с использованием 6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-она из примера 6а с получением соединения, указанного в заголовке, в виде белого осадка. MS (ESI, m/z): 361.6 [(M+H)+].
Пример 35
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
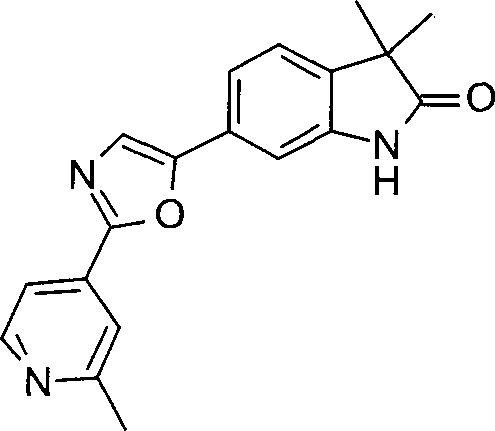
Пример 35 получили по аналогии с примером 22 с использованием 6-бромо-3,3-диметил-индолин-2-она из примера 1а с получением соединения, указанного в заголовке, в виде светло-желтого осадка. MS (ESI, m/z): 320.5 [(М+Н)+].
Пример 36
1,3,3-триметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
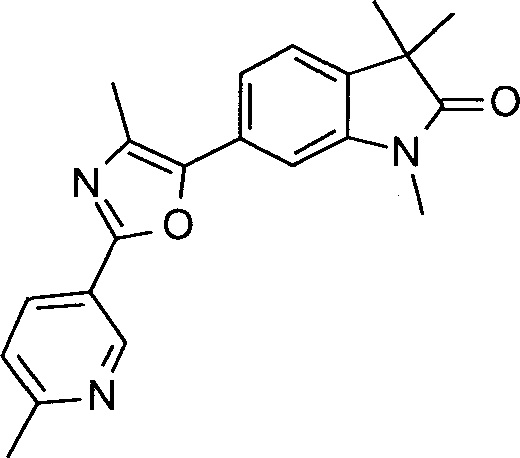
a) 4-метил-2-(6-метилпиридин-3-ил)оксазол
К раствору 4-метилоксазола (254 мг) в ТГФ (2 мл) добавили при -78°С раствор n-BuLi (1.6 М в ТГФ, 2.3 мл) с последующим хлоридом цинка (2 М в 2-метил-тетрагидрофуране, 2.3 мл) и перемешивание продолжили при 22°С в течение 30 мин. 5-бромо-2-метилпиридин (526 мг) и тетракис(трифенилфосфин)палладий(0) (353 мг) добавили и перемешивание продолжили при 60°С в течение 2 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 20% до 70% EtOAc в н-гептане) с получением соединения, указанного в заголовке (283 мг, 53%), в виде светло-желтого осадка. MS (ESI, m/z): 175.5 [(М+Н)+].
b) 1,3,3-триметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он (Пример 36)
6-бромо-1,3,3-триметилиндолин-2-он из примера 2а взаимодействовал с 4-метил-2-(6-метилпиридин-3-ил)оксазолом по аналогии с примером 14b с получением соединения, указанного в заголовке (57%), в виде белого осадка. MS (ESI, m/z): 334.6 [(М+Н)+].
Пример 37
1-циклопропил-3,3-диметил-6-(4-метил-2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
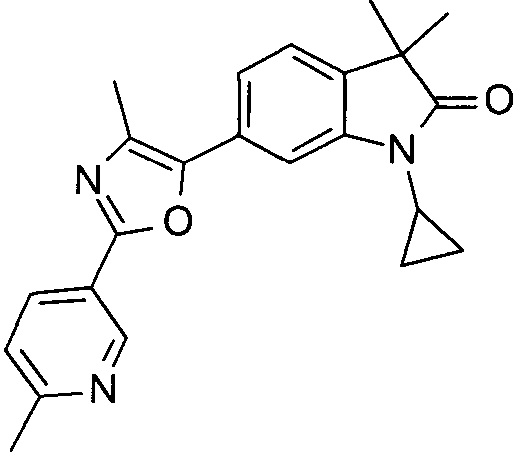
6-бромо-1-циклопропил-3,3-диметилиндолин-2-он из примера 1b взаимодействовал с 4-метил-2-(6-метилпиридин-3-ил)оксазолом из примера 36а по аналогии с примером 14b с получением соединения, указанного в заголовке (37%), в виде серо-белой пены. MS (ESI, m/z): 374.6 [(М+Н)+].
Пример 38
1,3,3-триметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
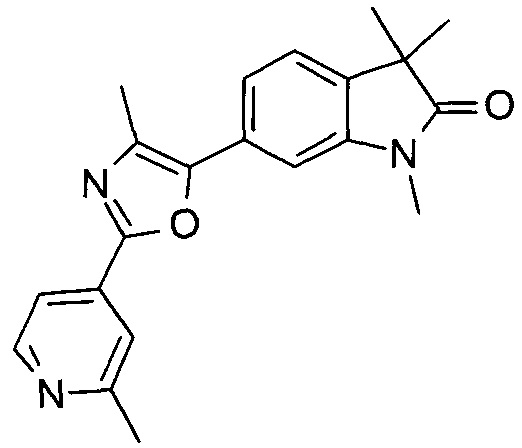
a) 4-метил-2-(2-метилпиридин-4-ил)оксазол
К раствору 4-метилоксазола (254 мг) в ТГФ (2 мл) добавили при -78°С n-BuLi (1.6 М в ТГФ, 2.3 мл) и хлорид цинка (2Mb 2-метил-тетрагидрофуране, 2.3 мл) и перемешивание продолжили при 22°С в течение 30 мин. 4-бромо-2-метилпиридин (526 мг) и тетракис(трифенилфосфин)палладий(0) (353 мг) добавили и перемешивание продолжили при 60°С в течение 2 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 30% до 70% EtOAc в н-гептане) с получением соединения, указанного в заголовке (375 мг, 70%), в виде светло-желтого вязкого масла. MS (ESI, m/z): 175.5 [(М+Н)+].
b) 1,3,3-триметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он (Пример 38) 6-бромо-1,3,3-триметилиндолин-2-он из примера 2а взаимодействовал с 4-метил-2-(2-метилпиридин-4-ил)оксазолом по аналогии с примером 14b с получением соединения, указанного в заголовке (70%), в виде светло-желтой пены. MS (ESI, m/z): 348.6 [(М+Н)+].
Пример 39
1-циклопропил-3,3-диметил-6-(4-метил-2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
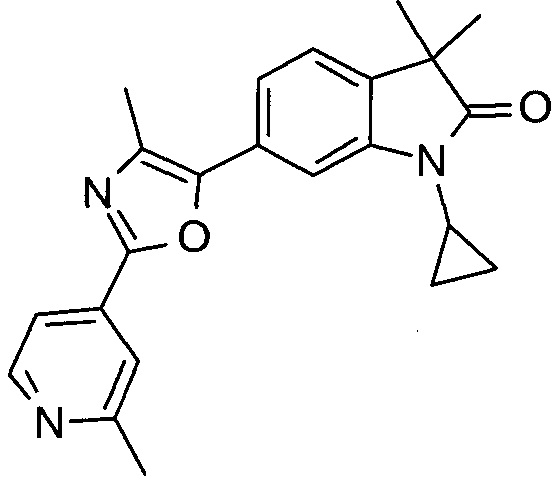
6-бромо-1-циклопропил-3,3-диметилиндолин-2-он из примера 1b взаимодействовал с 4-метил-2-(2-метилпиридин-4-ил)оксазолом из примера 38а по аналогии с примером 14b с получением соединения, указанного в заголовке (61%), в виде светло-желтой пены. MS (ESI, m/z): 374.6 [(М+Н)+].
Пример 40
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
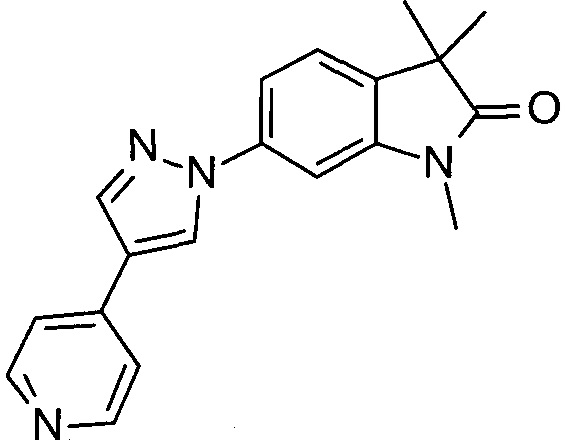
Суспензию 6-бромо-1,3,3-триметилиндолин-2-она (140 мг) из примера 2а, 4-(1Н-пиразол-4-ил)пиридина (80 мг, полученный в соответствии с Bauer et al., J. Med. Chem. 11, 981, 1968) и карбоната калия (190 мг) в безводном ДМСО (4 мл) продули аргоном. Йодид меди(I) (11 мг) и L-пролин (25 мг) добавили и перемешивание продолжили при 110°С в течение 16 ч. Реакционную смесь разделили между водой и дихлорметаном, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% MeOH/NH4OH в дихлорметане) с получением соединения, указанного в заголовке (74 мг, 42%), в виде белого осадка. MS (ESI, m/z): 319.4 [(М+Н)+].
Пример 41
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
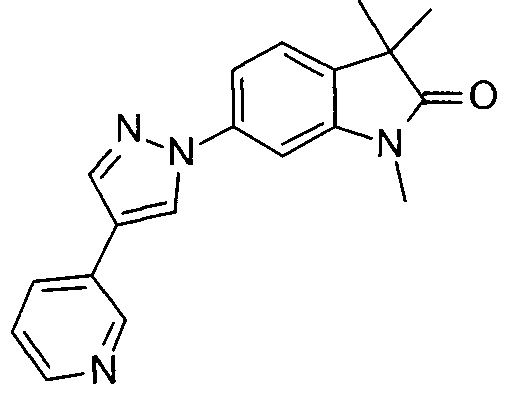
a) 3-(1Н-пиразол-4-ил)пиридин
К суспензии 3-бромопиридина (400 мг) и трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол-1-карбоксилата (745 мг) в 1,4-диоксане (12 мл) добавили водный карбонат натрия (1 М, 2.5 мл) и смесь продули аргоном в течение 5 мин. [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (103 мг) добавили и перемешивание продолжили при 110°С в течение 16 ч. Смесь разделили между водным гидрокарбонатом натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% MeOH/NH4OH в дихлорметане) с получением соединения, указанного в заголовке (234 мг, 64%), в виде светло-коричневого осадка. MS (ESI, m/z): 146.2 [(М+Н)+].
b) 1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он (Пример 41)
6-бромо-1,3,3-триметилиндолин-2-он из примера 2а взаимодействовал с 3-(1Н-пиразол-4-ил)пиридином по аналогии с примером 40 с получением соединения, указанного в заголовке (38%), в виде белого осадка. MS (ESI, m/z): 319.4 [(М+Н)+].
Пример 42
1,3,3-триметил-6-(3-пиридин-4-ил-изоксазол-5-ил)-1,3-дигидро-индол-2-он
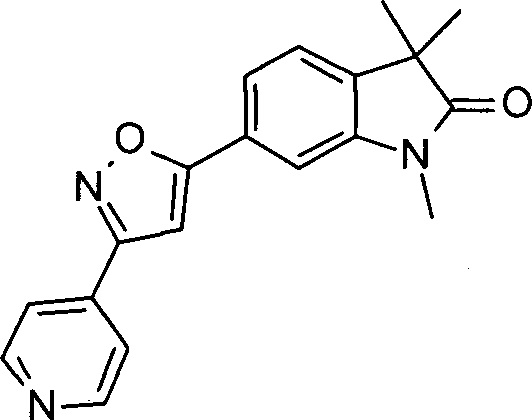
а) 1-(Пиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-дион
К раствору 6-ацетил-1,3,3-триметилиндолин-2-она (1.22 г) из примера 3а и метилизоникотината (770 мг) в безводном ТГФ (30 мл) добавили при 22°С гидрид натрия (515 мг) и перемешивание продолжили в течение 6 ч. Смесь эвапорировали и остаток разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток тритурировали с н-пентаном с получением соединения, указанного в заголовке (700 мг, 39%), в виде оранжевого осадка. MS (ESI, m/z): 321.4 [(М-Н)-].
b) 1,3,3-триметил-6-(3-пиридин-4-ил-изоксазол-5-ил)-1,3-дигидро-индол-2-он (Пример 42)
К раствору 1-(пиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона (300 мг) в безводном этаноле (6 мл) добавили гидрохлорида гидроксиламин (65 мг) и перемешивание продолжили при температуре кипения в течение 16 ч. Смесь эвапорировали и остаток разделили между водным гидрокарбонатом натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили посредством СКЖХ (Princeton, 4-этилпиридин 20×250 мм 100А, 5 мкм, 12% изопропанол / 88% диоксид углерода, 60 мл/мин, 40°С) с получением соединения, указанного в заголовке (141 мг, 47%), в виде более медленно элюируемого изомера в виде белого осадка. MS (ESI, m/z): 320.4 [(М+Н)+].
Более быстро элюируемый региоизомер, 1,3,3-триметил-6-(5-пиридин-4-ил-изоксазол-3-ил)-1,3-дигидро-индол-2-он (85 мг, 29%), получили в виде белого осадка. MS (ESI, m/z): 320.4 [(М+Н)+].
Пример 43
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
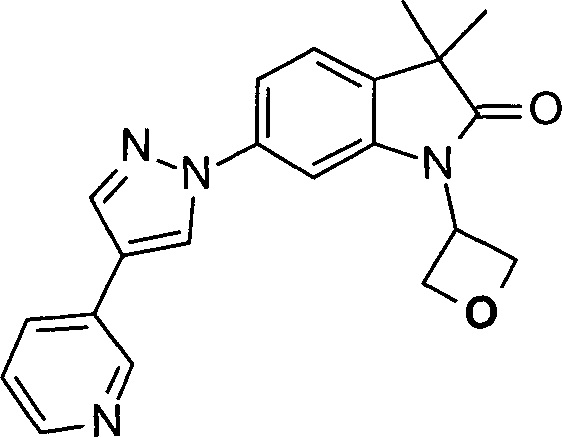
6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он из примера 6а конвертировали по аналогии с примером 41 в соединение, указанное в заголовке (42%), получили в виде белого осадка. MS (ESI, m/z): 361.4 [(М+Н)+].
Пример 44
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-4-ил)индолин-2-он
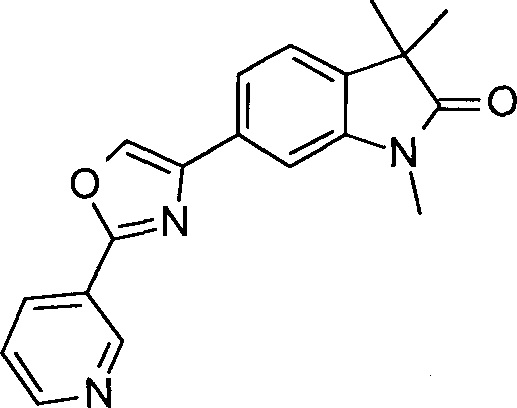
a) 1,3,3-триметил-6-(оксазол-4-ил)индолин-2-он
Суспензию 6-(2-бромоацетил)-1,3,3-триметилиндолин-2-она (1.05 г) из примера 3d и формамида (14.4 г) нагревали до 110°С в течение 2 ч. Смесь разделили между насыщенным водным гидрокарбонатом натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в н-гептане) с получением соединения, указанного в заголовке (335 мг, 39%), в виде белого осадка. MS (ESI, m/z): 243.6 [(М+Н)+].
b) 6-(2-Хлорооксазол-4-ил)-1,3,3-триметилиндолин-2-он
К раствору 1,3,3-триметил-6-(оксазол-4-ил)индолин-2-она (0.23 г) в безводном ТГФ (4 мл) добавили при -78°С раствор LiHMDS(1 М в ТГФ, 1.0 мл) и смеси дали нагреться до 22°С. Смесь охладили до -78°С и обработали гексахлорэтаном (238 мг) и перемешивание продолжили при 22°С в течение 3 ч. Смесь разделили между насыщенным водным хлоридом аммония и ТВМЕ, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 50% EtOAc в н-гептане) с получением соединения, указанного в заголовке (195 мг, 74%), в виде белого осадка. MS (ESI, m/z): 277.5 [(М+Н)+].
c) 1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-4-ил)индолин-2-он (Пример 44)
Смесь 6-(2-хлорооксазол-4-ил)-1,3,3-триметилиндолин-2-она (100 мг) и пиридин-3-бороновой кислоты (58 мг) в 1,4-диоксане (3 мл) и водного карбоната натрия (2 М, 0.7 мл) продули аргоном, бис(трифенилфосфин)палладий(М)дихлорид добавили (26 мг) и смесь нагрели до температуры кипения в течение 2 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с последующей очисткой ВЭЖХ (RP-18, градиент, ацетонитрил/вода) с получением соединения, указанного в заголовке (68 мг, 59%), в виде белого осадка. MS (ESI, m/z): 320.5 [(М+Н)+].
Пример 45
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он

6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-он из примера 6а конвертировали в соединение, указанное в заголовке (20%) по аналогии с примером 40, полученное в виде белого осадка. MS (ESI, m/z): 361.5 [(М+Н)+].
Пример 46
1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-пиразол-4-ил)индолин-2-он
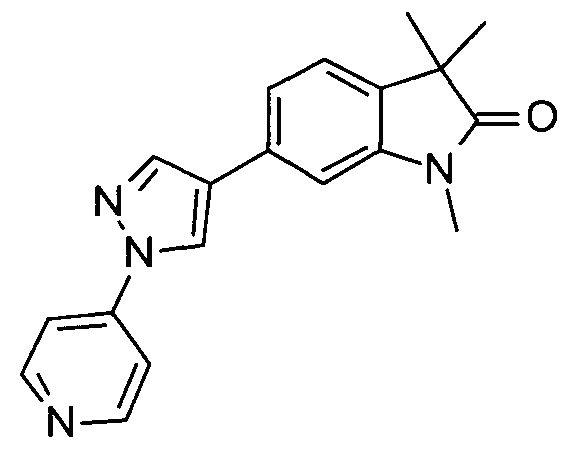
a) 1,3,3-триметил-6-(1Н-пиразол-4-ил)индолин-2-он
Смесь 6-бромо-1,3,3-триметилиндолин-2-она (200 мг) из примера 2а и трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол-1-карбоксилата (232 мг) в 1,4-диоксане (4.5 мл) и водного карбоната натрия (2 М, 0.8 мл) продули аргоном, [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (32 мг) добавили и перемешивание продолжили в микроволновой печи при 120°С в течение 30 мин. Раствор разделили между насыщенным водным гидрокарбонатом натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (115 мг, 61%), в виде коричневого вязкого масла. MS (ESI, m/z): 242.5 [(М+Н)+].
b) 1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-пиразол-4-ил)индолин-2-он (Пример 46)
Суспензию 1,3,3-триметил-6-(1Н-пиразол-4-ил)индолин-2-она (85 мг), 4-бромопиридина гидрохлорида (103 мг) и карбоната калия (166 мг) в безводном ДМСО (2.5 мл) продули аргоном, затем йодид меди(I) (14 мг) и L-пролин (32 мг) добавили и перемешивание продолжили при 110°С в течение 16 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 5% МеОН в дихлорметане), после которой провели вторую флеш-хроматографию (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (86 мг, 77%), в виде белого осадка. MS (ESI, m/z): 319.5 [(М+H)+].
Пример 47
3,3-диметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
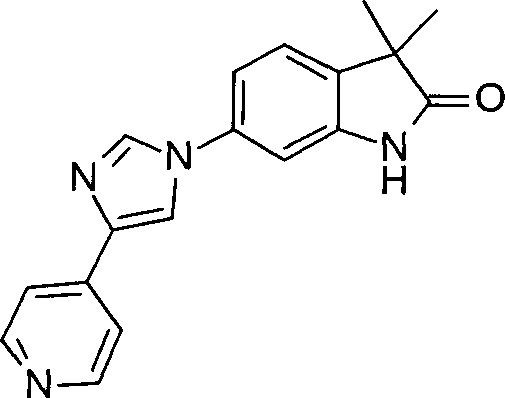
Пример 47 получили по аналогии с примером 20 с использованием 6-бромо-3,3-диметил-индолин-2-она из примера 1а с получением соединения, указанного в заголовке (15%), в виде белого осадка. MS (ESI, m/z): 305.5 [(М+Н)+].
Пример 48
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
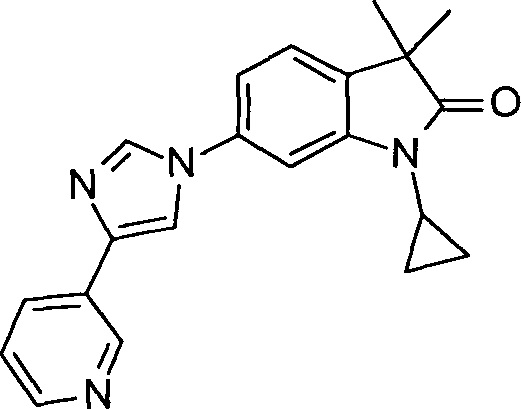
Пример 48 получили по аналогии с примером 32 с использованием 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b с получением соединения, указанного в заголовке (30%), в виде белого осадка. MS (ESI, m/z): 345.6 [(М+Н)+].
Пример 49
3,3-диметил-6-(5-(2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1-(оксетан-3-ил)индолин-2-он
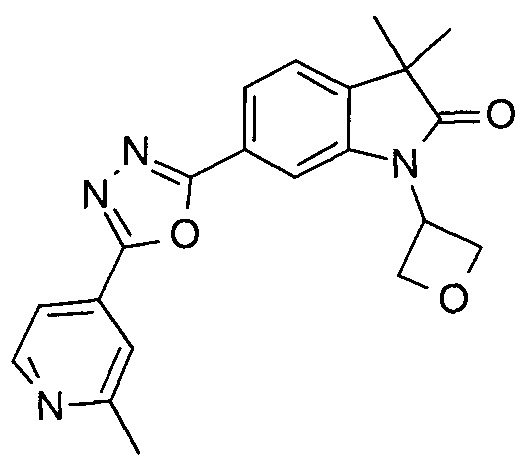
Пример 49 получили по аналогии с примером 11 с использованием 2-метилизоникотиногидразида с получением соединения, указанного в заголовке (47%), в виде белого осадка. MS (ESI, m/z): 377.6 [(М+Н)+].
Пример 50
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-пиразол-4-ил)индолин-2-он
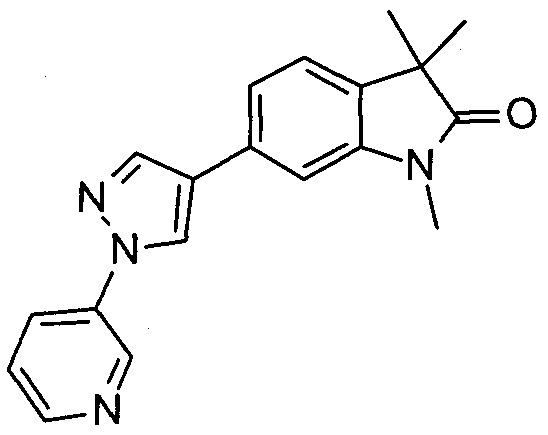
Пример 50 получили по аналогии с примером 46 с использованием 3-бромопиридина с получением соединения, указанного в заголовке (52%), в виде белого осадка. MS (ESI, m/z): 319.6 [(М+Н)+].
Пример 51
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
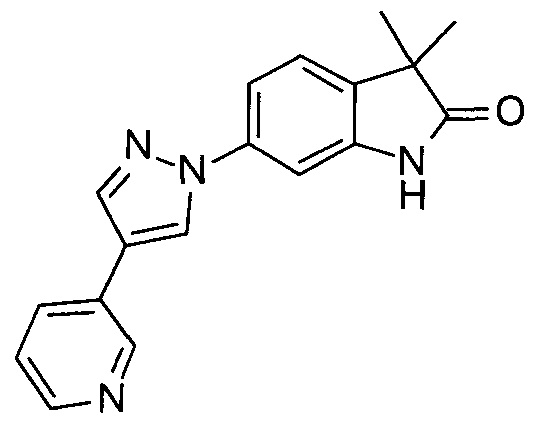
Пример 51 получили по аналогии с примером 40 с использованием 6-бромо-3,3-диметилиндолин-2-она из примера 1а и 3-(1Н-пиразол-4-ил)пиридина из примера 41а с получением соединения, указанного в заголовке (52%), в виде белой пены. MS (ESI, m/z): 305.6 [(М+Н)+].
Пример 52
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
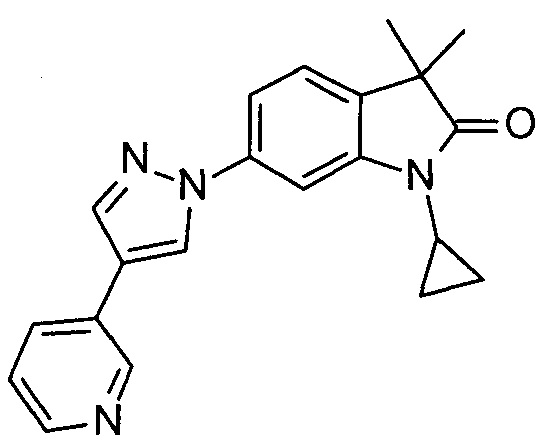
Пример 52 получили по аналогии с примером 40 с использованием 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b и 3-(1Н-пиразол-4-ил)пиридина из примера 41а с получением соединения, указанного в заголовке (34%), в виде белой пены. MS (ESI, m/z): 345.5 [(М+Н)+].
Пример 53
1-циклопропил-3,3-диметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
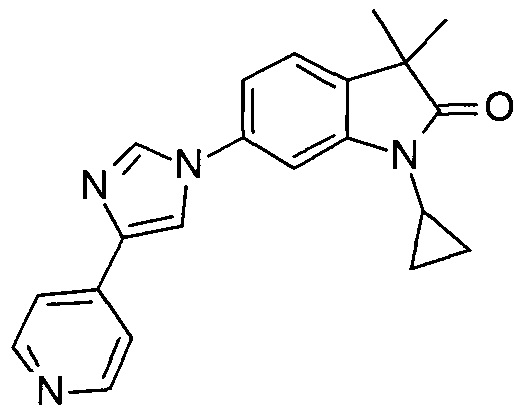
Пример 53 получили по аналогии с примером 20 с использованием 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b с получением соединения, указанного в заголовке (11%) в виде белого осадка. MS (ESI, m/z): 345.5 [(М+Н)+].
Пример 54
1,3,3-триметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
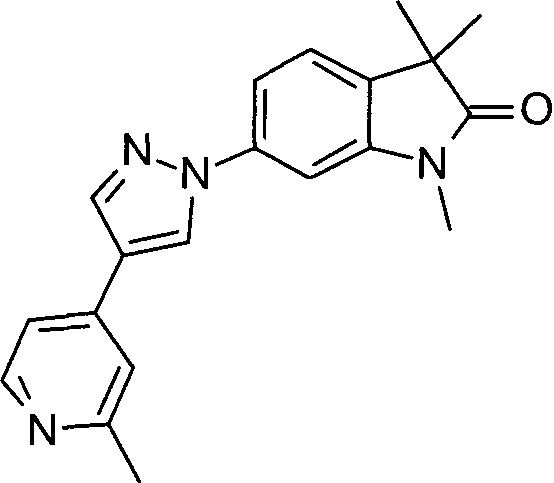
а) 2-метил-4-(1Н-пиразол-4-ил)пиридин
Соединение, указанное в заголовке (64%), получили по аналогии с примером 41а с использованием 4-бромо-2-метилпиридина, в виде светло-желтого осадка. MS (ESI, m/z): 160.3 [(М+Н)+].
b) 1,3,3-триметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он (Пример 54)
Пример 54 получили по аналогии с примером 40 с использованием 6-бромо-1,3,3-триметилиндолин-2-она из примера 2а и 2-метил-4-(1Н-пиразол-4-ил)пиридина с получением соединения, указанного в заголовке (25%), в виде белого осадка. MS (ESI, m/z): 333.5 [(М+Н)+].
Пример 55
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
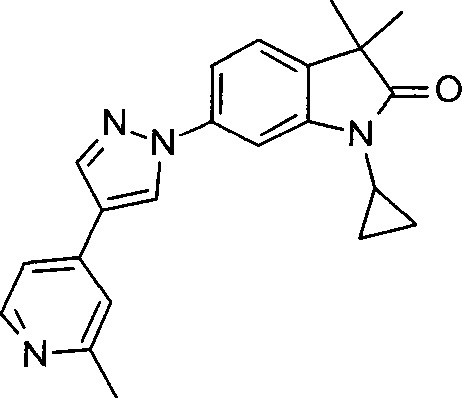
Пример 55 получили по аналогии с примером 40 с использованием 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b и 2-метил-4-(1Н-пиразол-4-ил)пиридина из примера 54а с получением соединения, указанного в заголовке (29%), в виде белого осадка. MS (ESI, m/z): 359.5 [(М+Н)+].
Пример 56
1,3,3-триметил-6-(5-(пиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
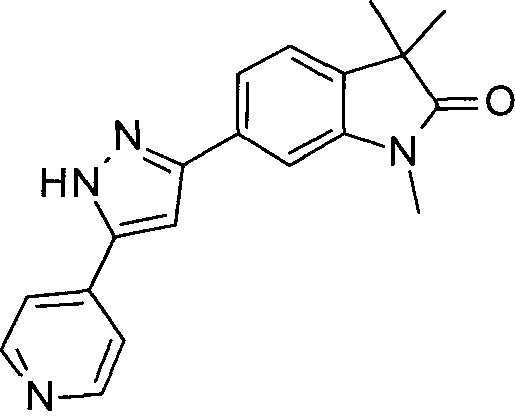
К раствору 1-(пиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона (170 мг) из примера 42а в безводном этаноле (3.5 мл) добавили DIPEA (82 мг) и гидразин (1 M в ТГФ, 0.6 мл) и перемешивание продолжили при температуре кипения в течение 18 ч. Реакционную смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 20% MeOH/NH4OH в дихлорметане) с последующей второй очисткой с помощью препаративной ВЭЖХ хроматографией (RP-18, градиент, ацетонитрил/вода) с получением соединения, указанного в заголовке (25 мг, 15%), в виде светло-желтого осадка. MS (ESI, m/z): 319.6 [(М+Н)+].
Пример 57
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-1,2,3-триазол-1-ил)индолин-2-он
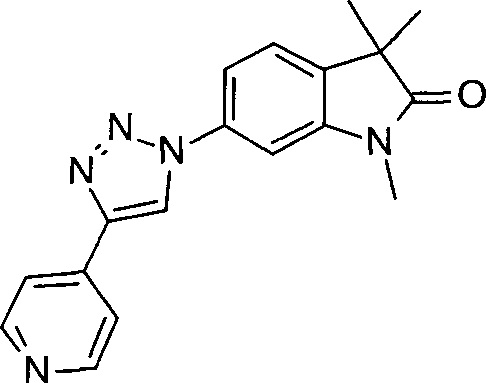
a) 6-азидо-1,3,3-триметилиндолин-2-он
Суспензию 6-бромо-1,3,3-триметилиндолин-2-она (500 мг) из примера 2а, азида натрия (258 мг), L(+)-аскорбиновой кислоты натриевой соли (20 мг) и транс-(1R,2R)-N,N'-бисметил-1,2-циклогександиамина (42 мг) в этаноле (3 мл) и воде (1 мл) продули аргоном. Йодид меди(I) (38 мг) добавили и перемешивание продолжили при температуре кипения в течение 1 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 40% EtOAc в н-гептане) с получением соединения, указанного в заголовке (366 мг, 86%), в виде светло-коричневого осадка. MS (ESI, m/z): 217.5 [(М+Н)+].
b) 1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-1,2,3-триазол-1-ил)индолин-2-он (Пример 57)
К раствору 6-азидо-1,3,3-триметилиндолин-2-она (100 мг) и 4-этинилпиридина (54 мг) в трет-BuOH (3 мл) добавили L(+)-аскорбиновой кислоты натриевую соль (46 мг) и пентагидрат сульфата меди(II) (12 мг) в воде (3 мл) и перемешивание продолжили при 22°С в течение 16 ч. Смесь разделили между водным карбонатом натрия (1 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 7% МеОН в дихлорметане) с получением соединения, указанного в заголовке (133 мг, 90%), в виде белого осадка. MS (ESI, m/z): 320.2 [(М+Н)+].
Пример 58
3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
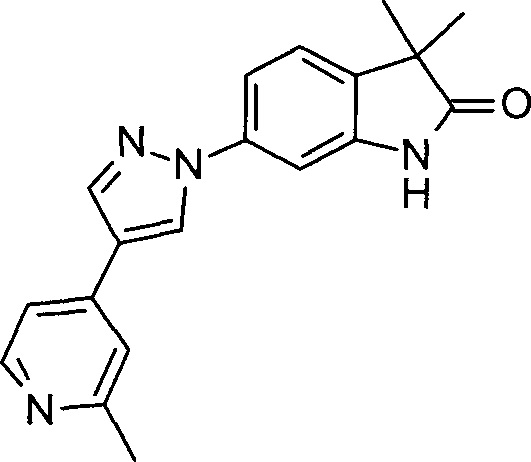
Пример 58 получили по аналогии с примером 40 с использованием 6-бромо-3,3-диметилиндолин-2-она из примера 1а и 2-метил-4-(1Н-пиразол-4-ил)пиридина из примера 54а с получением соединения, указанного в заголовке (16%), в виде светло-коричневого осадка. MS (ESI, m/z): 319.5 [(М+Н)+].
Пример 59
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
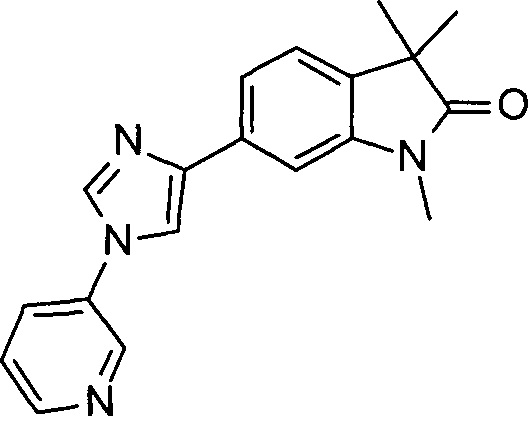
а) 6-(гидроксиметил)-1,3,3-триметилиндолин-2-он
К суспензии 1,3,3-триметил-2-оксоиндолин-6-карбоновой кислоты (150 мг) из примера 13а в ТГФ (1 мл) добавили при 0°С боран-тетрагидрофурановый комплекс (1 M в ТГФ, 1 мл) и перемешивание продолжили при 22°С в течение 2 ч. Смесь разделили между водным гидрокарбонатом натрия и EtOAc, органический слой промыли водой, высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (140 мг, колич.) в виде светло-желтой пены, которую использовали без дополнительной очистки. MS (ESI, m/z): 206.5 [(М+Н)+].
b) 1,3,3-триметил-2-оксоиндолин-6-карбальдегид
Суспензию 6-(гидроксиметил)-1,3,3-триметилиндолин-2-она (2.07 г) и диоксида марганца (6.1 г) в дихлорметане (30 мл) нагревали до температуры кипения 1 ч и перемешивание продолжили при 22°С в течение 16 ч. Суспензию отфильтровали и фильтрат эвапорировали с получением неочищенного соединения, указанного в заголовке (1.85 г, 90%) в виде оранжевого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 204.5 [(М+Н)+].
c) 1,3,3-триметил-6-(оксазол-5-ил)индолин-2-он
Суспензию 1,3,3-триметил-2-оксоиндолин-6-карбальдегида (1.68 г), карбоната калия (1.16 г) и тозилметилизоникотинцианида (1.61 г) в МеОН (12 мл) нагревали до 80°С в течение 16 ч. Смесь разделили между водой и дихлорметаном, органический слой промыли водой, высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (1.96 г, 98%), в виде светло-коричневого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 243.5 [(М+Н)+].
d) 6-(1Н-Имидазол-5-ил)-1,3,3-триметилиндолин-2-он
Раствор 1,3,3-триметил-6-(оксазол-5-ил)индолин-2-она (700 мг) в формамиде (24 мл) нагревали до 190°С в течение 7 ч. Смесь разделили между водой и EtOAc, органический слой промыли водой, высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (390 мг, 56%), в виде коричневой пены. MS (ESI, m/z): 242.5 [(М+Н)+].
e) 1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он (Пример 59)
Суспензию 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она (210 мг), 3-бромопиридина (165 мг), карбоната калия (361 мг) и 2-ацетилциклогексанона (61 мг) в ДМСО (4 мл) продули аргоном, затем хлорид меди(I) (22 мг) добавили и перемешивание продолжили при 130°С в течение 16 ч. Смесь разделили между водой и EtOAc, органический слой промыли водой, высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (189 мг, 68%), в виде светло-желтой пены. MS (ESI, m/z): 319.5 [(М+Н)+].
Пример 60
1,3,3-триметил-6-(1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
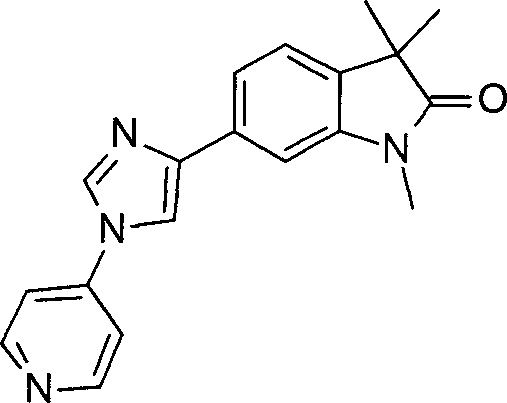
Пример 60 получили по аналогии с примером 59 с использованием 4-бромопиридина на стадии е с получением соединения, указанного в заголовке (60%), в виде светло-коричневого осадка. MS (ESI, m/z): 319.5 [(М+Н)+].
Пример 61
1,3,3-триметил-6-(5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
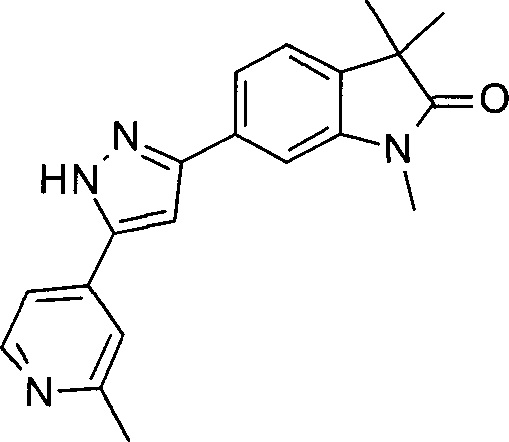
a) 1-(2-Метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-дион
6-ацетил-1,3,3-триметилиндолин-2-он из примера 3а и метил 2-метилизоникотинат взаимодействовали по аналогии с примером 42а с получением соединения, указанного в заголовке (47%), в виде оранжевой смолы. MS (ESI, m/z): 337.5 [(М+Н)+].
b) 1,3,3-триметил-6-(5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он (Пример 61)
Пример 61 получили из 1-(2-метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона по аналогии с примером 56 с получением соединения, указанного в заголовке (57%), в виде белого осадка. MS (ESI, m/z): 333.6 [(М+Н)+].
Пример 62
1,3,3-триметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
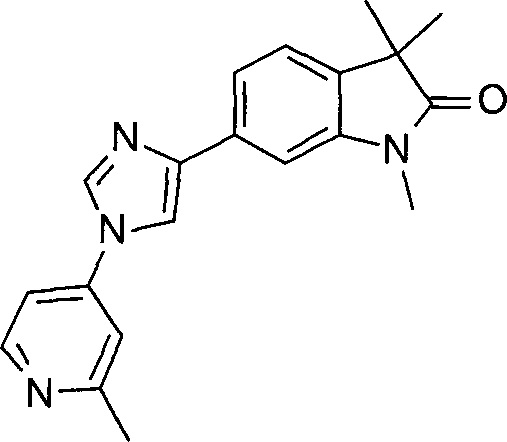
Пример 62 получили по аналогии с примером 59 с использованием 4-бромо-2-метилпиридина на стадии е с получением соединения, указанного в заголовке (81%), в виде светло-коричневой пены. MS (ESI, m/z): 333.5 [(М+Н)+].
Пример 63
6-(2-(3-Метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он
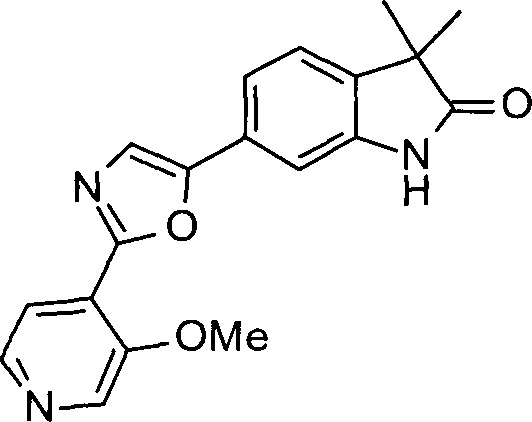
a) Метил 3,3-диметил-2-оксоиндолин-6-карбоксилат
Смесь 3,3-диметил-2-оксоиндолин-6-карбоновой кислоты (8.29 г) из примера 28а в МеОН (30 мл) и серной кислоты (825 мг) нагревали до температуры кипения в течение 16 ч. Смесь разделили между водным карбонатом натрия (2 М) и дихлорметаном, органический слой высушили, эвапорировали, остаток тритурировали с EtOAc и диизопропиловым эфиром (1:1, 70 мл), отфильтровали и остаток высушили с получением неочищенного соединения, указанного в заголовке (4.50 г, 51%), в виде светло-красного осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 220.5 [(М+Н)+].
b) 6-(гидроксиметил)-3,3-диметилиндолин-2-он
К раствору метил 3,3-диметил-2-оксоиндолин-6-карбоксилата (8.59 г) в ТГФ (390 мл) добавили при 22°С LiBH4 (5.12 г) и перемешивание продолжили при 50°С в течение 60 ч. Смесь разделили между насыщенным водным хлоридом аммония и EtOAc, органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (8.32 г, колич.) в виде желтого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 192.5 [(М+Н)+].
c) 3,3-диметил-2-оксоиндолин-6-карбальдегид
Суспензию 6-(гидроксиметил)-3,3-диметилиндолин-2-она (7.55 г) и диоксида марганца (20.6 г) в дихлорметане (395 мл) нагревали до температуры кипения в течение 16 ч. Смесь отфильтровали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% МеОН в дихлорметане) с получением соединения, указанного в заголовке (5.99 г, 80%), в виде коричневого осадка. MS (ESI, m/z): 190.4 [(М+Н)+].
d) 3,3-диметил-6-(оксазол-5-ил)индолин-2-он
К суспензии 3,3-диметил-2-оксоиндолин-6-карбальдегида (5.90 г) и карбоната калия (5.60 г) в метаноле (43 мл) добавили тозилметилизоцианид (6.09 г) и перемешивание продолжили при 80°С в течение 3 ч. Смесь разделили между водой и дихлорметаном, органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (6.45 г, 91%), в виде оранжевого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 229.5 [(М+Н)+].
e) 6-(2-Хлорооксазол-5-ил)-3,3-диметилиндолин-2-он
К раствору 3,3-диметил-6-(оксазол-5-ил)индолин-2-она (6.35 г) в ТГФ (110 мл) добавили при -78°С раствор LiHMDS (1 M в ТГФ, 58 мл) и смесь нагревали до 22°С в течение 1.5 ч. Гексахлорэтан (7.00 г) добавили и перемешивание продолжили при КТ в течение 1.5 ч. Смесь разделили между насыщенным водным гидрокарбонатом натрия и ТВМЕ, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (4.90 г, 67%), в виде оранжевого осадка. MS (ESI, m/z): 263.4 [(М+Н)+].
f) 6-(2-Хлорооксазол-5-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-он
Смесь 6-(2-хлорооксазол-5-ил)-3,3-диметилиндолин-2-она (2.00 г), 1-(хлорметил)-4-метоксибензола (1.31 г) и карбоната цезия (4.96 г) в ДМФ (51 мл) нагревали до 80°С в течение 3 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (2.13 г, 73%), в виде светло-желтого полутвердого вещества. MS (ESI, m/z): 383.4 [(М+Н)+].
q) 1-(4-Метоксибензил)-6-(2-(3-метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он
Смесь 6-(2-хлорооксазол-5-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-она (500 мг) и 3-метоксипиридин-4-илбороновой кислоты (367 мг) в 1,4-диоксане (10 мл) и водный карбонат натрия (2 М, 2.6 мл) продули аргоном, затем бис(трифенилфосфин)палладий(II)дихлорид (141 мг) добавили и перемешивание продолжили при температуре кипения в течение 16 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением все еще загрязненного соединения, указанного в заголовке (274 мг, 46%), в виде коричневой пены, которую использовали без дополнительной очистки. MS (ESI, m/z): 456.4 [(М+Н)+].
h) 6-(2-(3-Метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он (Пример 63)
Раствор 1-(4-метоксибензил)-6-(2-(3-метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-она (270 мг) в ТФУ (4 мл) нагревали до 120°С в течение 16 ч. Смесь разделили между водным карбонатом натрия (2 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (71 мг, 36%), в виде коричневого осадка. MS (ESI, m/z): 336.5 [(М+Н)+].
Пример 64
1,3,3-триметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он
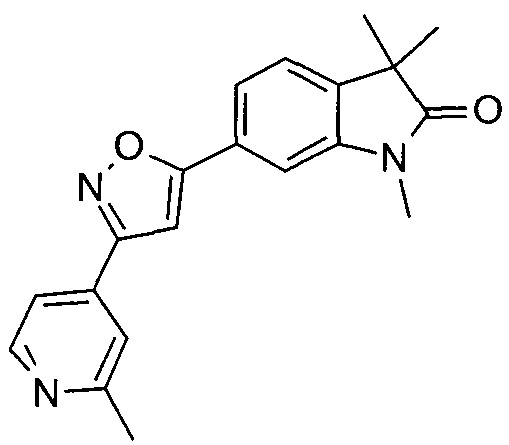
а) 1-(2-Метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-дион
Соединение, указанное в заголовке, получили из 6-ацетил-1,3,3-триметилиндолин-2-она из примера 3а и метил 2-метилизоникотината по аналогии с примером 42а с получением соединения, указанного в заголовке (76%), в виде оранжевого масла. MS (ESI, m/z): 337.5 [(М+Н)+].
b) 1,3,3-триметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он (Пример 64)
Пример 64 получили из 1-(2-метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона по аналогии с примером 42b с получением соединения, указанного в заголовке (18%), в виде светло-коричневого осадка. MS (ESI, m/z): 334.2 [(М+Н)+].
Пример 65
1,3,3-триметил-6-(5-(пиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
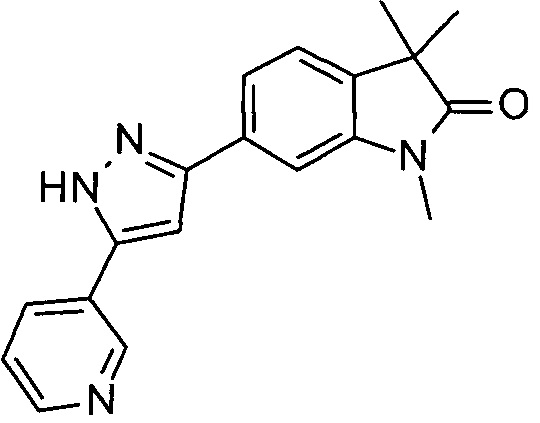
a) 1-(Пиридин-3-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-дион Соединение, указанное в заголовке, получили из 6-ацетил-1,3,3-триметилиндолин-2-она из примера 3а и метилникотината по аналогии с примером 42а с получением соединения, указанного в заголовке (79%), в виде желтого осадка. MS (ESI, m/z): 323.5 [(М+Н)+].
b) 1,3,3-триметил-6-(5-(пиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он (Пример 65)
Пример 65 получили из 1-(пиридин-3-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона по аналогии с примером 56 с получением соединения, указанного в заголовке (50%), в виде белого осадка. MS (ESI, m/z): 319.5 [(М+Н)+].
Пример 66
1-этил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
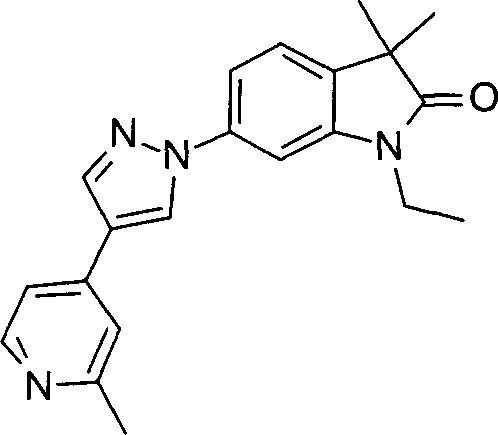
b) 6-бромо-1-этил-3,3-диметилиндолин-2-он
К раствору 6-бромо-3,3-диметилиндолин-2-она (465 мг) из примера 1а в безводном ТГФ (12 мл) добавили при 0°С раствор натрия бис(триметилсилил)амида (1 M в ТГФ, 6 мл) с последующим этилйодидом (1.03 г) и перемешивание продолжили при 0°С в течение 30 мин и при 50°С в течение 16 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (490 мг, 94%), в виде желтого масла. MS (ESI, m/z): 269.4 [(М+Н)+].
b) 1-этил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он (Пример 66)
Пример 66 получили из 6-бромо-1-этил-3,3-диметилиндолин-2-она и 2-метил-4-(1Н-пиразол-4-ил)пиридина из примера 54а по аналогии с примером 40 с получением соединения, указанного в заголовке (55%), в виде белого осадка. MS (ESI, m/z): 347.6 [(М+Н)+].
Пример 67
6-[1-(2-фторпиридин-4-ил)имидазол-4-ил]-1,3,3-триметилиндол-2-он
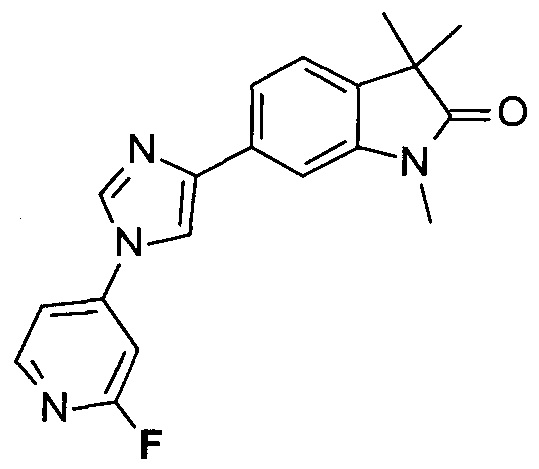
Пример 67 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d и 4-бромо-3-фторпиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (9%), в виде коричневого осадка. MS (ESI, m/z): 337.5 [(М+Н)+].
Пример 68
1,3,3-триметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
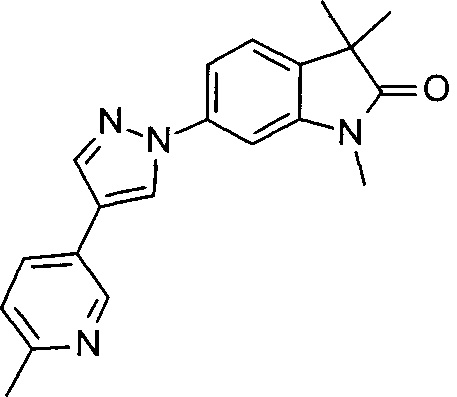
a) 2-метил-5-(1Н-пиразол-4-ил)пиридин
Соединение, указанное в заголовке, получили из 5-бромо-2-метилпиридина и трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол-1-карбоксилата по аналогии с примером 41а и получили в виде коричневого осадка (78%). MS (ESI, m/z): 158.2 [(М-Н)-].
b) 1,3,3-триметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он (Пример 68)
Пример 68 получили из 6-бромо-1,3,3-триметилиндолин-2-она из примера 2а и 2-метил-5-(1Н-пиразол-4-ил)пиридина по аналогии с примером 40 с получением соединения, указанного в заголовке (30%), в виде белого осадка. MS (ESI, m/z): 333.6 [(М+Н)+].
Пример 69
1-циклопропил-3,3-диметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
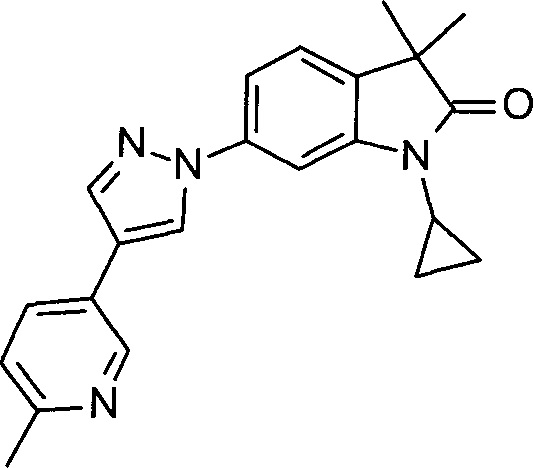
Пример 69 получили из 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b и 2-метил-5-(1Н-пиразол-4-ил)пиридина из примера 68а по аналогии с примером 40 с получением соединения, указанного в заголовке (34%), в виде белой пены. MS (ESI, m/z): 359.6 [(М+Н)+].
Пример 70
3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)-1-(оксетан-3-ил)индолин-2-он
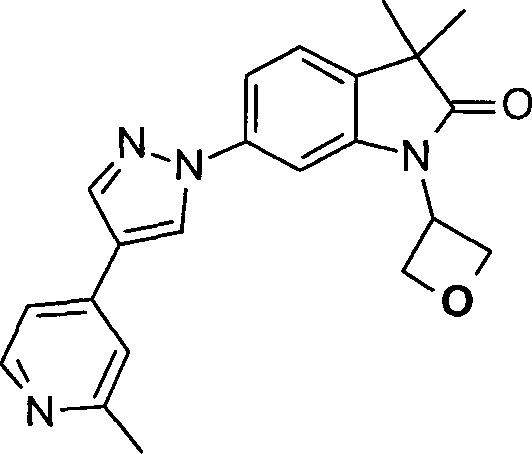
Пример 70 получили из 6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-она из примера 6а и 2-метил-4-(1Н-пиразол-4-ил)пиридина из примера 54а по аналогии с примером 40 с получением соединения, указанного в заголовке (30%), в виде серо-белого осадка. MS (ESI, m/z): 375.2 [(М+Н)+].
Пример 71
1-циклопропил-3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
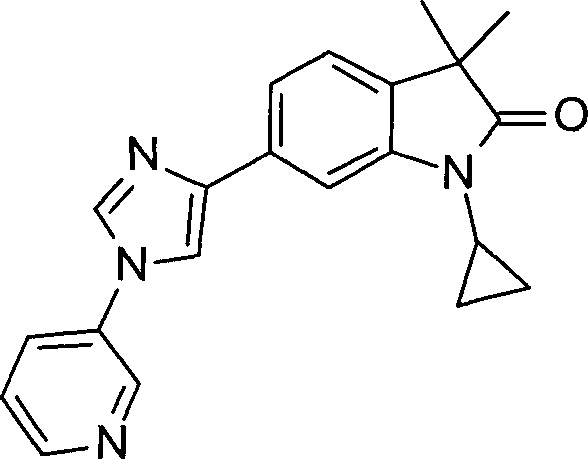
a) 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-он
Соединение, указанное в заголовке, получили из 1-циклопропил-3,3-диметил-2-оксоиндолин-6-карбоновой кислоты из примера 4b по аналогии с примером 59a-d и получили в виде светло-коричневой пены (48%). MS (ESI, m/z): 268.5 [(М+Н)+].
b) 1-циклопропил-3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он (Пример 71)
Пример 71 получили из 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она и 3-бромопиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (61%), в виде серо-белой пены. MS (ESI, m/z): 345.5 [(М+Н)+].
Пример 72
1-циклопропил-3,3-диметил-6-(1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
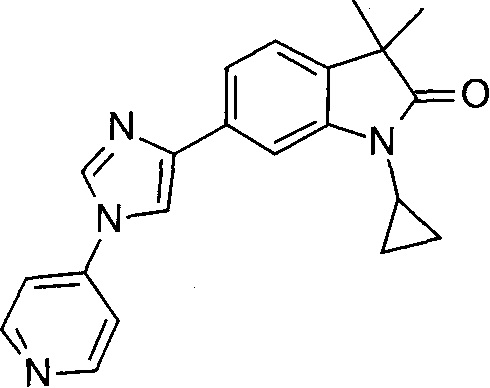
Пример 72 получили из 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она из примера 71а и 4-бромопиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (38%), в виде серо-белой пены. MS (ESI, m/z): 345.5 [(М+Н)+].
Пример 73
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметил индол ин-2-он
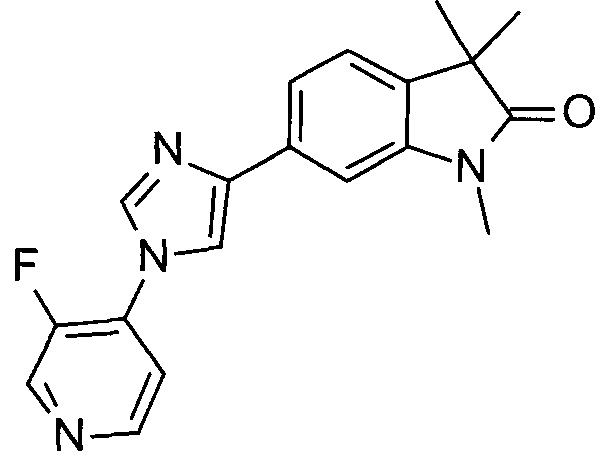
Пример 73 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d и 4-бромо-3-фторпиридина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (59%), в виде светло-коричневого осадка. MS (ESI, m/z): 337.2 [(М+Н)+].
Пример 74
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
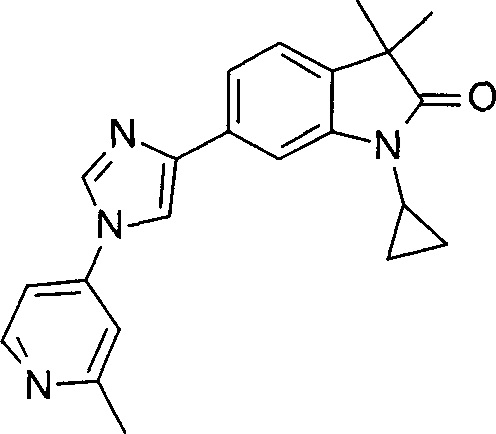
Пример 74 получили из 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она из примера 71а и 4-бромо-2-метилпиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (46%), в виде серо-белой пены. MS (ESI, m/z): 359.5 [(М+Н)+].
Пример 75
1-циклопропил-3,3-диметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он
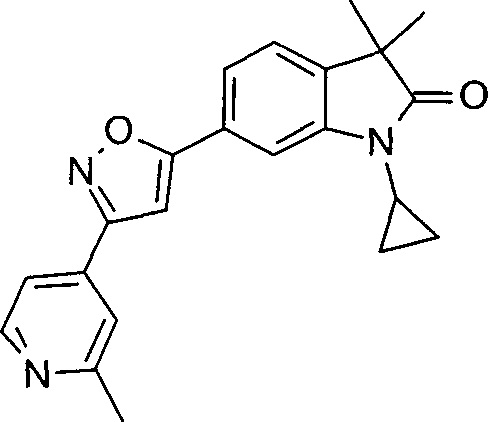
a) 6-ацетил-1-циклопропил-3,3-диметилиндолин-2-он
Соединение, указанное в заголовке, получили из 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b по аналогии с примером 3а и получили в виде светло-желтого осадка (76%). MS (ESI, m/z): 344.5 [(М+Н)+].
b) 1-ииклопропил-3,3-диметил-6-(3-(2-метилпиридин-4-ил)изоксазол-5-ил)индолин-2-он (Пример 75)
Пример 75 получили из 1-(1-циклопропил-3,3-диметил-2-оксо-индолин-6-ил)-3-(2-метил-4-пиридил)пропан-1,3-диона (полученный из 6-ацетил-1-циклопропил-3,3-диметилиндолин-2-она и метил 2-метилпиридин-4-карбоксилата по аналогии с примером 42а) по аналогии с примером 42b с получением соединения, указанного в заголовке (56%), в виде белой пены. MS (ESI, m/z): 360.8 [(М+Н)+].
Пример 76
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
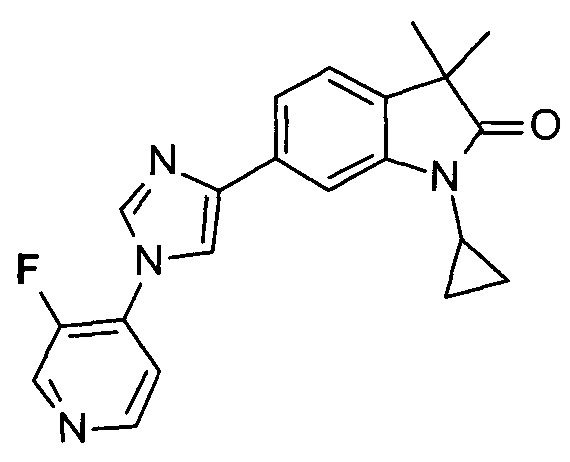
Пример 76 получили из 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она из примера 71а и 4-бромо-3-фторпиридина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (23%), в виде серо-белой пены. MS (ESI, m/z): 363.2 [(М+Н)+].
Пример 77
1,3,3-триметил-6-(2-метил-1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
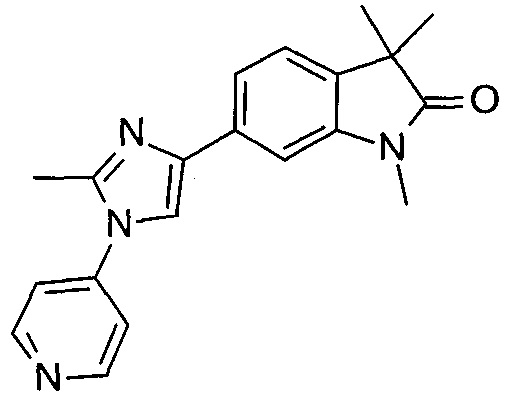
a) 1,3,3-триметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-он
К раствору ацетамида (735 мг) в дихлорметане (50 мл) добавили при 22°С раствор 6-(2-бромоацетил)-1,3,3-триметилиндолин-2-она (1.50 г) из примера 3b в дихлорметане (5 мл) и перемешивание продолжили в течение 16 ч. Смесь разделили между водным карбонатом натрия (2 М) и дихлорметаном, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% EtOAc в н-гептане) с получением соединения, указанного в заголовке (966 мг, 75%), в виде серо-белой пены. MS (ESI, m/z): 256.5 [(М+Н)+].
b) 1,3,3-триметил-6-(2-метил-1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он (Пример 77)
Пример 77 получили из 1,3,3-триметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-она и 4-бромопиридина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (50%), в виде светло-желтой пены. MS (ESI, m/z): 333.5 [(М+Н)+].
Пример 78
1,3,3-триметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
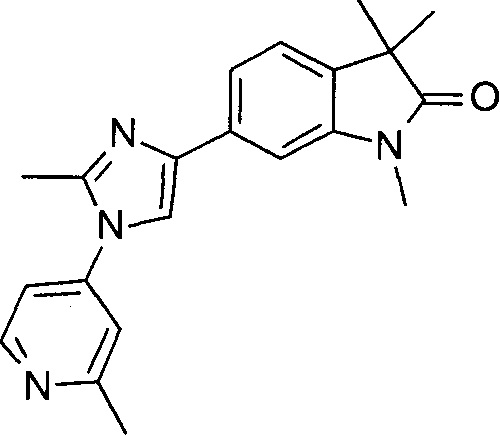
Пример 78 получили из 1,3,3-триметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-она из примера 77а и 4-бромо-2-метилпиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (46%), в виде светло-желтой пены. MS (ESI, m/z): 347.5 [(М+Н)+].
Пример 79
6-(1-(3-фторпиридин-4-ил)-2-метил-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
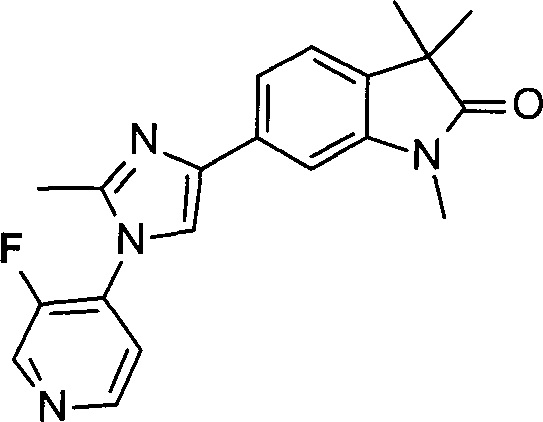
Пример 79 получили из 1,3,3-триметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-она из примера 77а и 4-бромо-3-фторпиридина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (23%), в виде светло-коричневой пены. MS (ESI, m/z): 351.5 [(М+Н)+].
Пример 80
1,3,3-триметил-6-(5-(6-метилпиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
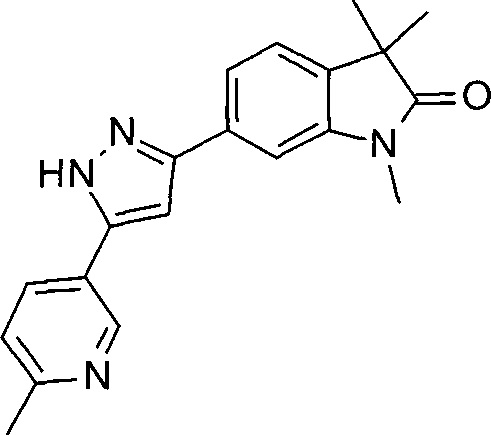
a) 1-(6-Метилпиридин-3-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-дион
Соединение, указанное в заголовке, получили из 6-ацетил-1,3,3-триметилиндолин-2-она из примера 3а и метил 6-метилникотината по аналогии с примером 42а и получили в виде желтого масла (48%). MS (ESI, m/z): 337.6 [(М+H)+].
b) 1,3,3-триметил-6-(5-(6-метилпиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он (Пример 80)
Пример 80 получили из 1-(6-метилпиридин-3-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона по аналогии с примером 56 с получением соединения, указанного в заголовке (69%), в виде желтого осадка. MS (ESI, m/z): 333.8 [(М+Н)+].
Пример 81
1,3,3-триметил-6-(1-метил-5-(2-метилпиридин-4-ил)-1Н-пиразол-3-ил)индолин-2-он
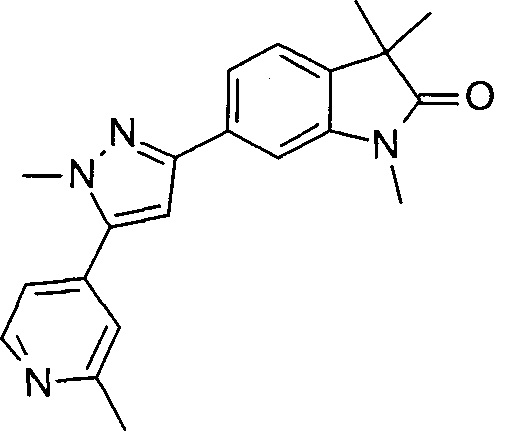
Пример 81 получили по аналогии с примером 61b с использованием метилгидразина. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 5% МеОН в дихлорметане) с получением 1,3,3-триметил-6-(1-метил-3-(2-метилпиридин-4-ил)-1Н-пиразол-5-ил)индолин-2-она (67%) в виде более быстро элюируемого изомера в виде белого осадка. Более медленно элюируемый изомер содержал соединение, указанное в заголовке (29%), в виде белого осадка. MS (ESI, m/z): 347.5 [(М+Н)+].
Пример 82
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)пиримидин-4-ил)индолин-2-он
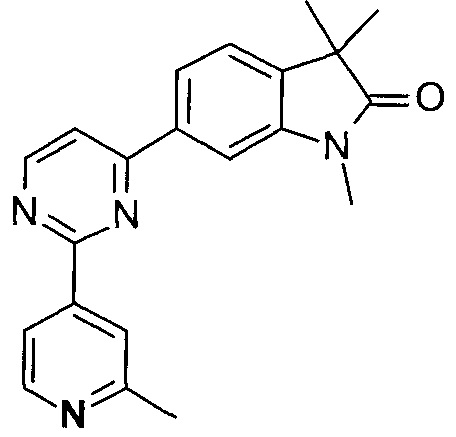
a) 1,3,3-триметил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)индолин-2-он
Смесь 6-бромо-1,3,3-триметилиндолин-2-она (5.00 г) из примера 2а, бис(пинаколато)дибора (7.57 г) и ацетата калия (3.90 г) в ДМСО (66 мл) продули аргоном, затем добавили [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (720 мг) и перемешивание продолжили при 110°С в течение 16 ч. Смесь отфильтровали, фильтрат разделили между водной соляной кислотой (0.1 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 40% EtOAc в н-гептане) с последующим тритурированием с EtOAc/н-гептаном (1:1) с получением соединения, указанного в заголовке (4.16 г, 70%), в виде белого осадка. MS (ESI, m/z): 302.2 [(М+Н)+].
b) 6-(2-Хлорпиримидин-4-ил)-1,3,3-триметилиндолин-2-он
Смесь 1,3,3-триметил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)индолин-2-она (450 мг), 4-бромо-2-хлорпиримидина (578 мг) и водного карбоната натрия (2 М, 1.5 мл) в 1,4-диоксане (8 мл) продули аргоном, затем добавили [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (61 мг) и перемешивание продолжили при 80°С в течение 2 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (Si-NH2, градиент, 0% до 50% EtOAc в н-гептане) с получением соединения, указанного в заголовке (367 мг, 85%), в виде белого осадка. MS (ESI, m/z): 288.4 [(М+Н)+].
c) 1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)пиримидин-4-ил)индолин-2-он (Пример 82)
Смесь 6-(2-хлорпиримидин-4-ил)-1,3,3-триметилиндолин-2-она (110 мг), 2-метилпиридин-4-илбороновой кислоты (106 мг) и карбоната цезия (500 мг) в ТГФ (3 мл) и воде (1.5 мл) продули аргоном, [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (32 мг) добавили и перемешивание продолжили при 80°С в течение 16 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (Si-NH2, градиент, 0% до 40% EtOAc в н-гептане) с получением соединения, указанного в заголовке (90 мг, 68%), в виде светло-желтой пены. MS (ESI, m/z): 345.6 [(М+Н)+].
Пример 83
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)индолин-2-он
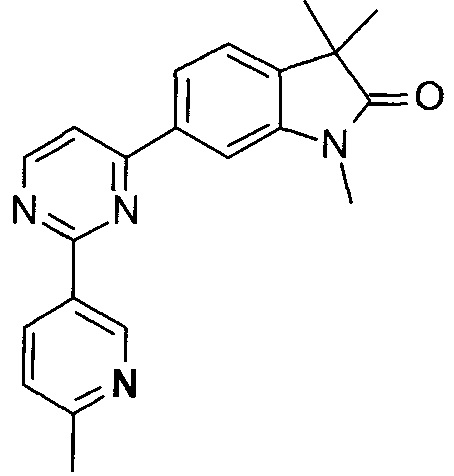
Пример 83 получили из 6-(2-хлорпиримидин-4-ил)-1,3,3-триметилиндолин-2-она из примера 82b и 6-метилпиридин-3-илбороновой кислоты по аналогии с примером 82с с получением соединения, указанного в заголовке (108 мг, 82%), в виде белого осадка. MS (ESI, m/z): 345.6 [(М+Н)+].
Пример 84
1,3,3-триметил-6-(4-метил-3-(2-метилпиридин-4-ил)-1Н-пиразол-5-ил)индолин-2-он
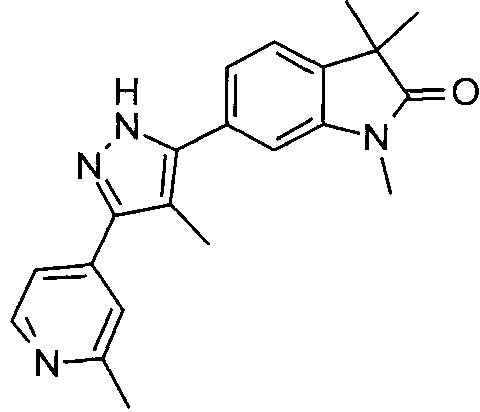
а) 2-метил-1-(2-метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-дион
К смеси 1-(2-метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона из примера 61а (433 мг) и карбоната калия (267 мг) в ДМФ (1.5 мл) добавили йодометан (201 мг) и перемешивание продолжили при 60°С в течение 16 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (Si-NH2, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (89 мг, 20%), в виде светло-коричневого осадка. MS (ESI, m/z): 351.6 [(М+Н)+].
b) 1,3,3-триметил-6-(4-метил-3-(2-метилпиридин-4-ил)-1Н-пиразол-5-ил)индолин-2-он (Пример 84)
Раствор 2-метил-1-(2-метилпиридин-4-ил)-3-(1,3,3-триметил-2-оксоиндолин-6-ил)пропан-1,3-диона (89 мг), моногидрата п-толуолсульфоновой кислоты (3 мг) и моногидрата гидразина (254 мг) в ТГФ (1.2 мл) перемешивали 70°С в течение 17 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (Si-NH2, градиент, 0% до 70% EtOAc в н-гептане) с получением соединения, указанного в заголовке (65 мг, 74%), в виде светло-желтого осадка. MS (ESI, m/z): 347.5 [(М+Н)+].
Пример 85
3,3-диметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)-1-(оксетан-3-ил)индолин-2-он
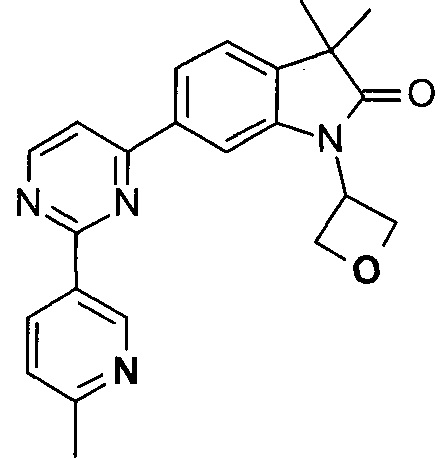
a) 6-(2-Хлорпиримидин-4-ил)-3,3-диметил-1-(оксетан-3-ил)индолин-2-он
Соединение, указанное в заголовке, получили из 6-бромо-3,3-диметил-1-(оксетан-3-ил)индолин-2-она из примера 6а по аналогии с примером 82а-b и получили в виде светло-коричневого осадка. MS (ESI, m/z): 330.1 [(М+Н)+].
b) 3,3-диметил-6-(2-(6-метилпиридин-3-ил)пиримидин-4-ил)-1-(оксетан-3-ил)индолин-2-он (Пример 85)
Пример 85 получили из 6-(2-хлорпиримидин-4-ил)-3,3-диметил-1-(оксетан-3-ил)индолин-2-она и 6-метилпиридин-3-илбороновой кислоты по аналогии с примером 82с с получением соединения, указанного в заголовке (85%), в виде коричневого осадка. MS (ESI, m/z): 387.2 [(М+Н)+].
Пример 86
1-циклопропил-3,3-диметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
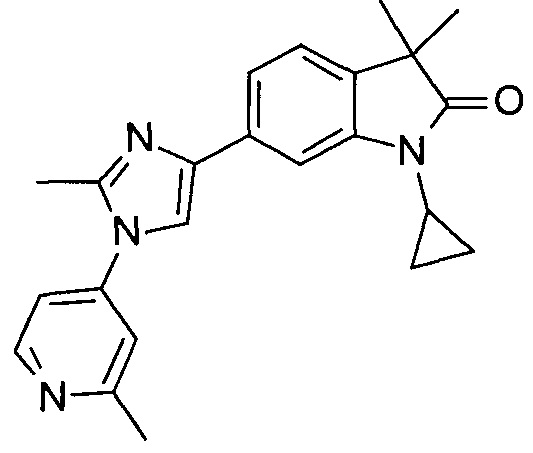
а) 6-ацетил-1-циклопропил-3,3-диметилиндолин-2-он
Соединение, указанное в заголовке, получили из 6-бромо-1-циклопропил-3,3-диметилиндолин-2-она из примера 1b по аналогии с примером 3а и получили в виде светло-желтого осадка (45%). MS (ESI, m/z): 244.6 [(М+Н)+].
b) 6-(2-Бромоацетил)-1-циклопропил-3,3-диметилиндолин-2-он
К раствору 6-ацетил-1-циклопропил-3,3-диметилиндолин-2-она (1.00 г) в ТГФ (24 мл) и МеОН (16 мл) добавили раствор тетра-н-бутиламмония трибромида (2.02 г) в ТГФ (8 мл) и перемешивание продолжили при 50°С в течение 5 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 30% EtOAc в н-гептане) с получением неочищенного соединения, указанного в заголовке (1.39 г, 87%), в виде желтого вязкого масла, которое использовали без дополнительной очистки. MS (ESI, m/z): 322.0/324.0 [(М+Н)+].
c) 1-циклопропил-3,3-диметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-он
К раствору ацетамида (631 мг) в дихлорметане (45 мл) добавили при 22°С раствор 6-(2-бромоацетил)-1-циклопропил-3,3-диметилиндолин-2-она (1.40 г) в дихлорметане (5 мл) и перемешивание продолжили в течение 16 ч. Смесь разделили между водным карбонатом натрия (2 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (543 мг, 44%), в виде фиолетовой пены. MS (ESI, m/z): 282.5 [(M+H)+]
d) 1-циклопропил-3,3-диметил-6-(2-метил-1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он (Пример 86)
Пример 86 получили из 1-циклопропил-3,3-диметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-она и 4-бромо-2-метилпиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (51%), в виде коричневого осадка. MS (ESI, m/z): 373.2 [(М+Н)+].
Пример 87
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-2-метил-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
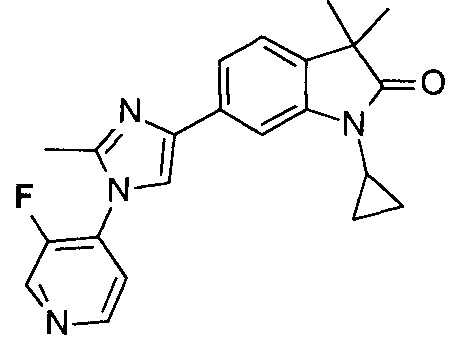
Пример 87 получили из 1-циклопропил-3,3-диметил-6-(2-метил-1Н-имидазол-5-ил)индолин-2-она из примера 86с и 4-бромо-3-фторпиридина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (25%), в виде светло-коричневой пены. MS (ESI, m/z): 377.2 [(М+Н)+].
Пример 88
1,3,3-триметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
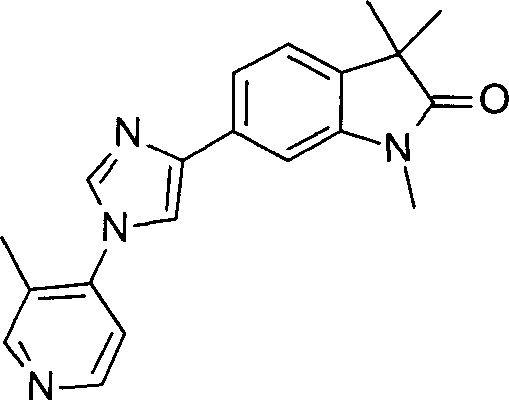
Пример 88 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d и 4-бромо-3-пиколина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (58%), в виде коричневого осадка. MS (ESI, m/z): 333.2 [(М+Н)+].
Пример 89
1-циклопропил-3,3-диметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
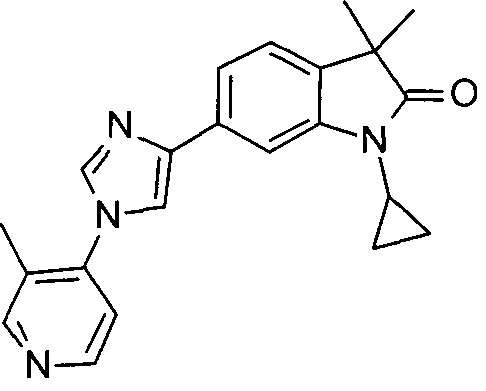
Пример 89 получили из 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она из примера 71а и 4-бромо-3-пиколина гидрохлорида по аналогии с примером 59е с получением соединения, указанного в заголовке (54%), в виде светло-желтой пены. MS (ESI, m/z): 359.2 [(М+Н)+].
Пример 90
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1Н-пирроло[3,2-с]пиридин-2(3Н)-он

a) 6-хлор-1-циклопропил-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
Смесь 6-хлор-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-она (600 мг, полученный в соответствии с Woolford et al., WO 2012143726), циклопропилбороновой кислоты (524 мг), ацетата меди(II) (582 мг) и DMAP (1.12 г) в толуоле (50 мл) продули аргоном, затем обработали натрия бис(триметилсилил)амидом (2 M в ТГФ, 1.6 мл) и перемешивание продолжили при 95°С в течение 16 ч. Смесь разделили между водной соляной кислотой (1 М) и ТВМЕ, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 30% EtOAc в н-гептане) с получением соединения, указанного в заголовке (547 мг, 76%), в виде белого осадка. MS (ESI, m/z): 237.5 [(М+Н)+].
b) 4-(1-циклопропил-3,3-диметил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6-ил)-N,N-диметил-1Н-имидазол-1-сульфонамид
Смесь 6-хлор-1-циклопропил-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-она (195 мг) и N,N-диметил-4-(трибутилстаннил)-1Н-имидазол-1-сульфонамида (478 мг, полученный в соответствии с Altenbach et al., J. Med. Chem. 51, 6571, 2008) в безводном ДМФ (4 мл) продули аргоном, затем добавили тетракис(трифенилфосфин)палладий(0) (114 мг) и перемешивание продолжили при 80°С в течение 16 ч. Смесь разделили между насыщенным водным гидрокарбонатом натрия и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (193 мг, 62%) в виде белого осадка.
c) 1-циклопропил-6-(1Н-имидазол-4-ил)-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
Суспензию 4-(1-циклопропил-3,3-диметил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6-ил)-N,N-диметил-1Н-имидазол-1-сульфонамида (193 мг) в водной соляной кислоте (2 М, 8 мл) нагревали до 100°С в течение 2 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 10% МеОН в дихлорметане, содержащем NH4OH) с получением соединения, указанного в заголовке (123 мг, 89%), в виде белой пены. MS (ESI, m/z): 269.2 [(М+Н)+].
d) 1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1Н-пирроло[3,2-с]пиридин-2(3Н)-он (Пример 90)
Суспензию 1-циклопропил-6-(1Н-имидазол-4-ил)-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-она (80 мг), 4-фтор-2-метилпиридина (42 мг) и карбоната цезия (185 мг) в ацетонитриле (1 мл) нагрели до температуры кипения в течение 3 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (59 мг, 55%), в виде белой пены. MS (ESI, m/z): 360.3 [(М+Н)+].
Пример 91
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-он
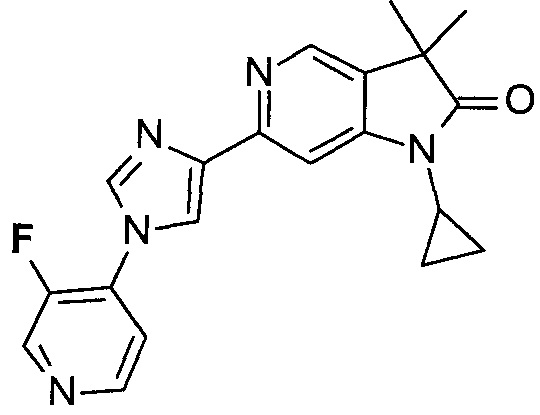
Пример 91 получили аналогично примеру 90d с использованием 3,4-дифторпиридина с получением соединения, указанного в заголовке (87%), в виде белой пены. MS (ESI, m/z): 364.2 [(М+Н)+].
Пример 92
3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
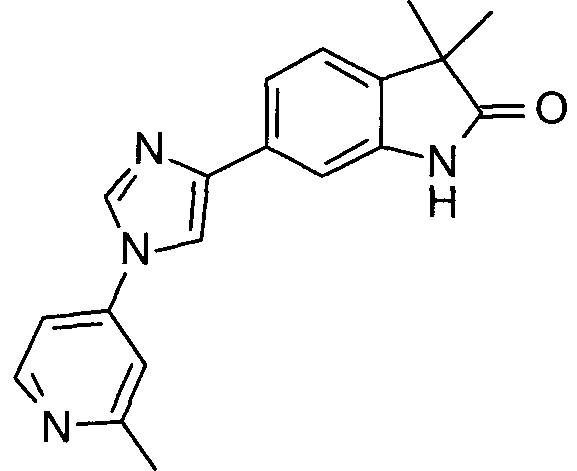
a) 6-(2-Бромоацетил)-3,3-диметилиндолин-2-он
Соединение, указанное в заголовке, получили из 6-бромо-3,3-диметилиндолин-2-она из примера 1а по аналогии с примером 3а-b и получили в виде белого осадка. MS (ESI, m/z): 282/284 [(М+Н)+].
b) 6-(1Н-Имидазол-4-ил)-3,3-диметилиндолин-2-он
Раствор 6-(2-бромоацетил)-3,3-диметилиндолин-2-она (1.00 г) в формамиде (24 мл) нагревали до 190°С в течение 5 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 15% МеОН в дихлорметане) с получением загрязненного соединения, указанного в заголовке (967 мг), в виде коричневого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 228.1 [(М+Н)+].
c) 3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он (Пример 92)
Смесь 6-(1Н-имидазол-4-ил)-3,3-диметилиндолин-2-она (100 мг), 4-фтор-2-метилпиридина (86 мг) и карбоната цезия (186 мг) в ацетонитриле (1 мл) нагревали до 110°С в течение 16 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 10% МеОН в дихлорметане) с последующей второй флеш-хроматографией (щелочной оксид алюминия, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (59 мг, 57%), в виде серо-белого осадка. MS (ESI, m/z): 319.3 [(М+Н)+].
Пример 93
3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он
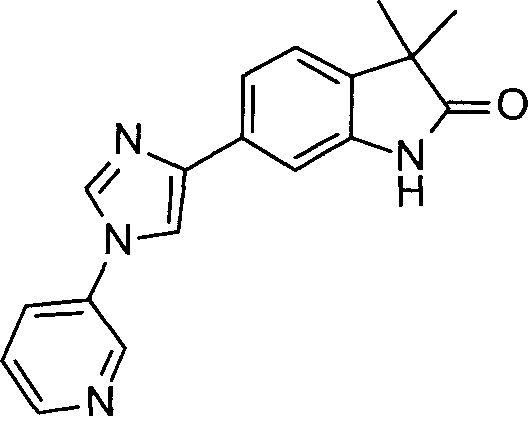
a) 6-(1Н-Имидазол-5-ил)-3,3-диметилиндолин-2-он
Соединение, указанное в заголовке, получили из 6-бромо-3,3-диметилиндолин-2-она по аналогии с примером 3а-b и использованием формамида в примере 3с и получили в виде коричневого осадка. MS (ESI, m/z): 228.1 [(М+Н)+].
b) 3,3-диметил-6-(1-(пиридин-3-ил)-1Н-имидазол-4-ил)индолин-2-он (Пример 93)
Суспензию 6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она (120 мг), 3-бромопиридина (200 мг), карбоната калия (219 мг) и 2-ацетилциклогексанона (37 мг) в ДМСО (2.5 мл) продули аргоном, затем хлорид меди(I) (26 мг) добавили и перемешивание продолжили при 130°С в течение 9 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, 0% до 10% МеОН в дихлорметане) с последующей ВЭЖХ хроматографией (RP-18, градиент, ацетонитрил/вода) с получением соединения, указанного в заголовке (19 мг, 12%), в виде белого осадка. MS (ESI, m/z): 305.1 [(М+Н)+].
Пример 94
1-циклопропил-3,3-диметил-6-[2-(2-метил-пиридин-4-ил)-оксазол-5-ил]-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
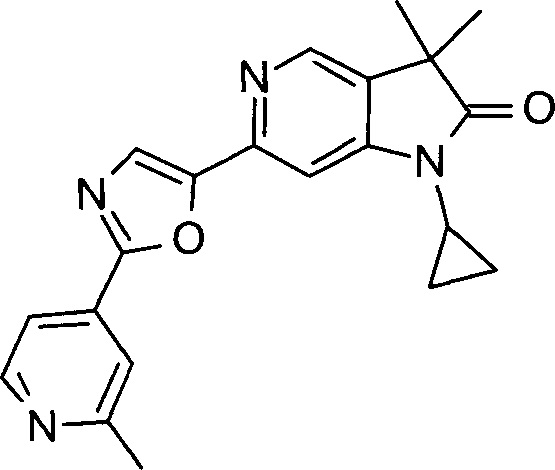
Смесь 2-(2-метилпиридин-4-ил)оксазола (0.13 г) из примера 22а, 6-хлор-1-циклопропил-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-она (0.384 г) из примера 90а и карбоната цезия (0.52 г) в диоксане (5 мл) продули аргоном, затем добавили Pd(OAc)2 (18 мг) и 2-(дициклогексилфосфино)бифенил (57 мг) и перемешивание продолжили при 110°С в течение 16 ч. Смесь разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 30% EtOAc в н-гептане) с получением соединения, указанного в заголовке (70 мг, 24%), в виде светло-желтого осадка. MS (ESI, m/z): 361.2 [(М+Н)+].
Пример 95
6-(1-(5-фтор-2-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
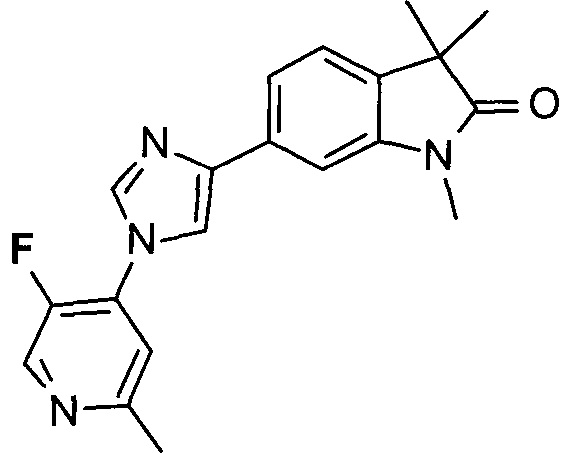
Пример 95 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d и 4-бромо-5-фтор-2-метилпиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (58%), в виде светло-коричневого масла. MS (ESI, m/z): 351.2 [(М+Н)+].
Пример 96
6-(2-(5-фтор-2-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он
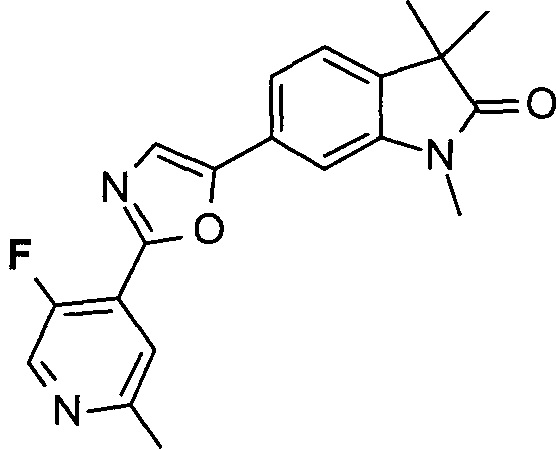
а) 6-(2-Азидоацетил)-1,3,3-триметилиндолин-2-он
К раствору 6-(2-бромоацетил)-1,3,3-триметилиндолин-2-она (1.75 г) из примера 3b в ацетоне (18 мл) добавили при 22°С азид натрия (767 мг) и перемешивание продолжили в течение 6 ч.
Смесь разделили между водой и дихлорметаном, органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (1.51 г, 99%), в виде светло-желтого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 259.1 [(М+Н)+].
b) 6-(2-(5-фтор-2-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он (Пример 96)
К раствору трифенилфосфина (570 мг) в толуоле (4 мл) последовательно добавили при 22°С 6-(2-азидоацетил)-1,3,3-триметилиндолин-2-он (330 мг) и раствор 5-фтор-2-метилизоникотиноилхлорид (222 мг) в толуоле (2 мл) и перемешивание продолжили в течение 2 ч.
Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 20% до 100% EtOAc в н-гептане) и с помощью препаративной ВЭЖХ (RP-18, градиент, ацетонитрил/вода) с получением соединения, указанного в заголовке (50 мг, 11%) в виде светло-желтого осадка. MS (ESI, m/z): 352.2 [(М+Н)+].
Пример 97
3,3-диметил-6-[5-(2-метил-пиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-1-оксетан-3-ил-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
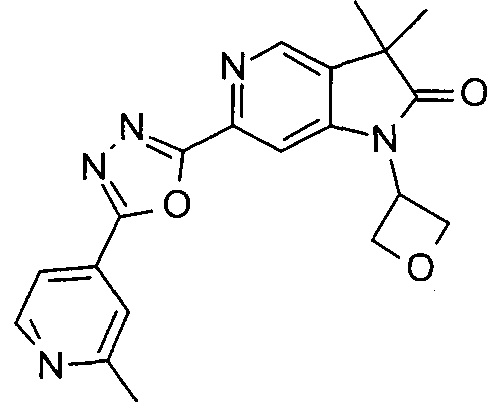
а) 6-хлор-3,3-диметил-1-оксетан-3-ил-1,3-дигидро-пирроло[3,2-с]пиридин-2-он
Смесь 6-хлор-3,3-диметил-1Н-пирроло[3,2-с]пиридин-2(3Н)-она (2.65 г, полученный в соответствии с Woolford et al., WO 2012143726), 3-бромооксетана (1.85 мл) и карбоната цезия (8.78 г) в ДМФ (20 мл) нагревали до 60°С в течение 16 ч. Смесь разделили между насыщенным водным хлоридом аммония и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 30% EtOAc в н-гептане), с получением соединения, указанного в заголовке (2.90 г, 85%) в виде белого осадка. MS (ESI, m/z): 252.8 [(М+Н)+].
b) 3,3-диметил-1-оксетан-3-ил-2-оксо-2,3-дигидро-1Н-пирроло[3.2-с1пиридин-6-карбоновой кислоты метиловый эфир
К раствору 6-хлор-3,3-диметил-1-оксетан-3-ил-1,3-дигидро-пирроло[3,2-с]пиридин-2-она (2.90 г) в МеОН (30 мл) и ДМФ (3 мл) добавили 1,1'-бис(дифенилфосфино)ферроцен-палладий(II)дихлорид дихлорметановый аддукт (0.87 г) и смесь карбонилировали при 100°С и давлении 150 фунт / кв. дюйм СО в течение 16 ч. Смесь эвапорировали и остаток разделили между водой и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (2.90 г, 92%), в виде коричневой смолы. MS (ESI, m/z): 276.8 [(М+Н)+].
c) 3,3-диметил-1-оксетан-3-ил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6-карбоновой кислоты гидразид
К раствору 3,3-диметил-1-оксетан-3-ил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6 карбоновой кислоты метилового эфира (0.50 г) в МеОН (10 мл) добавили при 22°С гидратгидразин (0.88 мл) и перемешивание продолжили в течение 3 ч. Смесь эвапорировали и остаток разделили между водой и дихлорметаном, органический слой высушили, эвапорировали и остаток тритурировали с н-пентаном с получением неочищенного соединения, указанного в заголовке (0.34 г, 68%), в виде коричневого осадка, который использовали без дополнительной очистки. MS (ESI, m/z): 276.8 [(М+Н)+].
d) 2-метил-изоникотиновой кислоты N'-(3,3-диметил-1-оксетан-3-ил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6-карбонил)-гидразид
К раствору 2-метил-изоникотиновой кислоты (100 мг) и тионилхлорида (3.0 мл) добавили ДМФ (0.05 мл) и перемешивание продолжили при 80°С в течение 4 ч. Смесь эвапорировали, остаток растворили в дихлорметане (5 мл), затем 3,3-диметил-1-оксетан-3-ил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6-карбоновой кислоты гидразид (180 мг) добавили при 22°С с последующим триэтиламином (0.2 мл) и перемешивание продолжали 12 ч. Смесь разделили между водным гидрокарбонатом натрия и дихлорметаном, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, дихлорметан/МеОН 99:1)) с получением соединения, указанного в заголовке (100 мг, 35%), в виде коричневого осадка. MS (ESI, m/z): 396.0 [(М+Н)+].
е) 3,3-диметил-6-[5-(2-метил-пиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-1-оксетан-3-ил-1,3-дигидро-пирроло[3,2-с]пиридин-2-он (Пример 97)
Пример 97 получили из 2-метил-изоникотиновой кислоты N'-(3,3-диметил-1-оксетан-3-ил-2-оксо-2,3-дигидро-1Н-пирроло[3,2-с]пиридин-6-карбонил)-гидразида по аналогии с примером 11b с получением соединения, указанного в заголовке (63%), в виде белого осадка. MS (ESI, m/z): 378.3 [(М+Н)+].
Пример 98
6-(1-(2-фтор-5-метилпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
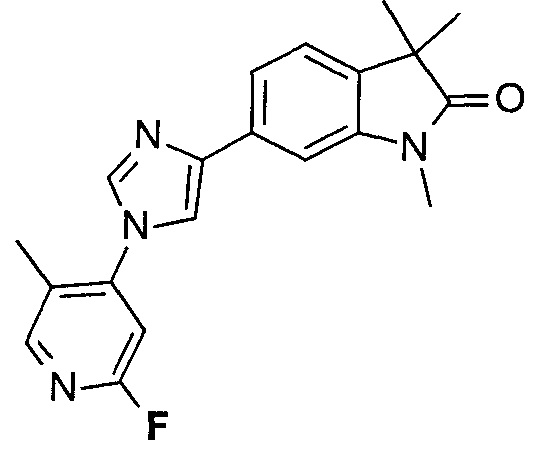
Пример 98 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d и 2-фтор-4-йод-5-метилпиридина по аналогии с примером 59е с получением соединения, указанного в заголовке (12%), в виде светло-желтого осадка. MS (ESI, m/z): 351.2 [(М+Н)+].
Пример 99
6-(2-(2-фтор-5-метилпиридин-4-ил)оксазол-5-ил)-1,3,3-триметилиндолин-2-он
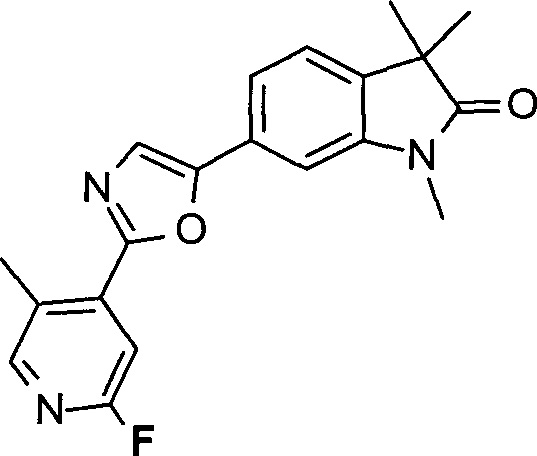
Пример 99 получили из 6-(2-азидоацетил)-1,3,3-триметилиндолин-2-она из примера 96а и 2-фтор-5-метилизоникотиноилхлорида по аналогии с примером 96b с получением соединения, указанного в заголовке (21%), в виде белого осадка. MS (ESI, m/z): 352.2 [(М+Н)+].
Пример 100
6-(5-(5-фтор-2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1,3,3-триметилиндолин-2-он
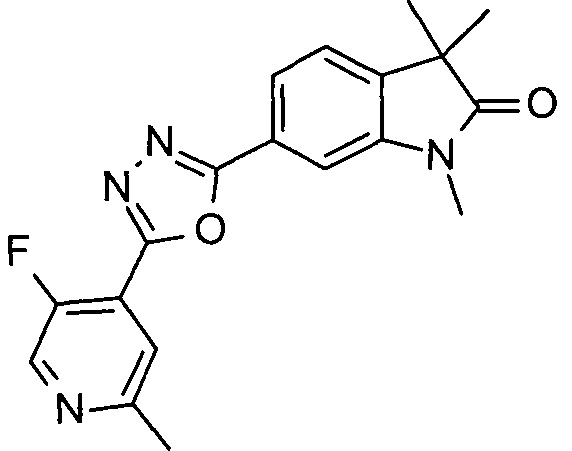
a) Метил 1,3,3-триметил-2-оксоиндолин-6-карбоксилат
К раствору метил 2-оксоиндолин-6-карбоксилата (4.08 г) и Mel (6.12 г) в ДМФ (61 мл) добавили при 22°С NaH (1.71 г) в течение 1.5 ч и перемешивание продолжили в течение 4 ч. Смесь разделили между водной соляной кислотой (1 М) и EtOAc, органический слой высушили, эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (0.64 г, 13%), в виде коричневого осадка. MS (ESI, m/z): 234.5 [(М+Н)+]. Вторую фракцию, содержащую 3,3-диметил-2-оксо-2,3-дигидро-1Н-индол-6-карбоновой кислоты метиловый эфир (3.82 г, 82%), выделили в виде коричневого осадка. MS (ESI, m/z): 220.5 [(М+Н)+].
b) 1,3,3-триметил-2-оксоиндолин-6-карбогидразид
Раствор метил 1,3,3-триметил-2-оксоиндолин-6-карбоксилата (350 мг) в метаноле (4 мл) и моногидратгидразина (751 мг) перемешивали при 22°С в течение 20 ч. Смесь эвапорировали и остаток разделили между водой и дихлорметаном, органический слой высушили и эвапорировали с получением неочищенного соединения, указанного в заголовке (340 мг, 97%), в виде белой пены, которую использовали без дополнительной очистки. MS (ESI, m/z): 234.1 [(М+Н)+].
c) N'-(5-фтор-2-метилизоникотиноил)-1,3,3-триметил-2-оксоиндолин-6-карбогидразид
В смесь 5-фтор-2-метилизоникотиновой кислоты (200 мг) в дихлорметане (7 мл) и ДМФ (1 мл) последовательно добавили при 22°С EDCI (198 мг), НОВТ (158 мг) и триэтиламин (163 мг) и перемешивание продолжили в течение 15 мин. 1,3,3-триметил-2-оксоиндолин-6-карбогидразид (165 мг) добавили и перемешивание продолжили в течение 18 ч. Смесь эвапорировали и остаток очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 10% МеОН в дихлорметане) с получением соединения, указанного в заголовке (186 мг, 62%), в виде желтого масла. MS (ESI, m/z): 371.1 [(М+Н)+].
d) 6-(5-(5-фтор-2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1,3,3-триметилиндолин-2-он (Пример 100)
Пример 100 получили из N'-(5-фтор-2-метилизоникотиноил)-1,3,3-триметил-2-оксоиндолин-6-карбогидразида по аналогии с примером 11b с получением соединения, указанного в заголовке (43%), в виде белого осадка. MS (ESI, m/z): 353.1 [(М+Н)+].
Пример 101
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-5-ил)индолин-2-он
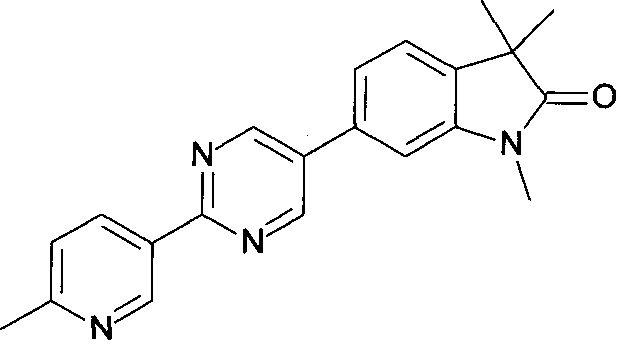
a) 6-(2-Хлорпиримидин-5-ил)-1,3,3-триметилиндолин-2-он
Пример 101а получили из 1,3,3-триметил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)индолин-2-она из примера 82а и 5-бромо-2-хлорпиримидина по аналогии с примером 82b с получением соединения, указанного в заголовке в виде белого осадка (195 мг, 58%). MS (ESI, m/z): 288.5 [(М+Н)+].
b) 1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-5-ил)индолин-2-он (Пример 101)
Пример 101 получили из 6-(2-хлорпиримидин-5-ил)-1,3,3-триметилиндолин-2-она и 6-метилпиридин-3-илбороновой кислоты по аналогии с примером 82с с получением соединения, указанного в заголовке, в виде белого осадка (85 мг 64%). MS (ESI, m/z): 345.5 [(М+Н)+].
Пример 102
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(6-метил-3-пиридил)индолин-2-он
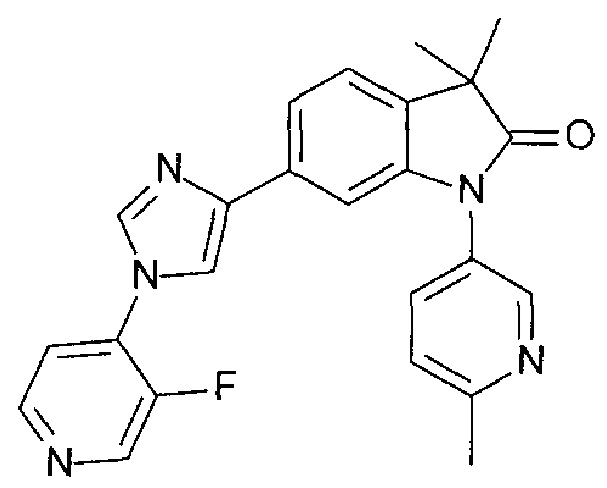
a) 6-(1Н-Имидазол-4-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-он Пример 102а получили из 6-бромо-1-(4-метоксибензил)-3,3-диметилиндолин-2-она (Пример 25а) по аналогии с примером 3а-b, 92b. Соединение, указанное в заголовке, получили в виде коричневого полутвердого вещества, и использовали без дополнительной очистки. MS (ESI, m/z): 348.3 [(М+Н)+].
b) 6-[1-(3-фтор-4-пиридил)имидазол-4-ил1-3,3-диметил-индолин-2-он
Пример 102b получили из 6-(1Н-имидазол-4-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-она по аналогии с примером 92 с (с использованием 3,4-дифторпиридин) и 63h. Соединение, указанное в заголовке, получили в виде серо-белого осадка. MS (ESI, m/z): 321.1 [(М+Н)+].
c) 6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(6-метил-3-пиридил)индолин-2-он (Пример 102)
К перемешанному раствору 6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-она (150 мг) в ацетонитриле (10 мл) добавили карбонат калия (141.4 мг) и 5-бромо-2-метил-пиридин (96.7 мг). Пробирку откачали и продули аргоном 3 раза. Получившуюся смесь перемешивали при комнатной температуре в течение ~2 минут. Затем смесь барботировали аргоном в течение 10 минут, CuI (10.0 мг) и N,N'-диметилэтилен-1,2-диамин (13.1 мг) добавили и барботирование продолжили в течение 10 минут. Затем реакционную смесь нагревали до 110°С в течение 5 часов. Реакционную смесь влили в воду со льдом и этилацетат. Слои разделили и водный слой экстрагировали этилацетатом. Объединенные органические слои высушили над сульфатом натрия, отфильтровали и сконцентрировали под вакуумом и остаток очистили с помощью колоночной флеш-хроматографии (силикагель, 0% до 10% МеОН в этилацетате). Соединение, указанное в заголовке, получили в виде серо-белого осадка (60 мг, 31%). MS (ESI, m/z): 414.2 [(М+Н)+].
Пример 103
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метил-4-пиридил)индолин-2-он
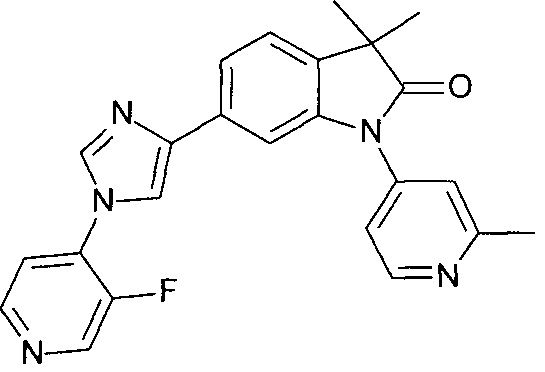
Пример 103 получили по аналогии с примером 102 с использованием 3,4-дифторпиридина для арилирвоания имидазола и 4-бромо-2-метилпиридина для арилирования лактама. Соединение, указанное в заголовке, получили в виде белого осадка (70 мг). MS (ESI, m/z): 414.4 [(М+Н)+].
Пример 104
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
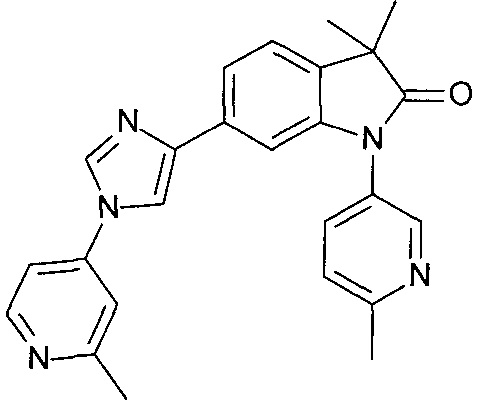
Пример 104 получили по аналогии с примером 102 с использованием 4-фтор-2-метилпиридина для арилирования имидазола и 5-бромо-2-метил-пиридина для арилирования лактама. Соединение, указанное в заголовке, получили в виде желтого осадка (60 мг). MS (ESI, m/z): 410.0 [(М+Н)+].
Пример 105
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
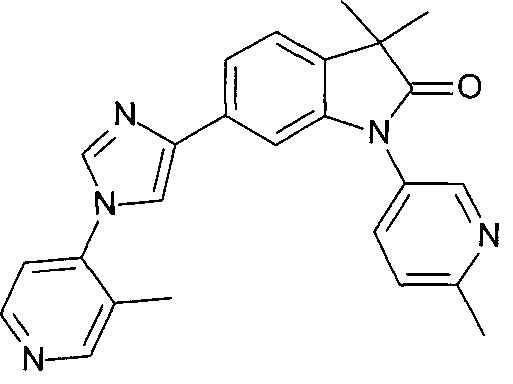
Пример 105 получили по аналогии с примером 102 с использованием 4-фтор-3-метилпиридина для арилирования имидазола и 5-бромо-2-метил-пиридина для арилирования лактама. Соединение, указанное в заголовке, получили в виде серо-белого осадка (55 мг). MS (ESI, m/z): 409.9 [(М+Н)+].
Пример 106
3,3-диметил-1-(2-метил-4-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
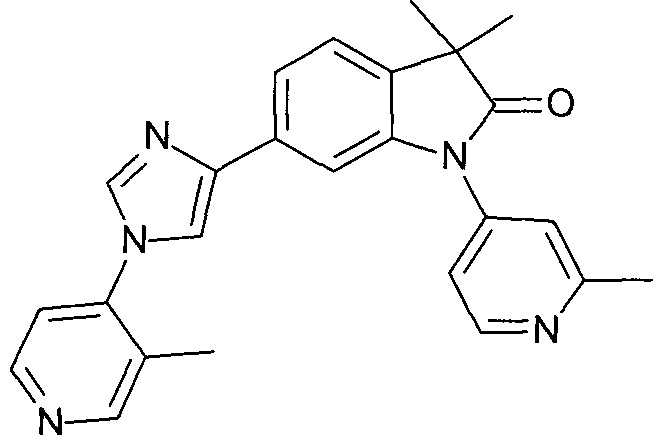
Пример 106 получили по аналогии с примером 102 с использованием 4-фтор-3-метилпиридина для арилирования имидазола и 4-бромо-2-метил-пиридина для арилирования лактама. Соединение, указанное в заголовке, получили в виде серо-белого осадка (52 мг). MS (ESI, m/z): 410.0 [(М+Н)+].
Пример 107
3,3-диметил-1-(2-метилпиридин-4-ил)-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
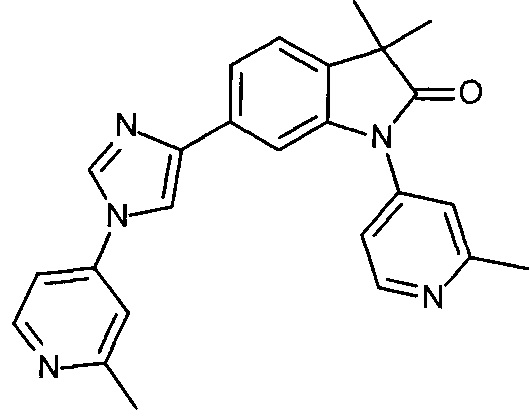
Пример 107 получили по аналогии с примером 102 с использованием 4-фтор-2-метилпиридина для арилирования имидазола и 4-бромо-2-метил-пиридина для арилирования лактама. Соединение, указанное в заголовке, получили в виде бесцветного аморфного осадка (35 мг). MS (ESI, m/z): 410.2 [(М+Н)+].
Пример 108
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1-(1-метил-1Н-имидазол-4-ил)индолин-2-он
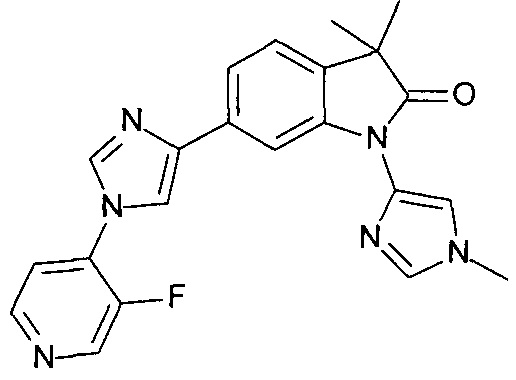
Пример 108 получили по аналогии с примером 102 с использованием 3,4-дифторпиридина для арилирования имидазола и 4-бромо-1-метил-1Н-имидазола для арилирования лактама. Соединение, указанное в заголовке, получили в виде коричневого аморфного осадка (25 мг). MS (ESI, m/z): 403.2 [(М+Н)+].
Пример 109
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметил-1-(1-метил-1Н-пиразол-3-ил)индолин-2-он
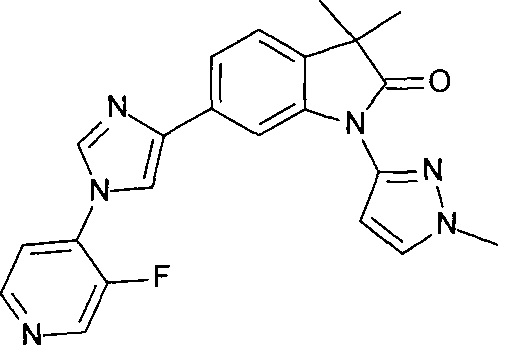
Пример 109 получили по аналогии с примером 102 с использованием 3,4-дифторпиридина для арилирования имидазола и 3-бромо-1-метил-1Н-пиразола для арилирования лактама. Соединение, указанное в заголовке, получили в виде серо-белого осадка (18 мг). MS (ESI, m/z): 403.2 [(М+Н)+].
Пример 110
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метилпиримидин-5-ил)индолин-2-он
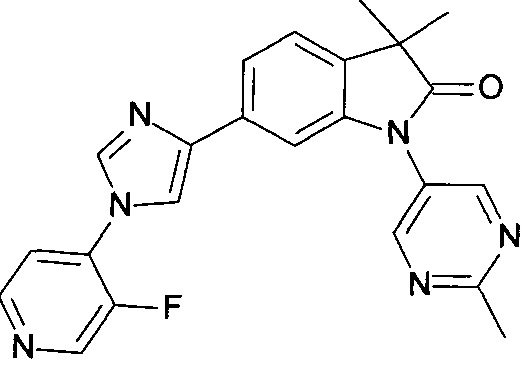
Пример 110 получили по аналогии с примером 102 с использованием 3,4-дифторпиридина для арилирования имидазола и 5-бромо-2-метил-пиримидина для арилирования лактама Соединение, указанное в заголовке, получили в виде светло-коричневого осадка (65 мг). MS (ESI, m/z): 415.2 [(М+Н)+].
Пример 111
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
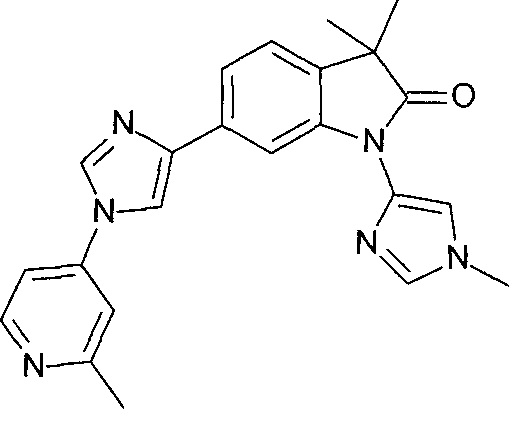
Пример 111 получили по аналогии с примером 102 с использованием 4-фтор-2-метилпиридина для арилирования имидазола и 4-бромо-1-метил-1Н-имидазола для арилирования лактама Соединение, указанное в заголовке, получили в виде светло-желтого осадка (60 мг). MS (ESI, m/z): 399.0 [(М+Н)+].
Пример 112
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
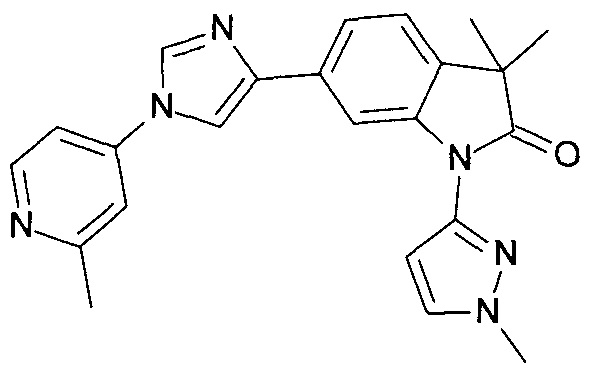
Пример 112 получили по аналогии с примером 102 с использованием 4-фтор-2-метилпиридина для арилирования имидазола и 3-бромо-1-метил-1Н-пиразола для арилирования лактама Соединение, указанное в заголовке, получили в виде оранжевого осадка (50 мг). MS (ESI, m/z): 399.4 [(М+Н)+].
Пример 113
3,3-диметил-6-[1-(2-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
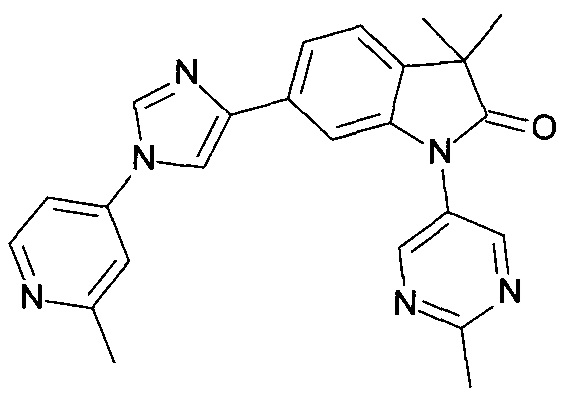
Пример 113 получили по аналогии с примером 102 с использованием 4-фтор-2-метилпиридина для арилирования имидазола и 5-бромо-2-метил-пиримидина для арилирования лактама Соединение, указанное в заголовке, получили в виде светло-желтого осадка (50 мг). MS (ESI, m/z): 411.3 [(М+Н)+].
Пример 114
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
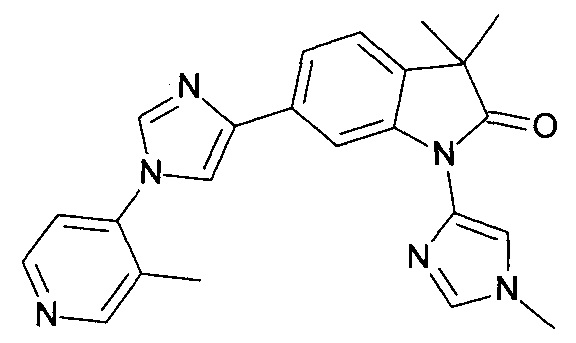
Пример 114 получили по аналогии с примером 102 с использованием 4-фтор-3-метилпиридина для арилирования имидазола и 4-бромо-1-метил-1Н-имидазола для арилирования лактама Соединение, указанное в заголовке, получили в виде серо-белого осадка (45 мг). MS (ESI, m/z): 399.4 [(М+Н)+].
Пример 115
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
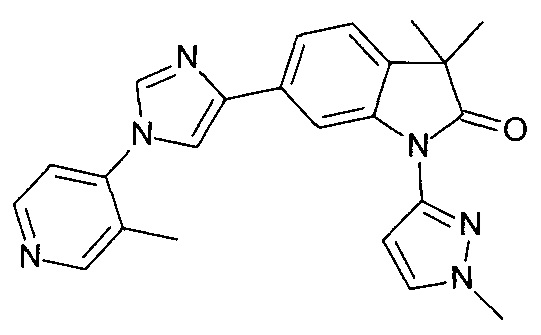
Пример 115 получили по аналогии с примером 102 с использованием 4-фтор-3-метилпиридина для арилирования имидазола и 3-бромо-1-метил-1Н-пиразола для арилирования лактама Соединение, указанное в заголовке, получили в виде серо-белого осадка (45 мг). MS (ESI, m/z): 399.2 [(М+Н)+].
Пример 116
3,3-диметил-6-[1-(3-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
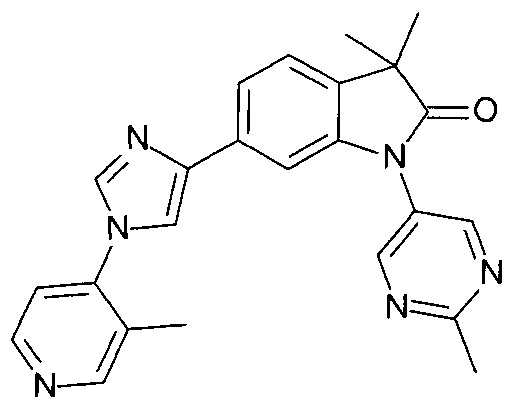
Пример 116 получили по аналогии с примером 102 с использованием 4-фтор-3-метилпиридина для арилирования имидазола и 5-бромо-2-метил-пиримидина для арилирования лактама Соединение, указанное в заголовке, получили в виде оранжевого осадка (70 мг). MS (ESI, m/z): 399.2 [(М+Н)+].
Пример 117
1-циклопропил-3,3-диметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
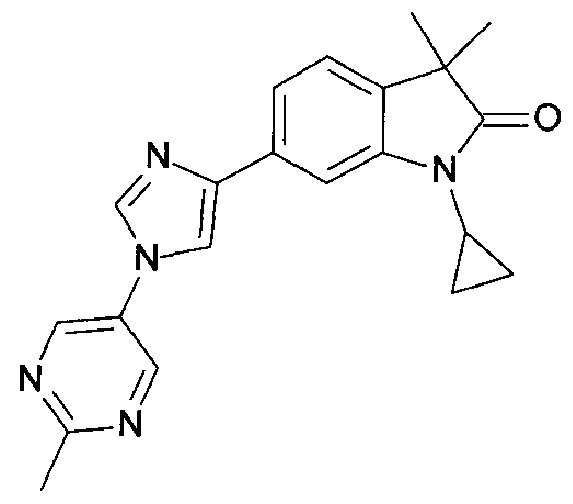
Пример 117 получили из 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она из примера 71а по аналогии с примером 59е с использованием 5-бромо-2-метилпиримидина. Соединение, указанное в заголовке, 10 получили в виде коричневого осадка (164 мг, 81%). MS (ESI, m/z): 360.2 [(М+Н)+].
Пример 118
1-циклопропил-3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
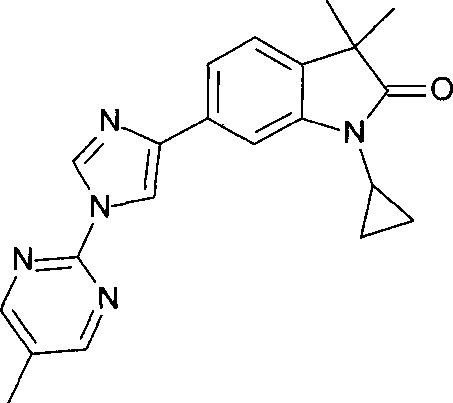
В закрытой стеклянной пробирке суспензию 1-циклопропил-6-(1Н-имидазол-5-ил)-3,3-диметилиндолин-2-она (Пример 71а, 70 мг), 2-хлор-5-метилпиримидина (37.0 мг) и карбоната цезия (158 мг) в ацетонитриле (1.05 мл) нагревали до 120°С в течение 30 минут при воздействии микроволнового излучения. Затем снова добавили 18 мг 2-хлор-5-метилпиримидина и 89 мг карбоната цезия и реакционную смесь нагревали до 120°С при обычном нагревании в течение 2 часов. Реакционную смесь сконцентрировали под вакуумом и очистили с помощью флеш-хроматографии (силикагель, градиент, 0% до 100% EtOAc в н-гептане). Соединение, указанное в заголовке, получили в виде серо-белого осадка (75 мг, 80%). MS (ESI, m/z): 360.2 [(М+Н)+].
Пример 119
1,3,3-триметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
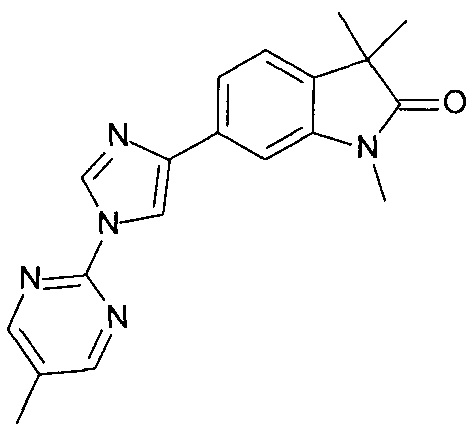
Пример 119 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d по аналогии с примером 118. Соединение, указанное в заголовке, получили в виде белого осадка (71 мг, 86%). MS (ESI, m/z): 334.2 [(М+Н)+].
Пример 120
1,3,3-триметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
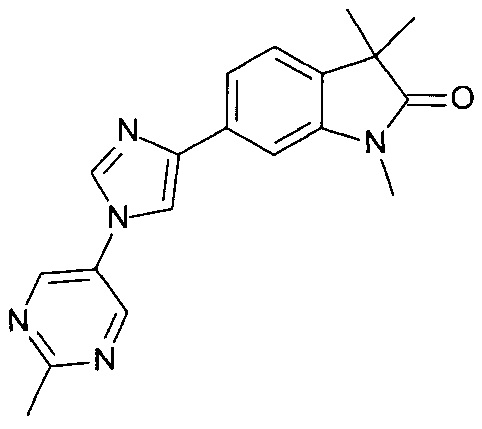
Пример 120 получили из 6-(1Н-имидазол-5-ил)-1,3,3-триметилиндолин-2-она из примера 59d по аналогии с примером 59е с использованием 5-бромо-2-метилпиримидина. Соединение, указанное в заголовке, получили в виде белого осадка (109 мг, 53%). MS (ESI, m/z): 334.2 [(М+Н)+].
Пример 121
3,3-диметил-6-(1-(2-метилпиримидин-5-ил)-1Н-имидазол-4-ил)индолин-2-он
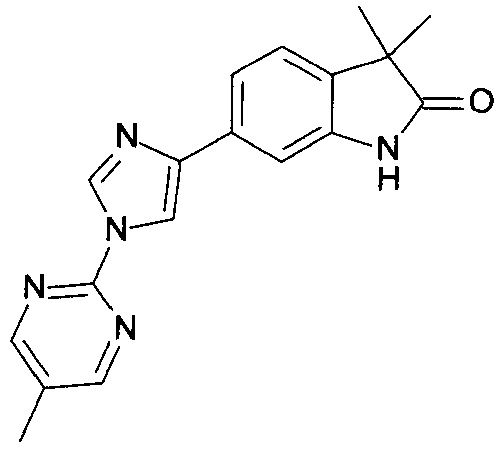
Пример 121 получили из 6-(1Н-имидазол-4-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-она (Пример 102а) по аналогии с примером 59е (с использованием 5-бромо-2-метилпиримидина) и примера 63h. Соединение, указанное в заголовке, получили в виде светло-желтого осадка (27 мг). MS (ESI, m/z): 320.2 [(М+Н)+].
Пример 122
3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
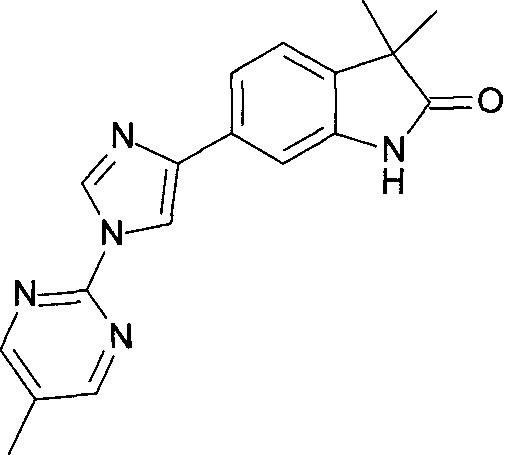
Пример 122 получили из 6-(1Н-имидазол-4-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-она из примера 102а по аналогии с примером 118 и 63h. Соединение, указанное в заголовке, получили в виде светло-желтого осадка (30 мг). MS (ESI, m/z): 320.2 [(М+Н)+].
Пример 123
3,3-диметил-6-(1-(6-метилпиридин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
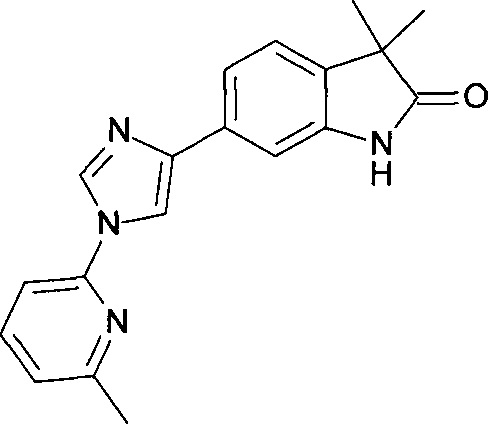
Пример 123 получили по аналогии с примером 102a-b с использованием 2-фтор-6-метилпиридина для арилирования имидазола. Соединение, указанное в заголовке, получили в виде светло-желтого осадка (41 мг). MS (ESI, m/z): 319.2 [(М+Н)+].
Пример 124
6-[4-(5-фтор-2-метил-4-пиридил)имидазол-1-ил]-1,3,3-триметил-индолин-2-он
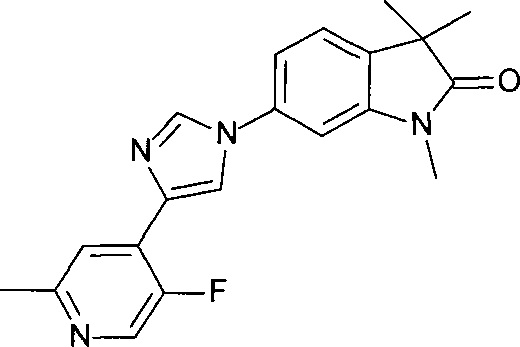
а) 6-(4-Бромоимидазол-1-ил)-1,3,3-триметил-индолин-2-он
К перемешанному раствору 6-бромо-1,3,3-триметилиндолин-2-она (Пример 2а, 1 г) в NMP (9 мл) добавили 4-бромо-1Н-имидазол (0.578 г), карбонат калия (1.71 г) и 2-ацетилциклогексанон (0.26 мл) и смесь барботировали аргоном в течение 15 минут. Затем CuCl (0.08 г) добавили в смесь и барботирование продолжили в течение дополнительных 10 минут. Реакционную пробирку закрыли и затем реакционную смесь нагревали до 130°С в течение 14 часов. Реакционную смесь разбавили водой и экстрагировали этилацетатом. Объединенные органические слои промыли водой с последующим солевым раствором. Органический слой высушили над сульфатом натрия и сконцентрировали под вакуумом. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, градиент 0-30% этилацетат в гексане). Соединение, указанное в заголовке, получили в виде серо-белого осадка (300 мг, 42%). MS (ESI, m/z): 320.1 [(М+Н)+].
b) 6-[4-(5-фтор-2-метил-4-пиридил)имидазол-1-ил1-1,3,3-триметил-индолин-2-он (Пример 124)
В пробирке для микроволновой печи к перемешанному раствору 6-(4-Бромоимидазол-1-ил)-1,3,3-триметил-индолин-2-она (100 мг) в смеси DME (3 мл) и воды (0.8 мл) добавили 5-фтор-2-метил-4-(тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (111 мг) и карбонат калия (259 мг). Реакционную смесь барботировали аргоном в течение 15 минут. Затем добавили PdCl2(PPh3)2 (11 мг) в реакционную смесь и барботирование продолжили в течение дополнительных 10 минут. Реакционную смесь нагревали до 130°С в течение 30 минут при воздействии микроволнового излучения. Получившуюся суспензию отфильтровали и фильтрат сконцентрировали под вакуумом. Неочищенный материал очистили с помощью флеш-хроматографии (силикагель, градиент 70-80% этилацетат в гексане) с последующей очисткой препаративной ТСХ с использованием этилацетата в качестве подвижной фазы. Соединение, указанное в заголовке, получили в виде серо-белого осадка (22 мг, 26%). MS (ESI, m/z): 350.9 [(М+Н)+].
Пример 125
1,3,3-триметил-6-[5-(3-метил-4-пиридил)изоксазол-3-ил]индолин-2-он
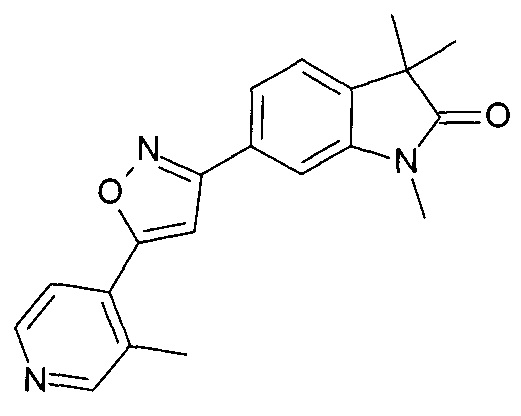
a) 1-(3-метил-4-пиридил)-3-(1,3,3-триметил-2-оксо-индолин-6-ил)пропан-1,3-дион
К перемешанному раствору of 6-ацетил-1,3,3-триметил-2,3-дигидро-1Н-индол-2-он (Пример 3а, 100 мг) в ТГФ (2 мл) добавили NaH (60% in oil, 39 мг) at 0°С и перемешивали в течение 30 минут при комнатной температуре. Then метил 3-метилпиридин-4-карбоксилат (63 мг) в ТГФ (1 мл) добавили и перемешивание при комнатной температуре continued в течение 21 часов. Затем реакционную смесь нагревали в течение 1 часа до 50°С. Реакционную смесь погасили водным насыщенным раствором хлорида аммония и экстрагировали EtOAc. Объединенные органические слои промыли солевым раствором, высушили над безводным сульфатом натрия и сконцентрировали под вакуумом. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, EtOAc в н-гексане 20%). Соединение, указанное в заголовке, получили в виде серо-белого осадка (60 мг, 52% на основании выделенного исходного соединения). MS (ESI, m/z): 337.0 [(М+Н)+].
b) 1,3,3-триметил-6-[5-(3-метил-4-пиридил)изоксазол-3-ил]индолин-2-он (Пример 125)
Пример 125 получили из 1-(3-метил-4-пиридил)-3-(1,3,3-триметил-2-оксо-индолин-6-ил)пропан-1,3-диона по аналогии с примером 42а. Соединение, указанное в заголовке, получили в виде серо-белого осадка (45 мг, 46%). Получили только данный изомер. MS (ESI, m/z): 334.1 [(М+Н)+].
Пример 126
1,3,3-триметил-6-[4-(3-метил-4-пиридил)имидазол-1-ил]индолин-2-он
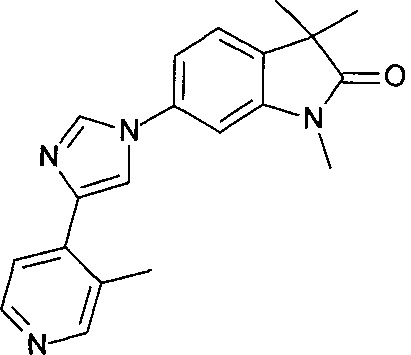
В пробирке для микроволновой печи к перемешанному раствору 6-(4-бромоимидазол-1-ил)-1,3,3-триметил-индолин-2-она (Пример 124а, 500 мг) в диоксане (5 мл) добавили (3-метил-4-пиридил)бороновую кислоту (256 мг) и NaOtBu (180 мг) и смесь барботировали аргоном. Затем добавили Brettphos (84 мг) и палладацикл Brettphos (125 мг) и снова барботировали аргоном. Реакционную смесь нагрели до 130°С при воздействии микроволнового излучения в течение 1 часа. Затем реакционную смесь охладили до комнатной температуры, отфильтровали и сконцентрировали под вакуумом. Неочищенное вещество очистили с помощью флеш-хроматографии (80% этилацетат в гексане). Соединение, указанное в заголовке, получили в виде серо-белого осадка (21.6 мг, 10% на основании выделенного исходного соединения). MS (ESI, m/z): 333.1 [(М+Н)+].
Пример 127
1,3,3-триметил-6-[4-(2-метил-4-пиридил)имидазол-1-ил]индолин-2-он
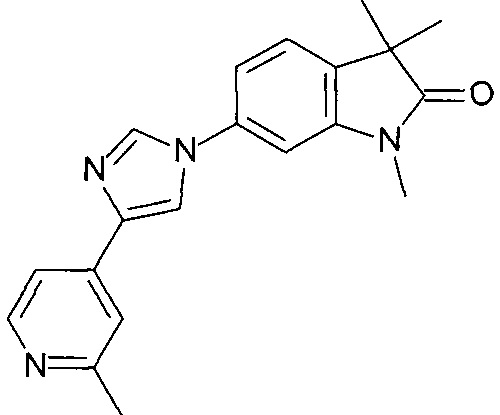
Пример 127 получили по аналогии с примером 126. Соединение, указанное в заголовке, получили в виде серо-белого осадка (20 мг, 9%). MS (ESI, m/z): 333.3 [(М+Н)+].
Пример 128
6-[4-(2-фтор-4-пиридил)имидазол-1-ил]-1,3,3-триметил-индолин-2-он
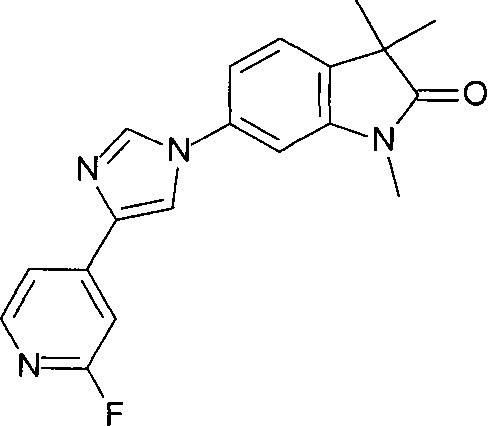
Пример 128 получили по аналогии с примером 126. Соединение, указанное в заголовке, получили в виде серо-белого осадка (8 мг, 14%). MS (ESI, m/z): 337.2 [(М+Н)+].
Пример 129
1-(3-циклопропилсульфонилпропил)-6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он
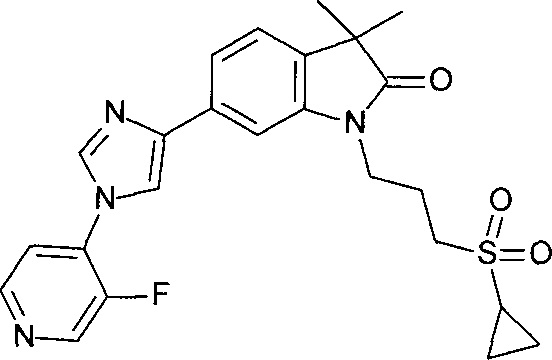
a) 6-бромо-1-(3-циклопропилсульфонилпропил)-3,3-диметил-индолин-2-он
Пример 129а получили из 6-бромо-3,3-диметил-индолин-2-она (Пример 1а) по аналогии с WO 2014/40969 А1, пример 65b и 70е. Соединение, указанное в заголовке, получили в виде серо-белого осадка (1.01 г). MS (ESI, m/z): 385.8, 387.8 [(М+Н)+].
b) 1-(3-циклопропилсульфонил пропил)-6-(1Н-имидазол-4-ил)-3,3-диметил-индолин-2-он
Пример 129b получили по аналогии с примером 3а-b и 92b. Соединение, указанное в заголовке, получили в виде коричневого осадка (0.6 г). MS (ESI, m/z): 374.1 [(М+Н)+].
c) 1-(3-циклопропилсульфонилпропил)-6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он (Пример 129)
Пример 129 получили по аналогии с примером 92с с сипользованием 3,4-дифторпиридина. Соединение, указанное в заголовке, получили в виде коричневого вязкообразного осадка (22 мг, 18%). MS (ESI, m/z): 469.3 [(М+Н)+].
Пример 130
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-1-(2-гидроксиэтил)-3,3-диметил-индолин-2-он
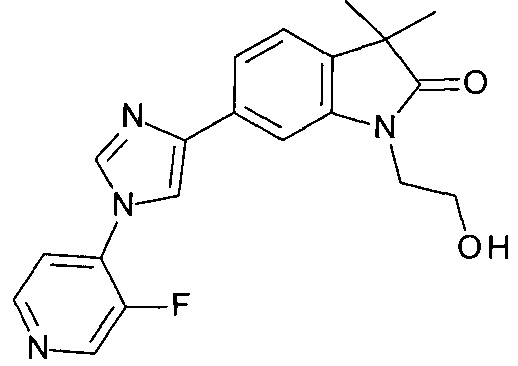
a) (2-Бромэтокси)(трет-бутил)диметилсилан
К перемешанному раствору TBDMSCI (3.5 г) в ДМФ (10 мл) добавили имидазол (1.77 г). Затем медленно добавили 2-бромоэтан-1-ол (2.5 г) по каплям и реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь погасили водой и экстрагировали гексаном. Объединенные органические слои высушили над безводным сульфатом натрия и сконцентрировали при пониженном давлении. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, градиент 0-3% этилацетат в гексане). Соединение, указанное в заголовке, получили в виде бесцветного масла (3.96 г, 83%). ЯМР совпал с литературными данными.
b) 1-[2-[трет-бутил(диметил)силил]оксиэтил]-6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он
К раствору соединения 6-[1-(3-фторо-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-она (Пример 102b, 430 мг) в ДМФ (3 мл) добавили Cs2CO3 (869.3 мг) и раствор 2-(2-бромэтокси)(трет-бутил)диметилсилана (638.3 мг) в ДМФ (2 мл). Пробирку закрыли и реакционную смесь нагревали до 70°С в течение 5 часов. Реакционную смесь влили в воду со льдом и этилацетат. Слои разделили и водный слой экстрагировали этилацетатом. Объединенные органические слои промыли водой, высушили над безводным сульфатом натрия и сконцентрировали при пониженном давлении. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, градиент 0-50% EtOAc в гексане). Соединение, указанное в заголовке, получили в виде коричневого осадка (260 мг, 33%). MS (ESI, m/z): 481.0 [(М+Н)+].
с) 6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-1-(2-гидроксиэтил)-3,3-диметил-индолин-2-он (Пример 130)
К раствору 1-[2-[трет-бутил(диметил)силил]оксиэтил]-6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-она (250 мг) в ТГФ (10 мл) добавили раствор TBAF (1 M в ТГФ, 0.5 мл) при 0°С. Через 15 минут реакционной смеси дали нагреться до комнатной температуры и перемешивали в течение 3 часов. Реакционную смесь разбавили водой (30 мл) и экстрагировали этилацетатом. Объединенные органические слои высушили над безводным сульфатом натрия и сконцентрировали при пониженном давлении. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, градиент 0-3% метанол в дихлорметане). Соединение, указанное в заголовке, получили в виде серо-белого осадка (71 мг, 37%). MS (ESI, m/z): 367.3 [(М+Н)+].
Пример 131
1-(3-циклопропилсульфонилпропил)-6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он
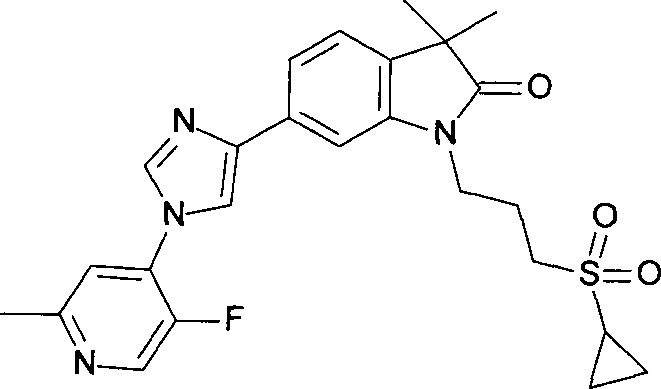
В закрытой пробирке к смеси 4-бромо-5-фтор-2-метилпиридина (66 мг), CsF (106 мг) и тетраметиламмония фторида (5 мг) в ДМСО (1 мл) нагревали до 120°С в течение 24 часов. Затем реакционную смесь охладили до комнатной температуры, 1-(3-циклопропилсульфонилпропил)-6-(1Н-имидазол-4-ил)-3,3-диметил-индолин-2-он (Пример 129b, 100 мг) и Cs2CO3 (131 мг) добавили, пробирку заново закрыли и реакционную смесь нагревали до 50°С в течение 12 часов. Реакционную смесь разбавили водой и экстрагировали этилацетатом. Объединенные органические слои промыли водой и солевым раствором, высушили над безводным сульфатом натрия и сконцентрировали под вакуумом. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, градиент 0-80% этилацетат в гексане) с последующей очисткой с помощью препаративной ТСХ. Соединение, указанное в заголовке получили в виде белого осадка (31 мг, 16%). MS (ESI, m/z): 483.1 [(М+Н)+].
Пример 132
6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он трифторацетат
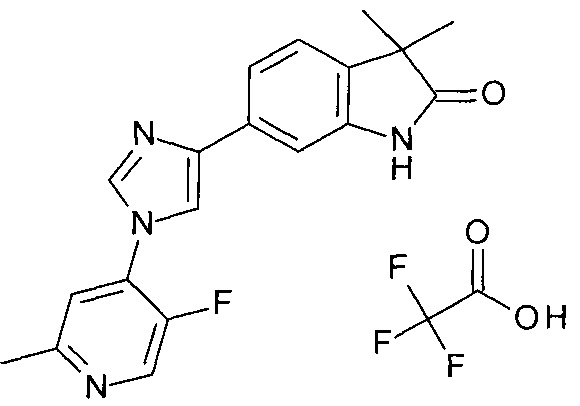
a) 6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-1-[(4-метоксифенил)метил]-3,3-диметил-индолин-2-он
Пример 132а получили по аналогии с примером 131 из 6-(1Н-имидазол-4-ил)-1-(4-метоксибензил)-3,3-диметилиндолин-2-она из примера 102а. Соединение, указанное в заголовке, получили в виде коричневого осадка (57 мг, 31%). MS (ESI, m/z): 457.0 [(М+Н)+].
b) 6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он трифторацетат (Пример 132)
В закрытой пробирке раствор 6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-1-[(4-метоксифенил)метил]-3,3-диметил-индолин-2-она (50 мг) в ТФУ (3 мл) нагревали до 110°С в течение 48 часов. Реакционную смесь сконцентрировали под вакуумом и остаток тритурировали эфиром и пентаном с получением соединения, указанного в заголовке, в виде зеленого воскообразного осадка. MS (ESI, m/z): 337.1 [(М+Н)+
Биологические анализы и данные
В настоящее время обнаружено, что соединения формулы I могут быть использованы для лечения заболеваний ЦНС.
Описанные соединения формулы I ослабляют L-687,414-индуцированную гиперлокомоцию. Это оценивали, используя компьютеризированную систему мониторинга физической активности животных Digiscan 16 (Omnitech Electronics, Columbus, Ohio) с целью количественного определения локомоторной активности. Животных содержали в условиях 12-ти часового цикла свет/темнота и эксперименты проводили во время светлого периода. Каждая камера для мониторинга физической активности состояла из бокса из оргстекла (41×41×28 см; ширина × длина × высота (W×L×H)) с подстилкой из опилок на полу, пересекаемого невидимыми горизонтальными и вертикальными инфракрасными лучами, регистрируемыми датчиками. Боксы для проведения испытаний были разделены крестом из оргстекла, обеспечивающим каждой мыши пространство для передвижения размером 20×20 см. Клетки подсоединяли к анализатору Digiscan, связанному с компьютером, который постоянно собирал информацию о состоянии лучей. Регистрации прерываний луча, падающего на фотоэлемент, для отдельных животных выполняли каждые 5 мин в продолжение сессии экспериментов и в качестве конечного параметра использовали сумму первых 6 периодов времени. Соединения вводили либо перорально (п./о.) за 15 мин до введения подкожной (п./к.) инъекции L-687,414 в концентрации 50 мг/кг, либо внутрибрюшинно (в./б.) одновременно с п./к. инъекцией L-687,414 в концентрации 50 мг/кг. Затем мышей переносили из клеток их пребывания в регистрирующие камеры для фазы привыкания в течение 15 мин, позволяющей осуществить свободное обследование нового окружения. Затем регистрировали горизонтальную активность в течение 30-минутного периода времени. Процент (%) ингибирования L-687,414-индуцированной гиперлокомоции рассчитывали согласно уравнению:
((Носитель+L-687,414 горизонтальная активность - лекарство+L-687,414 горизонтальная активность)/Носитель+L-687,414 горизонтальная активность) × 100
Величины ID50, определяемые как дозы каждого соединения, вызывающие 50%-ное ингибирование L-687,414-индуцированной гиперлокомоции, рассчитывали с применением линейного регрессионного анализа данных зависимости доза-ответ, используя компьютерную программу аппроксимации по точкам на основе Excel.
Поскольку данные не предполагают нормального распределения, статистическое сравнение групп, обработанных тестируемыми соединениями, с 5 контрольной группой (обработанной разбавителем) проводили, используя односторонние U-критерии Манна-Уитни. В статистике U-критерий Манна-Уитни (также называемый критерий Манна-Уитни-Уилкоксона (Mann-Whitney-Wilcoxon; MWW) или критерий суммы рангов Уилкоксона) представляет собой критерий непараметрической статистической гипотезы для оценки того, проявляет ли один 10 из двух образцов независимых наблюдений тенденцию иметь более высокие значения р по сравнению с другим. Это один из самых хорошо известных критериев непараметрической статистической значимости. Значение р дает вероятность того, что две группы будут существенно отличаться друг от друга, и в качестве меры оценки обычно принимают значение меньше 0,05; это означает, что имеется шанс более 95% для того, чтобы две группы реально отличались друг от друга. Значения р, приведенные в Таблице 1, являются односторонними, поскольку учитывали и тестировали только уменьшения локомоции (Mann Н.В., Whitney D.R. (1947), “On a Test of Whether one of Two Random Variables is Stochastically Larger than the Other”, Annals of Mathematical Statistics, 18 (1), 50-60.
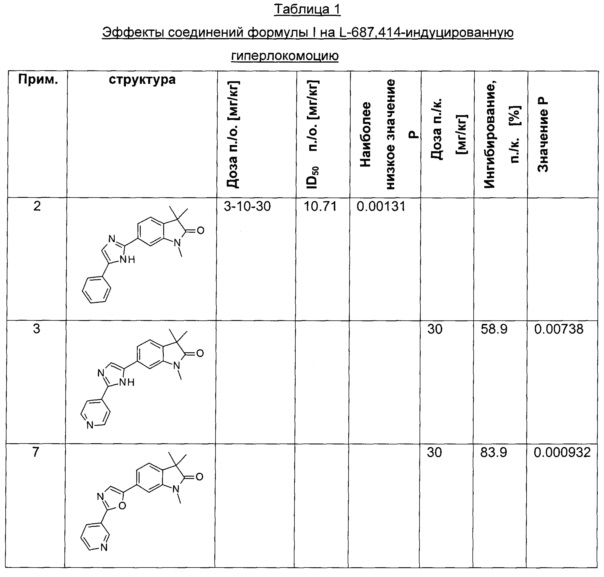
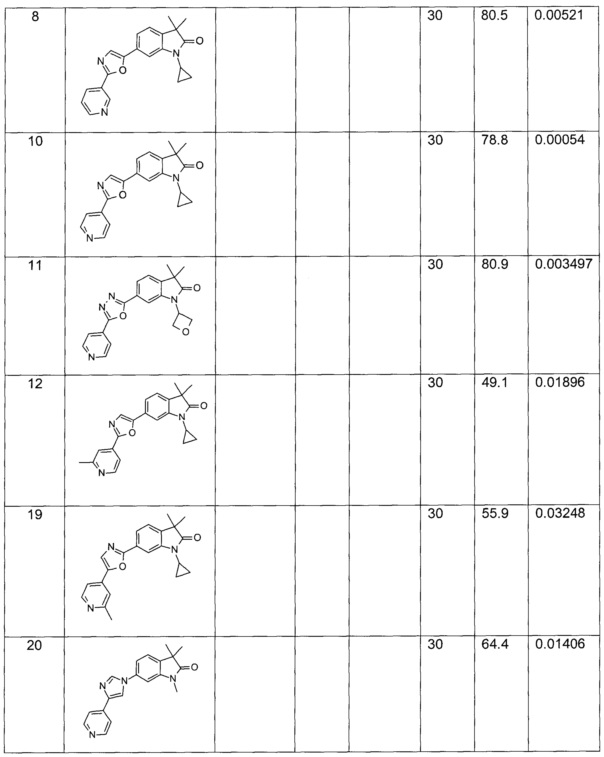
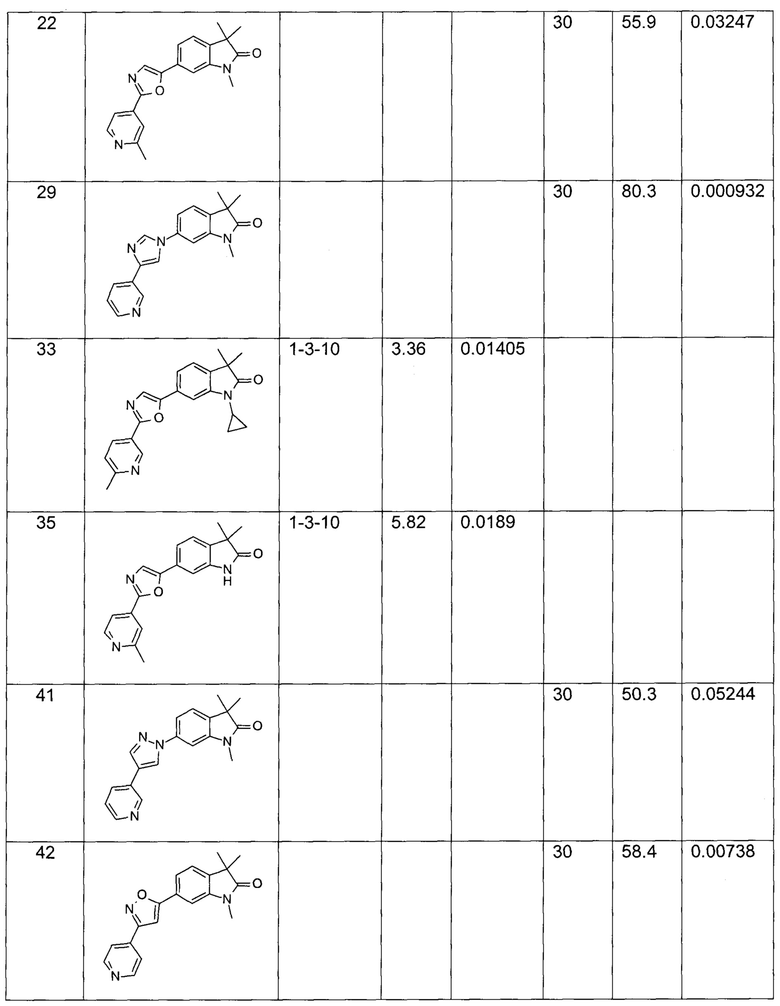
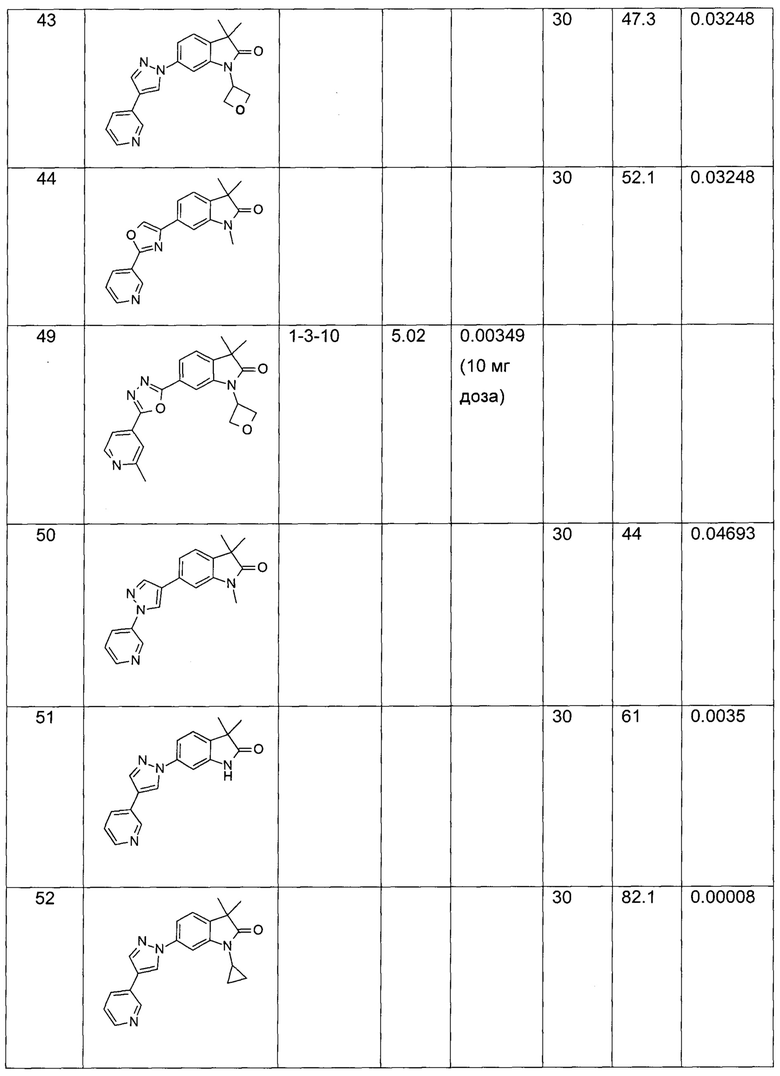
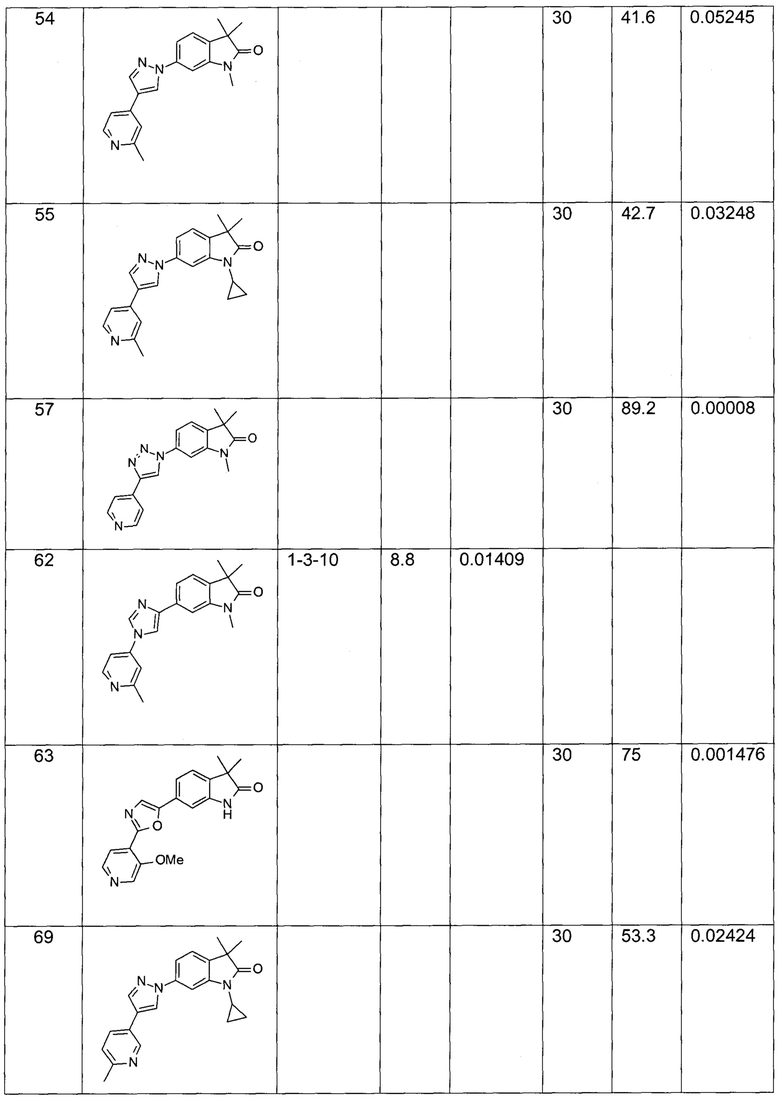
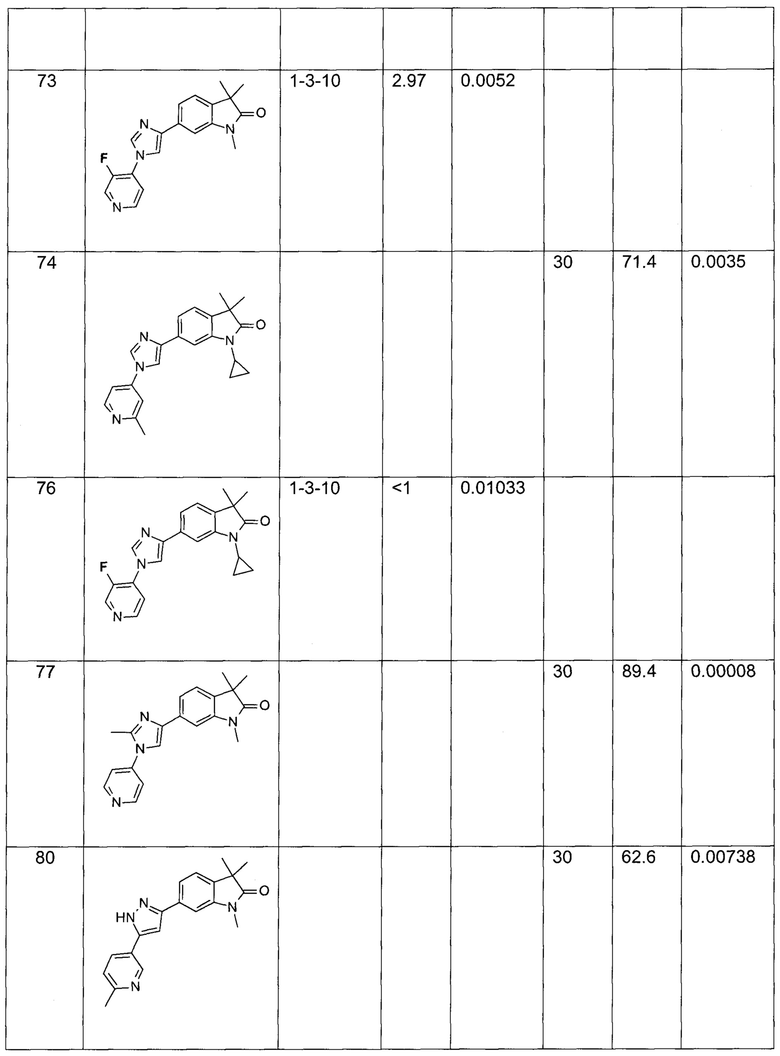
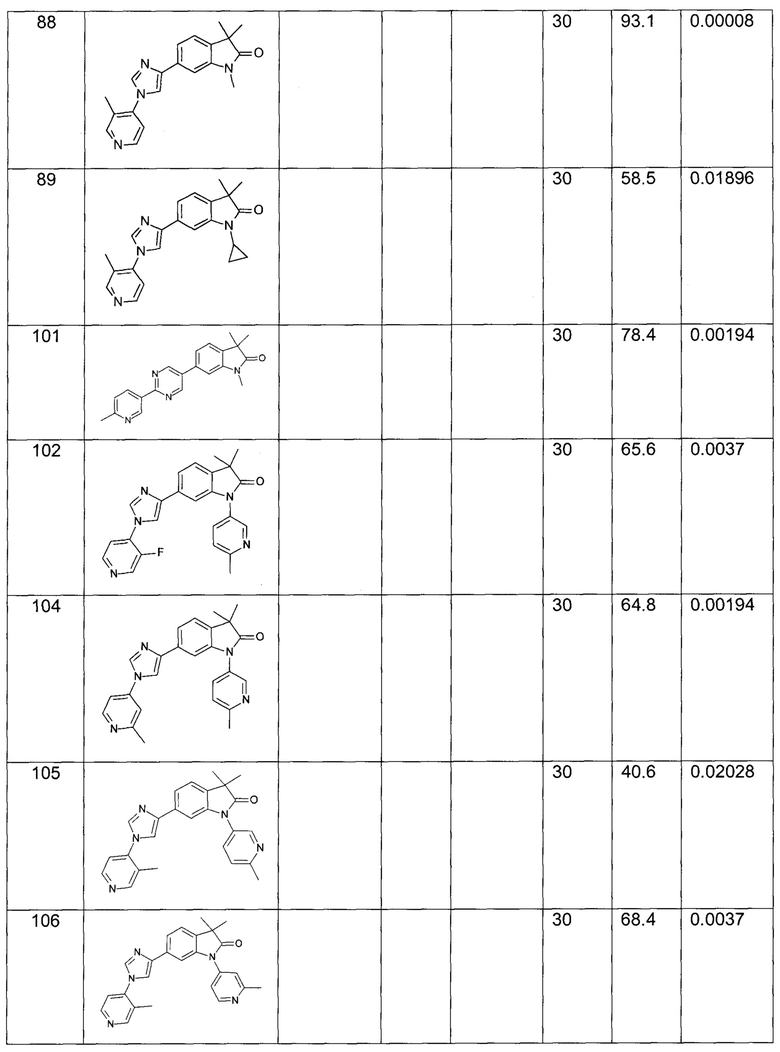
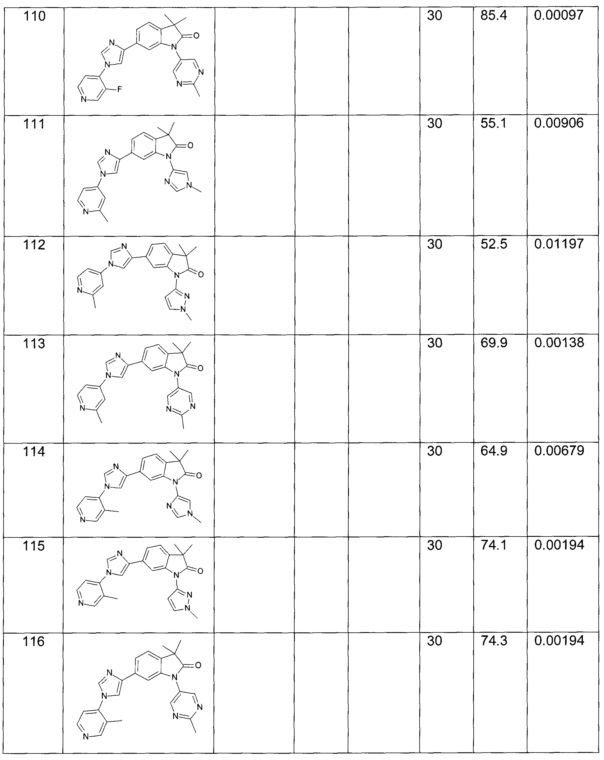
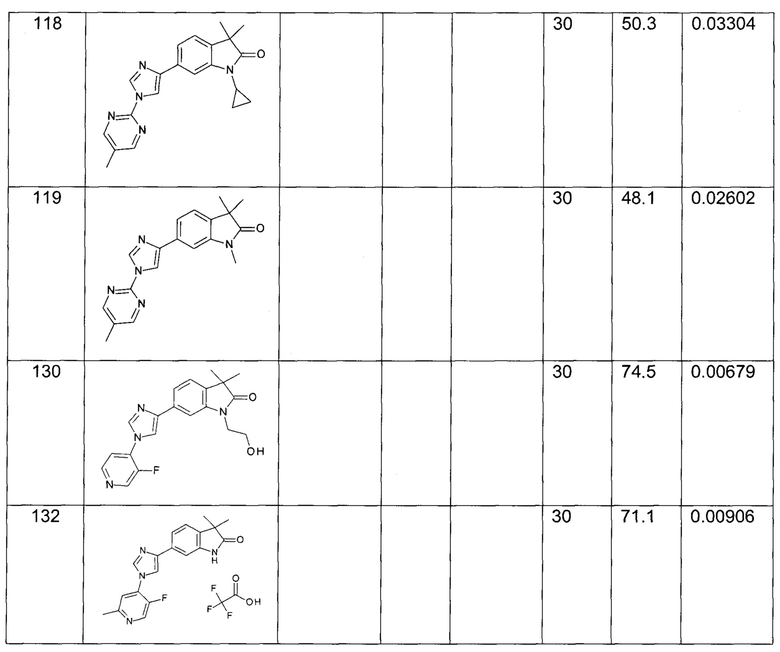
Как упомянуто выше, некоторые соединения были протестированы в SmartCube®, аналитической системе, разработанной PsychoGenics Inc.
SmartCube® использовали для сравнения поведенческой картины для тестируемого соединения с базой данных поведенческих картин, полученных из большого набора одобренных к клиническому применению эталонных лекарственных средств, сгруппированных по показаниям. Таким образом, нейрофармакологические эффекты тестируемого соединения могут быть предсказаны на основании сходства с основными классами соединений, такими как антипсихотические средства, анксиолитики и антидепрессанты. Этот подход идеально подходит для скрининга коллекций существующих лекарственных средств или лекарственных средств-кандидатов с ранее неизвестными нейрофармакологическими свойствами, что могло бы ускорить разработку новых и неожиданных методов лечения психических расстройств.
Некоторые соединения по настоящему изобретению вводили в./б. инъекцией в разных дозах за 15 минут до тестирования. В каждой обрабатываемой группе использовали по меньшей мере 8 мышей. Цифровые видеоизображения субъектов обрабатывали с использованием алгоритмов компьютерной обработки изображений для извлечения более 2000 зависимых измеряемых параметров, включая частоту появления и продолжительность многих различных поведенческих состояний. Результаты таких классификаций представлены в виде гистограмм для каждой дозы (мг/кг); на оси Y указана относительная вероятность того, что тестируемое соединение будет демонстрировать эффективность при конкретном показании ЦНС.
Гистограммы для соединений из примеров 35, 47, 62 и 93 при дозе 25 мг/кг показаны на Фиг. 1. Для сравнения на Фиг. 2 показана поведенческая картина для атипичного антипсихотического средства оланзапина и рисперидона. Соединения по настоящему изобретению демонстрируют картины, сходные с таковыми для атипичных антипсихотических средств. Независимый анализ осуществляли на неклассифицированных данных для определения сходства соединений из примеров с активными лекарственными формами известных атипичных антипсихотических средств. Для этого анализа авторы изобретения применяют показатель различения в качестве меры различимости таких лекарственных средств, т.е. ''возможности отличения'' одного лекарственного средства от другого. Показатель, равный 50% (или 0,5), соответствует нулевой возможности различения. Эмпирические данные показали, что пороговое значение показателя для надежного различения лежит около 70%, т.е. два лекарственных средства, демонстрирующие показатель различения 70% или меньше, считаются схожими, в то время как показатель различения больше 70% указывает на то, что два лекарственных средства являются различными. В приведенной ниже таблице показаны данные анализа сходства выбранных соединений по настоящему изобретению с несколькими атипичными антипсихотическими средствами. В большинстве случаев соединения из примеров демонстрируют сходство с рисперидоном, кпозапином и оланзапином с показателем различения не более 0,70.
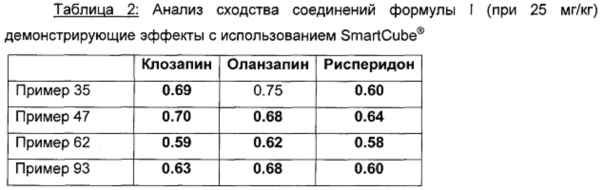
Таким образом, можно высказать предположение, что соединения по настоящему изобретению обладают аналогичной эффективностью известных атипичных антипсихотических средств.
Фиг. 1: SmartCube®-Картина для соединений 35, 47, 62, и 93 (при 25 мг/кг) показывающая профиль, аналогичный профилю атипичных антипсихотических средств.
Фиг. 2: SmartCube®-Картина для атипичных антипсихотических средств клозапина, оланзапина и рисперидона (каждый в двух дозах).
Соединения формулы (I) и их фармацевтически приемлемые соли можно применять в качестве лекарственных средств, например, в форме фармацевтических препаратов. Эти фармацевтические препараты можно вводить перорально, например, в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным также может быть их ректальное введение, например, в форме суппозиториев, или парентеральное, например, в форме растворов для инъекций.
Для изготовления фармацевтических препаратов соединения формулы (I) и их фармацевтически приемлемые соли можно обрабатывать, используя фармацевтически инертные неорганические или органические носители. Например, в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул можно использовать лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и тому подобное. Подходящими носителями для мягких желатиновых капсул являются, например растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобное; в случае мягких желатиновых капсул никаких носителей обычно не требуется, однако это зависит от природы активного вещества. Подходящими носителями для изготовления растворов и сиропов являются, например вода, полиолы, сахароза, инвертированный сахар, глюкоза и тому подобное. Для водных растворов для инъекций водорастворимых солей соединений формулы (I) можно использовать такие адъюванты, как спирты, полиолы, глицерин, растительные масла и тому подобное, однако, как правило, в этом нет необходимости.
Подходящими носителями для суппозиториев являются, например природные или отвержденные жиры, воски, жиры, полужидкие или жидкие полиолы и тому подобное.
Помимо этого фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, корригенты, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать другие дополнительные терапевтически полезные вещества.
Как упомянуто ранее, лекарственные средства, содержащие соединение формулы (I) или их фармацевтически приемлемые соли и терапевтически инертный эксципиент, также представляют собой объект настоящего изобретения, равно как и способ изготовления таких лекарственных средств, который включает внесение одного или более чем одного соединения формулы I либо одной или более чем одной их фармацевтически приемлемой соли и, при желании, одного или более чем одного другого терапевтически полезного вещества в лекарственную форму в виде галенова препарата вместе с одним или более чем одним терапевтически инертным носителем. Активные соединения также можно использовать в форме их пролекарств.
Как еще упоминалось ранее, применение соединений формулы (I) для изготовления лекарственных средств, полезных в предупреждении и/или лечении перечисленных выше заболеваний, также представляет собой объект настоящего изобретения.
Дозировку можно варьировать в широких пределах, и, несомненно, в каждом конкретном случае она должна быть подобрана с учетом индивидуальных потребностей. В общем случае эффективная дозировка для перорального или парентерального введения составляет 0,01-20 мг/кг/сутки, причем для всех описанных показаний предпочтительна дозировка 0,1-10 мг/кг/сутки. Суточная дозировка для взрослого человека массой 70 кг соответственно лежит в диапазоне 0,7-1400 мг в сутки, предпочтительно от 7 до 700 мг в сутки.
Получение фармацевтических композиций, содержащих соединения по изобретению:
Таблетки следующего состава производят обычным способом:
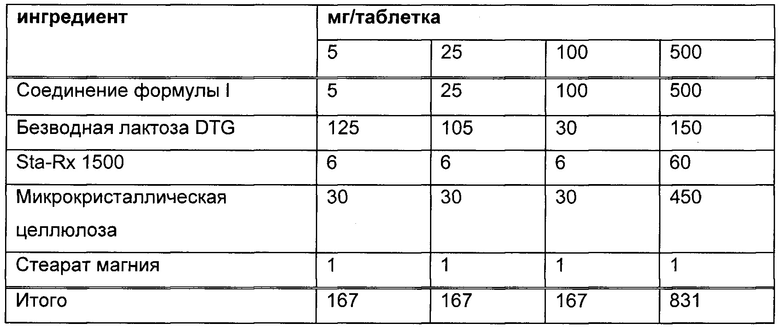
Методика производства
1. Смешать ингредиенты 1, 2, 3 и 4 и гранулировать с очищенной водой.
2. Высушить гранулы при 50°С.
3. Пропустить гранулы через подходящее измельчающее оборудование.
4. Добавить ингредиент 5 и перемешивать 3 минуты; спрессовать на подходящем прессе.
Производят капсулы следующего состава:
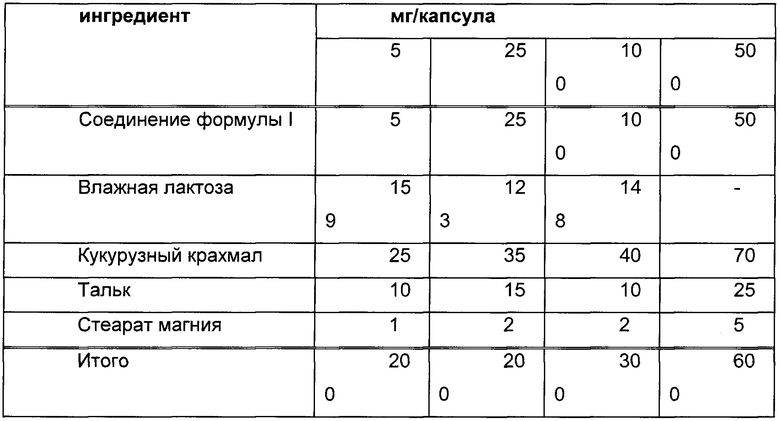
Методика производства
1. Смешивают ингредиенты 1, 2 и 3 в подходящем миксере в течение 30 минут.2. Добавляют ингредиенты 4 и 5 и смешивают в течение 3 минут.
3. Заполняют подходящие капсулы.
Соединение формулы I, лактозу и кукурузный крахмал сначала смешивают в миксере и затем в измельчителе. Смесь возвращают в миксер; туда добавляют тальк и тщательно смешивают. Смесью заполняют подходящие капсулы, например, твердые желатиновые капсулы, с помощью оборудования.
Производят раствор для инъекций следующего состава:

Методика производства
Соединение формулы I растворяют в смеси полиэтиленгликоля 400 и воды для инъекций (часть). Доводят рН до 5.0 с помощью уксусной кислоты. Объем доводят до 1.0 мл посредством добавления оставшегося количества воды. Раствор фильтруют, наливают во флаконы с использованием подходящего оборудования и стерилизуют.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ИНДОЛИН-2-ОНА ИЛИ ПИРРОЛОПИРИДИН/ПИРИМИДИН-2-ОНА | 2014 |
|
RU2666532C2 |
| ПРОИЗВОДНЫЕ ИНДОЛИН-2-ОНА | 2016 |
|
RU2727179C2 |
| ФЕНОКСИМЕТИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2016 |
|
RU2746481C1 |
| Бициклические производные пиридина, полезные в качестве ингибитора белков, связывающих жирные кислоты (FABP) 4 и/или 5 | 2013 |
|
RU2648247C2 |
| АМИНОТРИАЗОЛОПИРИДИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2009 |
|
RU2552642C2 |
| ФЕНИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ АГОНИСТОВ КАННАБИНОИДНОГО РЕЦЕПТОРА 2 | 2016 |
|
RU2728823C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛОПИРИДИНА В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2013 |
|
RU2652117C2 |
| ПРОИЗВОДНЫЕ ПИРИДИН-2-КАРБОКСАМИДА В КАЧЕСТВЕ АНТАГОНИСТОВ mGluR5 | 2006 |
|
RU2411237C2 |
| НОВЫЕ ЭФИРНЫЕ ПРОИЗВОДНЫЕ ИЗОКСАЗОЛА В КАЧЕСТВЕ ПОЗИТИВНЫХ АЛЛОСТЕРИЧЕСКИХ МОДУЛЯТОРОВ РЕЦЕПТОРА ГАМК А АЛЬФА 5 | 2017 |
|
RU2772862C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО ЦИАНОЕНОНА КАК МОДУЛЯТОРЫ KEAP1 | 2021 |
|
RU2822828C1 |
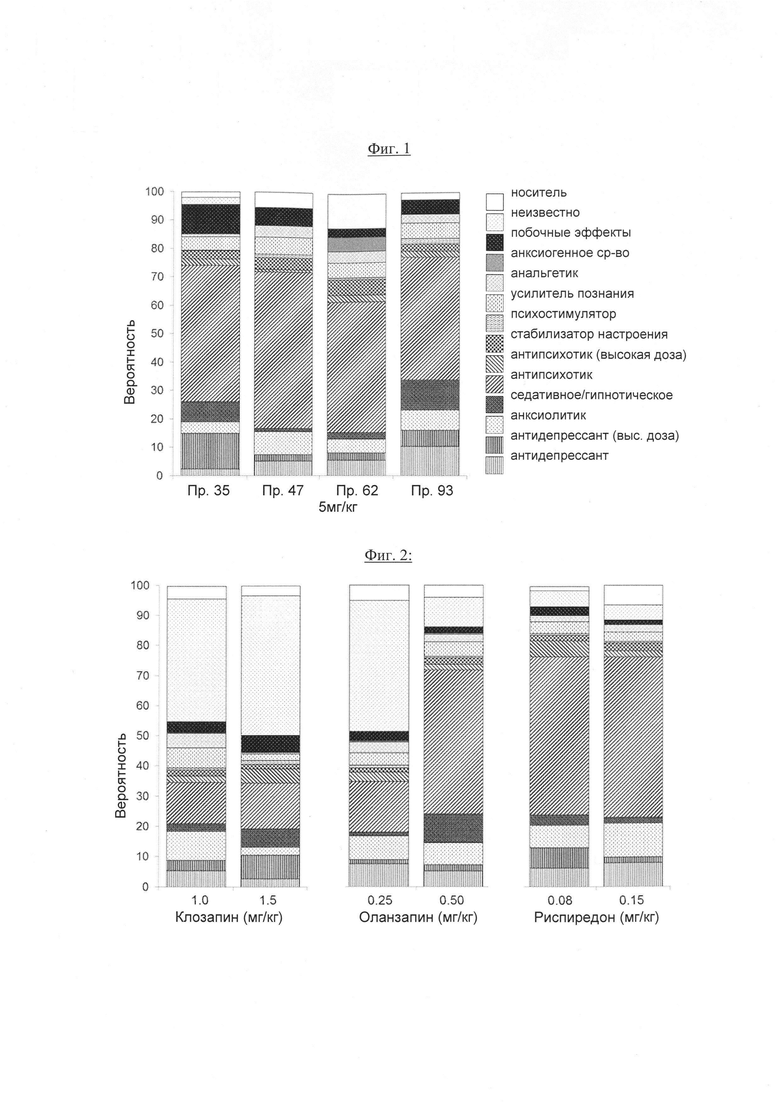
Настоящее изобретение относится к индолин-2-оновым и 1,3-дигидро-пирроло[3,2-с]пиридин-2-оновым производным общей формулы I, где Ar1 представляет собой фенил, пиридинил или пиримидинил; Ar2 представляет собой 5- или 6-членную гетероарильную группу, содержащую 2 или 3 гетероатома, выбранных из N, О; R1 представляет собой водород, С1-7-алкил, галоген или С1-7-алкокси; R2 представляет собой водород или С1-7-алкил; R3 представляет собой водород, С1-7-алкил, С1-7-алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены С1-7-алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил; X представляет собой СН; n представляет собой 1 или 2; а также его фармацевтически приемлемым солям, предназначенным для лечения некоторых расстройств центральной нервной системы (ЦНС), которые представляют собой симптомы шизофрении, злоупотребление лекарственными средствами, алкогольную и лекарственную зависимость, обсессивно-компульсивные расстройства, когнитивное нарушение, биполярные расстройства, расстройства настроения, глубокую депрессию, терапевтически резистентную депрессию, тревожные расстройства, аутизм, болезнь Паркинсона, хроническую боль, пограничное расстройство личности, нарушения сна, синдром хронической усталости, тугоподвижность, противовоспалительные эффекты при артрите и нарушения равновесия. Также изобретение относится к конкретным соединениям, приведенным в формуле изобретения. 16 н. и 2 з.п. ф-лы, 2 табл., 2 ил., 132 пр.
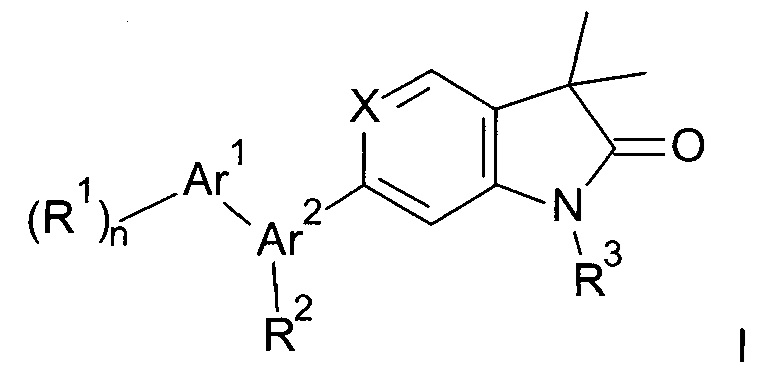
1. Применение соединения формулы I
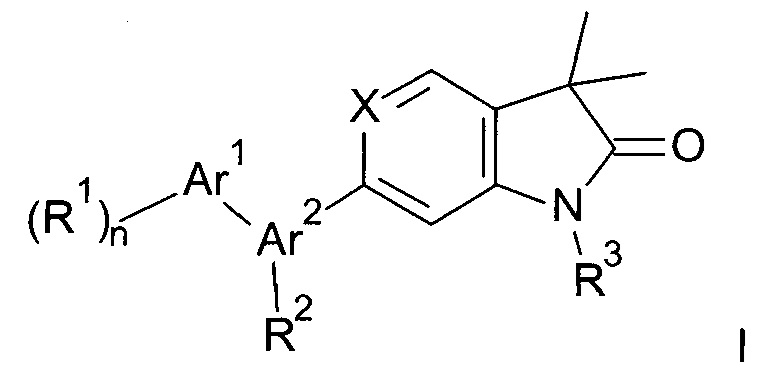
где Ar1 представляет собой фенил, пиридинил или пиримидинил;
Ar2 представляет собой 5- или 6-членную гетероарильную группу, содержащую 2 или 3 гетероатома, выбранных из N, О;
R1 представляет собой водород, С1-7-алкил, галоген или С1-7-алкокси;
R2 представляет собой водород или С1-7-алкил;
R3 представляет собой водород, С1-7-алкил, С1-7-алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены С1-7-алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
X представляет собой СН;
n представляет собой 1 или 2,
а также его фармацевтически приемлемых солей
при лечении некоторых расстройств центральной нервной системы (ЦНС), которые представляют собой симптомы шизофрении, злоупотребление лекарственными средствами, алкогольную и лекарственную зависимость, обсессивно-компульсивные расстройства, когнитивное нарушение, биполярные расстройства, расстройства настроения, глубокую депрессию, терапевтически резистентную депрессию, тревожные расстройства, аутизм, болезнь Паркинсона, хроническую боль, пограничное расстройство личности, нарушения сна, синдром хронической усталости, тугоподвижность, противовоспалительные эффекты при артрите и нарушения равновесия.
2. Применение соединения формулы I
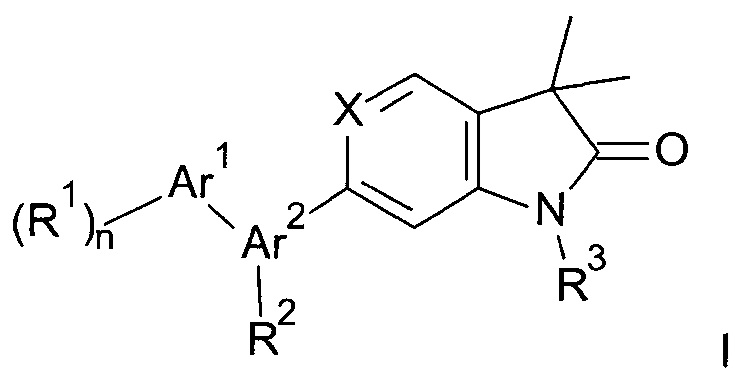
где Ar1 представляет собой фенил, пиридинил или пиримидинил;
Ar2 представляет собой 5- или 6-членную гетероарильную группу, содержащую 2 или 3 гетероатома, выбранных из N, О;
R1 представляет собой водород, С1-7-алкил, галоген или С1-7-алкокси;
R2 представляет собой водород или С1-7-алкил;
R3 представляет собой водород, С1-7-алкил, С1-7-алкил, замещенный гидрокси, циклоалкил, оксетан-3-ил, пиридинил, имидазолил, пиразолил, пиримидинил, где кольца возможно замещены С1-7-алкилом, или представляет собой -(СН2)3-S(O)2-циклопропил;
X представляет собой СН или N;
n представляет собой 1 или 2,
а также его фармацевтически приемлемых солей
для производства лекарственного средства для лечения некоторых расстройств центральной нервной системы (ЦНС), которые представляют собой симптомы шизофрении, злоупотребление лекарственными средствами, алкогольную и лекарственную зависимость, обсессивно-компульсивные расстройства, когнитивное нарушение, биполярные расстройства, расстройства настроения, глубокую депрессию, терапевтически резистентную депрессию, тревожные расстройства, аутизм, болезнь Паркинсона, хроническую боль, пограничное расстройство личности, нарушения сна, синдром хронической усталости, тугоподвижность, противовоспалительные эффекты при артрите и нарушения равновесия.
3. Применение соединений по п. 1 или 2, где соединения выбраны из следующих:
1,3,3-триметил-6-(5-фенил-1Н-имидазол-2-ил)индолин-2-он
1,3,3-триметил-6-(2-(пиридин-4-ил)-1Н-имидазол-5-ил)индолин-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-4-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-имидазол-1-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-имидазол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(3-пиридин-4-ил-изоксазол-5-ил)-1,3-дигидро-индол-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-4-ил)индолин-2-он
3,3-диметил-6-(5-(2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1-(оксетан-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-пиразол-4-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-1,2,3-триазол-1-ил)индолин-2-он
1,3,3-триметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
6-(2-(3-метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он
1-циклопропил-3,3-диметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-1,3,3-триметилиндолин-2-он
1-циклопропил-3,3-диметил-6-(1-(2-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-6-(1-(3-фторпиридин-4-ил)-1Н-имидазол-4-ил)-3,3-диметилиндолин-2-он
1,3,3-триметил-6-(2-метил-1-(пиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(5-(6-метилпиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(3-метилпиридин-4-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-5-ил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(6-метил-3-пиридил)индолин-2-он
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(6-метил-3-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(2-метил-4-пиридил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-3,3-диметил-1-(2-метилпиримидин-5-ил)индолин-2-он
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(2-метил-4-пиридил)имидазол-4-
ил]индолин-2-он
3,3-диметил-6-[1-(2-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
3,3-диметил-1-(1-метилимидазол-4-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-1-(1-метилпиразол-3-ил)-6-[1-(3-метил-4-пиридил)имидазол-4-ил]индолин-2-он
3,3-диметил-6-[1-(3-метил-4-пиридил)имидазол-4-ил]-1-(2-метилпиримидин-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
1,3,3-триметил-6-(1-(5-метилпиримидин-2-ил)-1Н-имидазол-4-ил)индолин-2-он
6-[1-(3-фтор-4-пиридил)имидазол-4-ил]-1-(2-гидроксиэтил)-3,3-диметил-индолин-2-он
6-[1-(5-фтор-2-метил-4-пиридил)имидазол-4-ил]-3,3-диметил-индолин-2-он.
4. Соединение формулы Ie
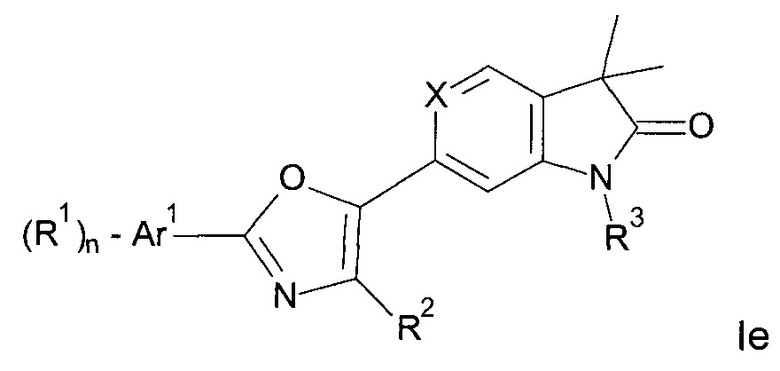
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил, галоген или С1-7-алкокси;
R2 представляет собой водород или C1-7-алкил;
R3 представляет собой водород, C1-7-алкил, циклопропил, оксетан-3-ил;
X представляет собой СН;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
5. Соединение формулы If
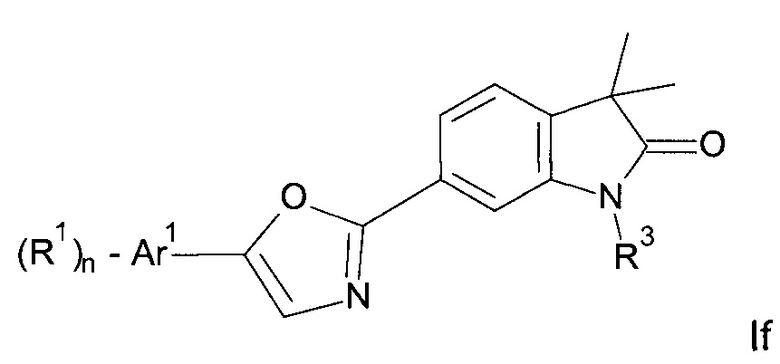
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил;
R3 представляет собой циклопропил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
6. Соединение формулы Ig
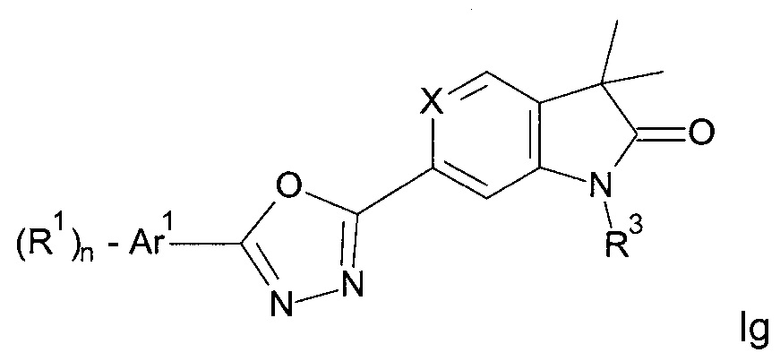
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил, галоген;
R3 представляет собой C1-7-алкил, C1-7-алкил, замещенный гидрокси, оксетан-3-ил;
X представляет собой СН;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
7. Соединение формулы Ii
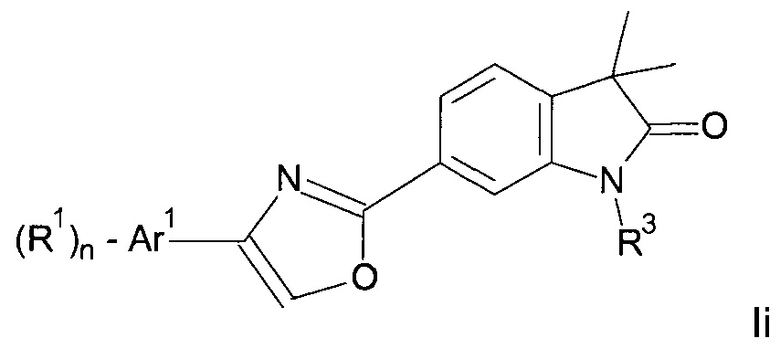
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил;
R3 представляет собой C1-7-алкил, циклопропил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
8. Соединение формулы Il
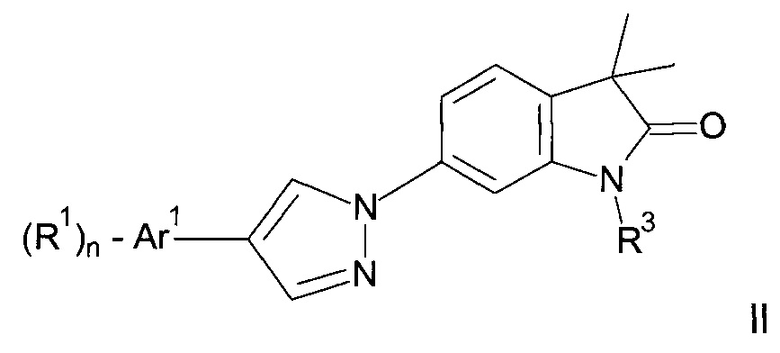
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил;
R3 представляет собой водород, C1-7-алкил, циклопропил, оксетан-3-ил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
9. Соединение формулы Im
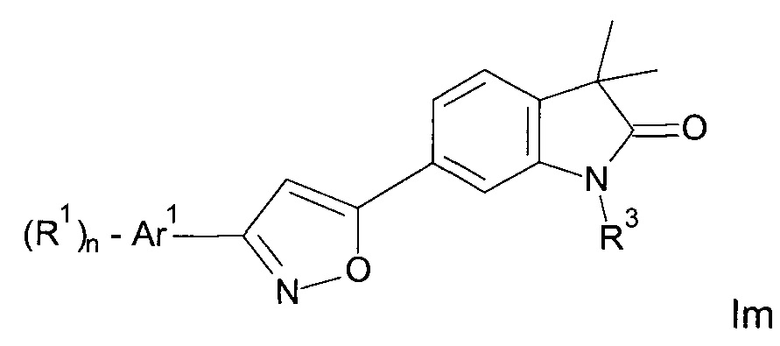
где Ar1 представляет собой пиридинил;
R1 представляет собой водород;
R3 представляет собой C1-7-алкил, циклопропил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
10. Соединение формулы In
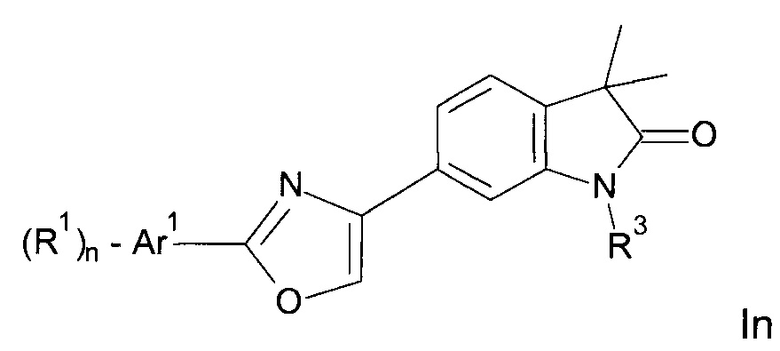
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил, C1-7-алкокси;
R3 представляет собой водород, C1-7-алкил, циклопропил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
11. Соединение формулы Io
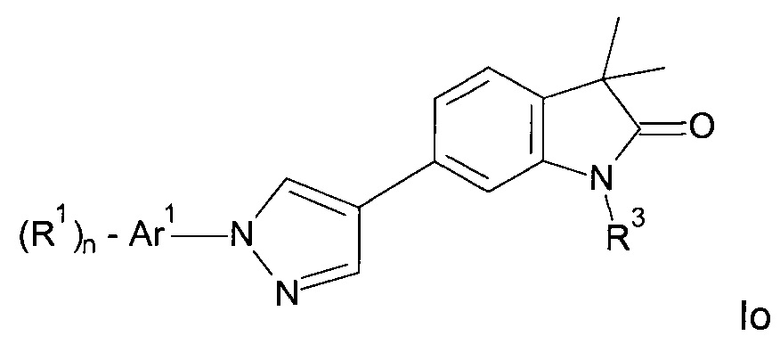
где Ar1 представляет собой пиридинил;
R1 представляет собой водород;
R3 представляет собой C1-7-алкил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
12. Соединение формулы Ip
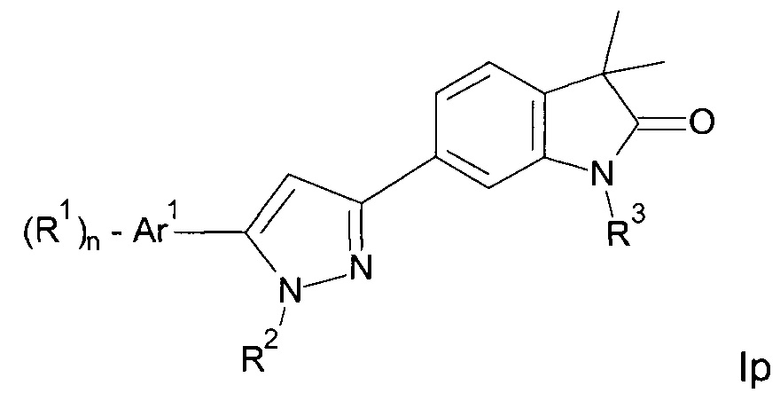
где Ar1 представляет собой пиридинил;
R1 представляет собой водород, C1-7-алкил;
R2 представляет собой водород или C1-7-алкил;
R3 представляет собой C1-7-алкил;
n представляет собой 1 или 2,
а также его фармацевтически приемлемые соли.
13. Соединение формулы Iq
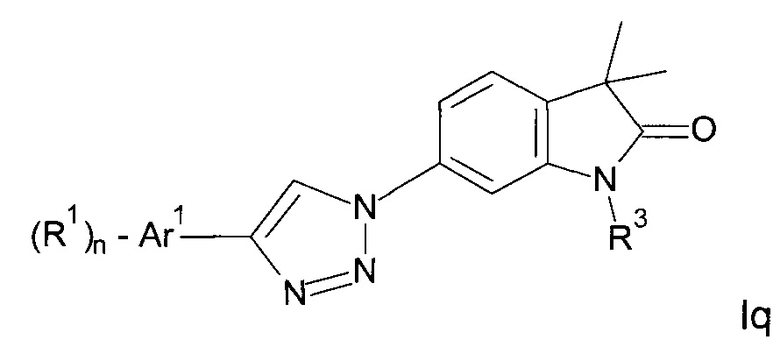
где Ar1 представляет собой пиридинил;
R1 представляет собой водород;
R3 представляет собой C1-7-алкил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
14. Соединение формулы Is
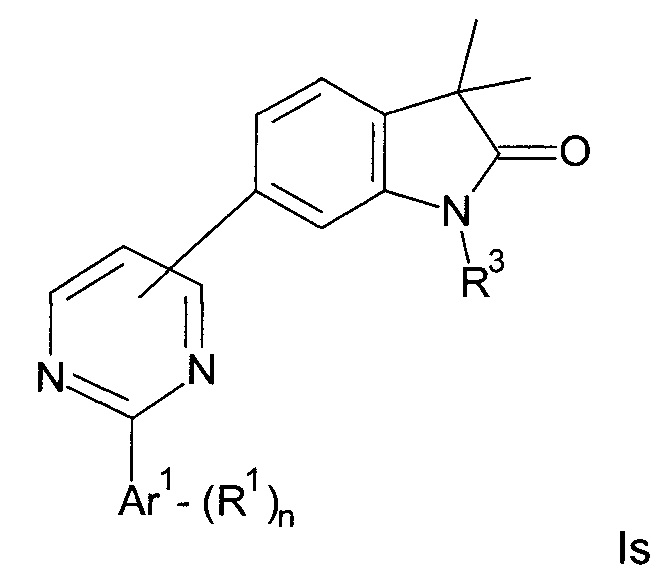
где Ar1 представляет собой пиридинил;
R1 представляет собой C1-7-алкил;
R3 представляет собой C1-7-алкил, оксетан-3-ил;
n представляет собой 1,
а также его фармацевтически приемлемые соли.
15. Соединение, выбранное из следующих:
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-3-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(пиридин-4-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(5-(пиридин-4-ил)-1,3,4-оксадиазол-2-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(5-(2-метилпиридин-4-ил)оксазол-2-ил)индолин-2-он
1,3,3-триметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(2-(6-метилпиридин-3-ил)оксазол-5-ил)индолин-2-он
3,3-диметил-6-(2-(2-метилпиридин-4-ил)оксазол-5-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(3-пиридин-4-ил-изоксазол-5-ил)-1,3-дигидро-индол-2-он
3,3-диметил-1-(оксетан-3-ил)-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(2-(пиридин-3-ил)оксазол-4-ил)индолин-2-он
3,3-диметил-6-(5-(2-метилпиридин-4-ил)-1,3,4-оксадиазол-2-ил)-1-(оксетан-3-ил)индолин-2-он
1,3,3-триметил-6-(1-(пиридин-3-ил)-1Н-пиразол-4-ил)индолин-2-он
3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(пиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1-циклопропил-3,3-диметил-6-(4-(2-метилпиридин-4-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(4-(пиридин-4-ил)-1Н-1,2,3-триазол-1-ил)индолин-2-он
6-(2-(3-метоксипиридин-4-ил)оксазол-5-ил)-3,3-диметилиндолин-2-он
1-циклопропил-3,3-диметил-6-(4-(6-метилпиридин-3-ил)-1Н-пиразол-1-ил)индолин-2-он
1,3,3-триметил-6-(5-(6-метилпиридин-3-ил)-1Н-пиразол-3-ил)индолин-2-он
1,3,3-триметил-6-(2-(6-метилпиридин-3-ил)пиримидин-5-ил)индолин-2-он.
16. Соединение по любому из пп. 4-15 для применения в качестве терапевтически активного вещества с антипсихотической активностью.
17. Фармацевтическая композиция, содержащая соединение по любому из пп. 4-15 и терапевтически активный носитель, для лечения некоторых расстройств центральной нервной системы (ЦНС), которые представляют собой симптомы шизофрении, злоупотребление лекарственными средствами, алкогольную и лекарственную зависимость, обсессивно-компульсивные расстройства, когнитивное нарушение, биполярные расстройства, расстройства настроения, глубокую депрессию, терапевтически резистентную депрессию, тревожные расстройства, аутизм, болезнь Паркинсона, хроническую боль, пограничное расстройство личности, нарушения сна, синдром хронической усталости, тугоподвижность, противовоспалительные эффекты при артрите и нарушения равновесия.
18. Способ лечения некоторых расстройств центральной нервной системы (ЦНС), которые представляют собой симптомы шизофрении, злоупотребление лекарственными средствами, алкогольную и лекарственную зависимость, обсессивно-компульсивные расстройства, когнитивное нарушение, биполярные расстройства, расстройства настроения, глубокую депрессию, терапевтически резистентную депрессию, тревожные расстройства, аутизм, болезнь Паркинсона, хроническую боль, пограничное расстройство личности, нарушения сна, синдром хронической усталости, тугоподвижность, противовоспалительные эффекты при артрите и нарушения равновесия, который включает введение эффективного количества соединения по любому из пп. 4-15.
| ВЕРТИКАЛЬНЫЙ МДП-ТРАНЗИСТОР ИНТЕГРАЛЬНОЙ СХЕМЫ | 1997 |
|
RU2108641C1 |
| Огнетушитель | 0 |
|
SU91A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ВОЗРАСТНЫХ И ДИАБЕТИЧЕСКИХ СОСУДИСТЫХ ОСЛОЖНЕНИЙ | 2002 |
|
RU2291154C2 |
Авторы
Даты
2019-08-15—Публикация
2015-05-19—Подача