Изобретение относится к биологии, медицине, а именно к фундаментальной и клинической биохимии, и позволяет выявлять влияние низкомолекулярных биологически активных лигандов на конформацию белка.
В настоящее время изучение роли низкомолекулярных лигандов в регуляции различных биологических процессов выходит на качественно новый уровень. Были получены данные, описывающие особенности поведения низкомолекулярных молекул как участников взаимодействия белок-белок [1-2]. Тем не менее, недостаточно изученным остается вопрос о конформации белковых молекул, в частности, каталитических белков, при взаимодействии с низкомолекулярными лигандами.
Известен способ определения наличия комплекса белок-лиганд методом постановки иммунно-ферментного анализа [3], суть которого заключается в иммобилизации одного из участников реакции (белка или лиганда) на планшете и последующем добавлении второго участника реакции и их специфическом связывании с образованием окрашенного комплекса, по изменению окраски раствора делается вывод о наличии или отсутствии искомого комплекса белок-лиганд, а также производится расчет их концентрации.
Недостатком данного метода является сложность использования в качестве участника реакции каталитического белка в виду нестабильных условий эксперимента (смена фаз, изменение температуры, применение химических реагентов), затрудненность количественной характеристики образованной связи и стабильности полученных комплексов, высокая времязатратность большинства известных методик.
Известен метод изотермической титрационной калориметрии [4], суть которого заключается в последовательном медленном введении аликвот первого компонента межмолекулярного взаимодействия - лиганда, находящегося в шприце, в кювету со вторым компонентом межмолекулярного взаимодействия - белком. Между опытной кюветой и контрольной, содержащей воду, поддерживается одинаковая температура. Если происходит образование комплекса белок-лиганд, то поглощенное или выделенное тепло измеряется калориметром. Полученное в результате измерения количество тепла находится в прямой зависимости от объема связывания.
Недостатком данного метода является сложность пробоподготовки, так как мельчайшие частицы пыли, других молекул, пузырьки газа могут приводить к появлению артефактов на термограмме; невозможность использования белков с лабильной структурой, поскольку перемешивание шприца может вызывать их дестабилизацию; высокая длительность эксперимента в виду необходимости проведения около 70 повторов с интервалом в 3-5 минут.
Известен способ дифференциальной сканирующей флуориметрии [5], суть которого заключается в установлении температуры плавления белковой молекулы путем постепенного ее нагревания. Температура плавления устанавливается по изменению флуоресценции, причем возможно использование как флуоресцентных меток, так и явление эндогенной флуоресценции. Результат выдается в градусах Цельсия. По изменению температуры плавления белка при добавлении лиганда относительно контрольной пробы с чистым белком делают вывод о влиянии лиганда на конформацию белковой молекулы. Данный способ был выбран нами за прототип.
Недостатком данного способа является отсутствие унифицированного подхода для обработки полученных данных; сложность сравнения влияния разных лигандов ввиду отсутствия значительных колебаний в температуре плавления; субъективность использования температуры плавления как параметра, описывающего конформационное состояние белка.
Целью является создание способа для выявления влияния низкомолекулярных биологически активных лигандов на конформацию белка.
Эта цель достигается тем, что биологически активный лиганд низкомолекулярной массы в концентрациях 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ, 0,5 мкМ вносят в микрокапилляры «nanoDSF grade» (NanoTemper Technologies, Германия), содержащие белок в конечной концентрации 1 мкМ, таким образом получая опытные пробы, контрольной пробой служит раствор, содержащий белок в такой же конечной концентрации без добавления низкомолекулярного соединения; 10 мкл каждой из полученных опытных проб инкубируют в течение пяти минут в темном месте при температуре 25°С; после чего проводят измерение эндогенной флуоресценции по остаткам тирозина и триптофана на приборе Prometheus NT.48 (NanoTemper Technologies, Германия) при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С/мин; строят график зависимости флуоресценции (соотношение 330 нм/350 нм) от температуры нагревания, затем строят графики первых производных для полученных кривых; рассчитывают значение температуры пика и значение первой производной в точке пика для контрольной и опытных проб, рассчитывают отношения значений первой производной в точке пика опытных и контрольной проб в процентах, значение первой производной в точке пика контрольной пробы принимают за 100%, при изменении отношения >15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону разворачивания, при изменении отношения <-15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону сворачивания, при изменении отношения от -15% до 15% включительно говорят об отсутствии влияния выбранного низкомолекулярного лиганда на конформацию белковой молекулы.
Предложенный способ позволяет стандартизировать процедуру обработки полученных результатов и получить объективную оценку конформационного состояния белковой молекулы, а также детализировать влияние отдельно взятых концентраций лиганда на конформационное состояние белка. Нами была проведена серия экспериментов с применением различных лигандов (пируват, лактат, малат, оксалоацетат и др.) и белковых молекул (лактатдегидрогеназа, глицерофосфатдегидрогеназа и др.), в которых мы производили подбор необходимых концентраций лигандов и молекул и оценивали конформационное состояние белковых молекул, в ходе эксперимента было эмпирически установлено, что предел измерений >15% и <-15% является точным для характеристики конформационного состояния молекулы белка, поскольку по результатам наших исследований заданный диапазон значений наиболее полно помогал исключить молекулы, не влияющие на конформацию белка, а также был удобен при необходимости дифференцирования в сложных случаях, когда температура плавления белка, расчет которой предусматривается оригинальной методикой, менялась незначительно, однако форма и глубина пиков первых производных опытных проб в сравнении с контрольной пробой свидетельствовала о значительном изменении конформации белка.
Способ выявления влияния низкомолекулярных биологически активных лигандов на конформацию белка реализуют следующим образом:
Для определения влияния исследуемого низкомолекулярного биологически активного лиганда на конформацию белка готовят 6 пробирок, в которые вносят по 100 мкл 2 мкМ раствора исследуемого белка. Затем в первую пробирку добавляют 100 мкл 32 мкМ раствора низкомолекулярного лиганда, получают раствор с конечной концентрацией каталитического белка 1 мкм и конечной концентрацией низкомолекулярного лиганда - 16 мкМ. Из первой пробирки переносят 100 мкл полученного раствора во вторую пробирку, получают неизменную концентрацию каталитического белка 1 мкМ и концентрацию низкомолекулярного лиганда 8 мкМ. Проделывают эти шаги со всеми пробирками и получают 6 опытных проб, в которых концентрация каталитического белка остается неизменной и составляет 1 мкМ, а концентрация низкомолекулярного лиганда соответственно - 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ и 0,5 мкМ. Контрольной пробой служит 1 мкМ раствор каталитического белка. Помещают по 10 мкл каждой из полученных опытных проб и контрольную пробу в капилляры Prometheus NT.48 (nanoDSF grade). Проводят сканирующую флуориметрию на приборе Prometheus NT.48 (NanoTemper Technologies, Германия) при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С /мин. Строят график зависимости флуоресценции (соотношение 330 нм/350 нм) от температуры нагревания, затем строят графики первых производных для полученных кривых; рассчитывают значение температуры пика и значение первой производной в точке пика для контрольной и опытных проб, рассчитывают отношения значений первой производной в точке пика опытной и контрольной проб в процентах, значение первой производной в точке пика контрольной пробы принимают за 100%, при изменении отношения >15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону разворачивания, при изменении отношения <-15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону сворачивания, при изменении отношения от -15% до 15% включительно говорят об отсутствии влияния выбранного низкомолекулярного лиганда на конформацию белковой молекулы.
Способ сопровождается лабораторными примерами.
Лабораторный пример №1.
Определение влияния оксалоацетата в концентрации 16 мкМ на конформацию лактатдегидрогеназы
В качестве низкомолекулярного лиганда была выбрана молекула оксалоацетата (Sigma), в качестве белка - каталитический белок лактатдегидрогеназа (Sigma). Готовили 1 М раствор оксалоацетата путем растворения 14 мг навески в 0,1 мл буферного раствора солянокислого триса рН=7,5. Затем из 1 М раствора готовили 32 мкМ раствор путем последовательных разведений. Также готовили 2 мкМ раствор лактатдегидрогеназы: растворяли лиофилизат белка массой 1,21 мг в 50 мкл солянокислого триса рН=7,5 с получением концентрации 168 мкМ, из полученного раствора брали 2 мкл и вносили в 168 мкл солянокислого триса с получением концентрации 2 мкМ.
Готовили 6 пробирок, в которые внесли по 100 мкл 2 мкМ раствора белка. Затем в первую пробирку добавили 100 мкл 32 мкМ раствора низкомолекулярного лиганда, получили раствор с конечной концентрацией каталитического белка 1 мкм и конечной концентрацией низкомолекулярного лиганда - 16 мкМ. Из первой пробирки перенесли 100 мкл полученного раствора во вторую пробирку, получили неизменную концентрацию каталитического белка 1 мкМ и концентрацию низкомолекулярного лиганда 8 мкМ. Путем последующего повторения описанных шагов получили 6 разведений, в которых концентрация каталитического белка оставалась неизменной и составляла 1 мкМ, а концентрация низкомолекулярного лиганда соответственно - 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ и 0,5 мкМ. Контролем служил 1 мкМ раствор каталитического белка. Помещали по 10 мкл каждого полученного раствора и контрольную пробу в капилляры Prometheus NT.48 (nanoDSF grade). Проводили сканирующую флуориметрию на приборе Prometheus NT.48 (NanoTemper Technologies, Германия) при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С /мин.
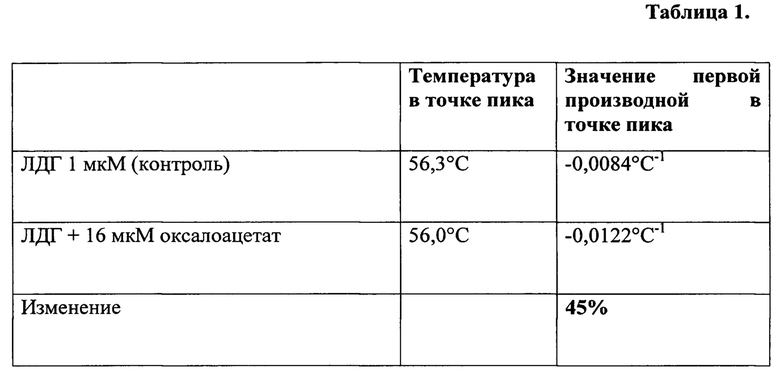
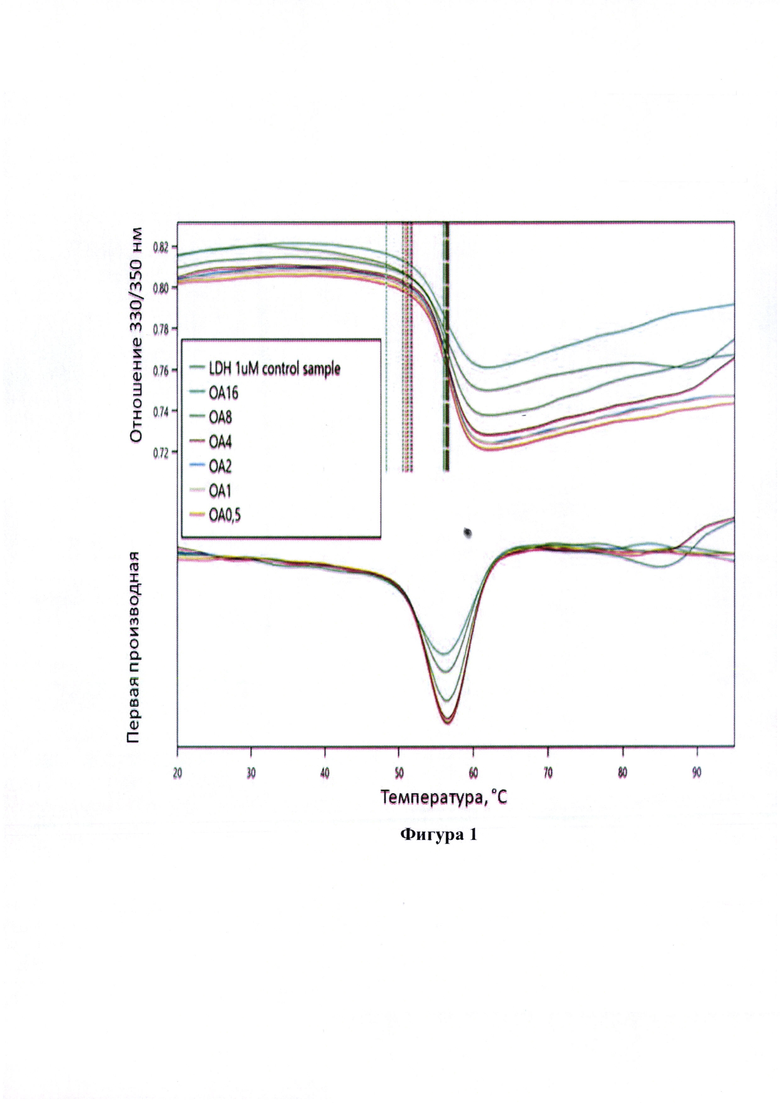
Строили график зависимости флуоресценции (соотношение 330/350 нм) от температуры нагревания для пробы, содержащий оксалоацетат в концентрации 16 мкМ и контрольной пробы, затем строили графики первых производных для полученных кривых (Фигура 1), находили значение первой производной в точке пика для контрольной и опытных проб (Таблица 1). Производили расчет отношения значения первой производной в точке пика опытной пробы к контрольной, где значение контрольной пробы принимали за 100%. Изменения отношения составило 45%, что входит в диапазон значений >15% и свидетельствует об изменении конформации лактатдегидрогеназы в сторону более развернутой в присутствии оксалоацетата в концентрации 16 мкМ.
Лабораторный пример №2.
Определение влияния оксалоацетата в концентрации 0,5 мкМ на конформацию лактатдегидрогеназы
В качестве низкомолекулярного лиганда была выбрана молекула оксалоацетата (Sigma), в качестве белка - каталитический белок лактатдегидрогеназа (Sigma). Готовили 1 М раствор оксалоацетата путем растворения 14 мг навески в 0,1 мл буферного раствора солянокислого триса рН=7,5. Затем из 1 М раствора готовили 32 мкМ раствор путем последовательного разведения. Также готовили 2 мкМ раствор лактатдегидрогеназы: растворяли лиофилизат белка массой 1,21 мг в 50 мкл солянокислого триса рН=7,5 с получением концентрации 168 мкМ, из полученного раствора брали 2 мкл и вносили в 168 мкл солянокислого триса с получением концентрации 2 мкМ.
Готовили 6 пробирок, в которые внесли по 100 мкл 2 мкМ раствора каталитического белка. Затем в первую пробирку добавили 100 мкл 32 мкМ раствора низкомолекулярного лиганда, получили раствор с конечной концентрацией каталитического белка 1 мкм и конечной концентрацией низкомолекулярного лиганда - 16 мкМ. Из первой пробирки перенесли 100 мкл полученного раствора во вторую пробирку, получили неизменную концентрацию каталитического белка 1 мкМ и концентрацию низкомолекулярного лиганда 8 мкМ. Путем последующего повторения описанных шагов получили 6 разведений, в которых концентрация каталитического белка оставалась неизменной и составляла 1 мкМ, а концентрация низкомолекулярного лиганда соответственно - 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ и 0,5 мкМ. Контролем служил 1 мкМ раствор каталитического белка. Помещали по 10 мкл каждого полученного раствора и контрольную пробу в капилляры Prometheus NT.48 (nanoDSF grade). Проводили сканирующую флуориметрию на приборе Prometheus NT.48 (NanoTemper Technologies, Германия) при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С /мин.
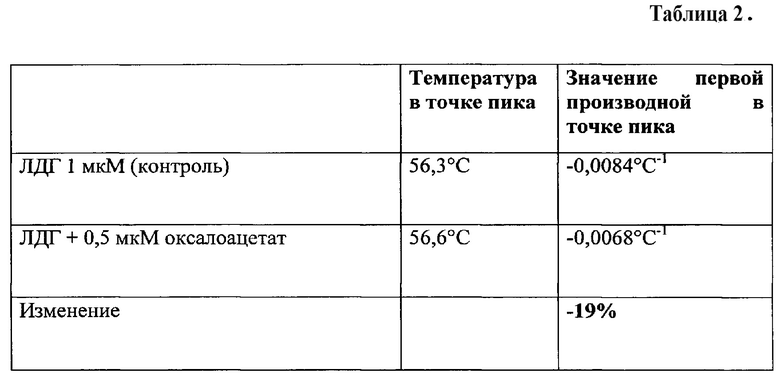
Строили график зависимости флуоресценции (соотношение 330/350 нм) от температуры нагревания для пробы, содержащий оксалоацетат в концентрации 0,5 мкМ и контрольной пробы, затем строили графики первых производных для полученных кривых (Фигура 1), находили значение первой производной в точке пика для контрольной и опытных проб (Таблица 2). Производили расчет отношения значений первой производной в точке пика опытной пробы к контрольной, где значение контрольной пробы принимали за 100%. Изменения отношения составило -19%, что входит в диапозон значений <-15% и свидетельствует об изменении конформации лактатдегидрогеназы в сторону более свернутой в присутствии оксалоацетата в концентрации 0,5 мкМ.
Лабораторный пример №3.
Определение влияния оксалоацетата в концентрации 8 мкМ на конформацию лактатдегидрогеназы
В качестве низкомолекулярного лиганда была выбрана молекула оксалоацетата (Sigma), в качестве белка - каталитический белок лактатдегидрогеназа (Sigma). Готовили 1 М раствор оксалоацетата путем растворения 14 мг навески в 0,1 мл буферного раствора солянокислого триса рН=7,5. Затем из 1 М раствора готовили 32 мкМ раствор путем последовательного разведения. Также готовили 2 мкМ раствор лактатдегидрогеназы: растворяли лиофилизат белка массой 1,21 мг в 50 мкл солянокислого триса рН=7,5 с получением концентрации 168 мкМ, из полученного раствора брали 2 мкл и вносили в 168 мкл солянокислого триса с получением концентрации 2 мкМ.
Готовили 6 пробирок, в которые внесли по 100 мкл 2 мкМ раствора каталитического белка. Затем в первую пробирку добавили 100 мкл 32 мкМ раствора низкомолекулярного лиганда, получили раствор с конечной концентрацией каталитического белка 1 мкм и конечной концентрацией низкомолекулярного лиганда - 16 мкМ. Из первой пробирки перенесли 100 мкл полученного раствора во вторую пробирку, получили неизменную концентрацию каталитического белка 1 мкМ и концентрацию низкомолекулярного лиганда 8 мкМ. Путем последующего повторения описанных шагов получили 6 разведений, в которых концентрация каталитического белка оставалась неизменной и составляла 1 мкМ, а концентрация низкомолекулярного лиганда соответственно - 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ и 0,5 мкМ. Контролем служил 1 мкМ раствор каталитического белка. Помещали по 10 мкл каждого полученного раствора и контрольную пробу в капилляры Prometheus NT.48 (nanoDSF grade). Проводили сканирующую флуориметрию на приборе Prometheus NT.48 (NanoTemper Technologies, Германия) при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С /мин.
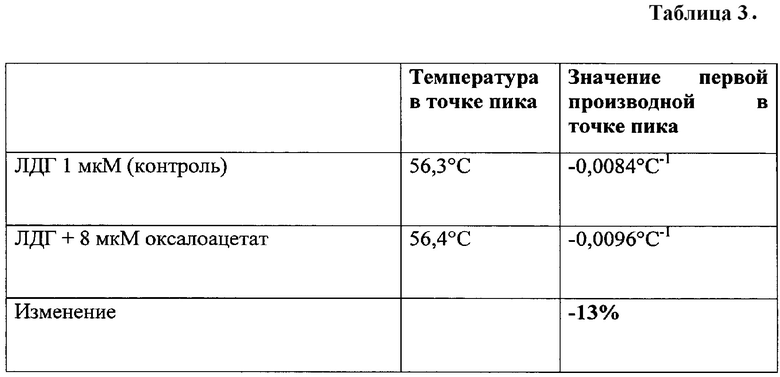
Строили график зависимости флуоресценции (соотношение 330/350 нм)от температуры нагревания для пробы, содержащий оксалоацетат в концентрации 8 мкМ и контрольной пробы, затем строили графики первых производных для полученных кривых (Фигура 1), находили значение первой производной в точке пика для контрольной и опытных проб (Таблица 3). Производили расчет отношения значений первой производной в точке пика опытной пробы к контрольной, где значение контрольной пробы принимай за 100%. Изменения отношения составило -13%, что входит в диапазон значений от 15% до -15% и свидетельствует об отсутствии влияния оксалоацетата в коцентрации 8 мкм на конформацию лактатдегидрогеназы.
Способ выявления влияния низкомолекулярных биологически активных лигандов на конформацию белка может быть использован в фундаментальных и клинических исследованиях, в области протеомики, метаболомики, энзимологии, а также в фармакологии при поиске малых молекул с теми или иными заданными терапевтическими ожиданиями или установления концентрации, в которой они оказывают действие на белок.
Источники информации
1. Гильмиярова Ф.Н., Рыскина Е.А., Колотьева Н.А., Потехина В.И., Горбачева И.В. Белок-лигандные взаимодействия: влияние минорных компонентов метаболизма. Сибирское медицинское обозрение. 2017;(6): 12-21. DOI: 10.20333/2500136-2017-6-12-21
2. Gilmiyarova F. Kolotyeva N., Radomskaya V., Gusyakova О., Gorbacheva I., Potekhina V. Role of the Metabolic Minor Components in the Regulation of Intermolecular Interaction // Journal of Biosciences and Medicines. 2016. Vol.4. pp. 28-35. doi: 10.4236/jbm.2016.47004
3. Kohl Т.O., Ascoli C.A. Direct Competitive Enzyme-Linked Immunosorbent Assay (ELISA) // Cold Spring Harbor Protocols. 2017. Vol.7. pp. 564-568. doi:10.1101/pdb.prot093740
4. Velazquez-Campoy A., Leavitt S. A., Freire E. Characterization of protein-protein interactions by isothermal titration calorimetry // Protein-Protein Interactions. 2015. Vol.1278. pp. 183-204. doi:10.1007/978-l-4939-2425-7_l 1
5. Jerabek-Willemsen M., Andre R., Wannera T., Roth H.M., Duhra S., Baaske P., Breitsprecher D. (2014) J. Mol. Struct, 5, 101-113.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ ВЛИЯНИЯ НИЗКОМОЛЕКУЛЯРНЫХ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ НА АФФИНИТЕТ БЕЛОК-ЛИГАНДНОЙ СВЯЗИ | 2018 |
|
RU2680408C1 |
| СТРУКТУРЫ СЛИТОГО БЕЛКА ШЕЛКА ПАУКОВ ДЛЯ СВЯЗЫВАНИЯ С ОРГАНИЧЕСКОЙ МИШЕНЬЮ | 2011 |
|
RU2624036C2 |
| СПОСОБ СИНТЕЗИРОВАНИЯ ФЛУОРЕСЦЕНТНО-МЕЧЕНОГО БЕЛКА | 1995 |
|
RU2162104C2 |
| СПОСОБ ПРЕОБРАЗОВАНИЯ ВОДОРАСТВОРИМЫХ АКТИВНЫХ БЕЛКОВ В ГИДРОФОБНЫЕ АКТИВНЫЕ БЕЛКИ, ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ МОНОМОЛЕКУЛЯРНЫХ СЛОЕВ ОРИЕНТИРОВАННЫХ АКТИВНЫХ БЕЛКОВ И УСТРОЙСТВА, ВКЛЮЧАЮЩИЕ ВОДОРАСТВОРИМЫЕ АКТИВНЫЕ БЕЛКИ, ПРЕОБРАЗОВАННЫЕ В ГИДРОФОБНЫЕ АКТИВНЫЕ БЕЛКИ | 2006 |
|
RU2420580C2 |
| Способ выявления влияния низкомолекулярных биологически активных соединений на взаимодействие антиген-антитело | 2020 |
|
RU2742210C1 |
| Способ получения профилактической противовирусной композиции на основе эпигаллокатехин-3-галлата (EGCG) | 2021 |
|
RU2771898C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ПРОДУКТОВ ПРОТЕОЛИЗА В ПЛАЗМЕ КРОВИ И ДИАГНОСТИЧЕСКАЯ ТЕСТ-СИСТЕМА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2015 |
|
RU2597782C1 |
| Комплексы на основе микропузырьков и способы применения | 2012 |
|
RU2613321C2 |
| СПОСОБЫ И ПРИМЕНЕНИЯ, ВКЛЮЧАЮЩИЕ ГЕМСВЯЗЫВАЮЩИЙ БЕЛОК 1 | 2009 |
|
RU2520748C2 |
| Пептиды, связывающие фактор роста эндотелия сосудов | 2019 |
|
RU2739246C1 |
Изобретение относится к биохимии. Предложен способ выявления влияния низкомолекулярных биологически активных лигандов на конформацию белка, при котором биологически активный лиганд низкомолекулярной массы в концентрациях 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ, 0,5 мкМ вносят в микрокапилляры «nanoDSF grade», содержащие белок в конечной концентрации 1 мкМ, получая опытные пробы, контрольной пробой служит раствор, содержащий белок в такой же конечной концентрации без добавления низкомолекулярного соединения; 10 мкл каждой из полученных опытных проб инкубируют в течение 5 минут в темном месте при температуре 25°С; проводят измерение эндогенной флуоресценции по остаткам тирозина и триптофана на приборе Prometheus NT.48 при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С/мин; строят график зависимости флуоресценции от температуры нагревания, строят графики первых производных для полученных кривых; рассчитывают значение температуры пика и значение первой производной в точке пика для контрольной и опытных проб, рассчитывают отношения значений первой производной в точке пика опытной и контрольной проб в процентах, значение первой производной в точке пика контрольной пробы принимают за 100%, при изменении отношения >15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону разворачивания, при изменении отношения <-15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону сворачивания, при изменении отношения от -15% до 15% включительно говорят об отсутствии влияния выбранного низкомолекулярного лиганда на конформацию белковой молекулы. Изобретение обеспечивает объективную оценку конформационного состояния белковой молекулы. 1 ил., 3 табл., 3 пр.
Способ выявления влияния низкомолекулярных биологически активных лигандов на конформацию белка, заключающийся в количественной характеристике конформационных изменений с использованием метода дифференциальной сканирующей флуориметрии, отличающийся тем, что биологически активный лиганд низкомолекулярной массы в концентрациях 16 мкМ, 8 мкМ, 4 мкМ, 2 мкМ, 1 мкМ, 0,5 мкМ вносят в микрокапилляры «nanoDSF grade», содержащие белок в конечной концентрации 1 мкМ, таким образом получая опытные пробы, контрольной пробой служит раствор, содержащий белок в такой же конечной концентрации без добавления низкомолекулярного соединения; 10 мкл каждой из полученных опытных проб инкубируют в течение пяти минут в темном месте при температуре 25°С; после чего проводят измерение эндогенной флуоресценции по остаткам тирозина и триптофана на приборе Prometheus NT.48 при интенсивности лазера 30%, длинах волн 330 и 350 нм, диапазоне нагрева от 20°С до 95°С, с шагом 1°С/мин; строят график зависимости флуоресценции - соотношения 330 нм/350 нм от температуры нагревания, затем строят графики первых производных для полученных кривых; рассчитывают значение температуры пика и значение первой производной в точке пика для контрольной и опытных проб, рассчитывают отношения значений первой производной в точке пика опытной и контрольной проб в процентах, значение первой производной в точке пика контрольной пробы принимают за 100%, при изменении отношения >15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону разворачивания, при изменении отношения <-15% по сравнению с контрольной пробой говорят об изменении конформации белковой молекулы в сторону сворачивания, при изменении отношения от -15% до 15% включительно говорят об отсутствии влияния выбранного низкомолекулярного лиганда на конформацию белковой молекулы.
| JERABEK-WILLEMSEN M., ET AL | |||
| MICROSCALE THERMOPHORESIS: INTERACTION ANALYSIS AND BEYOND/ J | |||
| Mol | |||
| Struct, 5, 2014, p.101-113 | |||
| СПОСОБ ВЫЯВЛЕНИЯ ВЛИЯНИЯ НИЗКОМОЛЕКУЛЯРНЫХ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ НА АФФИНИТЕТ БЕЛОК-ЛИГАНДНОЙ СВЯЗИ | 2018 |
|
RU2680408C1 |
| WO 2016210009 A2, 29.12.2016 | |||
| KOHL Т.O., ASCOLI C.A | |||
| DIRECT COMPETITIVE ENZYME-LINKED IMMUNOSORBENT ASSAY (ELISA)/ Cold Spring Harbor Protocols, Vol.7, 2017, p.564-568. | |||
Авторы
Даты
2019-08-28—Публикация
2019-06-13—Подача