ОБЛАСТЬ ТЕХНИКИ
[001] Данное техническое решение в общем относится к вычислительным системам и способам, а в частности к системам и способам оценки риска заболевания на основании генетических данных и/или данных о составе микробиоты кишечника, заполненного опросника.
УРОВЕНЬ ТЕХНИКИ
[002] Риск заболевания - это вероятность того, что случайно выбранный из популяции человек окажется больным данным заболеванием. В риск определенного заболевания у человека вносят вклад генетика и/или особенности микробиоты кишечника, факторы внешней среды, медицинская история, семейный анамнез и образ жизни человека.
[003] При расчете риска заболевания у человека, например, сахарного диабета 2-го типа, в качестве среднего риска заболевания в популяции используются показатели встречаемости заболевания.
[004] Понятие встречаемости относится к уже существующим событиям, в то время как понятие заболеваемости - к новым событиям. Встречаемость заболевания обычно рассчитывается как общее число диагностированных случаев данного заболевания относительно всей популяции.
[005] Заболеваемость обычно рассчитывается как число первично диагностированных случаев данного заболевания, зарегистрированных в некоторый период времени, относительно доли популяции, имеющей риск этого заболевания. Этот показатель отражает скорость, с которой новые случаи заболевания возникают в популяции.
[006] Из уровня техники известен патент US 7914449B2 "Diagnostic support system for diabetes and storage medium", патентообладатель: Sysmex Corp, дата публикации: 29.03.2011. В данном техническом решении приводится диагностическая система для выявления сахарного диабета 2-го типа, включающая устройство ввода, используемое для ввода диагностических данных, включая данные клинических испытаний; биологическую модель, имеющую параметры и представляющую функции органов, связанных с диабетом, в качестве числовой модели; средство для прогнозирования значений параметров, подходящих для пациента на основании диагностических данных и биологической модели; средство анализа патологического состояния пациента на основании значений параметров, предсказанных средством прогнозирования; средство формирования информации по диагностике на основании анализируемого патологического состояния; и средство вывода информации.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[007] Данное техническое решение направлено на устранение недостатков, свойственных решениям, известным из уровня техники.
[008] Технической задачей или, другими словами, технической проблемой, решаемой в данном техническом решении, является определение риска заболевания у пользователя.
[009] Техническим результатом, достигаемым при решении вышеуказанной технической задачи, является повышение точности оценки риска заболевания у пользователя за счет использования генетических данных и данных о составе микробиоты кишечника, заполненного опросника пользователя.
[0010] Дополнительным техническим результатом, достигаемым при осуществлении задачи, является обеспечение адресности рекомендаций по питанию, физической активности и образу жизни для пользователя за счет повышения точности оценки риска заболевания у пользователя.
[0011] Указанный выше технический результат достигается благодаря осуществлению способа оценки риска заболевания у пользователя на основании генетических данных и данных о составе микробиоты кишечника, в котором получают генетические данные, данные о составе микробиоты кишечника, генетические факторы риска, внешние факторы риска по меньшей мере одного пользователя, а также встречаемость по меньшей мере одного заболевания; по меньшей мере для одного пользователя определяют скорректированное отношение шанса заболеть заболеванием в группе с фактором риска к шансу заболеть во всей популяции для каждого фактора риска на основании полученных генетических данных пользователя и внешних факторов риска; формируют промежуточное значение риска заболевания у пользователя на основании встречаемости заболевания и скорректированного отношения шансов, полученного на предыдущем шаге; определяют относительную представленность микробных таксонов в кишечнике пользователя на основании данных о составе микробиоты кишечника посредством картирования чтений на референсный набор геномов; определяют меру отличия полученного состава микробиоты кишечника от микробиоты пациентов с данным заболеванием по данным о составе микробиоты кишечника данного пользователя; формируют итоговое значение риска заболевания у пользователя на основании промежуточного значения риска и меры отличия.
[0012] В некоторых вариантах осуществления технического решения дополнительно получают среднюю встречаемость заболевания в популяции и/или данные о связи состава микробиоты с заболеванием.
[0013] В некоторых вариантах осуществления технического решения генетическим фактором риска являются однонуклеотидные полиморфизмы (SNP).
[0014] В некоторых вариантах осуществления технического решения получают автоматически внешние факторы риска из статей, показывающих статистически значимую связь между риском и фактором.
[0015] В некоторых вариантах осуществления технического решения показатели внешних факторов риска для пользователя получают из заполняемого пользователем опросника.
[0016] В некоторых вариантах осуществления технического решения внешние факторы риска моделируются с использованием исследований ассоциации эпигеномов (EWAS).
[0017] В некоторых вариантах осуществления технического решения данные о составе микробиоты кишечника предоставлены в форматах FASTQ или FASTA.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0018] Признаки и преимущества настоящего технического решения станут очевидными из приведенного ниже подробного описания и прилагаемых чертежей, на которых:
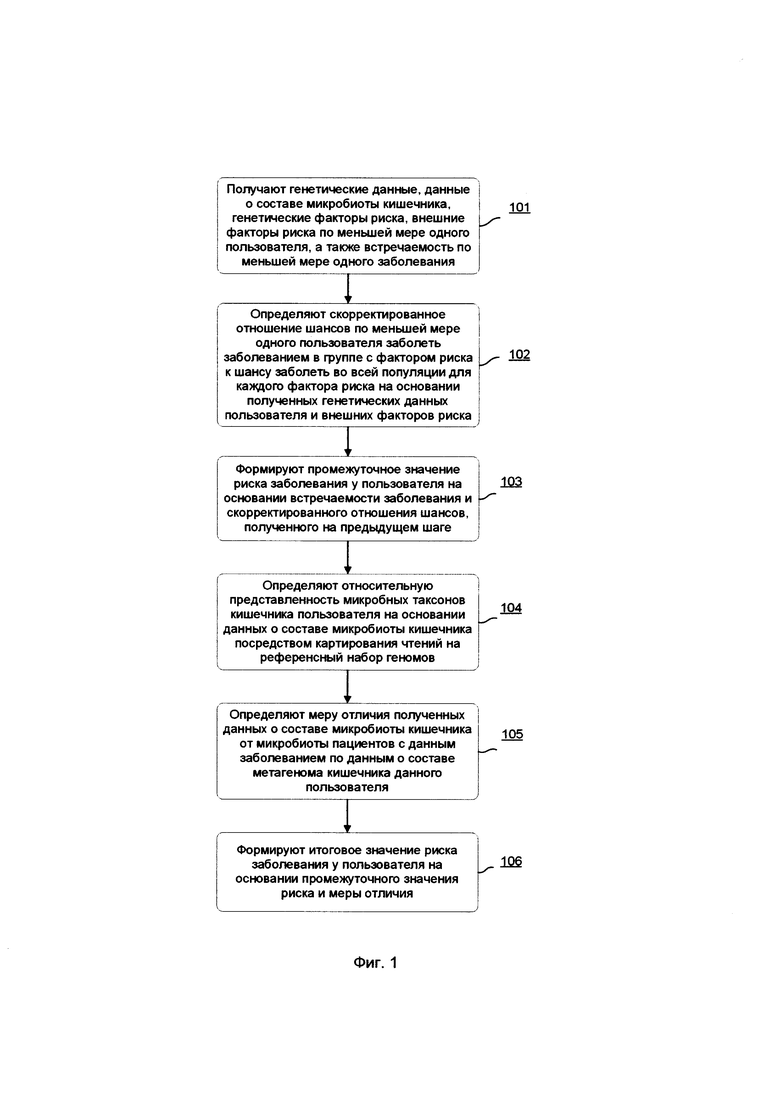
[0019] На Фиг. 1 показана блок-схема примера осуществления способа оценки риска заболевания у пользователя на основании генетических данных и/или данных о составе микробиоты кишечника, заполненного опросника;
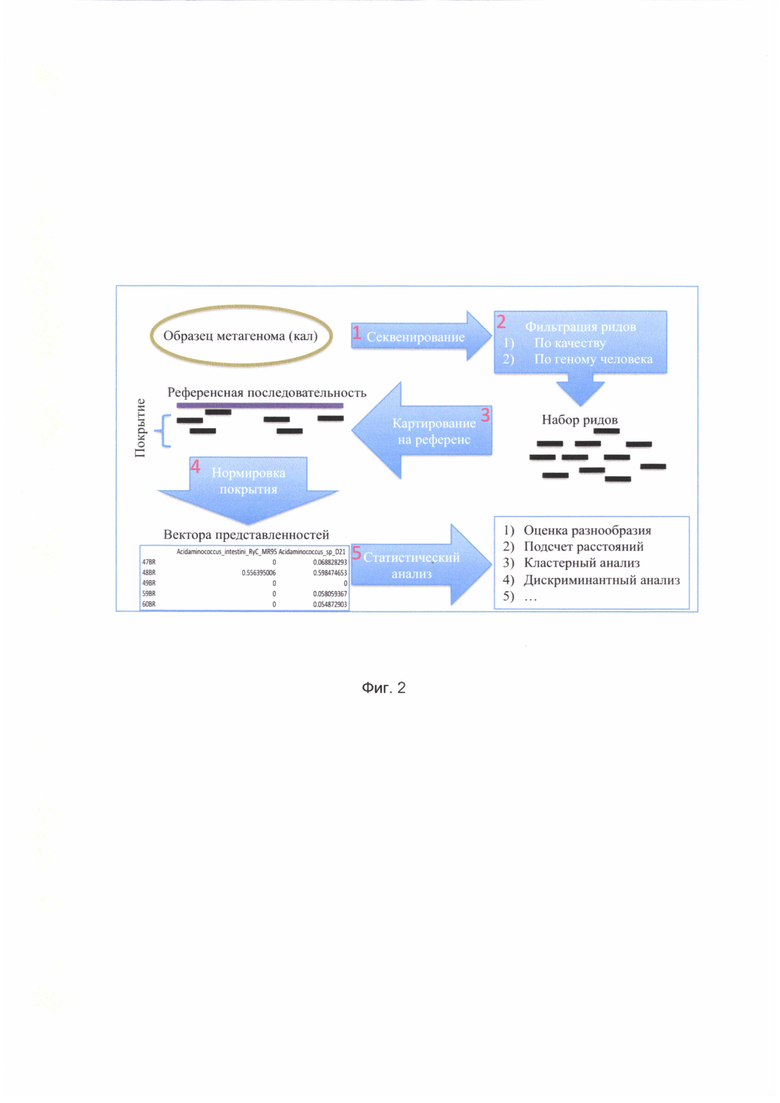
[0020] На Фиг. 2 показана схема анализа метагеномных данных от полногеномного секвенирования;
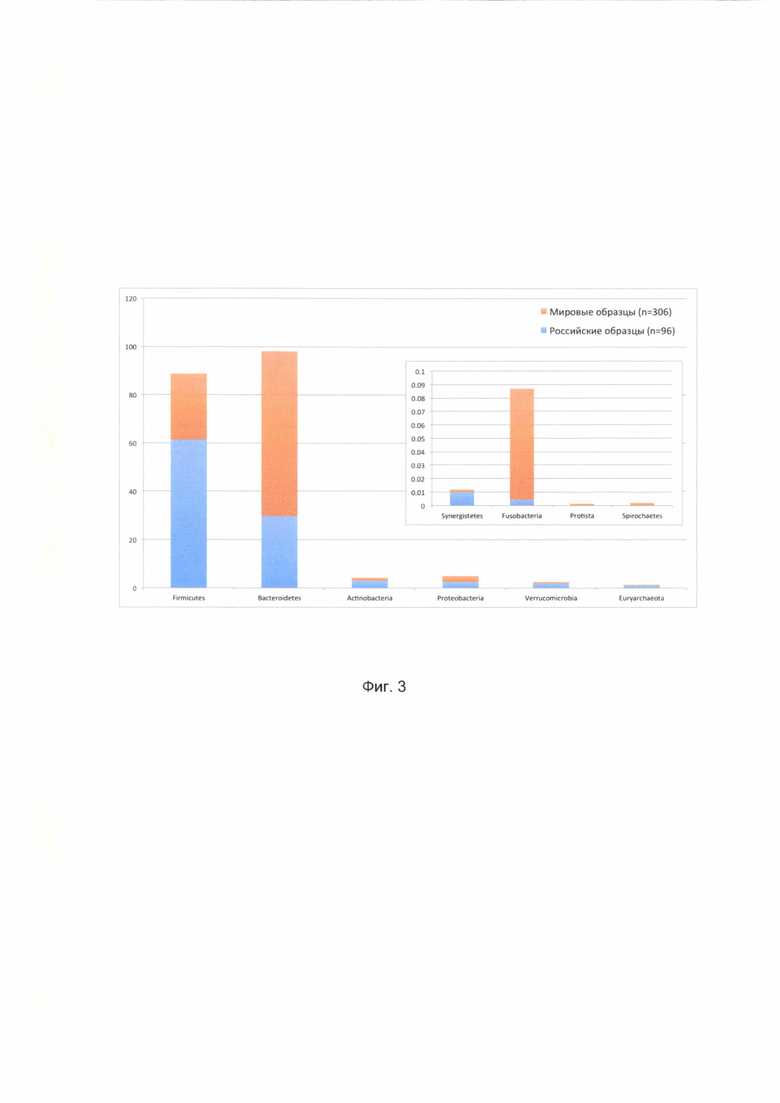
[0021] На Фиг. 3 показана гистограмма среднего процента представленности микробных отделов в российских образцах и в остальных;
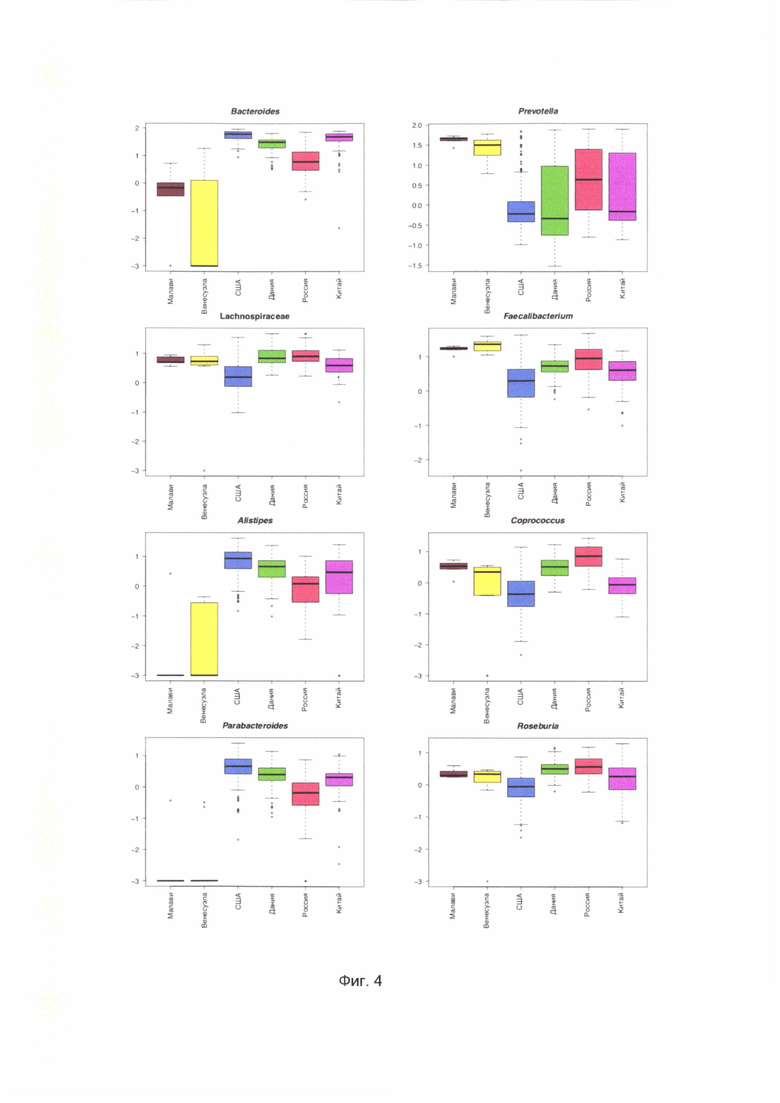
[0022] На Фиг. 4 показана относительная представленность микробных родов, составляющих 80% общего покрытия, по странам;
[0023] На Фиг. 5 показан пример осуществления картирования референсной последовательности ДНК;
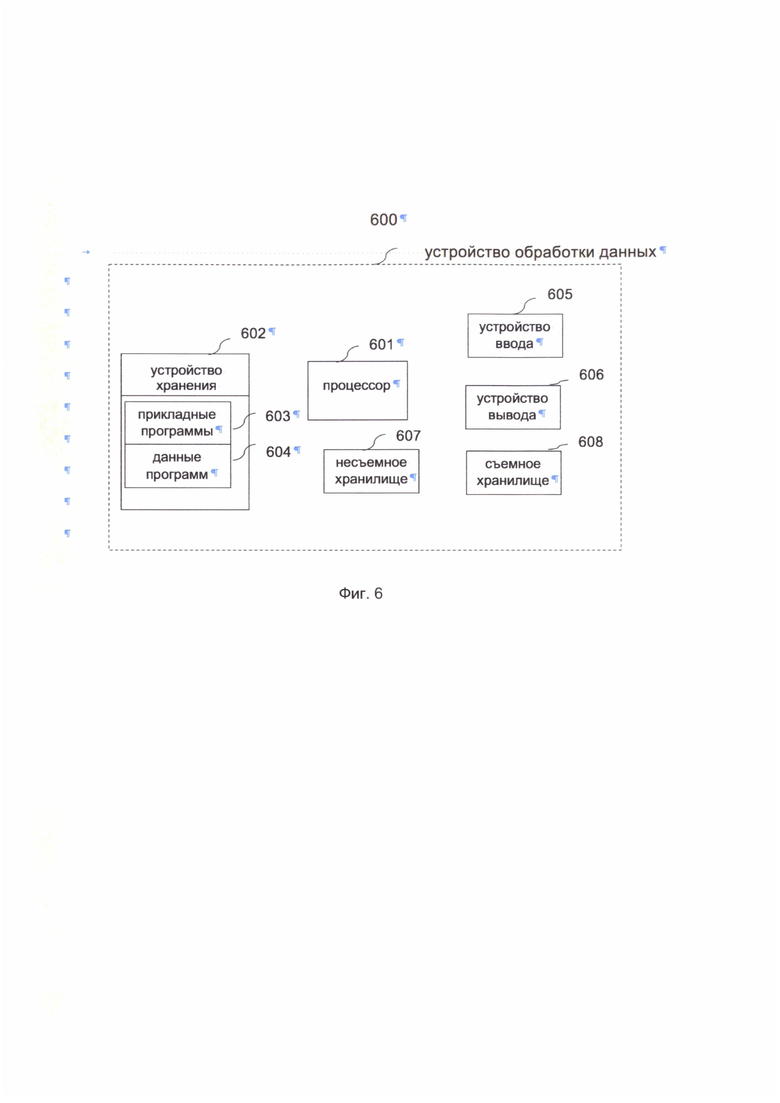
[0024] На Фиг. 6 показан пример осуществления системы оценки риска заболевания у пользователя на основании генетических данных и/или данных о составе микробиоты кишечника, заполненного опросника;
[0025] На Фиг. 7 показан вариант реализации, где диапазон значений генетического риска разбит на 2 отрезка, а меры отличия микробиоты от микробиоты больных пациентов - на 2 отрезка, то формируется 4 группы.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0026] Данное техническое решение может быть реализовано на компьютере или другом устройстве обработки данных, в виде автоматизированной системы или машиночитаемого носителя, содержащего инструкции для выполнения вышеупомянутого способа.
[0027] Техническое решение может быть реализовано в виде распределенной компьютерной системы, компоненты которой являются облачными или локальными серверами.
[0028] В данном решении под системой подразумевается компьютерная система или автоматизированная система (АС), ЭВМ (электронно-вычислительная машина), ЧПУ (числовое программное управление), ПЛК (программируемый логический контроллер), компьютеризированная система управления и любые другие устройства, способные выполнять заданную, четко определенную последовательность вычислительных операций (действий, инструкций).
[0029] Под устройством обработки команд подразумевается электронный блок либо интегральная схема (микропроцессор), исполняющая машинные инструкции (программы).
[0030] Устройство обработки команд считывает и выполняет машинные инструкции (программы) с одного или более устройства хранения данных. В роли устройства хранения данных могут выступать, но, не ограничиваясь, жесткие диски (HDD), флеш-память, ПЗУ (постоянное запоминающее устройство), твердотельные накопители (SSD), оптические приводы, облачные хранилища данных.
[0031] Программа - последовательность инструкций, предназначенных для исполнения устройством управления вычислительной машины или устройством обработки команд.
[0032] Ниже будут описаны термины и понятия, необходимые для осуществления настоящего технического решения.
[0033] Сахарный диабет 2-го типа (инсулиннезависимый диабет) - метаболическое заболевание, характеризующееся хронической гипергликемией, развивающейся в результате нарушения взаимодействия инсулина с клетками тканей.
[0034] Микробиота человека - это совокупность всех микроорганизмов в теле человека.
[0035] Генетические данные - это информация о структуре ДНК, последовательности нуклеотидов ДНК, одно- и олигонуклеотидных изменений в последовательности ДНК, включая все хромосомы конкретного организма. Генетическая информация частично определяет морфологическое строение, рост, развитие, обмен веществ, психический склад, предрасположенность к заболеваниям и пороки развития организма, не ограничиваясь.
[0036] Однонуклеотидный полиморфизм (ОНП, англ. single nucleotide polymorphism, SNP, произносится как "снип") - отличия последовательности ДНК размером в один или несколько нуклеотидов (А, Т, G или С) в геноме (или в другой сравниваемой последовательности) представителей одного вида или между гомологичными участками гомологичных хромосом.
[0037] Аллели - различные формы (значения) одного и того же гена или одного и того же локуса (позиции), расположенные в одинаковых участках (локусах) гомологичных хромосом.
[0038] Секвенирование ДНК - определение последовательности нуклеотидов в молекуле ДНК. Под этим может подразумеваться как амликонное секвенирование (прочтение последовательностей выделенных фрагментов ДНК, полученных в результате ПЦР реакции - таких, как ген 16S рРНК или его фрагменты), так и полногеномное секвенирование (прочтение последовательностей всей ДНК, присутствующей в образце).
[0039] Локус (лат.locus - место) в генетике означает местоположение определенного гена или нуклеотида на генетической или цитологической карте хромосомы.
[0040] Чтения (риды, reads) - данные, представляющие собой нуклеотидные последовательности фрагментов ДНК, полученные с помощью ДНК-секвенатора.
[0041] FASTA - формат записи последовательностей ДНК.
[0042] Картирование коротких прочтений - биоинформатический метод анализа результатов секвенирования нового поколения, состоящий в определении позиций в референсной базе геномов или генов, откуда с высокой и наибольшей вероятностью могло быть получено каждое конкретное короткое прочтение.
[0043] В результате секвенирования ДНК создается набор чтений. Длина чтения у современных секвенаторов составляет от нескольких сотен до нескольких тысяч нуклеотидов.
[0044] Таксономия - учение о принципах и практике классификации и систематизации сложноорганизованных иерархически соотносящихся сущностей.
[0045] Таксон - группа в классификации, состоящая из дискретных объектов, объединяемых на основании общих свойств и признаков.
[0046] Ген 16S рРНК - ген, присутствующий в геномах бактерий и архей, нуклеотидная последовательность которого используется для их таксономической классификации.
[0047] Фактор риска - это какое-либо свойство или особенность человека или какое-либо воздействие на него, изменяющее вероятность наличия болезни или травмы. Некоторые факторы могут являться наследственными или приобретенными, причем их влияние может проявляться при определенном воздействии.
[0048] Популяция (от лат.populatio - население) - это совокупность организмов одного вида, длительное время обитающих на одной территории.
[0049] В медицинских исследованиях, как показано в источнике информации [1], вероятность увидеть определенное событие в какой-то группе обычно называется риском, в то время как некоторые специалисты предпочитают термин "встречаемость". Для сравнения рисков между группами пациентов и/или здоровых индивидов используют соотношение рисков (англ. hazard ratio или HR) или относительный риск (англ. relative risk или RR), которые являются статистикой выбора.
[0050] Например, если π1 - вероятность события в первой группе, а π2 - вероятность события во второй группе, то относительный риск определяется по формуле:
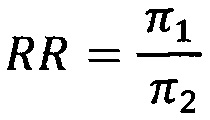
[0051] Другая статистика, обычно встречающаяся в медицинской литературе - это отношение шансов, как показано в источнике информации [2]. Шанс - это отношение вероятности того, что событие произойдет к вероятности того, что событие не произойдет. Отношение шансов (англ. Odds ratio или OR) - это отношение шансов для первой группы объектов к отношению шансов для второй группы объектов.
[0052] Ниже подробное описание данного технического решения будет раскрыто посредством использования в качестве примера заболевания сахарного диабета 2-го типа. Для любого специалиста в уровне техники очевидно, что данное заболевание является примерным, приведено для понимания сущности технического решения, и таким образом объем охраны не может им ограничиваться.
[0053] Способ оценки риска заболевания у пользователя может быть реализован как показано на Фиг. 1, включая следующие шаги.
[0054] Шаг 101: предварительно получают генетические данные, данные о составе микробиоты кишечника, генетические факторы риска, внешние факторы риска с их частотами и соответствующими значениями вклада в форме OR, встречаемость заболевания в популяции, данные о связи микробиоты кишечника с заболеванием.
[0055] В некоторых вариантах осуществления получает пробы биоматериала по меньшей мере одного пользователя. Вышеуказанные данные получают от пользователя посредством использования набора для отбора проб, включающий контейнер для образцов, имеющий компонент технологического реагента и сконфигурированный для приема образца из места сбора пользователем. Пользователь может предоставлять образцы с использованием службы доставки посылок (например, почтовой службы, службы доставки и т.д.). Дополнительно или альтернативно набор для отбора проб может быть предоставлен непосредственно через устройство, установленное в помещении или на улице, которое предназначено для облегчения приема пробы от пользователя. В других вариантах осуществления набор для отбора проб может быть сдан в клинику или другое медицинское учреждение медицинскому лабораторному технику или другому сотруднику. Однако предоставление набора(-ов) для отбора проб пользователя может дополнительно или альтернативно выполняться любым другим подходящим способом.
[0056] Набор для отбора проб предпочтительно выполнен с возможностью облегчения приема образцов от пользователей неинвазивным образом. В некоторых вариантах осуществления изобретения неинвазивные способы получения образца от человека могут использовать любой или несколько следующих вариантов: проницаемый субстрат (например, тампон, выполненный с возможностью протирать область тела человека, туалетная бумага, губка и т.д.), контейнер (например, флакон, трубка, мешок и т.д.), сконфигурированный для приема образца из области тела пользователя и любого другого подходящего элемента приема (слюна, кал, моча и т.д.). В конкретном примере образцы могут быть собраны неинвазивным образом из одного органа или нескольких, например, таких как нос, кожа, половой орган человека, полость рта и кишечник (например, с использованием тампона и флакона). Однако набор для отбора пробы может дополнительно или альтернативно быть использован для облегчения приема образцов полуинвазивным способом или инвазивным способом. В некоторых вариантах осуществления инвазивные способы приема образца могут использовать, например, иглу, шприц, биопсийные щипцы, трепан и любой другой подходящий инструмент для сбора образца полуинвазивным или инвазивным способом. В конкретных примерах пробы пользователей могут содержать один или несколько образцов крови, образцов плазмы / сыворотки (например, для экстракции бесклеточной ДНК) и образцов тканей. Дополнительно после помещения образца в набор для отбора пробы, образец обрабатывают специальным раствором или замораживают.
[0057] Входные образцы могут представлять из себя образцы (слюна, моча, кал, кровь), которые могут быть обработаны, например, в лаборатории, и из которых в дальнейшем получают генетические данные и данные о составе микробиоты кишечника путем генотипирования или секвенирования соответственно.
[0058] В некоторых вариантах осуществления получают дополнительные данные, которые учитываются при оценке риска заболевания у пользователя сахарного диабета 2-го типа, из датчиков, связанных с пользователем (пользователями) (например, датчиков носимых вычислительных устройств, датчиков мобильных устройств, биометрических датчиков, связанных с пользователем и т.д.). Данные могут быть о физической активности пользователя или физическом воздействии на него (например, данные акселерометра и гироскопа с мобильного устройства или носимого вычислительного устройства пользователя), данные об окружающей среде (например, данные о температуре, данные о высоте над уровнем моря, данные о климате, данные о параметрах света и т.д.), данные о питании пользователя или данные об используемой диете (например, данные из регистрационных записей о принимаемых пищевых продуктах, данные спектрофотометрического анализа и т.д.), биометрические данные (например, данные, регистрируемые с помощью датчиков в мобильном вычислительном устройстве пользователя), данные о местоположении (например, с использованием датчиков GPS), диагностические данные или любые другие подходящие данные. Дополнительно или альтернативно, дополнительный набор данных может быть получен из данных медицинской записи и/или клинических данных пользователя(ей). В некоторых вариантах осуществления дополнительный набор данных может быть получен из одной или нескольких электронных медицинских записей (EHR) пользователя(ей).
[0059] Затем на основании проб с образцами пользователя посредством генотипирования и секвенирования получают данные о генотипах однонуклеотидных полиморфизмов (SNP) и ДНК-прочтения (риды, англ. reads) бактерий пользователя.
[0060] Дополнительно получают среднюю встречаемость Р0, например, сахарного диабета 2-го типа в популяции, генетические факторы риска возникновения данного заболевания и внешние факторы риска возникновения заболевания.
[0061] Среднюю встречаемость Р0 заболевания, которая показывает, насколько широко заболевание встречается в популяции, например, для сахарного диабета 2-го типа получают из статей или регистров по встречаемости заболевания, где в выборке присутствует примерно равное число пользователей обоих полов, охвачен широкий диапазон возрастов, а сами пользователи принадлежат к этнически гомогенной группе, например, только европейцы.
[0062] Среднюю встречаемость Р0 заболевания автоматически могут получать по запросу, например, к API веб-платформы, содержащей набор статей, или посредством синтаксического анализа текста (другими словами, парсера) из материалов Национального центра статистики здравоохранения и/или Центра по контролю и профилактике заболеваний, Консорциума SIGMA (Slim Initiative in Genomic Medicine for the Americas) и т.д., не ограничиваясь. Различные компании, научные группы и исследовательские институты определяют среднюю встречаемость заболевания посредством определения общего количества заболеваний (как первичных, так и повторных, которые были выявлены ранее и послужили поводом для повторного визита к врачу) и его отношению к количеству населения той или иной страны, группы, компании и т.д. В некоторых вариантах осуществления может учитываться популяция за определенный промежуток времени, например, за 2007-й год или за 2017-й год.
[0063] Например, средняя встречаемость Р0 заболевания и процент диагностированных и не диагностированных случаев сахарного диабета 2-го типа среди взрослых в возрасте ≥18 лет в США представлена в следующей Таблице 1, где ДИ - доверительный интервал.
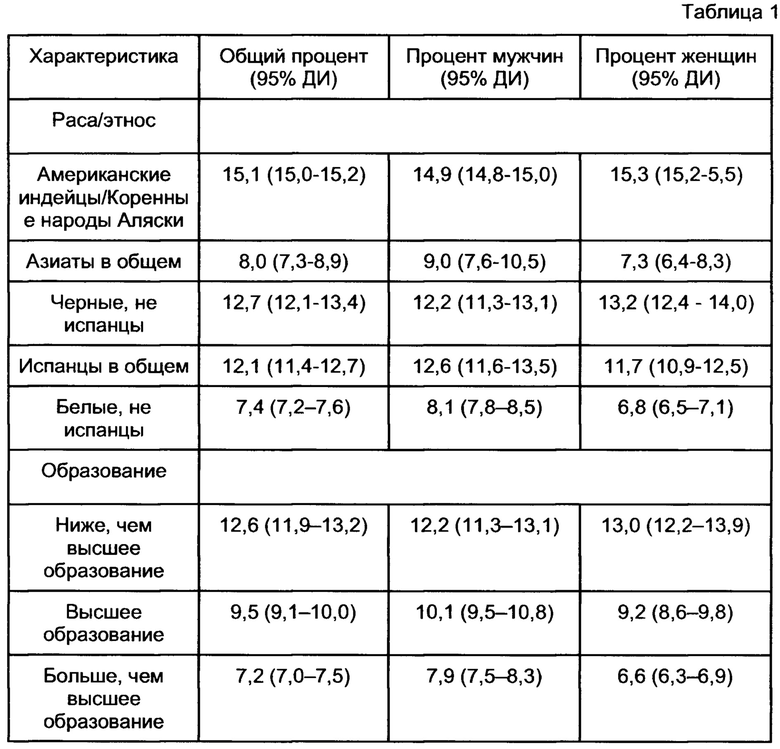
[0064] Встречаемость Р0 может зависеть от уровня доходов в стране и меняться с каждым годом, причем как увеличиваясь, так и уменьшаясь.
[0065] Общее количество заболеваний индивидов в стране, на материке, в городе, компании, по полу, возрастной или другой группе для определения встречаемости заболевания могут брать в конкретной временной точке, в течение некоторого периода времени или же как число индивидов, у которых заболевание было диагностировано в течение всей жизни.
[0066] В роли генетических факторов риска заболевания могут использовать однонуклеотидные полиморфизмы (SNP). Данные о вкладе SNP в общий риск заболевания извлекаются из исследований полногеномного поиска ассоциаций (GWAS) с предпочтением к GWAS мета-анализам, для поиска которых используют GWAS агрегаторы (например, GWAS Catalog, GWAS Central), а также, например, базу данных медицинских и биологических публикаций PubMed, не ограничиваясь.
[0067] К используемой информации для каждого генетического фактора риска (SNP) возникновения заболевания относятся:
- название SNP (например, rs5749482);
- локус, к которому принадлежит SNP (например, TIMP3);
- альтернативный аллель (вариант SNP из референсного генома, например, С) и эффекторный аллель (мутантный вариант/вариант данного SNP, отличный от референсного в популяции, например, G);
- значение риска (OR, RR или HR), связанное с эффекторным аллелем: берется либо из этапа повторного анализа GWAS, либо из этапа комбинирования данных первичного и повторного анализов. OR может принимать значение 1.31;
- p-value: могут браться только SNP с p-value ≤5*10-8. Например, может принимать значение 2.00Е-26.
[0068] Например, генетическими факторами риска сахарного диабета 2-го типа являются SNP из двух локусов в районе генов ARL15 и RREB1, которые в сильной степени связаны с регуляцией уровней инсулина и глюкозы в организме, что является двумя ключевыми характеристиками сахарного диабета 2-го типа.
[0069] Генетическим фактором риска может являться SNP в гене супрессора опухолевого роста PTEN, который является ответственным за чувствительность тканей к действию инсулина.
[0070] Каждый генетический фактор имеет частоту-значение, которое может быть неотрицательным числом. SNP имеет частоту для какого-либо своего аллеля. Например, SNP под названием rs334 имеет 4 аллеля: А, Т, G и С. При этом частота аллеля Т составляет 0.0274, или 2.74%.
[0071] В некоторых вариантах осуществления частота выражается в виде доли или процента, причем всегда рациональным числом. Доля при этом может быть равна не более 1, а процент не более 100.
[0072] Определение частоты аллеля является общеизвестным из уровня техники. Пусть при наличии n человек каждого генотипируют по одному SNP. После этого получают числа для трех возможных генотипов SNP: А/А, А/В, В/В, где частота аллеля А в таком случае будет равна: Р(А)=(2×N(A/A)+N(A/B))/2n.Частота аллеля В: Р(В)=1-Р(А). Процесс может быть модифицирован этапом контроля качества, когда проверяется, соответствует ли распределение генотипов равновесию Харди-Вайнберга или нет.
[0073] Например, у SNP rs10012946 есть три генотипа, обладатели которых представлены таким число людей:
[0074] С/С 359
[0075] С/Т 449
[0076] Т/Т 159
[0077] Исходя из этого частота аллеля определяется следующим образом по формуле Т=(2*Т/Т+Т/С)/2*N=(2*159+449)/(2*967)=0.3965873837.
[0078] Частота аллеля С=1-Т=1-0.3965873837=0.6034126163.
[0079] Список внешних факторов риска заболевания первично берется из систематического обзора по каждому заболеванию, например, по сахарному диабету 2-го типа. Далее для каждого внешнего фактора риска автоматически, в сети Интернет или на локальном хранилище данных, осуществляется поиск оригинальной статьи, показывающей статистически значимую связь между риском и фактором. Поиск и выявление связей осуществляют с помощью набора библиотек, фреймворков и пакетов для символического и статистического анализа естественного языка и обработки речи на основании названий внешних факторов риска, например, на английском языке (risk factors, prevention, smoking, physical activity, nutrition). Данные инструменты позволяют выполнять обнаружение предложений, токенизацию, определение частей речи, речевых оборотов, лемматизацию, анализ и разрешение кореферентности. Статистически значимой считается связь с p-value <0,05 с учетом поправки на множественное тестирование, и доверительным интервалом для значения риска (OR, RR или HR), не содержащим единицу.
[0080] Таблица 2, показанная ниже, иллюстрирует статистическую связь между определенными внешними факторами и риском заболевания, например, сахарного диабета 2-го типа. Сила связи выражена в форме отношения шансов (OR), статистическая значимость связи выражена в форме доверительного интервала (CI 95%) для OR и в форме p-value.
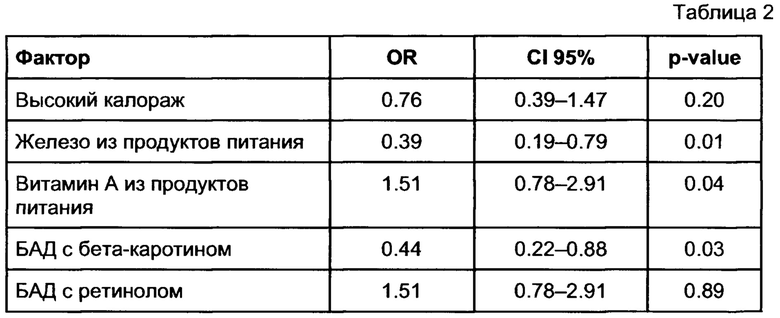
[0081] Итак, к основным внешним факторам риска, значительно повышающим риск заболевания, могут относиться курение, лишний вес, ожирение, алкоголь, инфекции, загрязненная атмосфера, воздействие радиации, плохая наследственность.
[0082] В некоторых вариантах осуществления внешние факторы риска могут иметь удельный вес, например, выраженный в процентах, или значение от 0 до 1 для каждого фактора, или от 0 до 100, как показано например в Таблице 3.

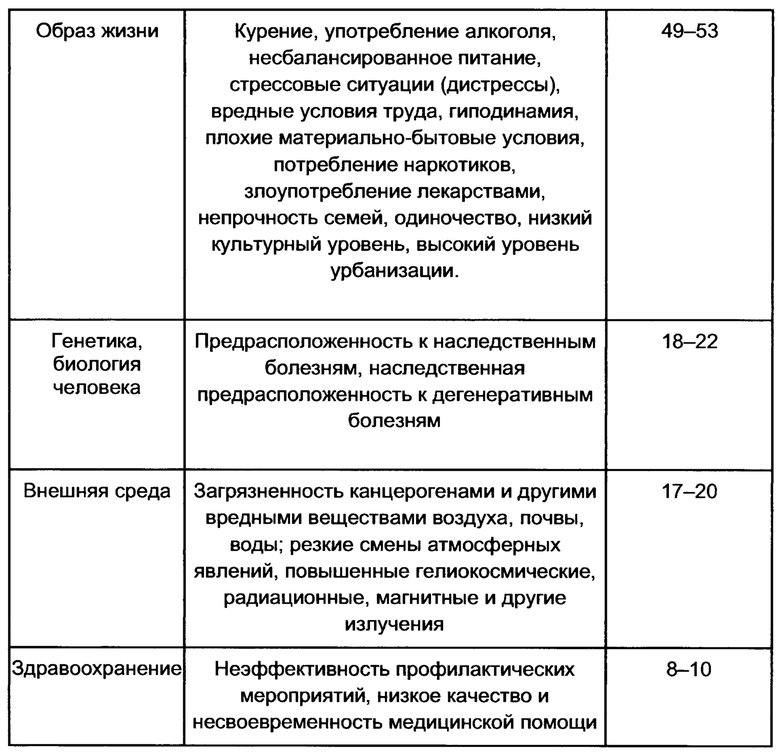
[0083] В некоторых вариантах осуществления показатели внешних факторов риска для пользователя получают из заполняемого пользователем опросника.
[0084] В опроснике для пользователя могут быть, например, следующие вопросы:
[0085] 1. Ваш пол
[0086] 2. Дата рождения
[0087] 3. Сколько вы сейчас весите в кг?
[0088] 4. Какой у вас рост в см?
[0089] 5. Вы курите?
a. Курю сейчас
b. Раньше курил(а)
с. Никогда
[0090] 6. Требует ли ваша работа среднеинтенсивной физической деятельности в течение минимум десяти минут, при которой учащается дыхание или пульс? Например, быстрая ходьба или поднимание небольших тяжестей.
a. Да
b. Нет
[0091] Например, если человек много курит или имеет лишний вес, это уже является факторами риска, которые могут повлиять на общий риск диабета 2-го типа.
[0092] В некоторых вариантах осуществления внешние факторы риска, которые могут вызывать, например, сахарный диабет 2-го типа (пестициды, тяжелые металлы, потребление пищевых добавок), могут быть смоделированы с использованием исследований ассоциации эпигеномов (англ. epigenome-wide association studies, EWAS).
[0093] Генетические данные, данные о составе микробиоты кишечника, генетические факторы риска, внешние факторы риска с их частотами и соответствующими значениями вклада в форме OR, встречаемость заболевания в популяции, данные о связи состава микробиоты с заболеванием получают с помощью настольной микро-ЭВМ или мобильного устройства связи, которым может являться мобильный телефон, смартфон, планшет, посредством использования беспроводной передачи данных. Мобильное устройство связи может быть выполнено с возможностью получения и передачи сигналов во время процесса получения/отправки данных. В частности, передаваемая базовой станцией информация обрабатывается одним или несколькими процессорами в системе после получения. В общем, мобильное устройство связи может содержать, помимо прочего, антенну, по меньшей мере, один усилитель, настроечное устройство, один или несколько излучателей, карточку модуля определения абонента (SIM), приемопередатчик, ответвитель, малошумящий усилитель (МШУ), дуплексную антенну и т.д. Кроме того, мобильное устройство связи может также поддерживать связь с сетью или другими устройствами посредством беспроводной связи. Беспроводная связь может использовать любой стандарт или протокол связи, включая, помимо прочего, глобальный стандарт цифровой мобильной сотовой связи (GSM), надстройку над технологией мобильной связи GSM, осуществляющую пакетную передачу данных (GPRS), множественный доступ с кодовым разделением каналов (CDMA), широкополосный множественный доступ с кодовым разделением каналов (WCDMA), стандарт беспроводной высокоскоростной передачи данных для мобильных телефонов (LTE), электронную почту, сервис обмена короткими сообщениями (SMS), PUSH-уведомления и пр.
[0094] Шаг 102: по меньшей мере для одного пользователя определяют скорректированное отношение шансов заболеть в группе с фактором риска к шансу заболеть во всей популяции для каждого фактора риска на основании генетических данных пользователя и ответов опросника.
[0095] На данном шаге определяют значение скорректированного отношения шансов (англ. adjusted odds ratio или aOR) посредством устройства обработки данных для каждого фактора риска, как генетического, так и внешнего, на основании генетических данных пользователя и его ответов в опроснике. Значение скорректированного отношения шансов является отношением шанса заболеть сахарным диабетом 2-го типа в группе с фактором риска к шансу заболеть во всей популяции.
[0096] Например, известно, что SNP называется rs17050272, эффекторный аллель имеет значение А, альтернативный аллель имеет значение G, а связанное с эффекторным аллелем OR=1.03.
[0097] Заболеванием является подагра, частота заболевания у мужчин равна 0.0397, а частота встречаемости генотипов следующая:
[0098] А/А 0.2332301342
[0099] A/G 0.4963880289
[00100] G/G 0.2703818369
[00101] Тогда aOR для каждого генотипа будет следующим:
[00102] А/А 1.030923417
[00103] A/G 1.000896521
[00104] G/G 0.9717441955
[00105] Отношение шансов близко к относительному риску в случае если заболеваемость очень мала (менее 1% обеспечивает точность оценки до десятых).
[00106] Шаг 103: формируют промежуточное значение риска заболевания у пользователя на основании встречаемости заболевания и скорректированного отношения шансов, полученного на предыдущем шаге;
[00107] Предварительно определяют промежуточное значение риска, например, сахарного диабета 2-го типа посредством взятия натурального логарифма произведения aOR всех факторов риска пользователя:
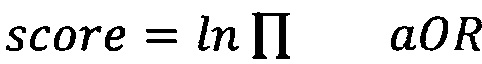 ;
;
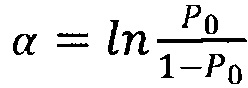 ;
;
[00108] где α - базовое значение для данного заболевания, a score - это индивидуальная компонента данного пользователя.
[00109] Значение α меняется только при изменении Р0, т.е. среднепопуляционной частоты встречаемости заболевания.
[00110] Итоговое значение риска заболевания, по генетическим и внешним факторам риска, определяют по формуле логистической регрессии следующим образом:
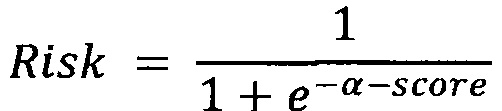
[00111] Логистическая регрессия применяется для предсказания вероятности возникновения некоторого события по значениям множества признаков. Таким образом, при определении риска сахарного диабета 2-го типа оценивается, насколько отклонился пользователь от среднего показателя встречаемости заболевания (средним показателем является a, a score - отклонением).
[00112] Например, для мужчины из популяции Великобритании со значением средней встречаемости 0.063, имея генетические и внешние факторы риска, получают следующий риск сахарного диабета 2-го типа у пользователя, как показано в Таблице 4.
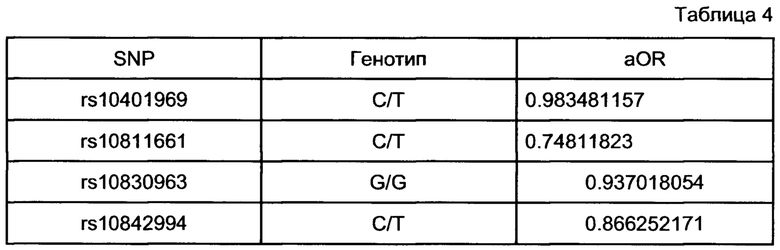
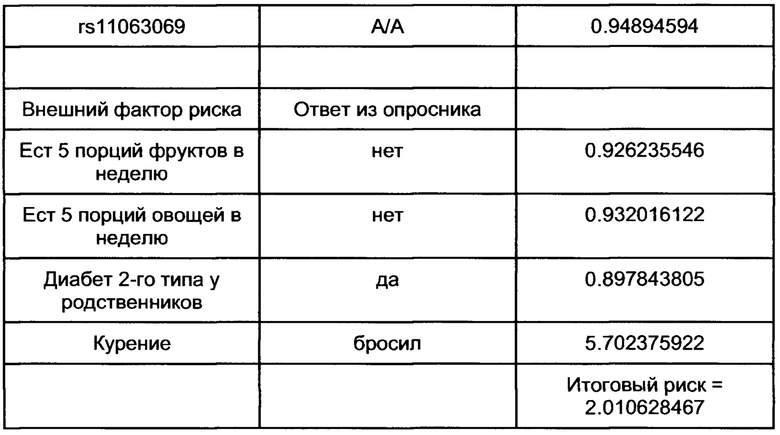
[00113] На основании вышеприведенных данных из Таблицы 4 риск сахарного диабета 2-типа у пользователя принимает численное значение 0.11908735.
[00114] Затем на основании определенных значений риска заболевания пользователя сахарным диабетом 2-го типа оценивают распределение риска, которое показывает, какая доля людей, прошедших анализ, имеет то или иное значение риска.
[00115] Например, для сахарного диабета 2-го типа для женщин из российской популяции границы между 5 группами могут быть следующие (в порядке возрастания):
[00116] 1-2: 0.0329063148;
[00117] 2-3: 0.0418203642;
[00118] 3-4: 0.0612654491;
[00119] 4-5: 0.0765442933;
[00120] Например, риск заболевания у некоего пользователя женского пола равен 0.0572001.
[00121] Это между 2 и 3 границами, то есть в III группе риска, причем риск
заболевания принимает значение как средний.
[00122] Для британских мужчин границы могут быть, например, такие:
[00123] 1-2: 0.0398192919
[00124] 2-3: 0.0503116186
[00125] 3-4: 0.0709393878
[00126] 4-5: 0.090999356
[00127] Это позволяет ранжировать людей в порядке возрастания риска заболевания и относить каждого человека в одну из следующих рисковых групп:
- низкая (ниже 10 процентиля);
- пониженная (между 10-ым и 30-ым процентилем);
- средняя (между 30-ым и 70-ым процентилем);
- повышенная (между 70-ым и 90-ым процентилем);
- высокая (между 90-ым и 100-ым процентилем).
[00128] На основании определенных значений риска заболевания располагают пользователей по возрастанию их индивидуального риска в рисковые группы, после чего делят эти значения на процентили как описано выше. Затем определяют, где проходят границы между описанными выше рисковыми группами, после чего оценивают риск заболевания у данного пользователя относительно выявленных границ и относят его в одну из групп.
[00129] Определение границ осуществляется на основании статистики, например следующим образом. Например, для заболевания "Болезнь Альцгеймера" определяют риск заболевания среди реальных пользователей: упорядочивают их по возрастанию риска и отсекают процентили, как описано выше. Для этого заболевания для женщин границы прошли через следующие значения в порядке возрастания:
[00130] 0.04515797
[00131] 0.06140678
[00132] 0.07983051
[00133] 0.11074957
[00134] Затем промежуточное значение риска заболевания пользователя корректируют на основании данных о составе микробиоты кишечника пользователя.
[00135] Каждое заболевание ассоциировано с определенными чертами - биомаркерами, определяемые по составу микробиоты кишечника, как известно из уровня техники. Было проведено исследование отличий микробиоты кишечника у людей, больных сахарным диабетом 2-го типа от здоровых людей: у них преобладали бактерии рода Bacteroides и было меньше бактерий рода Prevotella по сравнению с контрольной выборкой. Представленность Bifidobacterium spp и Bacteroides vulgatus была ниже в опытной группе, a Clostridium leptum - выше. Примечательно, что список этих биомаркеров различается в европейской и азиатской популяции, что говорит о вероятном вкладе образа жизни, социокультурных факторов и этнической группы.
[00136] Данные о составе микробиоты кишечника, полученные в результате метагеномного секвенирования, могут быть представлены в форматах FASTQ или FASTA, по одному файлу на каждый образец микробиоты.
[00137] Предпочтительно может применяться секвенирование генов 16S рРНК, но также может применяться полногеномное секвенирование (WGS). Для секвенирования могут применяться следующие платформы, не ограничиваясь, illumina/SOLEXA, lon Torrent, SOLiD, Helicos.
[00138] При анализе образца микробиоты с помощью секвенирования последовательностей генов 16S рРНК или полногеномного секвенирования осуществляется полуколичественный (процентное или долевое содержание в образце) таксономический анализ данных путем определения, к какой известной бактерии принадлежит каждое чтение.
[00139] Таксономический анализ метагеномных образцов могут определять посредством картирования нуклеотидных чтений на неизбыточный референсный каталог из репрезентативных геномов и/или генов микроорганизмов, но не ограничиваясь.
[00140] Референсный геном, как показано на Фиг. 5, представляет собой последовательность ДНК в цифровом виде, составленная как общий репрезентативный пример генетического кода того или иного вида.
[00141] Глубина покрытия нормируется на ряд параметров: общее количество нуклеотидов, картировавшихся на весь референсный набор и длину генома. Также проводится суммирование нормированной глубины покрытия по родам. Полученные значения, именуемые векторами представленности по образцам, приводятся к процентному содержанию микроорганизмов в образце и используются в дальнейшем анализе.
[00142] В результате обработки набора метагеномов в формате 16S рРНК получается таблица относительной представленности, как показано на Фиг. 2, которая отражает количество чтений, отнесенных к каждой таксономической единице (ОТЕ) из базы данных для каждого образца.
[00143] В некоторых вариантах осуществления относительная представленность метагенома нормируется (Фиг. 2, позиция 4). Для этого для каждого образца суммируется количество его чтений, которые успешно откартировались на референсную базу. Нормированная представленность для каждого таксона рассчитывается как количество чтений, отнесенных к этому таксону для данного образца, деленное на общую сумму откартированных чтений для этого образца и помноженное на 100%. Из полученных значений нормированной представленности составляется нормированная таблица представленности, содержащая процент чтений, отнесенных к каждому таксону из базы данных для каждого образца.
[00144] Далее осуществляется фильтрация (Фиг. 3, позиция 2) малопредставленных таксонов - например, по следующему принципу: оставляются бактериальные виды, представленность которых превышает 0,2% от общей микробной представленности не менее чем в 10% образцах, но не ограничивается этим примером.
[00145] Таблица относительной представленности бактериальных чтений агрегируются на различных таксономических уровнях, в частности до уровня родов, при этом суммируется относительная представленность всех присутствующих в образце представителей одного рода.
[00146] В целом, микробиотные образцы из России, также, как и в остальном мире, в основном состоят из микробов, принадлежащих к отделам Bacteroidetes и Firmicutes (Фиг. 3).
[00147] Наиболее представленными являются образцы рода Bacteroides, Prevotella, отдел Lachnospiraceae, Faecalibacterium, Alistipes, Coprococcus, Parabacteroides и Roseburia. Все вместе они составляют 80% от общей микробной представленности. Их относительная представленность по географическим группам в логарифмическом масштабе в сравнении с данными из более ранних исследований кишечной микробиоты населения стран мира показана на Фиг. 4.
[00148] Пример фрагмента Таблицы 5, на которой показана относительная представленность (%) в образцах (строки) некоторых бактериальных родов (столбцы).
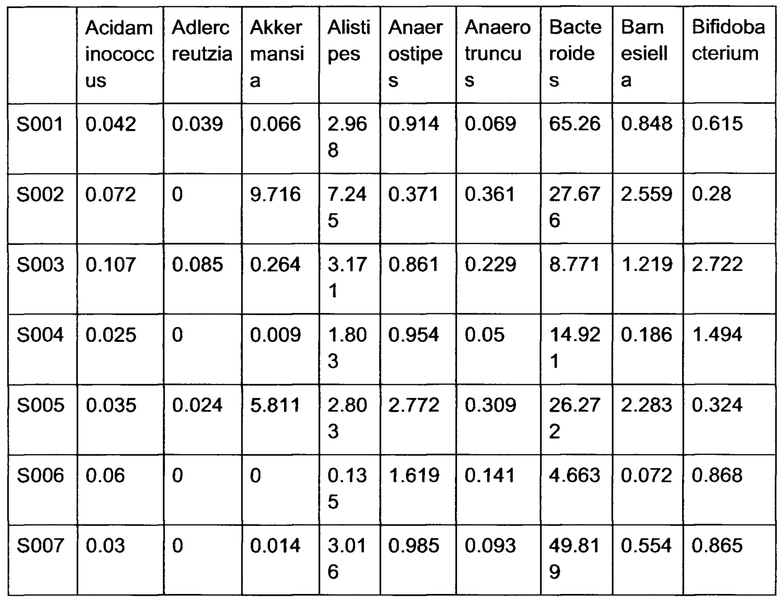
[00149] Предварительно из данных по составу образцов микробиоты кишечника популяционной выборки создается так называемый контекст, т.е. референсные данные для сравнения, следующим образом.
[00150] Для каждой бактерии (рода или иного таксона, не ограничиваясь) определяют набор фиксированных процентилей по представленности, например, 33%- и 67%-процентили. Иначе говоря, получают два порога представленности: треть образцов из популяционной выборки имеет меньшую представленность по данной бактерии, чем меньший порог; а треть образцов из популяционной выборки имеет большую представленность по данной бактерии, чем больший порог.
[00151] В некоторых вариантах реализации пороговые значения для процентилей могут быть заранее вычислены на основании результатов статистического анализа относительной представленности микробного таксона у пациентов с данным заболеванием (лиц с повышенным риском, например, сахарного диабета 2-го типа) по сравнению со здоровыми индивидами. Например, для бактериального рода Eubacterium, чья представленность используется как один из метагеномных биомаркеров диабета 2-го типа, такие значения представленности составляют менее 3,7% и более 6,1% для перехода в 33 и 67 процентили соответственно.
[00152] Определения степени отличия данного полученного образца микробиоты от микробиоты кишечника, характерной для людей с сахарным диабетом 2-го типа (далее именуемое мерой отличия от микробиоты пациентов) происходит с использованием набора прямо или обратно ассоциированных с ним микробных таксонов (биомаркеров).
[00153] Пример списка микробных таксонов-биомаркеров.

[00154] Шаг 105: определяют меру отличия полученных данные о составе микробиоты кишечника от микробиоты пациентов с данным заболеванием по данным о составе метагенома кишечника для данного пользователя.
[00155] Для образца пользователя по сахарному диабету 2-го типа выставляется мера отличия, которая может быть рассчитана по следующим правилам:
[00156] Для данного образца каждому микроорганизму, например, бактерии, (или таксону) из числа биомаркеров сахарного диабета 2-го типа присваивается значение 0, N(k) или М(k) (где k - номер биомаркера, a N(k) и М(k) - специфичные для данного биомаркера сахарного диабета 2-го типа константы) по следующим правилам:
i. Если данный биомаркер не содержится в данном образце, этому биомаркеру присваивается число 0.
ii. Если представленность данный биомаркер в данном образце ниже верхнего и выше нижнего процентиля, этому биомаркеру присваивается число 0.
iii. Если данный таксон по данным о связи биомаркеров и диабета второго типа не влияет на данную болезнь, этому таксону присваивается число 0.
iv. Если представленность данного биомаркера в данном образце превышает верхний процентиль и, по данным таблицы связей биомаркеров и диабета второго типа, положительно ассоциирован с этим заболеванием, этому биомаркеру присваивается число -М(k).
v. Если представленность данного биомаркера в данном образце ниже нижнего процентиля и, по данным о связи биомаркеров и диабета второго типа, положительно ассоциирован с этим заболеванием, этому биомаркеру присваивается число N(k).
vi. Если представленность данного биомаркера в данном образце выше верхнего процентиля и, по данным о связи биомаркеров и диабета второго типа, отрицательно ассоциирован с этим заболеванием, этому биомаркеру присваивается число 1.
vii. Если представленность данного биомаркера в данном образце ниже нижнего процентиля и, по данным о связи биомаркеров и диабета второго типа, отрицательно ассоциирован с этим заболеванием, этому биомаркеру присваивается число -1.
[00157] Например, у данного индивидуума представленность рода Eubacterium - 2%. Данный род входит в число биомаркеров диабета 2-го типа, он отрицательно ассоциирован с заболеванием и его представленность ниже нижнего процентиля (для Eubacterium нижнее пороговое значение составляет 3,7%). Соответственно в этом случае присваивается число -1.
[00158] В некоторых примерных вариантах реализации для всех биомаркеров (k=1, …) N(k)=M(k)=1.
[00159] Данному образцу присваивается мера отличия данных о составе микробиоты кишечника от микробиоты пациентов с данным заболеванием, равная сумме величин, присвоенных биомаркерам на предыдущем шаге. Например, по биомаркеру род Eubacterium получили число -1, по Akkermansia - 0. Если бы это были все биомаркеры сахарного диабета 2-го типа, то мера отличия была бы равна -1. В других вариантах осуществления обобщение вклада биомаркеров может производиться по другой формуле.
[00160] Затем мера отличия для пользователя шкалируется по следующему правилу:
a. Нижний процентиль меры отличия от сахарного диабета 2-го типа, вычисленный по контексту, принимается в новой шкале за 0;
b. Верхний процентиль меры отличия от сахарного диабета 2-го типа, вычисленный по контексту, принимается в новой шкале за 10;
c. Значение меры отличия пользователя пропорционально нормализуется по новой шкале.
[00161] Полученное значение является мерой отличия микробиоты от микробиоты пациентов, оцененной по полученному составу микробиоты кишечника пользователя.
[00162] В других вариантах осуществления технического решения могут быть использованы иные процентили. Также каждый таксон может иметь свой индивидуальный вес, складывающийся из оценки его влияния на признак и его представленности в конкретном образце, отличный от 1, -1 или 0.
[00163] Шаг 106: формируют итоговое значение группы риска заболевания у пользователя на основании промежуточного значения риска и меры отличия микробиоты кишечника пользователя от микробиоты пациентов с данным заболеванием.
[00164] На данном шаге осуществляют формирование итогового общего значения группы риска заболевания у пользователя на основании определенного промежуточного риска заболевания и меры отличия микробиоты кишечника пользователя от микробиоты пациентов.
[00165] Группа риска заболевания, рассчитанная на основании генетических данных, может корректироваться с учетом данных о составе микробиоты кишечника следующим образом.
[00166] При следующих значениях меры отличия по микробиоте принимают следующие значения:
- 0-5 добавляется 1 к значению группы риска заболевания, рассчитанного на основании генетических данных, вплоть до 5;
- 6-7: группа риска заболевания не меняется;
- 8-10: добавляется -1 к значению группы риска заболевания, вплоть до 1;
[00167] Если нет генетических данных, то группа риска может определяться по следующей таблице соответствия:

[00168] Способ определения риска заболевания не ограничивается предложенными вариантами, а также может включать в себя иную систему расчета баллов, рассчитываться на основе линейной модели зависимости риска заболевания от генетических данных и микробиоты на основе данных, полученных в ходе проспективных исследований и подтверждающих наличие таких связей.
[00169] Способ определения итогового риска заболевания не ограничивается предложенными вариантами реализации и также может включать учет известных зависимостей между генетическими данными, внешними факторами риска и составом микробиоты.
[00170] В одном из вариантов осуществления эти зависимости могут быть оценены через меры корреляции или ковариации между генетическими рисками заболевания у пользователя и относительной представленности микробных таксонов в микробиоте кишечника.
[00171] В одном из вариантов осуществления вместо микробных таксонов зависимости могут быть оценены для других признаков состава микробиоты, в том числе микробных генов, групп генов или метаболических путей, или же групп микробных таксонов, а также альфа-разнообразия.
[00172] Зависимости могут быть взяты из исследований, проведенных как на пациентах с наличием заболевания или другими метаболическими нарушениями, так и на здоровых добровольцах [4].
[00173] В одном из вариантов осуществления технического решения оценки зависимостей могут быть использованы для формирования взвешенной суммы генетических и микробиотных рисков заболевания.
[00174] В одном из вариантов осуществления технического решения значения весов в данной сумме могут быть вычислены по следующему принципу: чем выше корреляция представленности микроорганизма и набора генетических факторов риска данного заболевания, тем выше вес данного микроорганизма.
[00175] В одном из вариантов осуществления, если для конкретных зависимостей между составом микробиоты, внешними факторами риска, заболеванием и генетикой известен биологический механизм и прояснены причинно-следственные связи таких зависимостей и возможно оценить размер эффекта влияния представленности микроорганизма-биомаркера на развитие болезни, то для подсчета совокупного риска заболевания можно использовать интегральную оценку, включающую в себя известные ковариации между генетическими факторами риска, микробиотной представленностью и манифестацией заболевания [5].
[00176] В одном из вариантов осуществления, формирование групп риска может быть проведено следующим образом: диапазон возможных значений генетического риска разбивается на конечное число отрезков, аналогичная процедура проводится для меры отличия микробиоты индивида от микробиоты больного; после этого каждому из полученных минимальных прямоугольников, формирующих разбиение диапазонов двух признаков, соотносится одна группа. Для групп необязательно задание порядка возрастания (или убывания) риска. Например, если в одном из вариантов реализации диапазон значений генетического риска разбит на 2 отрезка, а меры отличия микробиоты от микробиоты больных - на 2 отрезка, то формируется 4 группы (соответствующие прямоугольникам и обозначенные символами А, В, С, D на Фиг. 7). Индивид относится к одной из групп в соответствии с диапазонами двух признаков, в который он попадает.
[00177] Данное техническое решение может быть реализовано посредством системы оценки риска заболевания у пользователя на основании генетических данных и данных о составе микробиоты кишечника пользователя. Примерная система для реализации технического решения включает в себя устройство обработки данных 600. Устройство обработки данных 600 может быть сконфигурировано как клиент, сервер, мобильное устройство или любое другое вычислительное устройство, которое взаимодействует с данными в системе совместной работы, основанной на сети. В зависимости от варианта реализации устройство обработки данных может быть одно одним устройством обработки данных и обеспечивать все шаги способа, а может включать несколько устройств обработки данных, каждое из которых будет осуществлять только отдельные шаги. В самой базовой конфигурации устройство обработки данных 600, как правило, включает в себя, по меньшей мере, один процессор 601 и устройство хранения данных 602. В зависимости от точной конфигурации и типа вычислительного устройства устройство хранения данных 602, которым является системная память, может быть энергозависимой (например, оперативное запоминающее устройство (ОЗУ, RAM)), энергонезависимой (например, постоянное запоминающее устройство (ПЗУ, ROM)) или некоторой их комбинацией. Устройство хранения данных 602, как правило, включает в себя одну или более прикладных программ 603, инструкции которых воплощают способ оценки риска заболевания у пользователя на основании генетических данных и данных о составе микробиоты кишечника пользователя, и может включать в себя данные 604 указанных программ. Устройство обработки данных 600 может иметь дополнительные особенности или функциональные возможности. Например, устройство обработки данных 600 может также включать в себя дополнительные устройства хранения данных (съемные и несъемные), такие как, например, магнитные диски, оптические диски или лента. Такие дополнительные хранилища проиллюстрированы на Фиг. 6 посредством съемного хранилища 607 и несъемного хранилища 608. Компьютерные носители данных могут включать в себя энергозависимые и энергонезависимые, съемные и несъемные носители, реализованные любым способом или при помощи любой технологии для хранения информации, такой как машиночитаемые инструкции, структуры данных, программные модули или другие данные. Устройство хранения данных 602, съемное хранилище 607 и несъемное хранилище 608 являются примерами компьютерных носителей данных. Компьютерные носители данных включают в себя, но не в ограничительном смысле, оперативное запоминающее устройство (ОЗУ), постоянное запоминающее устройство (ПЗУ), электрически стираемое программируемое ПЗУ (EEPROM), флэш-память или память, выполненную по другой технологии, ПЗУ на компакт-диске (CD-ROM), универсальные цифровые диски (DVD) или другие оптические запоминающие устройства, магнитные кассеты, магнитные ленты, хранилища на магнитных дисках или другие магнитные запоминающие устройства, или любую другую среду, которая может быть использована для хранения желаемой информации и к которой может получить доступ устройство обработки данных 600. Любой такой компьютерный носитель данных может быть частью устройства обработки данных 600. Устройство обработки данных 600 может также включать в себя устройство(а) 605 ввода информации, такие как клавиатура, мышь, перо, устройство с речевым вводом, устройство сенсорного ввода, и так далее. Устройство(а) 606 вывода, такие как дисплей, динамики, принтер и тому подобное, также могут быть включены в состав системы.
[00178] Устройство обработки данных 600 содержит коммуникационные соединения, которые позволяют устройству связываться с другими вычислительными устройствами, например по сети. Сети включают в себя локальные сети и глобальные сети наряду с другими большими масштабируемыми сетями, включая, но не в ограничительном смысле, корпоративные сети и экстрасети. Коммуникационное соединение является примером коммуникационной среды. Как правило, коммуникационная среда может быть реализована при помощи машиночитаемых инструкций, структур данных, программных модулей или других данных в модулированном информационном сигнале, таком как несущая волна, или в другом механизме, и включает в себя любую среду доставки информации. Для примера, но без ограничения, коммуникационные среды включают в себя проводные среды, такие как проводная сеть или прямое проводное соединение, и беспроводные среды, такие как акустические, радиочастотные, инфракрасные и другие беспроводные среды.
[00179] Настоящее подробное описание составлено с приведением различных не имеющих ограничительного и исчерпывающего характера вариантов осуществления. В то же время, специалистам, имеющим средний уровень компетентности в рассматриваемой области техники, очевидно, что различные замены, модификации или сочетания любых раскрытых здесь вариантов осуществления (в том числе частично) могут быть воспроизведены в пределах объема настоящего технического решения. Таким образом, подразумевается и понимается, что настоящее описание технического решения включает дополнительные варианты осуществления, суть которых не изложена здесь в явно выраженной форме. Такие варианты осуществления могут быть получены путем, например, сочетания, модификации или преобразования каких-либо действий, компонентов, элементов, свойств, аспектов, характеристик, ограничений и пр., относящихся к приведенным здесь и не имеющим ограничительного характера вариантам осуществления.
ИСПОЛЬЗУЕМЫЕ ИСТОЧНИКИ ИНФОРМАЦИИ
[00180] 1. Stare J., Maucort-Boulch D. Odds Ratio, Hazard Ratio and Relative Risk // Metodoloski Zvezki. - 2016. - T. 13. - №. 1. - C. 59.
[00181] 2. Bland J.M., Altman D.G. The odds ratio // Bmj. - 2000. - T. 320. - №. 7247. - C. 1468.
[00182] 3. Qin J. et al. A metagenome-wide association study of gut microbiota in type 2 diabetes // Nature. - 2012. - T. 490. - №. 7418. - C. 55-60.
[00183] 4. Imhann F., Vich Vila A., Bonder M.J., et al. Interplay of host genetics and gut microbiota underlying the onset and clinical presentation of inflammatory bowel disease // Gut. - 2018. T. 67. - C. 108-119.
[00184] 5. Dudbridge F., Pashayan N., Yang J. Predictive accuracy of combined genetic and environmental risk scores // Genet Epidemiol. - 2018. T. 42. - C. 4-19.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА И СПОСОБ ИНТЕРПРЕТАЦИИ ДАННЫХ И ПРЕДОСТАВЛЕНИЯ РЕКОМЕНДАЦИЙ ПОЛЬЗОВАТЕЛЮ НА ОСНОВЕ ЕГО ГЕНЕТИЧЕСКИХ ДАННЫХ И ДАННЫХ О СОСТАВЕ МИКРОБИОТЫ КИШЕЧНИКА | 2017 |
|
RU2699284C2 |
| СПОСОБ И СИСТЕМА ОТСЛЕЖИВАНИЯ РАЦИОНА И ФОРМИРОВАНИЯ ЗАКЛЮЧЕНИЯ О КАЧЕСТВЕ ПИТАНИЯ И/ИЛИ ИНДИВИДУАЛЬНЫХ РЕКОМЕНДАЦИЙ ПО ПИТАНИЮ | 2019 |
|
RU2721234C1 |
| СПОСОБ И СИСТЕМА ФОРМИРОВАНИЯ ИНДИВИДУАЛЬНОГО РАЦИОНА ПРОДУКТОВ ПИТАНИЯ ПОСЛЕ ПЕРЕСАДКИ МИКРОБИОТЫ | 2018 |
|
RU2699283C1 |
| Способ определения индивидуального генетического риска развития ишемического инсульта | 2014 |
|
RU2612630C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ПРИСУТСТВИЯ ИЛИ ОТСУТСТВИЯ АГРЕССИВНОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2013 |
|
RU2675370C2 |
| СПОСОБ ПРОГНОЗА ДЛЯ ИНДИВИДУУМОВ С РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2013 |
|
RU2669809C2 |
| КОМПЛЕКТ ДЛЯ ПРОГНОЗИРОВАНИЯ ИЛИ ДИАГНОСТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ И СПОСОБ ДИАГНОСТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ | 2020 |
|
RU2800086C1 |
| МАРКЕРЫ РИСКА ДЛЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ У ПАЦИЕНТОВ С ХРОНИЧЕСКИМ ЗАБОЛЕВАНИЕМ ПОЧЕК | 2014 |
|
RU2656148C2 |
| МАРКЕРЫ РИСКА СЕРДЕЧНО-СОСУДИСТОГО ЗАБОЛЕВАНИЯ | 2010 |
|
RU2524659C2 |
| СПОСОБ ДИАГНОСТИКИ ВОЛЧАНКИ У ЧЕЛОВЕКА | 2010 |
|
RU2596391C2 |


Настоящее изобретение относится к медицине. Предложен способ оценки риска заболевания у пользователя на основании генетических данных и данных о составе микробиоты кишечника, а также встречаемости заболевания, генетических и внешних факторов риска. Данное изобретение обеспечивает повышение точности оценки риска заболевания у пользователя. 6 з.п. ф-лы, 7 ил., 5 табл.
1. Компьютерно-реализуемый способ оценки риска заболевания у пользователя на основании генетических данных и данных о составе микробиоты кишечника, результатов опросника, выполняемый посредством устройства обработки данных и включающий следующие шаги:
- получают пробы биоматериала по меньшей мере одного пользователя, референсный набор геномов из базы данных;
- получают генетические данные, содержащие по меньшей мере данные о структуре ДНК, последовательности нуклеотидов ДНК, одно- и олигонуклеотидных изменений в последовательности ДНК, а также данные о составе микробиоты кишечника из пробы биоматериала пользователя посредством генотипирования и секвенирования, а генетические факторы риска, внешние факторы риска по меньшей мере одного пользователя, а также встречаемость по меньшей мере одного заболевания из базы данных;
- определяют скорректированное отношение шансов по меньшей мере одного пользователя заболеть заболеванием в группе с фактором риска к шансу заболеть во всей популяции для каждого фактора риска на основании полученных генетических данных пользователя и внешних факторов риска посредством устройства обработки данных;
- формируют промежуточное значение риска заболевания у пользователя на основании встречаемости заболевания и скорректированного отношения шансов, полученного на предыдущем шаге, посредством взятия натурального логарифма произведения скорректированных отношений шансов всех факторов риска пользователя;
- определяют относительную представленность микробных таксонов кишечника пользователя на основании данных о составе микробиоты кишечника посредством картирования чтений на референсный набор геномов;
- определяют меру отличия полученных данных о составе микробиоты кишечника от микробиоты пациентов с данным заболеванием по данным о составе метагенома кишечника данного пользователя;
- формируют итоговое значение риска заболевания у пользователя на основании промежуточного значения риска и меры отличия.
2. Способ по п. 1, характеризующийся тем, что дополнительно получают среднюю встречаемость заболевания в популяции и/или данные о связи микробиоты с заболеванием.
3. Способ по п. 1, характеризующийся тем, что генетическим фактором риска являются однонуклеотидные полиморфизмы (SNP).
4. Способ по п. 1, характеризующийся тем, что получают автоматически внешние факторы риска из статей, показывающих статистически значимую связь между риском и фактором.
5. Способ по п. 1, характеризующийся тем, что показатели внешних факторов риска для пользователя получают из заполняемого пользователем опросника.
6. Способ по п. 1, характеризующийся тем, что внешние факторы риска моделируются с использованием исследований ассоциации эпигеномов (EWAS).
7. Способ по п. 1, характеризующийся тем, что данные о составе микробиоты кишечника предоставлены в форматах FASTQ или FASTA.
| Токарный резец | 1924 |
|
SU2016A1 |
| DEURENBERG RUUD H | |||
| et al | |||
| "Application of next generation sequencing in clinical microbiology and infection prevention." Journal of biotechnology, 2017 (Available online 29 December 2016), 243: 16-24 | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| СПОСОБ ДИАГНОСТИКИ СОСТОЯНИЯ МИКРОБИОТЫ КИШЕЧНИКА НА ФОНЕ ЭРАДИКАЦИОННОЙ ТЕРАПИИ HELICOBACTER PYLORI И ЕГО ПРИМЕНЕНИЕ | 2015 |
|
RU2616280C1 |
| EP 3012760 A1, 27.04.2016 | |||
| КОСТРЮКОВА Е | |||
| С | |||
| и др., "Вариабельность относительного содержания геномной ДНК человека при метагеномном анализе микробиоты кишечника." Биомедицинская химия, 2014, 60(6): 695-701. | |||
Авторы
Даты
2019-09-05—Публикация
2018-02-15—Подача