Изобретение относится к химии биологически активных соединений и касается конкретно 2,3,4-триметокси-N'-(8-метил-8-азабицикло[3.2.1.] октан-3-илиден) бензогидразида гидрохлорида, соединение со структурной формулой (I):
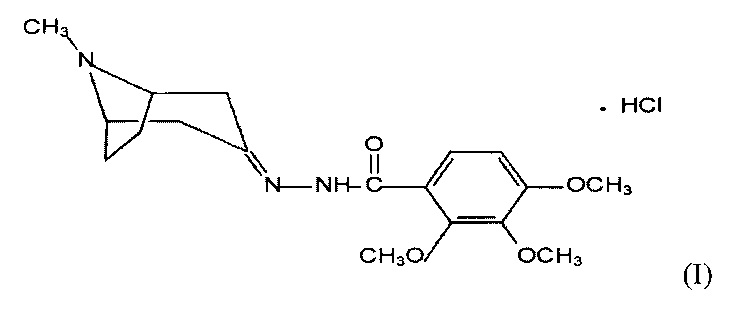
При изучении фармакологической активности соединения I было установлено, что оно обладает выраженными противомигреневыми и анксиолитическими свойствами.
Изыскание и изучение фармакологических средств лечения больных мигренью является одной из приоритетных проблем современной медицины, так как мигрень относится к наиболее распространенным и социально значимым заболеваниям. В развитых странах Европы и Америки мигренью страдает от 3 до 16% населения [P.M. Rist, J.E. Buring, C.S. Kaseetal., Migraine and functional out come from ischemic cerebral eventsin women.Circulation, 2010, 122, 24, 2551-2557; W.Dent, B.Stelzhammer, M.Meindl, W.B. Matujaetal, Migraine attack frequency, duration, and pain intensity: disease burden derived from a community-based survey in northern Tanzania, Headache, 2011, 51, 10, 1483-1492, doi: 10.1111/j. 1526-4610. 2011; A. Pezzini, E. Del Zotto, A. Giossi, et al., The migraine-ischemic stroke relation in young adults, Stroke Res. Treatment, 2010, 9, 304921, doi: 10.4061/2011/]. Несмотря на различия в представлениях о патогенезе мигрени, большинство исследователей указывает на существенную роль серотонина, нейрогенного и цереброваскулярного компонентов в патогенезе этого заболевания [M.A. Moskowitz, Genes, proteases, cortical spreading depression and migraine: impact on pathophysiology and treatment. FunctionalNeurology, 2007, 22,3, 133-136].
В настоящее время для лечения больных мигренью широко используются препараты, воздействующие на серотониновые рецепторы - агонисты 5HT1B/D- и антагонисты 5НТ2А/2B/2C-типа. Наибольшее распространение для лечения больных мигренью получили препараты, воздействующие на серотониновые рецепторы первого (5HT1Aa/1B/1D/1F) и второго (5HT2A/2B/2C) типов, что указывает на важную роль серотонина в патогенезе этого заболевания. Для купирования приступа мигрени применяют агонисты 5-НТ1В/1D/1F-рецепторов (суматриптан, золмитриптан, наратриптан и др.) [S.J. Tepper, A.M. Rapoport, F.D. Sheftell, Mechanisms of action of the 5-HT1B/1D receptor agonists. Arch Neurol., 2002, 59, 1084-1088; T. Muller, L. Lohse, Efficacy of parecoxib, sumatriptan, and rizatriptan in the treatment of acute migraine attacks. Clin. Neuropharmacol., 2011, 34, 6, 206-209], а для меж приступного лечения - антагонисты 5НТ2В/2C-рецепторов (метисергид, пизотифен, ципрогептадин, ницерголин), которые препятствуют сосудосуживающему эффекту серотонина [E.J. Mylecharane, J.Misbach, J.W. Duckworth, J.W. Lance, Effects of methysergide, pizotifen and ergotamine in the monkey cranial circulation. Eur. J. Pharmacol., 1978; 48, 1-9;K. Schmuck, C. Ullmer, H.O. Kalkman, et al., Activation of meningeal 5-HT2B receptors: an early step in the generation of migraine headache? Eur. J. Neurosci., 1996, 8, 5, 959-967; G. Casucci, V. Villani, F. Frediani,Central mechanism of action of antimigraine prophylactic drugs. Neurol. Sci., 2008, 29, 123-126; J.A. Charles, Pathophysiology of Chronic Migraine and Mode of Action of Preventive Medications: A Comment. Headache: The Journal off leadand Face Pain, 2011, 51, 10, 1550-1551].
Однако указанные препараты, применяемые для лечения мигрени, не всегда отличаются достаточной эффективностью и обладают выраженными нежелательными побочными свойствами. Этим определяется необходимость поиска новых препаратов для профилактики и лечения приступа мигрени.
Поэтому поиск новых препаратов для профилактики и лечения приступа мигрени является важнейшей задачей современной фармакологии и неврологии.
В ФГБНУ «НИИ фармакологии имени В.В. Закусова» создан оригинальный антагонист серотониновых рецепторов с противомигреневой активностью - тропоксин, который в настоящее время проходит клинические испытания [Т.С. Ганьшина и соавт., Тропоксин - новое средство для лечения мигрени. Химико-фармацевт. журнал, 2016, 50, 1, 19-23]. Тропоксин, блокируя 5HT2B/2C-рецепторы, предупреждает развитие констрикторных реакций мозговых сосудов, вызванных серотонином [Р.С. Мирзоян и соавт., Тропоксин - новый антагонист серотонина и потенциальное противомигреневое средство. Эксперим. и клин. фармакол., 1998, 61, 2, 28-31]. В то же время, при изучении фармакокинетики соединения, было установлено, что тропоксин в организме быстро подвергается метаболизму, чем, по-видимому, обусловлено его непродолжительное действие. Тропоксин не обладает анксиолитическим эффектом. Вместе с тем, желательным для противомигреневых препаратов является наличие у препарата анксиолитической активности, т.к. больные мигренью при приближении и во время приступа испытывают состояние тревоги.
В литературе имеются сведения о нескольких ацильных производных гидразонов тропан-3-она, заявленных в качестве средств с противотуберкулезным, стимулирующим и антидепрессивным действием [U.S. Pat. 2, 838, 914], а также с противомигреневыми свойствами [Р.С. Мирзоян и соавт., Цереброваскулярные антагонисты и агонист серотонина среди производных тропана. Эксперим. и клин. фармакол., 2008, 71, 1, 26-30]. Однако, среди ацильных производных гидразонов тропан-3-онов, соединений, проявивших как противомигреневую, так и анксиолитическую активность, до настоящего времени обнаружено не было.
Задачей настоящего изобретения является разработка нового противомигреневого средства, обладающего антисеротониновой активностью с анксиолитичекским компонентом действия.
Технический результат. Предложено новое химическое соединение, обладающее выраженной антисеротониновой цереброваскулярной активностью: 2,3,4-триметокси-N'-(8-метил-8-азабицикло[3.2.1.] октан-3-илиден) бензогидразид гидрохлорид. Отличительной особенностью настоящего изобретения является наличие в спектре действия анксиолитической активности. Изобретение расширяет арсенал средств для лечения мигрени.
Результатом применения предлагаемого соединения является наличие в одном препарате двух важных для лечения больных мигренью эффектов: устранение, характерного для первой фазы приступа, спазмов сосудов мозга, обусловленных блокадой серотониновых рецепторов сосудов мозга и устранение тревожности, обусловленное наличием у препарата анксиолитической активности.
Заявленное соединение обладает выраженным противомигреневым и анксиолитическим действием и может найти применение в медицинской практике в качестве препарата для лечения мигрени.
Заявленное соединение I синтезировано в виде гидрохлорида по следующей схеме:
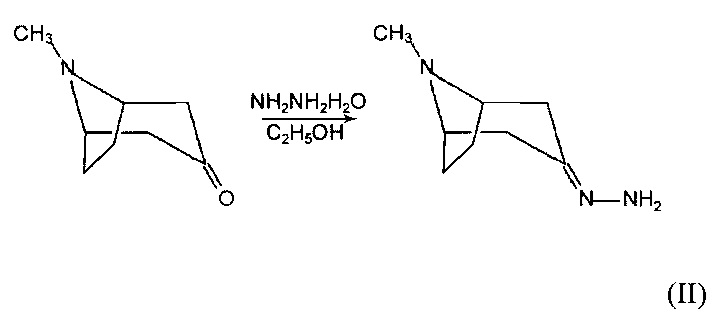
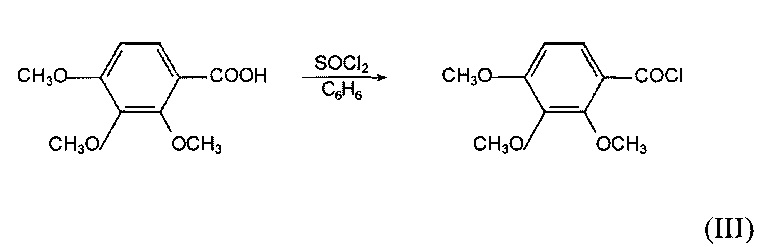
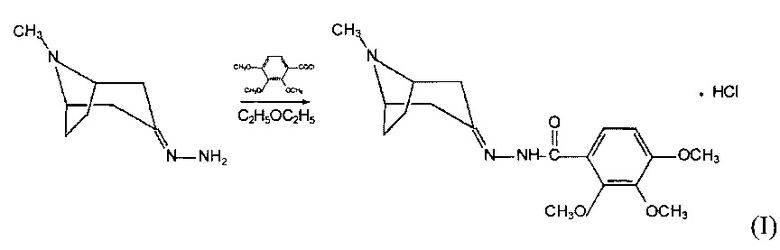
Ацилированием 2,3,4-триметоксибензоилхлоридом гидразона тропан-3-она в эфире при комнатной температуре в три стадии был получен конечный продукт 2,3,4-триметокси-N-(8-метил-8-азабицикло [3.2.1] октан-3-илиден) бензогидразид гидрохлорид (I). Соединение I представляет собой высокоплавкие белые кристаллы, растворимые в воде и нерастворимые в эфире и ароматических растворителях.
Используемые в качестве промежуточных продуктов: хлоангидрид 2,3,4-триметоксибензойной кислоты получен взаимодействием соответствующей кислоты с хлористым тионилом в сухом бензоле, а гидразон тропан-3-она реакцией последнего с гидразингидратом в спирте.
Экспериментальная химическая часть
Чистота полученного продукта определялась с помощью ЯМР спектроскопией и элементным анализом. Спектр ЯМР снят на приборе «Fourier-300» (Bruker) внутренний стандарт ТМС.
Получение 2,394-триметокси-N'-(8-метил-8-азабицикло[3.2.1.] октан-3-илиден) бензогидразида гидрохлорида
Получение 3-гидразоно-8-метил-8-азабицикло [3.2.1.]октана (II).
Растворяют 10,0 г тропинона (0,070 м) в 100 мл спирта и добавляют по каплям медленно при перемешивании к 50,0 г (1,000 м) гидразин гидрата, растворенного в 100 мл спирта при комнатной температуре. Раствор упаривают, остаток перегоняют в вакууме, получают 8,6 г (78,00% считая на тропинон), т.к. 115/3 мм и 2,0 г димера (побочный продукт, т.к. 171/1 мм).
Получение 2,3,4-триметоксибензоил хлорида (III).
Растворяют 6,0 г (0,028 м) 2,3,4-триметоксибензойной кислоты в 40 мл сухого бензола и по каплям добавляют 6,7 г (0,056 м) хлористого тионила при кипении бензола в течение 3 часов, бензол упаривают, остаток перегоняют в вакууме и получают 4,8 г (73,71%), т.к. 183/20 мм.
Получение 2,3,4-триметокси-N-(8-метил-8-азабицикло[3.2.1.]октан-3-илиден)бензогидразид гидрохлорида (I).
Растворяют 3,0 г (0,019 м) гидразонатропан -3-она в 30 мл абсолютного эфира и медленно по каплям добавляют растворенные в 10 мл эфира 4,5 г (0,019 м) хлорангидрид 2,3,4-триметоксибензойной кислоты при комнатной температуре. Полученный осадок отфильтровывают, промывают абсолютным эфиром, сушат и перекристаллизовывают из ацетона и спирта.
Получают 3,2 г (42,60%), т.пл. 210°С.
Найдено в % -С-56,39; Н-7,08; N-10,94; Cl-8,88, C18H25N3O4
Вычислено в %- С-56,32; H-6,77; N-10,95; Cl-9,35.
Спектр ЯМР - 'Н (СДСl3,  , м.д., JГц): 1.81, 2.13, 2.34 (м, 4Н; Н-6 и Н-7); 2.73, 3.52 (м, 4Н, Н-2 и Н-4); 3.92 (м, 2Н; Н-1 и Н-5); 3.85, 3.889, 3.99 (с.9Н, 3 ОСН3); 6.79, 7.94 (д. J=9, 2Н, аром. прот.); 10.84 (с, 1Н, NH группа).
, м.д., JГц): 1.81, 2.13, 2.34 (м, 4Н; Н-6 и Н-7); 2.73, 3.52 (м, 4Н, Н-2 и Н-4); 3.92 (м, 2Н; Н-1 и Н-5); 3.85, 3.889, 3.99 (с.9Н, 3 ОСН3); 6.79, 7.94 (д. J=9, 2Н, аром. прот.); 10.84 (с, 1Н, NH группа).
Фармакологическое изучение заявляемого соединения I.
Для оценки фармакологических эффектов заявляемого соединения были использованы базисные сертифицированные методики, рекомендуемые Фармакологическим комитетом МЗ РФ для исследования веществ, обладающих противомигреневым, анксиолитическим действием (Руководство по экспериментальному (доклиническому) изучению веществ с фармакологической активностью. М., Гриф и К, 2012, с. 255, с. 485).
Пример 1. Изучение антисеротониновой цереброваскулярной активности соединения I.
Известно, что для моделирования приступа мигрени используют констрикторные реакции сосудов мозга, вызванные серотонином. При внутривенном введении серотонина наблюдается кратковременное снижение мозгового кровотока и артериального давления. Эта реакция сохраняется и при повторном введении серотонина [Р.С. Мирзоян и соавт., Тропоксин - новый антагонист серотонина и потенциальное противомигреневое средство. Эксперим. и клин. фармакол., 1998, 61, 2, 28-31; Т.С. Ганьшина, Эксперим. и клин. фармакол., 2003, 66, 3, 17-20].
Известно, что в сосудах мозга, в основном, присутствуют 5НТ2В/2C-рецепторы. Поэтому для изучения констрикторных реакций сосудов мозга серотонинергической природы целесообразно наряду с серотонином использовать также избирательный агонист 5НТ2В/2C-рецепторов - мета-хлорфенилпиперазин (mCPP). Согласно литературным данным, мета-хлорфенилпиперазин провоцирует приступ головной боли у больных мигренью, в отличие от здоровых добровольцев [A. Pancoesi, Headache induced by serotoninergic agonists - a key to the interpretation of migraine pathogenesis? Cefalalgia, 1997,17, 3-14]. Показано также, что при внутривенном введении mCPP в дозе 0,1 мг/кг экспериментальным животным отмечается увеличение пропотевания альбуминов плазмы из менингеальных сосудов, что является количественным маркером нейрогенного воспаления в твердой мозговой оболочке. При этом происходит активация чувствительных волокон тригеминоваскулярной системы и высвобождение в стенку сосуда вазоактивных веществ, таких, как субстанция Р, глутамат и др. [А.В. Амелин и соавт., Мигрень - патогенез, клиника и лечение СПб медицинское издательство, 2001; А.Ю. Соколов и соавт., Роль серотониновых рецепторов в механизмах формирования мигрени, Нейрохимия, 2011, 2, 104-112].
Исследовали влияние соединения I на изменения кровотока в коре головного мозга крыс, вызванные внутривенным введением mCPP (Sigma-Aldrich) в дозе 0,1 мг/кг [А.В. Амелин и соавт., Мигрень - патогенез, клиника и лечение, СПб медицинское издательство, 2001].
Для оценки состояния микроциркуляции проводили регистрацию локального кровотока в теменной области коры головного мозга крыс с помощью лазерного допплеровского флоуметра ALF-21 фирмы "Transonic Systemlnc." (США). Для этой цели игольчатый датчик флоуметра диаметром 0,8 мм устанавливали на теменной области коры головного мозга на расстоянии 6-7 мм дистальнее основания средней мозговой артерии по направлению ее центральной ветви с помощью микроманипулятора и коромысла. Параллельно регистрировали уровень артериального давления через предварительно вставленный в бедренную артерию полиэтиленовый катетер. Запись показателей кровотока и артериального давления производили на полиграфе фирмы «BIOPAK» США, соединенным с персональным компьютером. Исследуемое соединение I в дозе 10 мг/кг и mCPP в дозе 0,1 мг/кг вводили внутривенно через полиэтиленовый катетер, вставленный предварительно в бедренную вену.
Статистическую обработку данных проводили с использованием пакета программ Stastistika 8,0 (Statistikalnc, США). Нормальность распределения определяли с помощью критерия Шапиро-Уилка. Для дальнейшей обработки данных использовали непараметрический двухвыборочный знаково-ранговый критерий Вилкоксона. Средние данные в тексте представлены в виде медианы. Результаты рассматривали как значимые при р≤0,05.
Исследование проведено на 20 наркотизированных (хлоралгидрат 350 мг/кг внутрибрюшинно) нелинейных крысах-самцах массой 250-300 г. Все животные содержались в условиях лабораторного вивария при 12-ти часовом световом режиме со свободным доступом к воде и стандартному корму. Эксперименты проводились в соответствии с этическими правилами гуманного обращения с животными, утвержденными этической комиссией ФГБНУ «НИИ фармакологии имени В.В. Закусова».
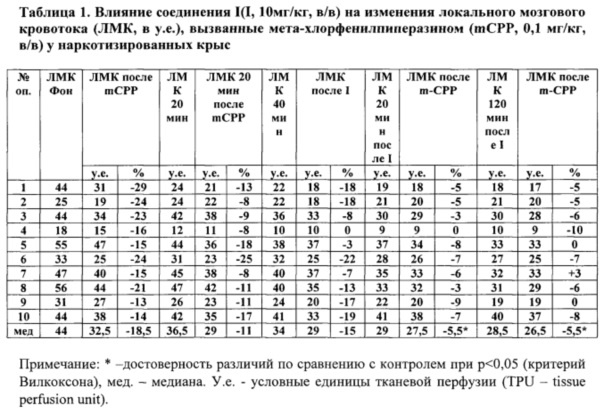
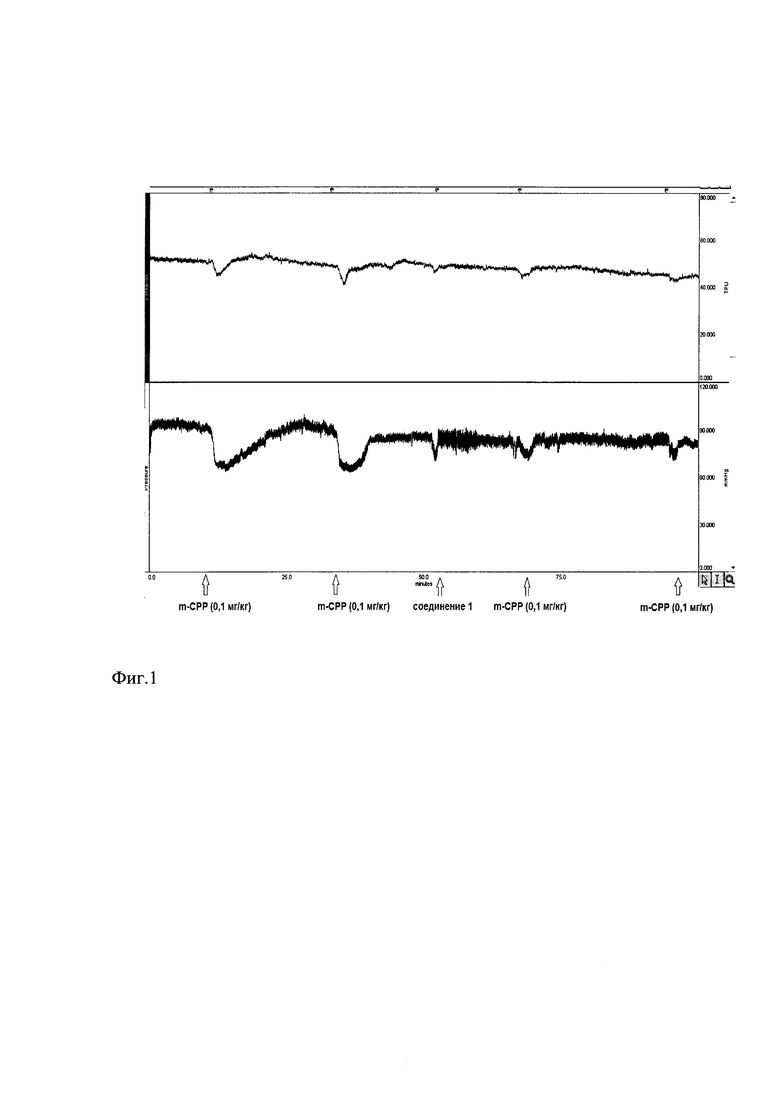
Проведенные опыты показали, что после введения mCPP наблюдается кратковременное снижение локального кровотока в коре мозга крыс в среднем на 18% и 11%) (табл. 1, фиг. 1). После регистрации контрольных реакций вводили соединение 1. Показано, что mCPP, введенный через 20 минут после инъекции соединения I вызывает снижение кровотока в коре мозга крыс в среднем на 5,5% (табл. 1, фиг. 1). Различие эффектов контрольных реакций на СРР и после соединения1является статистически значимым (р≤0,05). Ослабление констрикторной реакции сосудов мозга в ответ на введение СРР под влиянием соединения I наблюдается в течение 90-120 минут.
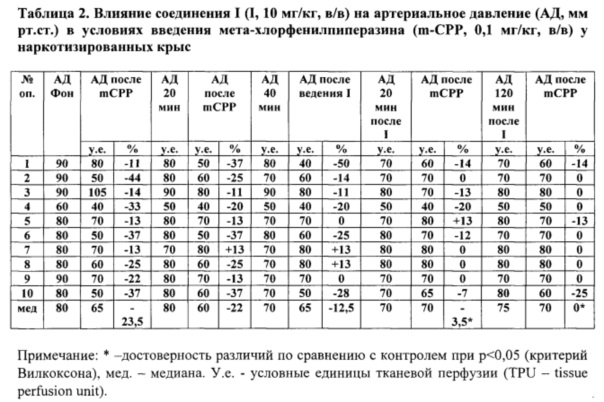
В контроле при введении mCPP у крыс наблюдается кратковременное снижение артериального давления в среднем на 22,5% (табл. 2, фиг. 1). Через 20 минут после введения соединения I mCPP вызывал снижение уровня артериального давления в среднем на 3,5%, а к концу эксперимента реакция артериального давления на введение mCPP полностью отсутствовала (табл. 3, фиг. 1).
Ранее было показано, что при предварительном введении препарата сравнения тропоксина mCPP вызывал снижение кровотока в сосудах мозга в среднем 19% и 11% через 20 минут и 40 минут соответственно. В контроле снижение кровотока под влиянием mCPP составляло 25% (р≤0,05). Однако, через 60 минут после тропоксина реакция сосудов мозга на mCPP, даже несколько усиливается [Горбунов А.А., Т.С. Ганьшина, Р.С. Мирзоян, Влияние тропоксина на цереброваскулярные эффекты метахлорфенилпиперазина и серотонина. Эксперим. и клин, фармакол., 2010, 73, 9, 13-16]. Следует отметить, что при введении соединения I эффект ослабления констрикторных реакций сосудов мозга на mCPP продолжается в течение 2-х часов. Тропоксин ослабляет реакцию артериального давления, вызванную mCPP, а соединение I почти полностью ее устраняет.
Таким образом, проведенное исследование позволило установить, что соединение I обладает антисеротониновой цереброваскулярной активностью, так как вызывает статистически значимое ослабление реакций локального мозгового кровотока и артериального давления, вызванные mCPP. По интенсивности антисеротониновых сосудистых эффектов соединение I не уступает тропоксину, а по продолжительности его превосходит.
Пример 2. Изучение анксиолитического эффекта соединения I
Эксперименты проведены на 100 белых беспородных мышах-самцах массой 20-25 г. Все животные содержались в условиях лабораторного вивария при 12-ти часовом световом режиме со свободным доступом к воде и стандартному корму. Для исключения влияния суточных биоритмов на скорость биосинтеза и метаболизма нейромедиаторов, эксперименты проводили между 10 и 12 часами дня. Эксперименты проводились в соответствии с этическими правилами гуманного обращения с животными, утвержденными этической комиссией ФГБНУ «НИИ фармакологии имени В.В. Закусова».
Для оценки анксиолитического действия применялась стандартная методика приподнятого крестообразного лабиринта (ПКЛ), основанная на возникновении у животного стресса и страха при реализации ориентировочно-исследовательского поведения и норкового рефлекса в сложных условиях (новизна обстановки, страх высоты и освещенность) [Т.А. Воронина, С.Б. Середенин, М.А. Яркова и др., Методические рекомендации по доклиническому изучению транквилизирующего (анксиолитического) действия лекарственных средств. «Руководство по проведению доклинических исследований лекарственных средств». Часть первая. - М.: Гриф и К, 2012. С. 264-275; S.Pellow, P.Chopin, S.E. File, M. Briley et al., Validation of openxlosed arm entries in an EPM as a measure of anxiety in the rat. J.Neurosci. Meth., 1985, 14, 3, 149-167].
Крестообразный лабиринт расположен на высоте 50 см от пола и состоит из двух открытых (не имеющих стенок) (ОР) и двух закрытых (имеющих стенки высотой 20 см) рукавов (ЗР), расположенных под углом 90°, а также центральной площадки (ЦП) размерами 5×5 см. Мышь помещали на центральную площадку ПКЛ головой к открытому рукаву. В течение 5 мин регистрировали время пребывания в OP, ЗР, число заходов (пересечение границы рукава четырьмя лапами) в ОР и ЗР. Заход в рукава ПКЛ засчитывали в случае, когда животное пересекало границу рукава четырьмя лапами. Известно, что чем активнее мыши выходят в ОР лабиринта, тем меньше степень их тревожности.
Соединение I было изучено в дозах 5, 10, 20 и 40 мг/кг, каждая доза вещества на 10-ти животных. Статистическую обработку полученных результатов и достоверность различий определяли с помощью критерия Стьюдента. Вычисляли средние величины количества заходов и времени пребывания в отсеках для каждой группы и стандартные отклонения.
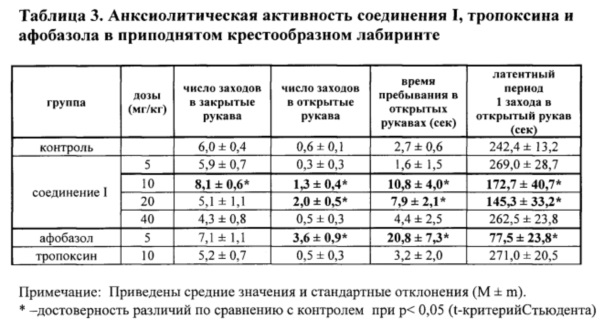
Установлено, что соединение I в дозе 10 и 20 мг/кг (внутрибрюшинно) проявляет отчетливую анксиолитическую активность, что выражается в значительном, статистически достоверном возрастании длительности пребывания животных в открытых рукавах ПКЛ, числа заходов в них и сокращении латентного периода первого захода в открытый рукав (табл. 3). В дозах 5 и 40 мг/кг соединение I не проявляет анксиолитической активности (табл. 3). Тропоксин в дозе 10 мг/кг не оказывает анксиолитического действия в тесте ПКЛ. Афобазол в дозе 5 мг/кг статистически достоверно увеличивает длительность пребывания животных в открытых рукавах ПКЛ, число заходов в них и уменьшает латентный период первого захода в открытый рукав, что свидетельствует о его анксиолитическом эффекте. Достоверных различий между эффектами соединения I и афобазола не наблюдается.
Таким образом, соединение I, также как афобазол, обладает выраженной анксиолитической активностью, тогда как тропоксин анксиолитической активностью не обладает.
Пример 3. Изучение токсичности и возможных побочных эффектов соединения I.
Острая токсичность и возможные побочные эффекты соединения I при внутрибрюшинном однократном введении в дозе 200 мг/кг оценивалась в опытах на беспородных мышах-самцах массой 20-25 г [Е.В. Арзамасцев, И.В. Березовская, Т.А. Гуськова и др. Руководство по проведению доклинических исследований лекарственных средств. Часть первая, Москва, 2012, 13-25]. Оценка общего состояния, поведения и гибели животных проводилась через 1 ч, 24 ч, 4 сут., 10 сут. и 14 сут. после введения соединения. Степень нарушения координации движений оценивали по способности животных удерживаться на вращающемся стержне RotaRod (UgoBasile, Италия). Животных помещали на горизонтальный стержень диаметром 2,5 см, вращающийся с постоянной скоростью 10 оборотов в минуту. В течение 300 с регистрировали время удерживания животных на вращающемся стержне.
Установлено, что через 1 ч, 24 ч, 4 сут., 10 сут. и 14 сут. после введения соединения 1 в дозе 200 мг/кг гибели животных не наблюдается. При изучении возможных побочных эффектов соединения I в дозе 200 мг/кг (т.е. в 10 раз превышающей терапевтическую - 20 мг/кг) было показано, что данное вещество не вызывает развития побочных эффектов и признаков неврологического дефицита как через 1 ч, так и в более отдаленные сроки (24 ч, 4 сут., 10 сут. и 14 сут.) после введения соединений. Соединение I в дозе 200 мг/кг не нарушает координации движений животных (100% мышей удерживаются на вращающемся стержне в течение 5 минут).
Таким образом, проведенное исследование позволило установить, что соединение I в дозе 10 мг/кг обладает антисеротониновой активностью, вызывает статистически значимые ослабления реакций локального мозгового кровотока и артериального давления, вызванных mCPP в той же степени, что и тропоксин, но превосходит его по длительности эффекта. В отличие от тропоксина, соединение I обладает анксиолитической активностью в дозах 10 и 20 мг/кг, и не вызывает при этом развития побочных эффектов и гибели животных в дозе, в 10 раз превышающей эффективную.
Описание чертежа.
Фигура 1. Влияние соединения I на изменения кровотока в коре мозга крыс в условных единицах и артериальное давление в мм рт. ст., вызванные mCPP. Обозначения сверху вниз: верхняя кривая - локальный мозговой кровоток, нижняя - артериальное давление; по оси ординат, в верхней части рисунка - условные единицы тканевой перфузии (TPU - tissue perfusion unit); на нижней - мм.рт.ст., по оси абсцисс - время в минутах, стрелками указано введение веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| Соединение 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден)бензогидразид гидрохлорид, обладающее антисеротониновой цереброваскулярной и противомигреневой активностью | 2022 |
|
RU2803750C1 |
| КОМБИНАЦИЯ ПРОИЗВОДНОГО ПИПЕРИДИНА С ПИКАМИЛОНОМ, ОБЛАДАЮЩАЯ АНТИСЕРОТОНИНОВОЙ И ПРОТИВОИШЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2822877C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ПРОТИВОМИГРЕНЕВЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ) | 2008 |
|
RU2424803C2 |
| Использование 3,4,5-триметокси-N'(2,2,6,6-тетраметил-пиперидин-4-илиден)бензогидразида гидрохлорида в качестве анксиолитического средства | 2016 |
|
RU2691454C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВОМИГРЕНОЗНОГО ДЕЙСТВИЯ В ТВЕРДОЙ ЛЕКАРСТВЕННОЙ ФОРМЕ В ВИДЕ ТАБЛЕТОК | 2019 |
|
RU2696866C1 |
| АНТИАГРЕГАЦИОННОЕ СРЕДСТВО | 2005 |
|
RU2353363C2 |
| ПРОИЗВОДНОЕ 8-АЗАБИЦИКЛО [3.2.1]ОКТ-2-ЕНА, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2186780C2 |
| СРЕДСТВА, ПРОЯВЛЯЮЩИЕ СВОЙСТВА АНТАГОНИСТОВ СЕРОТОНИНОВЫХ 5-HT-РЕЦЕПТОРОВ | 2011 |
|
RU2465901C2 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ СВОЙСТВА АНТАГОНИСТА СЕРОТОНИНОВЫХ 5-HT-РЕЦЕПТОРОВ | 2010 |
|
RU2438669C1 |
| 8-МЕТИЛ-8-ФЕНИЛ-3-ОКСОТИАЗОЛИДИНО-[3,2-A]ПИРЕРАЗИН ИЛИ ЕГО ГИДРОХЛОРИД, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1991 |
|
SU1829361A1 |
Изобретение относится к ацилгидразон (2,3,4-триметокси-N'-(8-метил-8-азабицикло[3.2.1.]октан-3-илиден) бензогидразид гидрохлорид) структурной формулы (I), который может быть использован в медицине:
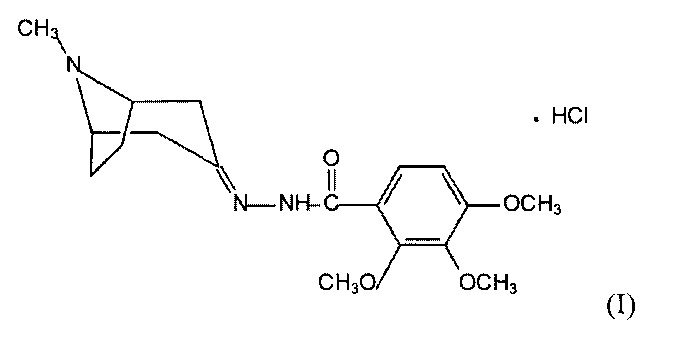 .
.
Предложено новое соединение с противомигреневой и анксиолитической активностью. 3 пр., 3 табл., 1 ил.
Соединение ацилгидразон (2,3,4-триметокси-N'-(8-метил-8-азабицикло[3.2.1.]октан-3-илиден)бензогидразид гидрохлорид):
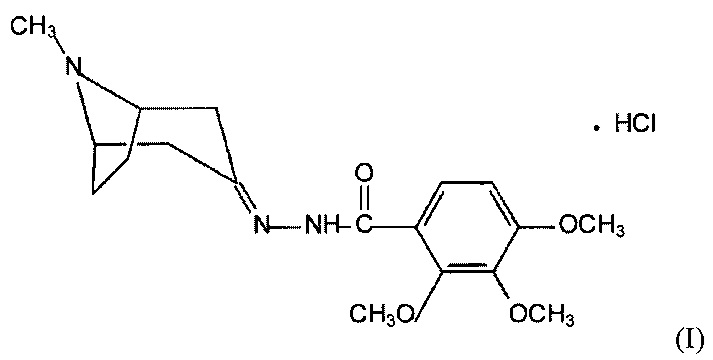 ,
,
обладающее противомигреневой и анксиолитической активностью.
| Переходная токопроводящая конструкция для сетевого переходника | 2024 |
|
RU2838914C1 |
| RU 2008115539 A, 10.12.2009 | |||
| Т.С | |||
| Ганьшина и др | |||
| Экспериментальная и клиническая фармакология, 2008, т | |||
| Контрольный стрелочный замок | 1920 |
|
SU71A1 |
Авторы
Даты
2019-09-09—Публикация
2016-08-19—Подача