Изобретение относится к химии биологически активных соединений и касается 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден)бензогидразида гидрохлорида (II). Общая формула:
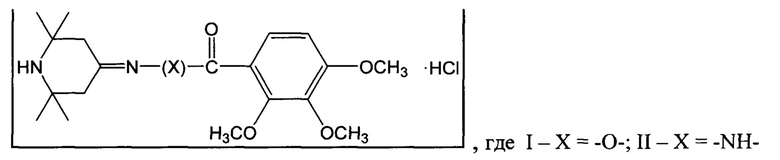
При изучении фармакологической активности соединений I и II было установлено, что они обладают выраженными антисеротониновыми противомигреневыми свойствами.
Мигрень, которая поражает около 15% населения земного шара и чаще всего женщин, является вторым по инвалидности заболеванием, существенно ухудшающим качество жизни и продуктивность работоспособного населения с тяжелыми социально-экономическими последствиями [GBD 2016 Headache Collaborators. Global, regional, and national burden of migraine and tension-type headache, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2018 Nov; 17(11):954-976; Agosti R. Migraine burden of disease: from the patient's experience to a socio-economic view. Headache. 2018; 58 (Sup 11): 17-32].
Лекарственные препараты для лечения мигрени принято делить на две группы: для неотложного лечения (купирования) приступа мигрени и для профилактики или предупреждения этого приступа. Для купирования приступа мигрени используются ненаркотические анальгетики и агонисты 5-HT1B/1D-рецепторов (суматриптан, золмитриптан, наратриптан и др.), получившие название триптаны [Antonaci F., Ghiotto N., Wu S., et al. Recent advances in migraine therapy. Springerplus. 2016; 5:637, 2-14; Осипова B.B., Филатова Е.Г., Артеменко A.P. и др. Диагностика и лечение мигрени: рекомендации российских экспертов. Журнал неврологии и психиатрии им. С.С. Корсакова. Спец выпуск. 2017; 117(1): 28-42]. Однако, в настоящее время, учитывая существенные побочные эффекты триптанов констрикторные реакции коронарных и мозговых сосудов был предложен агонист 5-HT1F- рецепторов (лазмидитан), который, в отличие от триптанов обладает только нейротропной (анальгетической) активностью и не влияет существенно на сосудистую систему организма. [Martinelli D, Bitetto V, Tassorelli С.Lasmiditan: an additional therapeutic option for the acute treatment of migraine. Expert Rev Neurother. 2021 May; 21(5):491-502; Novel synthetic drugs in migraine. Editors: Martelletti P., Edvinsson L., Springer, 2022, 109 p.].
Известно, что для профилактического лечения мигрени широкое распространение получил β-адреноблокатор пропранолол [Jackson J.L., Kuriyama A, Kuwatsuka Y, Nickoloff S, Storch D, Jackson W, Zhang ZJ, Hayashino Y. Beta-blockers for the prevention of headache in adults, a systematic review and meta-analysis. PLoSOne. 2019;14(3):e0212785], который, вместе с тем, проявляет высокое сродство к 5-HT1A,B рецепторам серотонина [Adham N, Tamm JA, Salon JA, et al. A single point mutation increases the affinity of serotonin 5-HT1D alpha, 5-HT1D beta, 5-HT1E and 5-HT1F receptors for beta-adrenergic antagonists. Neuropharmacology. 1994; 33(3- 4):387-91], блокирует, как и пизотифен, 5НТ2С-рецепторы в эндотелии яремной вены крыс в опытах in vitro [Fozard JR, Kalkman HO. 5-Hydroxytryptamine (5-HT) and the initiation of migraine: new perspectives. Naunyn Schmiedebergs Arch Pharmacol. 1994 Sep;350(3):225-9], а в опытах in vitro и in vivo угнетает спазмы сосудов мозга, вызванные серотонином [Романычева Н.А., Ганыпина Т.С., Мирзоян Р.С. Индивидуальная чувствительность к цереброваскулярному антисеротониновому действию пропранолола и толфенамовой кислоты. Экспер. и клин, фармакол.1995; 58(2):5-26]. Пропранолол обладает также обезболивающей активностью, усиливая антиноцицептивный эффект подпороговых доз морфина [Afify ЕА., Andijani NM. Potentiation of morphine-induced antinociception by propranolol: the involvement of dopamine and GAB A systems. Front Pharmacol. 2017; 8:794]. Он оказывает депримирующее влияние на процессы регуляции симпатического и вазомоторного тонуса, угнетая разряды с афферентных А5 и в большей степени с С-волокон соматических нервов, по которым, как известно, проводятся болевые импульсы [Бендиков Э.А., Бутузов В.Г., Мирзоян Р.С. О механизме действия пропранолола на центральные процессы регуляции кровообращения. Фармакол. и токсикол. 1969; 32(6): 678-683]. Показано также, что пропранолол дозозависимо угнетает соматосенсорные ответы тригемино-цервикального комплекса с Аδ и С-волокон твердой мозговой оболочки [Akerman S, Romero-Reyes М. Targeting the central projection of the dural trigeminovascular system for migraine prophylaxis. J Cereb Blood Flow Metab. 2019; 39(4): 704-717]. Следовательно, пропранолол, наряду с блокадой β-адренорецепторов, обладает антисеротониновой и обезболивающей активностью, что нельзя не учитывать при обсуждении его эффективности при лечении пациентов с мигренью.
Для профилактического лечения мигрени используются также известные антагонисты 5НТ2В/2С-рецепторов (пизотифен, ципрогептадин, ницерголин), которые препятствуют сосудосуживающему эффекту серотонина [Rau JC, Dodick DW. Other preventive anti-migraine treatments: ACE inhibitors, ARBs, calcium channel blockers, serotonin antagonists, and NMDA receptor antagonists. Curr Treat Options Neurol. 2019; 21(4): 17].
Для этой же цели используются также сосудорасширяющие препараты различного механизма действия - противоэпилептические средства (топирамат, натрия вальпроат), воздействующие на ГАМКА-рецепторы мозговых сосудов, ингибиторы ангиотензин-превращающего фермента (эналаприл, каптоприл), антагонист рецепторов ангиотензина II (кандесартан), блокаторы медленных кальциевых каналов (нифедипин, нимодипин, верапамил, флунаризин), мелатонин [Liampas I., SiokasV., BrotisA., Vikelis M., DardiotisE. Endogenous melatonin levels and therapeutic use of exogenous melatonin in migraine: systematic review and meta-analysis. Headache. 2020; head. 13828; Rau JC, DodickDW. Other preventive anti-migraine treatments: ACE inhibitors, ARBs, calcium channel blockers, serotonin antagonists, and NMDA receptor antagonists. Curr Treat Options Neurol. 2019; 21(4):17].
В последние годы внимание исследователей привлекает кальцитонин ген-связанный пептид (CGRP), который широко представлен в различных структурах мозга и обладает существенной сосудорасширяющей активностью. Сообщают об эффективности антагонистов CGRP, получивших название гепанты (атогепант, римегепант, уброгепант), при профилактическом лечении приступа мигрени и даже при его купировании [Novel synthetic drugs in migraine. Martelletti P., Edvinsson L. Editors, Springer, 2022, ISSN 2197-652Х]. Антагонисты CGRP обладают обезболивающей активностью и это указывает на условность деления препаратов на две группы - купирующие приступ и препятствующие его развитию. Вместе с тем, антагонисты CGRP (олцегепант и римегепант) усугубляют состояние ишемического поражения мозга у мышей, вызванное окклюзией средней мозговой артерии, что выражается в усилении неврологического дефицита, увеличении размера инфаркта мозга и смертности животных [Mulder IA, Li М, de Vries Т, et al. Anti-migraine calcitonin gene- related peptide receptor antagonists worsen cerebral ischemic outcome in mice. Ann Neurol. 2020 Oct;88(4):771-784]. Авторы вышеприведенного сообщения отмечают необходимость изучения цереброваскулярной безопасности этих противомигреневых препаратов.
Здесь уместно также подчеркнуть, что у пациентов с мигренью с аурой и без нее возникают очаги ишемии в ткани мозга, т.е. мигрень является фактором риска для инсульта [Zhang S., Zhang W., Zhou G. Extended risk factors for stroke prevention. J. of the National Medical Association, 2019, 111 (4), 447-456; ∅ie LR, Kurth T, Gulati S, Dodick DW. Migraine and risk of stroke. J Neurol Neurosurg Psychiatry. 2020 Jun;91(6):593-604; Saddik SE, Dawood SN, Rabih AM, et al. Risk of stroke in migrainous women, a hidden association: a systematic review. Cureus. 2022 Jul 21;14(7):e27103].
Поэтому, учитывая наличие ишемического компонента в формировании приступа мигрени, необходимо проводить также поиск препаратов, которые у пациентов с мигренью будут препятствовать развитию констрикторных реакции сосудов мозга.
Таким образом, несмотря на определенные успехи в разработке лекарственных препаратов для лечения мигрени, проблема фармакологической коррекции мигрени продолжает оставаться во многом нерешенной, так как препараты, применяемые для ее лечения, не всегда отличаются достаточной эффективностью и обладают выраженными нежелательными побочными свойствами. Этим определяется необходимость дальнейшего поиска новых лекарственных средств для профилактики и лечения приступа мигрени.
Ранее в ФГБНУ «НИИ фармакологии имени В.В. Закусова» разрабатывались оригинальные антагонисты серотониновых рецепторов с противомигреневой активностью - тропоксин и ЛК-933, которые, являясь производными тропана, блокируют 5НТ2В/2С-рецепторы и предупреждают развитие констрикторных реакций мозговых сосудов, вызванных серотонином [Патент РФ №1832683. Бюл. №17, 1996; Патент РФ №2699658, Бюл. №25; 09.09.2019; Мирзоян Р.С., Середенин С.Б., Ганынина Т.С. и др. Тропоксин - новый антагонист серотонина и потенциальное противоми-греневое средство. Экспер. и клин, фармак. 1998; 61(3): 28-31; Ганыпина Т.С., Горбунов А.А., Гнездилова А.В. и др. Тропоксин - новое средство для лечения мигрени. Хим.-фарм. журнал, 2016; 50(1): 19-23; Мирзоян Р.С., Ганыпина Т.С. Фармакология цереброваскулярных заболеваний и мигрени (сходство и различия). 2022. Издательский дом «Третьяковы), 370 стр. ISBN 978-5-6046890-0-4]. Основанием для этих разработок послужила методология поиска новых противомигреневых препаратов, которая учитывает существенную роль серотониновых спазмов сосудов мозга в патогенезе мигрени и заключается в изучении влияния фармакологических веществ на констрикторные реакции сосудов мозга, вызванные серотонином или агонистами серотониновых рецепторов [Mirzoyan RS, Ganshina TS, Pukhalskaya TG, et al. Effects of nicergoline in experimental models related to pathogenesis of migraine. Methods Find Exp. Clin. Pharmacol. 1989; 11(11): 671-676; Mirzoyan RS, Gan'shina TS, Kurdyumov IN, et al. Migraine pharmacology and brain ischemia. Research Results in Pharmacology. 2021;7(2):67-82].
Прототипами нового соединения являются производные тропана тропоксин и ЛК-933, а тропан, как известно, представляет собой конденсированную систему, состоящую из пирролидинового и пиперидинового циклов. Исходя из того, что синтез производных тропана для масштабного производства экономически не выгоден, были изучены антисеротониновые и противомигреневые свойства производных фрагмента тропана, а именно пиперидина. Оказалось, что пиперидиновые производные обладают выраженной антисеротониновой цереброваскулярной активностью, не уступающей тропоксину и ЛК-933, но при этом более выгодные в производстве препаратов. Действительно, исходный продукт синтеза изученных соединений - 2,2,6,6- Tetramethyl-4-piperidone более доступен и в 5,36 раз дешевле стоимости Tropinone - сырья для синтеза тропоксина или соединения ЛК-933 (Sigma-Aldrich 2022).
Из литературы известно несколько производных ацилгидразонов 2,2,6,6,-тетраметилпиперидона, обладающих стимулирующим, депрессивным, гипотензивным, спазмолитическим и анальгетическим действием [Zhelyazkov L., Bikova N., Krusteva L., Nikolova M., Taskov M., Synthesis and pharmacology study of new N-acyl-N1-(2,2,6,6-tetramethyl-4-piperidilidene) hydrazine. Trudovena Nauchnoizlledovatelskiya Khimicofarmatsevtichen Institut, v.9, p.19-26, 1974 (Bulg.)]. Однако среди производных ацилгидразонов 2,2,6,6,-тетраметилпиперидона препаратов, обладающих антисеротониновым действием, обнаружено не было.
Задачей настоящего изобретения является разработка средства, являющегося антагонистом серотонина с противомигреневым действием.
Предложено новое химическое соединение, обладающее выраженной антисеротониновой цереброваскулярной активностью: 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден) бензогидразида гидрохлорид.
Технический результат. Заявленное соединение обладает выраженными антисеротониновыми противомигреневыми свойствами, относится к малоопасным веществам (4 класс токсичности), не вызывает нежелательных побочных эффектов, по экономической целесообразности синтеза значительно превосходит производные тропана и может найти применение в медицинской практике в качестве препарата для лечения мигрени. Изобретение расширяет арсенал средств для лечения мигрени.
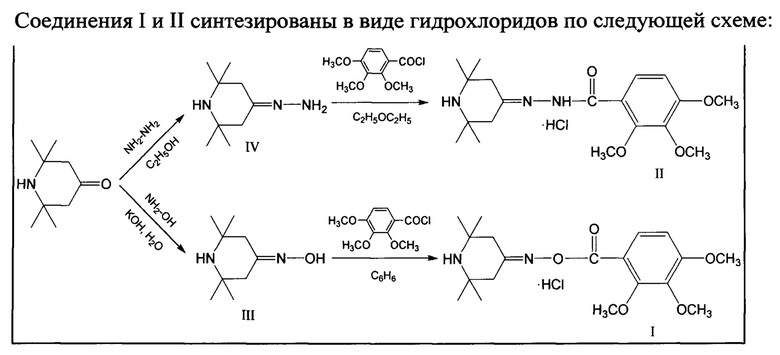
Синтез конечных продуктов проводился исходя из 2,2,6,6-тетраметилпиперидин-4-она в первом случае взаимодействием последнего с гидроксиламином в водной щелочной среде был получен оксим 2,2,6,6-тетраметилпиперидин-4-она III.
Во втором случае взаимодействием пиперидина с гидразингидратом в этаноле был получен соответствующий гидразон IV.
Хлорангидрид 2,3,4- триметоксибензойной кислоты был получен реакцией соответствующей кислоты с хлористым тионилом в кипящем сухом бензоле [Патент РФ №2699658, Бюл. №25; 09.09.2019].
Реакцией оксима 2,2,6,6-тетраметилпиперидин-4-она III с хлорангидридом 2,3,4- триметоксибензойной кислоты был получен 2,2,6,6-тетраметилпиперидин-4он O-(2,3,4-тримеоксибензоил)оксим гидрохлорид (I), а реакцией гидразона 2,2,6,6-тетраметилпиперидона IV в сухом эфире при комнатной температуре с хлорангидридом 2,3,4-триметоксибензойной кислоты был получен 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден) бензогидразид гидрохлорид (II).
Контроль за ходом реакции и чистотой полученных продуктов проводился с помощью ГЖХ на приборе «ЦВЕТ-100» (колонка L-0,7 м, ∅ 3 мм, SE-30/5%. ChromatonN-AW, скорость N2 - 60 мл/мин). Спектры ПМР Н сняты на приборе "Fourier-300". Внутренний стандарт ТМС. Температуру плавления определяли на приборе "Boetius".
Ниже приведены примеры получения новых соединений и демонстрации их фармакологических эффектов.
Пример 1. Получение 2,2,6,6-тетраметилпиперидин-4он 0-(2,3,4-тримеоксибензоил) оксима гидрохлорида (I)
Растворяют 2,0 г (0,011 М) оксима 2,2,6,6,-тетраметилпиперидин-4-она в абс.бензоле и по каплям добавляют 2,7 г (0,011 М) хлорангидрида 2,3,4-триметоксибензойной кислоты, растворенной в 15 мл абс.бензола при кипении последнего. После однодневного стояния осадок отфильтровывают и перекристаллизовывают из изопропенола. Получают 2,3 г Соединения I. Выход 49,04%, т.пл. 202-203°С.
Найдено в %: С-56,74; Н-7,29; N-6,80; Cl- 8,62
Вычислено в %: С-56,92; Н- 7,24; N-6,99; Cl-8,86
Спектр ПМР'Н (DMSO, м.д.) 1,1-1,8 (12Н, 2С, 4СН3); 2,8-3,0 (4Н, С, 2СН2, пипер. кольцо); 3,89-3,93 (9Н, 3С, 3ОСН3); 6,74 (1Н, 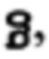 аром. кольцо); 7,60 (1Н,
аром. кольцо); 7,60 (1Н, 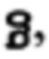 аром. кольцо); 9,61 (1Н, С, -NH- пипер. кольцо).
аром. кольцо); 9,61 (1Н, С, -NH- пипер. кольцо).
Пример 2. Получение 2,3,4-триметокси-N' -(2,2,6,6,-тетраметилпиперидин-4-илиден) бензогидразида гидрохлорида (II)
Растворяют 2,0 г (0,012 М) гидразона 2,2,6,6,-тетраметилпиперидона в 50 мл абс.эфира и по каплям при перемешивании добавляют 2,72 г (0,012 М) хлорангидрида 2,3,4-триметоксибензойной кислоты, растворенной в 20 мл абс. эфира при комнатной температуре. Осадок отфильтровывают и перекристаллизовывают из смеси ацетон-спирт. Получают 2,5 г Соединения II. Выход 52,9%, т.пл. 215°С.
Найдено в %: С-62,94%; Н-8,70; N-11,21; Cl- 9,31
Вычислено в %: С-62,63; Н- 8,24; N-11,53; Cl-9,75
Спектр ПМР'Н (DMSO, м.д.) 11,43 (12Н, 2С, 4СН3); 2,50 (4Н, С, 2СН2, пипер. кольцо); 3,78-3,87 (9Н, С, 3ОСН3); 6,91-6,94 (1Н, С, аромат, кольцо); 7,39-7,40 (1Н, С, аромат, кольцо); 9,35 (1Н, м, NHCO); 10,73 (1Н, С, пипер. кольцо).
Фармакологическое изучение Соединений I и II.
Для оценки фармакологических эффектов новых соединений были использованы базисные сертифицированные методики, рекомендуемые Фармакологическим комитетом МЗ РФ для исследования веществ, обладающих противомигреневым действием [Мирзоян Р.С., Плотников М.Б., Ганыпина Т.С. и др. Методические рекомендации по доклиническому изучению лекарственных средств для лечения нарушений мозгового кровообращения и мигрени. Руководство по проведению доклинических исследований лекарственных средств. Ч. 1. Гриф и К, Москва. 2012; 480-487].
Исследование проведено на 28 наркотизированных (хлоралгидрат 350 мг/кг внутрибрюшинно) нелинейных крысах-самцах массой 250-300 г. Все животные содержались в условиях лабораторного вивария при 12-ти часовом световом режиме со свободным доступом к воде и стандартному корму. Эксперименты проводились в соответствии с этическими правилами гуманного обращения с животными, утвержденными этической комиссией ФГБНУ «НИИ фармакологии имени В.В. Закусова».
С целью моделирования приступа мигрени изучали влияние Соединений I и II на констрикторные реакции сосудов мозга, вызванные серотонином. При внутривенном введении серотонина наблюдается кратковременное снижение мозгового кровотока и артериального давления. Эта реакция сохраняется и при повторном введении серотонина (каждые 20 минут) и может быть использована на протяжении всего эксперимента до 2-х часов наблюдения [Мирзоян Р.С., Середенин С.Б., Ганыпина Т.С., Косточка Л.М. и др. Тропоксин - новый антагонист серотонина и потенциальное противомигреневое средство. Эксперим. и клин. фарм. 1998; 61(3): 28-31; Ганыпина Т.С. Нейромедиаторный механизм действия тропоксина в сравнении с противомигреневыми препаратами. Эксперим. и клин, фармакол., 2003, 66, 3,17-20].
Для оценки состояния микроциркуляции проводили регистрацию локального кровотока в теменной области коры головного мозга крыс с помощью лазерного допплеровского флоуметра ALF-21 фирмы "Transonic System Inc." (США). Для этой цели игольчатый датчик флоуметра диаметром 0,8 мм устанавливали на теменной области коры головного мозга на расстоянии 6-7 мм дистальнее основания средней мозговой артерии по направлению ее центральной ветви с помощью микроманипулятора и коромысла. Параллельно регистрировали уровень артериального давления через предварительно вставленный в бедренную артерию полиэтиленовый катетер. Запись показателей кровотока и артериального давления производили на полиграфе фирмы «BIOPAK» США, соединенным с персональным компьютером. Исследуемые соединения в дозах 10 мг/кг и серотонин в дозе 50 мкг/кг (Sigma, USA) вводили внутривенно через полиэтиленовый катетер, вставленный предварительно в бедренную вену.
Статистическую обработку данных проводили с использованием пакета программ Stastistica 8,0 (Statistica Inc., США). Нормальность распределения определяли с помощью критерия Шапиро-Уилка. Для дальнейшей обработки данных использовали непараметрический двухвыборочный знаково-ранговый критерий Вилкоксона. Средние данные в тексте представлены в виде медианы. Результаты рассматривали как значимые при р ≤ 0,05.
Пример 3. Изучение антисеротониновой цереброваскулярной активности соединения 2,2,6,6,-тетраметилпиперидин-4-он О (2,3,4-триметоксибензоил) оксима гидрохлорида (I)
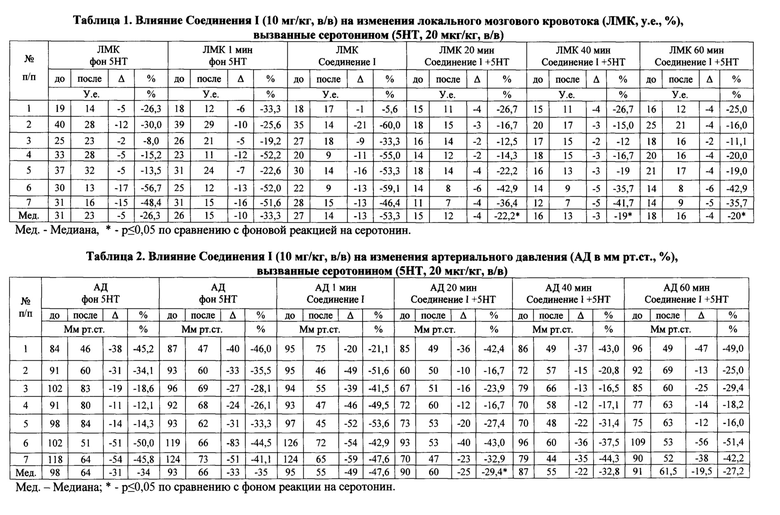
Соединение I в дозе 10 мг/кг при внутривенном введении у наркотизированных крыс ослабляет реакцию сосудов мозга, вызванную серотонином. Так в контроле снижение локального мозгового кровотока (ЛМК) под влиянием серотонина составляет в среднем 33,3%, а на фоне действия Соединения I это снижение составляет в среднем 22,2% (20 мин), 19% (40 мин) и 20% (60 мин). Разница значима при Р ≤ 0,05 (табл.1). Уровень артериального давления на серотонин в этих опытах снижается в среднем на 35%, а на фоне Соединения I давление понижается в меньшей степени только на 20 минуте и составляет 29,4% (Р ≤ 0,05, табл.2).
Анализ влияния Соединения I на мозговой кровоток в коре мозга крыс, который оценивали до введения серотонина и между его введениями, показал снижение локального мозгового кровотока. Уменьшение составляет 53% (1 мин), 40% (20 мин), 37% (40 мин) и 30% (60 мин) от исходного уровня (Р ≤ 0,05; табл.3). При анализе уровня артериального давления в этих условиях было показано, что Соединение I также снижает уровень артериального давления в среднем на 47% (1 мин), 26% (20 мин), на 24% (40 мин) и 12% (60 мин) (Р ≤ 0,05, табл.4).
Пример 4. Изучение антисеротониновой цереброваскулярной активности соединения 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден) бензогидразида гидрохлорида (II)
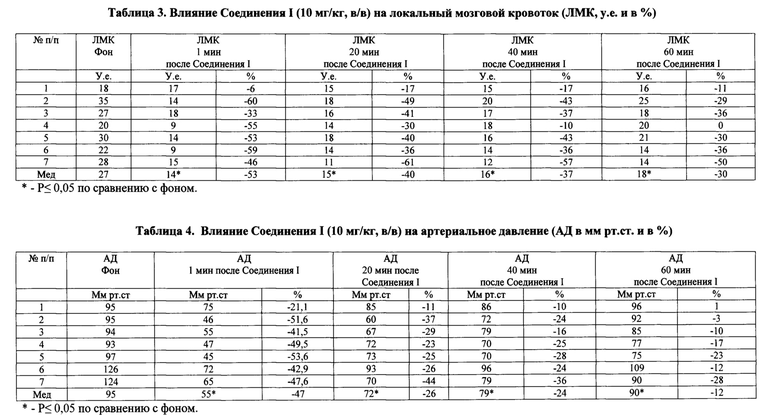
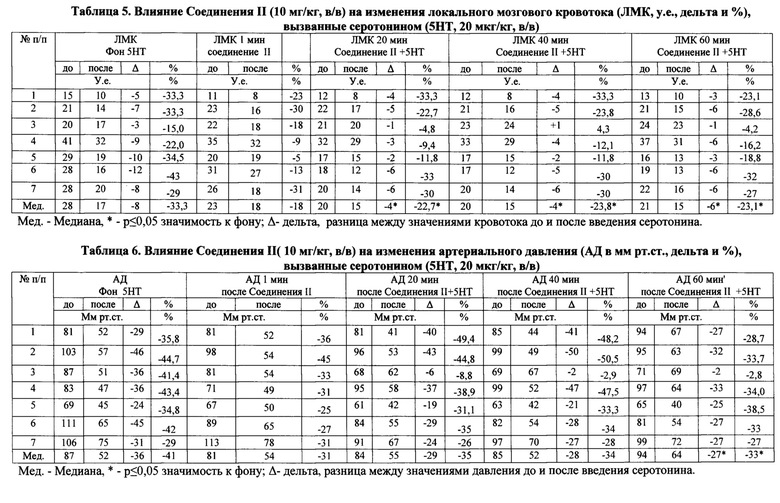
При изучении антисеротониновой цереброваскулярной активности Соединения II было показано, что оно также вызывает ослабление реакции сосудов мозга, вызванные серотонином. ЛМК в этих опытах под влиянием серотонина снижается в среднем на 33,3%, а на фоне действия Соединения II это снижение составляет - 22,7% (20 мин), 23,8% (40 мин) и 23,1% (60 мин). Разница между реакциями сосудов на серотонин в контроле и на фоне Соединения II значима при Р ≤ 0,05 (табл 5). Уровень артериального давления на серотонин в контроле снижается в среднем на 41% от исходного уровня. На фоне действия Соединения II уровень артериального давления снижается в меньшей степени, составляя на 40-60 минутах 33-34% (Р ≤ 0,05 по сравнению с контролем, табл.6).
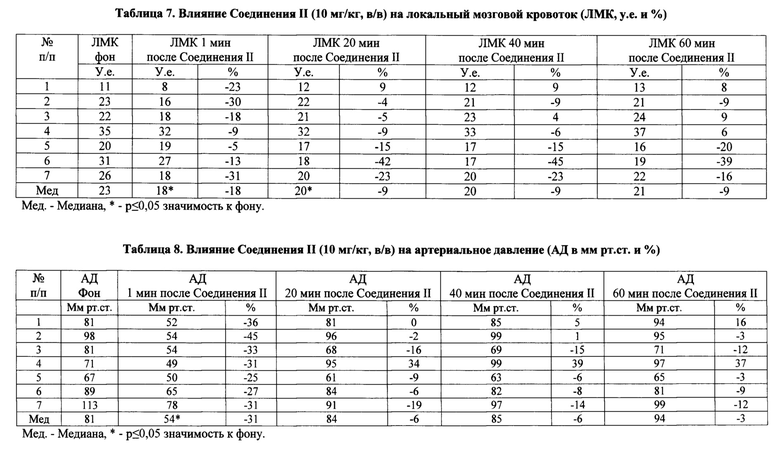
Далее было изучено влияние Соединения II на мозговой кровоток до и между введениями серотонина. Оказалось, что Соединение II в меньшей степени, чем Соединение I вызывает снижение ЛМК в коре мозга крыс, которое составляет в среднем 9% (табл.7, разница между эффектами Соединений I и II значима при Р ≤ 0,05). Уровень артериального давления под влиянием соединения II снижается только на первой минуте, а затем практически восстанавливается и до конца эксперимента не меняется (табл.8).
Проведенное исследование позволило выявить преимущество Соединения II перед Соединением I. Последнее в большей степени понижает уровень мозгового кровообращения и артериального давления, т.е. обладает нежелательными побочными эффектами. Поэтому дальнейшее более подробное изучение проводили с Соединением II. В частности, проводилось изучение острой токсичности и возможных побочных эффектов Соединения II, а также его влияния на исследовательское поведение экспериментальных животных.
Пример 5. Изучение острой токсичности и возможных побочных эффектов Соединения II
Острая токсичность и возможные побочные эффекты Соединения II при его однократном внутрибрюшинном (в/б) введении оценивали в опытах на 36 белых аутбредных мышах-самцах массой 20-25 г [Арзамасцев Е.В., Березовская И.В., Гуськова Т.А. и др. Руководство по проведению доклинических исследований лекарственных средств. Ч. 1, Москва, 2012, 13-25]. Оценку общего состояния, поведения и гибели животных проводили через 1 и 24 ч, 4, 10 и 14 суток после введения соединения. Острая токсичность изучалась в диапазоне доз от 200 до 450 мг/кг при в/б введении.
Соединения II в дозе 250 мг/кг не вызывало гибели животных на протяжении всего наблюдения (1 и 24 ч, 4, 10 и 14 суток после его введения). LD50=352 (313-396) мг/кг; LD16=286 (282-290) мг/кг; LD84=433 (427- 439) мг/кг при в/б введении (Фармастат по Митчфилду и Уилкоксону; pharm/pcsversion4 LitchfildandWilcoxonll). По острой токсичности (LD50=352 мг/кг, в/б) Соединение II относится к четвертому классу токсичности (LD50101-1000 мг/кг, в/б, Сидоров К.К. Токсикология новых промышленных химических веществ. Вып.13, Л.: Медицина, 1973. с. 47-51) (табл.9).

Соединение II в дозе 250 мг/кг (т.е. в 25 раз превышающей терапевтическую - 10 мг/кг) не вызывало развития побочных эффектов и признаков неврологического дефицита как через 1 ч, так и в более отдаленные сроки (24 ч, 4, 10 и 14 суток) после его введения, и не нарушало координацию движений животных (100% мышей удерживались на вращающемся стержне в течение 5 минут).
Пример 6. Изучение влияния Соединения II на исследовательскую и двигательную активность и анксиолитические свойства на мышах линии BALB/c
Влияние Соединения II (10 и 20 мг/кг, в/б) на поведение 60 мышей линии BALB/c изучали в условиях приподнятого крестообразного лабиринта и закрытого крестообразного лабиринта. Показано, что, несмотря на увеличение числа переходов в закрытом рукаве и суммарного количества заходов, соединение не влияет на исследовательскую и двигательную активности мышей линии BALB/c и не проявляет анксиолитический эффект в использованных поведенческих тестах (Табл. 10, 11).
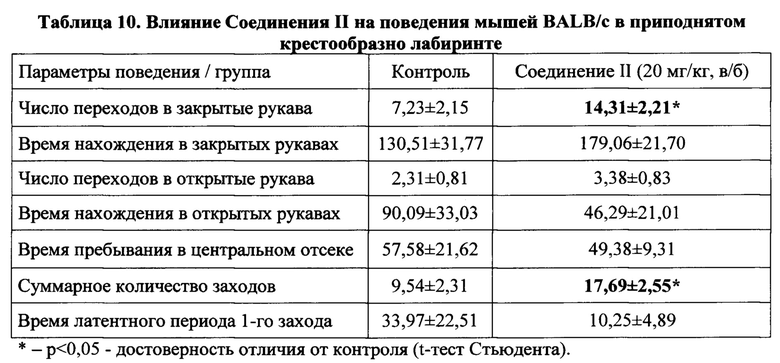
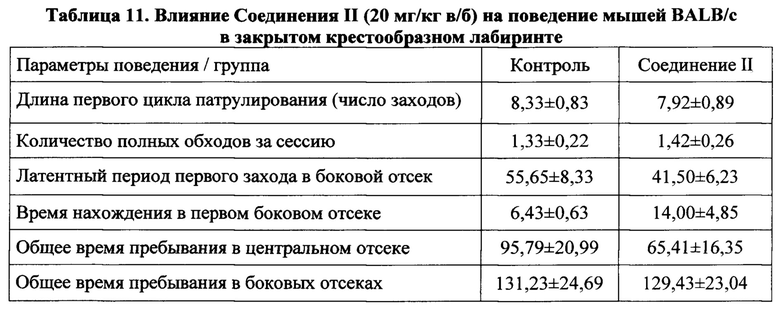
Таким образом, предложено новое соединение - 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден) бензогидразид гидрохлорид (II), которое в дозе 10 мг/кг обладает антисеротониновой цереброваскулярной активностью и противомигреневым действием - вызывает статистически значимые ослабления реакций локального мозгового кровотока в теменной области коры головного мозга и артериального давления, вызванных серотонином. Антисеротониновый эффект нового соединения выражен в той же степени, что и у потенциальных противомигреневых средств - тропоксина и ЛК-933, но Соединение II, значительно превосходит вышеупомянутые средства по экономической целесообразности синтеза (исходный продукт его синтеза более доступен и в 5,36 раза дешевле тропинона). Соединение не влияет на исследовательскую и двигательную активности мышей линии BALB/c и не проявляет нейротропной активности в исследованных тестах. Побочных эффектов и гибели животных в дозе, в 10 раз превышающей эффективную, не обнаружено. По острой токсичности (LD50=352 мг/кг, в/б) Соединение II относится к четвертому классу токсичности (LD50101-1000 мг/кг, в/б).
| название | год | авторы | номер документа |
|---|---|---|---|
| Ацилгидразон (2,3,4-триметокси-N'-(8-метил-8-азабицикло[3.2.1.] октан-3-илиден) бензогидразид гидрохлорид), обладающий противомигреневой и анксиолитической активностью | 2016 |
|
RU2699658C2 |
| КОМБИНАЦИЯ ПРОИЗВОДНОГО ПИПЕРИДИНА С ПИКАМИЛОНОМ, ОБЛАДАЮЩАЯ АНТИСЕРОТОНИНОВОЙ И ПРОТИВОИШЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2822877C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ПРОТИВОМИГРЕНЕВЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ) | 2008 |
|
RU2424803C2 |
| СРЕДСТВО, УЛУЧШАЮЩЕЕ КРОВОСНАБЖЕНИЕ ИШЕМИЗИРОВАННОГО МОЗГА | 2019 |
|
RU2747202C2 |
| Использование 3,4,5-триметокси-N'(2,2,6,6-тетраметил-пиперидин-4-илиден)бензогидразида гидрохлорида в качестве анксиолитического средства | 2016 |
|
RU2691454C2 |
| Эфиры янтарной кислоты 5-гидроксиадамантан-2-она, улучшающие кровоснабжение ишемизированного мозга | 2017 |
|
RU2658833C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВОМИГРЕНОЗНОГО ДЕЙСТВИЯ В ТВЕРДОЙ ЛЕКАРСТВЕННОЙ ФОРМЕ В ВИДЕ ТАБЛЕТОК | 2019 |
|
RU2696866C1 |
| АНТИАГРЕГАЦИОННОЕ СРЕДСТВО | 2005 |
|
RU2353363C2 |
| Средство, увеличивающее мозговой кровоток | 2016 |
|
RU2655810C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2750418C1 |
Изобретение относится к соединению 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден)бензогидразид гидрохлорида. Технический результат - соединение в качестве антисеротонинового цереброваскулярного и противомигреневого средства, относится к малоопасным веществам (4 класс токсичности), не вызывает нежелательных побочных эффектов, по экономической целесообразности синтеза значительно превосходит производные тропана. 11 табл., 6 пр.
Соединение 2,3,4-триметокси-N-(2,2,6,6-тетраметилпиперидин-4-илиден) бензогидразид гидрохлорид, обладающее антисеротониновой цереброваскулярной и противомигреневой активностью.
| Ацилгидразон (2,3,4-триметокси-N'-(8-метил-8-азабицикло[3.2.1.] октан-3-илиден) бензогидразид гидрохлорид), обладающий противомигреневой и анксиолитической активностью | 2016 |
|
RU2699658C2 |
| Замещенные 1,2,5-триметил- и 2,2,6,6-тетраметил-4-аминопиперидины, обладающие антиишемическим действием | 2015 |
|
RU2686317C2 |
| SU 1832633 A1, 20.06.1996 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2023-09-19—Публикация
2022-12-21—Подача