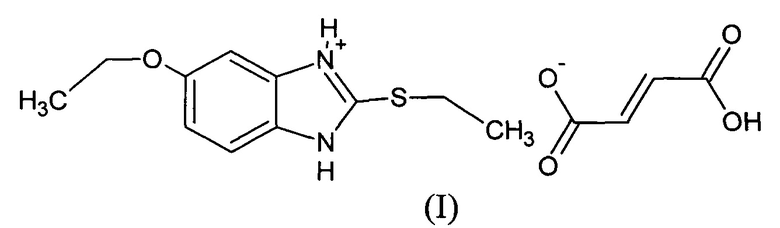
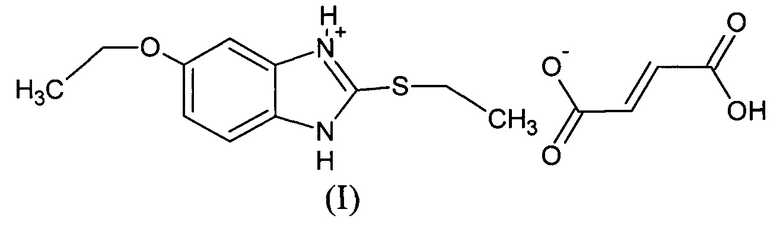
Группа изобретений относится к медицине и фармации и касается нового производного 5-этокси-2-этилтиобензимидазола, а именно: 5-этокси-2-(этилсульфанил)-1Н-бензимидазол-3-иум(2Е)-3-карбоксипроп-2-еноата (C11H14N2OS⋅C4H4O4) формулы I, способа его получения и содержащего его актопротекторного средства.
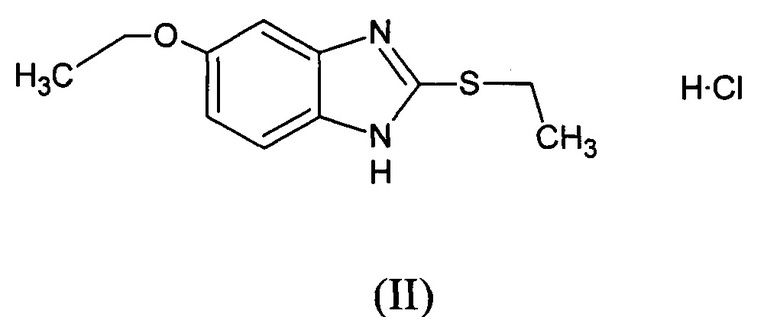
Наиболее близким по структуре и фармакологическим свойствам к заявляемому средству является 5-этокси-2-этилтиобензимидазола гидрохлорид формулы II (прототип):
В медицинской литературе известна антигипоксическая, стресспротекторная [Лозинский М.О, Бобков Ю.Г, Курочкин И.Г, Лосев А.С, Зарановская Е.В, Дмитруха В.С, Завацкий В.Н, Иванова И.А, Савельев В.Л, Середенин С.Б, Зурдинов А.З, Лещинюк И.И, Виноградов В.М, Катков В.Ф, Дюмаев К.М. Гидрохлорид 5-этокси-2-этилтиобензимидазола, обладающий антигипоксической и стрессопротекторной активностью / Заявка 3641355/04 от 13.07.1983. Патент №1259652. Опубл. 10.11.1996], а также противоастеническая [Шабанов П.Д. Клиническая фармакология метапрота, нового противоастенического препарата с психоактивирующими свойствами // Обзоры по клинической фармакологии и лекарственной терапии - том 7, вып, 3, С. 48-81] активность таких соединений, относящихся к производным 2-меркаптбензимидазола.
К недостаткам гидрохлорида 5-этокси-2-этилтиобензимидазола можно отнести недостаточно высокую актопротекторную активность.
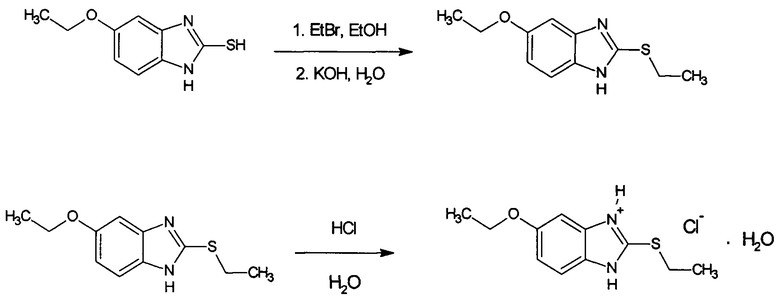
Известен способ получения 5-этокси-2-этилтиобензимидазола гидрохлорида конденсацией 4-этокси-1,2-фенилендиамина с этилксантогенатом калия с последующим алкилированием полученного соединения бромистым этилом и кристаллизацией из соляной кислоты [Лозинский М.О, Бобков Ю.Г, Курочкин И.Г, Лосев А.С, Зарановская Е.В, Дмитруха В.С, Завацкий В.Н, Иванова И.А, Савельев В.Л, Середенин С.Б, Зурдинов А.З, Лещинюк И.И, Виноградов В.М, Катков В.Ф, Дюмаев К.М. Гидрохлорид 5-этокси-2-этилтиобензимидазола, обладающий антигипоксической и стрессопротекторной активностью / Заявка 3641355/04 от 13.07.1983. Патент №1259652. Опубл. 10.11.1996].
Задачей группы изобретений является расширение арсенала актопротекторных средств, создание нового неописанного в литературе производного 5-этокси-2-этилтиобензимидазола, имеющего низкую токсичность и обладающего актопротекторной активностью, превышающей по своим показателям указанную активность используемых в медицинской практике препаратов.
Техническими результатами, на которые нацелено изобретение, является получение нового соединения формулы I, которое потенциально может выступать в качестве актопротекторного средства, и разработка способа его синтеза с высоким выходом продукта реакции.
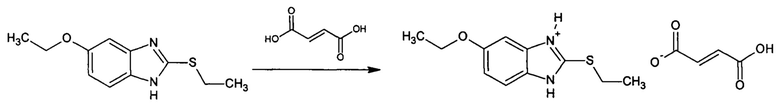
Поставленная задача осуществляется получением нового вещества 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноата формулы I путем взаимодействия 5-этокси-1Н-бензимидазол-2-тиола с диэтилсульфатом в присутствии основания в водной среде при мольном соотношении 1:1:1 и дальнейшей обработкой полученного 5-этокси-2-(этилсульфанил)-1H-бензимидазола фумаровой кислотой в среде ацетона при 50°С с дальнейшим выделением целевого продукта.
Задача осуществляется еще и тем, что целевой продукт выделяют отгонкой ацетона.
Задача осуществляется также доказательством низкой токсичности 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноата и исследованием его актопротекторной активности. Результаты данных испытаний позволяют предлагать заявляемое соединение в качестве потенциального актопротекторного средства.
Изобретение иллюстрируется примерами синтеза и исследования фармакологических свойств.
Пример 1.
Методика синтеза 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноата.
Способ получения 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноата проведен и изучен на стандартном товарном сырье.
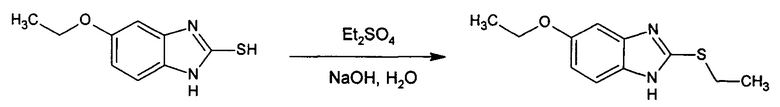
При взаимодействии 5-этокси-1H-бензимидазол-2-тиола с диэтилсульфатом в присутствии основания в водной среде был синтезирован 5-этокси-2-(этилсульфанил)-1H-бензимидазол.
К 19,4 г (0.1 моль) 5-этокси-1H-бензимидазол-2-тиола в 100 мл воды добавляли 4,4 г (0.11 моль) гидроксида натрия и 17,0 г (0.11 моль) диэтилсульфата. Смесь перемешивали 24 часа при комнатной температуре. Продукт отфильтровывали, промывали водой, сушили на воздухе и перекристаллизовывали из водного этанола. Выход 20 г (90%). Т. пл. 117-118°С.
1H ЯМР (500 МГц, ДМСО-d6): 1.28-1.38 (м, 6Н, СН3), 3.23 (к, j=5.7 Гц, 2Н, SCH2), 3.99 (к, j=5.7 Гц, 2Н, ОСН2), 6.73 (дд, j=8.0, 2.0 Гц, 1Н), 6.97 (с, 1Н), 7.33 (д, j=8.0 Гц, 1Н), 12.5 (шс, 1H, NH). 13С ЯМР (125 МГц, ДМСО-d6): 15.2, 15.7, 26.2, 63.8, 94.6, 111.1, 111.3, 118.4, 130.5, 149.4, 154.8.
В спектре ЯМР 1Н 5-этокси-2-(этилсульфанил)-1H-бензимидазола в ДМСО-d6 присутствуют характерные сигналы протонов этильных групп 1.28-1.38 (м, 6Н, СН3), 3.23 (к, j=5.7 Гц, 2Н, SCH2), 3.99 (к, j=5.7 Гц, 2Н, ОСН2) и мультиплеты ароматических протонов 6.73 (дд, j=8.0, 2.0 Гц, 1Н), 6.97 (с, 1Н), 7.33 (д, j=8.0 Гц, 1Н). Кроме того, наблюдаются уширенный синглет протона NH 12.5 (шс, 1Н, NH). В спектре ЯМР 13С 5-этокси-2-(этилсульфанил)-1H-бензимидазола в ДМСО-d6 присутствуют сигналы атомов углерода этильных групп (15.2, 15.7, 26.2 (SCH2), 63.8 (ОСН2) м. д.) и семь сигналов атомов углерода бензимидазола (94.6, 111.1, 111.3, 118.4, 130.5, 149.4 и 154.8 м. д.).
5-Этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноат был синтезирован при взаимодействии 5-этокси-2-(этилсульфанил)-1H-бензимидазола с фумаровой кислотой.
К 22,2 г (0.1 моль) 5-этокси-2-(этилсульфанил)-1H-бензимидазола в 100 мл ацетона добавляли 11,6 г (0.1 моль) фумаровой кислоты. Смесь перемешивали 1 час при 50°С. Ацетон отгоняли на роторном испарителе, кристаллы промывали эфиром и сушили на воздухе. Выход 31,1 г (92%).
Строение синтезированного вещества было доказано методами 1Н- и 13С-ЯМР-спектроскопией. 1Н ЯМР (500 МГц, ДМСО-d6): 1.31-1.41 (м, 6Н, СН3), 3.27 (к, j=5.7 Гц, 2Н, SCH2), 3.96 (к, j=5.7 Гц, 2Н, ОСН2), 6.51 (с, 2Н, СН=СН), 6.77 (дд, j=8.0, 2.0 Гц, 1H), 6.94 (с, 1H), 7.37 (д, j=8.0 Гц, 1Н), 12.1 (шс, 2Н, NH). 13С ЯМР (125 МГц, ДМСО-d6): 15.7, 16.2, 27.2, 64.7, 95.6, 113.3, 112.5, 118.7, 131.4, 134.1, 151.4, 156.3, 171.2.
В спектре ЯМР 1Н 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноата в ДМСО-d6 присутствуют характерные сигналы протонов этильных групп 1.31-1.41 (м, 6Н, СН3), 3.27 (к, j=5.7 Гц, 2Н, SCH2), 3.96 (к, j=5.7 Гц, 2Н, ОСН2), синглет этиленовых протонов фумаровой кислоты 6.51 (с, 2Н, СН=СН) и мультиплеты ароматических протонов 6.77 (дд, j=8.0, 2.0 Гц, 1H), 6.94 (с, 1Н), 7.37 (д, j=8.0 Гц, 1H). Кроме того, наблюдаются сильно уширенный сигнал протонов NH 12.1 (шс, 2Н, NH). В спектре ЯМР 13С 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипроп-2-еноата в ДМСО-d6 присутствуют сигналы атомов углерода этильных групп (15.7, 16.2, 27.2 (SCH2), 64.7 (ОСН2) м. д.), типичные сигналы атомов углерода протонированного бензимидазола (95.6, 113.3, 112.5, 118.7, 131.4, 151.4, 156.3 м. д.) и фумаровой кислоты (134.1, 171.2 м. д.).
Пример 2. Определение острой токсичности.
Острую токсичность 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипро-п-2-еноата определяли на аутбредных белых мышах-самцах массой тела 24±2 г. Перед испытанием животные были разделены на 2 группы по 5 мышей в каждой. Все 2 группы получали исследуемое вещество - 5-этокси-2-(этилсульфанил)- 1Н-бензимидазол-3-иум(2Е)-3-карбоксипроп-2-еноат. За 3-4 часа до введения животных ограничивали в пище, но поили. По прошествии периода голодания животных взвешивали и на основании данных массы тела высчитывали дозу, затем вводили им тестируемый препарат.
1-я и 2-я группы получали исследуемое соединение путем внутрижелудочного введения раствора с помощью зонда в дозе 2 г/кг и 1,5 г/кг соответственно. После введения препарата велось постоянное наблюдение за животными с регистрацией времени наступления первых клинических признаков интоксикации. Оценка выживаемости животных проводилась индивидуально после введения дозы не меньше, чем один раз в первые 30 минут, регулярно в течение первых 24 ч (особенно первые четыре часа), и затем ежедневно в течение 14 дней. Наблюдения, включающие отдельные отчеты о каждом животном, систематически отмечались. Регистрировали развитие основных симптомов и время гибели животных.
В результате в 1-ой и 2-ой группах выживаемость составила 100%.
На основании ГОСТа №32296-2013 «Методы испытаний по воздействию химической продукции на организм человека. Основные требования к проведению испытаний по оценке острой токсичности при внутрижелудочном поступлении методом фиксированной дозы» исследуемый препарат причислен к 5 классу острой токсической опасности по классификации СГС и является малотоксичным.
Острая токсичность заявляемого соединения сопоставима с острой токсичностью 5-этокси-2-этилтиобензимидазола гидрохлорида.
Пример 3. Определение актопротекторной активности.
Для оценки физической работоспособности 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2Е)3-карбоксипро-п-2-еноата в работе использовался стандартный для фармакологических исследований метод предельного плавания животных с нагрузкой и метод силовых нагрузок. Для проведения теста предельного плавания лабораторным животным в области межреберья с помощью специальных одноразовых креплений фиксировался груз, составляющий 7,5% от массы тела животного и соответствующий среднему уровню интенсивности аэробно-анаэробной нагрузки. Исследования выполнялись на 40 белых беспородных мышах самцах массой 22-25 г. Животные были разделены на 4 группы, по 10 мышей в каждой.
Лабораторным животным после взвешивания внутрижелудочно с помощью зонда однократно вводили исследуемое соединение 5-этокси-2-(этилсульфанил)-1Н-бензимидазол-3-иум(2Е)-3-карбоксипроп-2-еноат в дозировке 25 мг/кг и 12,5 мг/кг и референсный препарат - 5-этокси-2-этилтиобензимидазола гидрохлорид в дозировке 25 мг/кг. Животные контрольной группы получали 0,9% NaCl в эквиобъемных количествах.
Исследования проводили в плавательной установке, представляющей собой 200-литровый бассейн (высота 40 см, ширина 35 см и длина 80 см), заполняемый водой до половины. Внутри него располагался контур из оргстекла (высота 30 см, ширина 30 см и длинна 75 см), разделенный на 10 отсеков (15×15 см каждый). Установку заполняли до половины десатурированной водой температуры 22-24°С. Десатурацию воды проводили путем предварительного отстаивания в течение суток. Во время теста животных помещали в соответствующий отсек бассейна и сразу включали секундомер. Критерием окончания теста являлось погружение животного на дно бассейна без плавательных движений или неудачной попытки всплыть на поверхность более трех секунд, после чего животное извлекали из бассейна, обсушивали мягкой тканью и помещали в стандартную клетку.
Установлено, что заявляемое средство в дозировке 25 мг/кг при однократном введении достоверно (р<0,05) увеличивало физическую работоспособность мышей в 1,19 раза по сравнению с животными контрольной группы и превосходил эффект 5-этокси-2-этилтиобензимидазола гидрохлорида (доза 25 мг/кг) в 1,06 раза.
Для оценки силовых характеристик животных использовался тест на силу хватки лап. Для его проведения использовали динамометр (Grip Strength Meter, TSE Systems, Германия). Перед испытанием животные были разделены на 3 группы, по 8 мышей в каждой: 1-я - контрольная группа, внутрижелудочно с помощью зонда получала 0,9% NaCl в объеме 10 мл/кг, 2-я группа получала референсный препарат 5-этокси-2-этилтиобензимидазола гидрохлорид в дозе 25 мг/кг, 3-я группа получала исследуемое соединение 5-этокси-2-(этилсульфанил)- 1H-бензимидазол-3-иум(2E)3-карбоксипро-п-2-еноат в дозе 25 мг/кг. Все препараты вводили внутрижелудочно с помощью зонда за 30 минут до тренировки 3 раза в неделю в течение 1 месяца.
Выполнение тренировок проводилось в 3 подхода с перерывом в 1 минуту путем "негативных повторений" для передних лап с помощью проволоки динамометра. Животному давали ухватиться лапами за проволоку с возможностью подтянуть себя к ней по инерции, после этого плавно оттягивали обратно до полного выпрямления лап. Подход осуществлялся до момента, пока экспериментатор не чувствовал отсутствие силы у животного притянуть себя к проволоке.
В результате через 4 недели тренировок сила хвата животных, которым вводили исследуемое соединение 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)3-карбоксипро-п-2-еноат (доза 25 мг/кг), достоверно (р<0,05) увеличилась в 1,86 раза относительно исходных значений, в 1,11 раза относительно показателей контрольной группы ив 1,33 раза (р<0,005) относительно препарата сравнения 5-этокси-2-этилтиобензимидазола гидрохлорида (доза 25 мг/кг).
Таким образом, заявляемое средство является малотоксичным и проявляет наибольшую актопротекторную активность относительно препарата сравнения и контрольной группы и может быть рекомендовано в качестве потенциального актопротекторного средства для применения в медицинской практике.
| название | год | авторы | номер документа |
|---|---|---|---|
| Антигипоксическое и актопротекторное средство на основе 2-(этилсульфанил)-1Н-бензимидазол-3-ия (2Е)-3-карбоксипроп-2-еноата | 2017 |
|
RU2673338C1 |
| ЧЕТВЕРТИЧНЫЕ АММОНИЙНЫЕ ПРОИЗВОДНЫЕ 2-АМИНОТИОФЕН-3-КАРБОКСИЛАТОВ, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2629369C1 |
| ПРОИЗВОДНЫЕ ХИНОЛИН-2-ОНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ C-KIT | 2016 |
|
RU2754858C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛ-3-АМИНОМЕТИЛ-ХИНОЛОНА-2 В КАЧЕСТВЕ ИНГИБИТОРОВ NO-СИНТЕТАЗЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, БИОЛОГИЧЕСКИ АКТИВНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2003 |
|
RU2284325C2 |
| 1-(2-ИЗОПРОПОКСИЭТИЛ)-2-ТИОКСО-1,2,3,5-ТЕТРАГИДРО-ПИРРОЛО[3,2-d]ПИРИМИДИН-4-ОН И ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 2005 |
|
RU2409578C2 |
| 4-(ИМИДАЗО[1,2-а]ПИРИДИН-3-ИЛ)-ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2822388C2 |
| ПРОИЗВОДНЫЕ 3-МЕТИЛ-7-(ТИЕТАНИЛ-3)КСАНТИНА, ОБЛАДАЮЩИЕ ГЕМОРЕОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2316551C1 |
| ПРОИЗВОДНЫЕ 3-АМИНОМЕТИЛХИНОЛОНА-2 В КАЧЕСТВЕ ИНГИБИТОРОВ NO-СИНТЕТАЗЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ, БИОЛОГИЧЕСКИ АКТИВНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2003 |
|
RU2267485C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(АЗОЛ-1-ИЛ)ЭТАНАМИНОВ | 2006 |
|
RU2317984C2 |
| Смесь изомеров 3-{ (2E/Z)-2-[3-(гидроксимино)-4-оксо-4-пара-толилбутан-2-илиден]гидразинил} -хиноксалин-2(1H)-она | 2023 |
|
RU2814666C1 |
Изобретение относится к новому соединению - 5-этокси-2-(этилсульфанил)-1Н-бензимидазол-3-иум(2Е)-3-карбоксипроп-2-еноату (C11H14N2OS⋅C4H4O4) формулы I. Соединение обладает антигипоксической и стрессопротекторной активностью и может быть использовано в качестве активного компонента для актопротекторного средства. Изобретение также относится к способу получения соединения формулы I
Способ заключается в том, что смесь 5-этокси-1H-бензимидазол-2-тиола, диэтилсульфата и основания при мольном соотношении 1:1,1:1,1 в водной среде перемешивают при комнатной температуре. Образовавшийся продукт алкилирования - 5-этокси-2-(этилсульфанил)-1H-бензимидазол - в виде осадка отделяют и подвергают обработке фумаровой кислотой в мольном соотношении 1:1 в среде ацетона при 50°C с дальнейшим выделением целевого продукта. В качестве основания обычно используют NaOH. Для выделения целевого продукта проводят отгонку ацетона. 3 н. и 2 з.п. ф-лы, 3 пр.
1. 5-Этокси-2-(этилсульфанил)-1Н-бензимидазол-3-иум(2Е)-3-карбоксипроп-2-еноат формулы I.
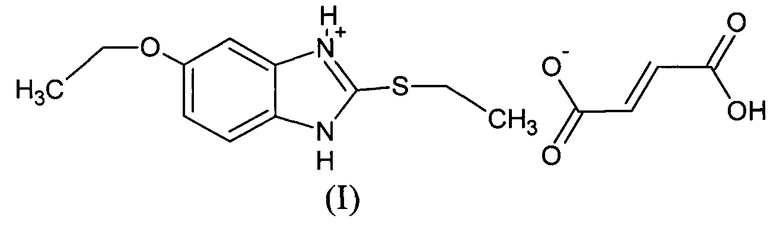
2. Способ получения 5-этокси-2-(этилсульфанил)-1H-бензимидазол-3-иум(2E)-3-карбоксипроп-2-еноата формулы I, характеризующийся тем, что смесь 5-этокси-1H-бензимидазол-2-тиола, диэтилсульфата и основания при мольном соотношении 1:1,1:1,1 в водной среде перемешивают при комнатной температуре, образовавшийся продукт алкилирования - 5-этокси-2-(этилсульфанил)-1H-бензимидазол - в виде осадка отделяют и подвергают обработке фумаровой кислотой в мольном соотношении 1:1 в среде ацетона при 50°C с дальнейшим выделением целевого продукта.
3. Способ по п. 2, отличающийся тем, что в качестве основания используют NaOH.
4. Способ по п. 2, отличающийся тем, что для выделения целевого продукта проводят отгонку ацетона.
5. 5-Этокси-2-(этилсульфанил)-1Н-бензимидазол-3-иум(2Е)-3-карбоксипроп-2-еноат формулы I в качестве активного компонента для актопротекторного средства.
| SU 1259652 А1, 10.11.1996 | |||
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, АКТОПРОТЕКТОРНОЙ, НООТРОПНОЙ АКТИВНОСТЯМИ И ВЛИЯЮЩЕЕ НА ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2011 |
|
RU2462245C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АКТОПРОТЕКТОРНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ТЕРМОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2460529C1 |
Авторы
Даты
2019-09-17—Публикация
2018-12-25—Подача