Изобретение относится к клиническим и лабораторным методам исследования и может быть использовано для количественного определения органических и неорганических гидропероксидов в модельных системах и биологических жидкостях.
Свободнорадикальные процессы играют важную роль в этиологии и патогенезе целого ряда заболеваний, таких как атеросклероз, сахарный диабет и др. Увеличение генерирования активных форм кислорода, включая супероксидный анион-радикал, может приводить к окислительным повреждениям липид-белковых надмолекулярных комплексов (биомембран и липопротеидов). Супероксидный анион-радикал способен дисмутировать с образованием пероксида водорода, причем в организме этот процесс катализирует фермент супероксиддисмутаза. В процессе окислительного стресса происходит одновременное накопление первичных продуктов свободнорадикального окисления - органических гидропероксидов (в частности, липогидропероксидов различного строения - ROOH) и неорганических гидропероксидов (пероксида водорода - Н2О2). Вследствие этого, существует необходимость в разработке способа для раздельного определения этих продуктов. Тем не менее, в настоящее время нет сведений о возможности одновременного определения органических и неорганических гидропероксидов в одних и тех же пробах. В работе Nourooz-Zadeh J. et al., Anal Biochem. 1994, 220: 403-409 была описана возможность раздельного определения ROOH и Н2O2 колориметрическим методом (с использованием реагента Fe-ксиленолоранж) после предварительного восстановления ROOH трифенилфосфином (ТФФ), который восстанавливал ROOH, но не Н2O2 (определение Н2O2 производили путем вычитания показаний пробы с ТФФ из показаний пробы без ТФФ).
Тем не менее, в проведенном исследовании способом индуцированной хемилюминесценции эти данные не нашли подтверждения, поскольку было установлено, что трифенилфосфин специфичным действием не обладает и не может быть использован в качестве реагента при раздельном определении органических и неорганических гидропероксидов.
Известные способы определения содержания органических гидропероксидов (ROOH, включая липопероксиды) были основаны либо на цветных реакциях, либо на определении поглощения конъюгированных диенов. Следует отметить, что колориметрические способы, в частности с использованием реагента Fe-ксиленолоранж (Nourooz-Zadeh J. et al., Anal Biochem. 1994, 220: 403-409), высокой чувствительностью не обладают и их использование для анализа биологического материала возможно только в случае концентрирования ROOH (например, путем препаративного выделения липопротеидов плазмы крови - Lankin V.Z. et al., Mol Cell Biochem. 2003, 249: 129-40). Очевидно, что подобные подходы непригодны для серийных клинических анализов.
Что касается спектрофотометрического определения уровня конъюгированных диенов, то обычно используемый способ по анализу спектра поглощения не может использоваться при анализе биологического материала, так как вследствие малого содержания ROOH пик их поглощения при 233 нм, как правило, не разрешен и для корректного определения необходим обсчет первых или вторых производных спектра, что позволяет делать далеко не каждый даже импортный спектрофотометр (Corongiu F.P. et. al., Methods Enzymol. 1994, 233: 303-10). Кроме того, при спектрофотометрическом определении в области поглощения 233 нм в природных системах определяются не только гидроперокси-производные липидов, но и продукты их восстановления - соответствующие окси-кислоты (при восстановлении гидропероксидов максимум поглощения практически не изменяется).
Известны также хемилюминесцентные способы определения органических гидропероксидов, обладающие большими преимуществами по сравнению с другими способами, ввиду весьма высокой чувствительности. Впервые использование хемилюминесцентного способа для определения органических гидропероксидов (ROOH) предложил Yamamoto Y. (Yamamoto Y. et al. Anal. Biochem. 1987, 160: 7-13). При этом гомолиз ROOH индуцировали микропероксидазой, а их разделение осуществляли при помощи высокоэффективной жидкостной хроматографии. Количественное определение ROOH осуществлялось при помощи хемилюминесцентного детектора после их разделения. Модификацию этого способа осуществили с применением люминола в качестве агента, увеличивающего квантовый выход хемилюминесценции (ХЛ). (Теселкин Ю.О. и Бабенкова И.В., Вестник РГМУ, 2011, 5: 54-58). А также с использованием в качестве усиливающего ХЛ агента изолюминола, что оказалось более целесообразным ввиду лучшей воспроизводимости результатов. (Проскурниной Е.В. и др. Журнал аналитической химии. - 2017, 72: 1-6).
Тем не менее, как следует из вышеизложенного, ни один из существующих способов, включая колориметрические,
спектрофотометрические и хемилюминесцентные, не позволяет проводить одновременно раздельное определение содержания органических и неорганических гидропероксидов в анализируемых пробах.
В связи с вышеизложенным, существует потребность в способе, позволяющем с высокой специфичностью проводить одновременное определение содержания органических и неорганических гидропероксидов в одной и той же пробе. Учитывая тот факт, что подобный способ может быть использован для проведения анализов в пробах биологического материала, одним из основных требований к способу определения является его высокая чувствительность.
Задачей изобретения является разработка простого и быстрого способа раздельного определения органических и неорганических гидропероксидов при помощи хемилюминесценции, позволяющего применять его в качестве доступного лабораторного теста.
Технический результат изобретения заключается в повышении специфичности и чувствительности способа.
Это достигается тем, что в заявляемом способе селективность определения ROOH и Н2O2 основана на предварительном высокоспецифичном ферментативном восстановлении Н2O2 с помощью каталазы, причем содержание ROOH рассчитывается путем вычитания светосуммы пробы после инкубации с каталазой из светосуммы под пиком общей хемилюминесцентной кривой.
Осуществление способа:
Хемилюминесцентный реагент (ХЛ-реагент), который используют в день приготовления и предварительно выдерживают в течение 20 мин при комнатной температуре в темноте до угасания собственной хемилюминесценции, содержит 200 нМ микропероксидазы-11 и 2 мкМ изолюминола в 20 мМ боратном буфере рН 10,0. Органический гидропероксид (ROOH - 13-гидропероксилинолеат) получают путем ферментативного окисления линолевой кислоты при катализе липоксигеназой-1 соевых бобов. Важно отметить, что липиды должны быть диспергированы без применения спиртовых растворов, поскольку в присутствии спиртов каталаза способна восстанавливать ROOM в ходе пероксидазной реакции. Далее, ROOH (13-гидропероксилинолеат) диспергируют в воде с помощью детергента дезоксихолата натрия (1/2; мкмоль/мкмоль).
Измерение ХЛ проводят на хемилюминометре Lum-100 (ДИсофт, Россия). Для проведения определения готовят две пробы.
Проба 1 (ROOH+H2O2): в хемилюминесцентную кювету помещают 25 мкл 1,2 мкМ дисперсии ROOH (13-гидропероксилинолеата) и 25 мкл 1,2 мкМ водного раствора H2O2.
Проба 2 (ROOH+H2O2 + каталаза) содержит те же ингредиенты, что и проба 1, но с добавлением 0,25 ед/мл каталазы и инкубируют при комнатной температуре в темноте в течение 10 мин. Кювету с пробой 1 помещают в хемилюминометр и регистрируют собственную ХЛ образца в течение 60 сек, а затем впрыскивают через капиллярную трубку 950 мкл ХЛ-реагента и производят запись в течение 5 мин, после чего определяют площадь под ХЛ-кривой (светосумма ХЛ за 4 мин). По истечении времени инкубации проводят регистрацию ХЛ пробы 2. Количество органического гидропероксида определяют путем вычитания светосуммы ХЛ пробы 2 из светосуммы ХЛ пробы 1. Количественное определение 13-гидропероксилинолеата и H2O2 проводят с использованием соответствующих калибровочных графиков, построенных в координатах: по абсциссе - концентрация гидропероксидов в нМ; по ординате - светосумма ХЛ.
Пример 1 раздельного определения ROOH и H2O2 в смеси этих компонентов.
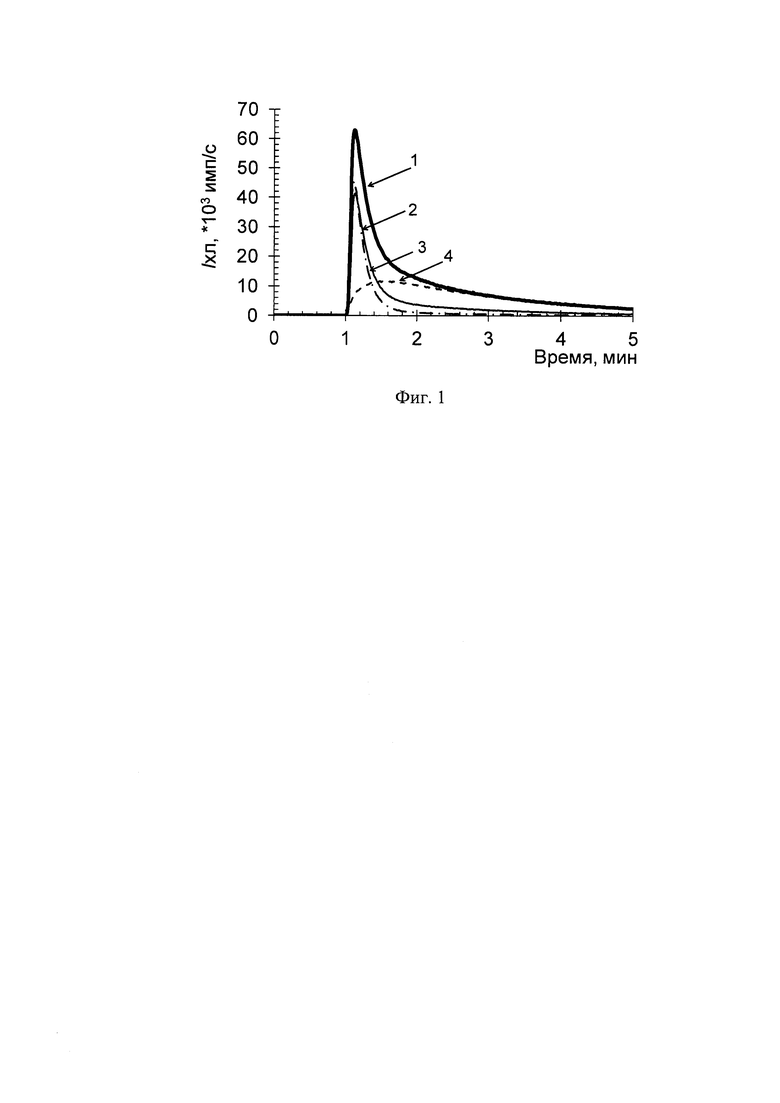
Раздельное хемилюминесцентное определение концентрации органического (13-гидропероксилинолеата) и неорганического (Н2О2) гидропероксидов в их смеси (1/1 в нмолях) предлагаемым способом показаны в таблице 1. Полученные ХЛ-кривые представлены на Фиг. 1, где ХЛ-кривые: 1 - смесь 13-гидропероксилинолеата и пероксида водорода (1/1), 2 - то же+каталаза (0,25 ед/мл), 3 - 13-гидропероксилинолеат (30 нМ), 4 - пероксид водорода (30 нМ). Результаты приведены в условных единицах ХЛ (светосумма за 4 мин в имп.х 10).

Экспериментально определенное содержание ROOH (13-гидропероксилинолеата) в пробе смеси эквимолярных количеств органического и неорганического (Н2O2) гидропероксидов после утилизации Н2O2 каталазой представляют данные пробы 2, причем расхождение с определенным тем же способом содержанием чистого ROOH - 13-гидропероксиксилинолеата (994±123) составляет 9,5%. Содержание Н2O2 в смеси эквимолярных количеств ROOH и Н2O2 определяется путем вычитания данных пробы 2 (после утилизации пероксида водорода каталазой) из данных пробы 1 (смесь 13-гидропероксилинолеата и Н2O2), причем расхождение с определенным тем же способом содержанием чистого Н2O2 (807±57) составляет 10%.
Следовательно, содержание органических гидропероксидов -ROOH (в данном примере - 13-гидроперокси линолеат) и неорганических гидропероксидов (Н2O2) по предлагаемому способу осуществляется по формулам:
1) [ROOH]=[ROOH+Н2O2+каталаза] или [ROOH]=показателю пробы 2;
2) [Н2O2]=[ROOH+Н2O2] - [ROOH] или
[Н2O2]=показатель пробы 1 минус показатель пробы 2, где [ROOH] и [Н2O2] - концентрации органического и неорганического гидропероксидов соответственно.
Таким образом, предлагаемый способ позволяет с достаточно высокой точностью и чувствительностью (определяются наномолярные количества веществ, что почти на 3 порядка превышает чувствительность спектрофотометрических методов) с абсолютной специфичностью (исходя из абсолютной специфичности каталазной реакции) производить раздельное определение органических гидропероксидов и пероксида водорода в средах, содержащих смесь этих компонентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ МЕТАБОЛИЗМА В ОРГАНИЗМЕ В УСЛОВИЯХ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2010 |
|
RU2436101C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ МАСТИТА У КОРОВ | 2011 |
|
RU2485914C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ИНТЕНСИВНОЙ ТЕРАПИИ У ПОСТРАДАВШИХ С ТЯЖЕЛОЙ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМОЙ | 2010 |
|
RU2441574C1 |
| СПОСОБ ГЕНЕРАЦИИ ПЕРОКСИДА ВОДОРОДА НА ОСНОВЕ НАНО- И/ИЛИ МИКРОЧАСТИЦ ZnO2 ДЛЯ ПРИМЕНЕНИЯ В СПЕКТРОФОТОМЕТРИЧЕСКОМ И ЛЮМИНЕСЦЕНТНОМ АНАЛИЗЕ С УЧАСТИЕМ ПЕРОКСИДАЗЫ | 2022 |
|
RU2800949C1 |
| СПОСОБ КОЛИЧЕСТВЕННОЙ ОЦЕНКИ БАЛАНСА ПРО- И АНТИОКСИДАНТОВ В ОТДЕЛАХ ГОЛОВНОГО МОЗГА ЖИВОТНОГО | 2013 |
|
RU2523403C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАСПРОСТРАНЕННОСТИ МЕТАСТАТИЧЕСКОГО ПОРАЖЕНИЯ ГОЛОВНОГО МОЗГА | 2005 |
|
RU2300104C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЯ АНТИОКСИДАНТНОЙ ТЕРАПИИ ПРИ ЛЕЧЕНИИ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ВНУТРЕННИХ ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ | 2010 |
|
RU2442163C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ КРОВИ | 1999 |
|
RU2157532C1 |
| СПОСОБ ОЦЕНКИ АНТИОКИСЛИТЕЛЬНОГО БАЛАНСА ОРГАНИЗМА ЧЕЛОВЕКА | 2001 |
|
RU2206891C1 |
| Устройство для хемилюминесцентного анализа | 2021 |
|
RU2781351C1 |
Изобретение относится к клиническим и лабораторным методам исследования и может быть использовано для количественного определения органических и неорганических гидропероксидов в модельных системах и биологических жидкостях. Способ раздельного определения органических и неорганических гидропероксидов при помощи хемилюминесценции включает диспергирование органических гидропероксидов в водных средах и последующее добавление 0,25 ед./мл каталазы в пробу с общим содержанием гидропероксидов, после чего определяют уровень органических гидропероксидов. Затем путем вычитания концентрации органических гидропероксидов из общего содержания гидропероксидов в смеси вычисляют содержание пероксида водорода. Диспергирование органических гидропероксидов в водных средах осуществляется без использования спиртов, индуцирующих запуск артефактных реакций. Изобретение обеспечивает повышение специфичности и чувствительности способа за счет предварительного высокоспецифичного ферментативного восстановления Н2О2 с помощью каталазы. 1 ил., 1 табл., 1 пр.
Способ раздельного определения органических и неорганических гидропероксидов при помощи хемилюминесценции, отличающийся тем, что осуществляют диспергирование органических гидропероксидов в водных средах, затем в пробу с общим содержанием гидропероксидов добавляют 0,25 ед./мл каталазы, после чего определяют уровень органических гидропероксидов, а путем вычитания их концентрации из общего содержания гидропероксидов в смеси вычисляют содержание пероксида водорода, причем диспергирование органических гидропероксидов в водных средах осуществляется без использования спиртов, индуцирующих запуск артефактных реакций.
| NOUROOZ-ZADEH J | |||
| et al | |||
| Measurement of plasma hydroperoxide concentrations by the ferrous oxidation-xylenol orange assay in conjunction with triphenylphosphine | |||
| Anal Biochem., 1994 Aug 1, vol.220(2), pp.403-409 | |||
| HONG ZHU et al | |||
| A Highly Sensitive Chemiluminometric Assay for Real-Time Detection of Biological Hydrogen Peroxide Formation | |||
| React Oxyg Species (Apex) | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| ДЖАТДОЕВА А.А | |||
| Источники супероксидного анион-радикала в тромбоцитах и тканях | |||
| Диссертация на соискание ученой степени кандидата биологических наук, Москва, 2017, с.51-52, [он-лайн], [наедено 02.07.2019] | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| ВОЛКОВА П.О., АЛЕКСЕЕВ А.В., ДЖАТДОЕВА А.А | |||
| и др | |||
| Определение гидропероксидов липидов методом активированной хемилюминесценции | |||
| Вестник Московского университета, серия 2, Химия, 2016, т.57, N1, с.41-52 | |||
| ЦАПЛЕВ Ю.Б | |||
| Хемилюминесцентное определение пероксида водорода | |||
| Журнал аналитической химии, 2012, т.67, N6, с.564-572 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЕРОКСИДОВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2005 |
|
RU2293334C2 |
| US 4647532 A1, 03.03.1987. | |||
Авторы
Даты
2019-09-19—Публикация
2018-12-10—Подача