Изобретение относится к медицине, а именно к онкологии, способу получения морфологического материала путем тонкоигольной аспирационной биопсии (пункции) лимфатических узлов с целью верификации состояния лимфатических узлов перед предстоящим лечением.
В практической онкологии невозможно начать адекватное лечение без правильно установленного диагноза и стадии заболевания.
Тонкоигольная аспирационная биопсия (ТИАБ) имеет важное лечебно-диагностическое значение в современной медицине. ТИАБ активно применяется в эндокринологии, диагностике очаговых заболеваний щитовидной железы, в экстренной хирургии, при диагностических пункциях брюшной и плевральной полостей, в онкологии, для получения диагностического материала при заболеваниях печени, поджелудочной железы, опухолях мягких тканей, молочных, слюнных и щитовидной желез. (Хоперия В.Г. Тонкоигольная аспирационная пункционная биопсия узлов щитовидной железы: показания, техника, клиническое применение. Украинский научно-практический центр эндокринной хирургии и трансплантации эндокринных органов и тканей МЗ Украины. Номер: 1 (35), 2011 г. С. 57-67. Федотов Ю.Н., Воробьев С.Л., Черников Р.А. Тонкоигольная аспирационная биопсия в диагностике заболеваний щитовидной железы. Корреляция между заключением цитолога и гистолога, технические аспекты. Клиническая и экспериментальная тиреоидология. 2009. Т. 5. №4. С. 28-32. Бурдюков М.С., Нечипай A.M. Тонкоигольная пункция под контролем эндоскопической ультрасонографии: осложнения и альтернативы. Российский электронный журнал лучевой диагностики. 2013. Т. 3. №2. С. 26-37. Марченко М.Г., Трофимов Е.И., Виноградов В.В. Современные методы выявления метастазов рака гортани и гортаноглотки в лимфатические узлы шеи. Российская оториноларингология. 2011. №1 (50). С. 114-117).
Методически тонкоигольная аспирационная биопсия выполняется как под контролем лучевых методов диагностики (РКТ, МРТ, УЗИ), так и без них. Выполнение ТИАБ без использования навигации, возможно при пальпируемых опухолях поверхностных локализаций и изначально больших размерах образования. Применение ТИАБ без навигации имеет ряд недостатков, таких как: повреждение глубжележащих структур, травмирование сосудов с последующим развитием кровотечения, плохое качество диагностического материала. Использование навигации, практически нивелирует вышеописанные риски. Навигация при помощи ультразвука позволяет провести манипуляцию «у постели больного», что делает данную технологию удобной для использования в отделениях реанимации и интенсивной терапии, в условиях операционной, в больницах и амбулаторном звене, не имеющих в своем оснащении аппаратов КТ и МРТ.
Технология ТИАБ под контролем ультразвуковой навигации имеет несколько модификаций. Возможно проведение процедуры методом «свободной руки» или применить специализированные насадки на УЗ-датчик, позволяющие жестко фиксировать направление и ход иглы. Методика «свободной руки» позволяет в режиме реального времени изменить ход и направлении иглы, а так же получить материал из различных участков опухолевого образования, что актуально при больших размерах опухоли.
При анализе отечественной и зарубежной научной и патентной литературы не найдено описания методики выполнения ТИАБ лимфатических узлов парастернальной области.
Для получения морфологического материала из лимфатических узлов парастернального коллектора ранее был предложен ряд методов, таких как:
1. Открытая биопсия парастернальных лимфатических узлов. В 1953 году McDonald предложил выполнять биопсию внутренних грудных лимфатических узлов на этапе дооперационного обследования, и в случае их метастатического поражения предполагалось отказываться от проведения радикального лечения. Учитывая высокую травматичность биопсии, которая сопровождалась пересечением II-III реберных хрящей, использование этой методики в качестве предоперационной диагностической процедуры в течение долгого времени не имела успеха у хирургов (McDonald Е, Haagensen C.D. In: Diseases of the breast. 2nd ed. Philadelphia: W.B. Saunders; 1971.). Так же предполагалось использовать срочное гистологическое исследование операционного материла полученного из парастернальной зоны, но методика не нашла широкого применения в связи с малым размером лимфатических узлов и сложностью срочной интерпретации морфологических данных, что приводило к высокому проценту неверных результатов (Hovnanian А.Р. А technique for the biopsy of intercostal parasternal lymph nodes // Surgery. - 1960. - Vol. 47, №6. - P. 891-894.).
2. Ретростерноскопия. Группа отечественных ученых под руководством В.П. Летягина (1996) разработала и внедрила методику визуального осмотра парастернальных лимфатических узлов. Суть методики состоит в следующем: во время проведения радикальной мастэктомии, во втором межреберье рассекают межреберные мышцы и обнажают парастернальное пространство, в результате чего становятся видны внутренние грудные сосуды, по ходу которых и располагаются лимфатические узлы. В парастернальное пространство вводится детский бронхоскоп, при помощи которого осматривают парастернальные лимфатические узлы. При определенном опыте данный вид оперативного вмешательства удлиняется на 10 минут (Летягин В.П., Лактионов К.П., Высоцкая И.В., Котов В.А. Рак молочной железы. - М., 1996. - 150 с.).
3. Видеоторакоскопическая лимфодиссекция. Применение видеоторакоскопии в хирургическом лечении рака молочной железы в России началось с разработки в 1995 году проф. Е.И. Сигалом и соавт. методики видеоторакоскопической парастернальной лимфодиссекции для преодоления недостатков расширенной мастэктомии по Урбану-Холдину и сохранения радикальности хирургического лечения РМЖ центральных и медиальных локализаций (Синяков А.Г. Видеоторакоскопическая парастернальная лимфодиссекця в лечении рака молочной железы. Международный журнал прикладных и фундаментальных исследований. №10, 2014). В ходе хирургического вмешательства на первом этапе пациенткам выполняется радикальная мастэктомия или радикальная резекция. На втором этапе - видеоторакоскопия парастернальных лимфатических узлов. Вмешательство проводится под эндотрахеальным наркозом с раздельной интубацией легких. После завершения радикального вмешательства на молочной железе больную поворачивают на здоровую сторону в полубоковое положение. По задне-подмышечной линии в V межреберье устанавливается торакопорт диаметром 12 мм для видеокамеры. Два аналогичных порта для манипуляторов устанавливаем по передней подмышечной линии в III и V межреберье. С помощью эндохирургических инструментов производится резекция внутренних грудных сосудов на стороне поражения с моноблочным широким иссечением окружающей клетчатки, содержащей лимфоколлектор, с I по IV межреберье. Через один из портов в плевральную полость устанавливается активный дренаж и производится ушивание троакарных отверстий и операционной раны. В послеоперационном периоде дренаж из плевральной полости извлекается, как правило, на 1-2-е сутки после рентгенологически доказанного расправления легкого (Видеоторакоскопическая парастернальная лимфодиссекция в оценке поражения парастернального лимфатического коллектора при раке молочной железы Синяков А.Г., Зуев В.Ю., Грибанова О.С. Медицинская наука и образование Урала. 2012. Т. 13. №2. С. 60-64.).
У описанных выше методик есть свои недостатки: необходимость применения наркоза, травматичность самой процедуры, высокая вероятность повреждения внутренних грудных сосудов, развитие пневмоторокса вследствие ранения париетальной плевры.
Задачей изобретения является создание безопасного и эффективного способа получения диагностического материала у больных раком молочной железы с подозрением на поражение парастернальных лимфатических узлов, с целью более точного стадирования заболевания.
Поставленная задача решается тем, морфологический материал из лимфатических узлов парастернального коллектора получают при помощи тонкоигольной аспирационной биопсии под контролем ультразвуковой навигации.
Технический результат заявляемого способа состоит в следующем: дооперационное стадирование заболевания; индивидуальный, эффективный подбор режима и вида терапевтического, лучевого или хирургического воздействия при лечении рака молочной железы; точное прогнозирование отдаленных результатов лечениям; безопасность и малая травматичность способа.
Заявляемый способ иллюстрируется фигурами 1-4.
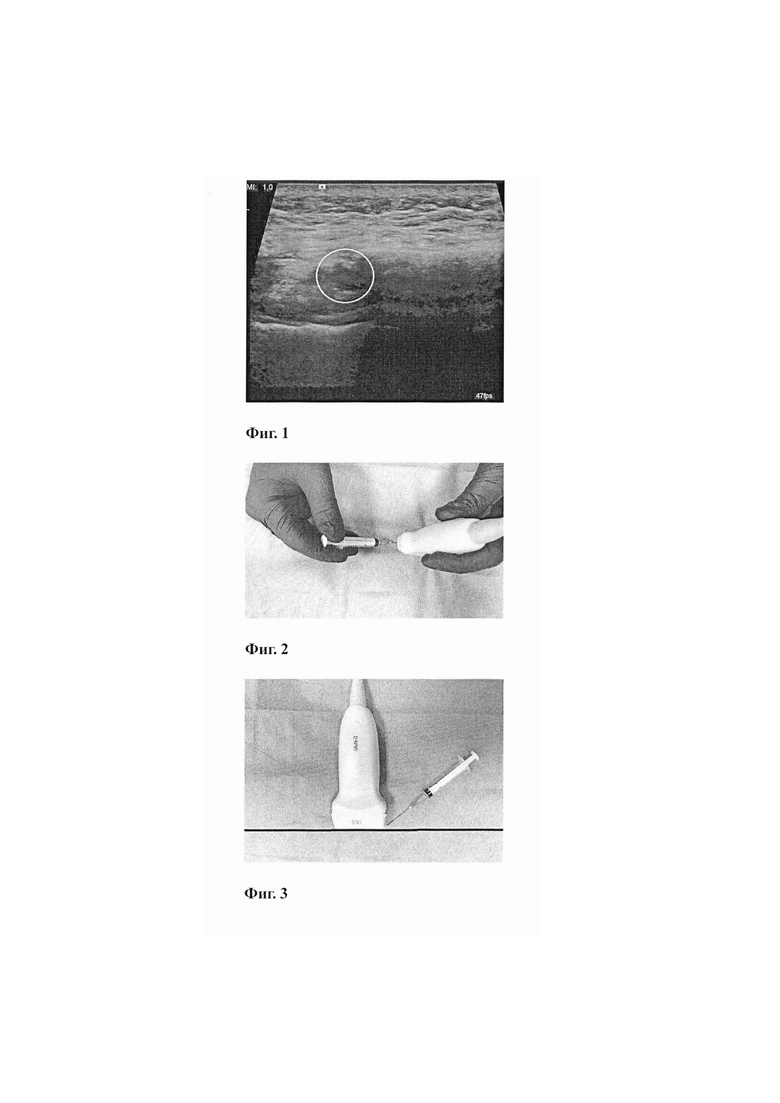
Фиг. 1. - представлена ультразвуковая картина лимфатического узла, перед проведением пункционной биопсии. В центре белого круга анэхогенное «черное» округлое образование - лимфатический узел.
Фиг. 2 -. при проведении процедуры иглу располагают непосредственно по центру боковой поверхности УЗ-датчика.
Фиг. 3. - игла располагается под углом 30-45 градусов к поверхности кожи. На рисунке, черной линией условно отмечена граница кожных покровов.
Фиг. 4. - ультразвуковая картина лимфатического узла во время процедуры проведения пункционной биопсии. Стрелкой указан яркий гиперэхогенный сигнал от кончика иглы.
Заявляемый способ осуществляется следующим образом.
Процедура проводится в условиях манипуляционного кабинета врачом ультразвуковой диагностики совместно с врачом хирургом, с применением аппарата ультразвуковой диагностики, оснащенного линейным датчиком.
На первом этапе выполняют обработку операционного поля и ультразвукового датчика раствором антисептика. На ультразвуковой датчик надевается стерильный полиэтиленовый мешок. В качестве проводящей среды между кожей и датчиком можно использовать раствор антисептика, например, препарат "Катеджель". Затем под УЗ-навигацией производят послойную инфильтрационную анестезию кожи, подкожно-жировой клетчатки, грудных и межреберных мышц. При этом необходимо соблюдать принцип «конец иглы следует за струей новокаина». При правильной технике выполнения, пациент ощущает только первый вкол, при прохождении кожных покровов. Проведение анестезии под УЗ-контролем, кроме задачи обезболивания также позволяет наметить ход иглы, для непосредственного проведения тонкоигольной биопсии. УЗ-контроль за ходом иглы осуществляется при одновременном продольном расположении УЗ-датчика и иглы.
После анестезии проводят процедуру тонкоигольной аспирационной биопсии. Для процедуры используют линейный датчик, который устанавливают в межреберье, таким образом, чтобы выявленный измененный лимфатический узел бы помещен на центр экрана (фиг. 1). С помощью режима цветового допплеровского кодирования визуализируют внутренние грудные сосуды и выбирают оптимальную плоскость прохождения иглы в обход выявленных сосудов. Тонкоигольная аспирационная биопсия проводится шприцем 20 мл с иглой G20-22 (0,7-0,9 мм). Пункционную иглу располагают непосредственно по центру боковой поверхности УЗ-датчика, под углом 30-45 градусов к поверхности кожи (фиг. 2, 3). Медленным движением послойно проходят кожу и подкожно-жировую клетчатку, при этом на экране изображения должен появиться кончик иглы. Далее, контролируя направление конца иглы и корректируя угол проникновения, направляют иглу к выявленному лимфатическому узлу. Дойдя до края лимфатического узла, аккуратно проводят иглу в центр лимфатического узла (фиг. 4), поршнем шприца создают отрицательное давление и аккуратными движениями руки с амплитудой 2-4 мм набирают в просвет иглы и канюлю шприца морфологический материал. После забора материала шприц с иглой извлекают, полученный материал наносят на предметное стекло и материал направляют на цитологическое исследование.
После проведения процедуры необходимо оценить место пункции на наличие гематом и возможного повреждения плевры и развития пневмоторакса.
Клинические примеры
1. Пациентка М. 57 лет. При поступлении жалобы: активно не предъявляет.
Анамнез заболевания: Считает себя больной с августа 2018 года, когда при плановом проведении маммографии молочных желез выявлено узловое образование в левой молочной железе. Выполнена биопсия опухоли. Выявлен рак. Направлена в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России для дообследования и дальнейшего лечения. По данным ММГ от 09.2018 г.: в нижне-внутреннем квадранте определяется гиперденсное образование неправильной формы с нечетким контуром. Размеры образования составляют 1,7×1,2×1,3 см. Злокачественных кальцинатов нет. При УЗИ молочных желез, регионарных зон: в нижнем внутреннем квадранте определяется гипоэхогенное образование, неправильной формы, с нечеткими контурами 1,5×1,0 см. В подмышечных, под- и надключичных областях патологически измененных лимфоузлов не выявлено. Парастернальные лимфоузлы справа не визуализируются, слева визуализируются. В парастернальной области слева, во 2-м межреберье визуализируется гипоэхогенный лимфоузел размером 1,5×1,0×1,9 см с ровным, четким контуром, структура не сохранена, округлой формы, корковый слой не дифференцируется. При эластографии - жесткий. В 3-м межреберье визуализируется гипоэхогенный лимфоузел размером 1,5×1,5×0,9 см с ровным, четким контуром, структура не сохранена, округлой формы, корковый слой не дифференцируется. При эластографии - жесткий.
Гистологически: инвазивный рак НСТ G3 с выраженной лимфоидной инфильтрацией. Опухоль отрицательна по всем параметрам, по Ki67 80%. Тройной негативный рак.
Пациентке проведена ТИАБ парастернальных лимфатических узлов под УЗ-контролем по заявляемому способу.
Заключение: В полученном материале найденные изменения соответствуют код: 8010/6 Рак, метастатический.
После проведения ТИАБ по заявляемому способу осложнений не зарегистрировано.
Учитывая поражение парастернальных лимфатических узлов, стадия заболевания с Ia увеличилась до стадии IIIa, что согласно рекомендациям NCCN, предполагает на первом этапе лечения проведение курса полихимиотерапии.
2. Пациентка О. 57 лет.
При поступлении жалобы: активно не предъявляет.
Анамнез заболевания: В 2010 г. у пациентки диагностирован рак правой молочной железы. 15.12.2010 г. была выполнена радикальная резекция правой молочной железы. Гистологическое исследование №41783: инфильтративный дольковый рак 2 степени злокачественности с небольшими фокусами долькового рака in situ. ИГХ-исследование: РЭ - 6б, РП - 3б, Her-2/neu - 0, Ki - 25%. В п/о периоде проведено 4 курса ПХТ по схеме АС, была проведена ДЛТ на правую молочную железу РОД=2 Гр, СОД=50 Гр и "буст" на ложе удаленной опухоли 16 Гр. До 2016 г. принимала Тамоксифен 20 мг/сут. В феврале 2018 г. самостоятельно обнаружила образование в области п/о рубца. Обратилась в ФГБУ «НМИЦ онкологии имени Н.Н. Блохина» Минздрава России. ММГ+УЗИ от 22.02.2018 г.: правая молочная железа деформирована за счет операции. В области послеоперационного рубца - узловое образование с нечеткими контурами 2,3×1,6 см. Выполнена ТАБ образования, цитологическое заключение №2018/3900: рак. В отделении радиохирургии 13.03.2018 г. было выполнено оперативное вмешательство в объеме секторальной резекции правой молочной железы. Гистологическое заключение №9609/2018: инфильтративно-дольковый рак. ИГХ - РЭ 7, РП 3, Her-2/neu 3+, Ki67=46%. В послеоперационном периоде проведено лекарственное лечение 1-ый блок: 4 курса АС (адриабластин 60 мг/м2 + эндоксан 600 мг/м2) в/в капельно с предварительной премедикацией с интервалом три недели. Затем 2-ой блок: 4 курса - паклитаксел 80 мг/м2 в/в еженедельно 12 введений + герцептин первое введение 8 мг/кг, последующие 6 мг/кг раз в три недели до года.
После окончания химиотерапии выполнено ПЭТ КТ, где выявлено прогрессирование заболевания в виде рецидива процесса в молочной железе, метастазы в парастернальные л/у.
Выполнена ТИАБ парастернальных лимфоузлов по заявляемому способу.
Заключение: в полученном материале обнаруженные клетки соответствуют код: 8010/6 Рак, метастатический (парастернальные лимфоузлы). Пациентка обсуждена с химиотерапевтами, учитывая раннее прогрессирование после химиотерапии и на фоне герцептина, рекомендовано выполнение условно радикального лечения с последующей лучевой терапией.
В период 2017-2018 гг., нами проведено 42 тонкоигольные аспирационные биопсии парастернальных лимфоузлов. Ближайших и отдаленных осложнений после проведения процедуры не зафиксировано.
Таким образом, заявленный способ является малоинвазивным, исключает применение наркоза и риски послеоперационных осложнений, снижает риски травматического повреждения плевральной полости и внутренних грудных сосудов, позволяет в кратчайшие сроки, на дооперационном уровне получить морфологический материал и более точно установить стадию заболевания, что повышает эффективность лечения пациентов с диагнозом рак молочной железы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ вакуумно-аспирационной биопсии и удаления новообразований молочной железы | 2022 |
|
RU2790769C1 |
| Способ многоточечной 3-D тонкоигольной аспирационной биопсии в картированном сторожевом лимфатическом узле у больных раком молочной железы | 2024 |
|
RU2840202C1 |
| Способ проведения пункционной биопсии | 2016 |
|
RU2634040C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЛЬЦИТОНИНА И РАКОВО-ЭМБРИОНАЛЬНОГО АНТИГЕНА В ПУНКТАТЕ ОЧАГОВОГО ОБРАЗОВАНИЯ ПЕЧЕНИ | 2020 |
|
RU2736693C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛЕЧЕБНОЙ ТАКТИКИ ПРИ ДИФФЕРЕНЦИРОВАННОМ РЩЖ В СОЧЕТАНИИ С АУТОИММУННЫМ ТИРЕОИДИТОМ С УЗЛООБРАЗОВАНИЕМ | 2013 |
|
RU2522388C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОБРАЗОВАНИЙ ШЕИ | 2014 |
|
RU2581521C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СИГНАЛЬНЫХ ЛИМФАТИЧЕСКИХ УЗЛОВ У БОЛЬНЫХ РМЖ С ПОМОЩЬЮ КОЛЛОИДНЫХ РФП С РАЗЛИЧНЫМ ДИАМЕТРОМ ЧАСТИЦ | 2011 |
|
RU2469334C1 |
| СПОСОБ РАСШИРЕННОЙ РАДИКАЛЬНОЙ РЕЗЕКЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2326608C2 |
| СПОСОБ ПРОВЕДЕНИЯ ПОИСКА СИГНАЛЬНЫХ ЛИМФОУЗЛОВ ПРИ РАКЕ МОЛОЧНОЙ ЖЕЛЕЗЫ С ПРИМЕНЕНИЕМ УЛЬТРАЗВУКОВОЙ ВИЗУАЛИЗАЦИИ И ВНУТРИКОЖНОГО ПАРААРЕОЛЯРНОГО ВВЕДЕНИЯ ЭХОКОНТРАСТНОГО ПРЕПАРАТА "СОНОВЬЮ" | 2022 |
|
RU2813026C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ОРГАНОСОХРАНЯЮЩЕЙ ОПЕРАЦИИ ПУТЕМ ВАКУУМ-АССИСТИРОВАННОЙ БИОПСИИ ЛОЖА ОПУХОЛИ МОЛОЧНОЙ ЖЕЛЕЗЫ ПОСЛЕ ПРОВЕДЕННОЙ НЕОАДЪЮВАНТНОЙ ХИМИОТЕРАПИИ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ HER2-ЗАВИСИМОГО ИЛИ ТРИЖДЫ НЕГАТИВНОГО ПОДТИПА | 2023 |
|
RU2810795C1 |

Изобретение относится к медицине, а именно к онкологии, и может быть использовано для взятия тонкоигольной аспирационной биопсии парастернальных лимфатических узлов у больных раком молочной железы. Под УЗ-навигацией проводят послойную инфильтрационную анестезию кожи, подкожно-жировой клетчатки, грудных и межреберных мышц с соблюдением принципа «конец иглы следует за струей новокаина». После анестезии проводят процедуру тонкоигольной аспирационной биопсии, под УЗ-наведением. Для этого линейный датчик, устанавливают в межреберье, таким образом, чтобы выявленный измененный лимфатический узел был помещен на центр экрана. С помощью режима цветового допплеровского кодирования визуализируют внутренние грудные сосуды и выбирают оптимальную плоскость прохождения иглы в обход выявленных сосудов. Пункционную иглу располагают непосредственно по центру боковой поверхности УЗ-датчика, под углом 30-45 градусов к поверхности кожи. Медленным движением послойно проходят кожу и подкожно-жировую клетчатку, при этом на экране изображения должен появиться кончик иглы. Далее, контролируя направление конца иглы и корректируя угол проникновения, направляют иглу к выявленному лимфатическому узлу. Дойдя до края лимфатического узла, проводят иглу в центр лимфатического узла, поршнем шприца создают отрицательное давление в шприце и движениями руки с амплитудой 2-4 мм, набирают в просвет иглы и канюлю шприца морфологический материал, после чего извлекают шприц. Способ обеспечивает эффективное и безопасное получение морфологического материала у больных раком молочной железы за счет контроля за ходом биопсии. 4 ил., 2 пр.
Способ тонкоигольной аспирационной биопсии парастернальных лимфатических узлов под ультразвуковым контролем у больных раком молочной железы, отличающийся тем, что на первом этапе под УЗ-навигацией проводят послойную инфильтрационную анестезию кожи, подкожно-жировой клетчатки, грудных и межреберных мышц с соблюдением принципа «конец иглы следует за струей новокаина»; после анестезии проводят процедуру тонкоигольной аспирационной биопсии, под УЗ-наведением: линейный датчик, устанавливают в межреберье, таким образом, чтобы выявленный измененный лимфатический узел был помещен на центр экрана, с помощью режима цветового допплеровского кодирования визуализируют внутренние грудные сосуды и выбирают оптимальную плоскость прохождения иглы в обход выявленных сосудов; пункционную иглу располагают непосредственно по центру боковой поверхности УЗ-датчика, под углом 30-45 градусов к поверхности кожи; медленным движением послойно проходят кожу и подкожно-жировую клетчатку, при этом на экране изображения должен появиться кончик иглы; далее, контролируя направление конца иглы и корректируя угол проникновения, направляют иглу к выявленному лимфатическому узлу; дойдя до края лимфатического узла, проводят иглу в центр лимфатического узла, поршнем шприца создают отрицательное давление в шприце и движениями руки с амплитудой 2-4 мм, набирают в просвет иглы и канюлю шприца морфологический материал, после чего извлекают шприц.
| СПОСОБ БИОПСИИ СИГНАЛЬНОГО ЛИМФОУЗЛА У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2549488C1 |
| СПОСОБ ДИАГНОСТИКИ ВЫСОКОДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2546011C1 |
| RU 2011107861 A, 02.03.2011 | |||
| Способ проведения пункционной биопсии | 2016 |
|
RU2634040C1 |
| WO 2009153723 A1, 23.12.2009 | |||
| Пранаб Д | |||
| Аспирационная пункция тонкой иглой | |||
| Трактовка результатов и диагностические проблемы | |||
| М., 2014, с.20-23 | |||
| Синюкава Г.Н | |||
| и др | |||
| Современные возможности ультразвуковой томографии в оценке эффективности химиотерапии рака молочной железы | |||
| ВЕСТНИК РОНЦ ИМ | |||
| Н.Н | |||
| БЛОХИНА РАМН, 2004, т | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Цилиндрический сушильный шкаф с двойными стенками | 0 |
|
SU79A1 |
Авторы
Даты
2019-09-25—Публикация
2019-04-29—Подача