Изобретение относится к микробиологии и биотехнологии и касается получения штамма дрожжей Pichia pastoris, способного продуцировать бета-глюканазу (β-глюканазу).
β-глюканы представляют собой семейство полисахаридов, состоящих из мономеров D-глюкозы, соединенных посредством β-гликозидных связей и являются естественным компонентом клеточных стенок бактерий, грибов, дрожжей или злаков, таких как овес или ячмень. β-глюканы различного происхождения различаются структурой, уровнем разветвления и молекулярной массой, а также физико-химическими свойствами.
β- глюканазы - группа ферментов, катализирующих расщепление β-глюканов с β-1,2-, β-1,3-, β-1,4- и β-1,6-связями.
Важное значение среди ферментов, относящихся к этой группе имеют β-1,3-1,4-глюканазы, которые находят широкое применение, в частности, при производстве пищевых добавок [FEBS Lett., 1975, 52, 202-207], где их используют в качестве добавки к кормам сельскохозяйственных животных с однокамерным желудком.
Корм для домашних животных, смешанный с ферментами β-1,3-1,4-глюканазы и ксиланазы, усиливает увеличение веса, потребление корма и усвояемость азота (+5,6%) и липидов (+6,2%), а также уменьшает образование липкого помета, что существенно уменьшает санитарные проблемы [Trends in Biotechnology, 1993, 11 (10), 424-430].
Природными источниками β-глюканаз являются различные микроорганизмы: бактерии, грибы, дрожжи и актиномицеты
Большинство кормовых ферментных препаратов, в состав которых входят β-глюканазы, имеют грибное происхождение. Однако, большой интерес представляет разработка рекомбинантных продуцентов ферментов на основе дрожжей, поскольку они более удобны для проведения генно-инженерных работ и быстрее накапливают целевой фермент в сравнении с грибными продуцентами.
Существенным преимуществом дрожжевых продуцентов является также то, что на их основе значительно легче создавать продуценты моноферментов, тогда как грибные продуценты обычно синтезируют комплексы целлюлитических ферментов. Промышленное получение моноферментов позволяет более эффективно решать задачи составления оптимальной композиции ферментов при использовании различных субстратов.
В настоящее время наиболее перспективным является создание продуцентов на основе рекомбинантных штаммов метилотрофных дрожжей рода Pichia, Komagataella или Hansenula [J Ind Microbiol Biotechnol 2009, 36: 1435-1438],
Использование метилотрофных дрожжей позволяет достичь высоких скоростей экспрессии гетерологичных белков с высокой плотностью клеток, а также высокого уровня и качества N-гликозилирования белков.
Особенно часто для высокоуровневой экспрессии геретологичных белков используют метилотрофные дрожжи Pichia pastoris [FEMS Microbiol.Rev., 2000, 24,45-66].
Показано [J. Ind. Microbiol. Biotechnol., 2012 39(6), 869-876], что ген bgl16C1 из Penicillium pinophilum, кодирующий эндо-1,3(4)-β-D-глюканазу, эффективно экспрессируется в клетках дрожжей Pichia pastoris, при этом активность рекомбинантной бета-глюканазы в культуральной жидкости при культивировании в 15-литровом ферментере составляет 28721 ед/мг.
Известны также рекомбинантные штаммы Pichia pastoris, продуцирующие термостабильную β-1,3-1,4-глюканазу из Bacillus amyloliquefaciens. [CN101899458]
В работе [Биотехнология, 2018, Т. 34, №5, С. 12-22] описан ген bgl из Bacillus pumilus, кодирующий бета-глюканазу, относящуюся к классу эндо-β-1,3(4)-D-глюканаз (Е.С. 3.2.1.6).
Поскольку гены β-глюканаз различного происхождения экспрессируются в дрожжах Pichia pastoris с различной эффективностью [Биотехнология, 2018, 34(4), 26-36], для конструирования эффективных продуцентов важным является выбор генов, кодирующих β-глюканазу и эффективно работающих в дрожжах Pichia pastoris.
Для создания промышленно значимых продуцентов ведут поиск новых высокоактивных β-глюканаз, обладающих свойствами, необходимыми для их индустриального использования и способных эффективно выражаться в дрожжах.
Задачей заявляемого изобретения является расширение арсенала рекомбинантных микроорганизмов, продуцирующих β-глюканазу.
Задача решена путем получения рекомбинантного штамма дрожжей Pichia pastoris ВКПМ Y-4463, продуцирующего β-глюканазу, содержащего ген bgl, кодирующий эндо-β-1,3(4)-D-глюканазу из Bacillus pumilus.
Заявляемый рекомбинантный штамм дрожжей Pichia pastoris получен путем интеграции в состав хромосомы штамма дрожжей Pichia pastoris (His4-) экспрессионной кассеты, в состав которой входит ген bgl из Bacillus pumilus.
Штамм является продуцентом эндо-β-1,3(4)-D-глюканазы и депонирован во Всероссийской Коллекции Промышленных Микроорганизмов (ВКПМ) НИЦ «Курчатовский институт» - ГосНИИгенетика как Pichia pastoris ВКПМ Y-4463.
Культурально-морфологические характеристики полученного штамма:
При культивировании при температуре 28°C в течение 48 часов на агаризованной среде YP состава (мас. %: пептон-2, дрожжевой экстракт - 1, агар - 2, вода - остальное) с добавлением глюкозы (2 мас. %), клетки имеют овальную форму, 3-4 мкм в диаметре. Клетки почкуются, при этом почкование истинное, многостороннее. Истинного мицелия не образуют.
Споруляция происходит при инкубации культуры на агаризованной среде следующего состава (мас. %): хлорид калия - 1.0, ацетат натрия - 0.5, глюкоза - 1.0, агар - 2.0, вода - остальное. Аски имеют тетраэдрическую форму, включают 4 аскоспора.
На агаризованной среде YP с добавлением глюкозы (2 мас. %) колонии светло-бежевого цвета с ровным краем, матовой поверхностью, линзовидным профилем и пастообразной консистенцией.
При росте в жидкой среде YP (мас. %: пептон-2, дрожжевой экстракт-1, вода - остальное) с добавлением глюкозы (мас.2%) при 28°С в течение 24 ч культивирования - жидкость мутная, осадок белый, коагуляции не наблюдается, пристеночных пленок не образует.
Физиолого-биохимические признаки полученного штамма:
Штамм способен к росту, как в аэробных, так и в анаэробных условиях.
В качестве единственного источника углерода способен использовать метанол, этанол, глюкозу, глицерин, лактат, сукцинат, не способен ассимилировать мальтозу, сахарозу, ацетат, крахмал, лактозу.
При культивировании в присутствии метанола штамм способен синтезировать β-глюканазу.
Изобретение проиллюстрировано следующими фигурами.
Фиг. 1. Экспрессионная кассета 1
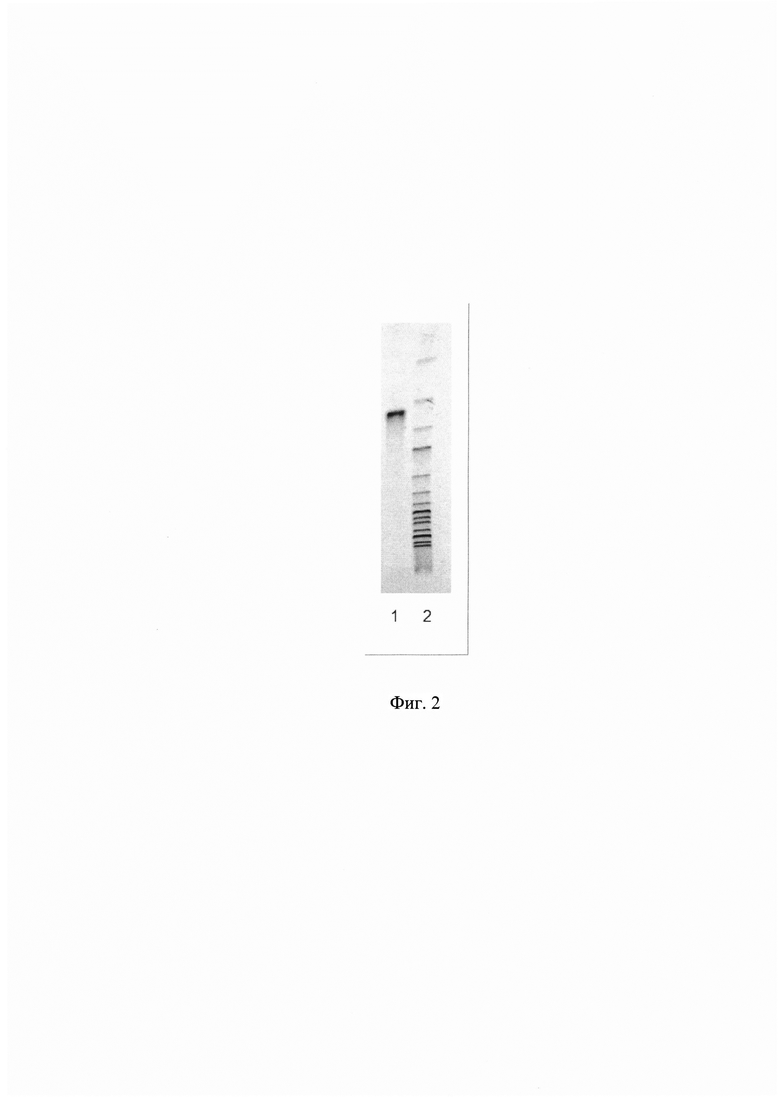
Фиг. 2 Электрофорез гена bgl Bacillus pumilus
Изобретение подтверждено следующими примерами.
Пример 1. Конструирование штамма дрожжей Pichia pastoris, несущего ген bgl из Bacillus pumilus
Получают плазмидный вектор pPIC-bglPum, содержащий интегративную экспрессионную кассету.
В качестве источника гена bgl используют тотальную геномную ДНК штамма Bacillus pumilus Bg57 ВКПМ В-13195. [Биотехнология, 2018, Т. 34, №5, С. 12-22] Синтезируют ДНК гена bgl методом ПЦР с использованием праймеров bgl-pum-1 и bgl-pum-2, содержащих на 5'-концах сайты рестрикции для клонирования - EcoRI и NotI, соответственно:
bgl-pum-1 5'-aagaattccaaacgggcgggtcgttttatga-3'
bgl-pum-2 5'- aagcggccgcttatctttttgtgtaacgca-3'
Полученный фрагмент ДНК обрабатывают рестриктазами EcoRI и NotI и клонируют в состав экспрессионного вектора pPIC9
(http://www.thermofisher.com/order/catalog/product/V17520).
В состав экспрессионного плазмидного вектора pPIC-bglPum входят следующие генетические элементы:
1. Ген bgl_Bacillus pumilus, встроенный в единую рамку считывания с нуклеотидной последовательностью сигнального пептида α-фактора, под контролем AOX1 промотора
2. Терминатор транскрипции TTAOX1
3. Дрожжевой селективный маркер His4
4. Область интеграции - нуклеотидная последовательность гена АОХ1
5. Селективный маркер для клеток Е.coli - ген bla, кодирующий β-лактамазу, придающий клеткам устойчивость к ампициллину.
6. Бактериальный pUC origin.
Для получения интегративной экспрессионной кассеты 1 (фиг. 1) плазмиду pPIC-bglPum обрабатывают эндонуклеазой рестрикции BglII.
Полученную интегративную экспрессионную кассету трансформируют в клетки штамма Pichia pastoris (His4-), которые предварительно выращивают в жидкой питательной среде YP с добавлением глюкозы (мас. 2 %) до концентрации 1×108 клеток на 1 мл. Клетки центрифугируют, промывают в ледяной стерильной воде, а затем в ледяном растворе 1М сорбитола. Промытые клетки инкубируют в 25 мМ растворе дитиотрейтола в течение 15 минут, затем промывают в ледяном растворе 1М сорбитола. Обработанные таким образом клетки ресуспендируют в ледяном растворе 1 М сорбитола в концентрации 1-5×109 клеток на 1 мл. Аликвоту, объемом 40 мкл клеточной суспензии, переносят в охлажденный эппендорф, добавляют 400 нг ДНК экспрессионной интеграционной кассеты, и инкубируют во льду 5 минут. Смесь клеток и ДНК переносят в предварительно охлажденную кювету для электропорации. Электропорацию проводят при следующих условиях: 1,5 кВ, 400 Ом, 25uF. После порации добавляют 1 мл ледяного раствора 1М сорбитола.
Селекцию трансформантов ведут на агаризованной среде YNB (HiMedia Laboratories Pvt. Limited, Индия) с добавлением глюкозы (2 мас. %) в течение 5 суток при температуре 30°С.
Для отбора наиболее продуктивных трансформантов проводят их культивирование в жидкой ферментационной питательной среде YP с добавлением метанола (3 мас. %) в 96-луночных планшетах при 30°С в течение 72 ч на качалке (250 об/мин). В качестве контроля используют штамм Pichia pastoris (His4-)
Определение активности β-глюканазы в культуральной жидкости проводят с использованием ДНС метода [Anal. Chem., 1959, 31 (3), 426-428] в 96-луночном планшете следующим образом. В каждой лунке смешивают 25 мкл 1% раствора субстрата β-глюкана ячменя в 0,5 М ацетатном буфере (рН 6) и 25 мкл культуральной жидкости. Инкубацию проводят при 50°С 10 минут, после чего добавляют в лунку 50 мкл раствора ДНС. Планшет прогревают при 99°С 10 минут и измеряют оптическую плотность окрашенного раствора при длине волны 546 нм. В качестве стандарта используют раствор глюкозы.
По результатам ферментации отбирают наиболее продуктивный трансформант №123, который при культивировании в планшете синтезирует β-глюканазу в количестве 118 ед/мл культуральной жидкости. Трансформант депонирован во Всероссийской Коллекции Промышленных Микроорганизмов (ВКПМ) НИЦ «Курчатовский институт» - ГосНИИгенетика как Pichia pastoris_ВКПМ Y-4463.
Для подтверждения наличия в хромосоме штамма вставки гена bgl Bacillus pumilus методом полимеразной цепной реакции (ПЦР) используют хромосомальную ДНК, выделенную из клеток штамма Pichia pastoris_ВКПМ Y-4463 и специфические праймеры BglPum-f и BglPum-r
BglPum -f 5'-ggttatgtgttctgggaacctc-3',
BglPum-r 5'-ttatctttttgtgtaacgca-3'
Режим реакции ПЦР:
95°С - 3 мин - 1 цикл
30 циклов:
95°С - 30 сек.
60°С - 30 сек.
72°С - 60 сек.
72°С - 5 мин. - 1 цикл
Для контроля величины амплифицированного фрагмента ДНК при электрофорезе использован молекулярный маркер GeneRuler 1 kb DNA Ladder (Fermentas) (линия 2, фиг. 2, размер фрагментов снизу вверх 10000, 8000, 6000, 5000, 4000, 3500, 3000, 2500, 2000, 1500, 1000, 750, 500, 250 п.н.). Наработка фрагмента ДНК размером 642 п.н. (линия 1 фиг. 2) свидетельствует о присутствии в хромосоме штамма вставки гена bgl Bacillus pumilus
Пример 2. Продукция фермента β-глюканазы заявляемым штаммом Pichia pastoris ВКПМ Y-4463
Посевную культуру выращивают в пробирках (50 мл) с 10 мл жидкой питательной среды YP с добавлением глюкозы (2 мас. %) при 30°С в течение 24 ч на качалке (250 об/мин). Посев ферментационной среды осуществляют в соотношении 1/10.
Ферментацию проводят при 30°С на качалке (250 об/мин) в питательной среде состава (мас. %): дрожжевой экстракт - 0,5, пептон - 1, вода - остальное с добавлением глюкозы (1 мас. %) в пробирках (50 мл) с рабочим объемом 5 мл. Через 18 часов добавляют метанол (1 мас. %) Ферментацию продолжают в течение 72 часов, добавляя метанол (1 мас. %) через каждые 24 часа. После окончания ферментации определяют количество фермента β-глюканазы в культуральной жидкости с использованием ДНС метода.
Через 72 часа ферментации количество фермента составило 618 ед/мл культуральной жидкости.
| название | год | авторы | номер документа |
|---|---|---|---|
| Трансформант дрожжей Pichia pastoris, продуцирующий бета-глюканазу | 2019 |
|
RU2720914C1 |
| Штамм дрожжей Komagataella kurtzmanii, продуцирующий бета-глюканазу из Bacillus pumilus и бета-глюканазу из Paenibacillus jamilae | 2019 |
|
RU2736441C1 |
| Рекомбинантный штамм дрожжей Komagataella kurtzmanii - продуцент бета-глюканазы | 2018 |
|
RU2701640C1 |
| Трансформант дрожжей Komagataella kurtzmanii, продуцирующий бета-глюканазу | 2019 |
|
RU2722563C1 |
| Рекомбинантный штамм дрожжей Komagataella kurtzmanii - продуцент бета-глюканазы из Paenibacillus jamilae | 2019 |
|
RU2730577C1 |
| Дрожжи Komagataella kurtzmanii - рекомбинантный продуцент бета-глюканазы | 2019 |
|
RU2736440C1 |
| Штамм дрожжей Pichia pastoris, продуцирующий ксиланазу из Paenibacillus brasilensis | 2019 |
|
RU2728243C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris - продуцент ксиланазы из Pyromyces finnis | 2019 |
|
RU2725475C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris - продуцент ксиланазы | 2018 |
|
RU2701308C1 |
| Трансформант дрожжей Pichia pastoris, продуцирующий эндо-1,4-β-ксиланазу из Paenibacillus brasilensis | 2019 |
|
RU2728033C1 |

Изобретение относится к микробиологии и биотехнологии. Предложен рекомбинантный штамм дрожжей Pichia pastoris ВКПМ Y-4463, продуцирующий β-глюканазу. Указанный штамм содержит ген bgl, кодирующий эндо-β-1,3(4)-D-глюканазу из Bacillus pumilus. Штамм продуцирует β-глюканазу в количестве 618 ед./мл культуральной жидкости. 2 ил., 2 пр.
Рекомбинантный штамм дрожжей Pichia pastoris ВКПМ Y-4463, содержащий ген bgl, кодирующий эндо-β-1,3(4)-D-глюканазу из Bacillus pumilus - продуцент β-глюканазы.
| БОРЩЕВСКАЯ Л.Н | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| Биотехнология, 2018, Т.34, N | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| CHEN X | |||
| ET AL | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| CN 101899458 A, 01.12.2010 | |||
| KAWAI R | |||
| ET AL | |||
| Устройство двукратного усилителя с катодными лампами | 1920 |
|
SU55A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2019-09-26—Публикация
2018-12-19—Подача