ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к органической химии, фармакологии и медицине, в частности, к веществам бензодиазепинового ряда, которые могут применяться для лечения болевых синдромов (анальгетики), регуляции веса, лечения психических расстройств, навязчивых состояний, страха и других нарушений функций центральной нервной системы.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Производные 1,4-бензодиазепинов широко используются в медицинской практике, поскольку обладают снотворным, седативным, анксиолитическим, миорелаксирующим и противосудорожным действием. Так, более 50 фармацевтических субстанций на основе 1,4-бензодиазепинов входят в состав лекарственных средств, которые используются для профилактики и лечения различных расстройств центральной нервной системы в качестве анксиолитиков (транквилизаторов), а также снотворных и противосудорожных средств.
За последние 20 лет в химии и фармакологии 1,4-бензодиазепинов достигнут значительный прогресс: синтезировано большое число новых соединений - лигандов бензодиазепиновых сайтов ГАМКА-рецепторов, некоторые из которых обладают не только анксиолитическими, но также и анальгетическими, анорексигенными, антидепрессантными, антигипоксическими, ноотропными и др. свойствами.
В частности, обнаружено, что производные 1,4-бензодиазепинов, которые содержат в третьем положении амидные остатки, проявляют значительную анальгетическую активность и высокий аффинитет к рецепторам брадикинина - сильного природного альгогена [1, 2].
Известно также, что некоторые 3-замещенные-1,2-дигидро-3Н-1,4-бензодиазепин-2-оны проявляют как анальгетическую, так и анорексигенную, антидепрессивную, антигипоксическую, ноотропную и другие виды активности. Фармакологические свойства этих соединений опосредованы их связыванием с бензодиазепиновыми, холецистокининовыми, брадикининовыми рецепторами [3, 4, 5, 6, 7].
Синтез новых производных 1,4-бензодиазепинов открывает, таким образом, перспективы создания новых лекарственных средств, нацеленных на решение актуальных медицинских проблем: снятия болевых синдромов, регуляции веса, лечения различных нарушений центральной нервной системы.
Так, хронические боли различного генеза, а также сопровождающие их депрессия, тревога, бессонница, представляют собой серьезную медицинскую и социальную проблему. Современные анальгетические препараты или недостаточно эффективны (в случае применения нестероидных противовоспалительных средств), или имеют опасные побочные эффекты, особенно выраженные при применении наркотических анальгетиков.
Более миллиарда людей в мире страдают от избыточного веса и ожирения [8], что представляет собой серьезную медицинскую проблему, поскольку увеличивается риск развития диабета, сердечно-сосудистых и других заболеваний. С другой стороны, информационная пропаганда похудения, отсутствие аппетита, резкое снижение массы тела при таких заболеваниях, как туберкулез, опухолевые процессы, СПИД, приводит к увеличению числа людей, страдающих анорексией [9]. В связи с этим растет интерес к проблеме регуляции веса и пищевого поведения.
Одной из актуальных задач современной фармакологии также является поиск лекарственных средств, повышающих продолжительность жизни и выживаемость человека в условиях острой гипоксии. Имеющийся арсенал лекарственных средств - антигипоксантов и ноотропов, не полностью отвечает требованиям практической медицины.
Высоко актуальной остается проблема лечения депрессий. Наблюдается количественный рост распространенности депрессивных расстройств в популяции, рост «стертых» форм с соматовегетативной окраской. По данным ВОЗ, в мире у более чем 110 млн. человек (3-6% популяции) выявлены те или иные клинически значимые проявления депрессии.
Наиболее близким к заявляемым соединениям - производным 1,4-бензодиазепин-2-она по химической структуре и фармакологическому действию прототипом является метил-2-(7-бром-3-этокси-2-оксо-5-фенил-2,3-дигидро-1H-бензо[е][1,4]диазепин-1-ил)ацетат, проявляющий анальгетическую активность в тесте "уксуснокислые корчи" с ЕД50=0,47±0,15 мг/кг [10]:
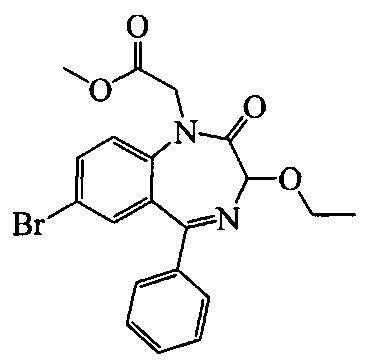
Аналогами заявляемых соединений - производных 1,4-бензодиазепин-2-она по отдельным видам фармакологической активности являются: диклофенак натрия, проявляющий анальгетическую активность в тесте "уксуснокислые корчи" с ЕД50=10,0±1,8 мг/кг; гормон лептин, который снижает аппетит и массу тела, но не обладает антигипоксической и антидепрессивной активностью; антидепресант амитриптилин, обладающий высоким антидепрессивным эффектом, но не проявляющий антигипоксического действия и не влияющий на аппетит.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В основу изобретения поставлена задача - расширить спектр фармакологически активных бензодиазепиновых соединений за счет 3-замещенных 1,2-дигидро-3Н-1,4-бензодиазепин-2-онов общей формулы I:

как потенциальных лекарственных средств, обладающих анальгетической активностью, регулирующих аппетит и вес, обладающих антигипоксическими, ноотропными, антидепрессивными и анксиолитическими свойствами.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Поставленная задача реализована синтезом 3-замещенных 1,2-дигидро-3Н-1,4-бензодиазепин-2-онов общей формулы I, включая синтез вариантов:
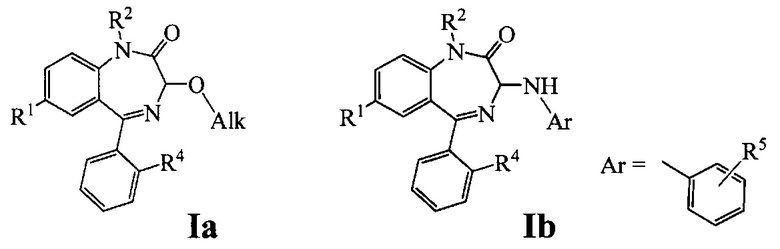
а) 1-замещенных 3-алкокси-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов, общей формулы Ia;
б) 1-замещенных 3-ариламино-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов общей формулы Ib.
Пример 1
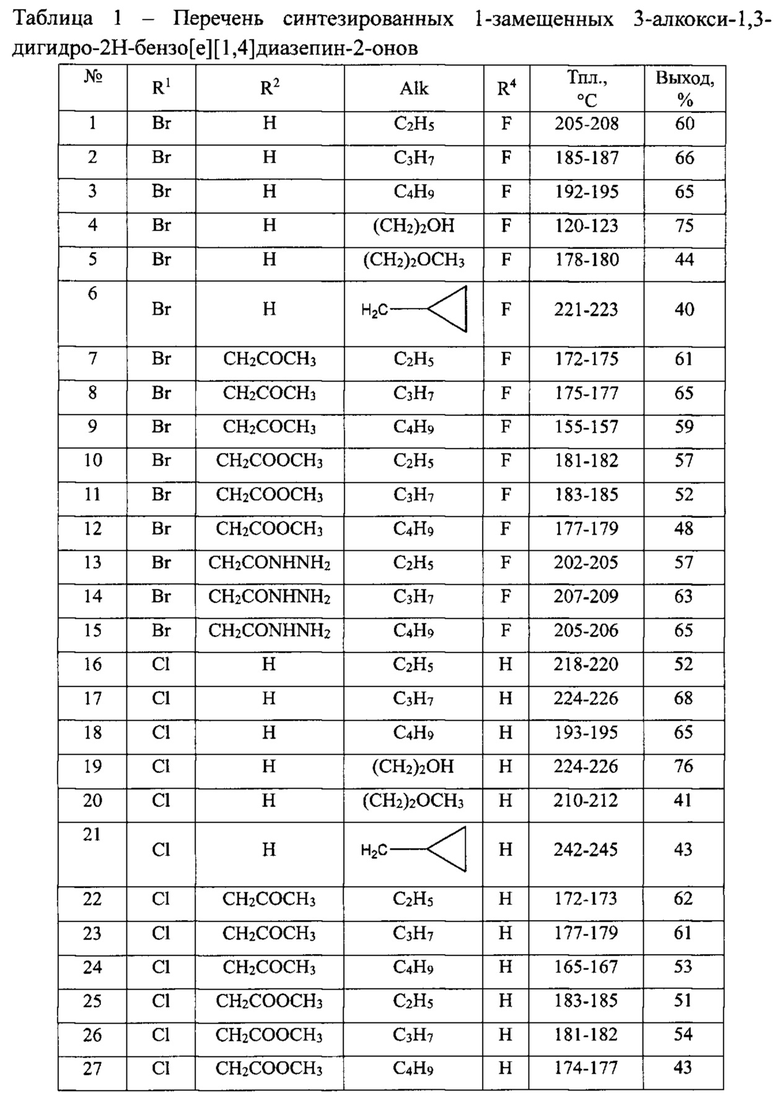
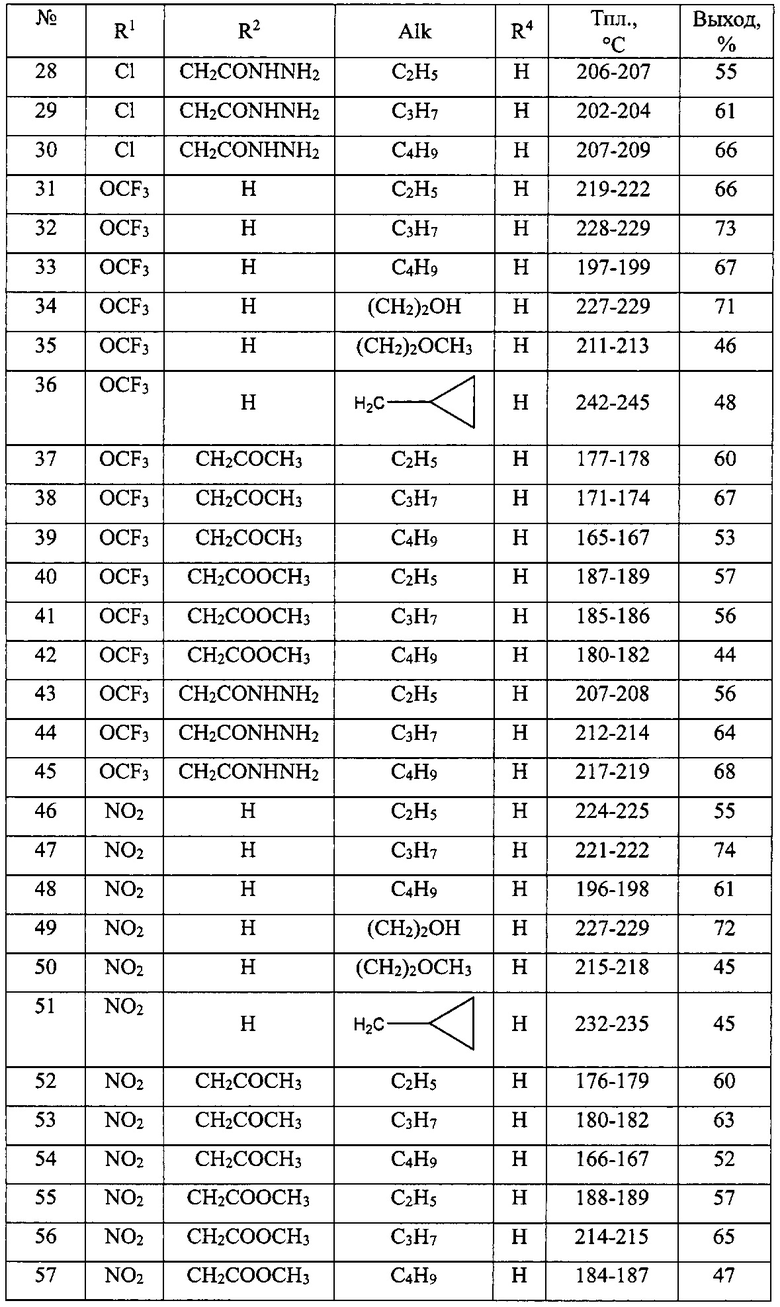
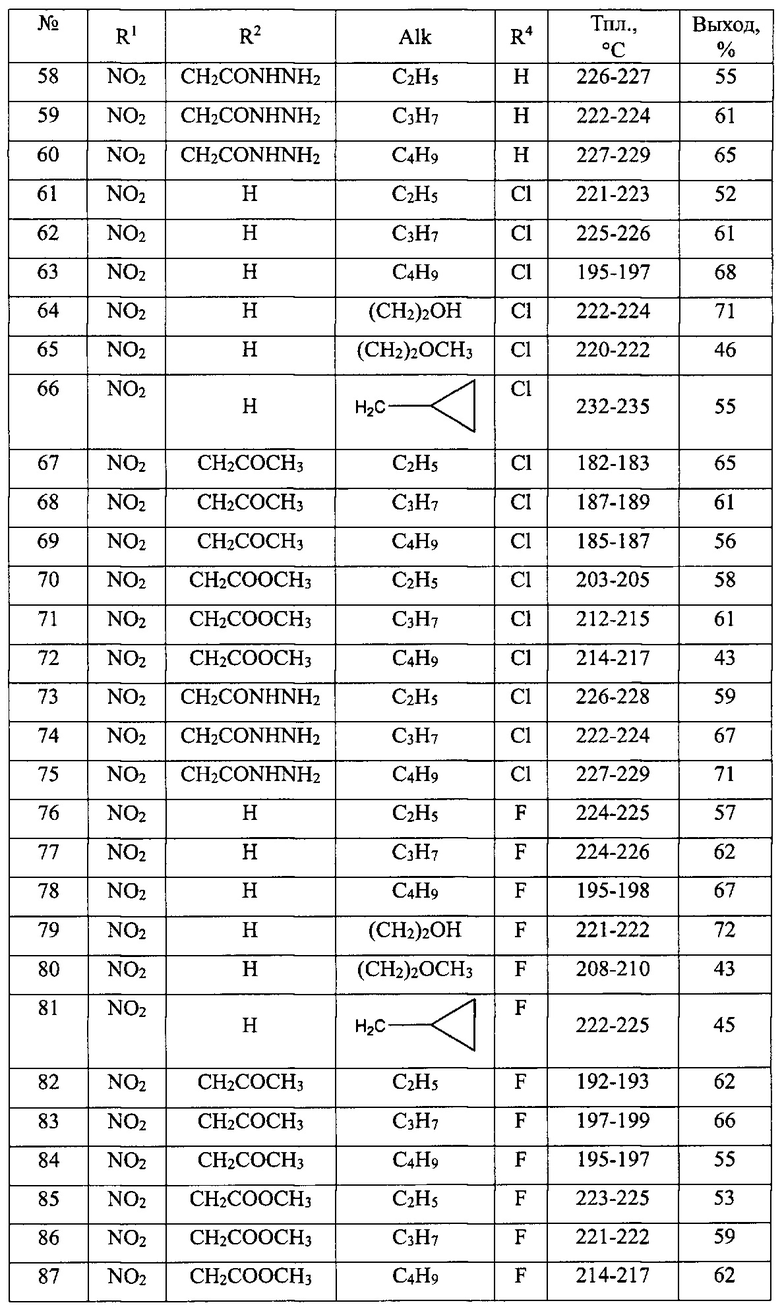
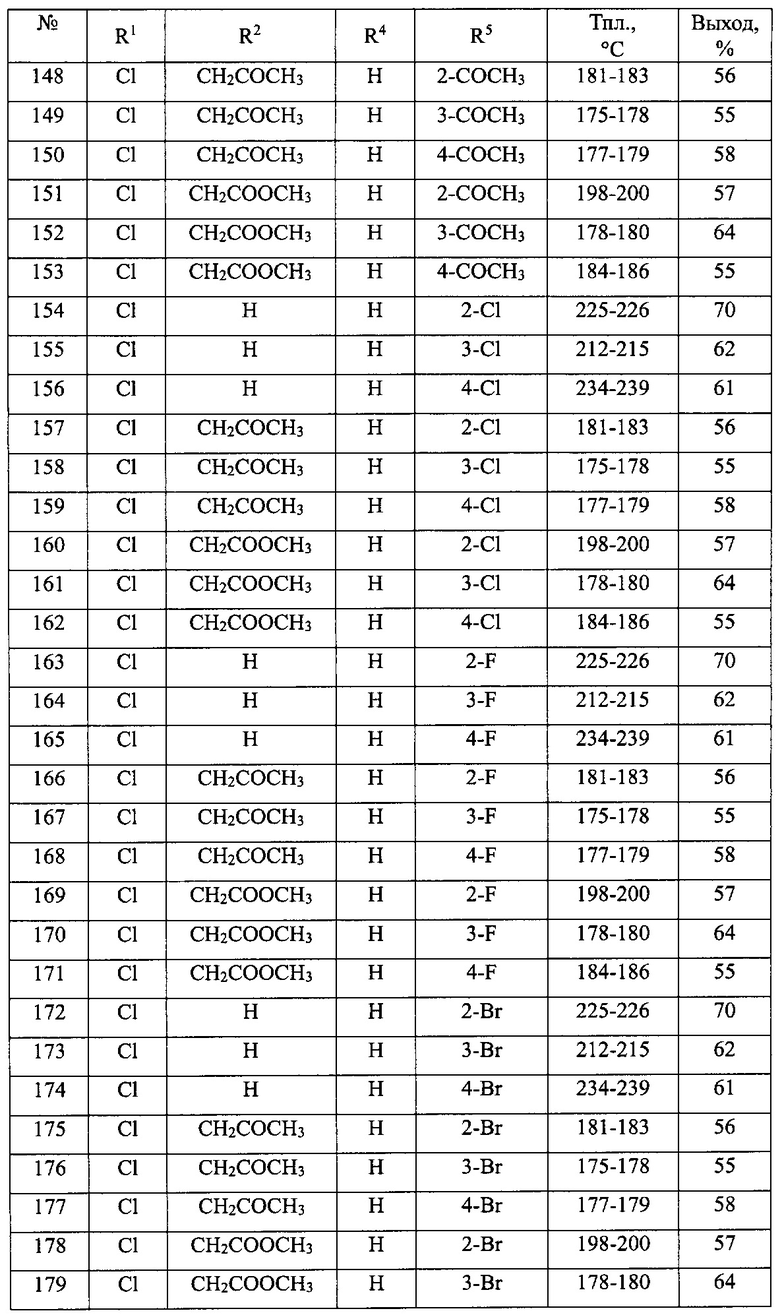
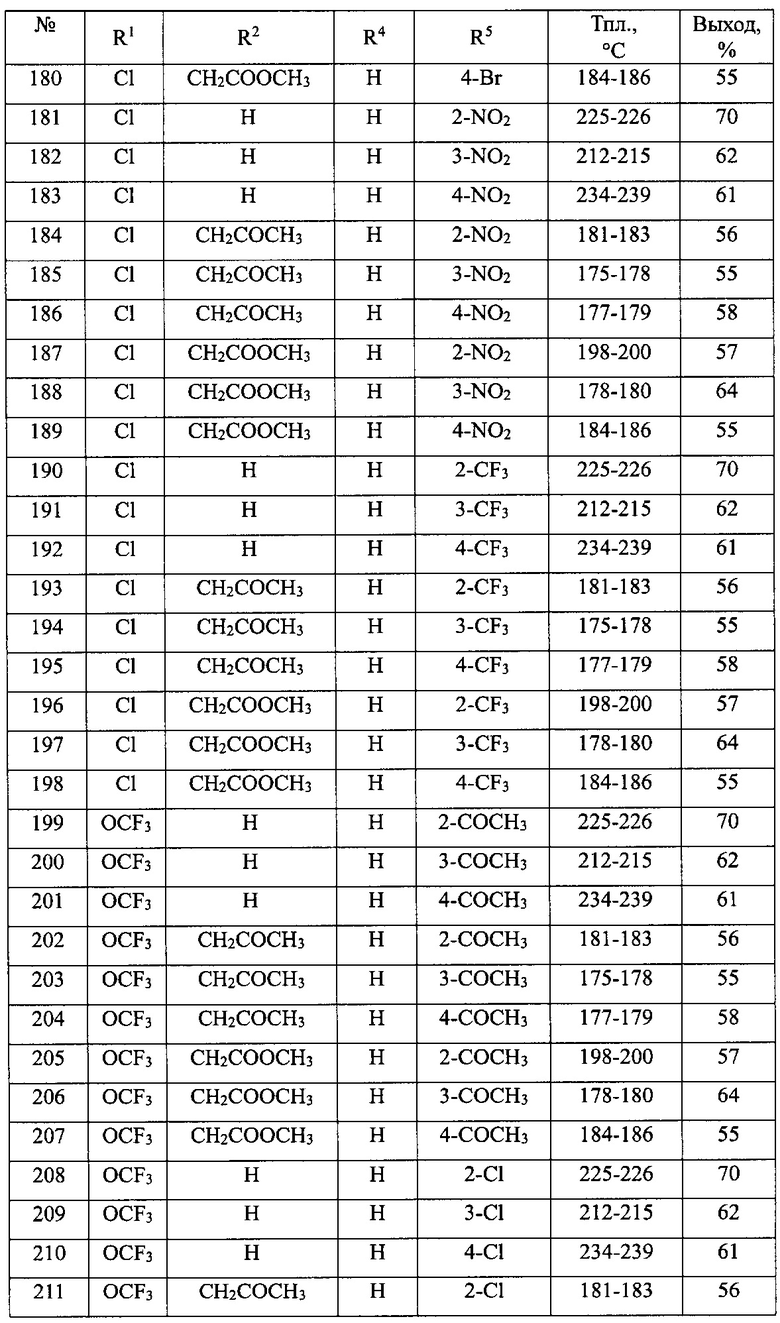
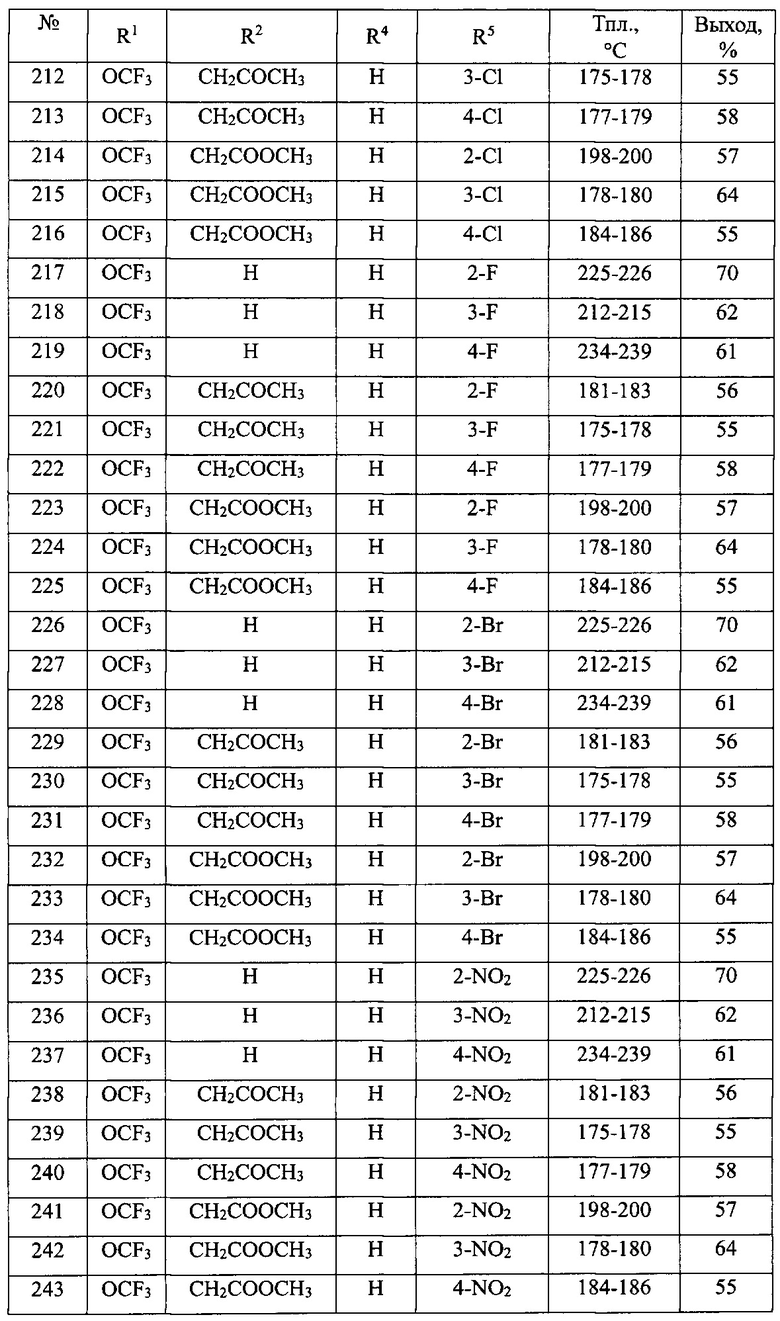
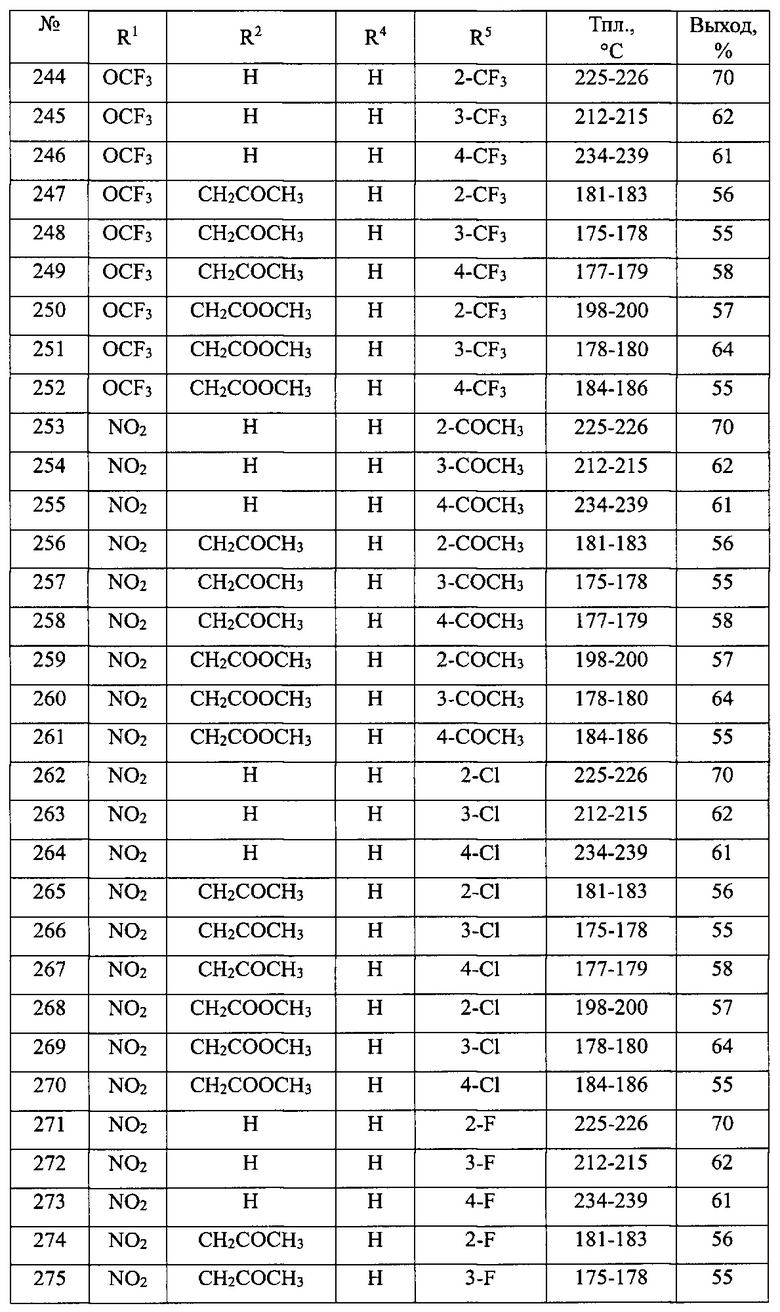
В таблице 1 приведен перечень синтезированных 1-замещенных 3-алкокси-1,3-дигидро-2Н-бензо[е][1,4]диазепин-2-онов(Ia).
Общая методика синтеза 1-замещенных 3-алкокси-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов(Ia) (№№1-90 табл. 1)
7-Нитро-5-фенил-3-пропокси-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-он (№47 табл. 1).
В колбу на 100 мл помещают 1 г (3,367 ммоль) 3-гидрокси-7-нитро-5-фенил-1,3-дигидро-2Н-бензо[е][1,4]диазепин-2-она, приливают 50 мл хлороформа безводного и прибавляют 1,0 мл (13,78 ммоль) тионилхлорида, кипятят 40 мин, осадок растворяется, затем приливают 5 мл безводного 1-пропанола. Кипятят 1 час. Реакционную смесь промывают водой (5×5 мл), хлороформ упаривают в ротационном испарителе. Осадок кристаллизуют из ксилола. Выход = 79%, (0,9 г); Тпл=220-222°C.
Метил-2-(7-нитро-2-оксо-5-фенил-3-пропокси-2,3-дигидро-1H-бензо[е][1,4]ди-азепин-1-ил)ацетат (№56 табл. 1)
В колбу на 100 мл помещают 1 г (3,367 ммоль) 7-нитро-5-фенил-3-пропокси-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-она (№47 табл. 1), приливают 40 мл диоксана и 20 мл насыщенного раствора поташа, прибавляют 10 мг тетрабутиламмоний иодида, затем приливают 1,5 мл (15,78 ммоль) метилбромацетата. Реакционную смесь перемешивают при комнатной температуре 2-3 часа. Диоксан отделяют на делительной воронке и упаривают в ротационном испарителе. Осадок кристаллизуют из ксилола. Выход = 65,0%, (0,9 г); Тпл=214-215°C белые игольчатые кристаллы с желтоватым оттенком. Аналогично получают соединения (№№1-46, 48-55, 57-90 табл. 1).
Пример 2
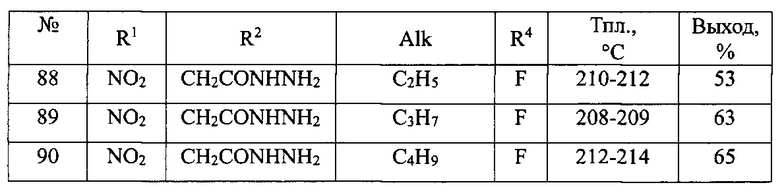
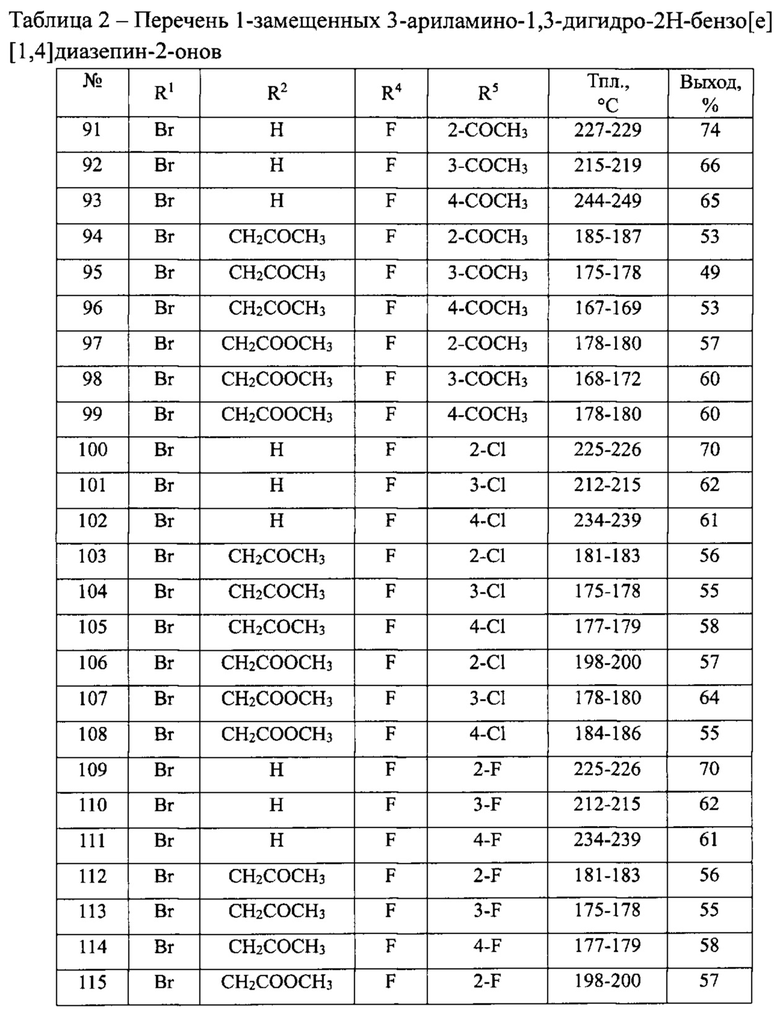
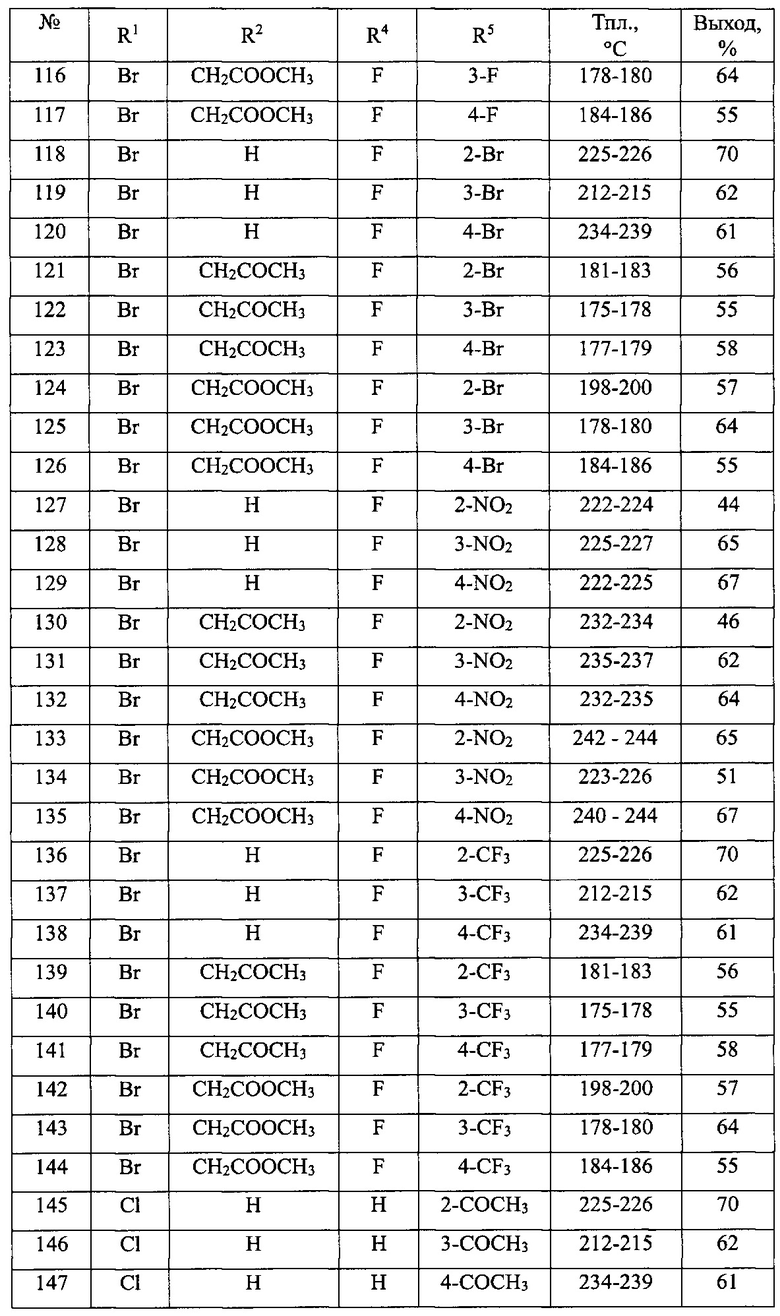
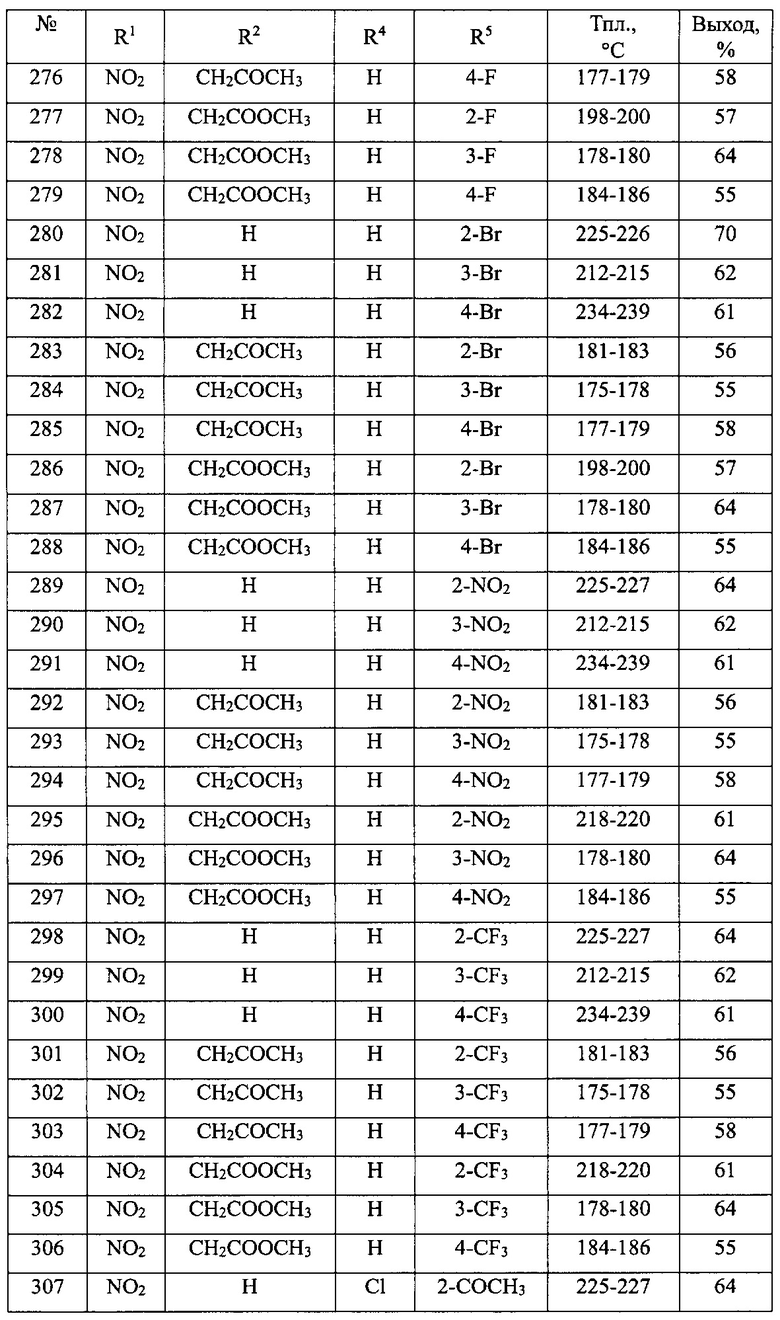
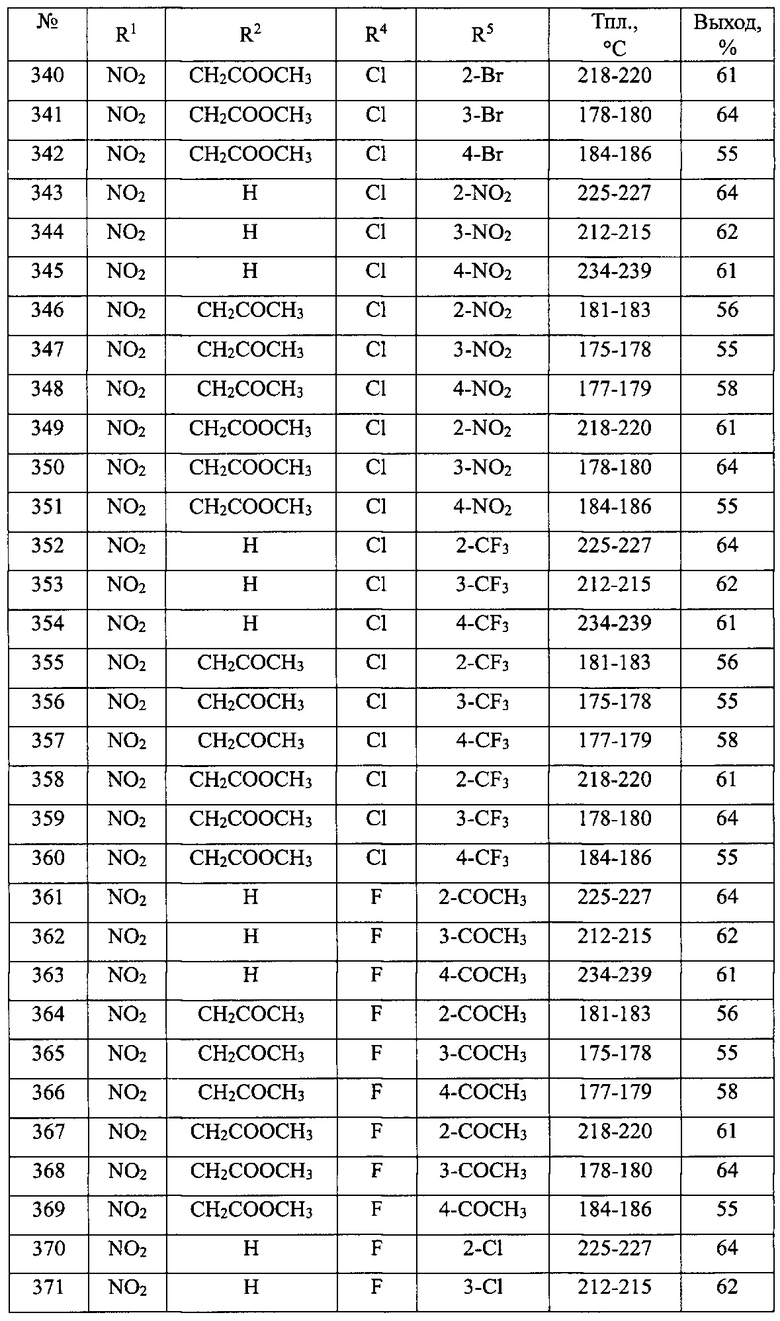
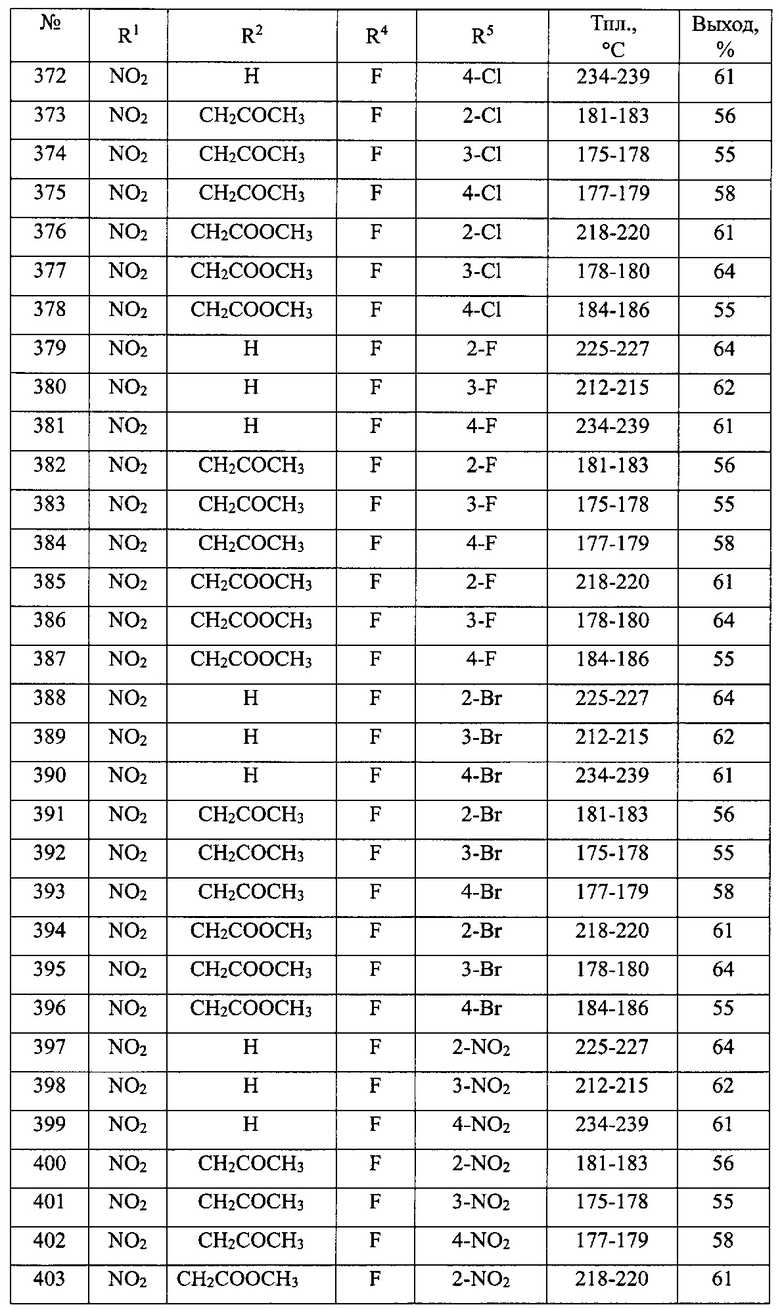
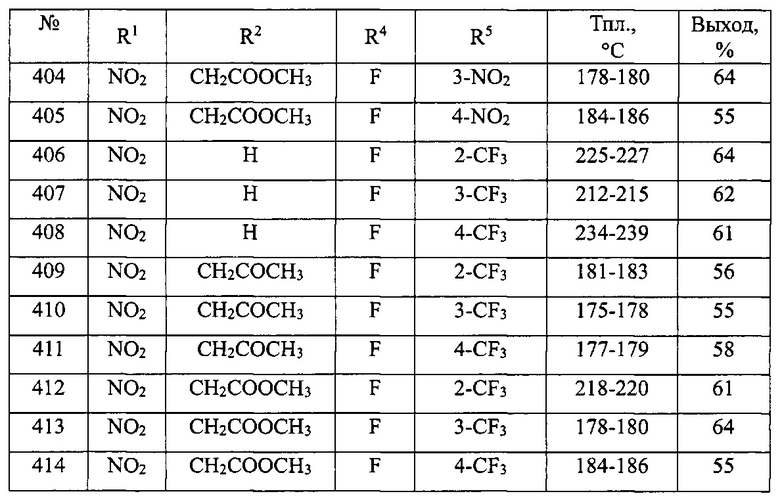
В таблице 2 приведен перечень 1-замещенных 3-ариламино-1,3-дигидро-2Н-бензо[е][1,4]диазепин-2-онов(Ib).
Общая методика синтеза 1-замещенных 3-ариламино-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов(Ib) (№№91-414 табл. 2)
7-Нитро-5-фенил-3-(2-нитрофенил)амино-1,3-дигидро-2H-бензо[е][1,4]диазе-пин-2-он (№289 табл. 2).
В колбу на 100 мл помещают 1 г (3,364 ммоль) 3-гидрокси-7-нитро-5-фенил-1,3-дигидро-2Н-бензо[е][1,4]диазепин-2-она, приливают 50 мл хлороформа безводного и прибавляют 1,0 мл (13,78 ммоль) тионилхлорида, кипятят 40 мин, осадок растворяется, затем прибавляют 0,93 г (6,73 ммоль) 2-нитроанилина. Кипятят 1 час. Реакционную смесь промывают водой (5×5 мл), хлороформ упаривают в ротационном испарителе. Осадок кристаллизуют из этилового спирта. Выход = 64%, (0,9 г); Тпл=225-227°C.
Метил-2-(7-нитро-2-оксо-5-фенил-3-(2-нитрофенил)амино-2,3-дигидро-1H-бензо[е][1,4]ди-азепин-1-ил)ацетат (№295 табл. 2)
В колбу на 100 мл помещают 1 г (3,367 ммоль) 7-нитро-5-фенил-(2-нитрофенил)амино-1,3-дигидро-2H-бензо[е] [1,4] диазепин-2-она (№289 табл. 2), приливают 40 мл диоксана и 20 мл насыщенного раствора поташа, прибавляют 10 мг тетрабутиламмоний иодида, затем приливают 1,5 мл (15,78 ммоль) метилбромацетата. Реакционную смесь перемешивают при комнатной температуре 2-3 часа. Диоксан отделяют на делительной воронке и упаривают в ротационном испарителе. Осадок кристаллизуют из ксилола. Выход = 65,0%, (0,9 г); Тпл=218-220°C желтые кристаллы. Аналогично получают соединения (№№91-288, 289-294, 296-414 табл. 2).
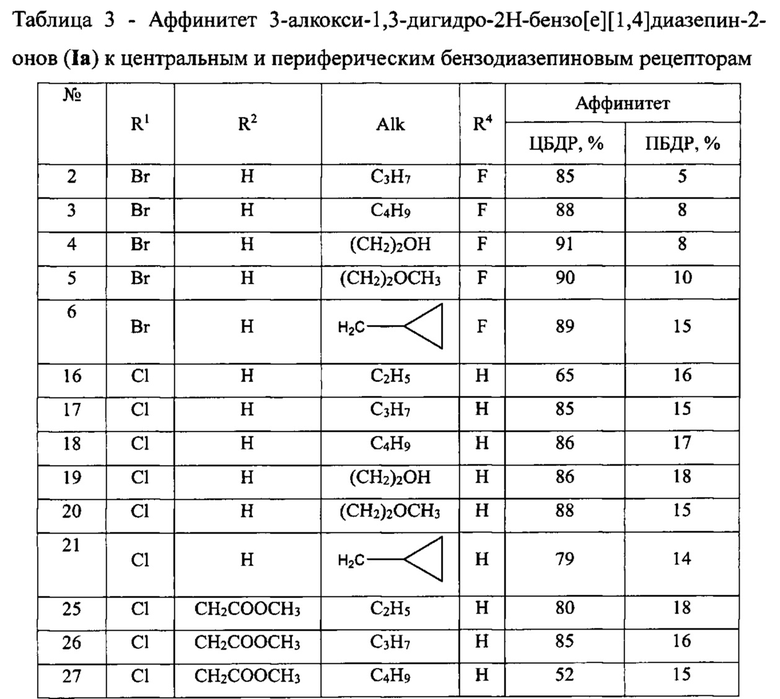
Пример 3. Аффинитет соединений Ia к центральным и периферическим бензодиазепиновым рецепторам
Изучение аффинитета соединений к центральным бензодиазепиновым рецепторам (ЦБДР) ЦНС проводили с использованием радиорецепторного метода конкурентного вытеснения радиолиганда [3Н]-флумазенила (Ro 15-1788) из мест его специфического связывания с рецептором. Вытеснение радиолиганда проводили в концентрации 1×10-6 моль/л.
Изучение аффинитета соединений Ia к периферическим бензодиазепиновым рецепторам (ПБДР) (TSPO-рецепторы) ЦНС проводили с использованием радиорецепторного метода конкурентного вытеснения радиолиганда [3Н] PK11195 из мест его специфического связывания с рецептором. Вытеснение радиолиганда проводили в концентрации 1×10-6 моль/л.
Данные аффинитета 3-алкокси-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов (Ia) к центральным и периферическим бензодиазепиновым рецепторам ЦНС представлены в таблице 3.
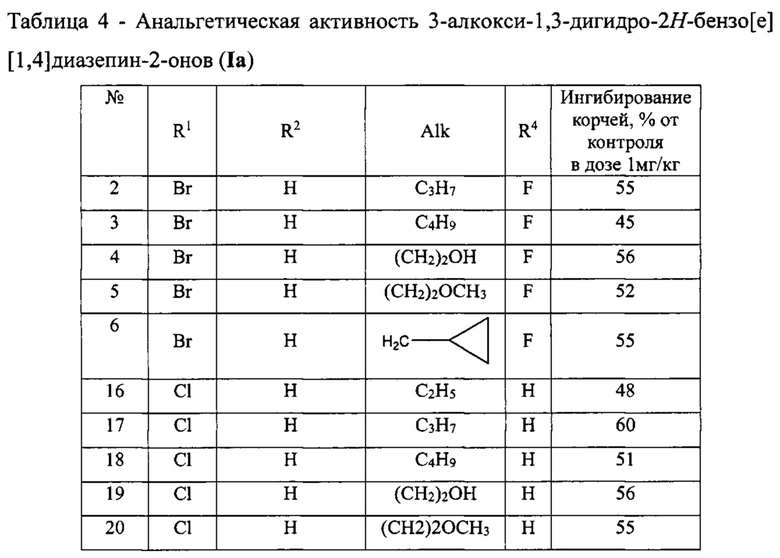
Пример 4. Оценка анальгетической активности соединений общей формулы I
Исследование анальгетической активности проводилось на модели периферической боли, в основе которой лежит химическое болевое раздражение, вызванное внутрибрюшинным введением уксусной кислоты, которое приводит к возникновению непроизвольных сокращений брюшных мышц живота - «корчей», сопровождающихся вытягиванием задних конечностей и выгибанием спины. «Корчи» у мышей вызывали 0,75%-ным раствором уксусной кислоты, которую вводили внутрибрюшинно через 40 мин после внутрибрюшинного введения исследуемых соединений в диапазоне доз от 0,001 до 5 мг/кг. За животными наблюдали в течение 20 мин и подсчитывали количество корчей для каждого животного. Анальгетическую активность оценивали по способности соединений уменьшать число корчей в опытной группе животных по сравнению с контролем и выражали в процентах, расчет проводили по нижеприведенной формуле:
АА=(Ск-Со/Ск)×100%,
где АА - анальгетическая активность в %;
Ск - среднее количество корчей в контрольной группе;
Со - среднее количество корчей в опытной группе.
Исследуемые соединения изучали в сравнении с эталонным препаратом - диклофенаком натрия в дозе 10 мг/кг [11]. ЕД50 рассчитывали по методу В.Б. Прозоровского [12].
Как видно из представленных данных в таблице 4, все изученные производные 3-алкокси-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов (Ia) оказывают выраженное анальгетическое действие - в дозе 1 мг/кг ингибируют корчи у животных на 45-88%т в сравнении с контролем. Для некоторых производных формулы Ia (№№2, 4, 17, 25, 26, 47, 55, 56 табл. 4) была установлена эффективная доза ЕД50 которая составила соответственно: 0,1±0,02; 0,13±0,03; 0,09±0,025; 0,08±0,02; 0,07±0,02; 0,89±0,27; 0,10±0,015, 0,049±0,014. Величины ЕД50 препаратов сравнения составили: для индометацина - 1,50±0,26 мг/кг, для диклофенака натрия - 10,0±1,8 мг/кг. Таким образом, заявляемые соединения формулы Ia превосходят препараты сравнения по анальгетической активности, так как характеризуются значительно меньшей (на 1-2 порядка) величиной ЕД50.
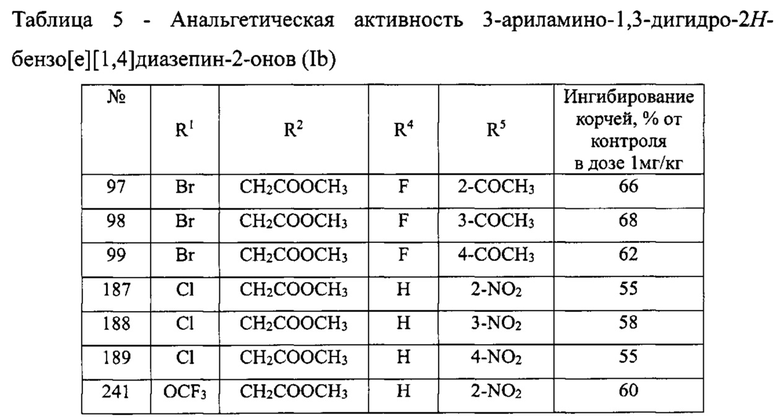
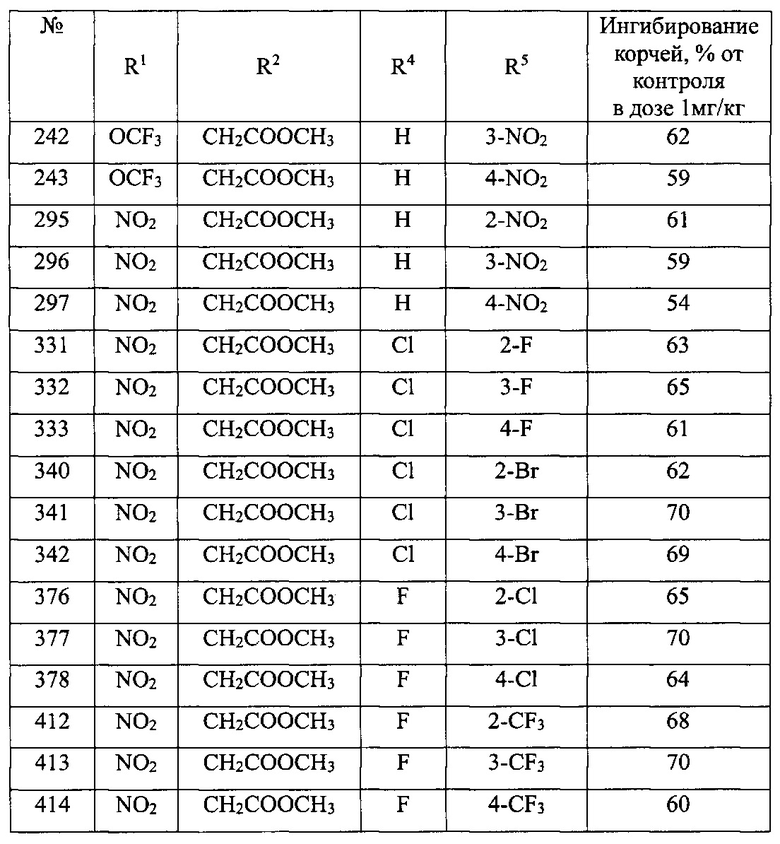
Производные -ариламино-1,3-дигидро-2Н-бензо[е][1,4]диазепин-2-онов (Ib) также характеризуются высокой анальгетической активностью - в дозе 1 мг/кг более чем на 50% ингибируют корчи у животных (данные по анальгетической активности в таблице 5).
Исследования фармакологической активности 3-ариламино-1,2-дигидро-3Н-1,4-бензодиазепин-2-онов, а именно их влияния на аппетит, оценку антигипоксической и антидепрессивной активности проводили на белых крысах-самцах массой 150-180 г и мышах-самцах массой 18-22 г. Животных содержали на стандартной лабораторной диете при естественном освещении. Животным контрольных групп вводили водно-твиновую взвесь. Исследуемые вещества вводили внутрибрюшинно в суспензии с Tween-80 фирмы «Serva». Препаратами сравнения служили гормон лептин фирмы «Sigma-Aldrich», который вводили в дозе 0,0002 мг/кг и известный антидепрессант амитриптилин (раствор для инъекций в амп.1 мл, «Московский эндокринный завод», Россия) в дозе 1 мг/кг. Исследуемые соединения и водно-твиновую взвесь вводили из расчета 0,2 мл/100 г массы крысы.
Пример 5. Оценка влияния на аппетит (анорексигенного действия) соединений формулы Ib
Влияние соединений на аппетит крыс изучали по методу «Анорексия». У крыс в течение 2-х недель в экспериментальной установке вырабатывался навык взятия жидкой пищи. Затем отработанной группе животных за день до опыта внутрибрюшинно вводили водно-твиновую взвесь исследуемых соединений. Животных допускали к жидкой пище через 40 мин, после чего регистрировали количество потребляемой пищи (в мл) каждой крысой в течение 3 ч каждые 30 мин. На следующий день после 2-х часов депривации крысам контрольной группы внутрибрюшинно вводили водно-твиновую взвесь, а опытной группе вводили исследуемые соединения. Через 40 мин после введения соединений крыс допускали к жидкой пище. Количество потребляемой пищи (в мл) фиксировали каждые 30 мин в течение 3 ч. Затем все показатели по потреблению пищи каждой крысой суммировали и сравнивали с контрольными значениями. Контрольная группа в среднем за 30 мин потребляла 7 мл жидкой пищи. Эффект выражали в процентах по отношению к контролю [13].
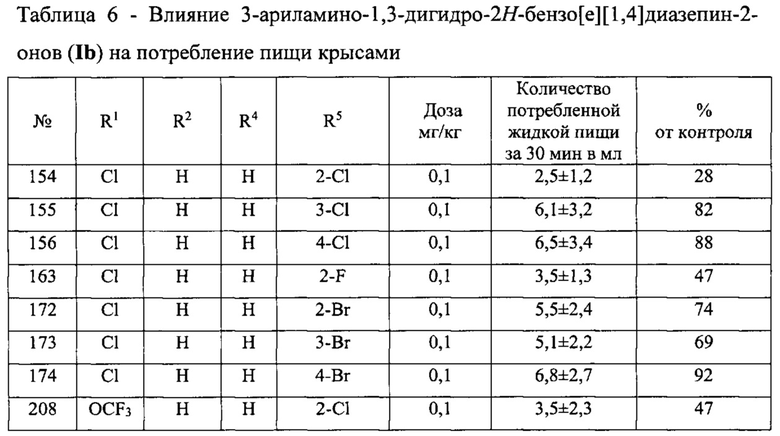
Влияние 3-ариламино-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов (Ib) на потребление пищи крысами по методу «Анорексия» представлено в таблице 6.
Среди исследуемых соединений вещества №№154, 208, 262 и 370 (табл. 6) обладают анорексигенным действием, которое выражается в снижении аппетита и потребления пищи экспериментальными крысами, соответственно, до 28%, 47%, 41% и 39%, по сравнению с контролем (см. табл. 5).
Гормон лептин снижал аппетит и потребление пищи на 63% по сравнению с контрольными значениями. Следует отметить, что соединения №362 и №363 (табл. 6) проявили гиперфагический эффект, т.е. повышался аппетит.
Пример 6. Оценка антигипоксической активности соединений Ib
Скрининг антигипоксической активности проводили на модели острой гипоксии замкнутого пространства (ГЗП). ГЗП моделировали путем размещения мышей в изолированные гермообъемы (V=200 мл). Каждая группа включала по 10 животных. Наблюдение продолжалось до момента гибели животных. Антигипоксический эффект оценивали по динамике показателя продолжительности жизни (в мин) относительно контроля, принятого за 100%, и исходя из расчета коэффициента антигипоксической защиты (Кз): кз=Ти/Тк, где Ти - средняя продолжительность жизни животных в исследовательской группе; Тк - средняя продолжительность жизни в контрольной группе [11].
Преимуществом исследуемых соединений перед препаратом сравнения гормоном лептином является наличие, помимо высокой анорексигенной активности, также выраженной антигипоксической и антидепрессивной активности. Так, было показано, что производные 3-ариламино-1,2-дигидро-3Н-1,4-бензодиазепин-2-оны в дозе 10 мг/кг обладают также антигипоксическим действием на модели острой гипоксии замкнутого пространства в опытах на мышах. Наибольшая эффективность при этом обнаружена у соединений №264 и 371, на фоне действия которых продолжительность жизни мышей в условиях острой гипоксии замкнутого пространства возрастает, соответственно, на 70% и 40,5% относительно контроля. Препарат сравнения - гормон лептин не проявляет противогипоксических свойств [14].
Пример 7. Оценка антидепрессивной активности соединений Ib
Антидепрессивную активность изучали по тесту «форсированного плавания» Порсолта [15], который заключается в создании стрессового состояния у мышей путем принудительного плавания в узком прозрачном цилиндре, на 1/3 заполненном водой с температурой 23-25°C. Антидепрессивное действие оценивали по сокращению времени иммобилизации, при котором экспериментальные животные совершают минимальное количество гребков в воде в секундах или процентах по сравнению с контролем. Поведение животных регистрировали в течение 4 мин после двухминутной акклиматизации.
Изучение влияния 3-ариламино-1,2-дигидро-3Н-1,4-бензодиазепин-2-онов формулы Ib на время иммобилизации мышей в условиях форсированного плавания показало, что все исследуемые соединения в дозе 1 мг/кг обладают антидепрессивным эффектом. Наиболее высокое антидепрессивное действие оказывают соединения №173 и №208 (табл. 2), которые на 32% и 40%, соответственно, уменьшают время иммобилизации (зависания) мышей по сравнению с контролем и действуют на уровне препарата сравнения амитриптилина в дозе 1 мг/кг (40%). Препарат гормон лептин в дозе 0,0002 мг/кг только на 14% снижает время зависания мышей по сравнению с контролем, т.е. проявляет слабый антидепрессивный эффект.
Проведенные исследования показали, что в ряду 3-ариламино-1,2-дигидро-3Н-1,4-бензодиазепин-2-онов формулы Ib обнаружены вещества, обладающие высокой анорексигенной активностью и представляющие интерес для дальнейших исследований в качестве потенциальных лекарственных средств, регулирующих пищевое поведение и снижающих аппетит и массу тела. Преимуществом заявленных соединений перед препаратами сравнения является также наличие высокой антигипоксической и антидепрессивной активности по сравнению с препаратами сравнения амитриптилином и гормоном лептином.
Пример 8. Оценка анксиолитической активности соединений Ib
Анксиолитическая активность изучалась на модели конфликтной ситуации, основанной на столкновении двух рефлексов (питьевого и оборонительного) в момент потребления воды из поилки. Критерием оценки анксиолитической активности служило число наказуемых взятий воды [16].
Общая двигательная активность оценивалась на модели открытого поля. Во время пребывания животных в открытом поле (3 мин) регистрировали число вставаний на задние лапы (вертикальная двигательная активность), число переходов из квадрата в квадрат (горизонтальная двигательная активность), число заглядываний в отверстия (исследовательское поведение). Сумма этих показателей представляет собой общую двигательную активность [17].
Эталоном для сравнения был препарат диазепам. Все исследуемые соединения и референс-препарат диазепам вводились в дозе 5 мг/кг за 30 мин до начала исследований в суспензии с Twin-80.
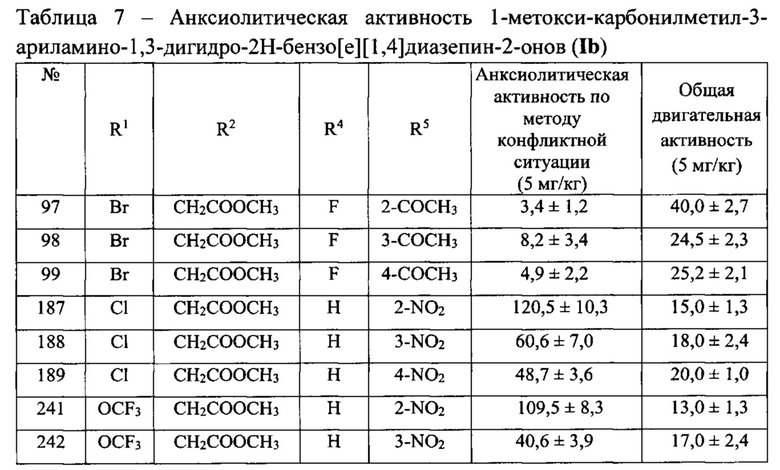
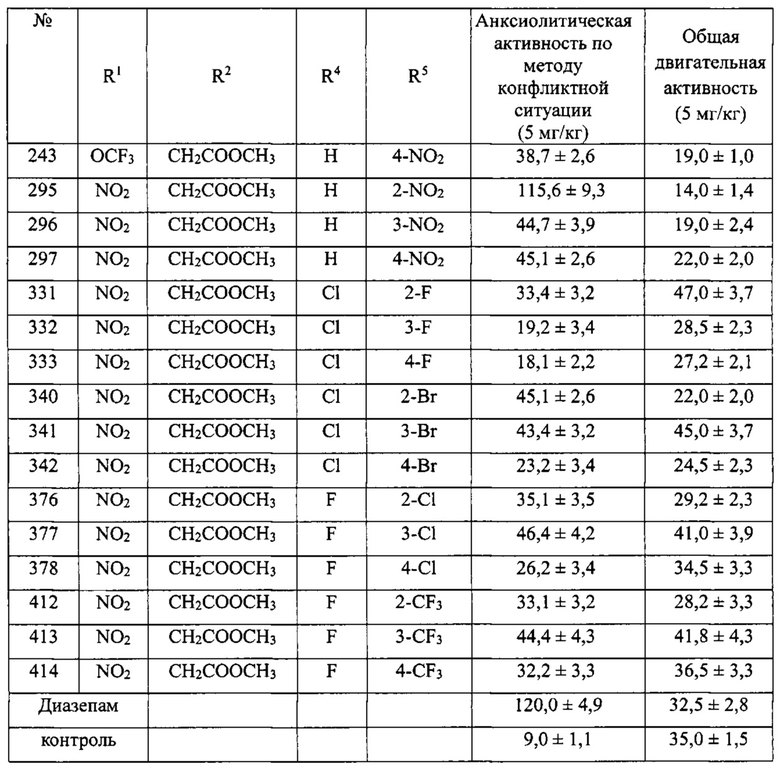
Анксиолитические свойства и общая двигательная активность 1-метокси-карбонилметил-3-ариламино-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов (Ib) представлены в таблице 7.
Из таблицы 7 видно, что соединения №№187, 241 и №295, обладали выраженными анксиолитическими свойствами, а соединения №№97, 331, 341, 377 и №413 не обладают седативными свойствами, значения их общей двигательной активности статистически не отличались от контрольной группы животных.
Таким образом, многие синтезированные соединения - производные 1,4-бензодиазепин-2-она общей формулы I, включая соединения формулы Ia и соединения формулы Ib, обладают высокой анальгетической активностью. Предложенные соединения можно применять в качестве неопиоидньгх анальгетиков для лечения болевых синдромов различного генеза и интенсивности. Вместе с тем, в ряду 3-ариламино-1,2-дигидро-3Н-1,4-бензодиазепин-2-онов формулы Ib, в отличие от соединений формулы Ia, выявлены также соединения с высокой анорексигенной активностью, которая выражается в снижении аппетита и массы тела у крыс под влиянием исследуемых соединений в низких дозах 0,1-0,05 мг/кг по методу «Анорексия» в сравнении с контролем и препаратом сравнения гормоном насыщения лептином (0,0002 мг/кг). Помимо анорексигенной активности у заявленных соединений формулы Ib обнаружены антигипоксические, антидепрессивные и анксиолитические свойства, что отличает их от препаратов сравнения - гормона похудения лептина и амитриптилина. Поэтому соединения формулы Ib, наряду с использованием в качестве анальгетиков, можно применять для регуляции веса (снижение или увеличение) в качестве анорексигенных или антианорексигенных средств, лечения психических расстройств в качестве антидепрессантов и анксиолитиков, а также для профилактики и лечения нарушений функций ЦНС в качестве антигипоксантов и ноотропных средств.
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Dziadulewicz E.K., Brown М.С., Dunstan A.R. et al. The design of non-peptide human bradykinin B2 antagonists employing the benzodiazepine peptidomimetic scaffold. Bioorg. Med. Chem. Lett. 1999. V. 9 P. 463-468.
2. Wood M.R., Kim J.J., Han V et al. Benzodiazepines as Potent and Selective Bradykinin B1 Antagonists. J. Med. Chem. 2003. V. 46 N 10 P. 1803-1806.
3. Андронати К.С., Костенко Е.А, Карасева Т.Л., Андронати С.А. Синтез и фармакологические свойства производных 3-амино-1,2-дигидро-3Н-, 4-бенздиазепин-2-она. Хим.-фарм. журнал. 2002. Т. 36 №7 С. 16-18.
4. Андронати С.А., Карасева Т.Л., Казакова А.А., Павловский В.И., Бачинский С.Ю. Синтез и нейротропные свойства 3-арилиден-1,2-дигидро-3Н-1,4-бензодиазепин-2-онов. Хим.-фарм. журн. 2011. Т. 45 №4 С. 101-102.
5. Petty F., Trivedi М.Н., Fulton М., and Rush A.J. Benzodiazepines as antidepressants: Does GAB A play a role in depression? Biol Psychiatry. 1995. Nov 1; 38(9): 578-591.
6. Furukawa T.A., Streiner D., Young L.T., Kinoshita Y. Antidepressants plus benzodiazepines for major depression (Review) Cochrane Database of Systematic Reviews 2001, Issue 3. Art. No.: CD001026. DOI: 10.1002/14651858.CD001026
7. Kunchandy J., Kulkarni S.K. Hypoxic stress-induced convulsion and death: protective effect of alpha 2-adrenoceptor and benzodiazepine receptor agonists and Ro 5-4864. Arch Int Pharmacodyn Ther. 1988, 292: 35-44.
8. Stevens G.A., Singh G.M., Lu Y. et al. National, regional, and global trends in adult overweight and obesity prevalences. Population Health Metrics. 2012. 10:22 https://doi.org/10.1186/1478-7954-10-22.
9. Halmi K.A., Tozzi E, Thornton L.M., et al. The relation among perfectionism, obsessive-compulsive personality disorder, and obsessive-compulsive disorder in individuals with eating disorders. International Journal of Eating Disorders. 2005. V. 38 P. 371-374. DOI: 10.1002/eat.20190
10. Патент Украины №102273 «3-алкокси-1,2-дигiдро-3Н-1,4-бенздiазепiн-2-они, якi мають високу анальгетичну активнiсть» / В.I. Павловський, К.О. Семенiшина, С.А. Андронатi та iн. - № а 201105837. Заявл. 10.05.2011. Опубл. 25.06.2013. Бюл. №12.
11. Гацура В.В. Методы первичного фармакологического исследования биологически активных веществ. М.: Медицина. 1974. 144 с.
12. Прозоровский В.Б. Статистическая обработка результатов фармакологических исследований. Психофармакология и биологическая наркология. 2007. Т. 7 №3-4 С. 2090-2120.
13. Pierson М.Е. et al. CCK Peptides with combined features of hexa- and tetrapeptide CCK-A agonists. J. Med Chem. 2000. Vol. 43 N 12 P. 2350-2355.
14. Yadav V.K., Oury R, Suda N. et al. A Serotonin-Dependent Mechanism Explains the Leptin Regulation of Bone Mass, Appetite, and Energy Expenditure. Cell. 2009. Vol. 138 Issue 5 P. 976-938. https://doi.org/10.1016/j.cell.2009.06.051
15. Porsolt R.D. Animal model of depression. Biomed. 1979. V. 30 (3). P. 139-140.
16. Андронати С.А., Авруцкий Г.Я., Воронина T.A., и др. в кн. Феназепам, отв. редактор Богатский А.В., К.: Наукова думка, 1982, с. 288.
17. Вихляев Ю.И., Воронина Т.А. Фармакология феназепама. Экспресс-информ. изд. ВНИИМИ - Сер. Новые лекарственные препараты. 1978. №3. С. 2-16.
ПРОИЗВОДНЫЕ 1,4-БЕНЗОДИАЗЕПИН-2-ОНА И ИХ ПРИМЕНЕНИЕ




| название | год | авторы | номер документа |
|---|---|---|---|
| ТРИАЗОЛО[4,3-А][1,4]-БЕНЗОДИАЗЕПИНЫ И ТИЕНО[3,2-F]-[1,2,4]-ТРИАЗОЛО[4,3-А] [1,4]ДИАЗЕПИНЫ, В СЛУЧАЕ НАЛИЧИЯ ПО МЕНЬШЕЙ МЕРЕ ОДНОГО АСИММЕТРИЧЕСКОГО ЦЕНТРА ИХ ЭНАНТИОМЕРЫ, РАЦЕМАТЫ И ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ПРИСОЕДИНЕНИЯ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИНГИБИРУЮЩАЯ ФАКТОР АКТИВАЦИИ ТРОМБОЦИТОВ. | 1992 |
|
RU2094436C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2,3-БЕНЗОДИАЗЕПИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 2000 |
|
RU2243228C2 |
| ПРОИЗВОДНЫЕ 1,4-БЕНЗОДИАЗЕПИНА, ОБЛАДАЮЩИЕ СЕЛЕКТИВНОЙ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2133248C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ БЕНЗОДИАЗЕПИНА И ИНГИБИТОР БЕЛКА СЛИЯНИЯ RSV | 2005 |
|
RU2388476C2 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ АРИТМИИ | 1994 |
|
RU2155587C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 3-[(4S)-8-БРОМ-1-МЕТИЛ-6-(2-ПИРИДИНИЛ)-4Н-ИМИДАЗО[1,2-А][1,4]БЕНЗОДИАЗЕПИН-4-ИЛ]ПРОПИОНОВОЙ КИСЛОТЫ ИЛИ ЕГО БЕНЗОЛСУЛЬФОНАТНОЙ СОЛИ И СОЕДИНЕНИЯ, ПРИМЕНЯЕМЫЕ В ЭТОМ СПОСОБЕ | 2010 |
|
RU2551848C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИАЗОЛО/4,3-А/ /1,4/ДИАЗЕПИНОВ | 1988 |
|
RU2071962C1 |
| АННЕЛИРОВАННЫЕ КАРБАМОИЛАЗАГЕТЕРОЦИКЛЫ, ФОКУСИРОВАННАЯ БИБЛИОТЕКА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ | 2005 |
|
RU2281947C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,6-ДИГИДРО-4H-БЕНЗО[f]ПИРРОЛО[1,2-α][1,4]ДИАЗЕПИН-6-ОНА | 2010 |
|
RU2425037C1 |
| АРИЛ-КОНДЕНСИРОВАННЫЕ 2,4-ДИАЗЕПИНОВЫЕ СОЕДИНЕНИЯ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ, АНТИАРИТМИЧЕСКИЙ АГЕНТ И КОМПОЗИЦИЯ | 1991 |
|
RU2114833C1 |
Изобретение относится к новым производным 1,4-бензодиазепин-2-она формулы I,
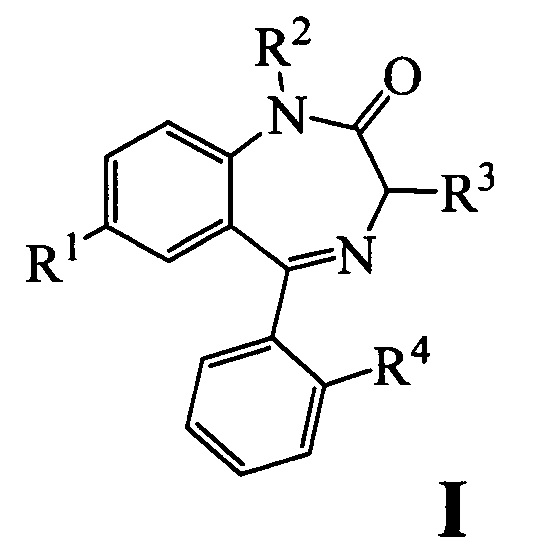
ограниченным следующими вариантами структуры 1-6:
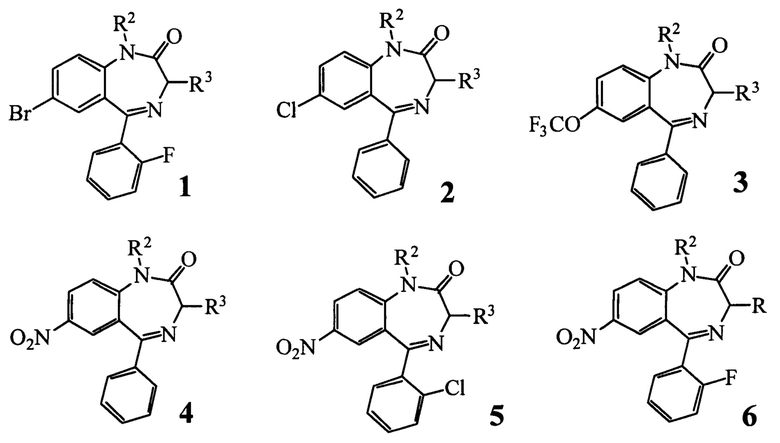
Технический результат: получены новые соединения формулы I, обладающие наряду с выраженными анальгетическими свойствами анорексигенными и анксиолитическими. 4 н. и 2 з.п. ф-лы, 7 табл., 8 пр.
1. Производные 1,4-бензодиазепин-2-она общей формулы I,
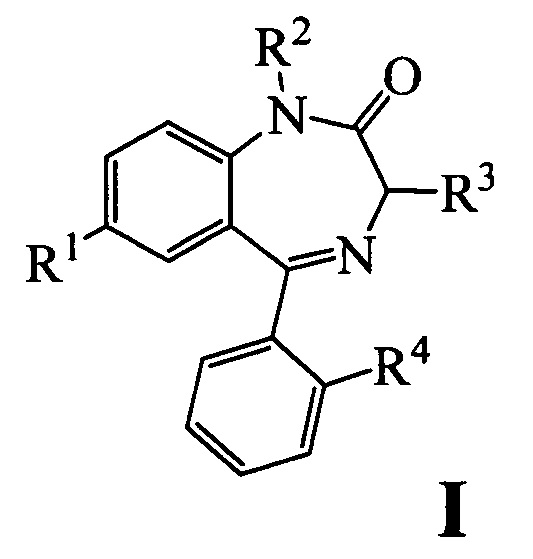
ограниченные следующими вариантами структуры 1-6:
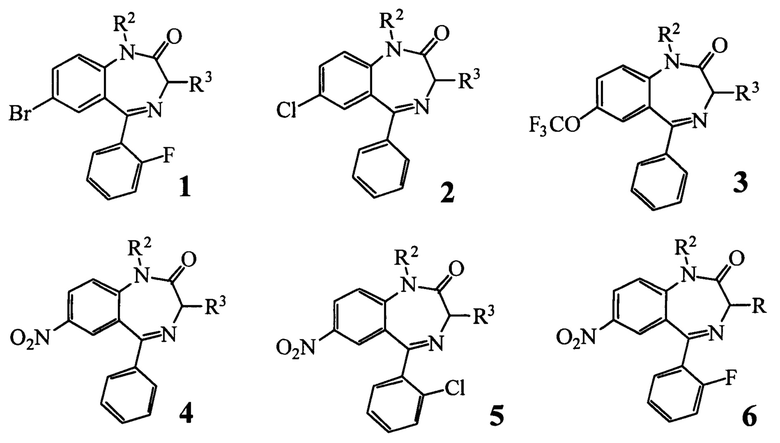
при условии, что:
а) структуры 1 (R1=Br, R4=F), 3 (R1=OCF3, R4=Н), 5 (R1=NO2, R4=Cl) и 6 (R1=NO2, R4=F) имеют следующие заместители R2 и R3:
- R2=Н, СН2СОСН3, СН2СООСН3, CH2CONHNH2;
- R3=OAlk, NHAr, где

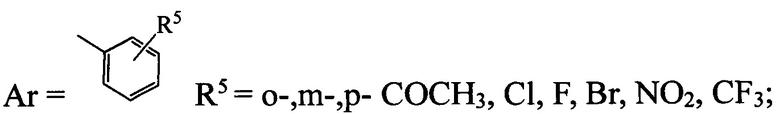
б) структура 2 (R1=Cl, R4=Н) имеет следующие заместители R2 и R3:
- в случае, если R2=Н,
тогда R3=OAlk, NHAr, где

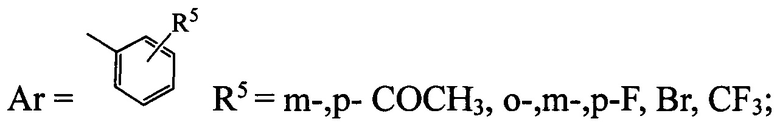
- в случае, если R2=СН2СОСН3, СН2СООСН3, CH2CONHNH2,
тогда R3=OAlk, NHAr, где
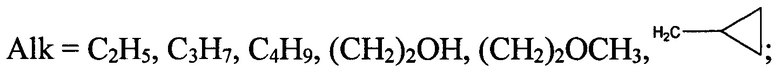
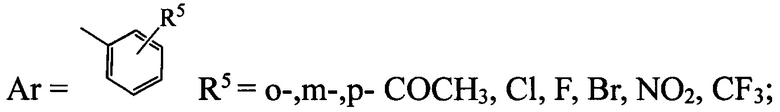
в) структура 4 (R1=NO2, R4=Н) имеет следующие заместители R2 и R3:
- в случае, если R2=Н,
тогда R3=OAlk, NHAr, где
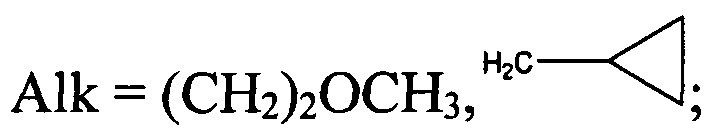
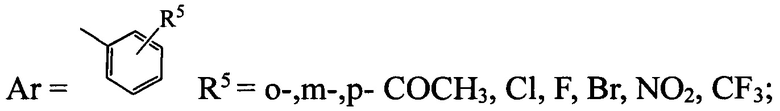
- в случае, если R2=СН2СОСН3, СН2СООСН3, CH2CONHNH2,
тогда R3=OAlk, NHAr, где
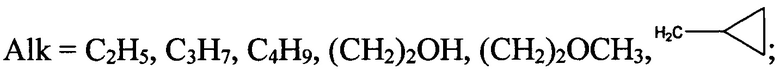
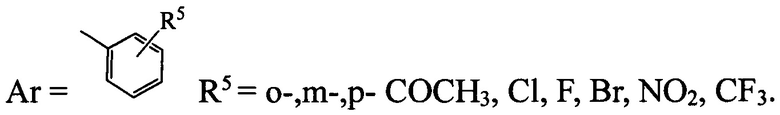
2. Соединения по п. 1, которые представляют собой 1-замещенные 3-алкокси-1,3-дигидро-2Н-бензо[е][1,4]диазепин-2-онов общей формулы Ia
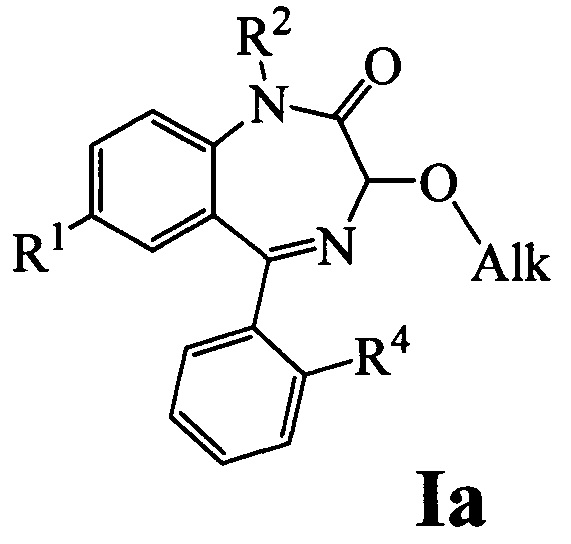
при условии, что:
а) структуры 1 (R1=Br, R4=F), 3 (R1=OCF3, R4=Н), 5 (R1=NO2, R4=Cl), 6 (R1=NO2, R4=F) имеют следующие заместители R2 и Alk:
- R2=Н, СН2СОСН3, СН2СООСН3, CH2CONHNH2;

б) структура 2 (R1=Cl, R4=Н) имеет следующие заместители R2 и Alk:
- в случае, если R2=Н,
тогда 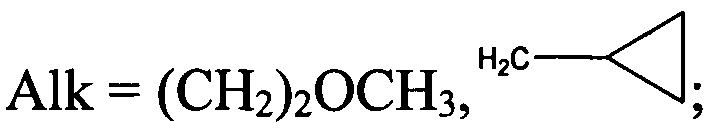
- в случае, если R2=СН2СОСН3, СН2СООСН3, CH2CONHNH2,
тогда 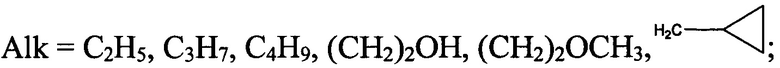
в) структура 4 (R1=NO2, R4=Н) имеет следующие заместители R2 и Alk:
- в случае, если R2=Н,
тогда 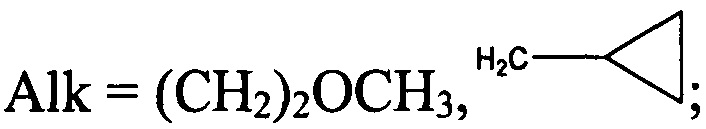
- в случае, если R2=СН2СОСН3, СН2СООСН3, CH2CONHNH2,
тогда 
3. Соединения по п. 1, которые представляют собой 1-замещенные 3-ариламино-1,3-дигидро-2H-бензо[е][1,4]диазепин-2-онов общей формулы Ib

при условии, что:
а) структуры 1 (R1=Br, R4=F), 3 (R1=OCF3, R4=Н), 5 (R1=NO2, R4=Cl), 6 (R1=NO2, R4=F) имеют следующие заместители R2 и Ar:
- R2=Н, СН2СОСН3, СН2СООСН3, CH2CONHNH2;
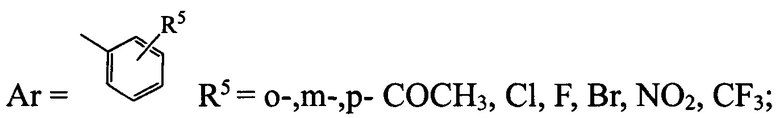
б) структура 2 (R1=Cl, R4=Н) имеет следующие заместители R2 и Ar:
- в случае, если R2=Н,
тогда 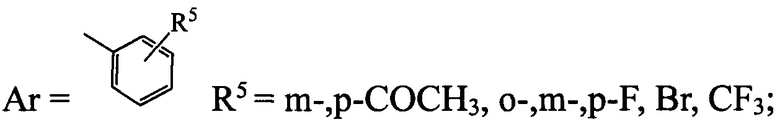
- в случае, если R2=СН2СОСН3, СН2СООСН3, CH2CONHNH2,
тогда 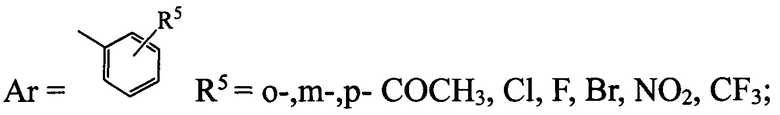
в) структура 4 (R1=NO2, R4=Н) имеет следующие заместители R2 и Ar:
- в случае, если R2=Н
тогда 
- в случае, если R2=СН2СОСН3, СН2СООСН3, CH2CONHNH2,
тогда 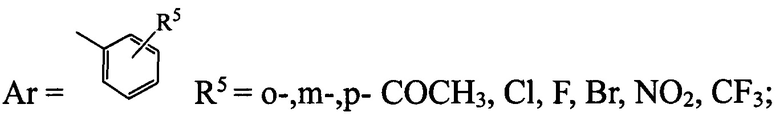
4. Применение соединений по пп. 1-3 в качестве анальгетиков.
5. Применение соединений по п. 3 для регуляции веса в качестве анорексигенных или антианорексигенных средств.
6. Применение соединений по п. 3 в качестве анксиолитиков.
| Karaseva, T | |||
| L.; Likhota, E | |||
| B.; Krivenko, Ya | |||
| R.; Semibrat'ev, S | |||
| A.; Pavlovskii, V | |||
| I | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Pharmaceutical Chemistry Journal, 51(4), 258-261, 2017 | |||
| Pavlovskii, V | |||
| I.; Ushakov, I | |||
| Yu.; Kabanova, T | |||
| A.; Khalimova, E | |||
| I.; Kravtsov, V | |||
| Kh.; Andronati, S | |||
| A | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Pharmaceutical Chemistry Journal, 49(9), 592-597, 2015 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Pavlovsky, V | |||
| I.; Tsymbalyuk, O | |||
| V.; Martynyuk, V | |||
| S.; Kabanova, T | |||
| A.; Semenishyna, E | |||
| A.; Khalimova, E | |||
| I.; Andronati, S | |||
| A | |||
| Neurophysiology, 45(5-6), 427-432, 2013 | |||
| Pavlovsky, V | |||
| I.; Semenishina, E | |||
| A.; Kravchenko, I | |||
| A.; Radaeva, I | |||
| N.; Simonov, Yu | |||
| A.; Gdaniec, M.; Samburskii, S | |||
| E.; Andronati, S | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Pharmaceutical Chemistry Journal, 46(9), 540-545, 2012 | |||
| Andronati, Sergey; Semenishyna, Ekaterina; Pavlovsky, Victor; Simonov, Yuriy; Makan, Svetlana; Boyko, Irina; Burenkova, Natalya; Gdaniec, Maria; Cardinael, Pascal; Bouillon, Jean-Philippe; Mazepa, Alexander Synthesis, structure and affinity of novel 3-alkoxy-1,2-dihydro-3H-1,4-benzodiazepin-2-ones for CNS central and peripheral benzodiazepine receptors | |||
| European Journal of edicinal Chemistry, 45(4), 1346-1351, 2010 | |||
| Offel, Michael; Lattmann, Pornthip; Singh, Harjit; Billington, D | |||
| C.; Bunprakob, Yodchai; Sattayasai, Jintana; Lattmann, Eric Synthesis of substituted 3-anilino-5-phenyl-1,3-dihydro-2H-1,4-benzodiazepine-2-ones and their evaluation as cholecystokinin-ligands | |||
| Archiv der Pharmazie, 339(4), 163-173, 2006 | |||
| Makan, S | |||
| Yu.; Tkachuk, N | |||
| A.; Korkhov, V | |||
| M.; Kostenko, S | |||
| V.; Boiko, I | |||
| A.; Smul'skii, S | |||
| P.; Andronati, K | |||
| S.; Kostenko, E | |||
| A.; Karaseva, T | |||
| L.; Andronati, S | |||
| A | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Pharmaceutical Chemistry Journal, 39(6), 300-302, 2005 | |||
| Yang, Shen K | |||
| Racemization and stereoselective alcoholysis of temazepam | |||
| Chirality, 11(3), 179-186, 1999 | |||
| Yang, Shen K | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Journal of Liquid Chromatography, 16(12), 2605-15, 1993 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Bell, Stanley C.; McCaully, Ronald J.; Gochman, Carl; Childress, Scott J.; Gluckman, Melvyn I | |||
| Journal of Medicinal Chemistry, 11(3), 457-61, 1968 | |||
| Тормозной цилиндр железнодорожного транспортного средства | 1982 |
|
SU1046145A2 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| WO 2004106310 A1, 09.12.2004 | |||
| US 3678043, 18.07.1972 | |||
| ПРОКЛАДКА УПРУГОТЕРМОСТОЙКАЯ | 1997 |
|
RU2127387C1 |
Авторы
Даты
2019-09-30—Публикация
2017-11-24—Подача