Изобретение относится к новым производным 1,4- бензодиазепина общей формулы,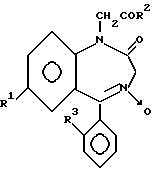
где R1 - бром
R2-CH3O, NHNH2;
R3 -H, галоген.
Широко известны анксиолитические средства - производные 1,4- бензодиазепин-2-она, такие как феназепам (А.В.Богадский, С.А.Андронати, Н.Я.Головенко. Транквилизаторы. Киев: Наукова Думка, 1980, с.257-260), альпрозалам (ксанкс) (Регистр лекарственных средств России. М.: ИНФАРМХИМ, 1993, с.502), гидазепам (Регистр лекарственных средств России. М.: ИНФАРМХИМ, 1993, с. 309). Однако феназепам и ксанкс наряду с мощным основным транквилизирующим действием обладают целым рядом серьезных побочных эффектов, таких как сонливость, головокружение, нарушение зрения, головная боль, амнезия и другие (А.В.Богадский, С.А.Андронати, Н.Я.Головенко. Транквилизаторы. Киев: Наукова Думка, 1980, с.257-260; K.Aranko, M.J.Mattila, D.Bordignon. Acta Pharmacol. Toxicol. , 1985, v.56, N5, p. 364-372). Гидазепам, обладая более селективным транквилизирующим действием, также не лишен побочных эффектов, свойственных другим представителям этого ряда в активном диапазоне доз ( Т.А.Воронина. Гидазепам. Киев: Наукова Думка, 1992, с.63-75).
Кроме того, в условиях клиники было показано, что транквилизирующий эффект сопровождается развитием активирующего или седативного компонентов. При этом если для феназепама характерно развитие анксиолитического действия прежде всего с седативным компонентом, то в спектре анксиолитического действия гидазепама представлен также и активирующий компонент (Ю.А.Александровский, М. В. Поюровский и Г.Г.Незнамов. Неврозы и перекисное окисление липидов. М.: Наука, 1991, с.79-82; Г.Г.Незнамов, С.И.Лыгалов, В.К.Бочкарев и соавт. Гидазепам. Киев: Наукова Думка, 1992, с. 137).Возможность подобного разделения анксиолитического эффекта бензодиазепинов была недавно продемонстрирована и в условиях эксперимента (Ю.А.Бледнев, М.М.Козловская, М.Маула и др. Актуальные вопросы экспериментальной и клинической фармакологии. Под ред. В.Е.Новикова. Смоленск, 1994, с. 13-15). Более того, последние клинические исследования показали, что меньшая выраженность седативного компонента в структуре индивидуальных реакций на бензодиазепиновые транквилизаторы является прогностически позитивным признаком для эффективной терапии этими препаратами ([Г. Г. Незнамов, С. А. Сюняков, Е.С.Телешова, Н.В.Колотилинская, Т.П.Сафарова. Транквилизаторы: индивидуальная чувствительность и терапевтическая эффективность. Тезисы докл. II Российского Национального Конгресса "Человек и лекарство", М., 10-15 апреля 1995 г., с. 100). Такими свойствами обладают заявляемые соединения.
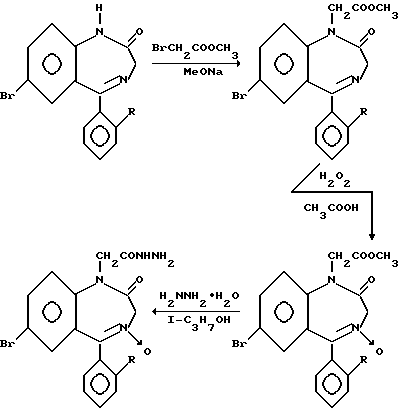
1-Метоксикарбонилметил-7-бром-5-фенил и 5-/о-хлор/фенил- 1,2-дигидро-3Н-1,4-бензодиазепин-2-ОН-4-оксиды получают действием на соответствующие незамещенные в положении 1 1,2-дигидро-3Н-1,4- бензодиазепин-2-оны метилбромацетата в присутствии метилата натрия с последующим окислением образующихся 1-метоксикарбонилметил-производных перекисью водорода в среде уксусной кислоты.
1-Гидразинокарбонилметил- 1,2-дигидро-3Н-1,4-бензодиазепин-2-он-4-оксиды получают взаимодействием соответствующих 1-метоксикарбонилметил-1,2-дигидро- 3Н-1,4-бензодиазепин-2-он-4-оксидов с гидразин-гидратом.
Пример 1. 1-Метоксикарбонилметил-7-бром-5-фенил-1,2-дигидро-ЗН- 1,4-бензидиазепин-2-он-4-оксид (la).
К 116,2 (0,3 моль) 1-метоксикарбонилметил-7-бром-5-фенил-1,2- дигидро-3H-1,4-бензодиазепин-2-она прибавляют 300 мл уксусной кислоты и 200 мл 33% перекиси водорода. Реакционную смесь нагревают при перемешивании до 60oC и продолжают перемешивание при этой температуре до исчезновения исходного продукта в течение 8 часов. Контроль хода реакции проводят с помощью тонкослойной хроматографии на пластинках Silufol UV 254 (элюент ацетон:гексан:хлороформ 1:2:2). Затем реакционную смесь охлаждают, выливают на лед или в холодную воду (1 л), разбавляют холодной водой в два раза при перемешивании, осадок отфильтровывают, промывают холодной водой и кристаллизуют их из этилового спирта с углем. Получают 104,5 г (88,4 %) 1- метоксикарбонилметил-7-бром-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин- 2-он-4-оксида с tпл=150-152oC.
Найдено, %: С - 53,8; H - 3,7; N - 7,0; C18H15BrN2O4.
Вычислено, % : С - 53,6; H - 3,7; N - 6,9.
ИК спектр (CHCl3): С=O 1675, 1740 см-1, C=N 1595 N--->O 1225 см-1 С - O - С 1080 см-1 и др.
УФ спектр: 200 lg∈ 4.30), 239 lg∈ 4.43), 308 lg∈ 3.96) нм
Масс-спектр, m/z: [М] + 402, [M-O]+ 386, [M-Br]+ 323, [M-CH2COOCH3-О]+ 313 и др.
Пример 2. 1-Метоксикарбонилметил-7-бром-5- /o-хлор/фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-он-4-оксид (16).
К 42,7 г (0,1 моль) 1-метоксикарбонилметил-7-бром-5- /o-хлор/фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-она прибавляют 100 мл уксусной кислоты и 80 мл 33% перекиси водорода. При перемешивании нагревают реакционную массу до 80oC и продолжают перемешивание при этой температуре до исчезновения в реакционной смеси исходного бензодиазепина в течение 6 часов, контролируя это с помощью тонкослойной хроматографии на пластинках Silufol UV 254, элюент: гексан:хлороформ 1:2:2. Охлажденную реакционную смесь выливают при перемешивании в 1 л холодной воды, затем добавляют еще 0,5 л холодной воды, выпавший осадок отфильтровывают, промывают водой и кристаллизуют из этилового спирта с углем. Получают 39,5 (90%) 1-метоксикарбонилметил-7-бром-/о-хлор/фенил-1,2-дигидро-3H- 1,4-бензодиазепин-2-он-4-оксида с tпл.=235-236oC.
Найдено, %: C - 49,5: H - 3,4; N - 6,5; C18H14BrClN2O4.
Вычислено %: C - 49,4: H - 3,2: N - 6,4.
ИК спектр (CHCl3): C-O 1685, 1750 см-1, C=N 1585 см-1,
N--->O 1220 см-1, C-O-C 1080 см-1 и др.
УФ спектр: 200 lg∈ 4.49), 242 lg∈ 4.45), 296 lg∈ 4.04) нм
Масс-спектр, m/z: [M]+ 436, [M-O]+ 420, [M-Cl]+ 401 и др.
Пример 3. 1-Гидразинокарбонилметил-7-бром-5-фенил-1,2-дигидро-1H- 1,4-бензодиазепин-2-он(1в).
К раствору 40,3 г (0,1 моль) 1-метоксикарбонилметил-7-бром-5-фенил-1,2-дигидро-3H-1,4-дигидро-2-он- 4-оксида в 200 мл изопропилового спирта прибавляют 50 мл гидразингидрата и перемешивают при 50oC в течение 6 часов. Выпавший осадок гидразида отфильтровывают и кристаллизуют из изопропилового спирта. Получают 30,3 г (90%) 1-гидразинкарбонилметил-7-бром-5-фенил-1,2-дигидро-3H- 1,4-бензодиазепин-2-он-4-оксида с tпл.=266-268oC.
Найдено, %: C - 50,6; H - 3,7; N - 14,0; C17H15 BrN4O3;
Вычислено, %: C - 50,6; H - 3,8; N - 13,9.
ИК спектр (таблетки KBr): N-H 3210, 3385 см-1; C=O 1660, 1680 см-1, C=N 1570 см-1; N--->O 1230 см-1.
УФ спектр: 200 lg∈ 4.54), 239 lg∈ 4.49), 308 lg∈ 4.01) нм.
Масс-спектр m/z: [M]+ 402, [M-O]+ 386, [M-NHNH2-O]+ 327, [M-CH2CONHNH2]+ 313 и др.
Пример 4. 1-Гидразинокарбонилметил-7-бром-5-/о-хлор/фенил-1,2- дигидро-3H-1,4-бензодиазепин-2-он-4-оксид (1 г).
Растворяют в 250 мл изопропилового спирта 43,8 г (0,1 моль) 1-метоксикарбонилметил-7- бром-5-/о-хлор/фенил-1,2-дигидро-3H-1,2-бензоди-азепин-2-он-4-оксида при нагревании до 30oC, прибавляют 45 мл гидразин-гидрата и перемешивают при температуре в течение 10 часов. Реакционную массу охлаждают, добавляют 400 мл холодной воды, отфильтровывают выпавший осадок и перекристаллизовывают из изопропилового спирта. Получают 40,7 г (90%)1-гидразинокарбонилметил-7-бром-5-/о-хлор/фенил-1,2-дигидро- 3H-бензодиазепин-2-он-4-оксида с tпл= 255-258oC.
Найдено, % : С - 46,8; H - 3,3; N - 12,9; C17H14BrClN4O3.
Вычислено, % : С - 46,6; H - 3,2; N - 12,8.
ИК спектр (таблетки KBr): NH 3235, 3400 см-1, С=O 1666, 1685 см-1, C=N 1570 см-1, N--->O 1225 см-1.
УФ спектр: 200 lg∈ 4.52), 243 lg∈ 4.45), 296 lg∈ 4.03) нм.
Масс-спектр, m/z: [M]+ 436, [M-О]+- 420, [M-Cl]+ 401, [M-NHNH2-O]+- 389, [M-CONHNH2-O]+ 363 и др.
Результаты фармакологического изучения заявляемых соединений.
Для демонстрации анксиолитического действия новых соединений был использован метод измерения двигательной активности в тесте "открытое поле", который позволяет не только оценить силу анксиолитического эффекта, но и степень его селективности (С.Б.Середенин, А.А.Ведерников, Бюлл.Эксп.Биол. Мед. , 1979, т.88, N7, с.38; S.B.Seredenin, Yu.A.Blednov, B.A.Badyshtov et al. Drug Dependence and Emotional Behavior. Neurophysiological and Neurochemical Approaches, Ed. By A.V.Valdman, Consult.Bureau, New York and London, 1987, p.49-77 ). Сутью данного подхода является сравнительный анализ поведенческих эффектов изучаемых соединений у мышей двух инбредных линий Balb/c и C 57 B 1/6, которые характеризуются различными генетически детерминированными типами эмоционально-стрессовой реакции (ЭСР). О наличии анксиолитического действия судили по выявлению активирующего эффекта на двигательную активность у животных с "пассивным" типом ЭСР (линия Balb/c). Показателем седативных свойств исследуемых соединений служило выявление их ингибирующего действия на двигательную активность мышей с "активным" типом ЭСР (линия C 57 B 1/6). Селективность анксиолитического эффекта оценивали по степени совпадения диапазонов доз, оказывавших либо активирующее, либо ингибирующее действие у животных разных линий. Ранее подобный подход был с успехом применен для оценки степени селективности анксиолитического действия таких ныне известных препаратов, как феназепам (С.Б.Середенин, А.А.Ведерников, Бюлл. Эксп. Биол.Мед., 1979, т.88, N7, с.38; S.B.Seredenin, Yu.A.BIednov, B.A.Badyshtov et al. Drug Dependence and Emotional Behavior. Neurophysiological and Neurochemical Approaches, Ed. By A.V.VaIdman, Consult.Bureau, New York and London, 1987, p.49-77), мексидол (С.Б.Середенин, Ю.А.Бледнов, М.Л.Гордей и соавт. Хим.-Фарм. Журнал, 1987, N2, с.134; T.A.Voronina, S.B.Seredenin, Ann. lst. Super.Sanita, 1988, v.24, N3, p. 461-466)и гидазепам (С.Б.Середенин, Ю. А. Бледнов, А.Д.Дурнев и соавт. Гидазепам. Киев: Наукова Думка, 1992, с.92; S.B.Seredenin, Yu.A.BIednov, Phys.Chem.Biol.&Med., 1993, v., N1, p. 53-60).
В работе были использованы мыши - самцы линий Balb/c и C 57 B 1/6 весом 20-22 г (питомник "Столбовая"). Животных содержали в условиях лабораторного вивария в клетках по 10 особей в каждой, в течение не менее двух недель до начала эксперимента, на стандартной диете, при свободном доступе к воде, при 12-часовом световом режиме (свет с 8.00 до 20.00). Все эксперименты проводили в период времени с 9.00 до 13.00. Все соединения вводили внутрибрюшинно в виде их водной суспензии после предварительного тщательного растирания субстанций с несколькими каплями Tween-80 за 30 мин до начала эксперимента из расчета 0,1 мл раствора на 10 г веса животного. Через 30 минут после введения препаратов животное выдерживали в темноте в течение 1 минуты и затем помещали в один из периферических квадратов "открытого поля", которое представляет из себя белую круглую арену диаметром 1 метр с белыми бортами высотой 50 см. Арена равномерно освещена 4-мя лампами по 75 Вт каждая, расположенными на высоте 1 м над поверхностью поля. Все пространство арены равномерно разделено 4-мя концентрическими окружностями, которые в свою очередь разбиты радиусами на сектора так, что периферическая окружность состоит из 16 одинаковых криволинейных квадратов. Наблюдение за животным производили в течение 3 минут, раздельно фиксировали число пересеченных квадратов на периферии и в центральных областях, а также число стоек. Суммарное число пересеченных квадратов вместе с числом стоек обозначали как общую активность. Статистическую обработку полученных результатов проводили используя t-критерий Стьюдента.
В табл. 1 представлены данные, демонстрирующие влияние соединения Ia на поведение мышей Balb/c. Показано, что в очень широком и, в целом, необычном для бензодиазепиновых производных диапазоне доз от 1.0 мг/кг до 25,0 мг/кг это соединение повышало двигательную активность животных данной линии. И только в дозе 30,0 мг/кг значения двигательной активности опытных животных не отличались от контрольных показателей. У мышей C 57 B 1/6 лишь начиная с дозы 20,0 мг/кг и выше наблюдали статистически достоверное снижение двигательной активности (табл.2).
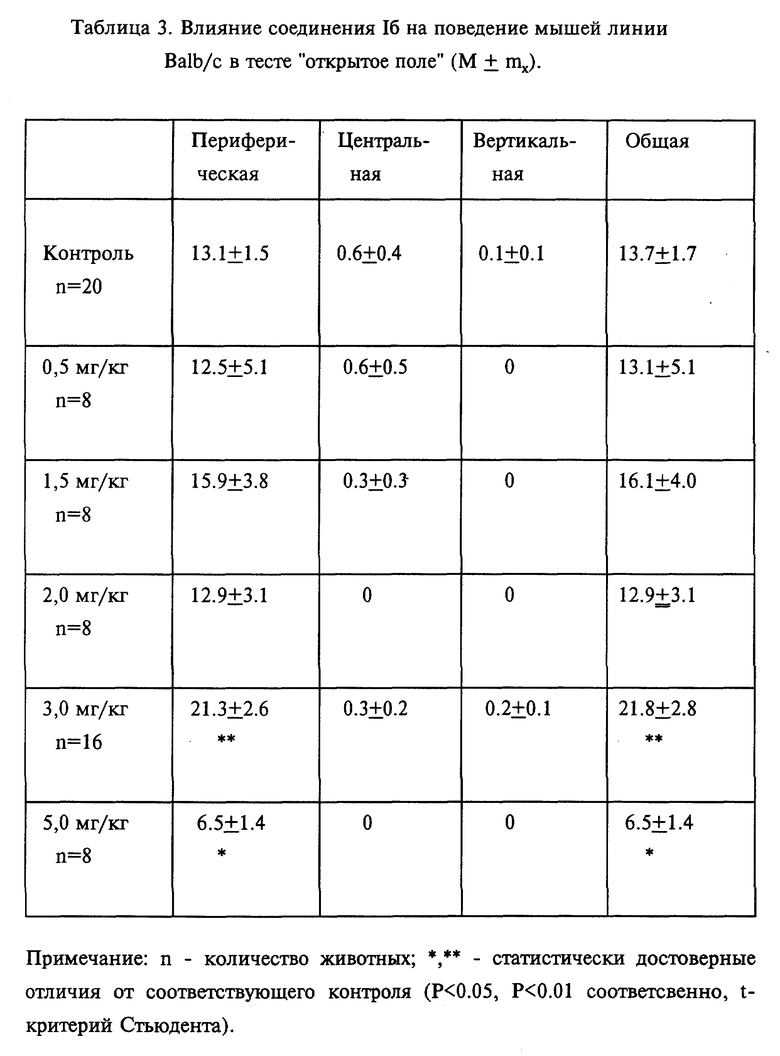
Результаты, представленные в табл. 3, свидетельствуют о том, что активация поведения животных Balb/c после введения соединения 16 достигала статистически значимых величин лишь в дозе 3,0 мг/кг, тогда как уже в дозе 5,0 мг/кг наблюдали снижение уровня двигательной активности ниже контрольных показателей. Поведение животных линии C 57 B 1/6 оставалось практически неизменным при использовании этого соединения в дозах 1,5 мг/кг и 3,0 мг/кг (табл. 4). Наблюдали лишь небольшое снижение величины периферической и вертикальной двигательной активности в дозе 1,5 мг/кг.
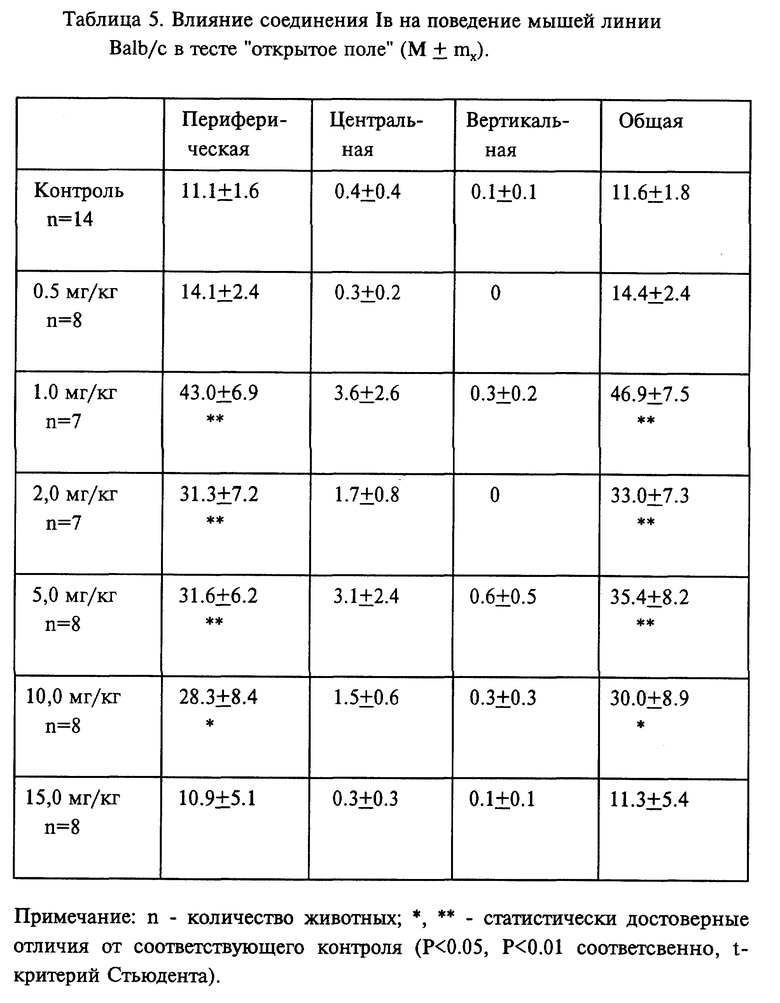
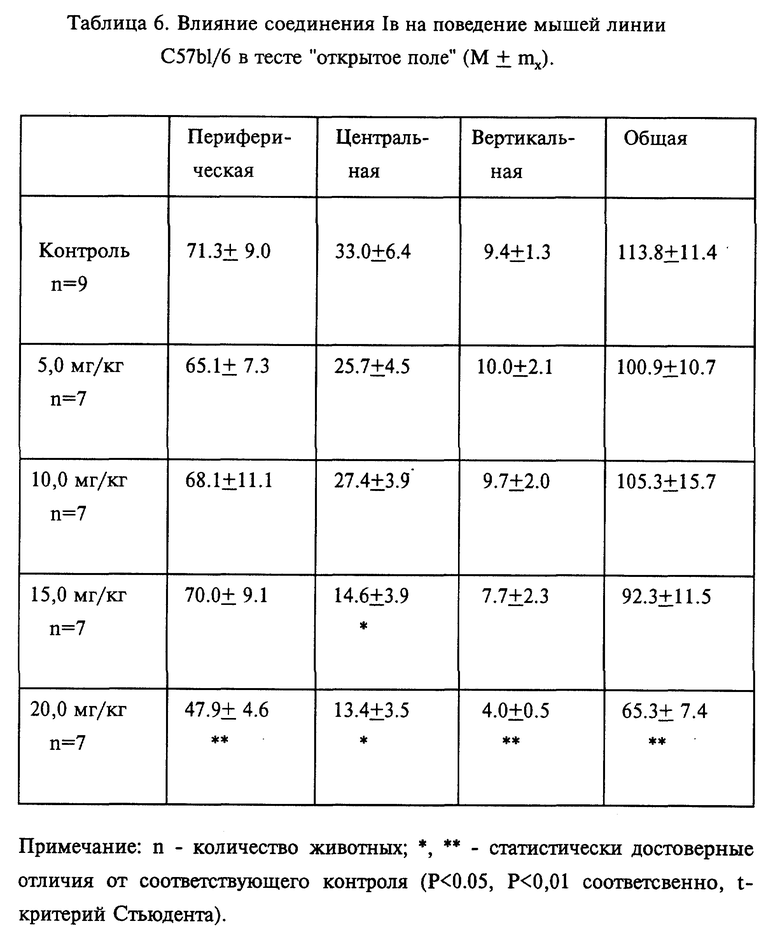
Соединение Iв, испытанное в диапазоне доз от 0,5 мг/кг до 15,0 мг/кг, в дозах 1,0 мг/кг, 2,0 мг/кг, 5,0 мг/кг и 10,0 мг/кг повышало периферическую и общую двигательную активность мышей линии Balb/c, тогда как в дозе 15,0 мг/кг уровень двигательной активности опытных животных не отличался от контрольной группы (табл. 5). У животных линии C 57 B 1/6 не наблюдали изменения поведения в диапазоне доз от 5,0 до 15,0 мг/кг. Лишь в дозе 20,0 мг/кг соединение 1в статистически достоверно снижало все виды двигательной активности мышей данной линии (табл. 6).
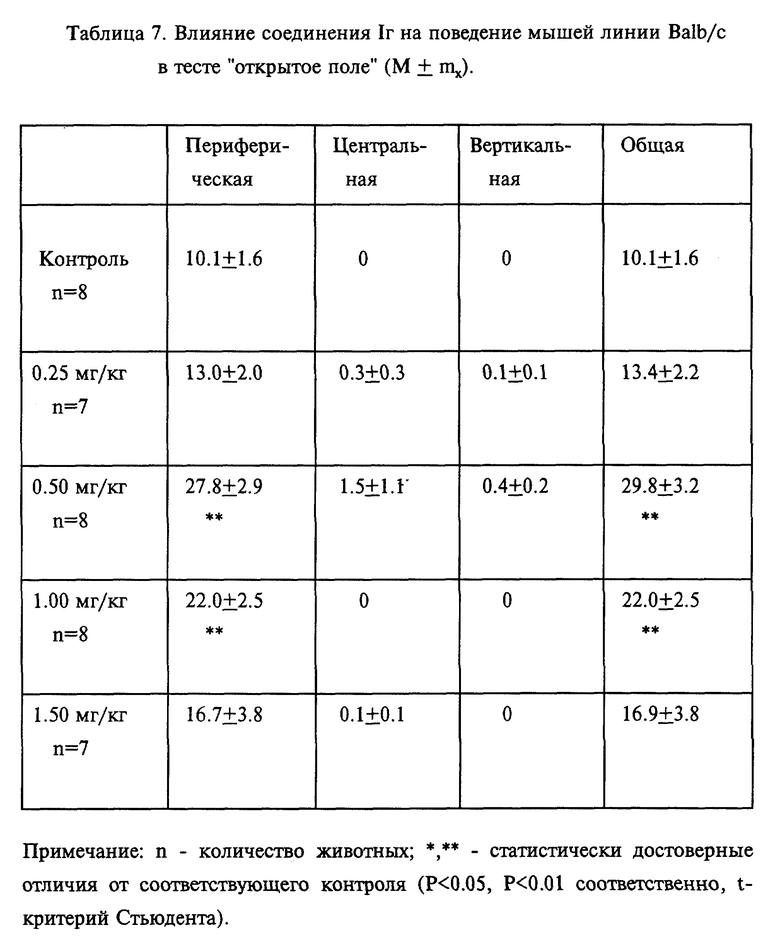
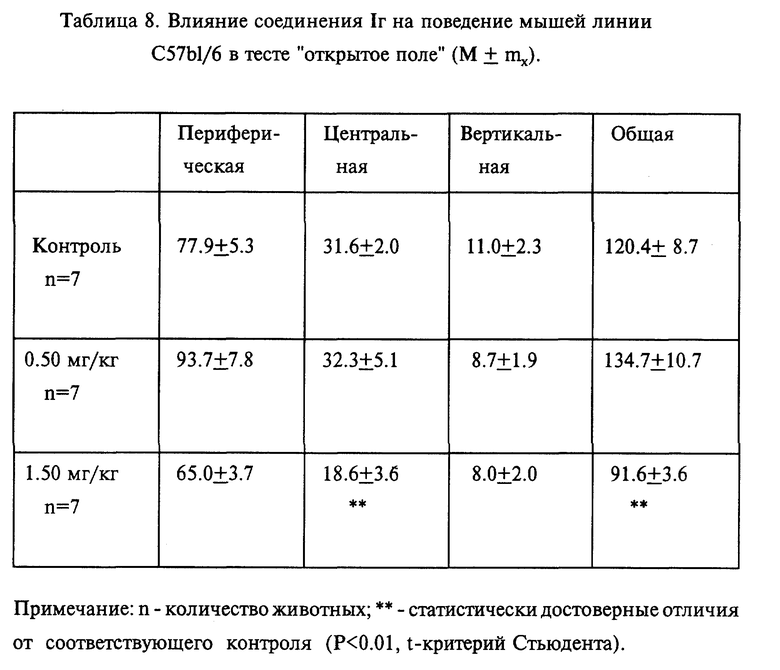
Данные, представленные в табл.7, показывают, что соединение 1 г повышает уровень двигательной активности мышей линии Balb/c в дозах 0,5 мг/кг и 1,0 мг/кг. В тоже время ингибирующий двигательную активность эффект этого соединения у мышей линии C 57 B 1/6 наблюдали уже в дозе от 1,5 мг/кг (табл.8).
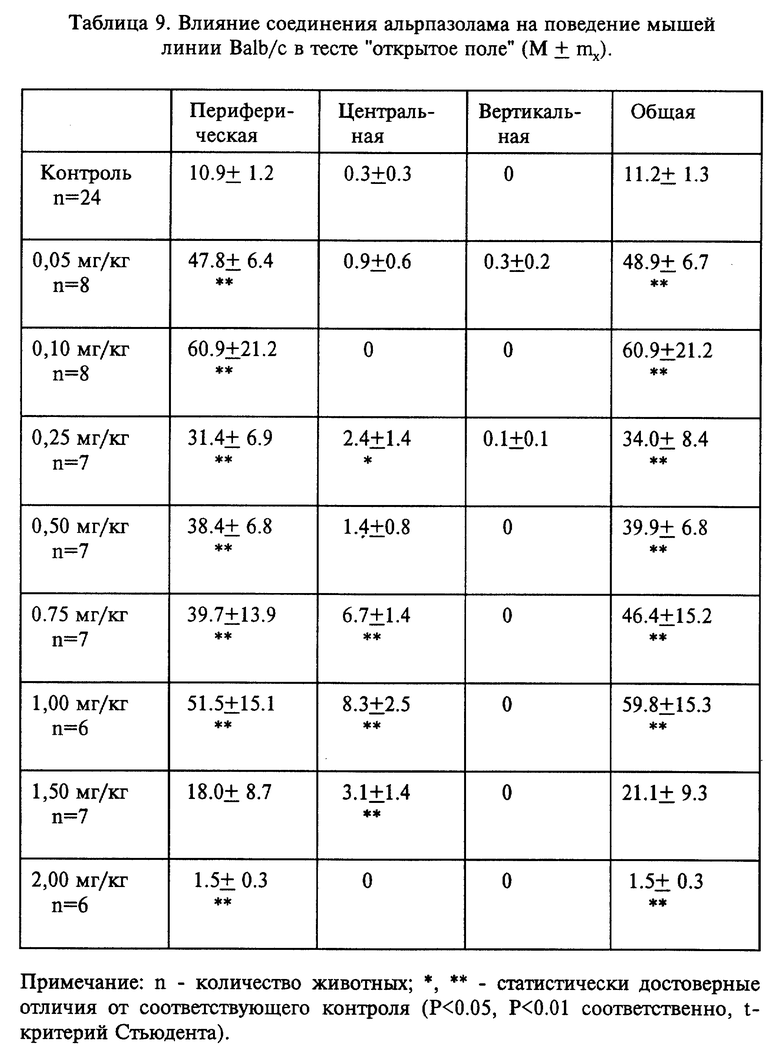
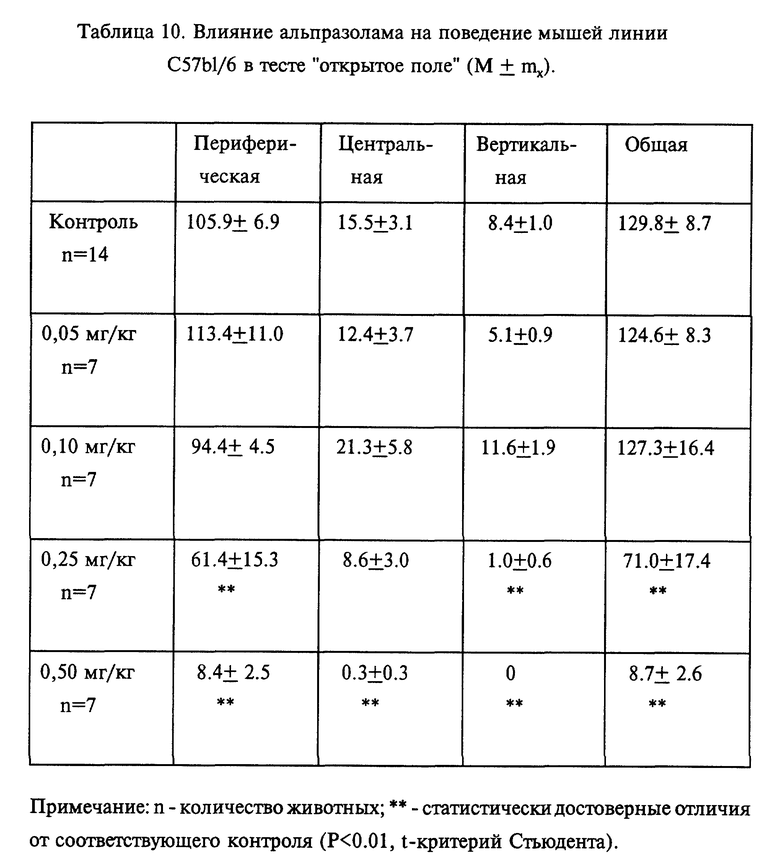
Использованный в качестве препарата сравнения альпразолам (ксанакс) заметно активировал поведение мышей Balb/c в диапазоне доз от 0,05 мг/кг до 1,0 мг/кг, тогда как в дозе 2,0 мг/кг двигательная активность животных данной линии была ниже контрольных показателей (табл. 9). Однако у мышей C 57 B 1/6 статистически значимое снижение уровня двигательной активности наблюдали, уже начиная с дозы 0,25 мг/кг (табл. 10).
Оценивая результаты проведенного скрининга с позиции использованного нами фармакогенетического подхода, основные принципы которого были изложены во введении к данному разделу, можно заключить, что наиболее интересными и перспективными с точки зрения анксиоселективности их фармакологического действия, являются соединения Iа и Iв. Действительно, оба эти препарата характеризовались диапазоном доз, активировавших поведение мышей линии Balb/c в тесте ОП, которые значительно превосходили аналогичный диапазон для гидазепама (С.Б.Середенин, Ю.А.Бледнов, А.Д.Дурнев и соавт. Гидазепам. Киев: Наукова Думка, 1992, с.92) и альпрозолама (Ю.А.Бледнов, М.М.Козловская, М. Маула и др. Актуальные вопросы экспериментальной и клинической фармакологии. Под ред. В.Е.Новикова. Смоленск, 1994, с.13-15).В то же время для обоих соединений было характерно снижение их седативной активности относительно препаратов сравнения, что проявлялось в увеличении дозировок, ингибировавших поведение мышей линии C 57 B 1/6 в тесте ОП. Исходя из ранее сформулированных принципов, можно предположить, что оба отобранных соединения обладают более выраженной степенью анксиселективности, чем ранее изученный гидазепам, а также альпразолам. Однако необходимо отметить заметное превосходство по данному показателю соединения Iа в сравнении с соединением Iв. Поэтому для дальнейшего более углубленного изучения транквилизирующего действия, а также оценки возможных побочных эффектов, было отобрано соединение Iа, обладавшее наиболее выраженным активирующим компонентом анксиолитического действия в первой серии экспериментов.
Изучение анксиолитического действия отобранного соединения проводилось в опытах на беспородных крысах-самцах весом 180-200 г в условиях общепринятой для этой цели методики столкновения питьевого и оборонительного рефлексов при действии внезапного болевого раздражителя как экстремального фактора (Т. А. Воронина, Ю.И.Вихляев, Т.Л.Гарибова, Л.Н.Неробкова и др. Феназепам. Киев: Наукова Думка, 1982, с. 89,93,146). Эксперимент начинали с тренировки крыс с целью выработки у них чувства жажды и навыка взятия воды из поилки в экспериментальной камере. Для этого животных содержали на сухом корме в течение 24 часов и затем помещали в камеру, где они получали воду в течение 5 минут. Через сутки после тренировки крысе через 5 сек после начала питья наносили электрическое раздражение пропусканием тока (0,5 А) через поилку. Таким образом, столкновением двух рефлексов питьевого и оборонительного создавалась экстремальная ситуация, при которой страх получения болевого раздражения удерживал животное от взятия воды. В дальнейшем в течение 5 мин регистрировали количество взятий воды из поилки, которые наблюдали несмотря на получение при этом каждый раз электроболевого раздражения.
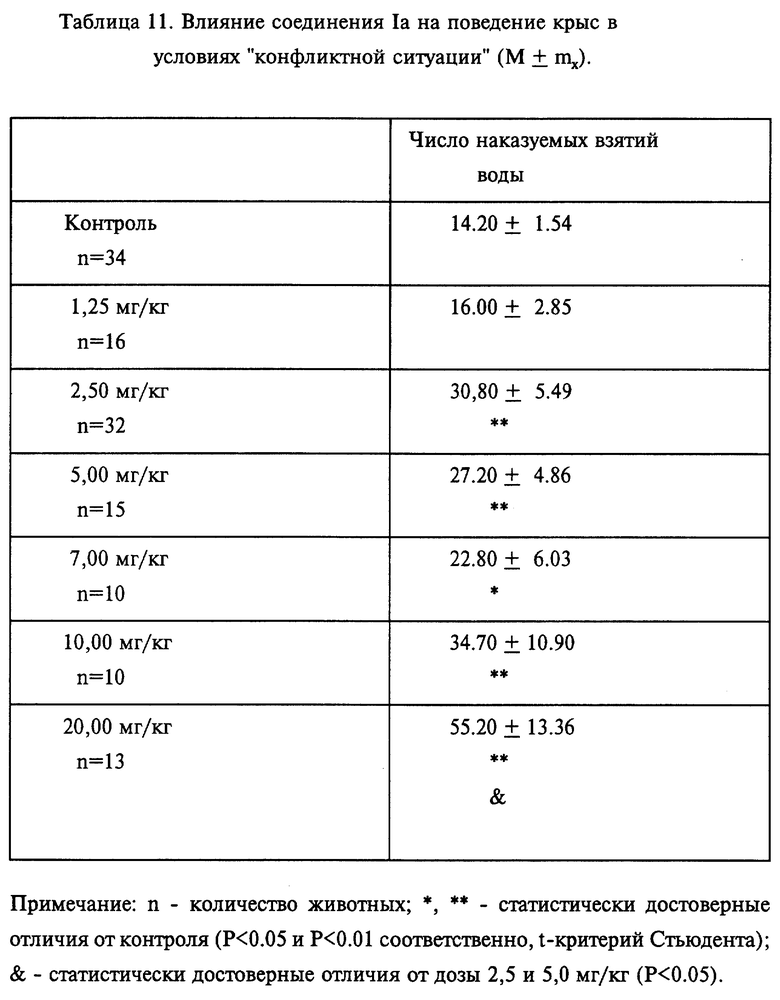
Контрольные животные в создаваемой ситуации делали в среднем от 8 до 14 попыток наказуемых взятий воды из поилки (табл. 11). Соединение Iа в широком диапазоне испытанных доз от 1 мг/кг до 20 мг/кг (в/бр) обладает отчетливым действием в создаваемой ситуации, устраняя чувство страха при действии болевого раздражителя, что обычно интерпретируется как анксиолитический эффект. Это выражается в увеличении в 2-4 раза по сравнению с контролем числа наказуемых взятий воды из поилки. При этом общая двигательная активность животных в экспериментальной камере заметно не изменялась. Таким образом, на основании проведенных экспериментов можно заключить, что соединение Iа обладает выраженным анксиолитическим действием в широком диапазоне доз без сопутствующих признаков седации или миорелаксации.
Анксиолитическую активность отобранного соединения Iа изучали также в тесте "приподнятого крестообразного лабиринта" (ПКС), который позволяет выявлять как анксиолитическую, так и анксиогенную активность различных фармакологических средств у крыс (S.Pellow, P.Chopin, S.E.File et al., J. Neurosci. Metohods, 1985, v. 14, p. 149-167) и мышей (J.Rateud, F.Darche, F. Piot et al., Brain Res.,1991, v.548, p.315-317]. Выполненный из плексиглаза лабиринт имеет форму креста с двумя открытыми (длина - 22 см, ширина - 5 см), двумя закрытыми (длина - 22 см, ширина - 5 см, высота стенок - 15 см) рукавами и центральной площадкой (5х5 см). Кроме того, лабиринт приподнят на высоту 25 см. В работе были использованы мыши-самцы линии Balb/c весом 20-22 г (питомник "Столбовая"). Животных содержали в условиях лабораторного вивария в клетках по 10 особей в каждой, в течение не менее двух недель до начала эксперимента, на стандартной диете, при свободном доступе к воде, при 12-часовом световом режиме (свет с 8.00 до 20.00). Все эксперименты проводили в период времени с 9.00 до 13.00. Все соединения вводили внутрибрюшинно в виде их водной суспензии после предварительного тщательного растирания субстанций с несколькими каплями Tween-80 за 30 мин до начала эксперимента из расчета 0,1 мл раствора на 10 г веса животного. Через 30 мин после введения препаратов животное выдерживали в темноте в течение 1 мин и затем помещали на центральную площадку в направлении к одному из открытых рукавов. В течение 5 мин фиксировали отдельно время пребывания животного в отмытых рукавах и центральной площадке, а также количество забегов в открытые и закрытые рукава. Эксперимент проводили при комнатном освещении. Статистическую обработку результатов проводили, оценивая на первом этапе влияние различных доз испытуемого соединения на поведение животных методом однофакторного дисперсионного анализа по методу Ньюмена-Кьюлса. Статистическую обработку проводили методами компьютерного анализа с помощью статистического пакета "Pharmacologic Calculation System" (R.J.Tallarida and R.B.Murray (Eds.), Manual of Pharmacologic Calculation with Computer Programs, 2end Edition, Springer-Verlag, New York, 1986).
На фиг. 1 представлены данные по влиянию одного из препаратов сравнения - альпразолама на поведение мышей линии Balb/c в условиях ПКС. Видно, что в дозах от 0.01 мг/кг до 0.25 мг/кг альпразолам статистически достоверно увеличивал время пребывания экспериментальных животных в открытых рукавах лабиринта (фиг. 1А), а также процент забегов в открытые рукава (в дозах 0.1 и 0.25 мг/кг) (фиг. 1Г), что интерпретируется как анксиолитический эффект. В то же время в диапазоне доз от 0.01 до 0.25 мг/кг повышение времени пребывания в открытых рукавах сопровождалось увеличением общего числа забегов в открытые и закрытые рукава (фиг. 1В), что может свидетельствовать о развитии активирующего действия, свойственного бензодиазепиновым транквилизаторам (Г. Я. Авруцкий, А.А.Недува. Лечение психических больных. М.: Медицина, 1981, с. 493). Однако в диапазоне доз от 0.25 мг/кг до 1.0 мг/кг наблюдалось дозозависимое увеличение времени задержки животного в центральной площадке лабиринта (фиг. 1Б), что, вместе со значительным снижением (ниже контрольного уровня) в дозе 1.0 мг/кг, как общего числа забегов (фиг. 1В), так и процента забегов в отмытые рукава (фиг. 1Г), свидетельствует об одновременном развитии седативного действия. Таким образом, полученные результаты позволяют вычленить три дозовых диапазона в спектре фармакологической активности альпразолама, в которых данный препарат обладает различными фармакологическими эффектами: 1-анксиолитическое действие с активирующим компонентом (транквило-активирующее); 2- анксиолитическое действие с седативным компонентом (транквило-седативное); 3- седация. Вместе с тем необходимо отметить, что все три группы эффектов, характерных для альпразолама, развиваются в достаточно узком диапазоне доз (от 0.01 мг/кг до 1.0 мг/кг) и взаимно перекрываются.
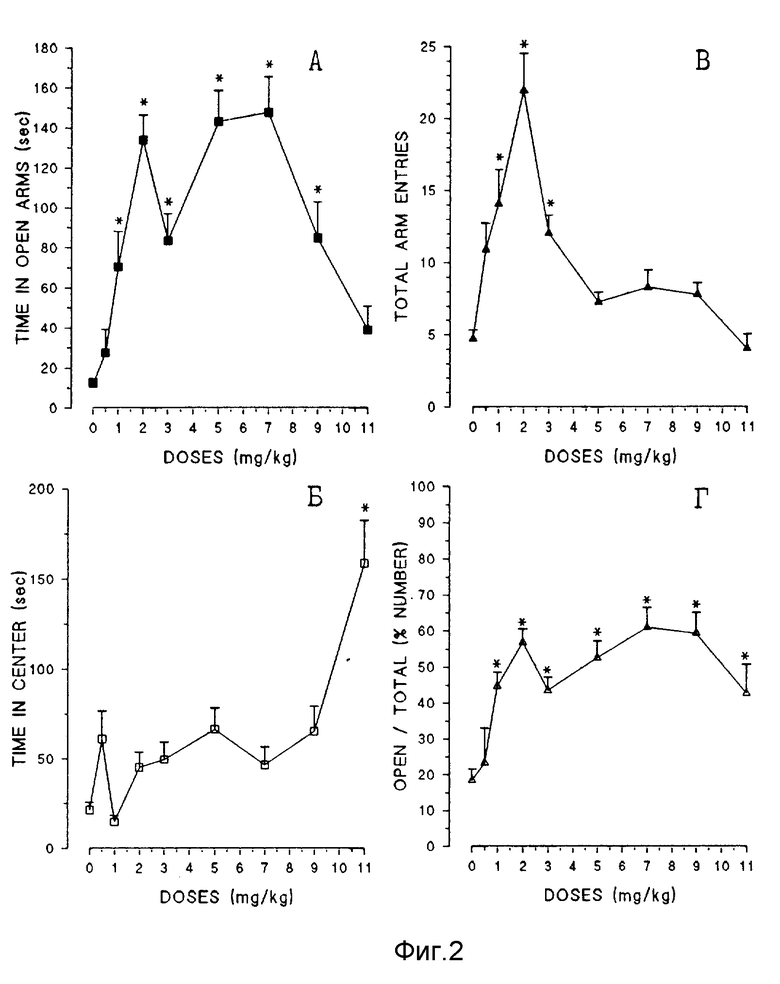
В следующей серии экспериментов было изучено действие другого препарата сравнения - гидазепама на поведение животных Balb/c в тесте ПКС. Оказалось, что в диапазоне доз от 1.0 мг/кг до 9.0 мг/кг гидазепам статистически достоверно увеличивал как общее время пребывания животных в открытых рукавах лабиринта (фиг. 2А), так и процент забегов в открытые рукава (фиг. 2Г), что можно оценить как развитие анксиолитического действия. Однако увеличение общего числа забегов (двигательная активность) наблюдали только в диапазоне доз от 1.0 мг/кг до 3.0 мг/кг (фиг. 2В), а стистически достоверное повышение времени задержки на центральной площадке только в максимально испытанной дозе -11.0 мг/кг (фиг.2Б). Таким образом, для гидазепама можно выделить те же три группы эффектов, развивающихся в различных дозовых диапазонах, что и для альпразолама. Однако селективность различных вариантов анксиолитического действия гидазепама оказалась значительно выше в сравнении с альпразоламом.
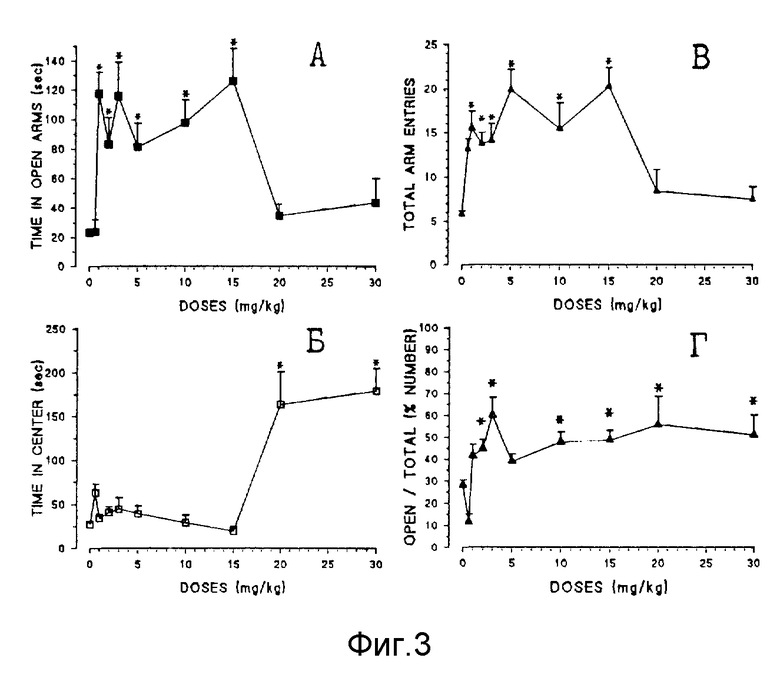
На фиг. 3 представлены данные по влиянию отобранного на первом этапе исследований соединения 1а на поведение мышей Balb/c в тесте ПКС. Видно, что время пребывания животных в открытых рукавах лабиринта (фиг. 3А) и процент забегов в открытые рукава (фиг. 3Г) были повышены в сравнении с контрольными показателями после введения соединения Iа в дозах от 1 мг/кг до 15 мг/кг. В том же дозовом диапазоне наблюдали статистически достоверное увеличение общего числа забегов в рукава лабиринта (фиг. 3В). В то же время заметное развитие седации выявлялось только после введения соединения Iа в дозах 20,0 и 30,0 мг/кг (фиг. 3Б). Таким образом, исходя из вышеприведенного фармакологического анализа поведения, описываемого в данной тестовой системе, можно заключить, что в сравнении с гидазепамом и альпразоламом, спектр психофармакологической активности соединения Iа характеризуется прежде всего наличием селективного анксиолитического эффекта с преимущественно активирующим компонентом, при резко сниженном седативном действии.
Для непосредственной оценки возможной седативной активности в следующей серии экспериментов было изучено влияние соединения Iа на спонтанную двигательную активность мышей Balb/c и C 57 B 1/6 в приборе "Optovarimex", как было описано ранее (С.Б.Середенин, Ю.А-Бледнов, А.Д.Дурнев и соавт. Гидазепам. Киев: Наукова Думка,1992, с.92). Животных помещали в прозрачные клетки группами по 3 мыши на клетку и выдерживали в течение 5-ти дней в условиях лабораторного вивария при свободном доступе к пище и воде. В день эксперимента животные получали в/бр инъекцию суспензии изучаемого соединения или физиологического раствора (контрольная группа) и в течение 30 минут содержались в знакомой клетке, после чего эти клетки помещали в прибор "Optovarimex", где с помощью инфракрасных датчиков измеряли суммарную двигательную активность экспериментальной группы животных. Данные, представленные в табл. 12, 13, демонстрируют, что лишь в дозе 30 мг/кг избранное вещество достоверно снижает уровень спонтанной двигательной активности (ниже контрольных показателей) у мышей обеих линий. Таким образом, представленные экспериментальные данные свидетельствуют, что соединение Iа в широком диапазоне доз (до 30 мг/кг) не обладает седативным действием.
Острая токсичность измерялась в опытах на белых беспородных мышах при внутрибрюшинном введении испытуемых соединений в виде их суспензии в 1% растворе крахмала. Для соединения Iа величина LD50, рассчитанная по общепринятому методу Литчфилда-Уилкоксона, оказалась равной 803,4 мг/кг (при 95% доверительном интервале 540,2-1194,7 мг/кг). Выявленная острая токсичность является довольно низкой и не сильно отличается от токсичности других известных препаратов с бензодиазепиновой структурой (Т.А.Воронина. Гидазепам. Киев: Наукова Думка,1992, с. 63-75).
Пояснения к чертежам.
Фиг. 1. Влияние альпразолама на поведение мышей Balb/c в "приподнятом крестообразном лабиринте".
По оси ординат: А - Время в открытых рукавах (сек); Б - время задержки в центре лабиринта (сек); В - общее число забегов в рукава; Г- % забегов в открытые рукава от общего числа забегов. По оси абсцисс: дозы препарата (мг/кг). * - статистически достоверные отличия от контроля (P<0,05, Ньоман-Кьюлс тест).
Фиг. 2. Влияние гидазепама на поведение мышей Balb/c в "приподнятом крестообразном лабиринте".
По оси ординат: А - Время в открытых рукавах (сек); Б - время задержки в центре лабиринта (сек); В - общее число забегов в рукава; Г - % забегов в открытые рукава от общего числа забегов. По оси абсцисс: дозы препарата (мг/кг). * - статистически достоверные отличия от контроля (P<0,05, Ньюман-Кьюлс тест).
Фиг. 3. Влияние соединения Iа на поведение мышей Balb/c в "приподнятом крестообразном лабиринте".
По оси ординат: А - Время в открытых рукавах (сек); Б - время задержки в центре лабиринта (сек); В - общее число забегов в рукава; Г - % забегов в открытые рукава от общего числа забегов. По оси абсцисс: дозы препарата (мг/кг). * - статистически достоверные отличия от контроля (P<0,05, Ньюман-Кьюлс тест).
| название | год | авторы | номер документа |
|---|---|---|---|
| АНКСИОЛИТИЧЕСКОЕ СРЕДСТВО | 1999 |
|
RU2175229C2 |
| АНКСИОЛИТИЧЕСКОЕ СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНКСИОЛИТИЧЕСКОГО ДЕЙСТВИЯ | 1999 |
|
RU2155065C1 |
| ЗАМЕЩЕННЫЕ 2-[2-(3-ОКСОМОРФОЛИН-4-ИЛ)ЭТИЛТИО]БЕНЗИМИДАЗОЛЫ, ОБЛАДАЮЩИЕ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2373202C2 |
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ СЕЛЕКТИВНОЙ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2061686C1 |
| СРЕДСТВА, ОБЛАДАЮЩИЕ АНКСИОЛИТИЧЕСКИМИ СВОЙСТВАМИ | 2008 |
|
RU2398761C2 |
| АНКСИОЛИТИЧЕСКОЕ СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНКСИОЛИТИЧЕСКОГО ДЕЙСТВИЯ | 2014 |
|
RU2580311C1 |
| 13-[(2S)2-АМИНО-4-КАРБОКСИБУТАНОИЛ]-1,4,7,10- ТЕТРАОКСА-13-АЗАЦИКЛОПЕНТАДЕКАН ГИДРОХЛОРИД, ОБЛАДАЮЩИЙ АНТИАМНЕСТИЧЕСКИМ И АНТИГИПОКСИЧЕСКИМ ДЕЙСТВИЕМ | 1987 |
|
RU1512079C |
| Фармацевтическая композиция на основе N-бензил-N-метил-1-фенилпирроло [1,2-a] пиразин-3-карбоксамида | 2017 |
|
RU2689396C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ ДЕЙСТВИЕМ | 2011 |
|
RU2475250C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 2011 |
|
RU2464990C1 |



Изобретение относится к новым производным 1,4-бензодиазепина общей формулы I, где R1-бром, R2-CH3O, NHNH2, R3-H, галоген, обладающим селективной анксиолитической активностью с преимущественно активирующим компонентом. Вышеуказанные соединения в широком диапазоне доз обладают выраженным анксиолитическим действием, которое не сопровождается побочными седативным и миорелаксантным эффектами. Они имеют низкую токсичность и могут найти применения в психиатрической практике, а также для профилактики эмоционально-стрессовых расстройств в качестве дневных транквилизаторов. 3 ил., 13 табл.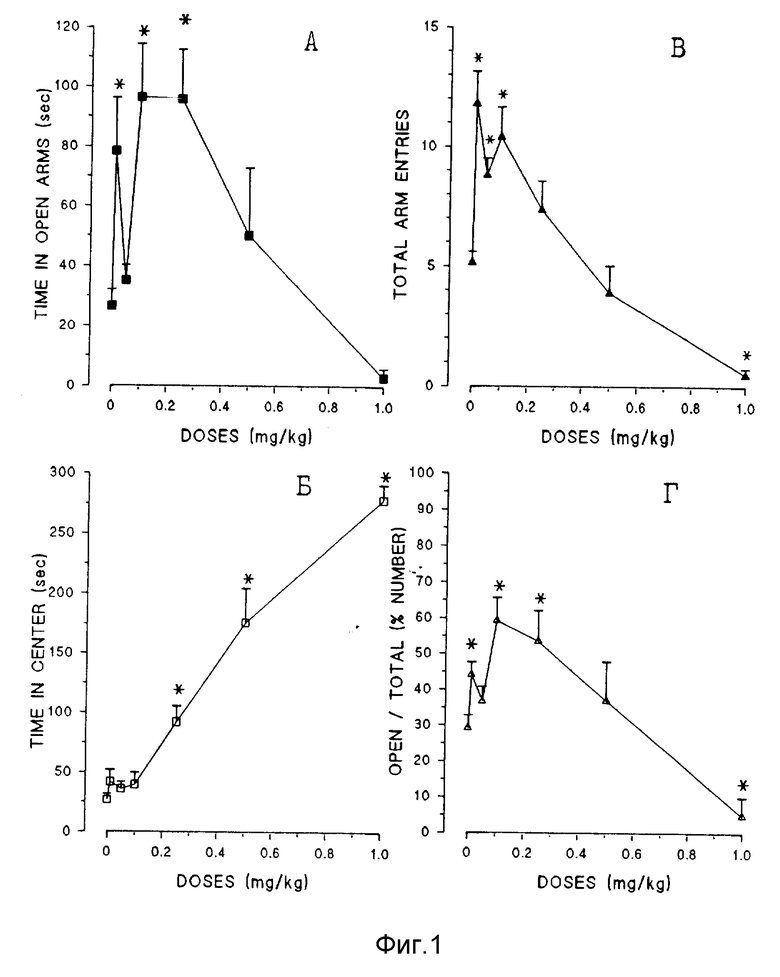
Производные 1,4-бензодиазепина общей формулы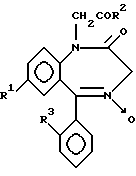
где R1 - бром;
R = CH3O, NHNH2;
R3 - H, галоген,
обладающие селективной анксиолитической активностью.
| А.В.Богатский, С.А.Андронати, Н.Я.Головенко | |||
| Транквилизаторы | |||
| - Киев: Наукова Думка, с | |||
| Аппарат для нагревания окружающей его воды | 1920 |
|
SU257A1 |
| SU, 953819 (Физико-химический институт АН УССР), 1988. | |||
Авторы
Даты
1999-07-20—Публикация
1995-07-12—Подача