ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится в целом к способам лечения или профилактики инфекционных респираторных агентов, в частности вирусов, в частности вируса гриппа, путем введения агентов, в частности антител или их активных фрагментов, в частности, нейтрализующих антител, непосредственно в дыхательные пути, в том числе интраназально или ингаляционно. Изобретение относится к композициям, подходящим для ингаляционного или интраназального введения, и лечению, и введению, протоколам и способам лечения или профилактики путем ингаляционного или интраназального введения антитела (антител) или сочетания интраназального или ингаляционного введения с внутрибрюшинным или внутривенным введением антител.
УРОВЕНЬ ТЕХНИКИ
[0002] Грипп является ведущей причиной смерти и заболеваний и поражает верхние и нижние дыхательные пути. Вирус гриппа вызывает высоко инфекционное заболевание органов дыхания, что приводит к более 200000 госпитализаций и 36000 жертв в США во время сезонов обострения. В глобальном масштабе у 20% детей и 5% взрослых развивается симптоматический грипп каждый год (Nicholson, K.G. et al (2003) Lancet 362: 1733-1745). Заболеваемость и смертность зависит от степени вирулентности штамма гриппа, взаимодействия хозяина с вирусом, возраста и иммунного статуса. В дополнение к сезонным эпидемиям с некоторой регулярностью появляются пандемические штаммы гриппа. Из-за отсутствия ранее существовавшего иммунитета против основных вирусных антигенов пандемический грипп может распространяться быстро, часто вызывая более тяжелое заболевание, чем сезонный грипп (Swartz, K.А. & Luby, J.P. (2007) Тех Med 103: 31-34). Например, пандемический штамм 1918-1919 "Испанка" был самой смертоносной чумой 20-го века, заразив 32% мирового населения и приведя к более чем 20 миллионам смертей (Webster, R.G. (1999) Proc Natl Acad Sci USA 96: 1164-1166). Недавний вирус 2009 года H1N1 распространился среди 61 миллионов человек в США, что привело, по оценкам, к 274000 госпитализаций с апреля 2009 года по апрель 2010 года (Lagace-Wiens, P.R. et al (2010) Crit Care Med 38: e1-9). Эта пандемия привела к закрытию школ и коммерческих учреждений из-за неопределенности, как реагировать на угрозу.
[0003] Есть три типа вирусов гриппа, гриппы А, В и С. Вирусы человеческого гриппа А и В вызывают сезонные эпидемии заболевания. Инфекции гриппа типа С вызывают умеренные респираторные заболевания и, как считается, не вызывают эпидемии. Вирусы гриппа А подразделяются на подтипы на основе двух белков на поверхности вируса: гемагглютинина (Н) и нейраминидазы (N). Есть 17 различных подтипов гемагглютинина и 10 различных подтипов нейраминидазы. Вирусы гриппа А могут быть далее разбиты на различные штаммы. Текущие подтипы вирусов гриппа А, найденные в людях, - грипп А (H1N1) и грипп A (H3N2). Вирусы гриппа В не делятся на подтипы, но могут быть разбиты на две различные линии. Грипп A (H1N1), A (H3N2) и грипп В включены в ежегодные вакцины против гриппа.
[0004] В настоящее время в человеческой популяции циркулируют пять видов клинически значимых вирусов гриппа, три гриппа А, а также два гриппа В. Вирус гриппа типа А подразделяется на две отдельные филогенетические группы, 1 и 2. Группа 1 включает подтипы гемагглютинина H1, Н2, Н5, Н6, Н8, Н9, Н11, Н13 и Н16. Группа 2 включает Н3, Н4, Н7, Н10, Н14 и Н15. В настоящее время соответствующие циркулирующие вирусы гриппа группы 1 имеют подтип H1, который дополнительно разделен на типы человеческого и свиного происхождения, и в настоящее время соответствующие циркулирующие вирусы гриппа группы 2 имеют подтип H3. Вирусы гриппа А ответственны за большую часть сезонных заболеваний, с доминированием H3 вирусов в восьми из последних двенадцати сезонов гриппа в Соединенных Штатах (CDC Seasonal flu; United States Surveillance Data). В 1968 году вирус H3 стал причиной одной из трех основных пандемий гриппа XX века, и с того времени H3 вирус остается заметным болезнетворным агентом человека. Помимо людей, вирусы гриппа H3 обычно заражают птиц, свиней и лошадей. Вирус гриппа В циркулирует в организме человека в течение более чем 100 лет, и современные штаммы разделены на две линии, Yamagata и Victoria. В последнее время трехвалентная вакцина против гриппа расширилась до четырехвалентной вакцины, охватывающей обе линии гриппа В, а также вирусы H1 и H3.
[0005] Современные способы лечения гриппа не являются адекватными и могут быть неэффективными. Несмотря на распространение вакцинации восприимчивость к гриппу остается. Факторы, способствующие восприимчивости, включают (1) неполный охват вакцинацией, например, в случае пандемии 2009 года H1N1, когда имел место дефицит вакцины, (2) годы, такие как 2008 год, когда в вакцинном препарате были слабо представлены циркулирующие штаммы, (3) уменьшение эффективности вакцинации у пожилых людей, поскольку в среднем диапазон эффективности составляет от 40-50% в возрасте 65 лет и только 15-30% в возрасте 70 лет, и (4) появление пандемических штаммов, не представленных в сезонных вакцинах. Кроме того, лекарственная устойчивость против антивирусной терапии для лечения гриппа в настоящее время стала серьезной проблемой. Устойчивость к адамантанам (амантидин и римантадин), препаратам, которые действуют на белок М2 и ингибируют вирусное слияние, увеличилась с 1,9% в 2004 году до 14,5% в течение первых 6 месяцев сезона гриппа 2004-2005, и в настоящее время превзошла 90% (Sheu, T.G. et al (2011) J Infect Dis 203: 13-17). Устойчивость к Тамифлю, противовирусному препарату, который ингибирует белок гриппа нейраминидазу, резко увеличилось с 1-2% для вирусов H1N1 в течение сезона гриппа 2006-2007 до 12% к 2007-2008 и превысила 99% для сезонных вирусов H1N1 в 2009 году. К счастью, пандемический штамм H1N1 в 2009 году был восприимчив к Тамифлю, что, вероятно, привело к уменьшению числа смертей во время пандемии. Таким образом, существует острая потребность в новых средствах против гриппа.
[0006] Разработка терапевтических антител против гриппа получает все больше внимания, так как недавно были обнаружены консервативные эпитопы молекулы гемагглютинина (НА). Было несколько сообщений о выделении и характеристике моноклональных антител (MAb) человека, способных распознавать и нейтрализовать широкий ряд подтипов вируса гриппа А. Многие из них ориентированы на гликопротеин гемагглютинина (НА), что выявляет наиболее надежные нейтрализующие антитела при вакцинации или природной инфекции. НА состоит из двух субъединиц НА1 и НА2, которые являются важнейшими компонентами при вирусной инфекции. НА1 участвует в присоединении к сиаловой кислоте клеточного рецептора хозяина, и НА2 опосредует слияние вирусной мембраны и мембраны эндосомы. MAb CR6261 является хорошо изученным антителом, которое связывается с вирусами H1 и другими подтипами (Н5) в группе 1, при этом связывается с НА2 субъединицами (Throsby M et al (2008) PLoS ONE 3: e3942; Eckert DC et al (2009) Science 324: 246-251; Friesen RHE et al (2010) PLoS ONE 5(2): e1906; US Patent 8,192,927). MAb CR8020 связывается с ближней к мембране областью НА2 вируса типа H3 и вируса другого подтипа (Н7), которые являются вирусами группы 2 (Eckert DC et al (2011) Science 333: 843-850). Антитело FI6v3 от исследователей из Швейцарии может связываться с эпитопом на вирусах группы 1 (H1) и 2 (H3), однако FI6 показало ограниченную эффективность у мышей (Corti D et al (2011) Science 333: 850-856). Палезе и его коллеги сообщили о защитных моноклональных антителах против вирусов гриппа H3 с использованием последовательной иммунизации мышей различными агглютининами (Wang ТТ et al (2010) PLoS Pathog 6(2): e1000796; US Application 20110027270). Используя этот подход, выделяли высоко реактивные антитела против H1 (Tan GS et al (2012) J Virol 86(11): 6179-6188).
[0007] В настоящее время хорошо разработаны обычные терапевтические дозы антител, составляющие несколько мг/кг, на основе научных исследований и клиническом опыте с многочисленными рекомбинантными антителами, в том числе для более чем двадцати моноклональных антител, которые были клинически утверждены в Соединенных Штатах (Newsome BW and Ernstoff MS (2008) Br J Clin Pharmacol 66(1): 6-19). Например, панитумумаб, полностью человеческое антитело против EGFR, одобренное для колоректального рака, вводят внутривенно в дозе 6 мг/кг в течение 1-1½ часов каждые 2 недели. При использовании среднего человеческого веса 70 кг это составляет 420 мг антитела на дозу.
[0008] Пока не существует моноклонального антитела, клинически одобренного для гриппа. Сообщения об исследованиях антител против гриппа в животных показывают, что необходимо, чтобы эффективный диапазон доз этих антител при введении внутривенно или внутрибрюшинно в терапевтических или профилактических целях составлял от 1 мг/кг до 100 мг/кг. В I фазе клинических испытаний в США некоторых из этих антител (CR6261, CR8020, TCN-032) используется эскалация дозы в исследованиях безопасности и толерантности от 2 мг/кг до 50 мг/кг (clinicaltrials.gov; NCT01390025, NCT01406418, NCT01756950). Большое количество материала представляет главное препятствие в развитии этой новой линии терапии антителами. В частности, системные дозы в этом диапазоне приводят к значительной стоимости материала, а также времени и кадровых расходам, связанных с введением. Таким образом, есть настоятельная необходимость либо увеличить эффективность и/или уменьшить количество материала, необходимого для терапии антителами или профилактики против гриппа, чтобы технология стала жизнеспособной альтернативой.
[0009] Цитирование ссылок в настоящем документе не должно истолковываться как допущение того, что они являются прототипом настоящему изобретению.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00010] В изобретении предложен новый способ и средство для эффективного лечения и профилактики вирусных инфекций, в том числе, в частности, вируса гриппа, путем введения нейтрализующего антитела (антител) непосредственно в респираторный тракт или дыхательные пути, в том числе путем интраназального или ингаляционного введения. Изобретение демонстрирует, что прямая доставка нейтрализующих антител в дыхательные пути, в том числе ингаляционная (IH) и/или интраназальная (IΝ) доставки и введения, является более эффективной при более низких дозах, чем системное введение (IV или IP) того же антитела в тех же количествах. Лечение или профилактика IN или IH доставляемым антителом до или даже после воздействия вируса или инфекции являются эффективными.
[00011] Настоящее изобретение относится к ингаляционным или интраназальным композициям, эффективным для лечения или профилактики вирусной инфекции у млекопитающего, включающим одно или более нейтрализующее вирус моноклональное антитело. В первом аспекте настоящее изобретение относится к ингаляционным или интраназальным композициям, эффективным для лечения или профилактики вирусной инфекции у млекопитающего, включающим нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы 1 мг/кг или менее. В изобретении предложены ингаляционные или интраназальные композиции, эффективные для лечения или профилактики вирусной инфекции у млекопитающего, включающие одно или более нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы 10 мг/кг или менее. В изобретении предложены ингаляционные или интраназальные композиции, эффективные для лечения или профилактики вирусной инфекции у млекопитающего, включающие одно или более нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы менее 1 мг/кг. В изобретении предложены ингаляционные или интраназальные композиции, эффективные для лечения или профилактики вирусной инфекции у млекопитающего, включающие одно или более нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы менее 0,5 мг/кг. В изобретении предложены ингаляционные или интраназальные композиции, эффективные для лечения или профилактики вирусной инфекции у млекопитающего, включающие одно или более нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы менее 0,1 мг/кг.
[00012] В конкретном аспекте, в изобретении предложены ингаляционные или интраназальные композиции, эффективные для лечения или профилактики вируса гриппа, в том числе инфекции вируса гриппа у млекопитающего, включающие одно или более нейтрализующие вирус моноклональное антитело. В дополнительном аспекте настоящее изобретение относится к ингаляционным или интраназальным композициям, эффективным для лечения, профилактики или уменьшения передачи вируса гриппа у млекопитающего, включающим комбинацию нейтрализующих грипп антител, направленных против циркулирующих штаммов вируса гриппа. В одном аспекте настоящее изобретение относится к композиции для интраназального введения, состоящей из комбинации нейтрализующих грипп антител, направленных против циркулирующих штаммов вируса гриппа, в частности, состоящих из антитела к H1 гриппа А антитела, антитела к H3 гриппа А и антитела против гриппа В. В одном аспекте композиция включает антитела против гриппа А, эффективные против или в дальнейшем эффективные против других штаммов вируса гриппа, в том числе, но не ограничиваясь ими, против штаммов Н2, Н5 и Н7.
[00013] Композиции подходят и применимы для использования и для лечения или профилактики вируса гриппа. В конкретном аспекте настоящего изобретения композиции пригодны для уменьшения передачи респираторного вируса. Композиции подходят для снижения уровня передачи вируса гриппа.
[00014] В одном аспекте композиция (композиции) содержат нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы 0,5 мг/кг или менее. В одном аспекте композиция (композиции) содержат нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы 0,1 мг/кг или менее. В другом аспекте композиция (композиции) содержат нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы 0,05 мг/кг или менее.
[00015] В одном аспекте композиция (композиции) содержат нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы менее 0,5 мг/кг. В одном аспекте композиция (композиции) содержат нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы менее 0,1 мг/кг. В другом аспекте композиция (композиции) содержат нейтрализующие вирус моноклональные антитела в виде единичной однократной дозы менее 0,05 мг/кг.
[00016] В примерном варианте осуществления изобретения композиции могут содержать одно или более нейтрализующих вирус моноклональных антител, которые являются нейтрализующими вирус гриппа антителами. Композиция может в частности содержать одно или более нейтрализующее вирус гриппа антитело, направленное против гриппа А, в частности, против гриппа А группы 1 и/или гриппа А группы 2. Композиция может в частности содержать одно или более нейтрализующие вирус гриппа антитело, направленное против гриппа В, в частности, против линий Yamagata и/или Victoria. Композиция может содержать одно или более нейтрализующее вирус гриппа антитело, направленное против вируса гриппа А, в частности направленное против вируса гриппа А группы 1 и группы 2, в том числе вируса H1 и/или вируса H3 и/или против вируса гриппа В, в том числе линий Yamagata и/или Victoria. В конкретном аспекте композиция может содержать одно или более нейтрализующее вирус гриппа антитело, направленное против вируса гриппа А, в частности в отношении вируса гриппа А группы 1 и группы 2, в том числе вируса H1 и/или вируса H3 и одного или более нейтрализующих вирус гриппа антител против вируса гриппа В, в том числе линий Yamagata и/или Victoria. Композиция может содержать комбинацию антител, содержащих одно или более антител, направленных против вируса гриппа А, в частности в отношении вируса гриппа А группы 1 и группы 2, в том числе вируса H1 и/или вируса H3, и одного или более нейтрализующих вирус гриппа антител против вируса гриппа В.
[00017] В соответствии с настоящим изобретением, в том числе в качестве примера в работах, в настоящем документе представлены многочисленные и разнообразные нейтрализующие антитела с повышенной эффективностью при более низких дозах при введении в дыхательный тракт или дыхательные пути, например, путем интраназального или ингаляционного введения. Таким образом, композиция согласно настоящему изобретению может содержать нейтрализующее антитело или его фрагмент, в том числе фрагмент Fab, которое способно нейтрализовать вирус гриппа, и которое может быть направлено против вируса гриппа А и/или вируса гриппа В. Композиция согласно изобретению может содержать одно или более нейтрализующее вирус гриппа антитело, выбранное из CR6261, CR8020, CR9114, 6F12, GG3, 5А7, Mab53 и Mab579, их фрагментов, синтетических или рекомбинантных производных, гуманизированных или химеризированных версий их, и антител, имеющих их CDR из тяжелой или легкой цепей..
[00018] Состав может содержать, в частности, нейтрализующее грипп антитело 6F12, его фрагменты, синтетические или рекомбинантные производные, его гуманизированные или химеризированное версии, и антитела, имеющие его CDR тяжелой и легкой цепей. Композиция может содержать, в частности, нейтрализующее грипп антитело GG3, его фрагменты, синтетические или рекомбинантные производные, его гуманизированные или химеризированное варианты, а также антитела, имеющие его CDR тяжелой и легкой цепей. Композиция может содержать, в частности, нейтрализующее грипп антитело 5А7, его фрагменты, синтетические или рекомбинантные производные, его гуманизированные или химеризированное версии, и антитела, имеющие его CDR тяжелой и легкой цепей. Композиция может содержать, в частности, нейтрализующее грипп антитело Mab53, его фрагменты, синтетические или рекомбинантные производные, его гуманизированные или химеризированное версии, и антитела, имеющие его CDR тяжелой и легкой цепей. Композиция может содержать, в частности, нейтрализующее грипп антитело Mab579 его фрагменты, синтетические или рекомбинантные производные, его гуманизированные или химеризированное версии, и антитела, имеющие его CDR тяжелой и легкой цепей.
[00019] Композиция может содержать, в частности, одно или более нейтрализующее вирус гриппа антитело, направленное против гриппа А, в частности, против гриппа А группы 1 и/или группы 2. В примерном варианте осуществления изобретения композиция может содержать одно или более нейтрализующее вирус гриппа антитело, направленное против гриппа А, в частности, против гриппа А группы 1, в частности, против подтипа вируса H1, где одно или более антитело выбрано из CR6261 или СА6261, 6F12, GG3, mAb53 или их активных фрагментов. Композиция может содержать одно или более нейтрализующее вирус гриппа антитело, направленное против гриппа А, в частности, против гриппа А группы 2, в особенности против подтипа вируса H3, где одно или более антитело выбрано из CR8020 или СА8020, mAb579 или их активных фрагментов. В одном аспекте настоящего изобретения композиция может содержать нейтрализующее грипп антитело CR9114 или СА9114, или их активные фрагменты, где указанное антитело обеспечивает нейтрализующее вирус гриппа антитело против гриппа А и/или против гриппа В. Композиция может содержать одно или более нейтрализующее вирус гриппа антитело, направленное против гриппа В, в частности, против линии Yamagata и/или Victoria, где одно или более антитело выбрано из 5А7, CR9114, СА9114 или их активных фрагментов.
[00020] Нейтрализующие вирус антитела могут быть фрагментами антител, способными к нейтрализации. В одном аспекте во фрагменте антитела не хватает Fc и/или у него недостаточная и сниженная эффекторная функция. Фрагмент антитела может быть выбран из Fab, Fab' и F(ab')2. Нейтрализующие вирус антитела или фрагменты могут быть получены из рекомбинантного белка, могут быть рекомбинантно экспрессированы, в том числе в качестве активного фрагмента, или могут быть получены или разработаны с помощью других средств или способов, в том числе средств или способов, доставляющих нейтрализующее антитело или фрагмент (фрагменты) в дыхательный тракт или дыхательные пути, в том числе путем доставки генетического материала или ДНК, или экспрессии векторной ДНК, например, путем доставки ДНК или РНК, кодирующей нейтрализующее антитело или фрагмент (фрагменты).
[00021] Композиция согласно изобретению может дополнительно содержать фармацевтически приемлемый наполнитель, носитель или разбавитель. Композиция может содержать наполнитель, носитель, разбавители или добавки, пригодные или подходящие для назального или легочного введения и интраназального или ингаляционного введения. Композиция может содержать наполнитель, носитель, разбавители или добавки, пригодные или целесообразные для стимуляции или усиления иммунного ответа и/или опосредованных антителами клеточных или системных эффектов. Композиция может включать иммунологический посредник или стимулятор иммунного ответа.
[00022] Изобретение относится к способам лечения, профилактики или уменьшению или ингибированию передачи вируса, в частности респираторного вируса, в частности вируса гриппа. Изобретение относится к способу лечения или профилактики вирусной инфекции у млекопитающего, подвергающегося, имеющего контракт или страдающего от респираторного вируса, включающему введение интраназально (IN) или инагляционно указанному млекопитающему одного или более моноклонального антитела, способного нейтрализовать респираторный вирус.
[00023] В одном из аспектов способа моноклональное антитело представляет собой антитело IgG. В одном из аспектов способа респираторный вирус является вирусом гриппа. Респираторный вирус может быть вирусом гриппа типа А или В, или неизвестного или неопределенного типа. В одном аспекте антитело представляет собой нейтрализующее антитело, способное нейтрализовать и направленное против гриппа А или В. В одном аспекте антитело представляет собой комбинацию моноклональных антител, способных нейтрализовать и направленных против вирусов гриппа А и В.
[00024] В соответствии со способом антитело можно вводить после инфицирования или после предположительной инфекции, экспозиции или проявления клинических симптомов. В одном аспекте антитело можно вводить в течение периода времени до 8 часов после инфицирования. Альтернативно, антитело вводят в течение периода времени до 24 часов после инфицирования. В другом альтернативном варианте осуществления изобретения антитело вводят в течение периода времени до 48 часов после инфицирования. В еще одном альтернативном варианте антитело вводят в период времени до 72 часов после инфицирования. Антитела могут быть введены, в том числе в одной дозе или в нескольких последовательных дозах, до 8 часов после инфицирования (8hpi), 12hpi, 18hpi, 24hpi, 36hpi, 48hpi, 72hpi, 1 день после инфицирования, 2 дня после инфицирования, 3 дня после инфицирования, 4 дня после инфицирования, 5 дней после инфицирования, 6 дней после инфицирования, 7 дней после инфицирования, неделю после инфицирования, 10 дней после инфицирования, 2 недели после инфицирования, 3 недели после инфицирования, 4 недели после инфицирования, месяц после инфицирования, месяцы после инфицирования.
[00025] Антитело можно вводить в виде единичной однократной дозы. Однократная доза может быть менее 10 мг/кг массы тела, менее 5 мг/кг массы тела, менее 2 мг/кг массы тела или менее 1 мг/кг массы тела. Однократная доза может быть менее 1 мг/кг массы тела, менее 0,5 мг/кг, менее 0,1 мг/кг, менее 0,05 мг/кг. Антитело можно вводить в виде многократных доз. Дозы могут быть одинаковыми, или каждая доза может варьировать в каждой дозе, или может быть первоначальная высокая доза, а затем более низкие дозы. Однократная доза или дозы, или любая доза, может быть менее 1 мг/кг массы тела, менее 0,5 мг/кг, менее 0,1 мг/кг, менее 0,05 мг/кг. Начальная доза может быть более 1 мг/кг и дальнейшие или последующие дозы могут быть ниже или могут быть менее 1 мг/кг.
[00026] Антитело можно вводить в дыхательный тракт или дыхательные пути в нескольких дозах менее 1 мг/кг на дозу. Антитело можно вводить интраназально или ингаляционно в виде многократных доз менее 1 мг/кг на дозу. В таком аспекте множественные дозы можно вводить по меньшей мере через 2 часа между дозами и до 72 часов или позже после предположительной инфекции, воздействия или проявления клинических симптомов. Таким образом, дозы антител можно вводить через минуты или часы, или дни друг от друга. Дозы антител могут быть введены после инфицирования или после предполагаемых инфекций или воздействия через часы или дни друг от друга. Дозы антител могут быть введены после инфицирования или после предполагаемого инфицирования или воздействия в течение 2, 4, 6, 8, 12, 24, 36, 48 или 72 часов после.
[00027] Протокол введения или способ согласно изобретению может, в частности, содержать первое введение антител в дыхательный тракт или дыхательные пути, в частности, инагаляционное или интраназальное введение антител в сочетании с или после второго, или одного или более дополнительных введений (введения) не ингаляционным или интраназальным путем, например системной доставкой, такой как введение (введения) IP (внутрибрюшинное введение) или IV (внутривенное введение). Таким образом, способ может включать дополнительное введение IP или IV вирус-специфического моноклонального антитела, где дополнительно вводимое антитело представляет собой нейтрализующее или не-нейтрализующее антитело. Антитело, дополнительно вводимое внутрибрюшинно или внутривенно, может быть тем же, как и антитело, вводимое интраназально или ингаляционно, или может быть другим или измененным антителом, как антитело, вводимое интраназально или ингаляционно. Антитела, введенные дополнительно, например, через IP или IV, могут быть введены одновременно, последовательно или после вводимых ингаляционно или интраназально антител. Любое такое последующее введение может быть осуществлено через несколько часов, и может быть через 2, 4, 6, 8, 12 или до 24 часов. Последующие введения могут быть осуществлены через дни, 1 дня, 2 дней или 3 дней. Последующее введение могут быть осуществлены через дни, до 7 дней, неделю спустя или недели спустя. Последующие введения могут быть в виде единичной однократной дозы или в виде многократных доз через несколько часов и/или дней, и/или недель.
[00028] В другом аспекте настоящее изобретение обеспечивает протокол для введения моноклонального антитела против респираторного вируса, в частности вируса гриппа, включающий введение первой интраназальной или инагаляционной дозы нейтрализующих антител и последующую или одновременно вводимую вторую дозу, или одну или более дополнительную дозу (доз) антител, которые не введены в дыхательные пути, и могут быть введены внутрибрюшинно или внутривенно, где антитело второй дозы или дополнительной дозы является таким же, как антитело первой дозы, или другим антителом. Антитело второй дозы или дополнительной дозы (доз) может быть измененным или модифицированным антителом, которое изменено или модифицировано, чтобы быть более эффективным при IV или IP-доставке. В одном аспекте настоящего изобретения антитело первой дозы может не иметь эффекторной функции, такое как Fab антитело, антитело второй дозы может иметь эффекторную функцию, иметь Fc, или может быть изменено, чтобы иметь повышенную эффекторную функцию.
[00029] Протокол может включать несколько ингаляционных или интраназальных доз антител, и может включать несколько доз того же или альтернативного антитела для IP или IV доставки. В одном аспекте настоящего протокола субъект или пациент, которому вводят антитела, может быть исследован, например, на клинические проявления заболевания или вирусной инфекции, и доза или дозы могут быть изменены, снижены или повышены, или введены чаще или реже в зависимости от статуса пациента или субъекта и от инфекции или болезни.
[00030] В одном из аспектов протокола, респираторный вирус может быть вирусом гриппа, и может быть вирусом гриппа А или вирусом гриппа В, или неизвестным или неопределенным вирусом гриппа. Антитело второй дозы, которая не вводится в дыхательный тракт, может быть нейтрализующим или не-нейтрализующим антителом и может иметь эффекторную функцию или повышенную эффекторную функцию.
[00031] В одном из аспектов протокола первая интраназальная или ингаляционная доза может составлять менее 1 мг/кг, не более 0,5 мг/кг, не более 0,1 мг/кг. Вторую или дополнительную IP или IV дозу, в частности, вводят в более высокой дозе, чем первую интраназальную или ингаляционную дозу. Вторую или дополнительную IP или IV дозу, в частности, вводят в дозе по меньшей мере в 10 раз выше количества антител, чем в первой интраназальной или ингаляционной дозе. Вторая или дополнительная IP или IV доза может быть по меньшей мере 1 мг/кг, по меньшей мере 5 мг/кг, по меньшей мере 10 мг/ кг, по меньшей мере 15 мг/кг, или больше 10 мг/кг, или больше 20 мг/кг, или больше 50 мг/кг.
[00032] В другом аспекте протокола первая интраназальная или ингаляционная доза может быть меньше 1 мг/кг, а вторая IP или IV доза по меньшей мере в 10 раз выше в мг/кг, чем первая интраназальная доза. В дополнительном аспекте протокола первая интраназальная или ингаляционная доза может быть меньше 1 мг/кг, а вторая IP или IV доза по меньшей мере в 50 раз выше в мг/кг, чем первая интраназальная доза. В дополнительном аспекте протокола первая интраназальная или ингаляционная доза может быть меньше 0,5 мг/кг, а вторая IP или IV доза составляет по меньшей мере 5 мг/кг.
[00033] Первая интраназальная или ингаляционная доза может быть меньше 1 мг/кг, и ее вводят в течение 24 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов. Первая интраназальная или ингаляционная доза может быть меньше 1 мг/кг, и ее вводят в течение 48 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов. Первая интраназальная или ингаляционная доза может быть меньше, чем 1 мг/кг, и ее вводят в течение 72 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов.
[00034] Еще один аспект настоящего изобретения относится к способу ингибирования передачи респираторного вируса, включающий введение интраназально или ингаляционно субъекту, подвергаемому воздействию, риску воздействия или проявляющему клинические признаки инфекции респираторного вируса, нейтрализующих вирус антител в единичной однократной единичной дозе 1 мг/кг или менее. Однократная единичная доза может быть меньше 10 мг/кг или меньше 1 мг/кг. Однократная единичная доза согласно способу может быть меньше 0,5 мг/кг или меньше 0,1 мг/кг, или меньше 0,05 мг/кг.
[00035] Вирус может быть, в частности, вирусом гриппа, может быть вирусом гриппа А или В, или неизвестным вирусом или неопределенным вирусом гриппа, и антитело может быть антителом IgG.
[00036] Нейтрализующее вирус антитело указанного способа может быть введено в течение 48 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов. Нейтрализующее вирус антитело может быть введено в течение 24 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов. Нейтрализующее вирус антитело может быть введено в течение 12 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов. Нейтрализующее вирус антитело может быть введено через более, чем 24 часа, и в течение 72 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов. Нейтрализующее вируса антитело может быть введено во время или после первоначального проявления клинических симптомов.
[00037] В соответствии со способом ингибирования передачи антитело можно вводить в дозе менее 0,5 мг/кг, в дозе менее 0,1 мг/кг, в дозе менее 0,05 мг/кг.
[00038] Другие цели и преимущества станут очевидны специалистам в данной области из рассмотрения следующего описания, которое выполнено со ссылкой на следующие иллюстративные фигуры.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[00039] ФИГУРА 1. Нейтрализующие и не-нейтрализующие Mab являются эффективными при введении IP после инфекции. Животных инокулировали 10XLD50 вируса гриппа H3 (адаптированный для мышей A/Victoria/361/2011, в настоящем документе обозначенный Vic/11 MA) и обрабатывали через 24 часа после инфицирования (24hpi) 10 мг/кг IP различными отмеченными антителами - 6Р15, 1Р19, 1K17 (все не нейтрализующие) и СА8020 (нейтрализующее) - и PBS, или без вируса в качестве контроля. Наблюдали за массой тела животных каждый день в течение 14 дней после инфицирования и строили график процента от начальной массы тела в день 0.
[00040] ФИГУРА 2. IP-доставка нейтрализующих и не-нейтрализующих Mab является профилактически эффективной. Животных инокулировали 10XLD50 вируса гриппа H3 VIC/11 MA и обрабатывали через 1 час до инфицирования (-1hpi) 10 мг/кг IP различными отмеченными антителами -1K17, 1Р19, 1Н16 (все не-нейтрализующие) и СА8020 (нейтрализующие) - и PBS, или контролем изотипа антител. Наблюдали за массой тела животных (10 животных в каждой группе) ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00041] ФИГУРА 3. Антитело, введенное IV или IP, показало схожую эффективность. Животных инокулировали 10XLD50 вируса гриппа H3 VIC/11 MA и обрабатывали через 1 ч после инфекции (1hpi) 10 мг/кг антителом СА8020 IP или IV PBS в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00042] ФИГУРА 4. Показано сравнение нейтрализующих и не-нейтрализующих антител при интраназальном (IN) введении в сравнении с внутрибрюшинным (IP) введением. Животных инокулировали 10XLD50 вируса гриппа H3 VIC/11 MA и обрабатывали через 24hpi 10 мг/кг нейтрализующим антителом СА8020 IN или IP или не-нейтрализующим антителом 6Р15 IN или IP, и PBS в качестве контроля. При доставке нейтрализующего Mab IN терапевтическая эффективность увеличивалась по сравнению с IP-введением такой же дозы того же антитела. В противоположность этому, когда вводили не нейтрализующее Mab IN, терапевтическая эффективность снижалась по сравнению с IP-ведением в той же дозе. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00043] ФИГУРА 5. Представлены результаты сравнения терапевтической эффективности IN и IP введения Fab-фрагмента антитела СА6261 антитела против вируса H1. Животных инокулировали 10XLD50 вируса гриппа H1 и обрабатывали через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующими СА6261 Fab IN или IP, с обработкой PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0. Все дозы Fab СА6261 антитела, вводимые IN, продемонстрировали большую эффективность, что любая доза при IP-введении. Введение нейтрализующего Fab IP не демонстрировало детектируемой эффективности даже при самой высокой дозе, 10 мг/кг.
[00044] ФИГУРА 6. Представлены результаты сравнения терапевтической эффективности IN введения Fab-фрагмента антитела СА8020 против Fab-фрагмента не-нейтрализующего антитела 6Р15 против вируса H3. Животных инокулировали 10XLD50 вируса гриппа H3 и обрабатывали 24hpi 10 мг/кг нейтрализующими Fab-фрагментами СА8020, не нейтрализующими Fab-фрагментами 6Р15 или Fab против вируса H1, и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0. Вводимые IN Fab-фрагменты антитела СА8020 продемонстрировали эффективность, за исключением Fab 6Р15.
[00045] ФИГУРА 7. Показано сравнение IN и IP введения в сопоставимых дозах, и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H1 (A/Puerto Rico/8/1934) и обрабатывали IN или IP через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующими Mab СА6261, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00046] ФИГУРА 8. Показано сравнение IN и IP-введения в сопоставимых дозах и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H3 и обрабатывали IN или IP через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующими Mab СА8020, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00047] ФИГУРА 9. Показано сравнение IN и IP-введения в сопоставимых дозах и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H1 и обрабатывали IN или IP через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующими Mab СА6261, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00048] ФИГУРА 10. Показано, что сверхмалые дозы, введенные IN, способны обеспечить защиту. Антитела СА8020, введенные через 8hpi, защищали от 10XLD50 вируса H3 в таких дозах, как 0,005 мг/кг. Животных инокулировали 10XLD50 вируса гриппа H3 и обрабатывали IN через 8hpi 0,1 мг/кг, 0,05 мг/кг, 0,01 мг/кг и 0,005 мг /кг нейтрализующими Mab СА8020, IP через 8hpi 0,1 мг/кг Mab СА8020 с PBS и без вируса в качестве контроля. IP-введение при 0,1 мг/кг было эквивалентно PBS и не показывало никакого эффекта. Все дозы IN показывали эффективность. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00049] ФИГУРА 11. Показано исследование эффективности повторной сверхнизкой дозировки нейтрализующих антител. Животных инокулировали 10XLD50 вируса гриппа H3 и обрабатывали повторно IN дозированием Mab СА8020 через 8hpi, 32hpi и еще раз через 56hpi. Повторное дозирование проводили при 0,005 мг/кг на дозу и при 0,001 мг/кг нейтрализующих Mab СА8020, с PBS и без вируса в качестве контроля. Оба повторных режима дозирования показали эффективность. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00050] ФИГУРА 12. Показана модель интраназального введения против пути системного введения. Клиренс вируса опосредован прежде всего эффекторной функцией (EF) на базолатеральной стороне в случае системного введения (в том числе IP и IV) и путем нейтрализации на апикальной стороне, взаимодействующей с дыхательными путями, в случае введения в дыхательные пути (в том числе интраназально и ингаляционно).
[00051] ФИГУРА 13A-13D. Показано исследование только IN введения или IP введения в сравнении с комбинацией введений по IN и IP пути, используя антитело СА6261 в качестве примера. Общая доза введения антитела составляла 2 мг/кг и показана на А и В, с базовой линией IN 0,3 мг/кг на А и IN введением 0,1 мг/кг на В. Общее введение 5 мг/кг показано на С и D, с базовой линией IN 0,3 мг/кг на С и IN введением 0,1 мг/кг на D. Во всех случаях введение IN совместно с IP намного превосходит только IP-введение и улучшено по сравнению только IN-введением. Введение 0,3 мг/кг IN СА6261 с 1,7 мг/кг IP, или 0,3 мг/кг IN СА6261 с 4,7 мг/кг IP не показало по существу никакого влияния вирусной инфекции и было эквивалентно результатам без вируса.
[00052] ФИГУРА 14. Показаны результаты сравнения терапевтической эффективности IN введения с введением антитела IP 6F12 против вируса H1. Животных инокулировали 10XLD50 вируса гриппа H1 PR8 и обрабатывали через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг 6F12, вводимого IN или IP, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0. Эквивалентные дозы Mab 6F12, вводимого IN, продемонстрировали большую эффективность, чем сопоставимые дозы при IP-введении. 6F12 вводили в дозах 1 мг/кг через 24hpi полностью защищенным от инфекции животным.
[00053] ФИГУРА 15. Показано сравнение IN и IP в сопоставимых дозах и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H1 (A/Puerto Rico/8/1934) и обрабатывали IP или IN через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующими Mab GG3, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00054] ФИГУРА 16. Показано сравнение IN и IP в сопоставимых дозах и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H1 (A/Puerto Rico/8/1934) и обрабатывали IN или IP через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующими Mab СА9114, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00055] ФИГУРА 17. Показано сравнение IN и IP в сопоставимых дозах и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H1 (A/California/07/09-мышь-адаптированный) и обрабатывали IN или IP через 24hpi 10 мг/кг, 1 мг/кг и 0,1 мг/кг нейтрализующим Mab СА6261, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных (10 животных в каждой группе) ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00056] ФИГУРА 18. Показано сравнение IN и IP в сопоставимых дозах и показано, что Mab, вводимые IN, от 10 до 100 раз более эффективны, чем Mab, вводимые IP. Животных инокулировали 10XLD50 вируса гриппа H1 (A/Puerto Rico/8/1934) и обрабатывали IN или IP через 72hpi 20 мг/кг, 10 мг/кг и 5 мг/кг нейтрализующими Mab СА6261, с PBS и без вируса в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00057] ФИГУРА 19. Показано комбинационное исследование введения только IN или IP в сравнении с комбинацией введения СА8020 антитела или 6Р15 путем IN или IP через 24hpi с 10XLD50 H3 вирусом (Victoria/11). Вводили общую дозу 0,6 мг/кг с введением 0,5 мг/кг IP и 0,1 мг/кг IN. В обоих случаях эффективность введения IN нейтрализующих антител была выше, чем при введении не-нейтрализующих антител.
[00058] ФИГУРА 20. Показано IN и IP-введение различных доз антител СА9114 через 24 hpi вирусом гриппа В (B/Malaysia). Антитела СА9114 вводили IN или IP в количестве 10 мг/кг, 1 мг/кг или 0,1 мг/кг. Антитела СА8020 и без вируса показаны в качестве контроля. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00059] ФИГУРА 21 демонстрирует исследования на мышах с вирусом гриппа В (B/Florida), чтобы оценить эффективность ряда антител против гриппа В. Все антитела вводили в дозе 1 мг/кг IN 24 hpi с 10-кратным LD50 вируса В. Испытуемыми антителами были 43K16, 59G1, 112А22, 11G23, 114022, СА9114 и 40J7, как указано. PBS и без вируса приведены в качестве контролей. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00060] ФИГУРА 22. Показаны различные антитела против вируса В, протестированные на эффективность против гриппа B/Malaysia. Все антитела вводили в дозе 1 мг/кг IN 24hpi с 10XLD50 вируса В. Испытуемыми антителами были 43K16, 59G1, 112А22, 114G23, 114022 и СА9114. В качестве контроля были изотипы Mab, PBS и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00061] ФИГУРА 23 демонстрирует исследование эффективности на животных различных антител против гриппа В, вводимых через 8hpi, против вируса B/Malaysia. Все антитела вводили в дозе 1 мг/кг через 8hpi с 10XLD50 вируса. Испытуемыми антителами были СА9114, 54Н5, 110С16, 43K16, 59G1, 114G23, 43J23, 112А22, 5808, 55K6, 114D22 и 40J7. В качества контроля были PBS и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00062] ФИГУРА 24. Показано исследование эффективности на животных с использованием смеси антител, содержащей антитело H1, антитело H3 и антитело против вируса гриппа В. В смеси антител использовали H1 антитело GG3, H3 антитело СА8020 и В антитело 43J23. В смеси каждое из антител вводили в дозе 1 мг/кг в одном объеме 50 мкл на дозу через 24hpi с 10xLD50 из B/Florida (вирус Yamagata В). Для сравнения В антитело 43J23 протестировали в одиночку против вируса B/Florida - 1 мг/кг 43J23 вводили через 24 hpi. Антитело СА9114 вводили IP в дозе 1 мг/кг 24hpi с B/Florida. В качества контроля использовали PBS и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00063] ФИГУРА 25 демонстрирует исследование эффективности использования смеси антител из H1 антитела GG3, H3 антитела СА8020 и антитела против вируса гриппа В 43J23 на животных. 1 мг/кг каждого из антител вводили через 24 часа после инфицирования (24hpi) с вирусом B/Malaysia. Для сравнения, антитело 43J23 против вируса В протестировали в одиночку против вируса B/Malaysia с введением 1 мг/кг 43J23 через 24 hpi, и антитело СА9114 вводили IP в дозе 1 мг/кг 24 hpi с B/Malaysia. В качества контроля были PBS и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00064] ФИГУРА 26. Показана эффективность смеси антитела (H1 антитела GG3, H3 антитела СА8020 и антител против вируса гриппа В 43J23), вводимой IN в сочетании каждого 1 мг/кг, с общим количеством 3 мг/кг антител в 50 мкл, 24hpi с вирусом гриппа А H1 PR8. Смесь сравнивали с антителом GG3 IN в одиночку, антителом СА6261, вводимом IP, и PBS. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00065] ФИГУРА 27 демонстрирует комбинационное исследование смеси антител против вируса H3 Vic/11. Антитела GG3, СА8020 и 43J23 вводили 24hpi каждое 1 мг/кг в смеси и наблюдали за массой тела. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0. Антитело СА8020 вводили отдельно в дозе 1 мг/кг IN или IP, и сравнивали с PBS в этом исследовании.
[00066] ФИГУРА 28. Показаны результаты смеси антител против гриппа GG3, СА8020 и 43J23, вводимой через 24hpi (каждое антитело в количестве 1 мг/кг в смеси, в общей сложности 3 мг/кг общего количества всех антител) против PBS после инфицирования каждым из подтипов вируса гриппа А H1, подтипов вируса гриппа А H3, вируса В (Yamagata) и вируса В (Victoria). Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0. Смесь трех антител была эффективна против всех протестированных вирусов, в частности в отношении всех и каждого из вирусов H1, H3, В (Yam) и В (Vic).
[00067] ФИГУРА 29. Показана оценка смеси из трех антител для защиты мышей от подтипов гриппа, используя массу тела как замену смерти. Мышей обрабатывали 10XLD50 гриппом А подтипа H1 или H3, или линиями вируса гриппа В Yamagata или Victoria и обрабатывали через 24 часа (24hpi) смесью антител Universal Influenza Cocktail, состоящей из трех антител - антитела 5а7, СА6261 и СА8020 - по 1 мг/кг каждое. Смесь трех антител была эффективной против инфекции, любых протестированных вирусов - вирусных инфекций H1, H3, В (Yam) и В (Vic).
[00068] ФИГУРА 30. Показана обработка подтипа вируса гриппа H3 через 24 часа после инфицирования антителом TRL579 (Mab579). Антитело 579 вводили в дозе 1 мг/кг IN через 24 hpi или 10 мг/кг IP через 24 часа после инфицирования вирусом 10XLD50 H3 Vic11. В качестве контроля были PBS и без вируса. Наблюдали за массой тела животных (5 животных в каждой группе) ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00069] ФИГУРА 31. Показана обработка вируса гриппа H1 через 24 часа после инфицирования антителом TRL53 (Mab53). Антитело 53 вводили в дозе 1 мг/кг IN через 24 hpi или 10 мг/кг IP через 24 часа после инфицирования вирусом 10XLD50 H1 Cal09. В качества контроля были PBS и без вируса. Наблюдали за массой тела животных (5 животных в каждой группе) ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00070] ФИГУРА 32. Показано исследование профилактического IN и IP введения за 3 или 4 дня до инфицирования вирусом. Антитела СА6261 вводили IN или IP за 3 или 4 дня до инфицирования 3XLD50 H1 вирусом гриппа A/Puerto Rico/8/1934 (обозначается как PR8). Антитело СА6261 вводили IN (0,1 мг/кг) или IP (0,1 мг/кг и 1 мг/кг) за 3 дня до инфицирования (-3dpi) или 4 дня до инфицирования (-4dpi) и инфицировали вирусом гриппа H1. В качестве контроля выступали без вируса и обработки. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00071] ФИГУРА 33. Показано исследования профилактического IN и IP введения за 5, 6 или 7 дней до инфицирования вирусом. Антитело СА6261 вводили IP (1 мг/кг) или IN (0,1 мг/кг) за 5, 6 или 7 дней до инфицирования вирусом 3XLD50 H1 гриппа PR8. В качестве контроля использовали Тамифлю (10 мг/кг перорально, два раза в день в течение пяти дней), без обработки и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00072] ФИГУРА 34. Показано исследования профилактического IN и IP введения за 5, 6 или 7 дней до инфицирования вирусом. Антитело СА6261 вводили IP (1 мг/кг) или в (1 мг на/кг) 5, 6 или 7 дней до инфицирования вирусом гриппа 3XLD50 H1 PR8. В качестве контроля использовали Тамифлю (10 мг/кг перорально, два раза в день в течение пяти дней), без обработки и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00073] ФИГУРА 35. Показано исследования профилактического IN и IP введения за 3 или 4 дня до инфицирования вирусом, с инфицированием вирусом при более высокой дозе 10XLD50. Антитело СА6261 вводили IN или IP в количестве 0,1 мг/кг за 3 или 4 дня до инфицирования вирусом 10XLD50 H1 PR8. В качестве контроля использовали без вируса и обработки. Наблюдали за массой тела животных (10 животных в каждой группе) ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[00074] ФИГУРА 36 показывает исследование профилактического IN и IP введения за 5, 6 или 7 дней до инфицирования вирусом, с проверкой вирусом при более высокой дозе 10XLD50. Антитело СА6261 вводили IP (1 мг/кг) или IN (1 мг на/кг) за 5, 6 или 7 дней до инфицирования вирусом 10XLD50 H1 гриппа PR8. В качестве контроля использовали Тамифлю (10 мг/кг перорально, два раза в день в течение пяти дней), без обработки и без вируса. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[0075] ФИГУРА 37 показывает IN введение антител 5А7, CR8033 и mAb809 через 24 hpi с 10XLD50 вируса гриппа В (B/Malaysia/2506/2004). Каждое антитело к гриппу В вводили IN в дозе 1 мг/кг. PBS использовали как контроль. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
[0076] Фигура 38 показывает IN введение антител 5А7, CR8033 и mAb809 через 24 hpi с 10XLD50 вируса гриппа В (B/Florida/05/2006). Каждое антитело к гриппу В вводили IN в дозе 1 мг/кг. PBS использовали как контроль. Наблюдали за массой тела животных ежедневно в течение 14 дней после инфицирования и строили график процентов от начальной массы тела в день 0.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00077] В соответствии с настоящим изобретением могут быть использованы обычные методики молекулярной биологии, микробиологии и рекомбинантной ДНК в пределах квалификации в данной области техники. Такие методы подробно описаны в литературе. См., например, Sambrook et al, "Molecular Cloning: A Laboratory Manual" (1989); "Current Protocols in Molecular Biology" Volumes I-III [Ausubel, R.M., ed. (1994)]; "Cell Biology: A Laboratory Handbook" Volumes I-III [J.E. Celis, ed. (1994))]; "Current Protocols in Immunology" Volumes I-III [Coligan, J.E., ed. (1994)]; "Oligonucleotide Synthesis" (M.J. Gait ed. 1984); "Nucleic Acid Hybridization" [B.D. Hames & S.J. Higgins eds. (1985)]; "Transcription And Translation" [B.D. Hames & S.J. Higgins, eds. (1984)]; "Animal Cell Culture" [R.I. Freshney, ed. (1986)]; "Immobilized Cells And Enzymes" [IRL Press, (1986)]; B. Perbal, "A Practical Guide To Molecular Cloning" (1984).
[00078] Таким образом, при использовании в настоящем документе, следующие термины будут иметь определения, изложенные ниже.
[00079] Антитела, использованные и названные в настоящем документе, включают те, которые имеют аминокислотные последовательности, опубликованные и общеизвестные, и включают антитела, белки, полипептиды, имеющие модификации известной или общеизвестной аминокислотной последовательности, сохраняющие или демонстрирующие по существу эквивалентную активность, включая нейтрализацию или активность узнавания и связывания. Соответственно, также рассматриваются белки, демонстрирующие по существу эквивалентную или измененную активность. Эти модификации могут быть преднамеренными, например, такие, как модификации, полученные с помощью сайт-направленного мутагенеза, или могут быть случайными, например, полученными путем мутаций в организме хозяев, которые производят комплекс или его названые субъединицы. Термин антитела включает белки, специфически указанные в настоящем документе, а также все их по существу гомологичные аналоги и аллельные варианты.
[00080] Ниже приведены примеры различных групп аминокислот: аминокислоты с неполярными группами R: аланин, валин, лейцин, изолейцин, пролин, фенилаланин, триптофан, метионин; аминокислоты с незаряженными полярными группами R: глицин, серии, треонин, цистеин, тирозин, аспарагин, глутамин; аминокислоты с заряженными полярными группами R (отрицательно заряженными при рН 6,0): аспарагиновая кислота, глутаминовая кислота; основные аминокислоты (положительно заряженными при рН 6,0): лизин, аргинин, гистидин (при рН 6,0); другой группой могут быть аминокислоты с фенильными группами: фенилаланин, триптофан, тирозин.
[00081] Еще одно группирование может быть в соответствии с молекулярной массой (то есть размером R-групп):
[00082] В частности предпочтительными заменами являются:
- Lys на Arg и наоборот, таким образом, что может быть сохранен положительный заряд;
- Glu на Asp и наоборот таким образом, что может быть сохранен отрицательный заряд;
- Ser на Thr таким образом, что может быть сохранена свободная -ОН-группа; и
- Gln на Asn таким образом, что может быть сохранена свободная NH2-группа.
[00083] Аминокислотные замены также могут быть введены, чтобы заменить аминокислоту с особенно предпочтительным свойством. Например, Cys может быть введен как потенциальный сайт для создания дисульфидных мостиков с другим Cys. His может быть введен, в частности, в качестве «каталитического» сайта (то есть His может действовать как кислота или основание и является наиболее распространенной аминокислотой в биохимическом катализе). Pro может быть введен из-за его особенной плоской структуры, которая вызывает -повороты в структуре белка.
[00084] Две аминокислотные последовательности являются «по существу гомологичными», когда по меньшей мере приблизительно 70% аминокислотных остатков (предпочтительно по меньшей мере 80%, и наиболее предпочтительно по меньшей мере приблизительно 90 или 95%) являются идентичными или представляют собой консервативные замены.
[00085] Нуклеиновые кислоты, кодирующие антитела, используемые в соответствии с применением и использованием в настоящем изобретении, могут быть использованы при подготовке и/или продуцировании антител или их активных фрагментов, использующихся в настоящем изобретении. Векторы, содержащие такие нуклеиновые кислоты, могут быть использованы для экспрессии или выделения антител, как это предусмотрено или используется в настоящем изобретении.
[00086] «Репликон» означает любой генетический элемент (например, плазмиду, хромосому, вирус), который функционирует в качестве автономной единицы репликации ДНК в естественных условиях; т.е. способен к репликации под своим собственным контролем.
[00087] «Вектор» означает репликон, такой как плазмида, фаг или космида, к которому другой сегмент ДНК могут быть присоединен таким образом, чтобы вызвать репликацию присоединенного сегмента.
[00088] «Молекула ДНК» относится к полимерной форме дезоксирибонуклеотидов (аденин, гуанин, тимин или цитозин) в любой их одноцепочечной форме, либо в виде двухцепочечной спирали. Этот термин относится только к первичной и вторичной структуре молекулы и не ограничивает ее какими-либо конкретными третичными формами. Таким образом, этот термин включает двухцепочечную ДНК, найденную, в частности, в линейных молекулах ДНК (например, рестрикционных фрагментах), вирусах, плазмидах и хромосомах. При обсуждении структуры конкретных двухцепочечных молекул ДНК, последовательности могут быть описаны в соответствии с обычными правилами, когда дается только последовательность в направлении 5' к 3' вдоль нетранскрибируемой цепи ДНК (т.е. цепи, имеющей последовательность, гомологичную мРНК).
[00089] Термин «сайт инициации репликации» относится к тем ДНК, которые участвуют в синтезе ДНК.
[00090] «Кодирующая последовательность» ДНК представляет собой последовательность двухцепочечной ДНК, которая транскрибируется и транслируется в полипептид в естественных условиях, когда находится под контролем соответствующих регуляторных последовательностей. Границы кодирующей последовательности определены стартовым кодоном на 5'(амино) конце и стоп-кодоном трансляции на 3' (карбоксильном) конце. Кодирующая последовательность может включать, но не ограничиваться ими, прокариотические последовательности, кДНК из эукариотической мРНК, геномные последовательности ДНК из эукариотических (от, например, млекопитающих) ДНК, и даже синтетические последовательности ДНК. Сигнал полиаденилирования и последовательность терминации транскрипции обычно будут расположены в 3'кодирующей последовательности.
[00091] Транскрипционные и трансляционные контролирующие последовательности - регуляторные последовательности ДНК, такие как промоторы, энхансеры, сигналы полиаденилирования, терминаторы и т.п., которые обеспечивают экспрессию кодирующей последовательности в клетке-хозяине.
[00092] «Последовательность промотора» представляет собой регуляторную область ДНК, способную связывать РНК-полимеразу в клетке и инициировать транскрипцию расположенной ниже (направление к 3') кодирующей последовательности. Для целей определения настоящего изобретения последовательность промотора ограничена на своем З'-конце по сайту инициации транскрипции и простирается вверх (5'направление), чтобы включить минимальное число оснований или элементов, необходимых для инициации транскрипции на уровнях, детектируемых выше фона. В промоторной последовательности будет найден сайт инициации транскрипции (удобно определяемый путем картирования с нуклеазой S1), а также белковые связывающие домены (консенсусные последовательности), ответственные за связывание РНК-полимеразы. Эукариотические промоторы часто, но не всегда, содержат «ТАТА»-боксы и «САТ»-боксы. Прокариотические промоторы содержат последовательности Шайна-Дальгарно в дополнение к -10 и -35 консенсусным последовательностям.
[00093] Термин «последовательность контроля экспрессии» представляет собой последовательность ДНК, которая контролирует и регулирует транскрипцию и трансляцию другой последовательности ДНК. Кодирующая последовательность находится «под контролем» транскрипционных и трансляционных управляющих последовательностей в клетке, когда РНК-полимераза транскрибирует кодирующую последовательность в мРНК, которая затем транслируется в белок, кодируемый кодирующей последовательностью.
[00094] Клетка была «трансформирована» экзогенной или гетерологичной ДНК, когда такая ДНК была введена внутрь клетки. Трансформирующая ДНК может быть или может не быть интегрирована (ковалентно связана) в хромосомную ДНК, составляющую геном клетки. У прокариот, дрожжей и клеток млекопитающих, например, трансформирующая ДНК может поддерживаться на эписомальном элементе, таком как плазмида. Что касается эукариотических клеток, то стабильно трансформированной клеткой является та, в которой трансформирующая ДНК интегрирована в хромосому так, что она наследуется дочерними клетками посредством хромосомной репликации. Эта стабильность демонстрируется способностью эукариотической клетки создавать клеточные линии или клоны, состоящие из популяции дочерних клеток, содержащих трансформирующую ДНК. «Клон» представляет собой популяцию клеток, полученных из одной клетки или общего предка митозом. «Клеточная линия» представляет собой клон первичной клетки, который способен к стабильному росту in vitro в течение многих поколений.
[00095] Две последовательности ДНК являются «по существу гомологичными», когда по меньшей мере приблизительно 75% (предпочтительно по меньшей мере приблизительно 80% и наиболее предпочтительно по меньшей мере приблизительно 90 или 95%) нуклеотидов перекрываются по определенной длине последовательности ДНК. Последовательности, которые по существу гомологичны, могут быть идентифицированы путем сравнения последовательностей с использованием стандартного программного обеспечения, доступного в базах данных последовательностей, или в эксперименте гибридизации по Саузерну при, например, жестких условиях, как определено для данной конкретной системы. Определение подходящих условий гибридизации известно специалистам в данной области техники. См., например, Maniatis et al., supra; DNA Cloning, Vols. I & II, supra; Nucleic Acid Hybridization, supra.
[00096] Следует отметить, что также входящими в объем настоящего изобретения являются последовательности ДНК, кодирующие антитела, или последовательности ДНК, использующиеся в настоящем изобретении, которые кодируют антитела, полипептиды или их имеющие такую же аминокислотную последовательность активные фрагменты, но которые являются вырожденными по отношению к исходной или известной кодирующей последовательности. Под «вырожденным» подразумевается, что используется другой трехбуквенный кодон для определения определенной аминокислоты. Хорошо известно в данной области, что следующие кодоны могут быть использованы как взаимозаменяемые для кодирования каждой конкретной аминокислоты:
Фенилаланин (Phe или F) UUU или UUC
Лейцин (Leu или L), UUA или UUG или CUU или CUC или CUA или CUG
Изолейцин (Не или I) AUU или AUC или AUA
Метионин (Met или М) AUG
Валин (Val или V), GUU или GUC of GUA или GUG
Серин (Ser или S) UCU или UCC или UCA или UCG или AGU или AGC
Пролин (Pro или Ρ) CCU или ССС или ССА или CCG
Треонин (Tre или Т) ACU или АСС или АСА или ACG
Алании (Ala или A) GCU или GCG или GCA или GCG
Тирозин (Tyr или Y), UAU или UAC
Гистидин (His или H) CAU или САС
Глютамин (Gln или Q) CAA или CAG
Аспарагин (Asn или N), AAU или ААС
Лизин (Lys или K), AAA или AAG
Аспарагиновая кислота (Asp или D), GAU или GAC
Глутаминовая кислота (Glu или Е) GAA или GAG
Цистеин (Cys или С) UGU или UGC
Аргинин (Arg или R) CGU или CGC или CGA или CGG или AGA или AGG
Глицин (Gly или G) GGU или GGC или GGA или GGG
Триптофан (Trp или W) UGG
Терминальный кодон UAA (охра) или UAG (янтарь) или UGA (опал)
[00097] Следует понимать, что кодоны, указанные выше, указаны для последовательностей РНК. В соответствующих кодонах ДНК U заменен на Т.
[00098] Мутации могут быть сделаны в последовательностях, кодирующих антитело или активный фрагмент, так что конкретный кодон заменен на кодон, кодирующий другую аминокислоту. Такие мутации, как правило, сделаны путем наименьших возможных изменений нуклеотидов. Мутационная замена такого рода может быть сделана, чтобы изменить аминокислоту в результирующем белке не-консервативным способом (т.е. путем изменения кодона аминокислоты, принадлежащей к группе аминокислот, имеющих определенный размер или характеристику, на аминокислоту, принадлежащей к другой группе) или консервативным способом (т.е. путем изменения кодона аминокислоты, принадлежащей к группе аминокислот, имеющих особый размер или характеристику, на аминокислоту, принадлежащую к той же группе). Такая консервативная замена, как правило, приводит к меньшим изменениям в структуре и функции полученного белка. Неконсервативная замена служит, скорее всего, для изменения структуры, активности или функции полученного белка. Настоящее изобретение следует рассматривать как включающее последовательности, содержащие консервативные замены, которые не по существу изменяют активность связывания или характеристики полученного белка.
[00099] Как упоминалось выше, последовательность ДНК, кодирующая антитело, полипептид или активный фрагмент, может быть получена синтетически, а не клонированием. Последовательность ДНК может быть создана с соответствующими кодонами для последовательности аминокислот антитела или фрагмента. В общем, будут выбраны предпочтительные кодоны для предполагаемого хозяина, если последовательность будет использоваться для экспрессии. Полную последовательность собирают из перекрывающихся олигонуклеотидов, полученных с помощью стандартных методов и собранных в полную кодирующую последовательность. См., например, Edge, Nature, 292: 756 (1981); Nambair et al., Science, 223: 1299 (1984); Jay et al., J. Biol. Chem., 259: 6311 (1984). Синтетические последовательности ДНК обеспечивают удобную структуру генов, которые будут экспрессировать аналоги или «мутеины». Кроме того, ДНК, кодирующая мутеины, может быть сделана путем сайт-направленного мутагенеза нативных генов или кДНК, также мутеины могут быть сделаны непосредственно с помощью обычного синтеза полипептида.
[000100] «Гетерологичная» область ДНК-конструкции - это идентифицируемый сегмент ДНК в более крупной молекуле ДНК, который не встречается в ассоциации с более крупной молекулой в природе. Таким образом, когда гетерологичный участок кодирует ген млекопитающего, ген обычно будет в окружении ДНК, которая не фланкирует геномную ДНК млекопитающего в геноме организма-источника. Другим примером гетерологичной кодирующей последовательности является конструкция, где сама кодирующая последовательность не встречается в природе (например, кДНК, где геномная кодирующая последовательность содержит интроны, или синтетические последовательности, имеющие кодоны, отличные от нативного гена). Аллельные варианты или природные мутационные события не дают гетерологичную область ДНК, как определено в настоящем документе.
[000101] Последовательность ДНК является «функционально связанной» с последовательностью, контролирующей экспрессию, когда последовательность контроля экспрессии контролирует и регулирует транскрипцию и трансляцию этой последовательности ДНК. Термин «функционально связанный» включает наличие соответствующего стартового сигнала (например, ATG) перед последовательностью ДНК для экспрессии и под держания правильной рамки считывания для обеспечения экспрессии последовательности ДНК под контролем последовательности, регулирующей экспрессию, и производства целевого продукта, кодируемого последовательностью ДНК. Если ген, который желательно вставить в рекомбинантную молекулу ДНК, не содержит соответствующего стартового сигнала, такой стартовый сигнал может быть вставлен перед геном.
[000102] Термин «стандартные условия гибридизации» относится к солевым и температурным условиям, по существу эквивалентным 5 x SSC и 65°С для гибридизации и промывки. Тем не менее, специалистам в данной области техники будет понятно, что такие «стандартные условия гибридизации» зависят от конкретных условий, в том числе концентрации натрия и магния в буфере, длины нуклеотидной последовательности и концентрации, процентного несоответствия, процента формамида, и тому подобного. Также важным в определении «стандартных условий гибридизации» будет, являются ли две гибридизующиеся последовательности РНК-РНК, ДНК-ДНК или РНК-ДНК. Такие стандартные условия гибридизации могут быть легко определены специалистами в данной области в соответствии с хорошо известными формулами, в которых гибридизация, как правило, ниже 10-20NC прогнозируемой или определяемой Tm с промывками в более жестких условиях, если это необходимо.
[000103] В своем первичном аспекте настоящее изобретение относится к идентификации нового способа, протоколу и средствам для эффективного лечения и профилактики вирусных инфекций, в частности, вируса гриппа, путем введения нейтрализующих антител в дыхательный тракт или дыхательные пути, например, путем интраназального или ингаляционного введения нейтрализующего антитела (антител). Интраназальное или ингаляционное введение нейтрализующего антитела (антител), в частности, нейтрализующего вирус гриппа антитела, является более эффективным для лечения или блокирования вируса в терапевтических или профилактических целях, чем альтернативные средства введения, такие как введение IP. В своем первичном аспекте настоящее изобретение относится к идентификации нового способа и средства для эффективного лечения и профилактики вирусных инфекций, в частности, вируса гриппа, путем интраназального введения нейтрализующего антитела (антител). Ингаляционная и/или интраназальная доставка и введение являются более предпочтительными и эффективным при более низких дозах, чем при системном введении (IV или IP) того же антитела в тех же количествах. Лечение или профилактика IN вводимым антителом до или даже после воздействия вируса или инфекции является эффективным.
[000104] Способы и протоколы, сочетающие интраназально вводимую дозу антитела с IP вводимой дозой антитела, являются особенно эффективными терапевтически или профилактически против вируса, в частности, вируса гриппа. Такие методы или протоколы включают те, в которых одна или более интраназально или ингаляционно вводимая доза антитела вводится в сочетании с одной или несколькими IP или IV вводимыми дозами антитела. Интраназальная или ингаляционная доза может быть введена до, после или одновременно с последующей IP или IV вводимой дозой. Может быть введена одна или более интраназально, ингаляционно, IP или IV вводимая доза (дозы). Интраназально вводимым антителом может быть фрагмент антитела, в котором нет Fc или эффекторной функции, такой как Fab, тогда как IP вводимое антитело может иметь эффекторную функцию или повышенную эффекторную функцию.
[000105] В соответствии с настоящим изобретением нейтрализующие антитела вводят в дыхательный тракт или дыхательные пути для повышенной эффективности в отношении вируса, в частности, вируса гриппа. Введение в дыхательный тракт или дыхательные пути может быть осуществлено любым признанным или известным способом и может включать ингаляционное или интраназальное введение. Для повышения эффективности нейтрализующее антитело доставляется к одному или более из верхних дыхательных путей и нижних дыхательных путей, а также может включать носовую полость, нос, пазухи, горло, глотку, гортань, трахею, бронхи и легкие.
[000106] Ингаляция относится к приему внутрь, в частности, в контексте принятия или введения/вводимого агента или соединения, включая антитело или активный фрагмент, или композиции, содержащей такие антитела, в результате чего вещество, соединение, антитело, фрагмент, в том числе в составе композиции, поступает в дыхательные пути. Дыхательные пути могут включать верхние и/или нижние дыхательные пути. Верхние дыхательные пути включают нос, полость носа, пазухи, гортань, трахею. Нижние дыхательные пути включает легкие, дыхательные пути (бронхи и бронхиолы) и воздушные мешочки (альвеолы). Ингаляция может происходить через нос или через рот, или через прямое введение в нижние дыхательные пути, например, в трахею. Таким образом, ингаляция может включать ингаляцию только через нос или, в первую очередь, через нос, ингаляцию через рот, пероральную ингаляцию, интратрахеальную ингаляцию, эндотрахеальное введение. Таким образом, ингаляция предусматривает для и предполагает любые средства введения, благодаря которым препарат, средство, состав, антитело, фрагмент достигает или осаждается на или в дыхательных путях, исключительно, в частности, или предпочтительно, в том числе верхних и/или нижних дыхательных путях.
[000107] Термин интраназальное, используемый в настоящем документе, включает, но не ограничивается, введение или попадание в или через нос или носовые структуры. Термин интраназальное, используемый в настоящем документе, и в качестве примера, и в качестве варианта в примерах, не предназначен для ограничения или подразумевания ограничения введения прямо или специально, или исключительно через нос или полость носа, в частности, служит, чтобы исключить другие средства введения, благодаря которым препарат, агент, антитело, фрагмент, состав доставляется или предоставляется, осаждается на или в или иным образом распределяется в дыхательных путях.
[000108] Устройства для введения или доставки в дыхательный тракт или дыхательный путь (пути) известны и признаны в данной области техники и квалифицированной клинической или медицинской практике и применимы в способах, протоколах и композициях согласно настоящему изобретению. Устройства включают дозированные ингаляторы, дозированные спринклерные насосы, ручные пульвелизаторы, маленькие или большие звуковые распылители, ультразвуковые ингаляторы и сухие порошковые ингаляторы.
[000109] Настоящее изобретение имеет применение и использование в лечении или профилактике, в частности, агентов или патогенов, которые нацелены, инфицируют или влияют на дыхательные пути. Таким образом, настоящее изобретение имеет применение и использование в лечении или профилактике инфекций дыхательных путей, в частности респираторных вирусов и агентов, которые связаны с или причинно связаны с респираторными заболеваниями. Распространенными вирусными респираторными заболеваниями являются болезни, вызванные различными вирусами, которые имеют аналогичные черты и влияют на верхние дыхательные пути. Вовлеченными вирусами могут быть вирусы гриппа, респираторно-синцитиальный вирус (РСВ), вирусы парагриппа и респираторные аденовирусы. Вирусы парагриппа являются основной причиной крупа у детей раннего возраста и могут вызвать бронхит, пневмонию и бронхиолит. Аденовирусы поражают в первую очередь дыхательные пути и желудочно-кишечный тракт и конъюнктиву глаз. Аденовирусы могут вызывать различные заболевания от фарингита до пневмонии, конъюнктивита и диареи. Симптомы могут появиться от 1 до 10 дней после воздействия вирусов.
[000110] Клиническое введение антител для лечения или облегчения состояний (рак, воспалительные заболевания, противовирусные, антибактериальные) использовало исключительно системное введение, обычно IV введение, которое требует больших и дорогостоящих количеств антител, помощь медицинского персонала и значительное время для введения (типичная доза IV вводится в течение 2 часов). В то время, как другие средства введения, такие как интраназальное, могут быть упомянуты, в частности, в патентах или заявках, охватывающих эти антитела, и считаются эквивалентной заменой, в лучшем случае игнорируются полностью, либо не используются, возможно, потому, что они являются менее понятными, как считается, менее привлекательным или менее эффективным, и считается, вызывают ответ иммунной системы опосредованно или менее непосредственно, чем через IP или IV пути введения. Тем не менее, настоящее изобретение и значительные исследования, представленные в настоящем документе, показывают, что интраназальное введение является действительно предпочтительной и более эффективной альтернативой, в частности для нейтрализующих антител. В частности, нейтрализующие антитела, которые могут действовать интраназально в месте или расположении первичного поражения или воздействия патогена, являются более эффективными, чем альтернативные способы введения.
[000111] Таким образом, в соответствии с настоящим изобретением, интраназальная доставка антител обеспечивает заметное и значительное улучшение эффективности по сравнению с системными способами, такими как IP или IV пути. Кроме того, повышенная эффективность интраназального введения продемонстрирована для нейтрализующих антител. He-нейтрализующие антитела, в частности антитела, которые не демонстрируют прямое ингибирование или блокирование респираторных агентов или вирусов, в частности, вируса гриппа, с использованием согласованных или известных анализов нейтрализации или блокирования вирусов, демонстрируют сниженную эффективность при доставке интраназально по сравнению с системным или IP введением. Настоящие исследования показывают, что интраназальная (IN) доставка нейтрализующих антител может значительно увеличить лечебно-профилактическую эффективность более чем в 10 раз по сравнению с внутрибрюшинным (IP) или внутривенным (IV) путем доставки, используя принятую и известную модель гриппа мыши. Сопоставимая эффективность может быть достигнута с помощью менее, чем одной десятой от той же дозы, при доставке IN, а не по IP или IV пути. Интраназальная доставка нейтрализующих антитела может резко увеличить терапевтическую эффективность на несколько порядков. Интраназальная доставка нейтрализующих антител может резко увеличить терапевтическую эффективность минимально от 10 до 100 раз. Интраназальная доставка нейтрализующих антител может резко увеличить терапевтическую эффективность, по меньшей мере, в 10 раз, по меньшей мере, в 50 раз, более, чем в 10 раз, более, чем в 50 раз, более, чем в 100 раз, до 100 раз по сравнению с внутрибрюшинным (IP) введением такого же антитела в аналогичных условиях. Интраназальное введение нейтрализующих антител обеспечивает новый и неожиданный подход к профилактике и лечению инфекции, в частности, в том числе инфекции гриппа. IN введение теперь может быть реализовано эффективно и в сочетании с другими формами введения, чтобы обеспечить более эффективные и менее дорогостоящие подходы к лечению и профилактике.
[000112] Опосредованная антителами нейтрализация вируса, как определено или принято в данной области и как указано в настоящем документе и использовано в настоящем документе, может быть проверена в различных анализах. Примеры анализов нейтрализации включают обычные анализы нейтрализации, основанные на ингибировании вирусного цитопатического эффекта (СРЕ) на клетки в культуре. Например, нейтрализация гриппа может быть проверена путем снижения или блокирования образования СРЕ в клетках MDCK, инфицированных гриппом. Вирус и нейтрализующий агент могут быть предварительно смешаны перед добавлением к клеткам с последующим измерением блокирования входа вируса. Ингибирование гемагглютинина (H1) могут быть проверено in vitro, и можно обнаружить блокировку способности вирусов связываться с эритроцитами. Примеры, известные и принятые для анализа нейтрализации, содержатся в WHO Manual on Animal Influenza (who/cds/csr/ncs/2002.5, стр. 48-54). Антитела, которые блокируют сайт связывания сиаловой кислоты с рецептором, будут нейтрализовать связывание вируса с клетками, тем самым блокируя инфекцию. И наоборот, анализы нейтрализации могут обнаружить блокирование выхода вируса, как в случае таких ингибиторов нейраминидазы, как Тамифлю. Недавно у нейтрализующих антител была идентифицирована эта функция аналогичным образом путем предотвращения выхода вируса, этот пример нейтрализации включает антитела CR9114 против вирусов гриппа В (Dreyfus et al (2012) Science 337: 1343-1348). Кроме того, используются анализы микронейтрализации, в которых вирусный нуклеопротеид (НП) обнаруживается в инфицированных клетках с использованием микротитрационных планшетов в сочетании с методом ELISA. Были описаны количественные ПЦР для измерения вирусных белков (Dreyfus С et al (2012) Emerging Inf Diseases 19(10: 1685-1687).
[000113] He-нейтрализующим антителом является антитело, которое не демонстрирует прямого взаимодействия или связывания с вирусом или вирусной целью на клетке, которую он заражает, и может быть истолковано как не-нейтрализующие. Не-нейтрализующие антитела могут связываться с вирусом, но не нейтрализуют или не подавляют вирус или вирусную репликацию в любых из указанных выше или признанных нейтрализующих тестах. He-нейтрализующие антитела могут связываться с консервативными белками или эпитопами на белках в вирусе. Например, антитела М2 в клинических испытаниях ТКС-032 могут связываться с широким спектром вирусов гриппа А, но не демонстрирует нейтрализацию в обычных анализах нейтрализации. Аналогичным образом, антитела, которые не являются нейтрализующими, могут быть идентифицированы, как связывающиеся с НА.
[000114] Мы определили не-нейтрализующие, но широко реактивные антитела к НА. Они включают антитела 6Р15 1Р19 и 1K17, которые были отрицательными в анализах нейтрализации, включая, ингибирование CPE, H1, микронейтрализации и уменьшения бляшек. Как показано в приведенных ниже примерах, эти антитела не обладают улучшенной терапевтической эффективностью при интраназальном введении по сравнению с внутрибрюшинным введением.
[000115] В другом аспекте настоящего изобретения связывающие вирус антитела или их связывающие фрагменты, в частности, когда антитело или фрагмент являются нейтрализующими, могут быть объединены с агентами или препаратами с образованием конъюгата антитело-лекарственное средство или антитело-агент для введения в дыхательный тракт или в дыхательные пути, в том числе для ингаляционного или интраназального введения, для применения в настоящем изобретении. Препарат или агент, в сочетании с или конъюгированные с антителом или фрагментом, может быть вирус нейтрализующим лекарственным средством или веществом.
[000116] В одном конкретном и дальнейшем аспекте изобретения, комбинированное или серийное введение нейтрализующих антител IN вместе с введением IP или IV антитела обеспечивает эффективное и усовершенствованное средство для синергического лечения и/или профилактики вирусной инфекции. Антитело, которое вводят системно, в том числе IP или IV, может быть нейтрализующим или не-нейтрализующим, и, таким образом, может быть таким же антителом, как вводимое IN, или может быть модифицированным антителом, или другим антителом. Таким образом, антитело для интраназальной доставки, нейтрализующее антитело, может быть другим антителом или отличающимся от антитела, используемого в комбинации с ними, для доставки с помощью другого средства, в частности, для доставки IP или IV.
[000117] Настоящее изобретение демонстрирует, что функция Fc и Fc-части нейтрализующих антител, таким образом, эффекторная функция, не требуется для интраназального повышения эффективности. Таким образом, антитела и фрагменты, такие как Fab фрагменты, или антитела, лишенные Fc или с отсутствием эффекторной функции, являются эффективными интраназально. В противоположность этому Fab фрагменты антител (нейтрализующие или не-нейтрализующие), или антитела, лишенные Fc или с отсутствием эффекторной функции, не являются эффективными IP или IV.
АНТИТЕЛА
[000118] Термин «антитело» описывает иммуноглобулин, природный или частично или полностью полученный синтетическим путем. Термин также охватывает любой полипептид или белок, имеющий связывающий домен, который является, или гомологичен, связывающему домену антитела. Антитела с пересаженными CDR также рассматриваются под этим термином. «Антитело» означает любой иммуноглобулин, включая антитела и их фрагменты, которые связываются со специфическим эпитопом. Термин охватывает поликлональные, моноклональные и химерные антитела, последние упомянутые более подробно описаны в патентах США №4816397 и 4816567. Термин «антитело (антитела)» включает молекулы иммуноглобулина дикого типа (Ig), как правило, включающие четыре полноразмерные цепи полипептида, две тяжелые (Н) цепи и две легкие (L) цепи, или эквивалентный Ig гомолог (например, нанотело верблюда, которое включает только тяжелую цепь); включая полноразмерные функциональные мутанты, варианты или их производные, которые сохраняют существенные черты связывания эпитопа молекулы Ig, и включая двойные специфические, биспецифические, мультиспецифические и антитела с двойными вариативными доменами. Молекулы иммуноглобулина могут быть любого класса (например, IgG, IgE, IgM, IgD, IgA и IgY), или подкласса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2). Предпочтительными являются антитела класса IgG. Также в значение термина «антитело» включены какие-либо «фрагменты антитела».
[000119] «Сайтом связывания антитела» является структурная часть молекулы антитела, состоящего из тяжелых и легких цепей, вариабельной и гипервариабельной областей, которая специфически связывается с антигеном.
[000120] Фраза «молекула антитела» в ее различных грамматических формах, используемая в настоящем документе, предполагает как интактный иммуноглобулин, так и иммунологически активную часть молекулы иммуноглобулина.
[000121] Термин «моноклональное антитело», используемый в настоящем документе, относится к антителу, полученному из популяции по существу гомогенных антител, т.е. индивидуальные антитела, составляющие популяцию, являются идентичными и/или связывают один и тот же эпитоп, за исключением возможных вариантов антител, например, содержащих природные мутации, возникающие в процессе производства препарата моноклональных антител, такие варианты обычно присутствуют в незначительных количествах. Моноклональное антитело представляет собой антитело, имеющее один тип сайта связывания антитела, способный иммунологически реагировать с конкретным антигеном. Моноклональное антитело, как правило, таким образом, демонстрирует единственное связывающее сродство к любому антигену, с которым он реагирует иммунологически. В отличие от препаратов поликлональных антител, которые обычно включают различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело, препарат моноклональных антител, направлено против одной детерминанты на антигене. Моноклональные антитела могут быть мультспецифичными, если они содержат молекулу антитела, имеющую множество сайтов объединения антител, каждый иммуноспецифический в отношении другого антигена; например, биспецифическое (химерное) моноклональное антитело. Определение «моноклональное» указывает на характер антитела, полученного из практически гомогенной популяции антител, и не должно быть истолковано как требующее получения антитела каким-либо конкретным способом. Например, моноклональные антитела, которые будут использоваться в соответствии с настоящим изобретением, могут быть изготовлены различными методами, в том числе, но не ограничиваясь, методом гибридом, методами рекомбинантной ДНК, методами фагового дисплея, а также методами, использующими трансгенных животных, содержащих все или часть локусов иммуноглобулина человека, такие методы и другие примерные способы получения моноклональных антител описаны в настоящем документе.
[000122] Термин «фрагмент антитела» относится к молекуле, кроме интактного антитела, которое содержит часть интактного антитела, которое связывается с антигеном, с которым связывается интактное антитело. Примеры фрагментов антитела включают, но не ограничиваются ими Fv, Fab', Fab'-SH, F(ab') 2; диатела; линейные антитела; одноцепочечные молекулы антитела (например, ScFv) и мультиспецифические антитела, образованные из фрагментов антител. Кроме того, фрагменты антител содержат единственную полипептидную цепь, имеющую характеристики домена VH, а именно возможность соединяться с доменом VL, или домена VL, а именно возможность соединяться вместе с доменом VH с функциональным антигенсвязывающим участком и тем самым обеспечивать антигенсвязывающее свойство полноразмерных антител. Термин «фрагмент антитела» включает молекулу, содержащую, по меньшей мере, одну не полноразмерную полипептидную цепь, включая (I) Fab-фрагмент, который является моновалентным фрагментом, состоящим из вариабельных легких (VL), вариабельные тяжелых (VH), невариабельных легких (CL) и невариабельных тяжелых 1 (СН1) доменов; (II) F(ab')2-фрагмент, который представляет собой бивалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области; (III) тяжелый участок цепи Fab (FD) фрагмента, состоящий из областей VH и CH1; (IV) фрагмент вариабельного участка (Fv), который состоит из VL и VH доменов одного плеча антитела, (v) фрагмент домена антитело (DAB), который содержит один вариабельный домен (Ward, E.S. et al., Nature 341, 544-546 (1989)); (VI) антитело верблюда; (VII) изолированный участок, определяющий комплементарность, (CDR); (VIII) Fv фрагмент с одной цепью, в котором домен VH и домен VL связаны пептидным линкером, который позволяет этим двум доменам ассоциировать с образованием антигенсвязывающего сайта (Bird et al, Science, 242, 423-426, 1988; Huston et al, PNAS USA, 85, 5879-5883, 1988); (IX) диатело, которое является двухвалентным биспецифическим антителом, в которых VH и VL домены экспрессируются на одной полипептидной цепи, но с использованием линкера, который является слишком коротким, чтобы позволить спаривание между двумя доменами на одной цепи, тем самым заставляя домены спариваться с дополнительности доменами другой цепи и создавать два антигенсвязывающих сайта (WO 94/13804; Р. Holliger et al Proc. Natl. Acad. Sci. USA 90 6444-6448, (1993)); и (x) линейное антитело, которое содержит пару тандемных сегментов Fv (VH-CH1-VH-CH1), которые вместе с комплементарной легкой цепью полипептидов образуют пару антигенсвязывающих областей; (XI) поливалентные фрагменты антител (ScFv димеры, тримеры и/или тетрамеры (Power and Hudson, J Immunol. Methods 242: 193-204 9 (2000)); (XII) минитела, который являются двухвалентной молекулой, состоящей из ScFv, слитых с константными доменами иммуноглобулина, СН3 или СН4, где константные СН3 или СН4 домены служат в качестве доменов димеризации (Olafsen Τ et al (2004) Prot Eng Des Sel 17(4):315-323; Hollinger Ρ and Hudson PJ (2005) Nature Biotech 23(9): 1126-1136) и (XIII) другие не полноразмерные части тяжелых и/или легких цепей, или мутантов, вариантов или их производных, в одиночку или в любой комбинации. Одноцепочечные Fabs (scFAb) известны и описаны в том числе в патенте США 20070274985.
[000123] Поскольку антитела могут быть модифицированы различными способами, термин «антитело» следует истолковывать как охватывающий любой специфически связывающий элемент или вещество, имеющий связывающий домен с требуемой специфичностью и способностью к нейтрализации, где это применимо, в соответствии с настоящим изобретением. Таким образом, этот термин охватывает фрагменты антител, производные, функциональные эквиваленты и гомологи антител, включая любой полипептид, содержащий домен связывания иммуноглобулина, будь то природный или полностью или частично синтетический. Химерные молекулы, содержащие связывающий домен иммуноглобулина, или эквивалент, слитый с другим полипептидом, таким образом, включены в данное изобретение. Клонирование и экспрессия химерных антител описаны в ЕР-А-0120694 и ЕР-А-0125023 в патентах США №4816397 и 4816567.
[000124] Используемый в настоящем документе, «Fab-фрагмент» относится к фрагменту антитела, содержащего фрагмент легкой цепи, содержащий домен VL и константный домен легкой цепи (CL), и домен VH и первый константный домен (СН1) тяжелой цепи. Fab и F(ab')2 части молекул антител могут быть получены путем протеолитической реакции папаином и пепсином, соответственно, с по существу интактными молекулами антител с помощью хорошо известных методов, или могут быть получены синтетически или рекомбинантно. Fab'-молекулы части антитела также хорошо известны и могут быть получены из F(ab')2 частей с последующим восстановлением дисульфидных связей, соединяющих части двух тяжелых цепей, меркаптоэтанолом и последующим алкилированием полученного меркаптана белка реагентом, таким как йодацетамид.
[000125] Термин «Fc-домен» используется в настоящем документе для определения С-концевой области тяжелой цепи иммуноглобулина, который содержит по меньшей мере часть константной области. Например, в природных антителах Fc-домен состоит из двух идентичных белковых фрагментов, полученных из второго и третьего константного домена антитела, двух тяжелых цепей в изотипах IgG, IgA и IgD; Fc домены IgM и IgE содержат три константных домена тяжелой цепи (домены 2-4 C.sub.H) в каждой полипептидной цепи.
[000126] Примерные молекулы антител являются интактными молекулами иммуноглобулина, по существу, интактными молекулами иммуноглобулина и теми частями молекулы иммуноглобулина, который содержит паратоп, в том числе теми частями, известными в данной области техники как Fab, Fab', F(ab')2 и F (V), которые являются предпочтительными частями для использования в терапевтических способах, описанных в настоящем документе.
[000127] В некоторых случаях, как описано в настоящем изобретении, требуются некоторый уровень или количество нейтрализующей активности и необходимые свойства антитела для использования, в частности, для интраназального или ингаляционного введения. Таким образом, любой фрагмент, вариант, производное или синтетическая часть антитела для применения интраназально в соответствии с настоящим изобретением должны сохранить способность к нейтрализации и активность против целевого вируса или патогена, в аспекте вируса гриппа. С другой стороны, антитела, которые могут быть введены с помощью альтернативных системных путей, в том числе внутрибрюшинно или внутривенно, необходимо должны связывать или узнавать целевой вирус или патоген, в аспекте вируса гриппа, однако, нейтрализация не требуется. Таким образом, в качестве примера, Fab-фрагменты антитела (антител), которые сохраняют способность к нейтрализации, могут быть использованы интраназально. Эффекторные функции, опосредованные Fc, не требуются для интраназальной эффективности и нейтрализации. Наоборот, системно доставляемые антитела будут управлять своей эффективностью через эффекторную функцию.
[000128] Термин «антигенсвязывающий домен» относится к части антиген-связывающей молекулы, который содержит область, которая специфически связывается с и комплементарна части или всему антигену. Если антиген является большим, его антиген-связывающая молекула может связываться только с конкретной частью антигена, которая называется эпитоп. Антиген-связывающий домен может быть обеспечен, например, одним или более вариабельным доменом антител (также называемым вариабельным участком антитела). Предпочтительно, чтобы антиген-связывающий домен содержал вариабельную область легкой цепи антитела (VL) и вариабельную область тяжелой цепи антитела (VH).
[000129] Термин «вариабельная область» или «вариабельный домен» относится к области антитела тяжелой или легкой цепи, который участвует в связывании антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL соответственно) нативного антитела обычно имеют аналогичные структуры, при этом каждый домен содержит четыре консервативные каркасные области (FR) и три гипервариабельные области (HVRs). (См., например, Kindt et al. Kuby Immunology, 6.sup.th ed., W.H. Freeman and Co., стр. 91 (2007).) Один VH или VL домен может быть достаточным для придания антиген-связывающей специфичности. Кроме того, антитела, которые связываются с конкретным антигеном, могут быть выделены с использованием VH или VL доменов антитела, которое связывается с антигеном, скринингом библиотеки дополнительных VL или VH доменов, соответственно. См., например, Portolano et al., J. Immunol. 150:880-887 (1993); Clarkson et al., Nature 352: 624-628 (1991).
[000130] Термин «антигенсвязывающий сайт антитела» при использовании в настоящем документе относится к аминокислотным остаткам антитела, которые ответственны за связывание антигена. Антиген-связывающая часть антитела содержит аминокислотные остатки из «области, определяющей комплементарность» или «CDR». «Структурными» или «FR» областями являются остатки вариабельные области домена, отличные от гипервариабельной области, как определено в настоящем документе. Таким образом, легкие и тяжелые цепи вариабельных доменов антитела содержат от N- к С-концу домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. В особенности, CDR3 тяжелой цепи представляет собой область, которая вносит наибольший вклад в связывание антигена и определяет свойства антитела. Антитела могут быть в достаточной степени определены по аминокислотной последовательности в соответствии с CDR их тяжелой и легкой цепи, и могут быть, в частности, описаны и охарактеризованы в соответствии с последовательностью их вариабельной области тяжелой цепи CDR1, CDR2 и CDR3 и последовательностью их вариабельной области легкой цепи CDR1, CDR2 и CDR3. Антитело может быть определено или охарактеризовано как антитело или фрагмент, содержащий тяжелую и легкую цепь, в котором вариабельная область тяжелой цепи включает специфические последовательности CDR1, CDR2 и CDR2 и вариабельная область легкой цепи содержит последовательности специфические последовательности CDR1, CDR2 и CDR3. Области антитела CDR и FR могут быть определены согласно стандартным методам и анализам, доступным и известным специалисту данной области техники. CDR и FR регионы определяются в соответствии со стандартом определения Kabat et al., Sequences of Proteins of Immunological Interest, 5th ed., Public Health Service, National Institutes of Health, Bethesda, Md. (1991) и/или остатками "гипервариабельной петли".
[000131] Термин «эпитоп» включает любую полипептидную детерминанту специфического связывания с антителом. В некоторых вариантах осуществления эпитопная детерминанта включает химически активные поверхностные группировки молекул, такие как аминокислоты, боковые цепи Сахаров, фосфорильные или сульфонильные группы, и в некоторых вариантах осуществления, могут иметь специфические трехмерные структурные характеристики и/или конкретные характеристики заряда. Эпитоп представляет собой область антигена, который связывается с антителом.
[000132] Методы и методики получения моноклональных антител с помощью гибридом или других средств и подходов хорошо известны. Панели моноклональных антител, продуцируемых против пептидов патогена, вируса или гриппа, могут быть подвергнуты скринингу на различные свойства; т.е. нейтрализацию, изотип, эпитоп, аффинность и т.д. Особый интерес представляют моноклональные антитела, которые нейтрализуют активность вируса или его субъединиц. Такие моноклональные антитела могут быть легко идентифицированы в анализах нейтрализации активности. Антитела с высоким сродством могут быть также использованы для эффективного связывания и/или нейтрализации, или когда целью является иммуноаффинная очистка нативного или рекомбинантного вируса.
[000133] Моноклональные антитела, полезные в практике настоящего изобретения, могут быть получены путем инициирования моноклональной культуры гибридомы, включающей питательную среду, содержащую гибридому, которая секретирует молекулы антитела с соответствующей антигенной специфичностью. Культуру выдерживают в условиях и в течение периода времени, достаточного для того, что гибридомы секретировали молекулы антитела в среду. Затем собирают антитело-содержащую среду. Молекулы антител могут быть дополнительно очищены с помощью хорошо известных методов.
[000134] Среды, полезные для приготовления этих композиций, хорошо известны в данной области техники и коммерчески доступны и включают синтетические культурные среды, инбредных мышей, и тому подобное. Примерной синтетической средой является минимально необходимая среда Игла (DMEM; Dulbecco et al., Virol. 8: 396 (1959)) с добавлением 4,5 г/л глюкозы, 20 мМ глутамина и 20% фетальной телячьей сыворотки. Примерным инбредным штаммом мыши является BALB/C.
[000135] Способы получения моноклональных антивирусных антител также хорошо известны в данной области. См Niman et al., Proc. Natl. Acad. Sci. USA, 80: 4949-4953. Как правило, вирус, вирусный белок или пептидный аналог используется либо самостоятельно, либо конъюгирован с иммуногенным носителем, в качестве иммуногена для получения моноклональных антител. Гибридомы подвергали скринингу на способность продуцировать антитела, которые иммунологически реагировали с вирусом, белком или пептидным аналогом.
[000136] Антитела могут быть также биспецифическими, например, те, в которых один связывающий домен антитела принадлежит нейтрализующему вирус антителу, использующемуся в изобретении, а другой связывающий домен имеет различную специфичность, например, способен связываться или ассоциировать с апикальной поверхностью клеток, чтобы быть связанным с эпителиальными клетками дыхательных путей и т.д. Биспецифические антитела согласно настоящему изобретению включают те, в котором один связывающий домен антитела является нейтрализатором, как используется в настоящем изобретении, в том числе его фрагмент, а другой связывания домен от отличного антитела или его фрагмента, в том числе отдельного противовирусного специфического антитела, в том числе альтернативного нейтрализующего антитела или не-нейтрализующего антитела. Другой связывающий домен может быть антителом, которое распознает и нацелено на конкретный тип клеток, как в эпителиальные клетки легких, альвеолярные макрофаги, антитела, специфические к нервным или глиальным клеткам. В биспецифических антителах согласно настоящему изобретению один связывающий домен антитела согласно изобретению могут быть объединен с другими связывающими доменами или молекулами, которые распознают специфические клеточные рецепторы и/или модулируют клетки определенным образом, как, например, иммуномодулятор (например, интерлейкин (интерлейкины)), модулятор роста или цитокин, или токсин (например, рицин) или анти-митотический или апоптический агент или фактор. Таким образом, антитела согласно изобретению могут быть использованы как прямые или целевые агенты, метки, другие молекулы или соединения, или антитела при симптомах таких, как инфекции, воспаления и т.д.
[000137] Биспецифические антитела, используемые в настоящем изобретении, может содержать по меньшей мере два Fab-фрагмента, в одном примере где происходит обмен либо вариабельных областей или константных областей тяжелой и легкой цепи второго фрагмента Fab. Из-за обмена либо вариабельных областей, либо константных областей указанный второй фрагмент Fab также упоминается как «кросс-Fab-фрагмент» или «xFab фрагмент» или «кроссоверный Fab-фрагмент». Такие биспецифичные антитела описаны в US 2013006011.
[000138] Иммуноконъюгаты или слитые белки антитела согласно настоящему изобретению, где антитела, молекулы антител или их фрагментов, из использования в настоящем изобретении, конъюгированы или присоединены к другим молекулам или агентам, дополнительно включают, но не ограничиваются, такие антитела, молекулы или фрагменты, конъюгированные с агентом химической абляции, токсином, иммуномодулятором, цитокином, цитотоксическим агентом, химиотерапевтическим агентом, противовирусным агентом, противомикробным агентом или пептидом, деструктором клеточной стенки и/или клеточной мембраны или лекарственным препаратом. В одном аспекте, иммуноконъюгаты или антитела слияния могут включать антитела, молекулы или фрагменты, конъюгированные с антивирусным агентом, в частности, агентом против гриппа. Агент против гриппа может быть ингибитором нейраминидазы. Агент против гриппа может быть выбран из Тамифлю и Реленза. Агент против гриппа может быть ингибитором М2, таким, как амантадин или римантадин. Агент против гриппа может быть вирусным ингибитором репликации.
[000139] Любые такие агенты против вируса гриппа также могут быть смешаны или быть в сочетании с в составе композиций, представленных в настоящем документе, или вводимы в сочетании с или отдельно с антителами или активными фрагментами их из данного документа. Агенты против гриппа можно вводить с помощью одних и тех же или альтернативных средств (например, ингаляционно или через рот (например, таблетки)) в качестве антитела или их фрагментов ингаляционных или интраназальных композиций согласно изобретению. Таким образом, антитела согласно настоящему изобретению и ингаляционные или интраназальные композиции согласно настоящему изобретению могут дополнительно содержать или могут быть введены в комбинации или последовательно с или перед агентом против вируса гриппа или антивирусным агентом, таким как, например, ингибитор нейраминидазы, в том числе агент, выбранный из Тамифлю и Реленза. Многочисленные антитела были охарактеризованы и находятся в разработке как терапевтические антитела против гриппа, в том числе на основании консервативных эпитопов вируса. Некоторые кросс-реактивные антитела нацелены на гемагглютинин (НА), гликопротеин, что создает наиболее надежные нейтрализующие антитела при вакцинации или природной инфекции. НА состоит из двух субъединиц, НА1 и НА2, которые являются важнейшими компонентами в вирусной инфекции. MAb CR6261 является хорошо изученным антителом, которое связывается с H1 вирусами и другими подтипами (Н5) в группе 1 и связывается с НА2 субъединицей ((Throsby М et al (2008) PLOS ONE 3: e3942; Eckert DC et al (2009) Science 324: 246-251; Friesen RHE et al (2010) PLoS ONE 5(2): e1906; Патент США 8,192,927). MAb CR8020 связывается с мембранной проксимальной областью НА2 на обоих H3 и другом подтипе (Н7) вируса, которые входят во 2 группу вирусов (Eckert DC et al (2011) Science 333: 843-850). FI6v3 антитела от исследователей в Швейцарии может связываться с эпитопом из вирусов обеих групп 1 (H1) и 2 (H3), однако FI6 продемонстрировало ограниченную эффективность у мышей (Corti D et al., (2011) Science 333: 850-856). Палезе и его коллеги сообщили о широко защитных моноклональных антителах против вирусов гриппа H3 с использованием последовательной иммунизации мышей различными агглютининами (Wang ТТ et al (2010) PLoS Pathog 6(2): e1000796; Заявка США 20110027270). Используя этот подход, выделяли широко реактивные H1 антитела (Tan GS et al (2012) J Virol 86(11): 6179-6188).
[000140] Перечень различных известных антител против гриппа приводятся ниже в таблице 1. Примеры исследований, оценивающих различные антитела в таблице в способах и композициях согласно изобретению, в частности, для повышенной эффективности путем интраназального введения или ингаляции, приведены в данном описании. Известные антитела, в том числе перечисленные в таблице 1, пригодны для оценки и применения в способах и композициях согласно настоящему изобретению. Если способность к нейтрализации не известна или не оценена, она может быть оценена с помощью способов, известных и доступных специалистам в данной области, в том числе, как описано в данном документе и ссылках.
[000141] В таблице 2 приведены иллюстративные примеры последовательности антител, представляющие CDR тяжелых и легких цепей для некоторых антител, показавших себя приемлимыми для настоящего изобретения. Последовательности CDR основаны на полученных из публикаций или доступных последовательностях, включая публикации, упомянутые в таблице 1.
[000142] Настоящее изобретение демонстрирует эффективность интраназального введения в низких дозах многочисленных различных нейтрализующих антител, в том числе известных антител и антител, вновь выделенных. В частности, примерная интраназальная эффективность обеспечивается для многочисленных различных известных антител, как например, антител CR6261 CR8020, CR9114, 6F12, GG3, 5а7, mAb53 и mAb579. Такая активность и эффективность не была продемонстрирована для этих конкретных антител, это несмотря на многочисленные исследования для примеров CR6261 и CR8020, в том числе доклинические испытания. Многочисленные различные антитела, в том числе известные и вновь выделенные антитела, оцениваются в настоящем документе и так же эффективны. Активные и эффективные антитела в соответствии с настоящим изобретением направлены на различные эпитопы и узнают различные подтипы, в том числе подтипы H1, H3, Н5 вируса гриппа А, а также гриппа В. Таким образом, настоящее изобретение относится к общеприменимому явлению, в котором антитело, способное нейтрализовать вирус, может быть использовано в способах и композициях для интраназального введения и для лечения или профилактики вируса, инфекции и/или доставки путем интраназального введения одного или более антитела, направленного против вируса, в частности, одного или нескольких моноклональных антител, в частности, против вируса гриппа. Предложенное антитело способное к нейтрализации, его цель или эпитоп и его изотип (IgG изотип) не важны. Дополнительные антитела, имеющие такие же или сопоставимые возможности и нейтрализующие способности, можно использовать в настоящем изобретении. Рассматриваются фрагменты антител, производные или их варианты. Фрагменты антител, в том числе, Fabs, как показано в настоящем документе, являются эффективным в соответствии с изобретением. В одном аспекте настоящего изобретения Fab-фрагменты антитела являются активными и эффективными при введении интраназально или ингаляционно, и являются неэффективными при введении IP или IV.
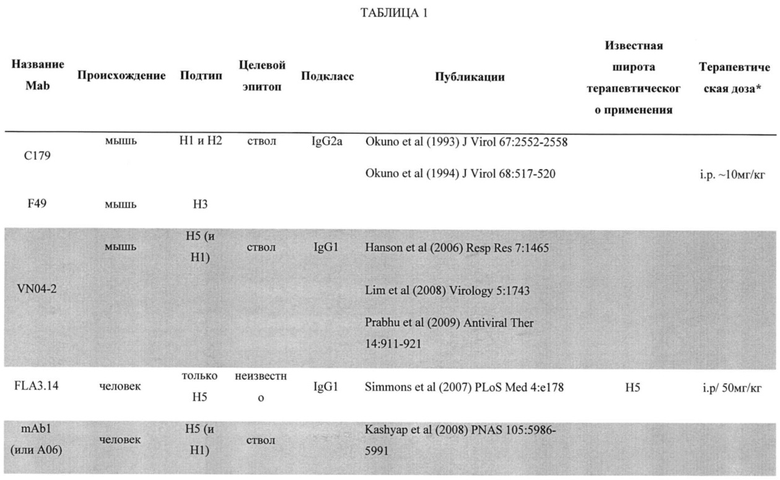
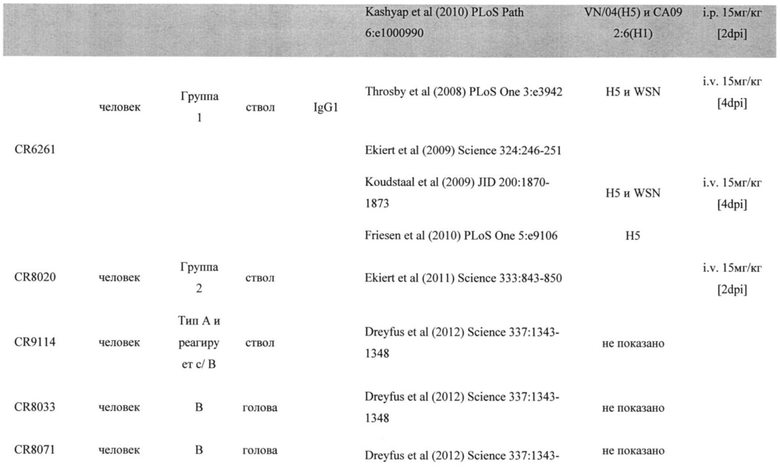
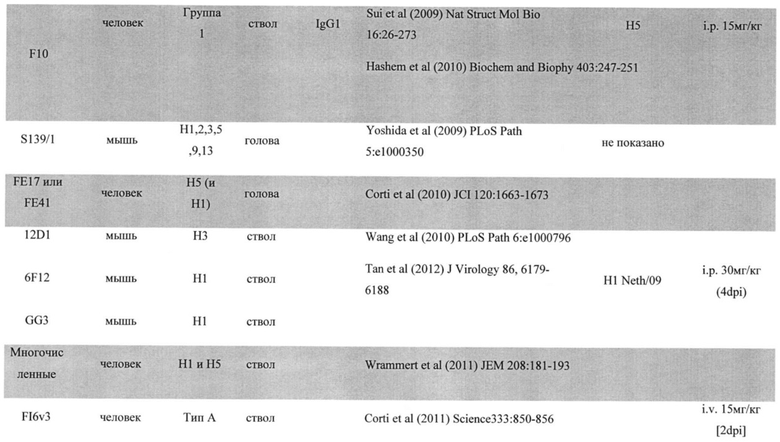


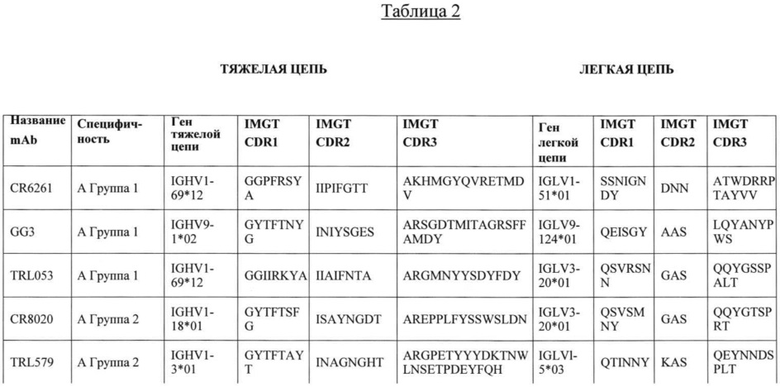

[000143] Нейтрализующие антитела, полезные для IN доставки и введения, могут быть объединены с не-нейтрализующими антителами. Настоящая заявка демонстрирует, что IN введение может быть объединено с альтернативными способами введения, в том числе IP или IV введением, чтобы дать общую и комбинированную повышенную эффективность. Как предусмотрено в данном документе, комбинированное IN и IP введение антитела дает повышенную синергетическую активность и эффективность по сравнению с только IN или IP введением. В дополнение для предоставления замены или альтернативного метода введения или лечения изобретение обеспечивает улучшенный комбинированный подход к терапии и профилактике, опосредованной антителом, где введение IN комбинируется с системным введением, в том числе введением IP, для превосходящей эффективности.
[000144] Альтернативные средства дозирования, сниженное дозирование, более низкие дозы состава и новые способы введения предложены в настоящем изобретении.
КОМПОЗИЦИИ
[000145] В соответствии с настоящим изобретением композиции предназначены для использования и интраназального введения. Композиции содержат, в частности, нейтрализующие антитела, в частности, моноклональное антитело или его активный фрагмент, в частности противовирусные антитела, в частности антитела против гриппа. Композиции могут содержать одно или более нейтрализующее антитело, в частности, одно или несколько моноклональных антител или их активных фрагментов, в частности противовирусные антитела, в частности антитела против гриппа. Композиции в частности могут содержать более одного нейтрализующего антитела, в частности, моноклональное антитело или его активный фрагмент, в частности противовирусное антитело, в частности антитело против гриппа. Нейтрализующее антитело может нейтрализовать более чем один тип или подтип гриппа или может быть объединено с антителами, нейтрализующими различные типы или группы гриппа. Композиция согласно изобретению в частности включает комбинацию нейтрализующих грипп антител, направленных против циркулирующих штаммов вируса гриппа. Композиция (композиции), в частности, может содержать комбинацию нейтрализующих грипп антител, направленных против циркулирующих штаммов вируса гриппа, в частности, антител против гриппа А и антител против гриппа В. Композиция (композиции), в частности, может содержать комбинацию нейтрализующих грипп антител, направленные против циркулирующих штаммов вируса гриппа, в частности, одно или несколько антител против гриппа А и одно или несколько и антител против гриппа В. Композиция (композиции), в частности, может содержать комбинацию нейтрализующих грипп антител, которая в совокупности направлена против соответствующих актуальных циркулирующих штаммов вируса гриппа, в частности, направлено в совокупности против гриппа А подтипов H1 и H3 и против гриппа В линий Yamagata и Victoria. Композиция (композиции) может содержать один, два, три или более нейтрализующих антител, при условии, что вирусы гриппа А и В будут нейтрализованы с помощью комбинации или антителами.
[000146] Композиция (композиции), в частности, может содержать комбинацию нейтрализующих грипп антител, направленных против циркулирующих штаммов вируса гриппа, в частности, анти-Н1 антитела против гриппа А, анти-H3 антитела против гриппа А и антитела против гриппа В. Композиция (композиции) могут включать антитела, эффективные против гриппа А, или в дальнейшем эффективные против штаммов гриппа Н5 и Н7. Антитело против гриппа может быть штамм специфическим или неспецифическим, или пан-специфическим и может нейтрализовать грипп А, в том числе подтип H1 и/или подтип H3, и/или подтип Н5, и/или подтип Н7, или другие штаммы гриппа А или их подтипы, и/или может нейтрализовать грипп В, в том числе линии Yamagata и/или Victoria. Композиции могут иметь одинаковые компоненты или отдельные компоненты или добавки в качестве композиций для альтернативного введения, такого как IV или IP антитела.
[000147] Настоящее изобретение относится к интраназально вводимым комбинированным композициям антител или композициям из комбинации антител, в частности антител против гриппа и в частности моноклональных антител против гриппа, пригодных или выбранных для интраназального введения, в котором комбинация антител включает или состоит из антител, направленных против циркулирующих штаммов вируса. Таким образом, согласно циркулирующим в настоящее время штаммам гриппа, гриппа В (Yamagata), гриппа В (Victoria), гриппа А подтипа H1 и гриппа А подтипа H3, комбинированная композиция согласно настоящему изобретению, имеющая или содержащая антитело (антитела), направлена против каждого из гриппа В (Yamagata), гриппа В (Victoria), гриппа А подтипа H1 и гриппа А подтипа H3.
[000148] Следует отметить, что антитела в комбинации, могут быть направлены против более, чем одного штамма вируса гриппа или подтипа, например, как показано в таблице 1, и показано в настоящем документе. Таким образом, как показано в настоящем документе, антитела CR9114 или СА9114, используемый в настоящем документе, эффективны против штаммов гриппа А и гриппа В. Антитела CR6261 или СА6261, используемые в описании, являются эффективными против различных подтипов гриппа группы 1, в том числе H1 или Н5 и т.д. Антитела CR8020 или СА8020, как в настоящем документе использовано, являются эффективными против различных подтипов гриппа группы 2, включая H3 и Н7. Антитела mAb53 являются эффективными против гриппа А подтипов H1, Н9, Н7 и Н5 группы 1 и 2. Антитела Mab579 являются эффективными против подтипов H3 и Н7. Таким образом, в то время, как в настоящее время циркулирующим штаммам вируса гриппа являются H1, H3 и В, типы комбинаций, имеющие эффективность против дополнительных штаммов и подтипов, в том числе подтипов, которые могут возникнуть и возникают в новом или одном сезоне гриппа, могут быть получены и предоставлены в настоящем документе.
[000149] Композиции могут быть в частности сформулированы и могут содержать более низкие дозы или количества антител, чем любая альтернативная лекарственная форма или тип введения, например, IP или IV. Таким образом, композиции, примененная в настоящем изобретении, может содержать в 5 раз, 10 раз, 20 раз, 50 раз, 100 раз, более, чем в 10 раз, более, чем в 100 раз меньшее количество нейтрализующих антител против или в сравнении с композициями для альтернативного введения, в частности, IP или IV введения.
[000150] Композиции согласно настоящему изобретению могут в частности включать дозы антитела, которое предназначено для введения, в частности, интраназально, в сумме меньше, чем 1 мг/кг на основании веса тела млекопитающего. В конкретном аспекте композиции содержат антитела в количестве для введения менее 1 мг/кг на основании веса тела человека. Композиции согласно настоящему изобретению могут в частности содержать дозу антитела, которое предназначено для введения, в частности, интраназально, в количестве, меньшем, чем 1 мг/кг, не более 0,5 мг/кг, не более 0,1 мг/кг, не более 0,05 мг/кг, не более 0,01 мг/кг, не более 0,005 мг/кг, не более 0,0025 мг/кг, не более 0,001 мг/кг на основании веса тела млекопитающего, в том числе клинически значимого млекопитающего, такого как мышь, собака, лошадь, кошка или человек.
[000151] Специалист в данной области может определить, в том числе на основе эффективности на животных моделях и при рассмотрении клинической и физиологической реакции, вирусной нагрузки и скорости передачи вируса, соответствующую и эффективную дозу для млекопитающих, включая человека. Таким образом, изобретение и параметры дозирования не ограничены примерами, приведенными в данном описании, или конкретными дозами, примеры которых приведены. Настоящее изобретение демонстрирует, что ингаляционное или интраназальное дозирование является предпочтительной альтернативой с точки зрения эффективности и снижения, ограничения или блокирования клинически проявляемого эффекта вирусной инфекции, в том числе инфекции вируса гриппа. Ингаляционное или интраназальное введение нейтрализующих антител обеспечивает улучшение и расширяет эффективность по сравнению с другими способами введения, в том числе IP или IV, что не было бы ожидаемо или прогнозируемо. Количества и сроки дозирования через IN или ингаляционные пути могут быть дополнительно оценены и определены специалистом в данной области техники. Исследования, представленные в настоящем документе, показывают, что IN или ингаляционное введение более эффективно при более низких дозах по сравнению с IP или IV, и что введение может произойти через несколько дней после инфекции и по-прежнему сохраняет эффективность.
[000152] Дозы и диапазоны дозы, применяемые и показанные в настоящем документе на мышиных моделях, могут быть превращены или применены, как соответствующие, с использованием параметров, известных в данной области специалисту в данной области техники или клиническому или медицинскому специалисту. Таким образом, дозирование мг/кг у мышей может быть экстраполировано на сопоставимую или разумно эквивалентную дозу для человека или другого животного. Например, средний вес лабораторной мыши составляет 20 г, тогда как средний вес человека составляет 70 кг.
[000153] Обычной практикой в клинических исследованиях является преобразование дозы для животных в человеческие дозы, и что специалист в данной области будет иметь твердое ожидание того, что такая преобразованная доза (дозы) будет успешна в организме человека. Межвидовое масштабирование и прогнозирование фармакокинетических параметров у человека были описаны (например, Mahmood et al. (2003) J Clin Pharmacol 43: 692-697; Mordenti (1986) Journal of Pharmaceutical Sciences, 75: 1028-1040). Например, терапевтические уровни часто считают параллельно токсичности и так, что переводные коэффициенты, применяемые к преобразованию токсичности для животных по отношению к человеческой токсичности, обычно используются для преобразования минимальных эффективных доз для животных в минимальные эффективные дозы для людей. Кроме того, FDA обеспечивает «Руководство для промышленности», которое обеспечивает коэффициенты преобразования для оценки максимальной безопасной начальной дозы в клинических испытаниях для терапии, включая факторы, используемые для преобразования животной (мышиной) дозы в человеческую дозу (например, в одном примере, умножить мышиную дозу на 0,08).
[000154] Фраза «фармацевтически приемлемый» относится к молекулярным частицам и композициям, которые являются физиологически переносимыми и обычно не вызывают аллергической или подобной неблагоприятной реакции, например расстройства желудка, головокружения и тому подобного при введении человеку.
[000155] «Терапевтически эффективное количество» означает, что количество лекарственного средства, соединения, противомикробного средства, антитела, или фармацевтического агента, будет вызывать биологическую или медицинскую реакцию у субъекта, который наблюдается врачом или другим клиническим специалистом. В частности, в связи с вирусными инфекциями и пролиферацией вируса, термин «эффективное количество» предназначен для включения эффективного количества соединения или агента, который приведет к биологически значимому уменьшению количества или объема репликации вируса или патогена, а также сократит длительность болезни (лихорадка, боли в суставах, дискомфорт) у субъекта, или снизит потери массы тела у инфицированного индивидуума. Фраза «терапевтически эффективное количество», используемая в настоящем документе, означает количество, достаточное для предотвращения и предпочтительного снижения по меньшей мере приблизительно на 30 процентов, более предпочтительно по меньшей мере на 50 процентов, наиболее предпочтительно, по меньшей мере на 90 процентов, клинически значимого изменения массы тела, вирусной нагрузки, репликации вируса, передачи вируса или другой особенности патологии, такой как, например, лихорадка или количество лейкоцитов, которые могут определять ее наличие и активность.
[000156] В некоторых вариантах осуществления «эффективное количество» в контексте введения терапии субъекту относится к количеству терапии, которая является достаточной для достижения одного, двух, трех, четырех или более из следующих эффектов: (I) уменьшение или облегчение тяжести вирусной инфекции гриппа, вирусного заболевания гриппа или симптомов, связанных с ним; (II) сокращение срока действия вирусной инфекции гриппа, вирусного заболевания гриппа или симптомов, связанных с ним; (III) предотвращение прогрессирования вирусной инфекции гриппа, вирусного заболевания гриппа или симптомов, связанных с ним; (IV) регрессия вирусной инфекции гриппа, вирусного заболевания гриппа или симптомов, связанных с ним; (V) предотвращение развития или наступлении вирусной инфекции гриппа, вирусного заболевания гриппа или симптомов, связанных с ним; (VI) предотвращение рецидива вирусной инфекции гриппа, вирусного заболевания гриппа или симптомов, связанных с ним; (VII) уменьшение или предотвращение распространения вируса гриппа от одной клетки к другой клетке, одной ткани к другой ткани, или от одного органа к другому органу; (VIII) предотвращение или уменьшение распространения/передачи вируса гриппа от одного субъекта к другому субъекту; (IX) снижение органной недостаточности, связанной с вирусной инфекцией гриппа или вирусным заболеванием; (х) снижение частоты госпитализации пациента; (XI) уменьшение длительности госпитализации; (XII) увеличение выживаемости субъекта с вирусной инфекцией гриппа или болезнью, связанной с ним; (XIII) ликвидация вирусной инфекции гриппа или болезни, связанной с ним; (XIV) ингибирование или уменьшение репликации вируса гриппа; (XV) ингибирование или уменьшение связывания или слияния вируса гриппа к клетке-хозяину (хозяевам); (XVI) ингибирование или уменьшение входа вируса гриппа в клетку-хозяина (хозяев); (XVII) ингибирование или снижение репликации генома вируса гриппа; (XVIII) ингибирование или уменьшение синтеза белков вируса гриппа; (XIX) ингибирование или снижение сборки вирусных частиц гриппа; (XX) ингибирование или уменьшение выхода вирусных частиц гриппа из клеток-хозяев; (XXI) снижение титра вируса гриппа; (XXII) уменьшение количества симптомов, связанных с инфекцией вируса гриппа или вирусного заболевания гриппа; (XXIII) повышение, улучшение, добавка, комплементация или увеличение в профилактическом или терапевтическом воздействии (воздействиях) другой терапии; (XXIV) предотвращение возникновения или прогрессирования вторичной инфекции, связанной с вирусом гриппа; и/или (XXV) предотвращение наступления или уменьшение тяжести заболевания бактериальной пневмонии в происходящих вторичных вирусных инфекций гриппа. В некоторых вариантах осуществления «эффективное количество» терапии оказывает благоприятное воздействие, но не вылечивает вирусную инфекцию гриппа или заболевание, ассоциированное с ним. В некоторых вариантах осуществления «эффективное количество» терапии может включать введение многократных доз терапии при определенной частоте, чтобы достичь количества терапии, которая оказывает профилактическое и/или терапевтическое действие. В других ситуациях, «эффективное количество» терапии может включать введение одной дозы терапии при определенном количестве.
[000157] Симптом или симптомы, связанные с вирусной инфекцией, в том числе в частности инфекцией гриппа, болезни или воздействия, могут включать, но не ограничиваются, лихорадку 100°F или выше, лихорадочное чувство, кашель и/или боли в горле, насморк или заложенность носа, головная боль и/или боль в теле, озноб, усталость, общая слабость, тошнота, рвота и/или диарея, боли в суставах и мышцах и/или вокруг глаз.
[000158] Термин «предотвращение» или «профилактика» относится к снижению риска приобретения или развития заболевания или расстройства (т.е. в результате чего по меньшей мере один из клинических симптомов заболевания не развивается) у субъекта, который может быть подвержен возбудителю заболевания, или предрасположен к заболеванию заранее до начала болезни.
[000159] Термин «профилактика» относится к и охватывает термин «предотвращение» и относится к измерению или процедурам, целью которых является предотвращение, а не лечение или излечение болезни. Не ограничивающие примеры профилактических мер могут включать введение антибактериальных препаратов или вакцин; введение низкомолекулярного гепарина пациентам больниц с риском тромбоза из-за, например, неподвижности; и введение анти-малярийного средства, такого как хлорохин, перед посещением географического региона, где малярия является эндемическим заболеванием или риск инфицирования малярией высок.
[000160] Термин «лечение» или «обработка» любого заболевания или инфекции относится, в одном варианте, к облегчению заболевания или инфекции (т.е. прекращение заболевания или роста инфекционного агента или вируса или снижение проявления, степени или тяжести по меньшей мере одного из клинических симптомов). В другом варианте «лечение» или «обработка» относится к облегчению по меньшей мере одного физического параметра, который не может быть различим субъектом. В еще одном варианте, «лечение» или «обработка» относится к модуляции болезни или инфекции, либо физически (например, стабилизация заметного симптома), либо физиологически (например, стабилизация физического параметра), или обоими способами. В дополнительном варианте осуществления изобретения, «лечение» или «обработка» относится к замедлению прогрессирования заболевания, передачи заболевания или снижению инфекции.
[000161] Используемый в настоящем документе, «пг» означает пикограмм, «нг» обозначает нанограмм, «μg» или «мкг» означает микрограмм, «мг» обозначает миллиграмм, «μl» или «мкл» означает микролитр, «мл» означает миллилитр, «л» означает литр.
[000162] Настоящее изобретение также предусматривает терапевтические композиции, применимые в практике терапевтических способов согласно настоящему изобретению. Терапевтическая композиция субъекта включает, в смеси, фармацевтически приемлемый наполнитель (носитель) и одно или более антитело или активный фрагмент, в частности нейтрализующее антитело, полипептидный аналог или его фрагмент, как описано в настоящем документе, в качестве активного ингредиента. В предпочтительном варианте осуществления изобретения композиция содержит антитело или фрагмент, способный нейтрализовать вирус, в частности вирус гриппа, в клетке-мишени или у субъекта или пациента.
[000163] Получение терапевтических композиций, которые содержат антитела, полипептиды, аналоги или активные фрагменты в качестве активных ингредиентов, хорошо известны в технике. Как правило, такие композиции получают для введения в виде жидких растворов или суспензий, однако, твердые формы, подходящие для растворения или суспендирования в жидкую форму перед введением, могут быть получены. Препарат также можно эмульгировать. Активный терапевтический ингредиент часто смешивают с вспомогательными веществами, которые являются фармацевтически приемлемыми и совместимыми с активным ингредиентом. Подходящими наполнителями являются, например, вода, физиологический раствор, декстроза, глицерин, этанол или тому подобное, и их комбинации. Кроме того, если желательно, композиция может содержать небольшие количества вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, рН буферные агенты, которые усиливают эффективность активного ингредиента.
[000164] Антитело, полипептид, аналог или активный фрагмент может быть сформулирован в виде терапевтической композиции в качестве нейтрализующих фармацевтически приемлемых солевых форм. Фармацевтически приемлемые соли включают кислотно-аддитивные соли (образованные со свободными аминогруппами полипептида или молекулы антитела) и которые образованы с неорганическими кислотами, такими как, например, соляная кислота или фосфорная кислота, или такими органическими кислотами, как уксусная, щавелевая, винная, миндальная и тому подобное. Соли, образованные из свободных карбоксильных групп, также могут быть получены из неорганических оснований, таких как, например, натрий, калий, аммоний, кальций, или железо, и таких органических оснований, как изопропиламин, триметиламин, 2-этиламино этанол, гистидин, прокаин и тому подобное.
[000165] Терапевтические композиции, содержащие антитело, полипептидный аналог или активный фрагмент, обычно вводят, например, путем введения единичной дозы. Термин «единичная доза», когда используется в отношении терапевтической композиции настоящего изобретения, относится к физически дискретным единицам, пригодным в качестве единичных доз для людей, причем каждая единица содержит заданное количество активного материала, рассчитанное на получение желаемого терапевтического эффекта, в сочетании с требуемым разбавителем; т.е. переносчиком или носителем.
[000166] Как предлагается в настоящем документе, стандартная доза нейтрализующих антител для интраназального введения, которая является эффективной и полезной для лечения или профилактики вируса, в частности вируса гриппа, сравнительно уменьшается по сравнению с той, что указана или требуется для альтернативного введения, такой, как требуется для IP или IV введения. Таким образом, в одном аспекте настоящего изобретения обеспечивается состав антител для введения, в частности, интраназального введения, в котором единичная доза уменьшается на несколько порядков, в частности несколько или несколько порядков по сравнению с той, что указана или требуется для альтернативного введения, такой, как требуется для IP или IV введения. Таким образом, в одном аспекте настоящего изобретения обеспечивается композиция антител для введения, в частности, интраназального введения, где унифицированная доза по меньшей мере в 10 раз, 10 раз, 20 раз, 25 раз, 50 раз, по меньшей мере, в 100 раз, 100 раз, 500 раз, до 1000 раз снижена. В частности, композиция, таким образом, сокращена по сравнению с эквивалентной единицей дозы для IP или IV введения, особенно по той же или сравнимой индикации или эффекта и/или активности. IN дозу можно комбинировать с дозой IP или IV для улучшения эффективности.
[000167] Композиции вводят способом, совместимым с лекарственной формой, и в терапевтически эффективном количестве. Количество, подлежащее введению, зависит от субъекта, подлежащего лечению, способности иммунной системы субъекта использовать активный ингредиент и степени ингибирования или нейтрализации желаемого вируса. Точные количества активного ингредиента, необходимые для введения, зависят от суждения врача и являются специфическими для каждого индивида. Однако подходящие дозы могут составлять от приблизительно 0,001 до 10, предпочтительно от приблизительно 0,005 до приблизительно 1, менее 1, менее 0,5, менее 0,1, менее 0,05, менее 0,01, а более предпочтительно ниже 1, ниже 0,5, ниже 0,1 мг активного ингредиента на килограмм массы тела индивидуума на дозу для интраназального введения. Подходящие режимы для первоначального введения и последующего введения также могут меняться. В одном режиме есть первоначальное введение с последующей повторной дозой (дозами), единственной или несколькими последующими дозами, с одним или более часовыми интервалами до последующей инъекции или другого введения.
[000168] За начальным IN введением может следовать введение высоких доз антитела IP или IV или другим подходящим способом. В одном аспекте настоящего изобретения предусмотрен новый подход дозирования или параметр, в котором пациенту или субъекту вводят интраназально нейтрализующие антитела, и либо одновременно, последовательно или после вводят нейтрализующие или не-нейтрализующие антитела IP или IV введением.
[000169] Терапевтические композиции, особенно интраназальные композиции, могут дополнительно включать эффективное количество нейтрализующего антитела или его фрагмента, и одного или более из следующих активных ингредиентов: антибиотик, противовирусное средство, стероид, противовоспалительное средство. В конкретном аспекте, композиции включают противовирусное средство. Композиции могут включать агент против гриппа. Агент против гриппа может быть ингибитором нейраминидазы, в том числе средством, выбранным из Тамифлю и Реленза.
[000170] Используемый в настоящем документе, «пг» означает пикограмм, «нг» обозначает нанограмм, «μg» или «мкг» означает микрограмм, «мг» обозначает миллиграмм, «μl» или «мкл» означает микролитр, «мл» означает миллилитр, «л» означает литр.
[000171] Композиции могут быть приготовлены в виде назальных спреев или ингаляционных растворов, или суспензий с использованием известных и приемлемых в данной области и в области медицины и медицинской практике подходов. FDA обеспечивает руководство в отношении таких спреев, растворов и суспензий и аэрозольных лекарственных средств, в том числе документы Руководство для промышленности, доступные на fda.gov. Примеры документов Руководства для промышленности от июля 2002 под названием Nasal Spray and Inhalation Solution, Suspension and Spray Drug Products - Chemistry, Manufacturing and Controls Documentation включают детали относительно компонентов состава и композиций, спецификации по ним, производства и закрытых контейнерных систем.
[000172] Назальным спреем являются препараты, которые содержат активные ингредиенты, растворенные или взвешенные в композиции, как правило, на водной основе, которые могут содержать другие наполнители и предназначены для использования носовым вдохом. Закрытые контейнерные системы для назальных спреев включают контейнер и все компоненты, которые отвечают за измерение, атомизацию и доставку препарата пациенту. Лекарства в виде назального спрея содержат терапевтически активные ингредиенты (лекарственные вещества), растворенные или суспендированные в растворе, или смеси наполнителей (например, консерванты, модификаторы вязкости, эмульгаторы, буферные агенты) в негерметичных дозаторах, которые обеспечивают аэрозоль, содержащий отмеренную дозу активного ингредиента. Доза может измеряться с помощью аэрозольного насоса или может быть измерена в процессе производства. Единица назального спрея может быть предназначена для единичного дозирования, или может составлять множество доз композиции в виде спрея, содержащей лекарственное вещество. Назальные спреи применяются в носовой полости для местного и/или системного действия.
[000173] Ингаляционный раствор и продукты лекарственной суспензии обычно представляют собой составы на водной основе, которые содержат терапевтически активные ингредиенты, а также могут содержать дополнительные наполнители. Пероральные ингаляционные растворы и суспензии на водной основе должны быть стерильными (21 CFR 200.51). Ингаляционные растворы и суспензии предназначены для доставки в легкие ингаляционно для пероральных местных и/или системных эффектов и должны быть использованы с указанным распылителем. Лекарственный продукт в виде ингаляционного спрея состоит из композиции и закрытой контейнерной системы. Композиции, как правило, на водной основе и не содержат какого-либо пропеллента.
[000174] Настоящая закрытая контейнерная система для лекарственного продукта в виде ингаляционного спрея включает как предварительно заданное, так и аппаратно-отмеренное представление с использованием механического или силового дозирования и/или энергии вдоха пациента для получения потока спрея. Заданные презентации содержат заданные дозы или часть дозы в каком-либо типе единиц (например, один или несколько блистеров или других емкостей), которые впоследствии вставляются в устройство во время изготовления или пациентом перед использованием. Типичные устройства с дозированными единицами имеют резервуар, содержащий препарат, достаточный для нескольких доз, которые доставляются в виде дозированных брызг самим устройством при активации его пациентом.
[000175] Пролонгированное время пребывания в полости носа также может быть достигнуто с помощью биоадгезивных полимеров, микросфер, хитозана или путем увеличения вязкости композиции. Назальный мукоцилиарный клиренс также можно стимулировать или ингибировать лекарственными средствами, наполнителями, консервантами и/или усилителями абсорбции и, таким образом, влиять на доставку лекарственных средств в место абсорбции.
[000176] Технология микросфер является одной из специализированных систем, используемых для создания назальных продукций. Микросферы могут обеспечить более длительный контакт со слизистой оболочкой носа и тем самым повысить эффективность или абсорбцию. Микросферы для назального применения были получены с использованием биосовместимых материалов, таких как крахмал, декстран, альбумин и желатин (Bjork E, Edman Ρ (1990) Int J Pharm 62: 187-192).
[000174] pH назального состава важен для того, чтобы избежать раздражения слизистой оболочки носа, чтобы позволить препарату быть доступным для поглощения в единой форме, чтобы предотвратить рост патогенных бактерий в носовом проходе, чтобы сохранить функциональность наполнителей, таких как консерванты, и для поддержания нормального физиологического движения ресничек. Желательно поддерживать состав при рН от 4,5 до 6,5, имея в виду физико-химические свойства препарата или активного ингредиента. Назальные составы обычно вводят в небольших объемах в пределах от 25 до 200 мкл, объем 100 мкл может быть наиболее распространенной дозой.
[000177] Растворимость в воде лекарственного средства может быть соответствующим ограничивающим параметром для назальной доставки лекарственного средства в растворе. Обычные растворители или сорастворители, такие как гликоли, небольшие количества спирта, Транскутол (моноэтиловый эфир диэтиленгликоля), глицериды со средней длиной цепи и Лабразол (насыщенный полигликозилированные С8- С10 глицериды) могут быть использованы для повышения растворимости лекарственных средств. Другие варианты включают использование поверхностно-активных веществ или циклодекстринов, таких как ΗΡ-β-циклодекстрин, которые служат в качестве биосовместимого солюбилизатора и стабилизатора в сочетании с липофильными усилителями абсорбции. В таких случаях, их влияние на носовое раздражение должно быть рассмотрено.
[000178] Большинство назальных препаратов приготовлены на водной основе и нуждаются в консервантах для предотвращения микробного роста. Парабены, бензалкония хлорид, фенилэтиловый спирт, ЭДТА и бензоиловый спирт являются одними из наиболее часто используемых консервантов в назальных композициях. Содержащие ртуть консерванты обладают быстрым и необратимым эффектом на движение ресничек и не рекомендуются для использования в назальных системах.
[000179] Может потребоваться небольшое количество антиоксидантов, чтобы предотвратить окисление лекарственных средств. Обычно используемыми антиоксидантами являются метабисульфит натрия, бисульфит натрия, бутилированный гидрокситолуол и токоферол. Как правило, антиоксиданты не влияют на всасывание препарата или не приводят к носовому раздражению. Химическое/физическое взаимодействие антиоксидантов и консервантов с лекарственными средствами, наполнителями, производственным оборудованием и упаковочными компонентами следует рассматривать как часть программы разработки состава.
[000180] Многие аллергические и хронические заболевания часто связаны с корками и иссушением слизистой оболочки. Некоторые консерванты/антиоксиданты среди других наполнителей также могут вызвать раздражение носовой оболочки, особенно при использовании в больших количествах. Адекватная интраназальная влажность имеет важное значение для предотвращения обезвоживания. Таким образом, могут быть добавлены увлажнители особенно в назальные продукты на гелевой основе. Увлажнители помогают избежать раздражения слизистой оболочки носа и, вероятно, не влияют на всасывание препарата. Общие примеры включают глицерин, сорбит и маннит.
[000181] Выбор системы доставки зависит от используемого препарата, предложенного указанием, популяции пациентов и, не в последнюю очередь, маркетинговых предпочтений. Некоторые из этих систем доставки включают капли в нос, назальные спреи, назальные гели и назальные порошки.
ВВЕДЕНИЕ
[000183] Снова следует отметить, что хорошо установлено, что нормальные и разумно ожидаемые дозы терапии антитела являются IV или IP дозами в мг диапазоне. Это основано на исследованиях и клиническом опыте на сегодняшний день с многочисленными рекомбинантными антителами. На сегодняшний день, более двадцати (20) моноклональных антител были утверждены клинически в Соединенных Штатах (см., например, Newsome BW and Ernstoff MS (2008) Br J Clin Pharmacol 66(1): 6-19). Клинически утвержденные антитела, используемых в настоящем изобретении, использовались и вводились IP или IV в диапазоне мг/кг.
[000184] Ни одно моноклональное антитело против гриппа не было клинически одобрено на сегодняшний день. Все испытания, находящиеся в процессе или заявленные в настоящее время, используют внутривенное введение в качестве стандарта. В частности, TheraClone Sciences антитело TCN-023 была оценено в единственной эскалации дозы в диапазоне от 1-40 мг/кг (NCT01390025, clinical trails.gov). Антитело TCN-023 представляет собой человеческое антитело, которое связывается с консервативным эпитопом аминоконцевого внеклеточного домена (М2е) матричного белка гриппа (М2) (Grandea AG et al (2010) PNAS USA 107(28): 12658-12663; Epub 2010 Jul 1). Антитела CR6261 и CR8020 в настоящее время оценивали аналогичным образом в исследованиях безопасности и переносимости с использованием возрастающих доз от 2 мг/кг до 50 мг/кг IV в течение 2 часов (Crucell Holland BV clinical trials NCT01406418 и NCT01756950 соответственно).
[000185] Вакцины против гриппа вводят в виде инъекций. Одним исключением в вакцинах против гриппа является FluMist, живая вакцина гриппа (MedImmune), которую вводят интраназально. FluMist представляет собой комбинацию трех живых штаммов гриппа - штамма A/H1N1, штамма A/H3N2 и штамма В, вводимую в дозе 0,2 мл суспензии с помощью прилагаемого в виде единичной однократной дозы предварительно заполненного интраназального распылителя. В дополнение к штаммам вируса каждая доза также содержит глутамат натрия, гидролизованный свиной желатин, аргинин, сахарозу, двухосновный фосфат калия и одноосновный фосфат калия, без консервантов (FluMist Highlights of Prescribing Information, 2012-2013 Formula, MedImmune, RAL-FLUV12, Component №.: 11294).
[000186] Изобретение обеспечивает новый и эффективный способ введения антитела (антител) и протокол введения антитела для лечения и профилактики вирусных инфекций, в частности вирусов, которые заражают или передаются через дыхательные пути, включая, в частности вирус гриппа. Таким образом, изобретение предусматривает лечение, профилактику или облегчение вирусной инфекции, в частности вируса гриппа, путем интраназального введения антитела, способного нейтрализовать вирус. Одно или более нейтрализующее антитело можно вводить интраназально, в том числе и в то же время, в комбинации или последовательно, или раздельно. Антитело можно вводить одной дозой или может быть введено в нескольких отдельных дозах. Индивидуальные дозы могут быть введены одна за другой, каждое введение разделено минутами, часами или днями.
[000187] В конкретном аспекте настоящее изобретение относится к лечению, профилактике или облегчению вирусной инфекции, в частности вируса гриппа, путем интраназального введения комбинации антител, направленных против циркулирующих штаммов гриппа. Таким образом, лечение, профилактика или облегчение вирусной инфекции, в частности вируса гриппа, предусмотрено и достигнуто в соответствии с изобретением путем интраназального введения комбинации антител, направленных против вируса гриппа В и циркулирующих вирусов гриппа типа А, в частности, в аспекте комбинации антитела против гриппа В, антитела против гриппа А группы 1, такого как анти-Н1 антитела, и антитела против гриппа А группы 2, такого как анти-H3 антитела. В соответствии с настоящим изобретением, интраназальное введение комбинации антитела против гриппа В, антитела против гриппа А группы 1, такого как анти-Н1 антитела, и антитела против гриппа А группы 2, такого как анти-H3 антитела, является эффективным в предотвращении инфекции или лечении инфекции вируса гриппа В или вируса гриппа А. В дополнение антитела доступны и испытаны в настоящем документе и продемонстрировали, что являются эффективными и направлены против более чем одного подтипа или штамма вируса, комбинации, предлагаемые и рассматриваемые в данном документе, служат в качестве универсальной смеси или комбинации, эффективной против многочисленных штаммов и/или подтипов вируса, в частности, вируса гриппа, в том числе известных и циркулирующих штаммов или подвидов, возникающих штаммов или подвидов и неизвестных, непредвиденных вариантов штаммов или подвидов.
[000188] Антитело, использованное в настоящем изобретении, можно вводить интраназально или ингаляционно, с последующим или вместе с, в том числе и в то же время, в комбинации или последовательно или раздельно, системным введением другого или того же антитела, в частности, IP или IV введением. Таким образом, протокол комбинированного введения или метода рассматривается и предусмотрен в настоящем документе, где интраназальное и IP (или внутривенное) введение находятся в сочетании для повышения эффективности в отношении агента, в частности вируса, в частности, вируса гриппа. Действительно, исследования, представленные в настоящем документе, показывают, что с помощью комбинированного интраназального дозирования с альтернативным введением (IP или IV) комбинированная эффективность является синергетической, и могут быть использованы низкие дозы, как IN, так и IP, в качестве примера.
[000189] Изобретение относится к способу лечения или профилактики вирусной инфекции у млекопитающего, подверженного, подверженного риску воздействия, имеющего контракт, демонстрирующего клинические симптомы или страдающего от респираторного вируса, включающему введение интраназально (IN) или ингаляционно указанному млекопитающему моноклонального антитела, способного нейтрализовать респираторный вирус. Моноклональные антитела могут быть в частности IgG антителами. Респираторный вирус может быть вирусом гриппа или подозреваемым вирусом гриппа, или неизвестным респираторным вирусом.
[000190] Антитела могут быть введены после инфицирования или после предполагаемого инфицирования. В аспекте их, антитело может вводиться в период времени до 8 часов после инфицирования (hpi), в том числе 2hpi, 4hpi, 6hpi, 8hpi. Альтернативно, антитело вводят в течение периода времени до 24 часов после инфицирования, в том числе 4hpi, 8hpi, 12hpi, 18hpi, 24hpi. В качестве дополнительной альтернативы, антитело вводят в период времени до 48 часов после инфицирования, в том числе 12hpi, 24hpi, 36hpi, 48hpi. В еще одном альтернативном варианте антитело вводят в период времени до 72 часов после инфицирования, в том числе 24hpi, 36hpi, 48hpi, 60hpi, 72hpi. Антитела могут быть введены через несколько дней после инфицирования, или после предполагаемого инфицирования, или после демонстрирования клинических симптомов, таких как лихорадка, боли, боли в суставах, вялость. Антитела могут быть введены через 1 день после инфицирования, 2 дня после инфицирования, 3 дня после инфицирования, 4 дня после инфицирования, 5 дней после инфицирования, 6 дней после инфицирования, через 7 дней после инфицирования, 10 дней после инфицирования, 12 дней после инфицирования, 14 дней после инфицирования. Антитела могут быть введены через недели после инфицирования или предполагаемой инфекции, в том числе через 1 неделю после инфицирования, 2 недели после инфицирования, 3 недели после инфицирования, 4 недели после инфицирования, через месяц после инфицирования.
[000191] Антитело можно вводить до инфицирования или для того, чтобы уменьшить или предотвратить передачу, или до любого клинического симптома болезни, заболевания или инфекции. В одном аспекте изобретения антитело можно вводить в течение периода нескольких дней времени до инфицирования или до возможного или предполагаемого воздействия или риска инфицирования в качестве профилактической меры. Антитело можно вводить за день до или до 2 дней до или перед, за 3 дня до или перед, 4 дня до или перед, за 5 дней до или перед, за 6 дней до или перед, за 7 дней до или перед, за неделю до или перед, больше, чем за 7 дней до или раньше, больше, чем за неделю до или раньше, до 9 дней до или перед, до 10 дней до или раньше. Антитело можно вводить один или несколько раз до или перед, в одной или нескольких дозах, разделенных часами, днями или неделями.
[000192] Антитело можно вводить в виде единичной однократной дозы или в виде нескольких доз. Каждая доза может быть идентичной единицей или в количестве мг/кг, или может отличаться по размеру. Например, начальная доза может быть более высокой относительной дозой, такой как, например, но не ограничиваясь, 1 мг/кг, более 1 мг/кг, не более 1 мг/кг, или максимальной или близкой к максимальной переносимой дозе или одной половиной от максимально переносимой дозы для введения млекопитающему. Последующие дозы могут быть такими же, как начальная доза, или могут быть меньше или больше, чем начальная доза, и могут зависеть от реакции или ответа субъекта или пациента или облегчения или степени клинических симптомов.
[000193] Несколько доз, тех же или разных по количеству каждой или любой дозы, можно вводить через минуты, часы, дни или недели. Время может варьироваться и может быть сокращено или удлинено в зависимости от реакции и симптомов. Дозы, например, и не ограничиваясь, могут быть, по меньшей мере через 2 часа друг от друга, по меньшей мере через 4 часа друг от друга, по меньшей мере через 6 часов друг от друга, по меньшей мере через 8 часов друг от друга, по меньшей мере через 24 часа друг от друга, по меньшей мере через 48 часов друг от друга, по меньшей мере через 72 часа друг от друга. Дозу или дозы антитела можно вводить после инфицирования или после предполагаемой инфекции до 2, 4, 6, 8, 12, 24, 36, 48, 72 часов после, до 1 суток, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, до недели, 2 недель, 3 недель, 4 недель, до месяца или дольше.
[000194] Способ может включать дополнительное IP или IV введение вирус-специфического моноклонального антитела, где антитело, вводимое дополнительно, представляет собой нейтрализующее или не-нейтрализующее антитело. Антитело, вводимое дополнительно IP или IV, может быть таким же, как антитело, вводимое IN или ингаляционно. Антитела, вводимые дополнительно IP или IV, могут быть введены одновременно, последовательно или последовательно с ингаляционно введенным антителом. Любое такое последующее введение может быть через несколько часов и может быть через 2, 4, 6, 8, 12, 24, 36, 48, 72 или более часов. После введения могут пройти дни, и оно может быть 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней спустя. После введения могут пройти недели, и оно может быть 1, 2, 3, 4 или 5 недель спустя.
[000195] Ингаляционная или интраназальная доза может быть использована для повышения эффективности реакции у пациента или субъекта, который особенно болен или демонстрирует продолжающиеся симптомы инфекции или болезни после начального введения IN или IP или IV или комбинированной дозы.
[000196] В другом аспекте настоящее изобретение обеспечивает протокол для введения моноклонального антитела против респираторного вируса, включающий первое интраназальное или ингаляционное введение дозы нейтрализующих антител и последующее или одновременное введение второй дозы антитела внутрибрюшинно или внутривенно, или также интраназально или ингаляционно, где антитело второй дозы является таким же или отличным от антитела первой дозы. Антитело второй дозы, или какой-либо дополнительной дозы, может быть нейтрализующим или не-нейтрализующим антителом.
[000197] Настоящее изобретение может быть лучше понято со ссылкой на следующие не ограничивающие примеры, которые приведены в качестве иллюстрации настоящего изобретения. Следующие примеры представлены для того, чтобы более полно проиллюстрировать предпочтительные варианты осуществления настоящего изобретения и никоим образом не должны быть истолкованы, однако, как ограничивающие широкий объем изобретения.
ПРИМЕР 1
[000198] Терапевтическое лечение гриппа моноклональными антителами к НА является дозозависимым, а также требует более высоких доз в более позднее время после инфицирования. Типичные терапевтические дозы, вводимые IP или IV, широкореактивных НА специфических антител требуют доз, начиная от 2 мг/кг до 50 мг/кг, чтобы наблюдать защиту от летального исхода. В более поздние времена после инфицирования тот же эффект требует дозирования в диапазонах выше 10 мг/кг. Средний вес взрослого в Северной Америке составляет приблизительно 80,7 кг и потребует 807 мг антител, если необходима доза 10 мг/кг. В настоящее время 2 исследования 1 фазы моноклональных антител против гриппа, CR6261 и CR8020, по Crucell Holland BV оценивают безопасность и переносимость в разовых дозах эскалации от 1 мг/кг до 50 мг/кг (испытания NCT01406418 и NCT01756950 соответственно; clinical trials.gov). Для мышей этих антител требуется 15 мг/кг, чтобы защитить мышей от смерти (Friesen, RHE et al (2010) PLoS ONE 5(2): e1906); Ekiert DC et al (2011) Science 333: 843-850). Таким образом, с использованием данных применимых подходов, приблизительно грамм антител на пациента будут необходимы в расчете на массу человека (приблизительно 70 кг). При любой терапии, направленной на нескольких подтипов гриппа, это усугубляется необходимостью более чем в одном антителе для лечения трех различных циркулирующих подтипов гриппа (гриппа А H3, гриппа А H1 и гриппа В), то есть присутствием порядка 3 граммов антитела, предполагая по грамму каждого антитела. Это большое количество антител становится экономически невыгодным и представляет главное препятствие в разработке терапевтических антител для гриппа.
[000199] Мы предложили решение, как значительно сократить количество антител, более чем в 10 раз, в то же время значительно сохраняя и даже улучшая эффективность. Мы обнаружили, что интраназальная доставка антител дает заметное и значительное улучшение эффективности по сравнению с IV или IP путем. Кроме того, это явление интраназальной эффективности является специфическим для антител, которые являются нейтрализующими, в то время, как не-нейтрализующие антитела обнаруживают нарушенную эффективность при доставке данным путем.
[000200] Проведенные исследования показывают, что интраназальная (IN) доставка нейтрализующих антител может значительно увеличить терапевтическую эффективность, более чем в 10 раз по сравнению с внутрибрюшинными (IP) или внутривенными (IV) путями доставки, используя принятую и известную модель гриппа мыши. Сопоставимая эффективность может быть достигнута с помощью менее чем одной десятой, от той же дозы при IN пути вместо IP или IV путей. Текущие терапевтические режимы для лечения гриппа использовали для внутривенного введения в качестве стандарта (ClinicalTrials.gov Identifier: NCT01390025, NCT01756950, NCT01406418). Этот подход доставки является стандартом в области, поскольку способность накапливать нейтрализующие характеристики антитела не известна. Подавляющее большинство исследований терапии антителами использует IV или IP доставку и не признают, что IN доставка нейтрализующих антител против респираторных патогенов будет улучшать эффективность по сравнению с IV или IP доставкой. С другой стороны, область изобретения не утверждает, что нейтрализация может не быть необходимой для системно доставляемых антител, так как не-нейтрализующие антитела против НА так же эффективны, как и нейтрализующие антитела. В связи с этим, антитела, которые способны быть более широко-реактивными, будет более клинически значимы, чем антитела с возможностью нейтрализации.
[000201] В предыдущих сообщениях о IN доставке оценили поликлональные сыворотки гамма-глобулин иммуноглобулинов или антител класса IgA (IgA антитела по сути характерны для легких) (Akerfeldt S et al (1973) Biochem Pharmacol 22: 2911-2917; Ramisse F et al (1998) Clin Exp Immmunol 111: 583-587; Ye J et al (2010) Clin Vaccine Immunol 17(9): 1363). Одна группа тестировала препарат асцитной жидкости антитела (С179) через IN доставку и описала, что защитная IN доставка (до инфицирования) была сравнима с IP доставкой (Sakabe S et al (2010) Antiviral Res 88(3): 249-255). С179 обладает низкой нейтрализующей активностью в отношении пандемического гриппа H1N1 в 2009 г., но может защитить мышей от инфекции.
[000202] В отличие от этого, мы обнаружили, что важно, что увеличение эффективности не происходит просто для перекрестно реагирующих антител против вируса гриппа, таких как перекрестно-реактивные анти-НА антитела, в действительности антитела, которые являются не-нейтрализующими, при IN доставке не демонстрируют эффективность против гриппа. Известные и более ранние исследования не признают, что этот эффект может быть применен в более широком смысле к антителам, которые обладают in vitro нейтрализующей активностью, независимо от их вирусного эпитопа или белка-мишени. Кроме того, антитела не должны быть перекрестно-реактивными в отношении НА, поскольку штамм-специфические антитела, которые имеют способность к нейтрализации, будут демонстрировать повышенную эффективность при назначении IN. Мы обнаружили, что нейтрализующие антитела (а не просто кросс-реагирующие анти-НА антитела) имеют важное значение для значительного уменьшения количества антитела, необходимого для достижения сравнимой эффективности в зависимости от пути введения. В самом деле, мы обнаружили, что обратное происходит при использовании кросс-реактивных анти-НА антител, которые являются не-нейтрализующими. Терапевтическое использование этих кросс-реактивных не-нейтрализующих анти-НА антител приводит к заметному снижению терапевтической эффективности при обработке мышей интраназально, несмотря на имеющуюся одинаковую эффективность при сравнении этих антител с использованием IP или IV путей доставки.
[000203] Можно заключить, что механизм этого явления состоит в том, что при интраназальной доставке достигается такой уровень антител IgG в дыхательных путях, что можно использовать нейтрализующие возможности антитела, тогда как IV или IP доставка антитела является Fc-зависимой. Иллюстрация показано на фиг. 12. В дыхательных путях ингибирующий механизм основан на нейтрализующих характеристиках антитела, и Fc-зависимый эффект сильно ограничен. При введении IgG антитела IP или IV количество антител, достигающих этого пространства в дыхательных путях, является слишком низким, чтобы извлечь выгоду из нейтрализующего эффекта антител. Например, когда нейтрализующие антитела вводят IP или IV, наблюдаемый терапевтический эффект, в первую очередь происходит из-за эффекторной функции антитела. Мы нашли сопоставимые уровни эффективности нейтрализующих или не-нейтрализующих антител при введении IP или IV, но не IN. Чтобы в дальнейшем проиллюстировать, что этот эффект зависит от нейтрализации, антитела против М2 белка не проявляют нейтрализующие свойства in vitro и только способны проявлять Fc-опосредованные эффекты. Предыдущая работа с использованием антител, направленных против ионного канала М2 (более генетически консервативной молекулы, чем НА), показала многообещающие результаты в доклинических моделях, и завершила первый этап исследования I (TN-032 from Theraclone; NCT01390025, NCT01719874; Grandea AG et al (2010) Proc Natl Acad Sci USA 107(28): 12658-12663). Антитела против белка М2 не могут нейтрализовать вирус, но могут иметь хорошо задокументированную терапевтическую эффективность, опосредованную эффекторной функцией (Wang, R. et al. (2008) Antiviral research 80: 168-177; Grandea, A.G., 3rd et al. (2010) Proc Natl Acad Sci USA 107(28): 12658-12663). Мы считаем, что оба нейтрализующее и не-нейтрализующее антитела при введении IP или IV действуют, прежде всего, через эффекторную функцию, аналогично М2-направленным антителам. Отметим, что, как известно, белка М2 значительно меньше, чем НА, а также он не находится из поверхности. Антитела против НА могут нейтрализовать вирус, предлагая потенциал для дальнейшего улучшения эффективности. Таким образом, как правило, антитела к НА более терапевтически эффективны анти-М2 антител. Тем не менее антитела, которые не являются нейтрализующими и все еще нацелены против НА, могут проявлять сопоставимые уровни эффективности, как нейтрализующие антитела при IP введении, предполагая, что этим путем доставки не удается накопить мощный эффект, который может быть использован при введении IN. Кроме того, доставка нейтрализующих Fabs через IN, но не IP, приводит к терапевтической эффективности. Нейтрализующие Fab-фрагменты, введенные IN, не проявляют терапевтическую эффективность. Все вместе, только нейтрализующие антитела, введенные IN, демонстрируют увеличение эффективности. Продолжая эту наблюдение, это явление будет происходить для нейтрализующих антител, нацеленных на другие белки (например, нейраминидазу), и нейтрализующих антител против возбудителей других респираторных вирусов (например, Palivizumab для RSV). Поскольку доставка антител как IN, так и IP/IV путями, может быть эффективна в различных способах самостоятельно, мы считаем, что использование обоих путей в комбинации будет использовать максимальный терапевтический потенциал нейтрализующего антитела. Такой подход позволит получить максимальную эффективность, используя повышенную нейтрализующую активность по IN пути, и увеличение Fc-зависимой активности по IP/IV пути.
[000204] МАТЕРИАЛЫ И МЕТОДЫ
Ниже приводятся Материалы и методы для примеров, приведенных в данном документе.
[000205] Антитела: Mab6P15, 1Р19 и 1K17 выделяли с использованием фагового дисплея, как описано ниже, и они являются широко-реактивными анти-H3 антителами и не нейтрализуют вирус в анализе микронейтрализации, уменьшении бляшек, или H1. Моноклональные антитела CR8020 CR6261 - хорошо описанные широко-реактивные антитела против вирусов группы 2 и группы 1, соответственно (Throsby M et al (2008) PL0S ONE 3: e3942; Eckert DC et al (2009) Science 324: 246-251; Friesen RHE et al (2010) PLoS ONE 5(2): e1906; US Patent 8,192,927; Eckert DC et al (2011) Science 333: 843-850). Антитела CR9114 связываются с консервативным эпитопом в стволе НА и защищают от летального исхода от вирусов гриппа А и В при введении IV (Dreyfus С et al (2012) Science Express 9 August 2012 10.1126/science.1222908). Эти нейтрализующие антитела мы клонировали путем синтеза вариабельной области и субклонирования в мышиный вектор экспрессии IgG2a. Вариабельную область CR8020 клонировали с помощью опубликованной тяжелой цепи GI: 339779688 и легкой цепи GI: 339832448. Вариабельную область CR6261 клонировали с помощью опубликованной тяжелой цепи GI: 313742594 и легкой цепи GI: 313742595. Вариабельную область CR9114 клонировали с использованием GenBank последовательности присоединения тяжелой цепи JX213639 и присоединения легкой цепи JX213640. Все моноклональные антитела, используемые в этих исследованиях, клонировали в экспрессионные векторы IgG, содержащие вариабельные области человека, слитые с мышиным IgG2a. Химерные антитела для антитела мыши CR6261, CR8020, CR9114 указаны в настоящем документе как СА6261 СА8020 и СА9114, соответственно. Моноклональные антитела 6F12 и GG3 получали из гибридом мыши и связывались с и нейтрализовали вирусы группы 1 и анти-Н1 вирусы (Wang ТТ et al (2010) PLoS Pathog 6(2): e1000796; Tan GS et al (2012) J Virol 86(11): 6179-6188; US Application 20110027270). Mab 5a7 связывались с общим эпитопом на НА вируса В и нейтрализовали вирус и защищали мышей от летального исхода при введении IP (Yasugi M et al (2013) PLoS Pathog 9(2): e1003150, doi: 10.1371/journal.ppat.1003150). Человеческое антитело mAb53 (также обозначается TRL53) описано в US 2012/0020971 и WO 2011/160083 и эффективно в нейтрализации групп 1 и 2 подтипов H1, Н9, Н7 и Н5. Антитело Mab579 (также обозначается TRL579) описывается в WO 2013/086052 и является эффективным в нейтрализации Н3 и Н7. Опубликованные последовательности, в том числе последовательности вариабельных областей тяжелой и легкой цепи антител, и в частности последовательности CDR домена тяжелой и легкой цепи (CDR1, CDR2 и CDR3) выше отмеченных и проиллюстрированных антител в данном описании, в частности, в том числе CR6261, CR8020, CR9114, 5а7, mAb53 и Mab579, известны и общедоступны, в том числе в ссылках, указанных выше, и включены в данное описание путем ссылки.
[000206] Фаговый дисплей: Фрагменты антител были отобраны путем множества циклов панорамирования против рекомбинантного гемагглютинина (НА) ((Immune Technologies Corp, New York) гриппа или очищенного центрифугированием на сахарозной подушке вируса гриппа. Вкратце, антиген разводили в PBS и инкубировали в течение ночи при 4°С в планшете MaxiSorp Nunc-Immuno (Nunc). Планшеты дважды промывали PBS. Планшеты инкубировали с 5% молоком в PBS в течение 2 ч при комнатной температуре при постоянном встряхивании. Фаговую библиотеку блокировали в 2,5% молоке в PBS с 2,5% фетальной бычьей сывороткой и 0,005% твином. Блокированный фаг добавляли в заблокированные планшеты в течение 2 ч при комнатной температуре на качалке при приблизительно 400rpm. Планшеты промывали PBST и связанный фаг элюировали DTT буфером для элюции. Элюированный фаг инкубировали с клетками TG1 в течение 45 минут при 37°С. Клетки высевали на 15 см чашки, содержащие культуральную среду LB, хлорамфеникол (САМ) и глюкозу (Glc) и инкубировали в течение ночи при 30°С.Скалывали колонии с планшета и осаждали полиэтиленгликолем для последующих раундов панорамирования. Три или четыре раунда панорамирования проводили с использованием либо антигена НА из того же штамма или НА другого штамма. Финальный раунд панорамирования высевали на большие Q лотки для Q-скола колоний комплектации в 384-луночные планшеты.
[000207] Проверка Fab: Fab кодирующие лизаты фагов скринировали ELISA в отношении рекомбинантного НА. Отдельные колонии скалывали в 384-луночные планшеты, содержащие 2XYT/Cam с низким содержанием глюкозы с использованием Qpix. Планшеты растили в течение 2-4 часов при 30°С при 400rpm. Fab экспрессию индуцировали 0,5 мМ IPTG и растили в течение ночи при 22°С и 400rpm. Fab-содержащие клетки лизировали в BEL буфере, содержащем Benzonase, при 22°С и в течение 1 часа при 400rpm. Fab-содержащие лизаты блокировали 12,5% MPBST в течение 30 мин при 22°С при 400rmp. Лизаты добавляли в планшеты ELISA с НА-подложкой в течение 1 часа при комнатной температуре. Планшеты промывали пять раз PBST, а затем инкубировали с анти-Fab IgG, конъюгированного с щелочной фосфатазой, в течение 1 часа при комнатной температуре. Планшеты промывали пять раз TBST и проявляли с AutoPhos (Roche, New Jersey). Планшеты считывали с помощью Infinite Pro F200. Положительные лизаты фагов секвенировали и уникальные Fabs субклонировали в экспрессионные конструкции, содержащие с-myc и его таг для дальнейшей характеристики.
[000208] Fab экспрессия: Fab экспрессирующими плазмидами трансформировали электротрансформацией TG1 F-клетки и их высевали на LB/САМ чашки с агаром. Чашки инкубировали при 37°С в течение ночи. 5 мл 2xYT/CAM/Glc инокулировали одной колонией и выращивали в течение ночи при 30°С и 350rpm. 500 мл 2xYT/CAM с низким содержанием Glc засевали 2 мл ночной культуры и, не встряхивая, растили при 30°С и 180rpm, пока OD при 600 нм 0,5 не была достигнута. Fab-экспрессию индуцировали добавлением IPTG в конечной концентрации 0,75 мМ. Культуры встряхивали при 30°С в течение ночи при 160rpm. Культуры центрифугировали в течение 30 мин при 5,000g и 4°С. Бактериальные осадки замораживали при -80°С в течение не менее 2 часов. Клетки лизировали и фильтровали через 0,22 мкм фильтр и подвергали очистке путем IMAC и вытеснительной хроматографией.
[000209] Клонирование и экспрессия антител: Fab-кодирующие фаги секвенировали и субклонировали в экспрессионные плазмиды IgG для соответствующих тяжелых и легких цепей. IgG нарабатывали в Invitrogen 293F или Invitrogen 293Expi клетках в шейкерных колбах. Клетки трансфицировали экспрессионными плазмидами для тяжелых и легких цепей. Культуральные супернатанты собирали через шесть дней после трансфекции и очищали с использованием белка А путем аффинной хроматографии и методом смены буфера.
[000210] Терапевтические исследования эффективности на мышах: Самцы мышей 6-7 недель BALB/c использовали во всех экспериментах. Всех мышей акклиматизировали и держали в течение периода по меньшей мере трех дней до начала эксперимента. Мышей взвешивали в день инфицирования вирусом, а затем ежедневно в течение 2 недель. Использовали клиническую систему подсчета в качестве критериев для клинической конечной точки и удаления из исследования. Клинические признаки считали следующим образом: выгибание спины = 3, пилоэрекция = 3, отказ от еды или питья = 2, потеря веса × 30% = 10, неврологические симптомы = 10. Мышей удаляли из исследования и умерщвляли при достижении счета 16 или больше. Исследования на животных проводили в соответствии с утвержденным протоколом Institutional Animal Care and Use Committee. Терапевтическую обработку мышей проводили через указанные дни после инфицирования. Мышей сначала анестезировали смесью кетамина/ксилазина до интраназального введения вируса, Mab, или Fab в 50 мкл объема на мышь. Перитонеальное введение Mab или Fab проводили в 100 мкл объема. Определяли средний вес тела для каждого дня в течение 14-дневного периода исследования и показывали относительно среднего веса тела в день 0.
[000211] Вирусы: Штаммы вируса гриппа (в том числе A/California/ 7/09, A/Victoria/ И) адаптировали для мышей в соответствии с Cottey, Rowe, and Bender (Current Protocols in Immunology, 2001). Проводили три раунда адаптации мышей с последующим одним раундом распространения вируса в эмбрионированных яйцеклетках. Вкратце, три 6-8 недельных мышей анестезировали и инфицировали интраназально 20 мкл вируса. Через три дня после инфицирования мышей умерщвляли и удаляли легкие. Легкие механически гомогенизировали, очищали и центрифугировали для удаления больших кусков дебриса. Дополнительные пассажи в наивных мышей 20 мкл гомогената легкого проводили в течение трех раундов.
[000212] ССЫЛКИ
Huber VC, Lynch JM, Bucher DJ, Le J, Metzger DW: Fc receptor-mediated phagocytosis makes a significant contribution to clearance of influenza virus infections. J Immunol 2001, 166: 7381-7388.
Jegerlehner A, Schmitz N, Storni T, Bachmann MF: Influenza A vaccine based on the extracellular domain of M2: weak protection mediated via antibody-dependent NK cell activity. J Immunol 2004, 172: 5598-5605.
Feng J, Mozdzanowska K, Gerhard W: Complement component C1q enhances the biological sctivity of influenza virus hemagglutinin-specific antibodies depending on their fine antigen specificity and heavy chain isotype. J Virol 2002, 76: 1369-1378.
Mozdzanowska K, Fcng J, Eid M, Zharikova D, Gerhard W: Enhancement of neutralizing activity of influenza virus-specific antibodies by serum components. Virology 2006, 352: 418-426.
ПРИМЕР 2
НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА ЭФФЕКТИВНЫ ИНТРАНАЗАЛЬНО ЭКСПЕРИМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
[000213] Терапевтическая эффективность системно доставляемых антител не полностью зависит от способности к нейтрализации, так как оба нейтрализующие и не-нейтрализующие антитела, введенные IP, обладают схожими эффектами в лечении и профилактике летальной инфекции. Нейтрализующие и не-нейтрализующие антитела были одинаково эффективны при введении IP 10 мг/кг через 24 часа после инфицирования (24hpi) (Фигура 1). Результаты, показанные на фиг. 1, показывают, что системно доставляемые антитела против НА могут оказывать надежную терапевтическую эффективность через эффекторную функцию, как несколько не-нейтрализующих антител (6Р15, 1Р19 и 1K17) защищают мышей от летального исхода в той же степени, как нейтрализующие антитела СА8020. Нейтрализующие и не-нейтрализующие антитела являются одинаково профилактически эффективными при IP введении за 1 час до инфицирования (1hpi) вирусом (фигура 2). Аналогичные результаты наблюдали при 1hpi и с использованием различных вирусов (данные не показаны). Эти результаты ставят под сомнение, значительно ли способствует нейтрализация в терапевтической эффективности при системной доставке. Доставка антител IV или IP путем не приводила к значительным различиям в эффективности (фиг. 3 и данные не показаны).
[000214] В отличие от этого, IN доставка нейтрализующих антител значительно повышала их терапевтическую эффективность по сравнению с системной доставкой (фигура 4). Это повышение в терапевтической эффективности специфично для нейтрализующих антител, а не-нейтрализующие антитела не проявляли аналогичной повышенной терапевтической эффективности. Фиугра 4 показывает, что способность Mab (СА8020) демонстрировать повышенную эффективность при IN доставке зависит от его способности к нейтрализации. Нейтрализующие моноклональные антитела, специфичные для вируса H3, обладают повышенной эффективностью при IN введении, но не нейтрализующие моноклональные антитела не показывают такой эффективности. В отличие от IP-доставки, как видно на фигуре 1, IN доставка нейтрализующих антител предлагает значительное терапевтическое преимущество по сравнению с не-нейтрализующими антителами. Эта расширенная эффективность в терапии коррелирует со способностью антитела нейтрализовать, в то время как не-нейтрализующие антитела, такие как 6Р15, 1K17 и 1Р19 не обладают улучшенной терапевтической эффективностью при IN введении. Наоборот, не-нейтрализующих моноклональные антитела демонстрируют заметно сниженную эффективность при ведении IN по сравнению с IP. Как видно на фиг. 4, не-нейтрализующие антитела (антитела с образцовым 6Р15), вводимые IP в 10 мг/кг, могут защитить мышей от 10xLD50 при 24hpi аналогично нейтрализующим антителам в аналогичных дозах. Однако, не-нейтрализующие антитела не продемонстрировали повышенный терапевтический эффект при введении IN. Репрезентативные данные для не-нейтрализующих антител 6Р15 показаны в качестве примера. Подобные результаты были получены для других не-нейтрализующих антител, включая антитела 1K17 и 1Р19 (данные не показаны).
[000215] Повышенная эффективность при введении IN также продемонстрирована широко узнающими антителами против H1 вируса СА6261 (антитело IgG2a, связывающее короткую альфа спираль НА2 субъединицы) (Фигура 7), антитело 6F12 (антитело IgG2b, нацеленное на область стебля НА) (фигура 14) и GG3 антитело (фигура 15) проверяя эффект для многочисленных различных антител и устанавливая, что IN эффективность согласуется для нейтрализующих антител, направленных против нескольких целей и подтипов вируса гриппа. При дальнейшей проверке эффект эффективности IN мы оценили еще кросс-защитные антитела CR9114 и показали, что они весьма эффективны IN (фигура 16). CR9114 связывают консервативный эпитоп в стволе НА и защищают от летального исхода вирусов гриппа А и В при введении IV (Dreyfus С et al (2012) Science Express 9 August 2012 10.1126/science. 1222908).
[000216] Мы не наблюдали значительную разницу в отношении антител, имеющих различные изотипы антител, так же как и при интраназальном введении. Изотипные различия были обнаружены при IP дозировании, предполагая, что эффекторная функция может быть актуальна. Кроме того, единичные нейтрализующие антитела были эффективны в блокировании инфекции нескольких штаммов их целевых H1 или H3 вирусов, что указывает на эффективность не является штамм-специфической или ограниченной. Мы показали, что нейтрализующее антитело CR6261 более чем в 10 раз более мощное при IN введении, чем при введении IP, против двух разных H1 вирусов, в частности PR8 (фигуры 5, 7 и 9) и мышь-адаптированного Cal/ 09 (фигура 17). Таким образом, IN введение представляет жизнеспособную и действительно более эффективную альтернативу для нейтрализующих антител, направленных против вируса гриппа.
ПРИМЕР 3
НЕЙТРАЛИЗУЮЩИЕ Fabs ЭФФЕКТИВНЫ ИНТРАНАЗАЛЬНО
[000217] Мы далее исследовали, отменит ли удаление Fc терапевтическую эффективность при IP или IN ведении нейтрализующих и не-нейтрализующих Fabs. Как видно на фиг. 5, Fab при IP-введении (Fab антитела СА6261) не обеспечивает терапевтическую эффективность против вируса H1 при 10 мг/кг или ниже. Мыши, обработанные Fab IP, все поддались инфекции, подобно PBS-обработанным мышам. В отличие от этого, мыши, обработанные нейтрализующими Fab IN в дозе 10 мг/кг и 1 мг/кг, смогли выжить при летальной инфекции (фигура 5). Все дозы, вводимые IN, (даже 0,1 мг/кг) показали большую эффективность, чем любая IP доза. Сравнимые результаты наблюдали при сравнении Fab СА6261 IN против IP или IV в том же эксперименте, в котором Fab-CA6261 не были защитными или эффективными при введении либо IP, либо IV, но показывали значительную эффективность (животные сохраняли 95% или больше веса тела) при той же дозе (5 мг/кг), вводимой IN (данные не показаны). Эти данные показывают, что Fab-фрагменты являются эффективными для блокирования или лечения вирусной инфекции интраназально для нейтрализующих антител. Кроме того, данные показывают, что системная доставка Mab требует эффекторной функции Fc для терапевтической эффективности, потому что Fab-фрагменты были неэффективны.
[000218] Fabs от не-нейтрализующих антител не сохраняют терапевтический эффект при введении IN путем. На фигуре 6, мышей, инфицированных вирусом H3, обрабатывали доставкой очищенных Fab примерных антител СА8020 и 6Р15. В то время как нейтрализующие Fabs способны показать терапевтическую эффективность, не нейтрализующие Fabs не способны защитить мышей от летального исхода. Эти данные показывают, что Fab-фрагменты от не-нейтрализующих антител не проявляют терапевтическую эффективность при введении IN.
ПРИМЕР 4
IN ДОСТАВКА В 10-100 РАЗ БОЛЕЕ АКТИВНАЯ, ЧЕМ IP-ДОСТАВКА
[000219] Мы обнаружили, что, на удивление, интраназальная (IN) доставка нейтрализующих антител в 10-100 раз более активная, чем внутрибрюшинная (IP) доставка. Мышей инфицировали вирусом 10xLD50 PR8 IN (вирус H1) и через 24hpi обрабатывали антителом (фигура 7). Нейтрализующие антитела СА6261 серийно разводили в десять раз и вводили либо IN, либо IP путем (7А). Мыши, обработанные IN путем, демонстрировали меньшую тяжесть заболевания, что указано потерей веса, и были на 100% защищены от смертельной инфекции при всех разведениях. Для сравнения, мыши, обработанные только IP, при самой высокой дозе (10 мг/кг) демонстрировали переходную потерю веса и защиту от летального инфицирования. Все низкие разведения не защищали мышей при введении IP-путем. В противоположность этому, IN обработка дозой 0,1 мг/кг приводила к транзиторной потери веса и выживаемости всех мышей. Мыши, обработанные IN доставкой дозы 10 мг/кг и 1 мг/кг, были защищены от обнаруживаемой потери веса во все времена после инфицирования. Антитела, введенные IP путем, при всех дозах демонстрировали некоторую степень потери веса, и только мыши, обработанные самой высокой дозой 10 мг/кг, выживали после инфекции.
[000220] Мы подтвердили, что интраназальная доставка нейтрализующих антител аналогично приводит к усилению терапевтической эффективности против H3 вирусов. Мышей инфицировали вирусом H3 и обрабатывали через 24hpi (фигура 8). Нейтрализующие антитела СА8020 серийно разводили в десять раз и вводили IN или IP. Как отмечается в наших исследованиях с вирусом H1, антитела, вводимые IN, обеспечивали 100% выживаемость при всех разведениях против вируса H3, и демонстрировали меньшую потерю веса, чем антитела, вводимые IP.
[000221] Вместе эти данные показывают, что нейтрализация имеет важное значение для повышения терапевтической эффективности при IN доставке. Кроме того, терапевтическая эффективность системно доставленных антител не зависит от нейтрализации, так как сходные уровни эффективности могут наблюдаться для обоих нейтрализующих и не-нейтрализующих антител. Поддерживая это наблюдения, терапевтическая эффективность нейтрализующего Fab отменена при введении IP, но нейтрализующий Fab демонстрирует эффективность при доставке IN. Нейтрализующие Fab, вводимые IN, демонстрируют аналогичное повышение эффективности по сравнению с введением IP так же, как и при доставке их полного Mab.
ПРИМЕР 5
ИНТРАНАЗАЛЬНАЯ ЭФФЕКТИВНОСТЬ. ПОДДЕРЖИВАЕМАЯ ПОСЛЕ ИНФИЦИРОВАНИЯ
[000222] Повышенная эффективность IN доставляемых нейтрализующих антител сохраняется в более поздние времена после инфицирования. На фигуре 8, мышей обрабатывали через 48hpi либо IN, либо IP. При IN доставке нейтрализующих антител снова более терапевтически эффективны, чем при IP доставке. Полная защита от летального исхода достигалась при 1 мг/кг при введении IN, в то время как IP-доставка обеспечивает полную защиту против летального исхода в дозах 10 мг/кг. IN дозирование показало сравнительно сниженную эффективность при 72hpi, но оставалось значительно улучшенным по сравнению с IP дозированием в том же количестве при 72hpi. График выживаемости демонстрирует эффективность СА6261 при введении IN через 72hpi, и очень значительно улучшенное выживание по сравнению с IP в тех же дозах показано на фигуре 18.
ПРИМЕР 6
IN ВВЕДЕНИЕ ЭФФЕКТИВНО В НИЗКИХ ДОЗАХ
[000223] Интраназальная доставка нейтрализующих антител может обеспечить полную защиту от летального исхода при очень низких дозах при введении после инфицирования. Как показано на фигуре 10, в дозах столь же низких, как 0,005 мг/кг антитела СА8020, введенные через 8hpi, приводили к 100% выживаемости против 10XLD50 вируса. Эти дозы в тысячу раз меньше, чем стандартные дозы для IV или IP обработки после инфекции. Эти результаты показывают, что удивительно низкие дозы при IN введении могут достичь терапевтической эффективности.
[000224] Оценивали эффективность повторного IN введения. Повторное IN дозирование Mab СА8020 через 8hpi, 32hpi и еще раз через 56hpi давало эффективность с использованием низкого повторного дозирования 0,005 мг/кг на дозу, а также при повторном дозировании 0,001 мг/кг (фигура 11). Эффективность была несколько улучшена по сравнению с одной дозой через 8hpi. Дополнительные исследования демонстрировали защиту с помощью антител СА6261, введенных через 8hpi, являющимися защитными при 0,045 мг/кг, и оценивали более низкие дозы (данные не показаны).
[000225] Вместе эти результаты показывают, что нейтрализация имеет важное значение для увеличения эффективности, поскольку не-нейтрализаторы не демонстрируют повышенную эффективность. Таким образом, Fab-фрагменты нейтрализующих антител при введении по IN пути сохраняют повышенную эффективность, тогда как Fabs от не-нейтрализующих антител не проявляют заметной эффективности. Наоборот, ни нейтрализующий, ни не-нейтрализующие FABs не демонстрируют эффективность при введении IP, предполагая, что оба нейтрализующие и не-нейтрализующие моноклональные антитела зависят от эффекторных функций области Fc при введении IP. Модель инфекции, показанная на фигуре 12, показывает, что усиление эффективности путем IN введения зависит от нейтрализации антитела, в то время как системная доставка опирается четко на эффекторную функцию.
ПРИМЕР 7
КОМБИНИРОВАННЫЙ IN/ΙΡ ПРОТОКОЛ ОБЕСПЕЧИВАЕТ ПОВЫШЕННУЮ ЭФФЕКТИВНОСТЬ
[000226] Основываясь на модели, показанной на фигуре 12, мы исследовали гипотезу, что IP и IN доставляемые антитела демонстрируют отдельные, неизбыточные функций. Если все верно, антитела при IN ведении, объединенном с IP-путем, будут проявлять повышенную эффективность по сравнению с единственным путем введения в одиночку. На фигуре 13A-13D мы показываем, что комбинированная IN и IP-доставка является более эффективной, чем только IP-доставка, при различных комбинированных режимах дозирования (общие дозы антител в этих исследованиях составляли 5 мг/кг или 2 мг/кг). Улучшенная эффективность обеспечивается с помощью комбинации IN и IP введения по сравнению с IP или IN группами подтверждает, что механизмы действия и требования к Mab, вводимых IN и IP, различны и могут быть не-вырожденными. Улучшенная противовирусная эффективность обеспечивается с помощью комбинированного режима IN и IP введения с использованием нейтрализующих антител для IN и нейтрализующих или не-нейтрализующих антител в комбинированном режиме введения по IP-пути. Дальнейшие исследования показали, что IN введение нейтрализующих антител (в качестве примера антитело СА8020), в сочетании с IP-введением такого же нейтрализующего антитела или отдельного не-нейтрализующего антитела (в качестве примера антитело 6Р15) является так же эффективным, даже при использовании низкой дозы 0,1 мг/кг IN и 0,5 мг/кг IP при общем количестве вводимого антитела только 0,6 мг/кг (фигура 19). Реализация IN введения в целом может снизить количество антитела, необходимого для эффективности, даже в сочетании со сравнительно низкими дозами IP-вводимых антител. Механизм действия IN-вводимого антитела может, прежде всего, ограничить распространение вируса, в то время как IP-вводимое антитело может в первую очередь уменьшить количество зараженных клеток, продуцирующих вирус, через эффекторную функцию.
[000227] Исследовали механизм действия путем изотипического переключения нейтрализующих антител при ведении IN или IP. Мышиные IgG1 обладают сниженной эффекторной функцией по сравнению с мышиными IgG2a. У IN-доставляемых антител установлены аналогичные уровни эффективности, независимо от изотипа, как видно для СА6261 и СА8020. У IP-вводимых антител установлены заметные различия в терапевтической эффективности, зависящие от изотипа. Антитела изотипа IgG2a были значительно более эффективными, чем мышиные IgG1 антитела, как для СА6261, так и СА8020 (данные не показаны). Это говорит о том, что основной механизм действия системно доставляемых антител происходит через эффекторную функцию. Как таковые, известные способы повышения эффекторной функции с помощью различных средств (например, но не ограничиваясь, модификацией Fc, либо а-фукозилированием) улучшили бы эффективность системно доставляемых антител и могли бы быть включены в антитела, доставляемые интраназальным или ингаляционным способом. Антитела, доставляемые интраназально или ингаляционно, могут активировать комплимент, привлечь альвеолярные макрофаги и/или иметь ограниченное распространение на базисной боковой поверхности, где участие эффекторной функции может обеспечить улучшенную эффективность.
ПРИМЕР 8
ЭФФЕКТИВНОСТЬ АНТИТЕЛА ПРОТИВ ВИРУСА ГРИППА В
[000228] Антитело CR9114 связывается и является эффективным против вирусов гриппа типа А и также типа В, как указано выше и показано в таблице 1 и сообщалось ранее (Dreyfus С et al (2012) Science 337(6100):1343-1348). Химерные антитела СА9114 (как описано выше, имеющие вариабельные области человека, слитые с мышиным IgG2a) испытывали в мышиной модели на эффективность против штамма гриппа B/Malaysia. IΝ и IP-дозирование 10 мг/кг, 1 мг/кг и 0,1 мг/кг испытывали через 24 hpi на эффективность против 10XLD50 B/Malaysia (обозначается как В/Mal). Результаты представлены на фигуре 20. IN введение было более эффективным, чем IP, при всех испытанных дозах. СА9114 антитела, доставленные интраназально, через 1 день после инфицирования вирусом гриппа В, были эффективными для обработки животных и устраняли потери массы тела вследствие вируса гриппа.
[000229] Серия моноклональных антител с продемонстрированной способностью связывать и нейтрализовать вирус гриппа типа В in vitro, в том числе многочисленные В антитела, выделенные с помощью фагового дисплея, как описано выше, а также антитела СА9114, испытывали интраназально против вируса B/Florida и B/Malaysia. Каждое антитело вводили в дозе 1 мг/кг через 24 hpi с вирусом гриппа В 10xLD50. Результаты, представленные на фиг. 21 и 22, демонстрируют эффективность интраназального введения различных моноклональных антител против гриппа B/Florida и B/Malaysia по сравнению с СА9114 антителом. Аналогичные исследования проводили с СА9114 и различными антителами против В/Mal, вводимые в дозе 1 мг/кг через 8hpi (фигура 23). Все антитела тестировали на эффективность против обоих типов вируса В. Эти исследования подтверждают эффективность антител против вируса гриппа, вводимых интраназально против вируса гриппа В, в том числе через 8 или 24 часов после инфицирования.
[000230] Дополнительные антитела к вирусу гриппа В тестировали на эффективность в животных против вируса B/Florida или B/Malaysia. Антитела 5А7, CR8033 и mAb809 оценивали при введении IN в дозе 1 мг/кг 24 hpi 10XLD50 вируса В, и вируса B/Florida, и вируса B/Malaysia (фигура 37 и фигура 38, соответственно). Все введенные IN антитела были полностью активны против инфеции против обоих вирусов типа В в количестве 10XLD50, обработанные антителами животные сохраняли до 100% массы тела.
ПРИМЕР 9
КОМБИНИРОВАННЫЕ ИССЛЕДОВАНИЯ АНТИТЕЛ
[000231] Современные вакцины гриппа включают антигены, вызывающие иммунитет к циркулирующим штаммам вируса гриппа в человеческой популяции. Квадривалентная вакцина против гриппа покрывают вирусы гриппа А, в частности, подтип вируса H1 и H3, а также вирус гриппа В линий Yamagata и Victoria. Учитывая выше эффективность, продемонстрированную интраназально вводимыми антителами, направленными против гриппа подтипов А и также В, и что несколько антител были эффективны в комбинации, проводили исследования с комбинациями антител. Эти комбинации включают комбинации, которые имитируют, и их можно сравнить с установленными трехвалентными и четырехвалентными вакцинами, используемыми в настоящее время. Таким образом, в целях лечения гриппа, предотвращения инфекции или предотвращения передачи, композиции комбинации интраназально вводимых антител оценивали в естественных условиях на животных моделях и оценивали против вирусов гриппа А и гриппа В.
[000232] Смесь из двух антител против гриппа А и гриппа В, в частности антитела 43J23 (моноклональное антитело против гриппа В, выделенное фаговым дисплеем), GG3 антитела (анти-Н1 антитела против гриппа А) и СА8020 (анти-H3 антитела против гриппа А), оценивали в комбинации на эффективность против инфекции гриппа А H1, H3 и гриппа В. Смесь с общим количеством антитела 3 мг/кг, 1 мг/кг каждого из антител 43J23, GG3 и СА8020, вводили интраназально в 50 мкл общего объема через 24 часа после инфицирования (24hpi) с вирусом гриппа. На фиг. 24 показаны результаты исследования эффективности использования смеси после инфицирования гриппом B/Florida (Yamagata). Эффективность смеси против инфекции вируса В была сравнима с эффективностью только антитела против вируса В 43J23 в дозе 1 мг/кг. IP-введение СА9114 антитела в дозе 1 мг/кг не защищало животных от вирусной инфекции В, что оценено в процентах к весу тела. Следует отметить, что приведенные выше примеры показали, что антитело СА9114 является эффективным против вируса В при введении в дозе 1 мг/кг интраназально (IN). Фигура 25 отображает результаты аналогичного исследования со смесью антител 43J23, GG3 и СА8020 против вируса B/Malaysia. Считая, что та же смесь аналогично эффективна против вируса гриппа А, смесь сохраняла массу тела у животных после инфицирования вирусом H1 (фигура 26). Эффективность смеси в этом исследовании (фиг. 26) была такой же, как и у анти-Н1 антитела GG3, вводимого IN отдельно в дозе 1 мг/кг. Смесь антител была так же эффективна против вируса гриппа А подтипа H3 (фигура 27), снова так же эффективна в смеси по сравнению с интраназальным дозированием только единственного анти-Н1 антитела (СА8020), в условиях, когда IP-введение СА8020 было не так эффективно при той же дозе. Фигура 28 отображает исследование смеси интраназально вводимых антител (анти-В антитело 43J23, анти-А H1 антитело GG3 и анти-А H3 антитела СА8020) против каждого из 4 циркулирующих подтипов вирусов гриппа, показывающее эффективность против H1, H3, В (Yamagata) и В (Victoria) в одном эксперименте.
[000233] Другую интраназально вводимую смесь оценивали в сопоставимых исследования с использованием другой комбинации антител против вируса гриппа В и антител против вируса гриппа А. В этом исследовании анти-H3 антитела СА8020 использовали в сочетании с анти-Н1 антителом СА6261 и анти-В антителом 5а7. 5а7 антитела недавно стали известны, как широко нейтрализующие штаммы гриппа В, изолированные от 1985 до 2006, принадлежащие к обеим линиям Yamagata и Victoria (Yasugi M et al (2013) PLoS Pathog 9(2): e1003150, doi: 10.1371/journal.ppat.1003150). Вариабельные области тяжелой и легкой цепи антитела, как сообщалось, были клонированы в IgG вектор экспрессии, содержащий вариабельные области, слитые с мышиным IgG2a (аналогично тому, как описано выше, и в примере 1). 1 мг/кг каждого из антител 5а7, СА6261 и СА8020 вводили в общей дозе 3 мг/кг антитела интраназально животным через 24 часа после инфицирования вирусом гриппа. Эту смесь испытывали против вируса H1, вируса H3), линий вируса В (Yamagata) и В (Victoria), и она была эффективной против любого и всех протестированных вирусов (фигура 29).
ПРИМЕР 10
АЛЬТЕРНАТИВНАЯ ЭФФЕКТИВНОСТЬ АНТИТЕЛ ПРОТИВ ВИРУСОВ ГРИППА H1 И Н3
[000234] Эффективность введения в дыхательные пути с помощью интраназального введения, оценивали дополнительными альтернативными антителами против гриппа. Человеческие моноклональные антитела выделяли непосредственно из человеческих субъектов, которые нейтрализуют и имеют эффективность против вирусов гриппа А обеих групп 1 и 2. Антитело человека mAb53 (также обозначается TRL53) описано в US 2012/0020971 и WO 2011/160083 и эффективно в нейтрализации групп 1 и 2 H1, Н9, Н7 и Н5 подтипов. Антитело Mab579 (также обозначается TRL579) описано в WO 2013/086052 и является эффективным в нейтрализации H3 и Н7. Mab579 и антитела 53 тестировали в мышиной модели терапевтической эффективности против инфекции вируса гриппа А. Mab579 тестировали против гриппа H3, и mAb53 тестировали против гриппа H1. Сравнивали IP-дозирование с IN-дозированием при 1 мг/кг и IP-дозированием в дозе в десять раз выше 10 мг/кг. Антитела Mab579 вводили через 24 часа после инфицирования (24hpi) для эффективности лечения против 10XLD50 H3 вируса гриппа Vic11 (фигура 30). Антитела mAb53 вводили через 24 часа после инфицирования (24hpi) для эффективности лечения против 10XLD50 H1 вируса гриппа Cal09 (фигура 31). IN введение было более эффективным, чем введение IP, даже при введении IP в 10 раз более высокой дозе в одном эксперименте.
ПРИМЕР 11
ИССЛЕДОВАНИЯ ПРОФИЛАКТИКИ ИНТРАНАЗАЛЬНО ВВОДИМЫМИ АНТИТЕЛАМИ
[000235] Учитывая значительную эффективность интраназального введения нейтрализующих антител после инфицирования, проводили исследования для оценки эффективности интраназального введения профилактически и до инфицирования вирусом. Эти исследования служат для оценки и демонстрации применимости интраназального введения в случаях, когда лицо подвергается вирусу гриппа, и в качестве эффективного подхода для предотвращения или уменьшения передачи в пределах подвергаемых групп или группах риска, или клинически больных, где инфекция или болезнь будет, в общем, большим риском для здоровья. Антитела СА6261 Группы 1 (H1) оценивали в течение нескольких дней на введение, предшествующее инфицированию вирусом гриппа в мышиной модели животных. Введение СА6261 оценивали через 3, 4, 5, 6, и 7 дней до вызова инфицирования, и IN и IP дозирование при различных дозах сравнивали непосредственно.
[000236] В первых исследованиях антитела СА6261 вводили IN или IP, мышей затем обрабатывали 3XLD50 дозой вируса H1 PR8. Фигура 32 отображает исследования IN и IP профилактического введения за 3 или 4 дня до инфицирования вирусом. Антитела СА6261 вводили IN или IP за 3 или 4 дня до инфицирования 3XLD50 PR8. СА6261 антитело вводили IN (0,1 мг/кг) или IP (0,1 мг/кг и 1 мг/кг). IN введение за 4 дня до инфицирования (-4dpi) (оценивается в 0,1 мг/кг) защищало мышей от инфицирования вирусом. IP введение за 3 или 4 дня до инфицирования в той же дозе (0,1 мг/кг) было полностью неэффективным. IP введение за 3 или 4 дня до инфицирования было эффективным при дозе 1 мг/кг. При сравнении IN (0,1 мг/кг) и IP (1 мг/кг) введения за -3dpi и -4dpi, в обоих случаях, в десять раз меньшая IN доза была более эффективна, чем IP.
[000237] Профилактическую эффективность оценивали за 5, 6 и 7 дней до инфицирования вирусом, с результатами, изображенными на фигуре 33. В десять раз более высокую IP-дозу оценивали в сравнении с IN введением. Антитело СА6261 вводили IP (1 мг /кг) или IN (0,1 мг/кг) либо за 5, 6 или 7 дней до инфицирования вирусом 3XLD50 H1 гриппа PR8. Введение Тамифлю (10 мг/кг перорально, дважды в день в течение пяти дней) оценивали также для сравнения. Эффективность была продемонстрирована при 0,1 мг/кг, при IN введении за -5dpi. Не все мыши выжили при 0,1 мг/кг при IN введении за 6 или 7 дней до инфицирования вирусом. Десятикратно высокие дозы IP (10 мг/кг) оказались эффективны за 5, 6 или 7 дней до инфицирования. IN введение антител в дозе 0,1 мг/кг за 5 дней до инфицирования было, по меньшей мере, так же эффективно, как IP-введение в дозе в десять раз выше (1 мг/кг) за 7 дней до инфицирования.
[000238] Более высокие IN дозы 1 мг/кг оценивали за 5, 6 и 7 дней до инфицирования вирусом. Фигура 34 отображает исследования IN введения в сравнении с IP введения антитела СА6261, вводимого IP или IN, в дозах по меньшей мере 1 мг/кг за 5, 6 или 7 дней до инфицирования вирусом 3XLD50PR8. IN введение 1 мг/кг антитела было эффективно профилактически за 7 дней до инфицирования вирусом, и в каждом случае IN было более эффективным, чем то же количество вводимого антитела, вводимого IP. Действительно, IN введение в любое время (за 5, 6 или 7 дней до инфицирования) было более эффективным, чем любое IP введение, даже если IP-введение проводили ближе к инфицированию вирусом по времени. Во всех случаях, антитело было более эффективным, чем Тамифлю.
[000239] Приведенные выше исследования показывают, что IN введение в самом деле превосходит IP введение для профилактической защиты. IN введение 0,1 мг/кг антитела защищает от инфицирования (3xLD50) за 5 дней до инфицирования (-5dpi). Та же доза 0,1 мг/кг, вводимая IP в любой из дней за 3-7 дней до инфицирования вирусом, не защищает животное (по сравнению с аналогичной 3xLD50 дозой вируса). При более высоких дозах IN введенного антитела (оценивали 1 мг/кг) IN введенное антитело может защитить от инфицирования при введении по меньшей мере за 7 дней. IN введение за более, чем 7 дней, не оценивали, но оно может быть эффективным.
[000240] Кроме того, многократное дозирование IN введением до инфицирования, по прогнозам, будет потенциально более эффективным (см. примеры выше и фигуру 11). Как показано на фиг. 11, повторяемое после инфекции дозирование является эффективным, и более низкие дозы интраназально эффективны при нескольких часах дозирования друг от друга (8 часов, 32 часа, 52 часа). Аналогично, повторное дозирование до вирусной инфекции или воздействия, по прогнозам, будет эффективным и может позволить более низкие IN дозы при профилактической дозировке.
[000241] Профилактическую эффективность оценивали при более высоких дозах до инфицирования вирусом, в частности введение антитела СА2621 за несколько дней до вызова 10XLD50 вируса PR8 H1. За три и четыре дня до инфицирования вирусом 10xLD50 PR8 H1 подтипа животным вводили 0,1 мг/кг антитела СА6261 IN или IP (Фигура 35). IP-введение 0,1 мг/кг антитела за 3 или 4 дня до инфицирования вирусом было совершенно неэффективным, IP-обработанные животные поддавались вирусным инфекциям подобно животным, которые не получали никакой обработки. В отличие от этого, животные, которым вводили 0,1 мг/кг антитела интраназально либо за 3 или 4 дня до вызова высоким титром вируса, были защищены от инфекции.
[000242] Введение антитела за 5, 6 и 7 дней до инфицирования высоким титром оценивали с введенным антителом в дозе 1 мг/кг IN или IP (Фигура 36). В этом исследовании только животные, которым вводили антитела в дыхательные пути (через интраназальное введение), полностью выживали после инфицирования вирусом. Мыши, которых обрабатывали 1 мг/кг вводимыми антител за 5, 6 или 7 дней до инфицирования вирусом, не были полностью защищены и погибали от инфекции. Тамифлю был совершенно неэффективным в защите. Мыши, обработанные 0,1 мг/кг антитела интраназально за 5 или 6 дней до инфицирования вирусом, выживали после инфицирования вирусом почти также, как контрольные животные, которые не были инфицированы.
[000243] Таким образом, интраназальное введение антител против гриппа является эффективным протоколом и способ для профилактики антителами против инфекции. Нейтрализующие грипп антитела вводят интраназально по меньшей мере за 7 дней до инфицирования вирусом были защитными против инфицирования вирусом. Защита с помощью интраназального введения, по меньшей мере, за 7 дней, было показана для большого титра вируса, даже выше, чем было бы разумно ожидать, чтобы представлять подверженность человека вирусу. Таким образом, уровень защиты, наблюдаемый в этих исследованиях, указывает, что интраназальное введение антитела будет эффективно для человека для защиты от инфицирования вирусом и блокирования или уменьшения передачи вируса. Интраназально вводимые антитела являются защитными в условиях и в тех случаях, когда IP введение неэффективно.
[000244] Настоящее изобретение может быть воплощено в других формах или осуществлено другими способами без отступления от сущности или существенных характеристик. Настоящее изобретение, таким образом, следует рассматривать как во всех аспектах, иллюстрирующих, но не ограничивающих, характер, объем изобретения, указанных в прилагаемой формуле изобретения, и все изменения, которые подпадают под значение и диапазон эквивалентности, являются предназначенными для включения в них.
[000245] Различные ссылки приведены в данном описании, каждая из которых включена в данное описание посредством ссылки во всей своей полноте.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА, ПОДХОДЯЩИЕ ДЛЯ ПАССИВНОЙ ИММУНИЗАЦИИ ПРОТИВ ГРИППА, И ИХ КОМПОЗИЦИИ, КОМБИНАЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ | 2015 |
|
RU2720282C1 |
| АНТИТЕЛА, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПАССИВНОЙ ВАКЦИНАЦИИ ПРОТИВ ГРИППА | 2012 |
|
RU2668802C2 |
| ЛЕЧЕНИЕ ВИРУСА ГРИППА А H7N9 | 2015 |
|
RU2682049C2 |
| АНТИТЕЛА, ПОДХОДЯЩИЕ ДЛЯ ПАССИВНОЙ ИММУНИЗАЦИИ ПРОТИВ ГРИППА | 2011 |
|
RU2635999C2 |
| НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА К ВИРУСУ ГРИППА А И ПУТИ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2683498C2 |
| НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА К ВИРУСУ ГРИППА А И ПУТИ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2803850C2 |
| ВАКЦИНЫ И СПОСОБЫ ЛЕЧЕНИЯ СОБАЧЬЕГО ГРИППА | 2006 |
|
RU2396976C2 |
| НЕЙТРАЛИЗУЮЩИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, НАПРАВЛЕННЫЕ ПРОТИВ ВИРУСА ГРИППА, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2721706C2 |
| ФУНКЦИОНАЛЬНЫЕ ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ ГРИППА (VLPs) | 2006 |
|
RU2483751C2 |
| НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА ПРОТИВ ВИРУСА ГРИППА А И ИХ ИСПОЛЬЗОВАНИЕ | 2009 |
|
RU2553325C2 |
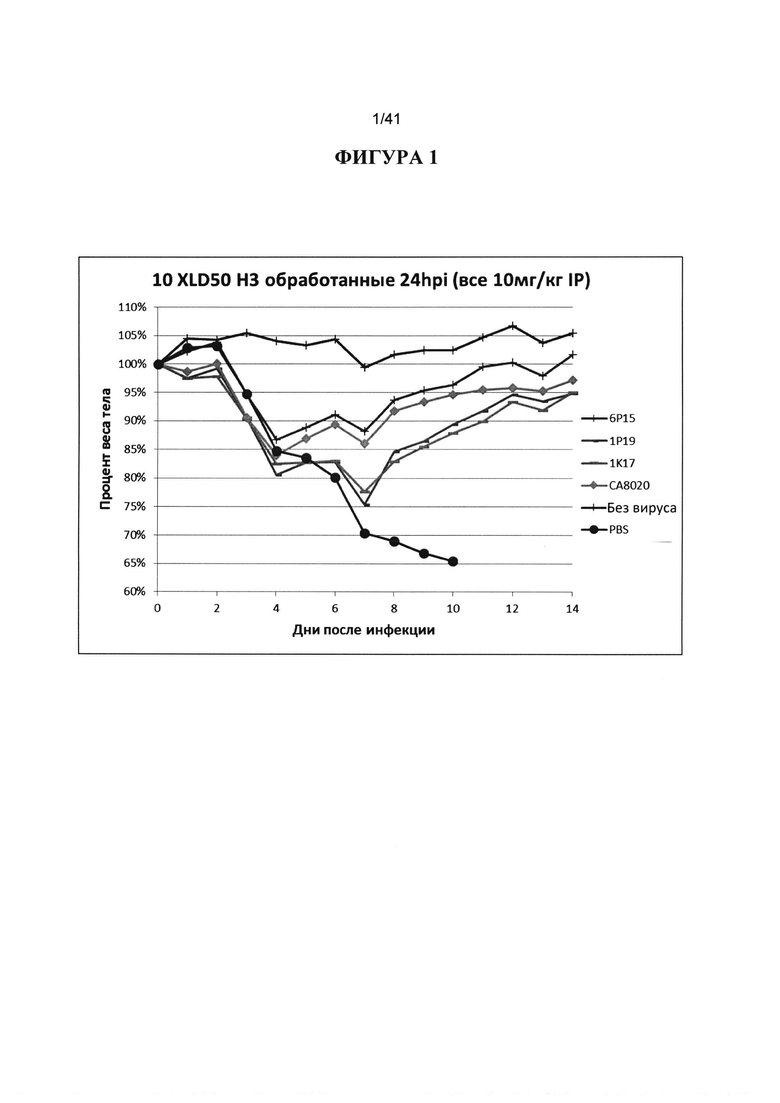
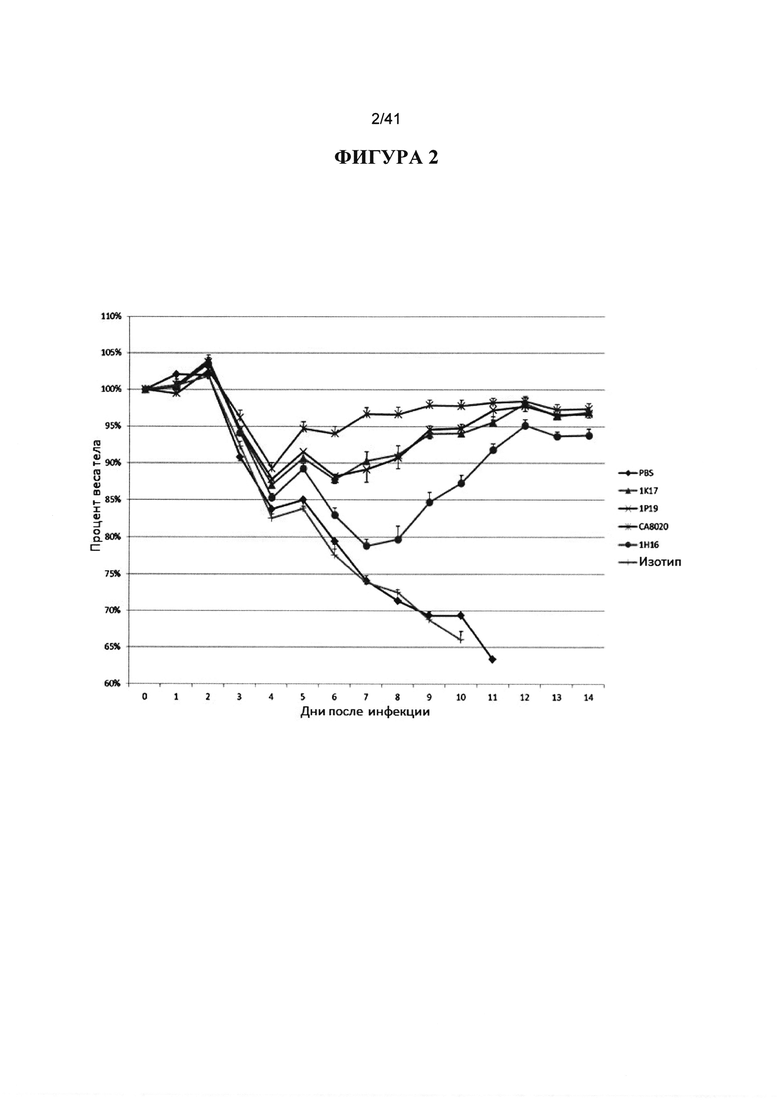

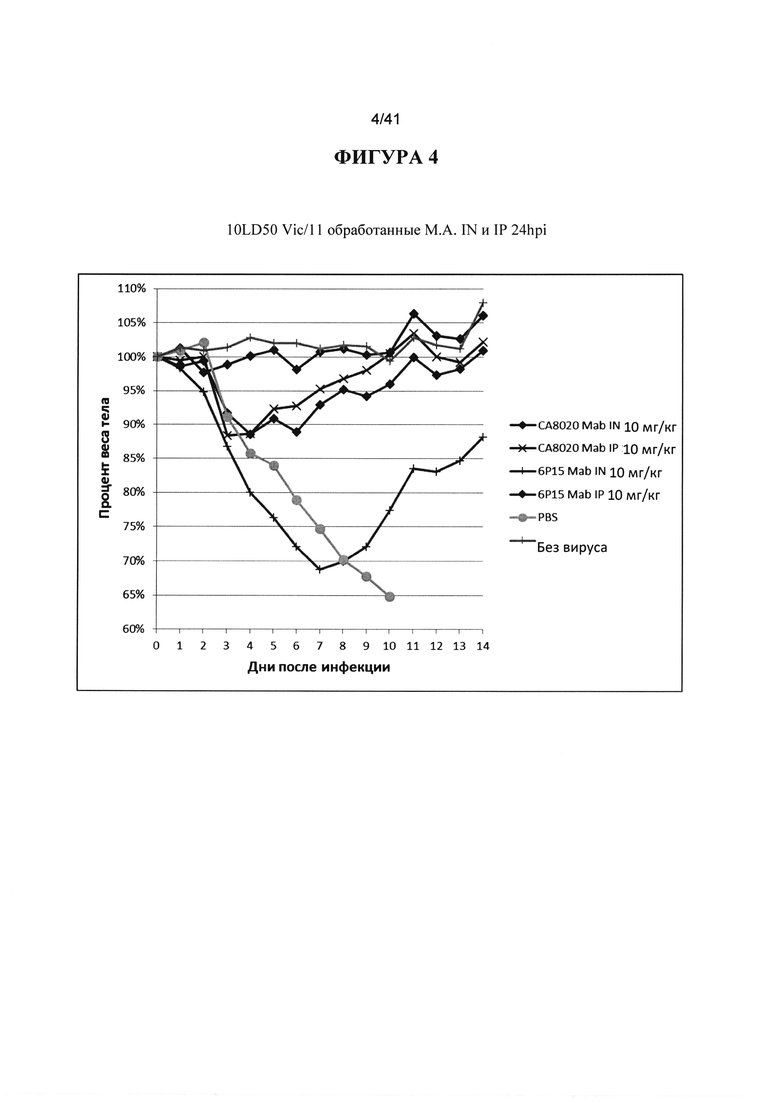
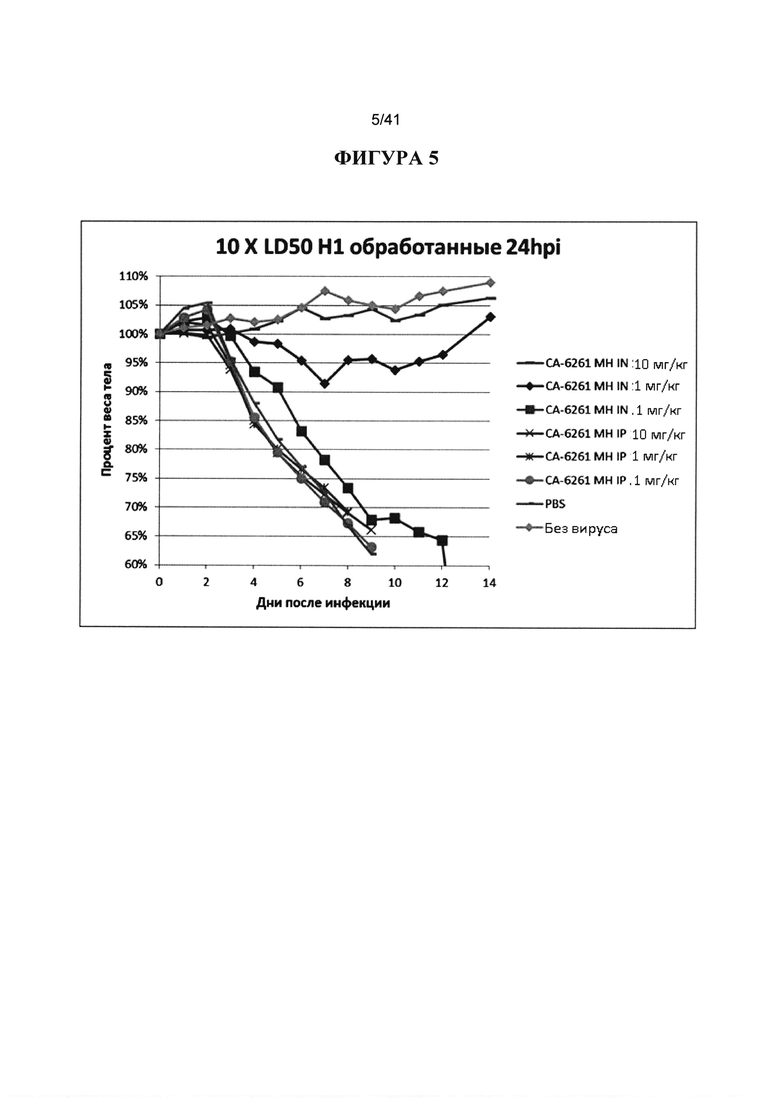
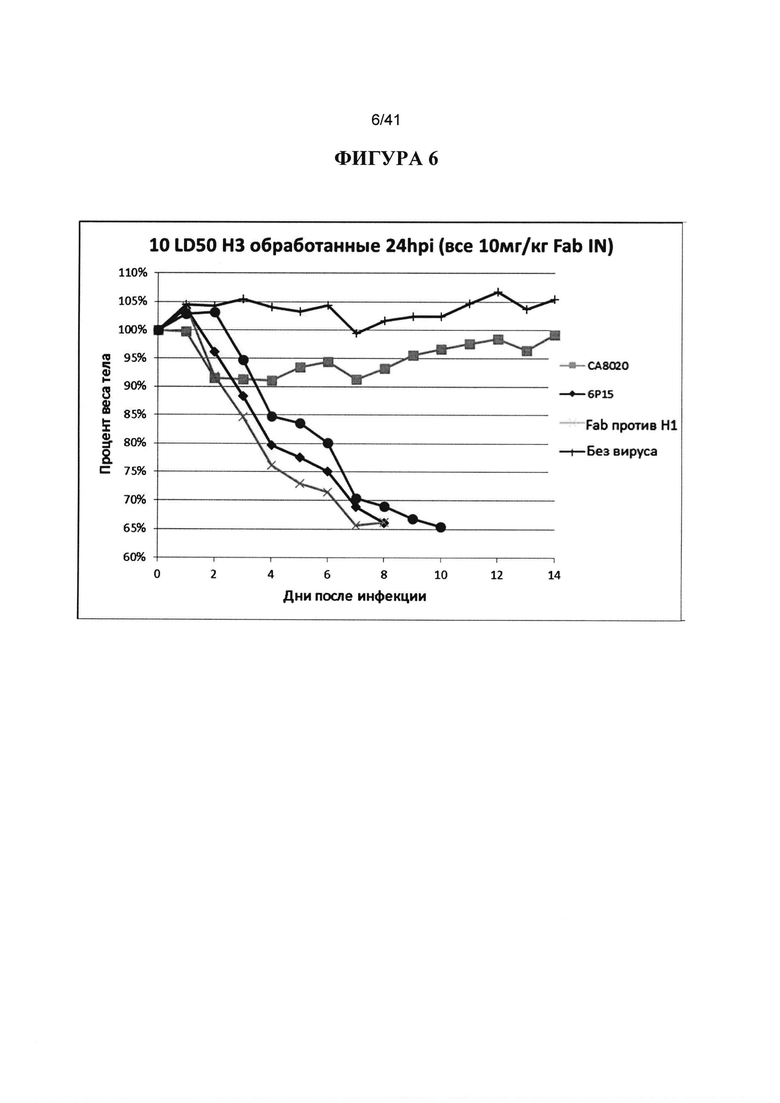
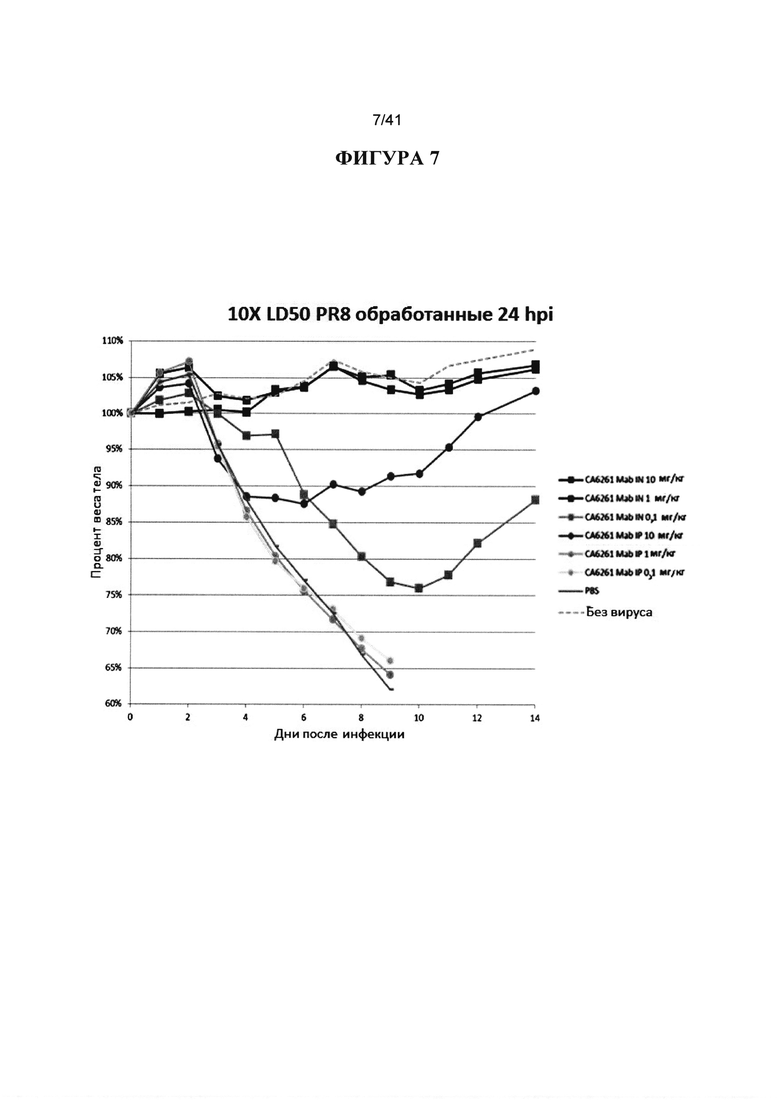
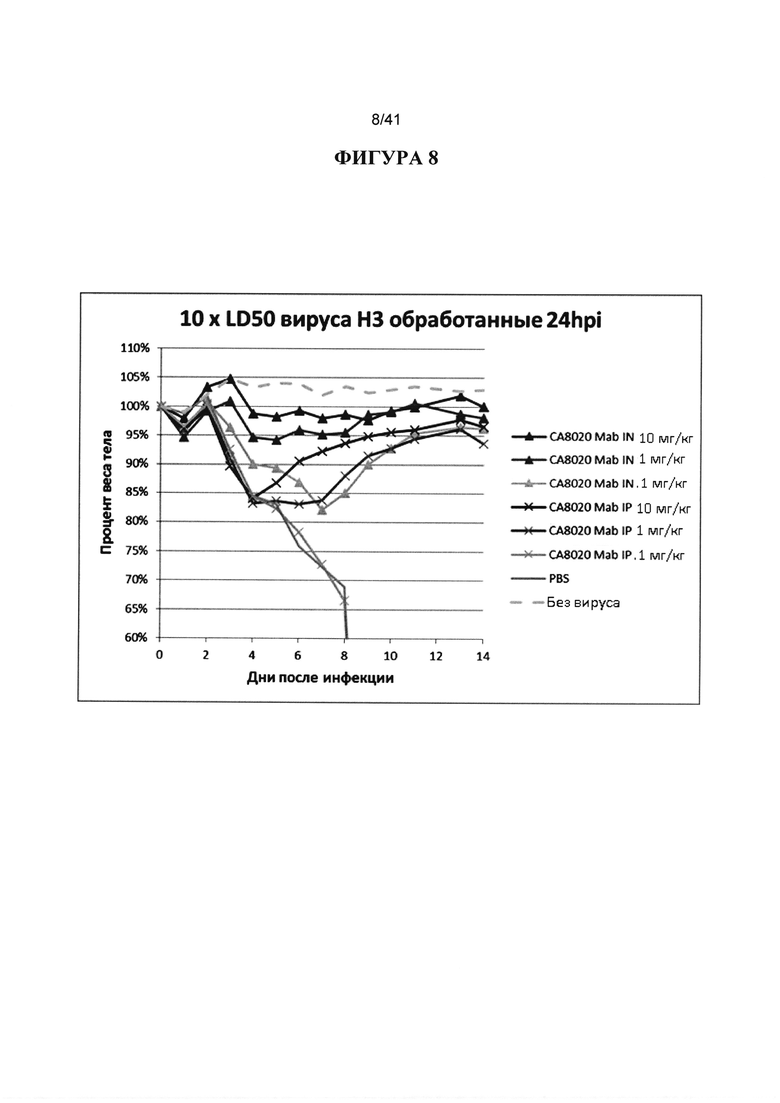
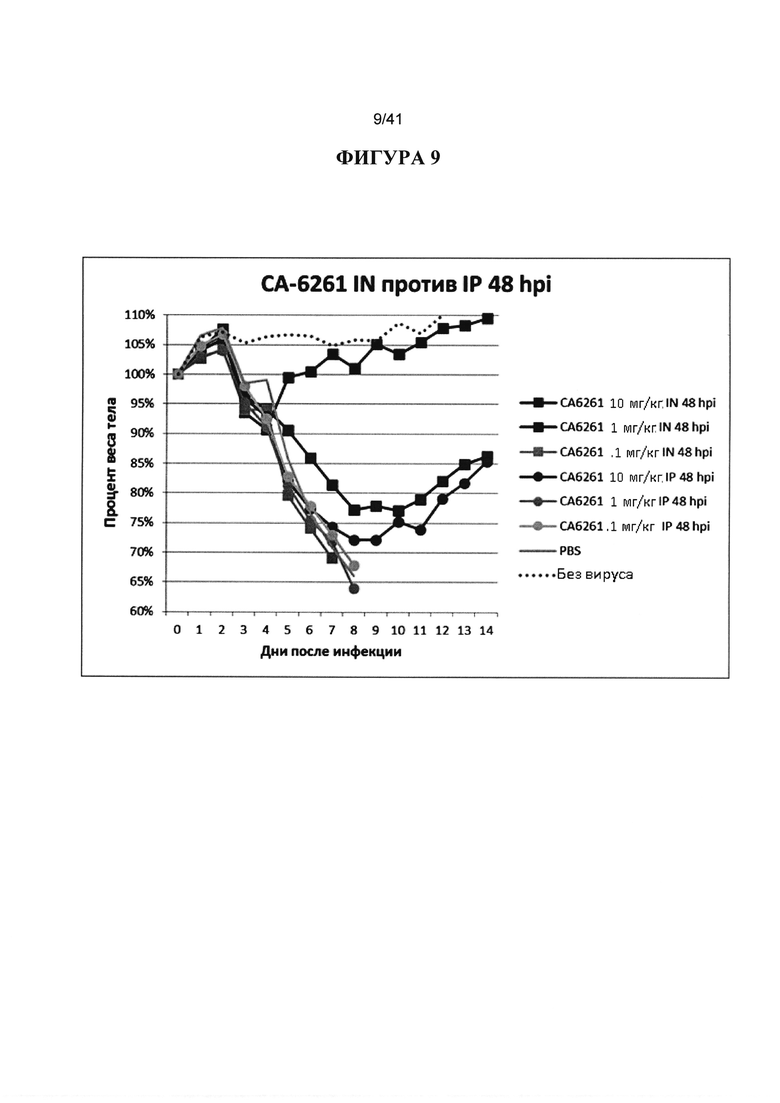
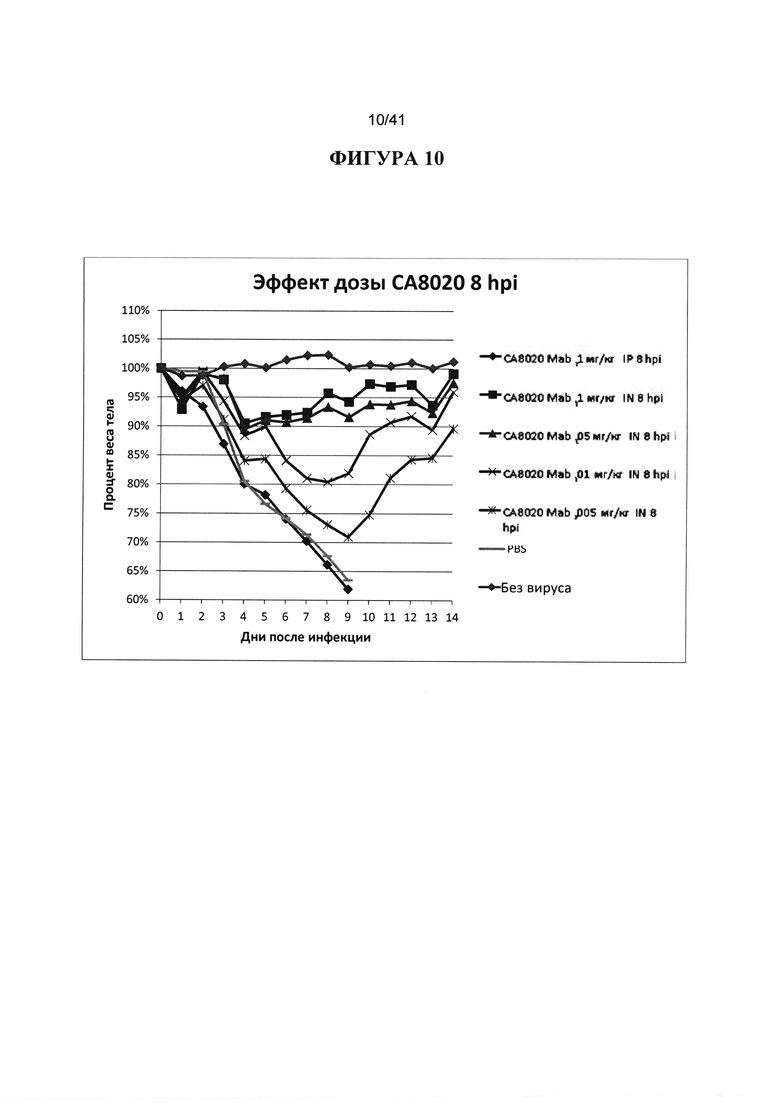

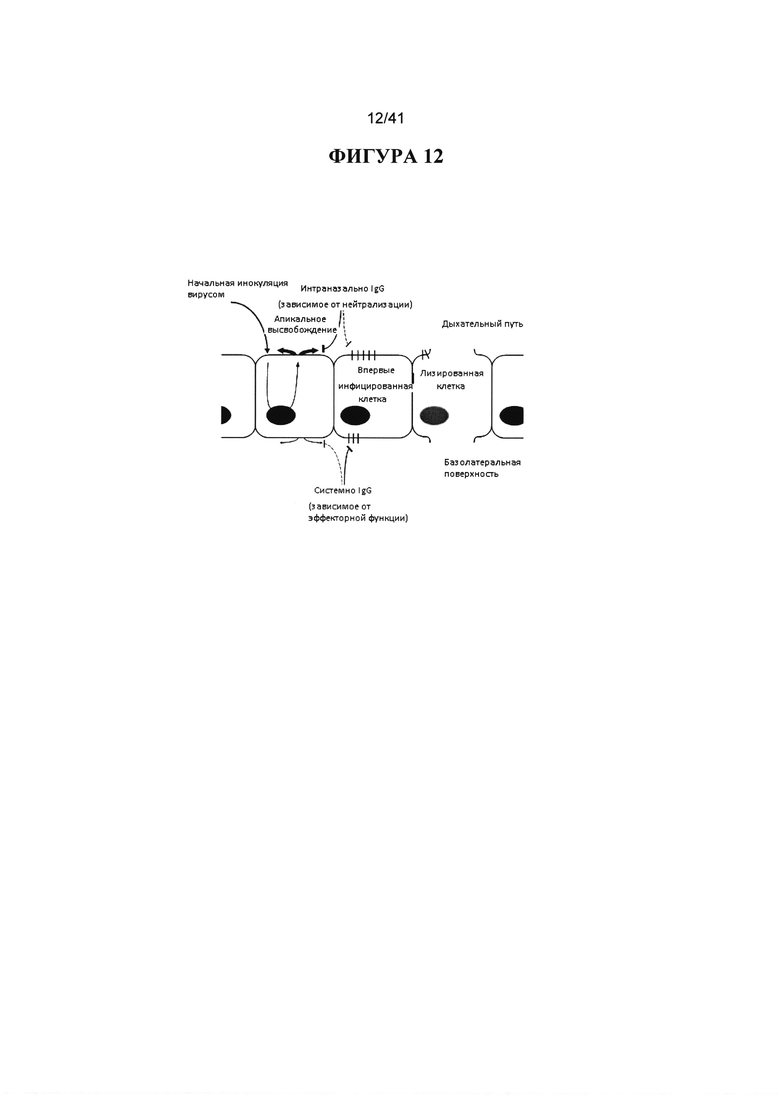
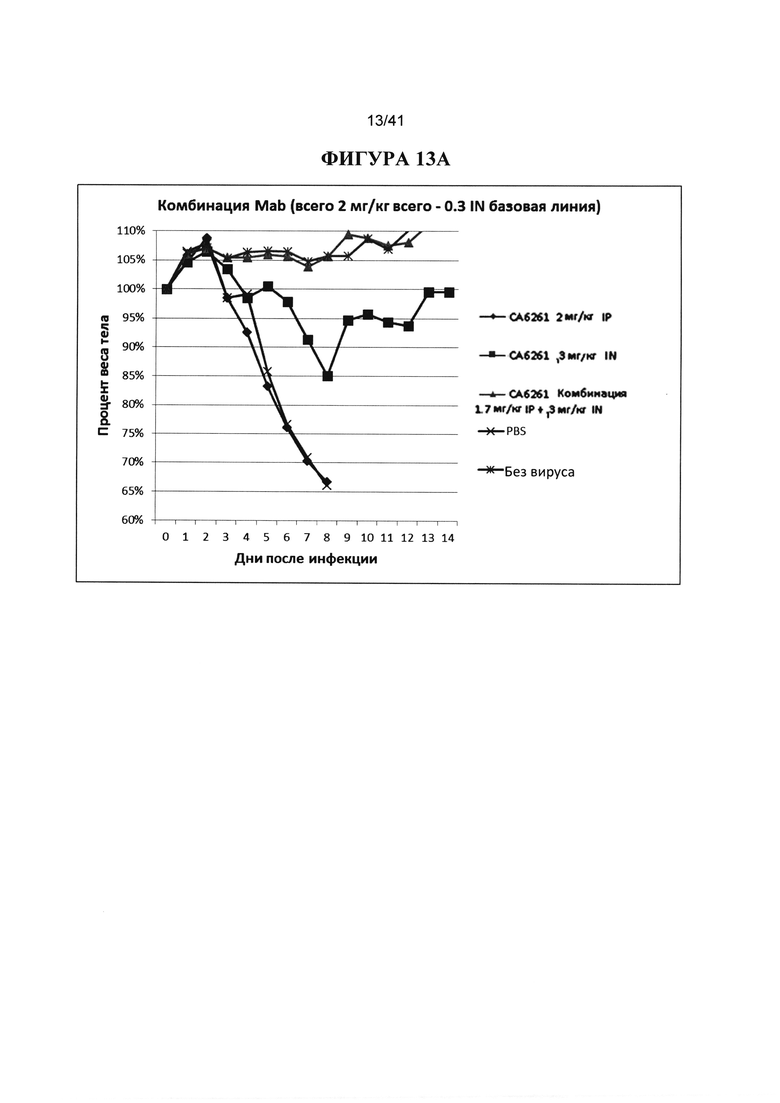
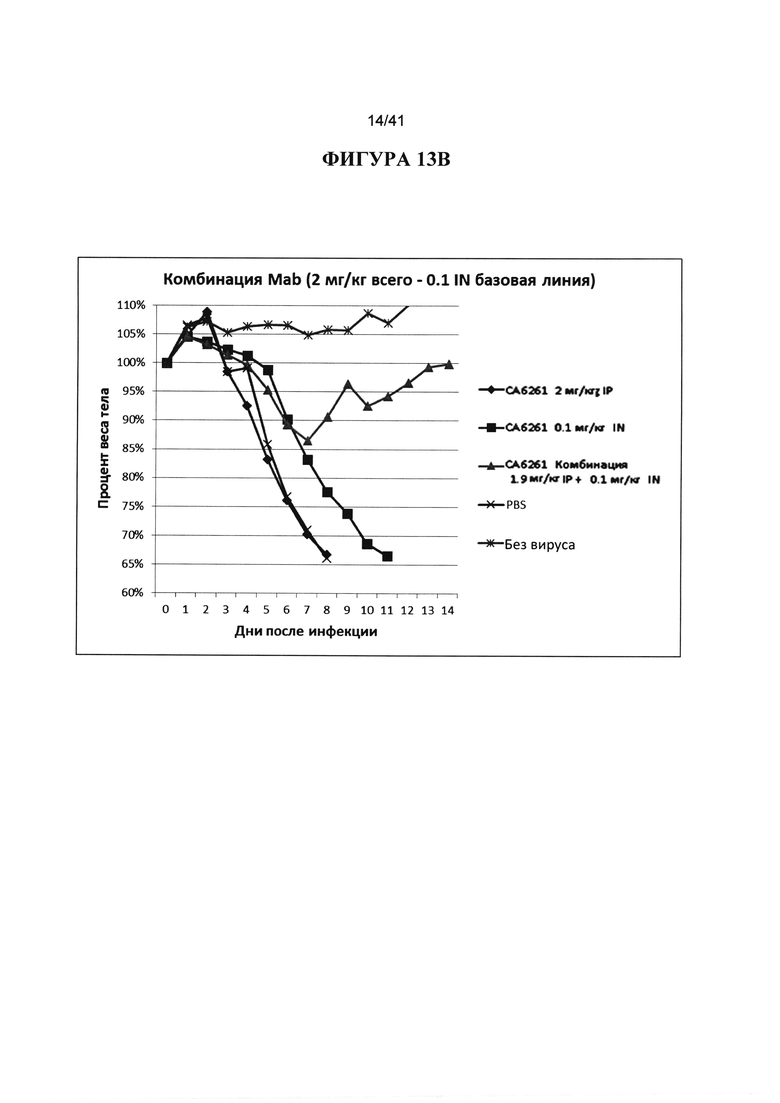
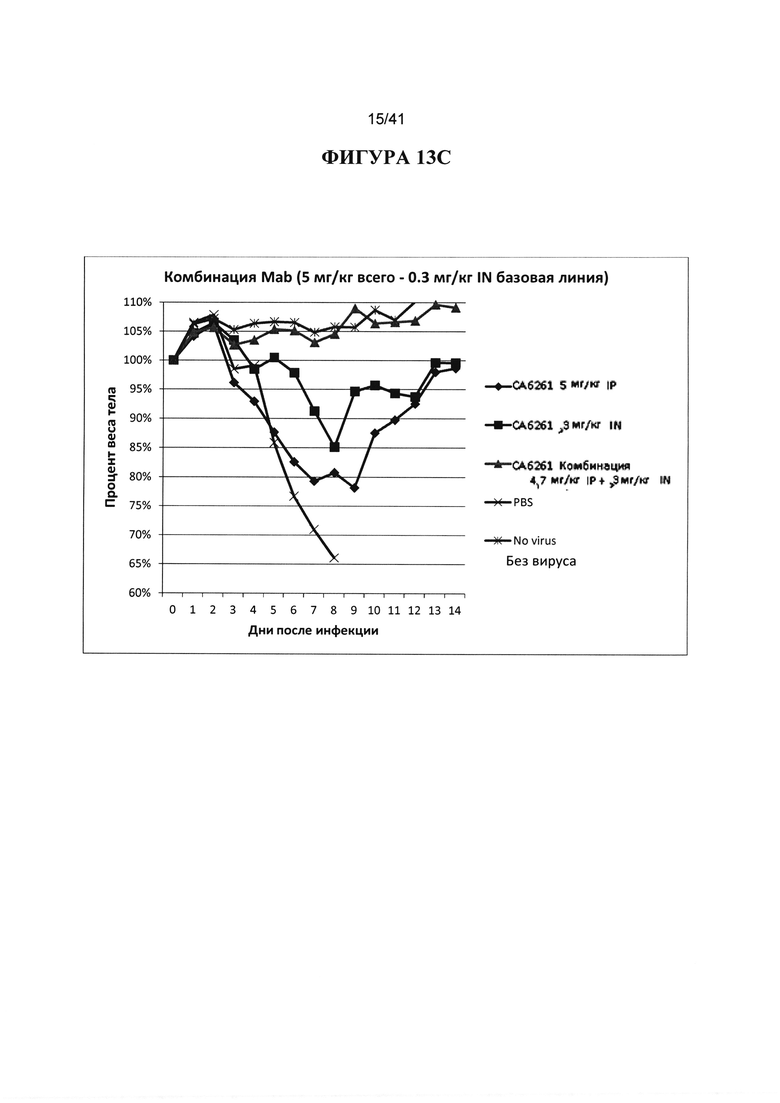
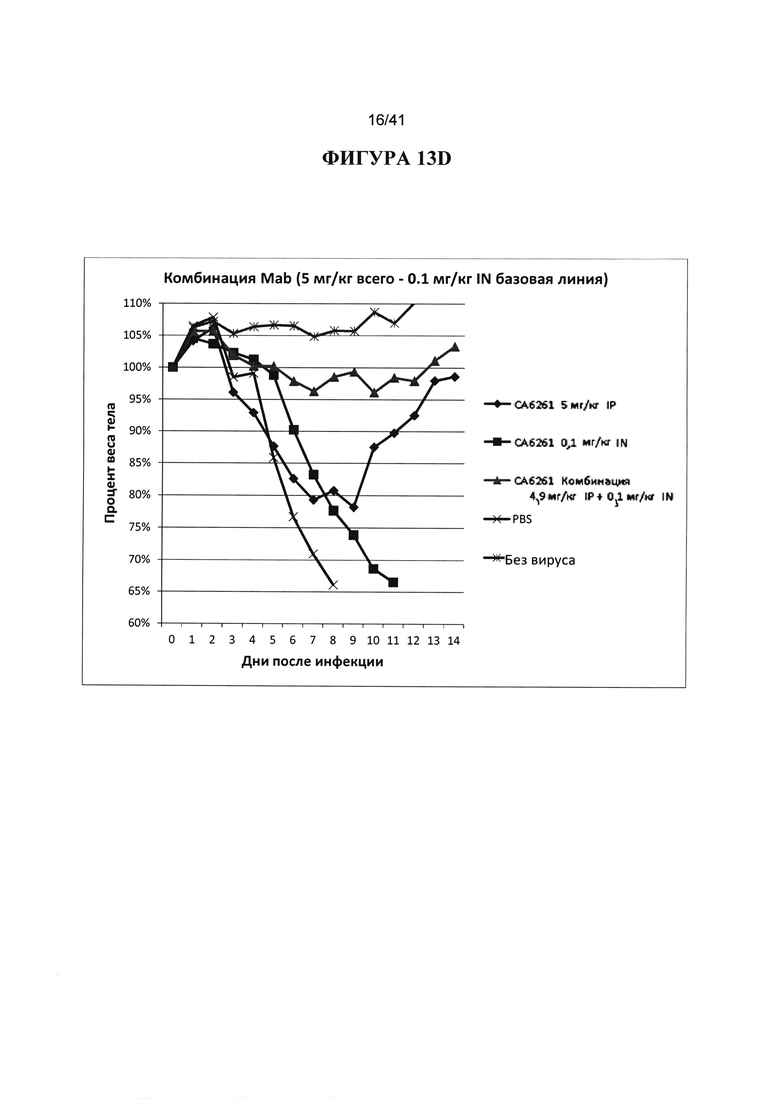
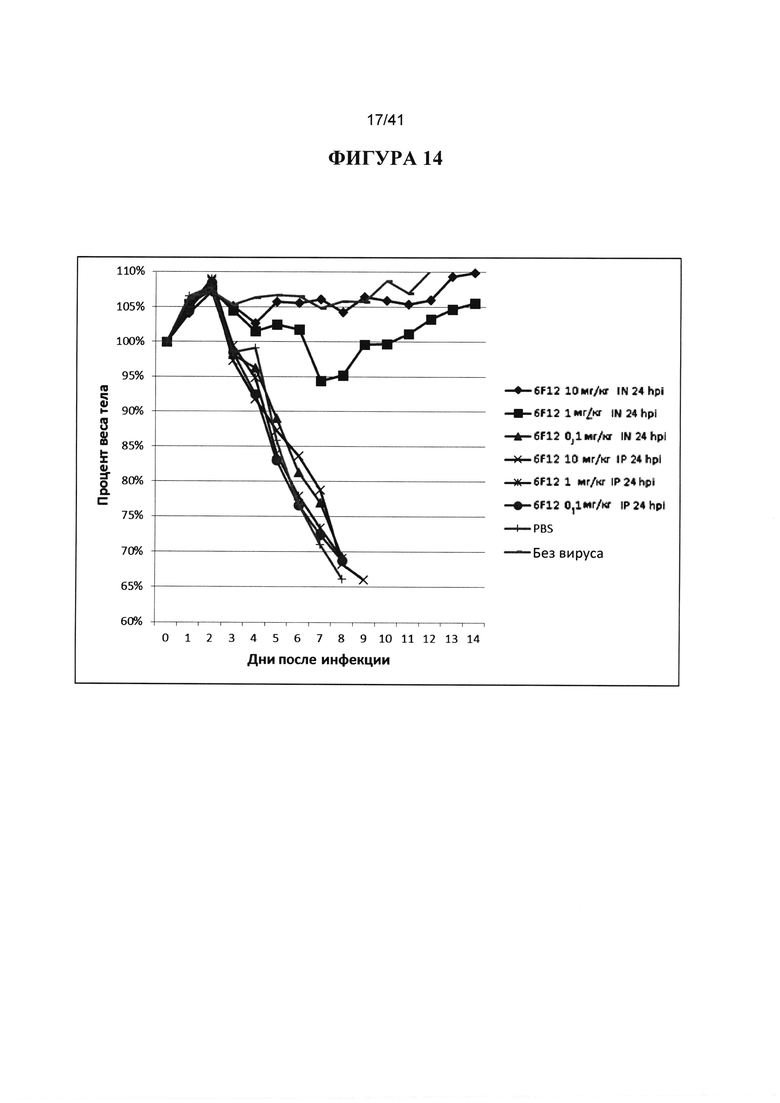


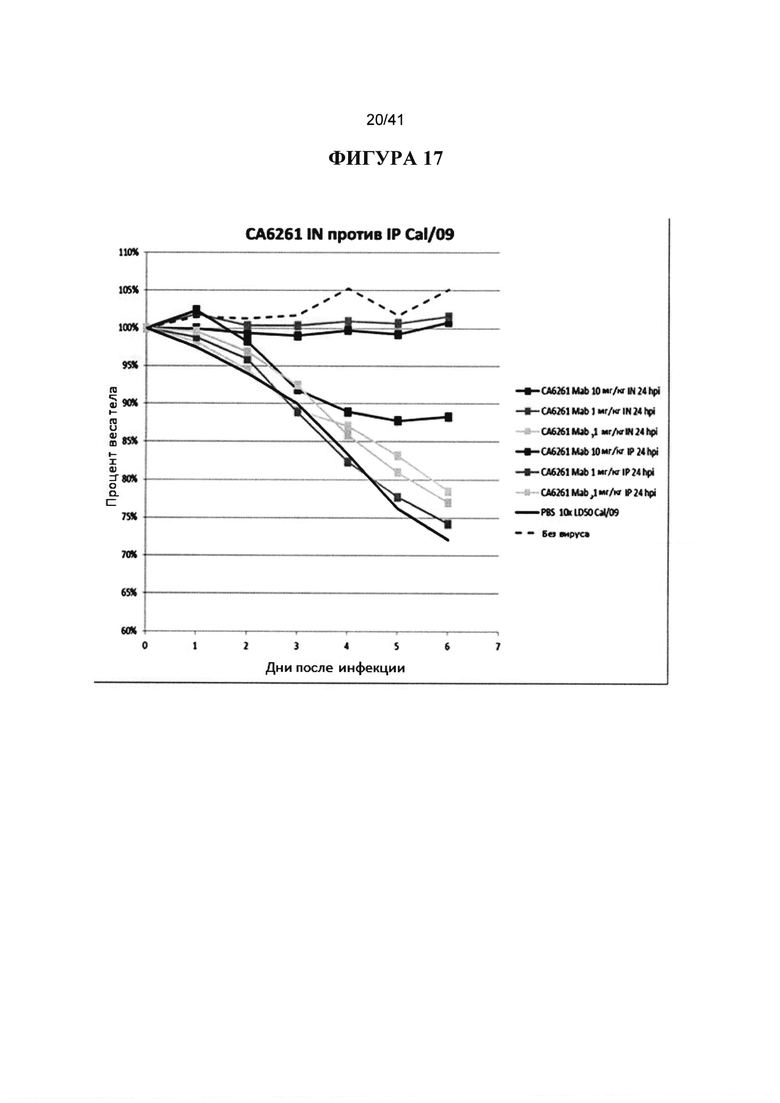
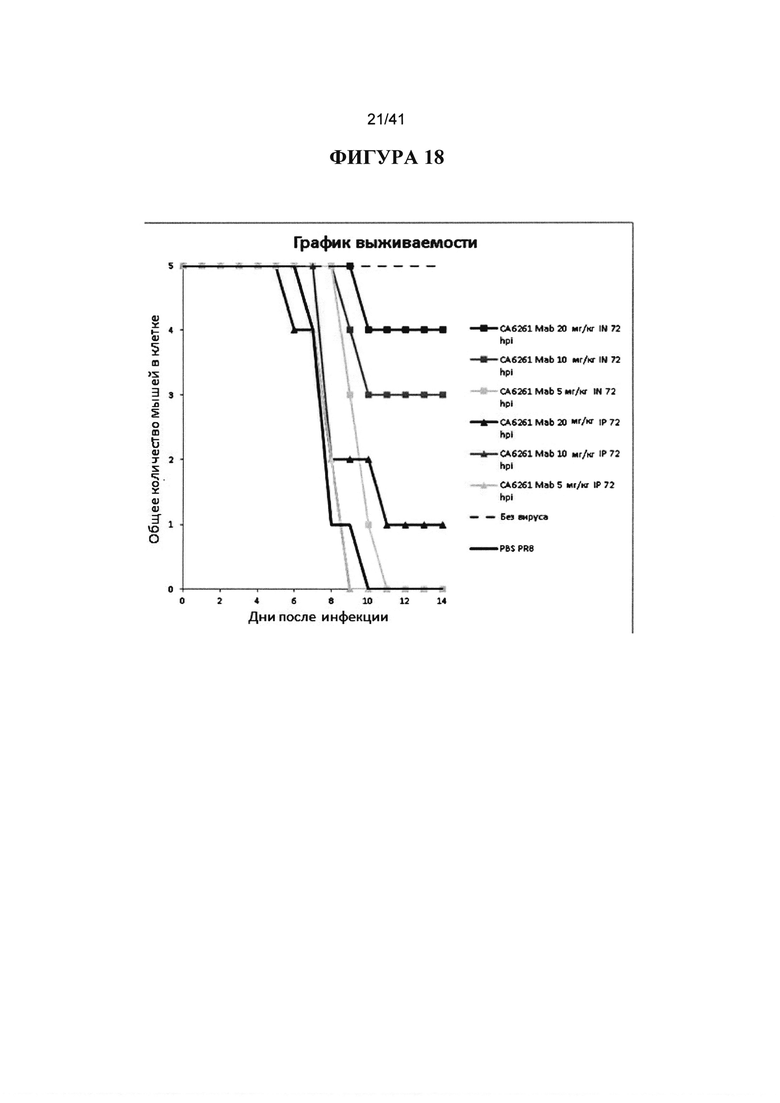
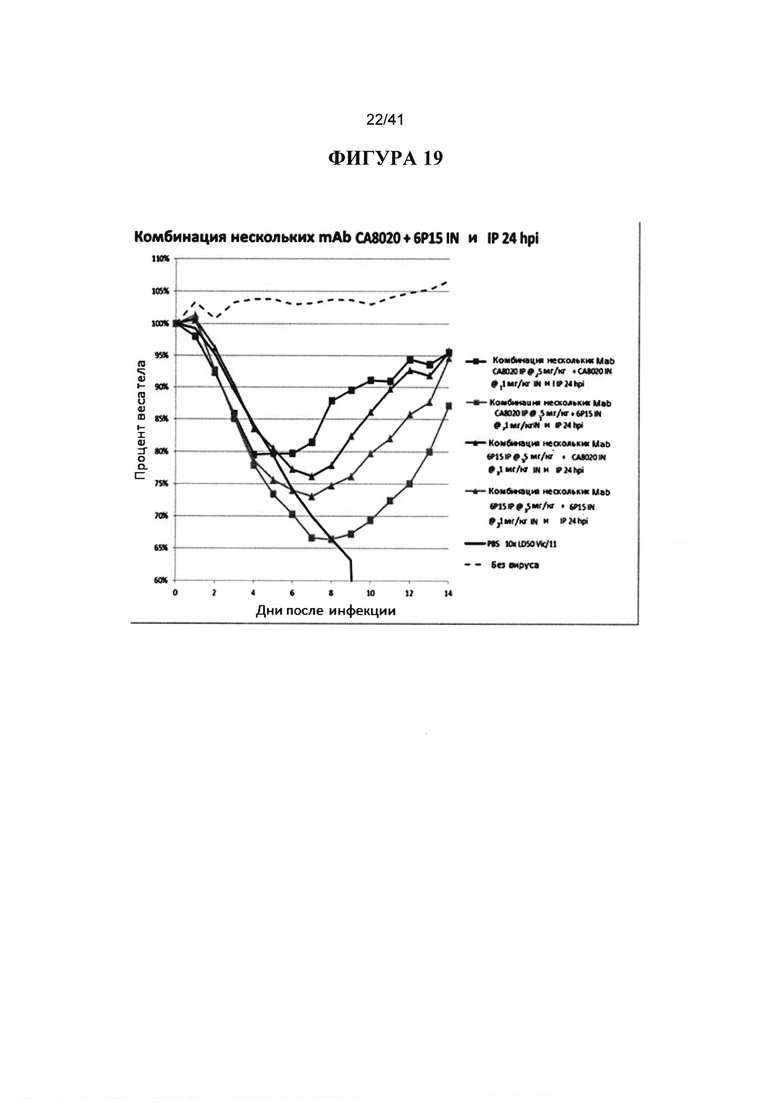
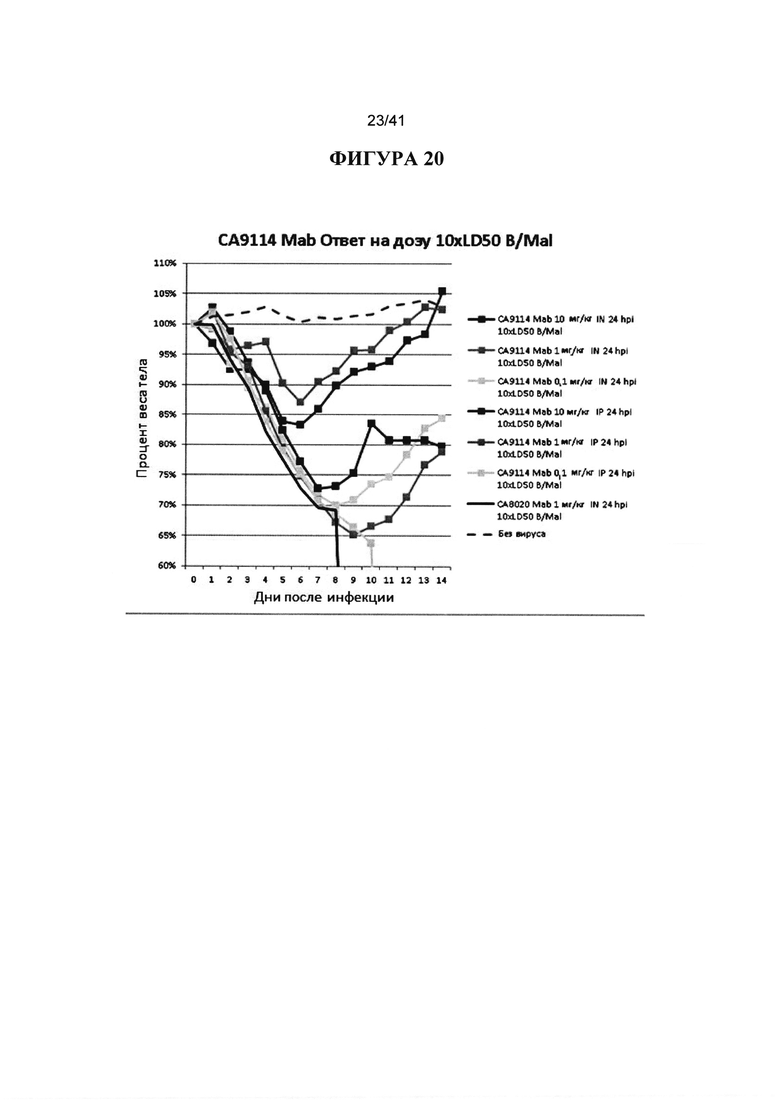
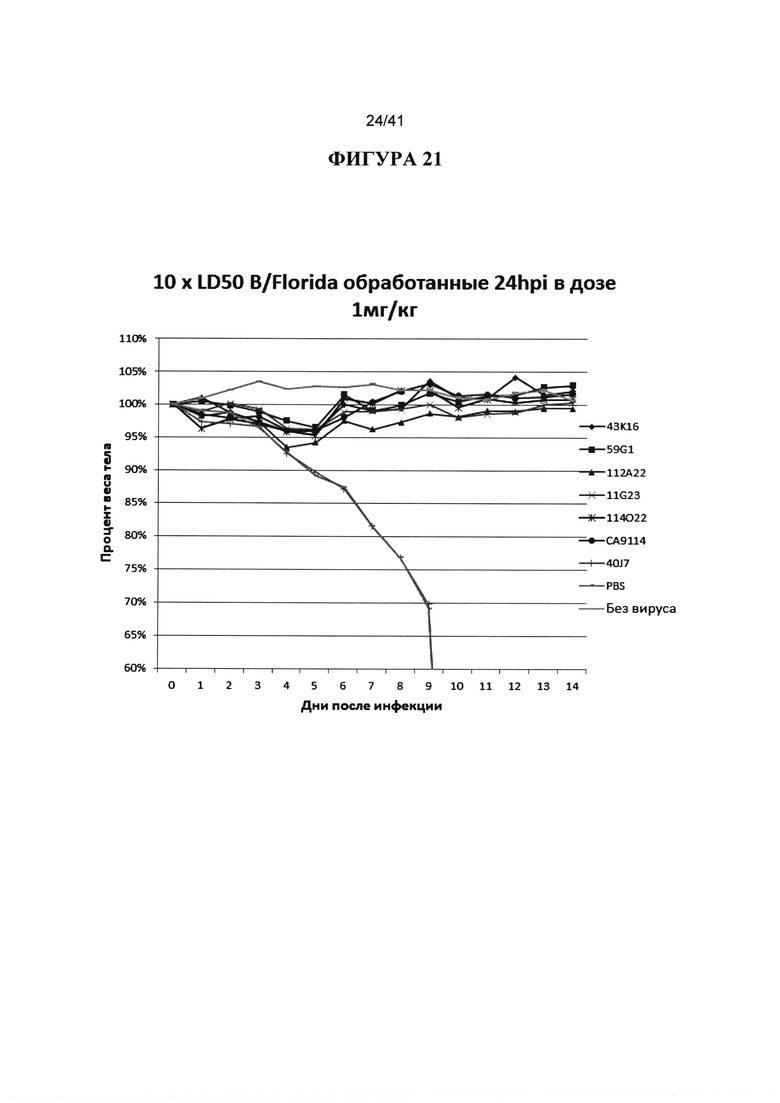
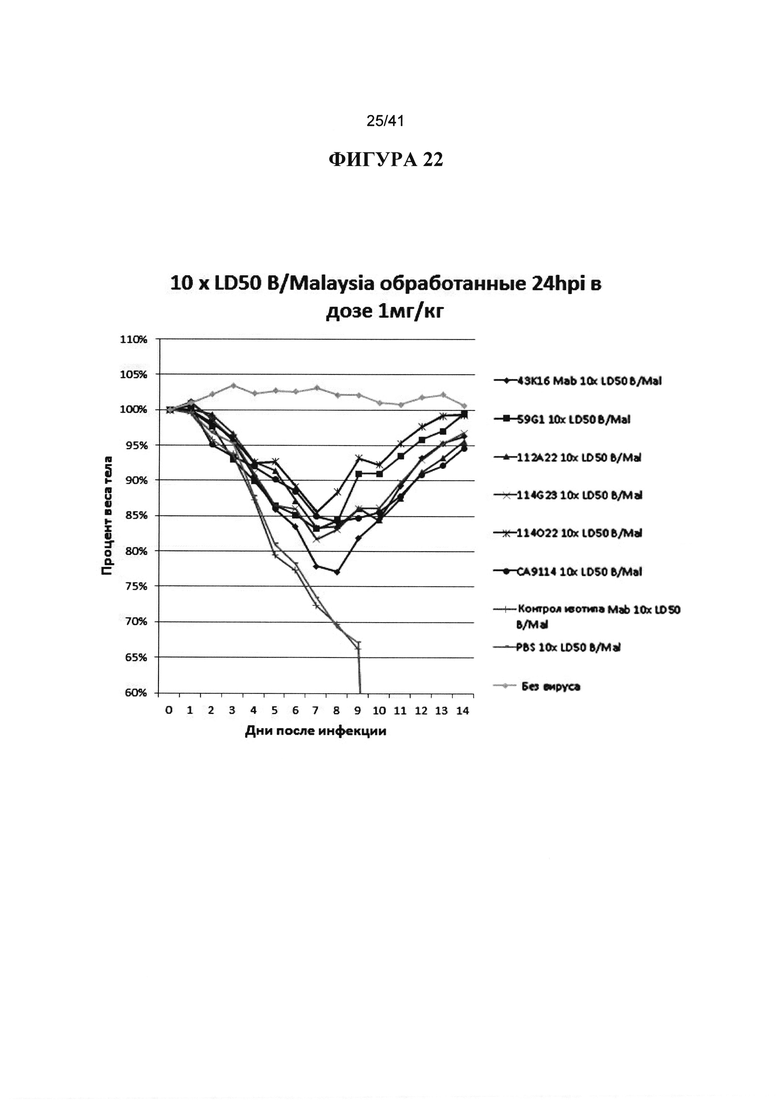
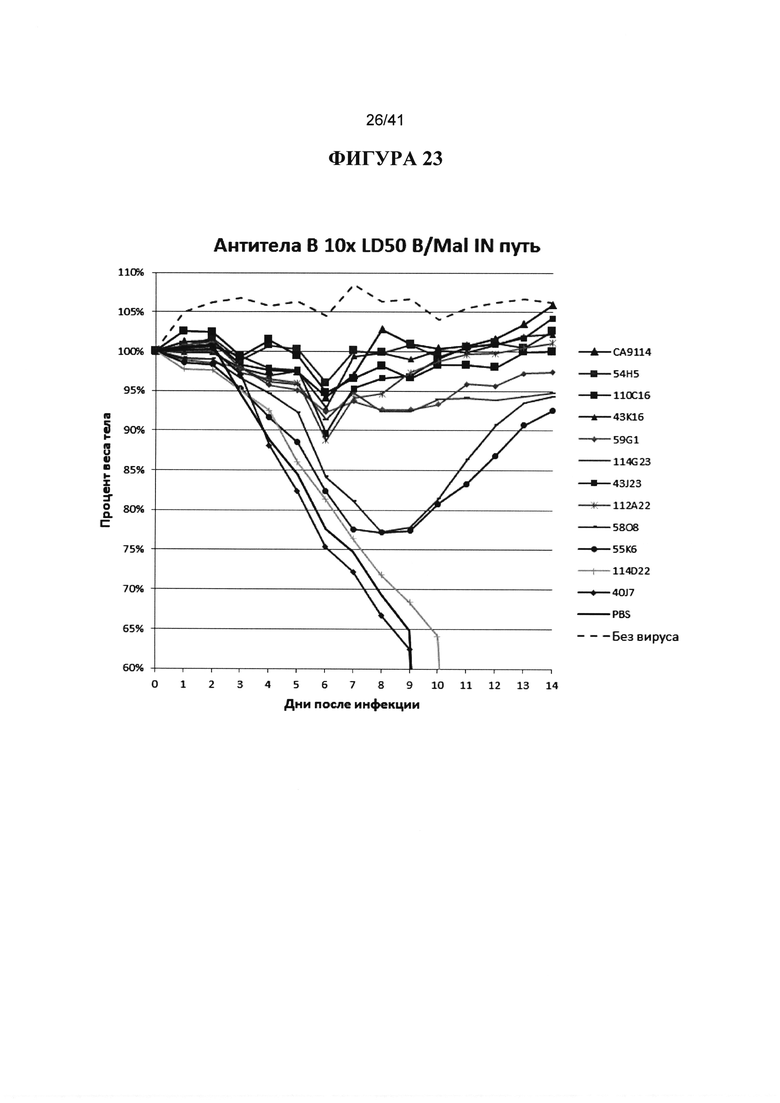

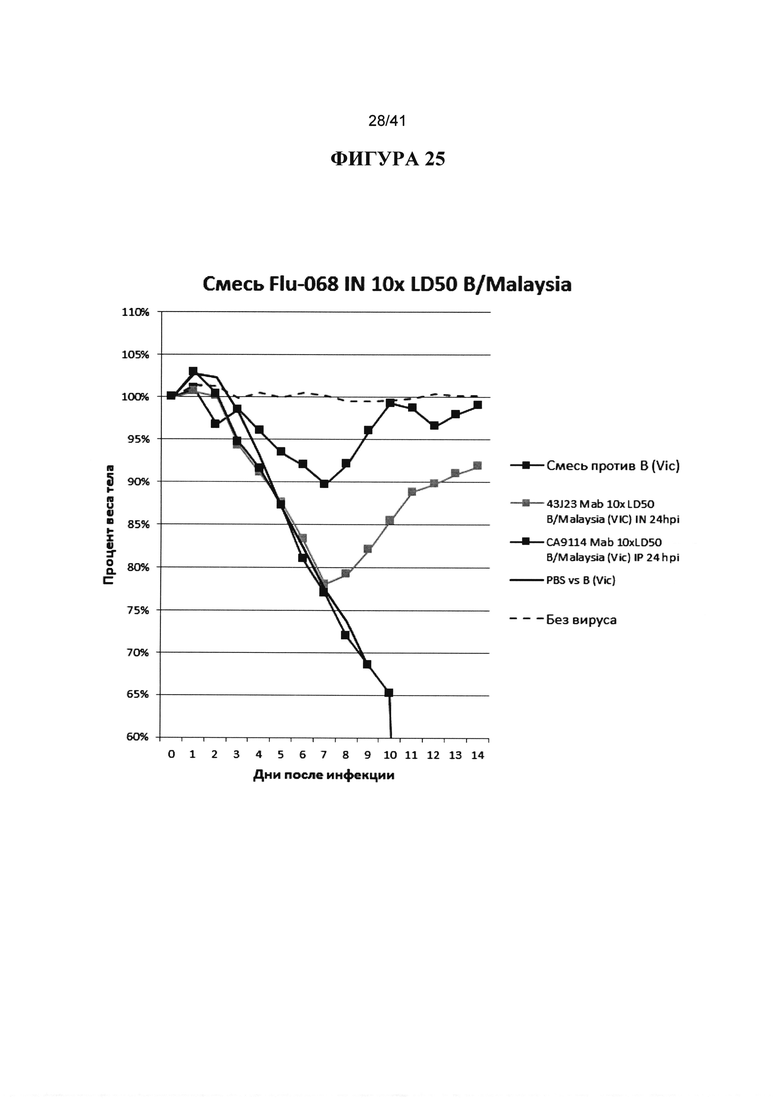
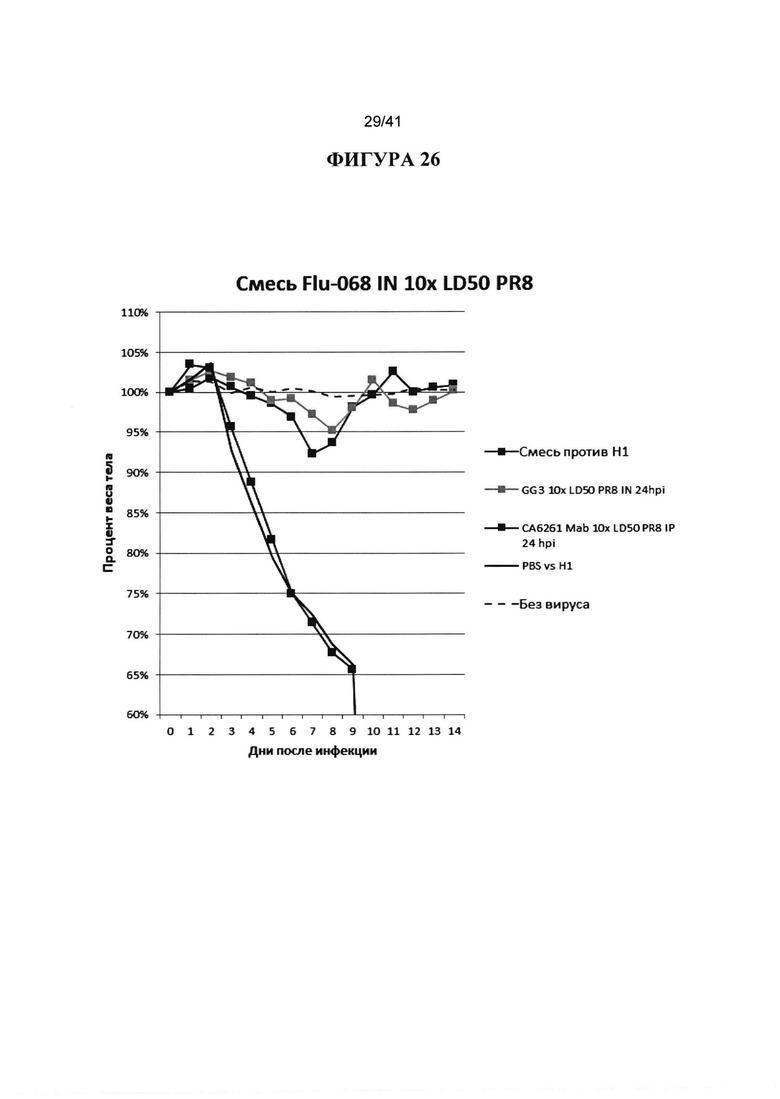
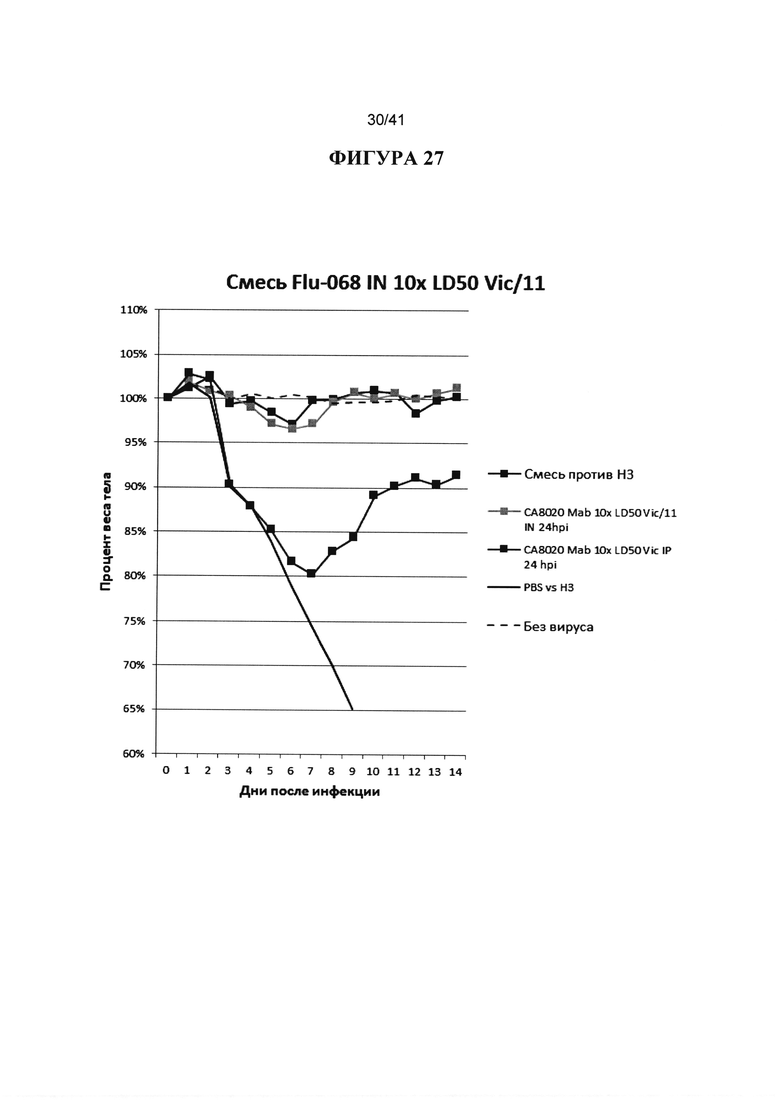
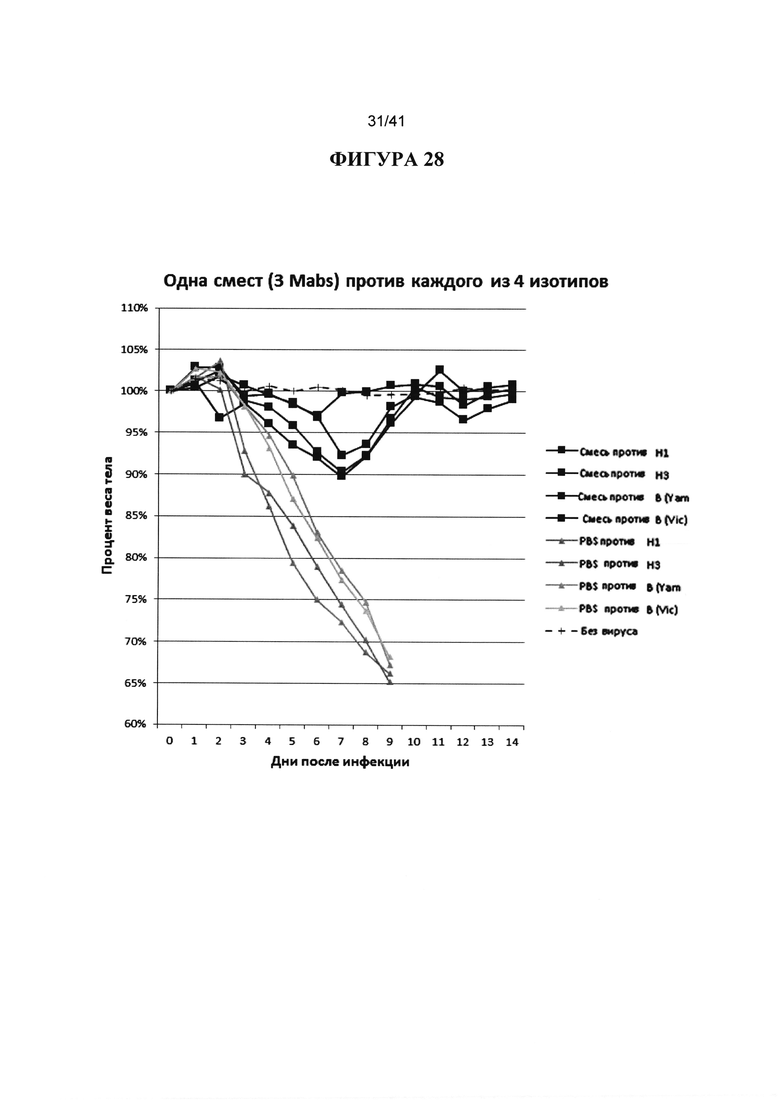
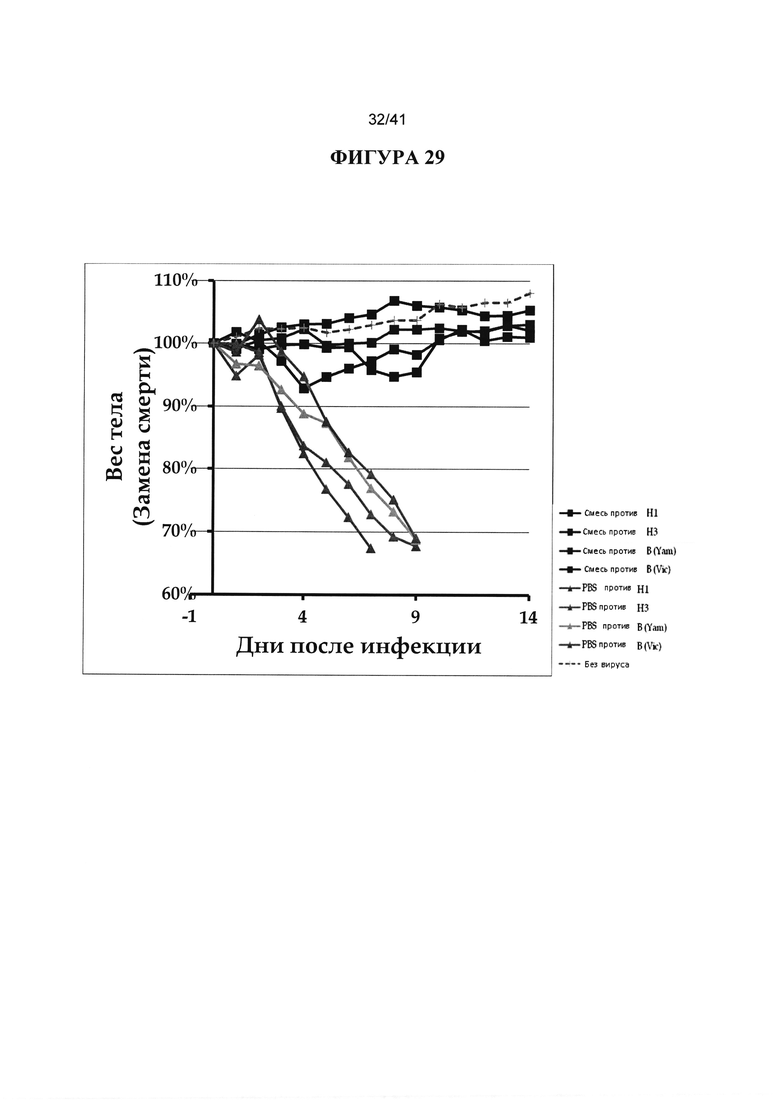
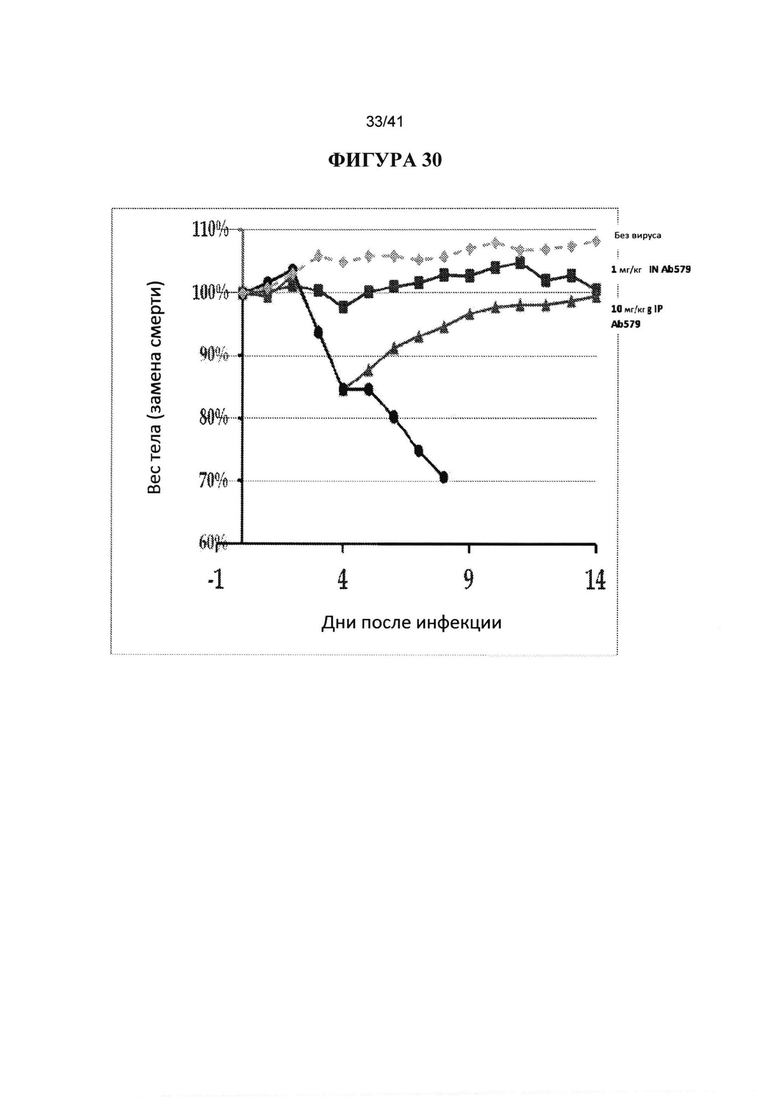
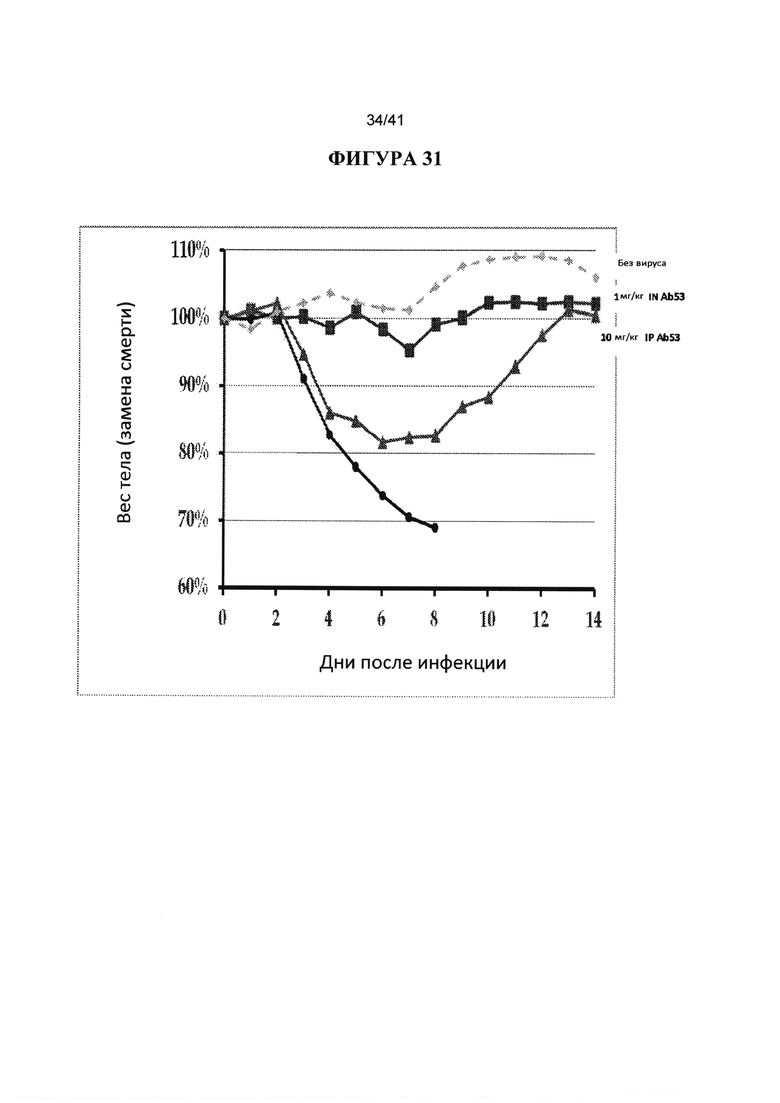
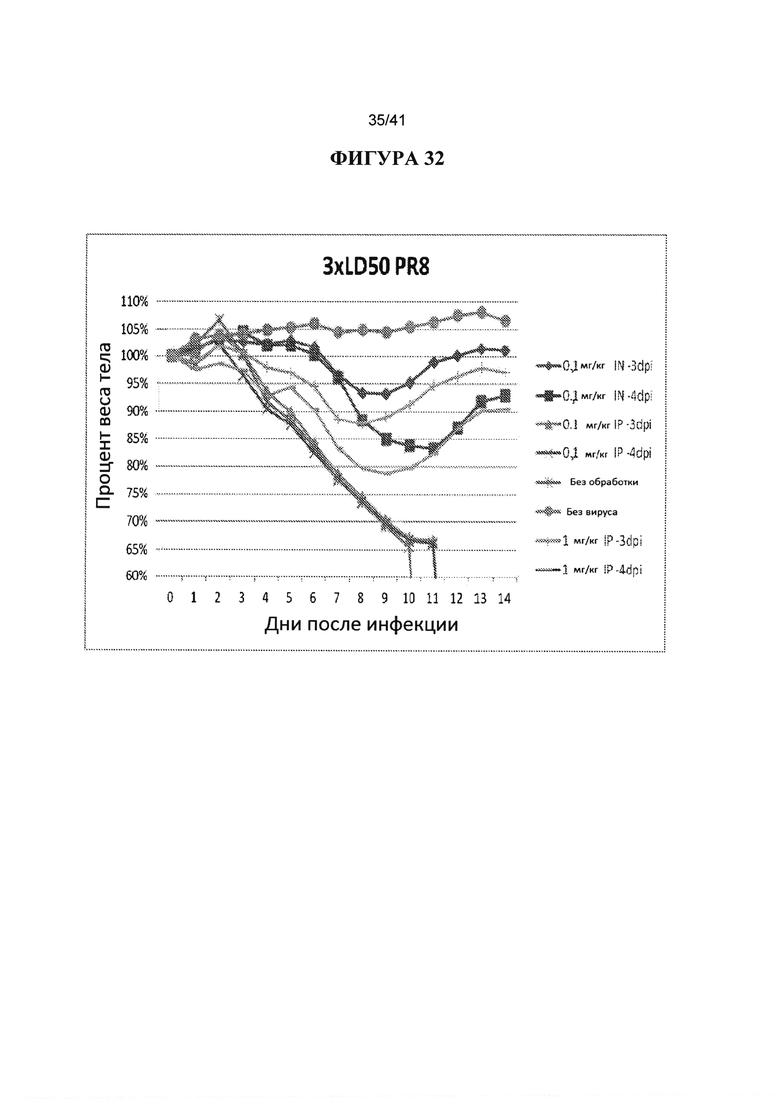
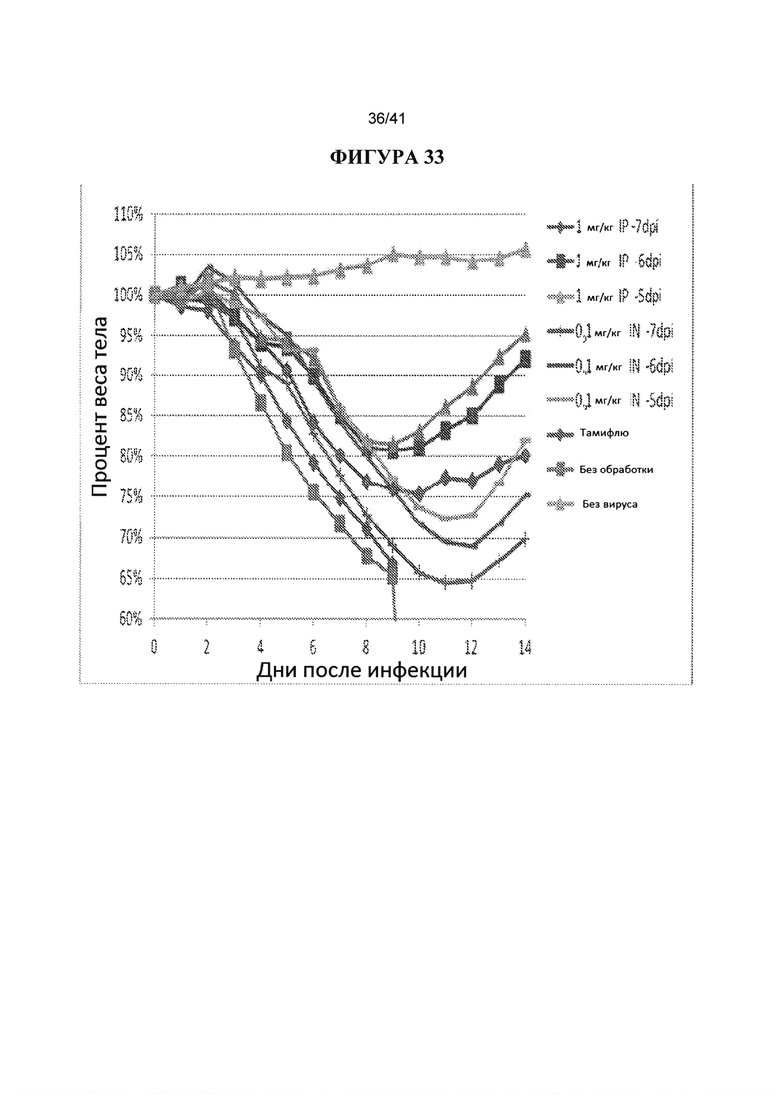
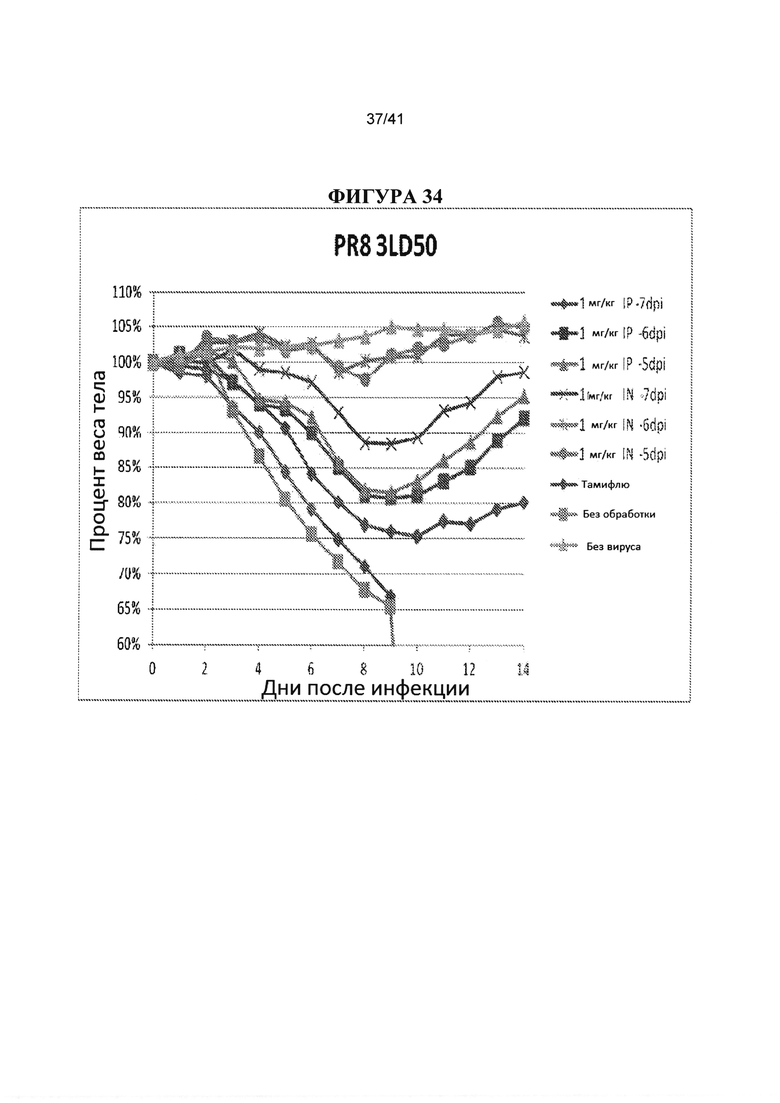
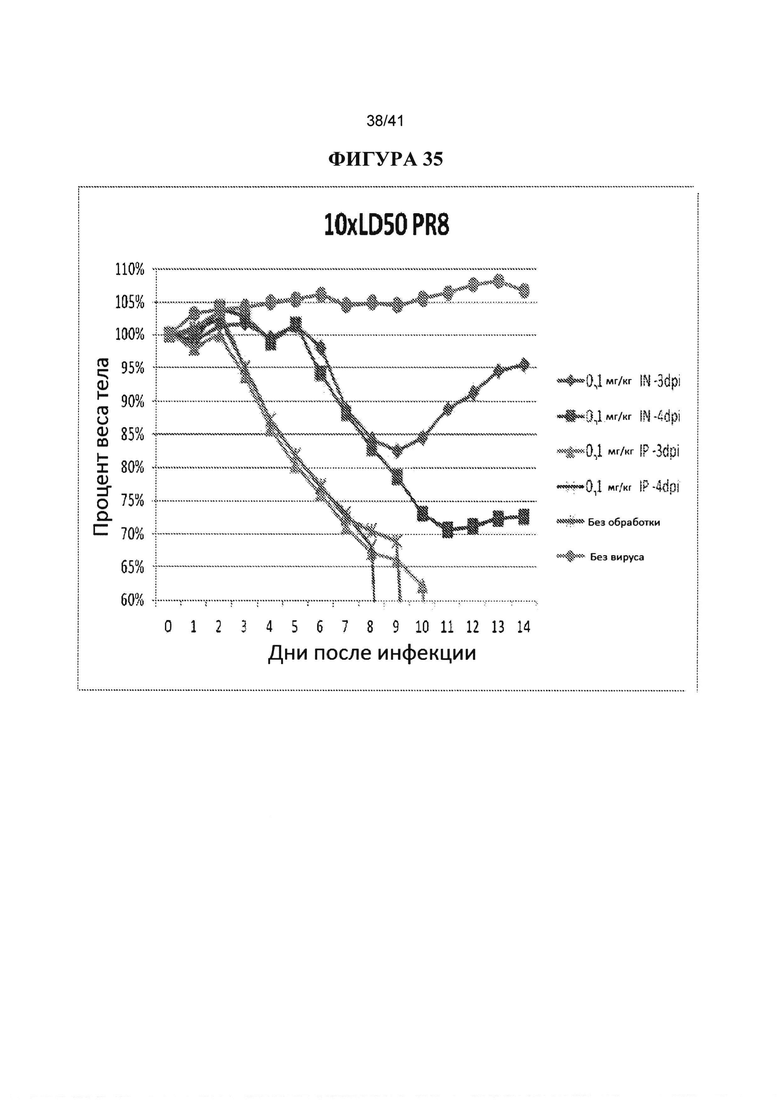
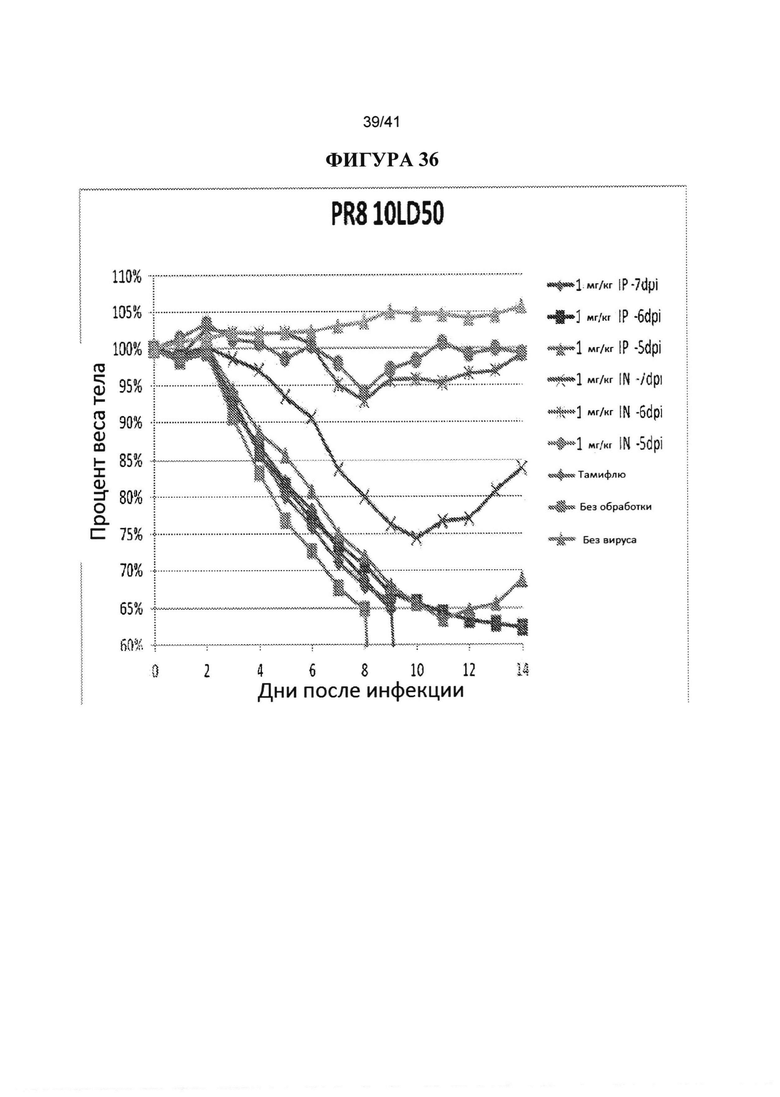
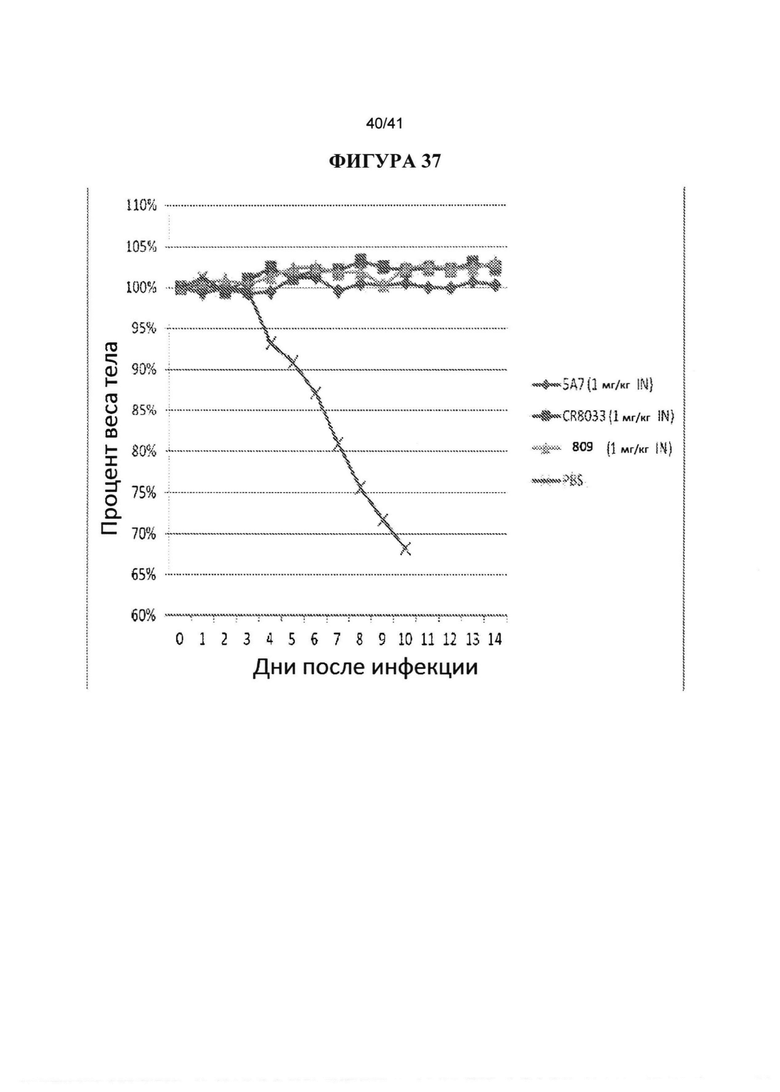
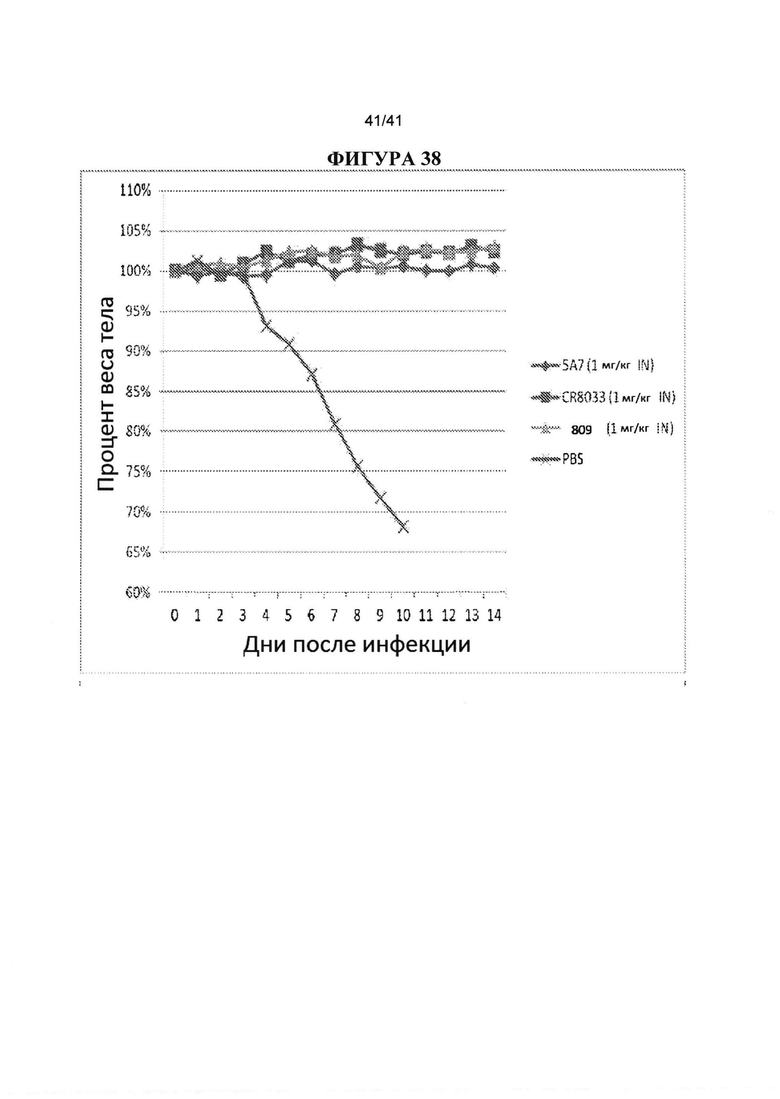
Изобретение относится к биотехнологии. Описана композиция для доставки в дыхательные пути, полученная и эффективная для лечения и/или профилактики инфекции вируса гриппа у млекопитающего, содержащая два или более нейтрализующих вирус гриппа моноклональных антител в виде единичной однократной дозы и в эффективном количестве от 0,005 мг/кг до 1 мг/кг и подходящий фармацевтически приемлемый носитель, разбавитель или наполнитель, где по меньшей мере первое антитело направлено против вируса гриппа А одного подтипа, и по меньшей мере второе антитело направлено против вируса гриппа A другого подтипа, чем указанное первое антитело, или против вируса гриппа B, или имеется по меньшей мере два вторых антитела, одно из которых направлено против вируса гриппа A указанного другого подтипа и другое антитело направлено против вируса гриппа B. Описан способ лечения или профилактики вируса гриппа у млекопитающего посредством указанной композиции. Представлена профилактическая и терапевтическая комбинация, включающая: первую композицию, полученную для интраназального или ингаляционного введения, содержащую два или более нейтрализующих вирус гриппа моноклональных антител в виде единичной однократной дозы от 0,005 мг/кг до 1 мг/кг против вирусов гриппа, имеющих различную специфичность, и вторую композицию, полученную для внутрибрюшинного или внутривенного введения, содержащую одно или более антител против гриппа в виде единичной однократной дозы от 1 мг/кг до 10 мг/кг, где одно или более антител во второй композиции являются такими же, как одно или более антител в первой композиции, или другими антителами. Представлен способ уменьшения передачи вируса гриппа, включающий введение указанной выше композиции интраназально или ингаляционно субъекту, подвергаемому, в риске воздействия вируса гриппа или проявляющему клинические признаки инфекции вирусом гриппа. Изобретение расширяет арсенал средств лечения и профилактики гриппа. 5 н. и 32 з.п. ф-лы, 38 ил., 2 табл., 11 пр.
1. Композиция для доставки в дыхательные пути, полученная и эффективная для лечения и/или профилактики инфекции вируса гриппа у млекопитающего, содержащая два или более нейтрализующих вирус гриппа моноклональных антител в виде единичной однократной дозы и в эффективном количестве от 0,005 мг/кг до 1 мг/кг и подходящий фармацевтически приемлемый носитель, разбавитель или наполнитель, где
по меньшей мере первое антитело направлено против вируса гриппа А одного подтипа, и
по меньшей мере второе антитело направлено против вируса гриппа A другого подтипа, чем указанное первое антитело, или против вируса гриппа B, или имеется по меньшей мере два вторых антитела, одно из которых направлено против вируса гриппа A указанного другого подтипа и другое антитело направлено против вируса гриппа B.
2. Композиция по п.1, отличающаяся тем, что указанные два или более нейтрализующих вирус гриппа моноклональных антител присутствуют каждое в виде единичной однократной дозы от 0,005 мг/кг до 0,5 мг/кг.
3. Композиция по п.1, отличающаяся тем, что указанные два или более нейтрализующих вирус гриппа моноклональных антител присутствуют каждое в виде единичной однократной дозы от 0,005 мг/кг до 0,1 мг/кг.
4. Композиция по п.1, содержащая одно или более нейтрализующих вирус гриппа моноклональных антител, каждое в виде единичной однократной дозы от 0,005 мг/кг до 0,05 мг/кг.
5. Композиция по п.1, отличающаяся тем, что два или более нейтрализующих вирус гриппа моноклональных антител представляют собой фрагмент антитела, способный к нейтрализации, и выбраны из Fab, Fab' и F(аb')2.
6. Композиция по п.1, дополнительно содержащая добавку для назального или легочного введения, или иммунологический посредник, или стимулятор иммунного ответа.
7. Композиция по п.1, содержащая комбинацию нейтрализующих грипп антител, содержащую антитело, способное нейтрализовать вирус гриппа А H1, антитело, способное нейтрализовать вирус гриппа А H3, и антитело, способное нейтрализовать вирус гриппа B.
8. Композиция по любому из пп.1-7, отличающаяся тем, что моноклональное антитело представляет собой антитело IgG.
9. Применение композиции по п.1 для лечения или профилактики вируса гриппа у млекопитающего, подвергающегося или подверженного риску воздействия вируса гриппа, или проявляющего клинические симптомы респираторной вирусной инфекции.
10. Способ лечения или профилактики вируса гриппа у млекопитающего, подвергающегося или подверженного риску воздействия вируса гриппа, или проявляющего клинические симптомы респираторной вирусной инфекции, включающий введение интраназально (IN) или ингаляционно указанному млекопитающему композиции по п. 1.
11. Способ по п.10, в котором моноклональное антитело вводимой композиции представляет собой антитело IgG.
12. Способ по п.10, включающий введение композиции, содержащей одно или более нейтрализующих вирус гриппа А моноклональных антител и одно или более антител, способных нейтрализовать вирус гриппа B.
13. Способ по п.10, включающий введение композиции, содержащей антитело, способное нейтрализовать вирус гриппа А H1, антитело, способное нейтрализовать вирус гриппа А H3, и антитело, способное нейтрализовать вирус гриппа B.
14. Способ по п.10, отличающийся тем, что композицию вводят в течение периода времени до 24 часов после инфицирования.
15. Способ по п.10, отличающийся тем, что композицию вводят в течение периода времени до 48 часов после инфицирования.
16. Способ по п.10, отличающийся тем, что композицию вводят в течение периода времени до 72 часов после инфицирования.
17. Способ по п.10, отличающийся тем, что композицию вводят в одной или более дозах до инфицирования или воздействия вируса или до клинического проявления вирусного заболевания или симптомов, ассоциированных с ним.
18. Способ по п.10, включающий введение композиции, содержащей два или более нейтрализующих вирус гриппа моноклональных антител каждое в виде единичной однократной дозы от 0,005 мг/кг до 1 мг/кг массы тела.
19. Способ по п.10, включающий введение композиции, содержащей два или более нейтрализующих вирус гриппа моноклональных антител каждое в виде единичной однократной дозы от 0,005 мг/кг до 0,5 мг/кг.
20. Способ по п.10, включающий введение композиции, содержащей два или более нейтрализующих вирус гриппа моноклональных антител каждое в виде единичной однократной дозы от 0,005 мг/кг до 0,1 мг/кг.
21. Способ по п.10, включающий введение композиции, содержащей два или более нейтрализующих вирус гриппа моноклональных антител каждое в виде единичной однократной дозы от 0,005 мг/кг до 0,05 мг/кг.
22. Способ по п.10, отличающийся тем, что композицию вводят интраназально или ингаляционно в многократных дозах, где многократные дозы вводят по меньшей мере с разницей в 2 часа, и вначале вводят через 72 часа после предположительной инфекции, воздействия или проявления клинических симптомов.
23. Профилактическая или терапевтическая комбинация, включающая:
первую композицию, полученную для интраназального или ингаляционного введения, содержащую два или более нейтрализующих вирус гриппа моноклональных антител в виде единичной однократной дозы от 0,005 мг/кг до 1 мг/кг против вирусов гриппа, имеющих различную специфичность, и
вторую композицию, полученную для внутрибрюшинного или внутривенного введения, содержащую одно или более антител против гриппа в виде единичной однократной дозы от 1 мг/кг до 10 мг/кг,
где одно или более антител во второй композиции являются такими же, как одно или более антител в первой композиции, или другими антителами.
24. Комбинация по п.23, отличающаяся тем, что антитело во второй композиции является не-нейтрализующим антителом.
25. Комбинация по п.23, отличающаяся тем, что интраназальная или ингаляционная доза составляет от 0,005 мг/кг до 1 мг/кг, и IP или IV доза составляет от 5 мг/кг до 10 мг/кг.
26. Комбинация по п.23, отличающаяся тем, что интраназальная или ингаляционная доза составляет от 0,005 мг/кг до 1 мг/кг, и IP или IV доза по меньшей мере в 10 раз выше, в мг/кг, чем интраназальная доза.
27. Комбинация по п.23, отличающаяся тем, что интраназальная или ингаляционная доза составляет от 0,005 мг/кг до 0,5 мг/кг, и IP или IV доза составляет от 5 мг/кг до 10 мг/кг.
28. Комбинация по п.23, отличающаяся тем, что первую композицию вводят в течение 24 часов после предполагаемых инфекции, воздействия или проявления клинических симптомов.
29. Комбинация по п.23, отличающаяся тем, что первую композицию вводят в течение 48 часов после предполагаемых инфекции, воздействия или проявления клинических симптомов.
30. Способ уменьшения передачи вируса гриппа, включающий введение композиции по п.1 интраназально или ингаляционно субъекту, подвергаемому, в риске воздействия вируса гриппа или проявляющему клинические признаки инфекции вирусом гриппа.
31. Способ по п.30, отличающийся тем, что антитело вводимой композиции представляет собой антитело IgG.
32. Способ по п.30, отличающийся тем, что композицию вводят в течение 48 часов после предполагаемых инфекции, воздействия или проявления клинических симптомов.
33. Способ по п.30, отличающийся тем, что композицию вводят в течение 24 часов после предполагаемых инфекции, воздействия или проявления клинических симптомов.
34. Способ по п.30, отличающийся тем, что композицию вводят более чем за 24 часа и в течение 72 часов после предполагаемой инфекции, воздействия или проявления клинических симптомов.
35. Способ по п.30, отличающийся тем, что композицию вводят в одной или более дозе до воздействия или проявления клинических симптомов.
36. Способ по п.30, отличающийся тем, что композиция содержит антитело в дозе от 0,005 мг/кг до 0,5 мг/кг.
37. Способ по п.30, отличающийся тем, что композиция содержит антитело в дозе от 0,005 мг/кг до 0,1 мг/кг.
| US 20120128671 A1, 01.08.1987 | |||
| WO 2008110937 A2, 18.09.2008 | |||
| WO 2009079259 A2, 25.06.2009 | |||
| Устройство для фильтрования канифоли | 1929 |
|
SU17203A1 |
Авторы
Даты
2019-09-30—Публикация
2014-03-14—Подача