Изобретение относится к аналитической и фармацевтической отрасли, а именно к определению остаточных количеств хлорида 2-[(Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия (ТДЗ) в биологических объектах при установлении фармакокинетических параметров и определении терапевтической дозы препарата. Предлагаемый способ может быть применен в испытательных лабораториях контроля качества лекарственных средств, лабораториях ОКК фармацевтических предприятий, а также в научно-исследовательских лабораториях.
Известен способ определения ТДЗ в таблетках, включающий растворение навески растертых таблеток ТДЗ в спирте этиловом с последующей фильтрацией раствора и определении оптической плотности испытуемого раствора и раствора стандартного образца на спектрофотометре в максимуме поглощения при длине волны 435 нм в кювете с толщиной слоя 10 мм, используя в качестве раствора сравнения спирт этиловый 96% [Государственный контракт от «20» июля 2015 г. №14.N08.12.0046 УДК 615.453.62. № госрегистрации 115080740020. Инв. №11-10.3/6 «Доклинические исследования лекарственного средства на основе производного тиадиазола, обладающего противогрибковой активностью» шифр темы «2017-14-N08-0042»].
Недостатками данного способа являются его низкая чувствительность и специфичность для проб биологического материала. Увеличение объема биологического материала приводит образованию большого количества соэкстрактивных веществ, мешающих проведению анализа и требующих включения этапа очистки экстракта, что ведет к снижению чувствительности метода и увеличению времени для проведения анализа.
Наиболее близким по технической сущности к заявляемому способу является определение ТДЗ в крови и моче кроликов и крыс, которое заключается в отборе проб биологических жидкостей, осаждении ацетонитрилом, фильтрации через мембранный фильтр с диаметром пор 0,45 мкм и хроматографировании фильтрата на жидкостном хроматографе «Flexar FX15» с масс-спектрометрическим детектором SQ300, при этом используют колонку Kromasil 100-3.5С8, 150 мм×2,1 мм, 3,5 мкм, в качестве элюента используют смесь ацетонитрил : 0,03% раствор трифторуксусной кислоты в соотношении 65:35. Расход подвижной фазы 0,2 мл/мин. Время удерживания ТДЗ 4,5 мин. Минимальное детектируемое количество ТДЗ 50 пг/мл. Линейный диапазон определения 50-2500 пг/мл и 2500-30000 пг/мл. Концентрацию ТДЗ в испытуемых растворах рассчитывают с помощью калибровочного графика в пк/мл [см., например, Quantification of new antifungal drug by HPLC-ESI/MS in biological liquids / N.Y. Sipkina, I.P. Yakovlev // 10th International Conference on Instrumental Methods of Analysis: Modern Trends and Applications September 17-21, 2017, Heraklion - Greece].
Недостатком данного метода определения ТДЗ является невозможность анализа образцов с концентрацией ТДЗ более 30 нг/мл из-за перегрузки масс-анализатора, низкая стабильность работы масс-спектрометра, в связи с чем требуется частая перекалибровка прибора, что приводит к увеличению стоимости и времени анализа, а также общая дороговизна использования масс-спектрометра и дополнительные затраты на обслуживание ионного капилляра и квадроуполя.
Техническим результатом предлагаемого изобретения является возможность определения ТДЗ в диапазоне концентраций от 10,0 нг/мл до 5,0 мкг/мл, повышение стабильности получаемых данных, снижение стоимости анализа и обслуживания прибора за счет использования флуориметрического детектора.
Технический результат достигается тем, что способ количественного определения ТДЗ в биологических объектах с использованием высокоэффективной жидкостной хроматографии состоит из отбора пробы, осаждения, центрифугирования, фильтрации, введения образца в жидкостный хроматограф, хроматографирования и обработки результатов анализа. При этом в качестве пробы берут 0,1-0,5 мл плазмы крови (мочи). Осаждение проводят ацетонитрилом с последующим центрифугированием образца, надосадочную жидкость фильтруют через мембранный фильтр с диаметром пор 0,45 мкм. Образец вводят в жидкостный хроматограф «Flexar» с флуориметрическим детектором, регистрируют хроматограммы при длине волны возбуждения 435 нм и длине волны испускания 520 нм, хроматографирование осуществляют на колонке Zorbax Eclipse Plus С8 длиной 250 мм, внутренним диаметром 4.6 мм и размером частиц 5 мкм, в качестве элюента используют смесь ацетонитрил : 0,03% раствор трифторуксусной кислоты в соотношении 65:35 при скорости потока подвижной фазы 1,0 мл/мин и объеме вводимой пробы 20 мкл.
Использование высокоэффективного жидкостного хроматографа «Flexar» с флуориметрическим детектором и колонки Zorbax Eclipse Plus С8 (250×4.6 мм) с размером частиц сорбента 5 мкм, а также элюента, состоящего из смеси ацетонитрил : 0,03% раствор трифторуксусной кислоты в соотношении 65:35 при скорости потока подвижной фазы 1,0 мл/мин и объеме вводимой пробы 20 мкл, позволяет получить острый, симметричный пик ТДЗ, коэффициент ассиметрии которого близок к 1, что вместе с использованием флуориметрического детектора позволяет определять ТДЗ в диапазоне концентраций от 10,0 нг/мл до 5,0 мкг/мл при высокой стабильности и повторяемости получаемых данных, снижение стоимости анализа и обслуживания прибора.
Способ количественного определения ТДЗ в биологических объектах с использованием высокоэффективной жидкостной хроматографии с флуориметрическим детектированием осуществляют согласно следующей методике.
Пример 1. Подготовка вспомогательных растворов.
Растворитель пробы. Смешивают 50 мл 0,03% раствора трифторуксусной кислоты и 50 мл ацетонитрила.
Основной раствор: 10,0 мг стандартного образца ТДЗ помещают в мерную колбу вместимостью 10 мл, прибавляют 5 мл ацетонитрила, выдерживают в ультразвуковой ванне 10 мин, доводят до метки тем же растворителем.
Исходный раствор 1: 1 мл основного раствора помещают в мерную колбу вместимостью 10 мл, доводят объем раствора ацетонитрилом до метки и перемешивают (С=10-4 г/мл).
Исходный раствор 2: 1 мл исходного раствора 1 помещают в мерную колбу вместимостью 10 мл, доводят объем раствора растворителем пробы до метки, перемешивают и фильтруют через фильтр с диаметром пор 0,45 мкм (С=10-5 г/мл).
Калибровочные растворы.
Калибровочные растворы готовят последовательным разбавлением исходных растворов 1 и 2, получая пять калибровочных растворов с концентрацией 0,01, 0,10, 0,5, 1,0 и 5,0 мкг/мл. В качестве растворителя используют растворитель пробы.
Раствор для определения предела количественного определения (LOQ): раствор LOQ готовят десятикратным разбавлением калибровочного раствора с концентрацией 0,10 мкг/мл (С=1*10-8 г/мл).
Раствор для определения предела обнаружения (LOD): раствор LOD готовят двукратным разбавлением раствора LOQ (С=5,0*10-9 г/мл).
Пример 2. Подготовка испытуемых растворов:
0,1-0,5 мл плазмы крови (мочи) переносят в пробирку из боросиликатного стекла, порционно прибавляют ацетонитрил (по 100-200 мкл) до конечного объема 3 мл при постоянном встряхивании. Затем пробирки центрифугируют 15 минут со скоростью 8000 об/мин при температуре +15°С. Надосадочную жидкость количественно переносят в мерную колбу вместимостью 5 мл, доводят до метки растворителем пробы и перемешивают. Полученные экстракты фильтруют через мембранный фильтр с диаметром пор 0,45 мкм.
Срок годности растворов 72 часа при температуре 25°С.
Пример 3. Хроматографирование и обработка результатов.
Хроматографические условия:
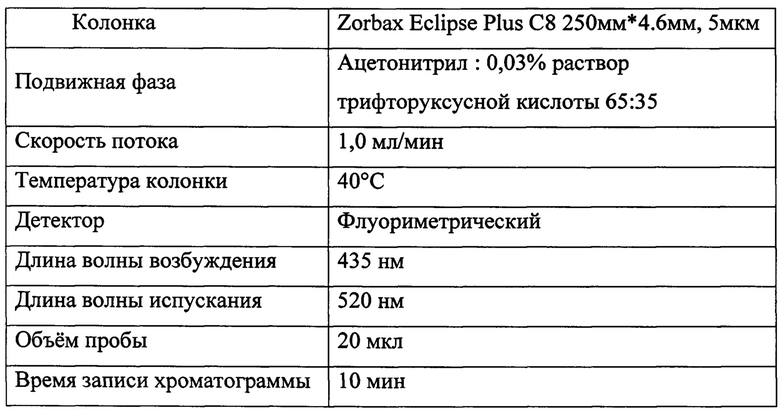
Хроматографируют калибровочные растворы, получая не менее 3 хроматограмм каждого раствора в заданных условиях. Время удерживания пика ТДЗ должно быть около 5,5 мин.
Хроматографическая система считается пригодной, если на хроматограмме калибровочного раствора с концентрацией 0,5 мкг/мл выполняются следующие условия:
эффективность хроматографической колонки, рассчитанная по пику ТДЗ, не менее 5000 теоретических тарелок;
фактор асимметрии пика ТДЗ от 0,8 до 1,8;
относительные стандартные отклонения времен удерживания и площадей пиков ТДЗ, рассчитанные по 5 последовательным хроматограммам, не более 2,0%.
Строят график зависимости в координатах площадь пика ТДЗ - концентрация (С, мкг/мл). Определяют коэффициент корреляции (R), который должен быть не менее 0,995, и коэффициент Стьюдента свободного члена (ta), который не должен превышать табличное значение.
Хроматографируют растворы для определения предела количественного определения и предела обнаружения не менее 10 раз. Рассчитывают среднее значение и относительное стандартное отклонение площадей пиков ТДЗ, а также значение сигнал/шум для пика ТДЗ. Относительное стандартное отклонение площадей пиков ТДЗ, рассчитанное по хроматограммам раствора для определения предела количественного определения и предела обнаружения должно быть не более 5 и 10% соответственно. Значения сигнал/шум, рассчитанные по хроматограммам раствора для определения предела количественного определения и предела обнаружения должно быть не менее 10 и 3 соответственно.
Хроматографируют испытуемые растворы, получая не менее 3 хроматограмм в заданных условиях.
Концентрацию ТДЗ в испытуемых растворах в мкг/мл находят, используя график линейности.
Анализ метрологических характеристик способа определения ТДЗ в биологических объектах (табл. 1) показывает высокую стабильность и повторяемость полученных результатов в диапазоне концентраций от 10,0 нг/мл до 5,0 мкг/мл за счет стабильной работы с высокой чувствительностью флуориметрического детектора, что приводит к снижению общей стоимости анализа.
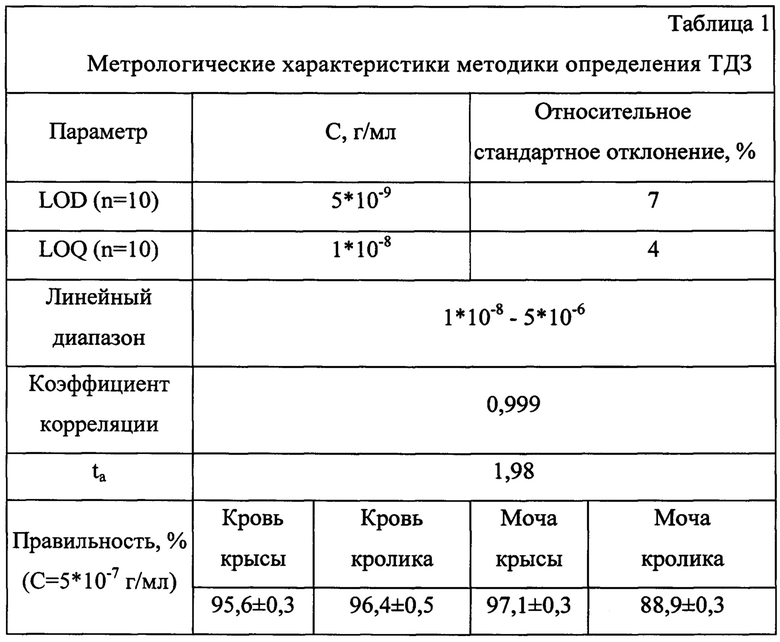
Способ определения ТДЗ в биологических объектах с использованием высокоэффективной жидкостной хроматографии с флуориметрическим детектированием прост и экономичен в осуществлении.
Предлагаемый способ определения ТДЗ в биологических объектах с использованием высокоэффективной жидкостной хроматографии с флуориметрическим детектированием может быть применен в испытательных лабораториях контроля качества лекарственных средств, лабораториях ОКК фармацевтических предприятий, а также в научно-исследовательских лабораториях.
Предлагаемый способ определения ТДЗ в биологических объектах с использованием высокоэффективной жидкостной хроматографии с флуориметрическим детектированием апробирован в Центре Контроля Качества Лекарственных Средств федерального государственного бюджетного образовательного учреждения высшего образования «Санкт-Петербургский государственный химико-фармацевтический университет» Министерства здравоохранения Российской Федерации.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения 2,2,6,6-тетраметил-N-{ 1-[5-(4-метил-3-хлоранилино)-1,2,4-тиадиазол-3-ил]пропан-2-ил} пиперидин-4-амина дигидрохлорида в биологических средах | 2016 |
|
RU2636231C1 |
| ХЛОРИД 2-[(1Z)-1-(3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-2(3Н)-ИЛИДЕН)МЕТИЛ]-3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-3-ИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2402550C1 |
| 6-(3,5-Дифенил-1,3,4-тиадиазол-2(3Н)-илиден)-2,4-дифенил-4Н-1,3,4-тиадиазин-5-он и способ его получения | 2016 |
|
RU2659574C2 |
| Способ количественного определения 4,4'-(пропандиамидо)дибензоата натрия в биологических объектах | 2021 |
|
RU2780870C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В КРОВИ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2014 |
|
RU2546530C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2011 |
|
RU2466406C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕОНИКОТИНОИДОВ В ПОДМОРЕ ПЧЕЛ С ИСПОЛЬЗОВАНИЕМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2019 |
|
RU2730399C1 |
| СПОСОБ ИЗМЕРЕНИЯ КОЛИЧЕСТВА ПОЛИСОРБАТА-80 С ПРИМЕНЕНИЕМ ЩЕЛОЧНОГО ГИДРОЛИЗА ОБРАЗЦА С ПОСЛЕДУЮЩЕЙ ВЭЖХ | 2017 |
|
RU2670965C9 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 2-ФЕНОКСИЭТАНОЛА В БИОЛОГИЧЕСКИХ СРЕДАХ | 2021 |
|
RU2776730C1 |
| Способ определения аминогликозидных антибиотиков методом обращенно-фазной высокоэффективной жидкостной хроматографии | 2022 |
|
RU2786839C1 |
Изобретение относится к аналитической и фармацевтической отрасли, а именно к определению остаточных количеств хлорида 2-[(Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия (ТДЗ) в биологических жидкостях при установлении фармакокинетических параметров и определении терапевтической дозы препарата. Раскрыт способ определения ТДЗ в биологических жидкостях с использованием высокоэффективной жидкостной хроматографии, включающий отбор пробы, осаждение, центрифугирование, фильтрацию, введение образца в жидкостный хроматограф, хроматографирование и обработку результатов анализа. При этом используют флуориметрический детектор, регистрируют хроматограммы при длине волны возбуждения 435 нм и длине волны испускания 520 нм, используют колонку Zorbax Eclipse Plus С8 длиной 250 мм, внутренним диаметром 4.6 мм и размером частиц 5 мкм при скорости потока подвижной фазы 1,0 мл/мин и объеме вводимой пробы 20 мкл. Изобретение обеспечивает возможность определения ТДЗ в диапазоне концентраций от 10,0 нг/мл до 5,0 мкг/мл, повышение стабильности получаемых данных, снижение стоимости анализа и обслуживания прибора за счет использования флуориметрического детектора. 2 табл., 3 пр.
Способ количественного определения хлорида 2-[(Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия в биологических объектах с использованием высокоэффективной жидкостной хроматографии, включающий отбор пробы, осаждение, центрифугирование, фильтрацию, введение образца в жидкостный хроматограф, хроматографирование и обработку результатов анализа, отличающийся тем, что в качестве детектора используют флуориметрический детектор, регистрируют хроматограммы при длине волны возбуждения 435 нм и длине волны испускания 520 нм, хроматографирование осуществляют на колонке Zorbax Eclipse Plus С8 длиной 250 мм, внутренним диаметром 4,6 мм и размером частиц 5 мкм, при скорости потока подвижной фазы 1,0 мл/мин и объеме вводимой пробы 20 мкл.
| SIPKINA N.Y | |||
| et al | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| ХЛОРИД 2-[(1Z)-1-(3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-2(3Н)-ИЛИДЕН)МЕТИЛ]-3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-3-ИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2402550C1 |
| КОШЕВЕНКО А.С | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2019-10-08—Публикация
2019-06-25—Подача