Изобретение относится к медицине и касается создания средств для лечения эндокринных и гормонозависимых опухолей.
Число больных с гормонозависимыми опухолями постоянно растет. Так, например, в год заболевают раком желудка около 60 тыс., кишечника - 40 тыс., поджелудочной железы - 15 тыс.человек. Эффективность существующих препаратов при лечении эндокринных опухолей составляет всего от 15 до 20% [1. Давыдов М.И., Аксель Е.М. Злокачественные новообразования в России и странах СНГ. М.: - 2005 г. ]. Поэтому создание принципиально новых отечественных противоопухолевых препаратов, существенно отличающихся по избирательности, токсичности и спектру действия от применяемых в медицинской практике цитостатиков, на сегодня весьма актуально.
В последние годы фундаментальная медико-биологическая наука достигла значительных успехов в изучении механизма злокачественной трансформации клеток и процесса метастазирования новообразований. Это позволило определить новые мишени воздействия потенциальных противоопухолевых средств [2. Личиницер М.Р., Степанова Е.В. Лекарственная терапия опухолей в XXI веке. Горбунова В.А. (ред), Артамонова Е.В., Базин С.Г. и др. Этюды химиотерапии - М: Литтерра, 2006. - С. 28-30.; 2. Личинщер М.Р., Степанова Е.В. Направленная терапия - новое направление лечения злокачественных опухолей. Горбунова В.А. (ред), Артамонова Е.В., Базин С.Г. и др. Этюды химиотерапии - М: Литтерра, 2006. - С. 31-38.].
В свете современных представлений о значении гормонов в развитии гормонозависимых опухолей, повышенный интерес вызывает поиск принципиально новых противоопухолевых веществ среди пептидных гормонов гипоталамуса, которые способны селективно воздействовать на процессы рецептороопосредованного взаимодействия и участвовать в передаче внутриклеточных сигналов [A.Schally A.V., Comary-Schally A.M., Nagy A. et. al. Hypotalamic hormones and cancer // Front. Neuroendocrinol. - 2001. - №22. - P. 248-291; b.Weckhecker G., Lewis I., Albert R., Schmidt H.A. et. al. Opportunities in somatostatin research: biological, chemical and therapeutic aspects //Nature Rev. Drug Discovery. - 2003. - Vol. 2. - P. 999-1017.].
Особое внимание привлекает гипоталамический гормон соматостатин. Одной из основных функций соматостатина в организме является ингибирование секреции гормона роста, наряду с этим соматостатин обладает широким спектром биологического действия - угнетает выделение пролактина, инсулина, глюкагона, гормонов поджелудочной железы и желудочно-кишечного тракта, стимулирующих пролиферативные процессы в клетке [6. Buscail L., Vernejoul K, Fame P., Torrisani J., Susini C. Regulation of cell proliferation by somatostatin // Ann Endocrinol. - 2002. - Vol. 63. - P. 2S13-8.]. Механизм ингибирования секреторных и пролиферативных процессов соматостатина и его аналогов реализуется через специфические рецепторы, которые широко представлены на клетках тканей-мишеней: в ЦНС (гипоталамус, гипофиз, спинной мозг) и желудочно-кишечном тракте (преимущественно в поджелудочной железе, желудке, верхних отделах тонкого кишечника). Показана высокая экспрессия рецепторов соматостатина на клетках злокачественных опухолей: гастриноме, глюкагономе, карциноидных опухолях, мелкоклеточном раке легкого и других [7. Nagy A., Schally А.V. Targeting cytotoxic conjugates of somatostatin, luteinizing hormone-releasing hormone and bombensin to cancer expressing their receptors: a "smarter" chemotherapy // Current Pharmaceutical Design. - 2005. - Vol. 11, №9 - P. 1167-1180.]. Отличительной особенностью соединений этого класса является отсутствие токсичности и высокая избирательность действия. Недостатком является то, что они быстро метаболизируют под действием протеиназ. Короткое время полужизни соматостатина в крови (три минуты) является нежелательным при его клиническом применении. Ферментативная устойчивость пептидных гормонов может быть достигнута путем химической модификации аминокислотной цепи молекулы соматостатина, в частное, л, заменой аминокислот в нативном пептиде на неприродные аминокислоты [8. Schally А.V. Oncological applications of somatostatin analogs // Cancer Research. - 1988. - Vol. 48. - P. 6977-6985.].
Применяемый в настоящее время в клинической практике зарубежный препарат, структурный аналог соматостатина - Сандостатин или октреотид, состоит из 8 аминокислот и имеет циклическое строение. Показаниями для применения сандостатина являются опухоли островкового аппарата поджелудочной железы, рак поджелудочной железы, карциноидные опухоли, медулярный рак щитовидной железы, аденомы гипофиза [9. Comary-Schally A.M., Schally А.V. A clinical overview of carcinoid tumors: respectives for improvement in treatment using peptide analogs (review) // International Journal Of Oncology. - 2005. - Vol. 26(2). - P. 301-309.; 10. Schally A.V., Szepeshazi K., Nagy A. et al. New approaches to therapy of cancers of the stomach, colon and pancreas based on peptide analogs // Cellular and Molecular Life Sciences. - 2004. - Vol. 61. - P. 1042-1048.]. Принят за базовый объект.
В ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России на протяжении ряда лет проводились исследования по поиску потенциальных противоопухолевых соединений в ряду аналогов гипоталамических гормонов, в частности аналогов соматостатина.
Известно средство, обладающее противоопухолевым действием, представляющее собой линейный пентапептид общей формулы:
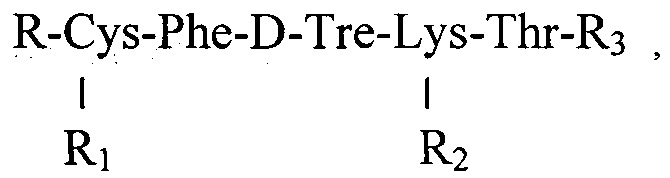
где
R - трет-бутилокарбонил или Н,
R1 - тетрагидропиранил или Н,
R2 - N3 - бензилоксикарбонил или Н,
R3 -О-метил или S-тетрагидропиранилцистеина метиловый эфир. [11. Патент РФ RU 2254139 С1, опубликовано 20.06.2005 г.]. Это соединение обладает большой активностью и биодоступностью при внутрибрюшинном введении, но имеет недостаточную растворимость в растворителях для инъекций (вводили суспензию внутрибрюшинно), в связи с чем возникает сложность их внутрисистемного введения для проведения терапии.
С использованием вышеуказанного соединения 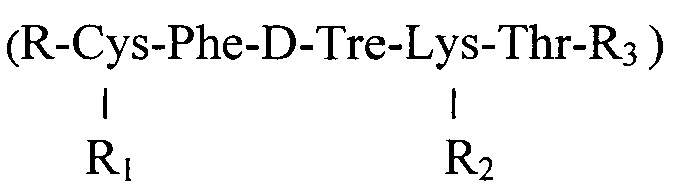 была создана пероральная лекарственная форма в виде таблеток, дополнительно содержащих в составе лактозу, микрокристаллическую целлюлозу, крахмал, поливилпирролидон (повидон), тальк и стеарат магния [12. Михаевич Е.И., Яворская Н.П., Голубева И.С., Орлова О.Л., Полозкова А.П., Партолина С.А., Оборотова Н.А. Вопросы биологической, медицинской и фармацевтической химии. - 2011. - №10. - С. 68-72.], которая в настоящий момент проходит первую фазу клинических исследований. При проведении клинических исследований выявлено, что биодоступность пероральной лекарственной формы слишком низкая, для больных необходима системная доставка препарата или значительного увеличения дозы активного вещества -
была создана пероральная лекарственная форма в виде таблеток, дополнительно содержащих в составе лактозу, микрокристаллическую целлюлозу, крахмал, поливилпирролидон (повидон), тальк и стеарат магния [12. Михаевич Е.И., Яворская Н.П., Голубева И.С., Орлова О.Л., Полозкова А.П., Партолина С.А., Оборотова Н.А. Вопросы биологической, медицинской и фармацевтической химии. - 2011. - №10. - С. 68-72.], которая в настоящий момент проходит первую фазу клинических исследований. При проведении клинических исследований выявлено, что биодоступность пероральной лекарственной формы слишком низкая, для больных необходима системная доставка препарата или значительного увеличения дозы активного вещества -
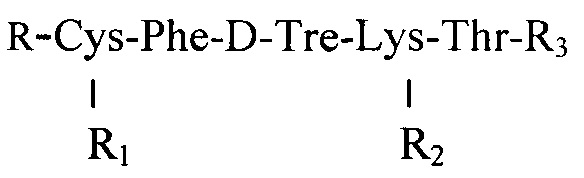
Это средство принято за прототип.
Недостатками прототипа являются:
1. Невозможность системной доставки препарата в организм больного.
2. Недостаточная биодоступность.
3. Большая доза для больного (большое количество таблеток на один прием).
4. Недостаточная противоопухолевая активность.
Задачей изобретения является создание инъекционного средства для лечения гормонозависимых опухолей.
Задача решается тем, что предлагается средство для лечения гормонозависимых опухолей, представляющее собой лиофилизат для приготовления раствора для инъекций, включающее 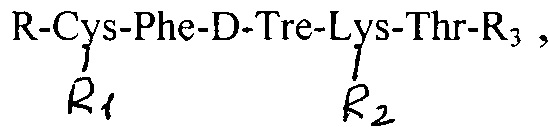 дополнительно содержащее фосфатидилхолин, холестерин, DSPE-PEG-2000 и сахарозу при следующем молярном соотношении компонентов: 1,0: 71,1: 13,9: 0,2: 346,5. Фосфатидилхолин для формирования нановезикул, холестерин - прочность липосом, пегилирование липосом (DSPE-PEG-2000) - для предотвращения захвата липосомы ретикулоэндотелиальной системой (РЭС), сахароза - криопротектор для избежания «слипания» липосом при сублимации. Данное молярное соотношение компонентов обеспечивает получение липосом приемлемого размера (180±6 нм) с минимальными потерями активного вещества на стадии фильтрации и экструзии, а соответственно с самым высоким уровнем его включения в везикулы - (97±1) %. Изменение доли указанных вспомогательных веществ в соотношении как в сторону их уменьшения, так и в сторону увеличения способствовало снижению количества включенного активного вещества и укрупнению липосом.
дополнительно содержащее фосфатидилхолин, холестерин, DSPE-PEG-2000 и сахарозу при следующем молярном соотношении компонентов: 1,0: 71,1: 13,9: 0,2: 346,5. Фосфатидилхолин для формирования нановезикул, холестерин - прочность липосом, пегилирование липосом (DSPE-PEG-2000) - для предотвращения захвата липосомы ретикулоэндотелиальной системой (РЭС), сахароза - криопротектор для избежания «слипания» липосом при сублимации. Данное молярное соотношение компонентов обеспечивает получение липосом приемлемого размера (180±6 нм) с минимальными потерями активного вещества на стадии фильтрации и экструзии, а соответственно с самым высоким уровнем его включения в везикулы - (97±1) %. Изменение доли указанных вспомогательных веществ в соотношении как в сторону их уменьшения, так и в сторону увеличения способствовало снижению количества включенного активного вещества и укрупнению липосом.
Предлагаемое средство получали с использованием метода Бенгема (Bangham) [13. Liposomes: a practical approach. In D.Rickwood and B.D. Hames (eds.). Practical Approach Series, oil Press at Oxford University Press, 1990; G. Gregoriadis (ed.), Liposome technology, Vol. 1, CRC Press, Boca Raton, Fl, 1984 г.], адаптированным для нерастворимых субстанций.
Заявляемое средство получали следующим образом: растворяли 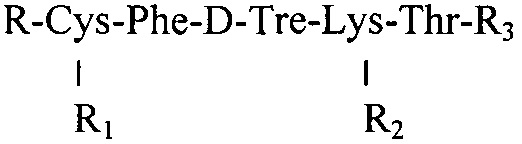 , фосфатидилхолин, холестерин и DSPE-PEG-2000 в хлороформе. Далее упаривали образовавшейся хлороформный раствор на роторном испарителе под вакуумом до полного удаления хлороформа. Затем, диспергировали образованную при упаривании пленку водой для инъекций встряхиванием. Затем проводили фильтрацию полученной липосомальной дисперсии и экструзию (для получения более мелких липосом). Средний размер липосом после экструзии, измеренный на приборе Submicron Particle Sizer NICOMP-380, составлял 160-190 нм. После экструзии в липосомальную дисперсию дополнительно вводили раствор сахарозы, после чего дисперсию стерилизовали фильтрацией и дозировали. Добавление раствора сахарозы после экструзии обеспечивает высокое (более 90%) включение
, фосфатидилхолин, холестерин и DSPE-PEG-2000 в хлороформе. Далее упаривали образовавшейся хлороформный раствор на роторном испарителе под вакуумом до полного удаления хлороформа. Затем, диспергировали образованную при упаривании пленку водой для инъекций встряхиванием. Затем проводили фильтрацию полученной липосомальной дисперсии и экструзию (для получения более мелких липосом). Средний размер липосом после экструзии, измеренный на приборе Submicron Particle Sizer NICOMP-380, составлял 160-190 нм. После экструзии в липосомальную дисперсию дополнительно вводили раствор сахарозы, после чего дисперсию стерилизовали фильтрацией и дозировали. Добавление раствора сахарозы после экструзии обеспечивает высокое (более 90%) включение 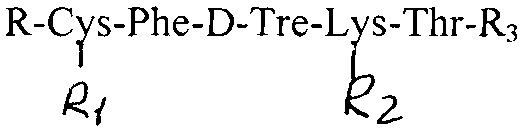 в липосомы.
в липосомы.
Полученная данным способом липосомальная дисперсия при условии хранения при температуре +2…+8°С стабильна непродолжительный период времени - в течение 5 суток. При более длительном хранении наблюдали постепенное слияние и образование везикул более крупных размеров и снижение уровня рН липосомальной дисперсии, что обусловлено процессами перекисного окисления липидов, входящих в состав лекарственной формы. Данный недостаток препятствует осуществлению серийного производства заявляемого средства. Для повышения устойчивости в процессе хранения и продления срока годности предложена стабилизация липосомальной дисперсии посредством сублимационной сушки, что позволило увеличить срок годности заявляемого средства до 2 лет. Сублимационная сушка осуществляется следующим образом:
0. Старт, комнатная температура +20…+25°С
1. -15-17°С. Охлаждение от комнатной температуры до застывания (произошло при температуре продуктов по датчикам -2…-4°С), доведение температуры до -7…-9°С, выдерживание в течение 50 мин. - 2,5-3 часа.
2. -25…-27°С. Охлаждение от -8…-10°С до -18…-20°С (по датчикам температуры продуктов), выдерживание в течение 50 мин. - 1,5-1,8 часа.
3. -35…-37°С. Охлаждение от -18…-20°С до -28…-30°С, выдерживание в течение 40 мин. -1,3-1,6 часа.
4. -45…-47°С. - Охлаждение от -28…-30°С до -38…-40°С, выдерживание в течение 40 мин. При достижении температуры полки -40°С - включение охлаждения конденсатора вакуумной ловушки-1,3-1,6 часа.
5. -50°С. Охлаждение продуктов от -38…-40°С до минимально достижимой температуры -42…-45°С, уравновешивание температуры -1,0-1,2 часа.
После достижения и уравновешивания минимальной температуры продукта флаконы с препаратом выдерживали в течение 3 часов, после чего начинали откачку воздуха. После включения вакуумного насоса, выравнивания вакуума и отсушивания поверхностного слоя замороженной дисперсии осуществляли:
1. Нагрев полок до температуры -20°С со скоростью +5°С/час.
2. Выдерживание полок на температуре -20°С в течение 2 часов
3. Нагрев полок до температуры -10°С со скоростью +3°С/час.
4. Нагрев полок до комнатной температуры +20…+22°С со скоростью +5°С/час. После этого осуществляли досушивание препарата продолжительностью около 3 часов по критерию неизменности остаточного давления паров в сублимационной камере при перекрывании вакуумной магистрали. Общее время замораживания и сушки препарата составило 36-38 часов.
Ниже приведены конкретные примеры предлагаемого инъекционного средства (Заявляемое средство) для лечения гормонозависимых опухолей (мг).
Сравнительные исследования биологической активности заявляемого лекарственного средства для лечения гормонозависимых опухолей и прототипа
Для изучения противоопухолевой эффективности Заявляемого средства использованы самки мышей-гибридов F1 (C57Bl/6 × DBA/2). Исследования проведены на перевиваемой аденокарциноме молочной железы Са-755 мышей из Банка опухолевых штаммов ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России. Штамм Са-755 поддерживали на самках линейных мышей C57Bl/6. Для опыта Са-755 перевивали мышам подкожно (п/к) в правую подмышечную область по 0,5 мл (50 мг) взвеси опухолевых клеток при разведении 1:10 в среде 199 [14. Экспериментальная оценка противоопухолевых препаратов в СССР и США. Под ред З.П. Софъиной, А.Б. Сыркина (СССР), А.Голджа, А.Кляйна (США) М.: «Медицина». - 1980. - С. 71-112.]. Контрольная группа состояла из 10 мышей, опытная группа - из 8 животных. Лечение начинали через 48 ч после трансплантации опухолей [15. Переводчикова Н.И., Горбунова В.А. (ред.) Руководство по химиотерапии опухолевых заболеваний. М.: Практическая медицина. - 2015. - 686 с.; 16. Руководство по проведению доклинических исследований. Часть первая, (под редакцией А.H. Миронова, ФГБУ НЦЭСМП Минздрава России.) - М., 2012 - 944 с.; 17. Большаков О.П., Незнанов Н.Г., Бабаханян Р.В. Дидактические и этические аспекты проведения исследований на биомоделях и на лабораторных животных. ВОЗ, 2000. Рекомендации комитетам по этике, проводящим экспертизу биомедицинских исследований // Качественная клиническая практика. - 2002. - №9. - С. 1-15.].
С целью определения оптимального пути введения, при котором достигается наибольшая эффективность, применяли п/к и внутривенный (в/в) способы введения заявляемого средства.
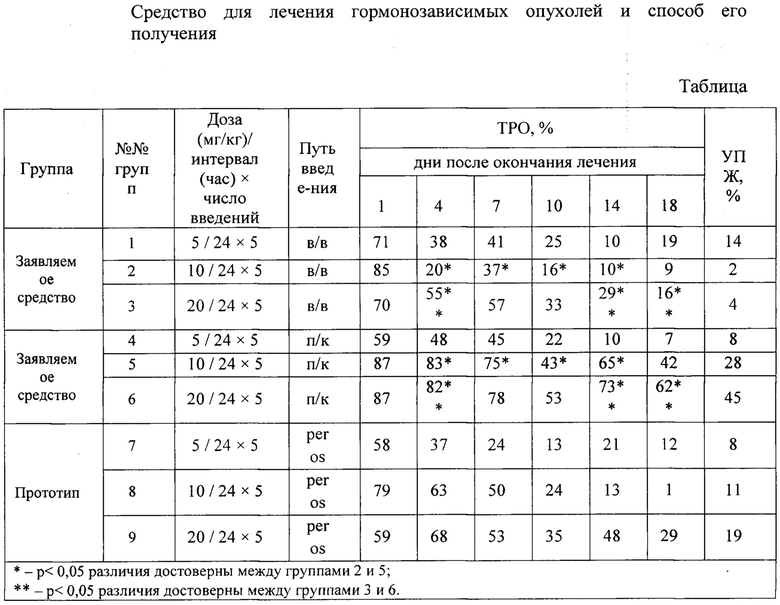
Сравнительное изучение противоопухолевой активности экспериментальной модели заявляемого средства в зависимости от способа введения на Са-755, показало преимущество п/к 5-кратного введения. Так статистически значимый высокий противоопухолевый эффект в дозах 10 и 20 мг/кг сохранялся в течение 14-18 дней после окончания лечения: торможение роста опухоли (ТРО)=83-65% и ТРО = 82-62%, соответственно. При этом увеличение продолжительности жизни (УПЖ) мышей с Са-755 при п/к введении Заявляемого средства дозе 10 и 20 мг/кг составляло 28 и 45%, соответственно, при минимальном критерии активности ≥25%.
При в/в введении в дозах 5 и 10 мг/кг наблюдался кратковременный противоопухолевый эффект заявляемого средства сразу после окончания лечения: ТРО = 71% и ТРО = 85%, соответственно. При в/в введении в дозе 20 мг/кг умеренная противоопухолевая активность сохранялась в течение 7 дней: ТРО = 70-57%. При сравнительной оценке эффективности заявляемого средства при в/в введении и Прототипа при пероральном (per os) введении мышам с Са-755, выявлен схожий противоопухолевый эффект в дозе 20 мг/кг в течение 7 дней после окончания лечения: ТРО = 10-51% и ТРО - 59-53%, соответственно.
Изобретение иллюстрируется таблицей, на которой представлено сравнительное изучение противоопухолевой активности заявляемого средства в зависимости от способа введения на Са-755.
Показано, что противоопухолевая активность заявляемого средства при п/к введении в сравнении с прототипом при per os применении на Са-755 мышей более эффективна. Так в дозах 10 и 20 мг/кг длительность противоопухолевого эффекта заявляемого средства при п/к введении наблюдалась в течение 14-18 дней и составляла ТРО = 87-65% и ТРО = 87-62%, соответственно. Тогда как, per os введение аналогичных доз прототипа тормозило рост Са-755: ТРО = 79-50% и ТРО = 59-53%, соответственно. Противоопухолевый эффект при этом сохранялся в течение 7 дней после окончания лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Противоопухолевое лекарственное средство для перорального применения | 2020 |
|
RU2748989C1 |
| СРЕДСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2016 |
|
RU2646834C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2254139C1 |
| ИММУНОЛИПОСОМАЛЬНАЯ ФОРМА ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2410090C1 |
| Комбинированная наноконструкция для терапии рака легкого | 2024 |
|
RU2841547C1 |
| Средство для терапии опухолей | 2019 |
|
RU2726801C1 |
| СРЕДСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ, СПОСОБ ПОЛУЧЕНИЯ ПРЕДЛАГАЕМОГО СРЕДСТВА И СПОСОБ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ПРЕДЛАГАЕМОГО СРЕДСТВА | 2010 |
|
RU2428981C1 |
| ЛИПОСОМАЛЬНЫЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2007 |
|
RU2494729C2 |
| Способ получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина | 2020 |
|
RU2755572C1 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
Группа изобретений относится к медицине и касается средства для лечения аденокарциномы молочной железы, включающего метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбониллизилтреонина (П), где средство представляет собой лиофилизат для приготовления раствора для инъекций, дополнительно содержит фосфатидилхолин (ФХ), холестерин (X) и DSPE-PEG-2000 (ПЭГ-липид) и сахарозу (С) при молярном соотношении компонентов: МП: МФХ: МХ: МПЭГ-липид: МС=1,0 : 71,1 : 13,9 : 0,2 : 346,5. Группа изобретений также касается способа получения указанного средства, включающего растворение П, ФС, X и ПЭГ-липида, взятых в пропорции 1,0 : 71,1 : 13,9 : 0,2, упаривание образовавшегося хлороформного раствора на роторном испарителе под вакуумом, диспергирование образованной при упаривании пленки, фильтрацию и экструзию полученной липосомальной дисперсии, добавление раствора криопротектора, дозирование и стабилизирование лиофилизацией. Группа изобретений обеспечивает повышение биодоступности и противоопухолевой активности лекарственного средства. 2 н.п. ф-лы, 1 табл., 3 пр.
1. Средство для лечения аденокарциномы молочной железы, включающее метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбониллизилтреонина (П), отличающееся тем, что оно представляет собой лиофилизат для приготовления раствора для инъекций, дополнительно содержит фосфатидилхолин (ФХ), холестерин (X) и DSPE-PEG-2000 (ПЭГ-липид) и сахарозу (С) при молярном соотношении компонентов:
МП: МФХ: МХ: МПЭГ-липид: МС=1,0 : 71,1 : 13,9 : 0,2 : 346,5.
2. Способ получения средства для лечения аденокарциномы молочной железы по п. 1, включающий растворение метилового эфира Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбониллизилтреонина (П), фосфатидилхолина (ФС), холестерина (X) и DSPE-PEG-2000, взятых в пропорции 1,0 : 71,1 : 13,9 : 0,2, упаривание образовавшегося хлороформного раствора на роторном испарителе под вакуумом до полного удаления хлороформа, диспергирование образованной при упаривании пленки водой для инъекций, фильтрацию и экструзию полученной липосомальной дисперсии, добавление раствора криопротектора - сахарозы до молярного соотношения МП: МС=1,0: 346,5, дозирование и стабилизирование лиофилизацией в течение 36-38 часов.
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2254139C1 |
| Противоопухолевый липосомальный препарат и способ его получения | 2017 |
|
RU2663291C1 |
| WO 2009033660 A2, 19.03.2009 | |||
| OBERG K | |||
| Cancer: antitumor effects of octreotide LAR, a somatostatin analog | |||
| Nat Rev Endocrinol | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2019-10-21—Публикация
2018-09-18—Подача