Изобретение относится к медицине и касается создания перорального лекарственного средства для лечения опухолей, экспрессирующих рецепторы к соматостатину. В настоящее время заболеваемость опухолями такого типа составляет 6,98 случаев/100000 населения. Эффективность существующих лекарственных препаратов при лечении нейроэндокринных опухолей составляет всего от 15 до 20% (Рациональная фармакотерапия в онкологии / под ред. М.И. Давыдова, В.А. Горбуновой. М: Литтерра, 2015).
Поэтому создание принципиально новых отечественных противоопухолевых препаратов, существенно отличающихся по избирательности, безопасности и спектру действия от применяемых в медицинской практике, на сегодня весьма актуально. В последние годы фундаментальная медико-биологическая наука достигла значительных успехов в изучении механизма злокачественной трансформации клеток и процесса метастазирования новообразований. Это позволило определить новые мишени воздействия потенциальных противоопухолевых средств (Корман Д.Б. Мишени и механизмы действия противоопухолевых препаратов / под ред. М.И. Давыдова, В.А. Горбуновой. М.: Литтерра, 2015. С. 116-130.).
В свете современных представлений о значении гормонов в развитии гормонозависимых опухолей, повышенный интерес вызывает поиск принципиально новых противоопухолевых веществ среди пептидных гормонов гипоталамуса, которые способны селективно воздействовать на процессы рецептороопосредованного взаимодействия и участвовать в передаче внутриклеточных сигналов (Oberg KE. The management of neuroendocrine tumours: current and future medical therapy options. Clin Oncol (R Coll Radiol) 2012; 24(4):282-93); (Patel P, Galoian K. Molecular challenges of neuroendocrine tumors. Oncol Lett 2018; 15(3):2715 - 25); (Bousquet C, Lasfargues C, Chakabi M et al. Current scientific rationale for the use of somatostatin analogs and mTOR inhibitors in neuroendocrine tumor therapy. J Clin Endocrinol Metab 2012; 97:727-37).
Особое внимание привлекает гипоталамический гормон соматостатин. Одной из основных функций соматостатина в организме является ингибирование секреции гормона роста. Наряду с этим соматостатин обладает широким спектром биологического действия - угнетает выделение пролактина, инсулина, глюкагона, гормонов поджелудочной железы и желудочно-кишечного тракта, стимулирующих пролиферативные процессы в клетке (Susini С, Buscail L. Rationale for the use of somatostatin analogs as antitumor agents. Ann Oncol 2006; 17:1733-42).
Механизм ингибирования секреторных и пролиферативных процессов соматостатина и его аналогов реализуется через специфические рецепторы, которые широко представлены на клетках тканей-мишеней: в центральной нервной системе (гипоталамус, гипофиз, спинной мозг) и желудочно-кишечном тракте (преимущественно в поджелудочной железе, желудке, верхних отделах тонкого кишечника). Показана высокая экспрессия рецепторов соматостатина на клетках злокачественных опухолей: гастриноме, глюкагономе, карциноидных опухолях, мелкоклеточном раке легкого и других (Unger N, Ueberberg В, Schulz S et al. Differential expression of somatostatin receptor subtype 1-5 proteins in numerous human normal tissues. Exp Clin Endocrinol. Diabetes 2012;120(8):482-89).
Отличительной особенностью соединений этого класса является отсутствие токсичности и высокая избирательность действия. Недостатком является то, что они быстро метаболизируют под действием протеиназ. Короткое время полужизни соматостатина в крови (не более трех мин) делает невозможным его клиническое применение. Ферментативная устойчивость пептидных гормонов может быть достигнута путем химической модификации аминокислотной цепи молекулы соматостатина, в частности, заменой аминокислот в нативном пептиде на неприродные аминокислоты (Massironi S, Zilli A, Conte D. Somatostatin analogs for gastric carcinoids: For many, but not all. World J Gastroenterol 2015; 21(22):6785-93). Применяемый в настоящее время в клинической практике структурный аналог соматостатина - октреотид - состоит из 8 аминокислот и имеет циклическое строение. Показаниями для применения октреотида являются опухоли островкового аппарата поджелудочной железы, рак поджелудочной железы, карциноидные опухоли, медуллярный рак щитовидной железы, аденомы гипофиза (Wolin ЕМ. The expanding role of somatostatin analogs in the management of neuroendocrine tumors. Gastrointest Cancer Res 2012; 5(5): 161-68; Crabtree JS. Clinical and Preclinical Advances in Gastroenteropancreatic Neuroendocrine Tumor Therapy. Front Endocrinol 2017;8:341).
Октреотид в виде раствора малопригоден для продолжительного лечения нейроэндокринных опухолей из-за необходимости частых инъекций (3-4 раза в день) (Anthony L, Freda PU. From somatostatin to octreotide LAR: evolution of a somatostatin analogue. Curr Med Res Opin 2009;25(12):2989-99).
В ФГБУ «НМИЦ онкологии им. H.H. Блохина» Минздрава России на протяжении ряда лет проводились исследования по поиску потенциальных противоопухолевых соединений в ряду аналогов гипоталамических гормонов, в частности аналогов соматостатина.
Известно средство, обладающее противоопухолевым действием, представляющее собой линейный пентапептид общей формулы:
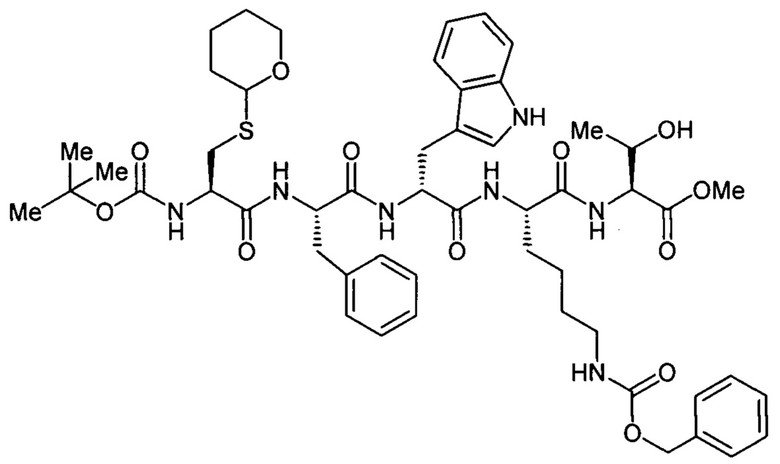
Метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина (Патент РФ RU 2254139 С1, опубликован 20.06.2005 г).
Это соединение обладает активностью на ряде опухолей мышей, экспрессирующих рецепторы к соматостатину. Создано средство для внутривенных инъекций, включающее метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина. Оно представляет собой липосомальный лиофилизат для приготовления раствора для инъекций, дополнительно содержащий фосфатидилхолин, холестерин и дистеароилфосфатидилэтаноламин пэгилированный-2000 и сахарозу (Патент РФ RU 2703533 С1, опубликован 21.10.2019 г. ).
Вышеуказанное средство может вводиться больным только в условиях стационара. К тому же в настоящее время в России отсутствует производство для выпуска липосомальных препаратов для парентерального применения. Поэтому с использованием вышеуказанного соединения метилового эфира Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина была создана лекарственная форма для неинвазивного введения в виде таблеток, дополнительно содержащих в составе лактозу, микрокристаллическую целлюлозу, крахмал, поливилпирролидон (повидон), тальк и стеарат магния. При проведении клинических исследований выявлено, что биодоступность пероральной лекарственной формы слишком низкая, что требует значительного увеличения дозы активного вещества - метилового эфира Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина. Это средство принято за Прототип (Михаевич Е.И, Яворская Н.П., Голубева И.С. и др. Исследование возможности создания лекарственной формы цифетрелина для перорального применения Российский биотерапевтический журнал. 2012; 11(1):3-6).
Прототип имеет следующие недостатки:
1. Неудобен в употреблении - единица лекарственной формы содержит малое количество активной субстанции (6 мг), что требует приема большого количества таблеток для достижения необходимой разовой дозы.
2. Единица лекарственной формы включает значительное количество лактозы, что приводит к выраженным побочным явлениям у пациентов с гиполактазией.
3. Технология производства таблеток прототипа включает дополнительную стадию гранулирования, что делает ее более сложной, требует дополнительного оборудования.
Целью изобретения является устранение описанных недостатков.
1. Поставленная цель достигается тем, что заявляемое средство для перорального применения в виде таблетки содержит активное вещество - метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина в количестве 0,04-0,1 г., дополнительно содержит в составе вспомогательные вещества, корректирующие технологические характеристики смеси для таблетирования.
2. Заявляемое противоопухолевое лекарственное средство для перорального применения представляет собой таблетки массой 0,250 г и содержит метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина в количестве 0,055-0,065 г
3. В качестве наполнителей и разрыхлителей могут быть использованы лактоза, микрокристаллическая целлюлоза, крахмал, повидоны, сахар свекловичный, сахар молочный, натрия хлорид, натрия гидрокарбонат, и др. В качестве наполнителей и разрыхлителей нами предложены крахмал картофельный и лактоза, как наиболее инертные вещества. Таким образом, заявляемое противоопухолевое лекарственное средство для перорального применения предлагает крахмал картофельный (0,1-0,2 г) и лактозу (0,005-0,03 г).
4. Вспомогательные вещества, корректирующие распадаемость таблеток. Вещества вводятся в таблетируемую массу для улучшения распадаемости таблеток в желудке или кишечнике. По характеру действия различают разрыхляющие вещества: набухающие, улучшающие растворимость; гидрофилизирующие; газообразующие. Экспериментальными исследованиями установлено, что для данной прописи наиболее подходят газообразующие вспомогательные вещества. В качестве таких веществ мы использовали лимонную кислоту и магния карбонат. При использовании вышеуказанных веществ распадаемость таблеток составляла 5-7 мин, что соответствовало требованиям ГФ 14 изд. (не более 15 мин).
5. Смазывающие вещества - вспомогательные вещества, позволяющие избежать залипания таблетируемой смеси на пресс инструмент. В качестве смазывающих веществ применяются жиры, жирные кислоты и их соли (стеариновая кислота, кальция и магния стеарат), углеводороды (вазелиновое масло) и некоторые высокомолекулярные соединения (твин-80, ПЭГ-4000), количество которых не должно превышать 1%. Находит применение также и тальк. Тальк обладает скользящим и одновременно смазывающим действием. В качестве таких веществ мы использовали опудривающию смесь, содержащую тальк и стеарат магния. Для наилучшего скольжения в опудривающую смесь добавляли крахмал. Таким образом, заявляемое противоопухолевое лекарственное средство для перорального применения содержит тальк (0,005-0,02), стеарат магния (0,001-0,01) и крахмал (0,005-0,01).
6. Таблетка по п. 1, массой 0,1-1,0 г должна быть с сохранением соотношения компонентов.
В процессе разработки лекарственной формы опытным путем установлены оптимальные соотношения компонентов для таблетки 0,250 г:
Пример 1.
Метилового эфира Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина - 0,055 г;
Крахмал - 0,163 г;
Лимонная кислота - 0,0046 г;
Магния карбонат - 0,0046 г;
Лактоза - 0,014 г;
Тальк - 0,007- г;
Стеарат магния - 0,0023 г
Пример 2.
Метилового эфира Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина - 0,060 г;
Крахмал - 0,155 г;
Лимонная кислота - 0,005 г;
Магния карбонат - 0,005 г;
Лактоза-0,015 г;
Тальк - 0,0075 г;
Стеарат магния - 0,0025 г
Пример 3.
Метилового эфира Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина - 0,065 г;
Крахмал - 0, 148 г;
Лимонная кислота - 0,0053 г;
Магния карбонат - 0,0053 г;
Лактоза - 0,016 г;
Тальк - 0,008 г;
Стеарат магния - 0,0027 г
Заявляемое средство получают следующим образом:
Метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина со вспомогательными веществами смешивают до получения однородного порошка. Затем опудривают опудривающей смесью, содержащую тальк, магния стеарат и крахмал. После опудривания, массу для получения таблеток просеивают для удаления излишка опудривающей смеси. Таблетируют, получая таблетки массой 0,250 г.
Таким образом, известные дополнительные вещества позволяют устранить вышеперечисленные недостатки.
Исследования биологической активности заявляемого средства для перорального применения.
Задача исследования: доказательство сохранения биологической активности заявляемого средства по сравнению с прототипом.
Работа выполнена на самках мышей - гибридов первого поколения F1(C57B1/6xDBA/2) массой 20-25 г. Мышей получали из экспериментально- биологической лаборатории (вивария) ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Все животные были здоровы, имели ветеринарный сертификат качества о состоянии здоровья. Мышей содержали в специальных, просторных клетках по 5 особей при температуре воздуха 20-23°С и относительной влажности 60-65% в условиях естественного освещения и принудительной вентиляции на подстилке из стружек лиственных пород деревьев, стерилизованных в сухожаровом шкафу. Для кормления животных использовали стандартный промышленный и сертифицированный брикетированный корм для грызунов с установленным сроком годности. Животные имели свободный доступ к корму и воде (Большаков О.П., Незнанов Н.Г., Бабаханян Р.В. Дидактические и этические аспекты проведения исследований на биомоделях и на лабораторных животных. Качественная клиническая практика. 2002;(1):58-61.).
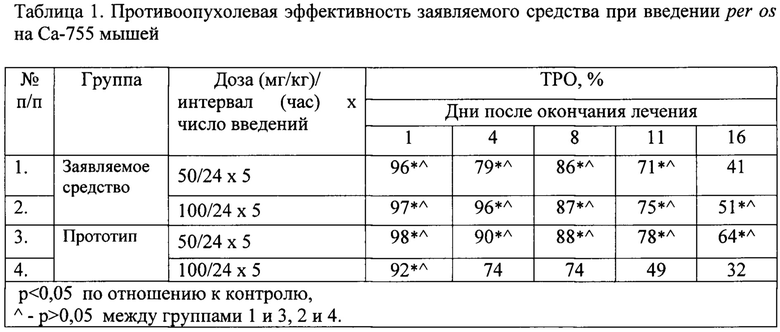
Исследования проведены на перевиваемой аденокарциноме молочной железы Са-755 мышей, экспрессирующей рецепторы к соматостатину. Штамм опухоли получен из Банка опухолевых штаммов ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Штамм Са-755 поддерживали подкожными перевивками на самках линейных мышей С57В 1/6. Для опыта Са-755 перевивали мышам-гибридам F1(C57B1/6xDBA/2) подкожно (п/к) в правую подмышечную область по 0,5 мл (50 мг) взвеси опухолевых клеток при разведении 1:10 в среде 199. Контрольная группа состояла из 10 мышей, опытная группа - из 7 животных. Лечение начинали через 48 ч после трансплантации опухолей (Экспериментальная оценка противоопухолевых препаратов в СССР и США / под ред З.П. Софьиной, А.Б. Сыркина, А.Голдина, А.Кляйна. М.: Медицина, 1980. С.71- 112.). Изобретение иллюстрируется таблицей 1, в которой представлены результаты изучения противоопухолевой эффективности заявляемого средства в зависимости от дозы в сравнении с прототипом на Са-755 мышей.
Проведение лечения.
Заявляемое средство и прототип вводили животным в испытуемых группах перорально ежедневно в течение 5 дней с интервалом 24 ч в разовых дозах 50 и 100 мг/кг. В связи с тем, что прототип и заявляемое средство нерастворимы в воде, взвесь препаратов готовили ex tempore в 30%-ном растворе коллидона с концентрацией действующего вещества 5 мг/мл. Взвесь с прототипом или заявляемым средством мышам вводили в желудок с помощью металлического зонда в объемах, соответствующих индивидуальным дозам для каждого животного.
Оценка эффективности лечения.
Критериями оценки противоопухолевой активности служили: торможение роста опухоли и увеличение продолжительности жизни подопытных животных по сравнению с контрольными животными (Руководство по проведению доклинических исследований. Часть первая / под редакцией А.Н. Миронова, ФГБУ НЦЭСМП Минздрава России. М., 2012. 944 с.
Торможение роста опухоли (ТРО, %) вычисляли по формуле:
ТРО (%) = (Vк-Vo)/Vк× 100, где (1)
Vк - средний объем опухолей в контрольной группе (мм3)
Vo - средний объем опухолей в опытной группе (мм3)
Увеличение продолжительности жизни (УПЖ, %) вычисляли по формуле:
УПЖ (%) = (СПЖо-СПЖк)/СПЖк×100, где (2)
СПЖк - средняя продолжительность жизни животных в контрольной группе (дни)
СПЖо - средняя продолжительность жизни животных в опытной группе (дни)
Изобретение иллюстрируется таблицей 1.
В таблице представлены результаты исследования противоопухолевой эффективности заявляемого средства в сравнении с прототипом на Са-755 мышей в дозах 50 и 100 мг/кг при пероральном пути введения ежедневно в течение 5-ти дней. Из данных таблицы 1 следует, что заявляемое средство в дозах 50 и 100 мг/кг оказывало высокий противоопухолевый эффект в виде ТРО=96-71% и ТРО=97-75% (р<0,05 по отношению к контролю), соответственно, в течение 11-ти дней после окончания лечения, в дозе 100 мг/кг минимальный противоопухолевый эффект сохранялся на уровне ТРО=51% (р<0,05) до 16-го дня наблюдения. При введении прототипа в дозе 50 и 100 мг/кг также наблюдался высокий противоопухолевый эффект в виде ТРО=98-64% (р<0,05 по отношению к контролю) до 16-го дня после окончания лечения. Прототип в дозе 100 мг/кг проявил высокий противоопухолевый эффект в виде ТРО=92-74% (р<0,05 по отношению к контролю) до 8-го дня наблюдения с сохранением минимального противоопухолевого эффекта ТРО=49% (р<0,05) до 11-дня наблюдения. Эффекта по критерию УПЖ не выявлено ни в одной из групп.
Таким образом, в результате проведенных исследований на аденокарциноме молочной железы мышей Са-755 установлено, что противоопухолевый эффект заявляемого средства идентичен противоопухолевому эффекту прототипа. В дозах 50 и 100 мг/кг при ежедневном пероральном введении в течение 5-ти дней заявляемое средство проявляет высокий длительный противоопухолевый эффект до 11-го и 16-го дней после окончания лечения в виде ТРО=96-71% и ТРО=97-75-51% (р<0,05 по отношению к контролю), соответственно, при введении прототипа в тех же дозах также наблюдается высокий противоопухолевый эффект в виде ТРО=98-64% и ТРО=92-74-49% (р<0,05 по отношению к контролю) до 16-го и 11-дней после окончания лечения, соответственно. Разница полученных значений ТРО в соответствующих группах лечения заявляемым средством и прототипом недостоверна (р>0,05 между группами), что показывает хорошую биологическую активность заявляемого средства.
Технический результат заявляемого средства заключаются в следующем:
1. Удобен в употреблении - необходимая доза действующего вещества в единице лекарственной формы (таблетки массой 0,250 г) увеличена в 10 раз.
2. В единице лекарственной формы уменьшено количество лактозы, что позволяет использовать лекарственное средство пациентами с гиполактазией.
3. Добавление к метиловому эфиру Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина известных вспомогательных веществ позволяет получить смесь, которая хорошо автоматически дозируется на любой имеющейся автоматической линии для производства таблеток.
4. Технология производства таблеток в отличие от прототипа, исключает стадию гранулирования, что делает ее более простой и значительно удешевляет производство.
5. Биологическая активность заявляемого средства эквивалентна прототипу.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство для лечения гормонозависимых опухолей и способ его получения | 2018 |
|
RU2703533C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2254139C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2007 |
|
RU2335284C1 |
| Средство для терапии опухолей | 2019 |
|
RU2726801C1 |
| ПРОТИВООПУХОЛЕВОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ИНГИБИТОР ТОПОИЗОМЕРАЗЫ I | 2022 |
|
RU2786727C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЭСТРОГЕНЗАВИСИМЫХ ОПУХОЛЕЙ | 2012 |
|
RU2510268C1 |
| ПРИМЕНЕНИЕ ТЕТРАНИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА С ТИОФЕНОЛОМ В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2007 |
|
RU2429242C2 |
| Способ получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина | 2020 |
|
RU2755572C1 |
| Низкотоксичная фармацевтическая композиция с противоопухолевой активностью в отношении холангиокарциномы | 2023 |
|
RU2825942C1 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
Изобретение относится к области медицины, а именно к противоопухолевым лекарственным средствам для перорального применения. Предлагаемое средство в форме таблетки содержит метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина и вспомогательные вещества: крахмал, лактозу, тальк, стеарат магния, магния карбонат и лимонную кислоту, при определенном количественном соотношении. Состав средства обеспечивает хорошее автоматическое дозирование на любой имеющейся автоматической линии для производства таблеток, при этом технология производства исключает стадию гранулирования. Средство удобно в употреблении, поскольку содержит необходимую дозу действующего вещества в единице лекарственной формы, может применяться амбулаторно. Низкое количество лактозы позволяет использовать лекарственное средство пациентами с гиполактазией. Заявляемое средство показывает высокую биологическую активность, которая эквивалентна прототипу. 1 з.п. ф-лы, 1 табл., 3 пр.
1. Противоопухолевое лекарственное средство для перорального применения в форме таблетки, содержащей метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина и вспомогательные вещества, включающие крахмал, лактозу, тальк и магния стеарат, отличающееся тем, что дополнительно содержит вспомогательные вещества, влияющие на распадаемость таблеток, такие как лимонная кислота и магния карбонат, при следующем соотношении компонентов для таблетки массой 0,250 г:
Метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина - 0,060 г;
Крахмал - 0,155 г;
Лимонная кислота - 0,005 г;
Магния карбонат - 0,005 г;
Лактоза - 0,015 г;
Тальк - 0,0075 г;
Стеарат магния - 0,0025 г
или
Метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина - 0,055 г;
Крахмал - 0,163 г;
Лимонная кислота - 0,0046 г;
Магния карбонат - 0,0046 г;
Лактоза-0,014 г;
Тальк - 0,007- г;
Стеарат магния - 0,0023 г
или
Метиловый эфир Nα-трет-бутилоксикарбонил-S-тетрагидропиранилцистеинил-фенилаланил-D-триптофил-Nε-бензил-оксикарбонил-лизилтреонина - 0,065 г;
Крахмал - 0, 148 г;
Лимонная кислота - 0,0053 г;
Магния карбонат - 0,0053 г;
Лактоза - 0,016 г;
Тальк - 0,008 г;
Стеарат магния - 0,0027 г.
2. Противоопухолевое лекарственное средство для перорального применения по п. 1 в виде таблетки массой 0,1-1,0 г с сохранением соотношения компонентов.
| МИХАЕВИЧ Е.И | |||
| и др | |||
| Исследование возможности создания лекарственной формы цифетрелина для перорального применения | |||
| Российский биотерапевтический журнал, 2012, N | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| CN 104667258 A, 03.06.2015 | |||
| US 4261885 A, 14.04.1981 | |||
| ВОСКОБОЙНИКОВА И.В | |||
| и др | |||
| Современные вспомогательные вещества в производстве таблеток | |||
| Использование | |||
Авторы
Даты
2021-06-02—Публикация
2020-08-06—Подача