Изобретение относится к фармацевтической химии, в частности к созданию лекарственных средств пептидной природы, обладающих противоопухолевым действием, и может быть использовано для лечения опухолей, в том числе эндокринных и гормонозависимых.
В современной практике противоопухолевой химиотерапии используется весьма широкий арсенал лекарственных средств, таких как алкилирующие вещества, антиметаболиты, противоопухолевые антибиотики, гормональные препараты и их антагонисты, ферменты. Широко применяют цитостатики сарколизин, циклофосфан, миелосан, производные нитрозометилмочевины, из антиметаболитов - метотрексат, меркаптопурин, фторурацил, фторафур, среди противоопухолевых антибиотиков - дактиномицин, рубомицин, доксорубицин, карминомицин и другие.
Для лечения гормонозависимых опухолей часто используют гормональные препараты, в частности андрогены, эстрогены, кортикостероиды, и антагонисты гормонов. Так, для лечения рака предстательной железы применяют эстрогены, так как в этом случае показано подавление действия в организме андрогенов или усиление активности эстрогенов. Андрогены используют, когда показано повышение активности андрогенов или уменьшение активности эстрогенов, например при раке молочной железы.
Для лечения злокачественных лимфом и острых лейкозов используют глюкокортикоиды.
В современной медицинской онкологической практике для лечения гормонозависимых опухолей используют такие препараты, как анастрозол, мегестрол, медроксипрогестерон, тамоксифен, флутамид и другие (РЛС Россия, Энциклопедия лекарств, выпуск 9, 2002 год). Однако упомянутые лекарственные средства, помимо серьезных побочных явлений, имеют и абсолютные противопоказания, такие как нарушение функции печени и почек, тромбофлебит, заболевания щитовидной железы и сердца, детский возраст, беременность.
В последние десятилетия ведется активный поиск противоопухолевых лекарственных средств пептидной природы, проявляющих высокую специфическую активность и в то же время не имеющих серьезных противопоказаний.
Известна фармацевтическая композиция, обладающая противоопухолевым действием, содержащая β-гептилгликозид-N-ацетилмурамил-L-аланил-D-изоглутамина в липосомальной форме для перорального и внутривенного введения (патент RU 2121363, 1997 г.), композиция обладает низкой токсичностью.
Известно противоопухолевое средство, представляющее собой комплексный препарат производных гематопорфирина и фактора некроза опухоли альфа в определенном молярном соотношении (Патент RU 2136278, 1998), средство обладает невысокой токсичностью.
Известен пентапептид, обладающий противоопухолевой активностью в форме гидрохлорида M2Val-Val-MVal-Pro-Pro-NH-Bzl НСl, где М - металл, Bzl - бензил (патент RU 2153504, 1995).
Известно противоопухолевое средство, представляющее собой нетоксичный гексапептид формулы Leu-Val-Val-Tyr-Pro-Trp (патент RU 2067870, 1993).
Известен фармацевтический состав на основе пептидов, обладающий антипролиферативным действием в отношении опухолей (патент RU 2156774, 1995).
Все более широкое применение в клинической терапии опухолей, особенно эндокринных опухолей, находит сандостатин, препарат на основе циклического октапептида, выпускаемый фирмой «Сандос» (Н.Ф.Орел и др., ж. «Современная онкология», т.2, №1, 2000).
По фармакологическому спектру действия и специфической противоопухолевой активности сандостатин является наиболее близким к заявляемому средству, поэтому выбран заявителем в качестве прототипа.
Задачей настоящего изобретения является создание отечественного противоопухолевого средства, обладающего высоким терапевтическим эффектом, широким спектром противоопухолевого действия и низкой токсичностью.
Поставленная задача решается тем, что предложено средство, обладающее противоопухолевым действием, представляющее собой пептид общей формулы:
 , где
, где
R - трет-бутилоксикарбонил, R1 - тетрагидропиранил, R2-Nε - бензилоксикарбонил, R3, - метил (I);
R-Н, R1 - тетрагидропиранил, R2-Nε - бензилоксикарбонил, R3 - метил (II);
R-Н, R1-H, R2-Н, R3 - метил (III);
R - трет-бутилоксикарбонил, R1 - тетрагидропиранил, R2-Nε - бензилоксикарбонил, R3-S - тетрагидропиранилцистеина метиловый эфир (IY).
Технический результат, получаемый при использовании изобретения, выражается в расширении арсенала противоопухолевых средств, снижении токсичности, повышении терапевтического эффекта.
Синтез заявляемого средства проводили классическими методами пептидной химии. Для блокирования боковой цепи лизина применяли карбобензилокси (Z) группу, цистеина - тетрагидропиранильную (Thp), a для временной защиты Nα-функций трет-бутилоксикарбонильную (Воc) группы.
Для повышения устойчивости к тканевым ферментам в состав пептидов введена неприродная аминокислота D-триптофан.
Полученные пептиды были охарактеризованы углом оптического вращения и данными элементного анализа, тонкослойной хроматографией, высокоэффективной жидкостной хроматографией, данными ЯМР-спектроскопии и аминокислотного анализа.
Изобретение поясняется следующими примерами
Пример 1
В качестве примера приводится синтез гидрохлорида метилового эфира S-тетрагидропиранилцистеинилфенилаланил-D-триптофил-Nε-карбобензоксилизилтреонина
HCl·H-Cys(Thp)-Phe-D-Trp-Lys(Z)-Thr-OMe (II)
Пентапептид (II) получали удалением Вос-защитной группы с пентапептида (I) 3,4 N НСl в этилацетате при комнатной температуре в течение 20 минут. В этих условиях не наблюдалась побочная реакция отщепления Z-группы с Nε-функции лизина. Выход (II) составил 98%.
Пример 2
Пептид, полученный по описанному способу, был испытан на адекватных моделях: аденокарциноме предстательной железы Даннинга крыс Copenhagen и раке молочной железы РМ-1 на бестимусных мышах. В эксперименте на крысах препарат вводили в дозе 100 мкг/кг в течение 30 дней, на мышах также в дозе 100 мкг/кг в течение 21 дня.
Как показали экспериментальные данные, пептид проявляет равный противоопухолевый эффект на аденокарциноме предстательной железы Даннинга R3327-H крыс и раке молочной железы РМ-1 бестимусных мышей. Пептид тормозит рост этих опухолей на 63-65%.
Экспериментально было установлено, что заявляемое средство обладает широким спектром противоопухолевого действия, а именно эффективно на перевиваемых опухолях: аденокарцинома молочной железы Са-755, меланома В-16, аденокарцинома легкого Льюис LLC, аденокарцинома предстательной железы Даннинга R-3327-H, рак молочной железы РМ-1 бестимусных мышей и ДМБА - индуцированных опухолях молочной железы.
Были проведены испытания заявленного средства.
1. Изучение токсичности.
2. Изучение специфической противоопухолевой активности.
1. Исследование токсичности заявляемого средства соединений I, II, III, IY проводили на мышах-гибридах BDF1 и беспородных крысах-самках. Все соединения не проявляют токсического действия на мышах в разовых дозах 60-80 мг/кг (суммарная доза 300-400 мг/кг). При пересчете на человека ежедневная доза составляет 300000-400000 мкг, что в 50-65 раз превышает применяемые при неоперабельном раке поджелудочной железы высокие дозы сандостатина (6000 мкг/сут). На беспородных крысах все соединения также не проявляют токсического действия при курсовой дозе 6000 мкг/кг.
Представленные данные показывают, что заявляемое средство не проявляет токсичность при использовании даже в высоких дозах.
2. Изучение противоопухолевой активности проводили на адекватных моделях. Критерием эффективности лечения служило торможение роста опухоли (ТРО). Противоопухолевую активность изучали на аденокарциноме предстательной железы Даннинга 3327-Н крыс Copenhagen. Данные представлены в таблице 1.
Как видно из таблицы 1, соединения I, III, IY на аденокарциноме предстательной железы Даннинга R3327-H крыс проявляют противоопухолевое действие: соединение I тормозит рост опухоли на 55%, соединение III - на 66%, соединение IY - на 46%.
Противоопухолевую активность заявляемого средства изучали на ДМБА-индуцированных опухолях молочной железы крыс в сравнении с сандостатином. Изучаемые препараты вводили подкожно в дозе 100 мкг/кг в течение 30 дней. Данные представлены в таблице 2.
Как видно из таблицы 2, все соединения проявляют высокий противоопухолевый эффект. Терапевтический эффект соединения I составляет 91% ТРО. У соединения III максимальный терапевтический эффект равен 75% ТРО, у соединения IY - 79% ТРО, а у сандостатина - 68% ТРО.
Противоопухолевую активность заявляемого средства изучали также на бестимусных мышах с подкожно перевитым раком молочной железы РМ-1 в сравнении с сандостатином. Соединение вводили подкожно в дозе 100 мкг/кг в течение 21 дня. Данные представлены в таблице 3. Как видно из данных таблицы 3, на фоне введения соединений максимальный терапевтический эффект составил для соединения I - 47% ТРО, для соединения II - 63% ТРО и превышал противоопухолевое действие сандостатина (39% ТРО). Непосредственно после окончания лечения терапевтический эффект сохранялся и составил для соединения I - 45% ТРО, для соединения II - 55% ТРО, для сандостатина - 40% ТРО.
В эксперименте показан статистически достоверный противоопухолевый эффект заявляемого средства на перевиваемых гормононезависимых опухолях: аденокарциноме молочной железы Са-755, аденокарциноме легкого Льюис LLC и меланоме В-16
Изучаемые препараты вводили в дозах 60-80 мг/кг подкожно в течение 5 дней.
Данные представлены в таблице 4. Как следует из данных таблицы 4, максимальное ТРО на аденокарциноме молочной железы Са-755 составляет 91%, на аденокарциноме легкого Льюис - 97% и на меланоме В-16 - 85%.
Таким образом, заявленное средство обладает высоким противоопухолевым эффектом на широком спектре опухолей, в том числе гормонозависимых, и низкой токсичностью, что позволит ему занять достойное место в онкологической практике.
Противоопухолевая активность соединений I, III, IV на аденокарциноме предстательной железы Даннинга 3327 Н крыс Copenhagen
** - р<0,05
Противоопухолевая активность соединений I, III, IV на ДМБА-индуцированных опухолях молочной железы крыс в сравнении с сандостатином
** - р<0,05
Индукция опухолей осуществлялась четырехкратным еженедельным внутривенным введением ДМБА (диметилбензантрацен) в водно-жировой эмульсии в суммарной дозе 8 мг на крысу.
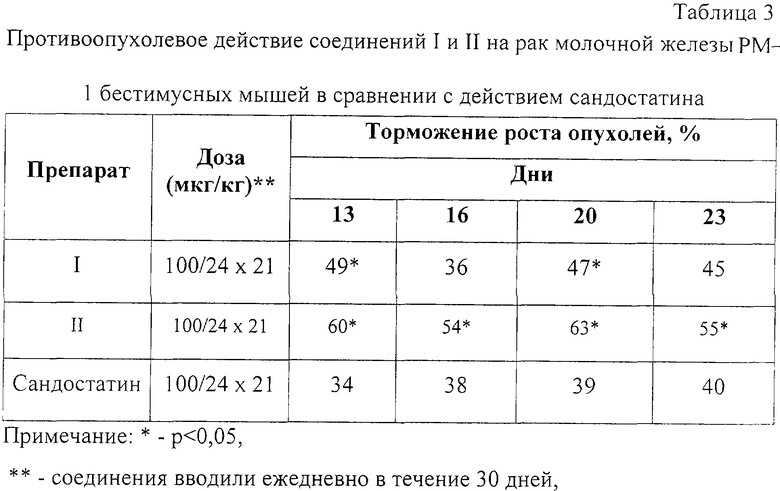
Противоопухолевая активность соединений I, III, IV на перевиваемых опухолях мышей
** - р<0,05
ЛИТЕРАТУРА
1. Romy Lea Topper, Pharm D.Ocreotide: Drug review and clinical indications. The cancer bulletin, 1989, 41, 5, 334-335.
2. Гарин А.М. Принципы и возможности современной эндокринной терапии опухолей. М., 2000, 82-85.
3. Agthony L.B., Krozely M.G., Jonhson D.H., Shaff M.I., Hande K.R., Oates J.A.Somatuline is antitumor efficacy and phase I trial in neuroendocrine tumors. Proc. Annu Meet Am Soc Clin Oncol, 1992, 11:А484.
4. Jean-Christophe Souget. Long-acting somatostatin analogues in pancreatic islet cell carcinoma. Horm. Res., 1989, 32, 74-76.
5. Weckbecker G., Raulf F., Stolz В., Bruns С. Somatostatin analogs for diagnosis and treatment of cancer. Pharm. Ther. Vol. 60, p. 245-264, 1993.
6. Cavanac et al. Somatostatin analogue composition and in treating beastm cancer U.S.P.
7. Н.Ф.Орел, Т.Н.Лопаткина. Возможности применения сандостатина у онкологических больных. Современная онкология, 2, 1, 2000.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство для лечения гормонозависимых опухолей и способ его получения | 2018 |
|
RU2703533C1 |
| Противоопухолевое лекарственное средство для перорального применения | 2020 |
|
RU2748989C1 |
| 3-OR-ДИ-(2-ХЛОРЭТИЛ)АМИНОСОДЕРЖАЩИЕ αАЦИЛ(ГИДР)ОКСИСТЕРОИДЫ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1998 |
|
RU2139292C1 |
| НОВЫЕ ПРОТИВООПУХОЛЕВЫЕ СОЕДИНЕНИЯ | 2003 |
|
RU2356908C2 |
| Пептид, обладающий противоопухолевой и антиметастатической активностью, и готовая лекарственная форма на его основе | 2018 |
|
RU2682039C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 1999 |
|
RU2144821C1 |
| ПЕПТИД С АНТИПРОЛИФЕРАТИВНОЙ АКТИВНОСТЬЮ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2446174C2 |
| ДЕКАПЕПТИД, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2084458C1 |
| ВЫСОКОЭФФЕКТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОЙ ФОРМЫ АДРЕСНОГО ДЕЙСТВИЯ ДЛЯ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2019 |
|
RU2727924C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ РАКА | 2006 |
|
RU2328294C1 |
Изобретение относится к фармацевтической химии, в частности к созданию лекарственных средств пептидной природы, обладающих противоопухолевым действием, и может быть использовано для лечения опухолей, в том числе эндокринных и гормонзависимых. Средство представляет собой пептид общей формулы:
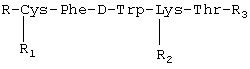
Изобретение обеспечивает повышение терапевтического эффекта, снижение токсичности. 2 з.п. ф-лы, 4 табл.
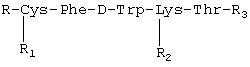 , где
, где
R - трет-бутилоксикарбонил или Н,
R1 - тетрагидропиранил или Н,
R2-Nε - бензилоксикарбонил или Н,
R3 - O-метил или S-тетрагидропиранилцистеина метиловый эфир.
| Н.Ф.Орел и др | |||
| Ж | |||
| «Современная онкология», т.2, №1, 2000 | |||
| ТЕРАПЕВТИЧЕСКИЕ ПЕПТИДЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1989 |
|
RU2088592C1 |
| ПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2146262C1 |
| АЛЛОФЕРОНЫ-ИММУНОМОДУЛИРУЮЩИЕ ПЕПТИДЫ | 1999 |
|
RU2172322C1 |
| DE 10147056, 12.12.2002 | |||
| US 5741892,.21.04.1998. | |||
Авторы
Даты
2005-06-20—Публикация
2003-11-14—Подача