Область техники, к которой относится изобретение
Настоящее изобретение относится к улучшенному золь-гель-способу производства аэрогелей диоксида кремния. Способ предпочтительно осуществляют исходя из материала растительного исходного сырья, в частности, из зол от рисовой соломы и рисовой шелухи, которая содержит относительно большие количества диоксида кремния, что, таким образом, обеспечивает также и дополнительное преимущество, заключающееся в отправлении при производстве на рецикл подходящего для использования материала, который в противном случае должен был бы быть утилизирован другим образом.
Уровень техники
Аэрогели представляют собой материалы, состоящие из твердой структуры, характеризующейся очень высокой пористостью. Хотя они могут состоять из оксидов различных металлов или металлоидов или их смесей, безусловно наиболее широко распространенными и промышленно важными аэрогелями являются аэрогели диоксида кремния; поэтому в настоящем изобретении внимание будет обращено на аэрогели диоксида кремния, но при использовании способов, описанных в настоящем документе, также могут быть получены и аэрогели, образованные смешанными оксидами, содержащие диоксид кремния в качестве основного компонента и характеризующиеся доходящими вплоть до 45 % уровнями процентного содержания оксидов других металлов, обычно трех-, четырех- или пятивалентных.
Аэрогели диоксида кремния представляют собой твердые вещества, у которых большую часть объема, доходящую вплоть до более, чем 99 %, занимает газ (обычно воздух), и только оставшаяся доля объема состоит из твердого материала; вследствие своей структуры данные материалы могут характеризоваться плотностью в несколько миллиграммов при расчете на один см3 и значениями площади поверхности в диапазоне от нескольких сотен до приблизительно 1000 м2/г. Вследствие демонстрации данных характеристик аэрогели разрабатывают и используют для некоторых конкретных научных областей применения (таких как поглотители частиц из объемного источника), в качестве катализаторов или носителей катализаторов, а главным образом в качестве теплоизоляторов вследствие их очень низкой теплопроводности (от 0,004 Вт/м-К до 0,03 Вт/м-К).
Аэрогели диоксида кремния производят при использовании способов, называемых золь-гель-способами.
Существуют многочисленные варианты золь-гель-способов, которые, однако, демонстрируют определенные общие характеристики. В данных способах одно или несколько соединений кремния (определяемых в промышленности как предшественники) растворяют в воде или водно-спиртовых смесях, получая раствор, называемый «золем»; после этого соединения, присутствующие в золе вступают в реакцию, в общем случае благодаря дестабилизации системы в результате изменения значения рН, что в результате приводит к получению влажного «геля»; затем гель высушивают в соответствии с различными способами, получая сухой гель.
Говоря более конкретно, в водном или водно-спиртовом растворе предшественник претерпевает реакцию начального гидролиза, при которой одна или несколько гидроксильных групп связываются с атомом кремния; формально реакция может быть записана следующим образом:
Предшественник + 4 Н2О ? 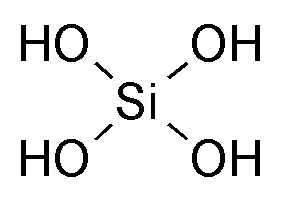
Соединения, полученные в результате гидролиза предшественника, обычно определяют как ортокремниевую кислоту; собственно говоря, как и в случае гидрокси-соединений других неметаллов, они представляют собой амфотерные соединения, чья формула может быть записана в виде H4SiO4, в соответствии с правилами записи формулы кислотных соединений или в виде Si(OH)4, что более часто встречается в области золь-гель-способов.
Ортокремниевую кислоту наблюдали только в высокоразбавленных растворах, поскольку она является чрезвычайно нестабильной и самопроизвольно стимулирует прохождение реакции конденсации, схематически представленной ниже:
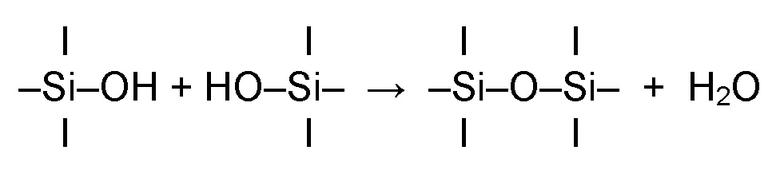
Данная реакция, повторенная для всех четырех групп -ОН, присутствующих на каждом атоме кремния, (поликонденсация) приводит к формированию трехмерного рисунка связей Si-O-Si, а после этого к получению оксидной структуры материала.
Предшественники, использующиеся в золь-гель-способах, могут быть металлоорганическими, такими как соединения, представляющие собой тетраметилортосиликат и тетраэтилортосиликат (описывающиеся формулами Si(OCH3)4 и Si(OC2H5)4, соответственно, которые обычно обозначают как TMOS и TEOS); или неорганическими, в числе которых наиболее широко распространенными предшественниками являются растворы силикатов щелочных металлов, описывающиеся общей формулой M2O x nSiO2 (M = Na, K, Li), где n находится в диапазоне от 0,5 до 4; данная общая формула включает как стехиометрические соединения, такие как силикат натрия, Na2SiO3 (n = 1), так и нестехиометрические композиции. Несмотря на широкое исследование и использование для научных областей применения золь-гель-способов исходя из металлоорганических предшественников стоимость данных соединений делает их неподходящими для использования в крупномасштабных областях применения.
Поэтому настоящее изобретение направлено на производство аэрогелей исходя из растворов силикатов щелочных металлов, которые могут быть произведены исходя из химических соединений или в качестве побочных продуктов химических способов или из растительного материала, содержащего большие количества кремния, такого как некоторые побочные продукты переработки риса.
Непосредственный продукт поликонденсации представляет собой влажный «гель», где рисунок вышеупомянутых связей Si-O-Si образует открытую структуру, которая содержит растворитель и побочные продукты реакции в своей пористости. Влажный гель обычно подвергают стадии промывания для устранения побочных продуктов (в частности, если исходить из неорганических предшественников) и любых растворимых примесей и/или замены исходного растворителя на другую жидкость в целях облегчения проведения последующих операций высушивания.
Высушивание влажного геля может быть проведено в результате простого выпаривания жидкости, содержащейся в порах, (при получении, таким образом, сухих гелей, называемых «ксерогелями») или в результате экстракции упомянутой жидкости в сверхкритических условиях, что в результате приводит к получению так называемых «аэрогелей».
Несмотря на более простое практическое осуществление выпаривания ксерогели обычно подвергаются значительному уменьшению объема в сопоставлении с исходными влажными гелями (при достижении объемов, составляющих приблизительно 1/8 в сопоставлении с объемом влажного геля) и обширным разрушениям в ходе осуществления способа, и, с точки зрения распределения пор, они характеризуются морфологией, совершенно отличной от исходной.
С другой стороны, гиперкритическое высушивание делает возможным получение целостных аэрогелей, называемых в промышленности монолитными, которые сохраняют форму и размер исходного влажного геля, но в особенности морфологию и распределение пор: данная последняя характеристика требуется для некоторых из вышеупомянутых областей применения, в частности, для тепло-, звуко- и электроизоляции.
Как это утверждалось выше, наиболее широко распространенным силикатом, использующимся в золь-гель-способах, является силикат натрия вследствие его низкой стоимости, широкой доступности, растворимости в воде и нетоксичности; поэтому в остальной части описания изобретения внимание будет обращено на данное соединение, полученное из растительных матриц, но изобретение в общем случае является применимым исходя из силикатов щелочных металлов, полученных любым образом.
Растворы силиката натрия характеризуются сильно основным значением рН; конденсацию золей, образованных из данных растворов, в общем случае получают или ускоряют в результате варьирования значения рН при доведении его от исходных значений (приблизительно 13 – 14) до значений в общем случае в диапазоне от 4 до 10 в результате добавления кислоты.
Способы, относящиеся к данному типу, описываются в нескольких документах, в том числе, например:
- патентная заявка CN 1449997, где к золю силиката натрия (который может иметь концентрацию в диапазоне от 0,01 до 1 кг/л) добавляют HCl вплоть до достижения значения рН в диапазоне от 5 до 9;
- патент CN 1317188 C, где к золю силиката натрия (имеющему концентрацию в диапазоне от 0,02 до 0,05 кг/л) добавляют HCl вплоть до достижения значения рН в диапазоне от 6 до 8;
- патент US 6210751 B1, где золь силиката натрия, характеризующийся сильно основным значением рН, перепускают на кислотной ионообменной смоле для удаления натрия или, в альтернативном варианте, в раствор силиката выливают кислоту для отделения после этого получающегося в результате осадка (Na2SO4) при охлаждении системы в целях достижения эффективного осаждения. В обоих случаях достигают значений рН, составляющих менее, чем 4, в золе, получающемся в результате обработки, к которому после этого добавляют основание (обычно NaOH) для доведения значения рН до значения, составляющего приблизительно 4,7;
- патент ЕР 1689676 B1, где рисовую шелуху подвергают термической обработке при 700°С вплоть до получения золы, которую возможно подвергают предварительному промыванию при использовании серной кислоты; золу подвергают обработке при использовании NaOH, получая, таким образом, золь силиката натрия, к которому добавляют серную кислоту, и после «старения» геля его промывают при использовании воды для удаления получающейся в результате соли Na2SO4; в заключение воду в геле при использовании методики с колонкой Сокслета заменяют на спирт (обычно этанол), который в заключение экстрагируют в сверхкритических условиях;
- патентная заявка WO 2005/044727 А1, где к раствору, содержащему Na2O и SiO2 при молярном соотношении в диапазоне от 1 : 3 до 1 : 4 и от 1 до 16% (масс.) SiO2, примешивают концентрированную серную кислоту (раствор при 96% (масс.); конечное полученное значение рН не указывается);
- статья «Rice husk ash as a renewable source for the production of value added silica gel and its application: an overview», R. Prasad et al., Bulletin of Chemical Reaction Engineering & Catalysis, 7 (1), 2012, 1 – 25;
- статья «A simple process to prepare silica aerogel microparticles from rice husk ash», R. S. Kumar et al., International Journal of Chemical Engineering and Applications, Vol. 4, No. October 5, 2013;
- и статья «Preparation of silica aerogel from rice hull ash by supercritical carbon dioxide drying», Qi Tang et al., J. of Supercritical Fluids 35 (2005) 91 – 94.
В данных трех статьях к растворам Na2O и SiO2, имеющим концентрацию, составляющую приблизительно 0,03 кг/л и полученным в результате растворения предшественника SiO2 при использовании раствора NaOH с концентрацией 1 моль/л, примешивают раствор HCl, в свою очередь, обычно с концентрацией 1 моль/л, вплоть до получения значения рН в диапазоне приблизительно от 6 до 7.
Данные известные способы приводят к появлению двух типов проблем.
Во-первых, при добавлении кислоты в основный раствор силиката создаются градиенты значений рН, которые могут привести к появлению структурной неоднородности в конечном геле.
Во-вторых, и это более важно, в ходе протекания стадии гелеобразования (начинается при приблизительно рН 10) наблюдается сохранение щелочных металлов вследствие слабой кислотности диоксида кремния в пористости, которая образуется после поликонденсации: они должны быть полностью удалены из влажного геля в целях предотвращения нежелательных последствий для конечного аэрогеля, таких как тенденция к превращению в плотное стекло уже при относительно низких температурах (таких как 600 – 700°С в случае натрия в зависимости от уровня содержания элемента).
Однако удаление щелочных и щелочноземельных элементов из влажных гелей представляет собой продолжительную операцию, принимая во внимание очень малый размер их пористости; в целях преодоления данной проблемы, как это известно, для растворов силиката натрия перед гелеобразованием проводят обработки при использовании ионообменных смол в целях замены щелочного иона (например, Na+) на Н+ или отделения солей, полученных в результате осаждения при добавлении кислоты. Данные операции увеличивают требуемое время и сложность и поэтому стоимость совокупного способа. Ионообменные обработки описываются, например, на странице 50 (chapter 3, paragraph 3.2.1) книги «Advances in Sol-Gel Derived Materials and Technologies», edited by M. A. Aegerter and M. Prassas, и одним примером данных обработок для удаления натрия является способ, описанный в публикации US 6210751 B1.
В патентной заявке CN 102757059 A следуют отчасти другому способу, в сопоставлении с предшествующими документами. Методика подобна методике из патента ЕР 1689676 В1, но раствор силиката натрия добавляют к раствору кислоты при регулировании добавления таким образом, чтобы добиться достижения конечного значения рН в диапазоне от 3 до 4. В целях эффективного отделения осажденных солей от геля его подвергают электрофоретической обработке при его введении в контейнер, заполненный водой, и приложении электрического поля к системе при использовании двух электродов, погруженных в воду, окружающую гель, таким образом, чтобы положительные ионы были бы извлечены из геля и притянуты к отрицательному электроду. Как это проверили авторы настоящего изобретения, в дополнение к усложнению способа, состоящему из данной дополнительной стадии, очень трудно регулировать значение рН системы при доведении его до значений в диапазоне от 3 до 4, и при данных значениях рН гелеобразование происходит на чрезмерно ранней стадии способа (приблизительно в течение двух минут после смешивания растворов), что приводит к получению неравномерной системы, в которой в объеме все еще жидкой фазы наблюдаются флокирующиеся фрагменты геля.
Поэтому в данной области все еще ощущается потребность в наличии способа получения аэрогелей диоксида кремния исходя из продуктов, имеющих приемлемые в промышленности стоимости, который свободен от недостатков и усложнений известных способов.
Раскрытие изобретения
Цель настоящего изобретения заключается в предложении улучшенного золь-гель-способа производства аэрогеля диоксида кремния, включающего стадии:
- получения водного раствора силиката щелочного металла;
- отдельного получения в контейнере концентрированного раствора неорганической кислоты, выбранной из серной, хлористо-водородной, азотной и фосфорной кислоты;
- объединения указанных растворов силиката и кислоты;
- выдерживания системы в состоянии покоя вплоть до формирования влажного геля;
- промывания только что произведенного влажного геля при использовании воды для замены после этого жидкой фазы, присутствующей в его порах, на жидкое летучее органическое соединение (ЛОС), а затем, возможно, на жидкий диоксид углерода;
- высушивания геля в результате экстракции в гиперкритических условиях упомянутого жидкого органического летучего соединения;
отличающегося тем, что упомянутую стадию объединения указанных растворов силиката и кислоты проводят в результате выливания раствора силиката в раствор кислоты, причем указанную операцию проводят таким образом, чтобы значение рН системы всегда оставалось бы меньшим, чем 1, а предпочтительно составляющим приблизительно 0 или менее.
Как это упоминалось выше, способ настоящего изобретения отличается от известных способов методами получения раствора, который подвергают гелеобразованию.
Во-первых, в противоположность тому, что обычно осуществляют во всех известных способах, в данном случае раствор силиката выливают в раствор кислоты: данным образом силикат всегда имеет значение рН, составляющее менее, чем 1, и не возникают сильные различия значений рН, которые имеют место при выливании кислоты в раствор силиката, (ситуация, при которой область добавления кислоты характеризуется значением рН, близким к 0, а более удаленные области раствора силиката характеризуются исходным значением рН, в общем случае составляющем более, чем 13), что становится причиной неравномерности конечного геля.
Во-вторых, согласно наблюдениям изобретателей гелеобразованию, которое имеет место в случае системы, постоянно выдерживаемой при значении рН, составляющем менее, чем 1, свойственно преимущество, заключающееся в том, что данное гелеобразование протекает медленнее, чем гелеобразование, которое имеет место при основных условиях, и поэтому является легче регулируемым (при отсутствии необходимости охлаждения системы, как в способе из патента US 6210751) и демонстрирует легкую применимость в промышленности; кроме того, в случае гелеобразования из основного раствора он первоначально содержит избыток щелочного металла (такого как Na+ или К+, которые вводятся в качестве противоионов гидроксильному иону), удаление которого, как это упоминалось выше, требует продолжительного времени, в то время как растворы кислоты настоящего изобретения содержат в качестве противоиона иону Н+ анионы, такие как Cl– или NO3–, удаление которых из влажного геля происходит быстрее и легче и может быть осуществлено в результате простого промывания при использовании воды.
Данные и другие преимущества становятся более очевидными после ознакомления со следующим далее подробным описанием изобретения.
Краткое описание чертежей
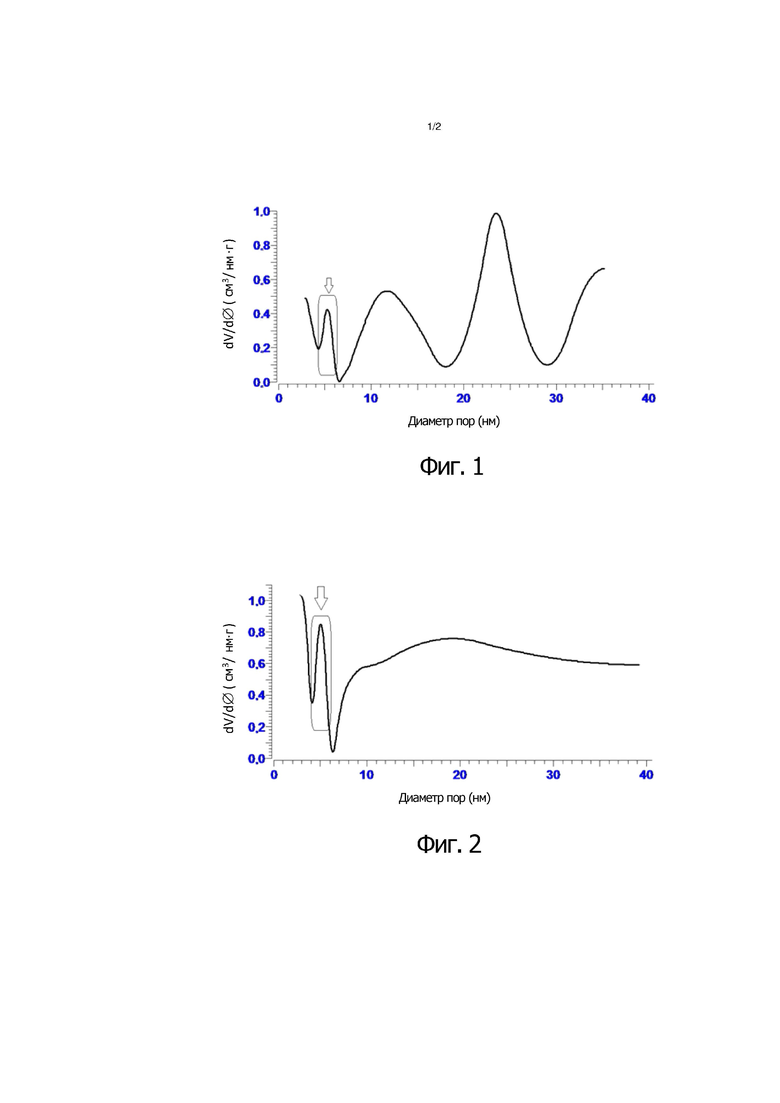
- Фигуры 1 и 2 демонстрируют распределение пористости для двух аэрогелей, произведенных в соответствии с изобретением;
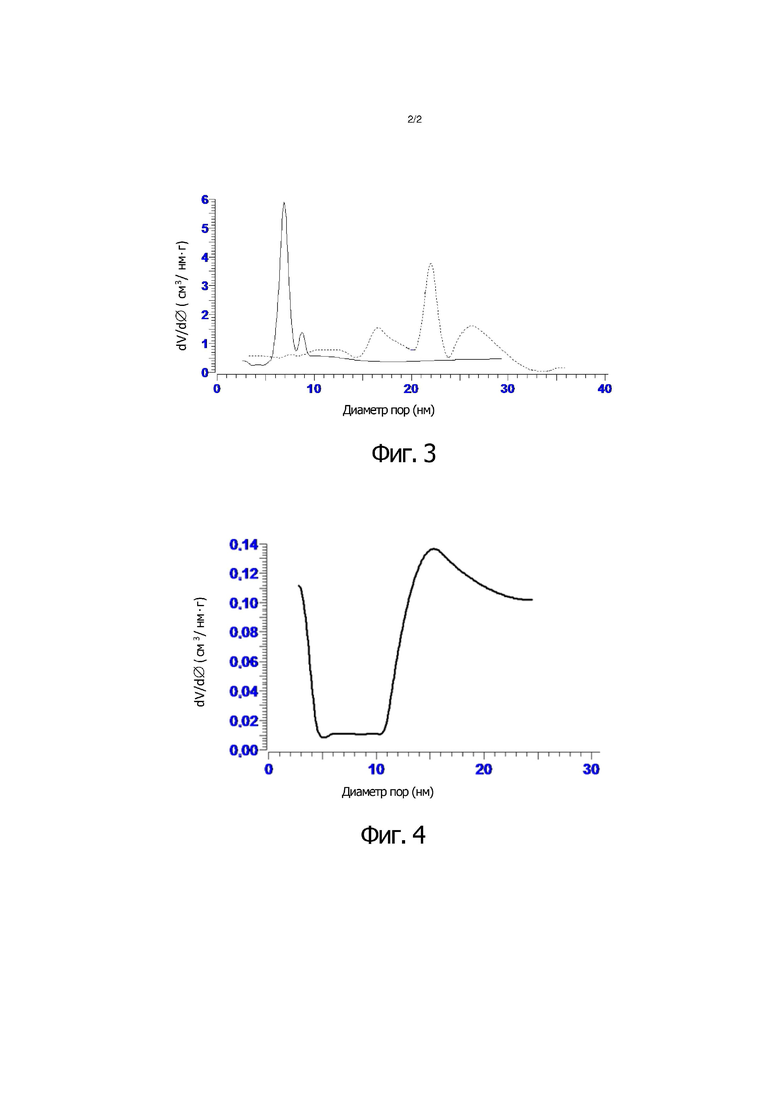
- Фигуры 3 и 4 демонстрируют распределение пористости для двух аэрогелей, произведенных в соответствии со способами предшествующего уровня техники.
Осуществление изобретения
Реагенты, использующиеся в способе изобретения, а также рабочие условия на определенных стадиях подобны реагентам и условиям на подобных стадиях способов предшествующего уровня техники и поэтому описываются ниже в настоящем документе кратко; отличительные рабочие условия и приемы настоящего изобретения будут описываться подробно. В качестве предшественника кремния в настоящем изобретения используют водный раствор, имеющий состав М2О × nSiO2 (M = Na, K, Li), где n находится в диапазоне от 0,67 до 4. Данные растворы могут быть получены в результате обработки соединений, содержащих диоксид кремния, при использовании гидроксидов щелочных металлов.
Например, возможным является получение раствора, относящегося к данному типу, после растворения стекла старых экранов электронно-лучевых трубок в способах, предназначенных для их утилизации, (с отделением свинцового содержимого при использовании надлежащих стадий селективного осаждения) в результате обработки стекла при использовании кипящих концентрированных растворов гидроксидов щелочных металлов.
В альтернативном и предпочтительном варианте, исходный раствор силиката получают в результате обработки при использовании гидроксида зол, произведенных в результате сжигания растительных биомасс, содержащих по меньшей мере 10% (масс.) диоксида кремния. Примеры биомасс, подходящих для использования в целях настоящего изобретения, представляют собой овес, бамбуковые листья, а, в особенности, рисовую шелуху или рисовую солому. Обычно золы из данных биомасс содержат по меньшей мере 50% (масс.), а зачастую более, чем 80% (масс.), диоксида кремния. Способ изобретения также может быть осуществлен исходя из зол, характеризующихся более низким уровнем содержания диоксида кремния, но это приводит к получению более низких выходов и вовлекает необходимость проведения стадий концентрирования растворов, полученных из зол, перед проведением стадий самого способа.
Перед проведением обработки при использовании гидроксида щелочного металла данные золы при необходимости могут быть подвергнуты промыванию при использовании кислот, таких как HNO3, для удаления всех растворимых в воде веществ и всех растворимых в кислоте оксидов/солей в целях получения более чистого исходного продукта; твердую долю, содержащую диоксид кремния, извлекают в результате фильтрования раствора. Способы осуществления данных необязательных предварительных промываний известны в данной области техники.
Золу (предварительно промытую или нет) суспендируют в растворе гидроксида щелочного металла, предпочтительно NaOH или КОН, при концентрации в диапазоне от 10% до 20% (масс.) (или растворе при 1 моль/л). Соотношение между щелочным металлом и диоксидом кремния (количество которых в золах, возможно, может быть определено в результате проведения предварительного наводящего анализа) может быть сверхстехиометрическим, стехиометрическим или субстехиометрическим, что может обеспечить достижение молярного соотношения в диапазоне от 1,5 : 1 до 1 : 4 между М2О и SiO2 в представленной выше формуле.
Суспензию нагревают для кипячения в условиях дефлегмирования в течение нескольких часов и получающийся в результате раствор подвергают воздействию стадий центрифугирования (для удаления тяжелого твердого остатка) и фильтрования (для удаления легкого твердого углеродистого остатка) с получением прозрачного раствора силиката. Растворами силикатов, подходящими для использования в изобретении, являются растворы, содержащие от 50 до 150 мг/мл SiO2.
Отдельно получают концентрированный раствор кислоты, предпочтительно хлористо-водородной или азотной кислоты, в подходящем контейнере; растворами, подходящими для использования в целях изобретения, являются, например, раствор HCl с концентрацией 37% (масс.) и раствор HNO3 с концентрацией от 40 до 65% (масс.).
Сначала выбирают контейнер в зависимости от его формы, поскольку, как это упоминалось выше, конечный аэрогель имеет форму контейнера, в котором получают гель. Кроме того, он должен демонстрировать некоторые химические характеристики: во-первых, он, само собой разумеется, должен быть инертным по отношению к концентрированным кислотам, а также к смесям, которые образуются в ходе осуществления способа; также он должен быть изготовлен из материала, такого, чтобы влажный гель не приставал бы к его стенкам. Обычно контейнер изготавливают из термопластических полимеров, таких как полиэтилен (РЕ), полипропилен (РР), полиэтилентерефталат (РЕТ) или политетрафторэтилен (PTFE); в альтернативном варианте, контейнер может быть изготовлен из сплавов, таких как стали AISI 321, AISI 316, AISI 316L, сплавы Inconel (содержащие по порядку следования величины уровня процентного содержания никель, хром, железо и другие элементы, в том числе молибден, марганец, кобальт и тому подобное) или сплавы, известные под сокращенным обозначением Alloy 20, (содержащие от 32,5 до 35% (масс.) никеля, от 19 до 21% хрома, менее, чем 5% других элементов, выбранных из углерода, меди, молибдена, марганца, кремния и ниобия, и остаток до 100% –от 31 до 44% железа); наконец, контейнер может быть изготовлен из металла с нанесенным внутренним покрытием из термопластического материала, предпочтительно полимера PTFE.
Количество кислоты должно быть таким, чтобы по завершении добавления всего раствора силиката значение рН системы составляло бы менее, чем 1: это обеспечивает достижение требуемого состояния, то есть, чтобы значение рН системы было бы меньшим, чем упомянутое значение на протяжении всей процедуры объединения основного раствора с кислотой. Упомянутое количество может быть получено в результате проведения простых стехиометрических вычислений химиком, работающим в лаборатории, или оно может быть определено в результате проведения предварительных ориентировочных испытаний в отношении небольших количеств растворов кислоты и силиката.
В соответствии с характерным вариантом осуществления настоящего изобретения полученный раствор силиката добавляют в контейнер, в котором уже присутствует концентрированный раствор кислоты. В целях промотирования смешивания двух растворов и, таким образом, предотвращения локального превышения значением рН значения 1 добавление раствора силиката проводят при интенсивном перемешивании и при регулировании значения рН; предпочтительно значение рН должно оставаться равным или меньшим 0. Возможным является достижение значений рН, составляющих менее, чем 0, в результате проведения работы с высококонцентрированными растворами кислот, но, как это известно, измерительные приборы дают не абсолютно точные показания в данном диапазоне значений рН, и чем меньшей будет точность, тем больше значение рН станет отрицательным; поэтому невозможно точно указать нижнее предельное значение для диапазона значений рН, но, принимая во внимание возможную максимальную погрешность в 50% от значения, указанного рН-метром, для практических целей можно предположить то, что нижнее предельное значение рН, подходящее для использования в целях изобретения, составляет приблизительно -1.
Как это также известно, значение, непосредственно считываемое рН-метром, не является значением рН, а представляет собой разность потенциалов, которая после этого преобразуется в значение рН при использовании внутреннего алгоритма прибора (формула вычисления для пересчета напряжения в значение рН на основании хорошо известного уравнения Нернста является общей для всех коммерческих приборов). Поэтому при желании во время проведения данной операции возможной также является и проверка значения разности потенциалов, непосредственно измеренной при использовании прибора, возможно после проверки при проведении предварительных наводящих испытаний значений разности потенциалов, которая приводит к получению аэрогелей, демонстрирующих желаемые характеристики; как это проверили в ориентировочных испытаниях, относящихся к данному типу, авторы настоящего изобретения, желаемые результаты (в первую очередь, легкость удаления ионов из конечного геля) будут получать постоянно в случае результата измерения разности потенциалов во время проведения данной стадии способа, составляющего более, чем 400 мВ.
Объемные соотношения между двумя растворами могут варьироваться в широком диапазоне при том условии, что удовлетворяется требование непревышения значением рН значения 1; в порядке приведения указания об относительных количествах двух растворов для специалиста в соответствующей области техники и всегда при рассмотрении раствора силиката, содержащего 100 мг/мл SiO2, типичные объемные соотношения между раствором силиката и раствором кислоты составят приблизительно 1 : 1 в случае раствора HCl с концентрацией 37% (масс.) и приблизительно 2 : 1 или 1 : 1 в случае раствора HNO3 с концентрацией 65% (масс.).
Объем раствора силиката, добавляемого к кислоте, должен быть таким, чтобы конечная плотность аэрогеля находилась бы в диапазоне от 0,01 до 0,3, предпочтительно от 0,05 до 0,12, г/мл при предварительном выборе в зависимости от области применения. Данная характеристика может быть предварительно определена во время разработки способа в результате определения объемов растворов силиката и кислоты, сумма которых при грубой оценке будет равна объему конечного аэрогеля, и количества SiO2, присутствующего в растворе силиката, которое будет определять его массу. Конечный аэрогель может демонстрировать небольшие отклонения от плотности, теоретически предварительно рассчитанной данным образом, вследствие неточной аддитивности объемов различных растворов и вследствие претерпевания влажным гелем легкого ограничения объема в сопоставлении с исходным раствором (явления, известного под названием «синерезис»); однако, данные легкие отклонения от идеальности могут быть приняты во внимание при исходном вычислении или компенсированы после предварительных наводящих испытаний.
По завершении добавления раствора силиката к раствору кислоты системе дают возможность оставаться в состоянии покоя для обеспечения гелеобразования: при комнатной температуре данная операция требует времени в диапазоне от 10 до 60 минут. После этого для полученного таким образом влажного геля проводят замену жидкой фазы, присутствующей в его порах, в результате простого погружения в ванну с жидкостью замены или под воздействием ее течения. Первая замена в общем случае представляет собой промывание, проводимое при использовании воды для эффективного удаления неорганических компонентов. После этого, как это известно в данной области, могут быть проведены дополнительные замены в зависимости от конечной жидкости, в которой будет проведена гиперкритическая экстракция.
В настоящем изобретении упомянутую конечную жидкость выбирают из этилацетата и СО2 в жидком состоянии. В случае гиперкритической экстракции этилацетата после промывания при использовании воды для геля предпочтительно сначала проводят замены на смеси ацетон/вода, постепенно все более обогащенные по ацетону, а в заключение на чистый ацетон, до конечной замены на этилацетат.
В зависимости от конечной области применения во время замен растворителя возможным является введение стадии силанизации геля, которая может быть проведена в результате добавления алкилхлорсиланов (соединений, описывающихся общей формулой R3-Si-Cl, где три заместителя R, одинаковые или отличные друг от друга, представляют собой алкильные радикалы) в целях введения групп R3-Si- на поверхность пор конечного аэрогеля и придания ему гидрофобности и совместимости с некоторыми органическими материалами.
В случае гиперкритической экстракции СО2 в жидком состоянии возможным является проведение замены исходя из геля, промытого при использовании воды, а после этого с использованием одного или нескольких промываний при использовании ацетона или другого жидкого летучего органического соединения. Способы замены жидкой фазы во влажном геле хорошо известны в данной области и доступны для специалистов в соответствующей области техники.
После этого для влажного геля, содержащего этилацетат или СО2 в жидком состоянии в качестве жидкой фазы, проводят гиперкритическую экстракцию упомянутой жидкой фазы в соответствии со способами, хорошо известными в данной области; операция будет проводиться в автоклаве и потребует использования температуры 251°С и давления 39 бар в случае этилацетата и температуры 31°С и давления 74 бара в случае СО2 в жидком состоянии.
После этого сухой гель, полученный в результате гиперкритической экстракции, при необходимости может быть подвергнут термической обработке в окислительной атмосфере, например, кислорода, воздуха или синтетических смесей кислород/азот, для удаления органических остатков; в случае несиланизированных аэрогелей обработка может быть проведена в широком диапазоне температур, в общем случае в диапазоне от 300 до 800°С, например, при 450°С, в то время как в случае силанизированных аэрогелей предпочтительным будет являться непревышение 300°С. В случае гиперкритической экстракции СО2 в жидком состоянии данная обработка не будет необходимой.
Аэрогели, полученные в соответствии с изобретением, являются мезопористыми и демонстрируют гидрофильные или гидрофобные характеристики для различных вариантов использования. Аэрогели, полученные в соответствии со способом изобретения, обычно демонстрируют характеристики, показанные в таблице 1.
Таблица 1
Изобретение будет дополнительно описываться при использовании следующих далее примеров. В примерах все концентрации и уровни процентного содержания будут являться массовыми, если только не будет указываться на другое.
Пример 1
15 г золы, полученной в результате сжигания рисовой шелухи, суспендируют в 180 мл 10%-ного раствора NaOH.
Полученную суспензию нагревают для кипячения в условиях дефлегмирования в течение 4 часов, что в результате приводит к получению частичной солюбилизации твердого вещества. Полученный раствор сначала подвергают воздействию стадии центрифугирования (5 мин, 6000 об./мин) для удаления твердого вещества, несолюбилизированного и представляющего собой тяжелую фракцию, а после этого стадии фильтрования для удаления легкого твердого углеродистого остатка. Таким образом получают прозрачный раствор силиката натрия. Небольшое количество данного раствора анализируют для определения концентрации по отношению к количеству диоксида кремния, которое равно 72 г/л.
Отдельно в надлежащий цилиндрический контейнер из тефлона вводят 165 мл 37%-ной хлористо-водородной кислоты.
К концентрированному раствору кислоты добавляют 150 мл раствора силиката натрия, полученного в соответствии с представленным выше описанием; данную операцию проводят при интенсивном перемешивании, обеспеченном механическим лопастным перемешивающим устройством.
Значение рН для полученного раствора измеряют на всем протяжении операции при использовании рН-метра: значение, выдаваемое прибором, постоянно остается составляющим менее, чем -0,5. Использующийся рН-метр представляет собой прибор Crison Basic 20 со стеклянным электродом Crison cat. No. 52-02. По завершении добавления перемешивание прекращают и раствор оставляют в состоянии покоя на протяжении 30 минут.
По завершении данного периода получают влажный хорошо консолидированный гель; гель, сохраненный в контейнере из тефлона, в котором он был получен, промывают в непрерывном режиме в результате создания потока воды, текущего по нему; вследствие высокой кислотности жидкости, содержащейся в порах геля, промывные воды, поступающие из контейнера, первоначально характеризуются значением рН, близким к 0; промывание продолжают вплоть до достижения значением рН промывных вод значения рН 2; после этого гель промывают при использовании ацетона вплоть до достижения концентрации воды в ацетоне, составляющей менее, чем 10 %, (согласно проверке в результате титрования по методу Карла Фишера); в заключение, ацетон заменяют на этилацетат. Влажный гель, все еще находящийся внутри контейнера, в котором его получили, помещают в автоклав и растворитель экстрагируют из геля в сверхкритических условиях: в ходе осуществления процесса экстракции жидкости, продолжающегося в течение 8 часов, максимальная температура варьируется в диапазоне от 275 до 295°С, а максимальное давление – в диапазоне от 55 до 65 бар.
После этого сухой аэрогель извлекают из автоклава и подвергают термической обработке при 450°С на воздухе в течение двух часов для удаления следовых количеств остаточных органических примесей от способа.
Полученный таким образом сухой гель характеризуется плотностью 0,056 г/мл, площадью удельной поверхности 553 м2/г, наличием мезопор со средним диаметром 14 нм, пористостью 97,5%, теплопроводностью 0,021 Вт/м-К и термостойкостью, доходящей вплоть до 1000°С.
Пример 2
15 г золы, полученной в результате сжигания рисовой шелухи, подвергают обработке при использовании 180 мл раствора HNO3 с концентрацией 1 моль/л в течение 2 часов.
Полученный раствор отфильтровывают и остаток, собранный на фильтровальной бумаге, промывают при использовании 25 мл воды. Фильтрату дают возможность высыхать в течение приблизительно 1 часа.
После этого высушенную золу подвергают обработке в соответствии с описанием в примере 1, получая по окончании сухой гель, демонстрирующий характеристики, подобные соответствующим характеристикам из примера 1.
Пример 3
Повторяют испытание из примера 1, но при использовании 300 мл 45 %-ной азотной кислоты; получают сухой гель, демонстрирующий характеристики, подобные соответствующим характеристикам из примера 1.
Пример 4
Повторяют испытание из примера 3, но конечное высушивание проводят при использовании СО2 в сверхкритическом состоянии.
Для осуществления этого полученный первоначально влажный гель промывают при использовании воды вплоть до достижения промывными водами значения рН 2, после чего его промывают в течение 12 часов при использовании объема ацетона, в 5 раз превосходящего объем геля. После удаления промывающего ацетона влажный гель (все еще находящийся в контейнере, в котором его получали) помещают в автоклав и сначала растворитель заменяют на СО2 в жидком состоянии, а после этого проводят высушивание в сверхкритических условиях. В ходе процесса экстракции, продолжающегося в течение 4 часов, максимальная температура варьируется в диапазоне от 40 до 50°С, максимальное давление – в диапазоне от 85 до 105 бар; получают сухой гель, демонстрирующий характеристики, подобные соответствующим характеристикам из примера 1.
Пример 5
Повторяют испытание из примера 1 при следующих далее изменениях параметров испытания:
- используют 45 г золы и 300 мл 10 %-ного раствора NaOH; данным образом в растворе получают молярное соотношение Na2O : SiO2, составляющее менее, чем 1 : 1, (субстехиометрический раствор);
- полученный таким образом раствор силиката (240 мл) имеет концентрацию SiO2, равную 102 г/л;
- для гелеобразования используют 80 мл 65 %-ной азотной кислоты;
- суспендирование проводят в течение периода времени в 80 минут при температуре Т кипения.
Получают сухой гель, демонстрирующий характеристики, подобные соответствующим характеристикам из примера 1.
Образец подвергают измерению распределения пористости по размерам. Использующийся прибор представляет собой порозиметр Carlo Elba Sorptomatic 1990, образцы подвергали предварительной обработке при 300°С в вакууме (10– 3/10– 4 бар) в течение 8 часов. Регистрировали изотерму абсорбции и десорбцию азота. Площадь удельной поверхности определяли при использовании классического метода Брунауэра, Эмметта и Теллера (ВЕТ), а анализ пористости поводили на основании кривой десорбции в соответствии с методом Баррета, Джойнера и Халенды (BJH). График, полученный в результате испытания, представлен на фигуре 1 при выражении через объем пор в зависимости от их диаметра; результат измерения получается как производная в виде приращения совокупного объема пор по отношению к вариации их размера, при этом кривая первообразной на фигуре не показана для лучшей читаемости фигуры, и демонстрирует тенденцию для объема пор (dV/d∅, при измерении в см3/нм⋅г; символ «∅» обозначает диаметр) в зависимости от их диаметра (нм). Как это можно видеть на фигуре, распределение пор образца достигает максимума в диапазоне приблизительно от 4 до 6 нм, при приблизительно 12 нм и приблизительно 23 – 24 нм. Максимум в области 4 – 6 нм (обозначенный рамкой, отмеченной стрелкой) является характеристическим для аэрогелей изобретения и не встречается для других аэрогелей, произведенных в соответствии с другими способами.
Пример 6
Данный пример относится к получению аэрогеля изобретения, в котором поверхность пор силанизируют.
Повторяют испытание из примера 5 при следующих далее изменениях параметров испытания:
- используют 100 мл раствора силиката и 100 мл 32,5 %-ной азотной кислоты;
- во время промывания при использовании ацетона добавляют растворитель при объеме триметилхлорсилана, равном 1/5 от объема геля, и гель выдерживают в течение 12 часов для прохождения реакции;
- в заключение, проводят 2 промывания при использовании этилацетата перед высушиванием в сверхкритической фазе.
Таким образом получают гидрофобный аэрогель.
Образец подвергают измерению распределения пористости по размерам в соответствии с методиками, продемонстрированными в примере 5. Результат испытания представлен на фигуре 2 и демонстрирует также и в данном случае наличие пика пористости, центрирующегося в диапазоне от 4 до 6 нм, что является характеристическим для аэрогелей изобретения.
Пример 7
Повторяют испытание из примера 1 при следующих далее изменениях параметров испытания:
- используют 19,1 г золы и 300 мл 10 %-ного раствора NaOH; данным образом в растворе получают молярное соотношение Na2O : SiO2, составляющее более, чем 1 : 1, (сверхстехиометрический раствор);
- полученный таким образом раствор силиката имеет концентрацию SiO2 70 г/л;
- для гелеобразования используют объемное соотношение 1 : 1 между раствором силиката и 65 %-ной азотной кислотой;
- суспендирование проводят в течение периода времени в 80 минут при температуре Т кипения.
Получают сухой гель, демонстрирующий характеристики, подобные соответствующим характеристикам из примера 1.
Пример 8
Повторяют испытание из примера 5, но при использовании 160 мл 40 %-ной азотной кислоты; получают сухой гель, демонстрирующий характеристики, подобные соответствующим характеристикам из примера 1.
Пример 9 (сравнительный)
Испытание на распределение пор по размерам проводят в отношении образца коммерческого аэрогеля ENOVA IC3120, изготовленного в компании Cabot Corporation. Результат продемонстрирован на фигуре 3 в виде сплошной линии. В данном случае пористость в диапазоне от 4 до 6 нм, характеристическая для аэрогелей изобретения, отсутствует.
Пример 10 (сравнительный)
Испытание на распределение пор по размерам проводят в отношении образца аэрогеля, произведенного из органического предшественника диоксида кремния (тетраэтоксисилана, TEOS) и полученного в соответствии с методикой, описанной в статье «Synthesis of GeO2-doped SiO2 aerogels and xerogels for optical glasses», S. Grandi et al., J. Non Cryst. Solids, 303 (2002) 208-217.
Результат продемонстрирован на фигуре 3 в виде пунктирной линии. Пористость в диапазоне от 4 до 6 нм, характеристическая для аэрогелей изобретения, отсутствует.
Пример 11 (сравнительный)
В данном примере воспроизводится способ получения аэрогелей предшествующего уровня техники, в котором к раствору силиката щелочного металла добавляют кислоту.
15 г золы, полученной в результате сжигания рисовой шелухи, суспендируют в 100 мл 10 %-ного раствора NaOH.
Полученную суспензию нагревают для кипячения в условиях дефлегмирования в течение 4 часов при интенсивном механическом перемешивании, что в результате приводит к получению частичной солюбилизации твердого вещества. Таким образом получают раствор силиката натрия, демонстрирующий рН = 12,6.
К данному раствору при перемешивании добавляют 190 мл раствора хлористо-водородной кислоты с концентрацией 1 моль/л при одновременном отслеживании значения рН во время добавления; при приблизительно рН = 10,5 может быть видна опалесценция раствора, и непосредственно после этого (приблизительно 2 минуты) происходит образование геля. Невозможно уменьшить значение рН системы до значений, составляющих менее, чем 10,5.
Стадию высушивания в сверхкритической фазе проводят в соответствии со способами, описанными в примере 1.
Полученный таким образом гель характеризуется плотностью 0,057 г/мл, площадью удельной поверхности 76 м2/г и объемом мезопор 0,16 см3/г.
В отношении полученного таким образом образца проводят измерение распределения пор по размерам. Результаты испытания продемонстрированы на фигуре 4. В данном случае пик пористости, центрирующийся в области 4 – 6 нм и характеристический для аэрогелей изобретения, также не продемонстрирован.
Пример 12
В соответствии с методикой из примера 5 получают аэрогель, имеющий объем 40 мл. Одновременно получают второй аэрогель, имеющий объем 40 мл, в соответствии с идентичной методикой, но в отличие от способа изобретения стадию, при которой объединяют два первоначальных раствора, проводят в результате выливания кислотного раствора в раствор силиката вплоть до момента гелеобразования, который имеет место при приблизительно рН = 11. Два аэрогеля промывают в одно и то же время и при использовании одних и тех же объемов воды (приблизительно 34 литра), а после этого подвергают обработке при использовании ацетона и этилацетата для высушивания в сверхкритической фазе в соответствии с описанием в примере 1. Два аэрогеля – первый, полученный в соответствии со способом изобретения (как и в примере 5), и второй, полученный при гелеобразовании в области рН = 11, – называют, соответственно, аэрогель А и аэрогель В. Химический состав двух образцов анализируют при использовании оптического устройства PERKIN-ELMER Optima 3300 DV ICP. Методология получения образца представляет собой нижеследующее: фрагмент в 0,4089 мг образца А и фрагмент в 0,4218 мг образца В подвергают обработке при использовании 7,5 мл 65%-ной азотной кислоты и 1 мл раствора перекиси водорода с концентрацией 30% (об./об.) и подвергают кипячению в условиях дефлегмирования в течение одного часа. После охлаждения два раствора разбавляют 1:10 при использовании тридистиллированной воды и фильтруют. Растворы анализируют при использовании вышеупомянутого прибора, получая результаты, представленные в таблице 2 для основных щелочных металлов и щелочноземельных металлов при выражении в миллиграммах металла при расчете на один килограмм аэрогеля (мг/кг), что соответствует ч./млн.
Таблица 2
Комментарии в отношении результатов испытаний
При проведении операций в соответствии со способами предшествующего уровня техники (сравнительный пример 11 и аэрогель В из примера 12) получают высушенные аэрогели, характеризующиеся плотностью, подобной соответствующим плотностям изобретения, но площадью удельной поверхности и меньшим объемом мезопор.
Кроме того, способу предшествующего уровня техники свойственны следующие далее проблемы, которые, однако, не встречаются при использовании способа изобретения:
- в способе требуется использование более разбавленной кислоты (HCl, 1 моль/л) по отношению к настоящему изобретению; это влечет за собой получение более значительных объемов жидкости, подвергаемых обработке, чрезмерно разбавленного раствора, полученного в результате объединения первоначальных кислотных и основных растворов, и, следовательно, геля, характеризующегося меньшей плотностью, с которым невозможно легко работать на последующих стадиях способа;
- несмотря на использование более разбавленной кислоты образование геля все еще невозможно регулировать;
- значение рН влажного геля остается основным, и щелочные металлы и щелочноземельные металлы, содержащиеся в порах, трудно удаляются, как это продемонстрировано в данных по испытаниям из примера 12.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗОЛЬ-ГЕЛЬ-ПРОЦЕСС | 2007 |
|
RU2445277C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЭРОГЕЛЕЙ И ПОЛУЧЕННЫЕ ИМ АЭРОГЕЛИ | 2019 |
|
RU2836464C2 |
| АРМИРОВАННЫЕ КОМПОЗИЦИИ АЭРОГЕЛЕЙ, СООТВЕТСТВУЮЩИЕ КЛАССУ ПОЖАРНОЙ БЕЗОПАСНОСТИ | 2019 |
|
RU2811474C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОПОРИСТОГО МАТЕРИАЛА ДЛЯ ЧУВСТВИТЕЛЬНЫХ ЭЛЕМЕНТОВ ГАЗОВЫХ СЕНСОРОВ И НАНОПОРИСТЫЙ МАТЕРИАЛ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2015 |
|
RU2614146C1 |
| УЛУЧШЕННЫЕ МАТЕРИАЛЫ ГИДРОФОБНЫХ АЭРОГЕЛЕЙ | 2015 |
|
RU2668657C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО КСЕРОГЕЛЯ SiO С ХАРАКТЕРНЫМ РАЗМЕРОМ ПОР ПОСРЕДСТВОМ ВОСХОДЯЩЕГО МЕТОДА С ИСПОЛЬЗОВАНИЕМ ПРЕДШЕСТВЕННИКА, ИМЕЮЩЕГО ОРГАНИЧЕСКИЕ ТВЕРДЫЕ СКЕЛЕТНЫЕ ОПОРЫ | 2010 |
|
RU2530049C2 |
| АЭРОГЕЛЕВЫЙ КОМПОЗИТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2729992C2 |
| Фармацевтическая композиция на основе белковых аэрогелей для применения в качестве интраназальных спреев и способ ее получения | 2022 |
|
RU2801351C1 |
| СЕГМЕНТИРОВАННЫЕ ГЕЛЕВЫЕ КОМПОЗИТЫ И ЖЕСТКИЕ ПАНЕЛИ, ИЗГОТОВЛЕННЫЕ ИЗ НИХ | 2013 |
|
RU2676289C1 |
| ЭЛЕКТРОДНЫЕ МАТЕРИАЛЫ НА ОСНОВЕ УГЛЕРОДНЫХ АЭРОГЕЛЕЙ И СПОСОБЫ ИХ ИЗГОТОВЛЕНИЯ | 2020 |
|
RU2801325C2 |
Предложен золь-гель-способ получения аэрогелей диоксида кремния из растительного сырья, в частности из отходов переработки риса. Способ включает следующие стадии: получение водного раствора силиката щелочного металла; отдельное получение в контейнере концентрированного раствора неорганической кислоты, выбранной из серной, хлористо-водородной, азотной и фосфорной кислоты; объединение указанных растворов силиката и кислоты путём выливания раствора силиката в раствор кислоты, таким образом, чтобы значение рН системы всегда оставалось меньшим 1; выдерживание системы в состоянии покоя вплоть до получения влажного геля; промывание произведенного влажного геля для замены жидкой фазы, присутствующей в его порах, на жидкое летучее органическое соединение (ЛОС), а после этого, возможно, на жидкий диоксид углерода; высушивание геля в результате экстракции в гиперкритических условиях упомянутого жидкого органического летучего соединения. Изобретение обеспечивает возможность получения аэрогеля диоксида кремния, характеризующегося распределением пор по размерам, имеющим пик в диапазоне от 4 до 6 нм, простым способом. 2 н. и 11 з.п. ф-лы, 4 ил., 2 табл., 12 пр.
1. Золь-гель-способ производства аэрогеля диоксида кремния, включающий следующие стадии:
- получение водного раствора силиката щелочного металла;
- отдельное получение в контейнере концентрированного раствора неорганической кислоты, выбранной из серной, хлористо-водородной, азотной и фосфорной кислоты;
- объединение указанных растворов силиката и кислоты;
- выдерживание системы в состоянии покоя вплоть до получения влажного геля;
- промывание только что произведенного влажного геля для замены жидкой фазы, присутствующей в его порах, на жидкое летучее органическое соединение (ЛОС), а после этого, возможно, на жидкий диоксид углерода;
- высушивание геля в результате экстракции в гиперкритических условиях упомянутого жидкого органического летучего соединения;
отличающийся тем, что упомянутую стадию объединения указанных растворов силиката и кислоты проводят в результате выливания раствора силиката в раствор кислоты, причем указанную операцию проводят таким образом, чтобы значение рН системы всегда оставалось бы меньшим чем 1.
2. Способ по п. 1, в котором во время упомянутых промываний влажного геля к растворителю примешивают алкилхлорсилан R3-Si-Cl, где три заместителя R, одинаковые или отличные друг от друга, представляют собой алкильные радикалы, в целях введения групп R3-Si- на поверхность пор конечного аэрогеля.
3. Способ по п. 1 или 2, в котором во время упомянутой стадии объединения растворов силиката и кислоты значение рН системы остается на уровне значений, равных или меньших 0.
4. Способ по любому из пп. 1-3, в котором упомянутый водный раствор силиката щелочного металла имеет состав М2О × nSiO2 (M = Na, K, Li), где n находится в диапазоне от 0,67 до 4 и от 50 до 150 мг/мл SiO2.
5. Способ по любому из пп. 1-4, в котором упомянутый водный раствор силиката щелочного металла получен в результате растворения материала, содержащего диоксид кремния, под воздействием раствора гидроксида щелочного металла с концентрацией в диапазоне от 10 до 20 мас.% .
6. Способ по п. 5, в котором упомянутый материал, содержащий диоксид кремния, представляет собой золу, произведенную в результате сжигания растительной биомассы, содержащей по меньшей мере 10 мас.% диоксида кремния.
7. Способ по п. 6, в котором упомянутая зола получена от сжигания рисовой шелухи или рисовой соломы.
8. Способ по любому из пп. 1-7, в котором упомянутая концентрированная неорганическая кислота выбрана из раствора HCl с концентрацией 37% (масс.) и раствора HNO3 с концентрацией от 40 до 65% (масс.).
9. Способ по любому из пп. 1-8, в котором раствор силиката щелочного металла добавляют к кислоте в таком количестве, чтобы конечная плотность аэрогеля находилась бы в диапазоне от 0,01 до 0,3 г/мл.
10. Способ по п. 9, в котором раствор силиката щелочного металла добавляют к кислоте в таком количестве, чтобы конечная плотность аэрогеля находилась бы в диапазоне от 0,05 до 0,12 г/мл.
11. Способ по любому из пп. 1-10, в котором упомянутые промывания влажного геля, непосредственно полученного со стадии гелеобразования, включают:
- одно или несколько начальных промываний при использовании воды для удаления неорганических соединений, растворенных в жидкой фазе;
- промывания при использовании смесей вода/ацетон, постепенно все более обогащенных по ацетону, промывание при использовании чистого ацетона и конечную замену на жидкость, для которой должна быть проведена гиперкритическая экстракция.
12. Способ по любому из пп. 1-11, в котором получающийся в результате сухой гель подвергают термической обработке в окислительной атмосфере, состоящей из кислорода, воздуха или синтетических смесей кислород/азот, при температуре в диапазоне от 300 до 800°С.
13. Аэрогель, полученный при использовании способа по любому из пп. 1-12, характеризующийся распределением пор по размерам, имеющим пик в диапазоне от 4 до 6 нм.
| DE 19541715 A1, 15.05.1997 | |||
| WO 2008044873 A1, 17.04.2008 | |||
| CN 102757059 A, 31.10.2012 | |||
| US 7618608 B1, 17.11.2009 | |||
| US 8137651 B2, 20.03.2012 | |||
| ЗОЛЬ-ГЕЛЬ СПОСОБ ПОЛУЧЕНИЯ СУХИХ ГЕЛЕЙ БОЛЬШИХ РАЗМЕРОВ И МОДИФИЦИРОВАННЫХ СТЕКОЛ | 2001 |
|
RU2278079C2 |
Авторы
Даты
2019-10-24—Публикация
2016-05-27—Подача