Область техники
Настоящее изобретение относится к композиции с желаемыми биологическими или терапевтическими свойствами, полученной из исходной композиции крови, содержащей тромбоциты. Настоящее изобретение также относится к способу приготовления этой композиции. Данная композиция служит в качестве тканевого адгезива.
Предпосылки создания изобретения
Приготовление композиций из крови человека или животных известно специалистам в данной области, при этом, кровь обрабатывают так, чтобы получить плазму, обогащенную тромбоцитами (PRP) и/или плазму, богатую факторами роста и обаладющую полезными биологическими и терапевтическими свойствами. Такая PRP или плазма, богатая факторами роста, была успешно использована в методах ex vivo, например, в качестве среды для культивирования клеток, и in vivo, например, для проведения операции по регенерации кости у пациента или для лечения пациента с заболеванием суставов посредством инфильтрации. В случае композиций, предназначенных для применения in vivo, технология приготовления композиций PRP и плазмы, богатой факторами роста, эволюционировала в сторону приготовления аутологичных композиций, то есть, их получения из собственной крови пациента. Примеры этих композиций и способов их приготовления можно найти в патентах US6569204 и ES2221770.
Кроме того, также известны композиции, состоящие из богатого тромбоцитами фибрина (PRF), полученного из крови. Подобно вышеупомянутой плазме, фибрин может быть аутологичным или гетерологичным. В отличие от плазмы, которая является жидкой, фибрин имеет твердую или полутвердую консистенцию.
Одним из известных примеров фибрина является фибриновый гель или фибриновая сеть, представляющие собой состав, полутвердая консистенция которого может оказаться очень полезной для применения в определенных целях. Процедура приготовления фибринового геля или фибриновой сети обычно начинается с первой фазы, в которой PRP или плазму, богатую факторами роста, получают соответствующим способом, например, путем центрифугирования крови, взятой у пациента, до тех пор, пока кровь не будет разделена на несколько фракций, и экстрагирования верхней фракции, то есть, фракции плазмы, богатой тромбоцитами (PRP), или плазмы, богатой факторами роста. Затем, тромбоциты, содержащиеся в PRP или в плазме, богатой факторами роста, активируют (в данном случае, под активацией подразумевается действие, инициирующее высвобождение тромбоцитами некоторых содержащихся в них факторов роста), например, путем добавления хлорида кальция. В результате активации и после достаточно длительного выдерживания происходит окончательная полимеризация фибрина из фибриногена, содержащегося в плазме, с образованием конечного соединения, которое представляет собой фибриновый сгусток (также называемый фибриновым гелем или фибриновой сетью из-за его полутвердоой консистенции, подобно разновидности биологической губки). Эту процедуру обычно осуществляют в целях получения фибринового геля из крови, модифицированной антикоагулянтом, таким как цитрат натрия. Однако, кровь может быть также обработана и без ее предварительного смешивания с антикоагулянтом, и в этом случае, путем центрифугирования крови можно отделить плазму от эритроцитов, и в то же время получить фибриновый гель без необходимости добавления хлорида кальция или любого другого активатора тромбоцитов. Некоторые примеры применения фибринового геля или фибриновой сети включают: формирование биологической основы для устранения дефектов костей; нанесение на раны или травмы для постепенного высвобождения факторов роста; использование в качестве матрицы для культивирования стволовых клеток; использование в качестве мембраны для устранения дефектов или заживления язв; использование в целях получения тканей, известного как тканевая инженерия, где в дополнение к клеткам и факторам роста особенно важно иметь матрицу или остов, на которых могут расти эти клетки.
Однако, препараты с высоким содержанием тромбоцитов (PRP, плазма, богатая факторами роста, PRF) имеют ограниченную способность действовать как тканевый адгезив. Важно, чтобы эти препараты обладали хорошими адгезивными свойствами, поскольку хирургические и хронические раны представляют собой глобальную социально-экономическую проблему как для пациентов, так и для системы здравоохранения, которая часто недооценивается. Одной из основных проблем, которая наблюдается в этой области, является обильное, непрерывное кровотечение, которое может возникать во время операции или при хронических ранах, а также послеоперационный дискомфорт и осложнения, вызываемые наложением хирургических швов, такие как абсцессы, образование гранулем или некроз тканей. За последние годы, в хирургии появились методы лечения широкого спектра, целью которых является уменьшение таких осложнений, в том числе, использование фибринового клея/герметика.
Коммерчески доступные аллогенные фибриновые герметики представляют собой хорошую неинвазивную альтернативу. Однако, хотя они и действуют эффективно, но тем не менее, они являются дорогостоящими, и могут быть доступны не во всех странах или регионах. Кроме того, поскольку коммерчески доступный аллогенный фибриновый герметик получают из плазмы человека, то существует риск передачи определенных заболеваний и реакций гиперчувствительности.
Самый безопасный способ приготовленияя фибринового герметика является его получение из собственной крови пациента. Тем не менее, для его приготовления (обычно с применением методов замораживания или лиофилизации) либо требуется очень много времени, а именно, по меньшей мере 24 часа для обработки, а поэтому это невозможно сделать во время операции, либо необходимо, чтобы пациент пришел за день до операции для забора крови. Эти методы замораживания или лиофилизации основаны на увеличении концентрации фибриногена и имеют такие ограничения, как низкая концентрация фибриногена или белков свертывания крови, а поэтому время герметизации является длительным и сильно варьируется из-за биологических особенностей каждого пациента. В других методах, используемых для ускорения приготовления аутологичного фибринового герметика, используются химические вещества, способствующие осаждению фибриногена, но такие продукты могут вызывать раздражение и воспаление тканей, на которые они наносятся.
Целью настоящего изобретения является получение препарата с желательными биологическими или терапевтическими свойствами, полученного из исходной композиции крови, богатой тромбоцитами и/или факторами роста, которая может быть приготовлена во время хирургического вмешательства и может иметь повышенную тканевую адгезию. Есть надежда, что такая композиция, помимо других применений, послужит альтернативой коммерчески доступному фибриновому герметику.
Краткое описание изобретения
Настоящее изобретение относится к композиции с желательными биологическими или терапевтическими свойствами, которая включает исходную композицию крови или была получена из этой композиции (человеческого или животного происхождения; аутологичной, гомологичной или гетерологичной), богатой тромбоцитами и/или факторами роста и содержащей белки самой исходной композиции крови, причем, отличительной особенностью композиции согласно изобретению является ее повышенная адгезивность. Эта композиция может быть аутологичной (приготовленной из крови одного донора и введенной этому донору), гомологичной (когда донор и реципиент принадлежат к одному виду) или гетерологичной (когда донор и реципиент принадлежат к разным видам) и может быть квалифицирована как «фибриновый герметик» (в данном случае используется терминология, аналогичная той, которая используется для обозначения фибриновых препаратов для герметизации), поскольку он имеет повышенную адгезивность и ускоряет свертывание крови. Эта композиция имеет новую морфологическую и биомеханическую конфигурацию по сравнению с другими фибриновыми герметиками, композициями крови, богатыми тромбоцитами и/или факторами роста, и аналогичными продуктами, известными специалистам в данной области.
Композиция согласно изобретению является биосовместимой, биоразлагаемой и обладает желаемыми биологическими или терапевтическими свойствами, обеспечиваемыми наличием тромбоцитов или факторов роста. Кроме того, такая композиция обладает повышенной тканевой адгезией и может быть быстро приготовлена. Таким образом, композиция согласно изобретению является выгодной альтернативой обычному фибриновому герметику, поскольку такая композиция является аутологичной, адгезивной и может быть быстро приготовлена без добавления химических веществ. Кроме того, такая композиция обладает хорошей адгезией при сжатии, которая аналогична адгезии или лучше, чем адгезия обычных аллогенных фибриновых герметиков Tisseel® и PRP (обычно используемых в качестве герметиков), и адекватно выдерживает любое сопротивление, которое может оказывать ткань, а поэтому, такая композиция очень подходит для ее использования в качестве фибринового герметика. Кроме того, она может быть введена путем инъекции.
Целью настоящего изобретения также является разработка способа приготовления такой композиции, где этот способ включает стадии: получения исходной композиции крови, богатой тромбоцитами и/или факторами роста, базовый состав которой может варьироваться; нагревания композиции крови до температуры 40-55°С; центрифугирования исходной композиции крови в течение по меньшей мере 1 минуты; и уменьшения объема исходной композиции. Этот способ согласно изобретению также включает добавление вещества, активирующего тромбоциты, и образование фибрина с получением композиции крови, богатой тромбоцитами и/или факторами роста, в форме геля.
Краткое описание чертежей
Подробное описание изобретения проиллюстрировано на прилагаемых чертежах, которые не рассматриваются как ограничение объема изобретения:
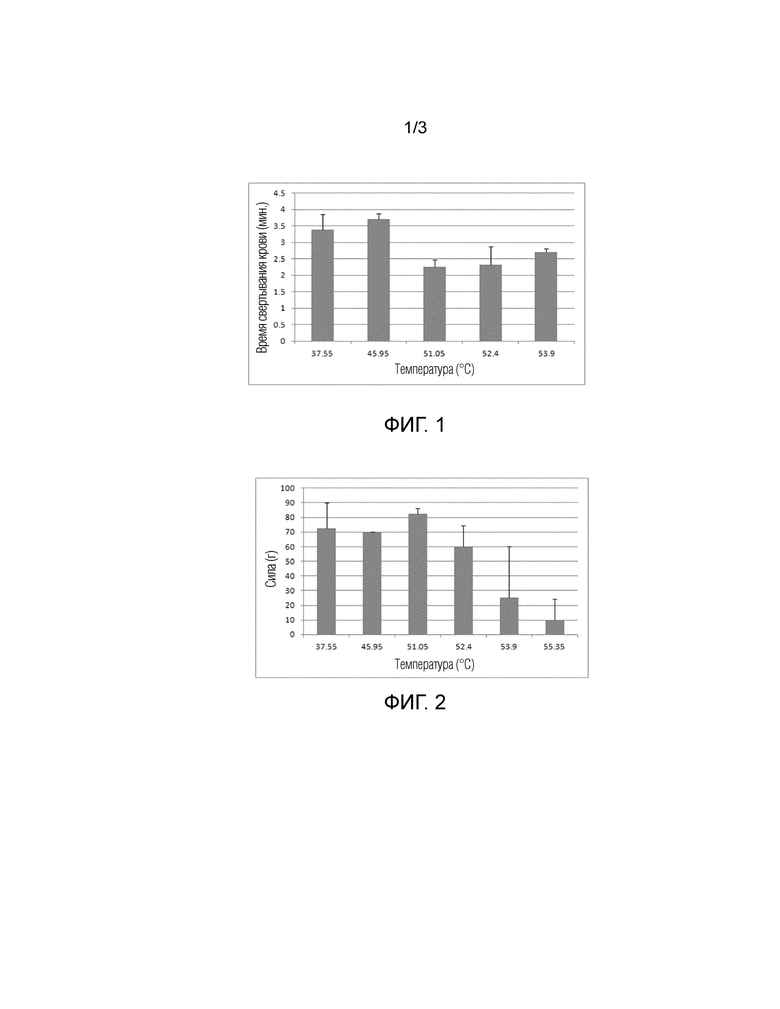
- На Фигуре 1 показано время свертывания крови для различных примеров композиций согласно изобретению.
- На Фигуре 2 показана адгезионная способность различных примеров композиций согласно изобретению.
- На Фигуре 3 показано влияние активатора и тромбоцитов на время свертывания крови для композиций согласно изобретению.
- На Фигуре 4 показано влияние активатора и тромбоцитов на адгезионную способность различных примеров композиций согласно изобретению.
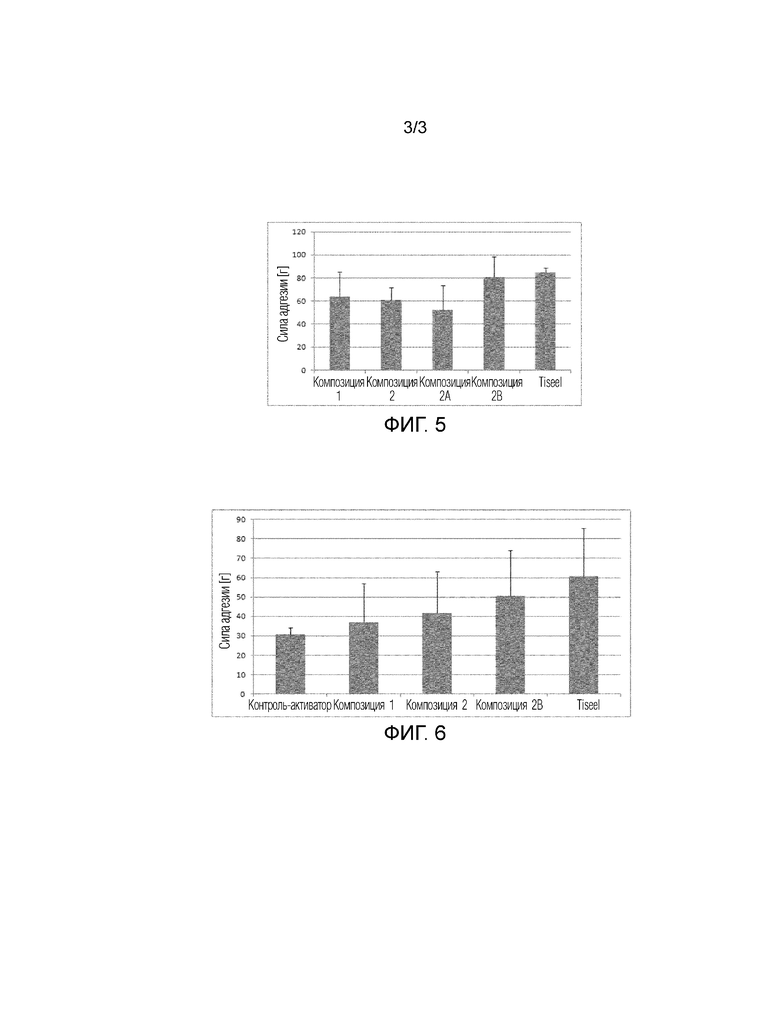
- На Фигуре 5 показано действие активатора и эффективность различных примеров композиций согласно изобретению и их сравнение с коммерчески доступным герметиком Tisseel® в отношении адгезии.
- На Фигуре 6 показана эффективность различных примеров композиций согласно изобретению в качестве тканевого адгезива по сравнению с коммерчески доступным герметиком Tisseel®, используемым в качестве тканевого адгезива.
Подробное описание изобретения
Для решения проблем, все еще существующих в области, относящейся к адгезивности PRP, была преложена альтернативная композиция с желательными биологическими или терапевтическими свойствами и с улучшенной адгезивностью. Эта композиция включает исходную композицию крови или была получена из исходной композиции крови, содержащей тромбоциты. Эта композиция становится адгезивной в результате термообработки и образования фибринового сгустка. Было обнаружено, что герметик, приготовленный в соответствии с настоящим изобретением, имеет тканевую адгезию, аналогичную фибриновому герметику Tisseel® и даже лучшую, чем адгезия богатой тромбоцитами плазмы или обычного богатого тромбоцитами фибрина.
Исходная композиция крови может, например, представлять собой плазму крови, богатую тромбоцитами, то есть, плазму с высокой концентрацией тромбоцитов. Эту плазму обычно получают методом центрифугирования крови (для разделения ее на фракцию эритроцитов, фракцию лейкоцитов и фракцию обогащенной тромбоцитами плазмы (PRP)) и разделения всей или части фракции на плазму, богатую тромбоцитами (PRP).
Исходная композиция крови может содержать, а может и не содержать лейкоциты.
Для активации исходной композиции крови могут быть использованы один или более из нижеследующих компонентов: хлорид кальция, тромбин, глюконат натрия, коллаген, супернатант (жидкое вещество, которое появляется после свертывания крови при свертывании плазмы, богатой тромбоцитами (PRP), и его последующая ретракция), супернатант плазмы крови, богатой факторами роста, или любой другой агент, который действует посредством активации тромбоцитов и индуцирования образования фибрина, в результате чего тромбоциты высвобождают определенные содержащиеся в них факторы роста.
Также предлагается способ приготовления композиции с желаемыми биологическими или терапевтическими свойствами, где указанный способ включает следующие стадии:
a) получения исходной композиции крови, богатой тромбоцитами и/или факторами роста с антикоагулянтом или без него, где такая композиция предпочтительно представляет собой богатую тромбоцитами плазму с лейкоцитами или без них, или плазму, богатую факторами роста с лейкоцитами или без них,
b) повышения температуры исходной композиции до температуры 40-55°С,
c) центрифугирования исходной композиции крови по меньшей мере в течение 1 минуты,
d) удаления по меньшей мере части фракции плазмы, полученной в результате центрифугирования,
e) активации оставшейся композиции крови после удаления по меньшей мере части фракции плазмы, как указано в стадии d). Активация может быть осуществлена, например, путем добавления хлорида кальция, тромбина, комбинации хлорида кальция и тромбина, глюконата натрия, коллагена, супернатанта (жидкого вещества, которое появляется после свертывания крови при свертывании плазмы, богатой тромбоцитами (PRP), и его последующей ретракции), супернатанта плазмы крови, богатой факторами роста, и/или любого другого агента, активирующего тромбоциты. В результате происходит активация тромбоцитов и индуцирование образования фибрина, что приводит к высвобождению тромбоцитами определенных факторов роста.
Этот метод позволает осуществлять осаждение белковых веществ без денатурации фибриногена, как можно видеть по появлению фибринового сгустка после активации. За счет удаления части объема исходной композиции повышается концентрация этих белковых веществ. Кроме того, этот способ дает заметное ускорение свертывания композиции крови и увеличивает ее адгезионную прочность. Таким образом, в результате нагревания могут быть получены новые биосовместимые и биоразлагаемые композиции с двумя основными преимуществами: коротким временем свертывания и большей адгезией, что делает эту композицию подходящей для использования в качестве фибринового адгезива или герметика.
Предпочтительно, температуру исходной композиции крови повышают до температуры в пределах 40-53°С.
Исходная композиция крови, богатая тромбоцитами и/или факторами роста, может иметь человеческое или животное происхождение. Кроме того, она может быть аутологичной (принадлежащей пациенту, который впоследствии будет подвергнут лечению конечной композицией), гомологичной (принадлежащей представителю того же вида, что и пациент, пациенты, клетки или другие биологические объекты, подлежащие лечению или обработке конечной композицией) или гетерологичной (принадлежащей представителю другого вида, отличающегося от пациента, пациентов, клеток или других биологических объектов, подлежащих лечению или обработке конечной композицией).
В настоящем изобретении предусматривается, что исходная композиция крови может, но необязательно, включать одно или более дополнительных веществ, добавленных до заявленной термообработки. Этими дополнительными веществами могут быть:
- один или более биоактивных агентов, выбранных из белков, пептидов, нуклеиновых кислот, полисахаридов, липидов, небелковых органических веществ и неорганических веществ;
- один или более биоразлагаемых полимеров, выбранных из: гиалуроновой кислоты, солей гиалуроновой кислоты, хондроитин-4-сульфата, хондроитин-6-сульфата, декстрана, силикагеля, альгината, гидроксипропилметилцеллюлозы, производных хитина, предпочтительно хитозана, ксантановой камеди, агарозы; полиэтиленгликоля (ПЭГ), полигидроксиэтиленметакрилата (HEMA), синтетических или природных белков и коллагенов;
- один или более органических полимеров, выбранных из группы, состоящей из поликапролактона, полигликолевой кислоты, полимолочной кислоты и их сополимеров;
- один или более из агентов, выбранных из антибиотиков, противомикробных средств, противораковых средств, аналгетиков, факторов роста, гормонов;
- один или более неорганических компонентов, выбранных из группы, состоящей из солей кальция, солей магния и/или солей стронция.
В настоящем изобретении также рассматривается возможность того, что любое из вышеперечисленных веществ может быть добавлено в композицию после проведения термообработки.
Композиция согласно изобретению включает различные варианты, где такая композиция может содержать, помимо заявленных технических аспектов, другие соединения, компоненты, молекулы и т.п., которые являются подходящими для конкретного применения рассматриваемой композиции.
Кроме того, могут быть проведены дополнительные стадии для композиции, полученной в соответствии со способом, описанным в настоящем изобретении, включая сушку для повышения универсальности композиции, то есть, перед активацией (активацией тромбоцитов и образованием фибрина), композиция согласно изобретению может быть высушена (путем подачи сухого тепла) или лиофилизована. Такая композиция может быть впоследствии регидратирована различными методами, такими как добавление физиологического раствора; плазмы, богатой тромбоцитами; супернатанта плазмы, богатой тромбоцитами; плазмы, богатой факторами роста; супернатанта плазмы, богатой факторами роста; или любого другого жидкого вещества.
Примеры
Пример 1
В этом примере сначала берут образец из 9 герметичных пробирок (9 мл), содержащих кровь, взятую у пациента. Пробирки центрифугируют со скоростью 580× g в течение 8 минут при комнатной температуре. В результате центрифугирования, кровь, содержащаяся в каждой пробирке, разделяется на несколько фракций. Верхнюю фракцию или фракцию богатой тромбоцитами плазмы (PRP) экстрагируют в белую пробирку с получением всего 36 мл плазмы. Плазму распределяют по 6 пробиркам, каждая из которых содержит 6 мл плазмы. Затем температуру каждой из 6 пробирок повышают до 37,55, 45,95, 51,05, 52,4, 53,9 и 55,35°C, соответственно. Затем 6 пробирок центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре, что приводит к осаждению тромбоцитов и новых белковых веществ. Для концентрирования этих белковых веществ после центрифугирования нагретой плазмы, верхнюю половину плазмы удаляют. И наконец, осадок ресуспендируют в плазме, оставшейся в пробирке.
Затем композиции в 6 пробирках активируют путем добавления супернатанта PRP (333 мкл) и 20 мкл кальция на каждый 1 мл композиции, что стимулирует образование фибрина в композициях.
Было измерено время свертывания крови (время, необходимое для перехода композиции крови из жидкого состояния в гелеобразное) в результате образования фибрина. На фигуре 1 показана возможность способа согласно изобретению ускорять время свертывания крови. Следует отметить, что время свертывания крови в случае обычной PRP, активированной таким же образом, как и композиция согласно изобретению, описанная выше (то есть, с супернатантом PRP (333 мкл) и 20 мкл кальция на каждый 1 мл), составляло 4,5 минуты. Как видно на графике, композиции согласно изобретению имели более низкое или ускоренное время свертывания крови по сравнению с этой стандартной PRP. Это ускорение свертывания крови является наибольшим при температуре 51,05°С, за которой следуют температуры 52,4 и 53,9°С. Стабильный сгусток не был получен при температуре 55,3°С.
Пример 2
В этом примере сначала берут образец из 9 герметичных пробирок (9 мл), содержащих кровь, взятую у пациента. Кровь центрифугируют со скоростью 580× g в течение 8 минут при комнатной температуре. В результате центрифугирования, кровь, содержащаяся в каждой пробирке, разделяется на несколько фракций. Верхнюю фракцию или фракцию богатой тромбоцитами плазмы (PRP) экстрагируют в белую пробирку с получением всего 36 мл плазмы. Плазму распределяют по 6 пробиркам, каждая из которых содержит 6 мл плазмы. Затем температуру каждой из пробирок повышают до 37,55, 45,95, 51,05, 52,4, 53,9 и 55,35°C, соответственно. Затем пробирки центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре, что приводит к осаждению тромбоцитов и новых белковых веществ. Для концентрирования этих белковых веществ после центрифугирования нагретой плазмы, верхнюю половину плазмы удаляют. И наконец, осадок ресуспендируют в плазме, оставшейся в пробирке.
Затем, композиции в 6 пробирках активируют путем добавления супернатанта PRP (333 мкл) и 20 мкл кальция на каждый 1 мл композиции, что стимулирует образование фибрина в композициях.
Два предметных стекла были склеены композицией после активации. После свертывания крови, склеенные предметные стекла инкубировали в дистиллированной воде в течение 3 минут, а затем измеряли силу адгезии композиции с использованием граммовых гирь. На фигуре 2 показана адгезионная прочность композиций. Самая высокая адгезионная прочность соответствовала температуре 51,05°С, а за нею следуют температуры 37,55 и 45,95°С. Самая низкая адгезионная прочность наблюдалась при температуре 55,3°С, а за ней следует температура 53,9°С.
Пример 3
В этом примере сначала берут образец из 9 герметичных пробирок (9 мл), содержащих кровь, взятую у пациента. Пробирки центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. В результате центрифугирования, кровь, содержащаяся в каждой пробирке, разделяется на несколько фракций. Верхнюю фракцию или фракцию богатой тромбоцитами плазмы (PRP) экстрагируют в белую пробирку с получением всего 36 мл плазмы. Плазму распределяют по 6 пробиркам, каждая из которых содержит 6 мл плазмы. Образцы обрабатывают следующим образом:
- Контрольный образец: PRP активируют ионами кальция в количестве 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Контрольный образец активатора: PRP активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Контрольный образец метода: PRP центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов ресуспендируют в оставшейся 1/3 начального объема. Затем его активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 1: Температуру PRP повышают до 51°С. Затем композицию центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/3 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 2: Температуру PRP повышают до 51°С. Затем композицию центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 1/2 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/2 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 3: Температуру PRP повышают до 51°С. Затем композицию центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Осадок тромбоцитов и белка ресуспендируют в общем исходном объеме. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 4: Тромбоциты PRP удаляют путем фильтрации с использованием фильтров с размером пор 20 мкл. Затем температуру PRP повышают до 51°С. После этого композицию центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/3 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
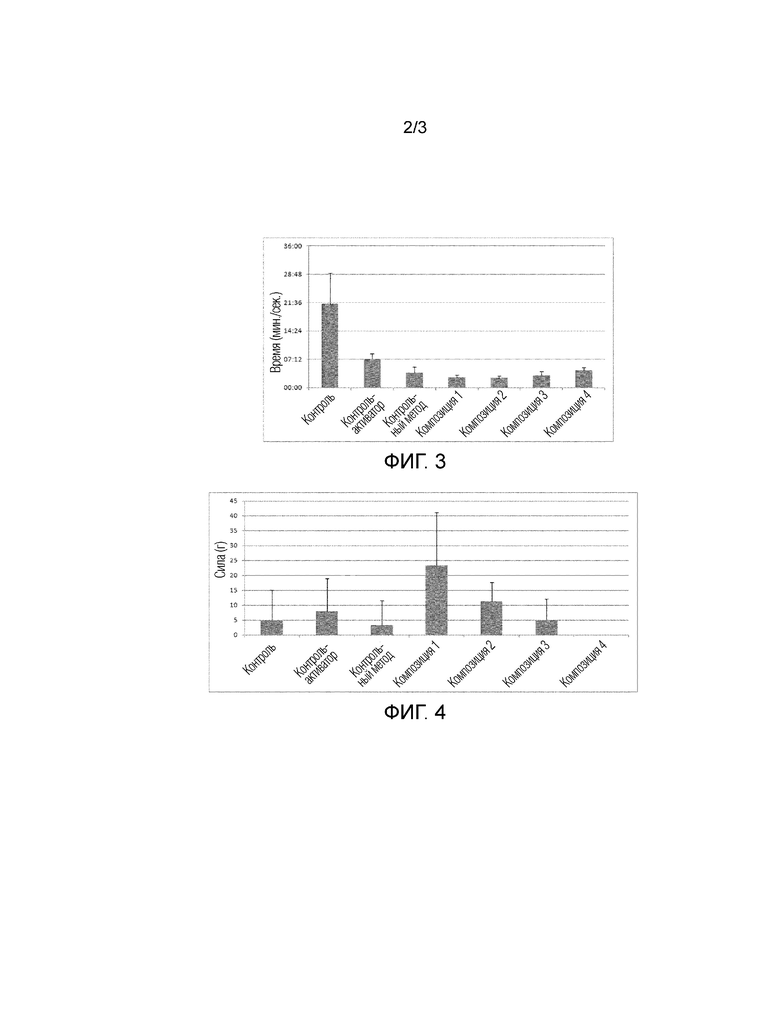
Результаты по времени свертывания крови, представленные на Фигуре 3, показали, что: использование активатора тромбина (супернатанта PRP) + кальция, используемых в контроле-активаторе, в контрольном способе и в композициях 1-4, ускоряет свертывание крови в случае PRP по сравнению с использованием только ионов кальция (контрольный образец). Кроме того, второе центрифугирование PRP перед активацией (контрольный способ и композиции 1-4) дополнительно ускоряет свертывание крови, возможно, из-за увеличения концентрации тромбоцитов за счет удаления части начального объема. Однако, способ согласно изобретению позволяет ускорять свертывание крови независимо от концентрации тромбоцитов, как показали результаты для композиции 3 (без увеличения концентрации тромбоцитов) и композиции 4 (без тромбоцитов). Самое короткое время свертывания крови соответствует композициям 1 и 2. Таким образом, время свертывания крови указывает на новизну и эффективность способа согласно изобретению для ускорения процесса свертывания крови.
Пример 4
В этом примере сначала берут образец из 9 герметичных пробирок (9 мл), содержащих кровь, взятую у пациента. Пробирки центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. В результате центрифугирования, кровь, содержащаяся в каждой пробирке, разделяется на несколько фракций. Верхнюю фракцию или фракцию богатой тромбоцитами плазмы (PRP) экстрагируют в белую пробирку с получением всего 36 мл плазмы. Плазму распределяют по 6 пробиркам, каждая из которых содержит 6 мл плазмы. Образцы обрабатывают следующим образом:
- Контрольный образец: PRP активируют ионами кальция в количестве 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Контрольный образец активатора: PRP активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Контрольный образец метода: PRP центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов ресуспендируют в оставшейся 1/3 начального объема. Затем его активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 1: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/3 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 2: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 1/2 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/2 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 3: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Осадок тромбоцитов и белка ресуспендируют в общем начальном объеме. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 4: Тромбоциты PRP удаляют путем фильтрации с использованием фильтров с размером пор 20 мкл. Затем температуру PRP повышают до 51°С. После этого композицию центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/3 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
Два предметных стекла были склеены вместе с образцами, как описано выше, после активации. Образцы инкубировали в дистиллированной воде, а затем измеряли силу адгезии композиции с использованием граммовых гирь. На фигуре 4 показана адгезионная прочность композиций. Результаты ясно показали, что повышение адгезии происходит только в композициях согласно изобретению (в композициях 1 и 2), поскольку использование тромбина+кальция (контроля-активатора) или повышенной концентрации тромбоцитов (контрольный способ) не повышало адгезию активированного PRP с ионами кальция. Наилучшая адгезия была достигнута с использованием композиций 1 и 2 согласно изобретению.
Пример 5
В этом примере сначала берут образец из 8 герметичных пробирок (9 мл), содержащих кровь, взятую у пациента. Пробирки центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. В результате центрифугирования, кровь, содержащаяся в каждой пробирке, разделяется на несколько фракций. Верхнюю фракцию или фракцию богатой тромбоцитами плазмы (PRP) экстрагируют в белую пробирку с получением всего 30 мл плазмы. Плазму распределяют по 5 пробиркам, каждая из которых содержит 6 мл плазмы. Образцы обрабатывают следующим образом:
- Контрольный образец активатора: PRP активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 1: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/3 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на 1 мл PRP.
- Образец композиции 2: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 1/2 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/2 начального объема. Композицию активируют при следующих соотношениях объема активатора/композиции:
1. Супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP (композиция 2).
2. Супернатантом PRP (235,8 мкл) и 14,2 мкл 10% хлорида кальция на каждый 1 мл PRP (композиция 2A).
3. Супернатантом PRP (166,7 мкл) и 10 мкл 10% хлорида кальция на каждый 1 мл PRP (композиция 2B).
- Образец Tisseel®: Коммерчески доступный адгезив и герметик Tisseel® (Baxter S. L., Valencia, Spain) были закуплены и использованы в соответствии с инструкциями производителя.
Два предметных стекла были склеены с использованием ранее описанных образцов после активации. Образцы инкубировали в дистиллированной воде, а затем измеряли силу адгезии композиции с использованием граммовых гирь. На фигуре 5 показано, что адгезионная прочность композиций согласно изобретению может быть также повышена путем оптимизации объема добавленного активатора (композиция 2В). Результаты также показали, что адгезионная прочность композиции согласно изобретению (композиции 2B) сравнима с адгезионной прочностью коммерчески доступного герметика Tisseel®.
Пример 6
В этом примере сначала берут образец из 7 герметичных пробирок (9 мл), содержащих кровь, взятую у пациента. Пробирки центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. В результате центрифугирования, кровь, содержащаяся в каждой пробирке, разделяется на несколько фракций. Верхнюю фракцию или фракцию богатой тромбоцитами плазмы (PRP) экстрагируют в белую пробирку с получением всего 24 мл плазмы. Плазму распределяют по 4 пробиркам, каждая из которых содержит 6 мл плазмы. Образцы обрабатывают следующим образом:
- Контрольный образец активатора: PRP активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 1: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 2/3 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/3 начального объема. Композицию активируют супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP.
- Образец композиции 2: Температуру PRP повышают до 51°С. Затем образец центрифугируют со скоростью 580 × g в течение 8 минут при комнатной температуре. Затем удаляют 1/2 начального объема, и осадок тромбоцитов и белка ресуспендируют в оставшейся 1/2 начального объема. Композицию активируют при следующих соотношениях объема активатора/композиции:
1. Супернатантом PRP (333 мкл) и 20 мкл 10% хлорида кальция на каждый 1 мл PRP (композиция 2).
2. Супернатантом PRP (166,7 мкл) и 10 мкл 10% хлорида кальция на каждый 1 мл PRP (композиция 2В).
- Образец Tisseel®: Коммерчески доступный адгезив и герметик Tisseel® (Baxter S. L., Valencia, Spain) были закуплены и использованы в соответствии с инструкциями производителя
Были приготовлены биологические образцы свиной кожи. Образцы кожи приклеивали к подложке с помощью универсального клея. Затем, к ранее описанным образцам приклеивали два образца кожи. После этого измеряли адгезионную прочность композиции с использованием граммовых гирь, которые подвешивали на подставке для образца кожи. На Фигуре 6 показана новизна и эффективность настоящего изобретения с точки зрения повышения адгезионной прочности, а также показано, что адгезионная прочность может быть дополнительно увеличена за счет оптимизации объема добавленного активатора (композиция 2В). Результаты также показали, что адгезионная прочность композиции согласно изобретению (композиции 2В) сравнима с адгезионной прочностью коммерчески доступного герметика Tisseel®.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ НА ОСНОВЕ КОМПОЗИЦИИ КРОВИ, КОТОРАЯ ЯВЛЯЕТСЯ ОБОГАЩЕННОЙ ТРОМБОЦИТАМИ И/ИЛИ ФАКТОРАМИ РОСТА И СОДЕРЖИТ ГЕЛЕОБРАЗНЫЕ БЕЛКИ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2697249C2 |
| СПОСОБ, ПРОБИРКА И УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2011 |
|
RU2667964C1 |
| СПОСОБ, ПРОБИРКА И УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2011 |
|
RU2614722C2 |
| СПОСОБ ПОЛУЧЕНИЯ БОГАТОЙ ТРОМБОЦИТАМИ ПЛАЗМЫ И СПОСОБ ПОЛУЧЕНИЯ ТРОМБОФИБРИНОВОГО ГЕЛЯ ИЛИ СГУСТКА С СЫВОРОТКОЙ, СОДЕРЖАЩИЕ ФАКТОРЫ РОСТА, ИЗ НЕСТАБИЛИЗИРОВАННОЙ ВЕНОЗНОЙ КРОВИ | 2019 |
|
RU2717448C1 |
| Способ получения обогащенного тромбоцитами фибринового матрикса с фиксированным в фибриновой сети остеозамещающим материалом или аутокрошкой из костной или хрящевой ткани | 2023 |
|
RU2802583C1 |
| Способ получения обогащенного тромбоцитами фибринового матрикса различных форм и размеров | 2023 |
|
RU2811233C1 |
| Способ лечения дефектов роговицы различной этиологии | 2023 |
|
RU2809012C1 |
| Нанодисперсная пластическая биоинженерная композиция на основе диоксида церия для восполнения объема костной ткани | 2021 |
|
RU2793324C1 |
| СЫВОРОТОЧНАЯ ФРАКЦИЯ ОБОГАЩЕННОГО ТРОМБОЦИТАМИ ФИБРИНА | 2014 |
|
RU2711330C2 |
| Способ приготовления аутологичного двухкомпонентного фибринового клея | 2019 |
|
RU2704256C1 |
Изобретение относится к области медицины, а именно к способу приготовления адгезивной композиции из исходной композиции крови. Способ приготовления адгезивной композиции из исходной композиции крови, где указанный способ включает следующие стадии: а) получение исходной композиции крови человеческого или животного происхождения, представляющей собой плазму крови, обогащенную тромбоцитами; b) повышение температуры исходной композиции крови до температуры 40-53°С; c) центрифугирование композиции крови и d) активация тромбоцитов с помощью супернатанта PRP 333 мкл и 20 мкл кальция на каждый 1 мл композиции и образование фибрин-содержащей композиции, содержащей фибриновый сгусток, со временем коагуляции менее 4,5 мин. Вышеописанный способ позволяет получать адгезивную композицию с желательными биологическими или терапевтическими свойствами, полученную из исходной композиции крови, богатой тромбоцитами и/или факторами роста, которая может быть приготовлена во время хирургического вмешательства и может иметь повышенную тканевую адгезию. 8 з.п. ф-лы, 6 ил., 6 пр.
1. Способ приготовления адгезивной композиции из исходной композиции крови, где указанный способ включает следующие стадии:
а) получение исходной композиции крови человеческого или животного происхождения, представляющей собой плазму крови, обогащенную тромбоцитами;
b) повышение температуры исходной композиции крови до температуры 40-53°С;
c) центрифугирование композиции крови и
d) активация тромбоцитов с помощью супернатанта PRP 333 мкл и 20 мкл кальция на каждый 1 мл композиции и образование фибрин-содержащей композиции, содержащей фибриновый сгусток, со временем коагуляции менее 4,5 мин.
2. Способ по п. 1, где исходная композиция крови дополнительно содержит высвобожденные факторы роста.
3. Способ по п. 1, также включающий дополнительную стадию удаления части объема исходной композиции после стадии b).
4. Способ по п. 1, где стадия активации тромбоцитов дополнительно включает добавление по меньшей мере одного из следующих компонентов: кальция, тромбина, глюконата натрия, коллагена, супернатанта плазмы крови и супернатанта плазмы крови, богатого факторами роста.
5. Способ по п. 1, где композиция включает один или более биоактивных агентов, выбранных из белков, пептидов, нуклеиновых кислот, полисахаридов, липидов, небелковых органических веществ и неорганических веществ.
6. Способ по п. 1, где композиция включает один или более биоразлагаемых полимеров, выбранных из гиалуроновой кислоты, солей гиалуроновой кислоты, хондроитин-4-сульфата, хондроитин-6-сульфата, декстрана, силикагеля, альгината, гидроксипропилметилцеллюлозы, производных хитина, предпочтительно хитозана, ксантановой камеди, агарозы, полиэтиленгликоля (ПЭГ), полигидроксиэтиленметакрилата (HEMA), синтетических или природных белков и коллагенов.
7. Способ по п. 1, где композиция включает один или более органических полимеров, выбранных из группы, состоящей из поликапролактона, полигликолевой кислоты, полимолочной кислоты и их сополимеров.
8. Способ по п. 1, где композиция содержит один или более из следующих агентов: антибиотиков, противомикробных средств, противораковых средств, анальгетиков, факторов роста, гормонов.
9. Способ по п. 1, где композиция включает один или более неорганических компонентов, выбранных из группы, состоящей из солей кальция, солей магния и/или солей стронция.
| US 2015037430 A1, 05.02.2015 | |||
| ЭЛЕКТРОННОЕ УСТРОЙСТВО, СПОСОБ И ПРОГРАММА УПРАВЛЕНИЯ ИМ И АККУМУЛЯТОР ДЛЯ ОБЕСПЕЧЕНИЯ РАБОТЫ ЭЛЕКТРОННОГО УСТРОЙСТВА | 2006 |
|
RU2369945C2 |
| СПОСОБ КРИСТАЛЛИЗАЦИИ КАРБОНОВОЙ КИСЛОТЫ | 1999 |
|
RU2221770C2 |
| Кишкун А.А | |||
| и др | |||
| Организация преаналитического этапа при централизации лабораторных исследований | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Ссылка на источник: https://web.archive.org/web/20181024162459/http://www.transfusion.ru/2016/08-31-2.pdf, стр | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
Авторы
Даты
2024-06-03—Публикация
2020-01-22—Подача