ПЕРЕКРЕСТНАЯ ССЫЛКА НА СМЕЖНУЮ ЗАЯВКУ
Настоящая заявка заявляет приоритет предварительной патентной заявки США, серийный номер 61/579351, поданной 22 декабря 2011 г., которая включена в настоящее описание посредством ссылки во всей своей полноте для всех целей.
ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области дифференцировки клеток. Более конкретно, настоящее изобретение относится к одногормональным инсулинпродуцирующим клеткам, дифференцированным из плюрипотентных стволовых клеток с использованием определенных условий на каждой стадии поэтапной дифференцировки. Более 10% дифференцированных инсулинпродуцирующих клеток из группы экспрессируют маркеры, характерные для одногормональных бета-клеток поджелудочной железы.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Последние достижения в области заместительной клеточной терапии для лечения сахарного диабета 1-го типа и нехватка островков Лангерганса для трансплантации заставили обратить внимание на разработку источников инсулинпродуцирующих клеток, или β-клеток, подходящих для трансплантации. Одним из подходов является формирование функциональных β-клеток из плюрипотентных стволовых клеток, таких как, например, эмбриональные стволовые клетки.
При эмбриональном развитии позвоночных плюрипотентные клетки дают начало группе клеток, содержащих три зародышевых листка (эктодерму, мезодерму и эндодерму), в ходе процесса, именуемого гаструляцией. Ткани, такие как ткань щитовидной железы, вилочковой железы, поджелудочной железы, кишечника и печени, будут развиваться из энтодермы через промежуточную стадию. Промежуточной стадией в этом процессе является формирование дефинитивной энтодермы. Дефинитивные клетки энтодермы экспрессируют ряд маркеров, таких как HNF3beta, GATA4, MIXL1, CXCR4 и SOX17.
К концу гаструляции энтодерма разделяется на передний и задний отделы, которые могут быть распознаны по экспрессии целого ряда факторов, однозначно выделяющих переднюю, среднюю и заднюю области энтодермы. Например, Hhex и Sox2 идентифицируют переднюю область, в то время как Cdx1, 2 и 4 идентифицируют заднюю половину энтодермы.
Миграция ткани энтодермы приближает энтодерму как можно ближе к различным мезодермальным тканям, которые способствуют регионализации кишечной трубки. Это достигается за счет целого ряда секретируемых факторов, таких как FGFs, Wnts, TGF-Bs, ретиноевой кислоты (RA), лигандов BMP и их антагонистов. Например, FGF4 и BMP способствуют экспрессии Cdx2 в предполагаемой энтодерме задней кишки и подавляют экспрессию передних генов Hhex и SOX2 (Development 2000, 127:1563-1567). Было продемонстрировано, что сигнализация WNT также действует параллельно с сигнализацией FGF, способствуя развитию задней кишки и препятствуя зачаткам передней кишки (Development 2007, 134:2207-2217). Наконец, ретиноевая кислота, секретируемая мезенхимой, регулирует границу между передней и задней кишкой (Curr Biol 2002, 12:1215-1220).
Уровень экспрессии специфических факторов транскрипции может использоваться для определения типа ткани. Во время преобразования дефинитивной энтодермы в примитивную кишечную трубку кишечная трубка становится разделенной на широкие отделы, которые можно наблюдать на молекулярном уровне с помощью ограниченных паттернов экспрессии генов. Например, регионализованный отдел поджелудочной железы в кишечной трубке демонстрирует очень высокую экспрессию PDX-1 и очень низкую экспрессию CDX2 и SOX2. Аналогично, наличие высоких уровней Foxe1 свидетельствует о ткани пищевода; в легочной ткани высок уровень экспрессии NKX2.1; в ткани желудка высок уровень экспрессии SOX2/Odd1 (OSR1); уровень экспрессии PROX1/Hhex/AFP высок в ткани печени; SOX17 имеет высокий уровень экспрессии в тканях желчного тракта; высок уровень экспрессии PDX1, NKX6.1/PTf1a и NKX2.2 в ткани поджелудочной железы; а уровень экспрессии CDX2 высок в ткани кишечника. Сводка, приведенная выше, взята из Dev Dyn 2009, 238:29-42 и Annu Rev Cell Dev Biol 2009, 25:221-251.
Формирование поджелудочной железы происходит в результате дифференцировки дефинитивной энтодермы в энтодерму поджелудочной железы (Annu Rev Cell Dev Biol 2009, 25:221-251; Dev Dyn 2009, 238:29-42). Дорсальный и вентральный отделы поджелудочной железы формируются из эпителия передней кишки. Передняя кишка также дает начало формирования пищевода, трахеи, легких, щитовидной железы, желудка, печени, поджелудочной железы и системы желчных протоков.
Клетки энтодермы поджелудочной железы экспрессируют панкрео-дуоденальный, содержащий гомеобокс ген PDX1. При отсутствии Pdx1 развитие поджелудочной железы не идет дальше формирования вентрального и дорсального зачатков. Таким образом, экспрессия PDX1 характеризует критическую стадию органогенеза поджелудочной железы. Зрелая поджелудочная железа содержит, помимо других типов клеток, экзокринную ткань и эндокринную ткань. Экзокринная и эндокринная ткани образуются при дифференцировке панкреатической эндодермы.
D'Amour и др. описывает производство обогащенных культур дефинитивной энтодермы, полученной из эмбриональных стволовых клеток человека в присутствии высокой концентрации активина и низкой концентрации сыворотки (Nature Biotechnol 2005, 23:1534-1541; патент США № 7704738). Трансплантация этих клеток под капсулу почки у мышей приводила к дифференцировке в более зрелые клетки с характеристиками ткани энтодермы (патент США № 7704738). Клетки дефинитивной энтодермы, полученные из эмбриональных стволовых клеток человека, могут быть далее дифференцированы в PDX1-позитивные клетки после добавления FGF-10 и ретиноевой кислоты (патентная публикация США № 2005/0266554A1). Последующая трансплантация этих клеток-предшественников поджелудочной железы под капсулу почки у мышей с иммунодефицитом приводила к формированию функциональных эндокринных клеток поджелудочной железы после этапа созревания в течение 3-4 месяцев (патент США № 7993920 и 7534608).
Fisk и др. сообщают о системе получения клеток панкреатических островков из эмбриональных стволовых клеток человека (патент США № 7033831). В данном случае процесс дифференцировки был разделен на три стадии. Эмбриональные стволовые клетки человека сначала были дифференцированы в энтодерму при помощи сочетания бутирата натрия и активина A (патент США № 7326572). Затем клетки культивировали с антагонистами BMP, такими как Noggin, в сочетании с EGF или бета-целлюлином для генерирования PDX1-позитивных клеток. Окончательная дифференцировка запускалась никотинамидом.
Ингибиторы в виде небольших молекул также использовались для индуцирования предшественников эндокринных клеток поджелудочной железы. Например, ингибиторы в виде небольших молекул рецепторов TGF-B и рецепторов BMP (Development 2011, 138:861-871; Diabetes 2011, 60:239-247) использовались для значительного увеличения количества получаемых эндокринных клеток поджелудочной железы. Кроме того, активирующие молекулы небольших размеров также использовались для генерирования клеток дефинитивной энтодермы или клеток-предшественников поджелудочной железы (Curr Opin Cell Biol 2009, 21:727-732; Nature Chem Biol 2009, 5:258-265).
Предыдущие попытки индуцирования предшественников клеток поджелудочной железы из эмбриональных стволовых клеток человека выявили важность совместной экспрессии PDX-1 и NKX6.1 для корректной идентификации энтодермы поджелудочной железы. Тем не менее, хотя исследования в данной области определили, что в группе клеток с положительной экспрессией PDX-1 и NKX6.1 экспрессия CDX2 невелика или отсутствует, предыдущие отчеты не смогли дать ответ на вопрос о наличии маркеров непосредственно перед развивающейся поджелудочной железой. SOX2, который является маркером передней энтодермы, не экспрессируется во взрослых островках и экспрессируется на очень низком уровне в развивающейся поджелудочной железе (Diabetes 2005, 54:3402-4309). Напротив, некоторые из примеров в данной заявке описывают группы клеток, в которых по меньшей мере 30% клеток энтодермы поджелудочной железы, полученных из эмбриональных стволовых клеток человека, положительны по экспрессии PDX-1 и NKX6.1 и отрицательны по экспрессии CDX2 и SOX2.
Все предыдущие попытки создания функциональных бета-клеток поджелудочной железы не привели к генерированию клеток с характеристиками зрелых бета-клеток. Отличительные особенности зрелых бета-клеток включают в себя экспрессию гормона инсулина, корректную переработку проинсулина в инсулин и С-пептид, сильную экспрессию PDX-1 и NKX6.1, соответствующее выделение инсулина в ответ на глюкозу, экспрессию транспортеров глюкозы и сильную экспрессию глюкокиназы. Все предшествующие отчеты сообщали об эндокринных клетках, которые производят два или более гормона поджелудочной железы. Например, D'Amour и др. (Nature Biotech 2006, 24:1392-1401) сообщают о получении группы клеток, содержащих ~10% инсулинположительных клеток и ~20% эндокринных клеток по измерению синаптофизином. Подобные сообщения других (Cell Res 2009, 19:429-438; Stem Cells 2007, 25:1940-1953; Diabetes Obes Metab 2008, 10:186-194) также продемонстрировали дифференцировку плюрипотентных клеток в нефункциональные инсулинположительные клетки. Действительно, недавние исследования определенно установили, что трансплантация полигормональных клеток у мышей с тяжелым комбинированным иммунодефицитом (ТКИД) не привела к образованию функциональных бета-клеток (Diabetes 2011, 60:239-247; Nature Biotech 2011, 29:750-756). В то время как в поджелудочной железе плода человека часть (~10-20%) эндокринных клеток является полигормональными клетками, полигормональные клетки исчезают и отсутствуют в поджелудочной железе взрослого человека (Histochem Cell Biol 1999, 112:147-153; J Histochem Cytochem 2009, 57:811-824).
По мере совершенствования растущей отрасли регенеративной медицины способ получения окончательно дифференцированных и надлежащим образом регулируемых эндокринных клеток поджелудочной железы становится весьма востребованным. Мы демонстрируем в настоящем документе, что при соответствующем и определенном воздействии на условия развития культуры клеток и точных сроках добавления активаторов/ингибиторов различных путей развития эмбриональные стволовые клетки человека могут быть дифференцированы in vitro в функционирующие бета-клетки поджелудочной железы. В частности, точный момент ингибирования BMP с использованием градиента ретиноевой кислоты наряду с использованием витамина C подтвердил свою эффективность при получении одногормональных эндокринных клеток поджелудочной железы.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает создание группы клеток линии дифференцировки энтодермы поджелудочной железы, полученной in vitro путем поэтапной дифференцировки плюрипотентных клеток. Среда, используемая на каждой стадии дифференцировки, дополняется глюкозой. В некоторых вариантах осуществления на каждой стадии дифференцировки клетки культивируются в среде, содержащей от 5 до 20 мМ глюкозы.
В некоторых вариантах осуществления дифференцировка плюрипотентных стволовых клеток генерирует группы клеток энтодермы поджелудочной железы, где больше 10% клеток в дифференцированной группе экспрессируют маркеры, характерные для одногормональных бета-клеток поджелудочной железы.
В некоторых вариантах осуществления дифференцировки плюрипотентных стволовых клеток генерирует группу клеток энтодермы поджелудочной железы, где более 30% дифференцированной группы положительны по экспрессии PDX-1 и NKX6.1, но в то же время отрицательны по экспрессии CDX2 и SOX2.
В некоторых вариантах осуществления поэтапная дифференцировка содержит культивирование недифференцированных эмбриональных стволовых клеток человека в среде, дополненной лигандом TGF-B. В некоторых вариантах осуществления поэтапная дифференцировка содержит культивирование недифференцированных эмбриональных стволовых клеток человека в среде, дополненной активатором WNT. В некоторых вариантах осуществления поэтапная дифференцировка содержит культивирование дефинитивных клеток энтодермы в среде, далее дополненной лигандом FGF. В некоторых вариантах осуществления поэтапная дифференцировка содержит культивирование клеток кишечной трубки в среде, далее дополненной ингибитором shh, лигандом FGF, активатором PKC, лигандом TGF-B, ретиноидом и градиентом ингибитора BMP. В некоторых вариантах осуществления поэтапная дифференцировка содержит культивирование задних клеток переднего кишечника в среде, далее дополненной активатором PKC, ингибитором shh, ретиноидом и ингибитором BMP. В некоторых вариантах осуществления поэтапная дифференцировка содержит культивирование клеток в среде, далее дополненной аскорбиновой кислотой.
В варианте осуществления изобретение обеспечивает способ in vitro для поэтапной дифференцировки плюрипотентных клеток в группу линии дифференцировки клеток энтодермы поджелудочной железы, которая содержит культивирование клеток на каждой стадии дифференцировки в среде, содержащей от 5 до 20 мМ глюкозы. В некоторых вариантах осуществления способ in vitro для поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку плюрипотентных клеток в клетки дефинитивной энтодермы (DE) путем культивирования плюрипотентных клеток в среде, дополненной лигандом TGF-B и активатором WNT. В некоторых вариантах осуществления способ in vitro поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку клеток DE в клетки кишечной трубки путем культивирования клеток DE в среде, дополненной лигандом FGF. В некоторых вариантах осуществления способ in vitro поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку клеток кишечной трубки в задние клетки энтодермы передней кишки путем культивирования клеток кишечной трубки в среде, дополненной ингибитором shh, лигандом FGF, активатором PKC, лигандом TGF-B, ретиноидом и ингибитором BMP. В некоторых вариантах осуществления способ in vitro поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку клеток кишечной трубки в задние клетки энтодермы передней кишки путем культивирования клеток кишечной трубки в среде, дополненной ингибитором shh, лигандом FGF, активатором PKC, лигандом TGF-B, ретиноидом и ингибитором BMP. В некоторых вариантах осуществления способ in vitro поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку задних клеток энтодермы передней кишки в клетки поджелудочной железы передней кишки путем культивирования задних клеток энтодермы передней кишки в среде, дополненной активатором PKC, ингибитором shh, ретиноидом и ингибитором BMP. В некоторых вариантах осуществления способ in vitro поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку клеток поджелудочной железы передней кишки в клетки энтодермы поджелудочной железы путем культивирования поджелудочной железы передней кишки в среде, дополненной ингибитором shh, ингибитором TGF-B и ретиноидом. В некоторых вариантах осуществления способ in vitro поэтапной дифференцировки плюрипотентных клеток дополнительно содержит дифференцировку клеток энтодермы поджелудочной железы в группу бета-клеток поджелудочной железы.
В варианте осуществления по меньшей мере на одной стадии способа in vitro поэтапной дифференцировки плюрипотентных клеток среда далее дополняется аскорбиновой кислотой. В некоторых вариантах осуществления более 10% клеток в дифференцированной группе являются одногормональными инсулинположительными клетками. В некоторых вариантах осуществления более 30% клеток энтодермы поджелудочной железы в культуре, полученной способами данного изобретения, являются PDX-1+, NKX6.1+, SOX2- и CDX2-.
В варианте осуществления изобретение относится к способу in vitro дифференцировки эмбриональных стволовых клеток человека в бета-клетки поджелудочной железы и содержит: а) культивирование недифференцированных эмбриональных стволовых клеток человека в среде, дополненной глюкозой, лигандом TGF-B и активатором WNT, для генерирования группы клеток дефинитивной энтодермы (DE); b) культивирование клеток DE в среде, дополненной глюкозой и лигандом FGF, для генерирования группы клеток кишечной трубки; c) культивирование клеток кишечной трубки в среде, дополненной глюкозой, ингибитором shh, лигандом FGF, активатором PKC, лигандом TGF-B, ретиноидом и градиентом ингибитора BMP, для генерирования группы задних клеток энтодермы передней кишки, экспрессирующих PDX-1 и SOX2; d) культивирование клеток передней кишки в среде, дополненной глюкозой, активатором PKC, ингибитором shh, ретиноидом и ингибитором BMP, для генерирования группы клеток передней кишки поджелудочной железы, экспрессирующих PDX-1 и NKX6.1 и экспрессирующих более низкий уровень SOX2 по сравнению с задними клетками передней кишки; e) культивирование клеток поджелудочной железы передней кишки в среде, дополненной глюкозой, ингибитором shh, ингибитором TGF-B и ретиноидом, для получения группы клеток энтодермы поджелудочной железы, экспрессирующих PDX-1, более высокий уровень NKX6.1 и более низкий уровень SOX2 по сравнению с клетками поджелудочной железы передней кишки; f) дифференцировка клеток энтодермы поджелудочной железы в группу бета-клеток поджелудочной железы. В некоторых вариантах осуществления группа бета-клеток поджелудочной железы, полученная способами данного изобретения, является PDX-1+, NKX6.1+, SOX2- и CDX2-. В некоторых вариантах осуществления среда по меньшей мере в одном этапе способа поэтапной дифференцировки далее дополняется аскорбиновой кислотой. В некоторых вариантах осуществления бета-клетки поджелудочной железы, полученные способами данного изобретения, являются одногормональными инсулин-продуцирующими клетками, у которых также NKX6.1+ и PDX-1+.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
Фиг. 1A-1G содержат гистограмму профилей экспрессии FACS следующих маркеров в S3, день 2 для клеток, дифференцирующихся согласно примеру 1. Фиг. 1A: изотипный контроль; фиг. 1В: хромогранин; фиг. 1C: KI-67; фиг. 1D: NKX6.1; фиг. 1E: SOX2; фиг. 1F: CDX2; фиг. 1G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
На фиг. 2А-2G показаны профили экспрессии гистограммы FACS следующих маркеров в клетках, дифференцированных согласно примеру 1 и собранных в S4, день 2. Фиг. 2A: изотипный контроль; фиг. 2B: хромогранин; фиг. 2C: KI-67; фиг. 2D: NKX6.1; фиг. 2E: SOX2; фиг. 2F: CDX2; фиг. 2G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
На фиг. 3А-3G показаны профили экспрессии гистограммы FACS следующих маркеров в клетках, дифференцированных согласно примеру 1 и собранных в S5, день 2. Фиг. 3A: изотипный контроль; фиг. 3B: хромогранин; фиг. 3C: KI-67; фиг. 3D: NKX6.1; фиг. 3E: SOX2; фиг. 3F: CDX2; фиг. 3G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
На фиг. 4А-4G показаны профили экспрессии гистограммы FACS следующих маркеров в клетках, дифференцированных согласно примеру 1 и собранных в S5, день 7. Фиг. 4A: изотипный контроль; фиг. 4B: хромогранин; фиг. 4C: KI-67; фиг. 4D: NKX6.1; фиг. 4E: SOX2; фиг. 4F: CDX2; фиг. 4G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
На фиг. 5А-5С изображены профили экспрессии гистограммы FACS следующих маркеров в клетках, дифференцированных согласно примеру 1 и полученных в клетках, собранных в S5, день 2. Фиг. 5A: хромогранин (ось y) и CDX2 (ось x); фиг. 5B: хромогранин (ось y) и SOX2 (ось x); фиг. 5C: хромогранин (ось y) и NKX6.1 (ось x). На каждой гистограмме показан процент совместной экспрессии для каждого графика.
На фиг. 6A-6Т показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 1 и собранных в S2, S3, S4 и S5. Фиг. 6A: CDX2; фиг. 6B: CD142; фиг. 6C: FOXE1; фиг. 6D: HNF4-alpha; фиг. 6E: NKX2.1; фиг. 6F: NKX2.2; фиг. 6G: NKX6.1; фиг. 6H: OSR1; фиг. 6I: PDX-1; фиг. 6J: PROX1; фиг. 6K: PTF1a; фиг. 6L: SOX17; фиг. 6M: SOX2; фиг. 6N: инсулин; фиг. 6O: ZIC1; фиг. 6P: хромогранин; фиг. 6Q: глюкагон; фиг. 6R: Ngn3; фиг. 6S: NeuroD; фиг. 6T: соматостатин.
На фиг. 7A-7G показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках линии Н1, дифференцированных согласно примеру 2 и собранных в день 3 S2, S3 или S4. Фиг. 7A: NKX6.1; фиг. 7B: PDX-1; фиг. 7C: хромогранин; фиг. 7D: NGN3; фиг. 7E: CDX2; фиг. 7F: альбумин; фиг. 7G: SOX2.
На фиг. 8A-8G показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих маркеров в клетках H1, дифференцированных согласно примеру 3 и собранных в S2, S3, S4 или S5. Фиг. 8A: NKX6.1; фиг. 8B: PDX-1; фиг. 8C: NGN3; фиг. 8D: NeuroD; фиг. 8E: хромогранин; фиг. 8F: CDX2; фиг. 8G: SOX2.
На фиг. 9A-9Н показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих маркеров в клетках H1, дифференцированных согласно примеру 4 и собранных в день 4 S3 и S4. Фиг. 9A: NKX6.1; фиг. 9B: PDX-1; фиг. 9C: хромогранин; фиг. 9D: NGN3; фиг. 9E: NeuroD; фиг. 9F: CDX2; фиг. 9G: альбумин; фиг. 9H: SOX2.
На фиг. 10A-10Н показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 5 и собранных на этапе 4. Фиг. 10A: NKX6.1; фиг. 10B: PDX-1; фиг. 10C: хромогранин; фиг. 10D: NGN3; фиг. 10E: NeuroD; фиг. 10F: CDX2; фиг. 10G: альбумин; фиг. 10H: SOX2.
На фиг. 11A-11Н показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 6 и собранных в день 3 S3 или S6. Фиг. 11A: NKX6.1; фиг. 11B: PDX-1; фиг. 11C: хромогранин; фиг. 11D: NGN3; фиг. 11E: NeuroD; фиг. 11F: CDX2; фиг. 11G: альбумин; фиг. 11H: SOX2.
На фиг. 12A-12G показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 7 и собранных в день 3 S3, S4 или S5. Фиг. 12A: NKX6.1; фиг. 12B: PDX-1; фиг. 12C: хромогранин; фиг. 12D: NGN3; фиг. 12E: NeuroD; фиг. 12F: CDX2; фиг. 12G: SOX2.
На фиг. 13A-13G показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 8 и собранных в S3, S4, S5 или S6. Фиг. 13A: NKX6.1; фиг. 13B: PDX-1; фиг. 13C: хромогранин; фиг. 13D: NGN3; фиг. 13E: NeuroD; фиг. 13F: CDX2; фиг. 13G: SOX2.
Фиг. 14A-14Р содержат гистограмму профилей экспрессии FACS следующих маркеров в S3, день 4 для клеток, дифференцирующихся согласно примеру 9. Фиг. 14A: изотипный контроль; фиг. 14B: хромогранин; фиг. 14C: KI-67; фиг. 14D: NKX6.1; фиг. 14E: SOX2; фиг. 14F: HNF3B; фиг. 14G: CDX2; фиг. 14H: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
Фиг. 15A-15G содержат гистограмму профилей экспрессии FACS следующих маркеров в S4, день 2 для клеток, дифференцирующихся согласно примеру 9. Фиг. 15A: изотипный контроль; фиг.15B: NKX6.1; фиг. 15C: KI-67; фиг. 15D: хромогранин; фиг. 15E: SOX2; фиг. 15F CDX2; фиг. 15G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
Фиг. 16A-16F содержат гистограмму профилей экспрессии FACS следующих маркеров в S4, день 4 для клеток, дифференцирующихся согласно примеру 9. Фиг. 16A: изотипный контроль; фиг. 16B: NKX6.1; фиг. 16C: хромогранин; фиг. 16D: SOX2; фиг. 16E: CDX2; фиг. 16F: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
На фиг. 17A-17J показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 9 и собранных в S1D3, S2D3, S3D4, S4D2 и S4D4. Фиг. 17A: CDX2; фиг. 17B: HHex; фиг. 17C: FOXE1; фиг. 17D: IPF1 (PDX-1); фиг. 17E: NKX2.1; фиг. 17F: NKX2.2; фиг. 17G: NKX6.1; фиг. 17H: PROX1; фиг. 17I: SOX2; фиг. 17J: SOX9.
Фиг. 18A-18G содержат гистограмму профилей экспрессии FACS следующих маркеров в S3, день 3 для клеток, дифференцирующихся согласно примеру 10. Фиг. 18A: изотипный контроль; фиг. 18B: NKX6.1; фиг. 18C: хромогранин; фиг. 18D: SOX2; фиг. 18E: CDX2; фиг. 18F: KI-67; фиг. 18G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
Фиг. 19A-19G показывают FACS-гистограмму профилей экспрессии следующих маркеров на этапе S4, день 5 у клеток, дифференцированных согласно примеру 10. Фиг. 19A: изотипный контроль; фиг. 19B: NKX6.1; фиг. 19C: хромогранин; фиг. 19D: SOX2; фиг. 19E: CDX2; фиг. 19F: KI-67; фиг. 19G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
На фиг. 20A-20J показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 11. Фиг. 20A: соматостатин; фиг. 20B: PDX1; фиг. 20C: Pax6; фиг. 20D: Pax4; фиг. 20E: NKX6.1; фиг. 20F: NGN3; фиг. 20G: глюкагон; фиг. 20H: NeuroD; фиг. 20I: инсулин; фиг. 20J: хромогранин.
На фиг. 21A-21J показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1 человека, дифференцированных согласно примеру 12 и собранных в S4, день 2, S5, день 2 и S5, день 9. Фиг. 21A: соматостатин; фиг. 21B: PDX1; фиг. 21C: Pax6; фиг. 21D: Pax4; фиг. 21E: NKX6.1; фиг. 21F: NGN3; фиг. 21G: NeuroD; фиг. 21H: инсулин; фиг. 21I: глюкагон; фиг. 21J: хромогранин.
На фиг. 22A-22L показаны данные анализов ПЦР в реальном времени относительно экспрессии следующих генов в клетках эмбриональных стволовых клеток линии H1, дифференцированных согласно примеру 13 и собранных на S5, день 3. Фиг. 22A: Pax4; фиг. 22B: Pax6; фиг. 22C: PDX1; фиг. 22D: PTF1a; фиг. 22E: глюкагон; фиг. 22F: инсулин; фиг. 22G: NeuroD; фиг. 22H: ngn3; фиг. 22I: Zic1; фиг. 22J: CDX2; фиг. 22K: альбумин; фиг. 22L: NKX6.1.
ПОДРОБНОЕ ОПИСАНИЕ
Для ясности описания, а не для ограничения изобретения, подробное описание изобретения разделено на следующие подразделы, описывающие или иллюстрирующие определенные особенности, варианты осуществления или области применения настоящего изобретения.
Определения
Стволовые клетки представляют собой недифференцированные клетки, определяемые как обладающие способностью на одноклеточном уровне к самообновлению и дифференцировке. Стволовые клетки могут производить клетки-потомки, включая самообновляющиеся прогениторные клетки, необновляющиеся прогениторные клетки и окончательно дифференцированные клетки. Стволовые клетки также характеризуются своей способностью дифференцироваться in vitro в функциональные клетки различных линий из множества зародышевых листков (энтодермы, мезодермы и эктодермы). Стволовые клетки также дают начало тканям множества зародышевых листков после трансплантации и вносят значительный вклад в образование большинства, если не всех тканей после инъекции в бластоцисты.
Стволовые клетки классифицируют по потенциалу развития: (1) тотипотентные, то есть способные преобразоваться в любой из эмбриональных и внеэмбриональных типов клеток; (2) плюрипотентные, то есть способные преобразоваться во все типы эмбриональных клеток; (3) мультипотентные, то есть способные преобразоваться во множество клеточных линий, но в рамках одной ткани, органа или физиологической системы (например, гемопоэтические стволовые клетки (ГСК) могут порождать ГСК (самообновление), олигопотентные ограниченные клетки-предшественники крови и все типы клеток и элементов (например, тромбоциты), являющиеся стандартными составляющими крови); (4) олигопотентные, то есть способные преобразоваться в более ограниченное подмножество клеточных линий, чем мультипотентные стволовые клетки; и (5) унипотентные, то есть способные преобразоваться в единственную клеточную линию (например, сперматогенные стволовые клетки).
Дифференцировка представляет собой процесс, при помощи которого неспециализированная («некоммитированная») или менее специализированная клетка приобретает свойства специализированной клетки, например нервной или мышечной клетки. Дифференцированная клетка или клетка, индуцированная дифференцировкой, представляет собой клетку, взятую на более специализированном («коммитированном») этапе линии развития клетки. Термин «коммитированный» в применении к процессу дифференцировки относится к клетке, которая прошла по пути дифференцировки до того этапа, на котором при нормальных условиях она продолжит дифференцироваться в клетку заданного типа или подмножества типов клеток и при этом не может в нормальных условиях дифференцироваться в клетку другого типа или возвращаться к клетке менее дифференцированного типа. Дедифференцировка относится к процессу, в ходе которого клетка возвращается на менее специализированный (или коммитированный) этап линии развития клетки. Используемый в настоящей заявке термин «линия дифференцировки клетки» определяет наследственность клетки, то есть определяет, из какой клетки произошла данная клетка и каким клеткам она может дать начало. В клеточной линии дифференцировки клетка помещается в наследственную схему развития и дифференцировки. Маркером, специфичным для линии дифференцировки, называется характерная особенность, специфически ассоциированная с фенотипом клеток конкретной линии дифференцировки, которая может использоваться для оценки дифференцировки некоммитированных клеток в клетки данной линии дифференцировки.
Используемый в настоящей заявке термин «маркеры» означает молекулы нуклеиновых кислот или полипептидов с дифференциальной экспрессией в интересующих клетках. В данном контексте под дифференциальной экспрессией подразумевается повышение уровня экспрессии для положительного маркера и понижение уровня экспрессии для отрицательного маркера. Поддающийся обнаружению уровень маркерной нуклеиновой кислоты или полипептида в интересующих клетках оказывается значительно выше или ниже по сравнению с другими клетками, что позволяет идентифицировать интересующую клетку и отличить ее от других клеток с помощью любого из множества известных в данной области способов.
В настоящем документе клетка «положительна по» заданному маркеру или «положительна», если заданный маркер обнаруживается в клетке. Аналогично клетка «отрицательна по» заданному маркеру или «отрицательна», если заданный маркер не обнаруживается в клетке.
В настоящем документе «этап 1» и «S1» используются взаимозаменяемо для обозначения клеток, экспрессирующих маркеры, характерные для дефинитивной энтодермы (DE).
«Сформированная энтодерма», как используется в настоящем документе, относится к клеткам, которые несут в себе характеристики клеток, появившиеся из эпибласта во время гаструляции, и которые формируют желудочно-кишечный тракт и его производные. Клетки дефинитивной энтодермы экспрессируют по меньшей мере один из следующих маркеров: HNF3 beta, GATA4, SOX17, CXCR4, Cerberus, OTX2, goosecoid, C-Kit, CD99 и MIXL1.
Выражение «кишечная трубка» в настоящем документе относится к клеткам, полученным из дефинитивной эндодермы, экспрессирующим по меньшей мере один из следующих маркеров: HNF3-beta, HNF1-beta или HNF4-alpha. Клетки кишечной трубки могут дать начало всем энтодермальным органам, таким как легкие, печень, поджелудочная железа, желудок и кишечник.
Используемые в настоящем документе взаимозаменяемые выражения «этап 2» и «S2» обозначают клетки, экспрессирующие маркеры, характерные для примитивной кишечной трубки.
«Энтодерма передней кишки» относится к клеткам энтодермы, которые дают начало пищеводу, легких, желудка, печени, поджелудочной железы, желчного пузыря и части двенадцатиперстной кишки.
«Задняя часть передней кишки» относится к клеткам энтодермы, которые могут дать начало задней части желудка, поджелудочной железы, печени и части двенадцатиперстной кишки.
«Энтодерма средней кишки» относится к клеткам энтодермы, которые могут дать начало кишечнику, частям двенадцатиперстной кишки, аппендикса и восходящей ободочной кишки.
«Энтодерма задней кишки» относится к клеткам энтодермы, которые могут дать начало дистальной трети поперечной ободочной кишки, нисходящей ободочной кишки, сигмовидной кишки и прямой кишки.
Как «этап 3», так и «S3» используются взаимозаменяемо для обозначения клеток, экспрессирующих маркеры, характерные для энтодермы передней кишки. «Клетки, экспрессирующие маркеры, характерные для линии передней кишки», как используется в настоящем документе, относятся к клеткам, экспрессирующим по меньшей мере один из следующих маркеров: PDX-1, FOXA2, CDX2, SOX2 и HNF4-альфа.
Используемые в настоящем документе взаимозаменяемо «этап 4» и «S4» обозначают клетки, экспрессирующие маркеры, характерные для предшественника передней кишки поджелудочной железы. Клетки, экспрессирующие маркеры, характерные для линии предшественника передней кишки поджелудочной железы, как используется в настоящем документе, относится к клеткам, экспрессирующим по меньшей мере один из следующих маркеров: PDX-1, NKX6.1, HNF6, FOXA2, PTF1a, Prox1 и HNF4-альфа.
В настоящем документе выражения «этап 5» и «S5» используются взаимозаменяемо для обозначения клеток, экспрессирующих маркеры, характерные для клеток энтодермы поджелудочной железы и предшественников эндокринной поджелудочной железы. Выражение «клетки, экспрессирующие маркеры, характерные для линии энтодермы поджелудочной железы» в настоящем документе относится к клеткам, экспрессирующим по меньшей мере один из следующих маркеров: PDX1, NKX6.1, HNF1 beta, PTF1 alpha, HNF6, HNF4 alpha, SOX9, HB9 или PROX1. Клетки, экспрессирующие маркеры, характерные для линии энтодермы поджелудочной железы, не экспрессируют существенно CDX2 или SOX2.
В настоящем документе выражения «этап 6» и «S6» используются взаимозаменяемо для обозначения клеток, обогащенных клетками эндокринной поджелудочной железы.
«Панкреатической эндокринной клеткой», или «клеткой, экспрессирующей гормон поджелудочной железы», или «клеткой, экспрессирующей характеристики эндокринной линии поджелудочной железы» в настоящем документе называется клетка, способная экспрессировать по меньшей мере один из следующих гормонов: инсулин, глюкагон, соматостатин, грелин и полипептид поджелудочной железы.
Выражение «клетка-предшественник эндокринной поджелудочной железы» или «прогениторная эндокринной поджелудочной железы» относится к клеткам энтодермы поджелудочной железы, обладающим возможностью стать клеткой поджелудочной железы, экспрессирующей гормон. Такая клетка может экспрессировать по меньшей мере один из следующих маркеров: NGN3, NKX2.2, NeuroD, ISL-1, Pax4, Pax6 или ARX.
Выражение «функциональная бета-клетка поджелудочной железы» в настоящем документе относится к одногормональной инсулинположительной клетке, имеющей возможность реагировать на глюкозу и положительной по PDX-1 и NKX6.1.
Используются в настоящем документе взаимозаменяемо «d1», «d 1» и «день 1»; «d2», «d 2» и «день 2»; «d3», «d 3» и «день 3» и так далее. Эти сочетания цифр и букв указывают день инкубации на различных этапах во время поэтапного протокола дифференцировки по данной заявке.
«Аскорбиновая кислота» и «витамин С» используются в настоящем документе взаимозаменяемо и относятся к важному питательному веществу для человека и других видов животных.
«Глюкоза» и «D-глюкоза» используются в настоящем документе взаимозаменяемо и относятся к декстрозе, сахару, обычно встречающемуся в природе.
Клетка, «положительная» по определенному маркеру или обозначаемая как маркер «+» (т.е. PDX-1+), представляет собой клетку, в которой обнаруживается данный маркер. Клетка, «отрицательная» по определенному маркеру или обозначаемая как маркер «-» (т.е. NKX6.1-), представляет собой клетку, в которой маркер не обнаруживается способами, изложенными в данном описании.
В данной заявке «хромогранин» и «CHGN» используются взаимозаменяемо для обозначения гена, кодирующего кислотный секреторный гликопротеин хромогранин.
Используются взаимозаменяемо в настоящем документе выражения «NeuroD» и «NeuroD1», обозначающие белок, экспрессируемый в клетках-прогениторах эндокринной поджелудочной железы, и ген, кодирующий его.
Используются взаимозаменяемо в настоящем документе выражения «LDN» и «LDN-193189», обозначающие ингибитор рецептора BMP, выпускаемый Stemgent, Калифорния, США.
Выделение, размножение и культивирование полипотентных стволовых клеток
Плюрипотентные стволовые клетки могут экспрессировать один или более стадийно-специфичных эмбриональных антигенов (SSEA) 3 и 4, а также маркеры, определяемые антителами, обозначенными как Tra-1-60 и Tra-1-81 (Thomson et al., Science 282:1145, 1998). Дифференцировка плюрипотентных стволовых клеток in vitro приводит к потере экспрессии SSEA-4, Tra-1-60 и Tra-1-81. Недифференцированные плюрипотентные стволовые клетки, как правило, имеют щелочно-фосфатазную активность, которую можно обнаружить путем обработки клеток 4%-м параформальдегидом, а затем выращивая с Vector Red в качестве субстрата, как описано производителем (Vector Laboratories, штат Калифорния, США). Недифференцированные плюрипотентные стволовые клетки также, как правило, экспрессируют OCT4 и TERT, определяемые с помощью ПЦР в реальном времени.
Другим желательным фенотипическим свойством выращенных плюрипотентных стволовых клеток является потенциал дифференцировки в клетки всех трех зародышевых листков: в эндодермальные, мезодермальные и эктодермальные ткани. Плюрипотентность стволовых клеток может быть подтверждена, например, путем инъекции клеток мышам с тяжелым комбинированным иммунодефицитом (SCID), обработкой всех образующихся тератом 4%-м раствором параформальдегида, а затем гистологическим исследованием на наличие типов клеток из трех зародышевых листков. В качестве альтернативы плюрипотентность можно определить по созданию эмбриоидных телец и анализа их на предмет присутствия маркеров, ассоциирующихся с тремя зародышевыми листками.
Выращенные линии плюрипотентных стволовых клеток могут быть кариотипированы с применением стандартного способа окрашивания с использованием красителя Гимза (G-banding) и сравнения с опубликованными кариотипами соответствующих видов приматов. Желательно получить клетки, имеющие «нормальный кариотип», т.е. эуплоидные клетки, в которых все человеческие хромосомы присутствуют и не имеют видимых изменений. Плюрипотентные клетки могут быть легко размножены в культуре путем использования различных питательных слоев или с помощью сосудов, покрытых белковой матрицей. Кроме того, химически определенные поверхности в сочетании с определенными средами, такими как среды mTesr™ 1 (StemCell Technologies, Ванкувер, Канада), могут использоваться для обычного накопления клеток. Плюрипотентные клетки могут быть легко удалены из чашек с культурой при помощи ферментативной, механической обработки или с использованием различных кальцийхелатирующих агентов, таких как EDTA (этилендиаминтетрауксусная кислота). Кроме того, плюрипотентные клетки могут быть накоплены в суспензии в отсутствии каких-либо матричных белков или питательного слоя.
Источники плюрипотентных стволовых клеток
Среди типов плюрипотентных стволовых клеток, которые могут использоваться, могут быть устойчивые линии плюрипотентных клеток, полученных из тканей, образующихся после беременности, в том числе преэмбриональная ткань (такая как, например, бластоцист), эмбриональная ткань или ткань плода, взятая в любой момент во время беременности, как правило, но не обязательно перед сроком приблизительно от 10 до 12 недель беременности. Неограничивающими примерами являются устойчивые линии эмбриональных стволовых клеток человека (ЭСК) или эмбриональные зародышевые клетки человека, такие как, например, эмбриональные стволовые клетки человека линий H1, H7 и H9 (WiCell Research Institute, Мэдисон, Висконсин, США). Также соответствуют целям настоящего изобретения клетки, взятые из популяции плюрипотентных стволовых клеток, уже культивированных в отсутствие питающих клеток. Также пригодными являются индуцибельные плюрипотентные клетки (IPS) или перепрограммированные плюрипотентные клетки, которые могут быть получены из взрослых соматических клеток с помощью принудительной экспрессии ряда факторов, относящихся к плюрипотентным транскрипционным факторам, таким как OCT4, Nanog, Sox2, KLF4 и ZFP42 (Annu Rev Genomics Hum Genet, 2011, 12:165-185). Эмбриональные стволовые клетки человека, используемые в способах данного изобретения, также могут быть подготовлены, как описано Thomson и др. (патент U.S. № 5843780; Science, 1998, 282:1145; Curr. Top. Dev. Biol., 1998, 38:133; Proc. Natl. Acad. Sci. U.S.A., 1995: 92:7844).
Формирование клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, из плюрипотентных стволовых клеток
Характеристики плюрипотентных стволовых клеток хорошо известны специалистам в данной области, и продолжается выявление дополнительных характеристик плюрипотентных стволовых клеток. К маркерам плюрипотентных стволовых клеток относится, например, экспрессия одного или нескольких следующих маркеров: ABCG2, CRIPTO, FOXD3, Connexin43, Connexin45, OCT4, SOX2, Nanog, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60, Tra 1-81.
К плюрипотентным стволовым клеткам, которые могут использоваться в настоящем изобретении, относятся, например, человеческие эмбриональные стволовые клетки линии H9 (код NIH: WA09), человеческие эмбриональные стволовые клетки линии H1 (код NIH: WA01), человеческие эмбриональные стволовые клетки линии H7 (код NIH: WA07) и человеческие эмбриональные стволовые клетки линии SA002 (Cellartis, Швеция). Также для использования в рамках настоящего изобретения подходят клетки, экспрессирующие по меньшей мере один из следующих маркеров, характерных для плюрипотентных клеток: ABCG2, cripto, CD9, FOXD3, CONNEXIN43, CONNEXIN45, OCT4, SOX2, Nanog, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60 и Tra 1-81.
Маркеры, характерные для сформированной линии энтодермы, выбираются из группы, содержащей SOX17, GATA4, HNF3 beta, GSC, CER1, Nodal, FGF8, Brachyury, Mix-подобный гомеобоксовый белок, FGF4, CD48, эомезодермин (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99 и Otx2. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии сформированной эндодермы. В одном из аспектов настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии сформированной эндодермы, представляет собой клетку-предшественник первичной полоски. В другом аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии сформированной эндодермы, представляет собой мезэндодермальную клетку. В другом аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии сформированной эндодермы, представляет собой клетку сформированной эндодермы.
Маркеры характерные для линии энтодермы поджелудочной железы, выбираются из группы, содержащей PDX1, NKX6.1, HNF1 beta, PTF1 alpha, HNF6, HNF4 alpha, SOX9, HB9 и PROX1. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатической эндодермы. В одном из аспектов данного изобретения экспрессируемые клеткой маркеры, характерные для линейки панкреатической энтодермы, представляют собой клетки панкреатической энтодермы, в которых экспрессия PDX-1 и NKX6.1 значительно превышает экспрессию CDX2 и SOX2.
Маркеры, характерные для линии эндокринной поджелудочной железы, выбираются из группы, состоящей из NGN3, NEUROD, ISL1, PDX1, NKX6.1, PAX4, ARX, NKX2.2 и PAX6. В одном варианте осуществления панкреатическая эндокринная клетка способна к экспрессии по меньшей мере одного из следующих гормонов: инсулин, глюкагон, соматостатин и панкреатический полипептид. Соответствующей целям настоящего изобретения является клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатических эндокринных клеток. В одном из аспектов настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии панкреатических эндокринных клеток, представляет собой панкреатическую эндокринную клетку. Панкреатическая эндокринная клетка может представлять собой панкреатическую клетку, экспрессирующую гормоны. В альтернативном варианте осуществления панкреатическая эндокринная клетка может представлять собой панкреатическую клетку, секретирующую гормоны.
В одном аспекте настоящего изобретения панкреатическая эндокринная клетка представляет собой клетку с экспрессией маркеров, характерных для линии дифференцировки β-клеток. Клетка с экспрессией маркеров, характерных для линии β-клеток, экспрессирует PDX1 и по меньшей мере один из следующих транскрипционных факторов: NKX2.2, NKX6.1, NEUROD, ISL1, HNF3 beta, MAFA, PAX4 и PAX6. В одном аспекте настоящего изобретения клетка с экспрессией маркеров, характерных для линии дифференцировки β-клеток, представляет собой β-клетку.
Настоящее изобретение описывает способ in vitro и группу клеток, обладающую возможностью генерировать одногормональные инсулинположительные клетки, которые также являются PDX-1- и NKX6.1-положительными. Способ, используемый в настоящем изобретении, включает в себя ряд этапов, которые поэтапно направляют дифференцировку плюрипотентных клеток человека в одногормональные клетки при помощи следующих промежуточных этапов:
а) получение клеток дефинитивной энтодермы (DE) из недифференцированных эмбриональных стволовых клеток человека, содержащее культивирование плюрипотентных клеток в среде, содержащей глюкозу, лиганд TGF-B и активатор WNT;
b) дифференцировка клеток DE в клетки кишечной трубки, содержащая культивирование клеток DE в среде, содержащей глюкозу, витамин С и лиганд FGF;
c) дифференцировка клеток кишечной трубки в клетки энтодермы задней части передней кишки, экспрессирующие PDX-1 и SOX2. Данная дифференцировка достигается путем культивирования клеток кишечной трубки в присутствии ингибитора shh, ингибитора BMP, лиганда TGF-B, лиганда FGF, ретиноевой кислоты, витамина С и активатора PKC;
d) дифференцировка клеток задней части передней кишки в клетки передней кишки поджелудочной железы, экспрессирующие PDX-1 и NKX6.1 и экспрессирующие более низкий уровень SOX2 по сравнению с клетками задней части передней кишки. Данная дифференцировка достигается путем культивирования клеток задней части передней кишки в присутствии ингибитора shh, ингибитора BMP, малой дозы ретиноевой кислоты, витамина С и активатора PKC;
е) дифференцировка клеток передней кишки поджелудочной железы в клетки энтодермы поджелудочной железы, экспрессирующие PDX-1, более высокий уровень NKX6.1 и более низкий уровень SOX2 по сравнению с клетками передней кишки поджелудочной железы. Дифференцировка достигается путем культивирования клеток передней кишки поджелудочной железы в среде, дополненной ингибитором shh, ингибитором TGF-B, малой дозы ретиноевой кислоты и витамина С;
f) дифференцировка клеток энтодермы поджелудочной железы в клетки-предшественники эндокринной поджелудочной железы и далее в одногормональные эндокринные клетки поджелудочной железы. Дифференцировка достигается путем культивирования клеток энтодермы поджелудочной железы в среде, обогащенной ингибитором shh, малой дозой ретиноевой кислоты и витамином С.
В варианте осуществления клетки на всех стадиях поэтапной дифференцировки культивируются в составе среды, содержащем менее 25 мМ глюкозы. В некоторых вариантах осуществления концентрация глюкозы находится в диапазоне от около 8 до около 20 мМ глюкозы.
В некоторых вариантах осуществления составы среды, используемой для генерирования клеток стадии кишечной трубки и всех последующих стадий, содержат аскорбиновую кислоту (также известную как витамин С). В варианте осуществления концентрация аскорбиновой кислоты составляет от около 0,01 до около 1 мМ. В варианте осуществления концентрация аскорбиновой кислоты составляет от около 0,1 до около 0,5 мМ.
Настоящее изобретение, кроме того, иллюстрируется среди прочих следующими примерами.
Пример 1
Дифференцировка эмбриональных стволовых клеток человека из клеток линии H1 в клетки-предшественники эндокринной поджелудочной железы в отсутствии сыворотки плода коровы; модуляция BMP/TGF-B-путей дифференцировки приводит к улучшению производства группы клеток энтодермы поджелудочной железы и снижает процент содержания группы клеток SOX2+
Этот пример был приведен, чтобы показать, что культуры энтодермы поджелудочной железы могут быть получены с весьма высокими уровнями экспрессии PDX-1 и NKX6.1, которые имеют при этом низкий уровень экспрессии CDX2 и SOX2.
Клетки эмбриональных стволовых клеток человека линии H1 (hESC H1) были собраны после нескольких пересевов (пересевы 40-52) и были посеяны как единичные клетки при плотности 100 000 клеток/см2 на покрытых MATRIGEL™ (разведение 1:30; BD Biosciences, Нью-Джерси, США) чашках в средах mTeSR®1 (StemCell Technologies, Ванкувер, Канада), дополненных 10 мкМ Y27632 (Rock inhibitor, номер по каталогу Y0503, SigmaAldrich, Монтана, США). Спустя 48 часов после посева культур были промыты и инкубированы в неполном солевом растворе PBS (фосфат-буферном солевом растворе без Mg или Ca) в течение приблизительно 30 секунд. Культуры были дифференцированы в линию эндокринной поджелудочной железы следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 3 дня). Клетки были культивированы на протяжении 1 дня в среде стадии 1: среда MCDB-131 (номер по каталогу 10372-019, Invitrogen, Калифорния, США), дополненная 0,1% не содержащего жирных кислот BSA (номер по каталогу 68700, Proliant, IA, США), бикарбоната натрия 0,0012 г/мл (номер по каталогу S3187, SigmaAldrich, MO, США), 1X GlutaMax™ (номер по каталогу 35050-079, Invitrogen), 5 мM D-глюкозы (номер по каталогу G8769, SigmaAldrich, MO, США), содержащие 100 нг/мл GDF8 (R&D Systems, Миннесота, США) и 1 мкM состава MCX (ингибитор GSK3B, 14-проп-2-ен-1-ил-3,5,7,14,17,23,27-гептаазотерацикло[19.3.1.1~2,6~.1~8, 12~]гептакоза-1(25),2(27),3,5,8(26),9,11,21,23-нонен-16-он, заявка на патент США, серийный номер 12/494789; включено в настоящий документ путем ссылки в полном объеме). Клетки затем культивировали на протяжении 1 дня в среде MCDB-131, обогащенной 0,1% не содержащего жирных кислот BSA, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мM D-глюкозы, 100 нг/мл GDF8 и 100 нМ состава MCX. Клетки затем культивировали на протяжении 1 дня в среде MCDB-131, к которой было добавлено 0,1% не содержащего жирных кислот BSA, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мM D-глюкозы и 100 нг/мл GDF8.
b. Этап 2 (первичная кишечная трубка - 2 дня). Клетки этапа 1 обрабатывались два дня средой MCDB-131, обогащенной 0,1% не содержащего жирных кислот BSA, бикарбонатом натрия 0,0012 г/мл, 1X GlutaMax ™, 5 мМ D-глюкозы и 25 нг/мл FGF7.
c. Этап 3 (передняя кишка - 2 дня). Клетки этапа 2 были культивированы на протяжении 1 дня в среде стадии 3: среда MCDB-131, дополненная разбавленным 1:200 ITS-X (Invitrogen), 2,5 мМ глюкозы, 1X GlutaMax™, бикарбоната натрия 0,0015 г/мл, 2% не содержащего жирных кислот BSA, 25 нг/мл FGF7, 10 нг/мл активина A (R&D systems), 0,25 мкМ SANT-1 (ингибитор shh, SigmaAldrich), 1 мкM ретиноевой кислоты (RА) (SigmaAldrich) и 200 нМ TPB (активатора PKC; номер по каталогу 565740; EMD, Нью-Джерси, США), содержащего 100 нМ LDN-193189 (ингибитор рецептора BMP; номер по каталогу 04-0019; Stemgent, Калифорния, США). Затем клетки культивировали в течение еще одного дня в среде этапа 3 с добавлением 10 нМ LDN-193189.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 2 дня). Клетки этапа 3 были культивированы в течение двух дней в среде MCDB-131, обогащенной разведенной 1:200 ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, бикарбонатом натрия 0,0015 г/мл, 2% не содержащего жирных кислот BSA, 0,25 мкМ SANT-1, 50 нМ RА, 200 нМ TPB и 50 нМ LDN-193189.
E. Этап 5 (панкреатическая энтодерма, 2-7 дней). Клетки этапа 4 были культивированы в течение 2-7 дней в среде MCDB-131, обогащенной разведенной 1:200 ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, бикарбонатом натрия 0,0015 г/мл, 2% не содержащего жирных кислот BSA, 0,25 мкМ SANT-1 и 50 нМ RА.
На указанных этапах образцы были собраны и проанализированы с помощью ПЦР в реальном времени, иммуногистохимически или флуоресцентно-активированной сортировкой клеток (FACS).
Для анализа FACS клетки, полученные из hESC, были выпущены в суспензию отдельных клеток путем инкубации в TrypLE Express (номер по каталогу 12604, Invitrogen) при 37°C в течение 3-5 минут. Клетки были затем промыты дважды в окрашивающем буферном растворе (PBS, содержащий 0,2% свободного от жирных кислот BSA) (номер по каталогу 554657, BD Biosciences, Нью-Джерси, США). Для окрашивания внутриклеточных антител клетки сначала инкубировали в течение 20 минут при температуре 4°C зеленым флуоресцентным красителем клеток ЖИВОЙ/МЕРТВЫЙ (Invitrogen, номер по каталогу L23101), чтобы дать возможность разделить живые/мертвые клетки во время анализа, за которым следовала одна промывка в холодном PBS. Клетки были обработаны в 250 мкл буферного раствора Cytofix/Cytoperm (BD Biosciences, номер по каталогу 554722) в течение 20 минут при температуре 4°C, за которой следовало две промывки в буферном растворе BD Perm/Wash (BD Biosciences, номер по каталогу 554723). Клетки были повторно взвешены до состояния суспензии в 100 мкл окрашивающего/блокирующего раствора, состоящего из буферного раствора Perm/Wash, дополненного 2% нормальной сыворотки (из соответствующих видов вторичных антител). Клетки затем инкубировали в течение 30 минут при температуре 4°C первичными антителами в эмпирически предварительно определенных разведениях, за которым следовало две промывки в буферном растворе Perm/Wash. Наконец, клетки инкубировали с соответствующими вторичными антителами в течение 30 минут при температуре 4°C, за которым следовало две промывки буферным раствором Perm/Wash перед анализами на BD FACS Canto II.
Были использованы следующие разведения первичных антител: кроличий антиинсулин (1:100; номер по каталогу C27C9; Cell Signaling, Mассачусетс, США), мышиный антиинсулин (1:100; номер по каталогу ab6999, Abcam, Массачусетс, США), мышиный антиглюкагон (1:1250; номер по каталогу G2654; Sigma-Aldrich), кроличий антисинаптофизин (1:100; номер по каталогу A0010, Dako, Калифорния, США), кроличий антихромогранин А (1:800; Dako), мышиный анти-NKX6.1 (1:50; DSHB, Университет штата Айова, Айова, США), мышиный анти-CDX2 (1:250; Invitrogen), козий анти-NeuroD (1:500; R&D Systems), мышиный анти-SOX2 (BD, Калифорния, США), мышиный анти-NKX2.2 (DSHB), мышиный анти-Pax6 (BD, Калифорния, США), мышиный анти-PDX-1 (BD, Калифорния, США). Вторичные антитела использовались в следующих разведениях: козий антимышиный Alexa 647 (1:500; Invitrogen), козий антикроличий PE (1:200; Invitrogen), ослиный антикозий (1:800; Invitrogen). Пробы инкубировали в течение 30 минут при 4°С после добавления вторичных антител с последующим заключительным промыванием в буферном растворе Perm/Wash. Клетки анализировали на BD FACS Canto II с использованием программного обеспечения BD FACS Diva с получением по меньшей мере 30 000 событий.
На фиг. 1A-1G изображены профили экспрессии гистограмм FACS изотипного контроля (фиг. 1А), хромогранина (фиг. 1В), клеток KI-67 (фиг. 1С), NKX6.1 (фиг. 1D), SOX2 (фиг. 1E), CDX2 (фиг. 1F), PDX-1 (фиг. 1С), дифференцированных в соответствии с примером 1 и проанализированных на S3, день 2. На каждой гистограмме показан процент экспрессии для каждого маркера. На 2-й день этапа 3 более 95% клеток были положительными по экспрессии PDX-1 (фиг. 1G) и около 60% клеток в группе были положительными по экспрессии SOX2 (фиг. 1E), в то время как менее 10% клеток были положительными по экспрессии CDX2 (фиг. 1F) или NKX6.1 (фиг. 1D) или хромогранина (фиг. 1В). Значительный процент клеток на этапе 3 был в активном клеточном цикле, как показывает высокий процент клеток, положительных по KI-67 (фиг. 1C).
На фиг. 2A-2G изображены профили экспрессии изотипного контроля (фиг. 2А), хромогранина (фиг. 2В), клеток KI-67 (фиг. 2С), NKX6.1 (фиг. 2D), SOX2 (фиг. 2E), CDX2 (фиг. 2F), PDX-1 (фиг. 2G) согласно определению окрашиванием FACS, клеток, дифференцированных в соответствии с примером 1 и собранных в день 2 на S4. На каждой гистограмме показан процент экспрессии для каждого маркера. Аналогично этапу 3 более 95% клеток были положительны по экспрессии PDX-1 (фиг. 2G), в то время как около 10% клеток были положительны по экспрессии CDX2 (фиг. 2F) и около 40% клеток были положительны по экспрессии NKX6.1 (фиг. 2D). Около 45% клеток были положительны по экспрессии SOX2 (фиг. 2Е), снижение с 60% на S3. Экспрессия хромогранина была равна приблизительно 3% (фиг. 2В). Значительный процент клеток на этапе 4 был в активном клеточном цикле, как показывает высокий процент клеток, положительных по KI-67 (фиг. 2C).
Фиг. 3А-3G иллюстрируют относительные профили экспрессии, определенные анализами клеток FACS, полученных на 2-й день этапа 5 в соответствии с протоколом дифференцировки, описанным в настоящем примере. Фиг. 3A: изотипный контроль; фиг. 3B: хромогранин; фиг. 3C: KI-67; фиг. 3D: NKX6.1; фиг. 3E: SOX2; фиг. 3F: CDX2; фиг. 3G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера. Аналогично этапам 3 и 4 более 95% клеток были положительны по экспрессии PDX-1, в то время как около 10% клеток были положительны по экспрессии CDX2 и около 67% клеток были положительны по экспрессии NKX6.1. Экспрессия SOX2 в приблизительно 50% была ниже по сравнению с этапом 3, но аналогична его экспрессии на S4.
На фиг. 4А-4G изображена экспрессия PDX-1 (фиг. 4G), NKX6.1 (фиг. 4D), CDX2 (фиг. 4F), SOX2 (фиг. 4E), Ki-67 (маркер распространения, фиг. 4С) и хромогранина (панэндокринный маркер, фиг. 4В) по измерению путем FACS-окрашивания клеток, собранных и проанализированных на 7-й день этапа 5 дифференцировки в соответствии с протоколом, описанным в настоящем примере. Как и на этапе 3 и 4, >90% клеток были положительными по экспрессии PDX-1, в то время как экспрессия CDX2 была менее 10%, а экспрессия NKX6.1 значительно возросла до >70%, при этом экспрессия SOX2 резко снизилась до около 2%.
Кроме того, большинство клеток, экспрессирующих SOX2, CDX2 и NKX6.1, были отрицательными по экспрессии хромогранина (см. фиг. 5А-5С). Таким образом, культуры S5, полученные в соответствии с протоколом, описанным в настоящем примере, позволяют получить группу клеток, в которой по меньшей мере 50% клеток экспрессируют PDX-1 и NKX6.1, проявляя при этом отрицательность по CDX-2, SOX2 и хромогранину. В таблице I дана сводка процента экспрессии различных маркеров энтодермы на этапах с S3 по S5.
Средняя экспрессия маркеров энтодермы на этапах от S3 до S5
2 дня
2 дня
2 дня
7 дней
На фиг. 6А-6T изображены профили экспрессии мРНК, измеренные с помощью ПЦР в реальном времени для клеток на S2, S3, S4 и S5, дифференцированных в соответствии с протоколом, изложенным в настоящем примере, и отраженных в отчете как обладающих многократным изменением экспрессии по сравнению с недифференцированными клетками H1. На этапе 3 была очень низкая экспрессия маркеров передней части передней кишки, таких как FOXe1 (фиг. 6C) и NKX2.1 (фиг. 6E). Тем не менее на стадии 3 SOX2 (фиг. 6M) и OSR1 (фиг. 6H), которые являются маркерами участка желудка на кишечной трубке, значительно повысили степень своего регулирования, а их экспрессия снизилась на этапах S4-S5. Маркеры энтодермы поджелудочной железы, такие как PTF1a (фиг. 6К), NKX6.1 (фиг. 6G) и PDX-1 (фиг. 6I), достигли максимальных уровней экспрессии на этапе культуры S5, день 2. Данные ПЦР свидетельствуют, что на стадии 3 клетки выходят из группы PDX-1+ SOX2+, становясь PDX-1+ NKX6.1+ SOX2- CDX2- на этапах S4-S5. (См. фиг. 6I, 6G, 6M и 6A.) Экспрессия эндокринных маркеров (хромогранин, инсулин, глюкагон и соматостатин) достигла максимального уровня экспрессии в конце этапа S5. Экспрессия маркеров предшественников эндокринной поджелудочной железы, NKX2.2, NeuroD и NGN3, достигла максимального уровня экспрессии на этапах S4-S5. Экспрессия маркеров других линий дифференцировки, таких как ZIC1 и SOX17, оставалась на низком уровне на этапах S4-S5.
В заключение клетки на этапе 5, день 2, которые были дифференцированы в соответствии с протоколом, изложенным в настоящем примере, экспрессируют низкие уровни CDX2 и SOX2, сохраняя высокий уровень экспрессии NKX6.1 и PDX-1. Считается, что уникальное сочетание своевременного ингибирования BMP, использование малых доз кислоты RА на этапах S4-S5, использование высокого содержания глюкозы на этапах S1-S2 позволяют получить группу клеток, описанных в примере 1.
Пример 2
Влияние ингибирования BMP и активации PKC на экспрессию SOX2 на этапах S3-S4
Протокол, изложенный в данном примере, был реализован с целью выяснить влияние ингибирования BMP, добавления FGF7 вместе с активацией PKC на экспрессию SOX2 на этапах S3-S4.
Клетки эмбриональных стволовых клеток человека линии Н1 были собраны после нескольких пересевов (пересевы 40-52) и были посеяны как единичные клетки при плотности 100 000 клеток/см2 на покрытых MATRIGEL™ (разведение 1:30) чашках в среде mTesr™1, обогащенной 10 мкМ Y27632. Через 48 часов после посева культуры были дифференцированы в клетки эндокринной линии поджелудочной железы следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 3 дня). Перед началом DE культуры промыли и инкубировали неполным раствором PBS (без Mg или Ca) в течение 30 секунд с последующим добавлением сред этапа 1. Эмбриональные стволовые клетки человека, культивируемые в чашках, покрытых MATRIGEL™, обрабатывали средой MCDB-131, обогащенной 0,1% не содержащего жирных кислот BSA, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™ и 2,5 мМ D-глюкозы, 100 нг/мл GDF8 и 1,5 мкM состава MCX (ингибитора GSK3B) в течение одного дня. Клетки затем обрабатывались средой MCDB-131, обогащенной 0,1% не содержащего жирных кислот BSA, бикарбонатом натрия 0,0012 г/мл, 1X GlutaMax™, 2,5 мМ глюкозы и 100 нг/мл GDF8 в дни 2-3.
b. Этап 2 (первичная кишечная трубка - 3 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% не содержащего жирных кислот BSA, бикарбонатом натрия 0,0012 г/мл, 1X GlutaMax ™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7 в течение трех дней.
c. Этап 3 (передняя кишка - 3 дня). Клетки этапа 2 обрабатывали средой MCDB131, обогащенной ITs-X в разведении 1:200, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% не содержащего жирных кислот BSA, 0,25 мкM SANT-1, 20 нг/мл активина A, 2 мкM кислоты RА в присутствии или отсутствии 50 нг/мл FGF7, 50 или 200 нМ LDN-193189 и/или 200 нМ TPB. Клетки инкубировали в течение трех дней в среде с использованием сочетаний, перечисленных в таблице II ниже.
Этап 3. Обработки
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 3 дня). Клетки этапа 3 обрабатывали средой MCDB131, обогащенной разбавленным 1:200 ITS-X, 2,5 мМ глюкозы, 1x GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% не содержащего жирных кислот BSA, 0,25 мкM SANT-1, 200 нМ TPB, 400 нМ LDN-193189, 2 мкM ингибитора ALk5 (SD-208, описанного в Molecular Pharmacology 2007, 72:152-161) и 100 нМ ингибитора CYP26A (N-{4-[2-этил-1-(1H-1,2,4-триазол-1-ил)бутил]фенил}-1,3-бензотиазол-2-амин, Janssen, Бельгия) в течение трех дней.
мРНК была собрана на этапах S2-S4 при всех перечисленных выше условиях и проанализирована с помощью ПЦР в реальном времени. Контрольные условия на этапе S3 относятся к культурам, где FGF7, АА, SANT, RА и 200 нМ LDN-193189 были использованы в концентрациях, перечисленных на этапе свыше. Как видно по данным ПЦР, приведенным на фиг. 7А-7G, удаление LDN-193189 на этапе S3 привело к значительному снижению эндокринных маркеров, таких как NGN3 (фиг. 7D), и панэндокринного маркера, такого как хромогранин (см. фиг. 7С). Добавление активатора PKC и удаление LDN-193189 на этапе S3 еще больше понизило эндокринные маркеры при одновременном повышении экспрессии NKX6.1 (см. фиг. 7A-7G). Кроме того, добавление 50 нМ LDN-193189 было так же эффективно, как и 200 нМ LDN-193189, для индукции эндокринных маркеров (хромогранин и NGN3). Удаление LDN-193189 и добавление TPB на этапе S3 повысило экспрессию CDX2 (фиг. 7Е) и альбумина (фиг. 7F), подавляя экспрессию SOX2 (фиг. 7G). Кроме того, удаление как FGF7, так и LDN-193189 значительно усилило экспрессию SOX2 (фиг. 7G) и ослабило экспрессию альбумина (фиг. 7F) по сравнению с культурами, где LDN-193189 был удален, а FGF7 был сохранен. Эти данные показывают, что точная модуляция ингибирования BMP, активация FGF и активация PKC могут позволить получить отдел энтодермы, который богат PDX-1 и NKX6.1, но имеет низкий CDX2, SOX2 и альбумин. Наконец, устойчивое ингибирование BMP на этапах S3-S4 усилило экспрессию проэндокринных генов и повысило регулируемость экспрессии SOX2. Это указывает на то, что ингибирование BMP требуется подбирать точно, чтобы увеличить гены эндокринной поджелудочной железы, в то же время не повышая регуляции экспрессии SOX2, которая отсутствует или низка при развитии поджелудочной железы, но присутствует в органах передней части энтодермы передней кишки, таких как желудок.
Пример 3
Раннее ингибирование BMP на этапе передней кишки требуется для последующего индуцирования эндокринных маркеров
Этот пример показывает, что раннее ингибирование сигнализации BMP на этапе S3 требуется для последующего индуцирования эндокринных маркеров. В то же время устойчивое ингибирование BMP на этапе 3 также приводит к сильной экспрессии SOX2. Чтобы получить как высокую экспрессию эндокринных маркеров, так и низкую экспрессию SOX2, потребовался градиент ингибирования BMP для индуцирования пропанкреатических эндокринных маркеров при одновременной низкой экспрессии SXO2 и CDX2.
Клетки эмбриональных стволовых клеток человека линии Н1 различных пересевов (пересевы 40-52) были посеяны как единичные клетки при плотности 100 000 клеток/см2 на покрытых MATRIGEL™ (разведение 1:30) чашках в среде mTesr™1, обогащенной 10 мкМ Y27632. Через сорок восемь часов после посева культуры были дифференцированы в клетки линии панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 4 дня). Перед началом DE клетки были промыты и инкубированы с помощью неполного PBS (без Mg или Ca) в течение 30 секунд, после чего была проведена инкубация в среде S1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, в течение одного дня обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы, 100 нг/мл GDF8, 1,5 мкM смеси MCX (ингибитор GSK3B). Затем клетки в течение двух дней обрабатывались (дни 2-4) средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ глюкозы и 100 нг/мл GDF8.
b. Этап 2 (первичная кишечная трубка - 3 дня). Клетки этапа 1 обрабатывались в течение трех дней средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7.
c. Этап 3 (передняя кишка - 3 дня). Клетки этапа 2 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 20 нг/мл активина A, 2 мкM RA, 50 нг/мл FGF7, 100 нМ LDN-193189 (только в день 1 или только в течение этапа 3) и 200 нМ TPB. У некоторых культур LDN-193189 был удален из этапа 3.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 3 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 100 нМ TPB, 200 нМ LDN-193189, 2 мкM ингибитора ALk5 и 100 нМ ингибитора CYP26A в течение трех дней.
E. Этап 5 (панкреатическая энтодерма/эндокрин - 4 дня). Клетки этапа 4 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 200 нМ LDN-193189 и 2 мкM ALk5 в течение четырех дней.
Как показывают результаты ПЦР на фиг. 8A-8G, удаление LDN-193189 (ингибитора BMP) из этапа 3 отменяет экспрессию проэндокринных генов NGN3 (фиг. 8C); NeuroD (фиг. 8D); хромогранин (фиг. 8E) на этапах 4 и 5. Тем не менее экспрессия PDX-1 (фиг. 8B) и NKX6.1 (фиг. 8A) незначительно снижается по сравнению с NGN3 и NeuroD на этапах 4 и 5. Также полное удаление LDN-193189 на этапе 3 приводит к значительному увеличению экспрессии CDX2 (фиг. 7F). Добавление LDN-193189 в течение первого дня этапа 3, после чего он удаляется в день 2-3 этапа 3, значительно повышает экспрессию NGN3 и NeuroD, в то же время уменьшая экспрессию CDX2 и SOX2 на этапе 4. Культуры, в которых LDN-193189 был сохранен в течение этапа 3, показали очень высокую экспрессию SOX2 (фиг. 8G) при S3-S4. Эти данные показывают, что ингибирование BMP в день 1 этапа 3 достаточно для запуска панкреатических эндокринных маркеров, в то же время подавляя экспрессию SOX2 и CDX2.
Подводя итоги, ингибирование BMP требуется в день 1 этапа 3, чтобы вызвать образование эндокринных клеток-предшественников на этапах 4 и 5 и поддерживать экспрессию PDX-1 и NKX6.1, в то же время подавляя экспрессию SOX2. Также добавление PKC активатора на этапе 3 также повышает экспрессию PDX-1 и NKX6.1.
Пример 4
Ингибирование BMP сигнализации в день 1 этапа 3 достаточно для генерирования панкреатических клеток-предшественниц на этапе 4, тогда как ингибирование BMP-сигнализации в последний день этапа 3 приводит к значительно меньшей экспрессии эндокринных маркеров
Этот пример показывает, что раннее ингибирование BMP сигнализации на этапе 3 обеспечивает индукцию маркеров панкреатических эндокринных клеток-предшественниц, при этом ингибирование BMP сигнализации позднее на этапе 3 значительно уменьшает уровень экспрессии маркеров эндокринных клеток-предшественниц на этапе 4.
Клетки линии человеческих эмбриональных стволовых клеток H1 в различных каналах (от канала 40 до канала 52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на покрытых MATRIGEL™ (1:30 раствор) чашках в среде mTesr™1, обогащенной 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в клетки линии панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 4 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались в течение одного дня средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы, 100 нг/мл GDF8 и 1,5 мкM смеси MCX (ингибитор GSK3B). Затем клетки обрабатывались в течение трех дней средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ глюкозы и 100 нг/мл GDF8.
b. Этап 2 (первичная кишечная трубка - 3 дня). Клетки этапа 1 обрабатывались в течение трех дней MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7.
c. Этап 3 (передняя кишка - 3 дня). Клетки этапа 2 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA и сочетаниями, указанными в таблице III ниже, в течение трех дней.
Этап 3. Обработки
D2-3
+
-
-
+200 нМ
D2-3
+
-
-
+ 200 нМ
D2-3
+
-
-
+200 нМ
D2-3
+
-
-
+200 нМ
D2-3
+
+ 100 нМ (только в день 3)
-
+ 100 нМ
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 3 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 100 нМ TPB, 200 нМ LDN-193189, 2 мкM ингибитора ALk5 и 100 нМ ингибитора CYP26A в течение трех дней.
Фиг. 9A-9H показывают профиль экспрессии генов панкреатической энтодермы, эндокринной клетки-предшественницы и маркеров энтодермы передней кишки для сочетаний условий культивирования, указанных выше. В соответствии с предыдущим примером блокирование BMP процесса в первый день этапа 3 очень важно для последующей индукции эндокринной программы, как показывают измерения экспрессии панэндокринного маркера, хромогранина. (См. фиг. 9C.) Тем не менее добавление ингибитора BMP в первый день этапа 3 запускает экспрессию эндокринных маркеров на последующих этапах. Также добавление ингибитора BMP в первый день этапа 3 уменьшает экспрессию маркера передней кишки SOX2 на этапах 3-4 (фиг. 9H). Тем не менее добавление ингибитора BMP только в последний день этапа 3 показало значительно большую экспрессию SOX2 в конце этапа 3 по сравнению с клетками, обработанными ингибитором BMP только в первый день этапа 3. Уровни экспрессии, показанные на фиг. 9A-9H, относятся к уровням экспрессии в недифференцированных клетках H1, которые имеют очень высокий уровень экспрессии SOX2. Кроме того, что он является маркером переднего отдела передней кишка, SOX2 - это хорошо известный фактор транскрипции, который важен для поддержания плюрипотентности клетки ES. Этот пример также поддерживает предыдущие результаты, указывающие на чувствительность культуры этапа 3 к длительности и кинетике BMP-сигнализации и последующему влиянию на панкреатическую эндокринную индукцию и экспрессию SOX2.
Пример 5
Оптимальная доза ингибирования BMP на этапе панкреатической передней кишки (этап 4)
Предыдущий пример показал оптимальную длительность ингибирования BMP на этапе 3. Этот пример устанавливает оптимальную дозу ингибитора BMP в среде S4.
Клетки линии эмбриональных стволовых клеток человека H1 от различных пересевов (пересевы 40-52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на покрытых MATRIGEL™ (1:30 раствор) чашках в среде mTesr™1 и 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в линию панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 4 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы, 100 нг/мл GDF8 и 1 мкM смеси MCX (ингибитора GSK3B) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ глюкозы и 100 нг/мл GDF8 в течение дней 2-4.
b. Этап 2 (первичная кишечная трубка - 3 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7 в течение трех дней.
c. Этап 3 (передняя кишка - 4 дня). Клетки этапа 2 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7A, 2 мкM RA, 20 нг/мл активина А, 100 нМ LDN-193189 и 100 нМ TPB в течение 1 дня. Затем клетки были культивированы в среде MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA, 20 нг/мл активина A и 100 нМ TPB в течение трех дней.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 4 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной раствором ITS-X 1:200, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 200 нМ LDN-193189-193189, 2 мкM ингибитора ALk5, 100 нМ ингибитора CYP26A и концентрациями LDN-193189, указанными в таблице IV (ниже) в течение дней 1-4 этапа 4.
Концентрации LDN-193189, использованные в S4
D. Этап 5 (панкреатическая энтодерма/эндокринная клетка-предшественница - 3 дня). Клетки этапа 4 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 50 нМ LDN-193189 и 1 мкM ингибитора ALk5 в течение трех дней.
Результаты анализов ПЦР в реальном времени для клеток, собранных после вышеуказанной обработки, показаны на фиг. 10A-10H. Эта фигура показывает, что добавление 50 или 100 нМ LDN-193189 в день 1, 2, 3 или 4 на этапе S4 может продлить экспрессию эндокринных маркеров, в то же время поддерживая низкую экспрессию SOX2 на этапах S4-S5. (См. фиг. 10A-10H.)
Пример 6
Оптимальная доза ингибирования BMP в передней кишке этапа (этап 3)
Этот пример устанавливает оптимальную дозу ингибирования BMP на этапе 3 и последующие влияния на эндокринные маркеры на этапе 6.
Клетки эмбриональных стволовых клеток человека линии Н1 различных пересевов (пересевы 40-52) были посеяны как единичные клетки при плотности 100 000 клеток/см2 на покрытых MATRIGEL™ (разведение 1:30) чашках в среде mTesr™1, обогащенной 10 мкМ Y27632. Через сорок восемь часов после посева культуры были дифференцированы в клетки линии панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 4 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы, 100 нг/мл GDF8 и 1,5 мкM смеси MCX (ингибитора GSK3B) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ глюкозы и 100 нг/мл GDF8 в течение дней 2-4.
b. Этап 2 (первичная кишечная трубка - 3 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7 в течение трех дней.
c. Этап 3 (передняя кишка - 3 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA, 20 нг/мл активина A, 100 нМ TPB и 10-50 нМ LDN-193189 в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA, 20 нг/мл активина A и 100 нМ TPB в течение двух дней.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 3 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 20 нМ LDN-193189; 2 мкM ингибитора ALk5; 100 нМ ингибитора CYP26 A и 100 нМ TPB в течение трех дней.
E. Этап 5 (панкреатическая энтодерма/эндокринная клетка-предшественница - 3 дня). Клетки этапа 4 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X; 2,5 мМ глюкозы; 1X GlutaMax™; 0,0015 г/мл бикарбоната натрия; 2% BSA без жирных кислот; ±25 нМ LDN-193189 и/или 2 мкM ингибитора ALk5 в течение трех дней.
F. Этап 6 (образование панкреатического эндокринного гормона - 3 дня). Клетки этапа 5 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X; 2,5 мМ глюкозы; 1X GlutaMax™; 0,0015 г/мл бикарбоната натрия; 2% BSA без жирных кислот в течение трех дней.
Фиг. 11A-11H показывают, что необходимо низкое либо умеренное ингибирование BMP в первый день этапа 3, чтобы запустить экспрессию эндокринных маркеров, в то же время поддерживая низкую экспрессию SOX2. Также ингибирование BMP на этапе 5 при увеличении эндокринных маркеров также привело к повышению экспрессии SOX2.
Данные в этом примере также подтверждают результаты, представленные в предыдущих примерах. Данные подтверждают, что точная модуляция BMP процесса на этапах 3-5 необходима для индукции панкреатических эндокринных маркеров, в то же время подавляет экспрессию SOX2.
Пример 7
Оптимальное окно для ингибирования BMP на этапе S3 (этап передней кишки)
Этот пример устанавливает оптимальное окно времени на этапе 3 для ингибирования BMP сигнализации, в то же время сохраняя эндокринную индукцию на последующих этапах и уменьшая экспрессию SOX2.
Клетки линии человеческих эмбриональных стволовых клеток H1 на различных этапах (пересевы 40-52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на покрытых MATRIGEL™ (1:30 раствор) чашках в среде mTesr™1 и 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в линию панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 4 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы, 100 нг/мл GDF8 и 1,5 мкM смеси MCX в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ глюкозы и 100 нг/мл GDF8 в течение дней 2-4.
b. Этап 2 (первичная кишечная трубка - 3 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7 в течение трех дней.
c. Этап 3 (передняя кишка - 3 дня). Клетки этапа 2 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA, 20 нг/мл активина A и 100 нМ TPB, содержащего 100 нМ LDN-193189, только в течение первых 2 часов, 6 часов или 24 часов этапа 3.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 3 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 25 нМ LDN-193189, 2 мкM ингибитора ALk5, 100 нМ ингибитора CYP26 A и 100 нМ TPB в течение трех дней.
E. Этап 5 (панкреатическая энтодерма/эндокринная клетка-предшественница - 3 дня). Клетки этапа 4 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот и 2 мкM ингибитора ALk5 в течение трех дней.
Фиг. 12A-12G показывают анализы ПЦР в реальном времени для данных, собранных в этом примере. Обработка на этапе 3 в течение по меньшей мере 2 часов при помощи ингибитора BMP может запустить экспрессию проэндокринных факторов транскрипции, таких как Ngn3 (фиг. 12D) и NeuroD (фиг. 12E), в то же время поддерживая очень низкую экспрессию SOX2 (фиг. 12G), и значительно повышает экспрессию NKX6.1 (фиг. 12A) и PDX-1 (фиг. 12B) на этапах S4-S5. Тем не менее на этапе 5 в день 3 экспрессия CDX2 была выше у клеток, обработанных в течение 2-6 часов ингибитором BMP, чем у клеток, обработанных ингибитором в течение 24 часов (фиг. 12F).
Данные из этого примера указывают на то, что 24-часовое ингибирование BMP процесса оптимально для поддержания низкого уровня экспрессии CDX2 и экспрессии SOX2 и для инициирования эндокринной дифференцировки, в то время как поддерживается высокая экспрессия маркеров панкреатической энтодермы.
Пример 8
Оптимальная продолжительность этапа 3 (этап передней кишки) и этапа 4 (этап панкреатической клетки-предшественницы передней кишки)
Этот пример был проведен, чтобы определить оптимальную продолжительность этапов S3 и S4 при пошаговой дифференцировки плюрипотентных клеток до популяции клеток линии панкреатических эндокринных клеток.
Клетки линии человеческих эмбриональных стволовых клеток H1 от различных пересевов (пересевы 40-52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на чашках, покрытых MATRIGEL™ (раствор 1:30), в среде mTesr™1, обогащенной 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в линию панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 4 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™; 2,5 мМ D-глюкозы; 100 нг/мл GDF8 и 1,5 мкM смеси MCX (ингибитор GSK3B) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот; 0,0012 г/мл бикарбоната натрия; 1X GlutaMax™; 2,5 мМ глюкозы и 100 нг/мл GDF8 в течение дней 2-4.
b. Этап 2 (первичная кишечная трубка - 2 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 2,5 мМ D-глюкозы и 50 нг/мл FGF7 в течение двух дней.
c. Этап 3 (передняя кишка - 2-3 дня). Клетки этапа 2 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA, 20 нг/мл активина A и 100 нМ TPB, содержащего 100 нМ LDN-193189, в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нг/мл FGF7, 2 мкM RA, 20 нг/мл активина A и 100 нМ TPB.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 2-3 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 25 нМ LDN-193189, 100 нМ ингибитора CYP26 A и 100 нМ TPB от двух до трех дней.
E. Этап 5 (панкреатическая энтодерма/эндокринный прекурсор - 2 дня). Клетки этапа 4 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот и 1 мкM ингибитора ALk5 в течение двух дней.
F. Этап 6 (панкреатический эндокринный прекурсор/гормон - 2 дня). Клетки этапа 5 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия и 2% BSA без жирных кислот в течение двух дней.
Данные из анализов ПЦР образцов в реальном времени, собранные на этапе 3, 4, 5 или 6, показаны на фиг. 13A-13G. Эти данные показывают, что увеличение S3 и S4 до трех дней увеличивает экспрессию NKX6.1 по сравнению с культурой, имеющей двухдневный S3 и S4 (фиг. 13A). Клетки, обработанные в течение трех дней на этапе 3, показывают уменьшение экспрессии проэндокринных маркеров по сравнению с культурами, где длительность S3 и S4 составляет только двух дней (фиг. 13D и 13E). Также увеличение этапа 4 до трех дней значительно увеличило экспрессию SOX2 (фиг. 13G).
Данные, полученные в этом примере, соответствуют данным, полученным в предыдущих примерах, относительно того, что продленное ингибирование BMP смещает клетки передней кишки в сторону популяции с высоким SOX2. На основании данных из этого примера и предыдущих примеров можно сделать вывод, что оптимальная продолжительность этапа 3 и этапа 4 составляет два дня. Идеальный протокол приведет к дифференцированным клеткам с высокими уровнями экспрессии проэндокринных маркеров, высокой экспрессией NKX6.1, низкой экспрессией CDX2 и низкой экспрессией SOX2.
Пример 9
Длительное воздействие ингибированием BMP при наличии высокой глюкозы и добавление B27 значительно увеличивают экспрессию SOX2 на этапе S3 и S4
Этот протокол был проведен для определения факторов, влияющих на экспрессию SOX2 на этапе S3 и S4 при пошаговой дифференцировке плюрипотентных клеток в производящие гормон клетки.
Клетки линии человеческих эмбриональных стволовых клеток H1 были культивированы на покрытых MATRIGEL™ (раствор 1:30) чашках в среде mTesr™1 до ~70% слияния и были дифференцированы следующим образом.
a. Недифференцированные клетки были культивированы в среде RPMI (инвитроген), обогащенной 0,2% FBS; 100 нг/мл активина A; 20 нг/мл WNT-3a в течение одного дня. Затем клетки были обработаны средой RPMI, обогащенной 0,5% FBS; 100 нг/мл активина A в течение еще двух дней (этап 1).
b. Клетки этапа 1 обрабатывались средой DMEM/F12, обогащенной 2% FBS; 50 нг/мл FGF7 в течение трех дней (этап 2).
c. Клетки этапа 2 были культивированы в DMEM-высокоглюкозной среде, обогащенной 1% B27; 0,25 мкM SANT-1; 2 мкM RA; 100 нг/мл Noggin (R & D systems, Миннесота, США) в течение четырех дней (этап 3).
D. Клетки этапа 3 обрабатывались DMEM-высокоглюкозной средой, обогащенной 1% B27; 100 нг/мл Noggin; 1 мкM ингибитора ALk5 II (Axxora, Калифорния, США); 50 нМ TPB в течение четырех дней (этап 4).
Фиг. 14A-14H показывают FACS-гистограммы для клеток, собранных на этапе 3, день 4, полученные для следующих маркеров: изотипный контроль (фиг. 14A), хромогранин (фиг. 14B), KI-67 (фиг. 14C), NKX6.1 (фиг. 14D), SOX2 (фиг. 14E), HNF3B (фиг. 14F), CDX2 (фиг. 14G), PDX-1 (фиг. 14H). На каждой гистограмме показан процент экспрессии для каждого маркера. Большинство клеток на этапе 3 были положительны по экспрессии PDX-1 (фиг. 14H) и HNF3B (фиг. 14F), отрицательны по экспрессии NKX6.1 (фиг. 14D) и показали низкую экспрессию хромогранина (фиг. 14B) и CDX2 (фиг. 14G). Тем не менее более 90% клеток также были сильно положительны на SOX2 (фиг. 14E). Это показывает, что на этапе 3 большинство клеток были положительны на PDX-1 и SOX2 и отрицательны на NKX6.1, что указывает на создание энтодермной популяции в соответствии с популяцией передней кишки, расположенной спереди от домена PDX-1 поджелудочной железы.
Также процент клеток, которые были SOX2+ на этапе 3 в популяции клеток, созданной с помощью протокола, приведенного в этом примере, был значительно выше, чем процент клеток, которые были SOX2+ в популяции клеток, созданной с помощью протокола, приведенного в примере 1. Эту разницу можно объяснить длительным воздействием антагониста BMP, Noggin, нехваткой FGF7 и активатора PKC в культурной среде на этапе 3 этого примера.
Фиг. 15A-15G показывают FACS-гистограмму профилей экспрессии следующих маркеров на этапе S4, день 2 у клеток, дифференцированных согласно примеру 9. Фиг. 15A: изотипный контроль, фиг. 15B: NKX6.1, фиг. 15C: KI-67, фиг. 15D: хромогранин, фиг. 15E: SOX2, фиг. 15F: CDX2, фиг. 15G: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
Фиг. 16A-16F содержат гистограмму профилей экспрессии FACS следующих маркеров в S4, день 4 для клеток, дифференцирующихся согласно примеру 9. Фиг. 16A: изотипный контроль, фиг. 16B: NKX6.1, фиг. 16C: хромогранин, фиг. 16D: SOX2, фиг. 16E: CDX2, фиг. 16F: PDX-1. На каждой гистограмме показан процент экспрессии для каждого маркера.
Таблица V ниже обобщает данные, полученные для% экспрессии маркеров энтодермы на этапе S3 и S4 у клеток, дифференцированных согласно протоколу, приведенному в этом примере.
% экспрессии маркеров энтодермы на этапе S3-S4
(сутки)
4 суток
2 дня
4 суток
Фиг. 17A-17J показывают результаты анализов ПЦР в реальном времени экспрессии следующих генов у клеток линии эмбриональных стволовых клеток человека H1, дифференцированных согласно примеру 9. Фиг. 17A: CDX2, фиг. 17B: HHex, фиг. 17C: FOXE1, фиг. 17D: IPF1 (PDX-1), фиг. 17E: NKX2.1, фиг. 17F: NKX2.2, фиг. 17G: NKX6.1, фиг. 17H: PROX1, фиг. 17I: SOX2, фиг. 17J: SOX9.
Как показано на фиг. 14-17 и в таблице V, на день 2-4 этапа 4 было значительное увеличение экспрессии NKX6.1, в то время как оставалась высокой экспрессия PDX-1. Несмотря на то что экспрессия SOX2 уменьшилась с этапа 3 до этапа 4, ~75% клеток оставались SOX2+. Так же как на фиг. 5, клетки CDX2+, SOX2+ и NKX6.1+ были взаимно исключающими из популяции хромогранина. Это подразумевает, что популяция клеток этапа 4 дня 4, полученная с помощью протокола, приведенного в примере 9, имеет хромогранин-отрицательную фракцию ~50% NKX6.1+ SOX2+ PDX-1+ CDX2-. Это отличается от клеточной популяции, полученной в примере 1, которая имеет 40-70% PDX-1+ NKX6.1+ SOX2-, CDX2-, хромогранин-отрицательную фракцию и 2-25% PDX-1+ NKX6.1+ SOX2+ на этапе S4-S5. Очевидно, что клетки, полученные с помощью протокола в примере 1, имеют гораздо больший процент панкреатической энтодермы, так как определено, что популяция имеет PDX-1+ и NXK6.1+ и в то же время малый или отрицательный SOX2 и CDX2 по сравнению с клетками, полученными в примере 9.
Данные, полученные в этом примере, подтверждают, что длительное воздействие ингибированием BMP при наличии высокой глюкозы и добавления B27 значительно увеличивает экспрессию SOX2 на этапе дифференцировки 3 и 4.
Пример 10
Ранее опубликованный протокол приводит к образованию значительного числа SOX2+ популяции на этапе 3-4
Kroon et al. опубликовали протокол для приготовления клеток линии панкреатической энтодермы из человеческих эмбриональных стволовых клеток (Nature Biotech 2008, 26: 443-452, далее указываемый как Kroon). В представленном здесь примере человеческие эмбриональные стволовые клетки были дифференцированы по протоколу Kroon и проверены на экспрессию маркеров, характерных для разных этапов дифференцировки.
Клетки линии человеческих эмбриональных стволовых клеток H1 были посеяны на чашках, покрытых MATRIGEL™ (раствор 1:30), культивированы в среде mTesr™1 до ~70% слияния и дифференцированы с помощью ранее опубликованного протокола Kroon следующим образом.
a. Недифференцированные клетки были подвергнуты воздействию среды RPMI, обогащенной 0,2% FBS, 100 нг/мл активина A, 20 нг/мл WNT-3a в течение одного дня, после чего были обработаны средой RPMI, обогащенной 0,5% FBS, 100 нг/мл активина A в течение еще двух дней (этап 1).
b. Клетки этапа 1 были подвергнуты воздействию среды RPMI, обогащенной 2% FBS, 50 нг/мл FGF7 в течение трех дней (этап 2).
c. Клетки этапа 2 обрабатывались DMEM-высокоглюкозной средой, обогащенной 1% B27, 0,25 мкM SANT-1, 2 мкM RA, 50 нг/мл Noggin (R & D systems, Миннесота) в течение трех дней (этап 3).
d. Клетки этапа 3 были культивированы в DMEM-высокоглюкозной среде, обогащенной 1% B27, в течение трех дней (этап 4).
e. Клетки этапа 4 были соскоблены со стенок и ресуспензированы как кластеры в DMEM-высокоглюкозной среде, обогащенной 1% B27, в течение двух дней.
Фиг. 18A-18G показывают FACS-гистограмму профилей экспрессии следующих маркеров на этапе S3, день 3 у клеток, дифференцированных согласно примеру 10: изотипный контроль (фиг. 18A), NKX6.1 (фиг. 18B), хромогранин (фиг. 18C), SOX2 (фиг. 18D), CDX2 (фиг. 18E), KI-67 (фиг. 18F), PDX-1 (фиг. 18G). На каждой гистограмме показан процент экспрессии для каждого маркера.
Фиг. 19A-19G показывают FACS-гистограмму профилей экспрессии следующих маркеров на этапе S4, день 5 у клеток, дифференцированных согласно примеру 10: изотипный контроль (фиг. 19A), NKX6.1 (фиг. 19B), хромогранин (фиг. 19C), SOX2 (фиг. 19D), CDX2 (фиг. 19E), KI-67 (фиг. 19F), PDX-1 (фиг. 19G). Процентная экспрессия для каждого маркера показана на каждой гистограмме.
Как показано на фиг. 18 и 19, к концу этапа 4 (день 5) кластеры клеток в суспензии были ~20% NKX6.1+ PDX-1+ SOX2- и ~20% PDX-1+ NKX6.1+ SOX2+. Эти результаты показывают, что значительная фракция популяции клеток на этапе 4, полученных согласно примеру 10, которые были NKX6.1+, также были SOX2+.
Таблица VI, приведенная ниже, обобщает процент маркеров энтодермы на этапе S3-S4 у клеток, полученных в этом примере.
Экспрессия маркеров энтодермы на этапе S3-S4 у клеток, дифференцированных согласно Kroon
(сутки)
3 дня
5 суток*
Пример 11
Добавление аскорбиновой кислоты приводит к значительному уменьшению числа полигормональных клеток и параллельному увеличению числа одногормональных инсулинположительных клеток
Было проверено влияние аскорбиновой кислоты на экспрессию маркеров при дифференцировке плюрипотентных клеток в производящие гормон клетки. Клетки были культивированы в среде, обогащенной глюкозой на каждой стадии дифференцировки и обогащенной аскорбиновой кислотой на образовании этапов 3, 4 и 5 следующим образом.
Клетки линии эмбриональных стволовых клеток человека H1 от различных пересевов (пересевы 40-52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на чашках, покрытых средой MATRIGEL™ (раствор 1:30), в среде mTesr™1 и 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в линию панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 3 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ D-глюкозы, 100 нг/мл GDF8 и 1 мкM смеси MCX (ингибитор GSK3B) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ глюкозы, 100 нг/мл GDF8 и 100 нМ смеси MCX в течение второго дня, после чего были еще день выдержаны в среде MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ глюкозы и 100 нг/мл GDF8.
b. Этап 2 (первичная кишечная трубка - 2 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ D-глюкозы и 25 нг/мл FGF7 в течение двух дней.
c. Этап 3 (передняя кишка - 2 дня). Клетки этапа 2 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 10 нг/мл активина A, 25 нг/мл FGF7, 0,25 мкM SANT-1, 1мкM RA, 200 нМ TPB (активатор PKC), 100 нМ LDN-193189 (ингибитор BMP-рецептора) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 10 нг/мл активина A, 25 нг/мл FGF7, 0,25 мкM SANT-1, 1мкM RA, 200 нМ TPB (активатор PKC), 10 нМ LDN-193189 в течение еще одного дня. Некоторые культуры обрабатывались 0,25 мМ аскорбиновой кислоты (номер по каталогу A4544, Sigma, Миссури, США) в течение этапа 3.
D. Этап 4 (панкреатическая клетка-предшественница передней кишки - 2 дня). Клетки этапа 3 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нМ RA, 200 нМ TPB, 50 нМ LDN-193189, с или без 0,25 мМ аскорбиновой кислоты в течение двух дней.
E. Этап 5 (панкреатическая энтодерма, 2-7 дней). Клетки этапа 4 обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нМ RA, с или без 0,25 мМ аскорбиновой кислоты в течение 2-7 дней.
Фиг. 20A-20J показывают анализы ПЦР экспрессии следующих генов в клетках линии эмбриональных стволовых клеток человека H1, дифференцированных согласно примеру 11, в реальном времени. Фиг. 20A: соматостатин, фиг. 20B: PDX1, фиг. 20C: Pax6, фиг. 20D: Pax4, фиг. 20E: NKX6.1, фиг. 20F: NGN3, фиг. 20G: глюкагон, фиг. 20H: NeuroD, фиг. 20I: инсулин, фиг. 20J: хромогранин. Эта фигура показывает, что добавление аскорбиновой кислоты на этапе 3 или на этапе 3 и 4 значительно уменьшает экспрессию соматостатина и глюкагона на этапе 4-5, в то же время увеличивая экспрессию инсулина (см. фиг. 20A, 20G и 20I). Также на этапе 4-5 экспрессия маркеров панкреатической энтодермы, таких как PDX-1 и NKX6.1, незначительно изменилась при добавлении 0,25 мМ аскорбиновой кислоты (см. фиг. 20B и 20D). На этапе 4-5 экспрессия Pax6 уменьшилась, а экспрессия Pax4 осталась прежней (см. фиг. 20C и 20D). В конце этапа 5 культуры, обработанные ± аскорбиновой кислотой на этапе S3-S5, были иммуногистохимически окрашены антителами к гормонам инсулину, глюкагону и соматостатину. Таблица VII обобщает средний процент инсулин-, глюкагон- и соматостатин-положительных клеток и полигормональных клеток (экспрессия еще двух гормонов в одной клетке).
Экспрессия гормонов как процент от общего числа гормонов
Пример 12
Оптимальная доза аскорбиновой кислоты на этапе 3
Этот пример был проведен, чтобы определить оптимальную дозу аскорбиновой кислоты, которую нужно использовать для генерирования инсулин-положительных клеток, которые являются одногормональными, PDX-1-положительными и NKX6.1-положительными.
Клетки линии эмбриональных стволовых клеток человека H1 от различных пересевов (пересевы 40-52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на чашках, покрытых средой MATRIGEL™ (раствор 1:30), в среде mTesr™1 и 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в линию панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 3 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ D-глюкозы и 100 нг/мл GDF8 плюс 1 мкM смеси MCX (ингибитор GSK3B) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ глюкозы и 100 нг/мл GDF8 плюс 100 нМ смеси MCX в течение второго дня, после чего еще один день в среде MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ глюкозы и 100 нг/мл GDF8.
b. Этап 2 (первичная кишечная трубка - 2 дня). Клетки этапа 1 обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ D-глюкозы, с добавлением или без добавления 0,25 мМ аскорбиновой кислоты и 25 нг/мл FGF7 в течение двух дней.
c. Этап 3 (передняя кишка - 2 дня). Клетки этапа 2 обрабатывались средой MCDB131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 10 нг/мл активина A, 25 нг/мл FGF7, 0,25 мкM SANT-1, ±0,25 мМ аскорбиновой кислоты, 1 мкM RA, 200 нМ TPB, 100 нМ LDN-193189 в течение дня 1, после чего были обработаны средой MCDB131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 10 нг/мл активина A, 25 нг/мл FGF7, 0,25 мкM SANT-1, ±0,25 мМ аскорбиновой кислоты, 1 мкM RA, 200 нМ TPB, 10 нМ LDN-193189 в течение еще одного дня.
d. Этап 4 (панкреатическая клетка-предшественница передней кишки - 2 дня). Клетки этапа 3 обрабатывались средой MCDB131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нM RА, 200 нМ TPB, 50 нМ LDN-193189, с добавлением или без добавления 0,25-1 мМ аскорбиновой кислоты в течение двух дней.
е. Этап 5 (панкреатическая энтодерма, 2-9 дней). Клетки этапа 4 обрабатывались средой MCDB131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нМ RA, с добавлением или без добавления 0,25 мМ аскорбиновой кислоты в течение 2-9 дней.
Фиг. 21A-21J показывают данные анализов ПЦР экспрессии следующих генов в клетках линии эмбриональных стволовых клеток человека H1, дифференцированных согласно примеру 12, в реальном времени. Фиг. 21A: соматостатин, фиг. 21B: PDX1, фиг. 21C: Pax6, фиг. 21D: Pax4, фиг. 21E: NKX6.1, фиг. 21F: NGN3, фиг. 21G: NeuroD, фиг. 21H: инсулин, фиг. 21I: глюкагон, фиг. 21J: хромогранин. В соответствии с данными из примера 10 добавление аскорбиновой кислоты на этапе 2-4 значительно уменьшило экспрессию соматостатина, глюкагона и Pax6, в то же время сохраняя экспрессию инсулина и Pax4 на этапе 5. Также было незначительное преимущество использования на этапе S4 0,5-1 мМ аскорбиновой кислоты по сравнению с 0,25 мМ аскорбиновой кислоты. И наконец, добавление аскорбиновой кислоты на этапе 2 также оказалось эффективным для уменьшения экспрессии глюкагона и соматостатина на этапе S3-5, в то же время сохраняя экспрессию инсулина. Таким образом, аскорбиновая кислота выступает как специфичный для этапа способ регулирования экспрессии единичных гормональных клеток. Добавление аскорбиновой кислоты важно на ранних этапах протокола дифференцировки, причем на более поздних этапах она не показала себя такой же эффективной в плане уменьшения числа полигормональных клеток.
Пример 13
Сочетание ретиноевой кислоты и аскорбиновой кислоты необходимо для генерирования единичных гормональных инсулин-положительных клеток
Этот пример был проведен, чтобы дать представление о требованиях к генерированию единичных гормональных инсулин-положительных клеток при дифференцировке плюрипотентных клеток.
Клетки линии эмбриональных стволовых клеток человека H1 от различных пересевов (пересевы 40-52) были посеяны как отдельные клетки с плотностью 100 000 клеток/см2 на чашках, покрытых средой MATRIGEL™ (раствор 1:30), в среде mTesr™1 и 10 мкM Y27632. Через сорок восемь часов после посева культуры были дифференцированы в линию панкреатических эндокринных клеток следующим образом.
a. Этап 1 (сформированная энтодерма (DE) - 3 дня). Перед началом DE культуры были промыты и инкубированы при помощи неполной PBS (без Mg или Ca) в течение 30 секунд, после чего произошло добавление среды этапа 1. Человеческие эмбриональные стволовые клетки, культивированные как отдельные клетки на чашках, покрытых средой MATRIGEL™, обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ D-глюкозы, 100 нг/мл GDF8, 1 мкM смеси MCX (ингибитор GSK3B) в течение одного дня. Затем клетки были обработаны средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, бикарбоната натрия, GlutaMax™, дополнительными 5 мМ глюкозы, 100 нг/мл GDF8 и 100 нМ смеси MCX в течение второго дня, после чего еще день обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ глюкозы и 100 нг/мл GDF8.
b. Этап 2 (первичная кишечная трубка - 2 дня). Клетки обрабатывались средой MCDB-131, обогащенной 0,1% BSA без жирных кислот, 0,0012 г/мл бикарбоната натрия, 1X GlutaMax™, 5 мМ D-глюкозы, 0,25 мМ аскорбиновой кислоты и 25 нг/мл FGF7 в течение двух дней.
c. Этап 3 (передняя кишка - 2 дня). Клетки обрабатывались средой MCDB131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 10 нг/мл активина A, 25 нг/мл FGF7, 0,25 мМ аскорбиновой кислоты, 0,25 мкM SANT-1, 1 мкM RA, 200 нМ TPB, 100 нМ LDN-193189 в течение дня 1, после чего обрабатывались tMCDB131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 10 нг/мл активина A, 25 нг/мл FGF7, 0,25 мМ аскорбиновой кислоты, 0,25 мкM SANT-1, 1 мкM RA, 200 нМ TPB, 10 нМ LDN-193189 в течение еще одного дня.
d. Этап 4 (панкреатическая клетка-предшественница передней кишки - 2 дня). Клетки обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот, 0,25 мкM SANT-1, 50 нМ RA, 200 нМ TPB, 50 нМ LDN-193189, 0,1 мМ аскорбиновой кислоты в течение двух дней.
е. Этап 5 (панкреатическая энтодерма, 3 дня). Клетки обрабатывались средой MCDB-131, обогащенной 1:200 раствором ITS-X, 2,5 мМ глюкозы, 1X GlutaMax™, 0,0015 г/мл бикарбоната натрия, 2% BSA без жирных кислот и следующими культурными условиями в течение 3 дней:
• +0,1 мМ аскорбиновой кислоты;
• 0,1 мМ аскорбиновой кислоты + 50 нМ RA;
• 0,1 мМ аскорбиновой кислоты + 50 нМ RA + 0,25 мкM SANT-1;
• 0,1 мМ аскорбиновой кислоты + 50 нМ RA + 0,25 мкM SANT-1+ 50 нМ LDN-193189;
• 0,1 мМ аскорбиновой кислоты + 50 нМ RA + 0,25 мкM SANT-1+ 1 мкM Alk5 инг;
• 0,1 мМ аскорбиновой кислоты + 50 нМ RA + 0,25 мкM SANT-1+ 1 мкM Alk5 инг + 50 нМ LDN-193189.
Фиг. 22A-22L показывают данные анализов ПЦР экспрессии Pax4 в реальном времени (фиг. 22A); Pax6 (фиг. 22B); PDX1 (фиг. 22C); PTF1a (фиг. 22D); глюкагон (фиг. 22E); инсулин (фиг. 22F); NeuroD (фиг. 22G); ngn3 (фиг. 22H); Zic1 (фиг. 22I); CDX2 (фиг. 22J); альбумин (фиг. 22K); NKX6.1 (фиг. 22L) в клетках линии эмбриональных стволовых клеток H1, дифференцированных согласно примеру 13 и собранных на этапе S5 в день 3.
В конце этапа 5 культуры, обработанные вышеуказанными сочетаниями реагентов, были окрашены методами иммуногистохимии для проверки наличия гормонов инсулина, глюкагона и соматостатина. Таблица VIII показывает средний процент инсулин-, глюкагон- и соматостатин-положительных клеток и полигормональных клеток (экспрессия еще двух гормонов в одной клетке).
Как показано на фиг. 22 и в таблице VIII ниже, добавление малой дозы ретиноевой кислоты плюс аскорбиновой кислоты на этапе 5 значительно уменьшает общее число гормон-положительных клеток, в то же время увеличивая процент единичных гормональных инсулин-положительных клеток по сравнению с культурами, обработанными только витамином C на этапе S5. Также сочетание ретиноевой кислоты, аскорбиновой кислоты, ингибитора гена sonic hedgehog и ингибитора ALk5 также увеличивает число единичных гормональных инсулин-положительных клеток по сравнению с культурами, обработанными только аскорбиновой кислотой (витамином C). Эти данные показывают, что необходима уникальная комбинация факторов для генерирования единичных гормональных инсулин-положительных клеток.
Экспрессия гормонов как процент от общего числа гормонов на этапе S5 в день 3
Плюс % соматостатин +
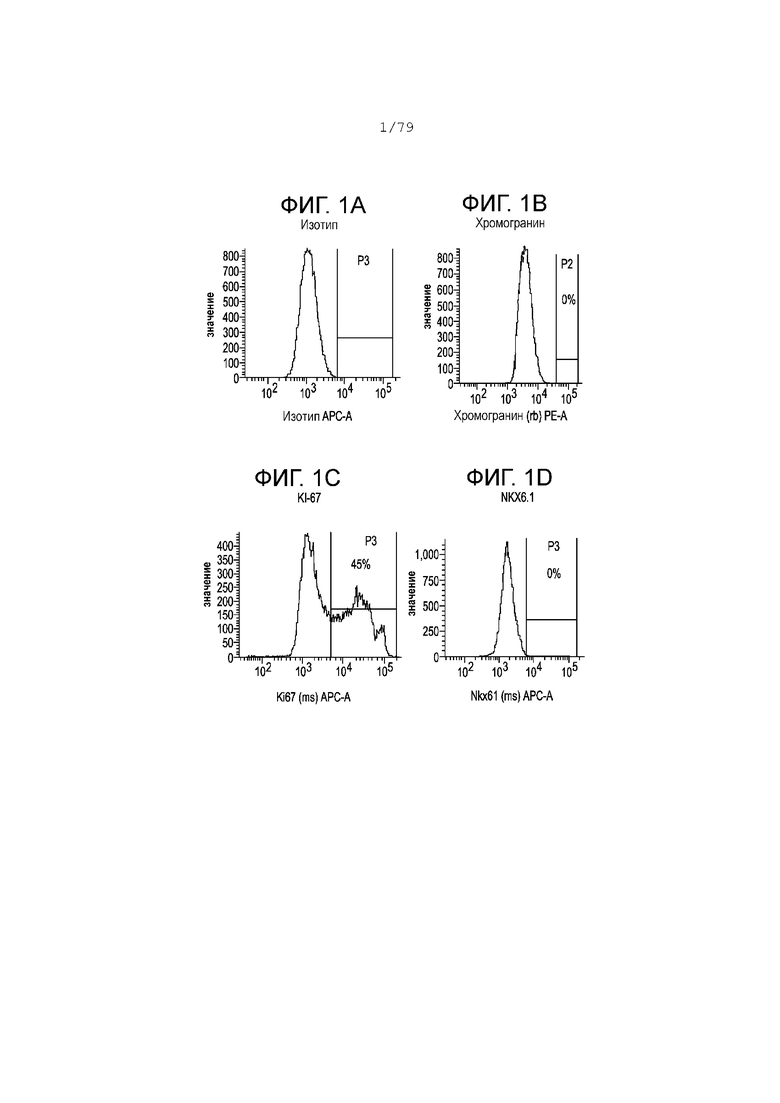
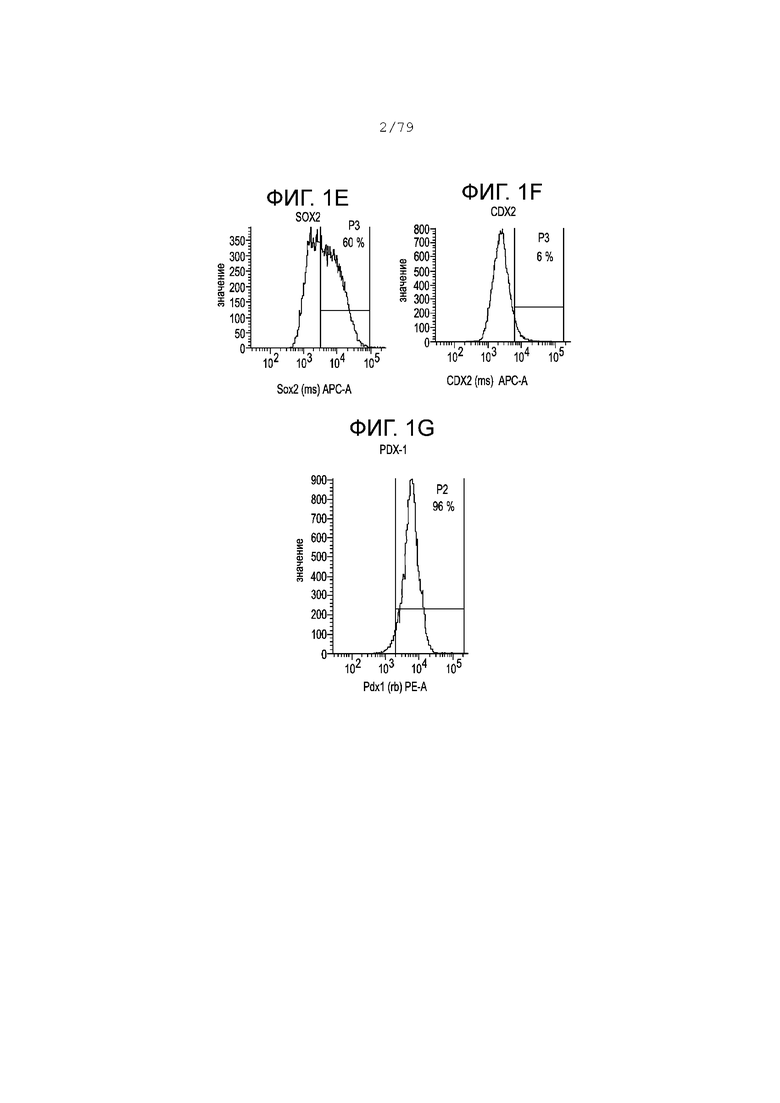
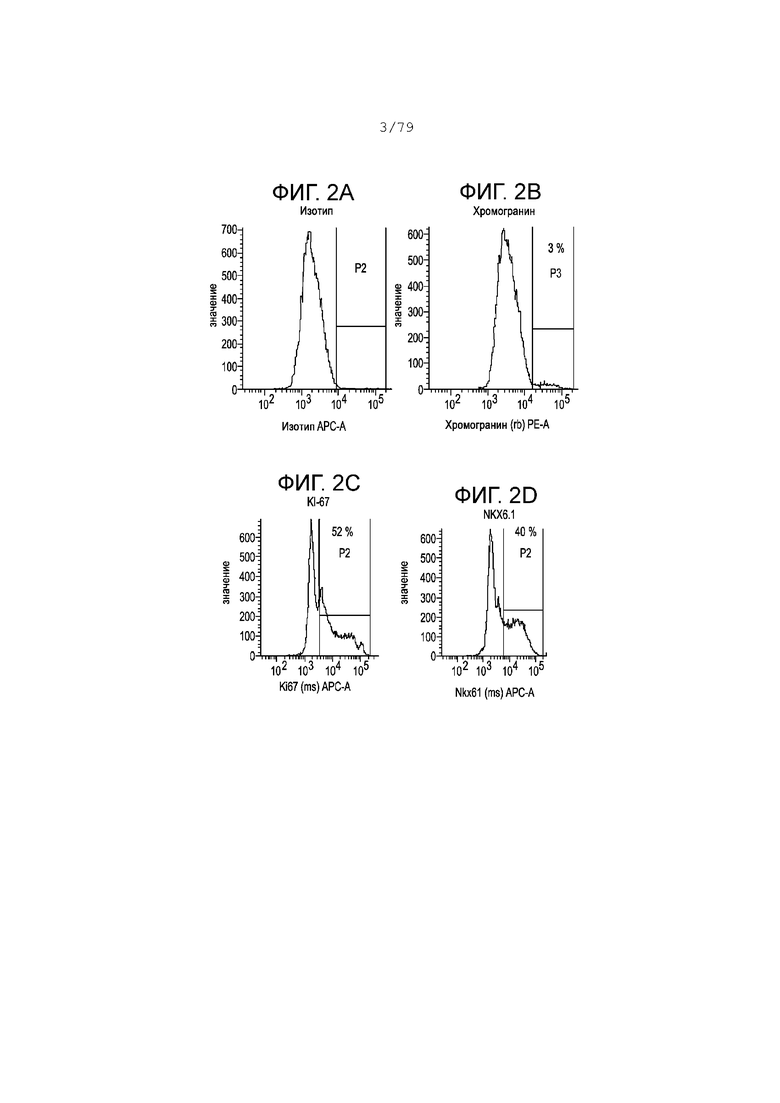
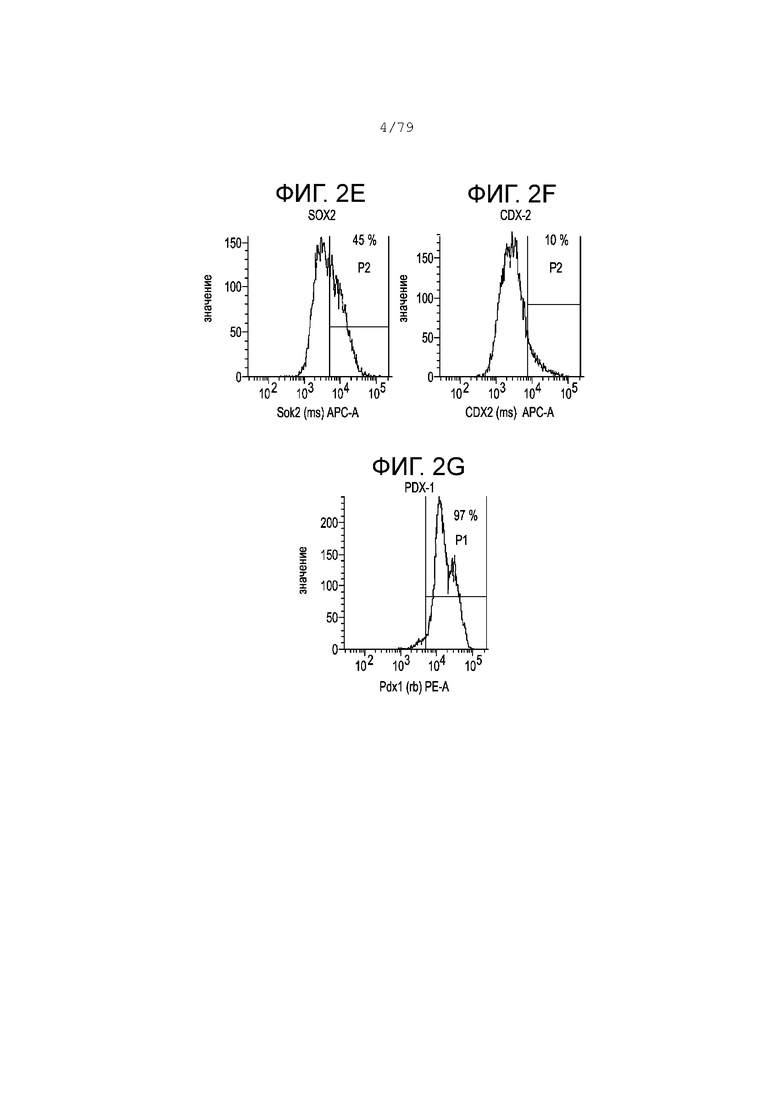
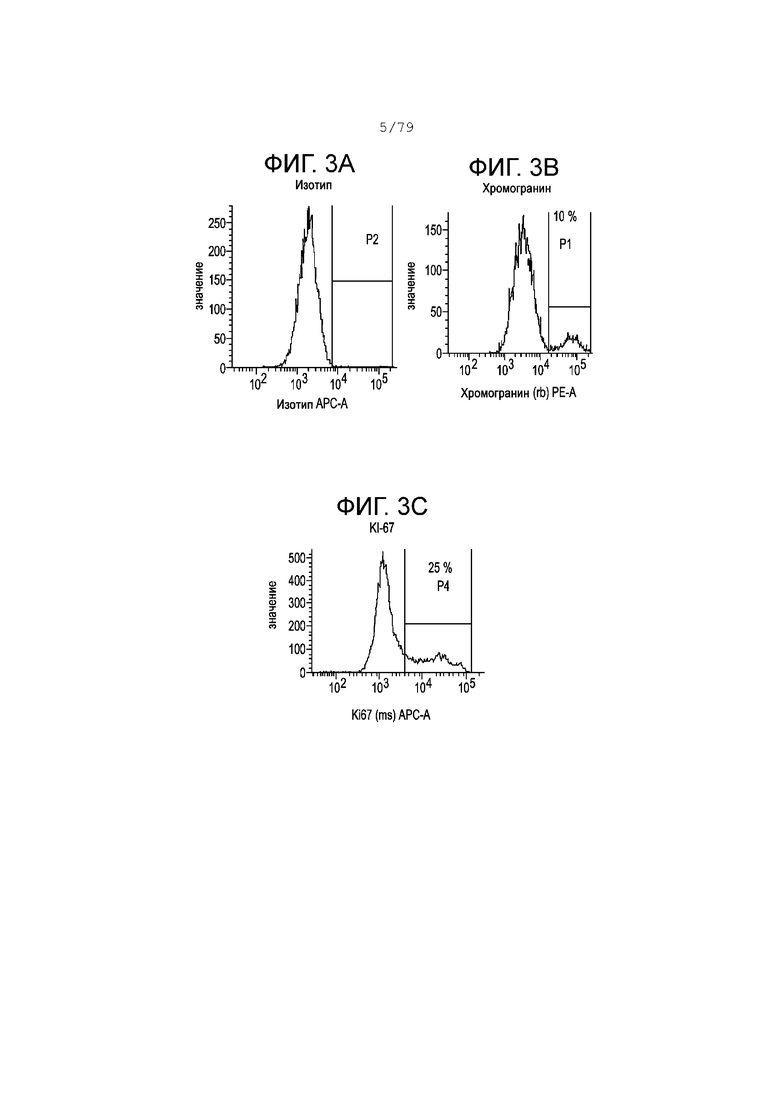
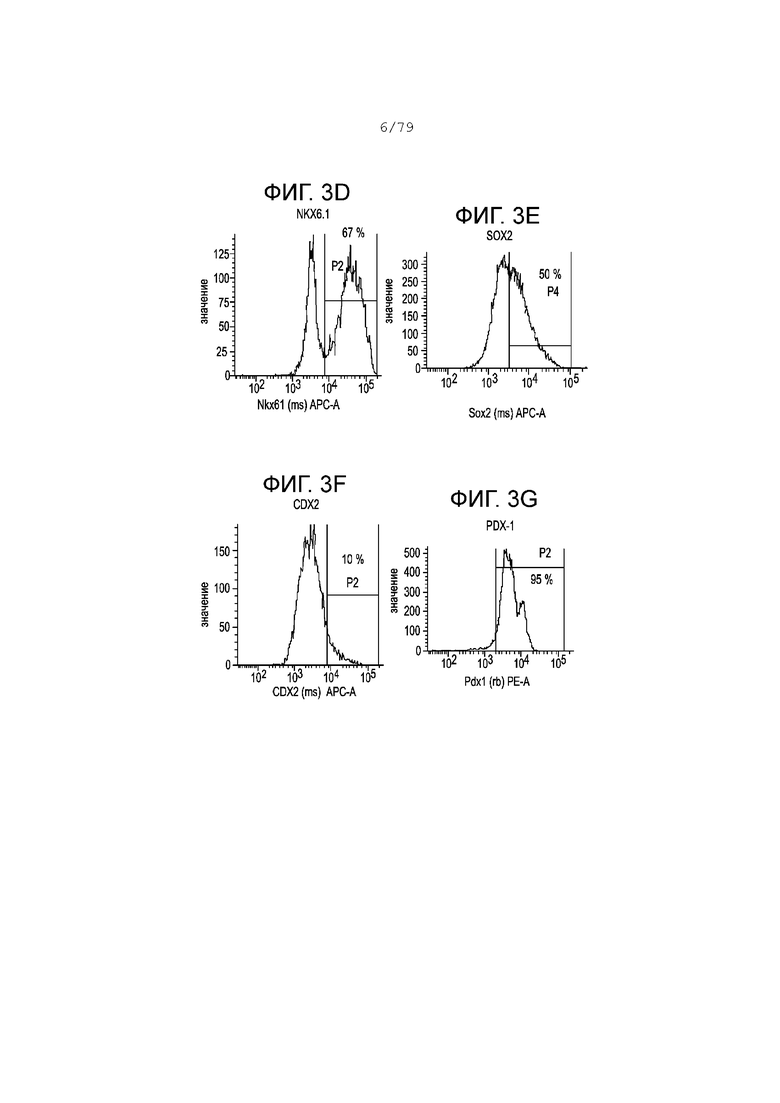
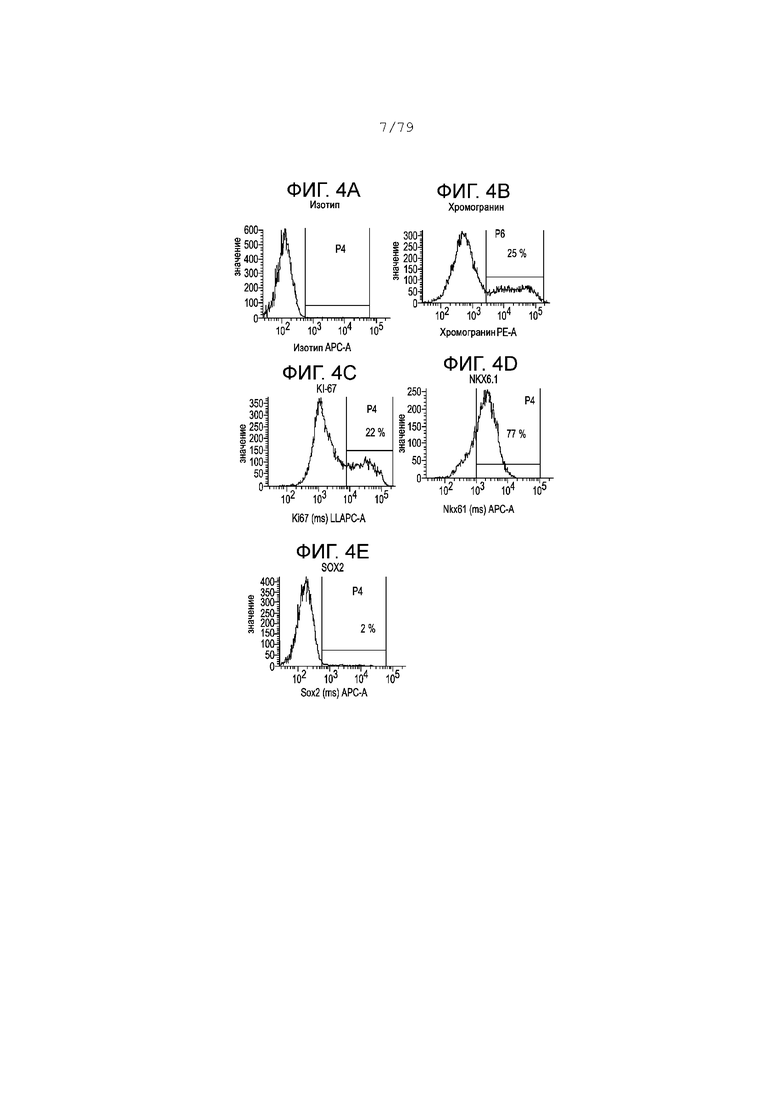
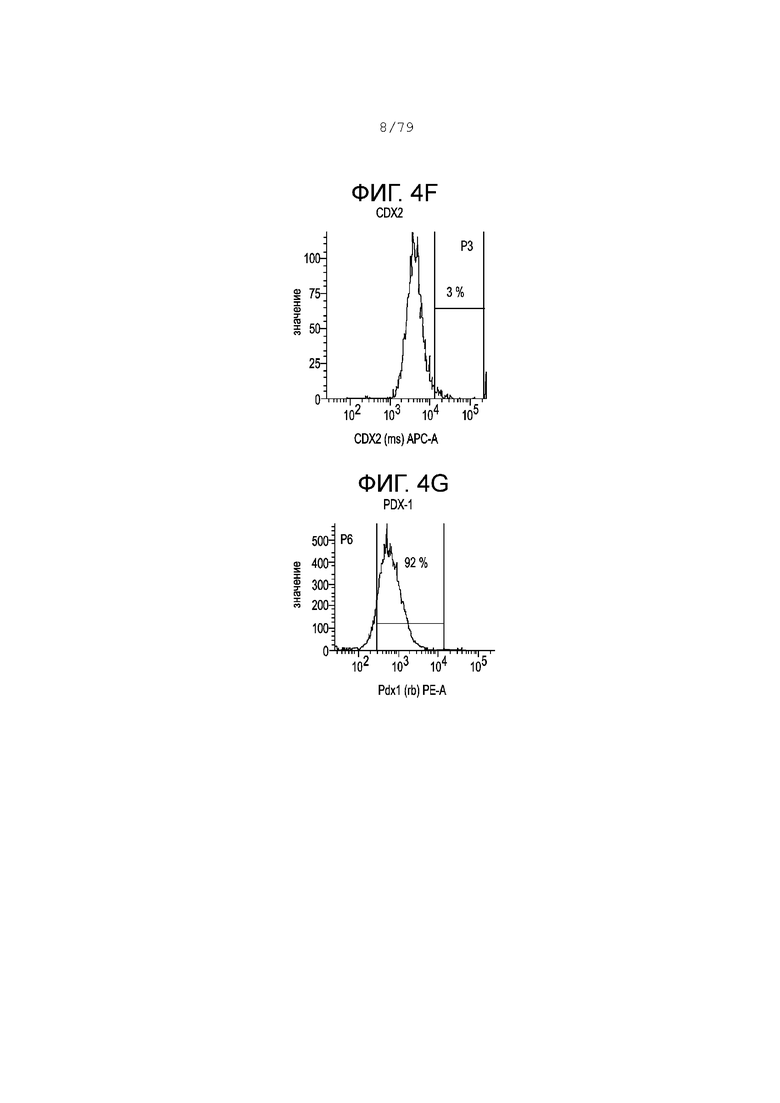
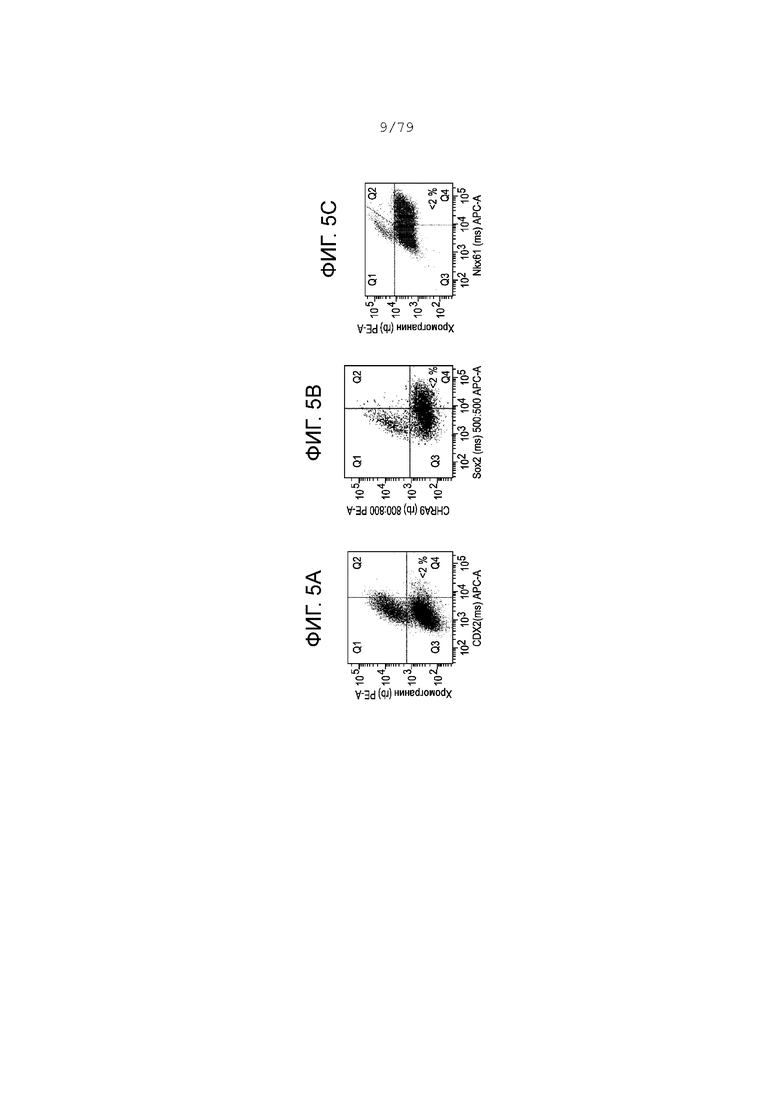
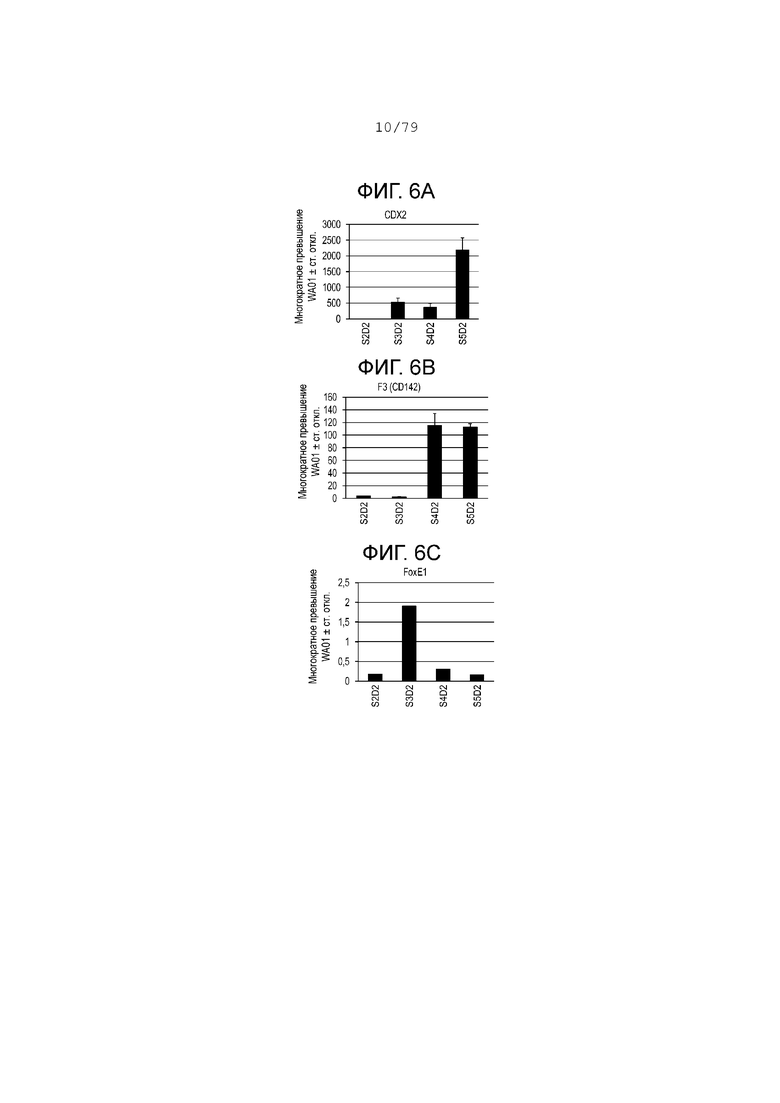
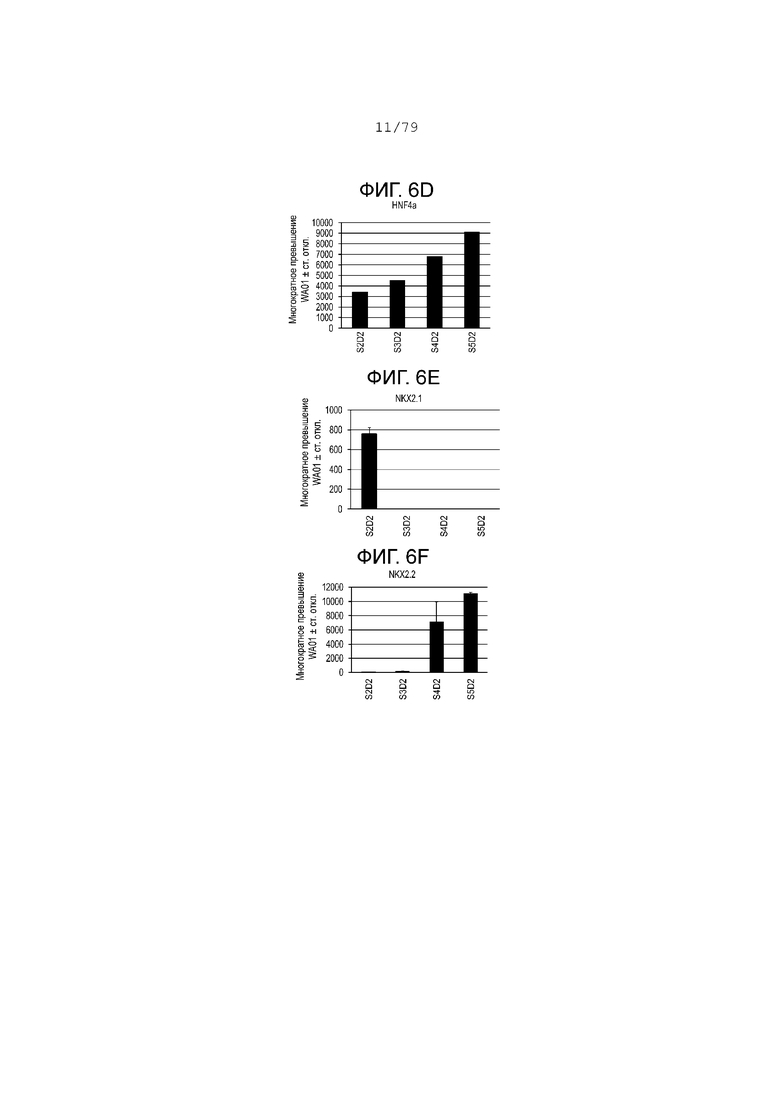
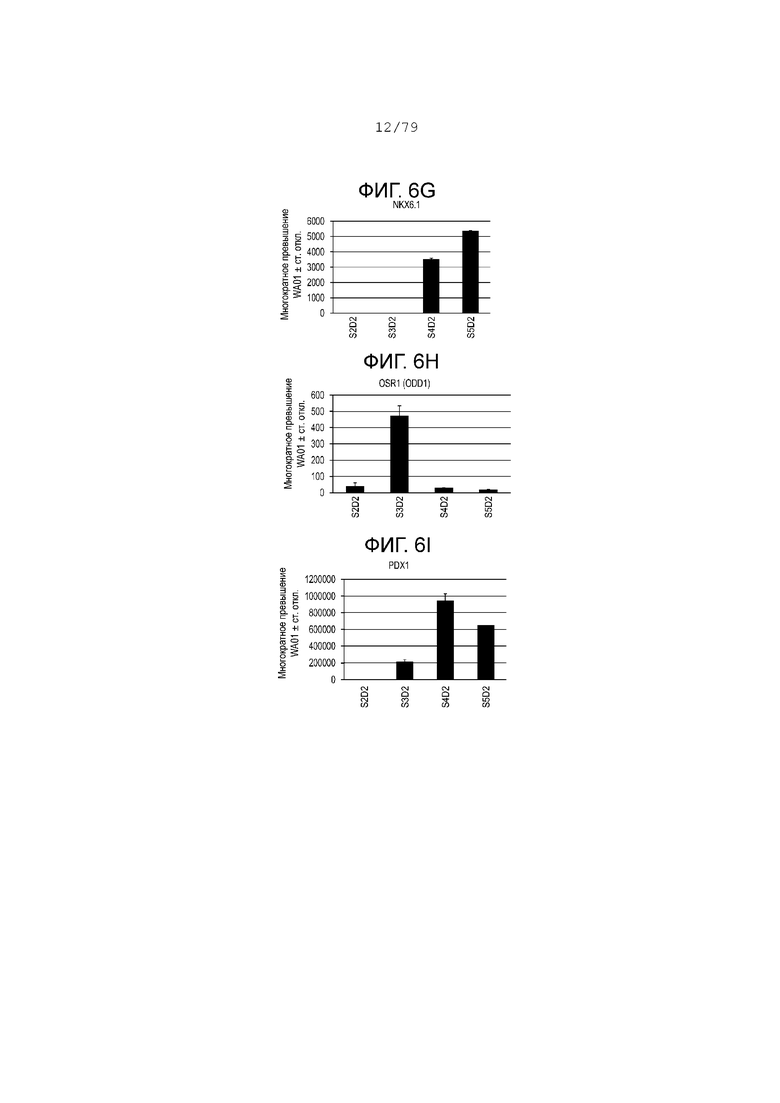
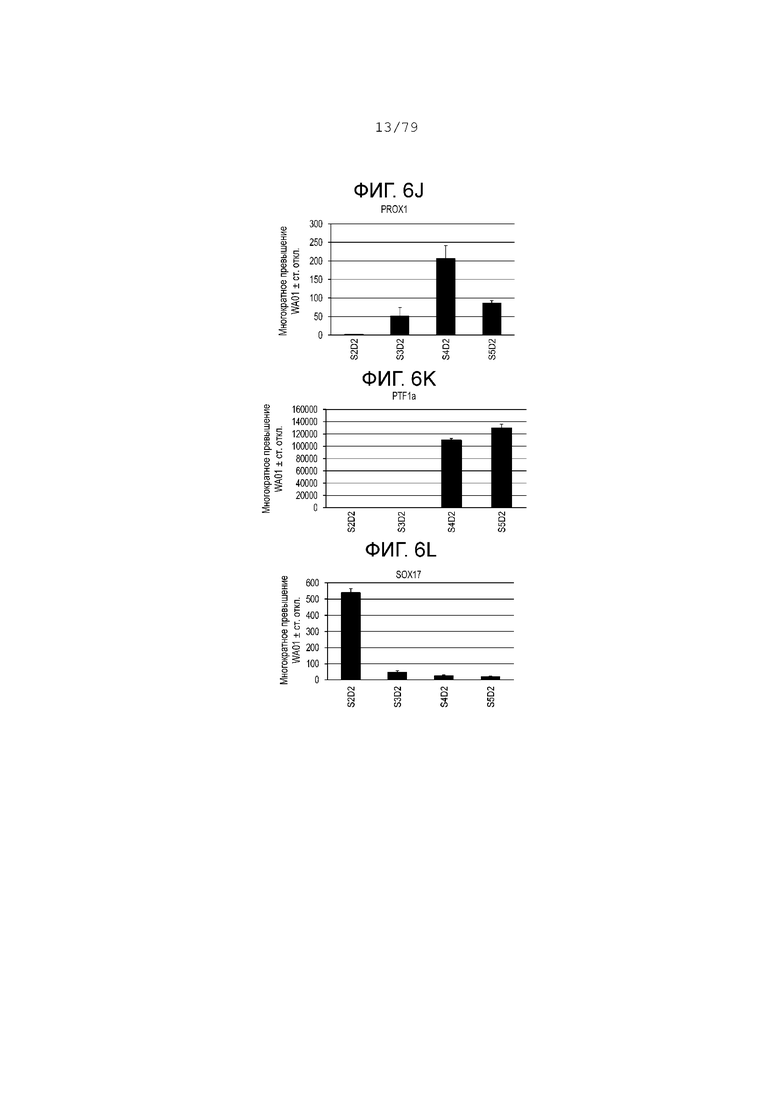
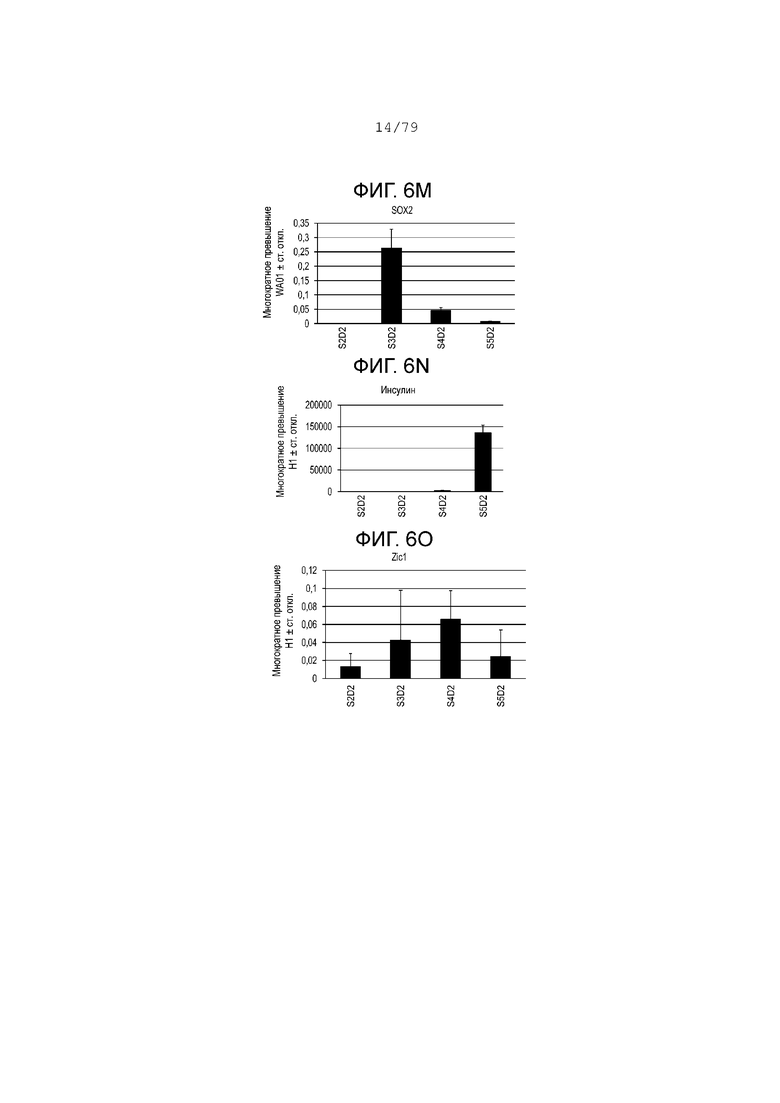
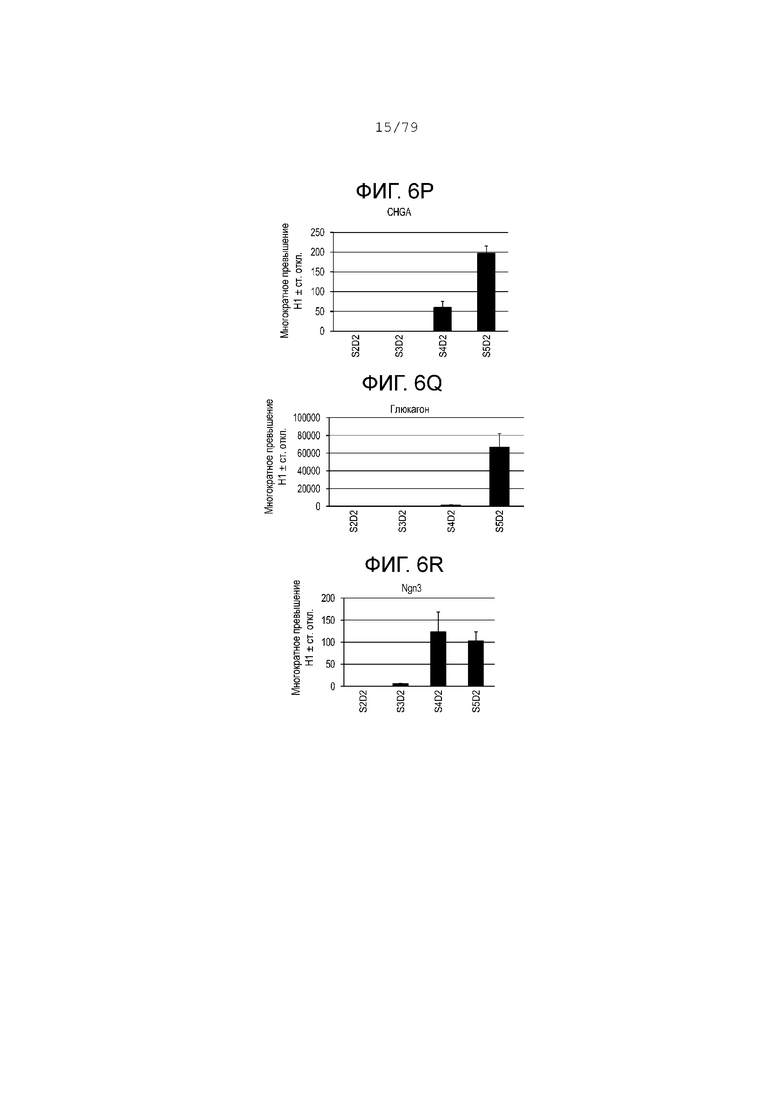
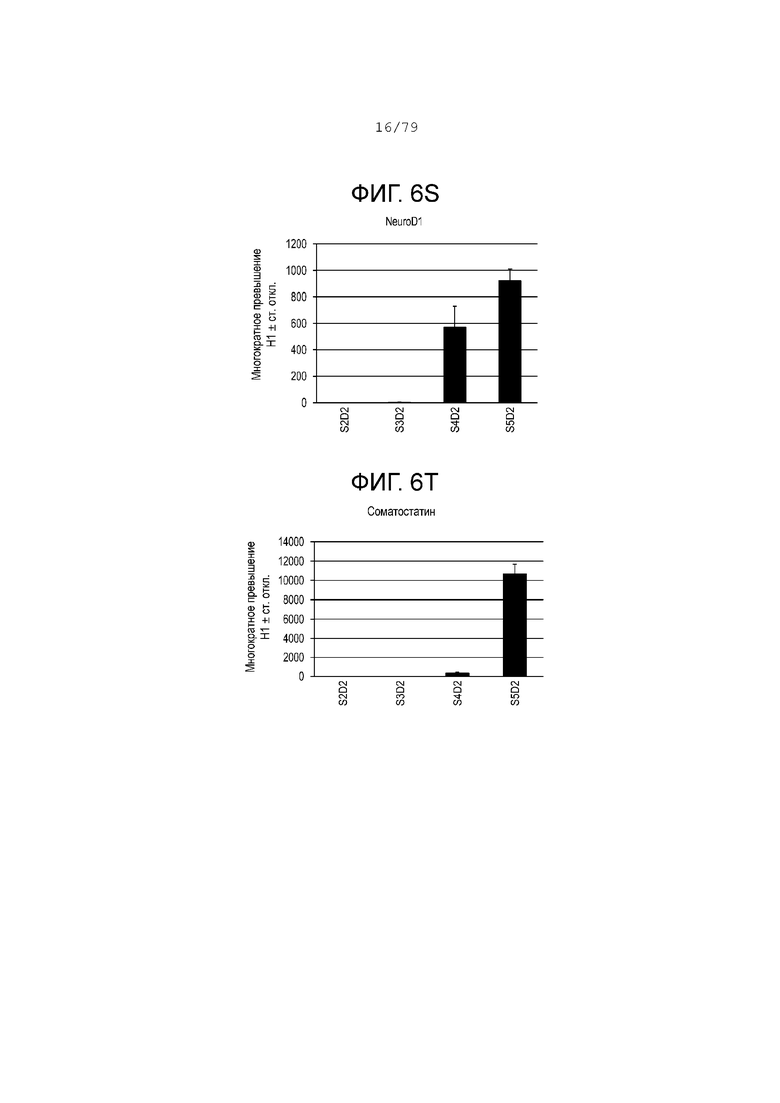
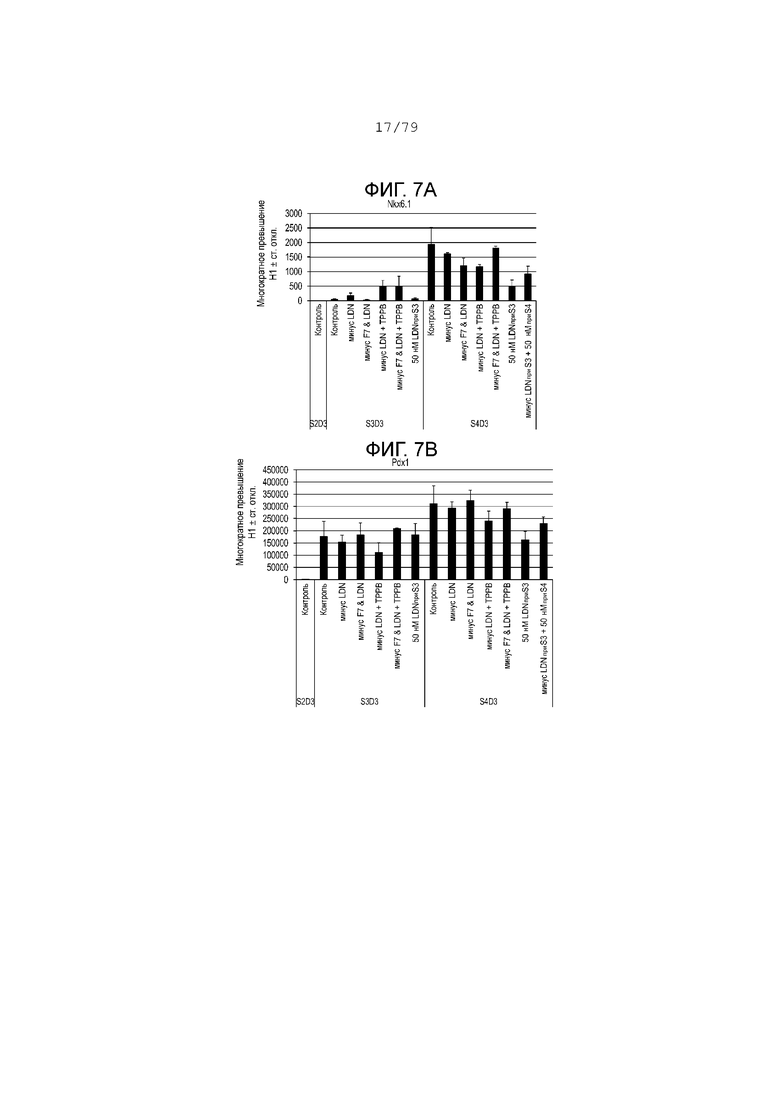
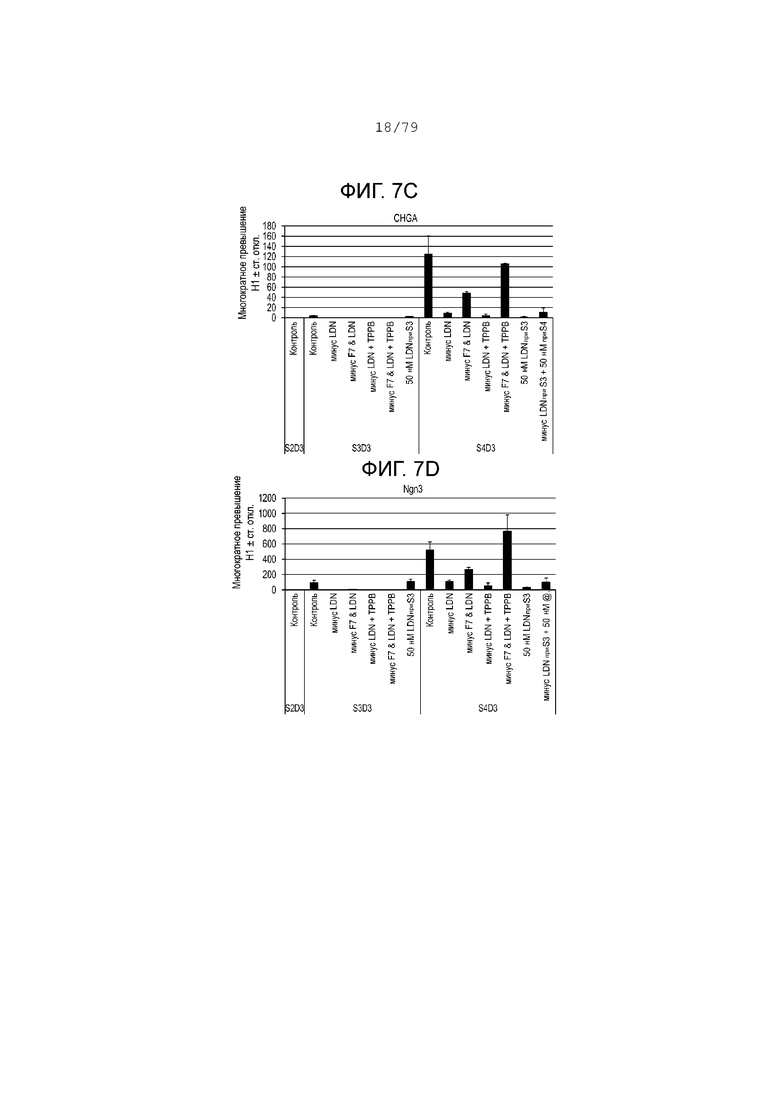
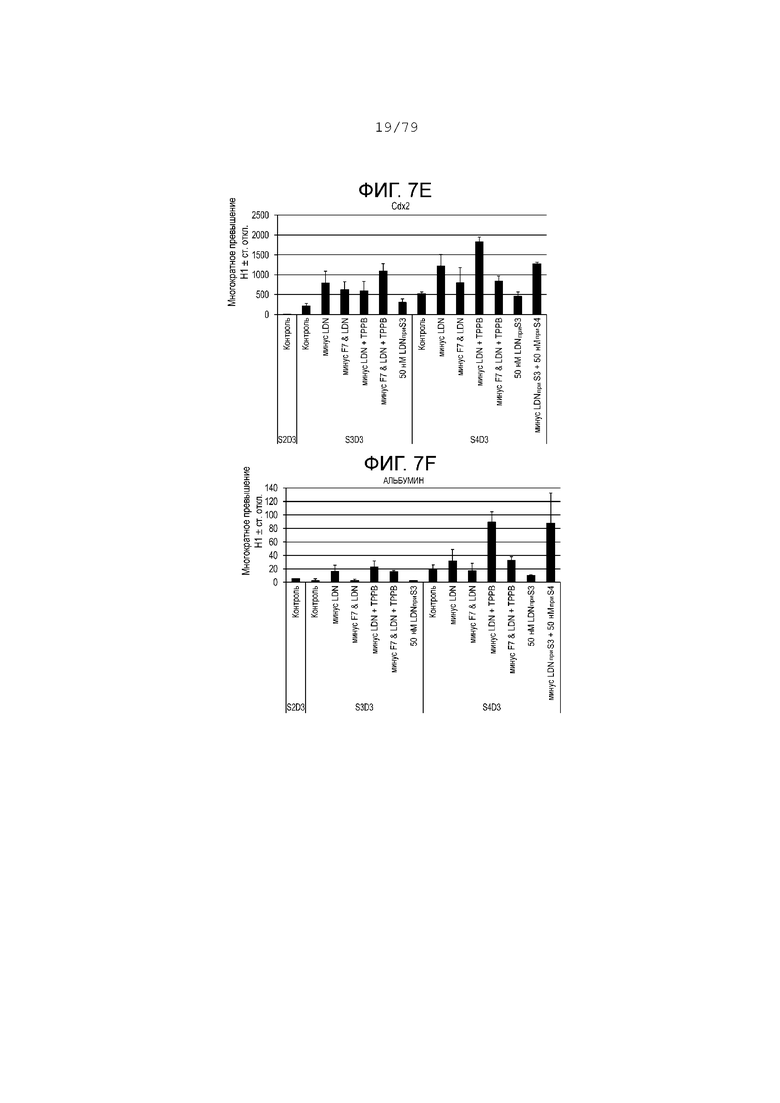

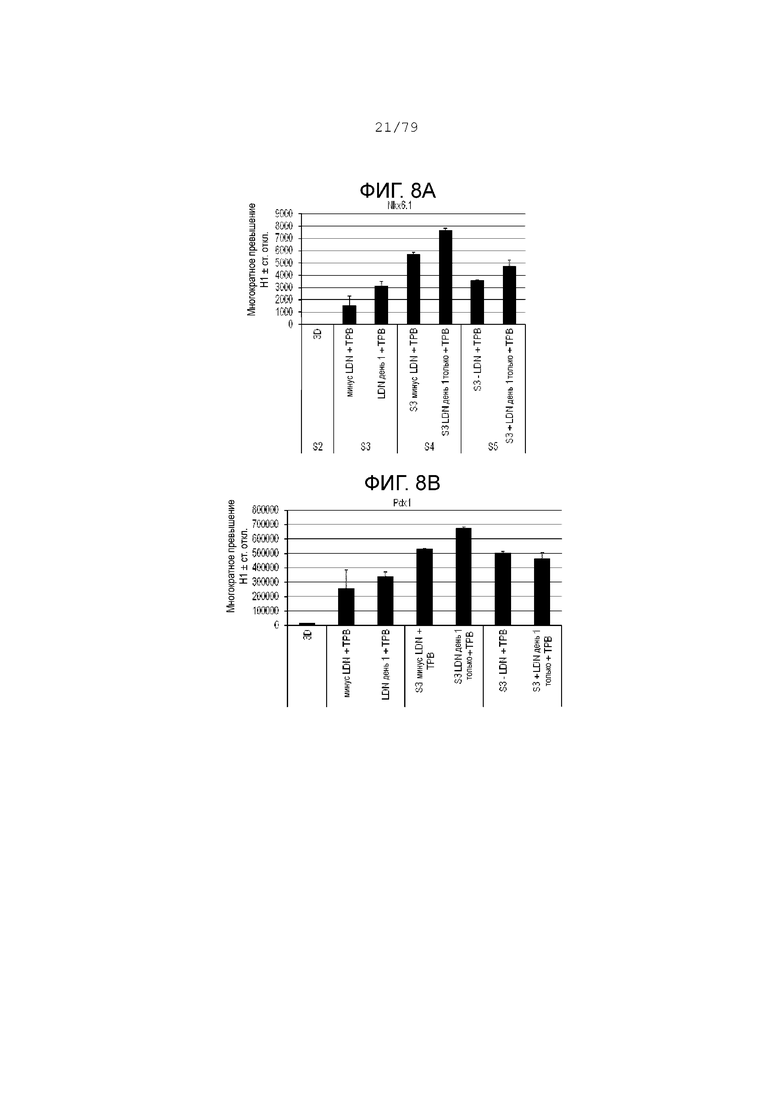
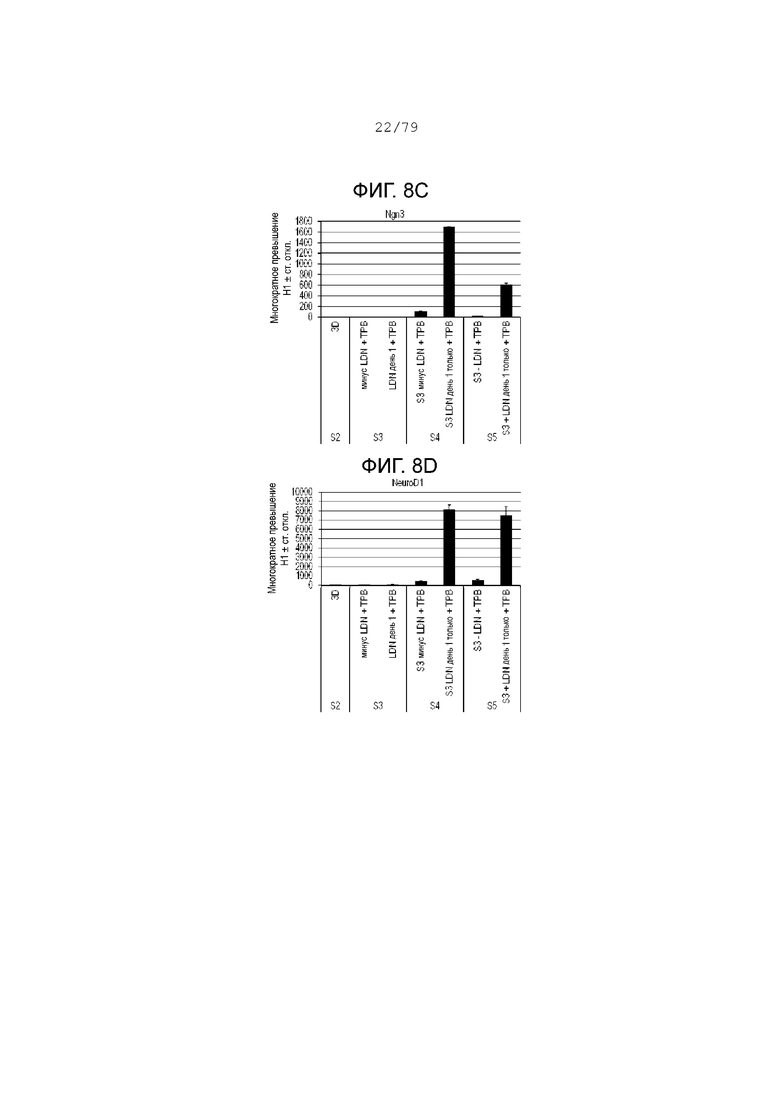
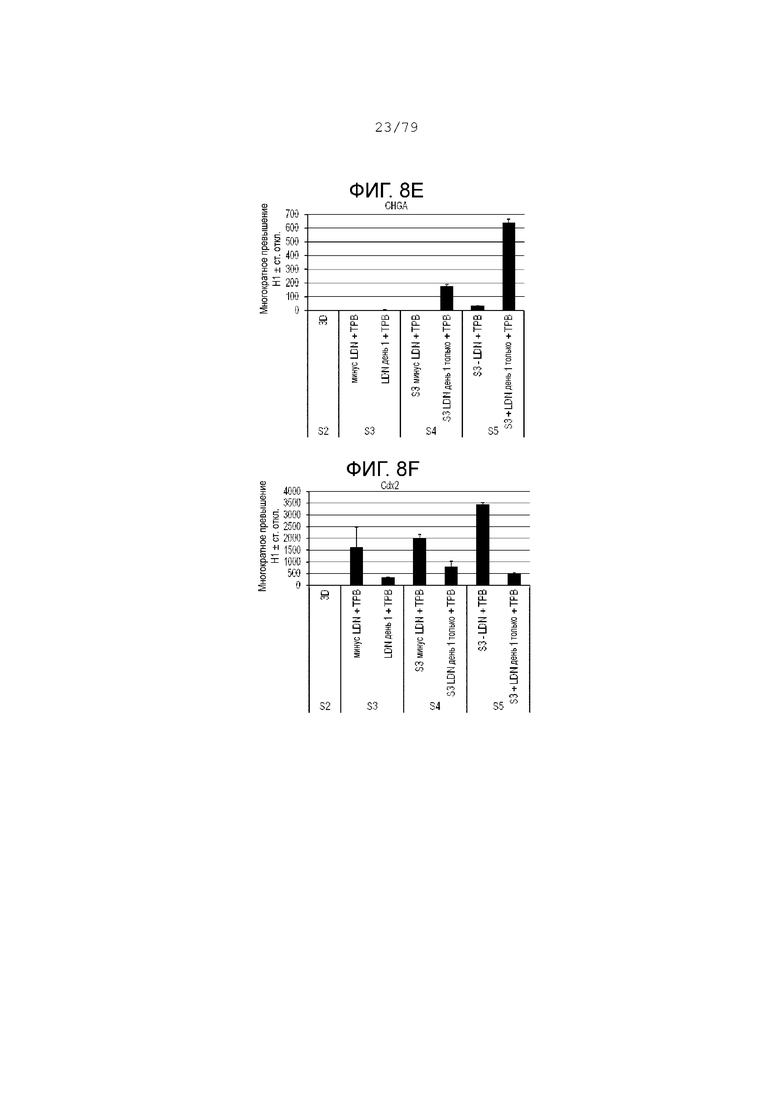
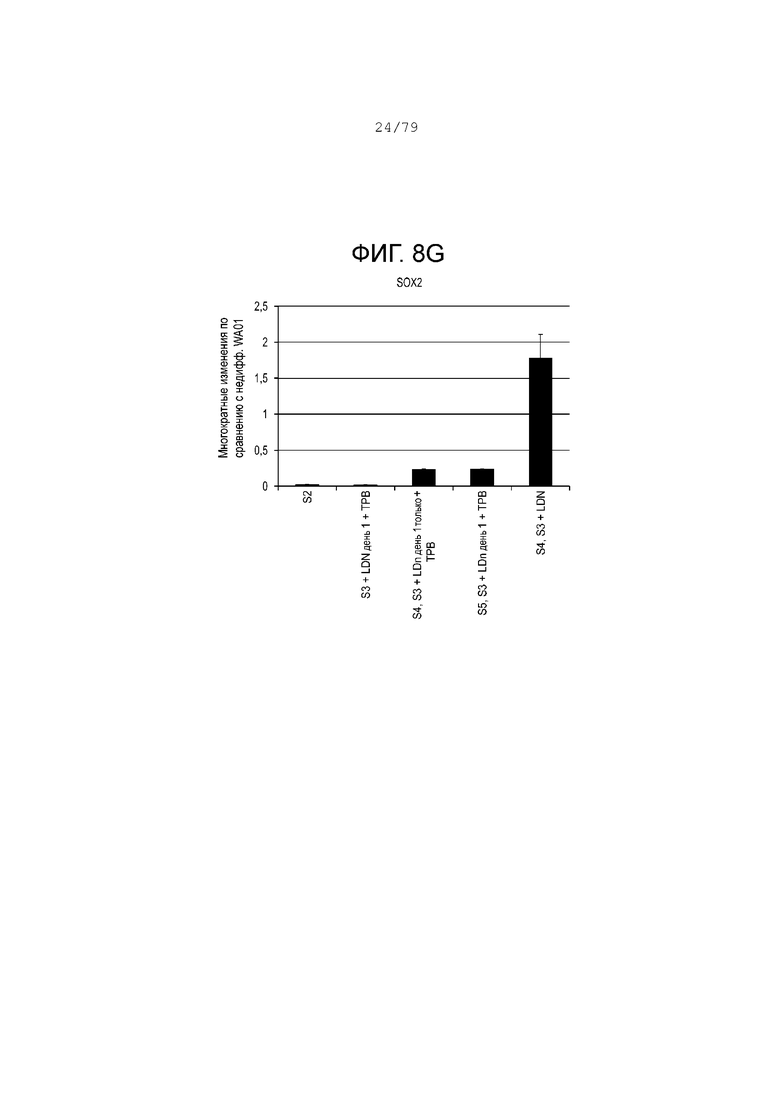
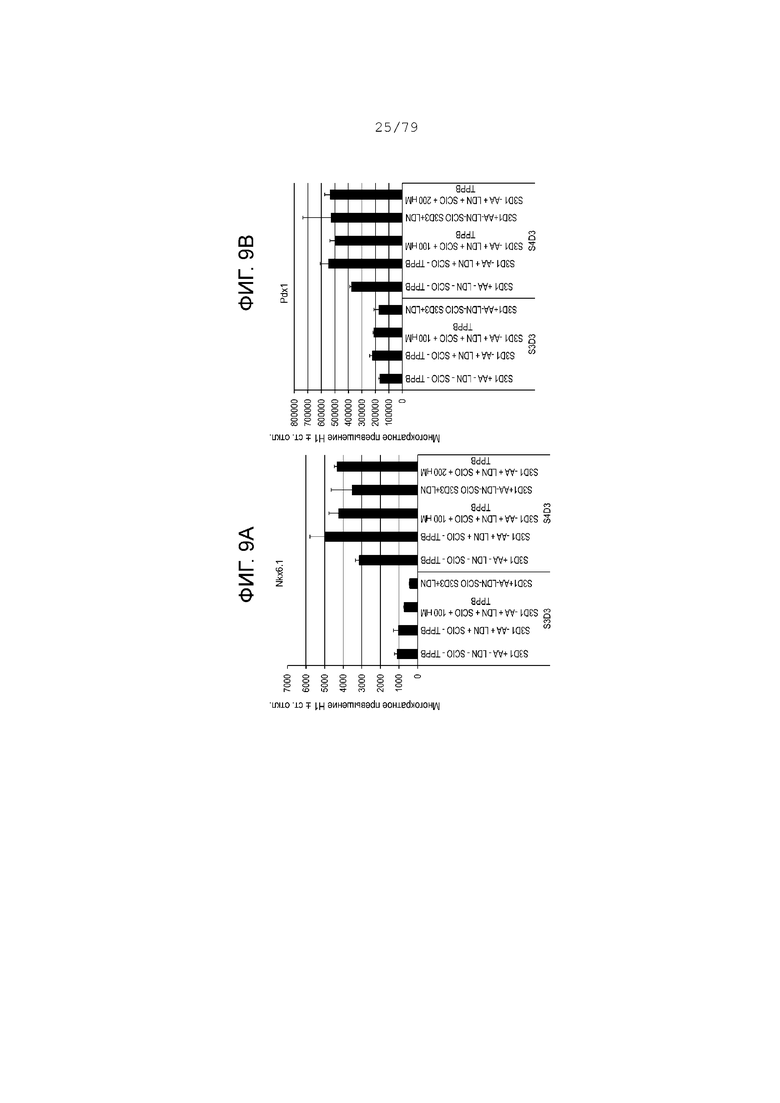

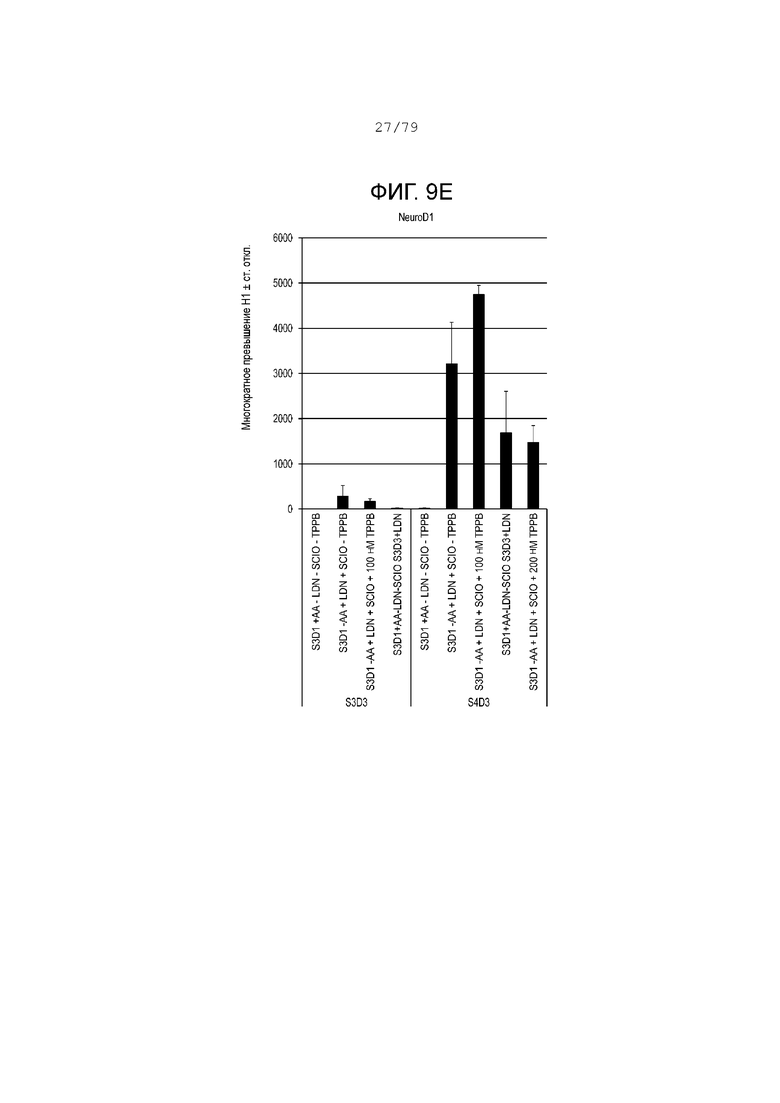

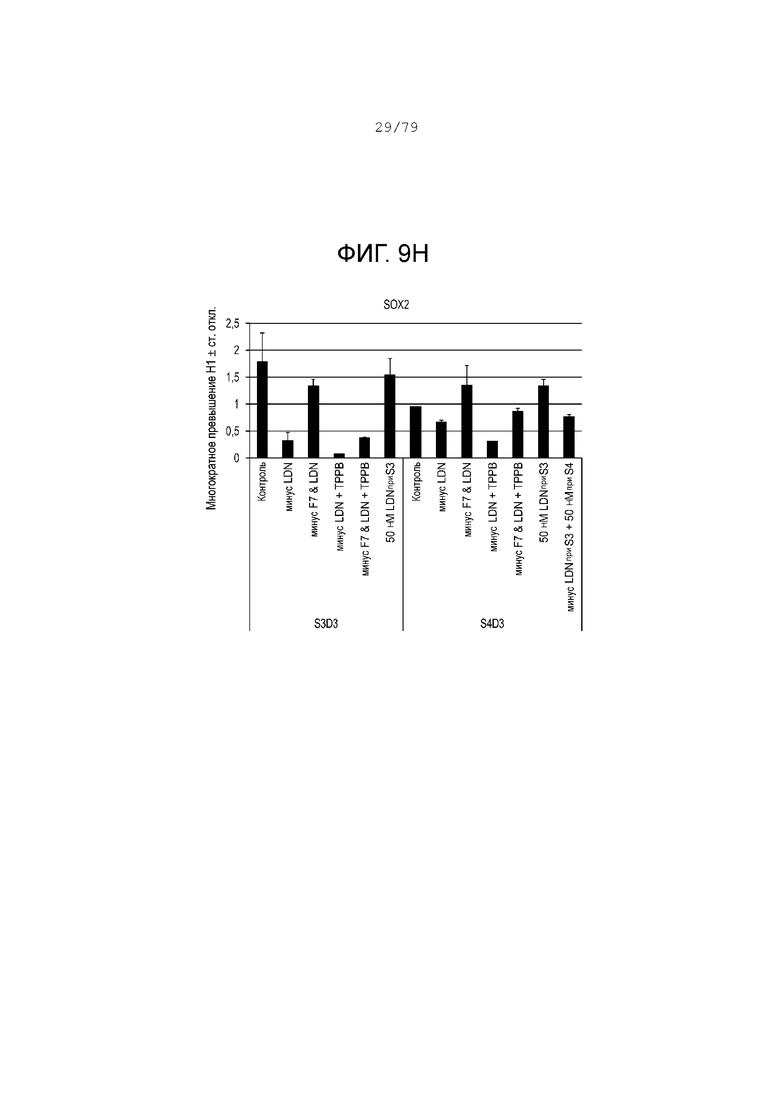
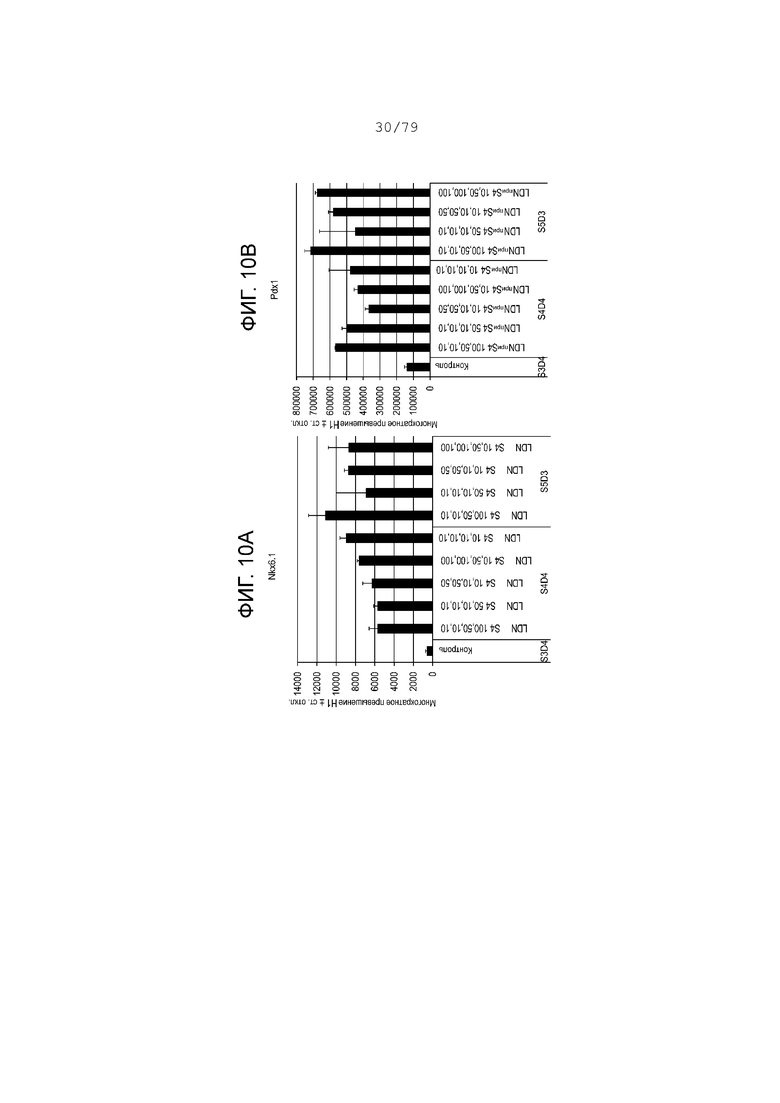
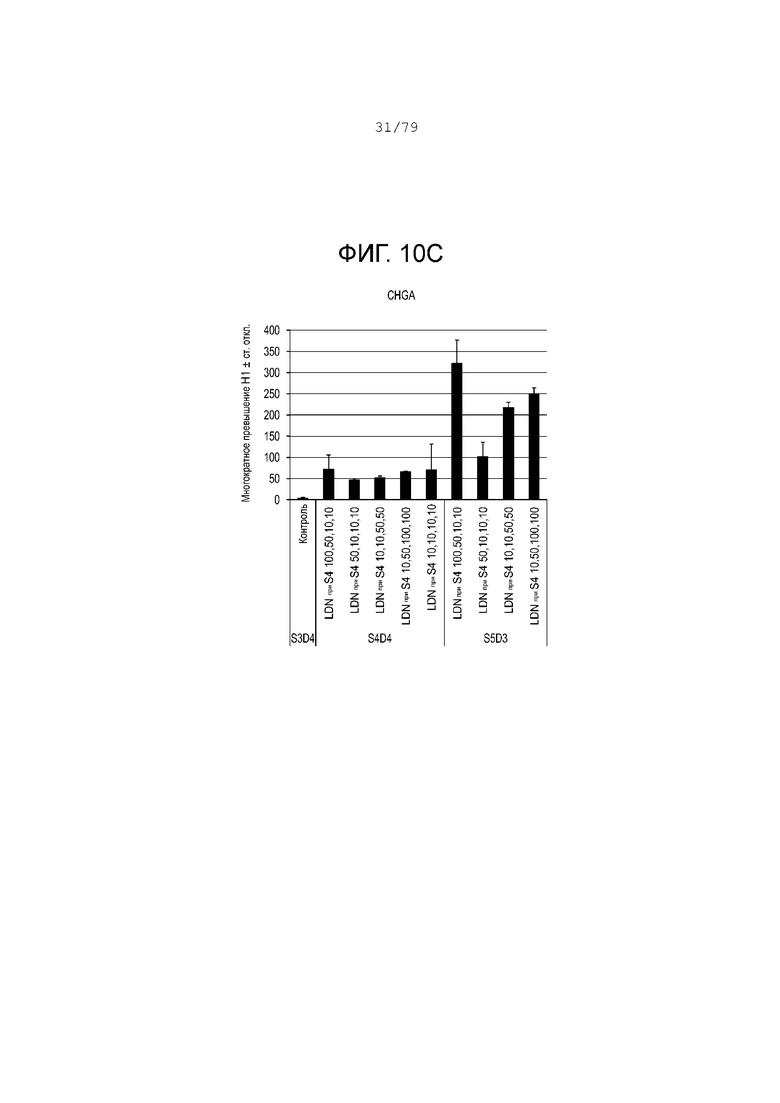
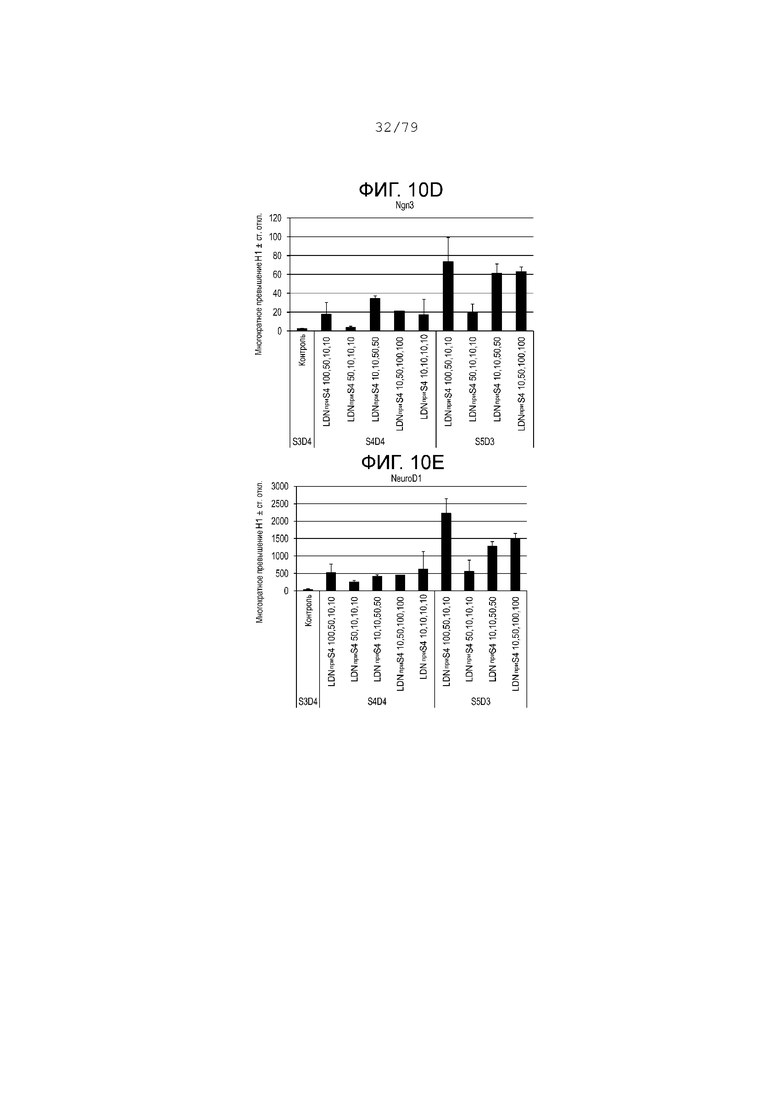
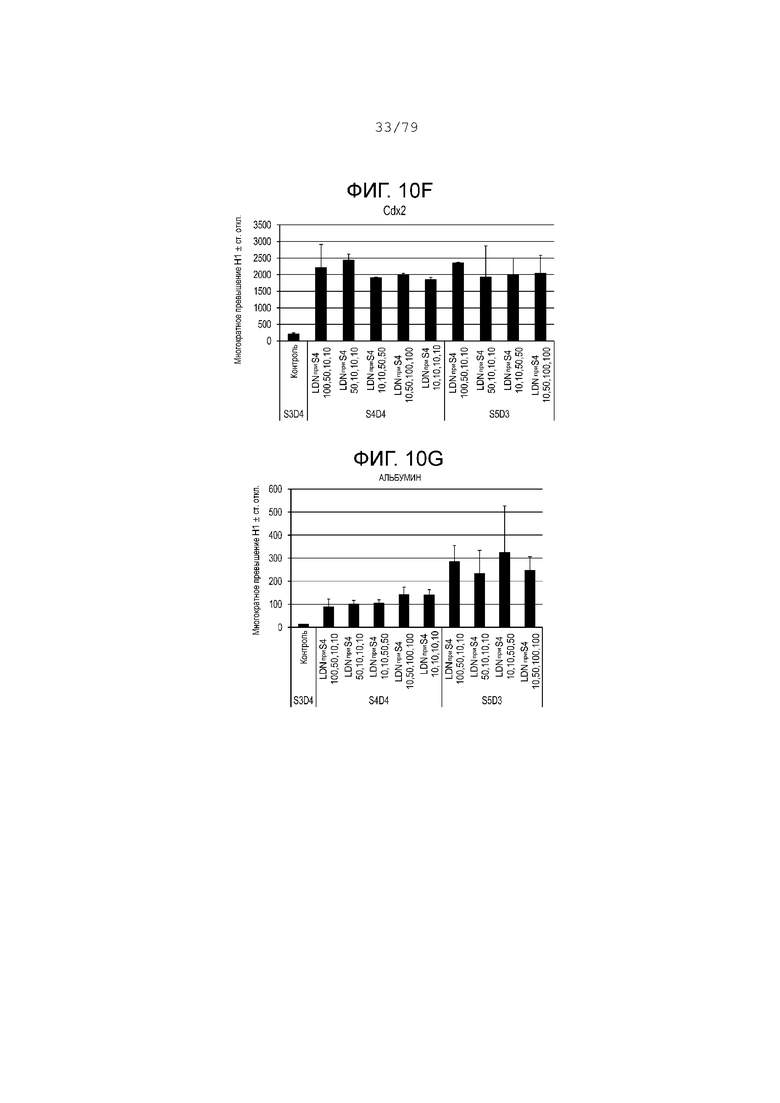
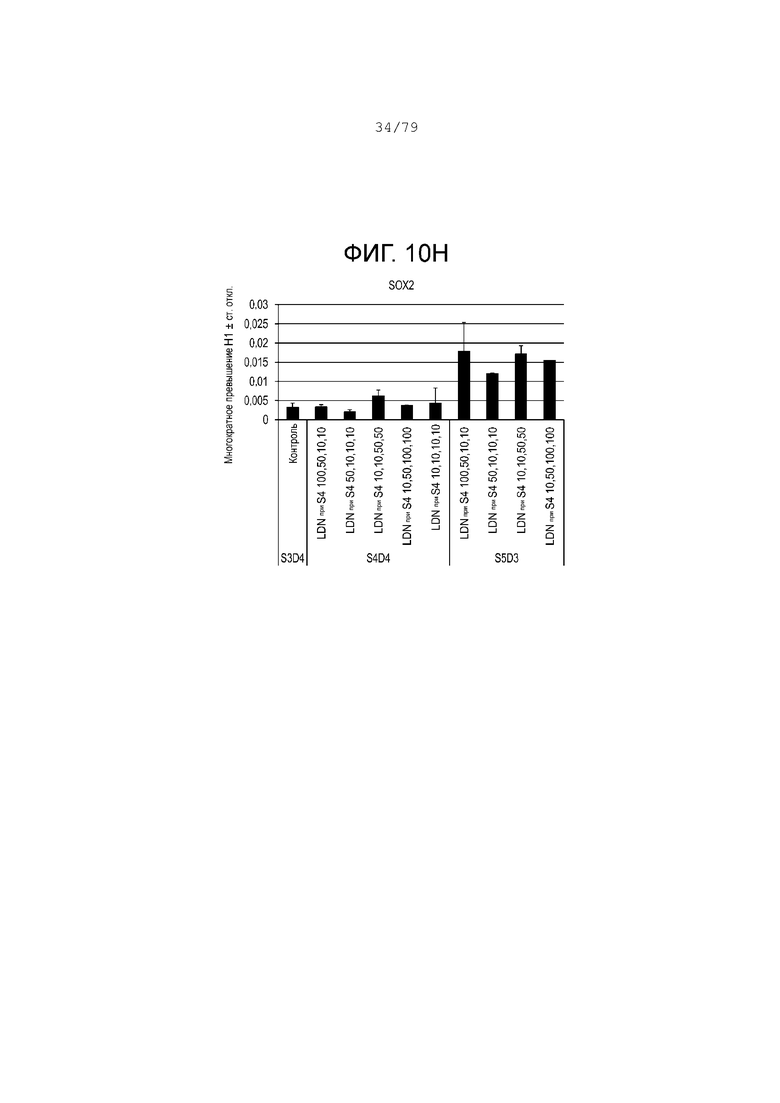
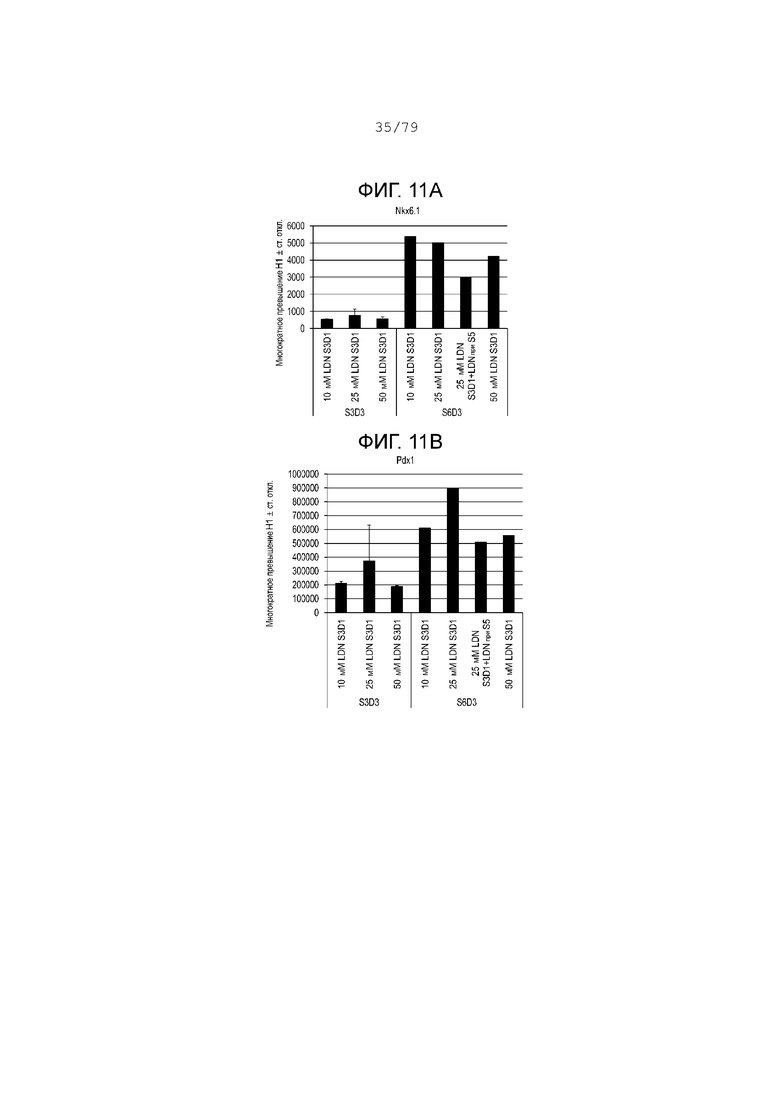
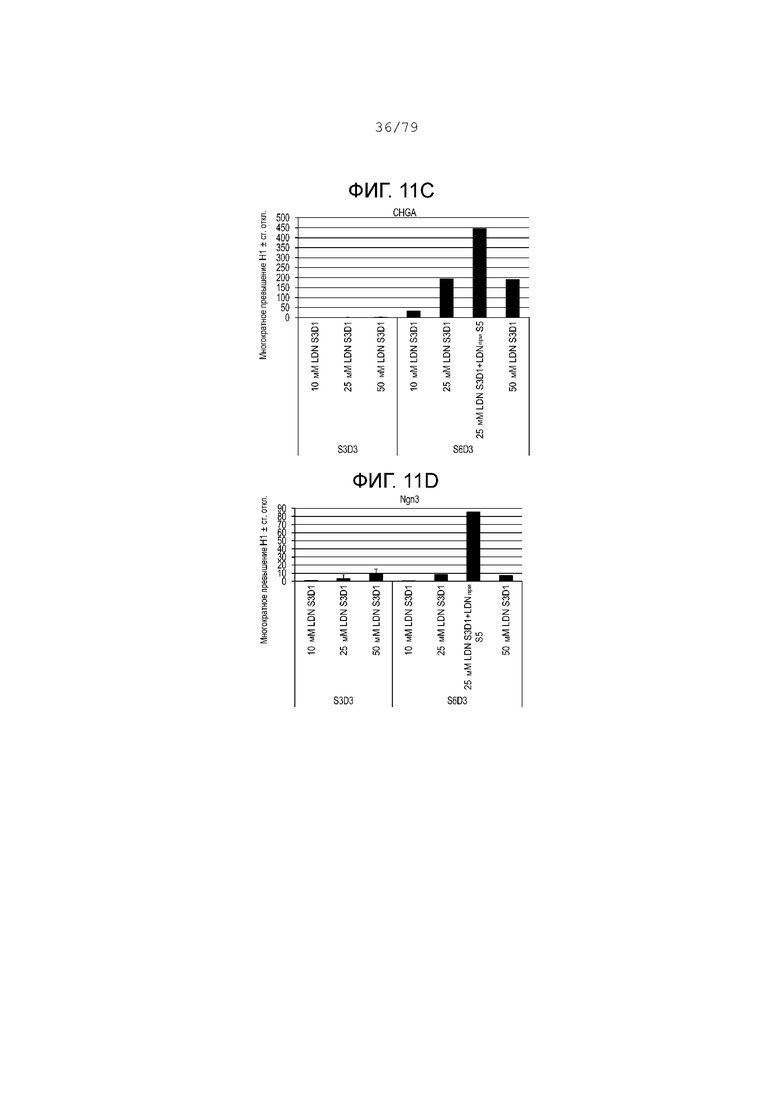
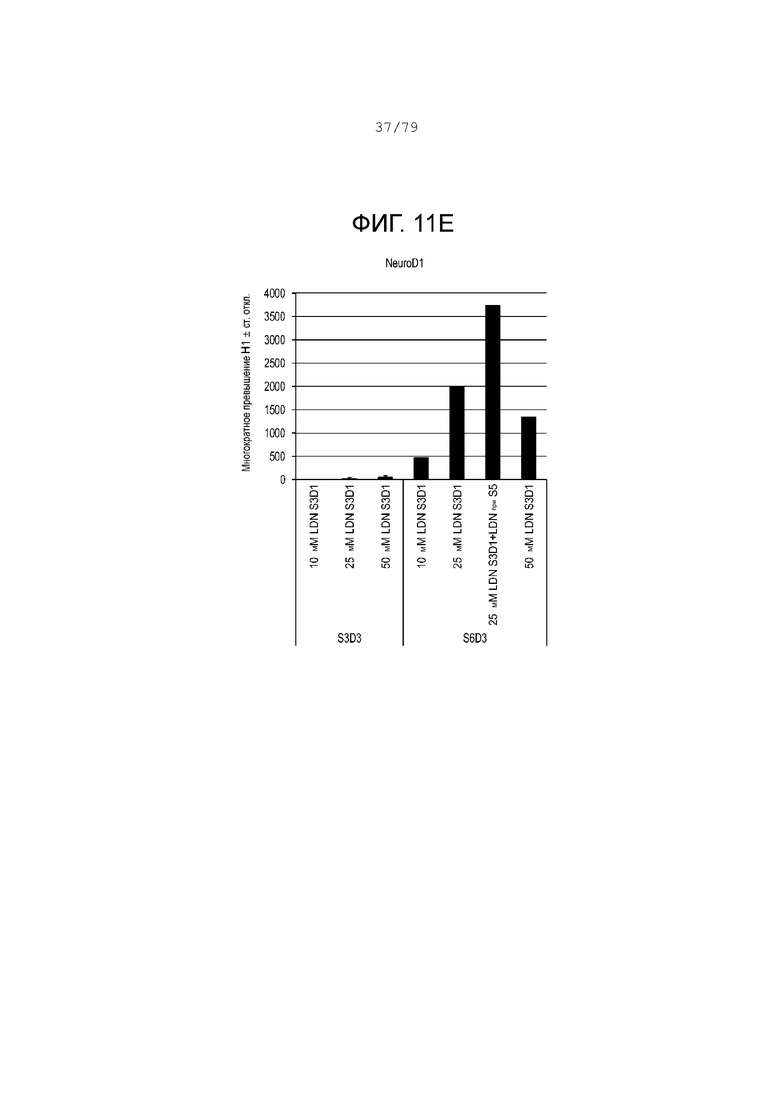
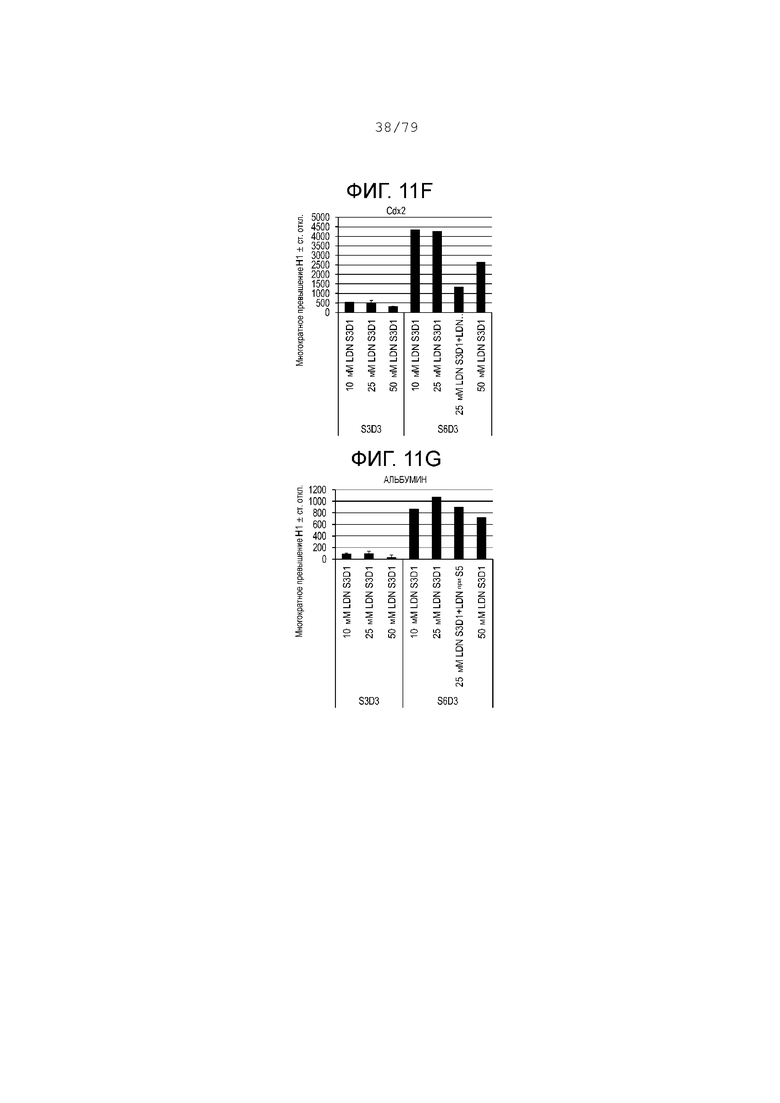
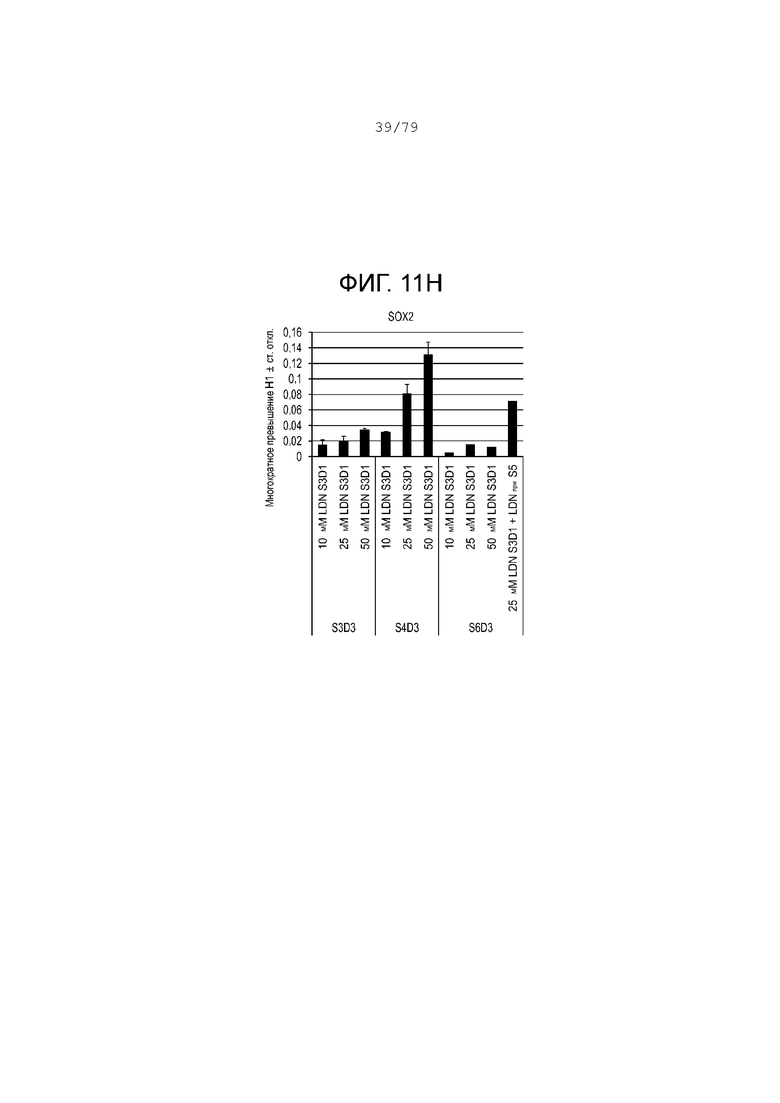


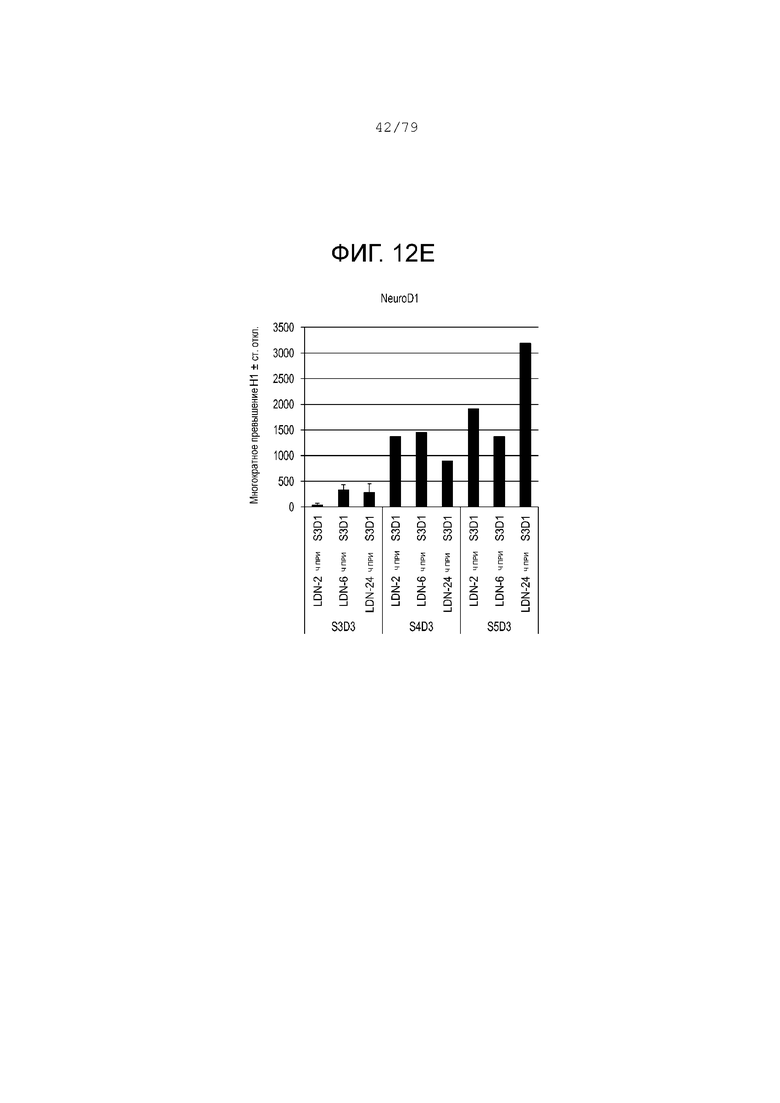

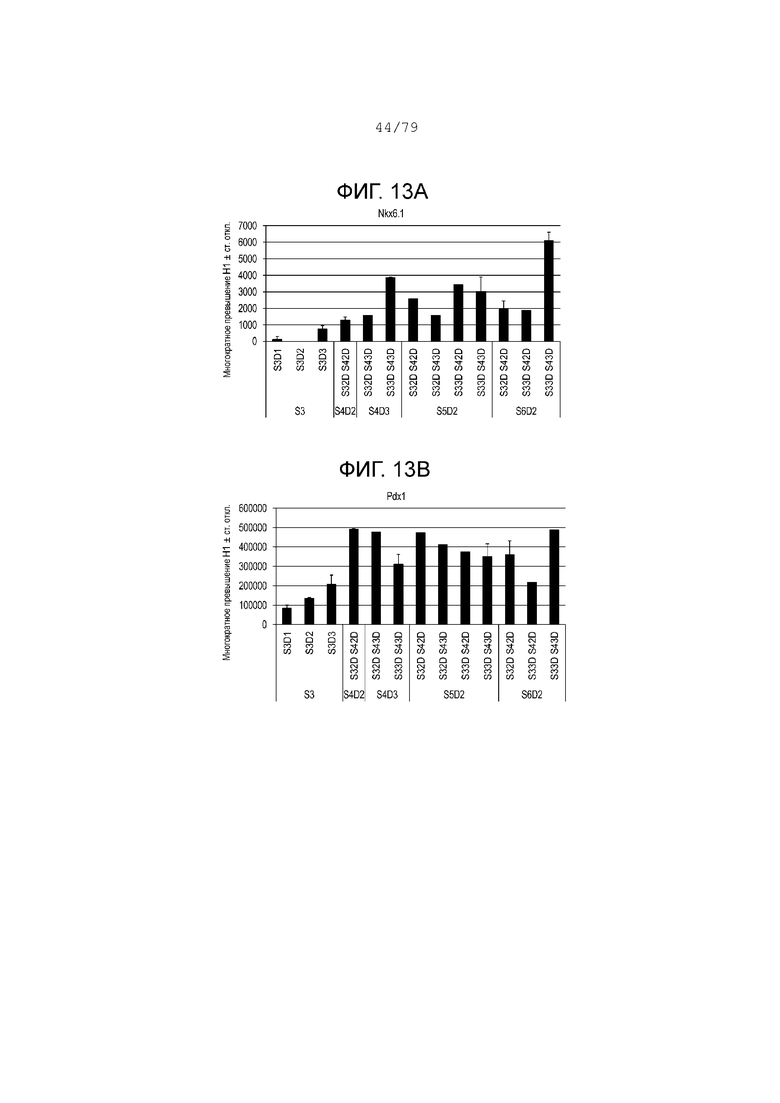
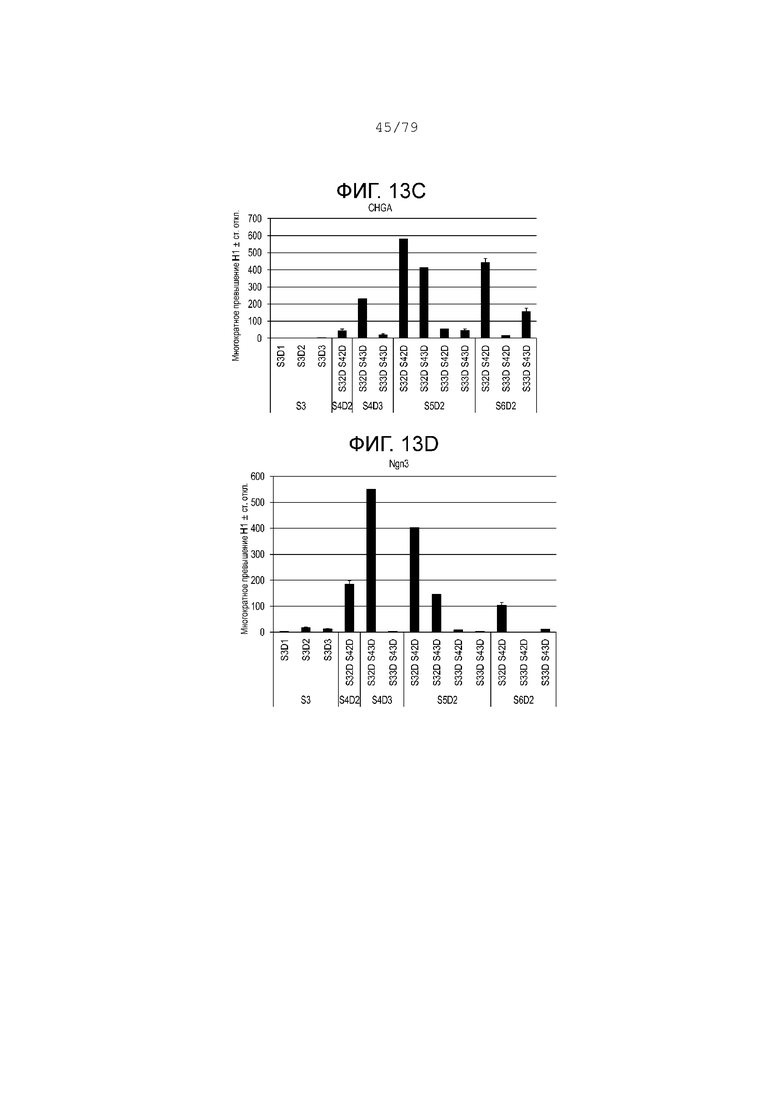
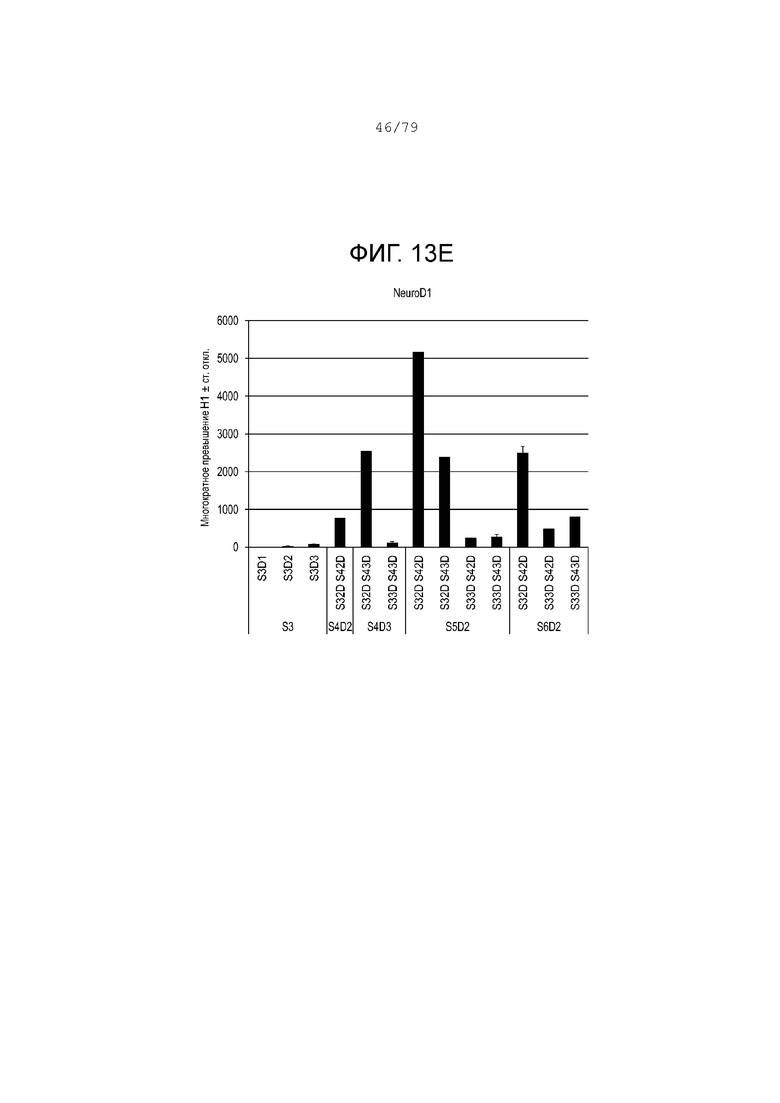
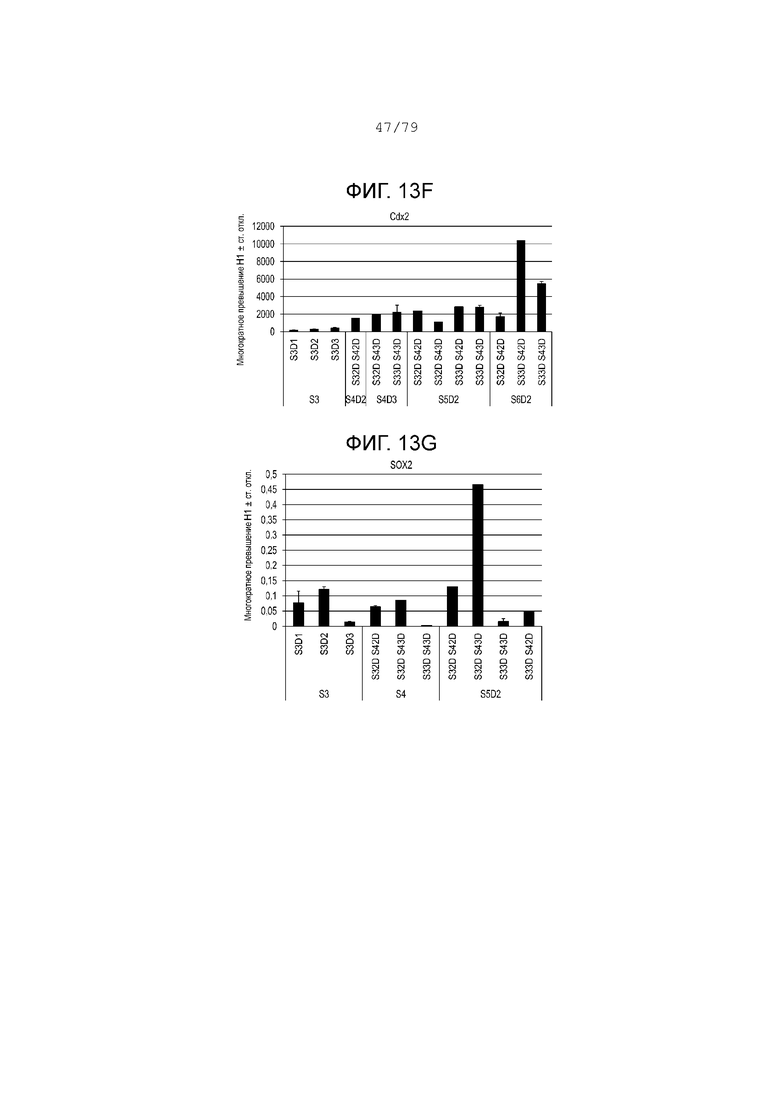
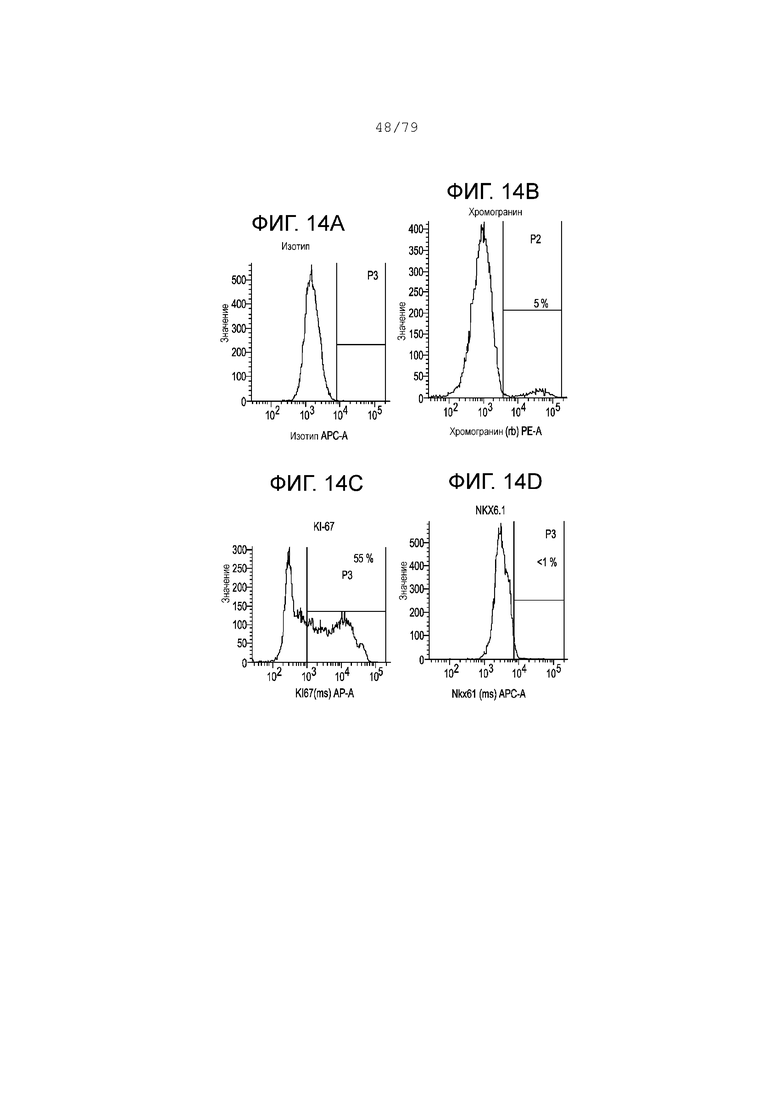
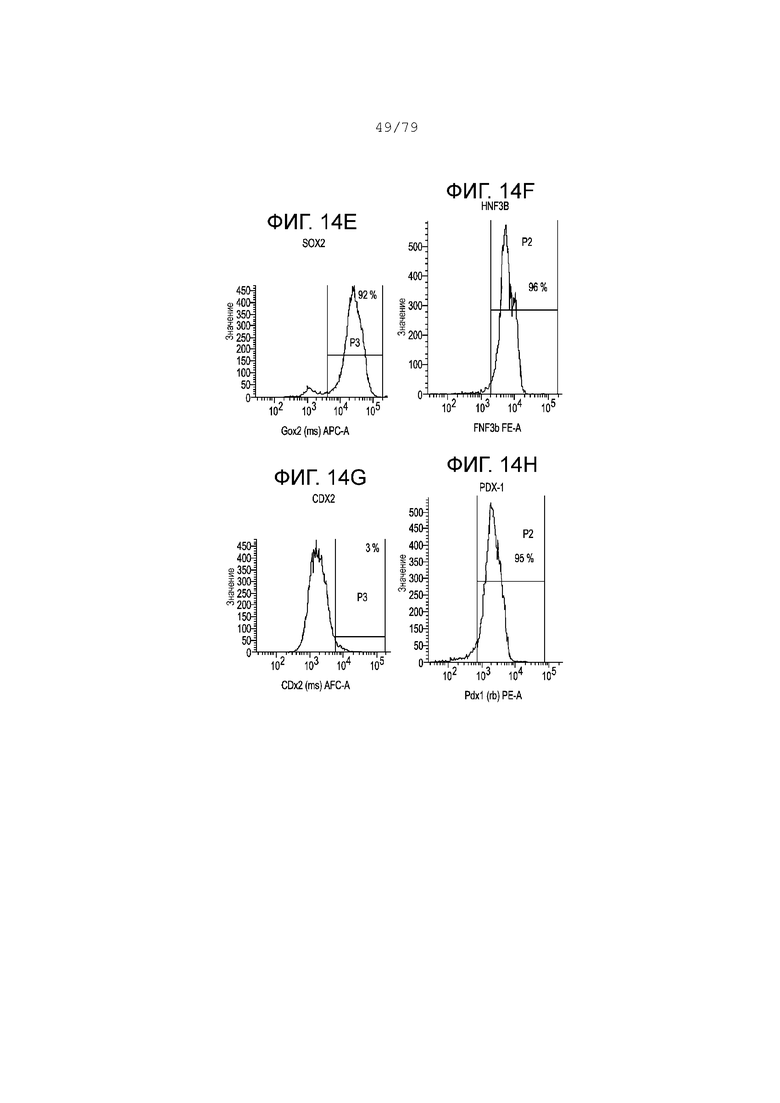
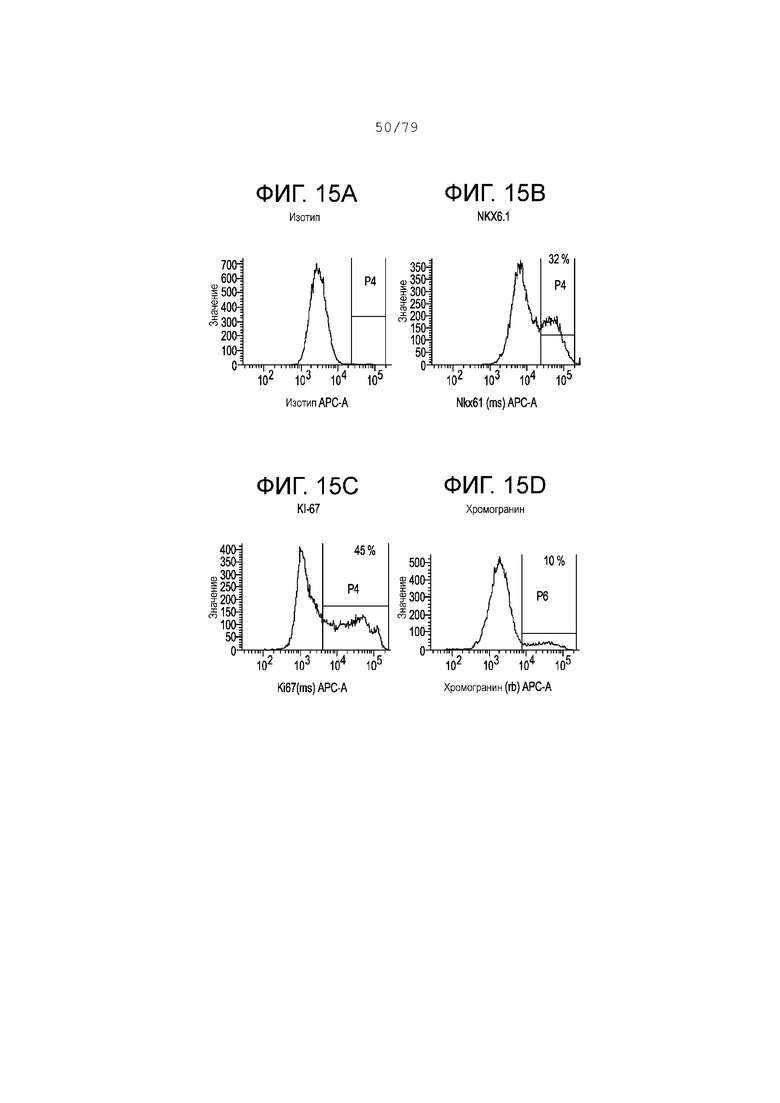
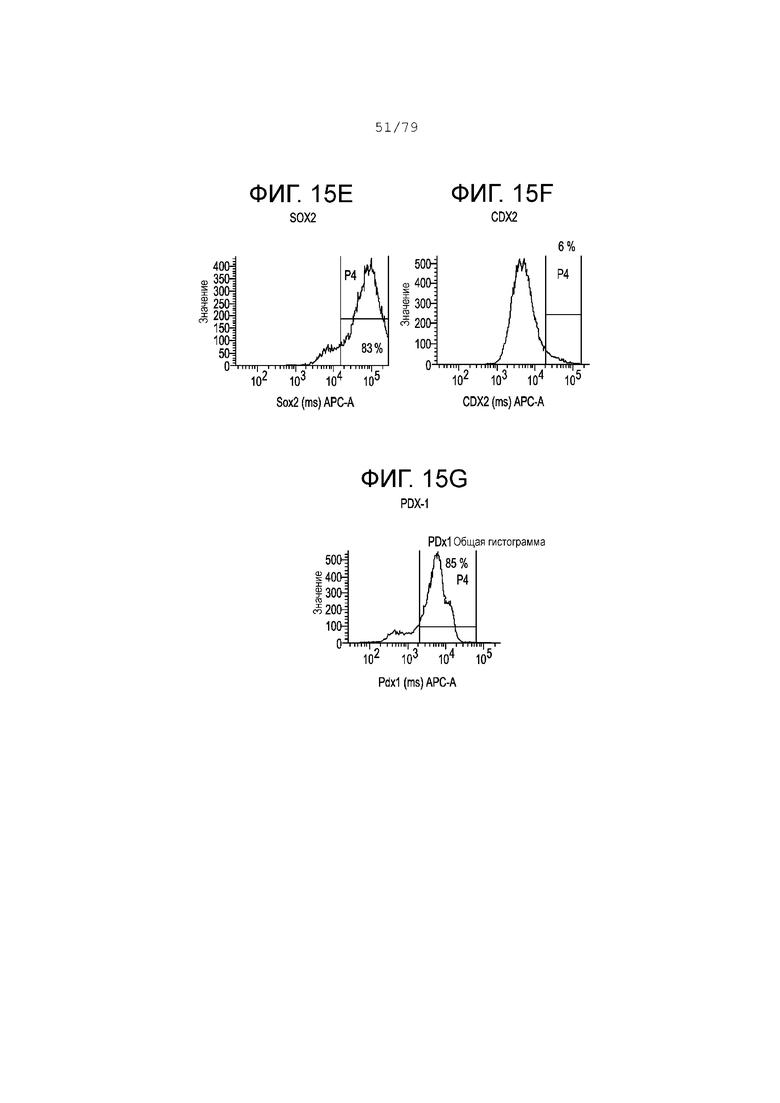
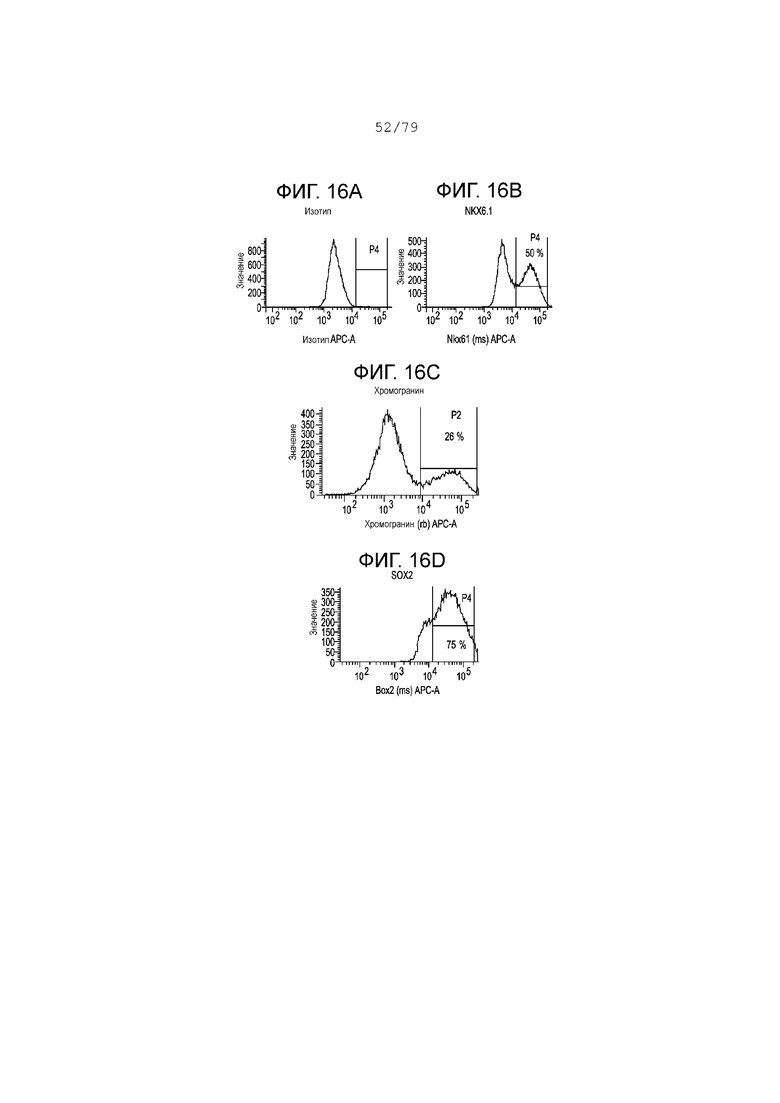
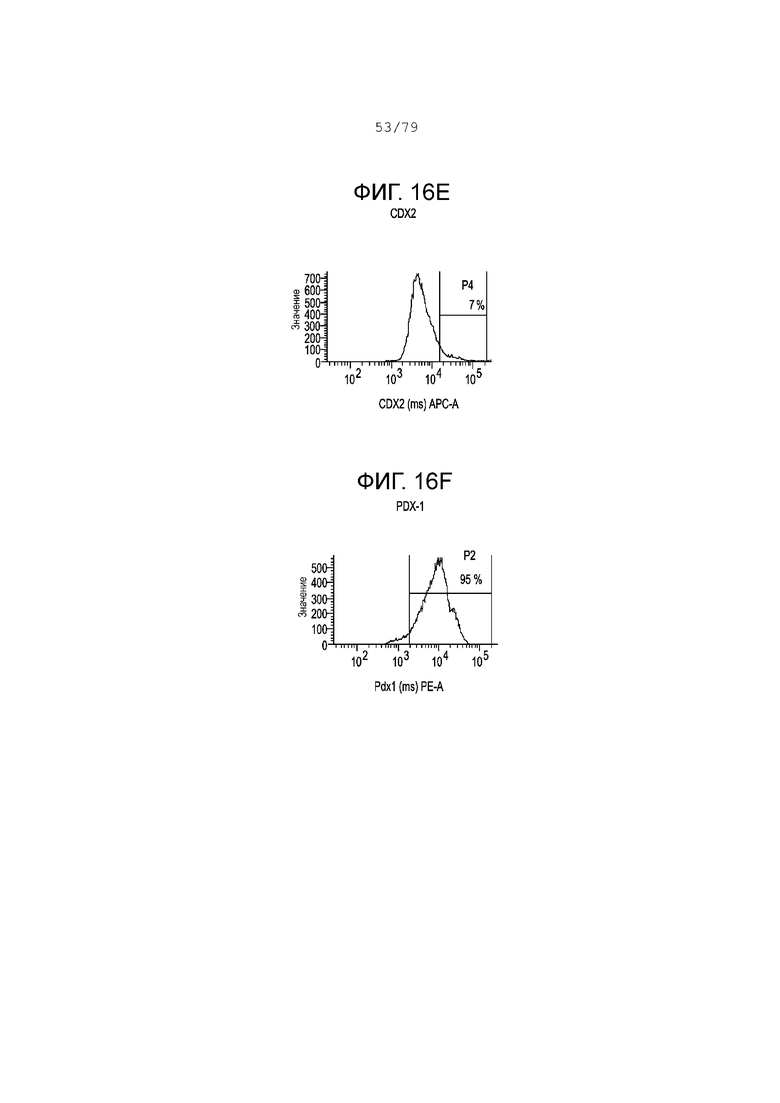
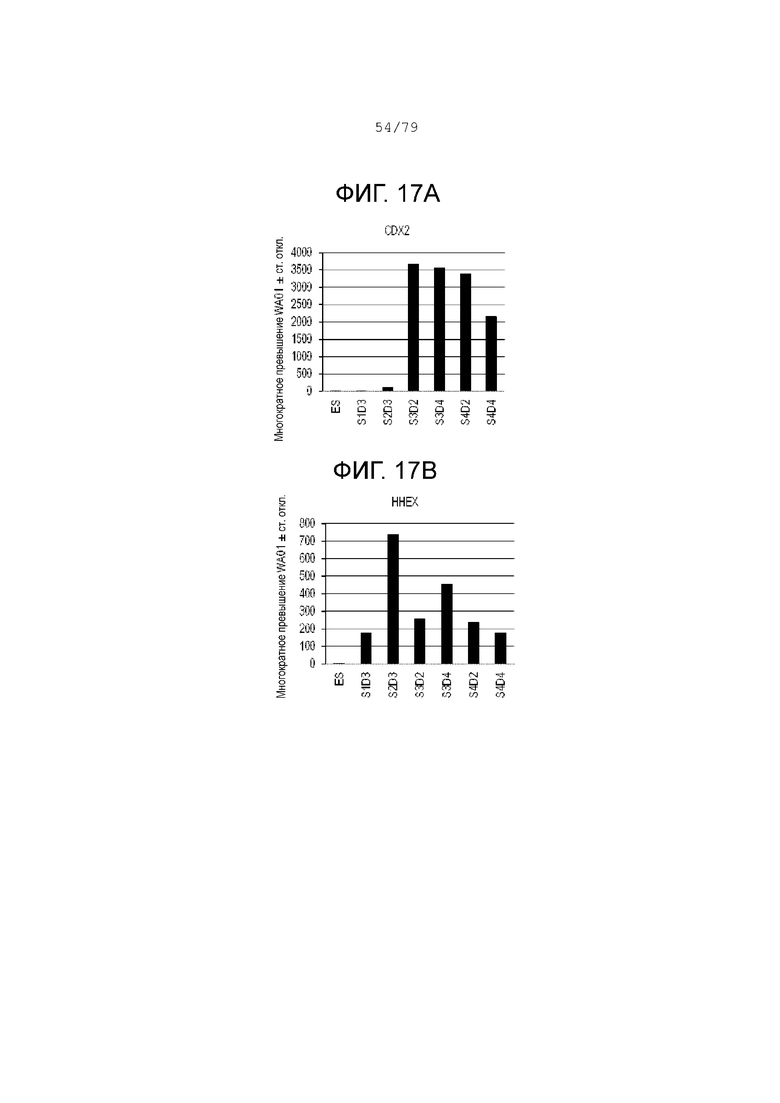
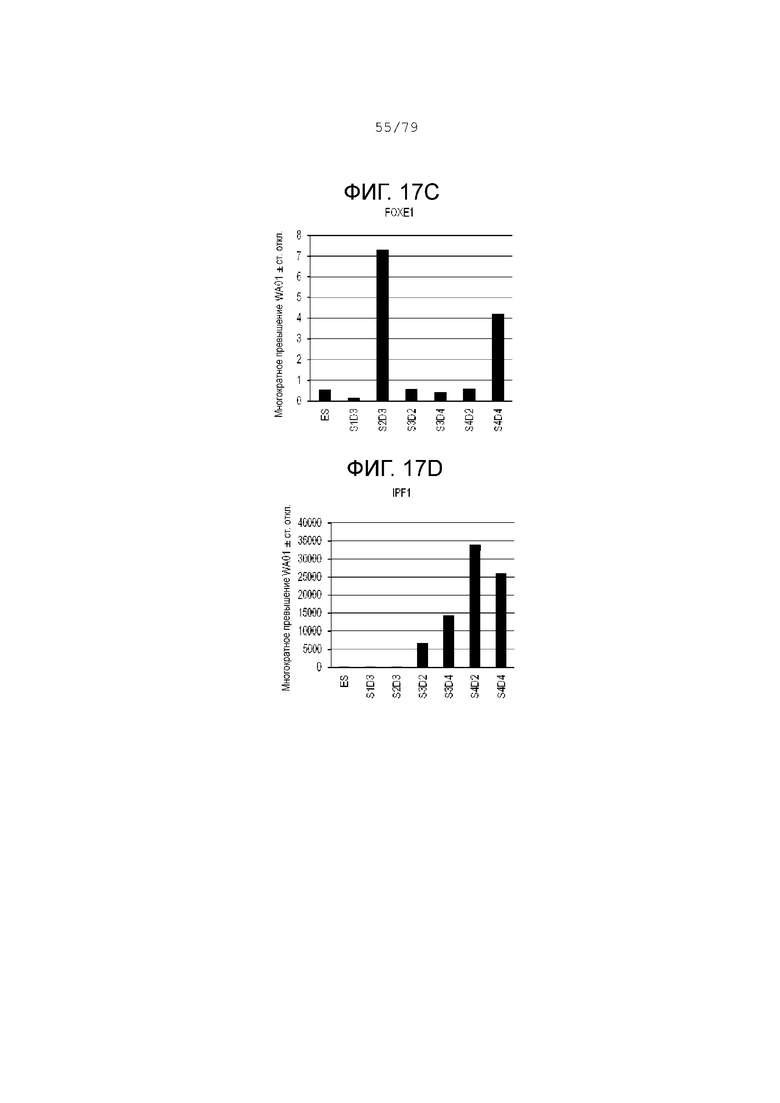
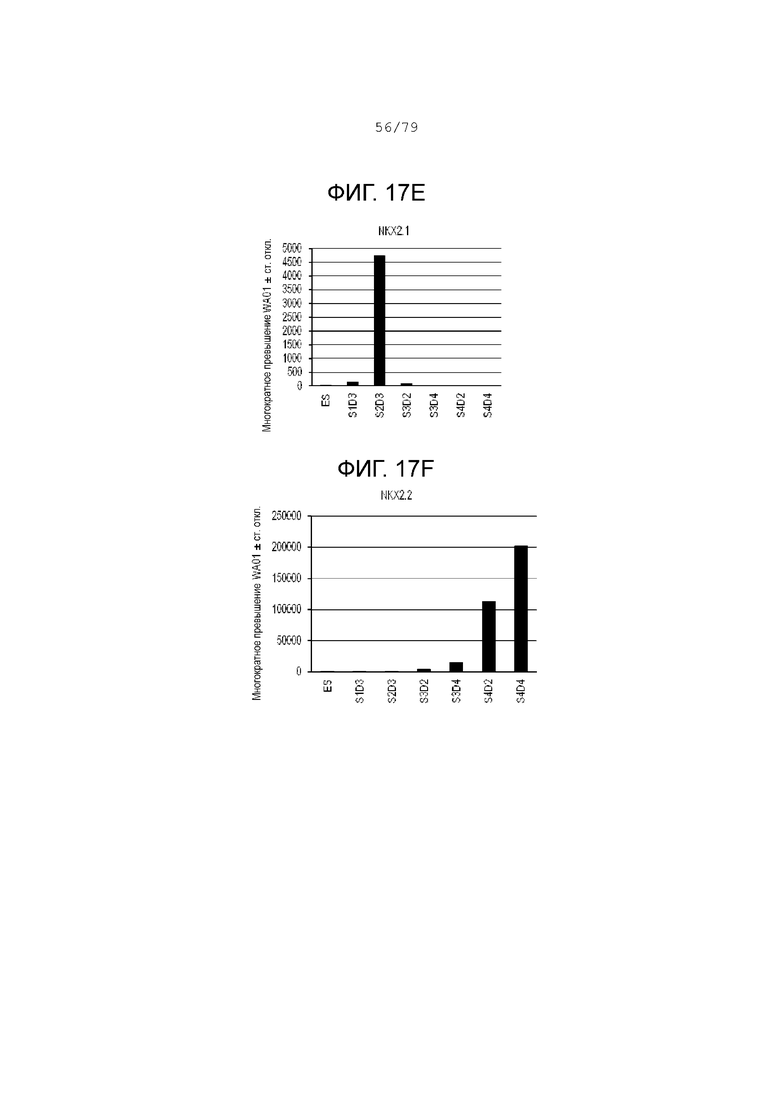
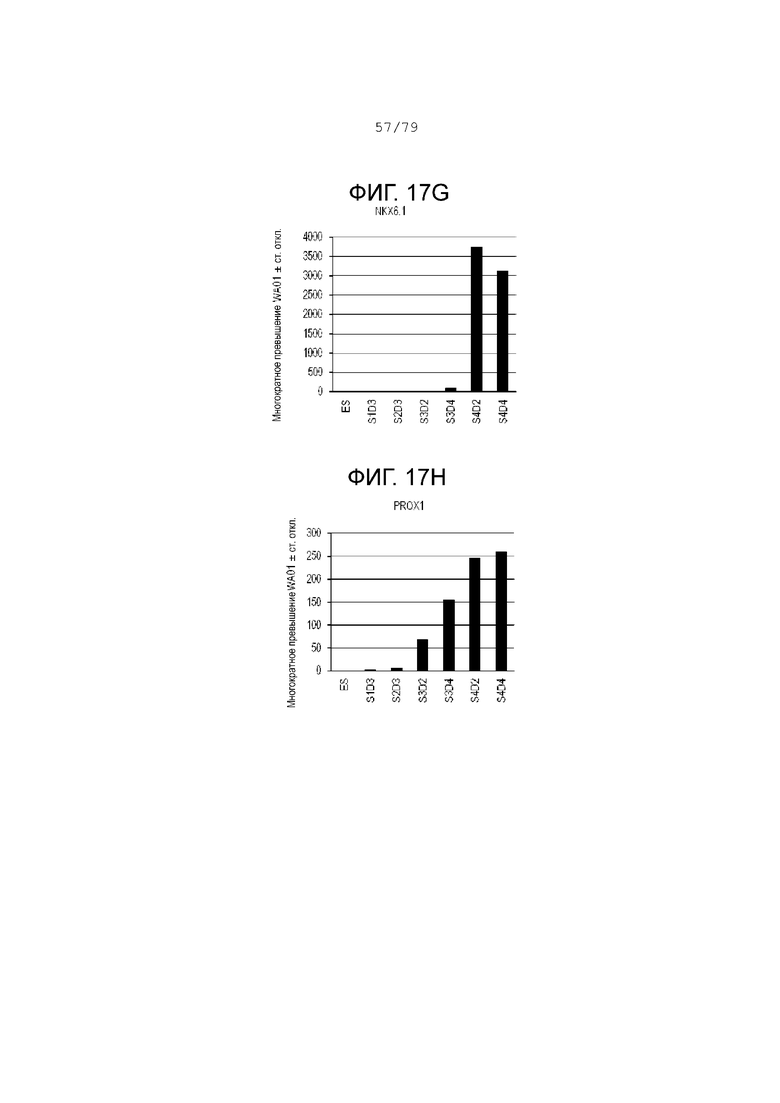
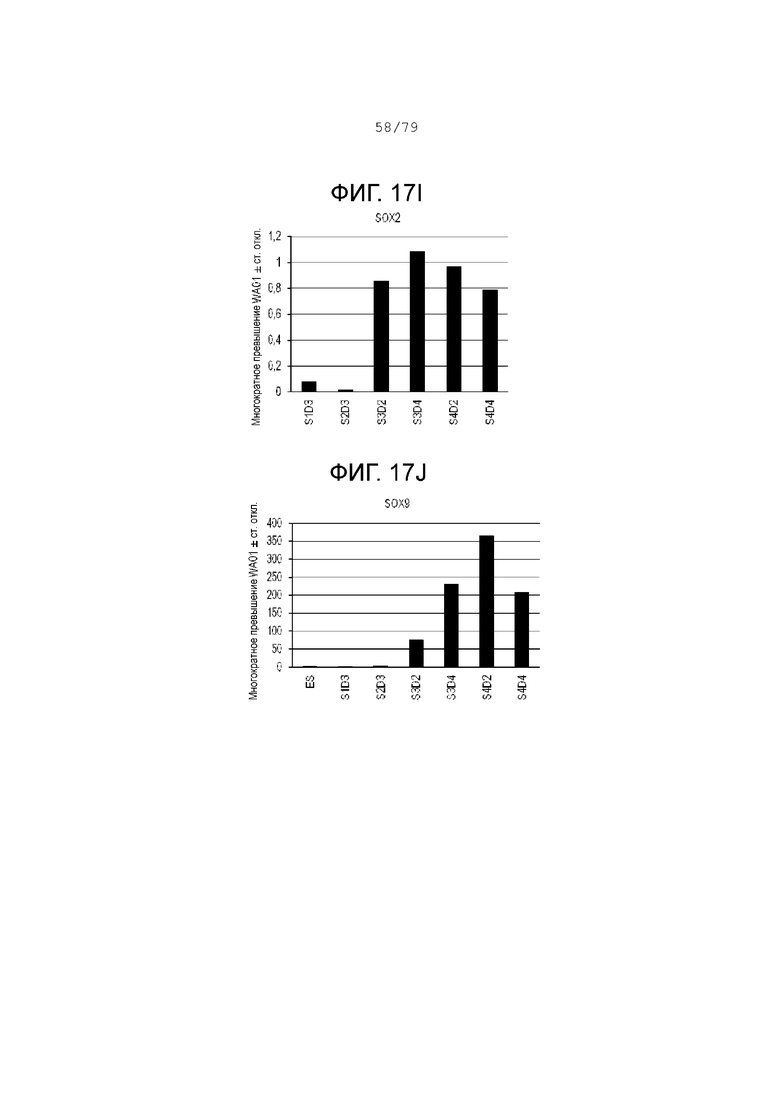
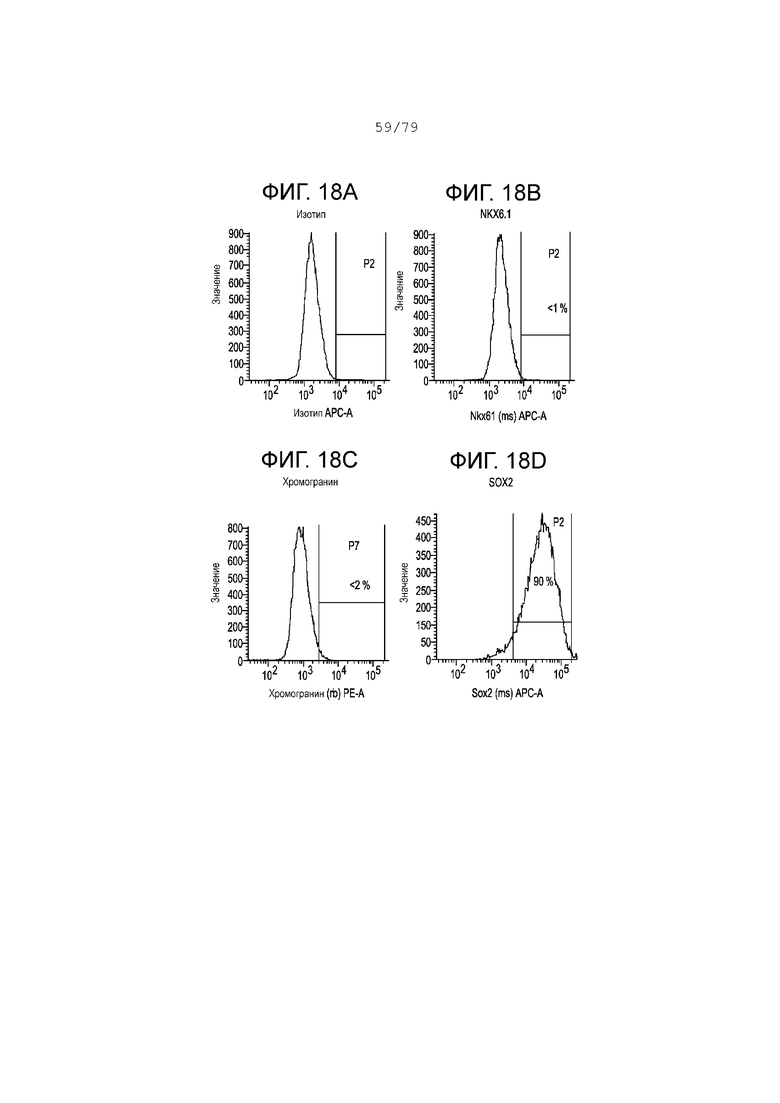
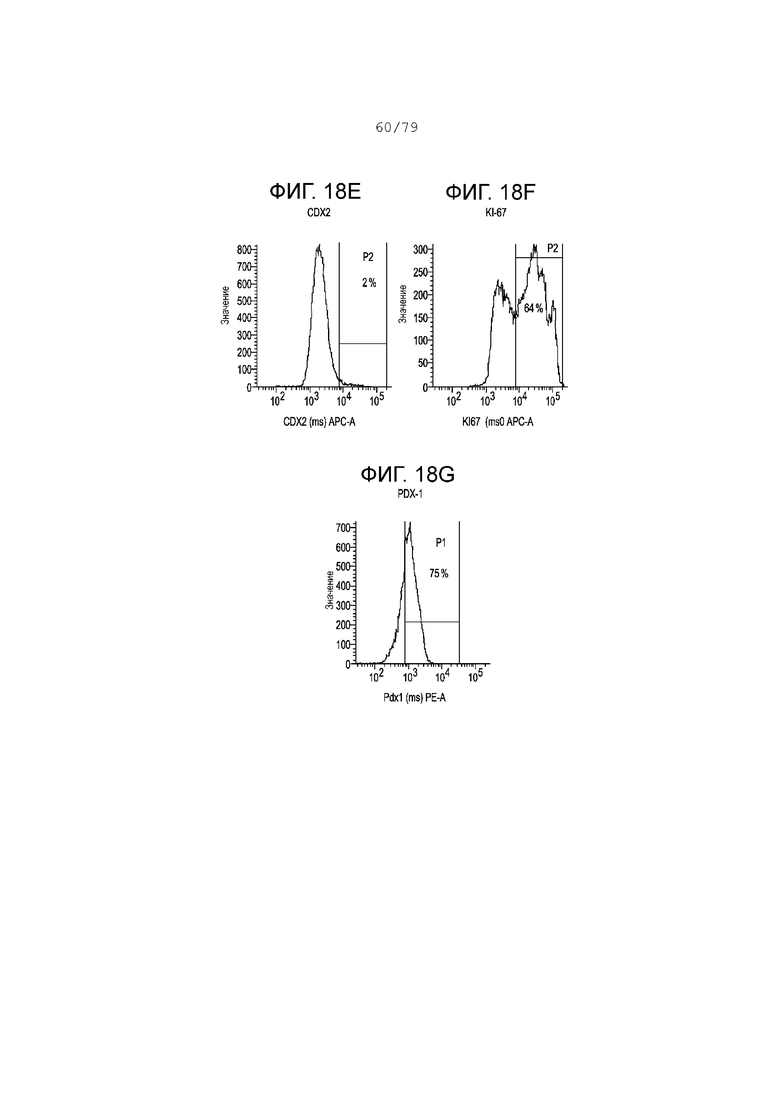
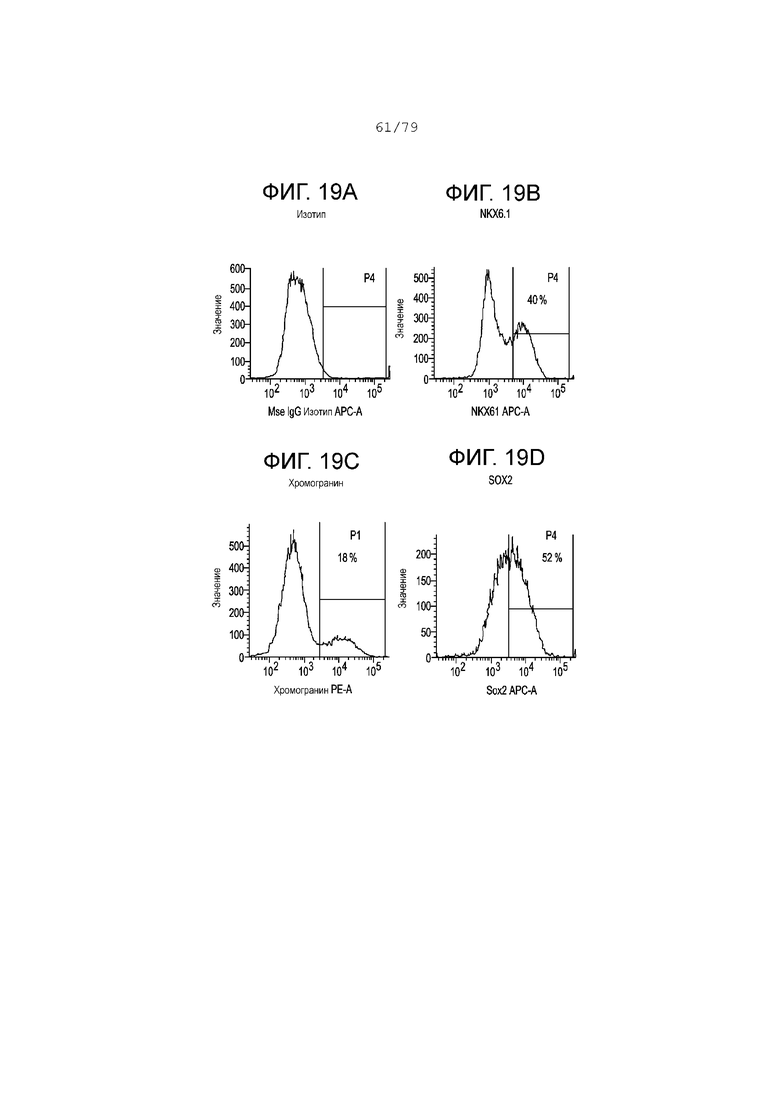
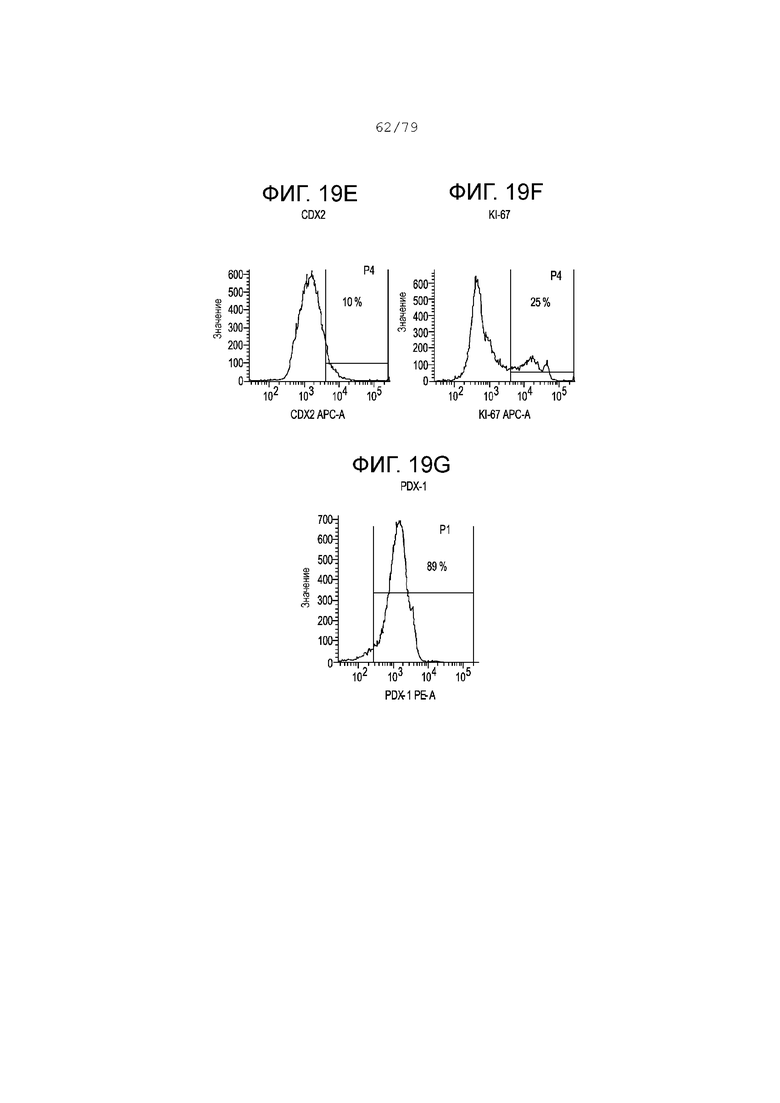

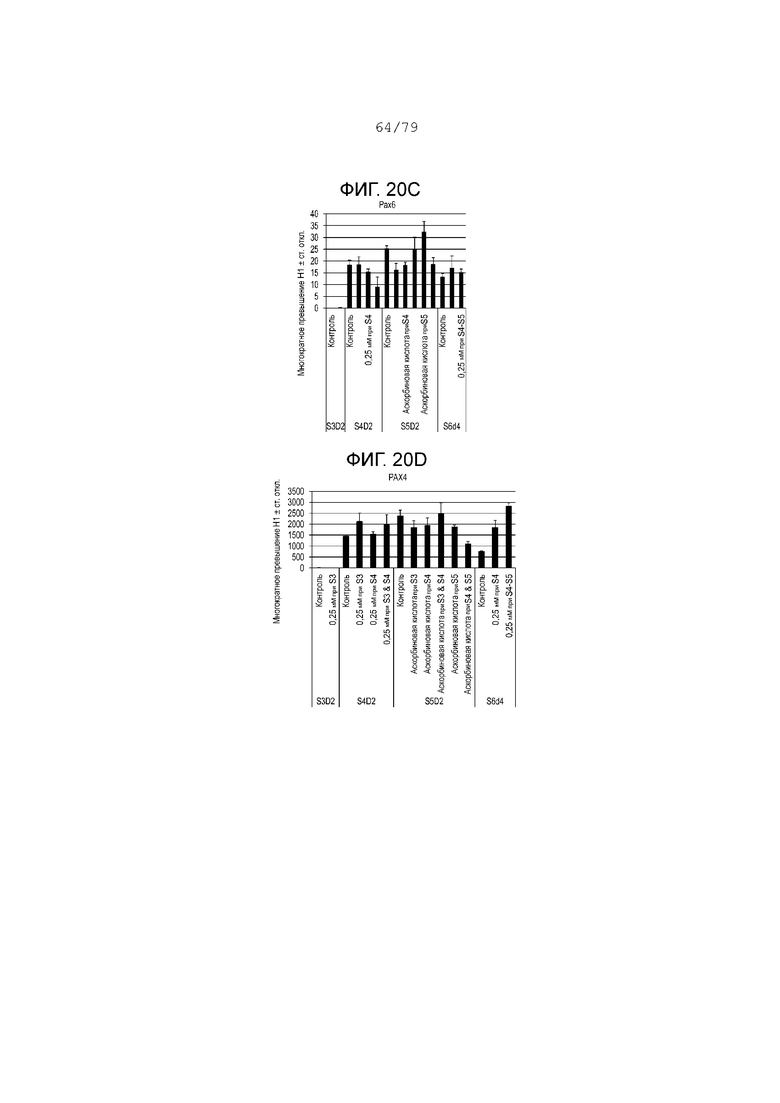




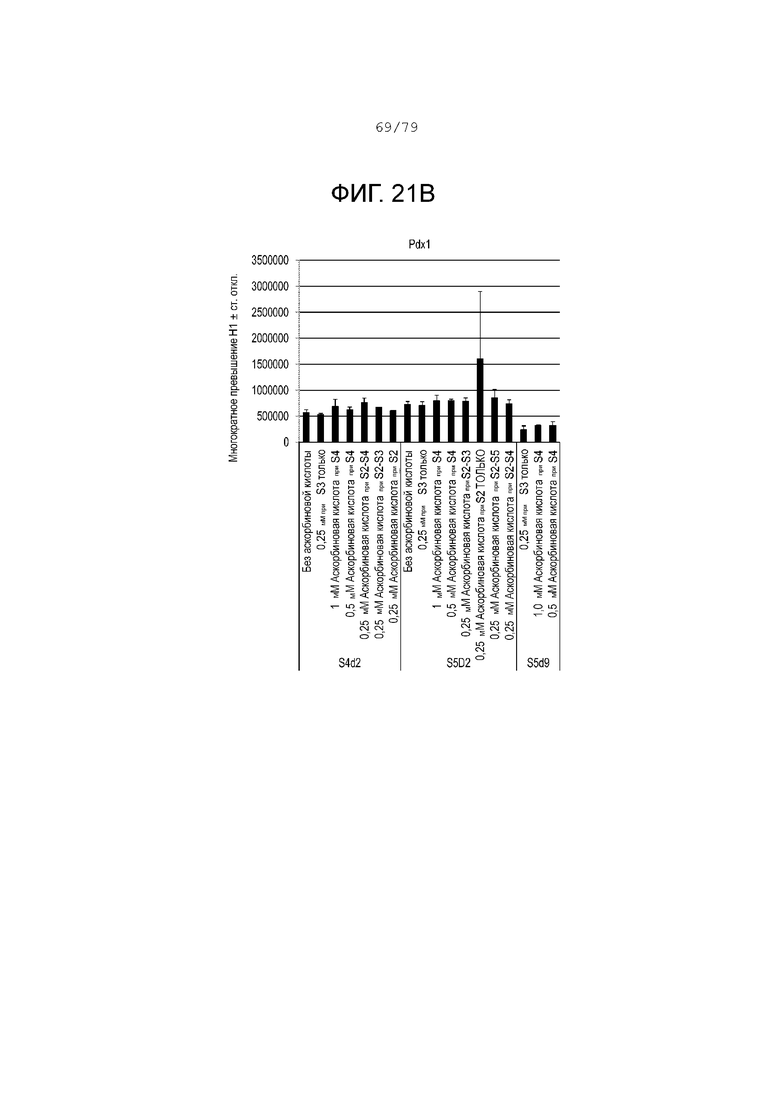





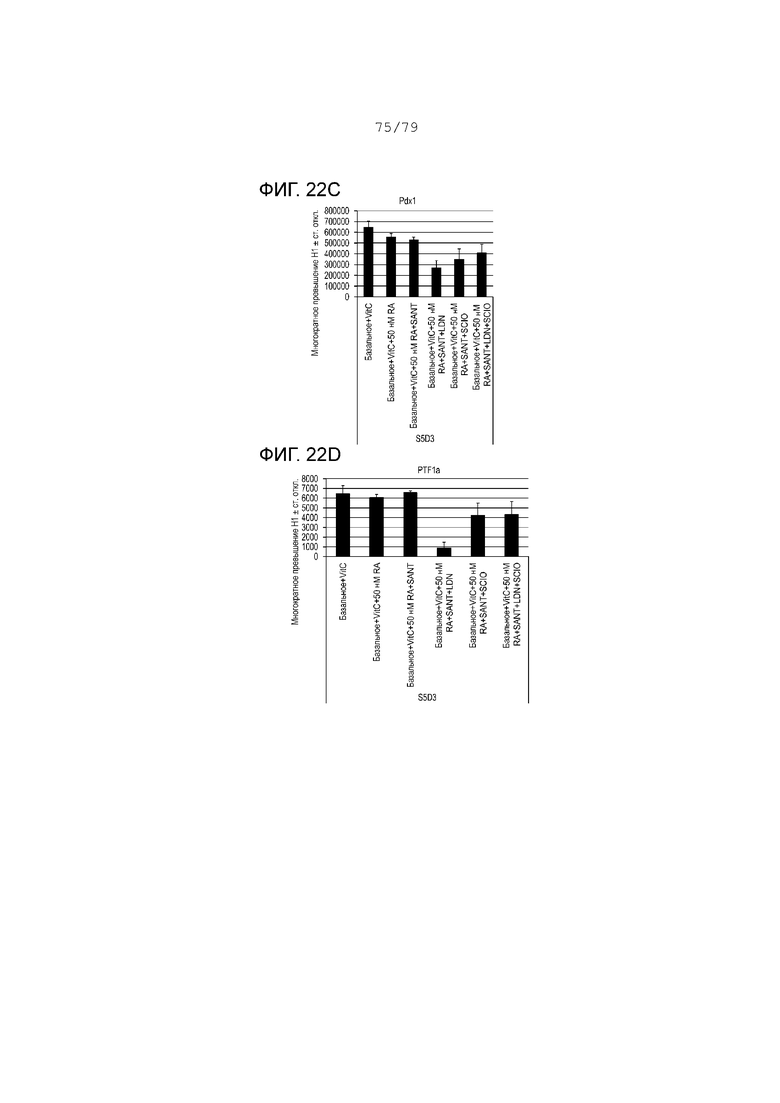




Изобретение относится к области биотехнологии, а именно к получению одногормональных инсулинположительных клеток. Способ, за исключением способа, в котором клетки поджелудочной железы передней кишки и клетки энтодермы поджелудочной железы получены с использованием человеческих эмбрионов, включает дифференцировку клеток поджелудочной железы передней кишки, экспрессирующих PDX-1 и NKX6.1, в клетки энтодермы поджелудочной железы путем обработки клеток поджелудочной железы передней кишки, экспрессирующих PDX-1 и NKX6.1, ингибитором shh, низкой дозой ретиноевой кислоты и аскорбиновой кислотой. Затем осуществляют дифференцировку клеток энтодермы поджелудочной железы в одногормональные эндокринные клетки поджелудочной железы в среде, дополненной ингибитором shh, низкой дозой ретиноевой кислоты и аскорбиновой кислотой. Изобретение позволяет расширить арсенал технических средств. 15 з.п. ф-лы, 22 ил., 8 табл., 8 пр.
1. Способ получения одногормональных инсулинположительных клеток, включающий:
(a) дифференцировку клеток поджелудочной железы передней кишки, экспрессирующих PDX-1 и NKX6.1, в клетки энтодермы поджелудочной железы путем обработки клеток поджелудочной железы передней кишки, экспрессирующих PDX-1 и NKX6.1, ингибитором shh, низкой дозой ретиноевой кислоты и аскорбиновой кислотой; и
(b) дифференцировку клеток энтодермы поджелудочной железы в одногормональные эндокринные клетки поджелудочной железы в среде, дополненной ингибитором shh, низкой дозой ретиноевой кислоты и аскорбиновой кислотой,
за исключением способа, в котором клетки поджелудочной железы передней кишки и клетки энтодермы поджелудочной железы получены с использованием человеческих эмбрионов.
2. Способ по п.1, в котором клетки энтодермы поджелудочной железы экспрессируют PDX-1, более высокий уровень NKX6.1 и более низкий уровень SOX2 по сравнению с клетками поджелудочной железы передней кишки.
3. Способ по п.1, в котором стадия (а) дополнительно включает обработку активатором PKC и ингибитором рецептора BMP.
4. Способ по п.3, в котором активатор PKC представляет собой TPB.
5. Способ по п. 3 или 4, в котором ингибитор BMP представляет собой LDN-193189.
6. Способ по п.3, в котором стадия (а) включает обработку с использованием 0,25 мкМ SANT-1, 200 нМ TPB, 50 нМ ретиноевой кислоты, 200 нМ TPB, 50 нМ LDN-193189 и 0,1 мМ аскорбиновой кислоты.
7. Способ по п.1, в котором стадия (b) дополнительно включает обработку ингибитором ALK5.
8. Способ по п.7, в котором ингибитор ALK5 представляет собой ингибитор ALK5 II.
9. Способ по п.7, в котором ингибитор ALK5 представляет собой SD208.
10. Способ по п.7, в котором стадия (b) включает обработку с использованием 0,1 мМ аскорбиновой кислоты, 50 нМ ретиноевой кислоты, 0,25 мкМ SANT-1 и 1 мкМ ингибитора Alk5.
11. Способ по любому из пп. 1, 3 или 7, где ингибитор shh на стадии (a), (b) или (a) и (b) представляет собой SANT-1.
12. Способ по любому из пп. 1, 3 или 7, где способ на стадии (a), (b) или (a) и (b) включает обработку с использованием от 0,01 мМ до 1 мМ аскорбиновой кислоты.
13. Способ по любому из пп.1, 3 или 7, где способ на стадии (a), (b) или (a) и (b) включает обработку с использованием от 0,1 мМ до 0,5 мМ аскорбиновой кислоты.
14. Способ по любому из пп.1, 3 или 7, где способ на стадии (a), (b) или (a) и (b) включает обработку в среде, содержащей менее 25 мМ глюкозы.
15. Способ по п.14, в котором концентрация глюкозы находится в диапазоне от 8 мМ до 20 мМ глюкозы.
16. Способ по любому из пп. 1-15, в котором клетки поджелудочной железы передней кишки представляют собой клетки поджелудочной железы передней кишки человека.
| WO 2009018453 А1, 05.02.2009 | |||
| WO 2010051213 А1, 06.05.2010 | |||
| WO 2011143299 А2, 17.11.2011 | |||
| ГИЛБЕРТ С | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| с англ | |||
| - М.: Мир, 1993 | |||
| Приспособление для нагрузки тендеров дровами | 1920 |
|
SU228A1 |
Авторы
Даты
2019-11-01—Публикация
2012-12-07—Подача