Изобретение относится к области электрохимии, а именно к материалам на основе безметальных электрокатализаторов для получения молекулярного водорода из воды в присутствии органических солей, и может быть использовано в качестве электрокатализаторов водородных электродов в системе с твердыми полимерными электролитами, а также в электролизерах воды, позволяющих производить высокочистый водород для использования в энергетике (в том числе, на атомных электростанциях) и т.п., в бифункциональных (регенеративных) системах) и электрохимических компрессорах/концентраторах водорода.
В последние годы изучалось использование структурно-функционального подхода к дизайну и синтезу металлокомплексных электрокатализаторов, то есть в тех случаях, когда приоритет отдавался функциональному моделированию действия гидрогеназ, а не их структурных особенностей; подход был использован для понимания природы и механизмов биохимических процессов (Y.H. Budnikova, ElectrochimicaActa, 2017,27, 467-472, Electrocatalysis 2015, 357-364, Chemistry – A EuropeanJournal 2014, 20, 3169-3182. F.A. Armstrong, Curr. Opin.Chem. Biol., 2004, 8, 133; P.M. Vignais, B. Billoud, J. Meyer, FEMS Microbiol. Rev., 2001, 25, 455; R. Cammack, Nature, 1999, 397, 214; M. Frey, Chembiochem, 2002, 3, 153; M.W. Adams, Biochim. Biophys. Acta, 1990, 1020, 115; E.C. Hatchikian, N. Forget, V.M. Fernandez, R. Williams, R. Cammack, Eur. J. Biochem., 1992, 209, 357; S. Ogo, Chem. Commun., 2009, 23, 3317), но проблема все еще далека от решения. До настоящего времени не описаны синтетические электрокаталитические системы получения водорода из воды и водных растворов, которые совмещали бы высокую каталитическую эффективность и химическую устойчивость при низких значениях pH. В целом, при создании таких функциональных моделей природных гидрогеназ, успешно работающих в современных генераторах водорода, необходимо совместить их высокую химическую устойчивость, высокую производительность в течение длительного периода времени, низкую стоимость (т.е. избежать использования дорогих и редких металлов группы платины) и технологичность получения неплатинового электрокатализатора (коммерчески-доступные исходные соединения, высокие выходы, отсутствие необходимости в специальных и анаэробных условиях синтеза и т.д.). Так, до недавнего времени лишь комплексы никеля с циклическими фосфиновымилигандами проявляли умеренную электрокаталитическую активность в процессах образования водорода (LeGolf с сотр., Science, 326, 1384 (2009). Новые электрокатализаторы на основе комплексов железа (Рис. 2; Liu с сотр., Angew.Chem. Int. Ed., 53, 5300-5304 (2014)) с приемлемыми значениями перенапряжений (160–220 мВ) также обладают слишком низкой активностью (TOF 2000 s-1) и недостаточной стабильностью, что не позволяет надеяться на их дальнейшее практическое применение для промышленного получения молекулярного водорода.
Имеющиеся на рынке катализаторы на основе благородных металлов дороги. Например, каталитическая система VT-Pt фирмы Nordic стоит 500 долл. США за 1 г. Использование в качестве катализаторов органических соединения позволит, при той же эффективности уменьшить стоимость каталитической системы до 100 долл. США за 1 г. Новый подход к молекулярному дизайну и получению электрокатализаторов этого типа основан на постадийном синтезе молекул.
Известен катализатор для получения молекулярного водорода. В решении описано применение органического стабильного электронно-избыточного радикала в качестве катализатора для получения молекулярного водорода (RU 2480283, МПК В01J 31/00, C01B 3/16, C25B 1/44, опубл. 27.04.2013).
Недостатком известного решения является низкая каталитическая активность и невозможность к иммобилизации на рабочем электроде.
Заявленное решение относится к так называемым «умным молекулам» и сочетает в себе наиболее важные для эффективной электрокаталитической реакции 2Н+/Н2 характеристики: дешевизну, синтетическую доступность и экологическую чистоту соединений с химической и термодинамической устойчивостью, по меньшей мере, в двух редокс-состояниях, а также в широком диапазоне редокс-потенциалов, рН и температуры, демонстрирующих высокую скорость переноса электрона и возможность тонкой настройки их окислительно-восстановительного потенциала.
Технический результат заявленного изобретения заключается в применении синтетически доступного и термодинамически устойчивого материала на основе безметального электрокатализатора для получения молекулярного водорода из воды в присутствии органических солей.
Сущность изобретения заключается в том, что предлагается применение материала на основе безметального электрокатализатора для получения молекулярного водорода из воды в присутствии органических солей.
Сущность изобретения поясняется чертежами, где:
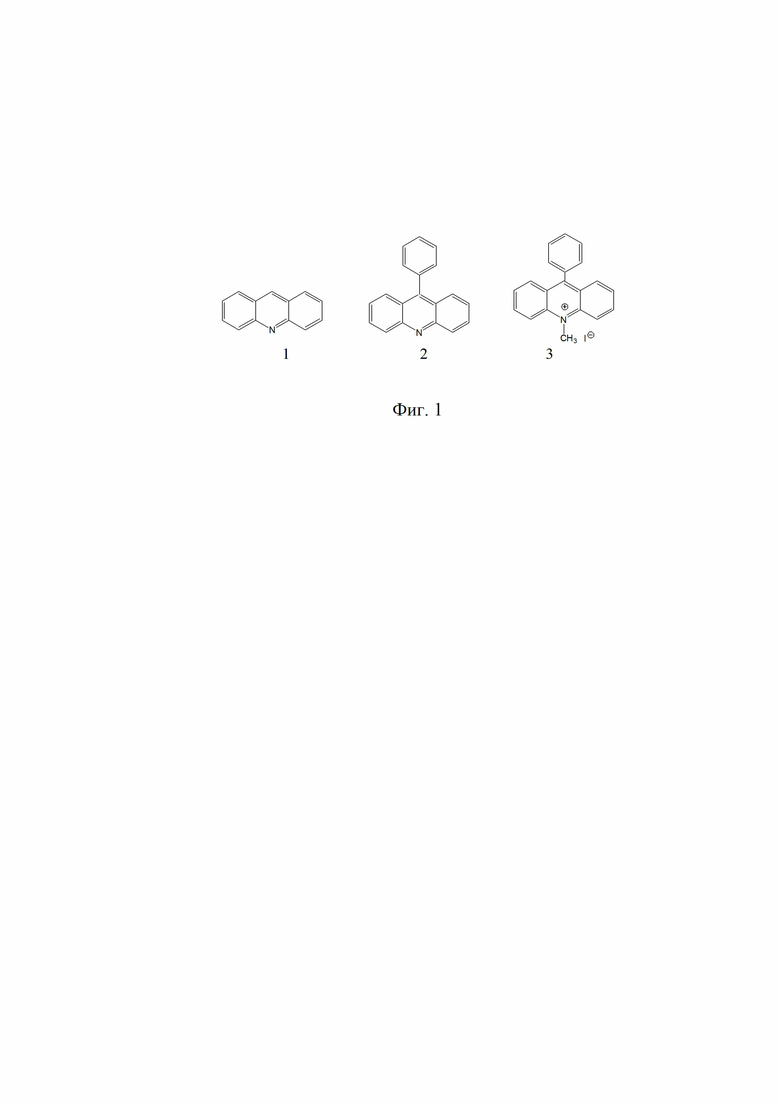
на Фиг. 1 показаны химические формулы акридина (1), 9-фенилакридина (2) и N-метил-9-фенилакридинаиодида (3);
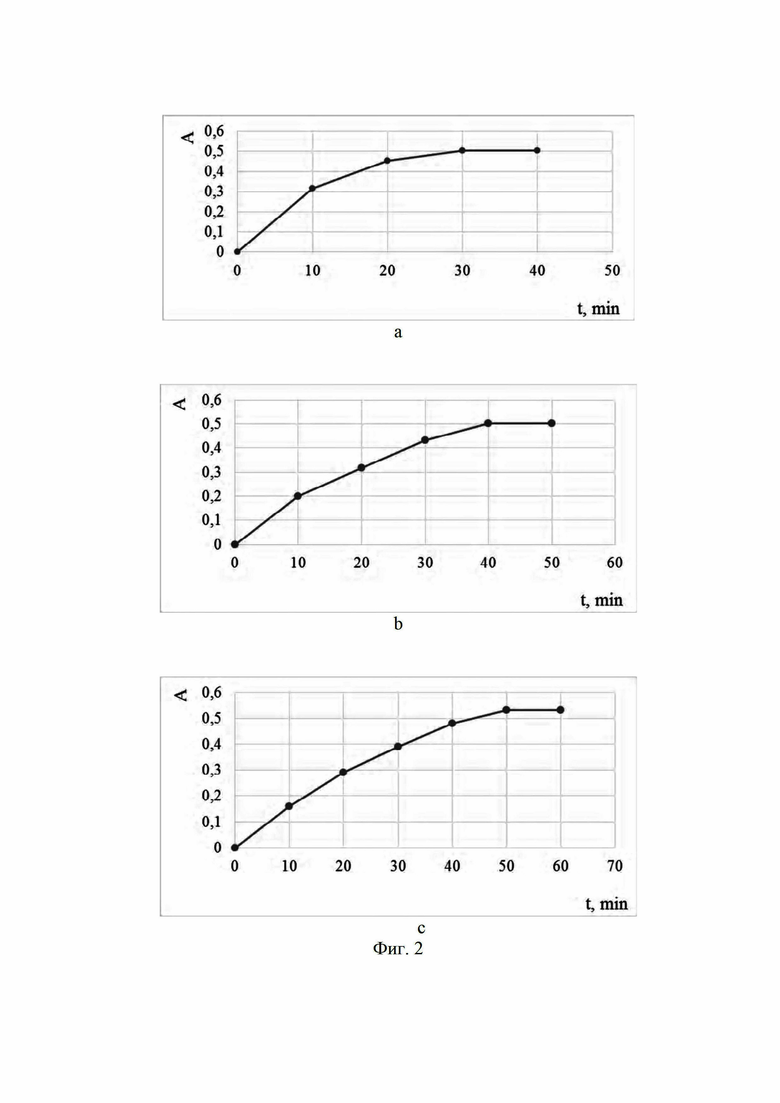
на Фиг. 2 представлена сорбция соединений 1 (a), 2 (b) и 3 (c) на углеродном носителе VulcanXC-72 в ацетонитриле;
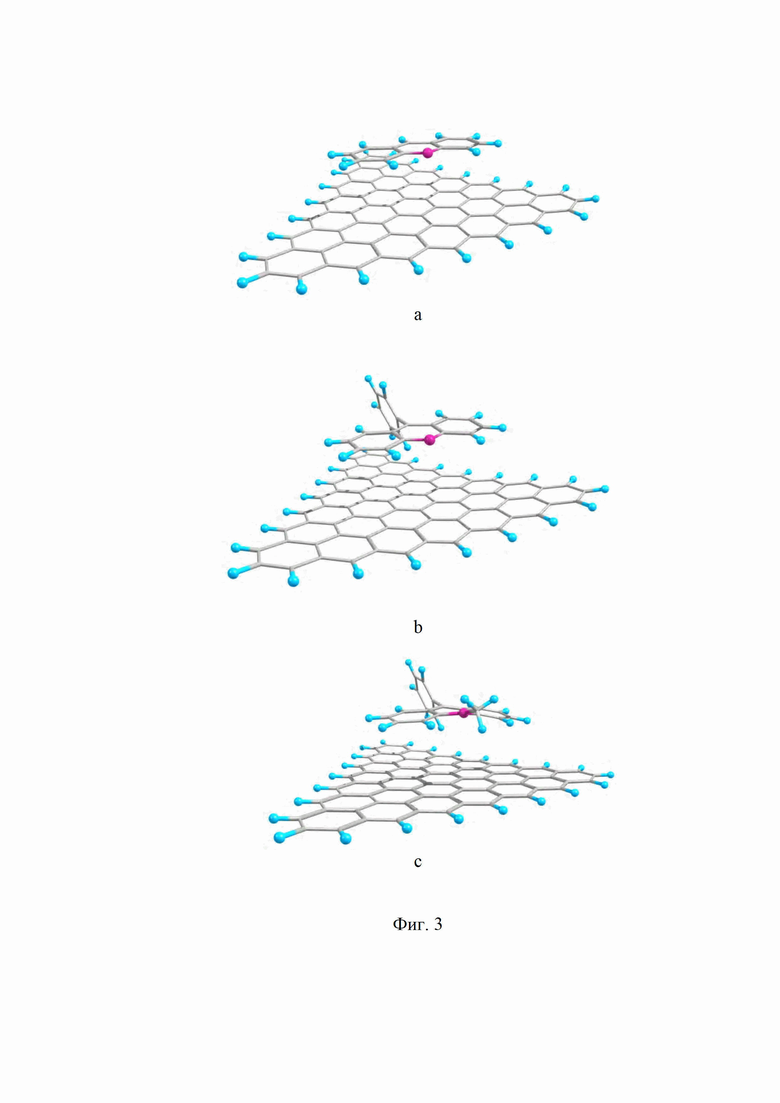
на Фиг. 3 изображены равновесные состояния, полученные при расчете методом B3LIP/6-311+G(2d,p) для адсорбции соединений 1-a, 2-b и 3-с на графеновых поверхностях;
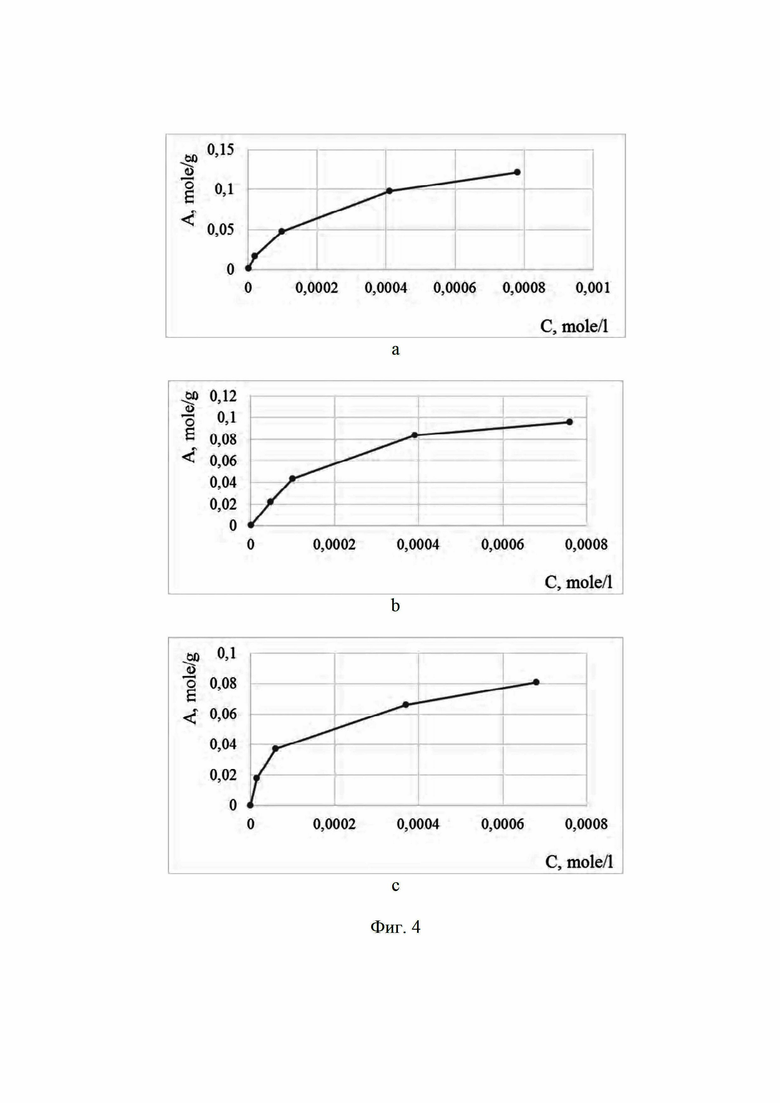
на Фиг. 4 показана изотерма адсорбции Ленгмюра для соединений 1-a, 2-b и 3-с на углеродсодержащем сорбенте;
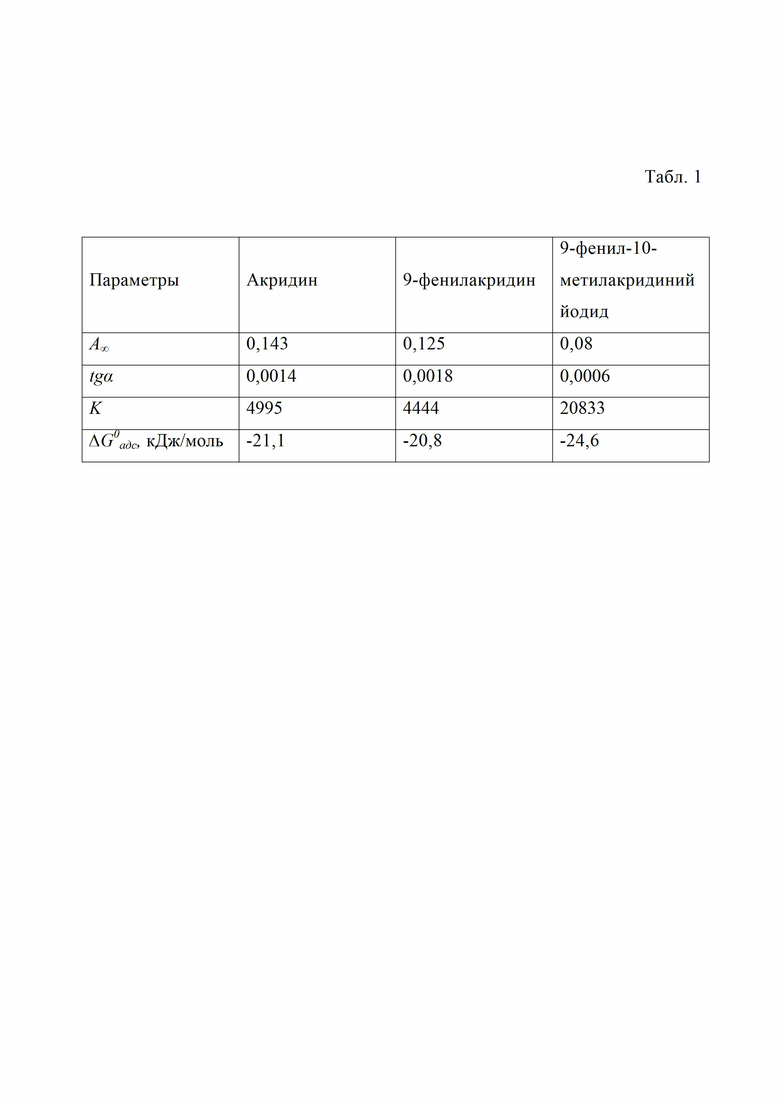
в Табл. 1 представлены рассчитанные параметры адсорбции органических веществ на углеродосодержащем сорбенте VulcanXC-72;
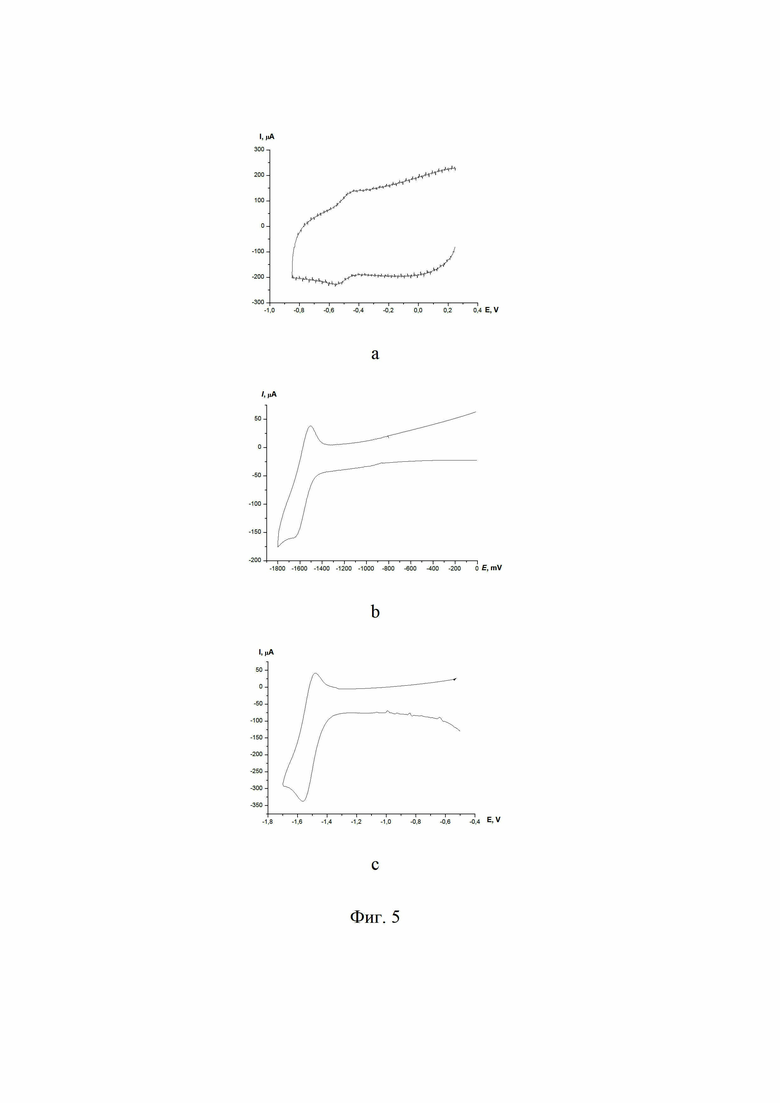
на Фиг. 5 показаны циклическая вольтамперометрия (ЦВА) для соединений 1, 2, 3, иммобилизованных на углеродном носители Vulcan 72. Условия съемки: хлористый метилен, V = 20 mV/s, Ag/AgCl/KCl.
Осуществление изобретения
Применяют материал на основе безметального электрокатализатора, иммобилизованного на углеродный носитель, для получения молекулярного водорода из воды в присутствии органических солей.
Способ приготовления материала на основе безметального электрокатализатора для получения молекулярного водорода из воды в присутствии органических солей включает гомогенизирование 10 мг углеродного носителя Vulcan ХС-72 и раствора Nafion® (5 мас. % диспергированного продукта марки D521 производства «DuPont») в изопропаноле с использованием ультразвуковой ванны с рабочей частотой 22-25 кГц в течение 20 мин. Полученную смесь наносят на стеклоуглеродный электрод с площадью поверхности 5 см2. Расчетная загрузка безметального электрокатализатора составляет 3–7∙10-4 мг∙см-2 (для всех представленных органических соединений).
Для получения заявленного решения используют следующие материалы.
1. Углеродный носитель Vulcan ХС-72 производства «CabotCorporation - Additives».
2. Nafion® производства «DuPont»
СЧ: Dupont. Происхождение товара: Texas, UnitedStates. Тип: Синтетические волокна, Синтетическая смола и пластмассы, Синтетические каучуки. Наименование: Нафионом. Степень чистоты: Высокий класс. Толщина: 127 микрометров (5 мил). Основной Вес (г/м2): 250.
3. Акридин (х.ч.)
Молекулярная формула: C13H9N. Молекулярный вес:179.22.
4. 9-фенилакридин (х.ч)
Молекулярная формула: C19H13N. Молекулярный вес:255.3132.
5. N-метил-9-фенилакридинаиодида (х.ч.)
Молекулярная формула: C20H16N. Молекулярный вес:397.2522.
6. Изопропанол (х.ч.)
Молекулярная формула: С3Н8О. Молекулярный вес:60,09.
Используют ультразвуковую ванну производства BandelinElectronic (Heintrichstrabe 3-4 D-12207 Berlin, Germany).
Акридин и его производные (Фиг. 1), можно классифицировать как полиароматические соединения, поэтому их иммобилизация на поверхности носителя углерода также позволит получать гетерогенные каталитические системы, проявляющие каталитическую активность в реакции электрокаталитического получения молекулярного водорода. В патенте представлены данные, полученные при изучении адсорбции акридина и его производных на углеродных материалах, а также электрохимических свойств полученных систем. Основной задачей исследования было нахождение оптимальных условий для процесса адсорбции органических соединений на углеродных носителях, с целью получения принципиально новых типов каталитических материалов, на основе иммобилизованных на поверхности органических молекул, за счет сильной физической сорбции (за счет π-π стекинга ароматических колец с sp2 – гибридизовыванными участками углеродного материала). В качестве углеродных материалов исследовались графитовая бумага (Sigraset GD39) , Vulcan XC-72 (VU) и стеклоуглерод. Для выявления основных закономерностей при изучении адсорбции органических соединений на выбранных углеродных материалах, нами были выбраны акридин (1), 9-фенилакридин (2) и N-метил-9-фенилакридин (3). Выявление основных мотивов при адсорбции модельных соединений позволит «управлять» процессом адсорбции более сложных соединений в ряду одних производных, и направлено модифицировать поверхность с целью придания ей нужных свойств.
Наличие у соединений 1, 2, 3 (Фиг. 1) протяженных сопряженных участков делает возможным их иммобилизацию за счет сильной физической сорбции на поверхности углеродных носителей по механизму π-π стейкинга. Однако оказалось, что графитовая бумага и стеклоуглерод не подходят для изучения процессов адсорбции. Их иммобилизация органическими соединениями не протекает даже при высоких концентрациях адсорбата в растворе. Поэтому все дальнейшие исследования проводились в присутствии углеродного материала Vulcan XC-72, показавшему прекрасные адсорбционные свойства. Изучение скорости адсорбции соединений 1, 2, 3 в присутствии Vulcan XC-72 проводили по известным методикам. Результаты представлены на Фиг. 2.
Время установления равновесных условий сорбции является наименьшим для соединения 1, затем для соединения 2, а для соединения 3 установление равновесия самое медленное. Соединение 1 имеет плоскую структуру, которая должна идеально подходить для адсорбции на поверхности углеродных носителей за счет π-π стейкинга. Вероятно, с этим и связанна его большая скорость при сорбции, поскольку у соединения 2 заместитель в 9-положении и по данным квантово-химических расчетов располагается ортогонально к π-системе акридинового остова. Такая геометрия молекулы в меньшей мере будет способствовать иммобилизации на поверхности носителя. В случае молекулы 3 ее структура еще больше искажена, по сравнению с 1 и 2. Для подтверждения полученных результатов мы провели квантово-химические расчеты процесса адсорбции соединений 1, 2, 3 на графеновой подложке, моделирующей участки углеродного носителя с графитоподобными участками с использованием метода DFT в базисе B3LYP/6-31+G; колебательные частоты подтвердили, что все структуры являются энергетическими минимумами (Фиг. 3). В расчетах использовалась модель графеновой поверхности, состоящая из 28 сопряженных циклов. Свободные валентности концевых атомов углерода графеновой поверхности «насыщались» атомами водорода.
Во всех трех случаях наблюдается слабое взаимодействие между молекулами и поверхностью с параллельной «face-to-face» ориентацией и расстоянием между плоскостями взаимодействующих фрагментов, во всех случаях, близким к 3 Å. Полученные значения находятся в хорошем соответствии с данными рентгеноструктурного анализа для систем, в которых присутствует π-π стейкинг (от 3 до 3.5 А). Рассчитанные энергии адсорбции имеют близкие и невысокие значения (1 ΔEads : -2.1603 кДж/моль, 2 ΔEads : -0.28 кДж/моль и 3 ΔEads : -1.30 кДж/моль). Поскольку энергия стейкинг-взаимодействия сильно зависит от степени перекрывания, то можно предположить, что орбитали взаимодействующих фрагментов перекрываются в слабой степени. Причиной такого слабого взаимодействия является большая разница в энергиях между граничными орбиталямиграфеновой поверхности и соединений 1, 2, 3, то есть большая разница в энергиях не приводит к стабилизации системы при адсорбции. Как видно из результатов расчета, максимальным значением ΔEadsпри близких значениях HOMO-LUMO и расстоянием между взаимодействующими фрагментами у соединений 1 и 2, обладает молекула плоского акридина, это может свидетельствовать о том, что орбитали полиароматических плоских систем перекрываются лучше, чем в неплоских.
Для более детального изучения процесса адсорбции были построены изотермы Ленгмюра и рассчитаны константа адсорбции (K), предельные значения адсорбции (А∞) и свободная энергия процесса адсорбции (∆G0адс). На Фиг. 4 представлены изотермы сорбции, по форме которых можно делать определенные выводы о характере поверхности сорбента.
Как видно из Фиг. 4, все изотермы сорбции органических веществ углеродсодержащим сорбентом соответствуют изотермам мономолекулярной адсорбции Ленгмюра и имеют выпуклую форму.
Это равновесие может быть описано уравнением Ленгмюра:
А=А∞
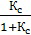 (1)
(1)
гдеА – величина адсорбции, моль/кг;
А∞– предельная мономолекулярная адсорбция (емкость монослоя);
К – константа адсорбционного равновесия (находится отношением констант адсорбции и десорбции и характеризуют энергию взаимодействия адсорбата с адсорбентом);
С – концентрация адсорбата в растворе, кмоль/м3.
Экспериментальные результаты адсорбции обрабатывают с помощью уравнения Ленгмюра, записанного в линейной форме:
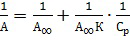 (2)
(2)
Графическая зависимость 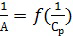 выражается прямой, пересекающей ось ординат. Отрезок, отсекаемый на оси ординат, определяет величину, обратную емкости монослоя
выражается прямой, пересекающей ось ординат. Отрезок, отсекаемый на оси ординат, определяет величину, обратную емкости монослоя 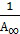 . Тангенс угла наклона прямой равен
. Тангенс угла наклона прямой равен 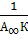 , что позволяет найти константу адсорбционного равновесия Кравн.
, что позволяет найти константу адсорбционного равновесия Кравн.
Изотермы приведены к линейной форме, для которых рассчитаны следующие параметры: tgα (тангенс угла наклона прямой), Kравн(константа адсорбционного равновесия), ∆G0адс (изменение энергии Гиббса адсорбции) по формулам (3), (4), (5).
Тангенс угла наклона прямой равен:
tgα=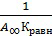 (3)
(3)
и позволяет найти константу адсорбционного равновесия Кравн.:
Кравн.=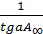 (4)
(4)
Зная константу адсорбционного равновесия, можно рассчитать изменение энергии Гиббса адсорбции:
∆G0адс = -RTlnK (5)
Рассчитанные параметры сорбции представлены в табл. 1.
Как видно из табл. 1, параметр A∞, характеризующий эффективность процесса, является наибольшим для соединения 1, затем для 2 и заметно уменьшается для 3. Увеличение как размера, так и объема молекулы для соединения 3, приводит к тому, что практически в два раза понижается максимальная адсорбция (параметр А∞) по сравнению с соединением 1. Полученные результаты хорошо согласуются с выводом о том, что адсорбция соединений 1, 2, 3 является структурно-зависимым процессом, который сильно зависит от наличия и размеров заместителей в ядре акридина. Интересно отметить, что введение в 9 положение исходного акридина (1) фенильного заместителя (2) приводит к незначительному уменьшению параметра А∞, тогда, как введение метильного радикала к атому азота приводит к тому, что параметр А∞ снижается практически в 1.5 раза по сравнению с соединением 2. Столь необычное поведение невозможно объяснить только размерными и объемными факторами. Также важно отметить, что при наименьшем значении А∞ для соединения 3, значение К практически в пять раз больше, чем значения К для соединений 1 и 2, и значение ∆G0адс также существенно выше. Высокие значения констант связанны с тем, что соединение 3 имеет положительный заряд и вследствие этого может взаимодействовать и стабилизироваться на поверхности углеродного носителя различными функциональными группами (-COOH, -COH, -OH). Наличие на поверхности функциональных групп подтверждается данными ИК-спектроскопии полученными для данного углеродного носителя. В ИК-спектрах имеются характерные полосы колебаний для -СООН группы, карбонильной и гидроксильной. Полученные данные хорошо согласуются с данными, представленными в работе, где показано, при использовании метода рентгеновской фотоэлектронной спектроскопии (XPS), наличие на поверхности углеродного материала VulcanXC-72 органических функциональных групп. Таким образом, соединение 3 за счет кулоновского взаимодействия сорбируется на поверхности носителя, стабилизируясь поверхностными группами, образуя поверхностный слой, который приводит к частичной блокировке каналов и пор в углеродном носителе, и как следствие этого к низкой эффективности процесса сорбции. Данное предположение хорошо согласуется с тем, что при переходе от соединения 2 к соединению 3 резко уменьшается параметр А∞, хотя объемно они не сильно отличаются. Кроме того, как видно из таблицы 2, значения ∆G0адс заметно превосходят теоретически полученные значения ΔEads. Схожие значения ∆G0адс были получены при изучении адсорбции на мезопористых углеродных материалов клатрохелатных комплексов кобальта, содержащих в апикальном положении полиароматические группы. На основе этого можно предположить, что и в случае соединений 1, 2, 3 протекает физическая адсорбция, представляющая собой структурно-зависимый процесс, на который сильно влияет структура абсорбента (количество и характер заместителей в акридине) и протекающая за счет взаимодействия адсорбента с порами материала, а не за счет π-π стейкинга.
Поскольку, основным параметром, влияющим на адсорбцию полиароматических соединений по механизму π-π стейкинга является энергетическая «совместимость» по энергии НОМО и LUMO орбиталей адсорбата и поверхности, следовательно, для протекания эффективной адсорбции за счет π-π стейкинга, необходимо контролировать энергии граничных орбиталей взаимодействующих фрагментов, и при необходимости химически модифицировать либо поверхность, либо структуру адсорбата. Так, уменьшение энергии LUMO адсорбата, достигнутое введением в молекулу 1 электронно-акцепторных заместителей, позволило заметно улучшить значение ΔEads.
Таким образом, можно сделать вывод, что неполярные молекулы 1 и 2 адсорбируются в порах на носителе углерода за счет физической адсорбции, однако не по механизму π-π стейкинга, а сорбционный механизм соединения 3 является сложным и может включать как физическую, так и химическую адсорбцию.
Электрохимические свойства были изучены с использованием метода циклической вольтамерометрии. ЦВА иммобилизованных соединений 1, 2, 3 на углеродном материале VulcanXC-72 содержит одну одноэлектронную волну в катодной области при потенциалах, близких к потенциалам исходных соединений в растворе (Фиг. 5).
Важно отметить, что при циклировании потенциала от 0 до -1.8 В для соединения 1 и 2 и от 0 до -0.8 для соединения 3 (50 циклов), ток в пике для соединений 1 и 2 не уменьшался, а для соединения 3 с увеличением числа циклов сканирования, значение тока уменьшалось. Вероятно, это связанно с тем, что та часть молекул, которая адсорбировалась на поверхности за счет кулоновской стабилизации поверхностными функциональными группами, вымывается с поверхности в раствор. Постоянное значение тока в пике для соединений 1 и 2 указывает на стабильность электродов в процессе электрохимических реакций и отсутствию процесса вымывания с поверхности электрода. Следует отметить, что для создания эффективных электрокаталитических систем передача электрона от электрода на каталитические центры, расположенные на поверхности электрода, должна быть достаточно быстрой и не ограничиваться скоростью переноса электронов между окислительно-восстановительным центрами. В противном случае, мы получим неэффективную каталитическую систему. Для всех иммобилизованных соединений была найдена линейная зависимость logIp vs logν с наклоном, близким к 1, что характерно для систем, в которых лимитирующий стадией является перенос электрона от поверхности электрода к катализатору, а не перенос заряда между окислительно-восстановительными центрами. Таким образом, электрохимические данные показывают, что органические соединения, иммобилизованные на углеродном носителе, могут использоваться в качестве гетерогенных каталитических системы процесса получения молекулярного водорода.
По сравнению с известным решением заявленное позволяет применять синтетически доступный и термодинамически устойчивый материал на основе безметального электрокатализатора для получения молекулярного водорода из воды в присутствии органических солей.
| название | год | авторы | номер документа |
|---|---|---|---|
| Применение гибридного материала на основе безметального электрокатализатора для генерирования водорода из воды | 2021 |
|
RU2781376C1 |
| Каталитическая система для электрохимического процесса получения молекулярного водорода | 2023 |
|
RU2805744C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛАТИНОСОДЕРЖАЩИХ ЭЛЕКТРОКАТАЛИЗАТОРОВ В БЕЗОРГАНИЧЕСКИХ СРЕДАХ | 2023 |
|
RU2815511C1 |
| Способ получения электрокатализатора платина на углероде | 2016 |
|
RU2646761C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРОВ С НАНОРАЗМЕРНЫМИ ЧАСТИЦАМИ ПЛАТИНЫ И ЕЕ СПЛАВОВ С МЕТАЛЛАМИ | 2018 |
|
RU2695999C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПЛАТИНО-РУТЕНИЕВЫХ ЭЛЕКТРОКАТАЛИЗАТОРОВ | 2010 |
|
RU2446009C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ МЕМБРАННО-ЭЛЕКТРОДНОГО БЛОКА С ТВЕРДЫМ ПОЛИМЕРНЫМ ЭЛЕКТРОЛИТОМ | 2023 |
|
RU2805994C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ И МОДИФИКАЦИИ ЭЛЕКТРОХИМИЧЕСКИХ КАТАЛИЗАТОРОВ НА УГЛЕРОДНОМ НОСИТЕЛЕ | 2015 |
|
RU2595900C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОКАТАЛИЗАТОРА ДЛЯ ТВЕРДОПОЛИМЕРНОГО ТОПЛИВНОГО ЭЛЕМЕНТА СО СТАБИЛИЗИРОВАННЫМ ВОДНЫМ БАЛАНСОМ | 2022 |
|
RU2788560C1 |
| Способ получения платиносодержащих катализаторов для топливных элементов и электролизеров | 2022 |
|
RU2775979C1 |
Изобретение относится к применению материала на основе безметального электрокатализатора, представляющего собой акридин, 9-фенил-акридин или N-метил-9-фенилакридин, адсорбированный на углеродном материале, для получения молекулярного водорода из воды в присутствии органических солей. Используемый материал является синтетически доступным и термодинамически устойчивым. 5 ил., 1 табл.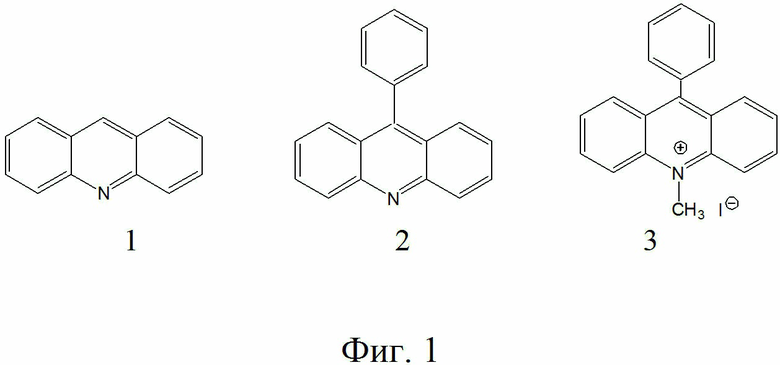
Применение материала на основе безметального электрокатализатора, представляющего собой акридин, 9-фенил-акридин или N-метил-9-фенилакридин, адсорбированный на углеродном материале, для получения молекулярного водорода из воды в присутствии органических солей.
| СПОСОБ ПОЛУЧЕНИЯ МОЛЕКУЛЯРНОГО ВОДОРОДА | 2011 |
|
RU2487965C2 |
| E.C | |||
| Hatchikian ET AL, Further characterization of the [Fe]-hydrogenase from Desulfovibrio desulfuricans ATCC 7757, Eur | |||
| J | |||
| Biochem., 1992, 209, 357 | |||
| US 5393615 A1, 28.02.1995. | |||
Авторы
Даты
2019-11-14—Публикация
2019-09-03—Подача