Сведения о родственной заявке
По этой заявке испрашивается приоритет от 7 октября 2016 по дате подачи предварительной патентной заявки США №62/405576, озаглавленной «Очистка растворов электролита посредством восстановления и соответствующие системы и способы», причем указанная заявка включена в данный документ во всей полноте посредством ссылки.
Область техники
Настоящее изобретение относится к очистке и получению растворов электролитов. Более конкретно, настоящее изобретение направлено на электрохимическую очистку растворов электролитов и связанные с ней системы и способы.
Уровень техники
Электролиты для батарей и других областей применения в общем не должны содержать примесей, которые вредны для этих областей применения. Например, в случае проточной окислительно-восстановительной батареи каждый используемый электролит не должен содержать примеси, которые загрязняют детали батареи. В конкретном примере, ванадиевая проточная окислительно-восстановительная батарея (ВПОВБ) является системой, которая преобразует электрическую энергию в химическую энергию и затем выделяет эту химическую энергию в виде электричества, когда это требуется. Этот тип батареи часто соединен с солнечной и/или ветряной электростанцией, чтобы способствовать сглаживанию прерывности производства энергии, связанной с этими возобновляемыми источниками энергии.
ВПОВБ содержит электрохимический элемент, который выполняет преобразование химической энергии в электрическую. Электрохимический элемент включает отрицательный электрод, электролитический сепаратор (часто протонообменную мембрану) и положительный электрод. Два отдельных ванадиевых раствора хранят в отдельных емкостях, где одна емкость содержит отрицательный раствор электролита, который подают на отрицательный электрод, а другая емкость содержит положительный раствор электролита, который подают на положительный электрод. В течение нормальной работы отрицательный раствор электролита содержит ионы ванадия (II) и (III), а положительный раствор электролита содержит ионы ванадия (IV) и (V). В течение заряда ионы ванадия (III) восстанавливаются до ионов ванадия (II) в отрицательном растворе электролита на отрицательном электроде и ионы ванадия (IV) окисляются до ионов ванадия (V) в положительном растворе электролита, противоположное происходит в течение разряда.
При запуске новой ВПОВБ сбалансированный раствор электролита со средней валентностью примерно 3,5, то есть раствор электролита с равной концентрацией ионов ванадия (III) и ионов ванадия (IV), перемещают в емкости как для отрицательного, так и для положительного электролитов. Батарея медленно заряжается до тех пор, пока отрицательный и положительный растворы электролитов не достигнут требуемого отношения ионов ванадия (II)/(III) и ионов ванадия (IV)/(V), соответственно. После этого начального заряда некоторые примеси, присутствующие в отрицательном растворе электролита, обычно осаждаются в виде осадка твердой металлической фазы. Эти примеси включают, но не ограничены перечисленным, As и Ge. Эти осадки вредны для электрохимического элемента, поскольку они засоряют отрицательный электрод и оказывают негативное воздействие на эксплуатационные качества батареи.
Большая часть обычных способов изготовления раствора электролита на основе ванадия включает один из двух следующих способов.
Способ 1. Смешивание V2O3 и V2O5 в молярном отношении 3:1 в избытке кислоты с получением раствора со средней валентностью 3,5.
Способ 2. Использование электрохимического элемента ВПОВБ, в котором отрицательный электрод используют для восстановления раствора электролита на основе ванадия до валентности 3,5, а положительный электрод окисляет раствор электролита на основе ванадия, который периодически или непрерывно восстанавливают, используя химический восстановитель. Такой подход требуется потому, что большинство органических восстановителей способны только восстановить ионы ванадия (V) до ионов ванадия (IV) (то есть большинство органических восстановителей не могут химически восстановить ионы ванадия (IV) до более низкой валентности).
Ни в одном из этих обычных способов нельзя надлежащим образом удалить примеси, которые часто загрязняют электрохимический элемент ВПОВБ. Скорее, в обоих способах требуется, чтобы ванадиевое сырье имело низкое содержание выбранных примесей для надлежащего функционирования и подавления загрязнения системы ВПОВБ. Следовательно, множество способов очистки направлено на очистку ванадиевого сырья. Хотя многие из этих способов являются эффективными, в них потребляется множество химикатов и конечный продукт требует высоких затрат.
Краткое описание изобретения
В одном воплощении настоящее изобретение направлено на способ получения очищенного раствора электролита. Способ включает предоставление раствора электролита, имеющего валентность осаждения и содержащего по меньшей мере одну примесь, которая осаждается из раствора электролита, когда валентность раствора электролита равна или ниже валентности осаждения, восстановление раствора электролита до валентности, которая ниже валентности осаждения, чтобы вызвать осаждение по меньшей мере одной примеси из раствора электролита в виде осадка, и механическое отделение осадка от раствора электролита, чтобы получить очищенный раствор электролита.
В другом воплощении настоящее изобретение направлено на способ запуска проточной окислительно-восстановительной батареи, имеющей положительную сторону и отрицательную сторону. Способ включает предоставление раствора электролита, имеющего начальную валентность и по меньшей мере четыре доступных степени окисления, включающих ряд более высоких степеней окисления и ряд более низких степеней окисления; восстановление раствора электролита до валентности ниже начальной валентности с получением восстановленного раствора электролита, имеющего валентность в пределах ряда более низких степеней окисления; окисление первой части восстановленного раствора электролита с получением раствора электролита положительной стороны, имеющего валентность в пределах ряда более высоких степеней окисления; предоставление для запуска раствора электролита положительной стороны для положительной стороны проточной восстановительно-окислительной батареи, и предоставление для отрицательной стороны проточной окислительно-восстановительной батареи, для запуска, второй части восстановленного раствора электролита в качестве раствора электролита отрицательной стороны, имеющего валентность в пределах ряда более низких степеней окисления.
В еще одном воплощении настоящее изобретение направлено на систему для получения очищенного раствора электролита из раствора электролита, содержащего по меньшей мере одну примесь, которая осаждается из раствора электролита при валентности, равной или ниже валентности осаждения. Система включает систему восстановления, которая включает электрохимический восстановительный элемент, выполненный и предназначенный для электрохимического восстановления раствора электролита с использованием восстановителя; контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части раствора электролита в электрохимический восстановительный элемент; систему регулирования процесса восстановления в оперативном соединении с системой восстановления, чтобы регулировать валентность раствора электролита в системе восстановления до требуемого значения, равного или ниже валентности осаждения, чтобы вызвать осаждение по меньшей мере одной примеси из раствора электролита в виде осадка, и систему механического отделения твердого вещества от жидкости, выполненную и предназначенную для удаления по меньшей мере части осадка из раствора электролита с получением очищенного раствора электролита.
В еще одном воплощении настоящее изобретение направлено на систему получения раствора электролита с регулируемой валентностью из раствора электролита, имеющего по меньшей мере четыре степени окисления. Система включает систему восстановления, которая включает электрохимический восстановительный элемент, выполненный и предназначенный для электрохимического восстановления раствора электролита с использованием восстановителя; контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части раствора электролита в электрохимический восстановительный элемент; систему регулирования процесса восстановления в оперативном соединении с системой восстановления, чтобы регулировать валентность раствора электролита в системе восстановления до требуемого значения; и выход, выполненный, предназначенный и расположенный для выпуска раствора электролита в виде предварительно восстановленного раствора электролита при примерно требуемом значении, и систему окисления, которая включает электрохимический окислительный элемент, выполненный и предназначенный для электрохимического окисления предварительно восстановленного раствора электролита с использованием окислителя; контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части предварительно восстановленного раствора электролита в электрохимический окислительный элемент, систему регулирования процесса окисления в оперативном соединении с системой окисления, чтобы регулировать валентность предварительно восстановленного раствора электролита в системе окисления до требуемого конечного значения, и выход, выполненный, предназначенный и расположенный для выпуска предварительно восстановленного раствора электролита при примерно требуемом конечном значении.
Краткое описание чертежей
Для иллюстрации изобретения на чертежах показаны аспекты одного или более воплощений изобретения. Однако нужно понимать, что настоящее изобретение не ограничено точно такими же конструкциями и устройствами, показанными на чертежах, где:
Фиг. 1 представляет собой график зависимости валентности от времени для приведенного в качестве примера способа образования/очистки электролита и регулирования валентности, где приведенный в качестве примера раствор электролита имеет четыре степени окисления, изменяющиеся от +2 до +5,
Фиг. 2 представляет собой схематическую диаграмму приведенного в качестве примера непрерывного способа образования/очистки электролита и регулирования валентности,
Фиг. 3А представляет собой диаграмму, показывающую приведенную в качестве примера конструкцию восстановительного элемента Фиг. 2,
Фиг. 3В представляет собой диаграмму, показывающую пример работы восстановительного элемента, имеющего конструкцию, показанную на Фиг. 3А, показывающую, что ванадиевый электролит восстанавливается, а газообразный водород окисляется,
Фиг. 4А представляет собой диаграмму, показывающую приведенную в качестве примера конструкцию окислительного элемента Фиг. 2,
Фиг. 4В представляет собой диаграмму, показывающую пример работы окислительного элемента, имеющего конструкцию, показанную на Фиг. 4А, показывающую, что ванадиевый электролит окисляется, при этом протоны восстанавливаются до газообразного водорода,
Фиг. 5 представляет собой схематическую диаграмму операции восстановления/очистки, используемой в экспериментальном испытании лабораторного масштаба,
Фиг. 6А представляет собой график работы элемента и напряжения разомкнутой цепи (НРЦ) в зависимости от времени (часы) в восстановительном элементе Фиг. 5 для партии 1, содержащей 3 литра электролита с примесями, содержащего большое количество As (5 частей на млн.) и Ge (0,2 части на млн.) и имеющего начальную валентность 3,5,
Фиг. 6В представляет собой график давления в зависимости от времени (часы) для партии 1 для давления непосредственно выше по потоку от фильтра перед восстановительным элементом Фиг. 5 и давления на входе в восстановительный элемент,
Фиг. 7А представляет собой график работы элемента и напряжения разомкнутой цепи в зависимости от времени (часы) в восстановительном элементе Фиг. 5 для порции 2, содержащей 3 литра электролита с примесями, содержащего большое количество As (5 частей на млн.) и Ge (0,2 части на млн.) и имеющего начальную валентность 3,5,
Фиг. 7В представляет собой график давления в зависимости от времени (часы) для партии 2 для давления непосредственно выше по потоку от фильтра перед восстановительным элементом Фиг. 5 и давления на входе в восстановительный элемент,
Фиг. 8 представляет собой схематическую диаграмму операции окисления, используемой в экспериментальном испытании лабораторного масштаба,
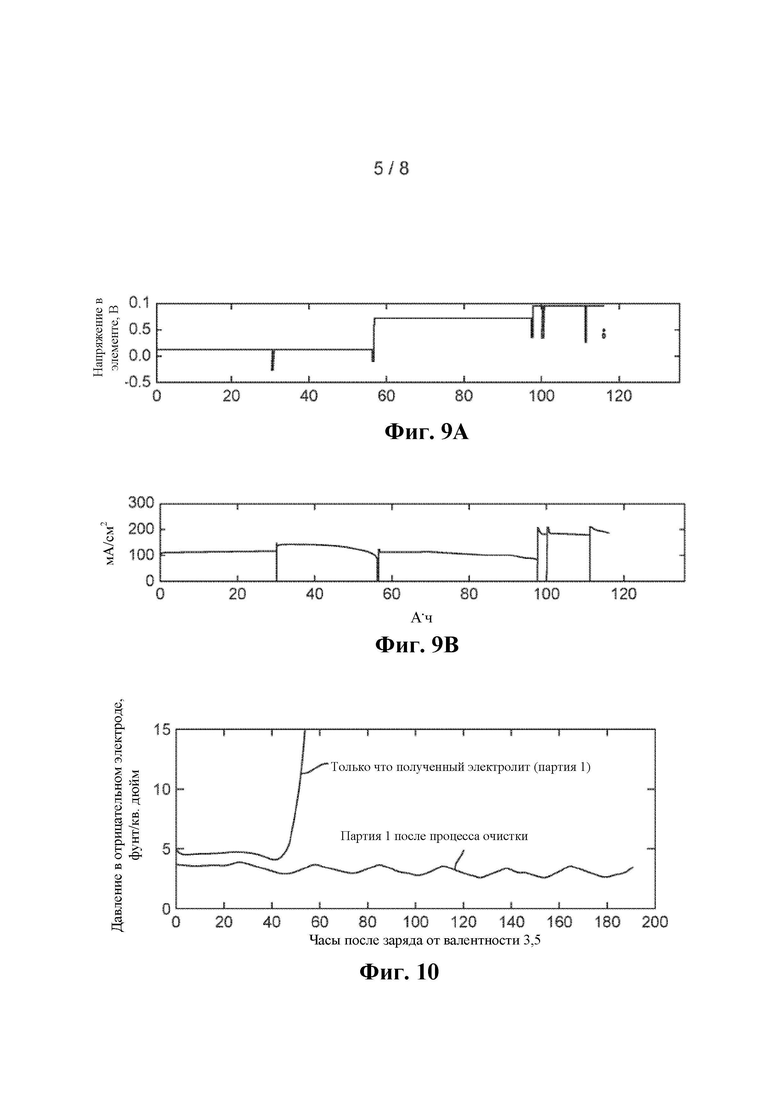
Фиг. 9А представляет собой график напряжения в зависимости от времени (часы) для окисления партии 1 электролита в операции окисления Фиг. 8,
Фиг. 9В представляет собой график плотности тока в зависимости от времени (часы) в окислительном элементе Фиг. 8,
Фиг. 10 представляет собой график давления отрицательного электрода в зависимости от времени (часы) для только что полученного электролита партии 1 и электролита партии 1 после восстановления/очистки с использованием экспериментального способа,
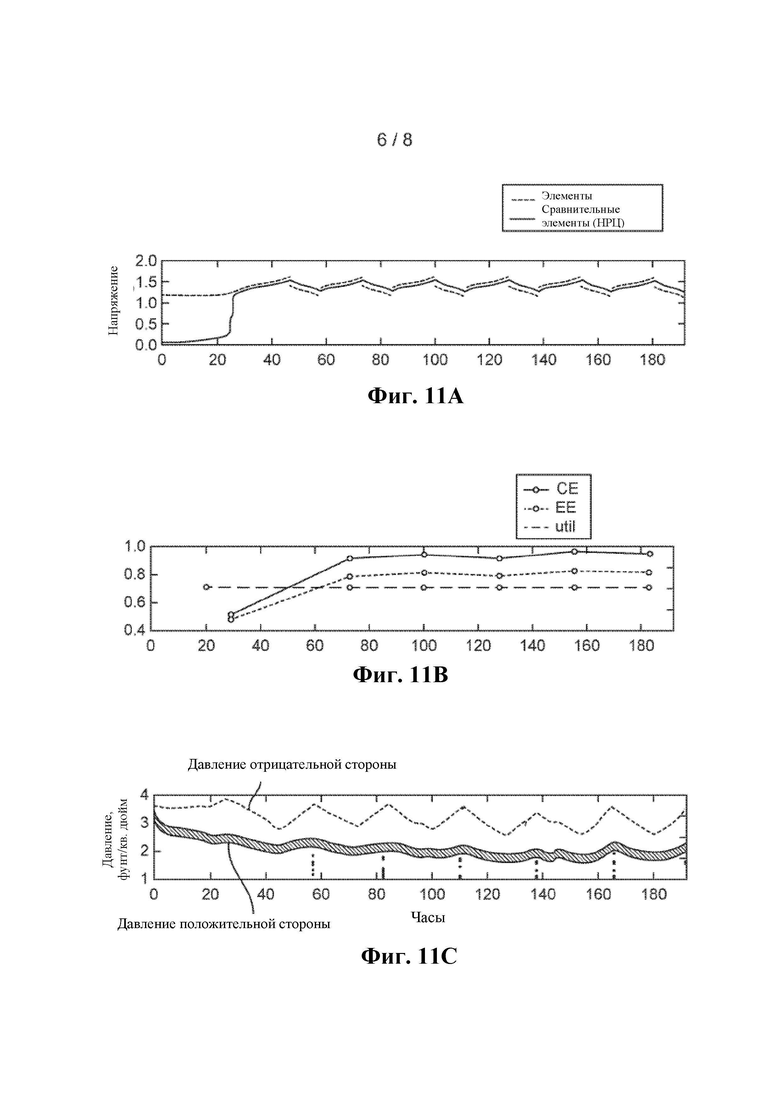
Фиг. 11А представляет собой график напряжений элемента и сравнительного элемента в зависимости от времени (часы) для порции 1 после восстановления/очистки с использованием экспериментального способа,
Фиг. 11В представляет собой график, показывающий кулоновскую эффективность, энергетическую эффективность и использование ванадия с течением времени (часы) для очищенной партии 1,
Фиг. 11С представляет собой график давления в зависимости от времени (часы), показывающий давления отрицательной стороны и положительной стороны электролита,
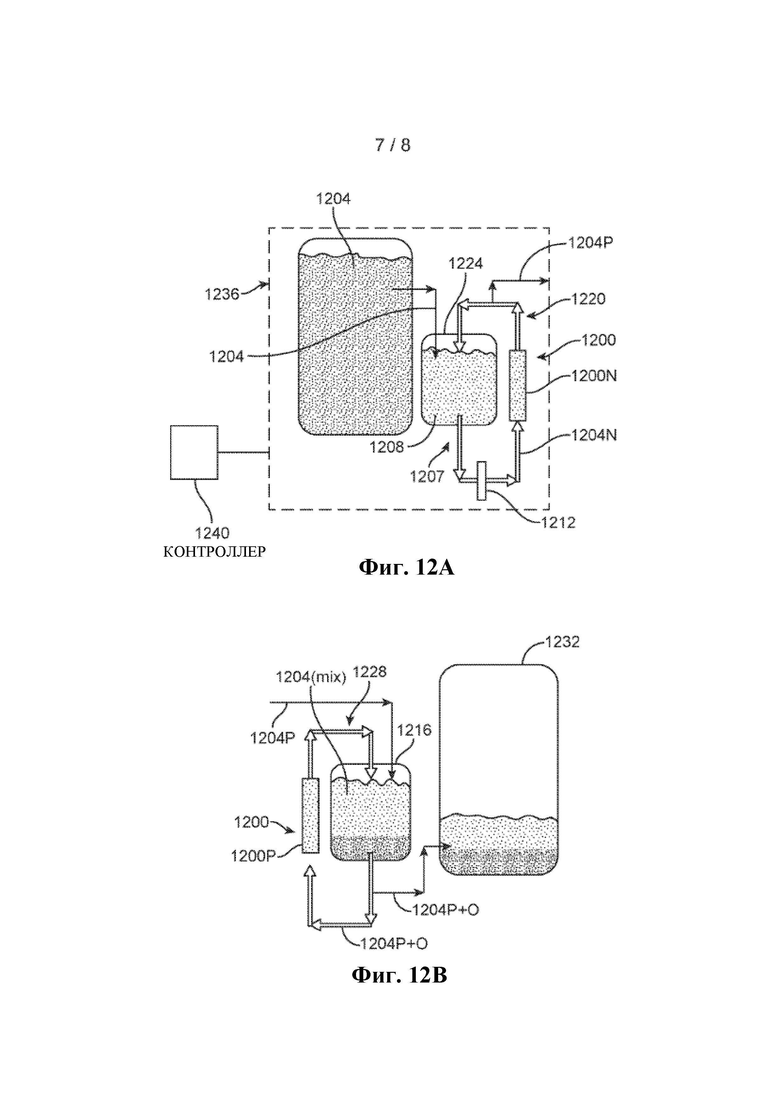
Фиг. 12А представляет собой диаграмму, показывающую операцию восстановления для системы очистки, в которой используют электрохимический элемент, который принимает электролит ВОВБ как на положительном, так и на отрицательном электродах,
Фиг. 12В представляет собой диаграмму, показывающую операцию окисления для системы очистки, в которой используют электрохимический элемент, который принимает электролит ВОВБ как на положительном, так и на отрицательном электродах,
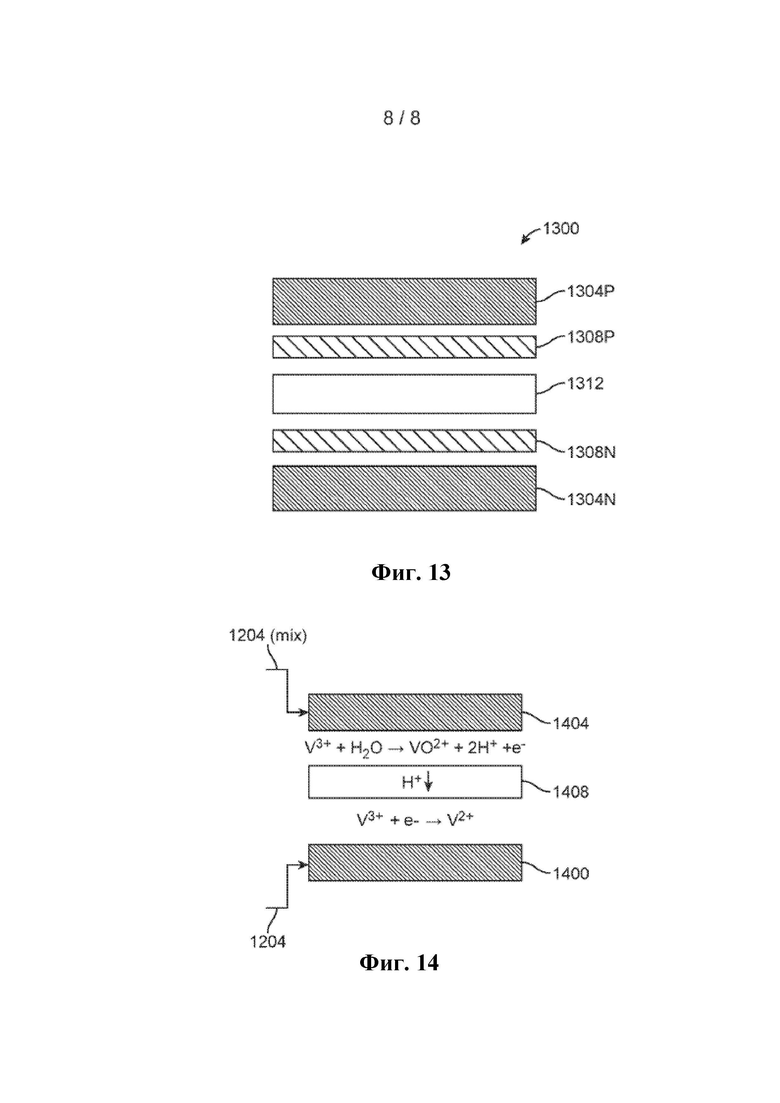
Фиг. 13 представляет собой диаграмму, показывающую электрохимический элемент, который можно использовать в каждой из операций восстановления и окисления, показанных на Фиг. 12А и 12В, соответственно, и
Фиг. 14 представляет собой диаграмму, показывающую реакции, протекающие в электрохимическом элементе Фиг. 13.
Подробное описание изобретения
В некоторых аспектах настоящее изобретение направлено на способы и системы удаления примесей из раствора электролита с использованием химического восстановления и способа фильтрации. Особенно полезное воплощение описано ниже в контексте ванадиевой проточной окислительно-восстановительной батареи (ВПОВБ), где в растворе электролита на основе ванадия удаляют одну или более примесей, которые в ходе обычной работы засоряли бы электрохимический элемент ВПОВБ в течение нормальной эксплуатации. Способ окисления, такой как способ электрохимического окисления, можно использовать после фильтрации для регулирования валентности восстановленного раствора электролита до требуемого значения, часто до валентности электролита 3,5.
В других аспектах настоящее изобретение направлено на способы и системы, направленные на запуск и связанные с запуском проточной окислительно-восстановительной батареи (ПОВБ). В конкретном воплощении раствор электролита сначала восстанавливают до относительно низкой степени окисления и затем окисляют, чтобы получить отрицательный и положительный растворы электролитов, имеющие различные валентности. Отрицательный и положительный растворы электролитов размещают на отрицательной и положительной стороне ПОВБ, соответственно, устраняя таким образом потребность в обычном способе заряда батареи, который сопровождает обычный запуск батареи. Эти и другие аспекты настоящего изобретения подробно описывают и поясняют на примерах ниже.
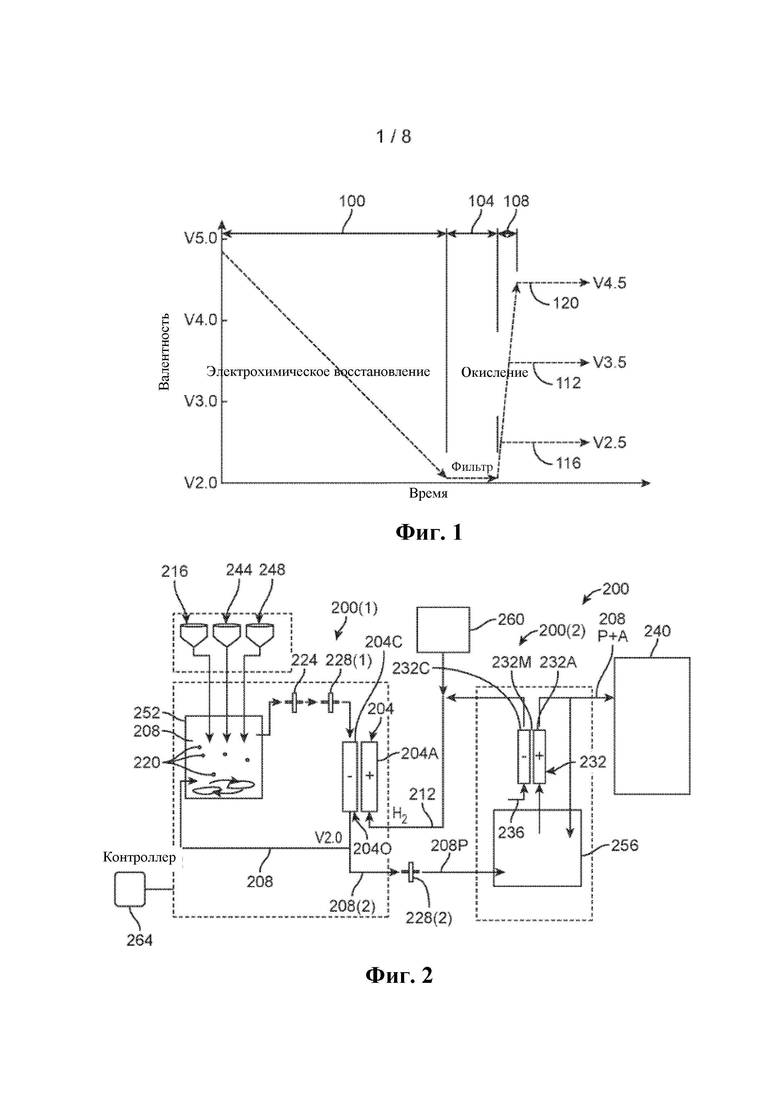
На Фиг. 1 в целом показан способ получения раствора электролита, имеющего требуемую валентность, путем очистки посредством восстановления, за которой следует фильтрация и регулирование валентности посредством окисления. Для понимания способа очистки, то есть электрохимического восстановления и фильтрации, показанных на Фиг. 1, нужно понимать, что рассматриваемая очистка включает удаление твердых осадков, которые образуются из примесей в растворе электролита при относительно низкой валентности ванадия. В некоторых растворах электролитов некоторые примеси находятся в растворенном в воде состоянии, когда валентность раствора электролита относительно высока, но они переходят в свои твердые формы, когда валентность раствора электролита является достаточно низкой. В зависимости от применения раствора электролита, твердые вещества, образованные при относительно низкой валентности раствора электролита, могут вредить его эксплуатации. Например, в случае ПОВБ, твердые примеси на отрицательной стороне электрохимического элемента ПОВБ могут засорять отрицательный электрод, приводя к ухудшению электрической характеристики ПОВБ по мере увеличения со временем загрязнения отрицательного электрода твердыми веществами.
В случае ВПОВБ, используемой в качестве примера, для экономичного изготовления растворов электролитов для ВПОВБ требуется недорогой источник оксидов ванадия. В общем, недорогие оксиды ванадия имеют высокие уровни примесей, которые оседают в растворах электролитов и оказывают большое негативное воздействие на эксплуатационные качества ВПОВБ. Как отмечали выше, наиболее вредными примесями являются те, которые растворены в воде в только что полученном растворе электролита, но осаждаются в виде твердых веществ, которые засоряют отрицательный электрод после начального заряда системы. Другими словами, наиболее вредные примеси являются растворимыми в растворе электролита с ионами ванадия (III)/(IV), но являются нерастворимыми (то есть образуют твердые осадки) в растворе с ионами ванадия (II)/(III). Показанный на Фиг. 1 способ очистки можно легко использовать для фильтрации осаждаемых примесей из раствора электролита до использования раствора в ВПОВБ.
В частности, на Фиг. 1 показаны очистка и регулирование валентности, выполняемые согласно настоящему изобретению для приведенного в качестве примера раствора электролита, где электролит имеет четыре возможные степени окисления, в данном случае, +2, +3, +4 и +5. Как видно в зоне 100 на Фиг. 1, способ очистки включает первое восстановление раствора электролита до валентности, которая ниже валентности, при которой целевая примесь (примеси) осаждается из раствора электролита. Начальная валентность в зоне 100 может быть любой валентностью от 3,5 до 5,0, в зависимости от используемого сырья оксида ванадия, в случае Фиг. 1 сделано допущение, что единственным сырьем является V2O5 и полученная начальная валентность равна 5,0. В показанном примере раствор электролита восстанавливают приблизительно до его низшей степени окисления (здесь степени окисления (II) (2,0)). Для раствора электролита на основе ванадия, например, целевые примеси осаждаются из раствора при валентности 3,0 или ниже. Следовательно, в некоторых воплощениях восстановление нужно проводить только до достижения валентности раствора электролита ниже примерно 3,0, например, от 2,9 до 2,0. Однако, более низкая валентность может потребоваться для ускорения процесса восстановления. Восстановление можно выполнять, используя любой подходящий способ, такой как электрохимическое восстановление с использованием электрохимического элемента. В одном примере можно использовать гибридный электрохимический элемент, в котором в одной половине элемента используют электролит ВОВБ, а в другой половине элемента используют восстановитель, отличный от ВОВБ. В другом примере электрохимический элемент можно выполнить с возможностью приема электролита ВОВБ в обеих половинах элемента.
После осаждения примесей из раствора электролита, в зоне 104 на Фиг. 1, твердые осадки удаляют из раствора. Удаление осадка можно выполнять, используя любые подходящие средства удаления, например, посредством одного или более пористых фильтров и/или одного или более циклонов, помимо прочего. В зависимости от применения раствора электролита, может потребоваться удалять только осадки определенного размера, так что соответственно можно сконструировать оборудование для удаления. Например, в ВПОВБ, которая включает отрицательный электрод, имеющий конкретный размер пор, может не требоваться фильтровать осадки определенного размера, который меньше этого размера пор, так как они могут протекать через отрицательный электрод и не засорять его.
На возможной стадии, показанной в зоне 108 на Фиг. 1, очищенный раствор электролита, то есть раствор, имеющий требуемое количество удаленного осадка, можно окислить до требуемой валентности. В качестве примера, используя ванадиевый электролит, очищенный раствор электролита можно окислить так, чтобы он содержал смесь ионов ванадия (III) и ванадия (IV) и имел валентность примерно 3,5, которая является валентностью обычного раствора электролита на основе ванадия, обычно предоставляемого для запуска ВПОВБ. Эта смесь представлена линией 112 на Фиг. 1.
В качестве другого примера с использованием ванадия в качестве электролита, как показано на Фиг. 1, очищенный раствор электролита можно окислить с созданием двух растворов электролитов с различными валентностями, например, одного раствора электролита с валентностью 3,0 или ниже, такой как валентность 2,5, содержащего ионы ванадия (II) и ванадия (III), и другого раствора электролита с валентностью 4,0 или выше, такой как валентность 4,5, содержащего ионы ванадия (IV) и ванадия (V). Эти два раствора электролитов представлены на Фиг. 1 линиями 116 и 120, соответственно. В этом примере эти два раствора электролитов можно использовать, соответственно, в качестве отрицательного и положительного растворов электролитов ВПОВБ.
Как отмечено выше, когда ВПОВБ запускают обычным образом, раствор электролита с валентностью 3,5 подают как в отрицательную, так и в положительную электролитические емкости ВПОВБ и затем батарею заряжают так, что раствор электролита отрицательной стороны устанавливается на валентности примерно 2,5, а раствор электролита положительной стороны устанавливается на валентности примерно 4,5. Однако, когда способ, показанный Фиг. 1, используют для получения отрицательного (с валентностью, например, 2,5) и положительного (с валентностью, например, 4,5) растворов электролитов и эти растворы электролитов добавляют в ВПОВБ, стадию заряда при запуске можно устранить. Следует отметить, что если сырьевой раствор электролита является достаточно чистым, то есть достаточно свободен от осаждаемых примесей, тогда стадию удаления примесей можно устранить в способе получения отрицательного и положительного растворов электролитов. Это воплощение может быть особенно полезным, когда для получения электролита в качестве единственного ванадиевого сырья используют материал с высокой степенью окисления, такой как V2O5.
В некоторых воплощениях любой из способов, представленных на Фиг. 1, можно выполнять на промышленном объекте по производству раствора электролита, так что получаемый раствор (растворы) электролита транспортируют в место использования, такое как установка ВПОВБ, довольно удаленная от промышленного объекта. Однако, стоимость транспортировки растворов электролитов может быть довольно высокой из-за таких факторов, как расстояние, коррозионная активность растворов электролитов и того факта, что большая доля массы растворов приходится на растворители (то есть кислоту и воду) в растворах. Следовательно, в другом воплощении любые из способов Фиг. 1 можно выполнять в месте использования или вблизи от него. Например, такие компоненты, как оборудование для восстановления, оборудование для удаления осадка и оборудование для окисления системы можно упаковать в контейнеры, уложить на поддоны или другим образом сделать легко транспортируемыми так, что способ(ы) можно было выполнять по месту.
В некоторых воплощениях для восстановления и окисления используют электрохимические элементы и эти элементы нужно снабжать электрической энергией для приведения в действие реакций. В таких воплощениях, которые используют вблизи мест использования произведенных растворов электролитов и в которых растворы используют для батарей для возобновляемых источников энергии, таких как ветряные энергетические установки и солнечные электростанции, электричество, необходимое для процессов восстановления и/или окисления можно обеспечить с помощью возобновляемых источников энергии.
Преимущества способов по настоящему изобретению по сравнению с существующими способами включают следующее.
Ни в одном известном способе не используют осаждение примесей для их удаления. Осажденные примеси удаляют механически, например, посредством фильтрации и/или гидроциклона.
Ни в одном известном способе не используют ни электрохимическое окисление, ни электрохимическое восстановление электролита для образования осадка ключевых примесей и его удаления.
Ни в одном предшествующем способе не используют электрохимические элементы для восстановления и окисления электролита ВОВБ. Одним примером элемента для восстановления электролита на основе ванадия является элемент водород/ВОВБ, где газообразный Н2 окисляется (потребляется) на катоде, и электролит ВОВБ восстанавливается на аноде. Окислительный элемент является похожим: Н2 получают на аноде и электролит ВОВБ окисляется на катоде.
Никакой другой способ не обеспечивает получение отдельных растворов как анолита, так и католита для системы ВПОВБ с использованием одной и той же электрохимической системы.
На Фиг. 2 показан приведенный в качестве примера способ 200 очистки, в котором используют две электрохимические операции, а именно операцию 200(1) восстановления/очистки для восстановления и очистки раствора электролита и операцию 200(2) окисления для доведения валентности раствора электролита до требуемой валентности. В способе 200 этого примера обеспечивают использование оксидов ванадия с единственной степенью окисления и пониженной чистотой. Образование и очистку раствора электролита в приведенном в качестве примера способе 200 выполняют непрерывным образом и способ разработан для работы при комнатной температуре.
В приведенном в качестве примера способе 200 удаляют примеси, которые наиболее вредны для характеристики ВПОВБ, а именно примеси, которые растворены в воде в смешанном растворе ванадия (III)/(IV), но которые образуют твердые осадки после заряда с получением раствора ванадия (II)/(III). Как отмечено выше, эти осадки могут засорять отрицательный электрод. Очистка, выполняемая с помощью способа 200, основана на обнаружении того, что наиболее вредные примеси осаждаются из раствора ванадия (II)/(III) и что эти примеси можно удалить механически, например, путем фильтрации и/или обработки в циклоне, помимо прочего. В этом примере другие примеси, такие как К, Na и Al, не удаляют в способе 200, потому что они остаются в виде ионов в растворе ванадия (II)/(III), однако воздействие этих ионов на характеристику батареи незначительно.
Электрохимическое восстановление и последующее окисление электролита на основе ванадия являются ключевыми для его образования и очистки. В этом примере восстановление и окисление раствора электролита выполняют за две отдельные операции, используя в каждой один или более их собственных электрохимических элементов. Необходимо отметить, что для иллюстрации только один электрохимический элемент показан для каждой из двух операций 200(1) и 200(2), хотя в каждой операции можно использовать два или более электрохимических элемента.
Операцию 200(1) восстановления/очистки, в которой происходит электрохимическое восстановления ванадиевого электролита, выполняют с помощью «восстановительного элемента» 204, такого как гибридный электрохимический элемент. Предоставляют электричество (не показано) для работы восстановительного элемента 204, и раствор 208 электролита на основе ванадия восстанавливают на катоде 204С, а восстановитель 212 окисляют на аноде 204А. В показанном примере восстановитель 212 представляет собой газообразный Н2, что обеспечивает относительно простую и недорогую систему. Однако в качестве восстановителя 212 можно использовать другие восстановители, в том числе такие как вода, муравьиная кислота, этиленгликоль.
На Фиг. 3А показана приведенная в качестве примера конструкция восстановительного элемента 300, которую можно использовать для восстановительного элемента 204 Фиг. 2. Как показано на Фиг. 3А, приведенный в качестве примера восстановительный элемент 300 включает поле течения 304 электролита, поле 308 течения газа (здесь газообразного Н2), протонообменную мембрану 312, электрод 316 из углеродной бумаги и газодиффузионный слой 320, покрытый катализатором реакции окисления Н2 (не показан). Раствор 208 электролита (Фиг. 2) протекает в поле 304 течения электролита, при этом восстановитель, здесь газообразный Н2, протекает в поле 308 течения газа. На Фиг. 3В показан пример работы восстановительного элемента 300 с блоком 324, представляющим сторону анода восстановительного элемента и принимающим восстановитель 212 (Н2); блоком 328, представляющим сторону катода восстановительного элемента и принимающим раствор 208 электролита, и блоком 332, представляющим протонообменную мембрану 312, которая обеспечивает проход протонов со стороны катода на сторону анода с потоком поступающих аналогичным образом электронов. На Фиг. 3В также показано восстановление раствора 208 электролита на основе ванадия и окисление восстановителя 212 (Н2). Специалистам легко понять, что конструкция восстановительного элемента 300, показанного на Фиг. 3А, является лишь примером и что по желанию можно использовать другие конструкции.
Снова со ссылкой на Фиг. 2, операция 200(1) восстановления/очистки выполняет две функции: 1) с ее помощью создают ионы ванадия (II), которые способствуют химическому растворению и восстановлению электролита 216, здесь порошка V2O5, и 2) с ее помощью осаждают наиболее вредные примеси 220 и обеспечивают их удаление посредством механических средств (например, фильтрации и/или обработки в циклоне). В примере, показанном на Фиг. 2, система 200 включает один или более подходящих фильтров, здесь фильтр 224 грубой очистки и пара фильтров 228(1) и 228(2) тонкой очистки. Результатом является очищенный раствор 208Р электролита, который очищают до степени, при которой часть или все осажденные примеси 220 удалены, здесь снова с помощью фильтров 224, 228(1) и 228(2).
Способ 200(1) восстановления/очистки можно регулировать с помощью соответствующего контроллера 264, который регулирует способ. Контроллер 264 может включать любое подходящее аппаратное обеспечение, такое как программируемый логический контроллер, компьютер общего назначения, специализированная интегральная микросхема или любое другое устройство(а) аппаратного обеспечения, способное выполнять подходящий алгоритм управления. Множество типов аппаратного обеспечения для контроллера 264 хорошо известны в уровне техники. В одном примере контроллер 264 выполнен, посредством программного обеспечения или другим образом, для регулирования валентности раствора электролита, вытекающего из восстановительного элемента 204, здесь раствора 208(2,0) электролита, путем регулирования потока раствора 208 электролита с примесями из емкости 252 в восстановительный элемент. В этом примере входные параметры алгоритма управления включают пользовательские параметры настройки, такие как электрический ток в восстановительном элементе 204, и измерение валентности электролита в емкости 252 с помощью подходящего датчика валентности (не показан). Например, с фиксированным током в элементе контроллер 264 определяет, находится ли измеренная валентность ниже целевого значения (например, валентности осаждения), и выдает один или более управляющих сигналов, которые управляют одним или более регуляторами потока (не показаны), которые, в свою очередь, регулируют поток раствора 208 электролита с примесями в восстановительную емкость 252. Такие регуляторы потока могут быть, например, одним или более насосами, одним или более клапанами или одним или более устройствами, которые изменяют поток сырья с примесями в емкость 252, или любым их сочетанием, помимо прочего. В другом воплощении контроллер 264 может быть выполнен для регулирования как тока в элементе, так и потока раствора 208 электролита с примесями, чтобы регулировать валентность раствора электролита внутри емкости 252. Специалисты легко поймут, как создать подходящий алгоритм для схемы управления, выбранной для контроллера 264, на основе этого описания и для используемого типа аппаратного обеспечения.
В операции 200(2) окисления в этом примере используют электрохимическое окисление для окисления очищенного раствора электролита, чтобы довести его до требуемого состояния валентности (например, валентность вблизи 3,5, валентность вблизи 2,5 и/или валентность вблизи 4,5, в зависимости от требуемого применения). В этом примере гибридный электрохимический элемент, называемый в данном документе «окислительным элементом» 232, используют для осуществления окисления в ответ на поставляемое в элемент электричество (не показано). Очищенный раствор 208Р электролита на основе ванадия окисляют на аноде 232А, и окислитель 236 восстанавливают на катоде 232С. В одном примере протоны восстанавливают с образованием газообразного Н2 на катоде 232С. Это особенно удобно, когда газообразный Н2 используют в качестве восстановителя 212 в восстановительном элементе 204, как отмечено выше. После окисления раствор(ы) электролита с отрегулированной валентностью можно, при необходимости, переместить в ВПОВБ, как показано блоком 240.
На Фиг. 4 показана приведенная в качестве примера конструкция окислительного элемента 400, который можно использовать для окислительного элемента 232 Фиг. 2. Как показано на Фиг. 4А, приведенный в качестве примера окислительный элемент 400 включает поле 404 течения электролита, поле 408 течения окислителя (здесь газообразного Н2), протонообменную мембрану 412, электрод 416 из углеродной бумаги стороны окисления, электрод 420 из углеродной бумаги стороны восстановления и газодиффузионный слой 424, покрытый катализатором реакции окисления Н2 (не показан). Раствор 208 электролита (Фиг. 2) протекает в поле 404 течения электролита, при этом окислитель 236, здесь протоны, образуется в поле 408 течения окислителя. На Фиг. 4В показана работа приведенного в качестве примера окислительного элемента 400 с блоком 428, представляющим сторону катода окислительного элемента, который принимает H2O 236; блоком 432, представляющим сторону анода окислительного элемента, который принимает раствор 208Р электролита, и блоком 436, представляющим протонообменную мембрану 412, которая обеспечивает проход протонов со стороны катода на сторону анода, с потоком поступающих аналогичным образом электронов. На Фиг. 4В также показано окисление раствора 208Р электролита на основе ванадия и восстановление протонов до газообразного Н2, который удаляют с помощью H2O 236. Специалистам легко понять, что конструкция окислительного элемента 400, показанного на Фиг. 4А, является лишь примером и что по желанию можно использовать другие конструкции.
Исходными ресурсами для приведенного в качестве примера способа 200 являются следующие ресурсы.
Материалы
В общем, растворитель 244 для растворения оксидов металлов 216, здесь порошка V2O5. Для соединения ванадия показанного примера этот растворитель состоит из одной или более сильных кислот, таких как серная кислота и/или соляная кислота. В других воплощениях можно использовать другие растворители, такие как бромистоводородная кислота и хлорноватая кислота, помимо прочих.
Если указанный растворитель не является полярным растворителем, полярный растворитель 248. Для показанного соединения ванадия используют воду.
Электролит, такой как электролит 216. В данном примере электролит является порошком пентоксида ванадия (V2O5). В других воплощениях можно использовать один или более оксидов ванадия, таких как оксид ванадия (III) (V2O3) один или в сочетании с оксидом ванадия (V) (V2O5). В других воплощениях можно использовать другие электролиты, в том числе такие, как в железно-хромовой проточной батарее и во всех урановых проточных батареях.
Протонодонорный восстановитель, такой как восстановитель 212. В данном примере используют газообразный Н2. В других воплощениях можно использовать другие восстановители, в том числе, такие как водород, вода, муравьиная кислота, этиленгликоль, H2O2.
Потребляющий протоны окислитель, такой как окислитель 232. В этом примере протоны восстанавливали до газообразного Н2. Альтернативой может быть использование кислорода или воздуха, где O2 восстанавливают до H2O.
Электричество
Электричество (не показано) обеспечивает подачу энергии как в восстановительный элемент, так и в окислительный элемент.
Конечный очищенный и отрегулированный раствор 208Р+А электролита в данном примере (то есть раствор электролита на основе ванадия, доведенный до валентности 3,5) может содержать:
электролит с несущим кислым раствором (обычно серной кислотой и/или соляной кислотой),
остальное составляют ионы ванадия (III) и (IV) в растворе, обычно в отношении 1:1, и
дополнительные добавки для термической стабилизации.
В этом примере операция 200(1) восстановления/очистки включает электрохимическое восстановление раствора 208 ванадиевого электролита. Химические/электрохимические реакции для этой приведенной в качестве примера операции 200(1) восстановления/очистки показаны ниже в таблице 1.
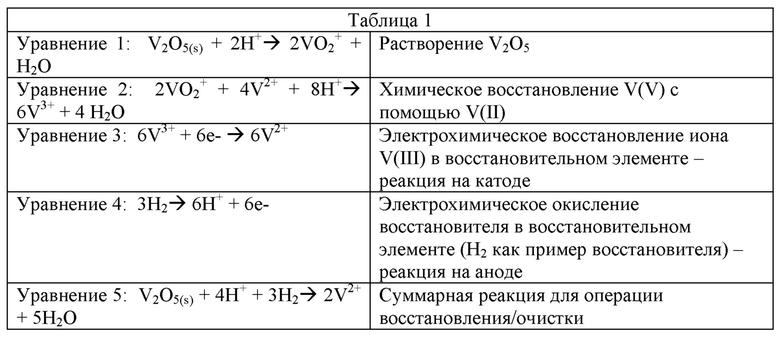
Одной из основных проблем использования порошка V2O5 (электролита 216) является его ограниченная растворимость в растворах сильных кислот. Вместо получения раствора электролита ванадия (V) в этом примере способа используют восстановленный раствор электролита, содержащий преимущественно ионы ванадия (II), как для растворения, так и для восстановления порошка V2O5. Порошок V2O5, воду и кислоту медленно добавляют в емкость с тщательным перемешиванием (емкость 252 на Фиг. 2), содержащую раствор 208 электролита преимущественно с ионами ванадия (II). Валентность раствора 208 преимущественно ионов ванадия (II) в емкости 252 поддерживают посредством восстановительного элемента 204. Когда порошок V2O5 (оксид металла 216) растворяют (таблица 1, уравнение 1) и восстанавливают (таблица 1, уравнение 2) в растворе 208 преимущественно ванадия (II), другие ионы ванадия окисляются (таблица 1, уравнение 2). Это окисление ионов ванадия уравновешивают, используя восстановительный элемент 204, который непрерывно восстанавливает раствор 208 электролита для подержания постоянной валентности. Результаты измерений наборов датчиков (не показаны), которые измеряют концентрацию и общий объем ванадия (II) и (III), можно использовать для регулирования расходов V2O5 (оксид металла 216), кислоты (растворитель 244) и воды (полярный растворитель 248) в емкости 252, электрического тока в восстановительном элементе 204 и скорости извлечения электролита 208 (2,0) с валентностью приблизительно 2,0 из выхода 204О восстановительного элемента в емкость 256 операции 200(2) окисления. Примеры датчиков для измерения концентрации ванадия (II) и (III) включают, помимо прочего, имеющиеся в продаже промышленные оптические датчики и электрохимические элементы, содержащие электроды сравнения.
Ионы ванадия (II) в емкости 252 служат двум целям. Во-первых, они способствуют быстрому растворению и восстановлению порошка V2O5 (оксид металла 216), как описано ранее. Во-вторых, ионы ванадия (II) обеспечивают восстановительную атмосферу для восстановления многих из наиболее вредных примесей (например, примесей 220) до их твердого, нейтрального состояния. Примеси отфильтровывают, когда они находятся в своем твердом состоянии, снова используя механические средства, в данном случае, набор из фильтра 224 грубой очистки и фильтра 228(1) тонкой очистки, помещенных выше по потоку от восстановительного элемента 204. В показанном примере фильтр 224 грубой очистки, например, фильтр из активированного угля, фильтрует относительно более крупные осажденные твердые вещества, а фильтры 228(1) и 228(2) тонкой очистки, например, гидрофильные фильтры из политетрафторэтилена, фильтруют относительно более мелкие осажденные частицы. Как отмечено выше, в случае ВПОВБ, степень фильтрации может зависеть от размера пор отрицательного электрода (электродов), используемого в целевой ВПОВБ.
В этом примере примеси 220, которые осаждаются из восстановленного раствора 208 электролита, могут включать, но не ограничены перечисленным, осадки металлического As и Ge. Фильтры 224, 228(1) и 228(2) перед восстановительным элементом 204 имеют две функции: они 1) удаляют примеси 220 из раствора 208 электролита и 2) защищают восстановительный элемент от осажденных примесей. Второй функции успешно достигают, если любой из фильтров 224, 228(1) и 228(2) имеет меньший эффективный размер пор, чем электрод из углеродной бумаги восстановительного элемента 204, например, электрод 316 из углеродной бумаги, показанный на Фиг. 3А. Система фильтров 224, 228(1) и 228(2) и восстановительный элемент 204, показанные на Фиг. 2, обеспечивают непрерывную работу восстановительного элемента. Способы, в которых используют электроосаждение/электровыделение, требуют частой химической очистки элемента или замены электрода, что временно прекращает работу.
Восстановительный элемент 204 работает путем восстановления ионов ванадия (III) на катоде 204(C) (таблица 1, уравнение 3) и окисления восстановителя 212 на аноде 204(A). Как отмечено выше, в этом примере газообразный Н2 используют в качестве восстановителя (таблица 1, уравнение 4), но как также отмечено выше, можно использовать другие химические восстановители, помимо прочего, такие как вода, муравьиная кислота или этиленгликоль. В этом примере восстановитель 212, здесь газообразный Н2, предоставляют как из источника 260 Н2, так и из окислительного элемента 232 операции 200(2) окисления, в котором получают газообразный Н2. Пример конструкции восстановительного элемента 204 и соответствующих реакций в половине элемента показаны на Фиг. 3А и 3В, соответственно. Ниже по потоку от выхода 204О (Фиг. 2) восстановительного элемента 204 часть очищенного раствора 208Р электролита возвращают в емкость 252, чтобы способствовать растворению и восстановлению порошка V2O5 (оксид металла 216), а часть перемещают в операцию 200(2) окисления.
Операция 200(2) окисления включает окисление очищенного раствора 208Р электролита. Химические/электрохимические реакции для этого приведенного в качестве примера способа показаны ниже в таблице II.

Очищенный раствор 208Р электролита со средней валентностью, которая ниже критической валентности осаждения (то есть ниже 2,9), перемещают из операции 200(1) в емкость 256. Очищенный раствор 208Р электролита в емкости 256 поддерживают при валентности, которая немного ниже конечной требуемой валентности (обычно 3,5 в этом примере). Очищенный раствор 208Р электролита из емкости 256 закачивают в окислительный элемент 232, в котором очищенный раствор электролита окисляют до требуемой конечной валентности с получением раствора электролита 208Р+А с отрегулированной валентностью. Часть выходящего из окислительного элемента 232 потока возвращают в емкость 256 для поддержания постоянной валентности и, в данном примере, остаток перемещают в ВПОВБ, как показано блоком 240.
В этом примере в электрохимическом окислительном элементе 232 окисляют очищенный раствор 208Р электролита и восстанавливают протоны (то есть получают газообразный Н2). Конкретно, в окислительном элементе 232 окисляют ионы ванадия (III) на аноде 232А посредством полуреакции, показанной в таблице II, уравнение 7, и восстанавливают протоны с образованием газообразного Н2 на катоде 232С, как описано полуреакцией, показанной в таблице II, уравнение 6. Суммарная реакция для приведенного в качестве примера окислительного элемента 232 приведена в таблице II, уравнение 8. В окислительном элементе 232 вода циркулирует на стороне получения Н2 (то есть на катоде 232С), так как она помогает смывать ионы ванадия, которые мигрируют через мембрану 232М к катоду.
Как описано выше, в альтернативном способе можно получать очищенный раствор 208Р+А электролита с отрегулированной валентностью для любой требуемой валентности. Например, в окислительном элементе 232 можно окислять первую партию очищенного раствора 208Р+А электролита с отрегулированной валентностью до валентности 2,5 для отрицательного раствора электролита ВПОВБ и вторую партию очищенного раствора электролита с отрегулированной валентностью до валентности 4,5 для положительного раствора электролита ВПОВБ. Перемещение этих двух отдельных растворов, соответственно, в емкость для католита и емкость для анолита ВПОВБ должно устранить потребность в процессе заряда, требуемом при запуске новой системы батарей.
В другом воплощении, показанном на Фиг. 12А и 12В, каждый из одного или более электрохимических элементов, здесь электрохимический элемент 1200, имеющий отрицательную сторону 1200N (Фиг. 12А) и положительную сторону 1200Р (Фиг. 12В), принимает раствор электролита, такой как раствор электролита на основе ванадия, как на положительной, так и на отрицательной стороне элемента. Это устраняет необходимость в отдельном восстановителе для операции восстановления/очистки и отдельном окислителе для операции окисления. На Фиг. 13 показан пример электрохимического элемента 1300, который можно использовать в качестве электрохимического элемента 1200 Фиг. 12А и 12В. Со ссылкой на Фиг. 13, электрохимический элемент 1300 может иметь симметричную конструкцию, состоящую из отрицательного и положительного полей 1304N, 1304Р течения, соответственно, отрицательного и положительного электродов 1308N и 1308Р из углеродной бумаги, соответственно, и протонообменной мембраны 1312 между отрицательной и положительной сторонами элемента.
В одном примере очистки раствора электролита на основе ванадия начальный раствор 1204 электролита с примесями (Фиг. 12А) можно получить из примерно равного количества ванадия (III) и ванадия (IV), и он содержит по меньшей мере одну примесь, удаляемую в способе. Раствор 1204 электролита с примесями можно получить, например, используя любой из способов, описанных выше в разделе «Уровень техники» (то есть либо способ 1, либо способ 2). В способе, показанном на Фиг. 12А и 12В, отрицательный электрод 1200N каждого электрохимического элемента 1200 восстанавливает раствор 1204 электролита до валентности ниже критической валентности осаждения примеси (см., например, зону 104 Фиг. 1), при этом положительный электрод 1200Р каждого электрохимического элемента окисляет ванадий (III) до ванадия (IV). Выше по потоку от отрицательного электрода (электродов) 1200N (Фиг. 12А) один или более фильтров, схематически представленных как 1212 Фиг. 12А, которые могут быть такими же как фильтры 224, 228(1) и 228(2) Фиг. 2 или отличными от них, улавливают осажденные примеси в растворе 1204N электролита отрицательной стороны до их поступления на отрицательный электрод 1200N.
После прохождения через фильтр (фильтры) 1212, часть этого теперь очищенного раствора 1204Р электролита можно переместить, например, в емкость 1216 для положительного электролита (Фиг. 12В). Этот процесс перемещения препятствует электрохимическому окислению текучей среды в контуре 1220 электролита положительной стороны (Фиг. 12В) и поддерживает валентность приблизительно 3,5. Аналогично, начальный раствор 1200 электролита (Фиг. 12А) пониженной чистоты медленно перемещают в емкость 1224 для электролита отрицательной стороны. Это перемещение химически препятствует электрохимическому восстановлению и поддерживает валентность на уровне критической валентности осаждения или ниже него. Раствор в контуре 1228 электролита положительной стороны (Фиг. 12В) (хранящийся в емкости 1216 положительной стороны) не содержит ключевых загрязнителей, которые осаждались бы в системе ВПОВБ. Очищенный и окисленный раствор 1204Р+О электролита положительной стороны не содержит вредных примесей и его перемещают в накопитель 1232, где его можно хранить до использования, например, в системе ВПОВБ. Хотя в этом воплощении добавляют дополнительные материальные затраты для электролита, обусловленные химическим восстановителем или восстановленным оксидом ванадия, его основной функцией является удаление ключевых примесей из электролита. Когда в отдельных электрохимических элементах используют одинаковый основной раствор электролита как на положительной, так и на отрицательной сторонах, эти элементы можно для удобства называть «электрохимическими элементами только с электролитом».
Необходимо отметить, что на стороне восстановления/очистки (Фиг. 12А) способ 1236 восстановления/очистки можно регулировать с помощью соответствующего контроллера 1240, который регулирует операцию восстановления/очистки. Подобно контроллеру 264 Фиг. 2, контроллер 1240 Фиг. 12А может включать любое подходящее аппаратное обеспечение, такое как программируемый логический контроллер, компьютер общего назначения, специализированная интегральная микросхема или любое другое устройство (устройства) аппаратного обеспечения, способное выполнять подходящий алгоритм управления. Множество типов аппаратного обеспечения, подходящих для контроллера 1240, хорошо известны в уровне техники. В одном примере контроллер 1240 выполнен, посредством программного обеспечения или другим образом, для регулирования валентности раствора электролита, вытекающего из отрицательной стороны 1200N восстановительного элемента 1200, здесь раствора 1204Р электролита, путем регулирования потока раствора 1204 электролита с примесями из емкости 1224 электролита отрицательной стороны в восстановительный элемент. В этом примере входные параметры алгоритма управления включают пользовательские параметры настройки, такие как электрический ток в восстановительном элементе 1200, и измерение валентности электролита 1208 в емкости 1224 с помощью подходящего датчика валентности. Например, с фиксированным током в элементе контроллер 1240 определяет, находится ли измеренная валентность ниже целевого значения (например, валентности осаждения), и выдает один или более управляющих сигналов, которые управляют одним или более регуляторами потока (не показаны), которые регулируют поток раствора 1204 электролита с примесями в восстановительный элемент 1200. Такие регуляторы потока могут быть, например, одним или более насосами, одним или более клапанами, или одним или более устройствами, которые изменяют поток сырья с примесями в емкость 1224 электролита отрицательной стороны, или любым их сочетанием, помимо прочего. В других воплощениях контроллер 1240 может быть выполнен для регулирования как тока в элементе, так и потока раствора электролита с примесями, чтобы регулировать валентность раствора электролита (здесь раствора 1208). Специалисты легко поймут, как создать подходящий алгоритм для схемы управления, выбранной для контроллера 1240, на основе этого описания и учитывая тип используемого аппаратного обеспечения.
На Фиг. 14 показана работа приведенного в качестве примера электрохимического элемента 1200 (Фиг. 12А и 12В) с блоком 1400, представляющим сторону катода электрохимического элемента, которая принимает раствор электролита 1204 из емкости 1224 для электролита отрицательной стороны (Фиг. 12А); блоком 1404, представляющим сторону анода электрохимического элемента, которая принимает раствор 1204(mix) электролита из емкости 1216 положительной стороны (Фиг. 12В) и блоком 1408, представляющим протонообменную мембрану 1312 (Фиг. 13), которая обеспечивает прохождение протонов со стороны катода на сторону анода. Специалист легко поймет, что конструкция электрохимического элемента 1200, показанного на Фиг. 12А и 12В, является лишь примером и что по желанию можно использовать другие конструкции.
Результаты экспериментов лабораторного масштаба
Обзор и краткое изложение результатов лабораторного масштаба
Способ очистки согласно аспектам настоящего изобретения был продемонстрирован в лабораторном масштабе. Далее следует обзор этого способа.
Требуемая система промышленного масштаба является системой, которая выполняет непрерывное образование/очистку электролита. Однако, для обоснования идеи в лабораторном масштабе использовали периодический способ.
Восстановление начального раствора электролита с валентностью 3,5 осуществляли, используя Н2/ВОВБ гибридный электрохимический элемент 500 (Фиг. 5), такой же как элемент, показанный на Фиг. 3А.
Окисление очищенного раствора электролита выполняли в гибридном электрохимическом элементе 800 (Фиг. 8), таком же как элемент, показанный на Фиг. 4А.
Демонстрация операции восстановления/очистки в лабораторном масштабе
Два образца начального раствора электролита, имеющих начальную валентность 3,5, то есть партию 1 и партию 2, подвергали описанному выше варианту способа восстановления/очистки. Каждый образец имел объем 3 литра и его восстанавливали до раствора с валентностью 2,0. Содержание ванадия в каждом образце составляло от 1,4 моль/литр до 1,65 моль/литр. Тот же самый восстановительный элемент 500 (Фиг. 5) (никакой замены электрода или замены мембраны) использовали для обоих образцов. Конструкция восстановительного элемента 500 и его работа являлись такими же, конструкция и работа восстановительного элемента 300, показанного на Фиг. 3А и 3В, соответственно. Активная площадь восстановительного элемента 500 (Фиг. 5) составляла 23 см2.
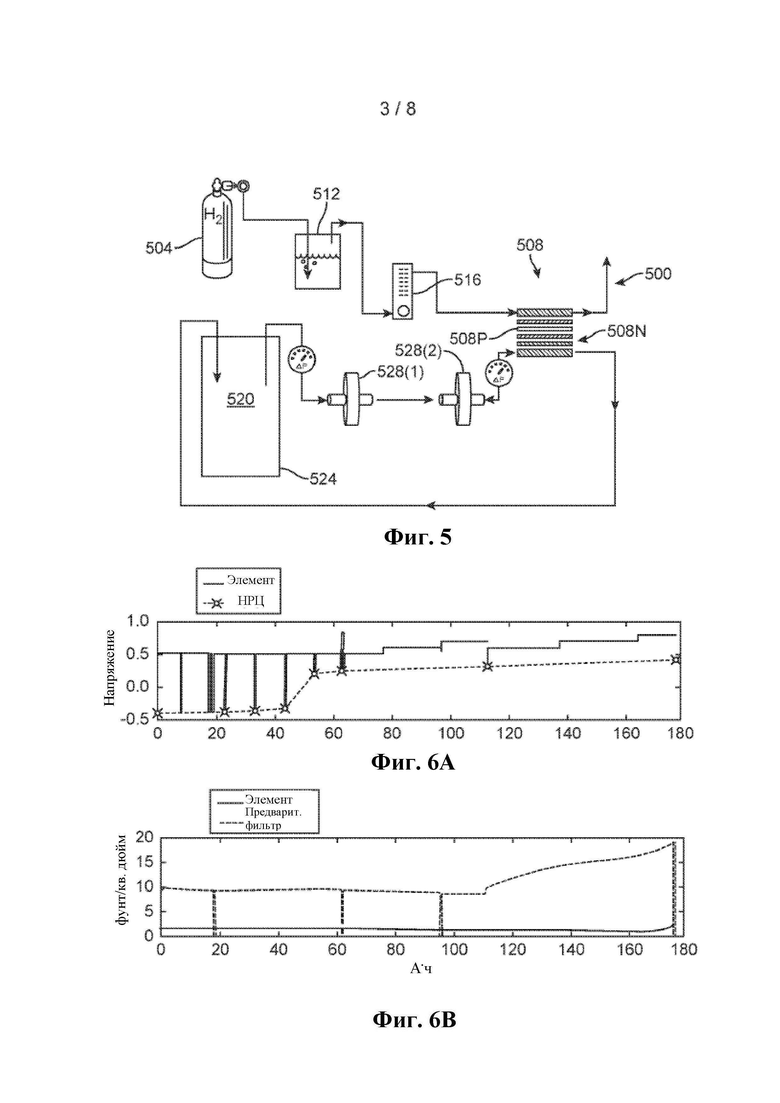
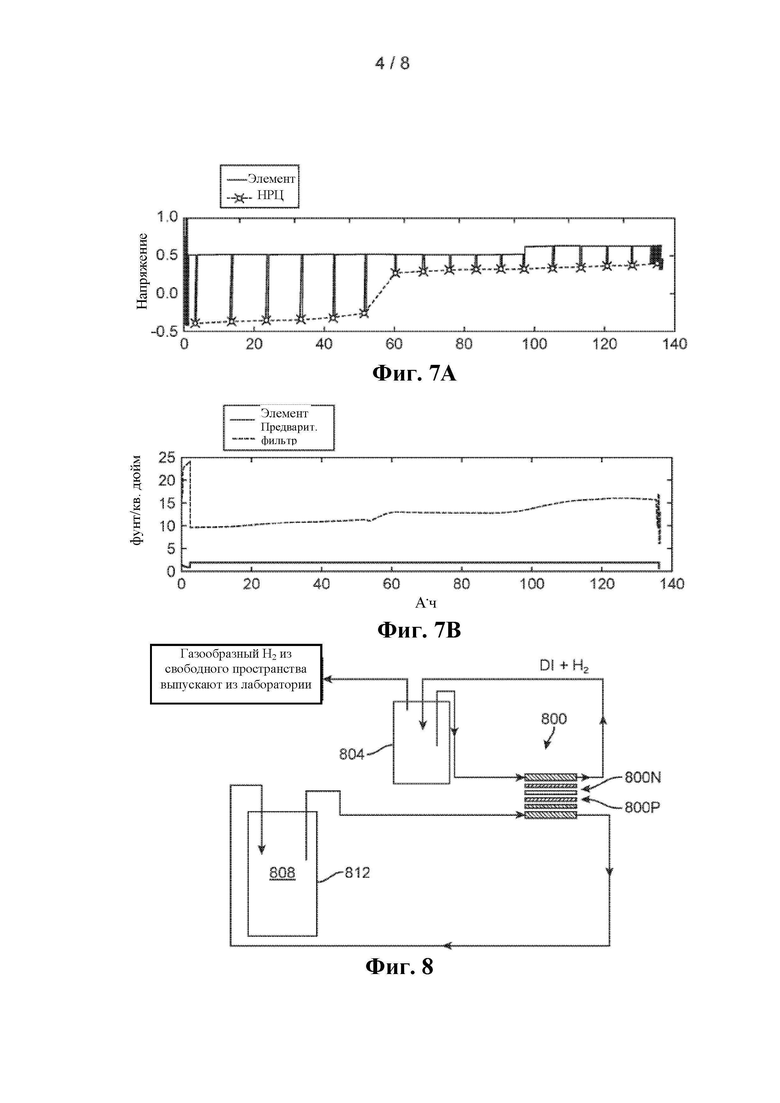
На Фиг. 5 показана операция восстановления/очистки лабораторного масштаба, использованная при испытании партий 1 и 2. Баллон 504 с водородом снабжал водородом Н2/ВОВБ элемент 508 на положительном электроде 508Р. Сухой водород увлажняли путем пропускания его через деионизированную (ДИ) воду в барботере 512. Регулятор 516 потока регулировал поток водорода в Н2/ВОВБ элемент 508. ВОВБ электролит 520 хранили в пластмассовой емкости 524. ВОВБ электролит 520 в емкости 524 рециркулировали через Н2/ВОВБ элемент 508 на отрицательный электрод 508N и пропускали через два фильтра 528(1) и 528(2) до поступления в элемент. Рециркуляцию выполняли с помощью шлангового насоса (не показан). К Н2/ВОВБ элементу 508 прикладывали постоянный ток (не показан), посредством которого окисляли водород и восстанавливали ванадий в ВОВБ электролите 520. Фильтры 528(1) и 528(2) выше по потоку от Н2/ВОВБ элемента 508 состояли, соответственно, из фильтра грубой очистки (активированный уголь) и фильтра тонкой очистки (фильтр из гидрофильного политетрафторэтилена с размером пор 0,5 микрона). Напряжения в элементе в Н2/ВОВБ элементе 508 показаны на Фиг. 6А для партии 1 и на Фиг. 7А для порции 2, а давления в элементе показаны на Фиг. 6В для партии 1 и на Фиг. 7В для партии 2. Напряжения разомкнутой цепи, представленные на Фиг. 6А и 7А, измеряли путем периодического отключения постоянного тока от элемента. Оказалось, что операция восстановления/очистки была успешной в обоих случаях, демонстрируя две ключевые идеи, а именно:
Давление (Фиг. 6В и 7В), измеренное выше по потоку от фильтров 528(1) и 528(2) (Фиг. 5), повышалось по мере продолжения способа. Этот подъем давления показывает, что фильтры 528(1) и 528(2) успешно захватывают осажденные примеси.
Давление (Фиг. 6В и 7В) сразу выше по потоку от восстановительного элемента 508 (Фиг. 5) не повышается в течение операции, что указывает на то, что фильтры 528(1) и 528(2) защищают восстановительный элемент от засорения осажденными примесями.
Демонстрация операции окисления в лабораторном масштабе
Партию 1 очищенного раствора электролита из операции восстановления/очистки окисляли до валентности 3,5, используя Н2/ВОВБ элемент 800 (Фиг. 8), который был идентичен по конструкции и работе с конструкцией и работой окислительного элемента 400, показанного на Фиг. 4А и 4В, соответственно. Операция окисления периодического типа, выполненная в лабораторном масштабе, показана на Фиг. 8. ДИ воду хранили в пластмассовой емкости 804, и ее рециркулировали через Н2/ВОВБ элемент 800 на отрицательный электрод. Поток ДИ воды способствовал удалению ванадия, который мигрирует через отрицательный электрод 800N. ВОВБ электролит 808 хранили в пластиковой емкости 812 и рециркулировали через Н2/ВОВБ элемент 800 на положительный электрод 800Р элемента. Постоянный ток (не показан) прикладывали к Н2/ВОВБ элементу 800, который восстанавливал протоны до газообразного водорода и окислял ванадий в ВОВБ электролите 808. Напряжение и плотности тока в Н2/ВОВБ элементе 800 показаны, соответственно, на Фиг. 9А и 9В. Активная площадь Н2/ВОВБ элемента 800 (Фиг. 8) составляла 23 см2.
Подтверждение очистки электролита в лабораторном масштабе
Партию 1 испытывали в системе ВОВБ лабораторного масштаба для подтверждения того, что ключевые примеси были удалены в электролите до приемлемого уровня. Характеристика электролита перед процессом очистки и после процесса очистки показана на Фиг. 10, где сравнивают давления в отрицательном электроде в течение работы перед процессом и после процесса очистки лабораторного масштаба. Показатели работы полного элемента для очищенной партии 1 электролита (напряжения, сопротивления элемента, характеристика цикла и давления) показаны на Фиг. 11А-11С. На Фиг. 11В «СЕ» означает кулоновскую эффективность, «ЕЕ» означает энергетическую эффективность и «Util» означает утилизацию ванадия. На Фиг. 11С представлены данные для давления отрицательной стороны и давления положительной стороны с полным элементом ВОВБ лабораторного масштаба с соответствующими растворами электролитов на основе ванадия, протекающими на соответствующих сторонах элемента.
Обзор параметров и технических характеристик системы приведен ниже и показан на Фиг. 11А-11С.
Параметры циклического испытания
Напряжение разомкнутой цепи в конце разряда = 1,28 В
Напряжение разомкнутой цепи в конце заряда = 1,52 В
Напряжение элемента при максимальном заряде = 1,6 В
Технические характеристики системы
1,46 моль/литр ванадия
Валентность 3,50
Полный объем системы 2,8 литра (положительный и отрицательный электролиты)
2 электрода из углеродной бумаги
Протонообменная мембрана
Активная площадь 11 см2
Выше представлено подробное описание иллюстративных воплощений изобретения. Следует отметить, что в данном техническом описании и приложенной к нему формуле изобретения объединяющие формулировки, такие как используют в выражениях «по меньшей мере один из X, Y и Z» и «один или более из X, Y и Z», если специально не заявлено или указано иное, означают, что каждый элемент в объединенном перечне может присутствовать в любом количестве при исключении каждого другой элемент в перечне, или в любом количестве в сочетании с любым или всеми другими элементами в объединенном перечне, каждый из которых также может присутствовать в любом количестве. Применяя это общее правило, объединяющие выражения в предшествующих примерах, в которых объединенный перечень состоит из X, Y и Z, должны охватывать: один или более из X, один или более из Y, один или более из Z, один или более из X и один или более из Y, один или более из Y и один или более из Z, один или более из X и один или более из Z, а также один или более из X, один или более из Y и один или более из Z.
Различные модификации и добавления можно получить, не отклоняясь от идеи и области защиты этого изобретения. Признаки каждого из различных описанных выше воплощений можно объединять с признаками других описанных воплощений по необходимости с получением множества сочетаний признаков в соответствующих новых воплощениях. Более того, хотя выше описано множество отдельных воплощений, они описаны в данном документе только лишь для иллюстрации применения принципов настоящего изобретения. К тому же, хотя конкретные способы в данном документе можно проиллюстрировать и/или описать как выполняемые в конкретном порядке, данный порядок может сильно изменяться специалистом для достижения аспектов настоящего изобретения. Соответственно, это описание понимают как взятое только для примера и никаким образом не ограничивающее область защиты изобретения.
Приведенные в качестве примера воплощения изложены выше и проиллюстрированы на приложенных чертежах. Специалист должен понимать, что можно выполнить различные изменения, пропуски и добавления к тому, что конкретно изложено в данном документе, не отклоняясь от идеи и области защиты настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА И СПОСОБ ПОЛУЧЕНИЯ ВАНАДИЕВОГО ЭЛЕКТРОЛИТА ВЫСОКОЙ ЧИСТОТЫ | 2017 |
|
RU2691058C1 |
| СИСТЕМА И СПОСОБ ПРОИЗВОДСТВА ВАНАДИЕВОГО ЭЛЕКТРОЛИТА ВЫСОКОЙ ЧИСТОТЫ И ВЫСОКОЙ АКТИВНОСТИ | 2017 |
|
RU2690013C1 |
| СИСТЕМА И СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРОЛИТА ВЫСОКОЙ ЧИСТОТЫ ДЛЯ ВАНАДИЕВОГО АККУМУЛЯТОРА | 2017 |
|
RU2690012C1 |
| ПРОТОЧНАЯ БАТАРЕЯ И РЕГЕНЕРАЦИОННАЯ СИСТЕМА С УЛУЧШЕННОЙ БЕЗОПАСНОСТЬЮ | 2014 |
|
RU2624628C2 |
| СИСТЕМА И СПОСОБ ПОЛУЧЕНИЯ ВАНАДИЕВОГО ЭЛЕКТРОЛИТА ВЫСОКОЙ ЧИСТОТЫ С ВАЛЕНТНОСТЬЮ 3,5 | 2017 |
|
RU2695083C1 |
| Способ измерения средней степени окисления и концентрации ионов ванадия в электролите ванадиевой проточной редокс-батареи и установка для его осуществления | 2022 |
|
RU2817409C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ | 2005 |
|
RU2308125C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЭЛЕКТРОЛИТА ДЛЯ ВАНАДИЕВЫХ РЕДОКС БАТАРЕЙ | 2019 |
|
RU2716148C1 |
| ПРИГОТОВЛЕНИЕ ВАНАДИЕВОГО ЭЛЕКТРОЛИТА С ПОМОЩЬЮ АСИММЕТРИЧНЫХ ЭЛЕКТРОЛИЗЕРОВ ВОССТАНОВЛЕНИЯ ВАНАДИЯ И ИСПОЛЬЗОВАНИЕ АСИММЕТРИЧНОГО ЭЛЕКТРОЛИЗЕРА ВОССТАНОВЛЕНИЯ ВАНАДИЯ ДЛЯ ВОССТАНОВЛЕНИЯ БАЛАНСА СОСТОЯНИЯ ЗАРЯДА ЭЛЕКТРОЛИТОВ РАБОТАЮЩЕЙ ВАНАДИЕВОЙ ВОССТАНОВИТЕЛЬНО-ОКИСЛИТЕЛЬНОЙ БАТАРЕИ | 2000 |
|
RU2251763C2 |
| СПОСОБ ОПРЕСНЕНИЯ И ОЧИСТКИ ВЫСОКОМИНЕРАЛИЗОВАННОЙ ШАХТНОЙ ВОДЫ | 1992 |
|
RU2048449C1 |

Изобретение относится к очистке и получению растворов электролитов. Изобретение направлено на электрохимическую очистку растворов электролитов и связанные с ней системы и способы. Согласно изобретению способы и системы для удаления примесей из растворов электролитов имеют три или более валентных состояния. В некоторых воплощениях способ включает электрохимическое восстановление раствора электролита для понижения его валентного состояния до уровня, при котором происходит осаждение примесей из раствора электролита, и затем фильтрацию осадка(ов) из раствора электролита. В воплощениях, в которых требуется, чтобы раствор электролита находился в более высоком валентном состоянии, чем валентное состояние осаждения, способ включает окисление очищенного раствора электролита до целевой валентности. Техническим результатом является улучшенные эксплуатационные качества батареи, уменьшение загрязнения системы ванадиевой проточной окислительно-восстановительной батареи. 4 н. и 47 з.п. ф-лы, 22 ил., 2 табл.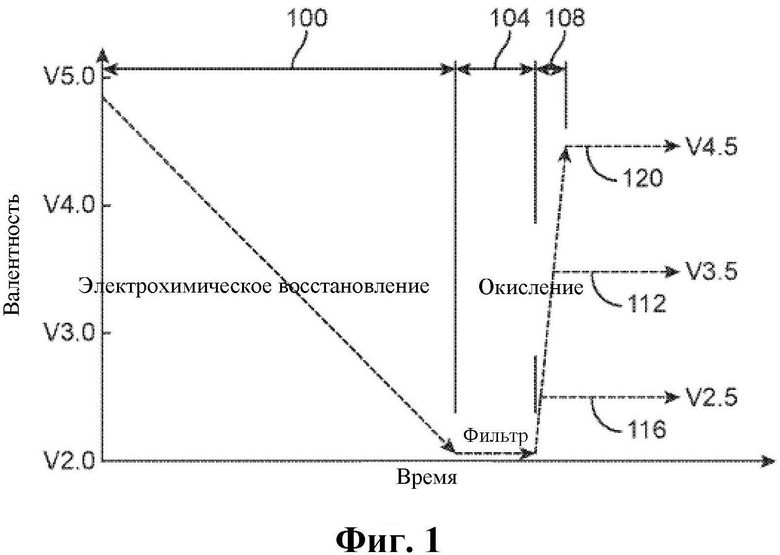
1. Способ получения очищенного раствора электролита, включающий:
предоставление раствора электролита, имеющего валентность осаждения и содержащего по меньшей мере одну примесь, которая осаждается из раствора электролита, когда валентность раствора электролита равна или ниже валентности осаждения,
восстановление раствора электролита до валентности, которая ниже валентности осаждения, чтобы вызвать осаждение по меньшей мере одной примеси из раствора электролита в виде осадка, и
удаление осадка из раствора электролита, чтобы получить очищенный раствор электролита.
2. Способ по п. 1, в котором раствор электролита включает раствор электролита на основе ванадия и восстановление раствора электролита включает восстановление раствора электролита на основе ванадия до валентности менее 3,0.
3. Способ по п. 2, в котором восстановление раствора электролита на основе ванадия до валентности менее 3,0 включает восстановление раствора электролита на основе ванадия до валентности менее 2,5.
4. Способ по п. 2, в котором восстановление раствора электролита на основе ванадия до валентности менее 3,0 включает восстановление раствора электролита на основе ванадия до валентности по существу 2,0.
5. Способ по п. 1, в котором восстановление раствора электролита выполняют с использованием гибридного электрохимического элемента.
6. Способ по п. 5, в котором при восстановлении раствора электролита используют газообразный водород в качестве восстановителя.
7. Способ по п. 1, дополнительно включающий окисление очищенного раствора электролита до требуемой валентности.
8. Способ по п. 7, в котором очищенный раствор электролита включает очищенный раствор электролита на основе ванадия и окисление очищенного раствора электролита включает окисление очищенного электролита на основе ванадия до требуемой валентности.
9. Способ по п. 8, в котором требуемая валентность составляет по существу 3,5.
10. Способ по п. 8, в котором требуемая валентность составляет по существу 4,5.
11. Способ по п. 8, в котором требуемая валентность составляет по существу 2,5.
12. Способ по п. 1, дополнительно включающий окисление очищенного раствора электролита до каждой из двух валентностей, чтобы создать очищенные растворы электролитов с отрегулированной валентностью, имеющие различающуюся валентность.
13. Способ по п. 12, в котором очищенный раствор электролита включает очищенный раствор электролита на основе ванадия и окисление очищенного раствора электролита до каждой из двух валентностей включает окисление первой части очищенного раствора электролита на основе ванадия до валентности более 3,5 и окисление второй части очищенного раствора электролита на основе ванадия до валентности менее 2,5.
14. Способ по п. 13, в котором окисление первой части очищенного раствора электролита на основе ванадия до валентности более 3,5 включает окисление первой части до валентности примерно 4,5 и окисление второй части очищенного раствора электролита на основе ванадия до валентности менее 2,5 включает окисление второй части до валентности примерно 2,5.
15. Способ по п. 12, в котором окисление очищенного раствора электролита выполняют с использованием гибридного электрохимического окислительного элемента.
16. Способ по п. 15, в котором при окислении очищенного раствора электролита используют образование газообразного водорода из протонов.
17. Способ по п. 16, в котором восстановление раствора электролита выполняют с использованием гибридного электрохимического восстановительного элемента.
18. Способ по п. 17, в котором при восстановлении раствора электролита используют газообразный водород, выходящий из гибридного электрохимического окислительного элемента.
19. Способ по п. 12, в котором восстановление раствора электролита и окисление очищенного раствора электролита выполняют с использованием электрохимического элемента только с электролитом, имеющего сторону восстановления и сторону окисления с раствором электролита на стороне восстановления и очищенным раствором электролита на стороне окисления.
20. Способ по п. 19, в котором каждый из раствора электролита и очищенного раствора электролита включает раствор электролита на основе ванадия.
21. Способ по п. 1, в котором предоставление раствора электролита включает предоставление раствора электролита на основе ванадия.
22. Способ по п. 21, в котором весь ванадий в растворе электролита на основе ванадия поступает по существу только из смешивания V2O5 по меньшей мере с одной сильной кислотой.
23. Способ по п. 22, в котором весь ванадий в растворе электролита на основе ванадия поступает по существу от V2O5 и V2O3, смешанных по меньшей мере с одной сильной кислотой.
24. Способ по п. 1, в котором раствор электролита имеет низшую возможную валентность и восстановление раствора электролита включает восстановление раствора электролита примерно до низшей валентности.
25. Способ запуска проточной окислительно-восстановительной батареи, имеющей положительную сторону и отрицательную сторону, включающий:
предоставление раствора электролита, имеющего начальную валентность и по меньшей мере четыре доступных степени окисления, включающих ряд более высоких степеней окисления и ряд более низких степеней окисления,
восстановление раствора электролита до валентности, которая ниже начальной валентности, с получением восстановленного раствора электролита, имеющего валентность в пределах ряда более низких степеней окисления,
окисление первой части восстановленного раствора электролита с получением раствора электролита положительной стороны, имеющего валентность в пределах ряда более высоких степеней окисления,
предоставление для запуска раствора электролита положительной стороны для положительной стороны проточной окислительно-восстановительной батареи и
предоставление для отрицательной стороны проточной окислительно-восстановительной батареи, для запуска, второй части восстановленного раствора электролита в качестве раствора электролита отрицательной стороны, имеющего валентность в пределах ряда более низких степеней окисления.
26. Способ по п. 25, в котором предоставление второй части восстановленного раствора электролита в качестве раствора отрицательной стороны включает окисление второй части для повышения валентности второй части до значения в пределах ряда более низких степеней окисления.
27. Способ по п. 25, дополнительно включающий добавление раствора электролита положительной стороны на положительную сторону проточной окислительно-восстановительной батареи и добавление раствора электролита отрицательной стороны на отрицательную сторону проточной окислительно-восстановительной батареи.
28. Способ по п. 25, в котором проточная окислительно-восстановительная батарея расположена на месте ее применения и способ выполняют на месте применения батареи.
29. Способ по п. 28, в котором раствор электролита содержит электролит, причем способ дополнительно включает получение электролита в сухих формах и предоставление раствора электролита, включающее смешивание электролита с другими материалами с получением раствора электролита.
30. Способ по п. 25, в котором проточная окислительно-восстановительная батарея является ванадиевой проточной окислительно-восстановительной батареей и способ включает:
предоставление раствора электролита на основе ванадия, имеющего начальную валентность,
восстановление раствора электролита до валентности ниже валентности осаждения (примерно 2,5),
окисление первой части восстановленного раствора электролита до валентности выше 4,0 с получением раствора электролита положительной стороны и
окисление второй части восстановленного раствора электролита до валентности ниже 3,0 с получением раствора электролита отрицательной стороны.
31. Способ по п. 30, в котором весь ванадий в растворе электролита на основе ванадия поступает по существу только из смешивания оксида или оксидов ванадия по меньшей мере с одной сильной кислотой.
32. Способ по п. 25, дополнительно включающий, перед окислением, механическое отделение одного или более осадков от восстановленного раствора электролита посредством разделения твердого вещества и жидкости.
33. Система для получения очищенного раствора электролита из раствора электролита, содержащего по меньшей мере одну примесь, которая осаждается из раствора электролита при валентности, равной или ниже валентности осаждения, включающая:
систему восстановления, которая включает:
электрохимический восстановительный элемент, выполненный и предназначенный для электрохимического восстановления раствора электролита с использованием восстановителя,
контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части раствора электролита в электрохимический восстановительный элемент,
систему регулирования способа восстановления в оперативном соединении с системой восстановления, чтобы регулировать валентность раствора электролита в системе восстановления до требуемого значения, равного или ниже валентности осаждения, чтобы вызывать осаждение по меньшей мере одной примеси из раствора электролита в виде осадка, и
систему механического отделения твердого вещества от жидкости, выполненную и предназначенную для удаления по меньшей мере части осадка из раствора электролита с получением очищенного раствора электролита.
34. Система по п. 33, в которой система восстановления является системой непрерывного потока.
35. Система по п. 33, в которой электрохимический восстановительный элемент является гибридным электрохимическим элементом.
36. Система по п. 33, в которой система фильтров содержит фильтр грубой очистки и фильтр тонкой очистки.
37. Система по п. 36, в которой фильтр грубой очистки содержит фильтр из активированного угля.
38. Система по п. 36, в которой фильтр тонкой очистки содержит фильтр с меньшим размером пор, чем у электродов восстановительного элемента и отрицательных электродов системы ВПОВБ.
39. Система по п. 33, в которой раствор электролита может иметь степень окисления от +2 до +5 и система регулирования способа восстановления установлена для поддержания валентности раствора электролита в системе восстановления ниже примерно 3,0.
40. Система по п. 39, в которой система регулирования установлена для поддержания валентности раствора электролита в системе восстановления в ряду значений от 2,0 до 2,9.
41. Система по п. 33, в которой восстановитель включает газообразный водород.
42. Система по п. 33, дополнительно содержащая систему окисления, которая включает:
электрохимический окислительный элемент, выполненный и предназначенный для электрохимического окисления очищенного раствора электролита с использованием окислителя,
контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части очищенного раствора электролита в электрохимический окислительный элемент, и
систему регулирования способа окисления в оперативном соединении с системой окисления, так чтобы регулировать валентность очищенного раствора электролита в системе окисления до требуемого конечного значения.
43. Система по п. 42, в которой окислитель включает образование газообразного водорода из протонов.
44. Система по п. 43, в которой выходящий из электрохимического окислительного элемента поток представляет собой газообразный водород и по меньшей мере часть газообразного водорода подают в электрохимический восстановительный элемент.
45. Система по п. 33, в которой раствор электролита может иметь степень окисления от +2 до +5 и система регулирования способа восстановления установлена для регулирования валентности очищенного раствора электролита так, чтобы выдавать раствор электролита с доведенной до требуемого уровня валентностью.
46. Система по п. 45, в которой требуемая валентность составляет менее 3,0.
47. Система по п. 45, в которой требуемая валентность составляет примерно 3,5.
48. Система по п. 45, в которой требуемая валентность составляет примерно 4,0.
49. Система по п. 33, где система включает электрохимический элемент только с электролитом, который действует в качестве как электрохимического восстановительного элемента, так и электрохимического окислительного элемента.
50. Система по п. 49, в которой электрохимический элемент только с электролитом имеет сторону восстановления и сторону окисления, причем контур рециркуляции системы восстановления соединен по текучей среде со стороной восстановления, а контур рециркуляции системы окисления соединен по текучей среде со стороной окисления.
51. Система получения раствора электролита с регулируемой валентностью из раствора электролита, имеющего по меньшей мере четыре степени окисления, включающая:
систему восстановления, которая включает:
электрохимический восстановительный элемент, выполненный и предназначенный для электрохимического восстановления раствора электролита с использованием восстановителя,
контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части раствора электролита в электрохимический восстановительный элемент,
систему регулирования способа восстановления в оперативном соединении с системой восстановления, чтобы регулировать валентность раствора электролита в системе восстановления до требуемого значения, и
выход, выполненный, предназначенный и расположенный для выпуска раствора электролита в виде предварительно восстановленного раствора электролита при примерно требуемом значении, и
систему окисления, которая включает:
электрохимический окислительный элемент, выполненный и предназначенный для электрохимического окисления ранее восстановленного раствора электролита с использованием окислителя,
контур рециркуляции, выполненный и предназначенный для рециркуляции по меньшей мере части предварительно восстановленного раствора электролита в электрохимический окислительный элемент,
систему регулирования способа окисления в оперативном соединении с системой окисления, чтобы регулировать валентность предварительно восстановленного раствора электролита в системе окисления до требуемого конечного значения, и
выход, выполненный, предназначенный и расположенный для выпуска ранее восстановленного раствора электролита при примерно требуемом конечном значении.
| ПРИГОТОВЛЕНИЕ ВАНАДИЕВОГО ЭЛЕКТРОЛИТА С ПОМОЩЬЮ АСИММЕТРИЧНЫХ ЭЛЕКТРОЛИЗЕРОВ ВОССТАНОВЛЕНИЯ ВАНАДИЯ И ИСПОЛЬЗОВАНИЕ АСИММЕТРИЧНОГО ЭЛЕКТРОЛИЗЕРА ВОССТАНОВЛЕНИЯ ВАНАДИЯ ДЛЯ ВОССТАНОВЛЕНИЯ БАЛАНСА СОСТОЯНИЯ ЗАРЯДА ЭЛЕКТРОЛИТОВ РАБОТАЮЩЕЙ ВАНАДИЕВОЙ ВОССТАНОВИТЕЛЬНО-ОКИСЛИТЕЛЬНОЙ БАТАРЕИ | 2000 |
|
RU2251763C2 |
| СПОСОБ ЭЛЕКТРОЛИТИЧЕСКОГО ОСАЖДЕНИЯ СПЛАВА ЖЕЛЕЗО-ВАНАДИЙ-КОБАЛЬТ | 2009 |
|
RU2401328C1 |
| US 5587132 A, 24.12.1996 | |||
| US2010143781 A1, 10.06.2010. | |||
Авторы
Даты
2019-12-04—Публикация
2017-10-06—Подача