ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
По данной заявке испрашивается приоритет по заявке № 61/661167, поданной 18 июня 2012 года.
ЗАЯВЛЕНИЕ В ОТНОШЕНИИ СПИСКА ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Список последовательностей, связанный с этой заявкой, представлен в текстовом формате вместо бумажной копии и включен, таким образом, в качестве ссылки в настоящее описание. Названием текстового файла, содержащего список последовательностей, является MP_1_0176_PCT_SequenceListingasFiled_20130614.txt, и он подан с помощью EFS-Web с подачей этого описания.
УРОВЕНЬ ТЕХНИКИ
Система комплемента представляет механизм раннего действия для инициирования, усиления и регуляции иммунного ответа на микробную инфекцию и другие острые повреждения (M.K. Liszewski и J.P. Atkinson, 1993, in Fundamental Immunology, Third Edition, edited by W.E. Paul, Raven Press, Ltd., New York) у людей и других позвоночных. Хотя активация комплемента обеспечивает важную защиту первой линии против потенциальных патогенов, активность комплемента, стимулирующего защитный иммунный ответ, также может представлять потенциальную угрозу для хозяина (K.R. Kalli, et al., Springer Semin. Immunopathol. 75:417-431, 1994; B.P. Morgan, Eur. J. Clinical Investig. 24:219-228, 1994). Например, протеолитические продукты C3 и C5 приводят к рекрутированию и активации нейтрофилов. Несмотря на то, что они необходимы для защиты хозяина, активированные нейтрофилы действуют беспорядочно в высвобождении деструктивных ферментов и могут вызывать повреждение органа. Кроме того, активация комплемента может вызывать накопление литических компонентов комплемента на ближайших клетках хозяина, а также на микроорганизмах-мишенях, приводя к лизису клетки хозяина.
Система комплемента также участвует в патогенезе многих острых и хронических заболеваний, включая: инфаркт миокарда, инсульт, ARDS, реперфузионное повреждение, септический шок, повышение проницаемости капилляров после термических ожогов, воспаление после операции с использованием искусственного кровообращения, отторжение трансплантата, ревматоидный артрит, рассеянный склероз, миастению гравис и болезнь Альцгеймера. При большинстве этих состояний комплемент является не причиной, а одним из нескольких факторов, участвующих в патогенезе. Как бы то ни было, активация комплемента может являться основным патологическим механизмом и представлять собой эффективную точку для клинического контроля при многих из этих заболеваний. Растущее понимание важности опосредуемого комплементом повреждения тканей при многих заболеваниях усиливает потребность в эффективных лекарственных средствах, ингибирующих комплемент. К настоящему времени, экулизумаб (Solaris®), антитело против C5, является единственным лекарственным средством, направленным против комплемента, одобренным для использования на людях. Тем не менее, C5 является одной из нескольких эффекторных молекул, расположенных "ниже в каскаде" системы комплемента, и блокада C5 не ингибирует активацию системы комплемента. Таким образом, ингибитор начальных этапов активации комплемента будет иметь значительные преимущества по сравнению с ингибитором "нижележащих в каскаде" компонентов комплемента.
В настоящее время широко признано, что система комплемента может активироваться тремя различными путями: классическим путем, лектиновым путем и альтернативным путем. Как правило, классический путь запускается комплексом, состоящим из антител хозяина, связанных с чужеродной частицей (т.е. антигеном), и, таким образом, для развития специфического гуморального ответа требуется предшествующее воздействие антигена. Поскольку активация классического пути зависит от предшествующего адаптивного иммунного ответа хозяина, классический путь является частью приобретенной иммунной системы. В отличие от этого, и лектиновый, и альтернативный путь не зависят от адаптивного иммунитета и являются частью врожденной иммунной системы.
Активация системы комплемента приводит к последующей активации зимогенов сериновых протеаз. Первым этапом активации классического пути является связывание специфичной распознающей молекулы C1q со связанными с антигеном молекулами IgG и IgM. C1q связан с проферментами сериновых протеаз C1r и C1s, этот комплекс называется C1. После связывания C1q с иммунным комплексом происходит аутопротеолитическое расщепление участка Arg-Ile C1r с последующим опосредованным C1r расщеплением и активацией C1s, который, таким образом, приобретает способность расщеплять C4 и C2. C4 расщепляется на два фрагмента, обозначаемых как C4a и C4b, и, аналогично, C2 расщепляется на C2a и C2b. Фрагменты C4b способны образовывать ковалентные связи со смежными гидроксильными группами или аминогруппами и образовывать конвертазу C3 (C4b2a) посредством нековалентного взаимодействия с фрагментом C2a активированного C2. Конвертаза C3 (C4b2a) активирует C3 посредством протеолитического расщепления на субкомпоненты C3a и C3b, что приводит к образованию конвертазы C5 (C4b2a3b), которая посредством расщепления C5 приводит к образованию мембраноатакующего комплекса (C5b, объединенный с C6, C7, C8 и C9, также обозначаемый как "MAC"), который может разрушать клеточные мембраны, что приводит к лизису клетки. Активированные формы C3 и C4 (C3b и C4b) посредством ковалентных связей накапливаются на поверхностях чужеродных мишеней и распознаются рецепторами комплемента на множестве фагоцитов.
Независимо от этого, первым этапом активации системы комплемента через лектиновый путь также является связывание специфических распознающих молекул, после которого следует активация ассоциированных проферментов сериновых протеаз. Однако, вместо связывания иммунных комплексов C1q, распознающие молекулы лектинового пути содержат группу углевод-связывающих белков (маннозо-связывающий лектин (MBL), H-фиколин, M-фиколин, L-фиколин и лектин C-типа CL-11), в совокупности обозначаемых как лектины. См. J. Lu et al., Biochim. Biophys. Acta 1572:387-400, (2002); Holmskov et al., Annu. Rev. Immunol. 21:547-578 (2003); Teh et al., Immunology 101:225-232 (2000)). See also J. Luet et al., Biochim Biophys Acta 1572:387-400 (2002); Holmskov et al, Annu Rev Immunol 21:547-578 (2003); Teh et al., Immunology 101:225-232 (2000); Hansen et al, J. Immunol 185(10):6096-6104 (2010).
Ikeda et al. впервые продемонстрировали, что, подобно C1q, MBL может активировать систему комплемента после связывания с эритроцитами, покрытыми маннозой дрожжей, C4-зависимым образом (Ikeda et al, J. Biol. Chem. 2(52:7451-7454, (1987)). MBL, член семейства белков коллектинов, является кальций-зависимым лектином, связывающимся с углеводами с 3- и 4-гидроксигруппами, ориентированными в горизонтальной плоскости пиранозного кольца. Таким образом, значимыми лигандами для MBL являются D-манноза и N-ацетил-D-глюкозамин, в то время как углеводы, не удовлетворяющие этому стерическому требованию, имеют неопределяемую аффинность для MBL (Weis et al., Nature 360:127-134, (1992)). Взаимодействие между MBL и моновалентными сахарами является крайне слабым с константами диссоциации, как правило, в однозначном миллимолярном диапазоне. MBL достигает сильного, специфического связывания с гликановыми лигандами посредством авидности, т.е. взаимодействия одновременно с множеством остатком моносахаридов, локализованных в непосредственной близости друг к другу (Lee et al., Archiv. Biochem. Biophys. 299: 129-136, (1992)). MBL распознает углеводные паттерны, как правило, декорирующие микроорганизмы, такие как бактерии, дрожжи, паразиты и определенные вирусы. В отличие от этого, MBL не распознает D-галактозу и сиаловую кислоту, предпоследние и последние сахара, как правило, входящие в "зрелые" сложные гликоконъюгаты, присутствующие на гликопротеинах поверхностей клеточной мембраны млекопитающих. Считают, что эта специфичность связывания способствует распознаванию "чужеродных" поверхностей и помогает защищать от "аутоактивации". Однако MBL не связывается с высокой активностью с кластерами богатых маннозой "предшественником" гликанов на N-связанных гликопротеинах и гликолипидах, изолированных в эндоплазматической сети и аппарате Гольджи клеток млекопитающих (Maynard et al., J. Biol. Chem. 257:3788-3794, (1982)). Кроме того, показано, что MBL может связываться с полинуклеотидами, ДНК и РНК, которые могут быть экспонированы на некротических и апоптотических клетках (Palaniyar et al, Ann. N.Y. Acad. ScL, 1010:467-470 (2003); Nakamura et al, J. Leuk. Biol. 86:737-748 (2009)). Таким образом, поврежденные клетки являются потенциальными мишенями для активации через лектиновый путь посредством связывания с MBL.
Фиколины содержат иной тип лектинового домена, чем MBL, называемый фибриногеноподобным доменом. Фиколины связываются с остатками сахаров Ca++-независимым образом. У людей идентифицировали три типа фиколинов (L-фиколин, M-фиколин и H-фиколин). Два фиколина в сыворотке, L-фиколин и H-фиколин, обладают общей специфичностью для N-ацетил-D-глюкозамина; однако, H-фиколин также связывается с N-ацетил-D-галактозамином. Различие в специфичности к сахарам L-фиколина, H-фиколина, CL-11 и MBL означает, что различные лектины могут являться взаимодополняющими и воздействовать на различные гликоконъюгаты благодаря перекрыванию. Эту концепцию подтверждают в недавней статье о том, что из известных лектинов лектинового пути только L-фиколин специфически связывается с липотейхоевой кислотой, гликоконъюгатом клеточной стенки, обнаруживаемым на всех грамположительных бактериях (Lynch et al., J. Immunol. 772: 1198-1202, (2004)). В дополнение к ацетилированным остаткам сахаров фиколины также могут связываться с ацетилированными аминокислотами и полипептидами (Thomsen et al, Mol. Immunol. 48(4):369-81 (2011)). Коллектины (т.е. MBL) и фиколины не имеют значительной схожести аминокислотной последовательности. Однако две группы белков имеют схожую организацию доменов и, как C1q, собираются в олигомерные структуры, максимизирующие их способность к мультисайтовому связыванию.
Концентрации MBL в сыворотке сильно варьируются в популяциях здоровых индивидуумов и генетически контролируются полиморфизмами/мутациями в промоторе и кодирующих областях гена MBL. Экспрессия MBL, как белка острой фазы, дополнительно повышающе регулируется при воспалении. L-фиколин присутствует в сыворотке в концентрациях, аналогичных MBL. Таким образом, L-фиколиновая ветвь лектинового пути потенциально сравнима с MBL по своей силе. MBL и фиколины также функционируют как опсонины, позволяющие фагоцитам воздействовать на MBL- и фиколин-декорированные поверхности (см. Jack et al, J Leukoc Biol., 77(3):328-36 (2004), Matsushita and Fujita, Immunobiology, 205(4-5):490-7 (2002), Aoyagi et al, J Immunol, 174(1):418-25(2005). Для этой опсонизации необходимо взаимодействие этих белков с рецепторами фагоцитов (Kuhlman et al, J. Exp. Med. 169: 1733, (1989); Matsushita et al, J. Biol. Chem. 277:2448-54, (1996)), идентичность которых не установлена.
MBL человека осуществляет специфичное и высокоаффинное взаимодействие через свой коллагеноподобный домен с уникальными C1r/C1s-подобными сериновыми протеазами, называемыми MBL-ассоциированными сериновыми протеазами (MASP). К настоящему моменту описано три MASP. Впервые, отдельный фермент "MASP" идентифицировали и охарактеризовали как фермент, ответственный за инициацию каскада комплемента (т.е. расщепление C2 и C4) (Matsushita et al., J Exp Med 176(6): 1497-1502 (1992); Ji et al, J. Immunol. 750:571-578, (1993)). Затем определили, что активность MASP фактически представлена смесью двух протеаз: MASP-1 и MASP-2 (Thiel et al, Nature 556:506-510, (1997)). Однако было показано, что комплекса MBL-MASP-2 в отдельности достаточно для активации комплемента (Vorup-Jensen et al, J. Immunol. 7(55:2093-2100, (2000)). Кроме того, только MASP-2 расщепляет C2 и C4 с высокой скоростью (Ambrus et al, J. Immunol. 770: 1374-1382, (2003)). Таким образом, MASP-2 является протеазой, ответственной за активацию C4 и C2 для образования конвертазы C3 C4b2a. Это является существенным отличием от комплекса C1 классического пути, где координированное действие двух специфичных сериновых протеаз (C1r и C1s) приводит к активации системы комплемента. Кроме того, выделена третья новая протеаза, MASP-3 (Dahl, M.R., et al, Immunity 75: 127-35, 2001). MASP-1 и MASP-3 являются продуктами альтернативного сплайсинга одного гена.
MASP имеют организацию доменов, идентичную C1r и C1s, ферментативным компонентам комплекса C1 (Sim et al., Biochem. Soc. Trans. 25:545, (2000)). Эти домены включают N-концевой домен C1r/C1s/VEGF морского ежа/морфогенетического белка кости (CUB), домен, подобный эпидермальному фактору роста, второй CUB домен, тандем доменов контролирующих комплемент белков и домен сериновой протеазы. Как и у протеаз C1, активация MASP-2 происходит посредством расщепления связи Arg-Ile, смежной с доменом сериновой протеазы, разделяющего фермент на связанные дисульфидной связью цепи A и B, последняя из которых состоит из домена сериновой протеазы.
MBL также может связываться с альтернативно сплайсированной формой MASP-2, известной как MBL-ассоциированный белок массой 19 кДа (MAp19) или малый MBL-ассоциированный белок (sMAP), у которого отсутствует каталитическая активность MASP-2. (Stover, J. Immunol. 7(52:3481-90, (1999); Takahashi et al, Int. Immunol. 77:859-863, (1999)). MAp19 содержит первые два домена MASP-2, за которыми следует дополнительная последовательность из четырех уникальных аминокислот. Функция MAp19 неясна (Degn et al., J Immunol. Methods, 2011). Гены MASP-1 и MASP-2 локализуются на хромосомах 3 и 1 человека, соответственно (Schwaeble et al, Immunobiology 205:455-466, (2002)).
Несколько линий доказательств позволяют предполагать, что существуют различные комплексы MBL-MASP, и большая фракция MASP в сыворотке не образует комплексы с MBL (Thiel, et al., J. Immunol. 7(55:878-887, (2000)). H- и L-фиколин связываются со всеми MASP и активируют лектиновый путь комплемента, как и MBL (Dahl et al., Immunity 75: 127-35, (2001); Matsushita et al., J. Immunol. 765:3502-3506, (2002)). И лектиновый, и классический путь приводят к образованию общей конвертазы C3 (C4b2a), и на этом этапе два пути пересекаются.
Распространено мнение, что лектиновый путь играет основную роль в защите против инфекции у наивного хозяина. Убедительное доказательство участия MBL в защите хозяина получено с помощью анализа пациентов со сниженными уровнями функционального MBL в сыворотке (Kilpatrick, Biochim. Biophys. Acta 7572:401-413, (2002)). Такие пациенты проявляют предрасположенность к рецидивирующим бактериальным и грибковым инфекциям. Эти симптомы, как правило, проявляются в начале жизни в течение выраженного "окна уязвимости" со снижением титров материнских антител, но до возникновения полного репертуара гуморальных ответов. Этот синдром часто является результатом мутаций в нескольких участках коллагеновой части MBL, мешающих правильному образованию олигомеров MBL. Однако, т.к. MBL может функционировать как опсонин независимо от комплемента, неизвестно, в какой мере повышается восприимчивость к инфекции по причине нарушенной активации комплемента.
Ранее показано, что в отличие от классического и лектинового путей, инициаторы альтернативного пути выполняют распознающие функции, которые C1q и лектины осуществляют в двух других путях. В настоящее время широко признано, что альтернативный путь спонтанно подвергается низкоуровневой циклической активации, которая может быстро повышаться в ответ на чужеродные или другие аномальные поверхности (бактерии, дрожжи, инфицированные вирусами клетки или поврежденную ткань) и в которой отсутствуют соответствующие молекулярные элементы, контролирующие спонтанную активацию комплемента. В сыворотке существуют четыре белка, напрямую участвующие в активации альтернативного пути: C3, факторы B и D и пропердин.
Хотя существует большое количество данных о вовлечении и классического, и альтернативного путей комплемента в патогенез неинфекционных заболеваний человека, роль лектинового пути только начинают оценивать. Недавние исследования показали, что активация лектинового пути может отвечать за активацию комплемента и связанное с ней воспаление при ишемическом/реперфузионном повреждении. Collard et al. (2000) показали, что культивируемые эндотелиальные клетки, подвергнутые оксидативному стрессу, связываются с MBL и демонстрируют накопление C3 после воздействия сывороткой человека (Collard et al, Am. J. Pathol. 75(5: 1549-1556, (2000)). Кроме того, обработка сывороток человека блокирующими моноклональными антителами против MBL ингибировала связывание MBL и активацию комплемента. Эти данные переносили на модель ишемии-реперфузии миокарда у крысы, в которой крысы, обработанные блокирующим антителом против MBL, демонстрировали значимо меньшее повреждение миокарда после окклюзии коронарной артерии, чем крысы, обработанные контрольным антителом (Jordan et al., Circulation 704: 1413-1418, (2001)). Молекулярный механизм связывания MBL с эндотелием сосудов после оксидативного стресса неясен; недавние исследования позволили предполагать, что активацию лектинового пути после оксидативного стресса может опосредовать связывание MBL с цитокератинами эндотелия сосудов, и а не с гликоконъюгатами (Collard et al., Am. J. Pathol. 159:1045-1054, (2001)). В других исследованиях делали вывод о вовлечении классического и альтернативного путей в патогенез ишемического/реперфузионного повреждения, и роль лектинового пути в этом заболевании остается спорной (Riedermann, N.C., et al., Am. J. Pathol. 162:363-361, 2003).
В недавних исследованиях показали, что MASP-1 и MASP-3 конвертируют фермент активации альтернативного пути фактор D из его зимогена в ферментативно активную форму (см. Takahashi M. et al., J Exp Med 207(1):29-37 (2010); Iwaki et al., J. Immunol. 187:3751-58 (2011)). Физиологическую значимость этого процесса подчеркивает отсутствие функциональной активности альтернативного пути в плазме мышей с дефицитом MASP-1/3. Протеолитическое образование C3b из нативного C3 необходимо для функционирования альтернативного пути. Поскольку конвертаза C3 (C3bBb) альтернативного пути содержит C3b в качестве необходимой субъединицы, вопрос об образовании первого C3b через альтернативный путь представляет сложную проблему и стимулирует обширные исследования.
C3 принадлежит к семейству белков (вместе с C4 и α-2 макроглобулином), содержащих редкую посттрансляционную модификацию, известную как тиоэфирная связь. Тиоэфирная группа состоит из глутамина, терминальная карбонильная группа которого образует ковалентную тиоэфирную связь с сульфгидрильной группой цистеина, расположенного в трех аминокислотах от него. Эта связь является нестабильной, и электрофильный глутамил-тиоэфир может реагировать с нуклеофильными остатками, такими как гидроксильная группа или аминогруппа, и, таким образом, образовывать ковалентную связь с другими молекулами. Тиоэфирная связь является вполне стабильной при секвестрации в гидрофобном кармане интактного C3. Однако протеолитическое расщепление C3 до C3a и C3b приводит к экспонированию тиоэфирной связи с высокой реакционной активностью на C3b и, после нуклеофильной атаки смежными остатками, содержащими гидроксильную группу или аминогруппу, C3b становится ковалентно связанным с мишенью. В дополнение к его убедительно подтвержденной роли в ковалентном присоединении C3b к мишеням комплемента, также считают, что тиоэфир C3 играет ключевую роль в запуске альтернативного пути. Согласно широко распространенной "теории tick-over", альтернативный путь инициируется образованием конвертазы жидкой фазы, iC3Bb, образующейся из C3 с гидролизованным тиоэфиром (iC3; C3(H2O)) и фактора B (Lachmann, P.J., et al, Springer Semin. Immunopathol. 7:143-162, (1984)). C3b-подобный C3(H2O) образуется из нативного C3 посредством медленного спонтанного гидролиза внутреннего тиоэфира в белке (Pangburn, M.K., et al., J. Exp. Med. 754:856-867, 1981). Несмотря на активность конвертазы C3(H2O)Bb, молекулы C3b накапливаются на поверхности мишени, таким образом, инициируя альтернативный путь.
До настоящего открытия, представленного в настоящем описании, об инициаторах активации альтернативного пути было известно очень мало. Считали, что активаторы включают клеточную стенку дрожжей (зимозан), многие чистые полисахариды, эритроциты кролика, определенные иммуноглобулины, вирусы, грибки, бактерии, опухолевые клетки животных, паразитов и поврежденные клетки. Единственным свойством, общим для этих активаторов, являлось наличие углевода, но сложность и многообразие структур углеводов затрудняло обнаружение распознаваемых общих молекулярных детерминант. Было общепризнанным, что активация альтернативного пути контролируется точным балансом между ингибиторными регуляторными компонентами этого пути, такими как фактор H, фактор I, DAF и CR1, и пропердином, последний из которых является единственным положительным регулятором альтернативного пути (см. Schwaeble W.J. and Reid K.B., Immunol Today 20(1): 17-21 (1999)).
В дополнение к, по-видимому, нерегулируемому механизму активации, описываемому выше, альтернативный путь также может обеспечивать мощную амплификационную петлю для конвертазы C3 лектинового/классического пути (C4b2a), т.к. любая образующаяся C3b может участвовать вместе с фактором B в образовании дополнительной конвертазы C3 альтернативного пути (C3bBb). Конвертазу C3 альтернативного пути стабилизирует связывание с пропердином. Пропердин повышает время полужизни конвертазы C3 альтернативного пути в шесть-десять раз. Добавление C3b к конвертазе C3 альтернативного пути приводит к образованию конвертазы C5 альтернативного пути.
Считают, что все три пути (т.е. классический, лектиновый и альтернативный) перекрываются через C5, расщепляемый для образования продуктов с многочисленными провоспалительными эффектами. Конвергентный путь обозначили как терминальный путь комплемента. C5a является наиболее сильным анафилотоксином, вызывающим изменения в гладких мышцах и тонусе сосудов, а также проницаемости сосудов. Он также является сильным хемотаксином и активатором нейтрофилов и моноцитов. Опосредованная C5a клеточная активация может значительно усиливать воспалительные ответы посредством индуцирования высвобождения многочисленных дополнительных медиаторов воспаления, включая цитокины, гидролитические ферменты, метаболиты арахидоновой кислоты и активные формы кислорода. Расщепление C5 приводит к образованию C5b-9, также известного как мембраноатакующий комплекс (MAC). В настоящее время существует убедительное доказательство того, что сублитическое накопление MAC может играть важную роль в воспалении в дополнение к его роли в качестве литического порообразующего комплекса.
В дополнение к ее важной роли в иммунной защите, система комплемента участвует в повреждении ткани при многих заболеваниях. Таким образом, существует острая необходимость разработки терапевтически эффективных ингибиторов комплемента для профилактики этих неблагоприятных воздействий.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном из аспектов настоящее изобретение относится к способу ингибирования MASP-3-зависимой активации комплемента у индивидуума, страдающего пароксизмальной ночной гемоглобинурией (PNH), возрастной дегенерацией желтого пятна (AMD), повреждением при ишемии-реперфузии, артритом, синдромом диссеминированного внутрисосудистого свертывания, тромботической микроангиопатией, астмой, болезнью плотного депозита, слабоиммунным некротизирующим гломерулонефритом с полулуниями, травматическим повреждением головного мозга, аспирационной пневмонией, эндофтальмитом, нейромиелитом зрительного нерва или болезнью Бехчета. Способ включает этап введения индивидууму композиции, содержащей количество средства, ингибирующего MASP-3, эффективное для ингибирования MASP-3-зависимой активации комплемента. В некоторых вариантах осуществления способ дополнительно включает введение индивидууму композиции, содержащей средство, ингибирующее MASP-2.
В другом аспекте настоящее изобретение относится к способу ингибирования MASP-2-зависимой активации комплемента у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета. Способ включает этап введения индивидууму композиции, содержащей количество средства, ингибирующего MASP-2, эффективное для ингибирования MASP-2-зависимой активации комплемента. В некоторых вариантах осуществления средство, ингибирующее MASP-2, является моноклональным антителом против MASP-2 или его фрагментом, специфически связывающимся с частью SEQ ID NO: 5. В некоторых вариантах осуществления антитело против MASP-2 является химерным, гуманизированным или человеческим антителом.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей по меньшей мере одно ингибирующее средство, где по меньшей мере одно ингибирующее средство содержит средство, ингибирующее MASP-2, и средство, ингибирующее MASP-3, и фармацевтически приемлемый носитель.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей средство, ингибирующее MASP-3, связывающееся с частью MASP-1 (полноразмерной SEQ ID NO: 10), а также связывающееся с частью MASP-3 (SEQ ID NO: 8), и фармацевтический носитель.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей средство, ингибирующее MASP-3, связывающееся с частью MASP-2 (полноразмерной SEQ ID NO: 5), а также связывающееся с частью MASP-3 (SEQ ID NO: 8), и фармацевтический носитель.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей средство, ингибирующее MASP-3, связывающееся с частью MASP-1 (полноразмерной SEQ ID NO: 10), а также связывающееся с частью MASP-2 (SEQ ID NO: 5), и фармацевтический носитель.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей средство, ингибирующее MASP-3, связывающееся с частью MASP-1 (полноразмерной SEQ ID NO: 10), связывающееся с частью MASP-2 (полноразмерной SEQ ID NO: 5), а также связывающееся с частью MASP-3 (SEQ ID NO: 8), и фармацевтический носитель.
В другом аспекте настоящее изобретение относится к способу производства лекарственного средства для применения в ингибировании эффектов MASP-3-зависимой активации комплемента у нуждающихся в этом живых индивидуумов, включающему комбинирование терапевтически эффективного количества средства, ингибирующего MASP-3, в фармацевтическом носителе. В некоторых вариантах осуществления способ по этому аспекту настоящего изобретения включает производство лекарственного средства для применения в ингибировании эффектов MASP-3-зависимой активации комплемента у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, синдрома диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии, астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета. В некоторых вариантах осуществления способ дополнительно включает комбинирование терапевтически эффективного количества средства, ингибирующего MASP-2, в лекарственном средстве, содержащем ингибитор MASP-3, или вместе с ним.
В другом аспекте настоящее изобретение относится к способу производства лекарственного средства для применения в ингибировании эффектов MASP-2-зависимой активации комплемента у нуждающихся в этом живых индивидуумов, включающему комбинирование терапевтически эффективного количества средства, ингибирующего MASP-2, в фармацевтическом носителе. В некоторых вариантах осуществления способ по этому аспекту настоящего изобретения включает производство лекарственного средства для применения в ингибировании эффектов MASP-2-зависимой активации комплемента у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета. В некоторых вариантах осуществления способ дополнительно включает комбинирование терапевтически эффективного количества средства, ингибирующего MASP-3, в лекарственном средстве, содержащем ингибитор MASP-2, или вместе с ним.
Как представлено в настоящем описании, в фармацевтических композициях по настоящему изобретению можно использовать различные варианты средств, ингибирующих MASP-3, и/или различные варианты средств, ингибирующих MASP-2.
Как представлено в настоящем описании, фармацевтические композиции по изобретению можно использовать в соответствии со способами по изобретению.
Эти и другие аспекты и варианты осуществления представленного в настоящем описании изобретения станут очевидными с учетом следующего подробного описания и чертежей. Все патенты США, публикации патентных заявок США, патентные заявки США, иностранные патенты, иностранные патентные заявки и непатентные публикации, цитируемые в настоящем описании, включены в настоящее описание в качестве ссылок в полном объеме, как если бы каждая из них была включена по отдельности.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Следующие аспекты и многие из сопутствующих преимуществ настоящего изобретения станут более понятными с учетом следующего подробного описания в комбинации с сопутствующими чертежами, где:
На фигуре 1 представлено новое понимание лектинового и альтернативного путей;
Фигура 2 является схемой, взятой из Schwaeble et al., Immunobiol 205:455-466 (2002), модифицированной в Yongqing et al, BBA 1824:253 (2012), на которой представлены белковые домены MASP-2 и MAp19 и кодирующие их экзоны;
Фигура 3 является схемой, взятой из Schwaeble et al., Immunobiol 205:455-466 (2002), модифицированной в Yongqing et al, BBA 1824:253 (2012), на которой представлены белковые домены MASP-1, MASP-3 и MAp44 и кодирующие их экзоны;
На фигуре 4 показано выравнивание аминокислотных последовательностей белков MASP-1, MASP-2 и MASP-3 и консенсусных областей между ними;
На фигуре 5 показано выравнивание аминокислотных последовательностей альфа-цепей MASP-1, MASP-2 и MASP-3;
На фигуре 6 показано выравнивание аминокислотных последовательностей бета-цепей MASP-1, MASP-2 и MASP-3;
На фигуре 7A показано попарное выравнивание аминокислотных последовательностей протеазных доменов MASP-1 и MASP-2 (бета-цепей);
На фигуре 7B показано попарное выравнивание аминокислотных последовательностей протеазных доменов MASP-1 и MASP-3 (бета-цепей);
На фигуре 7C оказано попарное выравнивание аминокислотных последовательностей протеазных доменов MASP-2 и MASP-3 (бета-цепей);
Фигура 8 представляет собой график Каплана-Мейера, на котором показан процент выживаемости мышей MASP-2 KO и WT после введения инфицирующей дозы 2,6×107 КОЕ N. meningitidis серогруппы A Z2491, свидетельствующий о том, что мыши с дефицитом MASP-2 защищены от вызванной N. meningitidis гибели, как описано в примере 1;
Фигура 9 представляет собой график Каплана-Мейера, на котором показан процент выживаемости мышей MASP-2 KO и WT после введения инфицирующей дозы 6×106 КОЕ N. meningitidis серогруппы B штамма MC58, свидетельствующий о том, что мыши с дефицитом MASP-2 защищены от вызванной N. meningitidis гибели, как описано в примере 1;
На фигуре 10 представлен график логарифма КОЕ/мл N. meningitidis серогруппы B штамма MC58 на мл крови, взятой у мышей MASP-2 KO и WT в разные моменты времени после i.p.-инфицирования 6×106 КОЕ N. meningitidis серогруппы B штамма MC58 (n=3 в разные моменты времени для обеих групп мышей), свидетельствующий о том, что, хотя мышей MASP-2 KO инфицировали той же дозой N. meningitidis серогруппы B штамма MC58, что и мышей WT, мыши MASP-2 KO имели повышений клиренс бактериемии по сравнению с WT, как описано в примере 1;
На фигуре 11 графически представлен индекс заболеваемости мышей MASP-2 KO и WT через 3, 6, 12 и 24 часов после инфицирования 6×106 КОЕ N. meningitidis серогруппы B штамма MC58, свидетельствующий о том, что мыши с дефицитом MASP-2 демонстрируют гораздо меньший индекс заболеваемости через 6 часов, 12 часов и 24 часов после инфицирования по сравнению с мышами WT, как описано в примере 1;
Фигура 12 представляет собой график Каплана-Мейера, на котором показан процент выживаемости мышей после введения инфицирующей дозы 4×106 КОЕ N. meningitidis серогруппы B штамма MC58 с последующим через 3 часа после инфицирования введением антитела, ингибирующего MASP-2, (1 мг/кг) или контрольного изотипического антитела, свидетельствующий о том, что антитело против MASP-2 эффективно в лечении и улучшает выживаемость у индивидуумов, инфицированных N. meningitidis, как описано в примере 2;
На фигуре 13 представлен график логарифма КОЕ/мл жизнеспособных N. meningitidis серогруппы B штамма MC58, выделенных в разные моменты времени из образцов сывороток человека, представленных в таблице 5, взятых в различные моменты времени после инкубации N. meningitidis серогруппы B штамма MC58, как описано в примере 3;
На фигуре 14 представлен график логарифма КОЕ/мл жизнеспособных N. meningitidis серогруппы B-MC58, выделенных в разные моменты времени из образцов сывороток человека, представленных в таблице 7, свидетельствующий о том, что комплемент-зависимая гибель N. meningitidis в 20% (об./об.) сыворотке человека является MASP-3- и MBL-зависимой, как описано в примере 3;
На фигуре 15 представлен график логарифма КОЕ/мл жизнеспособных N. meningitidis серогруппы B-MC58, выделенных в разные моменты времени из образцов сывороток мышей, представленных в таблице 9, свидетельствующий о том, что сыворотка нокаутных по MASP-2-/- мышей (обозначаемых как "MASP-2-/-") имеет более высокие уровни бактерицидной активности в отношении N. meningitidis, чем сыворотка мышей WT, одновременно, в отличие от этого, сыворотка мышей MASP-1/3-/- не имеет бактерицидной активности, как описано в примере 3;
На фигуре 16 графически представлена кинетика активации C3 в специфичных для лектинового пути условиях (1% плазма) в сыворотках мышей WT, C4-/-, MASP-1/3-/-, фактор B-/- и MASP-2-/-, как описано в примере 4;
На фигуре 17 графически представлен уровень запускаемого альтернативным путем (AP-запускаемого) накопления C3b на покрытых зимозаном планшетах для микротитрования в "традиционных" специфичных для альтернативного пути (AP-специфичных) условиях (т.е. BBS/EGTA/Mg++ без Ca++) как функция концентрации в образцах сыворотки, полученных от людей с дефицитом MASP-3, дефицитом C4 и дефицитом MBL, как описано в примере 4;
На фигуре 18 графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования в "традиционных" AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) как функция времени в образцах 10% сыворотки человека, полученных от людей с дефицитом MASP-3, дефицитом C4 и дефицитом MBL, как описано в примере 4;
На фигуре 19A графически представлен уровень накопления C3b на покрытых маннозой планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных от мышей WT, мышей с дефицитом MASP-2 и дефицитом MASP-1/3, в "традиционных" AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (AP) (BBS/Mg++/Ca++), как описано в примере 4;
На фигуре 19B графически представлен уровень накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных от мышей WT, мышей с дефицитом MASP-2 и дефицитом MASP-1/3, в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), как описано в примере 4;
На фигуре 19C графически представлен уровень накопления C3b на покрытых S. pneumoniae D39 планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных от мышей WT, мышей с дефицитом MASP-2 и дефицитом MASP-1/3, в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), как описано в примере 4;
На фигуре 20A графически представлены результаты анализа накопления C3b в сильно разведенных сыворотках, проведенного на покрытых маннозой планшетах для микротитрования в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), с использованием концентраций сыворотки в диапазоне от 0% до 1,25%, как описано в примере 4;
На фигуре 20B графически представлены результаты анализа накопления C3b, проведенного на покрытых зимозаном планшетах для микротитрования в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), с использованием концентраций сыворотки в диапазоне от 0% до 1,25%, как описано в примере 4;
На фигуре 20С графически представлены результаты анализа накопления C3b, проведенного на покрытых S. pneumoniae D39 планшетах для микротитрования в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), с использованием концентраций сыворотки в диапазоне от 0% до 1,25%, как описано в примере 4;
На фигуре 21 графически представлен уровень гемолиза (измеряемого с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши (Crry/C3-/-) в супернатант) покрытых маннозой эритроцитов мыши сывороткой человека в физиологических условиях (т.е. в присутствие Ca++) в диапазоне разведений сыворотки MASP-3-/-, термически инактивированной нормальной сыворотки человека (HI NHS), MBL-/-, NHS + моноклональное антитело против MASP-2 и контроля NHS, как описано в примере 5;
На фигуре 22 графически представлен уровень гемолиза (измеряемого с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши (Crry/C3-/-) в супернатант) покрытых маннозой эритроцитов мыши сывороткой человека в физиологических условиях (т.е. в присутствие Ca++) в диапазоне концентраций сыворотки MASP-3-/-, термически инактивированной (HI) NHS, MBL-/-, NHS + моноклональное антитело MASP-2 и контроля NHS, как описано в примере 5;
На фигуре 23 графически представлен уровень гемолиза (измеряемого с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши WT в супернатант) непокрытых эритроцитов мыши сывороткой человека в физиологических условиях (т.е. в присутствие Ca++) в диапазоне концентраций сыворотки пациента с 3MC (MASP-3-/-), термически инактивированной (HI) NHS, MBL-/-, NHS + моноклональное антитело MASP-2 и контроля NHS, как описано в примере 5;
На Фигура 24 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши (CD55/59-/-) в супернатант) непокрытых эритроцитов мыши сывороткой человека в физиологических условиях (т.е. в присутствие Ca++) в диапазоне концентраций термически инактивированной сыворотки (HI) NHS, MBL-/-, NHS + моноклональное антитело MASP-2 и контроля NHS, как описано в примере 5;
На фигуре 25 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами кролика в супернатант) покрытых маннозой эритроцитов кролика сывороткой мыши MASP-1/3-/- и контрольной сывороткой мыши WT в физиологических условиях (т.е. в присутствие Ca++) в диапазоне концентраций сыворотки, как описано в примере 6;
На фигуре 26 графически представлен уровень накопления C3b (OD при 405 нм) на покрытом зимозаном планшете для микротитрования как функция концентрации в образцах сывороток мышей с фактором D-/-, MASP-2-/- и мышей WT в анализе накопления C3, проведенного в AP-специфичных условиях, как описано в примере 7;
На фигуре 27 графически представлен уровень накопления C3b (OD при 405 нм) на покрытом зимозаном планшете для микротитрования как функция концентрации в образцах сыворотки мышей с фактором D-/-; MASP-2-/- и мышей WT в анализе накопления C3, проведенного в физиологических условиях (в присутствие Ca++), как описано в примере 7;
На фигуре 28 графически представлен уровень накопления C3b (OD при 405 нм) на покрытом зимозаном планшете для микротитрования как функция времени инкубации сыворотки (мин) в образцах сыворотки мыши, полученных из мышей с фактором D-/-; фактором B-/-; с моноклональным антителом против MASP-2 и без него в анализе накопления C3b, проведенном в физиологических условиях (в присутствие Ca++), как описано в примере 7;
На фигуре 29A графически представлено специфическое для лектинового пути накопление C4b на покрытом зимозаном планшете для микротитрования, измеряемое ex vivo в неразведенных образцах сыворотки, взятых из мышей (n=3 мышей/группу) в различные моменты времени после подкожного введения 0,3 мг/кг или 1,0 мг MoAb против MASP-2/кг массы тела мыши, как описано в примере 13;
На фигуре 29B графически представлена динамика восстановления лектинового пути в течение трех недель после однократного интраперитонеального введения мыши MoAb против MASP-2 в концентрации 0,6 мг/кг массы тела мыши, как описано в примере 13;
Фигура 30A представляет собой диаграмму FACS для связывания антиген MASP-3/антитело в случае клона M3J5, как описано в примере 15;
Фигура 30B представляет собой диаграмму FACS для связывания антиген MASP-3/антитело в случае клона M3M1, как описано в примере 15;
На фигуре 31 графически представлена кривая насыщения связывания клона M3J5 (клона 5) для антигена MASP-3, как описано в примере 15;
На фигуре 32A представлено выравнивание аминокислотных последовательностей областей VH M3J5, M3M1, D14 и 1E10 с последовательностью DT40 VH курицы, где точками указана идентичность аминокислот с последовательностью DT40 и пунктиром указано пространство, внесенное для максимизации выравнивания, как описано в примере 15;
На фигуре 32B представлено выравнивание аминокислотных последовательностей областей VL M3J5, M3M1, D14 и 1E10 с последовательностью DT40 VL курицы, где точками указана идентичность аминокислот с последовательностью DT40 и пунктиром указано пространство, внесенное для максимизации выравнивания, как описано в примере 15;
Фигура 33 представляет собой столбчатую диаграмму, на которой показана ингибиторная активность mAb1E10 в Wieslab Complement System Screen, MBL Pathway по сравнению с положительной сывороткой, поставляемой вместе с набором для анализа, а также изотипическим контрольным антителом, свидетельствующую о том, что mAb1E10 частично ингибирует LEA-2-зависимую активацию (посредством ингибирования MASP-1-зависимой активации MASP-2), а изотипическое контрольное антитело - нет, как описано в примере 15;
На фигуре 34 графически представлен уровень накопления C3b для 1% нормальной сыворотки человека с изотипическим контролем, SGMI-1Fc или SGMI-2Fc в диапазоне концентраций от 0,15 до 1000 нМ, свидетельствующий о том, что SGMI-1Fc и SGMI-2Fc ингибируют накопление C3b из нормальной сыворотки в покрытых маннозой лунках планшета для ELISA со значениями IC50 приблизительно 27 нМ и 300 нМ, соответственно, как описано в примере 16;
На фигуре 35A представлены результаты анализа проточной цитометрии для накопления C3b на убитых нагреванием Staphylococcus aureus, свидетельствующие о том, что в нормальной сыворотке человека в присутствие ЭДТА, которая, как известно, инактивирует лектиновый и альтернативный пути, не наблюдали накопление C3b (панель 1), в нормальной сыворотке человека, обработанной Mg++/EGTA, наблюдали запускаемое альтернативным путем накопление C3b (панель 2), и, как показано на панелях 3, 4 и 5, в сыворотке без фактора B, без фактора D и без пропердина (фактора P), соответственно, не наблюдали запускаемого альтернативным путем накопления C3b, как описано в примере 17;
На фигуре 35B представлены результаты анализа проточной цитометрии для накопления C3b на убитых нагреванием S. aureus, свидетельствующие о том, что, как и в обработанной ЭДТА нормальной сыворотке (панель 1), AP-запускаемое накопление C3b отсутствует в сыворотке пациента с 3MC в присутствие Mg++/EGTA (панель 3), в то время как на панелях 4 и 5 показано, что активная полноразмерная rMASP-3 (панель 4) и активная rMASP-3 (CCP1-CCP2-SP) (панель 5), обе, восстанавливают AP-запускаемое накопление C3b в сыворотке пациента с 3MC до уровней, наблюдаемых в нормальной сыворотке, обработанной Mg++/EGTA (панель 2), ни неактивная rMASP-3 (S679A) (панель 6), ни rMASP-1 дикого типа (панель 7) не могли восстановить AP-запускаемое накопление C3b в сыворотке пациента с 3MC, как описано в примере 17;
На фигуре 36 представлены результаты анализа вестерн-блоттинга для определения расщепления фактора B в ответ на S. aureus в сыворотке пациента с 3MC в присутствие или отсутствие rMASP-3, свидетельствующие о том, что нормальная сыворотка человека в присутствие ЭДТА (отрицательный контроль, линия 1) проявляет очень низкое расщепление фактора B относительно нормальной сыворотки человека в присутствие Mg++/EGTA, показанной в линии 2 (положительный контроль), как дополнительно показано в линии 3, сыворотка пациента с 3MC проявляет очень низкое расщепление фактора B в присутствие Mg++/EGTA. Однако, как показано в линии 4, расщепление фактора B восстанавливали добавлением в сыворотку пациента с 3MC полноразмерного, рекомбинантного белка MASP-3 и преинкубацией, как описано в примере 17;
На фигуре 37 показано окрашивание кумаси белкового геля, в котором анализировали расщепление фактора B, свидетельствующее о том, что расщепление фактора B является наиболее оптимальным в присутствие C3, MASP-3 и про-фактора D (линия 1), и, как показано в линиях 4 и 5, MASP-3 или про-фактор D в отдельности способны опосредовать расщепление фактора B при условии наличия C3, как описано в примере 17;
На фигуре 38 графически представлены средние интенсивности флуоресценции (MFI) при окрашивании C3b на S. aureus, получаемые с помощью mAbD14 (связывающегося с MASP-3), mAb1A5 (антитела отрицательного контроля) и изотипического контрольного антитела, графики которых построены как функция концентрации mAb в сыворотке пациента с 3MC в присутствие rMASP-3, свидетельствующие о том, что mAbD14 ингибирует MASP-3-зависимое накопление C3b в зависимости от концентрации, как описано в примере 17;
На фигуре 39 представлен анализ вестерн-блоттинга расщепления субстрата про-фактора D, где сравниваемый с про-фактором D в отдельности (линия 1) или неактивной полноразмерной рекомбинантной MASP-3 (S679A; линия 3) или MASP-1 (S646A; линия 4), полноразмерная рекомбинантная MASP-3 дикого типа (линия 2) и MASP-1 (линия 5) полностью или частично расщепляют про-фактор D с образованием зрелого фактора D, как описано в примере 18;
Фигура 40 представляет собой анализ вестерн-блоттинга, на котором показана ингибиторная активность связывающих MASP-3 mAb D14 (линия 2) и M3M1 (линия 3) в отношении MASP-3-зависимого расщепления про-фактора D по сравнению с контрольной реакционной смесью, содержащей только MASP-3 и про-фактор D (без mAb, линия 1), а также контрольной реакционной смесью, содержащей mAb, полученное из библиотеки DTLacO, связывающее MASP-1, но не MASP-3 (линия 4), как описано в примере 18;
На фигуре 41 графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных индивидуумов с дефицитом MASP-3 (3MC), дефицитом C4 и дефицитом MBL, свидетельствующий о том, что сыворотки без MASP-3 от пациента №2 и пациента №3 имеют остаточную активность AP при высоких концентрациях сыворотки (концентрации сыворотки 25%, 12,5%, 6,25%), но значимо более высокий AP50 (т.е. 8,2% и 12,3% сыворотки необходимо для достижения 50% от максимального накопления C3), как описано в примере 19;
На фигуре 42A графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования в "традиционных" AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) как функция времени в образцах 10% сыворотки человека, полученных от людей с дефицитом MASP-3, дефицитом C4 и дефицитом MBL, как описано в примере 19;
На фигуре 42B представлен вестерн-блоттинг с использованием плазмы, полученной от пациента №2 с 3MC (MASP-3(-/-), MASP-1(+/+)), пациента №3 с 3MC (MASP-3(-/-), MASP-1(-/-)) и сывороток нормальных доноров (W), где про-фактор D человека (25040 Да) и/или зрелый фактор D (24405 Да) определяли с использованием антитела против фактора D человека, как описано в примере 19;
На фигуре 42C графически представлены результаты анализов Weislab классического, лектинового и альтернативного путей с использованием плазмы, полученной от пациента №2 с 3MC, пациента №3 с 3MC, и нормальной сыворотки человека, как описано в примере 19;
На фигуре 43 графически представлен процент гемолиза (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами кролика в супернатант) покрытых маннозой эритроцитов кролика в диапазоне концентраций сыворотки от двух нормальных людей (NHS) и двух пациентов с 3MC (пациента №2 и пациента №3), измеряемого в отсутствие Ca++, свидетельствующий о том, что дефицит MASP-3 снижает процентную долю опосредованного комплементом лизиса покрытых маннозой эритроцитов по сравнению с нормальной сывороткой человека, как описано в примере 19;
На фигуре 44 графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации рекомбинантного полноразмерного белка MASP-3, добавляемого в образцы сыворотки, получаемые от пациента №2 с 3MC (MASP-3-/-), свидетельствующий о том, что, по сравнению с неактивной рекомбинантной MASP-3 отрицательного контроля (MASP-3A; S679A), активный рекомбинантный белок MASP-3 восстанавливает AP-запускаемое накопление C3b на покрытых зимозаном планшетах в зависимости от концентрации, как описано в примере 19;
На фигуре 45 графически представлен процент гемолиза (измеряемого с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами кролика в супернатант) покрытых маннозой эритроцитов кролика в диапазоне концентраций (1) нормальной сыворотки человека (NHS); (2) сыворотке пациента с 3MC; (3) сыворотке пациента с 3MC с активной полноразмерной рекомбинантной MASP-3 (20 мкг/мл); и (4) термически инактивированной сыворотки человека (HIS), измеряемый в отсутствие Ca++, свидетельствующий о том, что процент лизиса эритроцитов кролика значимо повышается в сыворотке пациента с 3MC, содержащей rMASP-3, по сравнению с процентом лизиса в сыворотке пациента с 3MC без рекомбинантной MASP-3 (p=0,0006), как описано в примере 19;
На фигуре 46 графически представлен процент лизиса эритроцитов кролика в 7% сыворотке человека от пациента №2 с 3MC и пациента №3 с 3MC, содержащей активную рекомбинантную MASP-3 в диапазоне концентраций от 0 до 110 мкг/мл (в BBS/Mg++/EGTA, свидетельствующий о том, что процент лизиса эритроцитов кролика повышается с повышением количества рекомбинантной MASP-3 в зависимости от концентрации, как описано в примере 19; и
На фигуре 47 графически представлен уровень LEA-2-запускаемого накопления C3b на покрытых маннозой планшетах для ELISA как функция концентрации сыворотки человека, разведенной в буфере BBS, для нормальной сыворотки человека (NHS), сывороток двух пациентов с 3MC (пациента №2 и пациента №3), родителей пациента №3 и индивидуума с дефицитом MBL.
На фигуре 48A представлены результаты, демонстрирующие исходные уровни белка VEGF в комплексах RPE-хориоидеа, выделенных из мышей дикого типа (WT) (+/+) и MASP-2(-/-), как описано в примере 20;
На фигуре 48B представлены результаты, демонстрирующие уровни белка VEGF в комплексах RPE-хориоидеа в день 3 у мышей (WT) (+/+) и MASP-2(-/-) после лазер-индуцированного повреждения в модели дегенерации желтого пятна, как описано в примере 20;
На фигуре 49 представлены результаты, демонстрирующие средний объем хороидальной неоваскуляризации (CNV) у мышей (WT) (+/+) и MASP-2(-/-) в день 7 после лазер-индуцированного повреждения, как описано в примере 20;
На фигуре 50 представлена средняя площадь хороидальной неоваскуляризации (CNV) в день 7 после лазер-индуцированного повреждения у мышей (WT) (+/+), которым предварительно проводили одну i.p.-инъекцию 0,3 мг/кг или 1,0 мг/кг моноклонального антитела против MASP-2 мыши, как описано в примере 21;
На фигуре 51A представлены результаты, демонстрирующие размер области инфаркта у мышей (WT) (+/+) и сниженный размер области инфаркта у мышей MASP-2(-/-) после повреждения в модели окклюзии коронарных артерий и реперфузии, как описано в примере 22;
На фигуре 51B представлены результаты, демонстрирующие распределение отдельных животных, тестируемых в модели окклюзии коронарных артерий и реперфузии, как описано в примере 22;
На фигуре 52A графически представлены средняя область риска (AAR) и объемы инфарктов (INF) в виде процентной доли общего объема миокарда у мышей (WT) (+/+) и MASP-2(-/-) после окклюзии левой передней нисходящей коронарной артерии и реперфузии, как описано в примере 23;
На фигуре 52B графически представлен объем инфаркта (INF), график которого построен в зависимости от средней площади области риска (AAR), в виде процентной доли объема миокарда левого желудочка у мышей (WT) (+/+) и MASP-2(-/-) после окклюзии артерии и реперфузии, как описано в примере 23;
На фигуре 52C графически представлен объем инфаркта (INF) в перфузируемых буфером сердцах мышей (WT) (+/+) и MASP-2(-/-), полученных согласно модели изолированного сердца мыши по Лангендорфу, в которых глобальную ишемию и реперфузию осуществляли в отсутствие сыворотки, как описано в примере 23;
На фигуре 52D графически представлена взаимосвязь объема инфаркта (INF) и зоны риска (RZ) в перфузируемых буфером сердцах мышей (WT) (+/+) и MASP-2(-/-),полученных согласно модели изолированного сердца мыши по Лангендорфу, как описано в примере 23;
На фигуре 53A графически представлены результаты анализа накопления C3b на покрытых иммунными комплексами планшетах, где символом "*" указывают сыворотку мыши WT (MASP-2(+/+)); символом "•" указывают сыворотку мыши WT (с истощением C1q); символом "□" указывают сыворотку мыши MASP-2(-/-); и символом "Δ" указывают сыворотку мыши MASP-2(-/-) (с истощением C1q), свидетельствующие о том, что у мышей MASP-2(-/-) сохраняется функциональный классический путь, как описано в примере 24;
На фигуре 53B графически представлены результаты анализа накопления C3b на покрытых зимозаном планшетах, где символом "*" указывают сыворотку мыши WT (MASP-2(+/+)), и символом "□" указывают сыворотку мыши MASP-2(-/-); свидетельствующие о том, что у мышей MASP-2(-/-) сохраняется функциональный альтернативный путь, как описано в примере 24;
На фигуре 54A графически представлена утрата ткани, индуцированная повреждением при ишемии миокарда/реперфузии (MIRI), после наложения лигатуры на левую переднюю нисходящую ветвь коронарной артерии (LAD) и реперфузии у мышей C4(-/-) (n=6) и совпадающих однопометных контролей WT (n=7), где показана площадь области риска (AAR) и размер инфаркта (INF), как описано в примере 24;
На фигуре 54B графически представлен размер инфаркта (INF) как функция площади области риска (AAR) у мышей C4(-/-) и WT, обработанных, как представлено на фигуре 42A, свидетельствующий о том, что мыши C4(-/-) также восприимчивы к MIRI, как контроли WT (пунктирная линия), как описано в примере 24;
На фигуре 55A графически представлены результаты анализа накопления C3b с использованием сыворотки мышей WT, мышей C4(-/-) и сыворотки мышей C4(-/-), предварительно инкубированной с маннозой, как описано в примере 24;
На фигуре 55B графически представлены результаты анализа накопления C3b с использованием сыворотки мышей WT, C4(-/-) и MASP-2(-/-), смешанной с различными концентрациями mAb против MASP-2 мыши (mAbM11), как описано в примере 24;
На фигуре 55C графически представлены результаты анализа накопления C3b с использованием сыворотки человека от индивидуумов WT (с достаточным C4) и с дефицитом C4 и сыворотки индивидуумов с дефицитом C4, предварительно инкубированной с маннозой, как описано в примере 24;
На фигуре 55D графически представлены результаты анализа накопления C3b с использованием сыворотки человека от индивидуумов WT (с достаточным C4) и с дефицитом C4, смешанной с mAb против MASP-2 человека (mAbH3), как описано в примере 24;
На фигуре 56A графически представлен сравнительный анализ активности конвертазы C3 в плазме мышей различных линий с дефицитом комплемента, тестируемых в условиях, специфичных для активации лектинового пути, или условиях, специфичных для активации классического пути, как описано в примере 24;
На фигуре 56B графически представлена временная кинетика активности конвертазы C3 в плазме мышей различных линий с дефицитом комплемента, тестируемых в условиях, специфичных для активации лектинового пути, как описано в примере 24;
На фигуре 57A графически представлена степень повреждения ткани у мышей WT и MASP-2(-/-) после индукции повреждения при транзиторной ишемии/реперфузии в желудочно-кишечном тракте (GIRI), где показано, что мыши MASP-2(-/-) обладают значительной степенью защиты по сравнению с контролями WT, как описано в примере 25;
На фигуре 57B графически показаны результаты анализа накопления C4b, осуществляемого с использованием сыворотки, полученной из мышей (n=3) в течение периода времени после интраперитонеальной болюсной инъекции однократной дозы рекомбинантного антитела против MASP-2 мыши (mAbM11), свидетельствующие об абляции функциональной активности лектинового пути in vivo, как описано в примере 25;
На фигуре 57C графически представлен эффект обработки mAb против MASP-2 в отношении тяжести патологии GIRI, свидетельствующий о том, что у мышей, которым вводили mAb против MASP-2 мыши (mAbM11) за 24 часа до подвергания повреждению при транзиторной ишемии/реперфузии в желудочно-кишечном тракте (GIRI), наблюдали значимо сниженное повреждение ткани по сравнению с мышами, которым вводили физиологический раствор (*p<0,05 при сравнении животных, обработанных антителом mAbM11, ингибирующим MASP-2, или неродственным изотипическим контрольным антителом), как описано в примере 25;
На фигуре 57D представлена гистологическая картина GIRI-опосредованной патологии тонкого кишечника у мышей, которым предварительно, за 12 часов до индукции GIRI, делали интраперитонеальную инъекцию однократной дозы физиологического раствора, изотипического контрольного антитела или рекомбинантного антитела против MASP-2 мыши (mAbM11), как описано в примере 25;
На фигуре 58 графически представлен объем ишемического инсульта у мышей WT (MASP-2(+/+)) и MASP-2(-/-) после 30 минут ишемии и 24 часов реперфузии, как описано в примере 26;
На фигуре 59A представлена серия фотографий окрашенных срезов мозга мыши WT (MASP-2(+/+)) через 30 минут ишемии и 24 часов реперфузии. На панелях 1-8 фигуры 52A показаны различные области срезов мозга, соответствующие точке Брегма 1-8, соответственно, в отношении выхода слухового нерва (точка Брегма 0), как описано в примере 26;
На фигуре 59B представлена серия фотографий окрашенных срезов мозга мыши MASP-2(-/-) через 30 минут ишемии и 24 часов реперфузии. На панелях 1-8 фигуры 52B показаны различные области срезов мозга, соответствующие точке Брегма 1-8, соответственно, в отношении выхода слухового нерва (точка Брегма 0), как описано в примере 26;
На фигуре 60 показаны результаты, представляющие средние баллы по клинической шкале артрита у мышей (WT) (+/+) и MASP-2 (-/-) с течением времени после развития ревматоидного артрита, индуцированного mAb против Col2, как описано в примере 27;
На фигуре 61 графически представлены результаты анализа накопления C3 в образцах сыворотки, полученной из мышей WT, в присутствие клеща домашней пыли или зимозана, как описано в примере 28;
На фигурах 62A и 62B представлены кривые дозозависимого ответа для ингибирования накопления C4b (фиг. 62A) и ингибирования активации тромбина после введения антитела Fab2 против MASP-2 (H1) в нормальной сыворотке крысы, как описано в примере 29;
На фигурах 63A и 63B представлена измеряемая агрегация тромбоцитов (выраженная как площадь агрегата) у мышей MASP-2(-/-) (фиг. 63B) по сравнению с агрегацией тромбоцитов у необработанных мышей дикого типа и мышей дикого типа, у которых путь комплемента ингибировали с помощью истощающего средства фактора яда кобры (CVF) и ингибитора терминального пути (антагониста C5aR) (фигура 63A) в модели локализованного феномена Санарелли-Шварцмана диссеминированного внутрисосудистого свертывания, как описано в примере 30;
На фигуре 64 представлены результаты анализа вестерн-блоттинга, демонстрирующие активацию C3 человека, наблюдаемую по наличию а'-цепи, субстратами тромбина FXIa и FXa, как описано в примере 31;
На фигуре 65 графически представлены результаты анализа накопления C3b в образцах сыворотки, полученных из мышей WT, MASP-2(-/-), F11(-/), F11(-/-)/C4(-/-) и C4(-/-), свидетельствующие о том, что функциональный лектиновый путь существует даже при полном отсутствии C4 или F11, в то время как у мышей с комбинированным дефицитом F11(-/-)/C4(-/-) функциональный лектиновый путь отсутствует, как описано в примере 31;
На фигуре 66 графически представлено время до начала микрососудистой окклюзии после инъекции LPS мышам MASP-2-/- и WT, где показана процентная доля мышей с образованием тромбов, измеряемым в течение 60 минут, свидетельствующая о том, что у мышей WT образование тромбов определяют через 15 минут, при этом до 80% мышей WT демонстрируют образование тромбов через 60 минут; в отличие от этого, ни у одной из мышей MASP-2-/- не наблюдали какого-либо образования тромбов в течение 60 минут (логарифмический ранговый критерий: p=0,0005), как описано в примере 32;
На фигуре 67 графически представлен процент выживаемости контрольных мышей, которым вводили физиологический раствор, (n=5) и мышей, которым вводили антитело против MASP-2, (n=5) в модели STX/LPS-индуцированного HUS с течением времени (часы), свидетельствующий о том, что все контрольные мыши умирали к 42 часам, в то время как 100% мышей, которым вводили антитело против MASP-2, выживали в течение эксперимента, как описано в примере 33;
На фигуре 68 в качестве функции времени после индукции повреждения графически представлена процентная доля мышей с микрососудистой окклюзией в модели FITC/декстран-УФ после обработки изотипическим контрольным антителом или антителом против MASP-2 человека mAbH6 (10 мг/кг), вводимым за 16 часов и 1 час до инъекции FITC/декстрана, как описано в примере 34;
На фигуре 69 графически представлено время окклюзии в минутах в случае мышей, которым вводили антитело против MASP-2 человека (mAbH6) или изотипическое контрольное антитело, где данные представлены как рассеянные точки со средними значениями (горизонтальные линии) и среднеквадратическими ошибками (вертикальные линии). Статистическим тестом, используемым для анализа, являлся двухвыборочный t-критерий Стьюдента для независимых выборок; где символом "*" указывают p=0,0129, как описано в примере 34;
На фигуре 70 графически представлено время до наступления окклюзии в минутах для мышей дикого типа, мышей MASP-2 KO и мышей дикого типа, которым предварительно вводили антитело против MASP-2 человека (mAbH6) i.p. в дозе 10 мг/кг за 16 часов и снова за 1 час до индукции тромбоза в модели тромбоза при индуцированном FITC-декстраном/светом повреждении клеток эндотелия с низкой интенсивностью света (800-1500), как описано в примере 34.
ОПИСАНИЕ СПИСКА ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO: 1 - кДНК MAp19 человека
SEQ ID NO: 2 - белок MAp19 человека (с лидерной последовательностью)
SEQ ID NO: 3 - белок MAp19 человека (зрелый)
SEQ ID NO: 4 - кДНК MASP-2 человека
SEQ ID NO: 5 - белок MASP-2 человека (с лидерной последовательностью)
SEQ ID NO: 6 - белок MASP-2 человека (зрелый)
SEQ ID NO: 7 - кДНК MASP-3 человека
SEQ ID NO: 8 - белок MASP-3 человека (с лидерной последовательностью)
SEQ ID NO: 9 - кДНК MASP-1 человека
SEQ ID NO: 10 - белок MASP-1 человека (с лидерной последовательностью)
SEQ ID NO: 11 - белок MAp44 человека (с лидерной последовательностью)
SEQ ID NO: 12 - кДНК MASP-2 крысы
SEQ ID NO: 13 - белок MASP-2 крысы (с лидерной последовательностью)
SEQ ID NO: 14 - ДНК, кодирующая вариабельную область тяжелой цепи (VH) 17D20_dc35VH21N11VL (OMS646) (без сигнального пептида)
SEQ ID NO: 15 - полипептид вариабельной области тяжелой цепи (VH) 17D20_dc35VH21N11VL (OMS646)
SEQ ID NO: 16 - полипептид вариабельной области тяжелой цепи (VH) 17N16mc
SEQ ID NO: 17 - полипептид вариабельной области легкой цепи (VL) 17D20_dc21N11VL (OMS644)
SEQ ID NO: 18 - ДНК, кодирующая вариабельную область легкой цепи (VL) 17N16_dc17N9 (OMS641) (без сигнального пептида)
SEQ ID NO: 19 - полипептид вариабельной области легкой цепи (VL) 17N16_dc17N9 (OMS641)
SEQ ID NO: 20 - полноразмерный полипептид дочернего клона scFv 17N16m_d17N9
SEQ ID NO: 21 - полноразмерный полипептид дочернего клона scFv 17D20m_d3521N11
SEQ ID NO: 22 - ДНК дочернего клона scFv 17N16m_d17N9, кодирующая полноразмерный полипептид (без сигнального пептида)
SEQ ID NO: 23 - ДНК дочернего клона scFv 17D20m_d3521N11, кодирующая полноразмерный полипептид (без сигнального пептида)
SEQ ID NO: 24 - полипептид вариабельной области тяжелой цепи (VH) родительского DTLacO
SEQ ID NO: 25 - полипептид вариабельной области тяжелой цепи (VH) MASP-3-специфичного клона M3J5
SEQ ID NO: 26 - полипептид вариабельной области тяжелой цепи (VH) MASP-3-специфичного клона M3M1
SEQ ID NO: 27 - полипептид вариабельной области легкой цепи (VL) родительского DTLacO
SEQ ID NO: 28 - полипептид вариабельной области легкой цепи (VL) MASP-3-специфичного клона M3J5
SEQ ID NO: 29 - полипептид вариабельной области легкой цепи (VL) MASP-3-специфичного клона M3M1
SEQ ID NO: 30 - полипептид вариабельной области тяжелой цепи (VH) MASP-3-специфичного клона D14
SEQ ID NO: 31 - полипептид вариабельной области легкой цепи (VL) MASP-3-специфичного клона D14
SEQ ID NO: 32 - полипептид вариабельной области тяжелой цепи (VH) MASP-1-специфичного клона 1E10
SEQ ID NO: 33 - полипептид вариабельной области легкой цепи (VL) MASP-1-специфичного клона 1E10
SEQ ID NO: 34 - пептид SGMI-1
SEQ ID NO: 35 - пептид SGMI-2
SEQ ID NO: 36 - полипептид IgG1-Fc человека;
SEQ ID NO: 37 - пептидный линкер #1 (12 а/к);
SEQ ID NO: 38 - пептидный линкер #2 (10 а/к);
SEQ ID NO: 39 - нуклеиновая кислота, кодирующая слитый полипептид, содержащий сигнальную последовательность IL-2 человека, SGMI-1, линкер #1 и IgG1-Fc человека;
SEQ ID NO: 40 - зрелый слитый полипептид, содержащий SGMI-1, линкер #1 и IgG1-Fc человека (SGMI-1Fc);
SEQ ID NO: 41 - нуклеиновая кислота, кодирующая слитый полипептид, содержащий человеческую. сигнальную последовательность IL-2, SGMI-2, линкер #1 и IgG1-Fc человека;
SEQ ID NO: 42 - зрелый слитый полипептид, содержащий SGMI-2, линкер #1 и IgG1-Fc человека (SGMI-2Fc).
ПОДРОБНОЕ ОПИСАНИЕ
I. ОПРЕДЕЛЕНИЯ
Если в настоящем описании не указано иначе, все термины, используемые в настоящем описании, обладают тем значением, которое будет понятно специалистам в области, к которой принадлежит настоящее изобретение. Следующие определения представлены для обеспечения ясности в отношении терминов, т.к. их используют в описании и формуле изобретения для описания настоящего изобретения.
Как применяют в настоящем описании, термин "эффекторная ветвь лектинового пути 1" ("LEA-1") относится к лектин-зависимой активации фактора B и фактора D с помощью MASP-3.
Как применяют в настоящем описании, термин "эффекторная ветвь лектинового пути 2" ("LEA-2") относится к MASP-2-зависимой активации комплемента.
Как применяют в настоящем описании, термин "MASP-3-зависимая активация комплемента" включает два компонента: (i) лектиновую MASP-3-зависимую активацию фактора B и фактора D, включенную в опосредованную LEA-1 активацию комплемента, происходящую в присутствие Ca++, как правило, приводящую к конвертации C3bB в C3bBb и про-фактора D в фактор D; и (ii) лектин-независимую конвертацию фактора B и фактора D, которая может происходить в отсутствие Ca++, как правило, приводящую к конвертации C3bB в C3bBb и про-фактора D в фактор D. Определено, что опосредованная LEA-1 активация комплемента и лектин-независимая конвертация фактора B и фактора D вызывают опсонизацию и/или лизис. Без желания быть связанными какой-либо конкретной теорией, полагают, что только когда многочисленные молекулы C3b ассоциируются и связываются в непосредственной близости, конвертаза C3 C3bBb изменяет их субстратную специфичность и расщепляет C5, как конвертаза C5 альтернативного пути, называемая C3bBb(C3b)n.
Как применяют в настоящем описании, термин "MASP-2-зависимая активация комплемента", также обозначаемая в настоящем описании как опосредованная LEA-2 активация комплемента, включает MASP-2- и лектин-зависимую активацию, происходящую в присутствие Ca++, приводящую к образованию конвертазы C3 лектинового пути C4b2a и после накопления продукта расщепления C3 C3b после конвертазы C5 C4b2a(C3b)n, что, как определено, вызывает опсонизацию и/или лизис.
Как применяют в настоящем описании, термин "традиционное понимание альтернативного пути", также обозначаемый как "традиционный альтернативный путь", относится к альтернативному пути до настоящего открытия, представленного в настоящем описании, т.е. активации комплемента, запускаемой, например, зимозаном клеточной стенки грибов и дрожжей, липополисахаридом (LPS) внешних мембран грамотрицательных бактерий и эритроцитами кролика, а также многими чистыми полисахаридами, вирусами, бактериями, опухолевыми клетками животных, паразитами и поврежденными клетками, и, как общепринято считают, возникающей при спонтанном протеолитическом образовании C3b из фактора комплемента C3. Как применяют в настоящем описании, активацию "традиционного альтернативного пути", также обозначаемого в настоящем описании как "альтернативный путь", измеряют в буфере Mg++/EGTA (т.е. в отсутствие Ca++).
Как применяют в настоящем описании, термин "лектиновый путь" относится к активации комплемента, происходящей посредством специфического связывания сывороточных и несывороточных углевод-связывающих белков, включая маннозо-связывающий лектин (MBL), CL-11 и фиколины (H-фиколин, M-фиколин, или L-фиколин). Как представлено в настоящем описании, авторы настоящего изобретения обнаружили, что лектиновый путь запускается двумя эффекторными ветвями, эффекторной ветвью лектинового пути 1 (LEA-1), которая, как теперь известно, является MASP-3-зависимой, и эффекторной ветвью лектинового пути 2 (LEA-2), являющейся MASP-2-зависимой. Как применяют в настоящем описании, активацию лектиновых путей оценивают с использованием Ca++-содержащих буферов.
Как применяют в настоящем описании, термин "классический путь" относится к активации комплемента, запускаемой антителом, связанным с чужеродной частицей и нуждающейся в связывании распознающей молекулы C1q.
Как применяют в настоящем описании, термин "HTRA-1" относится к сериновой пептидазе A1 из семейства высокотемпературных сериновых протеаз.
Как применяют в настоящем описании, термин "средство, ингибирующее MASP-3" относится к любому средству, прямо или косвенно ингибирующему MASP-3-зависимую активацию комплемента, включая средства, связывающиеся или напрямую взаимодействующие с MASP-3, включая антитела против MASP-3 и их MASP-3-связывающие фрагменты, природные и синтетические пептиды, конкурентные субстраты, низкомолекулярные соединения, ингибиторы экспрессии и выделенные природные ингибиторы, и также включает пептиды, конкурирующие с MASP-3 за связывание с другой распознающей молекулой (например, MBL, CL-11, H-фиколином, M-фиколином или L-фиколином) в лектиновом пути. В одном из вариантов осуществления средство, ингибирующие MASP-3, является специфичным для MASP-3 и не связывается с MASP-1 или MASP-2. Ингибирующее средство, прямо ингибирующее MASP-3, можно обозначать как прямое средство, ингибирующее MASP-3 (например, антитело против MASP-3), в то время как ингибирующее средство, косвенно ингибирующее MASP-3, можно обозначать как непрямое средство, ингибирующее MASP-3 (например, антитело против MASP-1, ингибирующее активацию MASP-3). Примером прямого средства, ингибирующего MASP-3, является специфическое средство, ингибирующее MASP-3, такое как средство, ингибирующее MASP-3, специфически связывающееся с частью MASP-3 (SEQ ID NO: 8) с аффинностью связывания по меньшей мере в 10 выше, чем с другими компонентами системы комплемента. В одном из вариантов осуществления средство, ингибирующее MASP-3, косвенно ингибирует активность MASP-3, такое как, например, ингибитор активации MASP-3, включая ингибитор опосредованной MASP-1 активации MASP-3 (например, антитело против MASP-1 или его MASP-1-связывающие фрагменты, природные и синтетические пептиды, низкомолекулярные соединения, ингибиторы экспрессии и выделенные природные ингибиторы, и также включает пептиды, конкурирующие с MASP-1 за связывание с MASP-3). В другом варианте осуществления средство, ингибирующее MASP-3, ингибирует опосредованное MASP-3 созревание фактора D. В другом варианте осуществления средство, ингибирующее MASP-3, ингибирует опосредованную MASP-3 активацию фактора B. Средства, ингибирующие MASP-3, применимые в способе по изобретению, могут снижать MASP-3-зависимую активацию комплемента более чем на 10%, например, более чем на 20%, более чем на 50% или более чем на 90%. В одном из вариантов осуществления средство, ингибирующее MASP-3, снижает MASP-3-зависимую активацию комплемента более чем на 90% (т.е. приводит к MASP-3-зависимой активации комплемента только на 10% или менее). Ожидают, что ингибирование MASP-3 будет полностью или частично блокировать связанный с LEA-1 лизис и опсонизацию и лектин-независимую конвертацию фактора B и связанный с фактором D лизис и опсонизацию.
Как применяют в настоящем описании, термин "средство, ингибирующее MASP-1" относится к любому средству, связывающемуся или прямо взаимодействующему с MASP-1 и ингибирующему по меньшей мере одно из (i) MASP-3-зависимой активации комплемента, и/или (ii) MASP-2-зависимой активации комплемента, и/или (iii) лектин-независимого или лектин-зависимого опосредованного MASP-1 созревания фактора D, где MASP-1- и лектин-зависимое созревание фактора D включает прямую активацию фактора D, включая антитела против MASP-1 и их MASP-1-связывающие фрагменты, природные и синтетические пептиды, низкомолекулярные соединения, ингибиторы экспрессии и выделенные природные ингибиторы, и также включает пептиды, конкурирующие с MASP-1 за связывания с другой распознающей молекулой (например, MBL, CL-11, H-фиколином, M-фиколином или L-фиколином) в лектиновом пути. В одном из вариантов осуществления средства, ингибирующие MASP-1, применимые в способе по изобретению, снижают MASP-3-зависимую активацию комплемента более чем на 10%, например, более чем на 20%, более чем на 50% или более чем на 90%. В одном из вариантов осуществления средство, ингибирующее MASP-1, снижает MASP-3-зависимую активацию комплемента более чем на 90% (т.е. приводит к MASP-3-зависимой активации комплемента только на 10% или менее). В другом варианте осуществления средства, ингибирующие MASP-1, применимые в способе по изобретению, снижают MASP-2-зависимую активацию комплемента более чем на 10%, например, более чем на 20%, более чем на 50% или более чем на 90%. В одном из вариантов осуществления средство, ингибирующее MASP-1, снижает MASP-2-зависимую активацию комплемента более чем на 90% (т.е. приводит к MASP-2-зависимой активации комплемента только на 10% или менее).
В другом варианте осуществления средства, ингибирующие MASP-1, применимые в способе по изобретению, снижают MASP-3-зависимую активацию комплемента (LEA-1), лектин-независимую конвертацию фактора B и фактора D и MASP-2-зависимую активацию комплемента (LEA-2) более чем на 10%, например, более чем на 20%, более чем на 50% или более чем на 90%. В одном из вариантов осуществления средство, ингибирующее MASP-1, снижает MASP-3-зависимую активацию комплемента (LEA-1), лектин-независимую конвертацию фактора B и фактора D и MASP-2-зависимую активацию комплемента (LEA-2) более чем на 90% (т.е. приводит к MASP-3-зависимой активации комплемента только на 10% или менее и MASP-2-зависимой активации комплемента только на 10% или менее).
Примером прямого средства, ингибирующего MASP-1, является MASP-1-специфичное ингибирующее средство, такое как средство, ингибирующее MASP-1, специфически связывающееся с частью MASP-1 (SEQ ID NO: 10) с аффинностью связывания по меньшей мере в 10 раз выше, чем с другими компонентами системы комплемента. Во многих случаях, учитывая то, что MASP-1 может активировать MASP-3, и то, что MASP-1 может активировать MASP-2, ожидают, что ингибирование MASP-1 будет эффективным в ингибировании MASP-3 и/или MASP-2. Однако, в некоторых случаях ингибирование MASP-1, или MASP-3, или MASP-2 может являться предпочтительным вариантом осуществления относительно ингибирования других мишеней MASP. Например, показано, что в условиях инфекции Staphylococcus aureus (S. aureus) MASP-3 активируется и отвечает за опсонизацию S. aureus в отсутствие MASP-1 (см. Iwaki D. et al., J Immunol 187(7):3751-8 (2011)). Таким образом, в лечении пароксизмальной ночной гемоглобинурии (PNH), например, предпочтительным может являться прямое ингибирование MASP-1, а не MASP-3, таким образом, снижающее потенциальную восприимчивость к S. aureus при ингибирующем LEA-1 лечении PNH.
Как применяют в настоящем описании, термин "средство, ингибирующее MASP-2" относится к любому средству, связывающемуся или напрямую взаимодействующему с MASP-2 и ингибирующему по меньшей мере одно из (i) MASP-2-зависимой активации комплемента и/или (ii) MASP-1-зависимой активации комплемента, включая антитела против MASP-2 и их MASP-2-связывающие фрагменты, природные и синтетические пептиды, низкомолекулярные соединения, ингибиторы экспрессии и выделенные природные ингибиторы, и также включает пептиды, конкурирующие с MASP-2 за связывание с другой распознающей молекулой (например, MBL, CL-11, H-фиколином, M-фиколином или L-фиколином) в лектиновом пути. Средства, ингибирующие MASP-2, применимые в способе по изобретению, могут снижать MASP-2-зависимую активацию комплемента более чем на 10%, например, более чем на 20%, более чем на 50% или более чем на 90%. В одном из вариантов осуществления средство, ингибирующее MASP-2, снижает MASP-2-зависимую активацию комплемента более чем на 90% (т.е. приводит к MASP-2-зависимой активации комплемента только на 10% или менее). Примером прямого средства, ингибирующего MASP-2, является MASP-2-специфичное ингибирующее средство, такое как средство, ингибирующее MASP-2, специфически связывающееся с частью MASP-2 (SEQ ID NO: 5) с аффинностью связывания по меньшей мере в 10 раз выше, чем с другими компонентами системы комплемента.
Как применяют в настоящем описании, термин "антитело" включает антитела и фрагменты антител, полученные из любого антитело-продуцирующегося млекопитающего (например, мыши, крысы, кролика и примата, включая человека) или из гибридомы, с помощью фаговой селекции, рекомбинантной экспрессии или трансгенных животных (или другими способами получения антител или фрагментов антител), специфически связывающиеся с полипептидом-мишенью, таким как, например, полипептиды MASP-1, MASP-2 или MASP-3 или их части. Не следует понимать, что термин "антитело" ограничен источником антител или способом их получения (например, гибридомой, фаговой селекцией, рекомбинантной экспрессией, трансгенным животным, пептидным синтезом и т.д.). Примеры антител включают поликлональные, моноклональные и рекомбинантные антитела; панспецифические, полиспецифические антитела (например, биспецифические антитела, триспецифические антитела); гуманизированные антитела; антитела мыши; химерные моноклональные антитела мыши-человека, мыши-примата, примата-человека; и антиидиотипические антитела, и антитело может являться любым интактным антителом или его фрагментом. Как применяют в настоящем описании, термин "антитело" включает не только интактные поликлональные или моноклональные антитела, но также и их фрагменты (такие как dAb, Fab, Fab', F(ab')2, Fv), одноцепочечные варианты (ScFv), их синтетические варианты, природные варианты, слитые белки, содержащие часть антитела с антигенсвязывающим фрагментом необходимой специфичности, гуманизированные антитела, химерные антитела и многие другие конфигурации молекулы иммуноглобулина, содержащие антигенсвязывающий участок или фрагмент (участок распознавания эпитопа) необходимой специфичности.
Термин "моноклональное антитело" относится к гомогенной популяции антител, где моноклональное антитело состоит из аминокислот (природных и неприродных), участвующих в селективном связывании эпитопа. Моноклональные антитела являются высокоспецифичными в отношении антигена-мишени. Термин "моноклональное антитело" включает не только интактные моноклональные антитела и полноразмерные моноклональные антитела, но также и их фрагменты (такие как Fab, Fab', F(ab')2, Fv), одноцепочечные варианты (ScFv), их варианты, слитые белки, содержащие антигенсвязывающую часть, гуманизированные моноклональные антитела, химерные моноклональные антитела и любые другие модифицированные конфигурации молекулы иммуноглобулина, содержащие антигенсвязывающий фрагмент (участок распознавания эпитопа) с необходимой специфичностью и способностью связываться с эпитопом. Термин не предназначен для ограничения источником антител или способом их получения (например, гибридомой, фаговой селекцией, рекомбинантной экспрессией, трансгенными животными и т.д.). Термин включает целые иммуноглобулины, а также фрагменты и т.д., описываемые выше под определением "антитело".
Как применяют в настоящем описании, термин "фрагмент антитела" относится к части, полученной из полноразмерного антитела или относящейся к нему, такому как, например, антитело против MASP-1, MASP-2 или MASP-3, как правило, включающему его антигенсвязывающую или вариабельную область. Иллюстративные примеры фрагментов антител включают фрагменты Fab, Fab', F(ab)2, F(ab')2 и Fv, фрагменты scFv, диатела, линейные антитела, одноцепочечные молекулы антител и полиспецифические антитела, образованные из фрагментов антител.
Как применяют в настоящем описании, "одноцепочечное Fv" или "scFv"-фрагмент антитела содержит домены VH и VL антитела, где эти домены присутствуют в одной полипептидной цепи. Как правило, полипептид Fv дополнительно содержит полипептидный линкер между доменами VH и VL, позволяющий scFv образовывать желаемую структуру для связывания антигена.
Как применяют в настоящем описании, "химерное антитело" является рекомбинантным белком, содержащим вариабельные домены и определяющие комплементарность области антитела, полученные из не являющихся человеком видов (например, грызунов), в то время как остальную часть молекулы антитела получают из антитела человека.
Как применяют в настоящем описании, "гуманизированное антитело" является химерным антителом, содержащим минимальную последовательность, соответствующую специфичным определяющим комплементарность областям, полученным из не принадлежащего человеку иммуноглобулина, трансплантированным на каркас антитела человека. Гуманизированные антитела, как правило, являются рекомбинантными белками, в которых только определяющие комплементарность области антитела имеют нечеловеческое происхождение (включая антитела, полученные с помощью фагового дисплея или дрожжей).
Как применяют в настоящем описании, термин "маннозо-связывающий лектин" ("MBL") эквивалентен маннозо-связывающему белку ("MBP").
Как применяют в настоящем описании, "мембраноатакующий комплекс" ("MAC") относится к комплексу пяти терминальных компонентов комплемента (C5 в комбинации с C6, C7, C8 и C9), встраивающемуся в мембрану и разрушающему ее (также обозначаемому как C5b-9).
Как применяют в настоящем описании, термин "индивидуум" включает всех млекопитающих, включая, в качестве неограничивающих примеров, людей, не являющихся человеком приматов, собак, кошек, лошадей, овец, коз, коров, кроликов, свиней и грызунов.
Как применяют в настоящем описании, названия аминокислотных остатков сокращают следующим образом: аланин (Ala; A), аспарагин (Asn; N), аспарагиновая кислота (Asp; D), аргинин (Arg; R), цистеин (Cys; C), глутаминовая кислота (Glu; E), глутамин (Gln; Q), глицин (Gly; G), гистидин (His; H), изолейцин (Ile; I), лейцин (Leu; L), лизин (Lys; K), метионин (Met; M), фенилаланин (Phe; F), пролин (Pro; P), серин (Ser; S), треонин (Thr; T), триптофан (Trp; W), тирозин (Tyr; Y) и валин (Val; V).
В самом широком смысле, природные аминокислоты можно разделять на группы в зависимости от химических свойств боковой цепи соответствующих аминокислот. "Гидрофобная" аминокислота означает Ile, Leu, Met, Phe, Trp, Tyr, Val, Ala, Cys или Pro. "Гидрофильная" аминокислота означает Gly, Asn, Gln, Ser, Thr, Asp, Glu, Lys, Arg или His. Эти группы аминокислот можно дополнительно подразделять следующим образом. "Незаряженная гидрофильная" аминокислота означает Ser, Thr, Asn или Gln. "Кислая" аминокислота означает Glu или Asp. "Основная" аминокислота означает Lys, Arg или His.
Как применяют в настоящем описании, термин "консервативная аминокислотная замена" иллюстрируют заменой среди аминокислот в каждой из следующих групп: (1) глицин, аланин, валин, лейцин и изолейцин, (2) фенилаланин, тирозин и триптофан, (3) серин и треонин, (4) аспарагиновая кислота и глутаминовая кислота, (5) глутамин и аспарагин, и (6) лизин, аргинин и гистидин.
Как применяют в настоящем описании, термин "олигонуклеотид" относится к олигомеру или полимеру рибонуклеиновой кислоты (РНК) или дезоксирибонуклеиновой кислоты (ДНК) или их имитациям. Этот термин также включает олигонуклеотиды, состоящие из природных нуклеотидов, сахаров и ковалентных межнуклеозидных связей (остов), а также олигонуклеотиды, имеющие неприродные модификации.
Как применяют в настоящем описании, термин "эпитоп" относится к участку белка (например, белка MASP-3 человека), связываемому антителом. "Перекрывающиеся эпитопы" включают по меньшей мере один (например, два, три, четыре, пять или шесть) общий аминокислотный остаток(-и), включая линейные и нелинейные эпитопы.
Как применяют в настоящем описании, термины "полипептид", "пептид" и "белок" используют взаимозаменяемо, и они означают любую цепь аминокислот, соединенных пептидной связью, независимо от длины или посттрансляционной модификации. Белки MASP (MASP-1, MASP-2 или MASP-3), представленные в настоящем описании, могут содержать или являться белками дикого типа или могут являться вариантами, имеющими не более 50 (например, не более одной, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, 12, 15, 20, 25, 30, 35, 40 или 50) консервативных аминокислотных замен. Консервативные замены, как правило, включают замены в следующих группах: глицин и аланин; валин, изолейцин и лейцин; аспарагиновая кислота и глутаминовая кислота; аспарагин, глутамин, серин и треонин; лизин, гистидин и аргинин; и фенилаланин и тирозин.
Белок MASP-1 человека (приведенный как SEQ ID NO: 10), белок MASP-2 человека (приведенный как SEQ ID NO: 5) и белок MASP-3 человека (приведенный как SEQ ID NO: 8), представленные в настоящем описании, также включают "пептидные фрагменты" белков, более короткие, чем полноразмерные и/или незрелые (пре- и про-) белки MASP, включая пептидные фрагменты белка MASP, включая концевые, а также внутренние делетационные варианты белка. В делетационных вариантах могут отсутствовать один, два, три, четыре, пять, шесть, семь, восемь, девять, десять, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 аминокислотных сегментов (из двух или более аминокислот) или несмежных отдельных аминокислот. В некоторых вариантах осуществления белок MASP-1 человека может иметь аминокислотную последовательность, являющуюся на 70% или более (например, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, или 100) идентичной белку MASP-1 человека, имеющему аминокислотную последовательность, приведенную в SEQ ID NO: 10.
В некоторых вариантах осуществления белок MASP-3 человека может иметь аминокислотную последовательность, являющуюся на 70% или более (например, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100) идентичной белку MASP-3 человека, имеющему аминокислотную последовательность, приведенную в SEQ ID NO: 8.
В некоторых вариантах осуществления белок MASP-2 человека может иметь аминокислотную последовательность, являющуюся на 70% или более (например, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100) идентичной белку MASP-2 человека, имеющему аминокислотную последовательность, приведенную в SEQ ID NO: 5.
В некоторых вариантах осуществления пептидные фрагменты могут составлять по меньшей мере, 6 (например, по меньшей мере 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 350, 400, 450, 500 или 600 или более) аминокислотных остатков в длину (например, по меньшей мере 6 смежных аминокислотных остатков в любой из SEQ ID NO: 5, 8 или 10). В некоторых вариантах осуществления антигенный пептидный фрагмент белка MASP человека составляет менее 500 (например, менее 450, 400, 350, 325, 300, 275, 250, 225, 200, 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 95, 90, 85, 80, 75, 70, 65, 60, 55, 50, 49, 48, 47, 46, 45, 44, 43, 42, 41, 40, 39, 38, 37, 36, 35, 34, 33, 32, 31, 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7 или 6) аминокислотных остатков в длину (например, менее 500 смежных аминокислотных остатков в любой из SEQ ID NOS: 5, 8 или 10).
В некоторых вариантах осуществления, относящимся к получению антитела, связывающегося с MASP-1, MASP-2 и/или MASP-3, пептидные фрагменты являются антигенными и сохраняют по меньшей мере 10% (например, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98%, по меньшей мере 99%, по меньшей мере 99,5%, или 100% или более) способности полноразмерного белка индуцировать антигенный ответ у млекопитающего (см. "Способы получения антитела" ниже).
Процент (%) идентичности аминокислотных последовательностей определяют как процентную долю аминокислот в вероятной последовательности, идентичных аминокислотам в референсной последовательности, после выравнивания последовательностей и, при необходимости, вставки пропусков для достижения максимального процента идентичности последовательностей. Выравнивание в целях определения процента идентичности последовательностей можно осуществлять различными способами, известными специалистам в этой области, например, с использованием общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN, ALIGN-2 или Megalign (DNASTAR). Подходящие параметры для измерения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по отношению к полной длине сравниваемых последовательностей, можно определять известными способами.
В типичных вариантах осуществления белок MASP-1 человека (SEQ ID NO: 10) кодируется последовательностью кДНК, приведенной как SEQ ID NO: 9; белок MASP-2 человека (SEQ ID NO: 5) кодируется последовательностью кДНК, приведенной как SEQ ID NO: 4; и белок MASP-3 человека (SEQ ID NO: 8) кодируется последовательностью кДНК, приведенной как SEQ ID NO: 7. Специалистам в этой области понятно, что последовательности кДНК, приведенные в SEQ ID NO: 9, SEQ ID NO: 4 и SEQ ID NO: 7 представляют один аллель MASP-1, MASP-2 и MASP-3 человека, соответственно, и ожидают, что могут иметь место аллельные варианты и альтернативный сплайсинг. Аллельные варианты нуклеотидных последовательностей, приведенных в SEQ ID NO: 9, SEQ ID NO: 4 и SEQ ID NO: 7, включая содержащие молчащие мутации и те, в которых мутации приводят к изменениям аминокислотной последовательности, входят в объем настоящего изобретения. Аллельные варианты последовательностей MASP-1, MASP-2 или MASP-3 можно клонировать посредством зондирования кДНК или геномных библиотек от различных индивидуумов с помощью стандартных способов, или можно идентифицировать посредством поиска со сравнением гомологии (например, поиска с помощью BLAST) в базах данных, содержащих такую информацию.
II. ЛЕКТИНОВЫЙ ПУТЬ: НОВОЕ ПОНИМАНИЕ
i. Обзор: Пересмотр лектинового пути
Как представлено в настоящем описании, авторы настоящего изобретения сделали удивительное открытие, заключающееся в том, что лектиновый путь комплемента имеет две эффекторные ветви для активации комплемента, обе запускаемые комплексами активации лектинового пути, образованными распознающими углеводы компонентами (MBL, CL-11 и фиколинами): i) эффекторная ветвь, образованная ассоциированными с лектиновым путем сериновыми протеазами MASP-1 и MASP-3, обозначаемыми в настоящем описании как "эффекторная ветвь лектинового пути 1" или "LEA-1"; и (ii) эффекторная ветвь запускаемой MASP-2 активации, обозначаемая в настоящем описании как "эффекторная ветвь лектинового пути 2" или "LEA-2". И LEA-1, и LEA-2 могут осуществлять лизис и/или опсонизацию.
Также определяли, что лектин-независимая конвертация фактора B MASP-3 и лектин-независимая конвертация фактора D HTRA-1, MASP-1 и MASP-3, происходящие в отсутствие Ca++, как правило, приводят к конвертации C3bB в C3bBb и про-фактора D в фактор D. Таким образом, ингибирование MASP-3 может ингибировать и LEA-1, и лектин-независимую активацию фактора B и/или фактора D, что может приводить к ингибированию лизиса и/или опсонизации.
На фигуре 1 представлено это новое понимание путей активации комплемента. Как показано на фигуре 1, LEA-1 запускается лектин-связанной MASP-3, что может активировать зимоген фактора D с превращением его в активную форму и/или расщеплять C3b- или C3b(H2O)-связанный фактор B, что приводит к конвертации комплекса зимогена C3bB в его ферментативно активную форму C3bBb. Активированный фактор D, образующийся с помощью MASP-3, также может конвертировать комплексы зимогенов C3bB или C3b(H20) в их ферментативно активную форму. MASP-1 способна к быстрой аутоактивации, в то время как MASP-3 - нет. Во многих случаях, MASP-1 является активатором MASP-3.
Хотя во многих примерах лектины (т.е. MBL, CL-11 или фиколины) могут направлять активность на клеточные поверхности, на фигуре 1 также показаны лектин-независимые функции MASP-3, MASP-1 и HTRA-1 в активации фактора B и/или созревании фактора D. Как и лектин-ассоциированная форма MASP-3 в LEA-1, лектин-независимая форма MASP-3 способна опосредовать конвертацию C3bB или C3b(H2O) в C3bBb (также см. фигуры 36 и 37) и про-фактора D в фактор D (см. фигуру 39). MASP-1 (также см. фигуру 39) и не относящийся к MASP белок HTRA-1 также могут активировать фактор D (Stanton et al., Evidence That the HTRA1 Interaction Influences Susceptibility to Age-Related Macular Degeneration, представленный 4 мая 2011 года на конференции The Association for Research in Vision and Ophthalmology 2011) способом, для которого не нужен лектиновый компонент.
Таким образом, MASP-1 (через LEA-1 и лектин-независимые формы), MASP-3 (через LEA-1 и лектин-независимые формы) и HTRA-1 (только лектин-независимый) способны к прямой или опосредованной активации в одной или нескольких точках оси MASP-3-фактор D-фактор B. При этом они приводят к образованию C3bBb, конвертазы C3 альтернативного пути, и стимулируют продукцию и накопление C3b на поверхностях микроорганизмов. Накопление C3b играет критическую роль в опсонизации, мечении поверхностей микроорганизмов для их деструкции фагоцитирующими клетками хозяина, такими как макрофаги. В качестве примера, приведенного в настоящем описании (фигура 35), MASP-3 критична для опсонизации S. aureus. На S. aureus, подвергнутых воздействию сыворотки человека, быстро происходит накопление C3b MASP-3-зависимым образом (фигура 35).
Однако участие LEA-1 и лектин-независимые функции MASP-3, MASP-1 или HTRA-1 не ограничены опсонизацией. Как схематически показано на фигуре 1, эти три компонента также могут вызывать лизис клеток посредством прямой или опосредованной активации фактора B и продукции C3b. Эти компоненты образуют комплексы, приводящие к образованию конвертазы C5 альтернативного пути, C3bBb(C3b)n. Как дополнительно представлено в настоящем описании, необходимость MASP-3 и MBL, но не MASP-2 (и, таким образом, не LEA-2 в этом примере) в лизисе N. meningitidis (см. фигуры 13, 14 и 15) свидетельствует о роли LEA-1 в лизисе. В совокупности, данные об опсонизации, полученные в исследованиях на S. aureus, и данные о лизисе, полученные в исследованиях на N. meningitidis, подтверждают роль LEA-1 в обоих процессах (как схематически показано на фигуре 1). Кроме того, эти исследования свидетельствуют о том, что опсонизация и лизис могут являться результатом конвертации C3bB или C3b(H2O) и/или про-фактора D в фактор D; таким образом, оба процесса могут являться результатом лектин-независимого действия MASP-3, MASP-1 или HTRA-1. Таким образом, модель, разработанная авторами настоящего изобретения и представленная на фигуре 1, подтверждает применимость ингибиторов преимущественно MASP-3, но также и MASP-1 и/или HTRA-1, для блокирования опсонизации и/или лизиса и для лечения патологий, вызываемых нарушением регуляции этих процессов.
1. Эффекторная ветвь лектинового пути (LEA-1)
Первая эффекторная ветвь лектинового пути, LEA-1, образована ассоциированными с лектиновым путем сериновыми протеазами MASP-1 и MASP-3. Как представлено в настоящем описании, авторы настоящего изобретения к настоящему времени показали, что в отсутствие MASP-3 и в присутствие MASP-1 альтернативный путь не активируется эффективно в ответ на поверхностные структуры. Эти результаты свидетельствуют о том, что MASP-3 играет ранее не описанную роль в инициации альтернативного пути, и это подтверждено с использованием сыворотки пациентов с 3MC с дефицитом MASP-3, полученной от пациентов с редким аутосомным рецессивным нарушением 3MC (Rooryck C, et al., Nat Genet. 43(3): 197-203 (2011)) с мутациями, делающими домен сериновой протеазы MASP-3 нефункциональным. Учитывая эти новые данные, ожидают, что активация комплемента, включающая альтернативный путь, как общепринято определяют, является MASP-3-зависимой. Фактически, MASP-3 и ее активация LEA-1 могут представлять собой прежде неясный инициатор альтернативного пути.
Как дополнительно описано в примерах 1-4 в настоящем описании, в сыворотках при дефиците MASP-2 авторы настоящего изобретения наблюдали более высокую активность лектин-зависимой активации альтернативным путем, приводящую к более высокой бактерицидной активности (т.е. литической активности) в отношении N. meningitidis. Без желания быть связанными какой-либо конкретной теорией, полагают, что в отсутствие MASP-2, MASP-1-содержащие комплексы, распознающие углеводы, более вероятно близко связываются с MASP-3-содержащими комплексами, распознающими углеводы, для активации MASP-3. Известно, что во многих случаях активация MASP-3 зависит от активности MASP-1, т.к. MASP-3 не является аутоактивирующимся ферментом, и для ее конвертации из зимогена в ферментативно активную форму необходима активность MASP-1. MASP-1 (подобно MASP-2) является аутоактивирующимся ферментом, в то время как MASP-3 не подвергается аутоактивации, и во многих случаях для ее конвертации в ферментативно активную форму необходима ферментативная активность MASP-1. См., Zundel S, et al, J Immunol., 172(7):4342-50 (2004). В отсутствие MASP-2 все распознающие комплексы лектинового пути нагружены MASP-1 или MASP-3. Таким образом, отсутствие MASP-2 облегчает опосредованную MASP-1 конвертацию MASP-3 в ее ферментативно активную форму. При активации MASP-3 активированная MASP-3 инициирует альтернативный путь активации, в настоящем описании обозначаемый как активация "LEA-1", через опосредованную MASP-3 конвертацию C3bB в C3bBb и/или конвертацию про-фактора D в фактор D. C3bBb, также обозначаемый как конвертаза C3 альтернативного пути, расщепляет дополнительные молекулы C3, что приводит к накоплению опсонических молекул C3b. Если несколько фрагментов C3b связываются в непосредственной близости с комплексом конвертазы C3bBb, это приводит к образованию конвертазы C5 альтернативного пути C3bBb(C3b)n, стимулирующей образование MAC. Дополнительно, молекулы C3b, накопленные на поверхности, образуют новые участки для связывания фактора B, которые теперь могут подвергаться расщеплению фактором D и/или MASP-3 для образования дополнительных участков, где могут образовываться комплексы конвертаз C3 и C5 альтернативного пути. Последний процесс необходим для эффективного лизиса и не требует наличия лектинов, т.к. происходит исходное накопление C3b. Недавняя публикация (Iwaki D. et al, J Immunol 187(7):3751-8 (2011)), а также данные, полученные авторами настоящего изобретения (фигура 37), свидетельствуют о том, что комплекс зимогена конвертазы C3 альтернативного пути C3bB конвертируется в свою ферментативно активную форму активированной MASP-3. К настоящему времени авторы настоящего изобретения обнаружили, что опосредованное MASP-3 расщепление фактора B представляет подкомпонент недавно описанной LEA-1, стимулирующий лектин-зависимое образование конвертазы C3 альтернативного пути C3bBb.
2. Эффекторная ветвь лектинового пути (LEA-2)
Вторая эффекторная ветвь лектинового пути, LEA-2, образована ассоциированной с лектиновым путем сериновой протеазой MASP-2. MASP-2 активируется после связывания распознающих компонентов с соответствующим им паттерном, а также может активироваться MASP-1, и затем расщепляет компонент комплемента C4 на C4a и C4b. После связывания продукта расщепления C4b с C2 в плазме C4b-связанный C2 становится субстратом второго опосредованного MASP-2 этапа расщепления, в котором C4b-связанный C2 конвертируется в ферментативно активный комплекс C4bC2a и небольшой фрагмент C2b. C4b2a является конвертирующей C3 конвертазой C3 лектинового пути, конвертирующей многочисленный плазматический компонент C3 на C3a и C3b. C3b связывается с любой поверхностью в непосредственной близости посредством тиоэфирной связи. Если несколько фрагментов C3b связываются в непосредственной близости с комплексом конвертазы C3 C4b2a, эта конвертаза изменяет свою специфичность для конвертации C5 в C5b и C5a, образуя комплекс конвертазы C5 C4b2a(C3b)n. Хотя эта конвертаза C5 может инициировать образование MAC, считают, что этот процесс недостаточно эффективен для самостоятельной стимуляции лизиса. Скорее исходные опсонины C3b, продуцируемые LEA-2, образуют ядро для образования новых участков конвертазы C3 и конвертазы C5 альтернативного пути, что, в конечном итоге, приводит к избыточному образованию MAC и лизису. Последний процесс опосредован активацией фактором D фактора B, связанного с образующимся через LEA-2 C3b, и, таким образом, зависит от LEA-1 благодаря значительной роли MASP-1 в созревании фактора D. Также существует MASP-2-зависимый путь активации в обход C4 для активации C3 в отсутствие C4, играющий важную роль в патофизиологии повреждения при ишемии/реперфузии, т.к. мыши с дефицитом C4 не защищены от повреждения при ишемии/реперфузии, в то время как мыши с дефицитом MASP-2 защищены (Schwaeble et al., PNAS, 2011, выше). LEA-2 также связана с путем коагуляции, включающим расщепление протромбина до тромбина (общий путь), а также расщеплением фактора XII (фактора Хагемана) для его конвертации в ферментативно активную форму XIIa. В свою очередь, фактор XIIa расщепляет фактор XI до XIa (внутренний путь). Активация внутреннего пути каскада тромбообразования приводит к образованию фибрина, крайне важного для образования тромба.
На фигуре 1 показано новое понимание лектинового пути и альтернативного пути с учетом результатов, представленных в настоящем описании. На фигуре 1 обозначена роль LEA-2 и в опсонизации, и в лизисе. Хотя MASP-2 является инициатором "нижележащего в каскаде" накопления C3b (и последующей опсонизации) во многих лектин-зависимых физиологических условиях (фигуры 20A, 20B, 20C), он также играет роль в лизисе серологически типируемых бактерий. Как показано на фигуре 1, предлагаемый молекулярный механизм, ответственный за повышенную бактерицидную активность сыворотки/плазмы при дефиците MASP-2 или MASP-2-обедненной сыворотки/плазмы в отношении серологически типируемых патогенов, таких как N. meningitidis, в случае лизиса бактерий состоит в том, что распознающие комплексы лектинового пути, связанные с MASP-1 и MASP-3, связываются в непосредственной близости друг с другом на поверхности бактерии, таким образом, позволяя MASP-1 расщеплять MASP-3. В отличие от MASP-1 и MASP-2, MASP-3 не является аутоактивирующимся ферментом, но во многих случаях для нее необходима активация/расщепление MASP-1 для конвертации в свою ферментативно активную форму.
Как дополнительно показано на фигуре 1, активированная MASP-3 затем может расщеплять C3b-связанный фактор B на поверхности патогена для инициации каскада альтернативной активации посредством образования ферментативно активных конвертаз C3 и C5 альтернативного пути C3bBb и C3bBb(C3b)n, соответственно. MASP-2-содержащие комплексы активации лектинового пути не участвуют в активации MASP-3 и в отсутствие или после истощения MASP-2, все комплексы активация лектинового пути будут нагружены MASP-1 или MASP-3. Таким образом, в отсутствие MASP-2 значительно повышается вероятность того, что MASP-1- и MASP-3-содержащие комплексы активации лектинового пути на поверхности микроорганизма будут располагаться в непосредственной близости друг к другу, что приводит к большей активации MASP-3 и, таким образом, к более высокой скорости опосредованного MASP-3 расщепления C3b-связанного фактора B для образования конвертаз C3 и C5 альтернативного пути C3bBb и C3bBb(C3b)n на поверхности микроорганизма. Это приводит к активации терминальных каскадов активации C5b-C9, образующих мембраноатакующий комплекс, состоящий из связанного с поверхностью C5b, связанного с C6, C5bC6, связанного с C7, C5bC6C7, связанного с C8, и C5bC6C7C8, что приводит к полимеризации C9, встраивающегося в поверхностную структуру бактерии и образующего пору в бактериальной стенке, что будет приводить к осмолитической гибели бактерии, на которую воздействует комплемент.
Ядром этой новой концепции является то, что данные, представленные в настоящем описании, четко свидетельствуют о том, что комплексы активации лектинового пути запускают два следующих отдельных пути активации, как показано на фигуре 1:
i) LEA-1: MASP-3-зависимый путь активации, инициирующий и запускающий активацию комплемента посредством образования конвертазы C3bBb альтернативного пути через исходное расщепление и активацию фактора B на поверхностях активатора, который затем катализирует накопление C3b и образование конвертаза C3bBb альтернативного пути. Запускаемый MASP-3 путь активации играет важную роль в опсонизации и лизисе микроорганизмов и запускает альтернативный путь на поверхности бактерий, что приводит к оптимальным скоростям активации для образования мембраноатакующих комплексов; и
ii) LEA-2: MASP-2-зависимый путь активации, приводящий к образованию конвертазы C3 лектинового пути C4b2a, а затем, после накопления продукта расщепления C3 C3b, к образованию конвертазы C5 C4b2a(C3b)n. В отсутствие компонента комплемента C4 MASP-2 может образовывать альтернативный комплекс конвертазы C3, включающий C2 и фактор свертываемости крови XI.
В дополнение к его роли в лизисе запускаемый MASP-2 путь активации играет важную роль в опсонизации бактерий, приводящей к покрыванию микроорганизмов ковалентно связанным C3b и его продуктами расщепления (т.е. iC3b и C3dg), нацеленными на захват и уничтожение несущими рецептор C3 фагоцитами, такими как гранулоциты, макрофаги, моноциты, клетки микроглии и ретикулоэндотелиальной системы. Это наиболее эффективный путь клиренса бактерий и микроорганизмов, устойчивых к лизису посредством комплемента. Они включают большинство грамположительных бактерий.
В дополнение к LEA-1 и LEA-2, существует потенциал для лектин-независимой активации фактора D посредством MASP-3, MASP-1 и/или HTRA-1, а также существует потенциал для лектин-независимой активации фактора B посредством MASP-3.
Без желания быть связанными какой-либо конкретной теорией, полагают, что каждая из (i) LEA-1, (ii) LEA-2 и (iii) лектин-независимой активации фактора B и/или фактора D приводит к опсонизации и/или образованию MAC с последующим лизисом.
ii. Основные данные о MASP-1, MASP-2 и MASP-3
Как известно в настоящее время, ассоциированные с маннозо-связывающим лектином сериновые протеазы (MASP-1, MASP-2 и MASP-3) в сыворотке человека связаны с маннозо-связывающим лектином (MBL). В литературе маннозо-связывающий лектин также называют "маннозо-связывающим белком". Комплекс MBL-MASP играет важную роль во врожденном иммунитете благодаря связыванию MBL с углеводными структурами, присутствующими на широком спектре микроорганизмов. Взаимодействие MBL со специфическими наборами углеводных структур приводит к активации проферментов MASP, в свою очередь, активирующих комплемент посредством расщепления компонентов комплемента C4 и C2 для образования конвертазы C3 C4b2b (Kawasaki et al, J. Biochem 106:483-489 (1989); Matsushita & Fujita, J. Exp Med. 176: 1497-1502 (1992); Ji et al., J. Immunol 150:571-578 (1993)).
До недавнего времени считали, что комплекс MBL-профермент MASP содержит только один тип протеазы (MASP-1), но в настоящее время очевидно, что существует две отдельных протеазы (т.е. MASP-2 и MASP-3), ассоциированных с MBL (Thiel et al., Nature 386:506-510 (1997); Dahl et al., Immunity 15:127-135 (2001)), а также дополнительный сывороточный белок массой 19 кДа, обозначаемый как "MAp19" или "sMAP" (Stover et al., J. Immunol 162:3481-3490 (1999); Stover et al, J. Immunol 163:6848-6859 (1999); Takahashi et al, Int. Immunol 11:859-63 (1999)).
MAp19 является продуктом альтернативного сплайсинга структурного гена MASP-2, и в нем отсутствуют четыре C-концевых домена MASP-2, включая серин-эндопептидазный домен. Избыточно экспрессирующийся транскрипт мРНК, кодирующий MAp19, образуется посредством альтернативного сплайсинга/полиаденилирования гена MASP-2. С помощью аналогичного механизма из гена MASP-1/3 образуются три основных продукта гена, две сериновые протеазы MASP-1 и MASP-3 и укороченный продукт гена массой 44 кДа, обозначаемый как "MAp44" (Degn et al, J. Immunol 183(11):7371-8 (2009); Skjoedt et al, J Biol Chem 285:8234-43 (2010)).
Впервые MASP-1 был описан как протеазный компонент P-100 сывороточного Ra-реактивного фактора, который, как считают в настоящее время, представляет собой комплекс, состоящий из MBL и MASP (Matsushita et al, Collectins and Innate Immunity, (1996); Ji et al., J Immunol 150:571-578 (1993). Способность MBL-ассоциированной эндопептидазы в комплексах MBL-MASP действовать на компоненты комплемента C4 и C2 способом, очевидно идентичным тому, которым действует фермент C1s в комплексе C1q-(C1r)2-(C1s)2 классического пути комплемента, позволяет предполагать, что существует комплекс MBL-MASP, являющийся функциональным аналогом комплекса C1q-(C1r)2-(C1s)2. Комплекс C1q-(C1r)2-(C1s)2 активируется посредством взаимодействия C1q с Fc-областями антител IgG или IgM, присутствующих в иммунных комплексах. Это приводит к аутоактивации профермента C1r, в свою очередь, активирующего профермент C1s, который затем действует на компоненты комплемента C4 и C2.
Стехиометрия комплекса MBL-MASP отличается от обнаруженной для комплекса C1q-(C1r)2-(C1s)2 тем, что различные олигомеры MBL, по-видимому, связываются с различными пропорциями MASP-1/MAp19 или MASP-2/MASP-3 (Dahl et al, Immunity 15: 127-135 (2001). Большая часть MASP и MAp19, обнаруживаемых в сыворотке, не находится в комплексах с MBL (Thiel et al., J Immunol 165:878-887 (2000)) и может частично связываться с фиколинами, недавно описанной группой лектинов, имеющих фибриногеноподобный домен, способный связываться с остатками N-ацетилглюкозамина на поверхности микроорганизмов (Le et al., FEBS Lett 425:367 (1998); Sugimoto et al, J. Biol Chem 273:20721 (1998)). Среди них, L-фиколин, H-фиколин и M-фиколин человека связываются с MASP, а также MAp19 и могут активировать лектиновый путь после связывания со специфичными углеводными структурами, распознаваемыми фиколинами (Matsushita et al, J Immunol 164:2281-2284 (2000); Matsushita et al, J Immunol 168:3502-3506 (2002)). В дополнение к фиколинами и MBL, в качестве распознающей молекулы лектинового пути идентифицирован MBL-подобный лектин коллектин, называемый CL-11 (Hansen et al. J Immunol 185:6096-6104 (2010); Schwaeble et al. PNAS 108:7523-7528 (2011)). Существует убедительное доказательство, подчеркивающее физиологическую важность этих альтернативных распознающих углеводы молекул, и, таким образом, важно понимать, что MBL не является единственным распознающим компонентом лектинового пути активации, и что дефицит MBL нельзя путать с дефицитом лектинового пути. Существование возможного набора альтернативных распознающих углеводы комплексов, структурно родственных MBL, может расширить спектр структур микроорганизмов, инициирующих прямой ответ врожденной иммунной системы посредством активации комплемента. Все распознающие молекулы лектинового пути отличаются конкретным MASP-связывающим мотивом внутри гомологичной коллагену области стебля (Wallis et al. J. Biol Chem 279: 14065-14073 (2004)). ASP-связывающий участок в MBL, CL-11 и фиколинах отличается другим мотивом внутри этого домена: Hyp-Gly-Lys-Xaa-Gly-Pro, где Hyp представляет собой гидроксипролин, и Xaa, как правило, представляет собой алифатический остаток. Точечные мутации в этой последовательности нарушают связывание MASP.
1. Соответствующие структуры, последовательности, хромосомная локализация и варианты сплайсинга
Фигура 2 является схемой, на которой показана доменная структура полипептида MASP-2 (SEQ ID NO: 5) и полипептида MAp19 (SEQ ID NO: 2) и кодирующие их экзоны. Фигура 3 является схемой, на которой показана доменная структура полипептида MASP-1 (SEQ ID NO: 10), полипептида MASP-3 (SEQ ID NO: 8) и полипептида MAp44 (SEQ ID NO: 11) и кодирующие их экзоны. Как показано на фигурах 2 и 3, сериновые протеазы MASP-1, MASP-2 и MASP-3 состоят из шести отдельных доменов, расположенных как обнаруживают для C1r и C1s; т.е. (I) N-концевой домен C1r/C1s/VEGF морского ежа/морфогенетического белка кости (или CUBI); (II) домен, подобный эпидермальному фактору роста (EGF); (III) второй домен CUB (CUBII); (IV и V) два домена контролирующего комплемент белка (CCP1 и CCP2); и (VI) домен сериновой протеазы (SP).
Полученные с помощью кДНК аминокислотные последовательности MASP-1 человека и мыши (Sato et al., Int Immunol 6:665-669 (1994); Takada et al., Biochem Biophys Res Commun 196: 1003-1009 (1993); Takayama et al., J. Immunol 152:2308-2316 (1994)), MASP-2 человека, мыши и крысы (Thiel et al., Nature 386:506-510 (1997); Endo et al., J Immunol 161:4924-30 (1998); Stover et al., J. Immunol 162:3481-3490 (1999); Stover et al., J. Immunol 163:6848-6859 (1999)), а также MASP-3 человека (Dahl et al., Immunity 15: 127-135 (2001)) свидетельствуют о том, что эти протеазы являются сериновыми пептидазами, содержащими характерную триаду остатков His, Asp и Ser в своих предполагаемых каталитических доменах (регистрационные номера Genbank: MASP-1 человека: BAA04477.1; MASP-1 мыши: BAA03944; MASP-1 крысы: AJ457084; MASP-3 человека: AAK84071; MASP-3 мыши: AB049755, как указано в Genbank на 2/15/2012, каждый из которых, таким образом, включен в настоящее описание в качестве ссылки).
Как дополнительно показано на фигурах 2 и 3, после конвертации зимогена в активную форму тяжелая цепь (альфа- или A-цепь) и легкая цепь (бета- или B-цепь) разделяются для образования соединенных дисульфидной связью A-цепи и меньшей B-цепи, представляющей домен сериновой протеазы. Одноцепочечный профермент MASP-1 активируется (как профермент C1r и C1s) посредством расщепления связи Arg-Ile, локализованной между вторым доменом CCP (доменом V) и доменом сериновой протеазы (доменом VI). Считают, что проферменты MASP-2 и MASP-3 активируются аналогично MASP-1. Каждый белок MASP образует гомодимеры и отдельно связывается с MBL и фиколинами Ca++-зависимым образом.
2. MASP-1/3
Полипептид MASP-1 (SEQ ID NO: 10) и полипептид MASP-3 человека (SEQ ID NO: 8) синтезируются со структурного гена (Dahl et al., Immunity 15: 127-135 (2001), картированного в области 3q27-28 длинного плеча хромосомы 3 (Takada et al., Genomics 25:757-759 (1995)). Транскрипты мРНК MASP-3 и MASP-1 образуются из первичного транскрипта с помощью альтернативного сплайсинга/полиаденилирования. Продукт трансляции MASP-3 состоит из альфа-цепи, общей для MASP-1 и MASP-3, и бета-цепи (домена сериновой протеазы), уникального для MASP-3. Как показано на фигуре 3, ген MASP-1 человека содержит 18 экзонов. кДНК MASP-1 человека (приведенная как SEQ ID NO: 9) кодируется экзонами 2, 3, 4, 5, 6, 7, 8, 10, 11, 13, 14, 15, 16, 17 и 18. Как дополнительно показано на фигуре 3, ген MASP-3 человека содержит двенадцать экзонов. кДНК MASP-3 человека (приведенная как SEQ ID NO: 7) кодируется экзонами 2, 3, 4, 5, 6, 7, 8, 10, 11 и 12. Альтернативный сплайсинг приводит к образованию белка, называемого MBL-ассоциированным белком 44 ("MAp44)," (приведенного как SEQ ID NO: 11), образующегося из экзонов 2, 3, 4, 5, 6, 7, 8 и 9.
Полипептид MASP-1 человека (SEQ ID NO: 10 из Genbank BAA04477.1) содержит 699 аминокислотных остатков, включая лидерный пептид из 19 остатков. Если пренебречь лидерным пептидом, вычисленная молекулярная масса MASP-1 составляет 76976 Да. Как показано на фигуре 3, аминокислотная последовательность MASP-1 содержит четыре N-связанных участков гликозилирования. Домены белка MASP-1 человека (со ссылкой на SEQ ID NO: 10) показаны на фигуре 3 и включают N-концевой домен C1r/C1s/VEFG морского ежа/морфогенетического белка кости (CUBI) (а/к 25-137 в SEQ ID NO: 10), домен, подобный эпидермальному фактору роста (а/к 139-181 в SEQ ID NO: 10), второй домен CUB (CUBII) (а/к 185-296 в SEQ ID NO: 10), а также тандем доменов контролирующего комплемент белка (CCP1 а/к 301-363 и CCP2 а/к 367-432 в SEQ ID NO: 10) и домен сериновой протеазы (а/к 449-694 в SEQ ID NO: 10).
Полипептид MASP-3 человека (SEQ ID NO: 8 из Genbank AAK84071) содержит 728 аминокислотных остатков, включая лидерный пептид из 19 остатков. Если пренебречь лидерными пептидами, вычисленная молекулярная масса MASP-3 составляет 81,873 Да. Как показано на фигуре 3, в MASP-3 есть семь N-связанных участков гликозилирования. Домены белка MASP-3 человека (со ссылкой на SEQ ID NO: 8) показаны на фигуре 3 и включают N-концевой домен C1r/C1s/VEGF морского ежа/морфогенетического белка кости (CUBI) (а/к 25-137 в SEQ ID NO: 8), домен, подобный эпидермальному фактору роста (а/к 139- 181 в SEQ ID NO: 8), второй домен CUB (CUBII) (а/к 185-296 в SEQ ID NO: 8), а также тандем доменов контролирующего комплемент белка (CCP1 а/к 301-363 и CCP2 а/к 367-432 в SEQ ID NO: 8) и домен сериновой протеазы (а/к 450-711 в SEQ ID NO: 8).
Продукт трансляции MASP-3 состоит из альфа-цепи (тяжелой цепи), содержащей домены CUB-1-EGF-CUB-2-CCP-1-CCP-2 (альфа-цепь: а/к 1-448 в SEQ ID NO: 8), общей для MASP-1 и MASP-3, и легкой цепи (бета-цепи: а/к 449-728 в SEQ ID NO: 8), содержащей домен сериновой протеазы, уникальный для MASP-3 и MASP-1.
3. MASP-2
Ген MASP-2 человека локализован на хромосоме 1p36,3-2 (Stover et al., Cytogenet and Cell Genet 84: 148-149 (1999) и включает двенадцать экзонов, как показано на фигуре 2. MASP-2 (SEQ ID NO: 5) и MAp19 (SEQ ID NO: 2) кодируются транскриптами одного структурного гена, образующимися в результате альтернативного сплайсинга/полиаденилирования (Stover et al, Genes and Immunity 2: 119-127 (2001)). кДНК MASP-2 человека (SEQ ID NO: 4) кодируется экзонами 2, 3, 4, 6, 7, 8, 9, 10, 11 и 12. Белок массой 20 кДа, называемый MBL-ассоциированным белком 19 ("MAp19", также обозначаемый как "sMAP") (SEQ ID NO: 2), кодируемый (SEQ ID NO: 1), образуется из экзонов 2, 3, 4 и 5. MAp19 является неферментативным белком, содержащим N-концевую область CUB1-EGF MASP-2 с четырьмя дополнительными остатками (EQSL), происходящими из экзона 5, как показано на фигуре 2.
Полипептид MASP-2 (SEQ ID NO: 5) содержит 686 аминокислотных остатка, включая лидерный пептид из 15 остатков, отщепляемый после секреции, что приводит к образованию зрелой формы MASP-2 человека (SEQ ID NO: 6). Как показано на фигуре 2, аминокислотная последовательность MASP-2 не содержит каких-либо N-связанных участков гликозилирования. Полипептид MASP-2 имеет молекулярную структуру, аналогичную MASP-1, MASP-3, и C1r и C1s, протеазам C1 системы комплемента. Домены белка MASP-2 человека (пронумерованные со ссылкой на SEQ ID NO: 5) показаны на фигуре 2 и включают N-концевой домен C1r/C1s/VEGF морского ежа/морфогенетического белка кости (CUBI) (а/к 24-136 в SEQ ID NO: 5), домен, подобный эпидермальному фактору роста (а/к 138-180 в SEQ ID NO: 5), второй домен CUB (CUBII) (а/к 184-295 в SEQ ID NO: 5), а также тандем доменов контролирующего комплемент белка (CCP1 а/к 300-359 и CCP2 а/к 364-431 в SEQ ID NO: 5) и домен сериновой протеазы (а/к 445-682 в SEQ ID NO: 5).
Как показано на фигуре 2, полипептид MASP-2 содержит альфа-цепь (тяжелую цепь), содержащую домены CUB-1-EGF-CUB-2-CCP-1-CCP-2 (альфа-цепь: а/к 1-443 в SEQ ID NO: 5) и бета-цепь (легкую цепь), содержащую домен сериновой протеазы (бета-цепь: а/к 444-686). Домены CUB-1, EGF и CUB-2 необходимы для димеризации, и домены CUB-1, EGF, CUB-2 и CCP-1 содержат участок связывания для MBP. Как описано в Wallis et al, J. Biol Chem 279: 14065-14073 (2004), каждый димер MASP-2 связывается с двумя субъединицами MBL.
4. Сравнение аминокислотных последовательностей MASP-1, MASP-2 и MASP-3
На фигуре 4 представлено аминокислотное выравнивание последовательностей белка MASP-1 (SEQ ID NO: 10), MASP-2 (SEQ ID NO: 6) и MASP-3 (SEQ ID NO: 8), где показаны домены CUBI, EGF, CUBII, CCP1, CCP2 и остатки консервативной каталитической триады (H, D, S) в доменах сериновой протеазы (SP). Символом "." указана идентичная аминокислотная последовательность.
На фигуре 5 представлено аминокислотное выравнивание последовательностей альфа-цепи, включая CUBI-EGF-CUBII-CCP1-CCP2, MASP-1 (альфа-цепь: а/к 1-447 в SEQ ID NO: 10), MASP-2 (альфа-цепь: а/к 1-443 в SEQ ID NO: 5) и MASP-3 (альфа-цепь: а/к 1-448 в SEQ ID NO: 8). В доменах CUBI, EGF, и CUBII есть несколько участков идентичности, указанные на фигуре 5 пунктирными рамками. Домены CCP1 и CCP2 указаны темными заштрихованными рамками. Общий процент идентичности альфа-цепей MASP1/3 человека и MASP-2 человека представлен в таблице 1 ниже.
На фигуре 6 представлено аминокислотное выравнивание последовательностей бета-цепей (включая домены сериновой протеазы) MASP-1 (бета-цепь: а/к 448-699 в SEQ ID NO: 10), MASP-2 (бета-цепь: а/к 444-686 в SEQ ID NO: 5) и MASP-3 (бета-цепь: а/к 449-728 в SEQ ID NO: 8). На фигуре 7A представлено попарное аминокислотное выравнивание последовательностей бета-цепи MASP-1 (бета-цепь: а/к 448-699 в SEQ ID NO: 10) и MASP-2 (бета-цепь: а/к 444-686 в SEQ ID NO: 5). На фигуре 7B представлено попарное аминокислотное выравнивание последовательностей бета-цепи MASP-1 (бета-цепь: а/к 448-699 в SEQ ID NO: 10) и MASP-3 (бета-цепь: а/к 449-728 в SEQ ID NO: 8). На фигуре 7C представлено попарное аминокислотное выравнивание последовательностей бета-цепи MASP-2 (бета-цепь: а/к 444-686 в SEQ ID NO: 5) и MASP-3 (бета-цепь: а/к 449-728 в SEQ ID NO: 8). Области идентичности на фигурах 5-7 указаны пунктирными рамками, окружающими идентичные аминокислоты (указанные символом ".").
Процент идентичности альфа- и бета-цепей белков MASP-1, MASP-2 и MASP-3 человека представлен в таблице 1 ниже.
Процент идентичности белков MASP человека
Что касается альфа-цепей (тяжелых цепей), как указано выше в таблице 1, альфа-цепи MASP-1 и MASP-3 являются идентичными (за исключением последовательности из 15 аминокислот на 3'-конце). Общий % идентичности альфа-цепи MASP-2 и MASP-3 составляет 45,4% с несколькими участками идентичности в доменах CUBI-EGF-CUBII, как показано на фигуре 5.
Что касается бета-цепей (легких цепей), общий процент идентичности трех бета-цепей является низким в диапазоне от 27% до 28%. Однако, хотя общая идентичность трех B-цепей является низкой, есть несколько участков идентичности, как показано на фигуре 6. Как дополнительно показано на фигурах 7A-C, идентичные участки последовательности более обширно распределены между MASP-2 и 3, чем между 1 и 2 или 1 и 3.
Все остатки цистеина, присутствующие в MASP-2, MASP-3, C1r и C1s выравнивают с эквивалентными остатками в MASP-1; однако MASP-1 содержит два остатка цистеина (в положениях 465 и 481 L-цепи), не обнаруживаемые в MASP-2, MASP-3, C1r и C1s. Эти два остатка цистеина в MASP-1 находятся в ожидаемых положениях, используемых для образования "гистидиновой петли" дисульфидного мостика, как обнаруживают в трипсине и химотрипсине. Это позволяет предполагать, что MASP-2, MASP-3, C1r, и C1s могли эволюционировать посредством дупликации генов и дивергенции из MASP-1 (Nonaka & Miyazawa, Genome Biology 3 Reviews 1001.1-1001.5 (2001)).
5. Соответствующие биологические функции/активности, включая соответствующие данные о генетике человека
Роль комплексов MBL/фиколин-MASP во врожденном иммунитете опосредована кальций-зависимым связыванием лектиновых доменов C-типа (присутствующих в молекуле MBL) или связыванием фибриногеноподобных доменов (присутствующих в молекуле фиколина) с углеводными структурами, обнаруживаемыми у дрожжей, бактерий, вирусов и грибков. Эта фаза распознавания приводит к активации профермента MASP-2, имитирующего действие активированного C1s в комплексе C1q-(C1r)2-(C1s)2 посредством расщепления C4 и C2 для образования конвертазы C3 C4b2b. Это делает возможным накопление C4b и C3b на патогенах-мишенях и, таким образом, стимулирует гибель и клиренс посредством фагоцитоза.
Данные в современной литературе позволяют предполагать, что для комплекса активации лектинового пути необходима только активность MASP-2 для расщепления C4 и C2: i) восстановление минимального комплекса активации лектинового пути с использованием рекомбинантного MBL и рекомбинантно экспрессирующейся MASP-2, по-видимому, является достаточным для эффективного расщепления C4 и C2 in vitro (Vorup-Jensen et al., J. Immunol 165:2093-2100 (2000); Rossi et al., J Biol Chem 276:40880-40887 (2001); Ambrus et al, J Immunol 170: 1374-1382 (2003); Gal et al, J Biol Chem 280:33435-33444 (2005)); хотя ii) сыворотка мышей с генетическим дефектом MASP-2 лишена какой-либо функциональной активности лектинового пути (Schwaeble et al, PNAS 108:7523-7528 (2011)). Недавно описан генетически детерминированный дефицит MASP-2 (Stengaard-Pedersen et al, New Eng. J. Med. 349:554-560, (2003)). Мутация одного нуклеотида приводит к замене Asp-Gly в домене CUB1 и делает MASP-2 неспособной к связыванию с MBL.
Кроме того, определение функциональных свойств сывороток мышей с дефицитом MASP-1 и MASP-3, показывает, что активность лектинового пути является более медленной, но не отсутствует, по сравнению с сыворотками мышей дикого типа и нокаутных по MASP-1/MASP-3 (MASP-1/3-/-) мышей в физиологических условиях (Takahashi et al., J. Immunol 180:6132-6138 (2008); Schwaeble et al, PNAS (2011)). Эти исследования позволяют предполагать, что в отличие от эффекторной эндопептидазы классического пути C1s, активация MASP-2 необязательно включает или требует активности какой-либо из других MBL-ассоциированных сериновых эндопептидаз (т.е. MASP-1 или MASP-3), и что протеолитической активности MASP-2 достаточно для перевода связывания распознающих углеводы молекул лектинового пути (т.е. MBL, фиколинов или CL-11) в активацию комплемента. Однако недавние исследования показали, что, хотя MASP-2 не обладает способностью к аутоактивации, скорость каталитической реакции активации MASP-1 зимогена MASP-2 превышает скорость расщепления MASP-2 собственного зимогена приблизительно в 85000 раз (Heja et al, PNAS 106: 10498-503 (2011); Megyeri et al, J. Biol. Chem. 288(13):8922-34 (2013)). Таким образом, вероятно, что первичным активатором MASP-2 в физиологических условиях является MASP-1. Как можно судить по размеру фрагментов образующегося C4 и функциональной активности образующейся конвертазы C3, вероятно, активированная MASP-2 расщепляет C4 и C2 идентично действию активированного C1s, т.е. по одной аргиниловой связи (Arg76 Ala77) в альфа-цепи C4 и по одной аргиниловой связи (Arg223 Lys224) в цепи профермента C2. Также сообщают, что MASP мыши (в форме комплекса MBL-MASP мыши, обозначаемого как Ra-реактивный фактор), в отличие от C1s, может расщеплять альфа-цепь компонента комплемента C3 с образованием биологически активных фрагментов C3a и C3b (Ogata et al, J. Immunol 154:2351-2357 (1995)). Если это происходит у человека, то для этого необходимо расщепление одной аргиниловой связи (Arg77 Ser78) в альфа-цепи C3. Активированная MASP-2, как и активированный C1s, неспособна расщеплять компонент комплемента C5. Протеолитические активности MASP-1 и MASP-2 ингибируют ингибитором C1 (Matsushita et al., J Immunol 165:2637-2642 (2000), в то время как ингибитор C1 не реагирует с MASP-3 (Dahl et al, Immunity 15: 127-135 (2001); Zundel et al, J Immunol 172:4342-4350 (2004)).
Биологические функции MASP-1 и MASP-3 выявляли медленно. Субстратная специфичность и физиологическая роль MASP-1 является предметом споров с момента ее открытия. В последние годы идентифицировали несколько потенциальных субстратов. Предполагали, что MASP-1 может медленно расщеплять нативный C3, и это прямое расщепление C3 может инициировать каскад комплемента, возможно, с участием альтернативного пути (Matsushita et al., J Immunol 165:2637-2642 (2000)). В дальнейшем было показано, что рекомбинантная MASP-1 расщепляет неактивную форму (с гидролизованной тиоэфирной связью) C3, непродуктивную в отношении инициирования каскада комплемента (Ambrus et al., J Immunol 170: 1374-1382 (2003)). Учитывая дефицит активности лектинового пути в разведениях сыворотки мышей с дефицитом MASP-2, однозначно доказали, что запускаемого MASP-1 механизма в обход C3 не существует (Schwaeble et al, PNAS 108:7523-7528 (2011)). Компонентами комплемента, расщепляемыми MASP-1 со значительной эффективностью, являются C2 (Rossi et al, J Biol Chem 276:40880-40887 (2001); Ambrus et al, J Immunol 170: 1374-1382 (2003)) и зимоген фактора D (Takahashi et al., J Exp Med 207:29-37 (2010)). Как и в случае способности MASP-1 расщеплять C2, возможно, таким образом, что MASP-1 может повышать способность MASP-2 к образованию конвертазы C3 (C4b2a) посредством расщепления C2. Это предположение подтверждают данные о том, что активность лектинового пути снижается в MASP-1-обедненной сыворотке человека и в сыворотке мышей с дефицитом MASP-1/3 (Takahashi et al., J Immunol 180:6132-6138 (2008)), эти данные также подтверждают, что MASP-1 играет роль в активации MASP-2. Кроме того, хотя каждый C4b, депонируемый комплексом MBL-MASP, может образовывать конвертазу C4b2a, только один из четырех C4b, депонируемых комплексом C1 классического пути, может делать то же самое (Rawal et al., J Biol Chem 283 (12):7853-63 (2008)).
MASP-1 также расщепляет MASP-2 и MASP-3 (Megyeri M., et al, J Biol Chem. 2013 Mar 29;288(13):8922-34). Недавние эксперименты подтверждают, что, хотя MASP-2 может аутоактивироваться, MASP-1 является первичным активатором зимогена MASP-2. Активация MASP-2 замедляется в сыворотке нокаутных по MASP-1 мышей (Takahashi et al., J Immunol 180: 6132-6138 (2008)), и аналогичные результаты получали, когда активность MASP-1 блокировали специфичным ингибитором в нормальной сыворотке человека (Kocsis et al., J Immunol 185(7):4169-78 (2010)). Кроме того, Degn et al. (J. Immunol. 189(8): 3957-69 (2012)) обнаруживали, что MASP-1 является критичной для активации MASP-2 и последующего расщепления C4 в сыворотке человека. Скорость каталитической реакции конвертации зимогена MASP-2 в активную MASP-2 более чем в 85000 раз выше скорости, с которой MASP-2 может аутоактивироваться (Megyeri et al, J. Biol. Chem. 288:8922-8934 (2013); Heja et al, J. Biol. Chem. 287(24):20290-300 (2012); Heja et al, PNAS 109: 10498-503 (2012)).
В последних исследованиях MASP-1 также связывали с альтернативным путем. MASP-1 может конвертировать зимоген фактора D в его ферментативно активную форму (Фигура 39; Takahashi et al, J Exp Med 207:29-37 (2010)). Кроме того, MASP-1 активирует зимоген MASP-3 (Megyeri et al, J. Biol. Chem. 288:8922-8934 (2013); Degn et al. J. Immunol. 189(8): 3957-69 (2012)), который самостоятельно может активировать зимоген фактора D (фигура 39), а также расщеплять фактор B, другой важный компонент альтернативного пути, до его активной формы (Iwaki et al., J. Immunol. 187:3751-58 (2011)). Однако, вероятно, что конвертация про-фактора D и про-фактора B не зависит от состояния активации LEA-2 и может происходить через не связанную с комплексами MASP-1.
Некоторые данные показывают, что MASP-1 является тромбиноподобным ферментом и важна для активации пути свертывания крови. MASP-1 может расщеплять некоторые субстраты тромбина, включая фибриноген (Hajela K. et al., Immunobiology 205(4-5):467-75 (2002)), фактор XIII (Krarup et al, Biochim Biophys Acta 1784(9): 1294-1300 (2008)) и активируемый протеазами рецептор 4 (PAR4) (Megyeri et al., J Immunol 183(5):3409-16 (2009)). Кроме того, антитромбин в присутствие гепарина является более эффективным ингибитором MASP-1, чем ингибитор C1 (Dobo et al, J Immunol 183: 1207-1214 (2009)). Связь между комплементом и путем свертывания крови также подтверждается данными о том, что MASP-2 способна активировать протромбин (Krarup A. et al, PLoS One 2(7):e623 (2007)). Ограниченное свертывание крови представляет собой древний тип врожденного иммунитета, когда распространение поступающих патогенов предотвращается образованием фибринового тромба. Высвобождающийся фибринопептид B обладает провоспалительной активностью. Опосредованное MASP-1 расщепление PAR4 активирует инициируемую эндотелиальными клетками воспалительную реакцию (Megyeri et al, J Immunol 183(5):3409-16 (2009)).
MASP-3 не обладает протеолитической активностью в отношении субстратов C4, C2 или C3. В отличие от этого, сообщали, что MASP-3 действует как ингибитор лектинового пути (Dahl et al., Immunity 15: 127-135 (2001)). Этот вывод может проистекать из того, что в отличие от MASP-1 и MASP-2, MASP-3 не является аутоактивирующимся ферментом (Zundel S. et al, J Immunol 172:4342-4350 (2004); Megyeri et al, J. Biol. Chem. 288:8922-8934 (2013).
Недавно при исследованиях трансгенных мышей с использованием линии мышей с комбинированным дефицитом MASP-1 и MASP-3 получили доказательство физиологических функций MASP-1 и MASP-3. Хотя у нокаутных по MASP-1/3 мышей есть функциональный лектиновый путь (Schwaeble et al, PNAS 108:7523-7528 (2011)), по-видимому, у них отсутствует активность альтернативного пути (Takahashi et al, JEM 207(1):29-37 (2010)). Вероятно, отсутствие активности альтернативного пути является результатом дефекта процессинга фактора D комплемента, необходимого для активности альтернативного пути. У нокаутных по MASP-1/3 мышей весь фактор D циркулирует в виде протеолитически неактивной про-формы, в то время как в сыворотке нормальных мышей, по существу весь фактор D находится в активной форме. С помощью биохимического анализа подтверждали, что MASP-1 может быть способна конвертировать фактор D комплемента из его зимогена в ферментативно активную форму (Фигура 39; Takahashi et al, JEM 207(1):29-37 (2010)). MASP-3 также расщепляет зимоген про-фактора D и приводит к образованию активного фактора D in vitro (фигура 39; Takahashi et al, JEM 207(1):29-37 (2010)). Фактор D присутствует в виде активного фермента в кровотоке у нормальных индивидуумов, и MASP-1 и MASP-3, а также HTRA-1, могут отвечать за его активацию. Кроме того, мыши с комбинированными дефицитами MBL и фиколина все равно продуцируют нормальные уровни фактора D и имеют полностью функциональный альтернативный путь. Таким образом, эти физиологические функции MASP-1 и MASP-3 необязательно вовлекают лектины и, таким образом, не относятся к лектиновому пути. Рекомбинантная MASP-3 мыши и человека, по-видимому, также расщепляет фактор B и поддерживает накопление C3 на S. aureus in vitro (фигура 36; Iwaki D. et al, J Immunol 187(7):3751-8 (2011)).
В недавних исследованиях пациентов с синдромом 3MC (ранее обозначаемым как синдром Carnevale, Mingarelli, Malpuech и Michels; OMIM № 257920) обнаруживали неожиданную физиологическую роль MASP-3. У этих пациентов наблюдали тяжелые аномалии развития, включая волчью пасть, заячью губу, мальформации черепа и задержку умственного развития. С помощью генетического анализа определяли, что пациенты с 3MC являлись гомозиготами по нефункциональному гену MASP-3 (Rooryck et al, Nat Genet. 43(3): 197-203 (2011)). Обнаруживали, что пациенты с 3MC из другой группы являлись гомозиготами по мутации гена MASP-1, приводящей к отсутствию функциональных белков MASP-1 и MASP-3. У пациентов с 3MC из еще одной группы отсутствовал функциональный ген CL-11 (Rooryck et al., Nat Genet. 43(3): 197-203 (2011)). Таким образом, ось CL-11-MASP-3, по-видимому, играет роль в эмбриональном развитии. Молекулярные механизмы этого пути развития неясны. Однако, маловероятно, что он опосредуется общепринятым запускаемым комплементом процессом, т.к. у индивидуумов с дефицитами общепринятых компонентов комплемента C3 не развивается этот синдром. Таким образом, как представлено в настоящем описании, до открытия авторов настоящего изобретения функциональная роль MASP-3 в лектин-зависимой активации комплемента не была установлена.
Структуры каталитического фрагмента MASP-1 и MASP-2 определяли с помощью рентгенокристаллографии. При структурном сравнении протеазного домена MASP-1 с таковыми в других протеазах комплемента выявляли основу ее ослабленной субстратной специфичности (Dobo et al, J. Immunol 183: 1207-1214 (2009)). Хотя доступность связывающей субстрат борозды MASP-2 ограничена поверхностными петлями (Harmat et al, JMol Biol 342: 1533-1546 (2004)), MASP-1 имеет открытый связывающий субстрат карман, похожий на таковой в трипсине, а не в других протеазах комплемента. Тромбиноподобным свойством структуры MASP-1 является наличие необычно большой петли в 60 аминокислот (петли B), которая может взаимодействовать с субстратами. Другим интересным свойством структуры MASP-1 является внутренний солевой мостик между SI Asp189 и Arg224. Аналогичный солевой мостик можно найти в связывающем субстрат кармане фактора D, который может регулировать свою протеазную активность. C1s и MASP-2 имеют почти идентичные субстратные специфичности. Неожиданно, что некоторые из восьми поверхностных петель MASP-2, определяющих субстратную специфичность, имеют совершенно другие конформации по сравнению с таковыми в C1s. Это означает, что два функционально родственных фермента взаимодействуют с одними и теми же субстратами разными способами. В структуре зимогена MASP-2 обнаруживали неактивный протеазный домен с разрушенным оксианионным отверстием и связывающим субстрат карманом (Gal et al, J Biol Chem 280:33435-33444 (2005)). Неожиданно, зимоген MASP-2 демонстрирует существенную активность в отношении большого белкового субстрата, C4. Вероятно, структура зимогена MASP-2 является довольно гибкой, делающей возможным переход между неактивной и активной формами. Эта гибкость, отраженная в структуре, может играть роль в процессе аутоактивации.
Анализ нозерн-блоттинга показывает, что печень является основным источником мРНК MASP-1 и MASP-2. Используя 5'-специфичный зонд кДНК для MASP-1, получали основной транскрипт MASP-1 размером 4,8 т.п.н. и минорный транскрипт размером приблизительно 3,4 т.п.н., оба присутствовали в печени человека и мыши (Stover et al, Genes Immunity 4:374-84 (2003)). В ткани печени избыточно экспрессировались мРНК MASP-2 (2,6 т.п.н.) и мРНК MAp19 (1,0 т.п.н.). MASP-3 экспрессировалась в печени, а также во многих других тканях, включая нервную ткань (Lynch N. J. et al, J Immunol 174:4998-5006 (2005)).
Обнаруживали, что пациент с инфекциями и хроническим воспалительным заболеванием в анамнезе имеет мутантную форму MASP-2, неспособную образовывать активный комплекс MBL-MASP (Stengaard-Pedersen et al, N Engl J Med 349:554-560 (2003)). Некоторые исследователи определяли, что дефицит MBL приводит к склонности к частым инфекциям в детстве (Super et al, Lancet 2: 1236-1239 (1989); Garred et al, Lancet 346:941-943 (1995) и сниженной устойчивости к ВИЧ-инфекции (Nielsen et al., Clin Exp Immunol 100:219-222 (1995); Garred et al, Mol Immunol 33 (suppl 1):8 (1996)). Однако в других исследованиях не показали значимой корреляции низких уровней MBL с усилением инфекций (Egli et al, PLoS One. 8(1):e51983(2013); Ruskamp et al, J Infect Dis. 198(11): 1707-13 (2008); Israels et al, Arch Dis Child Fetal Neonatal Ed. 95(6):F452-61 (2010)). Хотя в литературе мнения смешаны, дефицит или неиспользование MASP может оказывать неблагоприятное воздействие на способность индивидуума осуществлять немедленную антитело-независимую защиту от конкретных патогенов.
iii. Подтверждающие данные для нового понимания, пересмотр общепринятых условий анализа в отсутствие Ca++ и результаты, полученные с использованием более физиологического набора условий, включающих Ca++
В настоящем описании представлено несколько независимых линий убедительных экспериментальных доказательств, указывающих на то, что лектиновый путь активации комплемента активирует комплемент посредством двух независимых эффекторных механизмов: i) LEA-2: запускаемый MASP-2 путь, опосредующий запускаемую комплементом опсонизацию, хемотаксис (Schwaeble et al., PNAS 108:7523-7528 (2011)) и лизис клеток, и ii) LEA-1: новый MASP-3-зависимый путь активации, инициирующий активацию комплемента с помощью образования конвертазы альтернативного пути C3bBb через расщепление и активацию фактора B на поверхности активатора, затем катализирующего накопление C3b и образование конвертазы альтернативного пути C3bBb, что может приводить к лизису клеток, а также опсонизации микроорганизмов. Кроме того, как представлено в настоящем описании, раздельная лектин-независимая активация фактора B и/или фактора D MASP-1, MASP-3, или HTRA-1 или комбинацией любых из них трех также может приводить к активации комплемента через альтернативный путь.
По-видимому, лектин-зависимая запускаемая MASP-3 активация альтернативного пути участвует в общепринятом опосредуемом фактором D расщеплении C3b-связанного фактора B для достижения оптимальной скорости активации комплемент-зависимого лизиса через терминальный каскад активации для лизиса бактериальных клеток посредством образования мембраноатакующих комплексов (MAC) C5b-9 на поверхности клеток (фигуры 14-15). По-видимому, для этого скорость-лимитирующего процесса необходима оптимальная координация, т.к. он является дефектным в отсутствие функциональной активности MASP-3, а также в отсутствие функциональной активности фактора D. Как описано в примерах 1-4 в настоящем описании, авторы настоящего изобретения обнаруживали эту MASP-3-зависимую функцию лектинового пути при исследовании фенотипа дефицита MASP-2 и ингибирования MASP-2 на экспериментальных моделях мыши с инфекцией N. meningitidis. Генетически дефектные по MASP-2 мыши и мыши дикого типа, обработанные ингибиторами MASP-2 на основе антител, являлись высоко резистентными к экспериментальной инфекции N. meningitidis (см. фигуры 8-12). Когда инфекционную дозу корректировали для достижения смертности приблизительно 60% у однопометных животных дикого типа, у всех мышей с дефицитом MASP-2 или MASP-2-обедненных мышей инфекция подвергалась клиренсу, и они выживали (см. фигуру 8 и фигуру 12). Эта крайняя степень резистентности отражалась в значимом повышении бактерицидной активности сыворотки мышей с дефицитом MASP-2 или MASP-2-обедненных мышей. Дальнейшие эксперименты показали, что эта бактерицидная активность зависела от запускаемого альтернативным путем лизиса бактерий. Сыворотки мышей с дефицитом фактора B, или фактора D, или C3 не проявляли бактерицидной активности в отношении N. meningitidis, что свидетельствует о том, что альтернативный путь необходим для запуска терминального каскада активации. Неожиданным результатом являлось то, что сыворотки мышей с дефицитом MBL-A и MBL-C (являющихся распознающими молекулами лектинового пути, распознающими N. meningitidis), а также сыворотки мышей с дефицитом ассоциированных с лектиновым путем сериновых протеаз MASP-1 и MASP-3 утрачивали всю бактериолитическую активность в отношении N. meningitidis (Фигура 15). В недавно опубликованной статье (Takahashi M. et al, JE 207: 29-37 (2010)) и исследовании, представленном в настоящем описании (фигура 39), показали, что MASP-1 может конвертировать зимоген фактора D в его ферментативно активную форму, и можно частично объяснить утрату литической активности отсутствием ферментативно активного фактора D в этих сыворотках. Это не объясняет отсутствия бактерицидной активности у мышей с дефицитом MBL, т.к. эти мыши имеют нормальный ферментативно активный фактор D (Banda et al., Mol Imunol 49(l-2):281-9 (2011)). Поразительно, что при тестировании сывороток человека от пациентов с редким аутосомно рецессивным нарушением 3MC (Rooryck C, et al, Nat Genet. 43(3): 197-203) с мутациями, делающими домен сериновой протеазы MASP-3 нефункциональным, не определяли бактерицидную активность в отношении N. meningitidis (N.B.: Эти сыворотки содержали MASP-1 и фактор D, но не MASP-3).
Гипотезу о том, что сыворотке человека необходима опосредуемая лектиновым путем MASP-3-зависимая активность для развития бактерицидной активности, дополнительно подтверждают данные о том, что сыворотки людей с дефицитом MBL также не могут лизировать N. meningitidis (фигуры 13-14). MBL является единственной распознающей молекулой лектинового пути человека, связывающейся с этим патогеном. Поскольку MASP-3 не аутоактивируется, авторы настоящего изобретения выдвинули гипотезу о том, что более высокую бактериолитическую активность в сыворотках при дефиците MASP-2 можно объяснить предпочтительной активацией MASP-3 через MASP-1, т.к. в отсутствие MASP-2 все комплексы активации лектинового пути, связывающиеся с поверхностью бактерий, будут нагружены MASP-1 или MASP-3. Поскольку активированная MASP-3 расщепляет фактор D (фигура 39) и фактор B с образованием соответствующих ферментативно активных форм in vitro (фигура 37 и Iwaki D., et al, J. Immunol.187(7):3751-3758 (2011)), наиболее вероятной функцией MASP-3 является облегчение образования конвертазы C3 альтернативного пути (т.е. C3bBb).
Хотя данные о лектин-зависимой роли являются убедительными, многочисленные эксперименты позволяют предполагать, что MASP-3 и MASP-1 не являются обязательными для функционирования в комплексе с молекулами лектинов. Эксперименты, такие как показано на фигуре 35B, демонстрируют способность MASP-3 активировать альтернативный путь (что демонстрирует накопление C3b на S. aureus) в условиях (т.е. в присутствие EGTA), в которых комплексы с лектином не будут присутствовать. На фигуре 35A показано, что накопление в этих условиях зависит от фактора B, фактора D и фактора P, всех критических компонентов альтернативного пути. Кроме того, активация фактора D MASP-3 и MASP-1 (фигура 39) и активация фактора B MASP-3 (фигура 37) может происходить in vitro в отсутствие лектина. В конечном итоге, исследования гемолиза эритроцитов мыши в присутствие сыворотки человека демонстрируют очевидную роль MBL и MASP-3 в лизисе клеток. Однако дефицит MBL не полностью воспроизводит тяжесть дефицита MASP-3, в отличие от ожидаемого в случае, если все функциональные MASP-3 образовали комплексы с MBL. Таким образом, авторы настоящего изобретения не хотят быть ограниченными мнением о том, что все роли MASP-3 (и MASP-1), представленные в настоящем описании, можно отнести исключительно к функции, ассоциированной с лектином.
Идентификация двух эффекторных ветвей лектинового пути, а также возможных лектин-независимых функций MASP-1, MASP-3 и HTRA-1 открывает новые возможности для терапевтических вмешательств с целью эффективного лечения определенных патологий человека, вызываемых избыточной активацией комплемента в присутствие микробиологических патогенов, или измененных клеток хозяина или метаболических отложений. Как представлено в настоящем описании, авторы настоящего изобретения к настоящему времени обнаружили, что в отсутствие MASP-3 и в присутствие MASP-1 альтернативный путь не активируется на поверхностных структурах (см. фигуры 17-18, 35B, 41-42, 45-46). Поскольку альтернативный путь важен для запуска скорость-лимитирующих событий, приводящих к бактериальному лизису, а также лизису клеток (Mathieson PW, et al, J Exp Med 177(6): 1827-3 (1993)), представленные результаты свидетельствуют о том, что активированная MASP-3 играет важную роль в литической активности комплемента. Как показано на фигурах 14-15, 21-23, 43-44 и 46-47, в сыворотке пациентов с 3MC с дефицитом MASP-3, но не MASP-1, активация литического терминального каскада комплемента является дефектной. Данные, представленные на фигурах 14 и 15, свидетельствуют об утрате бактериолитической активности в отсутствие функциональной активности MASP-3 и/или MASP-1/MASP-3. Аналогично, утрата гемолитической активности в сыворотке человека с дефицитом MASP-3 (фигуры 21-23, 43-44 и 46-47), совместно со способностью восстанавливать гемолиз посредством добавления рекомбинантной MASP-3 (фигуры 46-47), убедительно подтверждает вывод о том, что активация альтернативного пути на поверхностях мишеней (необходимых для запуска опосредованного комплементом лизиса) зависит от присутствия активированной MASP-3. Учитывая новое понимание лектинового пути, подробно описанное выше, активация альтернативного пути поверхностями мишеней, таким образом, зависит от LEA-1 и/или лектин-независимой активации фактора B и/или фактора D, также опосредуемой MASP-3, и, таким образом, средства, блокирующие MASP-3-зависимую активацию комплемента, будут предотвращать активацию альтернативного пути на поверхностях мишеней.
Описывая важную роль MASP-3-зависимой инициации активации альтернативного пути, предполагают, что альтернативный путь не является независимым, отдельным путем активации комплемента, как описано по существу во всех современных медицинских руководствах и недавно опубликованных обзорных статьях на тему комплемента. Современной и распространенной научной точкой зрения является то, что альтернативный путь активируется на поверхности конкретных мишеней в виде частиц (микроорганизмов, зимозана и эритроцитов кролика) посредством амплификации спонтанной "tick-over" активации C3. Однако, отсутствие какой-либо активации альтернативного пути в сыворотках мышей с двойным дефицитом MASP-1 и MASP-3 и сыворотке людей с 3MC на покрытых зимозаном планшетах и двух различных бактериях (N. meningitidis и S. aureus) и снижение гемолиза эритроцитов в сыворотке человека и мыши с дефицитом MASP-3 свидетельствуют о том, что для инициации активации альтернативного пути на этих поверхностях необходима функциональная MASP-3. Необходимая функция MASP-3 может являться лектин-зависимой или независимой и приводит к образованию комплексов конвертаз C3 и C5 альтернативного пути, т.е. C3bBb и C3bBb(C3b)n, соответственно. Таким образом, авторы настоящего изобретения описывают существование ранее неописанных путей инициации альтернативного пути. Этот путь инициация зависит от (i) LEA-1, недавно обнаруженной ветви активации лектинового пути, и/или (ii) лектин-независимых функций белков MASP-3, MASP-1 и HTRA-1.
III. РОЛЬ MASP-2 И MASP-3 В ПАРОКСИЗМАЛЬНОЙ НОЧНОЙ ГЕМОГЛОБИНУРИИ И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
i. Обзор PNH
Пароксизмальная ночная гемоглобинурия (PNH), иногда также обозначаемая как синдром Маркиафавы-Микели, является острым, потенциально угрожающим жизни заболеванием крови. PNH может развиваться самостоятельно, в этом случае ее обозначают как "первичную PNH", или на фоне других нарушений костного мозга, таких как апластическая анемия, в этом случае ее обозначают как "вторичную PNH". В большинстве случаев она является первичной PNH. PNH отличается индуцируемой комплементом деструкцией эритроцитов (гемолизом), низким количеством эритроцитов (анемией), тромбозом и недостаточностью костного мозга. Лабораторные анализы при PNH свидетельствуют об изменениях, соответствующих внутрисосудистой гемолитической анемии: низком уровне гемоглобина, повышении лактатдегидрогеназы, повышении количества ретикулоцитов (незрелых эритроцитов, высвобождаемых костным мозгом на замену разрушенным клеткам), повышении билирубина (продукта распада гемоглобина) в отсутствие аутореактивных связывающихся с RBC антител в качестве возможной причины.
Отличительной чертой PNH является хронический опосредованный комплементом гемолиз, вызываемый нерегулируемой активацией терминальных компонентов комплемента, включая мембраноатакующий комплекс, на поверхности циркулирующих RBC. RBC при PNH являются объектом неконтролируемой активации комплемента и гемолиза по причине отсутствия регуляторов комплемента CD55 и CD59 на их поверхности (Lindorfer, M.A., et al, Blood 115(11):2283-91 (2010), Risitano, et al, Mini-Reviews in Medicinal Chemistry, 11:528-535 (2011)). CD55 и CD59 в большом количестве экспрессируются на нормальных RBC и контролируют активацию комплемента. CD55 действует в качестве негативного регулятора альтернативного пути, ингибируя сборку комплекса конвертазы C3 альтернативного пути (C3bBb) и усиливая распад уже образовавшейся конвертазы, таким образом, блокируя образование мембраноатакующего комплекса (MAC). CD59 напрямую ингибирует мембраноатакующий комплекс комплемента, связываясь с комплексом C5b678 и предотвращая связывание и полимеризацию C9.
Хотя гемолиз и анемия являются доминирующими клиническими признаками PNH, заболевание является комплексным гематологическим нарушением, помимо этого включающим тромбоз и недостаточность костного мозга как часть клинических данных (Risitano et al, Mini Reviews in Med Cheml l:528-535 (2011)). На молекулярном уровне PNH вызывается аномальной клональной экспансией гемопоэтических стволовых клеток с отсутствием функционального гена PIG A. PIG A является X-сцепленным геном, кодирующим гликозил-фосфатидилинозитолтрансферазу, необходимую для стабильной поверхностной экспрессии GPI-заякоренных гликопротеинов класса A, включая CD55 и CD59. По причинам, в настоящее время являющимся объектом исследований, гемопоэтические стволовые клетки с нефункциональным геном PIG A, образующимся в результате спонтанных соматических мутаций, могут подвергаться клональной экспансии до этапа, когда их потомки составляют значительную часть периферического пула гематопоэтических клеток. Хотя в потомках и эритроцитов, и лимфоцитов от мутантного клона стволовой клетки отсутствуют CD55 и CD59, только RBC подвергаются выраженному лизису после входа в кровоток.
Современное лечение PNH включает переливание крови от анемии, антикоагулянты от тромбоза и использование моноклонального антитела экулизумаб (Soliris®), защищающего клетки крови от деструкции иммунными клетками посредством ингибирования системы комплемента (Hillmen P. et al, N. Engl. J. Med. 350(6):552-559 (2004)). Экулизумаб (Soliris®) является гуманизированным моноклональным антителом против компонента комплемента C5, блокирующим его расщепление конвертазами C5, таким образом, предотвращающим продукцию C5a и сборку MAC. Лечение пациентов PNH экулизумабом приводит к снижению внутрисосудистого гемолиза, измеряемого по лактатдегидрогеназе (LDH), приводящему к стабилизации гемоглобина и независимости от переливаний крови приблизительно у половины пациентов (Risitano et al, Mini-Reviews in Medicinal Chemistry, 11(6) (2011)). Хотя почти все пациенты, подвергаемые терапии экулизумабом, достигают нормальных или почти нормальных уровней LDH (благодаря контролю внутрисосудистого гемолиза), только приблизительно треть пациентов достигает уровней гемоглобина приблизительно 11 г/дл, и оставшиеся пациенты, подвергаемые терапии экулизумабом, продолжают проявлять анемию от умеренной до тяжелой (т.е. зависимую от переливаний крови) приблизительно в равных пропорциях (Risitano A.M. et al, Blood 113:4094-100 (2009)). Как описано в Risitano et al, Mini-Reviews in Medicinal Chemistry 11:528-535 (2011), показано, что пациенты с PNH, подвергаемые терапии экулизумабом, имеют большие количества фрагментов C3, связывающихся с их эритроцитам (в отличие от не подвергнутых лечению пациентов). Эти данные привели к выводу о том, что у пациентов с PNH, подвергнутых терапии Soliris, RBC, далее не подвергающиеся гемолизу в результате блокады C5, теперь могут накапливать большое количество мембраносвязанных фрагментов C3, действующих как опсонины, что приводит к их захвату клетками ретикулоэндотелиальной системы через специфичные рецепторы C3 и последующему внесосудистому гемолизу. Таким образом, одновременно предотвращая внутрисосудистый гемолиз и последующие осложнения, терапия экулизумабом просто перенаправляет предрасположенность этих RBC с внутрисосудистого во внесосудистый гемолиз, что приводит к значительной остаточной неподвергнутой лечению анемии у многих пациентов (Risitano A.M. et al, Blood 113:4094-100 (2009)). Таким образом, необходимы терапевтические стратегии в дополнение к применению экулизумаба для тех пациентов, у которых развивается опосредуемый фрагментами C3 внесосудистый гемолиз, т.к. они продолжают нуждаться в переливаниях эритроцитов. Такие подходы, нацеленные на фрагменты C3, показали свою применимость в экспериментальных системах (Lindorfer et al., Blood 115:2283-91, 2010).
ii. Комплемент-инициирующие механизмы PNH
Причинная связь между дефектной поверхностной экспрессией негативных регуляторов комплемента CD55 и CD59 при PNH в комбинации с эффективностью экулизумаба в профилактике внутрисосудистого гемолиза позволяет четко определять PNH как состояние, опосредуемое системой комплемента. Хотя эта парадигма является широко распространенной, природа явлений, инициирующих активацию комплемента, и вовлеченные в нее пути активации комплемента остаются неясными. Поскольку CD55 и CD59 негативно регулируют терминальные этапы амплификации каскада комплемента, общие для всех путей инициации комплемента, недостаточность этих молекул будет приводить к чрезмерному образованию и интеграции в мембраны мембраноатакующих комплексов независимо от того, инициируется ли активация комплемента лектиновым путем, классическим путем или спонтанным циклом альтернативного пути. Таким образом, у пациентов PNH любые события активации комплемента, приводящие к накоплению C3b на поверхности RBC, могут запускать последующую амплификацию и патологический гемолиз (внутрисосудистый и/или внесосудистый) и ускорять гемолитический криз. Ясное понимание механизма молекулярных событий, запускающих гемолитический криз у пациентов с PNH, остается труднодостижимым. По причине отсутствия очевидных комплемент-инициирующих событий у пациентов PNH, у которых развивается гемолитический криз, преобладающее мнение состоит в том, что активация комплемента при PNH может происходить спонтанно вследствие низкоуровневой "tick-over"-активации альтернативного пути, в дальнейшем усиливаемой ненадлежащим контролем терминальной активации комплемента в результате отсутствия CD55 и CD59.
Однако необходимо отметить, что в анамнезе жизни PNH, как правило, развивается или обостряется после конкретных событий, таких как инфекция или травма (Risitano, Biologies 2:205-222 (2008)), которые, как показано, запускают активацию комплемента. Этот ответ с активацией комплемента не зависит от уже существующего иммунитета хозяина в отношении патогена возбудителя и, таким образом, вероятно, не вовлекает классический путь. Скорее, судя по всему, этот ответ с активацией комплемента инициируется связыванием лектина с чужеродными или "собственными измененными" углеводными паттернами, экспрессирующимися на поверхности микроорганизмов или поврежденной ткани хозяина. Таким образом, события, ускоряющие гемолитический криз при PNH, тесно связаны с активацией комплемента, инициируемой лектинами. Это делает очень вероятным то, что лектиновые пути активации представляют собой инициирующий пусковой механизм, в конечном итоге приводящий к гемолизу у пациентов с PNH.
Используя в качестве экспериментальных моделей четко определенные патогены, активирующие комплемент через лектины, для разделения каскадов активации на молекулярном уровне, авторы настоящего изобретения показали, что, в зависимости от микроорганизма-возбудителя, активация комплемента может инициироваться LEA-2 или LEA-1, приводя к опсонизации и/или лизису. Этот принцип двойных ответов (т.е. опсонизации и/или лизиса) на события лектиновой инициации, вероятно, также применим для других типов инфекционных агентов или для активации комплемента лектинами после повреждения ткани хозяина, или других событий запускаемой лектинами активации комплемента, которые могут усиливать PNH. Учитывая эту двойственность лектинового пути, авторы настоящего изобретения делают вывод о том, что инициируемая LEA-2 и/или LEA-1 активация комплемента у пациентов с PNH способствует опсонизации и/или лизису RBC посредством C3b и последующему внесосудистому и внутрисосудистому гемолизу. Таким образом, в случае PNH ожидают, что ингибирование LEA-1 и LEA-2 будет воздействовать на внутрисосудистый и внесосудистый гемолиз, представляя значительное преимущество относительно ингибитора C5 экулизумаба.
Определяли, что воздействие S. pneumoniae запускает преимущественно лектин-зависимую активацию LEA-2, что приводит к опсонизации этого микроорганизма C3b. Поскольку S. pneumoniae устойчива к опосредуемому MAC лизису, ее клиренс из кровотока происходит посредством опсонизации C3b. Эта опсонизация и последующее удаление из кровотока являются LEA-2-зависимыми, на что указывает нарушенный бактериальный контроль у мышей с дефицитом MASP-2 и мышей, обрабатываемых моноклональным антителом против MASP-2 (PLOS Pathog., 8: e1002793. (2012)).
При исследовании роли LEA-2 во врожденных ответах хозяина на микроорганизмы авторы настоящего изобретения тестировали дополнительные патогены. Наблюдали значительно отличающийся результат при исследовании Neisseria meningitidis в качестве модельного организма. N. meningitidis также активирует комплемент через лектины, и для активации комплемента необходим очаг инфекции N. meningitidis у наивного хозяина. Однако LEA-2 не играет защитной функциональной роли в этом ответе: как показано на фигурах 8 и 9, блокада LEA-2 посредством генетической абляции MASP-2 не снижает выживаемость после инфекции N. meningitidis. Наоборот, в этих исследованиях блокада LEA-2 посредством абляции MASP-2 значимо улучшает выживаемость (фигуры 8 и 9), а также индексы заболеваемости (Фигура 11). Блокада LEA-2 посредством введения антитела против MASP-2 приводила к тому же результату (фигура 12), исключая вторичные или компенсаторные эффекты у линии нокаутных мышей в качестве возможной причины. Эти благоприятные исходы у животных, подвергнутых абляции LEA-2, были ассоциированы с более быстрой элиминации N. meningitidis из крови (фигура 10). Кроме того, как представлено в настоящем описании, инкубация N. meningitidis с нормальной сывороткой человека приводила к гибели N. meningitidis (фигура 13). Добавление функционального моноклонального антитела, специфичного для MASP-2 человека, блокирующего LEA-2, но не введение изотипического контрольного моноклонального антитела, может повышать этот элиминационный ответ. Однако этот процесс зависит от лектинов и по меньшей мере частично функциональной системы комплемента, т.к. сыворотка человека с дефицитом MBL или термически инактивированная сыворотка человека были неспособны уничтожать N. meningitidis (фигура 13). В совокупности, эти новые данные позволяют предполагать, что инфекции N. meningitidis в присутствие функциональной системы комплемента контролируются лектин-зависимым, но LEA-2-независимым, путем активации комплемента.
Гипотезу о том, что LEA-1 может являться путем комплемента, ответственным за лектин-зависимую гибель N. meningitidis, тестировали с использованием образца сыворотки от пациента с 3MC. Этот пациент являлся гомозиготным по нонсенс-мутации экзона 12 гена MASP-1/3. В результате у этого пациента отсутствовал функциональный белок MASP-3, но остальные компоненты комплемента являлись достаточными (экзон 12 является специфичным для транскрипта MASP-3; мутация не оказывала эффекта на функцию или уровни экспрессии MASP-1) (см. Nat Genet 43(3): 197-203 (2011)). Нормальная сыворотка человека эффективно уничтожает N. meningitidis, но термически инактивированная сыворотка при дефиците MBL (одной из распознающих молекул лектинового пути) и сыворотка при дефиците MASP-3 были неспособны уничтожать N. meningitidis (фигура 14). Таким образом, LEA-1, по-видимому, опосредует гибель N. meningitidis. Этот результат подтверждали с использованием образцов сыворотки линий нокаутных мышей. Хотя содержащая комплемент нормальная сыворотка мыши легко уничтожала N. meningitidis, сыворотка мыши с дефицитом MBL или дефицитом MASP-1/3 являлась неэффективной, как и термически инактивированная сыворотка, в которой отсутствовал функциональный комплемент (Фигура 15). В отличие от этого, сыворотка при дефиците MASP-2 демонстрировала эффективное уничтожение N. meningitidis.
Эти данные представляют доказательство прежде неизвестной двойственности лектинового пути благодаря обнаружению существования отдельных путей LEA-2 и LEA-1 лектин-зависимой активации комплемента. В примерах подробно описанных выше, LEA-2 и LEA-1 не являются дублирующими и опосредуют различные, функциональные исходы. Данные позволяют предполагать, что конкретные типы активаторов лектинового пути (включая, в качестве неограничивающих примеров, S. pneumoniae) преимущественно инициируют активацию комплемента через LEA-2, что приводит к опсонизации, в то время как другие (например, N. meningitidis) преимущественно инициируют активацию комплемента через LEA-1 и способствуют цитолитическим процессам. Однако данные не ограничивают LEA-2 обязательно опсонизацией, а LEA-1-цитолитическими процессами, т.к. оба пути в других условиях могут опосредовать опсонизацию и/или лизис.
Что касается лектин-зависимой активации комплемента N. meningitidis, ветви LEA-2 и LEA-1, по-видимому, конкурируют друг с другом, т.к. блокада LEA-2 повышала LEA-1-зависимую литическую деструкцию организма in vitro (фигура 15). Как подробно описано выше, этот результат можно объяснить повышенной вероятностью нахождения лектиновых комплексов MASP-1 в непосредственной близости с лектиновыми комплексами MASP-3 в отсутствие MASP-2, что будет усиливать активацию LEA-1 и, таким образом, способствовать более эффективному лизису N. meningitidis. Поскольку лизис N. meningitidis является основным защитным механизмом у наивного хозяина, блокада LEA-2 in vivo повышает клиренс N. meningitidis и приводит к усиленному уничтожению.
Хотя в описанных выше примерах проиллюстрированы противоположные эффекты LEA-2 и LEA-1 в отношении исходов инфекции N. meningitidis, могут иметь место и другие условия, в которых LEA-2 и LEA-1 могут действовать синергично для достижения конкретного исхода. Как подробно описано ниже, в других ситуациях патологической активации комплемента через лектины, таких как при PNH, запускаемая LEA-2 и LEA-1 активация комплемента может объединяться синергичным образом, внося свой вклад в общую патологию PNH. Кроме того, как представлено в настоящем описании, MASP-3 также может участвовать в лектин-независимой конвертации фактора B и фактора D, которая может происходить в отсутствие Ca++, как правило, приводя к конвертации C3bB в C3bBb и про-фактора D в фактор D, которые в дальнейшем могут участвовать в патологии PNH.
iii. Биология и ожидаемая функциональная активность при PNH
В этом разделе описывают ингибиторные эффекты блокады LEA-2 и LEA-1 в отношении гемолиза в модели PNH in vitro. Результаты подтверждают применимость средств, блокирующих LEA-2 (включая, в качестве неограничивающих примеров, антитела, связывающиеся и блокирующие функционирование MASP-2), и средств, блокирующих LEA-1 (включая, в качестве неограничивающих примеров, антитела связывающиеся и блокирующие функционирование опосредованной MASP-1 активации MASP-3, MASP-3 или их обоих), в лечении индивидуумов, страдающих одним или несколькими проявлениями PNH, а также использование ингибиторов LEA-2 и/или LEA-1, и/или MASP-3-зависимой, лектин-независимой активации комплемента (включая ингибиторы MASP-2, ингибиторы MASP-3, ингибиторы с двойной специфичностью или биспецифические ингибиторы MASP-2/MASP-3 или MASP-1 /MASP-2 и панспецифические ингибиторы MASP-1/MASP-2/MASP-3) для снижения эффектов опосредованного фрагментами C3 внесосудистого гемолиза у пациентов с PNH, подвергаемых терапии ингибитором C5, таким как экулизумаб.
iv. Ингибиторы MASP-2 для блокирования опсонизации и внесосудистого гемолиза RBC при PNH через ретикулоэндотелиальную систему
Как подробно описано выше, у пациентов с PNH анемия развивается за счет двух различных механизмов клиренса RBC из кровотока: внутрисосудистого гемолиза посредством активации мембраноатакующих комплексов (MAC) и внесосудистого гемолиза после опсонизации C3b и последующего клиренса после связывания рецептора комплемента и захвата ретикулоэндотелиальной системой. Внутрисосудистый гемолиз, главным образом, предотвращают при лечении пациента экулизумабом. Поскольку экулизумаб блокирует терминальный литический эффекторный механизм, имеющий место в каскаде ниже инициирующей комплемент активации, а также последующей опсонизации, экулизумаб не блокирует внесосудистый гемолиз (Risitano A.M. et al, Blood 113:4094-100 (2009)). Фактически, RBC, которые подвергались бы гемолизу у неподвергнутых лечению пациентов с PNH, теперь могут накапливать на своей поверхности активированные белки C3b, усиливающие захват ретикулоэндотелиальной системой и их внесосудистый гемолиз. Таким образом, лечение экулизумабом эффективно перенаправляет RBC с внутрисосудистого гемолиза в потенциальный внесосудистый гемолиз. В результате, у некоторых пациентов с PNH, подвергнутых лечению экулизумабом, остается анемия. Из этого следует, что средства, блокирующие активацию комплемента выше в каскаде и предотвращающие опсонизацию RBC при PNH, в частности, могут подходить для блокирования внесосудистого гемолиза, иногда наблюдаемого при лечении экулизумабом.
Данные микробиологических анализов, представленные в настоящем описании, позволяют предполагать, что LEA-2 часто является доминирующим путем лектин-зависимой опсонизации. Кроме того, при анализе лектин-зависимой опсонизации (измеряемой по накоплению C3b) с использованием трех прототипных поверхностей для лектиновой активации (маннозы, фигура 19A; зимозана, фигура 19B, и S. pneumoniae; фигура 19C) LEA-2 оказывалась доминирующим путем лектин-зависимой опсонизации в физиологических условиях (т.е. в присутствие Ca++, где все пути комплемента являются функциональными). В этих экспериментальных условиях сыворотка при дефиците MASP-2 (в которой отсутствует LEA-2) по существу являлась менее эффективной в опсонизации тестовых поверхностей, чем сыворотка WT. Сыворотка при дефиците MASP-1/3 (в которой отсутствовал LEA-1) также является дефектной, т.к. ее эффект являлся гораздо менее выраженным по сравнению с сывороткой с отсутствием LEA-2. Относительная степень участия LEA-2 и LEA-1 в запускаемой лектинами опсонизации дополнительно проиллюстрирована на фигурах 20A-20C. Хотя сообщают о том, что альтернативный путь комплемента поддерживает опсонизацию поверхностей, активирующих лектины, в отсутствие лектинового пути или классического пути (Selander et al., J Clin Invest 116(5): 1425-1434 (2006)), альтернативный путь в отдельности (измеряемый в условиях анализа в отсутствие Ca++) оказывается по существу менее эффективным, чем инициируемые LEA-2 и LEA-1 процессы, представленные в настоящем описании. При экстраполяции эти данные позволяют предполагать, что опсонизация RBC при PNH также преимущественно может инициироваться LEA-2, и в меньшей степени LEA-1 (возможно амплифицируемой через петлю амплификации альтернативного пути), чем в результате лектин-независимой активации альтернативного пути. Таким образом, можно ожидать, что ингибиторы LEA-2 будут наиболее эффективными в ограничении опсонизации и профилактике внесосудистого гемолиза при PNH. Однако, понимание того факта, что лектины, иные, чем MBL, такие как фиколины, связываются с неуглеводными структурами, такими как ацетилированные белки, и что MASP-3 предпочтительно связывается с H-фиколином (Skjoedt et al., Immunobiol. 215:921-931, 2010), также оставляет возможность значительной роли LEA-1 в ассоциированной с PNH опсонизации RBC. Таким образом, ожидают, что ингибиторы LEA-1 будут иметь дополнительные антиопсонизирующие эффекты, и ожидают, что комбинация ингибиторов LEA-1 и LEA-2 будет оптимальной и будет опосредовать наиболее сильный благоприятный эффект лечения в отношении ограничения опсонизации и внесосудистого гемолиза у пациентов с PNH. Эту концепцию дополнительно подтверждают данные об опсонизации, представленные на фигуре 28: сыворотка мыши с дефицитом фактора D (у которой отсутствует способность активировать альтернативный путь в жидкой фазе, но есть функциональный классический путь, а также функциональные пути LEA-1 и LEA-2) не проявляет дефицита опсонизации по сравнению с сывороткой WT. Сыворотка при дефиците фактора B, в которой отсутствует LEA-1, проявляет сниженную опсонизацию, в то время как сыворотка при дефиците фактора D, обработанная моноклональным антителом против MASP-2 для блокирования опосредованной LEA-2 активации комплемента, проявляет более сильную супрессию опсонизации (фигура 28). Важно, что добавление моноклонального антитела против MASP-2 в сыворотку при дефиците фактора B подавляло опсонизацию более эффективно, чем блокада MASP-2 или блокада фактора D в отдельности. Таким образом, LEA-2 и LEA-1 действуют аддитивно или синергично для стимуляции опсонизации, и ожидают, что перекрестно-реагирующий или биспецифический ингибитор LEA-1/LEA-2 будет наиболее эффективным в блокировании опсонизации и внесосудистого гемолиза при PNH.
v. Роль ингибиторов MASP-3 при PNH
Используя модель PNH in vitro, авторы настоящего изобретения показали, что активация комплемента и последующий гемолиз при PNH фактически инициируется активацией LEA-2 и/или LEA-1, и это не является независимой функцией альтернативного пути. В этих исследованиях исследовали сенсибилизированные маннозой RBC различных линий мышей, включая RBC мышей с дефицитом Crry (важного негативного регулятора терминального пути комплемента у мышей), а также RBC мышей с дефицитом CD55/CD59, у которых отсутствуют те же регуляторы комплемента, которые отсутствуют у пациентов с PNH). Когда сенсибилизированные маннозой RBC с дефицитом Crry подвергали воздействию сыворотки человека с достаточным комплементом, RBC эффективно подвергались гемолизу при концентрации в сыворотке 3% (фигура 21 и 22), в то время как сыворотка при дефиците комплемента (HI: термически инактивированная) не обладала гемолитическим действием. Удивительно, что сыворотка с достаточным комплементом, в которой LEA-2 блокировали добавлением антитела против MASP-2, имела сниженную гемолитическую активность, и для эффективного гемолиза была необходима 6% сыворотка. Аналогичные результаты получали при тестировании RBC с дефицитом CD55/CD59 (фигура 24). Сыворотка человека с достаточным комплементом, дополненная моноклональным антителом против MASP-2 (т.е. сыворотка, в которой супрессировали LEA-2), являлась приблизительно в два раза менее эффективной в поддержании гемолиза, чем необработанная сыворотка. Кроме того, для стимуляции эффективного гемолиза необработанных RBC WT были необходимы более высокие концентрации сыворотки с блокированным LEA-2 (т.е. обработанной моноклональным антителом против MASP-2) по сравнению с необработанной сывороткой (фигура 23).
Даже более удивительно, что сыворотка пациента с 3MC, гомозиготного по аллелю нефункционального белка MASP-3 (и, таким образом, с отсутствием LEA-1), полностью неспособна гемолизировать сенсибилизированные маннозой RBC с дефицитом Crry (фигура 22 и фигура 23). Аналогичный результат наблюдали при использовании несенсибилизированных нормальных RBC: как показано на фигуре 23, сыворотка при дефиците LEA-1, выделенная из пациента с 3MC, была полностью неэффективна в опосредовании гемолиза. В совокупности, эти данные свидетельствуют о том, что, в то время как LEA-2 в значительной степени участвует в ответе с внутрисосудистым гемолизом, LEA-1 является преобладающим инициирующим комплемент путем, приводящим к гемолизу. Таким образом, хотя ожидают, что средства, блокирующие LEA-2, будут значительно снижать внутрисосудистый гемолиз RBC у пациентов с PNH, ожидают, что средства, блокирующие LEA-1, будут иметь более глубокий эффект и в значительной степени устранять запускаемый комплементом гемолиз.
Следует отметить, что сыворотка пациента с 3MC с дефицитом LEA-1, используемая в этом исследовании, имела ослабленный, но функциональный альтернативный путь при тестировании в условиях общепринятого анализа альтернативного пути (фигура 17). Этот результат позволяет предполагать, что LEA-1 делает больший вклад в гемолиз, чем активность альтернативного пути, как общепринято определяют в этих экспериментальных условиях PNH. В заключение, предполагают, что средства, блокирующие LEA-1 будут по меньшей мере такими же эффективными, как средства, блокирующие другие аспекты альтернативного пути, в профилактике или лечении внутрисосудистого гемолиза у пациентов с PNH.
vi. Роль ингибиторов MASP-2 в PNH
Данные, представленные в настоящем описании, подтверждают следующие патогенетические механизмы анемии при PNH: внутрисосудистый гемолиз по причине нерегулируемой активации терминальных компонентов комплемента и лизиса RBC посредством образования MAC, инициируемых преимущественно, но не исключительно, LEA-1, и внесосудистый гемолиз, вызываемый опсонизацией RBC C3b, по-видимому, инициируемый преимущественно LEA-2. Хотя наблюдаемая роль LEA-2 в инициации активации комплемента и стимуляции образования MAC и гемолизе является очевидной, этот процесс, по-видимому, значительно менее эффективен, чем инициируемая LEA-1 активация комплемента, приводящая к гемолизу. Таким образом, ожидают, что средства, блокирующие LEA-2, будут значительно снижать внутрисосудистый гемолиз у пациентов с PNH, хотя ожидают, что их терапевтическая активность будет только частичной. Для сравнения, в случае средств, блокирующих LEA-1, ожидают более значительного снижения внутрисосудистого гемолиза у пациентов с PNH.
Внесосудистый гемолиз, менее сильный, но в равной степени важный механизм деструкции RBC, приводящей к анемии при PNH, главным образом, является результатом опсонизации посредством C3b, по-видимому, преимущественно опосредованной LEA-2. Таким образом, можно ожидать, что средства, блокирующие LEA-2, будут предпочтительно блокировать опсонизацию RBC и последующий внесосудистый гемолиз пре PNH. Ожидают, что эта уникальная терапевтическая активность средств, блокирующих LEA-2, будет обеспечивать значительный благоприятный лечебный эффект для всех пациентов с PNH, т.к. в настоящее время не существует лечения для тех пациентов с PNH, у которых развивается этот патогенетический процесс.
vii. Ингибиторы LEA-2 в качестве лечения, дополняющего ингибиторы LEA-1 или средства, блокирующие терминальные компоненты комплемента
С помощью данных, представленных в настоящем описании, подробно описывают два патогенетических механизма клиренса RBC и анемии при PNH, на которые можно раздельно или в комбинации воздействовать различными классами терапевтических средств: внутрисосудистый гемолиз инициируется преимущественно, но не исключительно, LEA-1, и, таким образом, ожидают, что его будут эффективно предотвращать с помощью средства, блокирующего LEA-1, и внесосудистый гемолиз по причине опсонизации C3b запускается преимущественно LEA-2, и, таким образом, его будут эффективно предотвращать с помощью средства, блокирующего LEA-2.
Хорошо известно, что внутрисосудистый и внесосудистый механизмы гемолиза приводят к анемии у пациентов с PNH (Risitano et al, Blood 113:4094-4100 (2009)). Таким образом, ожидают, что средство, блокирующее LEA-1, предотвращающее внутрисосудистый гемолиз, в комбинации со средством, блокирующим LEA-2, преимущественно предотвращающим внесосудистый гемолиз, будет более эффективным, чем любое средство в отдельности, в профилактике анемии, развивающейся у пациентов с PNH. Фактически, ожидают, что комбинация средств, блокирующих LEA-1 и LEA-2, будет предотвращать все соответствующие механизмы инициации комплемента при PNH и, таким образом, блокировать все симптомы анемии при PNH.
Также известно, что средства, блокирующие C5 (такие как экулизумаб), эффективно блокируют внутрисосудистый гемолиз, но не противодействуют опсонизации. Это оставляет некоторых пациентов с PNH, подвергнутых лечению средством против C5, со значительной остаточной анемией по причине внесосудистого гемолиза, опосредованного LEA-2, остающейся неподвергнутой лечению. Таким образом, ожидают, что средство, блокирующее C5 (такое как экулизумаб), предотвращающее внутрисосудистый гемолиз, в комбинации со средством, блокирующим LEA-2, снижающим внесосудистый гемолиз, будет более эффективным, чем любое средство в отдельности, в профилактике анемии, развивающейся у пациентов с PNH.
Также ожидают, что другие средства, блокирующие терминальную петлю амплификации системы комплемента, приводящую к активации C5 и накоплению MAC (включая, в качестве неограничивающих примеров, средства, блокирующие пропердин, фактор B или фактор D или повышающие ингибиторную активность фактора I, фактора H или других ингибирующих комплемент факторов), будут ингибировать внутрисосудистый гемолиз. Однако не ожидают, что эти средства будут противодействовать опосредованной LEA-2 опсонизации у пациентов с PNH. Это оставляет некоторых пациентов с PNH, подвергнутых лечению такими средствами, со значительной остаточной анемией по причине внесосудистого гемолиза, опосредованного LEA-2 и остающегося неподвергнутым лечению. Таким образом, ожидают, что лечение такими средствами, предотвращающими внутрисосудистый гемолиз, в комбинации со средством, блокирующим LEA-2, минимизирующим внесосудистый гемолиз, будет более эффективным, чем любое средство в отдельности, в профилактике анемии, развивающейся у пациентов с PNH. Фактически, ожидают, что комбинация таких средств и средства, блокирующего LEA-2, будет предотвращать развитие всех соответствующих механизмов деструкции RBC при PNH и, таким образом, блокировать все симптомы анемии при PNH.
viii. Применение многочисленных, биспецифических или панспецифических антител против LEA-1 и LEA-2 в лечении PNH
Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, в отдельности блокирующих LEA-1 и LEA-2 и, таким образом, в комбинации блокирующих все явления активации комплемента, опосредующие внутрисосудистый, а также внесосудистый гемолиз, будет обеспечивать лучший клинический исход у пациентов с PNH. Этого исхода можно достигать, например, посредством совместного введения антитела, обладающего LEA-1-блокирующей активностью, с антителом, обладающим LEA-2-блокирующей активностью. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие действия комбинируют в одной молекуле, такая молекула с комбинированной LEA-1- и LEA-2-блокирующей активностью будет эффективно блокировать внутрисосудистый, а также внесосудистый гемолиз и предотвращать анемию при PNH. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1, блокирует LEA-1 и ослабляет LEA-2, а второй антигенсвязывающий участок специфически распознает MASP-2 и дополнительно блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1 и ослабляет LEA-2, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и дополнительно блокирует LEA-2. Учитывая схожесть общей последовательности и архитектуры белка, также можно предполагать, что общепринятое антитело с двумя идентичными участками связывания можно разрабатывать специфически функционально связывающимся с MASP-1, MASP-2 и MASP-3, таким образом, достигая функциональной блокады LEA-1 и LEA-2. Ожидают, что такое антитело с панспецифической ингибирующей MASP активностью будет блокировать внутрисосудистый, а также внесосудистый гемолиз и, таким образом, приводить к эффективному лечению анемии у пациентов с PNH.
IV. РОЛЬ MASP-2 И MASP-3 В ВОЗРАСТНОЙ ДЕГЕНЕРАЦИИ ЖЕЛТОГО ПЯТНА И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Возрастная дегенерация желтого пятна (AMD) является основной причиной нарушения зрения и слепоты у пожилых людей, и на нее приходятся до 50% случаев слепоты в развитых странах. Распространенность AMD составляет приблизительно 3% среди взрослых, и повышается с возрастом таким образом, что почти две трети популяции людей старше 80 лет будут иметь некоторые ее признаки. Считают, что более 1,75 миллиона индивидуумов в США имеют AMD поздней стадии, и распространенность повышается со старением популяции, и ожидают, что к 2020 году она достигнет 3 миллионов (Friedman, D.S., et al., Arch. Ophthalmol. 122:564-572, 2004). AMD является нарушением пигментного эпителия сетчатки (RPE), приводящим к дегенерации фоторецепторов вышележащей центральной зоны сетчатки, или желтого пятна, и утрате центрального зрения. Ранние и промежуточные формы AMD отличаются прогрессирующим накоплением друз, желтоватого материала, содержащего липид, белок, липопротеин, и продукты распада клеток, в субретинальном пространстве, прилегающем к RPE, вместе с пигментными неровностями сетчатки. AMD поздней стадии состоит из двух клинических подтипов: атрофической AMD без неоваскуляризации ("сухой") и неоваскулярной экссудативной ("влажной") AMD. Хотя на сухую AMD приходится 80-90% AMD поздней стадии, большинство случаев внезапной и тяжелой потери зрения происходит у пациентов с влажной AMD. Неизвестно, представляют ли два типа AMD различные фенотипы, возникающие при схожей патологии, или являются двумя различными состояниями. В настоящее время не существует терапии, одобренной Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для лечения сухой AMD. Одобренные FDA варианты лечения влажной AMD включают интравитреальные инъекции анти-ангиогенных лекарственных средств (ранибизумаба, пегаптаниба натрия, афлиберцепта), лазерную терапию, фотодинамическую лазерную терапию и имплантируемый телескоп.
Этиология и патофизиология AMD является сложной и не вполне понятной. Несколько линий доказательств подтверждают роль дисрегуляции системы комплемента в патогенезе AMD. В исследованиях ассоциации генов идентифицировали многочисленные генетические локусы, ассоциированные с AMD, включая гены, кодирующие ряд белков комплемента, факторов и регуляторов. Наиболее сильную ассоциацию наблюдают с полиморфизмами гена фактора комплемента H (CFH), при этом гомозиготы по варианту Y402H имеют приблизительно 6-кратный, а гетерозиготы приблизительно 2,5-кратный повышенный риск развития AMD по сравнению с генотипом с пониженным риском (Khandhadia, S., et al., Immunobiol. 217:127-146, 2012). Мутации в других генах, кодирующих компоненты путей комплемента, также ассоциированы с повышенным или пониженным риском AMD, включая фактор комплемента B (CFB), C2, C3, фактор I и CFH-родственные белки 1 и 3 (Khandhadia et al.). Иммуногистохимические и протеомные исследования глаз доноров от пациентов с AMD показали, что белки каскада комплемента повышены и локализованы в друзах (Issa, P.C., et al, Graefes. Arch. Clin. Exp. Ophthalmol. 249: 163-174, 2011). Кроме того, пациенты с AMD имеют повышенную системную активацию комплемента, измеряемую в периферической крови (Issa et al, 2011, выше).
По-видимому, альтернативный путь комплемента более важен в патогенезе AMD, чем классический путь. При иммуногистохимических анализах в друзах не определяли C1q, необходимый распознающий компонент для активации классического пути (Mullins et al, FASEB J. 74:835-846, 2000; Johnson et al, Exp. Eye Res. 70:441-449, 2000). Исследования генетической ассоциации включали гены CFH и CFB. Эти белки участвуют в петле амплификации альтернативного пути, при этом CFH является ингибитором жидкой фазы, а CFB является компонентом альтернативного пути, активирующим протеазы. Вариант Y402H CFH влияет на взаимодействие со связыванием лиганда, включая связывание C-реактивного белка, гепарина, протеина M и гликозаминогликанов. Это измененное связывание с лигандами может снижать связывание с клеточными поверхностями, что, в свою очередь, может приводить к сниженной деградации активирующего фрагмента C3b, опосредованной фактором I, и нарушенной регуляции конвертазы C3 альтернативного пути, приводящей к гиперактивации альтернативного пути (Khandhadia et al., 2012, выше). Варианты гена CFB ассоциированы с протективным эффектом в отношении развития AMD. Функциональный вариант fB32Q имеет в 4 раза меньшую аффинность связывания с C3b, чем вариант риска fB32R, приводящий к снижению образования конвертазы C3 (Monies, T. et al., Proc. Natl. Acad. Sci. U.S.A. 106:4366-4371, 2009).
Комплемент-инициирующие механизмы при AMD
Исследования генетического сцепления у человека, обсуждаемые выше, подтверждают важную роль системы комплемента в патогенезе AMD. Кроме того, продукты активации комплемента в избытке присутствуют в друзах (Issa, P.C., et al, Graefes. Arch. Clin. Exp. Ophthalmol. 249:163-174, 2011), отличительном патологическом повреждении при влажной и сухой AMD. Однако, природа явлений, инициирующих активацию комплемента, и вовлекаемые пути активации комплемента остаются не вполне понятными.
Необходимо отметить, что накопления-друзы состоят из продуктов распада клеток и побочных продуктов окисления, возникающих из сетчатки, накапливающихся под RPE при старении глаза. Кроме того, по-видимому, важную роль играет оксидативный стресс (Cai et al; Front Biosci., 17: 1976-95, 2012), и показано, что он вызывает активацию комплемента в RPE (J Biol Chem., 284(25): 16939-47, 2009). Общепринято, что оксидативный стресс и повреждение клеток или ткани активируют лектины системы комплемента. Например, Collard et al. показали, что эндотелиальные клетки, подвергнутые оксидативному стрессу, запускают избыточное накопление комплемента, опосредованное лектинами (Collard CD et al, Mol Immunol, 36(13-14):941-8, 1999; Collard CD. et al, Am J Pathol, 156(5): 1549-56, 2000), и что блокада связывания лектинов и лектин-зависимой активации комплемента улучшает исходы в экспериментальных моделях повреждения при оксидативном стрессе (Collard CD. et al., Am J Pathol, 156(5): 1549-56, 2000). Таким образом, вполне вероятно, что побочные продукты окисления, присутствующие в друзах, также активируют комплемент через лектины. Подразумевают, что лектин-зависимая активация комплемента может играть ключевую роль в патогенезе AMD.
Роль системы комплемента оценивали на моделях AMD мыши. В мышиной модели повреждения светом, экспериментальной модели дегенерации фоторецепторов, опосредованной оксидативным стрессом, нокаутные мыши с выключенным классическим путем (C1qα-/- с фоном C57BL/6) имели ту же чувствительность к повреждению светом, что и однопометные мыши дикого типа, в то время как выключение фактора комплемента D альтернативного пути (CFD-/-) приводило к защите от повреждения светом (Rohrer, B. et al., Invest. Ophthalmol. Vis. Sci. 48:5282-5289, 2007). В мышиной модели хороидальной неоваскуляризации (CNV), индуцируемой лазерной фотокоагуляцией мембраны Бруха, нокаутные мыши без фактора комплемента B (CFB-/-) были защищены от CNV по сравнению с мышами дикого типа (Rohrer, B. et al, Invest. Ophthalmol. Vis. Sci. 50:3056-3064, 2009). В той же модели внутривенное введение рекомбинантной формы фактора комплемента H, направленной в участки активации комплемента, (CR2-fH) снижало степень CNV. Этот протективный эффект наблюдали, когда CR2-fH вводили во время повреждения лазером или терапевтически (после повреждения лазером). Терапевтический вариант CR2-fH человека (TT30) также являлся эффективным в мышиной модели CNV (Rohrer, B. et al. J. Ocul. Pharmacol. Ther., 28:402-409, 2012). Поскольку fB активируется посредством LEA-1, и т.к. MASP-1 и MASP-3 участвуют в созревании фактора D, эти результаты означают, что ингибиторы LEA-1 могут оказывать благоприятный терапевтический эффект в отношении пациентов с AMD.
Первоначальные экспериментальные исследования модели AMD грызунов с использованием мышей с дефицитом MBL, не подтверждали критическую роль лектинового пути в патологической активации комплемента (Rohrer et al., Mol Immunol. 48:el-8, 2011). Однако MBL является лишь одним из нескольких лектинов, и лектины, иные, чем MBL, могут запускать активацию комплемента при AMD. Фактически, в предыдущей работе авторы настоящего изобретения показали, что MASP-2, скорость-лимитирующая сериновая протеаза, критически необходимая для функционирования лектинового пути, играет критическую роль при AMD. Как описано в патенте США № 7919094 (закрепленном за Omeros Corporation), включенном в настоящее описание в качестве ссылки, и в примерах 20 и 21 в настоящем описании, мыши с дефицитом MASP-2 и мыши, которым вводили антитело против MASP-2, были защищены в мышиной модели индуцируемой лазером CNV, подтвержденной доклинической модели влажной AMD (Ryan et al, Tr Am Opth Soc LXXVII: 707-745, 1979). Таким образом, ожидают, что ингибиторы LEA-2 будут эффективно предотвращать CNV и улучшать исходы у пациентов AMD.
Таким образом, в свете изложенного выше, ожидают, что ингибиторы LEA-1 и LEA-2 будут оказывать независимый благоприятный терапевтический эффект при AMD. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного эффекта лечения по сравнению с любым из средств в отдельности, или они могут представлять собой эффективное лечение для более широкого спектра подгрупп пациентов. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфический участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения возрастной дегенерации желтого пятна (влажной и сухой форм) посредством введения индивидууму, страдающему таким состоянием, композиции, содержащей терапевтически эффективное количество средства, ингибирующего MASP-1, средства, ингибирующего MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить местно в глаз, например, посредством промывания, интравитреального введения или введения композиции в форме геля, мази или капель. Альтернативно, средство, ингибирующее MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
В одном из вариантов осуществления способ по этому аспекту изобретения дополнительно включает ингибирование LEA-2-зависимой активации комплемента у индивидуума, страдающего возрастной дегенерацией желтого пятна, включающее введение нуждающемуся в этом индивидууму терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP 1/3. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход у пациентов AMD по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать например, посредством совместного введения антитела, обладающего LEA-1-блокирующей активностью, вместе с антителом, обладающим LEA-2-блокирующей активностью. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула обладает комбинированной LEA-1- и LEA-2-блокирующей активностью. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенраспознающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Композицию, ингибирующую MASP-2, можно вводить местно в глаз, например, посредством промывания, интравитреальной инъекции или местного применения композиции в форме геля, мази или капель. Альтернативно, средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения, или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения AMD. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения AMD.
V. РОЛЬ MASP-2 И MASP-3 В ПОВРЕЖДЕНИИ ПРИ ИШЕМИИ/РЕПЕРФУЗИИ И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Ишемия ткани является основой широкого спектра клинических нарушений. Хотя своевременное восстановление кровотока необходимо для сохранения ишемизированной ткани, уже давно общепринято, что реперфузия, которая может происходить спонтанно или посредством терапевтического вмешательства, может приводить к дополнительному повреждению ткани, явлению, названному повреждением при ишемии/реперфузии (I/R) (Eltzschig, H.K. and Tobias, E., Nat. Med. 17: 1391-1401, 2011). I/R-повреждение может затрагивать отдельные органы, такие как сердце (острый коронарный синдром), почки (острое повреждение почек), кишечник (кишечная I/R) и головной мозг (инсульт). I/R-повреждение также может затрагивать несколько органов, например, после обширной травмы и реанимации (полиорганная недостаточность), остановки кровообращения (гипоксическое поражение мозга, острое повреждение почек), заболевания периферических сосудов и серповидноклеточной анемии (острый грудной синдром, острое повреждение почек). Обширное оперативное вмешательство может быть ассоциировано с I/R-повреждением, включая операции на сердце (острая сердечная недостаточность после использования аппарата искусственного кровообращения), операции на органах грудной полости (острое повреждение легких), операции на периферических сосудах (компартмент-синдром), операции на сосудах (острое повреждение почек) и операции по трансплантации паренхиматозных органов (острое отторжение трансплантата). В настоящее время не существует конкретных способов терапии, направленных на I/R-повреждение, и существует потребность в эффективных способах лечения для максимизации сохранения ткани в ишемизированной зоне и улучшения функционального исхода в этих распространенных ситуациях.
Патофизиология I/R-повреждения является сложной и отличается сильным воспалительным ответом после реперфузии. Активация системы комплемента является важным компонентом I/R-повреждения, и ингибирование активности комплемент является эффективным во множестве моделей на животных (Diepenhorst, G.M.P., et al., Ann. Surg. 249:889-899, 2009). Относительная важность классического, лектинового и альтернативного путей при I/R-повреждения является непостоянной и может отличаться в зависимости от пораженных органов. В последнее время доступность нокаутных мышей с дефицитом конкретных белков комплемента и специфичных для пути ингибиторов привела к получению данных об участии лектинового и альтернативного путей в I/R-повреждении.
Роль альтернативного пути при желудочно-кишечном I/R-повреждении исследовали с использованием мышей с дефицитом фактора D (-/-) и гетерозиготных мышей (+/-) (Stahl, G.L., et al. Am. J. Pathol. 162:449-455, 2003). После транзиторной желудочно-кишечной ишемии, кишечные и легочные повреждения снижались, но не предотвращались у мышей с дефицитом фактора D по сравнению с гетерозиготными мышами, и добавление фактора D человека мышам -/- восстанавливало I/R-повреждение. Ту же модель оценивали с использованием мышей с дефицитом C1q и дефицитом MBL-A/C, и результаты показали, что желудочно-кишечное I/R-повреждение не зависит от C1q и активации классического пути, но для повреждения кишечника необходимы MBL и активация лектинового пути (Hart, M.L., et al. J. Immunol. 174:6373-6380, 2005). С другой стороны, распознающая молекула C1q классического пути отвечает за повреждение легких после кишечной I/R (Hart, M., et al. J. Immunol. 174:6373-6380, 2005). Одной из гипотез является то, что активация комплемента в течение I/R-повреждения происходит посредством естественного связывания IgM с аутоантигенами, присутствующими на поверхности ишемизированной (но не нормальной) ткани, например тяжелыми цепями немышечного миозина типа II. В модели желудочно-кишечного I/R-повреждения мыши иммунные комплексы из ткани кишечника оценивали на наличие инициирующих факторов классического (C1q), лектинового (MBL) или альтернативного (фактор B) путей (Lee, H., et al., Mol. Immunol. 47:972-981, 2010). Результаты показали, что в этих иммунных комплексах определяли C1q и MBL, но не определяли фактор B, что свидетельствует об участии классического и лектинового путей, но не альтернативного пути. В той же модели мыши с дефицитом фактора B не являлись защищенными от локального повреждения тканей, что представляет дополнительное доказательство отсутствия вовлечения альтернативного пути. Роль лектинового пути в желудочно-кишечном I/R-повреждении напрямую оценивали у мышей с дефицитом MASP-2, и результаты показали, что у этих мышей желудочно-кишечное повреждение снижено по сравнению с контролями дикого типа; введение моноклонального антитела против MASP-2 аналогично оказывало протективный эффект (Schwaeble, W.J., et al, Proc. Natl. Acad. Sci. 108:7523-7528, 2011), см. также пример 23 в настоящем описании. В совокупности, эти результаты представляют доказательство участия лектинового пути в желудочно-кишечном I/R-повреждении, несмотря на противоречивые данные в отношении участия альтернативного пути.
На модели I/R-повреждения миокарда мыши демонстрировали патогенетическую роль лектинового пути, т.к. мыши с дефицитом MBL были защищены от повреждения миокарда, в то время как мыши с дефицитом C1q и дефицитом C2/fB - нет (Walsh, M.C. et al., J. Immunol. 175:541-546, 2005). Защиту от I/R-повреждения миокарда также наблюдали у мышей с дефицитом MASP-2 (Schwaeble, W.J., et al, Proc. Natl. Acad. Sci. 108:7523- 7528, 2011); см. также примеры 22 и 23 в настоящем описании. Введение моноклональных антител против MBL крысам в модели I/R миокарда приводило к снижению постишемического реперфузионного повреждения (Jordan, J.E., et al, Circulation 704: 1413-18, 2001). В исследовании пациентов с инфарктом миокарда, которым проводили ангиопластику, дефицит MBL был ассоциирован со сниженной 90-дневной смертностью при сравнении с пациентами с достаточным MBL (M Trendelenburg et al., Eur Heart J. 31: 1181, 2010). Кроме того, пациенты с инфарктом миокарда, у которых после ангиопластики развивалась дисфункция сердца, имели приблизительно в три раза более высокие уровни MBL по сравнению с пациентами с функциональным восстановлением (Haahr-Pedersen S., et al, J Inv Cardiology, 21: 13, 2009). Антитела против MBL также снижали накопление комплемента на эндотелиальных клетках in vitro после оксидативного стресса, что свидетельствует о роли лектинового пути в I/R-повреждении миокарда (Collard, CD., et al, Am. J. Pathol. 156: 1549-56, 2000). В модели I/R-повреждения у мыши с гетеротопическим изотрансплантатом сердца роль альтернативного пути исследовали с использованием специфичного для пути слитого белка CR2-fH (Atkinson, C, et al, J. Immunol. 185:7007-7013, 2010). Системное введение CR2-fH непосредственно после трансплантации приводило к снижению I/R-повреждения миокарда до степени, сравнимой с лечением с использованием CR2-Crry, который ингибирует все пути комплемента, что свидетельствует о том, что альтернативный путь играет ключевую роль в этой модели.
В модели I/R-повреждения почек мыши участвовал альтернативный путь, т.к. мыши с дефицитом фактора B были защищены от снижения функции почек и повреждения канальцев по сравнению с мышами дикого типа (Thurman, J.M., et al, J. Immunol. 170: 1517-1523, 2003). Введение ингибирующего моноклонального антитела против фактора B предотвращало активацию комплемента и снижало I/R-повреждение почек у мыши (Thurman, J.M., et al., J. Am. Soc. Nephrol. 17:707-715, 2006). В модели билатерального I/R-повреждения почек мыши с дефицитом MBL-A/C были защищены от повреждения почек по сравнению с мышами дикого типа, и рекомбинантный MBL человека реверсировал протективный эффект у мышей с дефицитом MBL-A/C, что свидетельствует о роли MBL в этой модели (Moller-Kristensen, M., et al., Scand. J. Immunol. 61:426-434, 2005). В модели унилатерального I/R-повреждения почек крысы ингибирование MBL с использованием моноклонального антитела против MBL-A позволяло сохранять функцию почек после I/R (van der Pol, P., et al, Am. J. Transplant. 12:877-887, 2010). Интересно, что роль MBL в этой модели, по-видимому, не включает активацию терминальных компонентов комплемента, т.к. введение антитела против C5 являлось неэффективным в профилактике повреждения почек. Точнее, MBL, по-видимому, оказывает прямой токсический эффект на клетки канальцев, т.к. клетки проксимальных канальцев человека, инкубируемые с MBL in vitro, интернализировали MBL с последующим апоптозом. В модели I/R почек свиньи Castellano G. et al, (Am J Pathol, 176(4): 1648-59, 2010) тестировали ингибитор C1, необратимо инактивирующий протеазы C1r и C1s классического пути, а также протеазы MASP-1 и MASP-2 в комплексах MBL лектинового пути, и обнаружили, что ингибитор C1 снижал накопление комплемента в околоканальцевых капиллярах и клубочках и снижал повреждение канальцев.
Альтернативный путь, по-видимому, участвует в экспериментальной модели травматического повреждения головного мозга, т.к. у мышей с дефицитом фактора B наблюдали сниженную системную активацию комплемента, измеряемую по уровням C5a в сыворотке и сниженную посттравматическую гибель нейронов по сравнению с мышами дикого типа (Leinhase, I., et al, BMC Neurosci. 7:55-67, 2006). При инсульте человека компоненты комплемента C1q, C3c и C4d определяли в очагах ишемического повреждения посредством иммуногистохимического окрашивания, подтверждая активацию через классический путь (Pedersen, E.D., et al, Scand. J. Immunol. 69:555-562, 2009). При воздействии на классический путь в моделях ишемии головного мозга на животных получали смешанные результаты, при этом в некоторых исследованиях демонстрировали протективный эффект, в то время как в других не наблюдали благоприятного эффекта (Arumugam, T.V., et al, Neuroscience 158: 1074-1089, 2009). С помощью экспериментальных и клинических исследований получали убедительные доказательства участия лектинового пути. В экспериментальных моделях инсульта дефицит MBL или MASP-2 приводил к снижению размеров очага инсульта по сравнению с мышами дикого типа (Cervera A, et al; PLoS One 3;5(2):e8433, 2010; Osthoff M. et al, PLoS One, 6(6):e21338, 2011, и пример 26 в настоящем описании). Кроме того, пациенты с инсультом с низкими уровнями MBL имеют лучший прогноз по сравнению с пациентами с достаточным MBL (Osthoff M. et al, PLoS One, 6(6):e21338, 2011).
В модели искусственного кровообращения у павиана введение моноклонального антитела против фактора D ингибировало системное воспаление, измеряемое по уровням C3a, sC5b-9 и IL-6 в плазме, и снижало повреждение ткани миокарда, что свидетельствует об участии альтернативного пути в этой модели (Undar, A., et al, Ann. Thorac. Surg. 74:355-362, 2002).
Таким образом, в зависимости от органа, поврежденного при I/R, в патогенезе и неблагоприятных исходах могут участвовать все три пути комплемента. С учетом экспериментальных и клинических результатов, подобно описанных выше, ожидают, что ингибиторы LEA-2 будут оказывать протективный эффект в большинстве случаев I/R. Лектин-зависимая активация LEA-1 может вызывать активацию комплемента через альтернативный путь по меньшей мере в некоторых условиях. Кроме того, инициируемая LEA-2 активация комплемента может дополнительно усиливаться через петлю амплификации альтернативного пути и, таким образом, усугублять связанное с I/R повреждение ткани. Таким образом, ожидают, что ингибиторы LEA-1 будут оказывать дополнительный благоприятный терапевтический эффект у пациентов, страдающих связанным с ишемией состоянием.
В свете изложенного выше, ожидают, что ингибиторы LEA-1 и LEA-2 будут оказывать независимые благоприятные терапевтические эффекты при лечении, профилактике или снижении тяжести состояний, связанных с ишемией-реперфузией. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности. Таким образом, оптимально эффективное лечение связанного с I/R состояния включает активные фармацевтические ингредиенты, которые в отдельности или в комбинации блокируют LEA-1 и LEA-2. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Предпочтительно, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитела с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики или снижения тяжести повреждений при ишемии-реперфузии посредством введения индивидууму, испытывающему ишемию- реперфузию, композиции, содержащей терапевтически эффективное количество LEA-1-ингибирующего средства, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму посредством внутриартериального, внутривенного, интракраниального, внутримышечного, подкожного или другого парентерального введения и, потенциально, перорально в случае непептидергических ингибиторов, и наиболее предпочтительно - посредством внутриартериального или внутривенного введения. Введение LEA-1-ингибирующих композиций по настоящему изобретению соответствующим образом начинают непосредственно после или как можно скорее после события ишемии-реперфузии. В случаях, когда реперфузия происходит в контролируемой обстановке (например, после реконструкции аорты при аневризме, трансплантации органа или реплантации отделенных или травмированных конечностей или пальцев), LEA-1-ингибирующее средство можно вводить перед, и/или в течение, и/или после реперфузии. Для оптимального терапевтического эффекта введение можно повторять периодически по решению лечащего врача.
В некоторых вариантах осуществления способы используют для лечения или профилактики повреждения при ишемии-реперфузии, связанной по меньшей мере с одним из реконструкции аорты при аневризме, искусственного кровообращения, реанастамозированием сосудов в связи с трансплантацией органов и/или реплантацией конечностей/пальцев, инсульта, инфаркта миокарда и восстановления гемодинамики после шока и/или хирургических операций.
В некоторых вариантах осуществления способы используют для лечения или профилактики повреждения при ишемии-реперфузии у индивидуума, которого будут подвергать, подвергают или подвергали трансплантации органа. В некоторых вариантах осуществления способы используют для лечения или профилактики повреждения при ишемии-реперфузии у индивидуума, которого будут подвергать, подвергают или подвергали трансплантации органа при условии, что трансплантация органа не является трансплантацией почки.
В одном из вариантов осуществления способ по этому аспекту изобретения дополнительно включает ингибирование LEA-2-зависимой активации комплемента у индивидуума, испытывающего ишемию-реперфузию, включающее введение индивидууму терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход при лечении, профилактике или снижении тяжести повреждений при ишемии-реперфузии по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3, и таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Композицию, ингибирующую MASP-2, можно вводить нуждающемуся в этом индивидууму посредством внутриартериального, внутривенного, интракраниального, внутримышечного, подкожного или другого парентерального введения и, потенциально, перорально в случае непептидергических ингибиторов, и наиболее предпочтительно - посредством внутриартериального или внутривенного введения. Введение композиций, ингибирующих MASP-2, по настоящему изобретению соответствующим образом начинают непосредственно после или как можно скорее после события ишемии-реперфузии. В случаях, когда реперфузия происходит в контролируемой обстановке (например, после реконструкции аорты при аневризме, трансплантации органа или реплантации отделенных или травмированных конечностей или пальцев), средство, ингибирующее MASP-2, можно вводить перед, и/или в течение, и/или после реперфузии. Для оптимального терапевтического эффекта введение можно повторять периодически по решению лечащего врача.
Введение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения или профилактики повреждений при ишемии-реперфузии. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения индивидуума, испытывающего ишемию-реперфузию.
VI. РОЛЬ MASP-2 И MASP-3 В ВОСПАЛИТЕЛЬНЫХ И НЕВОСПАЛИТЕЛЬНЫХ АРТРИТАХ И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Ревматоидный артрит (RA) является хроническим воспалительным заболеванием суставов, которое также может иметь системные проявления. RA страдает приблизительно 1% населения в мире, при этом у женщин вероятность заболеть в 2-3 раза выше. Воспаление сустава проявляется отеком, болью и тугоподвижностью. При прогрессировании заболевания может происходить эрозия и деструкция сустава, приводящие к нарушенному объему движений и деформациям. Цели лечения при RA включают профилактику или контроль повреждения сустава, профилактику потери функции сустава и прогрессирования заболевания, облегчение симптомов и улучшение качества жизни, и достижение ремиссии без необходимости приема лекарственных средств. Фармакологическое лечение RA включает модифицирующие заболевание противоревматические лекарственные средства (DMARD), анальгетики и противовоспалительные средства (глюкокортикоиды и нестероидные противовоспалительные лекарственные средства). DMARD являются наиболее важным лечением, т.к. они индуцируют долговременную ремиссию и задержку или прекращение прогрессирования деструкции сустава, которая является необратимой. Общепринятые DMARD включают низкомолекулярные соединения, такие как метотрексат, сульфасалазин, гидроксихлорохин, соли золота, лефлуномид, D-пеницилламин, циклоспорин и азатиоприн. Если общепринятых DMARD недостаточно для контроля заболевания, то доступными вариантами лечения являются некоторые биологические средства, воздействующие на воспалительные клетки или медиаторы, такие как ингибиторы фактора некроза опухоли (этанерцепт, инфликсимаб, адалимумаб, цертолизумаб пегол и голимумаб), антагонисты цитокинов (анакинра и тоцилизумаб), ритуксимаб и абатацепт.
Хотя приобретенный иммунитет очевидно является центральным в патогенезе RA, о чем свидетельствует генетическая ассоциация с генами активации T-клеток и наличие аутоантител, в нем участвуют и механизмы врожденного иммунитета (Mclnnes, LB. and Schett, G. New Engl. J. Med. 365:2205-2219, 2011). При RA человека уровни отщепленного фрагмента Bb альтернативного пути в синовиальной жидкости в несколько раз выше, чем в образцах от пациентов с микрокристаллическим артритом или остеоартритом, что свидетельствует о предпочтительной активации альтернативного пути у пациентов с RA (Brodeur, J.P., et al., Arthritis Rheum. 34: 1531-1537, 1991). В экспериментальной модели артрита с пассивным переносом антител против коллагена типа II у мышей с дефицитом фактора B наблюдали пониженное воспаление и повреждение сустава по сравнению с мышами дикого типа, в то время как мыши с дефицитом C4 имели аналогичную активность заболевания по сравнению с мышами дикого типа, что свидетельствует о необходимости альтернативного пути в этой модели, а не классического пути (Banda, N.K. et al., J. Immunol. 177: 1904-1912, 2006). В той же экспериментальной модели артрита, индуцированного антителами против коллагена (CAIA), у мышей только с активным классическим путем или только активным лектиновым путем не наблюдали развития артрита (Banda, N.K. et al., Clin. Exp. Immunol. 159: 100-108, 2010). Данные, полученные в этом исследовании, подтверждают, что классический или лектиновый пути способны к низкоуровневой активации C3 in vitro. Однако в отсутствие петли амплификации альтернативного пути уровень накопления C3 в суставе являлся недостаточным для развития клинического заболевания. Ключевым этапом в активации альтернативного пути является конвертация зимогена фактора D (про-фактора D) в зрелый фактор D, опосредованная MASP-1 и/или MASP-3 (Takahashi, M., et al, J. Exp. Med. 207:29-37, 2010) и/или HTRA1 (Stanton et al., Evidence That the HTRA1 Interactome Influences Susceptibility to Age-Related Macular Degeneration, представленный на конференции The Association for Research in Vision and Ophthalmology 2011 4 мая 2011 года). Роль MASP-1/3 оценивали в CAIA мыши, и результаты показали, что мыши с дефицитом MASP-1/3 были защищены от артрита по сравнению с мышами дикого типа (Banda, N.K., et al, J. Immunol. 185:5598-5606, 2010). У мышей с дефицитом MASP-1/3 при развитии CAIA в сыворотке определяли про-фактор D, но не зрелый фактор D, и добавление фактора D человека in vitro восстанавливало активацию C3 и образование C5a с использованием сывороток этих мышей. В отличие от этого, в мышиной модели эффекторной фазы артрита у мышей с дефицитом C3 развивался очень умеренный артрит по сравнению с мышами WT, в то время как у мышей с дефицитом фактора B все равно развивался артрит, что свидетельствует о независимом участии классического/лектинового и альтернативного путей (Hietala, M.A. et al., Eur. J. Immunol. 34: 1208-1216, 2004). В модели воспалительного артрита у мышей K/BxN, трансгенных по T-клеточному рецептору, у мышей без C4 или C1q развивался артрит, аналогичный таковому у мышей дикого типа, в то время как у мышей без фактора B не развивался артрит или развивался умеренный артрит, что свидетельствует о необходимости альтернативного пути в этой модели, а не классического пути (Ji H. et al., Immunity 16: 157-168, 2002). В модели K/BxN мыши без MBL-A не были защищены от индуцируемого сывороткой артрита, но т.к. роль MBL-C не исследовали, нельзя исключать потенциальную роль лектинового пути (Ji et al, 2002, выше).
Две исследовательские группы независимо предположили, что лектин-зависимая активация комплемента стимулирует воспаление у пациентов с RA через взаимодействие MBL со специфичными гликоформами IgG (Malhotra et al, Nat. Med. 7:237-243, 1995; Cuchacovich et al., J. Rheumatol. 25:44-51, 1996). Отмечают, что ревматоидные состояния ассоциированы со значительным повышением гликоформ IgG без галактозы (обозначаемых как гликоформы IgG0) в Fc-области молекулы (Rudd et al, Trends Biotechnology 22:524-30, 2004). Процентная доля гликоформ IgG0 повышается при прогрессировании ревматоидных состояний и возвращается к норме, когда у пациентов происходит ремиссия. In vivo IgG0 накапливаются на синовиальных тканях, и у индивидуумов с RA в синовиальной жидкости присутствуют повышенные уровни MBL. Агрегированные агалактозил-IgG (IgG0), ассоциированные с RA, могут связываться с MBL и, таким образом, могут инициировать лектин-зависимую активацию комплемента через LEA-1 и/или LEA-2. Кроме того, результаты клинического исследования, в котором изучали аллельные варианты MBL у пациентов с RA, подтверждают то, что MBL может играть роль в усилении воспаления при заболевании (Garred et al, J. Rheumatol. 27:26-34, 2000). Таким образом, лектин-зависимая активация комплемента через LEA-1 и/или LEA-2 может играть важную роль в патогенезе RA.
Активация комплемента также играет важную роль в ювенильном ревматоидном артрите (Mollnes, T.E., et al, Arthritis Rheum. 2M359-64, 1986). Аналогично RA у взрослых, при ювенильном ревматоидном артрите повышаются уровни продукта Bb альтернативного пути активации комплемента в сыворотке и синовиальной жидкости по сравнению с C4d (маркером классической или LEA-2-зависимой активации), что свидетельствует о том, что активация комплемента опосредована преимущественно LEA-1 (El-Ghobarey, A.F. et al, J. Rheumatology 7:453-460, 1980; Agarwal, A., et al, Rheumatology 39: 189-192, 2000).
Аналогично, активация комплемента играет важную роль при псориатическом артрите. Пациенты с этим состоянием имеют повышенные уровни продуктов активации комплемента в кровотоке, и их эритроциты, по-видимому, имеют более низкие уровни регулятора комплемента CD59 (Triolo,. Clin Exp Rheumatol., 21(2):225-8, 2003). Уровни комплемента ассоциированы с активностью заболевания и имеют большое прогностическое значение для определения исходов лечения (Chimenti at al., Clin Exp Rheumatol., 30(1):23-30, 2012). Фактически, недавние исследования подтверждают, что эффект анти-TNF терапии этого состояния обусловлен модуляцией комплемента (Ballanti et al., Autoimmun Rev., 10(10):617-23, 2011). Хотя точная роль комплемента при псориатическом артрите не определена, наличие продуктов активации комплемента C4d и Bb в кровотоке этих пациентов подтверждает его важную роль в патогенезе. С учетом наблюдаемых продуктов, полагают, что LEA-1 и, возможно, также LEA-2 отвечают за патологическую активацию комплемента у этих пациентов.
Остеоартрит (OA) является наиболее распространенной формой артрита, поражающей более 25 миллионов людей в США. OA отличается разрушением и последующей утратой суставного хряща, сопровождающейся образованием новой костной ткани и синовиальной пролиферации, что приводит к боли, тугоподвижности, утрате функции сустава и инвалидизации. Суставами, часто поражаемыми при OA, являются суставы кистей рук, шеи, нижнего отдела спины, коленные и тазобедренные суставы. Заболевание является прогрессирующим, и современные способы лечения направлены на симптоматическое облегчение боли и не изменяют течение заболевания. Патогенез OA неясен, но предполагают, что в нем играет роль комплемент. При протеомных и транскриптомных анализах синовиальной жидкости пациентов с OA обнаруживали аномальную экспрессию нескольких компонентов комплемента по сравнению с образцами от здоровых индивидуумов, включая классический (C1s и C4A) и альтернативный (фактор B) пути, а также C3, C5, C7 и C9 (Wang, Q., et al, Nat. Med. 17: 1674- 1679, 2011). Кроме того, в модели OA мыши, индуцированного медиальной менискэктомией, у мышей с дефицитом C5 наблюдали меньшую утрату хряща, образование остеофитов и синовит, чем у C5-позитивных мышей, и лечение мышей дикого типа слитым белком CR2-fH, ингибирующим альтернативный путь, ослабляло развитие OA (Wang et al., 2011 выше).
Вирус реки Росс (RRV) и вирус чикунгунья (CHIKV) принадлежат к группе вирусов, передаваемых комарами, которые могут вызывать острый и персистирующий артрит и миозит у людей. В дополнение к эндемическому заболеванию, эти вирусы могут вызывать эпидемии, поражающие миллионы инфицированных индивидуумов. Считают, что артрит инициирует репликация вируса и индукция воспалительного ответа хозяина в суставе, и в этом процессе в качестве ключевого компонента задействована система комплемента. Синовиальная жидкость людей с RRV-индуцированным полиартритом содержит более высокие уровни C3a, чем синовиальная жидкость людей с OA (Morrison, T.E., et al., J. Virol. 81:5132-5143, 2007). В модели инфекции RRV мыши у мышей с дефицитом C3 развивался менее тяжелый артрит по сравнению с мышами дикого типа, что позволяет предполагать роль комплемента (Morrison et al., 2007, выше). Исследовали конкретный вовлеченный путь комплемента, и у мышей с инактивированным лектиновым путем (MBL-A-/- и MBL-C-/-) развивался более слабый артрит по сравнению с мышами дикого типа. В отличие от этого, у мышей с инактивированным классическим путем (C1q-/-) или альтернативным путем (фактор B-/-) развивался тяжелый артрит, что свидетельствует о том, что лектиновый путь, инициируемый MBL, играет важную роль в этой модели (Gunn, B.M., et al., PLoS Pathog. 8:e1002586, 2012). Поскольку артриты включают повреждение суставов, исходное повреждение сустава различной этиологии может запускать вторую волну активации комплемента через LEA-2. В подтверждение этой концепции, в предыдущей работе авторы настоящего изобретения показали, что у мышей MASP-2 KO наблюдали меньшее повреждение суставов по сравнению с мышами WT в модели коллаген-индуцированного RA, как представлено в примере 27 в настоящем описании.
Ввиду совокупности доказательств, изложенных выше, ожидают, что ингибиторы LEA-1 и LEA-2 в отдельности или в комбинации будут терапевтически применимыми для лечения артритов. Таким образом, оптимально эффективное лечение артритов может включать активные фармацевтические ингредиенты, которые в отдельности или в комбинации могут блокировать LEA-1 и LEA-2. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA2. Предпочтительно, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, состоящие из MASP-1/3- и MASP-2-специфичного участка связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их. В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести воспалительных или невоспалительных артритов, включая остеоартрит, ревматоидный артрит, ювенильный ревматоидный артрит и псориатический артрит, посредством введения индивидууму, страдающему или имеющему риск развития воспалительных или невоспалительных артритов, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, подкожного или другого парентерального введения или посредством перорального введения. Альтернативно, введение можно осуществлять посредством местной доставки, такой как внутрисуставная инъекция. Средство, ингибирующее LEA-1, можно вводить периодически в течение длительного периода времени для лечения или контроля хронического состояния, или можно осуществлять однократное или повторное введение в период до, в течение и/или после острой травмы или повреждения, включая хирургические операции на суставе.
В одном из вариантов осуществления способ по этому аспекту изобретения дополнительно включает ингибирование LEA-2-зависимой активации комплемента у индивидуума, страдающего или имеющего риск развития воспалительных или невоспалительных артритов (включая остеоартрит, ревматоидный артрит, ювенильный ревматоидный артрит и псориатический артрит), посредством введения индивидууму терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP1/3. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения или профилактики артритов по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Композицию, ингибирующую MASP-2, можно вводить нуждающемуся в этом индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических ингибиторов. Альтернативно, введение можно осуществлять посредством местной доставки, такой как внутрисуставная инъекция. Средство, ингибирующее MASP-2, можно вводить периодически в течение длительного периода времени для лечения или контроля хронического состояния, или можно осуществлять однократное или повторное введение в период до, в течение и/или после острой травмы или повреждения, включая хирургические операции на суставе.
Введение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести воспалительных или невоспалительных артритов. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения индивидуума, страдающего воспалительными или невоспалительными артритами.
VII. РОЛЬ MASP-2 И MASP-3 В ДИССЕМИНИРОВАННОМ ВНУТРИСОСУДИСТОМ СВЕРТЫВАНИИ (DIC) И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Диссеминированное внутрисосудистое свертывание (DIC) является синдромом патологической гиперстимуляции системы свертывания, который может клинически проявляться в виде геморрагии и/или тромбоза. DIC не возникает как первичное состояние, а связано со множеством патологических процессов, включая повреждение тканей (травму, ожоги, тепловой удар, трансфузионную реакцию, острое отторжение трансплантата), новообразование, инфекции, состояния, связанные с беременностью и родовспоможением (предлежание плаценты, амниотическую эмболию, гестоз), и различные состояния, такие как кардиогенный шок, утопление, жировая эмболия, аневризма аорты. Тромбоцитопения является частым нарушением у пациентов в отделении интенсивной терапии с частотой от 35% до 44%, и DIC представляет собой этиологию приблизительно 25% этих случаев, т.е. DIC развивается у приблизительно 10% пациентов в критическом состоянии (Levi, M. and Opal, S.M. Crit. Care 10:222-231, 2006). Патофизиология DIC заключается в том, что лежащий в основе патологический процесс запускает физиологический коагуляционный ответ. Однако, протромботические вещества преодолевают нормальные механизмы компенсации таким образом, что происходит неприемлемое накопление фибрина и тромбоцитов в капиллярах, что приводит к ишемии органов, гипофибриногенемии и тромбоцитопении. Диагностика DIC основывается на клинической картине соответствующего лежащего в основе заболевания или процесса вместе с нарушениями лабораторных показателей (протромбиновое время, активированное частичное тромбопластиновое время, продукты деградации фибрина, D-димеры или количество тромбоцитов). Первичное лечение DIC направлено на лежащее в основе состояние, являющееся пусковым механизмом. Для лечения или профилактики клинических осложнений необходимым может являться использование препаратов крови в форме эритроцитов, тромбоцитов, свежезамороженной плазмы и криопреципитатов.
В нескольких исследованиях изучали роль путей комплемента в DIC. Активацию комплемента оценивали у пациентов детского возраста с менингококковой инфекцией, сравнивая течение заболевания в зависимости от генотипа MBL (Sprang, T. et al., Clin. Infect. Dis. 49: 1380-1386, 2009). При поступлении в клинику пациенты с дефицитом MBL имели более низкие уровни C3bc, комплексов терминальных компонентов комплемента, C4bc и C3bBbP в кровотоке, чем пациенты с достаточным MBL, что свидетельствует о меньшей степени активации общих компонентов комплемента, терминальных компонентов комплемента и альтернативного пути. Кроме того, степень системной активации комплемента коррелировала с тяжестью заболевания и показателями DIC, и пациенты с дефицитом MBL имели более мягкое течение заболевания, чем с пациенты достаточным MBL. Таким образом, хотя дефицит MBL является фактором риска для восприимчивости к инфекциям, дефицит MBL при септическом шоке может быть ассоциирован с меньшей тяжестью заболевания.
Как показано в примерах 1-4 в настоящем описании, экспериментальные исследования показали важную роль MBL и MASP-1/3 во врожденном иммунном ответе на Neisseria meningitidis, возбудителя менингококковой инфекции. Сыворотки мышей или людей с дефицитом MBL, сыворотки человека с дефицитом MASP-3 или мышей, нокаутных по MASP-1/3, являлись менее эффективными в активации комплемента и лизировании менингококков in vitro по сравнению с сыворотками дикого типа. Аналогично, наивные мыши, нокаутные по MASP-1/3, являлись более восприимчивыми к инфекции Neisseria meningitidis, чем соответствующие мыши дикого типа. Таким образом, в отсутствие приобретенного иммунитета, путь LEA-1 участвует во врожденной защите хозяина против инфекции Neisseria meningitidis. С другой стороны, LEA-1 повышает патологическую активацию комплемента, запускающую вредоносный ответ хозяина, включая DIC.
В модели артериального тромбоза мыши MBL-нулевые мыши и мыши, нокаутные по MASP-1/-3, имели пониженное FeCl3-индуцированное тромбообразование по сравнению с мышами дикого типа или C2/фактор B-нулевыми мышами, и дефект восстанавливали с использованием рекомбинантного MBL человека (La Bonte, L.R., et al, J. Immunol. 188:885-891, 2012). In vitro сыворотки MBL-нулевых мышей или мышей, нокаутных по MASP-1/-3, имели пониженное расщепление субстрата тромбина по сравнению с сыворотками мышей дикого типа или C2/фактор B-нулевых мышей; добавление рекомбинантной MASP-1 человека восстанавливало расщепление субстрата тромбина в сыворотках мышей, нокаутных по MASP-1/-3 (La Bonte et al, 2012, выше). Эти результаты свидетельствуют о том, что комплексы MBL/MASP, в частности, MASP-1, играют ключевую роль в тромбообразовании. Таким образом, LEA-1 может играть важную роль в патологическом тромбозе, включая DIC.
В экспериментальных исследованиях определяли в равной степени важную роль LEA-2 в патологическом тромбозе. Как описано в примере 30 в настоящем описании, в модели локализованного DIC мыши авторы настоящего изобретения показали, что мыши, нокаутные по MASP-2, гораздо меньше предрасположены к LPS-индуцированному микрососудистому свертыванию, чем мыши дикого типа. В исследованиях in vitro дополнительно показали, что LEA-2 представляет молекулярную связь между системой комплемента и системой свертывания. Как описано в примерах 29 и 31 в настоящем описании, MASP-2 имеет фактор Xa-подобную активность и активирует протромбин посредством расщепления с образованием тромбина, который впоследствии может расщеплять фибриноген и стимулировать образование фибринового сгустка (см. также Krarup et al, PLoS One, 18:2(7):e623, 2007).
В отдельных исследованиях показано, что комплексы лектин-MASP могут стимулировать тромбообразование, накопление фибрина и высвобождение фибринопептида в MASP-2-зависимом процессе (Gulla et al, Immunology, 129(4):482-95, 2010). Таким образом, LEA-2 стимулирует одновременную лектин-зависимую активацию комплемента и активацию системы свертывания.
В исследованиях in vitro дополнительно показано, что MASP-1 имеет тромбиноподобную активность (Presanis J.S., et al, Mol Immunol, 40(13):921-9, 2004) и расщепляет фибриноген и фактор XIII (Gulla K. C. et al., Immunology, 129(4):482-95, 2010), что позволяет предполагать, что LEA-1 может активировать пути свертывания независимо или совместно с LEA-2.
Представленные выше данные позволяют предполагать, что LEA-1 и LEA-2 представляют собой независимые связи между лектин-зависимой активацией комплемента и свертыванием. Таким образом, в свете изложенного выше, ожидают, что ингибиторы LEA-1 и LEA-2 будут оказывать независимые благоприятные терапевтические эффекты при лечении индивидуума, страдающего диссеминированным внутрисосудистым свертыванием. В некоторых вариантах осуществления индивидуум страдает диссеминированным внутрисосудистым свертыванием, вторичным по отношению к сепсису, травме, инфекции (бактериальной, вирусной, грибковой, паразитической), злокачественному новообразованию, отторжению трансплантата, трансфузионной реакции, осложнению состояния, связанного с беременностью и родовспоможению, сосудистой аневризме, печеночной недостаточности, тепловому удару, ожогу, радиационному облучению, шоку или тяжелой токсической реакции (например, при укусе змеи, укусе насекомого, трансфузионной реакции). В некоторых вариантах осуществления травма является неврологической травмой. В некоторых вариантах осуществления инфекция является бактериальной инфекцией, такой как инфекция Neisseria meningitidis.
Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительных благоприятных терапевтических эффектов по сравнению с любым из средств в отдельности. Поскольку известно, что LEA-1 и LEA-2 активируются при состояниях, приводящих к DIC (например, инфекции или травме), ожидают, что средства, блокирующие LEA-1 и LEA-2, раздельно или в комбинации будут иметь терапевтическую применимость в лечении DIC. С помощью средств, блокирующих LEA-1 и LEA-2, можно противодействовать различным перекрестным механизмам между комплементом и свертыванием. Таким образом, средства, блокирующие LEA-1 и LEA-2, могут обладать взаимодополняющим, аддитивным или синергическим действием при профилактике DIC и других нарушений тромбообразования.
Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительных благоприятных терапевтических эффектов по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп пациентов. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее из MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести диссеминированного внутрисосудистого свертывания у нуждающегося в этом индивидуума, включающему введение индивидууму, страдающему или имеющему риск развития диссеминированного внутрисосудистого свертывания, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым. Для лечения или профилактики DIC, вторичного относительно травмы или другого острого явления, композицию, ингибирующую LEA-1, можно вводить непосредственно после травматического повреждения или профилактически до, в течение, непосредственно после или в течение от одного до семи дней или более, например, в пределах от 24 часов до 72 часов, после травматического повреждения или ситуаций, таких как хирургическая операция у пациентов, которые, как полагают, имеют риск развития DIC. В некоторых вариантах осуществления композицию, ингибирующую LEA-1, можно соответствующим образом вводить в виде быстродействующей лекарственной формы, например, посредством внутривенной или внутриартериальной доставки болюса раствора, содержащего композицию средства, ингибирующего LEA-1.
В одном из вариантов осуществления способ по этому аспекту изобретения дополнительно включает ингибирование LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести диссеминированного внутрисосудистого свертывания у нуждающегося в этом индивидуума, включающее введение индивидууму терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения или профилактики диссеминированного внутрисосудистого свертывания по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить нуждающемуся в этом индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым. Для лечения или профилактики DIC, вторичного относительно травмы или другого острого явления, композицию, ингибирующую MASP-2, можно вводить непосредственно после травматического повреждения или профилактически до, в течение, непосредственно после или в течение от одного до семи дней или более, например, в пределах от 24 часов до 72 часов, после травматического повреждения или ситуаций, таких как хирургическая операция у пациентов, которые, как полагают, имеют риск развития DIC. В некоторых вариантах осуществления композицию, ингибирующую MASP-2, можно соответствующим образом вводить в виде быстродействующей лекарственной формы, например, посредством внутривенной или внутриартериальной доставки болюса раствора, содержащего композицию средства, ингибирующего MASP-2.
Введение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики и снижения тяжести диссеминированного внутрисосудистого свертывания у нуждающегося в этом индивидуума. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения индивидуума, страдающего или имеющего риск развития диссеминированного внутрисосудистого свертывания.
VIII. РОЛЬ MASP-2 И MASP-3 В ТРОМБОТИЧЕСКОЙ МИКРОАНГИОПАТИИ (TMA), ВКЛЮЧАЯ ГЕМОЛИТИКО-УРЕМИЧЕСКИЙ СИНДРОМ (HUS), АТИПИЧНЫЙ ГЕМОЛИТИКО-УРЕМИЧЕСКИЙ СИНДРОМ (AHUS) И ТРОМБОТИЧЕСКУЮ ТРОМБОЦИТОПЕНИЧЕСКУЮ ПУРПУРУ (TTP), И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Тромботическая микроангиопатия (TMA) относится к группе нарушений, клинически отличающихся тромбоцитопенией, микроангиопатической гемолитической анемией и ишемией различных органов. Характерными патологическими признаками TMA являются активация тромбоцитов и образование микротромбов в небольших артериолах и венулах. Классическими TMA являются гемолитико-уремический синдром (HUS) и тромботическая тромбоцитопеническая пурпура (TTP). HUS отличается от TTP наличием острой почечной недостаточности. HUS развивается в двух формах: ассоциированный с диареей (D+) или типичный HUS и HUS без диареи (D-) или атипичный HUS (aHUS).
HUS
D+HUS ассоциирован с продромальным состоянием с диареей, как правило, вызываемым Escherichia coli O157 или другим штаммом бактерий, продуцирующих токсин Шиги, на него приходится более 90% случаев HUS у детей, и он является наиболее распространенной причиной острой почечной недостаточности у детей. Хотя инфицирование человека Escherichia coli O157 является относительно частым, процентная доля случаев кровавой диареи, прогрессирующей в D+HUS, находится в диапазоне от 3% до 7% в спорадических случаях и от 20% до 30% во время некоторых вспышек заболевания (Zheng, X.L. and Sadler, J.E., Annu. Rev. Pathol. 3:249-277, 2008). HUS, как правило, развивается в течение от 4 до 6 дней после начала диареи, и приблизительно для двух третей детей необходим диализ в острой фазе заболевания. Лечение D+HUS является поддерживающим, т.к. не была показана эффективность какого-либо специфического лечения. Прогноз D+HUS является благоприятным, при этом у большинства пациентов восстанавливается функция почек.
Патогенез D+HUS включает продуцируемые бактериями токсины Шиги, связывающиеся с мембранами эндотелиальными клетками микрососудов, моноцитами и тромбоцитами. Микроциркуляторное русло почек поражается наиболее часто. После связывания токсин интернализуется, что приводит к высвобождению провоспалительных медиатором и последующей гибели клетки. Считают, что повреждение эндотелиальных клеток запускает тромбоз микроциркуляторного русла почек, стимулируя активацию каскада свертывания. Существует доказательство активации системы комплемента при D+HUS. У детей с D+HUS уровни Bb и SC5b-9 в плазме являлись повышенными на момент госпитализации по сравнению с нормальными контролями, а ко дню 28 после выписки из больницы они нормализовались (Thurman, J.M. et al., Clin. J. Am. Soc. Nephrol. 4: 1920-1924, 2009). Обнаруживали, что токсин Шиги 2 (Stx2) активирует комплемент человека в жидкой фазе in vitro, преимущественно, через альтернативный путь, т.к. активация происходила в присутствие этиленгликоль-тетрауксусной кислоты, блокирующей классический путь (Orth, D. et al, J. Immunol. 182:6394-6400, 2009). Кроме того, Stx2 связывался с фактором H, но не фактором I, и препятствовал кофакторной активности фактора H на поверхности клеток (Orth et al, 2009, выше). Эти результаты позволяют предполагать, что токсин Шиги может вызывать повреждение почек с помощью множества потенциальных механизмов, включая прямой токсический эффект и, косвенно, посредством активации комплемента или ингибирования регуляторов комплемента. Ожидают, что токсические эффекты в отношении эндотелия сосудов будут активировать комплемент через LEA-2, о чем свидетельствует эффективность блокады MASP-2 в профилактике комплемент-опосредованного реперфузионного повреждения в различных сосудистых сетях, как показано в примерах 21-23 в настоящем описании, см. также Schwaeble, W.J., et al, Proc. Natl. Acad. Sci. 108:7523-7528, 2011.
В модели HUS мыши, индуцированном одновременной инъекцией токсина Шиги и липополисахарида, у мышей с дефицитом фактора B наблюдали меньшую тромбоцитопению, и они были защищены от почечной недостаточности по сравнению с мышами дикого типа, что свидетельствует о LEA-1-зависимой активации альтернативного пути при микрососудистом тромбозе (Morigi, M. et al., J. Immunol. 187: 172-180, 2011). Как описано в примере 33 в настоящем описании, в той же модели введение антитела против MASP-2 также являлось эффективным и повышало выживаемость после введения STX, что свидетельствует о LEA-2-зависимом пути активации комплемента при микрососудистом тромбозе.
С учетом изложенного выше, ожидают, что ингибиторы LEA-1 и LEA-2 будут оказывать независимый благоприятный терапевтический эффект в лечении или профилактике HUS. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп пациентов. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее из MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
aHUS
Атипичный HUS является редким заболеванием с предполагаемой частотой 2 на миллион в США (Loirat, C. and Fremeaux-Bacchi, V. Orphanet J. Rare Dis. 6:60-90, 2011). Атипичный HUS может развиваться в любом возрасте, хотя у большинства пациентов дебют заболевания происходит в детстве. Атипичный HUS является гетерогенным: некоторые случаи являются семейными, некоторые являются рецидивирующими, а некоторые запускаются инфекционным заболеванием, как правило, заболеванием верхних дыхательных путей или гастроэнтеритом. Дебют aHUS, как правило, является внезапным, и большинству пациентов на момент госпитализации необходим диализ. Внепочечные проявления присутствуют у приблизительно 20% пациентов и могут затрагивать центральную нервную систему, включать инфаркт миокарда, ишемическую гангрену конечностей или полиорганную недостаточность. Лечение aHUS включает поддерживающую терапию против дисфункции органов, инфузию плазмы или плазмаферез и экулизумаб, гуманизированное моноклональное антитело против C5, недавно одобренное для применения в США и Европейском Союзе. Прогноз при aHUS не столь благоприятный, как при D+HUS, с приблизительно 25% смертностью в течение острой фазы, и у большинства выживших развивается терминальная стадия почечной недостаточности.
Атипичный HUS характеризуют как заболевание с дисрегуляцией комплемента, при котором приблизительно 50% пациентов имеют мутации в генах, кодирующих белки-регуляторы комплемента (Zheng and Sadler, 2008, выше). Большинство мутаций обнаруживают в гене фактора H (FH); другие мутации затрагивают мембранный кофакторный белок (MCP), фактор I (FI), фактор B и C3. Функциональные исследования показали, что мутации в FH, MCP и FI приводят к утрате функции и, таким образом, большей активации комплемента, в то время как мутации в гене фактора B восстанавливают функцию. Эффекты этих мутаций преимущественно затрагивают альтернативный путь. Эти генетические аномалии являются скорее факторами риска, чем единственной причиной заболевания, т.к. у приблизительно 50% членов семей, несущих мутацию, к 45 годам заболевание не развивается (Loirat and Fremeaux-Bacchi, 2011, выше).
Фактор H является белком, контролирующим комплемент, защищающим ткань хозяина от разрушающего действия альтернативного пути комплемента. FH регулирует петлю амплификации альтернативного пути тремя способами: он является кофактором FI, расщепляющего C3b, он ингибирует образование конвертазы C3 альтернативного пути C3bBb, и он связывается с полианионами на поверхности клеток и клеточного матрикса и блокирует накопление C3b (Atkinson, J.P. and Goodship, T.H.J., J. Exp. Med. 6: 1245-1248, 2007). Большинство мутаций FH у пациентов с aHUS происходят в C-концевых коротких консенсусных повторяющихся доменах белка, приводя к дефектному связыванию FH с гепарином, C3b и эндотелием, но не изменяя регуляцию C3 в плазме, что свойственно N-концевым доменам (Pickering, M.C. et al., J. Exp. Med. 204: 1249- 1256, 2007). У мышей с дефицитом FH наблюдают неконтролируемую активацию C3 в плазме и спонтанно развивающийся мембранопролиферативный гломерулонефрит типа II, но не aHUS. Однако, у мышей с дефицитом FH, трансгенно экспрессирующих белок FH мыши, функционально эквивалентный aHUS-ассоциированным мутантам FH человека, спонтанно развивается HUS, но не мембранопролиферативный гломерулонефрит типа II, представляя in vivo доказательство того, что дефектный контроль активации альтернативного пути в эндотелии сосудов почек является ключевым событием в патогенезе FH-ассоциированного aHUS (Pickering et al, 2007, выше). Другая форма FH-ассоциированного aHUS развивается у пациентов, имеющих аутоантитела против FH, приводящие к утрате функциональной активности FH; большинство из этих пациентов имеют делеции в генах, кодирующих пять родственных FH белков (Loirat and Fremeaux-Bacchi, 2011, выше).
Аналогично FH, MCP ингибирует активацию комплемента, регулируя накопление C3b на клетках-мишенях. Мутации MCP приводят к образованию белков с низкой C3b-связывающей и кофакторной активностью, таким образом, делая возможной дисрегуляцию активации альтернативного пути. FI является сериновой протеазой, расщепляющей C3b и C4b в присутствие кофакторов, таких как FH и MCP, и, таким образом, предотвращает образование конвертаз C3 и C5 и ингибирует альтернативный и классический пути комплемента. Большинство из aHUS-ассоциированных мутаций FI приводят к сниженной активности FI в отношении деградации C3b и C4b (Zheng and Stadler, 2008, выше). FB является зимогеном, несущим каталитические участки конвертазы альтернативного пути C3bBb. Функциональный анализ показал, что aHUS-ассоциированные мутации FB приводят к повышенной активации альтернативного пути (Loirat and Fremeaux-Bacchi, 2011, выше). Гетерозиготные мутации в C3 ассоциированы с aHUS. Большинство мутаций C3 вызывают дефект связывания C3 с MCP, что приводит к повышению способности FB связываться с C3b и повышенному образованию конвертазы C3 (Loirat and Fremeaux-Bacchi, 2011, выше). Таким образом, aHUS является заболеванием, тесно связанным с мутациями в генах системы комплемента, приводящим к некорректному контролю петли амплификации альтернативного пути. Поскольку петля амплификации альтернативного пути зависит от протеолитической активности фактора B и поскольку LEA-1 необходимо для активации фактора B (посредством MASP-3-зависимого расщепления или фактор D-опосредованного расщепления, где MASP-1 участвует в созревании фактора D), ожидают, что средства, блокирующие LEA-1, будут предотвращать неконтролируемую активацию комплемента у предрасположенных индивидуумов. В результате, ожидают, что с помощью средств, блокирующих LEA-1, будут эффективно лечить aHUS.
Хотя центральная роль дисрегуляции петли амплификации альтернативного пути при aHUS является общепринятой, пусковые механизмы, инициирующие активацию комплемента, и участвующие в ней молекулярные пути остаются неизвестными. Не у всех индивидуумов, несущих описываемые выше мутации, развивается aHUS. Фактически, семейные исследования позволяют предполагать, что пенетрантность aHUS составляет лишь ~50% (Sullivan M. et al, Ann Hum Genet 74: 17-26 2010). Течение заболевания позволяет предполагать, что наиболее часто aHUS развивается после инициирующего события, такого как инфекция или повреждение. Хорошо известно, что возбудители инфекционных заболеваний активируют систему комплемента. В отсутствие заранее существующего приобретенного иммунитета активация комплемента возбудителями инфекционных заболеваний, главным образом, может инициироваться через LEA-1 или LEA-2. Таким образом, лектин-зависимая активация комплемента, запускаемая инфекцией, может представлять собой исходный пусковой механизм для последующей патологической амплификации активации комплемента у предрасположенных к aHUS индивидуумов, что, в конечном итоге, может приводить к прогрессированию заболевания. Таким образом, другой аспект настоящего изобретения включает лечение пациента, страдающего aHUS, вторичным по отношению к инфекции, посредством введения эффективного количества средства, ингибирующего LEA-1 или LEA-2.
Другие формы повреждения ткани хозяина, в частности, повреждение эндотелия сосудов, будут активировать комплемент через LEA-2. Эндотелиальные клетки сосудов человека, подвергнутые, например, оксидативному стрессу, отвечают, экспрессируя поверхностные молекулы, связывающиеся с лектинами и активирующие путь LEA-2 комплемента (Collard et al., Am J. Pathol 156(5): 1549-56, 2000). Повреждение сосудов после ишемии/реперфузии также активирует комплемент через LEA-2 in vivo (Moller-Kristensen et al, Scand J Immunol 61(5):426-34, 2005). Активация лектинового пути в этих условиях имеет патологические последствия для хозяина, и, как показано в примерах 22 и 23, ингибирование LEA-2 посредством блокирования MASP-2 предотвращает дальнейшее повреждение ткани хозяина и неблагоприятные исходы (см. также Schwaeble PNAS, 2011, выше).
Таким образом, известно, что другие процессы, вызывающие aHUS, также активируют LEA-1 или LEA-2. Таким образом, вероятно, что путь LEA-1 и/или LEA-2 может представлять собой исходный механизм активации комплемента, некорректно амплифицируемый при дисрегуляции у индивидуумов, генетически предрасположенных к aHUS, таким образом, инициируя патогенез aHUS. Косвенно, ожидают, что средства, блокирующие активацию комплемента через LEA-1 и/или LEA-2, будут предотвращать прогрессирование заболевания или снижать рецидивирование у предрасположенных к aHUS индивидуумов.
В качестве дополнительного доказательства этой концепции, в недавних исследованиях в качестве важного этиологического фактора случаев aHUS в детском возрасте идентифицировали Streptococcus pneumoniae (Lee, C.S. et al, Nephrology, 17(1):48-52 (2012); Banerjee R. et al, Pediatr Infect Dis J, 30(9):736-9 (2011)). В случае этой конкретной этиологии, по-видимому, имеет место неблагоприятный прогноз со значительной смертностью и продолжительным течением заболевания. Причем, эти случаи включали некишечные инфекции, приводящие к проявлениям микроангиопатии, уремии и гемолиза без доказательств одновременного наличия мутаций в генах системы комплемента, о которых известно, что они предрасполагают к aHUS. Необходимо отметить, что S. pneumoniae является особенно эффективным в активации комплемента, и преимущественно - через LEA-2. Таким образом, в случаях некишечного HUS, ассоциированного с пневмококковой инфекцией, ожидают, что проявления микроангиопатии, уремии и гемолиза запускаются, преимущественно, активацией LEA-2, и ожидают, что средства, блокирующие LEA-2, включая антитела против MASP-2, будут предотвращать прогрессирование aHUS или снижать тяжесть заболевания у этих пациентов. Таким образом, другой аспект настоящего изобретения включает лечение пациента, страдающего некишечным aHUS, ассоциированным с инфекцией S. pneumoniae, посредством введения эффективного количества средства, ингибирующего MASP-2.
TTP
Тромботическая тромбоцитопеническая пурпура (TTP) является угрожающим жизни нарушением системы свертывания крови, вызываемым аутоиммунной или наследственной дисфункцией, активирующей каскад свертывания или систему комплемента (George, JN, N Engl J Med; 354: 1927-35, 2006). Это приводит к образованию многочисленных микроскопических тромбов, или тромбозу, в небольших кровеносных сосудах по всему организму, что является характерной чертой TMA. Эритроциты подвергаются механическому воздействию, повреждающему их мембраны, что приводит к внутрисосудистому гемолизу. В результате снижается кровоток, а повреждение эндотелия приводит к повреждению органов, включая головной мозг, сердце и почки. TTP клинически отличается тромбоцитопенией, микроангиопатической гемолитической анемией, неврологическими изменениями, почечной недостаточностью и повышением температуры. В эру до плазмафереза смертность составляла 90% в течение острых эпизодов. Даже при использовании плазмафереза выживаемость в течение шести месяцев составляет приблизительно 80%.
TTP может возникать в результате генетического или приобретенного ингибирования фермента ADAMTS-13, металлопротеазы, ответственной за расщепление больших мультимеров фактора фон Виллебранда (vWF) на меньшие единицы. Ингибирование или дефицит ADAMTS-13, в конечном итоге, приводят к повышению свертывания (Tsai, H. J Am Soc Nephrol 14: 1072-1081, 2003). ADAMTS-13 регулирует активность vWF; в отсутствие ADAMTS-13 vWF образует большие мультимеры, по всей вероятности связывающиеся с тромбоцитами и вызывающие предрасположенность пациентов к агрегации тромбоцитов и тромбозу в микрососудистом русле.
У индивидуумов с TTP идентифицировали многочисленные мутации ADAMTS13. Заболевание также может развиваться по причине наличия аутоантител против ADAMTS-13. Кроме того, TTP может развиваться при раке молочной железы, желудочно-кишечного тракта или предстательной железы (George JN., Oncology (Williston Park). 25:908-14, 201 1), беременности (во втором триместре или после родов), (George JN., Curr Opin Hematol 10:339-344, 2003) или являться ассоциированной с заболеваниями, такими как ВИЧ или аутоиммунные заболевания, такие как системная красная волчанка (Hamasaki K, et al, Clin Rheumatol.,22:355-8, 2003). TTP также может быть вызвана терапией конкретными лекарственными средствами, включая гепарин, хинин, иммуноопосредованный ингредиент, противораковые химиотерапевтические средства (блеомицин, цисплатин, цитозинарабинозид, дауномицин, гемцитабин, митомицин C и тамоксифен), циклоспорин A, пероральные контрацептивы, пенициллин, рифампин и антиагреганты, включая тиклопидин и клопидогрел (Azarm, T. et al, J Res Med Sci., 16: 353-357, 2011). Другими факторами или состояниями, ассоциированными с TTP, являются токсины, такие как пчелиный яд, сепсис, секвестрация селезенки, трансплантация, васкулит, операции на сосудах и инфекции, такие как инфекция Streptococcus pneumoniae и цитомегаловирусная инфекция (Moake JL., N Engl J Med., 347:589-600, 2002). TTP по причине транзиторного функционального дефицита ADAMTS-13 может возникать как следствие повреждения эндотелиальных клеток, ассоциированного с инфекцией S. pneumoniae (Pediatr Nephrol, 26:631-5, 2011).
Плазмаферез является стандартным лечением при TTP (Rock GA, et al., N Engl J Med 325:393-397, 1991). Плазмаферез заменяет активность ADAMTS-13 у пациентов с генетическими дефектами, и с помощью него удаляют аутоантитела против ADAMTS-13 у пациентов с приобретенной аутоиммунной TTP (Tsai, H-M, Hematol Oncol Clin North Am., 21(4): 609-v, 2007). Общепринято, в терапию добавляют дополнительные средства, такие как иммуносупрессорные лекарственные средства (George, TN, N Engl J Med, 354: 1927-35, 2006). Однако, плазмаферез не является успешным для приблизительно 20% пациентов, рецидив возникает более чем у трети пациентов, и плазмаферез является дорогостоящим и технически сложным. Кроме того, многие пациенты не могут переносить плазмаферез. Таким образом, остается критическая потребность в дополнительных и лучших способах лечения TTP.
Поскольку TTP является нарушением каскада свертывания крови, лечение антагонистами системы комплемента может помочь стабилизировать и скорректировать заболевание. В то время как патологическая активация альтернативного пути комплемента связана с aHUS, роль активации комплемента при TTP является менее ясной. Функциональный дефицит ADAMTS13 важен для предрасположенности к TTP, однако его недостаточно, чтобы вызывать острый эпизод. В манифестации TTP могут участвовать факторы окружающей среды и/или другие генетические варианты. Например, гены, кодирующие белки, участвующие в регуляции каскада свертывания, vWF, функции тромбоцитов, компонентов поверхности эндотелия сосудов или системы комплемента, могут участвовать в развитии острой тромботической микроангиопатии (Galbusera, M. et al, Haematologica, 94: 166-170, 2009). В частности, показано, что критическую роль играет активация комплемента; показано, что сыворотка пациентов с тромботической микроангиопатией, ассоциированной с дефицитом ADAMTS-13, вызывает накопление C3 и MAC и последующую активацию нейтрофилов, которую можно отменять инактивацией комплемента (Ruiz-Torres MP, et al., Thromb Haemost, 93:443-52, 2005). Кроме того, недавно показано, что при острых эпизодах TTP наблюдают повышенные уровни C4d, C3bBbP и C3a (M. Reti et al, J Thromb Haemost. 10(5):791-798, 2012), что соответствует активации классического, лектинового и альтернативного путей. Эта повышенная степень активации комплемента в острых эпизодах может инициировать активацию терминального пути, и она может отвечать за дальнейшее рецидивирование TTP.
ADAMTS-13 и vWF при TTP очевидно отвечают за активацию и агрегацию тромбоцитов и их последующую роль в механическом воздействии и накоплении при микроангиопатиях. Активированные тромбоциты взаимодействуют с классическим и альтернативным путями комплемента и запускают их. Опосредованная тромбоцитами активация комплемента повышает уровни воспалительных медиаторов C3a и C5a (Peerschke E. et al., Mol Immunol, 47:2170-5 (2010)). Таким образом, тромбоциты могут служить в качестве мишеней активации классического пути комплемента при наследственной или аутоиммунной TTP.
Как описано выше, лектин-зависимая активация комплемента посредством тромбиноподобной активности MASP-1 и LEA-2-опосредованной активации протромбина является доминирующим молекулярным путем, связывающим повреждение эндотелия со свертыванием и микрососудистым тромбозом, развивающимся при HUS. Аналогично, активация LEA-1 и LEA-2 может напрямую запускать систему свертывания при TTP. Активация пути LEA-1 и LEA-2 может инициироваться в ответ на исходное повреждение эндотелия, вызываемое дефицитом ADAMTS-13 при TTP. Таким образом, ожидают, что ингибиторы LEA-1 и LEA-2, включая, в качестве неограничивающих примеров, антитела, блокирующие функцию MASP-2, функцию MASP-1, функцию MASP-3 или функцию MASP-1 и MASP-3, будут смягчать микроангиопатии, ассоциированные с микрососудистым свертыванием, тромбозом и гемолизом у пациентов, страдающих TTP.
Пациенты, страдающие TTP, как правило, поступают в отделение неотложной помощи с одним или несколькими из следующих признаков: пурпурой, почечной недостаточностью, низким уровнем тромбоцитов, анемией и/или тромбозом, включая инсульт. Современный стандарт терапии TTP включает осуществление замещающего плазмафереза с помощью катетера (например, внутривенного или другой формы катетера) в течение периода двух недель или более, как правило, три раза в неделю, но вплоть до ежедневного. Если индивидуум при тестировании является положительным на наличие ингибитора ADAMTS13 (т.е. эндогенного антитела против ADAMTS13), то плазмаферез можно осуществлять в комбинации с иммуносупрессорной терапией (например, кортикостероидами, ритуксаном или циклоспорином). Индивидуумы с рефрактерной TTP (приблизительно 20% пациентов с TTP) не отвечают на терапию плазмаферезом по меньшей мере в течение двух недель.
В соответствии с изложенным выше, в одном из вариантов осуществления в условиях первичного диагноза TTP или в случае индивидуума, проявляющего один или несколько симптомов, соответствующих диагнозу TTP (например, поражение центральной нервной системы, тяжелая тромбоцитопения (количество тромбоцитов, меньшее или равное 5000/мкл без использования аспирина, меньшее или равное 20000/мкл при использовании аспирина), тяжелое поражение сердца, тяжелое поражение легких, инфаркт кишечника или гангрена), способ относится к лечению индивидуума с использованием эффективного количества средства, ингибирующего LEA-2 (например, антитела против MASP-2), или средства, ингибирующего LEA-1 (например, антитела против MASP-1 или MASP-3), в качестве терапии первой линии в отсутствие плазмафереза или в комбинации с плазмаферезом. В качестве терапии первой линии средство, ингибирующее LEA-1 и/или LEA-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения. В некоторых вариантах осуществления средство, ингибирующее LEA-1 и/или LEA-2, вводят индивидууму в качестве терапии первой линии в отсутствие плазмафереза для избежания потенциальных осложнений плазмафереза, таких как геморрагия, инфекция и воздействия нарушений и/или аллергии, свойственных донору плазмы, или индивидууму, имеющему иные противопоказания к плазмаферезу, или в условиях, когда плазмаферез невозможен. В некоторых вариантах осуществления средство, ингибирующее LEA-1 и/или LEA-2, вводят индивидууму, страдающему TTP, в комбинации (включая совместное введение) с иммуносупрессорным средством (например, кортикостероидами, ритуксаном или циклоспорином) и/или в комбинации с концентрированным ADAMTS-13.
В некоторых вариантах осуществления способ включает введение индивидууму, страдающему TTP, средства, ингибирующего LEA-1 и/или LEA-2, с помощью катетера (например, внутривенно) в течение первого периода времени (например, острой фазы, длящейся по меньшей мере от одного дня до недели или двух недель) с последующим введением индивидууму средства, ингибирующего LEA-1 и/или LEA-2, подкожно в течение второго периода времени (например, хронической фазы по меньшей мере двух недель или более). В некоторых вариантах осуществления введение в первый и/или второй период времени осуществляют в отсутствие плазмафереза. В некоторых вариантах осуществления способ используют для профилактики у индивидуума одного или нескольких симптомов, ассоциированных с TTP.
В другом варианте осуществления способ относится к лечению индивидуума, страдающего рефрактерной TTP (т.е. индивидуума, не отвечающего на терапию плазмаферезом по меньшей мере в течение двух недель), посредством введения количества ингибитора LEA-1 и/или LEA-2, эффективного для уменьшения одного или нескольких симптомов TTP. В одном из вариантов осуществления ингибитор LEA-1 и/или LEA-2 вводят индивидууму с рефрактерной TTP на постоянной основе, в течение периода времени по меньшей мере две недели или более посредством подкожного или другого парентерального введения. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
В некоторых вариантах осуществления способ дополнительно включает определение уровня по меньшей мере одного фактора комплемента (например, C3, C5) у индивидуума до лечения и, необязательно, в течение лечения, где определение сниженного уровня по меньшей мере одного фактора комплемента по сравнению со стандартным значением или здоровым индивидуумом свидетельствует о необходимости длительного лечения с использованием средства, ингибирующего LEA-1 и/или LEA-2.
В некоторых вариантах осуществления способ включает подкожное или внутривенное введение средства, ингибирующего LEA-1 и/или LEA-2, индивидууму, страдающему или имеющему риск развития TTP. Лечение, предпочтительно, является ежедневным, но его можно осуществлять так редко, как раз в месяц. Лечение продолжают до тех пор, пока уровень тромбоцитов индивидуума не будет составлять более 150000/мл в течение по меньшей мере двух последовательных дней.
Таким образом, ожидают, что ингибиторы LEA-1 и LEA-2 будут оказывать независимый благоприятный терапевтический эффект в лечении TMA, включая HUS, aHUS и TTP. Кроме того, ожидают, что с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, будут достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп пациентов, страдающих различными формами TMA. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести тромботической микроангиопатии, такой как гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) или тромботическая тромбоцитопеническая пурпура (TTP), включающему введение индивидууму, страдающему или имеющему риск развития тромботической микроангиопатии, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
В одном из вариантов осуществления способ по этому аспекту изобретения дополнительно включает ингибирование LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести тромботической микроангиопатии, такой как гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) или тромботическая тромбоцитопеническая пурпура (TTP), включающее введение индивидууму, страдающему или имеющему риск развития тромботической микроангиопатии, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, или профилактики, или снижения тяжести тромботической микроангиопатии по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифических или двойных ингибирующих средств, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести тромботической микроангиопатии у индивидуума, страдающего или имеющего риск развития тромботической микроангиопатии. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
IX. РОЛЬ MASP-2 И MASP-3 В АСТМЕ И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Астма является распространенным хроническим воспалительным заболеванием дыхательных путей. Приблизительно 25 миллионов людей в США страдают астмой, включая семь миллионов детей младше 18 лет, при этом более половины испытывают по меньшей мере один приступ астмы каждый год, что приводит более чем к 1,7 миллионам посещений отделений неотложной помощи и 450000 госпитализаций ежегодно (веб-сайт gov/health/prof/lung/asthma/naci/asthma-info/index.htm., доступный на 4 мая 2012 года). Заболевание является гетерогенным со множеством клинических фенотипов. Наиболее распространенным фенотипом является аллергическая астма. Другие фенотипы включают неаллергическую астму, аспиринчувствительную бронхиальную астму, постинфекционную астму, профессиональную астму, астму, индуцируемую раздражителями, находящимися в воздухе, и астму физического усилия. Главные отличительные черты аллергической астмы включают гиперчувствительность дыхательных путей (AHR) к различным специфическим и неспецифическим стимулам, избыточная продукция слизи в дыхательных путях, легочная эозинофилия и повышенная концентрация сывороточного IgE. Симптомы астмы включают кашель, свистящее дыхание, ощущение сдавленности в груди и одышка. Целью лечения астмы являются контроль заболевания и минимизация обострений, ежедневных симптомов и улучшение физической активности пациентов. В современных руководствах по лечению рекомендуют поэтапное лечение до достижения контроля астмы. Первым этапом лечения является, по мере необходимости, быстродействующий ингаляционный β2-агонист с последующим добавлением контролирующих лекарственных средств, таких как ингаляционные кортикостероиды, ингаляционные β2-агонисты длительного действия, лейкотриеновые модификаторы, теофиллин, пероральные глюкокортикостероиды и моноклональное антитело против IgE.
Хотя астма является мультифакториальной по своему происхождению, как правило, общепринятым считают, что она возникает в результате некорректных иммунных ответов на распространенные антигены окружающей среды у генетически предрасположенных индивидуумов. Астма ассоциирована с активацией комплемента, и анафилотоксины (AT) C3a и C5a обладают провоспалительными и иммунорегуляторными свойствами, соответствующими развитию и модуляции аллергического ответа (Zhang, X. and Kohl, J. Expert. Rev. Clin. Immunol., 6:269-277, 2010). Однако, относительное участие классического, альтернативного и лектинового путей комплемента в астме остается не вполне понятным. Альтернативный путь может активироваться на поверхности аллергенов, и лектиновый путь может активироваться посредством распознавания полисахаридных структур аллергенов, при этом оба процесса приводят к образованию AT. Комплемент может активироваться различными путями в зависимости от являющегося причиной аллергена. Например, высокоаллергенная пыльца трав семейства Parietaria является очень эффективной в стимуляции MBL-зависимой активации C4, затрагивающей LEA-2. С другой стороны, в случае аллергена клеща домашней пыли MBL не является необходимым для активации комплемента (Varga et al. Mol Immunol, 39(14):839-46, 2003).
Триггеры астмы из окружающей среды могут активировать комплемент альтернативным путем. Например, подвергание in vitro сыворотки человека воздействию сигаретного дыма или частицам дизельного топлива приводило к активации комплемента, и на эффект не влияло присутствие ЭДТА, что позволяет предполагать активацию через альтернативный, а не классический путь (Robbins, R.A. et al, Am. J. Physiol. 260:L254-L259, 1991; Kanemitsu, H., et al., Biol. Pharm. Bull. 21: 129-132, 1998). Роль путей комплемента в аллергическом воспалении дыхательных путей оценивали в модели сенсибилизации и провокационной пробы мыши овальбумином. У мышей дикого типа развивалась AHR и воспаление дыхательных путей в ответ на провокационную пробу аэроаллергеном. В овальбуминовой модели аллергического воспаления легких мыши слитый белок Crry-Ig, ингибирующий все пути активации комплемента, являлся эффективным в профилактике AHR и воспаления легких при введении системно или местно посредством ингаляции (Taube et al., Am J Respir Crit Care Med., 168(11): 1333-41, 2003).
По сравнению с мышами дикого типа мыши с дефицитом фактора B демонстрировали меньшую AHR и воспаление дыхательных путей, в то время как у мышей с дефицитом C4 наблюдали эффекты, аналогичные таковым у мышей дикого типа (Taube, C, et al, Proc. Natl. Acad. Sci. USA 103:8084-8089, 2006). Эти результаты подтверждают роль альтернативного пути, а не классического пути, в мышиной модели провокационной пробы аэроаллергеном. Дополнительно доказательство важности альтернативного пути получали в исследовании фактора H (FH) с использованием той же мышиной модели (Takeda, K., et al, J. Immunol. 188:661-667, 2012). FH является отрицательным регулятором альтернативного пути и действует, предотвращая аутологичное повреждение собственных тканей. Обнаруживали, что эндогенный FH присутствует в дыхательных путях в течение провокационной пробы аллергеном, и ингибирование FH с использованием рекомбинантного конкурентного антагониста повышало степень AHR и воспаление дыхательных путей (Takeda et al., 2012, выше). Терапевтическая доставка CR2-fH, химерного белка, в котором соединены область связывания iC3b/C3d CR2 и комплемент-регуляторная область FH, направляющего комплемент-регуляторную активность fH в участки действующей активации комплемента, обеспечивала развитие AHR и эозинофильной инфильтрации в дыхательных путях после провокационной пробы аллергеном (Takeda et al., 2012, выше). Демонстрировали протективный эффект с использованием овальбумина, а также аллергена амброзии, являющегося важным аллергеном у людей.
Роль лектин-зависимой активации комплемента при астме оценивали в модели грибковой астмы мыши (Hogaboam et al, J. Leukocyte Biol. 75:805-814, 2004). В этих исследованиях использовали мышей с генетическим дефицитом маннозо-связывающего лектина-A (MBL-A), углевод-связывающего белка, функционирующего в качестве распознающего компонента для активации лектинового пути комплемента. Мышей MBL-A(+/+) и MBL-A(-/-), сенсибилизированных Aspergillus fumigatus, оценивали через 4 и 28 дней после i.t.-провокационной пробы с использованием конидии A. fumigatus. AHR у сенсибилизированных мышей MBL-A(-/-) являлась значимо меньшей в оба момента времени после провокационной пробы с использованием конидий по сравнению с группой сенсибилизированных мышей MBL-A(+/+). Уровни TH2-цитокинов в легких (IL-4, IL-5 и IL-13) являлись значимо меньшими у сенсибилизированных A. fumigatus мышей MBL-A(-/-) по сравнению с группой дикого типа через 4 дня после провокационной пробы с использованием конидий. Эти результаты свидетельствуют о том, что MBL-A и лектиновый путь играют главную роль в развитии и поддержании AHR при хронической грибковой астме.
Результаты, подробно описываемые выше, позволяют предполагать участие лектин-зависимой активации комплемента в патогенезе астмы. Экспериментальные данные подтверждают, что ключевую роль играет активация фактора B. В свете основополагающей роли LEA-1 в лектин-зависимой активации фактора B и последующей активации альтернативного пути, ожидают, что средства, блокирующие LEA-1, будут полезными для лечения конкретных форм астмы, опосредованных альтернативным путем. Таким образом, такое лечение может являться особенно полезным при астме, индуцированной клещом домашней пыли, или астме, вызываемой триггерами из окружающей среды, такими как сигаретный дым или дизельное топливо. С другой стороны, астматические ответы, запускаемые пыльцой трав, вероятно, вызывают LEA-2-зависимую активацию комплемента. Таким образом, ожидают, что средства, блокирующие LEA-2, будут особенно полезными в лечении астматических состояний у этой подгруппы пациентов.
В свете данных, подробно изложенных выше, авторы настоящего изобретения считают, что LEA-1 и LEA-2 опосредуют патологическую активацию комплемента при астме. В зависимости от аллергена-возбудителя может предпочтительно вовлекаться LEA-1 или LEA-2. Таким образом, средство, блокирующее LEA-1, в комбинации со средством, блокирующим LEA-2, может иметь применимость в лечении множества форм астмы, независимо от лежащей в основе этиологии. Средства, блокирующие LEA-1 и LEA-2, могут обладать взаимодополняющим, аддитивным или синергическим действием при профилактике, лечении или реверсировании воспалительного процесса в легких и симптомов астмы.
Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести астмы, включающему введение индивидууму, страдающему или имеющему риск развития астмы, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
В одном из вариантов осуществления способ по этому аспекту изобретения дополнительно включает ингибирование LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести астмы, включающее введение индивидууму, страдающему или имеющему риск развития астмы, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, или профилактики или снижения тяжести астмы по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести астмы у индивидуума, страдающего или имеющего риск развития астма. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
X. РОЛЬ MASP-2 И MASP-3 В БОЛЕЗНИ ПЛОТНОГО ДЕПОЗИТА И ТЕРАПЕВТИЧЕСК СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Мембранопролиферативный гломерулонефрит (MPGN) является заболеванием почек, морфологически отличающимся пролиферацией мезангиальных клеток и утолщением стенок клубочковых капилляров по причине субэндотелиального разрастания мезангия. MPGN классифицируют как первичный (также обозначаемый как идиопатический) или вторичный на фоне таких заболеваний, как инфекционные заболевания, системные болезни иммунных комплексов, неоплазии, хронические заболевания печени и т.п. Идиопатический MPGN включает три морфологических типа. Тип I, или классический MPGN, отличается субэндотелиальным накоплением иммунных комплексов и активацией классического пути комплемента. Тип II, или болезнь плотного депозита (DDD), отличается дополнительными интрамембранозным накоплением плотного депозита. Тип III отличается дополнительными субэпителиальными отложениями. Идиопатический MPGN является редким, на него приходится от приблизительно 4 до 7% первичных почечных причин нефротического синдрома (Alchi, B. and Jayne, D. Pediatr. Nephrol. 25: 1409-1418, 2010). MPGN, главным образом, поражает детей и молодежь и может присутствовать в виде нефротического синдрома, острого нефритического синдрома, бессимптомной протеинурии и гематурии, или рецидивирующей макрогематурии. Дисфункция почек развивается у большинства пациентов, и заболевание имеет медленно прогрессирующее течение, при этом у приблизительно 40% пациентов развивается терминальная стадия почечной недостаточности в течение 10 лет после постановки диагноза (Alchi and Jayne, 2010, выше). Современные варианты лечения включают кортикостероиды, иммуносупрессорные, антитромбоцитарные схемы лечения и плазмаферез.
DDD диагностируют по отсутствию иммуноглобулинов и наличию C3 при иммунофлуоресцентном окрашивании биоптатов почек, и при электронной микроскопии обнаруживают характерное накопление осмофильного плотного депозита вдоль гломерулярных базальных мембран. DDD вызывает дисрегуляция альтернативного пути комплемента (Sethi et al, Clin J Am Soc Nephrol. 6(5): 1009-17, 2011), которая может являться результатом ряда различных механизмов. Наиболее распространенным нарушением системы комплемента при DDD является наличие нефритических факторов C3, являющихся аутоантителами против конвертазы C3 альтернативного пути (C3bBb), повышающими его время полужизни и, таким образом, активацию пути (Smith, R.J.H. et al, Mol. Immunol. 48: 1604-1610, 2011). Другие нарушения альтернативного пути включают аутоантитела против фактора H, блокирующие функционирование фактора H, возникновение функциональных мутаций C3 и генетический дефицит фактора H (Smith et al., 2011, выше). В недавних сообщениях о клинических случаях показано, что лечение экулизумабом (моноклональным антителом против C5) ассоциировано с улучшением функции почек у двух пациентов с DDD (Daina, E. et al, New Engl. J. Med. 366: 1161-1163, 2012; Vivarelli, M. et al, New Engl. J. Med. 366: 1163-1165, 2012), что позволяет предполагать этиологическую роль активации комплемента при исходах нарушений функции почек.
Учитывая представленные выше генетические, функциональные и иммуногистохимические данные и данные о клинических случаях, твердо установлена центральная роль комплемента в патогенезе DDD. Таким образом, ожидают, что воздействия, блокирующие механизмы активации комплемента, вызывающие заболевание, или продукты последующей активации комплемента, будут терапевтически применимыми для лечения этого состояния.
Хотя данные генетических исследований человека позволяют предполагать, что ключевую роль играет ненадлежащий контроль или избыточная активация петли амплификации альтернативного пути, комплемент-инициирующие явления не идентифицированы. С помощью иммуногистохимических исследований биоптатов почек доказали накопление MBL в пораженной ткани, что позволяет предполагать участие лектинового пути в инициации патологической активации комплемента при DDD (Lhotta et al, Nephrol Dial Transplant., 14(4):881-6, 1999). Затем важность альтернативного пути доказали на экспериментальных моделях. У мышей с дефицитом фактора H развивалась прогрессирующая протеинурия и патологические нарушения почек, характерные для нарушения у человека (Pickering et al., Nat Genet., 31(4):424, 2002). Pickering et al. дополнительно показали, что абляция фактора B, опосредующего LEA-1-зависимую активацию альтернативного пути, полностью защищает мышей с дефицитом фактора H от DDD (Pickering et al, Nat Genet., 31(4):424, 2002).
Таким образом, ожидают, что средства, блокирующие LEA-1, будут эффективно блокировать лектин-зависимую активацию альтернативного пути и, таким образом, будут обеспечивать эффективное лечение DDD. Учитывая дисрегуляцию петли амплификации альтернативного пути у пациентов DDD, дополнительно можно ожидать, что эффективными будут средства, блокирующие петлю амплификации. Поскольку средства, воздействующие на LEA-1, блокирующие MASP-1 или MASP-1 и MASP-3, ингибируют созревание фактора D, прогнозируют, что такие средства будут эффективно блокировать петлю амплификации альтернативного пути.
Как подробно описано выше, в образцах поврежденных почек обнаруживали выраженное накопление MBL, указывающее на возможно участие явлений лектин-зависимой активации в патогенезе DDD. Поскольку установлено исходное повреждение ткани в клубочковых капиллярах, возможно, что происходит дополнительное связывание MBL с поврежденным клубочковым эндотелием и нижележащими мезангиальными структурами. Хорошо известно, что такие повреждения ткани приводят к активации LEA-2, которая, таким образом, может вызывать дальнейшую активацию комплемента. Таким образом, также ожидают, что средства, блокирующие LEA-2, будут иметь применимость в профилактике дальнейшей активации комплемента на поврежденных клубочковых структурах и, таким образом, препятствовать дальнейшему прогрессированию заболевания в терминальную стадию почечной недостаточности.
Данные, подробно изложенные выше, позволяют предполагать, что LEA-1 и LEA-2 стимулируют отдельные процессы патологической активации комплемента при DDD. Таким образом, ожидают, что средство, блокирующее LEA-1, и средство, блокирующее LEA-2, в отдельности или в комбинации будут применимыми в лечении DDD.
Ожидают, что при использовании в комбинации средства, блокирующие LEA-1 и LEA-2, будут более эффективными, чем любое из средств в отдельности, или будут применимыми для лечения различных стадий заболевания. Таким образом, средства, блокирующие LEA-1 и LEA-2, могут иметь взаимодополняющее, аддитивное или синергическое действие при профилактике, лечении или реверсировании DDD-ассоциированной дисфункции почек.
Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA2. Оптимально, средства, блокирующие LEA-1 и LEA-2, с функцией ингибирования можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3 и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести болезни плотного депозита, включающему введение индивидууму, страдающему или имеющему риск развития болезни плотного депозита, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Другой аспект относится к способу ингибированию LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести болезни плотного депозита, включающему введение индивидууму, страдающему или имеющему риск развития болезни плотного депозита, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1 и LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести болезни плотного депозита, включающему введение индивидууму, страдающему или имеющему риск развития болезни плотного депозита, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3.
В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, профилактики или снижения тяжести болезни плотного депозита по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средства, ингибирующие LEA-1 и/или LEA-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести болезни плотного депозита у нуждающегося в этом индивидуума. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XI. РОЛЬ MASP-2 И MASP-3 В СЛАБОИММУННОМ НЕКРОТИЗИРУЮЩЕМ ГЛОМЕРУЛОНЕФРИТЕ С ПОЛУЛУНИЯМИ И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Слабоиммунный некротизирующий гломерулонефрит с полулуниями (NCGN) является формой быстропрогрессирующего гломерулонефрита, при котором стенки клубочковых капилляров демонстрируют признаки воспаления, а также имеют небольшую степень накопления детектируемых иммунных комплексов или антител против базальной мембраны клубочков. Состояние ассоциировано с быстрым снижением функции почек. Обнаружено, что у большинства пациентов с NCGN присутствуют антинейтрофильные цитоплазматические аутоантитела (ANCA), и, таким образом, его относят к группе заболеваний, называемых ANCA-ассоциированными васкулитами. Васкулит является нарушением кровеносных сосудов, отличающимся воспалением и фибриноидным некрозом стенок сосудов. Системные васкулиты классифицируют на основании размера сосудов: большие, средние и мелкие. Несколько форм мелкососудистого васкулита ассоциировано с наличием ANCA, а именно гранулематоз Вегенера, микроскопический полиангиит, синдром Чарга-Стросса и почечно-ограниченный васкулит (NCGN). Они также могут являться проявлением основного состояния, такого как системная красная волчанка. Антигены-мишени ANCA включают протеиназу-3 (PR3) и миелопероксидазу (MPO). Слабоиммунный NCGN является редким, с зарегистрированной заболеваемостью приблизительно 4 на миллион В Уэссексе, Великобритания (Hedger, N. et al., Nephrol. Dial. Transplant. 15: 1593-1599, 2000). Среди группы 128 пациентов со слабоиммунным NCGN из Уэссекса 73% являлись ANCA-положительными, и 59% пациентов нуждались в первичном диализе, а 36% - в длительном диализе. Лечение слабоиммунного NCGN включает кортикостероиды и иммуносупрессорные средства, такие как циклофосфамид и азатиоприн. Дополнительные варианты лечения ANCA-ассоциированных васкулитов включают ритуксимаб и плазмаферез (Chen, M. and Kallenberg, C.G.M. Nat. Rev. Rheumatol. 6:653-664, 2010).
Хотя NCGN отличается низкой степенью накопления комплемента, альтернативный путь комплемента участвует в его патогенезе. При оценке биоптатов почек 7 пациентов с MPO-ANCA-ассоциированным слабоиммунным NCGN определяли наличие мембраноатакующих комплексов, C3d, фактора B и фактора P (не определенные в биоптатах от нормальных контролей или пациентов с болезнью с минимальными изменениями), в то время как не определяли C4d и маннозо-связывающий лектин, что позволяет предполагать избирательную активацию альтернативного пути (Xing, G.Q. et al. J. Clin. Immunol. 29:282-291, 2009). Экспериментальный NCGN можно индуцировать переносом IgG против MPO в мышей дикого типа или спленоцитов против MPO в мышей с иммунодефицитом (Xiao, H. et al. J. Clin. Invest. 110:955-963, 2002). В этой модели NCGN мыши исследовали роль конкретных путей активации комплемента с использованием нокаутных мышей. После инъекции IgG против MPO у мышей C4-/- развивалось заболевание почек, сравнимое с таковым у мышей дикого типа, в то время как у мышей C5-/- и фактор B-/- не развивалось заболевание почек, что свидетельствует об участии альтернативного пути в этой модели, но не классического и лектинового путей (Xiao, H. et al. Am. J. Pathol. 170:52-64, 2007). Кроме того, инкубация MPO-ANCA или PR3-ANCA IgG от пациентов с TNF-α-примированными нейтрофилами человека вызывала высвобождение факторов, приводившее к активации комплемента в нормальной сыворотке человека, определяемой по образованию C3a; этот эффект не наблюдали при использовании IgG здоровых индивидуумов, что позволяет предполагать потенциальную патогенетическую роль ANCA в активации нейтрофилов и комплемента (Xiao et al., 2007, выше).
Учитывая описанную выше роль альтернативного пути в этом состоянии, ожидают, что блокирование активации альтернативного пути будет иметь применимость в лечение ANCA-положительного NCGN. Учитывая необходимость активации fB для развития патогенеза, ожидают, что ингибиторы LEA-1 будут особенно применимыми в лечении этого состояния и в профилактике дальнейшего снижения функции почек у этих пациентов.
У другой подгруппы пациентов развивается прогрессирующий почечный васкулит с серповидными образованиями, сопровождающийся быстрым снижением функции почек в отсутствие ANCA. Эту форму состояния обозначают как ANCA-негативный NCGN, и на него приходится приблизительно одна треть всех пациентов со слабоиммунным NCGN (Chen et al, JASN 18(2): 599-605, 2007). Эти пациенты, как правило, моложе, и исходы почечных нарушений, как правило, являются особенно тяжелыми. (Chen et al, Nat Rev Nephrol, 5(6):313-8, 2009). Дифференциальным патологическим признаком у этих пациентов является накопление MBL и C4d в очагах повреждения почек (Xing et al., J Clin Immunol. 30(1): 144-56, 2010). Интенсивность окрашивания биоптатов почек на MBL и C4d отрицательно коррелирует с функцией почек (Xing et al, 2010, выше). Эти результаты подтверждают важную роль лектин-зависимой активации комплемента в патогенезе. То, что, как правило, в образцах поврежденной ткани обнаруживают C4d, но не фактор B, свидетельствует об участии LEA-2.
Учитывая описываемую выше роль лектин-зависимой активации комплемента в ANCA-отрицательном NCGN, ожидают, что блокирование активации пути LEA-2 будет иметь применимость в лечении ANCA-отрицательного NCGN.
Данные, подробно изложенные выше, позволяют предполагать, что LEA-1 и LEA-2 опосредуют патологическую активацию комплемента при ANCA-положительном и ANCA-отрицательном NCGN, соответственно. Таким образом, ожидают, что средство, блокирующее LEA-1, в комбинации со средством, блокирующим LEA-2, будет иметь применимость в лечении всех форм слабоиммунного NCGN, независимо от лежащей в основе этиологии. Таким образом, средства, блокирующие LEA-1 и LEA-2, могут иметь взаимодополняющее, аддитивное или синергическое действие при профилактике, лечении или реверсировании NCGN-ассоциированной дисфункции почек.
С помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп пациентов. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитела с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести слабоиммунного некротизирующего гломерулонефрита с полулуниями, включающему введение индивидууму, страдающему или имеющему риск развития слабоиммунного некротизирующего гломерулонефрита с полулуниями, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Другой аспект относится к способу ингибирования LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести слабоиммунного некротизирующего гломерулонефрита с полулуниями, включающему введение индивидууму, страдающему или имеющему риск развития слабоиммунного некротизирующего гломерулонефрита с полулуниями, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1- и LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести слабоиммунного некротизирующего гломерулонефрита с полулуниями, включающему введение нуждающемуся в этом индивидууму терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3.
В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, или профилактики, или снижения тяжести слабоиммунного некротизирующего гломерулонефрита с полулуниями по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести слабоиммунного некротизирующего гломерулонефрита с полулуниями. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XII. РОЛЬ MASP-2 И MASP-3 В ТРАВМАТИЧЕСКОМ ПОВРЕЖДЕНИИ ГОЛОВНОГО МОЗГА И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Травматическое повреждение головного мозга (TBI) является значительной проблемой мирового здравоохранения, приводящей по меньшей мере к 10 миллионам летальных исходов или госпитализаций ежегодно (Langlois, J. A. et al., J. Head Trauma Rehabil. 21:375-378, 2006). В 2003 году зарегистрировано приблизительно 1,6 миллиона TBI в США, включая 1,2 миллиона посещений отделений неотложной помощи, 290000 госпитализаций и 51000 летальных исходов (Rutland-Brown, W. et al, J. Head Trauma Rehabil. 21:544-548, 2006). Большинство TBI в США вызвано падениями и дорожно-транспортными происшествиями. TBI может приводить к длительным или пожизненным физическим, когнитивным, поведенческим и эмоциональным последствиям. Более 5 миллионов американцев живут с длительной или пожизненной недееспособностью, ассоциированной с TBI (Langlois et al, 2006, выше).
TBI может включать проникновение в ткань головного мозга ("проникающие" повреждения) или повреждения без проникновения в ткань головного мозга ("закрытые" повреждение). При проникающей и закрытой TBI профили повреждения и ассоциированные нейропсихические остаточные явления могут различаться. Хотя каждое повреждение является уникальным, некоторые области головного мозга особенно уязвимы при травматическом повреждении головного мозга, включая лобную кору и субфронтальное белое вещество, базальные ганглии и промежуточный мозг, передний отдел ствола мозга и височные доли, включая гиппокамп (McAllister, T.W. Dialogues Clin. Neurosci. 13:287-300, 2011). TBI может приводить к изменениям в системах некоторых нейромедиаторов, включая высвобождение глутамата и других возбуждающих аминокислот в течение острой фазы, и хроническим изменениям катехоламинергической и холинергической систем, которые могут быть связаны с нейроповеденческими нарушениями (McAllister, 2011, выше). Выжившие после значительных TBI часто страдают когнитивными нарушениями, изменениями личности и усилением психиатрических расстройств, в частности, депрессии, тревожности и посттравматическое стрессовое расстройство. Несмотря на интенсивные исследования, не обнаружено клинически эффективного лечения TBI, которое могло бы снижать смертность и клинические проявления и улучшать функциональный исход.
Факторы комплемента и TBI
В ряде исследований идентифицировали взаимосвязь белков комплемента и неврологических нарушений, включая болезнь Альцгеймера, рассеянный склероз, миастению, синдром Гийена-Барре, нейролюпус и инсульт (обзор в Wagner, E., et al, Nature Rev Drug Disc. 9: 43-56, 2010). Недавно показана роль C1q и C3 в элиминации синапсов, таким образом, вероятно, факторы комплемента участвуют в нормальном функционировании ЦНС и нейродегенеративных заболеваниях (Stevens, B. et al, Cell 131: 1164-1178, 2007). Ген MASP-1 и MASP-3 интенсивно экспрессируется в головном мозге, а также в линии глиомных клеток T98G (Kuraya, M. et al, Int Immunol., 15:109-17, 2003), что согласуется с ролью лектинового пути в ЦНС.
MASP-1 и MASP-3 являются ключевыми для непосредственной защиты против патогенов и измененных собственных клеток, но лектиновый путь также отвечает за тяжелое повреждение тканей после инсульта, инфаркта миокарда и других повреждениях при ишемии-реперфузии. Аналогично, MASP-1 и MASP-3 являются вероятными медиаторами повреждения тканей, вызываемого TBI. Показано, что ингибирование фактора B альтернативного пути смягчает TBI в двух моделях на мышах. Нокаутные по фактору B мыши защищены от комплемент-опосредованного нейровоспаления и нейропатологии после TBI (Leinhase I, et al, BMC Neurosci. 7:55, 2006). Кроме того, антитело против фактора B снижало повреждение тканей головного мозга и гибель нейронов у мышей с индуцированной TBI (Leinhase I, et al, J Neuroinflammatory 4: 13, 2007). MASP-3 напрямую активирует фактор B (Iwaki, D. et al., J Immunol. 187:3751-8, 2011) и, таким образом, также является вероятным медиатором TBI. Аналогично ингибированию фактора B, ожидают, что ингибиторы LEA-1, такие как антитела против MASP-3, будут представлять многообещающую стратегию лечения повреждения тканей и последующих остаточных явлений при TBI.
Таким образом, ингибиторы LEA-1 и LEA-2 могут оказывать независимый благоприятный терапевтический эффект при TBI. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп больных. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания может связываться с MASP-1/3 или MASP-2 и блокировать их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения или снижения тяжести травматического повреждения головного мозга, включающему введение индивидууму, страдающему травматическим повреждением головного мозга, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, интракраниального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Другой аспект относится к способу ингибирования LEA-2-зависимой активации комплемента для лечения или снижения тяжести травматического повреждения головного мозга, включающему введение индивидууму, страдающему травматическим повреждением головного мозга, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1- и LEA-2-зависимой активации комплемента для лечения или снижения тяжести травматического повреждения головного мозга, включающему введение индивидууму, страдающему травматическим повреждением головного мозга, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3.
В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения или снижения тяжести травматического повреждения головного мозга по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного, интракраниального или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения или снижения тяжести травматического повреждения головного мозга. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XIII. РОЛЬ MASP-2 И MASP-3 В АСПИРАЦИОННОЙ ПНЕВМОНИИ И ТЕРАПЕВТИЧЕСК СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Аспирацию определяют как вдыхание содержимого ротоглотки или желудка с его попаданием в нижние дыхательные пути. Аспирация может приводить к осложнениям: аспирационному (химическому) пневмониту, первичной бактериальной аспирационной пневмонии или бактериальной инфекции, вторичной по отношению к химическому пневмониту. Факторы риска аспирации включают пониженные уровни сознания (например, при травме головы, индуцируемых алкоголем или лекарственными средствами изменениях чувствительности, инсульте), различные желудочно-кишечные и пищеводные нарушения и нервно-мышечные заболевания. Считают, что 5-15% из 4,5 миллиона случаев внебольничной пневмонии являются результатом аспирационной пневмонии (Marik, P.E. New Engl. J. Med. 344:665-671, 2001). Лечение химического пневмонита, в основном, является поддерживающим, и использование эмпирической терапии антибиотиками является спорным. Лечение бактериальной аспирационной пневмонии осуществляют с использованием соответствующих антибиотиков, учитывая то, произошла ли аспирация вне больницы или в больнице, т.к. в этих условиях вероятные возбудители различаются. Необходимо принимать меры для профилактики аспирации у пациентов с высоким риском, например, пожилых пациентов в домах престарелых, имеющих нарушенный глоточный рефлекс. Меры, показавшие свою эффективность в профилактике, включают поднятие головной части кровати при кормлении, профилактическую санацию зубов и хорошую гигиену ротовой полости. Профилактические антибиотики не показали свою эффективность, и их не рекомендуют, т.к. они могут приводить к появлению резистентных организмов.
Предлагают модуляцию компонентов комплемента для ряда клинических показаний, включая инфекционное заболевание - сепсис, вирусные, бактериальные и грибковые инфекции - и легочные нарушения - респираторный дистресс-синдром, хроническую обструктивную болезнь легких и кистозный фиброз (обзор в Wagner, E., et al, Nature Rev Drug Disc. 9: 43-56, 2010). Основания для этого предложения представлены в многочисленных клинических и генетических исследованиях. Например, наблюдают значимо меньшую частоту пациентов с низкими уровнями MBL с клиническим туберкулезом (Soborg et al, Journal of Infectious Diseases 188:777-82, 2003), что позволяет предполагать, что низкие уровни MBL ассоциированы с защитой от заболевания.
В модели кислотного аспирационного повреждения у мыши, Weiser MR et al., J. Appl. Physiol. 83(4): 1090-1095, 1997, показали, что мыши, нокаутные по C3, были защищены от значительного повреждения; в то время как мыши, нокаутные по C4, защещены не были, что свидетельствует о том, что активация комплемента опосредована альтернативным путем. Таким образом, ожидают, что блокирование альтернативного пути с использованием ингибиторов LEA-1 будет оказывать благоприятный терапевтический эффект при аспирационной пневмонии.
Таким образом, ингибиторы LEA-1 и LEA-2 могут оказывать независимый благоприятный терапевтический эффект при аспирационной пневмонии. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп больных. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания связывается с MASP-1/3 или MASP-2 и блокирует их.
Один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения аспирационной пневмонии посредством введения индивидууму, страдающему таким состоянием или другой комплемент-опосредованной пневмонией, композиции, содержащей терапевтически эффективное количество средства, ингибирующего MASP-1, средства, ингибирующего MASP-3, или комбинации средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить местно в легкие, например, с помощью ингалятора. Альтернативно, средство, ингибирующее MASP-1 MASP-3, или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, перорального введения. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики или снижения тяжести аспирационной пневмонии, включающему введение индивидууму, страдающему или имеющему риск развития аспирационной пневмонии, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Другой аспект относится к способу ингибирования LEA-2-зависимой активации комплемента для лечения, профилактики или снижения тяжести аспирационной пневмонии, включающему введение индивидууму, страдающему или имеющему риск развития аспирационной пневмонии, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1 и LEA-2-зависимой активации комплемента для лечения или снижения тяжести аспирационной пневмонии, включающему введение индивидууму, страдающему аспирационной пневмонии, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3. В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения или снижения тяжести аспирационной пневмонии по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1 а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести аспирационной пневмонии у нуждающегося в этом индивидуума. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XIV. РОЛЬ MASP-2 И MASP-3 В ЭНДОФТАЛЬМИТЕ И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Эндофтальмит является воспалительным нарушением полости глазного яблока и, как правило, вызван инфекцией. Эндофтальмит может являться эндогенным, возникающим в результате гематогенного распространения организмов из отдаленного очага инфекции (например, эндокардита), или экзогенным, возникающим в результате прямого заражения организмом из внешней среды, как осложнения офтальмологической операции, попадания инородных тел и/или тупой или проникающей травмы глаза. Экзогенный эндофтальмит является гораздо более распространенным, чем эндогенный, и большинство случаев экзогенного эндофтальмита являются результатом офтальмологической операции. В США операция по поводу катаракты является основной причиной эндофтальмита, и он развивается в 0,1-0,3% случаев этой операции с существенным повышением частоты заболеваемости в течение последнего десятилетия (Taban, M. et al, Arch. Ophthalmol. 123:613-620, 2005). Постоперационный эндофтальмит может развиваться остро, в течение 2 недель после операции, или замедленно, в течение месяцев после операции. Острый эндофтальмит, как правило, начинается с боли, покраснения, отека век и уменьшения остроты зрения. Эндофтальмит с замедленным началом менее распространен, чем острая форма, и пациенты могут сообщать только об умеренной боли и фоточувствительности. Лечение эндофтальмита зависит от первопричины и может включать системные и/или интравитреальные антибиотики. Эндофтальмит может приводить к снижению или потере зрения. Как описано выше в случае AMD, множество генов путей комплемента ассоциировано с офтальмологическими нарушениями, и они, в особенности, включают гены лектинового пути. Например, при разных подтипах AMD идентифицировали MBL2 (Dinu V, et al., Genet Epidemiol 31: 224-37, 2007). Вероятно, пути LEA-1 и LEA-2 участвуют в воспалительных нарушениях глаза, таких как эндофтальмит (Chow SP et al, Clin Experiment Ophthalmol. 39:871-7, 2011). Chow et al. исследовали уровни MBL у пациентов с эндофтальмитом и показали, что уровни MBL и функциональной активности лектинового пути значимо повышаются в воспаленных глазах человека, но фактически неопределимы в невоспаленных контрольных глазах. Это позволяет предполагать роль MBL и лектинового пути в угрожающих потерей зрения воспалительных нарушениях глаза, в частности, эндофтальмите. Кроме того, в модели грибкового кератита мыши ген MBL-A являлся одним из пяти генов воспалительных путей, подверженных повышающей регуляции (Wang Y., et al, Mol Vis 13: 1226-33, 2007).
Таким образом, ожидают, что ингибиторы LEA-1 и LEA-2 будут оказывать независимый благоприятный терапевтический эффект при лечении эндофтальмита. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп больных. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания связывается с MASP-1/3 или MASP-2 и блокирует их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести эндофтальмита, включающему введение индивидууму, страдающему или имеющему риск развития эндофтальмита, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить местно в глаз, например, посредством промывания или нанесения композиции в форме местного геля, мази или капель или посредством интравитреального введения. Альтернативно, средство, ингибирующее MASP-1, MASP-3, или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Другой аспект относится к способу ингибирования LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести эндофтальмита, включающему введение индивидууму, страдающему или имеющему риск развития эндофтальмита, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1- и LEA-2-зависимой активации комплемента для лечения или снижения тяжести эндофтальмита, включающему введение индивидууму, страдающему эндофтальмитом, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3.
В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, или профилактики или снижения тяжести эндофтальмита по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Средство, ингибирующее MASP-2, можно вводить местно в глаз, например, посредством промывания или нанесения композиции в форме местного геля, мази или капель или посредством интравитреальной инъекции. Альтернативно, средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести эндофтальмита у нуждающегося в этом индивидуума. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XV. РОЛЬ MASP-2 И MASP-3 В НЕЙРОМИЕЛИТЕ ЗРИТЕЛЬНОГО НЕРВА И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Нейромиелит зрительного нерва (NMO) является аутоиммунным заболеванием, поражающим зрительные нервы и спинной мозг. Это приводит к воспалению зрительного нерва, известному как неврит зрительного нерва, и спинного мозга, известному как миелит. Повреждения спинного мозга при NMO могут приводить к слабости или параличу нижних или верхних конечностей, слепоте, дисфункции мочевого пузыря и пищеварительного тракта и нарушениям чувствительности.
NMO имеет несколько общих черт с рассеянным склерозом (MS), т.к. оба являются результатом иммунной агрессии против мишеней в CNS и оба приводят к демиелинизации (Papadopoulos and Verkman, Lancet Neurol, 11(6):535-44, 2013). Однако, молекулярные мишени, лечение и повреждения при NMO отличаются от таковых при MS. В то время как MS, в большей степени, опосредован T-клетками, у пациентов NMO, как правило, обнаруживают антитела против белка водных каналов аквапорина 4 (AQP4), белка, обнаруживаемого в астроцитах, окружающих гематоэнцефалический барьер. Интерферон бета является наиболее общеупотребительной терапией при MS, но, как правило, считают, что он вреден при NMO. Очаги воспаления при NMO обнаруживают в спинном мозге и зрительном нерве, и они могут прогрессировать в головной мозг, включая белое и серое вещество. Демиелинизация, происходящая в очагах NMO, опосредована комплементом (Papadopoulos and Verkman, Lancet Neurol, 11(6):535-44, 2013).
По-видимому, комплементзависимая цитотоксичность является основным механизмом, вызывающим развитие NMO. У более 90% пациентов с NMO обнаруживают антитела IgG против AQP4 (Jarius and Wildemann, Jarius S, Wildemann B., Nat Rev Neurol. 2010 Jul; 6(7):383-92). Эти антитела инициируют образование повреждений гематоэнцефалического барьера. Исходный комплекс антиген-антитело - AQP4/AQP4-IgG - на поверхности астроцитов активирует классический путь комплемента. Это приводит к образованию мембраноатакующих комплексов на поверхности астроцитов, приводящему к гранулоцитарной инфильтрации, демиелинизации, и в конечном итоге, к некрозу астроцитов, олигодендроцитов и нейронов (Misu et al, Acta Neuropathol 125(6):815-27, 2013). Эти события на клеточном уровне отражаются в деструкции ткани и образованию кистозных, некротических очагов.
Очевидно, классический путь комплемента критичен для патогенеза NMO. В очагах NMO обнаруживают накопление вокруг сосудов иммуноглобулинов и активированных компоненты комплемент (Jarius et al, Nat Clin Pract Neurol. 4(4):202-14, 2008). Кроме того, из цереброспинальной жидкости пациентов с NMO выделяют белки комплемента, такие как C5a (Kuroda et al, J Neuroimmunol., 254(l-2): 178-82, 2013). Кроме того, сывороточные IgG, полученные от пациентов с NMO, могут вызывать комплемент-зависимую цитотоксичность в модели NMO мыши (Saadoun et al, Brain, 133(Pt 2):349-61, 2010). Моноклональное антитело против C1q предотвращает комплемент-опосредованное разрушение астроцитов и повреждения в модели NMO мыши (Phuan et al, Acta Neuropathol, 125(6):829-40, 2013).
Альтернативный путь комплемента служит для усиления общей активности комплемента. Harboe and colleagues (2004) показали, что селективная блокада альтернативного пути ингибировала образование более 80% мембраноатакующих комплексов, индуцируемое классическим путем (Harboe et al, Clin Exp Immunol 138(3):439-46, 2004). Tϋzϋn and colleagues (2013) исследовали продукты классического и альтернативного путей у пациентов с NMO (Tϋzϋn E, et al, J Neuroimmunol. 233(1-2): 211-5, 2011). Для оценки активности классического пути измеряли C4d, продукт расщепления C4, и он был повышен в сыворотках пациентов с NMO по сравнению с контролями (повышение в 2,14 раза). Кроме того, у пациентов с NMO наблюдали повышение фактора Bb, продукта расщепления фактора B альтернативного пути, по сравнению с пациентами с MS или нормальными контрольными индивидуумами (повышение в 1,33 раз). Это позволяет предполагать, что функционирование альтернативного пути при NMO также повышено. Ожидают, что эта активация будет повышать общую активацию комплемента, и, фактически, sC5b-9, конечный продукт каскада комплемента, был значимо повышен (повышение в 4,14 раза).
Ожидают, что специфические ингибиторы MASP-3 будут оказывать благоприятный эффект при лечении пациентов, страдающих NMO. Как показано в примерах 17 и 18, сыворотка с дефицитом MASP-3 не способна активировать фактор B, необходимый компонент конвертазы C5, или фактор D, центральный активатор альтернативного пути. Таким образом, также ожидают, что блокирование активности MASP-3 с использованием ингибирующего средства, такого как антитело или низкомолекулярное соединение, будет ингибировать активацию фактора B и фактора D. Ингибирование этих двух факторов будет прекращать амплификацию альтернативного пути, приводя к снижению общей активности комплемента. Таким образом, ингибирование MASP-3 будет значительно улучшать терапевтические исходы при NMO.
Таким образом, ожидают, что ингибиторы LEA-1 и/или LEA-2 будут оказывать независимый благоприятный терапевтический эффект при лечении NMO. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп больных. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания связывается с MASP-1/3 или MASP-2 и блокирует их.
В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести NMO, включающему введение индивидууму, страдающему или имеющему риск развития NMO, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить местно в глаз, например, посредством промывания или нанесения композиции в форме местного геля, мази или капель или посредством интравитреального введения. Альтернативно, средство, ингибирующее MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Другой аспект относится к способу ингибирования LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести NMO, включающему введение индивидууму, страдающему или имеющему риск развития NMO, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1- и LEA-2-зависимой активации комплемента для лечения или снижения тяжести NMO, включающему введение индивидууму, страдающему NMO, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3.
В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, или профилактики или снижения тяжести NMO по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула оптимально может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить местно в глаз, например, посредством промывания или нанесения композиции в форме местного геля, мази или капель или посредством интравитреальной инъекции. Альтернативно, средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести NMO у нуждающегося в этом индивидуума. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XVI. РОЛЬ MASP-2 И MASP-3 В БОЛЕЗНИ БЕХЧЕТА И ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ С ИСПОЛЬЗОВАНИЕМ СРЕДСТВ, ИНГИБИРУЮЩИХ MASP-2 И MASP-3
Болезнь Бехчета является редким иммуноопосредованным системным васкулитом мелких сосудов, часто начинающимся с язв на слизистых оболочках и проблем со зрением. Болезнь Бехчета (BD) названа в 1937 году именем турецкого дерматолога Хулуси Бехчета, впервые описавшего тройной симптомокомплекс симптом рецидивирующих язв полости рта, генитальных язв и увеита. BD является системным рецидивирующим воспалительным нарушением неизвестной этиологии. Воспалительный периваскулит при BD может затрагивать желудочно-кишечный тракт, дыхательную, скелетно-мышечную, сердечно-сосудистую и нервную системы. BD может являться смертельным по причине разрывов аневризм сосудов или тяжелых неврологических осложнений. Оптическая невропатия и атрофия могут являться результатом васкулита и окклюзии сосудов, питающих зрительный нерв. См. Al-Araji A, et al., Lancet Neurol, 8(2): 192-204, 2009.
Наибольшая заболеваемость BD приходится на Ближнем и Среднем Востоке и Дальнем Востоке, но она является редкой в Европе и Северной Америке. BD часто исходно контролируют с использованием кортикостероидов и иммуносупрессоров, но многие случаи являются рефрактерными с серьезными клиническими проявлениями и смертностью. Биологические средства, включая интерферон-альфа, IVIG, средства против TNF, против IL-6 и против CD20, в некоторых случаях показали благоприятный эффект, но до сих пор не существует консенсуса по вопросу лучшего лечения.
Хотя BD, очевидно, является воспалительным нарушением, его патология не ясна. Наблюдают генетическую ассоциацию с антигенами HLA, и в полногеномных исследованиях ассоциации определяли участие генов множества цитокинов (Kirino et al, Nat Genet, 45(2):202-7, 2013). По-видимому, гиперактивность иммунной системы регулируется системой комплемента. В сыворотках пациентов с BD обнаруживают повышенные уровни C3 (Bardak and Aridogan, Ocul Immunol Inflamm 12(1):53-8, 2004), и повышение C3 и C4 в цереброспинальной жидкости коррелирует с заболеванием (Jongen et al, Arch Neurol, 49(10): 1075-8, 1992).
Tüzün and colleagues (2013) исследовали продукты классического и альтернативного путей в сыворотках пациентов с BD (Tüzün E, et al, J Neuroimmunol, 233(1-2):211-5, 2011). C4d, продукт расщепления C4, образуется ниже альтернативного пути в каскаде комплемента, и его измеряли для оценки исходной активности классического пути. C4d был повышен в сыворотках пациентов с BD по сравнению с контролями (повышение в 2,18 раза). Фактор Bb является продуктом расщепления фактора B, и его измеряли для определения активности альтернативного пути. У пациентов с BD наблюдали повышение фактора Bb по сравнению с нормальными контрольными индивидуумами (повышение в 2,19 раза), что соответствует повышению функционирования альтернативного пути при BD. Поскольку альтернативный путь комплемента служит для усиления общей активности комплемента, ожидают, что его активация будет повышать общую активацию комплемента. Harboe and colleagues (2004) показали, что селективная блокада альтернативного пути ингибировала образование более 80% мембраноатакующих комплексов, индуцируемое классическим путем (Harboe M, et al., Clin Exp Immunol, 138(3):439-46, 2004). Фактически, у пациентов BD был значимо повышен sC5b-9, конечный продукт каскада комплемента (повышение в 5,46 раза). Специфичные ингибиторы MASP-3 должны оказывать благоприятный эффект при BD. Блокирование MASP-3 должно ингибировать активацию фактора B и фактора D. Это будет останавливать амплификацию альтернативного пути, приводя к снижению общей активности комплемента. Таким образом, ингибирование MASP-3 должно значительно улучшать терапевтические исходы при BD. Таким образом, ожидают, что ингибиторы LEA-1 и/или LEA-2 будут оказывать независимый благоприятный терапевтический эффект при лечении BD. Кроме того, с помощью ингибиторов LEA-1 и LEA-2, используемых совместно, можно достигать дополнительного благоприятного терапевтического эффекта по сравнению с любым из средств в отдельности или можно обеспечивать эффективное лечение более широкого спектра подгрупп больных. Комбинированное ингибирование LEA-1 и LEA-2 можно осуществлять посредством совместного введения средства, блокирующего LEA-1, и средства, блокирующего LEA-2. Оптимально, функцию ингибирования LEA-1 и LEA-2 можно осуществлять в одной молекуле, такой как биспецифическое антитело, содержащее MASP-1/3- и MASP-2-специфичный участок связывания, или антитело с двойной специфичностью, где каждый участок связывания связывается с MASP-1/3 или MASP-2 и блокирует их. В соответствии с изложенным выше, один из аспектов изобретения, таким образом, относится к способу ингибирования LEA-1-зависимой активации комплемента для лечения, профилактики и снижения тяжести BD, включающему введение индивидууму, страдающему или имеющему риск развития BD, композиции, содержащей терапевтически эффективное количество средства, ингибирующего LEA-1, содержащего средство, ингибирующее MASP-1, средство, ингибирующее MASP-3, или комбинацию средств, ингибирующих MASP-1/3, в фармацевтическом носителе. Композицию, ингибирующую MASP-1, MASP-3 или MASP-1/3, можно вводить местно в глаз, например, посредством промывания или нанесения композиции в форме местного геля, мази или капель или посредством интравитреального введения. Альтернативно, средство, ингибирующее MASP-1, MASP-3 или MASP-1/3, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым. Другой аспект относится к способу ингибирования LEA-2-зависимой активации комплемента для лечения, профилактики и снижения тяжести BD, включающему введение индивидууму, страдающему или имеющему риск развития BD, терапевтически эффективного количества средства, ингибирующего MASP-2. Другой аспект относится к способу, включающему ингибирование LEA-1- и LEA-2-зависимой активации комплемента для лечения или снижения тяжести BD, включающему введение индивидууму, страдающему BD, терапевтически эффективного количества средства, ингибирующего MASP-2, и средства, ингибирующего MASP-1, MASP-3 или MASP-1/3.
В некоторых вариантах осуществления способ включает ингибирование LEA-1-зависимой активации комплемента и LEA-2-зависимой активации комплемента. Как подробно описано выше, ожидают, что использование комбинации фармакологических средств, по-отдельности блокирующих LEA-1 и LEA-2, будет обеспечивать улучшенный терапевтический исход лечения, или профилактики или снижения тяжести BD по сравнению с ингибированием LEA-1 в отдельности. Этого исхода можно достигать, например, посредством совместного введения антитела, имеющего LEA-1-блокирующую активность, вместе с антителом, имеющим LEA-2-блокирующую активность. В некоторых вариантах осуществления LEA-1- и LEA-2-блокирующие активности комбинируют в одной молекуле, и такая молекула имеет комбинированную LEA-1- и LEA-2-блокирующую активность. Такая молекула может содержать или состоять из биспецифического антитела, где один антигенсвязывающий участок специфически распознает MASP-1 и блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Альтернативно, такая молекула может состоять из биспецифического моноклонального антитела, где один антигенсвязывающий участок специфически распознает MASP-3 и, таким образом, блокирует LEA-1, а второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2. Такая молекула, оптимально, может состоять из биспецифического моноклонального антитела, где один комбинированный антигенсвязывающий участок специфически распознает MASP-1 и MASP-3 и, таким образом, блокирует LEA-1, в то время как второй антигенсвязывающий участок специфически распознает MASP-2 и блокирует LEA-2.
Средство, ингибирующее MASP-2, можно вводить местно в глаз, например, посредством промывания или нанесения композиции в форме местного геля, мази или капель или посредством интравитреальной инъекции. Альтернативно, средство, ингибирующее MASP-2, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, ингаляционного, назального, подкожного или другого парентерального введения или, потенциально, посредством перорального введения в случае непептидергических средств. Введение можно повторять по решению лечащего врача до тех пор, пока состояние не разрешиться или не станет контролируемым.
Введение композиций, ингибирующих MASP-3, и/или композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять посредством однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и/или MASP-3, или биспецифические или двойные ингибирующие средства, или посредством совместного введения отдельных композиций) или ограниченной последовательности введений для лечения, профилактики или снижения тяжести BD у нуждающегося в этом индивидуума. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, два раза в неделю, еженедельно, через неделю, ежемесячно или два раза в месяц в течение длительного периода времени для лечения нуждающегося в этом индивидуума.
XVII. СРЕДСТВА, ИНГИБИРУЮЩИЕ MASP
Учитывая то, что лектиновый путь комплемента состоит из двух основных ветвей активации комплемента, LEA-1 и LEA-2, и что также существует лектин-независимая ветвь активации комплемента, приходит понимание того, что крайне желательным будет специфическое ингибирование одной или нескольких из этих эффекторных ветвей, вызывающих патологию, ассоциированную по меньшей мере с одним из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета без полного выключения иммунологических защитных способностей комплемента (т.е. оставляя классический путь интактным). Это будет оставлять C1q-зависимую систему активации комплемента интактной для осуществления процессинга иммунных комплексов и для участия в защите хозяина против инфекции.
i. Композиции для ингибирования опосредованной LEA-1 активации комплемента
Как представлено в настоящем описании, авторы настоящего изобретения неожиданно обнаружили, что активация LEA-1, приводящая к лизису, является MASP-3-зависимой. Как дополнительно представлено в настоящем описании, в физиологических условиях MASP-3-зависимая активация LEA-1 также участвует в опсонизации, таким образом, обеспечивая аддитивный эффект по отношению к опосредованной LEA-2 активации комплемента. Как показано в примере 7, в присутствие Ca++ фактор D не является необходимым, т.к. MASP-3 может запускать активацию LEA-1 в сыворотках с фактором D-/-. MASP-3, MASP-1 и HTRA-1 способны конвертировать про-фактор D в активный фактор D. Аналогично, активация MASP-3, по-видимому, во многих случаях зависит от MASP-1, т.к. MASP-3 (в отличие от MASP-1 и MASP-2) не является аутоактивирующимся ферментом и неспособна конвертироваться в свою активную форму без помощи MASP-1 (Zundel, S. et al., J. Immunol. 172: 4342-4350 (2004); Megyeri et al, J. Biol. Chem. 288:8922-8934 (2013). Поскольку MASP-3 не аутоактивируется, и во многих случаях необходима активность MASP-1 для ее конвертации в ферментативно активную форму, опосредованную MASP-3 активацию конвертазы C3 альтернативного пути C3Bb можно ингибировать, воздействуя на зимоген MASP-3, или уже активированную MASP-3 или на опосредованную MASP-1 активацию MASP-3, или и то, и другое, т.к. во многих случаях в отсутствие функциональной активности MASP-1 MASP-3 остается в форме своего зимогена и неспособна запускать LEA-1 через прямое образование конвертазы C3 альтернативного пути (C3bBb).
Таким образом, в одном аспектов изобретения предпочтительным белковым компонентом в качестве объекта для разработки терапевтических средств для специфического ингибирования LEA-1 является ингибитор MASP-3 (включая ингибиторы опосредованной MASP-1 активации MASP-3 (например, ингибитор MASP-1, ингибирующий активацию MASP-3)).
В соответствии с изложенным выше, в одном из аспектов изобретение относится к способам ингибирования неблагоприятных воздействий LEA-1 (т.е. гемолиза и опсонизации) у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, включающим введение индивидууму фармацевтической композиции, содержащей количество средства, ингибирующего MASP-3, эффективное для ингибирования MASP-3-зависимой активации комплемента, и фармацевтически приемлемый носитель.
Средства, ингибирующие MASP-3, вводят в количестве, эффективном для ингибирования MASP-3-зависимой активации комплемента у живого индивидуума, страдающего или имеющего риск развития пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета. В практическом осуществлении этого аспекта изобретения типичные средства, ингибирующие MASP-3, включают: молекулы, ингибирующие биологическую активность MASP-3, включая молекулы, ингибирующие по меньшей мере одно или несколько из следующего: лектиновую MASP-3-зависимую активацию фактора B, лектиновую MASP-3-зависимую активацию про-фактора D, MASP-3-зависимую лектин-независимую активацию фактора B и MASP-3-зависимую лектин-независимую активацию про-фактора D (такие как низкомолекулярные ингибиторы, антитела против MASP-3 и их фрагменты или блокирующие пептиды, взаимодействующие с MASP-3 или мешающие белок-белковому взаимодействию), и молекулы, снижающие экспрессию MASP-3 (такие как антисенс-молекулы нуклеиновой кислоты против MASP-3, специфические молекулы РНКи против MASP-3 и рибозимы MASP-3). Средство, ингибирующее MASP-3, может эффективно блокировать белок-белковые взаимодействия MASP-3, мешать димеризации или сборке MASP-3, блокировать связывание Ca++, противодействовать активному центру сериновой протеазы MASP-3 или снижать экспрессию белка MASP-3, таким образом, предотвращать активацию MASP-3 опосредованной LEA-1 или лектин-независимой активации комплемента. Средства, ингибирующие MASP-3, можно использовать в отдельности в качестве основной терапии или в комбинации с другими терапевтическими средствами в качестве вспомогательной терапии для повышения благоприятных терапевтических эффектов других способов лечения, как дополнительно представлено в настоящем описании.
В одном из вариантов осуществления средство, ингибирующее MASP-3, специфически связывается с частью MASP-3 (SEQ ID NO: 8) с аффинностью связывания, по меньшей мере в 10 раз выше, чем с другими компонентами системы комплемента. В другом варианте осуществления средство, ингибирующее MASP-3, специфически связывается с частью MASP-3 (SEQ ID NO: 8) с аффинностью связывания, по меньшей мере в 100 раз выше, чем с другими компонентами системы комплемента. В одном из вариантов осуществления средство, ингибирующее MASP-3, специфически связывается с доменом сериновой протеазы MASP-3 (а/к 450-711 в SEQ ID NO: 8) и ингибирует MASP-3-зависимую активацию комплемента при условии, что ингибирующее средство не связывается с доменом сериновой протеазы MASP-1 (SEQ ID NO: 10) и не связывается с доменом сериновой протеазы MASP-2 (SEQ ID NO: 5). В одном из вариантов осуществления средство, ингибирующее MASP-3, является моноклональным антителом против MASP-3 или его фрагментом, специфически связывающимся с MASP-3.
В другом варианте осуществления средство, ингибирующее MASP-3, специфически связывается с частью MASP-1 (SEQ ID NO: 10) с аффинностью связывания, по меньшей мере в 10 раз выше, чем с другими компонентами системы комплемента, и ингибирует опосредованную MASP-1 активацию MASP-3. В другом варианте осуществления средство, ингибирующее MASP-3, специфически связывается с частью MASP-1 (SEQ ID NO: 10) с аффинностью связывания, по меньшей мере в 100 раз выше, чем с другими компонентами (т.е. полипептидами или их фрагментами) системы комплемента, и ингибирует опосредованную MASP-1 активацию MASP-3. В некоторых вариантах осуществления средство, ингибирующее MASP-3, специфически связывается с доменом сериновой протеазы MASP-1 (а/к 449-694 в SEQ ID NO: 10) и ингибирует опосредованную MASP-1 активацию MASP-3 при условии, что ингибирующее средство не связывается с доменом сериновой протеазы MASP-2 (SEQ ID NO: 5) и не связывается с доменом сериновой протеазы MASP-3 (SEQ ID NO: 8). В одном из вариантов осуществления средством, ингибирующим MASP-3, является моноклональное антитело против MASP-1 или его фрагмент, специфически связывающиеся с MASP-1 и ингибирующие опосредованную MASP-1 активацию MASP-3. В некоторых вариантах осуществления средство, ингибирующее MASP-3, связывающееся с MASP-1, ингибирует опосредованную MASP-1 активацию MASP-3 и дополнительно ингибирует опосредованное MASP-1 созревание фактора D.
В другом варианте осуществления средство, ингибирующее MASP-3, связывается с частью MASP-3 (SEQ ID NO:8), а также связывается с частью MASP-1 (SEQ ID NO: 10) при условии, что ингибирующее средство не связывается с MASP-2 (SEQ ID NO: 5) или MAp19 (SEQ ID NO: 3). В одном из вариантов осуществления средство, ингибирующее MASP-3, связывается с частью MASP-3 (SEQ ID ON:8), а также связывается с частью MASP-1 (SEQ ID NO: 10) при условии, что ингибирующее средство не связывается с MASP-2 (SEQ ID NO: 5) или MAp19 (SEQ ID NO: 3). В одном из вариантов осуществления средство, ингибирующее MASP-3, связывается с частью MASP-3 (SEQ ID NO:8), а также связывается с частью MASP-1 (SEQ ID NO: 10) при условии, что ингибирующее средство не связывается с MASP-2 (SEQ ID NO: 5), MAp19 (SEQ ID NO: 3) или MAp44 (SEQ ID NO: 11), таким образом, делая возможной меньшую эффективную дозу для ингибирования MASP-3-зависимой активации комплемента по причине отсутствия связывания с MAp44, присутствующей в сыворотке человека в высокой концентрации.
В одном из вариантов осуществления средство, ингибирующее MASP-3, является двойным средством, ингибирующим MASP-1/MASP-3, связывающимся с эпитопом в аминокислотной области, являющейся консервативной для MASP-1 и MASP-3, такой как домен CUBI-CCP2 (а/к 25-432 в SEQ ID NO: 10), как показано на фигурах 3-5. В одном из вариантов осуществления средство, ингибирующее MASP-3, является двойным средством, ингибирующим MASP-1/MASP-3, связывающимся с эпитопом в аминокислотной области, являющейся консервативной для MASP-1 и MASP-3, при условии, что ингибирующее средство не связывается с MAp44, такой как домен CCP (а/к 367-432 в SEQ ID NO: 10). В другом варианте осуществления средство, ингибирующее MASP-3, является биспецифическим ингибирующим средством, таким как биспецифическое моноклональное антитело, специфически связывающееся с эпитопом белка MASP-3 (SEQ ID NO: 8) и эпитопом белка MASP-1 (SEQ ID NO: 10). В некоторых вариантах осуществления средство, ингибирующее MASP-3, является биспецифическим моноклональным антителом, связывающимся с доменом сериновой протеазы MASP-1 (а/к 449-694 в SEQ ID NO: 10), а также связывается с доменом сериновой протеазы MASP-3 (а/к 450-711 в SEQ ID NO: 8).
Аффинность связывания средств, ингибирующих MASP-3, можно определять с использованием подходящего анализа связывания.
Ингибирование MASP-3-зависимой активации комплемента отличается по меньшей мере одним из следующих изменений компонентов системы комплемента, происходящих в результате введения средства, ингибирующего MASP-3, в соответствии со способами по изобретению: ингибирования опосредованной LEA-1 активации комплемента (ингибирования гемолиза и/или опсонизации); ингибирования лектин-независимой конвертации фактора B; ингибирования лектин-независимой конвертации фактора D, ингибирования субстрат-специфичного расщепления сериновой протеазой MASP-3, снижения гемолиза (измеряемого, например, как описано в примере 5) или снижения расщепления C3 и накопления C3b (измеряемого, например, как описано в примере 4 и примере 11).
В некоторых вариантах осуществления средства, ингибирующие MASP-3, селективно ингибируют MASP-3-зависимую активацию комплемента (т.е. опосредованную LEA-1 активацию комплемента, и/или лектин-независимую конвертацию фактора B, и/или лектин-независимую конвертацию фактора D), оставляя C1q-зависимую систему активации комплемента функционально интактной.
В некоторых вариантах осуществления средствами, ингибирующими MASP-3, являются антитела или их фрагменты, включая антитела против MASP-3 и их MASP-3-связывающие фрагменты, антитела против MASP-1 и их фрагменты, природные и синтетические пептиды или низкомолекулярные соединения. В некоторых вариантах осуществления средствами, ингибирующими MASP-3, являются низкомолекулярные ингибиторы протеаз, являющиеся селективными для MASP-1, или селективными для MASP-3, или селективными для MASP-1 и MASP-3.
ii. Композиции для ингибирования активации LEA-2
Как представлено в настоящем описании, опосредованная LEA-2 активация комплемента является MASP-2-зависимой, приводя к опсонизации и/или лизису. Таким образом, предпочтительным белковым компонентом для разработки терапевтических средств для специфического ингибирования LEA-2 лектин-зависимой системы комплемента является MASP-2. Показано, что некоторые белки связываются или взаимодействуют с MASP-2 посредством белок-белковых взаимодействий. Например, известно, что MASP-2 связывается и образует кальций-зависимые комплексы с лектиновыми белками MBL, H-фиколином и L-фиколином и коллектином-11. Ma Y., et al., J Innate Immun. Epub Dec 4 (2012). Показано, что каждый комплекс MASP-2/лектин активирует комплемент через MASP-2-зависимое расщепление белков C4 и C2 (Ikeda, K., et al, J. Biol. Chem. 2(52:7451-7454, (1987); Matsushita, M., et al, J. Exp. Med. 776: 1497-2284, (2000); Matsushita, M., et al, J. Immunol. 765:3502-3506, (2002)). Исследования показали, что домены CUB1-EGF MASP-2 важны для связывания MASP-2 с MBL (Thielens, N.M., et al, J. Immunol. 7(5(5:5068, (2001)). Также показано, что домены CUBI-EGF-CUBII опосредуют димеризацию MASP-2, необходимую для образования активного комплекса MBL (Wallis, R., et al., J. Biol. Chem. 275:30962-30969, 2000). Таким образом, можно идентифицировать средства, ингибирующие MASP-2, связывающиеся или противодействующие целевым областям MASP-2, о которых известно, что они важны для MASP-2-зависимой активации комплемента.
В соответствие с изложенным выше, в одном из аспектов изобретение относится к способам ингибирования неблагоприятных воздействий опосредованной LEA-2 активации комплемента у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, включающим введение индивидууму фармацевтической композиции, содержащей количество средства, ингибирующего MASP-2, эффективное для ингибирования MASP-2-зависимой активации комплемента, и фармацевтически приемлемый носитель.
В некоторых вариантах осуществления изобретение относится к способам ингибирования неблагоприятных воздействий LEA-2-опосредованной активации комплемента у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, включающим введение индивидууму фармацевтической композиции, содержащей количество средства, ингибирующего MASP-2, эффективное для ингибирования MASP-2-зависимой активации комплемента, и фармацевтически приемлемый носитель. Средства, ингибирующие MASP-2, вводят в количестве, эффективном для ингибирования MASP-2-зависимого LEA-2 у живого индивидуума, страдающего или имеющего риск развития PNH, возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета. В практическом осуществлении этого аспекта изобретения типичные средства, ингибирующие MASP-2, включают: молекулы, ингибирующие биологическую активность MASP-2 (такие низкомолекулярные ингибиторы, антитела против MASP-2 или блокирующие пептиды, взаимодействующие с MASP-2 или мешающие белок-белковому взаимодействию), и молекулы, снижающие экспрессию MASP-2 (такие как антисенс-молекулы нуклеиновой кислоты против MASP-2, специфичные молекулы РНКи против MASP-2 и рибозимы MASP-2), таким образом, предотвращающие активацию LEA-2 MASP-2.
Средство, ингибирующее MASP-2, может эффективно блокировать белок-белковые взаимодействия MASP-2, мешать димеризации или сборке MASP-2, блокировать связывание Ca++, противодействовать активному центру сериновой протеазы MASP-2 или может снижать экспрессию белка MASP-2, таким образом, предотвращая активацию LEA-2 MASP-2. Средства, ингибирующие MASP-2, можно использовать в отдельности в качестве основной терапии или в комбинации с другими терапевтическими средствами в качестве вспомогательной терапии для усиления благоприятных терапевтических эффектов других способов лечения, как дополнительно представлено в настоящем описании.
В одном из вариантов осуществления средство, ингибирующее MASP-2, специфически связывается с частью MASP-2 (SEQ ID NO: 5) с аффинностью связывания, по меньшей мере в 10 раз выше, чем с другими антигенами системы комплемента. В другом варианте осуществления средство, ингибирующее MASP-2, специфически связывается с частью MASP-2 (SEQ ID NO: 5) с аффинностью связывания по меньшей мере в 100 раз выше, чем с другими антигенами системы комплемента. В одном из вариантов осуществления средство, ингибирующее MASP-2, специфически связывается с по меньшей мере одним из (i) домена CCP1-CCP2 (а/к 300-431 в SEQ ID NO: 5) или домена сериновой протеазы MASP-2 (а/к 445-682 в SEQ ID NO: 5) и ингибирует MASP-2-зависимую активацию комплемента при условии, что ингибирующее средство не связывается с доменом сериновой протеазы MASP-1 (SEQ ID NO: 10) и не связывается с доменом сериновой протеазы MASP-3 (SEQ ID NO: 8). В одном из вариантов осуществления средством, ингибирующим MASP-2, является моноклональное антитело против MASP-2 или его фрагмент, специфически связывающиеся с MASP-2.
Аффинность связывания средства, ингибирующего MASP-2, можно определять с использованием подходящего анализа связывания.
Ингибирование MASP-2-зависимой активации комплемента отличается по меньшей мере одним из следующих изменений компонентов системы комплемента, происходящих в результате введения средства, ингибирующего MASP-2, в соответствии со способами по изобретению: ингибирования образования или продукции продуктов MASP-2-зависимой системы активации комплемента C4b, C3a, C5a и/или C5b-9 (MAC) (измеряемого, например, как описано в примере 2 патента США № 7919094), снижения расщепления C4 и накопления C4b (измеряемого, например, как описано в примере 8 или примере 9) или снижения расщепления C3 и накопления C3b (измеряемого, например, как описано в примере 11).
В некоторых вариантах осуществления средства, ингибирующие MASP-2, селективно ингибируют активацию комплемента MASP-2 (т.е. LEA-2), оставляя C1q-зависимую систему активации комплемента функционально интактной.
В некоторых вариантах осуществления средствами, ингибирующими MASP-2, являются антитела или их фрагменты, включая антитела против MASP-2 и их MASP-2-связывающие фрагменты, природные и синтетические пептиды или низкомолекулярные соединения. В некоторых вариантах осуществления средствами, ингибирующими MASP-2, являются низкомолекулярные ингибиторы протеаз, селективные для MASP-2.
iii. Композиции для ингибирования опосредованной LEA-1 активации комплемента и опосредованной LEA-2 активации комплемента
В другом аспекте изобретение относится к способам ингибирования неблагоприятных воздействий LEA-1 и ингибирования неблагоприятных воздействий LEA-2 у индивидуума, страдающего или имеющего риск развития заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, включающим введение индивидууму композиции, содержащей количество по меньшей мере одного из средства, ингибирующего MASP-1, и/или средства, ингибирующего MASP-3, эффективное для ингибирования MASP-3-зависимой активации комплемента.
В одном из вариантов осуществления композиция содержит средство, ингибирующее MASP-1. В одном из вариантов осуществления средство, ингибирующее MASP-1, ингибирует опосредованную MASP-3 активацию комплемента, а также ингибирует опосредованную MASP-2 активацию комплемента.
В одном из вариантов осуществления композиция содержит средство, ингибирующее MASP-3. В одном из вариантов осуществления средство, ингибирующее MASP-3, ингибирует по меньшей мере одно из: лектиновой MASP-3-зависимой активации фактора B; лектиновой MASP-3-зависимой активации фактора D; MASP-3-зависимой лектин-независимой активации фактора B и/или MASP-3-зависимой лектин-независимой активации фактора D.
В одном из вариантов осуществления композиция содержит средство, ингибирующее MASP-1, и средство, ингибирующее MASP-3.
В некоторых вариантах осуществления способ дополнительно включает введение индивидууму композиции, содержащей средство, ингибирующее MASP-2.
В другом варианте осуществления этот аспект изобретения включает введение индивидууму, страдающему PNH, фармацевтической композиции, содержащей количество средства, ингибирующего MASP-2, эффективное для ингибирования MASP-2-зависимой активации комплемента, и количество средства, ингибирующего MASP-3, эффективное для ингибирования MASP-3-зависимой активации комплемента, и фармацевтически приемлемый носитель.
В некоторых вариантах осуществления композиция содержит отдельное средство, ингибирующее и LEA-1, и LEA-2 (т.е. двойное средство, ингибирующее MASP-2/MASP-3, двойное средство, ингибирующее MASP-1/MASP-2, биспецифическое средство, ингибирующее MASP-2/MASP-3, биспецифическое средство, ингибирующее MASP-1/MASP-2, или панспецифическое средство, ингибирующее MASP-1/2/3, или триспецифическое средство, ингибирующее MASP-1/2/3). В некоторых вариантах осуществления композиция содержит комбинацию средств, ингибирующих LEA-1 и LEA-2, например, комбинацию двойного ингибирующего средства и отдельного ингибирующего средства, комбинацию биспецифических ингибирующих средств и отдельного ингибирующего средства или комбинацию любых из средств, ингибирующих MASP-1, MASP-2 и/или MASP-3, как представлено в настоящем описании, которые в комбинации ингибируют и LEA-1, и LEA-2, как дополнительно представлено в настоящем описании.
В одном из вариантов осуществления изобретение относится к фармацевтической композиции для ингибирования и LEA-1, и LEA-2, содержащей по меньшей мере одно средство, ингибирующее MASP-3, и по меньшей мере одно средство, ингибирующее MASP-2, и фармацевтически приемлемый носитель. В одном из вариантов осуществления фармацевтическая композиция содержит комбинацию первой молекулы, являющейся средством, ингибирующим MASP-3, и второй молекулы, являющейся средством, ингибирующим MASP-2. В другом варианте осуществления фармацевтическая композиция содержит одно вещество, имеющее активность в качестве средства, ингибирующего MASP-3, и активность в качестве средства, ингибирующего MASP-2 (т.е. ингибирующее средство, ингибирующее опосредованную MASP-2 активацию LEA-2 и опосредованную MASP-3 активацию LEA-1). В одном из вариантов осуществления ингибирующим средством является двойное средство, ингибирующее MASP-2/MASP-3, связывающееся с эпитопом в аминокислотной области, являющейся консервативной для MASP-2 (SEQ ID NO: 5) и MASP-3 (SEQ ID NO: 8), такой как домен сериновой протеазы, например, N-концевая область бета-цепи (например, первые 150 а/к N-концевой области бета-цепи SEQ ID NO: 5 и SEQ ID NO: 8), как показано на фигурах 4, 6 и 7C. В одном из вариантов осуществления ингибирующим средством является биспецифическое ингибирующее средство, такое как биспецифическое моноклональное антитело, специфически связывающееся с эпитопом белка MASP-2 (SEQ ID NO: 5) и эпитопом белка MASP-3 (SEQ ID NO: 8). В некоторых вариантах осуществления ингибирующим средством является биспецифическое моноклональное антитело, связывающееся по меньшей мере с одним из домена CCP1-CCP2 MASP-2 (а/к 300-431 в SEQ ID NO: 5) или домена сериновой протеазы MASP-2 (а/к 445-682 в SEQ ID NO: 5), а также связывающееся с эпитопом домена сериновой протеазы MASP-3 (а/к 450-711 в SEQ ID NO: 8).
В другом варианте осуществления изобретение относится к композиции для ингибирования и LEA-1, и LEA-2, содержащей ингибирующее средство, ингибирующее опосредованную MASP-2 активацию LEA-2 и опосредованную MASP-1 активацию MASP-3, таким образом, ингибирующее опосредованную MASP-3 активацию LEA-1 (и, необязательно, также ингибирующее опосредованное MASP-1 созревание фактора D). В одном из вариантов осуществления ингибирующим средством является двойное средство, ингибирующее MASP-1/MASP-2, связывающееся с эпитопом в аминокислотной области, являющейся консервативной для MASP-1 (SEQ ID NO: 10) и MASP-2 (SEQ ID NO: 5), такой как домен сериновой протеазы, как показано на фигурах 4, 6 и 7A. В одном из вариантов осуществления ингибирующим средством является биспецифическое ингибирующее средство, такое как биспецифическое моноклональное антитело, специфически связывающееся с эпитопом белка MASP-1 (SEQ ID NO: 10) и эпитопом белка MASP-2 (SEQ ID NO: 5). В некоторых вариантах осуществления ингибирующим средством является биспецифическое моноклональное антитело, связывающееся с доменом сериновой протеазы MASP-1 (а/к 449-694 в SEQ ID NO: 10), а также связывающееся с по меньшей мере одним из домена CCP1-CCP2 MASP-2 (а/к 300-431 в SEQ ID NO: 5) или домена сериновой протеазы MASP-2 (а/к 445-682 в SEQ ID NO: 5).
В другом варианте осуществления изобретение относится к композиции для ингибирования и LEA-1, и LEA-2, содержащей ингибирующее средство, ингибирующее опосредованную MASP-2 активацию LEA-2, опосредованную MASP-3 активацию LEA-1 посредством прямого связывания с MASP-3, а также ингибирующее опосредованную MASP-1 активацию MASP-3, таким образом, ингибирующее опосредованную MASP-3 активацию LEA-1 (и, необязательно, также ингибирующее опосредованное MASP-1 созревание фактора D). В одном из вариантов осуществления ингибирующим средством является панспецифический ингибитор MASP, связывающийся с аминокислотной областью, являющейся консервативной для MASP-1 (SEQ ID NO: 10), MASP-2 (SEQ ID NO: 5) и MASP-3 (SEQ ID NO: 8), например, консервативной областью домена CUBI-EGF-CUB2, как показано на фигурах 4 и 5. Как показано на фигурах 4 и 5, в доменах CUBI-EGF-CUBII существует несколько участков идентичности, общих для MASP-1, MASP-2 и MASP-3, что, таким образом, позволяет получать панспецифические антитела против MASP. В некоторых вариантах осуществления панспецифическое антитело против MASP может связываться с эпитопом в домене CUB2 MASP-1 (а/к 185-296 в SEQ ID NO: 10), MASP-2 (а/к 184-295 в SEQ ID NO: 5) и MASP-3 (а/к 185-296 в SEQ ID NO: 8). Необходимо отметить, что панспецифический ингибитор MASP, связывающийся с CUBI-EGF MASP-1, MASP-2 и MASP-3, также будет связываться с MAp19 и MAp44, таким образом, эффективную терапевтическую дозу такого ингибитора будут доводить до более высокого уровня для компенсации этого связывания. Также необходимо отметить, что панспецифический ингибитор MASP, связывающийся с доменом CUBII MASP-1, MASP-2 и MASP-3, также будет связываться с MAp44, таким образом, эффективную терапевтическую дозу такого ингибитора будут доводить до более высокого уровня для компенсации этого связывания.
В одном из вариантов осуществления ингибирующим средством является триспецифический ингибитор MASP-1/2/3, связывающийся с эпитопом белка MASP-1 (SEQ ID NO: 10), эпитопом белка MASP-2 (SEQ ID NO: 5) и эпитопом белка MASP-3 (SEQ ID NO: 8). В некоторых вариантах осуществления ингибирующим средством является триспецифическое моноклональное антитело, связывающееся с доменом сериновой протеазы MASP-1 (а/к 449-694 в SEQ ID NO: 10), связывающееся по меньшей мере с одним из домена CCP1-CCP2 MASP-2 (а/к 300-431 в SEQ ID NO: 5) или домена сериновой протеазы MASP-2 (а/к 445-682 в SEQ ID NO: 5), а также связывающееся с эпитопом домена сериновой протеазы MASP-3 (а/к 450-711 в SEQ ID NO: 8).
Примеры ингибирующих средств для ингибирования LEA-1, LEA-2 или LEA-1 и LEA-2 описывают ниже в таблице 2.
Средства, ингибирующие MASP
В некоторых вариантах осуществления композиция содержит комбинацию средств, ингибирующих LEA-1 и LEA-2, например, комбинацию отдельных ингибирующих средств, как описано выше и представлено в таблице 2. Например, в одном из вариантов осуществления композиция содержит комбинацию антитела против MASP-1 и антитела против MASP-2. В одном из вариантов осуществления композиция содержит комбинацию антитела против MASP-1 и антитела против MASP-3. В одном из вариантов осуществления композиция содержит комбинацию антитела против MASP-2 и антитела против MASP-3. В одном из вариантов осуществления композиция содержит комбинацию антител против MASP-1, MASP-2 и MASP-3. В некоторых вариантах осуществления способы по изобретению включают введение отдельной композиции, содержащей комбинацию ингибирующих средств. В других вариантах осуществления способы по изобретению включают совместное введение отдельных композиций.
В некоторых вариантах осуществления композиции содержат комбинацию двойного ингибирующего средства и отдельного ингибирующего средства (т.е. двойного ингибитора MASP-2/3 и ингибитора MASP-1; двойного ингибитора MASP-1/3 и ингибитора MASP-2 или двойного ингибитора MASP-1/2 и ингибитора MASP-3). В других вариантах осуществления способы по изобретению включают совместное введение отдельных композиций, содержащих двойной ингибитор и отдельный ингибитор.
В некоторых вариантах осуществления композиции содержат комбинацию биспецифического ингибирующего средства и отдельного ингибирующего средства (т.е. биспецифического ингибитора MASP-2/3 и ингибитора MASP-1; биспецифического ингибитора MASP-1/3 и ингибитора MASP-2 или биспецифического ингибитора MASP-1/2 и ингибитора MASP-3). В других вариантах осуществления способы по изобретению включают совместное введение отдельных композиций, содержащих биспецифический ингибитор и отдельный ингибитор.
Согласно различным вариантам осуществления изобретения, необходимо отметить, что средства, ингибирующие MASP-3, и/или средства, ингибирующие MASP-2, и/или средства, ингибирующие MASP-1, будут использовать для клиренса белка-мишени из плазмы по сравнению с антителом против C5, которое должно локализоваться в месте действия.
АНТИТЕЛА ПРОТИВ MASP
В некоторых вариантах осуществления этого аспекта изобретения средство, ингибирующее MASP, содержит антитело против MASP (например, антитело против MASP-1, MASP-2 или MASP-3), ингибирующее по меньшей мере один из путей активации комплемента LEA-1 и/или LEA-2. Антитела против MASP, применимые в этом аспекте изобретения, включают поликлональные, моноклональные или рекомбинантные антитела, полученные из любого млекопитающего, продуцирующего антитела, и оно может являться полиспецифическим (т.е. биспецифическим или триспецифическим), химерным, гуманизированным, полностью человеческим, антиидиотипическим и фрагментами антител. Фрагменты антител включают фрагменты Fab, Fab', F(ab)2, F(ab')2, Fv, scFv-фрагменты и одноцепочечные антитела, как дополнительно представлено в настоящем описании.
Антитела против MASP можно подвергать скринингу на способность ингибировать LEA-1 или LEA-2-зависимую систему активации комплемента с использованием анализов, представленных в настоящем описании. Некоторые антитела против MASP-1, MASP-2 и MASP-3 описывают в литературе, и некоторые получены недавно, некоторые из которых приведены ниже в таблице 3. Эти примеры антител против MASP можно подвергать скринингу на способность ингибировать LEA-1- и/или LEA-2-зависимую систему активации комплемента с использованием анализов, представленных в настоящем описании. Например, как описано в примерах 11-13 в настоящем описании, идентифицированы Fab2 антитела против MASP-2 крысы, блокирующие MASP-2-зависимую активацию комплемента. Как дополнительно описано в примере 14, идентифицированы полностью человеческие scFv-антитела против MASP-2, блокирующие MASP-2-зависимую активацию комплемента. Как дополнительно описано в примере 15, получены антитела против MASP-3. При идентификации антитела против MASP, функционирующего как ингибитор LEA-1 или LEA-2, его можно использовать в фармацевтической композиции, как представлено в настоящем описании, и его также можно использовать для получения биспецифических и триспецифических ингибирующих средств, приведенных в таблице 2 и дополнительно представленных в настоящем описании (см. например, пример 8).
СПЕЦИФИЧЕСКИЕ АНТИТЕЛА ПРОТИВ MASP-1, MASP-2 и MASP-3
MoAb мыши (N-конец)
NimoAb104, получаемое с помощью гибридомной линии клеток M0545YM035 (DSMZ)
NimoAb108, получаемое с помощью гибридомной линии клеток M0545YM029 (DSMZ)
NimoAb109, получаемое с помощью гибридомной линии клеток M0545YM046 (DSMZ)
NimoAb110, получаемое с помощью гибридомной линии клеток M0545YM048 (DSMZ)
MoAb 1E2 и 2B11, получаемые с помощью гибридомной линии клеток 1E2 и 2B11 (перекрестно не реагируют с MASP-2). Оба антитела распознают тяжелую цепь, общую для MASP-1 и MASP-3
MoAb 1E2: коммерчески доступно в Hycult Biotech, кат. № HM2092
MoAb 2B11: коммерчески доступно в Hycult Biotech, кат. № HM2093
MoAb-7D8; MoAb-7B7; MoAb-8B3 и MoAb-5H3 MoAb-7D8 и MoAb-5H3 являются MASP-3-специфичными, другие перекрестно реагируют с MASP-1
i. Антитела против MASP со сниженной эффекторной функцией
В некоторых вариантах осуществления этого аспекта изобретения антитела против MASP, представленные в настоящем описании, имеют сниженную эффекторную функцию для снижения воспаления, которое может возникать в результате активации классического пути комплемента. Показано, что способность молекул IgG запускать классический путь комплемента свойственна Fc-части молекулы (Duncan, A.R., et al, Nature 552:738-740 (1988)). Молекулы IgG, в которых удаляют Fc-часть молекулы с помощью ферментативного расщепления, лишены этой эффекторной функции (см. Harlow, Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1988). Таким образом, антитела со сниженной эффекторной функцией можно получать как антитела с отсутствием Fc-части молекулы, используя генетически модифицированную последовательность Fc, минимизирующую эффекторную функцию или имеющую изотип IgG2 или IgG4 человека.
Антитела со сниженной эффекторной функцией можно получать общепринятыми молекулярно-биологическими манипуляциями с Fc-частью тяжелых цепей IgG, как описано в Jolliffe et al, Int'l Rev. Immunol. 70:241-250, (1993) и Rodrigues et al, J. Immunol. 757:6954-6961, (1998). Антитела со сниженной эффекторной функцией также включают изотипы IgG2 и IgG4 человека, имеющие сниженную способность активировать комплемент и/или взаимодействовать с Fc-рецепторами (Ravetch, J.V., et al, Annu. Rev. Immunol.:457-492, (1991); Isaacs, J.D., et al, J. Immunol. 745:3062-3071, 1992; van de Winkel, J.G., et al, Immunol. Today 74:215-221, (1993)). Гуманизированные или полностью человеческие антитела, специфичные для MASP-1, MASP-2 или MASP-3 человека (включая антитела с двойной специфичностью, панспецифические, биспецифические или триспецифические антитела), состоящие из изотипов IgG2 или IgG4, можно получать одним из нескольких способов, известных специалисту в этой области, как описано в Vaughan, T.J., et al, Nature Biotechnical 7(5:535-539, (1998).
ii. Получение антител против MASP
Антитела против MASP-1, MASP-2 или MASP-3 можно получать с использованием полипептидов MASP-1, MASP-2 или MASP-3 (например, полноразмерных MASP-1, MASP-1 или MASP-3) или с использованием антигенных пептидов, несущих эпитопы MASP-1, 2 или 3 (например, часть полипептида MASP-2). Иммуногенные пептиды могут составлять всего лишь пять аминокислотных остатков в длину. Например, полипептид MASP-2, включающий полную аминокислотную последовательность SEQ ID NO: 5, можно использовать для получения антител против MASP-2, применимых в способе по изобретению. Конкретные домены MASP, которые, как известно, участвуют в белок-белковых взаимодействиях, такие как домены CUBI и CUBI-EGF, а также область, включающую активный центр сериновой протеазы, например, как приведено в таблице 2, можно экспрессировать в виде рекомбинантных полипептидов с использованием способов, хорошо известных в этой области, и использовать в качестве антигенов. Кроме того, пептиды, содержащие по меньшей мере часть 6 аминокислот полипептида MASP-1 (SEQ ID NO: 10), или полипептида MASP-2 (SEQ ID NO: 5) или полипептида MASP-3 (SEQ ID NO: 8), также применимы для получения антител против MASP-1, MASP-2 или MASP-3, соответственно. Пептиды и полипептиды MASP, используемые для получения антител, можно выделять в виде природных полипептидов, или рекомбинантных или синтетических пептидов и каталитически неактивных рекомбинантных полипептидов. Антигены, применимые для получения антител против MASP, также включают слитые полипептиды, такие как продукты слияния полипептида MASP или его части с иммуноглобулиновым полипептидом или мальтозо-связывающим белком. Полипептидный иммуноген может являться полноразмерной молекулой или ее частью. Если полипептидная часть является гаптено-подобной, такую часть предпочтительно можно соединять или связывать с макромолекулярным носителем (таким как гемоцианин морского блюдца (KLH), бычий сывороточный альбумин (BSA) или столбнячный токсин) для иммунизации.
iii. Поликлональные антитела
Поликлональные антитела против MASP-1, MASP-2 или MASP-3 можно получать, иммунизируя животное полипептидом MASP-1, MASP-2 или MASP-3 или его иммуногенной частью с использованием способов, хорошо известных специалистам в этой области. См., например, Green et al., "Production of Polyclonal Antisera," in Immunochemical Protocols (Manson, ed.). Иммуногенность полипептида MASP можно повышать с использованием адъюванта, включая минеральные гели, такие как гидроксид алюминия или адъювант Фрейнда (полный или неполный), поверхностно-активные вещества, такие как лизолецитин, полиолы-плюроники, полианионы, масляные эмульсии, KLH и динитрофенол. Поликлональные антитела, как правило, получают с использованием животных, таких как лошади, коровы, собаки, куры, крысы, мыши, кролики, морские свинки, козы или овцы. Альтернативно, антитело против MASP, применимое в настоящем изобретении, также можно получать из не относящихся к человеку приматов. Общие способы получения диагностически и терапевтически применимых антител у бабуинов можно найти, например, в Goldenberg et al., международной патентной публикации № WO 91/11465 и Losman, M.J., et al, Int. J. Cancer 46: 10, (1990). Затем из крови таких иммунизированных животных получают сыворотки, содержащие иммунологически активные антитела, с использованием общепринятых способов, хорошо известных в этой области.
iv. Моноклональные антитела
В некоторых вариантах осуществления средством, ингибирующим LEA-2, является моноклональное антитело против MASP-2, и/или средством, ингибирующим LEA-1, является моноклональное антитело против MASP-3 или моноклональное антитело против MASP-1. Как описано выше, в некоторых вариантах осуществления моноклональные антитела против MASP-1, MASP-2 и MASP-3 являются высокоспецифичными, направленными против одного эпитопа MASP-1, MASP-2 или MASP-3. Как применяют в настоящем описании, модификатор "моноклональное" указывает на свойство антитела, как получаемого по существу из гомогенной популяции антител, и не следует истолковывать его как требующий получения антитела любым конкретным способом. Моноклональные антитела можно получать с использованием любого способа, обеспечивающего получение молекул антител с помощью стабильных клеточных линий в культуре, такого как гибридомный способ, описываемый Kohler, G., et al, Nature 256:495, (1975), или их можно получать с помощью способов рекомбинантной ДНК (см., например, патент США № 4816567 Cabilly). Моноклональные антитела также можно выделять из фаговых библиотек антител с использованием способов, описываемых Clackson, T., et al, Nature 552:624-628, (1991), и Marks, J.D., et al, J. Mol. Biol. 222:581-597, (1991). Такие антитела могут представлять любой класс иммуноглобулинов, включая IgG, IgM, IgE, IgA, IgD, и любые их подклассы.
Например, моноклональные антитела можно получать, инъецируя подходящему млекопитающему (например, мыши BALB/c) композицию, содержащую полипептид MASP-1, полипептид MASP-2 или полипептид MASP-3, или его часть. После заранее определенного периода времени из мыши выделяют спленоциты и суспендируют их в среде для культивирования клеток. Затем спленоциты сливают с иммортализированной клеточной линией для образования гибридомы. Образованные гибридомы выращивают в культуре клеток и подвергают скринингу на их способность продуцировать моноклональное антитело против MASP-1, MASP-2 или MASP-3. (См. также Current Protocols in Immunology, Vol. 1., John Wiley & Sons, стр. 2.5.1-2.6.7, 1991.).
Моноклональные антитела человека можно получать с использованием трансгенных мышей, сконструированных для продукции специфичных антител человека в ответ на стимуляцию антигеном. В этом способе элементы локуса тяжелой и легкой цепи иммуноглобулина человека встраивают в линии мышей, полученных из линии эмбриональных стволовых клеток, содержащих направленные нарушения в эндогенных локусах тяжелой цепи и легкой цепи иммуноглобулина. Трансгенные мыши могут синтезировать антитела человека, специфичные для антигенов человека, таких как антигены MASP-2, представленные в настоящем описании, и можно использовать мышей для получения гибридом, секретирующих антитело против MASP-2 человека, посредством слияния B-клеток от таких животных с подходящими линиями миеломных клеток с использованием общепринятого способа Колера-Мильштейна. Способы получения антител человека из трансгенных мышей описывают, например, в Green, L.L., et al, Nature Genet. 7: 13, 1994; Lonberg, N., et al, Nature 368:856, 1994; и Taylor, L.D., et al, Int. Immun. 6:579, 1994.
Моноклональные антитела можно выделять и очищать из гибридомных культур множеством хорошо известных способов. Такие способы выделения включают аффинную хроматографию с протеином-A-сефарозой, эксклюзионную хроматографию и ионообменную хроматографию (см., например, Coligan, стр. 2,7,1-2,7,12 и стр. 2,9,1-2,9,3; Baines et al, "Purification of Immunoglobulin G (IgG)", в Methods in Molecular biology, The Humana Press, Inc., Vol. 10, pages 79-104, 1992).
При получении поликлональные антитела, моноклональные антитела или антитела, полученные с помощью фагов, сначала тестируют на специфическое связывание с MASP-1, MASP-2 или MASP-3 или, при желании, двойное связывание с MASP-1/3, MASP-2/3 или MASP-1/2. Способы определения того, связывается ли антитело с белковым антигеном, и/или определения аффинности антитела к белковому антигену известны в этой области. Например, связывание антитела с белковым антигеном можно определять и/или количественно анализировать с использованием множества способов, в качестве неограничивающих примеров, таких как, вестерн-блоттинг, дот-блот, способ поверхностного плазмонного резонанса (например, с использованием системы BIAcore; Pharmacia Biosensor AB, Uppsala, Sweden и Piscataway, NJ) или твердофазных иммуноферментных анализов (ELISA). См., например, See, e.g., Harlow and Lane (1988) "Antibodies: A Laboratory Manual" Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N. Y.; Benny K. C. Lo (2004) "Antibody Engineering: Methods and Protocols," Humana Press (ISBN: 1588290921); Borrebaek (1992) "Antibody Engineering, A Practical Guide," W.H. Freeman and Co., NY; Borrebaek (1995) "Antibody Engineering," 2nd Edition, Oxford University Press, NY, Oxford; Johne et al. (1993), Immunol. Meth. 160:191-198; Jonsson et al. (1993) Ann. Biol. Clin. 51: 19-26; and Jonsson et al. (1991) Biotechniques 11:620-627. See also, U.S. Patent No. 6,355,245. См. также патент США № 6355245.
Аффинность моноклональных антител против MASP легко может определять специалист в этой области (см., например, Scatchard, A., NY Acad. Sci. 57:660-672, 1949). В одном из вариантов осуществления моноклональные антитела против MASP-1, MASP-2 или MASP-3, применимые в способах по изобретению, связываются с MASP-1, MASP-2, или MASP-3 с аффинностью связывания <100 нМ, предпочтительно <10 нМ, и наиболее предпочтительно <2 нМ.
При идентификации антител, специфически связывающихся с MASP-1, MASP-2 или MASP-3, антитела против MASP-1, MASP-2 или MASP-3 тестируют на способность функционировать в качестве средства, ингибирующего LEA-1, или средства, ингибирующего LEA-2, в одном из нескольких функциональных анализов, например, как описано в таблице 2. Например, идентифицированные антитела, специфически связывающиеся с MASP-2, тестируют на способность функционировать в качестве средства, ингибирующего LEA-2, в одном из нескольких анализов, таких как, например, описано в таблице 2 (например, анализе лектин-специфического расщепления C4 (таком как анализ, описываемый в примере 8 или примере 9), или анализе накопления C3b (таком как анализ, описываемый в примере 4 или примере 11)). В качестве дополнительного примера, идентифицированные антитела, специфически связывающиеся с MASP-1 или MASP-3, тестируют на способность функционировать в качестве средства, ингибирующего LEA-1, в одном из нескольких анализов, таком как, например, описано в таблице 2 (например, снижение гемолиза, измеряемое, например, как описано в примере 5, или снижение расщепления C3 и накопления C3b, измеряемое, например, как описано в примере 4 и примере 11).
v. Химерные/гуманизированные антитела
Моноклональные антитела, применимые в способе по изобретению, включают химерные антитела, в которых часть тяжелой и/или легкой цепи является идентичной или гомологичной соответствующим последовательностям в антителах, полученных из конкретного вида или принадлежащих конкретному классу или подклассу антител, в то время как остальная часть цепи(-ей) является идентичной или гомологичной соответствующим последовательностям в антителах, полученных из другого вида или принадлежащих другому классу или подклассу антител, а также фрагментам таких антител (патент США № 4816567, до Cabilly; и Morrison, S.L., et al, Proc. Nat'l Acad. Sci. USA 57:6851-6855, (1984)).
Одной из форм химерного антитела, применимого в изобретении, является гуманизированное моноклональное антитело против MASP-1, MASP-2 или MASP-3. Гуманизированными формами не принадлежащих человеку антител (например, мыши) являются химерные антитела, содержащие минимальную последовательность, полученную из не принадлежащего человеку иммуноглобулина. Гуманизированные моноклональные антитела получают переносом не принадлежащих человеку определяющих комплементарность областей (CDR) (например, мыши) из вариабельных областей тяжелой и легкой цепей иммуноглобулина мыши в вариабельный домен человека. Как правило, затем остатками антител человека замещают каркасные области не принадлежащих человеку соответствующих элементов. Кроме того, гуманизированные антитела могут содержать остатки, необнаруживаемые в реципиентном антителе или донорном антителе. Эти модификации осуществляют для дополнительного улучшения свойств антитела. В основном, гуманизированное антитело будет содержать по существу все из по меньшей мере одного и, как правило, двух вариабельных доменов, в которых все или по существу все из гипервариабельных петель соответствуют таковым в не принадлежащем человеку иммуноглобулине, и все или по существу все из каркасных областей Fv имеют последовательность иммуноглобулина человека. Необязательно, гуманизированное антитело также будет содержать по меньшей мере часть константной области иммуноглобулина (Fc), как правило, иммуноглобулина человека. Более подробно см. Jones, P.T., et al, Nature 321:522-525, (1986); Reichmann, L., et al, Nature 552:323-329, (1988); и Presta, Curr. Op. Struct. Biol. 2:593-596, (1992).
Гуманизированные антитела, применимые в изобретении, включают моноклональные антитела человека, включающие по меньшей мере область CDR3, связывающуюся с MASP-1, MASP-2 или MASP-3. Кроме того, Fc-части можно замещать так, чтобы получать антитела IgA или IgM, а также антитела IgG человека. Такие гуманизированные антитела будут иметь конкретную клиническую применимость, т.к. они будут специфически распознавать MASP-1, MASP-2 или MASP-3 человека, но не будут вызывать иммунный ответ у людей на само антитело. Таким образом, они больше подходят для введения людям in vivo, особенно при необходимости повторного или длительного введения.
Способы получения гуманизированных моноклональных антител также описывают, например, в Jones, P.T., et al., Nature 321:522, (1986); Carter, P., et al., Proc. Nat'l. Acad. Sci. USA 89:4285, (1992); Sandhu, J.S., Crit. Rev. Biotech. 12:437, (1992); Singer, I.I., et al., J. Immun. 150:2844, (1993); Sudhir (ed.), Antibody Engineering Protocols, Humana Press, Inc., (1995); Kelley, "Engineering Therapeutic Antibodies," in Protein Engineering: Principles and Practice, Cleland et al. (eds.), John Wiley & Sons, Inc., p. 399-434, (1996); и патент США № 5,693,762, Queen, 1997. Кроме того, существуют коммерческие организации, которые будут синтезировать гуманизированные антитела из конкретных областей антител мыши, такие как Protein Design Labs (Mountain View, CA).
vi. Рекомбинантные антитела
Антитела против MASP-1, MASP-2 или MASP-3 также можно получать с использованием рекомбинантных способов. Например, антитела человека можно получать с использованием библиотек, экспрессирующих иммуноглобулины человека (поставляемых, например, Stratagene, Corp., La Jolla, CA) для получения фрагментов антител человека (VH, VL, FV, фактор D, Fab или F(ab')2). Затем эти фрагменты используют для конструирования целых антител человека с использованием способов, аналогичных способам получения химерных антител.
vii. Антиидиотипические антитела
После идентификации антител против MASP-1, MASP-2 или MASP-3 с желательной ингибиторной активностью эти антитела можно использовать для получения антиидиотипических антител, сходных с частью MASP-1, MASP-2 или MASP-3, с использованием способов хорошо известных в этой области. См., например, Greenspan, N.S., et al, FASEB J. 7:437, (1993). Например, антитела, связывающиеся с MASP-2 и конкурентно ингибирующие взаимодействие белка MASP-2, необходимое для активации комплемента, можно использовать для получения антиидиотипических антител, сходным с участком связывания MBL в белке MASP-2, и, таким образом, связывать и нейтрализовать лиганд, связывающийся с MASP-2, такой как, например, MBL.
viii. Фрагменты иммуноглобулинов
Средства, ингибирующие MASP-2 и MASP-3, применимые в способе по изобретению, включают не только интактные молекулы иммуноглобулинов, но также и хорошо известные фрагменты, включая фрагменты Fab, Fab', F(ab)2, F(ab')2 и Fv, scFv-фрагменты, диатела, линейные антитела, одноцепочечные молекулы антител и полиспецифические антитела (например, биспецифические и триспецифические), полученные из фрагментов антител.
В этой области хорошо известно, что только небольшая часть молекулы антитела, паратоп, участвует в связывании антитела со своим эпитопом (см., например, Clark, W.R., The Experimental Foundations of Modern Immunology, Wiley & Sons, Inc., NY, 1986). pFc'- и Fc-области антитела являются эффекторами классического пути комплемента, но участвуют не только в связывании антигена. Антитело, от которого ферментативно отщепили pFc'-область, или антитело, полученное без pFc'-области, обозначают как F(ab')2-фрагмент, и он сохраняет оба антигенсвязывающих участка интактного антитела. Выделенный F(ab')2-фрагмент обозначают как бивалентный моноклональный фрагмент из-за двух его антигенсвязывающих участков. Аналогично, антитело, от которого ферментативно отщепили Fc-область, или антитело, полученное без Fc-области, обозначают как Fab-фрагмент, и он сохраняет один из антигенсвязывающих участков интактной молекулы антитела.
Фрагменты антител можно получать протеолитическим гидролизом, таким как расщепление целых антител пепсином или папаином с помощью общепринятых способов. Например, фрагменты антител можно получать ферментативным расщеплением антител пепсином для получения фрагмента 5S, обозначаемого как F(ab')2. Этот фрагмент далее можно расщеплять с использованием тиолового восстановителя для получения моновалентных фрагментов 3,5S Fab'. Необязательно, реакцию расщепления можно проводить с использованием блокирующей группы для сульфгидрильных групп, образующихся при расщеплении дисульфидных связей. Альтернативно, при ферментативном расщеплении с использованием пепсина напрямую получают два моновалентных Fab-фрагмента и Fc-фрагмент. Эти способы описывают, например, в патенте США № 4331647 Goldenberg; Nisonoff, A., et al, Arch. Biochem. Biophys. 89:230, (1960); Porter, R.R., Biochem. J. 75:119, (1959); Edelman, et al, в Methods in Enzymology 7:422, Academic Press, (1967); и Coligan, стр. 2.8.1-2.8.10 и 2.10-2.10.4.
В некоторых вариантах осуществления использование фрагментов антител без Fc-области является предпочтительным для избежания активации классического пути комплемента, инициируемого после связывания Fc с рецептором Fcγ. Существует несколько способов, которыми можно получать моноклональное антитело, избегающее взаимодействия с рецептором Fcγ. Например, Fc-область моноклонального антитела можно удалять химически с использованием частичного расщепления протеолитическими ферментами (такого как расщепление фицином), таким образом, получая, например, антигенсвязывающие фрагменты антител, такие как Fab или F(ab)2-фрагменты (Mariani, M., et al., Mol. Immunol. 28:69-71, (1991)). Альтернативно, при конструировании гуманизированного антитела, представленного в настоящем описании, можно использовать изотип IgG γ4 человека, не связывающийся с рецептором Fcγ. Антитела, одноцепочечные антитела и антигенсвязывающий домены, в которых отсутствует домен Fc, также можно конструировать с использованием рекомбинантных способов, представленных в настоящем описании.
ix. Одноцепочечные фрагменты антител
Альтернативно, можно получать связывающиеся молекулы с одной пептидной цепью, специфичные для MASP-1, MASP-2 или MASP-3, в которых соединяют Fv-области тяжелой и легкой цепи. Fv-фрагменты можно соединять с помощью пептидного линкера для получения одноцепочечного антигенсвязывающего белка (scFv). Эти одноцепочечные антигенсвязывающие белки получают, конструируя структурный ген, содержащий последовательности ДНК, кодирующие домены VH и VL, соединенные олигонуклеотидом. Структурный ген встраивают в экспрессирующий вектор, затем встраиваемый в клетку-хозяина, такую как E. coli. Рекомбинантные клетки-хозяева синтезируют одну полипептидную цепь с линкерным пептидом, соединяющим два V-домена. Способы получения scFv описывают например, в Whitlow, et al., "Methods: A Companion to Methods in Enzymology" 2:97, (1991); Bird, et al, Science 242:423, (1988); патенте США № 4946778 Ladner; Pack, P., et al, Bio/Technology 77:1271, (1993).
В качестве иллюстративного примера, MASP-3-специфичные scFv можно получать, подвергая лимфоциты воздействию полипептида MASP-3 in vitro и выбирая библиотеки антител в фаговом или аналогичных векторах (например, используя иммобилизированный или меченый белок или пептид MASP-3). Гены, кодирующие полипептиды, имеющие потенциальные домены, связывающие полипептид MASP-3, можно получать с помощью скрининга рандомных пептидных библиотек, экспонируемых на фаге или бактериях, таких как E. coli. Эти рандомные пептидные библиотеки можно использовать для скрининга на пептиды, взаимодействующие с MASP-3. Способы получения и скрининга таких рандомных пептидных библиотек хорошо известны в этой области (патент США № 5223409 Lardner; патент США № 4946778 Ladner; патент США № 5403484 Lardner; патент США № 5571698 Lardner; и Kay et al, Phage display of Peptides and Proteins, Academic Press, Inc., 1996), и рандомные пептидные библиотеки и наборы для скрининга таких библиотек являются коммерчески доступными, например, в CLONTECH Laboratories, Inc. (Palo Alto, Calif), Invitrogen Inc. (San Diego, Calif), New England Biolabs, Inc. (Beverly, Mass.) и Pharmacia LKB Biotechnology Inc. (Piscataway, N.J.).
Другой формой фрагмента антитела против MASP-3, применимой в этом аспекте изобретения, является пептид, кодирующий одну определяющую комплементарность область (CDR), связывающуюся с эпитопом антигена MASP-3 и ингибирующую MASP-3-зависимую активацию комплемента (т.е. LEA-1). Другой формой фрагмента антитела против MASP-1, применимой в этом аспекте изобретения, является пептид, кодирующий одну определяющую комплементарность область (CDR), связывающуюся с эпитопом антигена MASP-1 и ингибирующую MASP-3-зависимую активацию комплемента (т.е. LEA-1). Другой формой фрагмента антитела против MASP-2 применимой в этом аспекте изобретения, является пептид, кодирующий одну определяющую комплементарность область (CDR), связывающуюся с эпитопом антигена MASP-2 и ингибирующую MASP-2-зависимую активацию комплемента (т.е. LEA-2).
Пептиды CDR ("минимальные распознающие единицы") можно получать, конструируя гены, кодирующие CDR интересующего антитела. Такие гены получают, например, с использованием полимеразной цепной реакции для синтеза вариабельной области из РНК антитело-продуцирующих клеток (см., например, Larrick et al., Methods: A Companion to Methods in Enzymology 2:106, (1991); Courtenay-Luck, "Genetic Manipulation of Monoclonal Antibodies", Monoclonal Antibodies: Production, Engineering and Clinical Application, Ritter et al. (eds.), p. 166, Cambridge University Press, (1995); и Ward et al., "Genetic Manipulation and Expression of Antibodies," Monoclonal Antibodies: Principles and Applications, Birch et al. (eds.), p. 137, Wiley-Liss, Inc., 1995).
Антитела против MASP, представленные в настоящем описании, вводят нуждающемуся в этом индивидууму для ингибирования LEA-1, LEA-2 или комбинации LEA-1 и LEA-2 активации комплемента. В некоторых вариантах осуществления средство, ингибирующее MASP, является высокоаффинным человеческим или гуманизированным моноклональным антителом против MASP-1, MASP-2 или MASP-3 со сниженной эффекторной функцией.
x. Биспецифические антитела
Средства, ингибирующие MASP-2 и MASP-3, применимые в способе по изобретению, включают полиспецифические (т.е. биспецифические и триспецифические) антитела. Биспецифические антитела являются моноклональными, предпочтительно, человеческими или гуманизированными антителами, обладающими специфичностью связывания для по меньшей мере двух различных антигенов. Как описано выше и представлено в таблице 2, в одном из вариантов осуществления способ включает использование биспецифического антитела, имеющего специфичность связывания для MASP-2 (например, связывающегося с по меньшей мере одним из домена CCP1-CCP2 или домена сериновой протеазы MASP-2) и специфичность связывания для MASP-3 (например, связывающегося с доменом сериновой протеазы MASP-3). В другом варианте осуществления способ включает использование биспецифического антитела, имеющего специфичность связывания для MASP-1 (например, связывающегося с доменом сериновой протеазы MASP-1) и специфичность связывания для MASP-2 (например, связывающегося по меньшей мере с одним из домена CCP1-CCP2 или домена сериновой протеазы MASP-2). В другом варианте осуществления способ включает использование биспецифического антитела, имеющего специфичность связывания для MASP-1 (например, связывающегося с доменом сериновой протеазы MASP-1) и специфичность связывания для MASP-3 (например, связывающегося с доменом сериновой протеазы MASP-3). В другом варианте осуществления способ включает использование триспецифического антитела, имеющего специфичность связывания для MASP-1 (например, связывающегося с доменом сериновой протеазы MASP-1), специфичность связывания для MASP-2 (например, связывающегося с по меньшей мере одним из домена CCP1-CCP2 или домена сериновой протеазы MASP-2) и специфичность связывания для MASP-3 (например, связывающегося с доменом сериновой протеазы MASP-3).
Способы получения биспецифических антител известны специалистам в этой области. Общепринято, рекомбинантное получение биспецифических антител основано на коэкспрессии двух пар тяжелых цепей/легких цепей иммуноглобулина, где две тяжелые цепи имеют различные специфичности (Milstein and Cuello, Nature 305:537-539 (1983)). Вариабельные домены антитела с желательной специфичностью связывания (комбинированные участки антитело-антиген) можно подвергать слиянию с последовательностями константных доменов иммуноглобулина. Предпочтительно, осуществляют слияние с константным доменом тяжелой цепи иммуноглобулина, включающим по меньшей мере часть из шарнирной области, областей CH2 и CH3. ДНК, кодирующая продукты слияния тяжелых цепей иммуноглобулина и, при желании, легких цепей иммуноглобулина, встраивают в отдельные экспрессирующие векторы и котрансфицируют в подходящего организма-хозяина. Более подробно известные в настоящее время иллюстративные способы получения биспецифических антител см., например, в Suresh et al., Methods in Enzymology 121:210 (1986); WO 96/27011; Brennan et al., Science 229:81 (1985); Shalaby et al., J. Exp. Med. 175:217-225 (1992); Kostelny et al., J. Immunol. 148(5):1547-1553 (1992); Hollinger et al. Proc. Natl. Acad. Sci USA 90:6444-6448 (1993); Gruber et al., J. Immunol. 152:5368 (1994); и Tutt et al., J. Immunol. 147:60 (1991). Биспецифические антитела также включают перекрестно сшитые или гетероконъюгированные антитела. Гетероконъюгированные антитела можно получать с использованием любых удобных способов перекрестного сшивания. Подходящие средства для перекрестного сшивания хорошо известны в этой области и описаны в патенте США № 4676980 вместе с рядом способов перекрестного сшивания.
Также описаны различные способы получения и выделения фрагментов биспецифических антител непосредственно из культуры рекомбинантных клеток. Например, биспецифические антитела получают с использованием лейциновых молний. (См., например, Kostelny et al. J.Immunol. 148(5): 1547-1553 (1992)). Технология "диател", описываемая в Hollinger et al. Proc. Natl. Acad. Sci USA 90:6444-6448 (1993), представляет собой альтернативный механизм получения фрагментов биспецифических антител. Фрагменты содержат вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL) с помощью линкера, слишком короткого, чтобы сделать возможным образование пары между двумя доменами на одной цепи. Таким образом, домены VH и VL одного фрагмента заставляют образовывать пары с соответствующими доменами VL и VH другого фрагмента, таким образом, образовывать два антигенсвязывающих участка. Биспецифические диатела, в отличие от целых биспецифических антител, могут также являться особенно подходящими, т.к. их легко можно конструировать и экспрессировать в E. coli. Диатела (и многие другие полипептиды, такие как фрагменты антител) с соответствующей специфичностью связывания, легко можно выбирать с использованием фагового дисплея (WO 94/13804) из библиотек. Если одно плечо диатела сохраняют константным, например, со специфичностью, направленной против антигена X, то затем можно получать библиотеку, в которой варьируют другое плечо и выбирают антитело с соответствующей специфичностью.
Также сообщают о другой стратегии получения фрагментов биспецифических антител с использованием димеров одноцепочечного Fv (scFv). (См., например, Gruber et al. J. Immunol., 152:5368 (1994)). Альтернативно, антитела могут являться "линейными антителами", как описано, например, в Zapata et al, Protein Eng. 8(10): 1057-1062 (1995). В кратком изложении, эти антитела содержат пару тандемных сегментов фактора D (VH-CHI-VH-CHI), образующих пару антигенсвязывающих областей. Линейные антитела могут являться биспецифическими или моноспецифическими. Способы по изобретению также включают использование вариантов форм биспецифических антител, таких как тетравалентные молекулы с двойным вариабельным доменом иммуноглобулина (DVD-Ig), описываемые в Wu et al, Nat Biotechnol 25: 1290-1297 (2007). Молекулы DVD-Ig конструируют таким образом, что два различных вариабельных домена легких цепей (VL) из двух различных родительских антител соединяют способами рекомбинантной ДНК в тандем напрямую или через короткий линкер со следующим за ними константным доменом легкой цепи. Способы получения молекул DVD-Ig из двух родительских антител дополнительно описывают, например, в WO 08/024188 и WO 07/024715, описание каждого из которых включено в настоящее описание в качестве ссылки в полном объеме.
НЕПЕПТИДНЫЕ ИНГИБИТОРЫ
В некоторых вариантах осуществления средством, ингибирующим MASP-3 или MASP-2, является пептид, ингибирующий MASP-3, или MASP-2, или MASP-1, или непептидный ингибитор MASP-3, или MASP-2, или MASP-1. Непептидные средства, ингибирующие MASP, можно вводить индивидууму системно, например, посредством внутриартериального, внутривенного, внутримышечного, подкожного или другого парентерального введения или перорального введения. Средство, ингибирующее MASP, можно вводить периодически в течение длительного периода времени лечения или мониторинга хронического состояния, или введение может являться однократным или повторным введением в период до, в течение или после острой травмы или повреждения.
XVIII. ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ДОСТАВКИ
Дозировка
В другом аспекте изобретение относится к композициям для ингибирования неблагоприятных воздействий MASP-3-зависимой активации комплемента у индивидуума, страдающего гемолитическим заболеванием, таким как PNH, или заболевания или нарушения, выбранного из группы, состоящей из возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, включающего введение индивидууму композиции, содержащей количество средства, ингибирующего MASP-3, эффективное для ингибирования MASP-3-зависимой активации комплемента, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления способ дополнительно включает введение композиции, содержащей средство, ингибирующее MASP-2. Средства, ингибирующие MASP-3 и MASP-2, можно вводить нуждающемуся в этом индивидууму в терапевтически эффективных дозах для лечения или облегчения состояний, ассоциированных с MASP-3-зависимой активацией комплемента (LEA-1) и, необязательно, также MASP-2-зависимой активацией комплемента (LEA-2). Терапевтически эффективная доза относится к количеству средства, ингибирующего MASP-3, или комбинации средства, ингибирующего MASP-3, и средства, ингибирующего MASP-2, достаточному для облегчения симптомов состояния.
Токсичность и терапевтическую эффективность средств, ингибирующих MASP-3 и MASP-2, можно определять стандартными фармацевтическими способами с использованием экспериментальных моделей на животных. Используя такие модели на животных можно определять NOAEL (отсутствие наблюдаемого уровня неблагоприятных воздействий) и MED (минимальную эффективную дозу) с использованием стандартных способов. Соотношение доз между эффектами NOAEL и MED является терапевтическим соотношением, выражаемым как соотношение NOAEL/MED. Наиболее предпочтительными являются средства, ингибирующие MASP-3, и средства, ингибирующие MASP-2, проявляющие высокие терапевтические соотношения или индексы. Данные, получаемые при анализах культур клеток и исследованиях на животных, можно использовать при составлении диапазона доз для применения у людей. Предпочтительно, доза средства, ингибирующего MASP-3, и средства, ингибирующего MASP-2, попадает в диапазон концентраций в кровотоке, включающих MED с невысокой токсичностью или ее отсутствием. Доза может варьироваться в этом диапазоне в зависимости от используемой лекарственной формы и пути введения.
В случае любого состава соединения терапевтически эффективную дозу можно оценивать с использованием моделей на животных. Например, дозу можно определять с использованием модели на животных для получения диапазона концентрации в плазме, включающего MED. Количественные уровни средства, ингибирующего MASP-3, или средства, ингибирующего MASP-2, в плазме также можно измерять, например, с помощью высокоэффективной жидкостной хроматографии.
В дополнение к исследованиям токсичности эффективную дозу также можно оценивать с учетом количества белка-мишени MASP, присутствующего у живого индивидуума, и аффинности связывания средства, ингибирующего MASP-3 или MASP-2.
Сообщают, что уровни MASP-1 у нормальных людей сыворотке находятся в диапазоне от 1,48 до 12,83 мкг/мл (Terai I. et al, Clin Exp Immunol 1 10:317-323 (1997); Theil et al, Clin. Exp. Immunol. 169:38 (2012)). Сообщают, что средние концентрации MASP-3 в сыворотке у нормальных людей находятся в диапазоне от приблизительно 2,0 до 12,9 мкг/мл (Skjoedt M et al, Immunobiology 215(11):921-31 (2010); Degn et al, J. Immunol Methods, 361-37 (2010); Csuka et al, Mol. Immunol. 54:271 (2013). Показано, что MASP-2 у нормальных людей присутствует в сыворотке на низких уровнях в пределах 500 нг/мл, и уровни MASP-2 у конкретного индивидуума можно определять с использованием количественного анализа MASP-2, описываемого в Moller-Kristensen M., et al., J. Immunol. Methods 282:159-167 (2003) и Csuka et al., Mol. Immunol. 54:271 (2013).
Как правило, доза вводимых композиций, содержащих средства, ингибирующие MASP-3, или средства, ингибирующие MASP-2, варьируется в зависимости от таких факторов, как возраст индивидуума, масса тела, рост, пол, общее состояние здоровья и анамнез. В качестве иллюстрации, средства, ингибирующие MASP-3, или средства, ингибирующие MASP-2 (такие как антитела против MASP-3, антитела против MASP-1 или антитела против MASP-2), можно вводить в диапазонах доз от приблизительно 0,010 до 100,0 мг/кг, предпочтительно от 0,010 до 10 мг/кг, предпочтительно от 0,010 до 1,0 мг/кг, более предпочтительно от 0,010 до 0,1 мг/кг массы тела индивидуума. В некоторых вариантах осуществления средства, ингибирующие MASP-2 (такие как антитела против MASP-2), вводят в диапазонах доз от приблизительно предпочтительно 0,010 до 10 мг/кг, предпочтительно от 0,010 до 1,0 мг/кг, более предпочтительно от 0,010 до 0,1 мг/кг массы тела индивидуума. В некоторых вариантах осуществления средства, ингибирующие MASP-1 (такие как антитела против MASP-1), или средства, ингибирующие MASP-3 (такие как антитела против MASP-3), вводят в диапазонах доз от приблизительно 0,010 до 100,0 мг/кг, предпочтительно от 0,010 до 10 мг/кг, предпочтительно от 0,010 до 1,0 мг/кг, более предпочтительно от 0,010 до 0,1 мг/кг массы тела индивидуума.
Терапевтическую эффективность композиций, ингибирующих MASP-3, необязательно в комбинации с композициями, ингибирующими MASP-2, или композициями, ингибирующими MASP-1, необязательно в комбинации с композициями, ингибирующими MASP-2, способы по настоящему изобретению для указанного индивидуума и подходящие дозы можно определять в соответствии с анализами комплемента, хорошо известными специалистам в этой области. Комплемент образует множество конкретных продуктов. В последнее десятилетие разработаны чувствительные и специфичные анализы, и они коммерчески доступны для большинства этих продуктов активации, включая небольшие фрагменты продуктов активации C3a, C4a и C5a и большие фрагменты продуктов активации iC3b, C4d, Bb и sC5b-9. В большинстве из этих анализов используют моноклональные антитела, реагирующие с новыми антигенами (неоантигенами), экспонированными на фрагменте, но не на нативных белках, из которых они образуются, что делает эти анализы очень простыми и специфичными. Большинство из них основано на технологии ELISA, хотя все еще иногда в случае C3a и C5a используют радиоиммунологический анализ. В этих последних анализах измеряют непроцессированные фрагменты и их "desArg"-фрагменты, являющиеся основными формами, обнаруживаемыми в кровотоке. Непроцессированные фрагменты и C5adesArg быстро выводятся посредством связывания с рецепторами поверхности клетки и, таким образом, присутствуют в очень низкой концентрации, в то время как C3adesArg не связывается с клетками и накапливается в плазме. Измерение C3a представляет чувствительный, не зависящий от пути индикатор активации комплемента. Активацию альтернативного пути можно оценивать, измеряя уровень фрагмента Bb и/или измеряя активацию фактора D. Определение продукта мембраноатакующего пути активации, sC5b-9, в жидкой фазе представляет доказательство того, что комплемент активируется до полного завершения. Поскольку в лектиновом и классическом пути образуются одни и те же продукты активации, C4a и C4d, измерение этих двух фрагментов не предоставляет какой-либо информации о том, каким из этих двух путей образовались продукты активации.
Ингибирование MASP-3-зависимой активации комплемента отличается по меньшей мере одним из следующих изменений компонентов системы комплемента, возникающих в результате введения средства, ингибирующего MASP-3, в соответствии со способами по изобретению: ингибирование опосредованной LEA-1 активации комплемента (ингибирование гемолиза и опсонизации); ингибирование субстрат-специфичного расщепления сериновой протеазы MASP-3, снижение гемолиза (измеряемого, например, как описано в примере 5) или снижение расщепления C3 и накопления C3b (измеряемое, например, как описано в примере 4 или примере 11).
Ингибирование MASP-2-зависимой активации комплемента отличается по меньшей мере одним из следующих изменений компонентов системы комплемента, возникающих в результате введения средства, ингибирующего MASP-2, в соответствии со способами по изобретению: ингибирование образования или продукции продуктов MASP-2-зависимой системы активации комплемента C4b, C3a, C5a и/или C5b-9 (MAC) (измеряемое, например, как описано в примере 2 патента США № 7919094), снижение расщепления C4 и накопления C4b (измеряемое, например, как описано в примере 8 или примере 9) или снижение расщепления C3 и накопления C3b (измеряемое, например, как описано в примере 11).
i. Фармацевтические носители и средства доставки
В целом, композиции средства, ингибирующего MASP-3, и композиции средства, ингибирующего MASP-2, по настоящему изобретению или композиции, содержащие комбинацию средств, ингибирующих MASP-2 и MASP-3, можно комбинировать с любыми другими выбранными терапевтическими средствами, их соответствующим образом включают в фармацевтически приемлемый носитель. Носитель является нетоксичным, биосовместимым, и его выбирают таким образом, чтобы он не влиял определяемо на биологическую активность средства, ингибирующего MASP-3, или средства, ингибирующего MASP-2 (и любых других терапевтических средств, комбинируемых с ними). Примеры фармацевтически приемлемых носителей для пептидов описывают в патенте США № 5211657 Yamada. Как представлено в настоящем описании, антитела против MASP, применимые в изобретении, можно составлять в препаратах в твердой, полутвердой, гелевой, жидкой или газообразных формах, таких как таблетки, капсулы, порошки, гранулы, мази, растворы, депозитории, ингалянты и инъекции, делающие возможным пероральное, парентеральное или хирургическое введение. Изобретение также включает местное введение композиций с помощью покрытых медицинских устройств и т.п.
Подходящие носители для парентеральной доставки посредством инъекции, вливания или промывания и местной доставки включают дистиллированную воду, физиологический фосфатно-солевой буфер, нормальный или лактатный раствор Рингера, раствор декстрозы, раствор Хенкса или пропандиол. Кроме того, в качестве растворителя или среды для суспендирования можно использовать стерильные жирные масла. Для этой цели можно использовать любое биосовместимое масло, включая синтетические моно- или диглицериды. Кроме того, в получении инъецируемых средств находят свое применение жирные кислоты, такие как олеиновая кислота. Носитель и средство можно объединять в виде жидкости, суспензии, полимеризующегося или неполимеризующегося геля, пасты или мази.
Носитель также может содержать средство доставки для поддержания (т.е. продления, замедления или регуляции) доставки средств или для усиления доставки, захвата, стабильности или фармакокинетики терапевтических средств. Такое средство доставки может включать, в качестве неограничивающего примера, микрочастицы, микросферы, наносферы или наночастицы, состоящие из белков, липосом, углеводов, синтетических органических соединений, неорганических соединений, полимерных или сополимерных гидрогелей и полимерных мицелл. Подходящие системы доставки на основе гидрогелей и мицелл включают coполимеры PEO:PHB:PEO и комплексы coполимер/циклодекстрин, описываемые в WO 2004/009664 A2, и PEO и комплексы PEO/циклодекстрин, описываемые в публикации патентной заявки США № 2002/0019369 A1. Такие гидрогели можно инъецировать местно в участок предполагаемого действия или подкожно или внутримышечно для образования депо для замедленного высвобождения.
Композиции по настоящему изобретению можно составлять для подкожной, внутримышечной, внутривенной, внутриартериальной доставки или доставки в виде ингалянта.
В случае внутриартериальной доставки средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2, можно включать в описанные выше жидкие или гелевые носители, являющиеся инъецируемыми, описанные выше средства доставки с замедленным высвобождением, являющиеся инъецируемыми, или гиалуроновую кислоту или производное гиалуроновой кислоты.
В случае перорального введения непептидергических средств средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2, можно включать в инертный наполнитель или разбавитель, такой как сахароза, кукурузный крахмал или целлюлоза.
В случае местного введения средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2, можно включать в мазь, лосьон, крем, гель, капли, суппозиторий, спрей, жидкость или порошок или в гелевые или микрокапсулярные системы доставки с помощью трансдермального пластыря.
Разрабатывают различные системы назальной и легочной доставки, включая аэрозоли, дозирующие ингаляторы, порошковые ингаляторы и небулайзеры, их можно соответствующим образом адаптировать для доставки по настоящему изобретению в аэрозоле, ингалянте или распыляемом средстве доставки, соответственно.
В случае интратекальной (IT) или интрацеребровентрикулярной (ICV) доставки для введения настоящего изобретения можно использовать соответствующие стерильные системы доставки (например, жидкости, гели, суспензии и т.д.).
Композиции по настоящему изобретению также могут включать биосовместимые эксципиенты, такие как диспергирующие средства или увлажнители, суспендирующие средства, разбавители, буферы, усилители проницаемости, эмульгаторы, связывающие средства, загустители, ароматизаторы (в случае перорального введения).
ii. Фармацевтические носители для антител и пептидов
Более конкретно в отношении антител против MASP, как представлено в настоящем описании, примеры составов можно вводить парентерально в виде инъецируемых доз раствора или суспензии соединения в физиологически приемлемом разбавителе с фармацевтическим носителем, который может являться стерильной жидкостью, такой как вода, масла, физиологический раствор, глицерин или этанол. Дополнительно, в композициях, содержащих антитела против MASP, могут присутствовать вспомогательные средства, такие как увлажнители или эмульгаторы, поверхностно-активные вещества, pH-буферные вещества и т.п. Дополнительные компоненты фармацевтических композиций включают вазелин (например, животного, растительного или синтетического происхождения), например, соевое масло и минеральное масло. В основном, предпочтительными жидкими носителями для инъецируемых растворов являются гликоли, такие как пропиленгликоль или полиэтиленгликоль.
Антитела против MASP также можно вводить в форме инъекции вещества с замедленным всасыванием или имплантируемого препарата, который можно составлять так, чтобы делать возможным замедленное или пульсирующее высвобождение активных средств.
XVIX. СПОСОБЫ ВВЕДЕНИЯ
Фармацевтические композиции, содержащие средства, ингибирующие MASP-3, или средства, ингибирующие MASP-,2 можно вводить рядом способов в зависимости от того, местный или системный способ введения является наиболее подходящим для состояния, подлежащего лечению. Кроме того, можно доставлять композиции по настоящему изобретению, покрывая или включая композиции в имплантируемое медицинское устройство.
i. Системная доставка
Как применяют в настоящем описании, термины "системная доставка" и "системное введение" предназначены для включения, в качестве неограничивающих примеров, перорального и парентерального путей, включая внутримышечный (IM), подкожный, внутривенный (IV), внутриартериальный, ингаляционный, сублингвальный, буккальный, местный, трансдермальный, назальный, ректальный, вагинальный и другие пути введения, эффективно приводящие к распределению доставляемого средства в один или множество участков предполагаемого терапевтического действия. Предпочтительные пути системной доставки настоящих композиций включают внутривенный, внутримышечный, подкожный, внутриартериальный и ингаляционный. Следует понимать, что конкретный путь системного введения выбранных средств, используемых в конкретных композициях по настоящему изобретению, будут определять частично с учетом чувствительности средства к путям метаболической трансформации, ассоциированным с указанным путем введения. Например, пептидергические средства наиболее предпочтительно можно вводить путями, иными, чем пероральным.
Как представлено в настоящем описании, антитела, ингибирующие MASP, можно доставлять нуждающемуся в этом индивидууму любыми подходящими способами. Способы доставки антител и полипептидов против MASP включают введение пероральным, легочным, парентеральным путем (например, с помощью внутримышечной, интраперитонеальной, внутривенной (IV) или подкожной инъекции), с помощью ингаляции (например, с помощью тонкодисперсного порошкового состава), трансдермальным, назальным, вагинальным, ректальным или сублингвальным путями введения, и их можно составлять в лекарственных формах, подходящих для каждого пути введения.
В качестве типичного примера, антитела и пептиды, ингибирующие MASP, можно вводить в живой организм с использованием физической мембраны, способной абсорбировать полипептиды, например, назальных, желудочно-кишечных и ректальных мембран. Как правило, полипептиды наносят на абсорбирующуюся мембрану в комбинации с усилителем проницаемости. (См., например, Lee, V.H.L., Crit. Rev. Ther. Drug Carrier Sys. 5:69, (1988); Lee, V.H.L., J. Controlled Release 13:213, (1990); Lee, V.H.L., Ed., Peptide and Protein Drug Delivery, Marcel Dekker, New York (1991); DeBoer, A.G., et al., J. Controlled Release 13:241, (1990). Например, STDHF является синтетическим производным фусидовой кислоты, стероидного поверхностно-активного вещества, аналогичного по структуре солям желчных кислот и используемого в качестве усилителя проницаемости для назальной доставки (Lee, W.A., Biopharm. 22, Nov./Dec. 1990.).
Как представлено в настоящем описании, антитела, ингибирующие MASP, можно вводить в соединении с другой молекулой, такой как липид, для защиты полипептидов от ферментативной деградации. Например, ковалентное присоединение полимеров, в частности, полиэтиленгликоля (PEG), используют для защиты конкретных белков от ферментативного гидролиза в организме и, таким образом, повышения времени полужизни (Fuertges, F., et al, J. Controlled release 11: 139, (1990)). Сообщают о многих полимерных системах для доставки белков (Bae, Y.H., et al., J. Controlled Release 9:271, (1989); Hori, R., et al., Pharm. Res. 6:813, (1989); Yamakawa, I., et al., J. Pharm. Sci. 79:505, (1990); Yoshihiro, I., et al., J. Controlled Release 10:195, (1989); Asano, M., et al., J. Controlled Release 9:111, (1989); Rosenblatt, J., et al., J. Controlled Release 9:195, (1989); Makino, K., J. Controlled Release 12:235, (1990); Takakura, Y., et al., J. Pharm. Sci. 78:117, (1989); Takakura, Y., et al., J. Pharm. Sci. 78:219, (1989)).
Недавно разработаны липосомы с улучшенной стабильностью в сыворотке и временем полужизни в кровотоке (см., например, патент США № 5741516 Webb). Кроме того, описывают различные способы с использованием липосом и липосомо-подобных препаратов в качестве потенциальных носителей для лекарственных средств (см., например, патент США № 5567434 Szoka; патент США № 5552157 Yagi; патент США № 5565213 Nakamori; патент США № 5738868 Shinkarenko и патент США № 5795587 Gao).
Как представлено в настоящем описании, в случае трансдермального применения антитела, ингибирующие MASP, можно комбинировать с другими подходящими ингредиентами, такими как носители и/или адъюванты. Не существует ограничений по природе таких других ингредиентов, за исключением того, что они должны являться фармацевтически приемлемыми для их предполагаемого введения и не снижают активность активных ингредиентов композиции. Примеры подходящих средств включают мази, кремы, гели или суспензии с очищенным коллагеном или без него. Антителами, ингибирующими MASP, также можно пропитывать трансдермальные пластыри, пластыри и перевязочные материалы, предпочтительно, в жидкой или полужидкой форме.
Композиции по настоящему изобретению можно вводить системно на периодической основе с определенными интервалами для поддержания желаемого уровня терапевтического эффекта. Например, композиции можно вводить, например, посредством подкожной инъекции каждые две-четыре недели или с большими интервалами. Режим дозирования будет определять лечащий врач с учетом различных факторов, которые могут влиять на действие комбинации средств. Эти факторы будут включать длительность прогрессирования состояния, подвергаемого лечению, возраста пациента, пола и массы тела, и других клинических факторов. Доза каждого отдельного средства будет варьироваться как функция средства, ингибирующего MASP-3, или средства, ингибирующего MASP-2, включаемого в композицию, а также наличия и природы любого средства доставки лекарственного средства (например, средства доставки с замедленным высвобождением). Кроме того, дозируемое количество можно корректировать с учетом изменения частоты введения и фармакокинетических свойств доставляемых средств.
ii. Местная доставка
Как применяют в настоящем описании, термин "местный" включает применения лекарственного средства в участке или вокруг участка предполагаемого локализованного действия и может включать, например, местную доставку в кожу или другие поврежденные ткани, офтальмологическую доставку, интратекальное (IT), интрацеребровентрикулярное (ICV), внутрисуставное, внутриполостное, внутричерепное введение или введение в мочевой пузырь, распределение или промывание. Местное введение может являться предпочтительным для осуществления введения меньшей дозы, для избежания системных побочных эффектов и для более точного контроля времени доставки и концентрации активных средств в участке местной доставки. Местное введение обеспечивает известную концентрация в целевом участке, независимо от межиндивидуальной вариабельности метаболизма, кровотока и т.д. Улучшенный контроль дозировки также обеспечивают с помощью прямого способа доставки.
Местную доставку средства, ингибирующего MASP-3, или средства, ингибирующего MASP-2, можно осуществлять в рамках хирургических способов лечения заболевания или состояния, например, в течение процедур, таких как аортокоронарное шунтирование, атерэктомия, лазерные процедуры, ультразвуковые процедуры, баллонная ангиопластика и замена стента. Например, средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2, можно вводить индивидууму в комбинации с процедурой баллонной ангиопластики. Процедура баллонной ангиопластики включает введение в артерию катетера, содержащего спущенный баллон. Спущенный баллон располагают вблизи атеросклеротической бляшки и накачивают его таким образом, что бляшку вдавливают в стенку сосуда. В результате, поверхность баллона приводят в контакт со слоем эндотелиальных клеток на поверхности кровеносного сосуда. Средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2, можно присоединять к катетеру для баллонной ангиопластики способом, делающим возможным высвобождение средства в участке атеросклеротической бляшки. Средство можно присоединять к баллонному катеру стандартными способами, известными в этой области. Например, средство можно хранить в отделении баллонного катетера до надувания баллона, в момент которого оно высвобождается в локальное окружение. Альтернативно, средством можно пропитывать поверхность баллона таким образом, что его приводят в контакт с клетками стенки артерии при надувании баллона. Средство также можно доставлять с помощью перфорированного баллонного катетера, такого как описываемый в Flugelman, M.Y., et al, Circulation 55:1110-1117, (1992). Пример способа присоединения терапевтического белка к катетеру для баллонной ангиопластики см. также в опубликованной заявке PCT WO 95/23161. Аналогично, средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2, можно включать в гелевое или полимерное покрытие, наносимое на стент, или его можно включать в материал стента таким образом, что после помещения в сосуд из стента высвобождается средство, ингибирующее MASP-3, или средство, ингибирующее MASP-2.
Средства, ингибирующие MASP-3, или средства, ингибирующие MASP-2, используемые в лечении артритов и других скелетно-мышечных нарушений, можно доставлять местно с помощью внутрисуставной инъекции. Такие композиции соответствующим образом могут включать средство доставки с замедленным высвобождением. В качестве дополнительного примера случаев, в которых местная доставка может являться желательной, композиции, ингибирующие MASP-2, используемые в лечении урогенитальных состояний можно соответствующим образом инстилировать в мочевой пузырь или в другую структуру мочеполовой системы.
XX. СХЕМЫ ЛЕЧЕНИЯ
При профилактическом применении фармацевтические композиции вводят индивидууму, предрасположенному к заболеванию или нарушению, выбранному из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, или имеющему риск его развития, в количестве, достаточном для устранения или снижения риска развития симптомов состояния. При терапевтическом применении фармацевтические композиции вводят индивидууму, предрасположенному к заболеванию или нарушению, выбранному из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, или уже страдающему им, в терапевтически эффективном количестве, достаточном для облегчения или по меньшей мере частичного снижения симптомов состояния.
В одном из вариантов осуществления фармацевтическую композицию вводят индивидууму, страдающему или имеющему риск развития PNH. В соответствии с этим, эритроциты индивидуума опсонизируются фрагментами C3 в отсутствие композиции, и введение композиции индивидууму повышает выживаемость эритроцитов у индивидуума. В одном из вариантов осуществления у индивидуума в отсутствие композиции развивается один или несколько симптомов, выбранных из группы, состоящей из (i) уровней гемоглобина ниже нормальных, (ii) уровней тромбоцитов ниже нормальных; (iii) уровней ретикулоцитов выше нормальных и (iv) уровней билирубина выше нормальных, и введение композиции индивидууму улучшает по меньшей мере один или несколько из симптомов, приводя к (i) повышенным, нормальным или почти нормальным уровням гемоглобина, (ii) повышенным, нормальным или почти нормальным уровням тромбоцитов, (iii) сниженным, нормальным или почти нормальным уровням ретикулоцитов и/или (iv) сниженным, нормальным или почти нормальным уровням билирубина.
В профилактических и терапевтических схемах для лечения, профилактики или снижения тяжести заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, композиции, содержащие средства, ингибирующие MASP-3, и, необязательно, средства, ингибирующие MASP-2, можно вводить в нескольких дозах до достижения достаточного терапевтического исхода у индивидуума. В одном из вариантов осуществления изобретения средство, ингибирующее MASP-3 и/или MASP-2, содержит антитело против MASP-1, антитело против MASP-2 или антитело против MASP-3, которое соответствующим образом можно вводить взрослому пациенту (например, взрослому со средней массой тела 70 кг) в дозе от 0,1 мг до 10000 мг, более предпочтительно от 1,0 мг до 5000 мг, более предпочтительно от 10,0 мг до 2000 мг, более предпочтительно от 10,0 мг до 1000 мг, и еще более предпочтительно от 50,0 мг до 500 мг или от 10 до 200 мг. В случае пациентов детского возраста дозу можно корректировать пропорционально массе тела пациента.
Применение композиций, ингибирующих MASP-3, и, необязательно, композиций, ингибирующих MASP-2, по настоящему изобретению можно осуществлять с помощью однократного введения композиции (например, одной композиции, содержащей средства, ингибирующие MASP-2 и MASP-3, или биспецифические ингибирующие средства или средства с двойной специфичностью, или с помощью совместного введения отдельных композиций) или ограниченной последовательности введений для лечения заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета. Альтернативно, композицию можно вводить с периодическими интервалами, например, ежедневно, дважды в неделю, еженедельно, через неделю, ежемесячно или дважды в месяц в течение длительного периода времени, определяемого лечащим врачом для оптимального терапевтического эффекта.
В некоторых вариантах осуществления индивидууму, страдающему или имеющему риск развития заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета, вводят первую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-3, и вторую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-2. В одном из вариантов осуществления первую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-3, и вторую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-2, вводят одновременно (т.е. с временным интервалом не более приблизительно 15 минут или менее, таким как не более 10, 5 или 1 минуты). В одном из вариантов осуществления первую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-3, и вторую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-2, вводят последовательно (т.е. первую композицию вводят до или после введения второй композиции, где временной интервал между введениями составляет более 15 минут). В некоторых вариантах осуществления первую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-3, и вторую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-2, вводят одновременно (т.е. период введения первой композиции перекрывается с периодом введения второй композиции). Например, в некоторых вариантах осуществления первую композицию и/или вторую композицию вводят в течение периода по меньшей мере одной, двух, трех или четырех недель или более. В одном из вариантов осуществления по меньшей мере одно средство, ингибирующее MASP-3, и по меньшей мере одно средство, ингибирующее MASP-2, комбинируют в стандартной лекарственной форме. В одном из вариантов осуществления первую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-3, и вторую композицию, содержащую по меньшей мере одно средство, ингибирующее MASP-2, упаковывают вместе в набор для применения в лечении заболевания или нарушения, выбранного из группы, состоящей из пароксизмальной ночной гемоглобинурии (PNH), возрастной дегенерации желтого пятна (AMD), повреждения при ишемии-реперфузии, артрита, диссеминированного внутрисосудистого свертывания, тромботической микроангиопатии (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, эндофтальмита, нейромиелита зрительного нерва или болезни Бехчета.
В некоторых вариантах осуществления индивидуума, страдающего PNH, возрастной дегенерацией желтого пятна (AMD), повреждением при ишемии-реперфузии, артритом, диссеминированным внутрисосудистым свертыванием, тромботической микроангиопатией (включая гемолитико-уремический синдром (HUS), атипичный гемолитико-уремический синдром (aHUS) и тромботическую тромбоцитопеническую пурпуру (TTP)), астмой, болезнью плотного депозита, слабоиммунным некротизирующим гломерулонефритом с полулуниями, травматическим повреждением головного мозга, аспирационной пневмонией, эндофтальмитом, нейромиелитом зрительного нерва или болезнью Бехчета, ранее подвергали лечению или в настоящее время подвергают лечению ингибитором терминальных компонентов комплемента, ингибирующим расщепление белка комплемента C5. В некоторых вариантах осуществления способ включает введение индивидууму композиции по изобретению, содержащей ингибитор MASP-3, и, необязательно, ингибитор MASP-2, и дополнительное введение индивидууму ингибитора терминальных компонентов комплемента, ингибирующего расщепление белка комплемента C5. В некоторых вариантах осуществления ингибитором терминальных компонентов комплемента является гуманизированное антитело против C5 или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления ингибитором терминальных компонентов комплемента является экулизумаб.
XXI. ПРИМЕРЫ
В следующих примерах иллюстрируют исключительно лучший способ, предлагаемый для практического осуществления изобретения, но их не следует истолковывать как ограничивающие изобретение. Все литературные источники, приведенные в настоящем описании, напрямую включены в настоящее описание в качестве ссылок.
ПРИМЕР 1
В этом примере показано, что мыши с дефицитом MASP-2 защищены от вызываемой Neisseria meningitidis гибели после инфицирования N. meningitidis серогруппы A или N. meningitidis серогруппы B.
Способы:
Мышей, нокаутных по MASP-2 (мышей MASP-2 KO), получали, как описано в примере 1 патента США № 7919094, таким образом, включенного в настоящее описание в качестве ссылки. Мышей MASP-2 KO (n=10) и мышей дикого типа (WT) C57/BL6 (n=10) возрастом 10 недель инокулировали с помощью интраперитонеальной (i.p.) инъекции дозы 2,6×107 КОЕ N. meningitidis серогруппы A Z2491 в объеме 100 мкл. Инфицирующую дозу вводили мышам в комбинации с декстраном железа в конечной концентрации 400 мг/кг. Выживаемость мышей после инфицирования контролировали в течение 72-часового периода времени.
В отдельном эксперименте мышей MASP-2 KO (n=10) и мышей WT C57/BL6 (n=10) возрастом 10 недель инокулировали с помощью i.p. инъекции дозой 6×106 КОЕ N. meningitidis серогруппы B штамма MC58 в объеме 100 мкл. Инфицирующую дозу вводили мышам в комбинации с декстраном железа в конечной дозе 400 мг/кг. Выживаемость мышей после инфицирования контролировали в течение 72-часового периода времени. Индекс заболеваемости также определяли для мышей WT и MASP-2 KO в течение 72-часового периода времени после инфицирования с учетом параметров по шкале заболеваемости, описываемой ниже в таблице 4, основанной на схеме Fransen et al. (2010) с небольшими модификациями.
Шкала заболеваемости, ассоциированная с клиническими признаками у инфицированных мышей
Образцы крови брали у мышей с часовыми интервалами после инфицирования и анализировали для определения уровня N. meningitidis в сыворотке (log КОЕ/мл) для подтверждения инфекции и определения скорости клиренса бактерий из сыворотки.
Результаты:
Фигура 8 представляет собой график Каплана-Мейера, на котором показан процент выживаемости мышей MASP-2 KO и WT после введения инфицирующей дозы 2,6×107 КОЕ N. meningitidis серогруппы A Z2491. Как показано на фигуре 8, 100% мышей MASP-2 KO выживали на всем протяжении 72-часового периода после инфицирования. В отличие от этого, только 80% мышей WT (p=0,012) все еще являлись живыми через 24 часа после инфицирования, и только 50% мышей WT все еще являлись живыми через 72 часа после инфицирования. Эти результаты свидетельствуют о том, что мыши с дефицитом MASP-2 защищены от индуцируемой N. meningitidis серогруппы A Z2491 гибели.
Фигура 9 представляет собой график Каплана-Мейера, на котором показан процент выживаемости мышей MASP-2 KO и WT после введения инфицирующей дозы 6×106 КОЕ N. meningitidis серогруппы B штамма MC58. Как показано на фигуре 9, 90% мышей MASP-2 KO выживали на всем протяжении 72-часового периода после инфицирования. В отличие от этого, только 20% мышей WT (p=0,0022) все еще являлись живыми через 24 часа после инфицирования. Эти результаты свидетельствуют о том, что мыши с дефицитом MASP-2 защищены от индуцируемой N. meningitidis серогруппы B штамма MC58 гибели.
На фигуре 10 графически проиллюстрирован log КОЕ/мл N. meningitidis серогруппы B штамма MC58, выделенных в разные моменты времени из образцов крови, взятых из мышей MASP-2 KO и WT после инфицирования i.p. 6×106 КОЕ N. meningitidis серогруппы B штамма MC58 (n=3 в разные моменты времени для обоих групп мышей). Результаты выражали как среднее ± SEM. Как показано на фигуре 10, у мышей WT уровень N. meningitidis в крови достигал пика приблизительно 6,0 log КОЕ/мл через 24 часа после инфицирования и снижался до приблизительно 4,0 log КОЕ/мл через 36 часов после инфицирования. В отличие от этого, у мышей MASP-2 KO уровень N. meningitidis достигал пика приблизительно 4,0 log КОЕ/мл через 12 часов после инфицирования и снижался до приблизительно 1,0 log КОЕ/мл через 36 часа после инфицирования (символом "*" указывают p<0,05; символом "**" указывают p=0,0043). Эти результаты свидетельствуют о том, что, хотя мышей MASP-2 KO инфицировали той же дозой N. meningitidis серогруппы B штамма MC58, что и мышей WT, мыши MASP-2 KO имели повышенный клиренс бактериемии по сравнению с WT.
На фигуре 11 графически представлен средний индекс заболеваемости мышей MASP-2 KO и WT через 3, 6, 12 и 24 часа после инфицирования 6×106 КОЕ N. meningitidis серогруппы B штамма MC58. Как показано на фигуре 11, мыши с дефицитом MASP-2 демонстрировали высокую резистентность по отношению к инфекции с гораздо меньшим индексом заболеваемости через 6 часов (символом "*" указывают p=0,0411), 12 часов (символом "**" указывают p=0,0049) и 24 часа (символом "***" указывают p=0,0049) после инфицирования по сравнению с мышами WT. Результаты, представленные на фигуре 11, выражали как среднее ± SEM.
В совокупности, результаты в этом примере свидетельствуют о том, что мыши с дефицитом MASP-2 защищены от индуцируемой N. meningitidis гибели после инфицирования N. meningitidis серогруппы A или N. meningitidis серогруппы B.
ПРИМЕР 2
В этом примере показано, что введение антитела против MASP-2 после инфицирования N. meningitidis повышает выживаемость мышей, инфицированных N. meningitidis.
Уровень техники/Обоснование:
Как описано в примере 24 патента США № 7919094, включенном в настоящее описание в качестве ссылки, белок MASP-2 крысы использовали для пэннинга библиотеки фагового дисплея Fab, из которой Fab2 #11 идентифицировали как функционально активное антитело. Полноразмерные антитела изотипов IgG2c крысы и IgG2a мыши получали из Fab2 #11. Полноразмерное антитело против MASP-2 изотипа IgG2a мыши охарактеризовывали по фармакодинамическим параметрам (как описано в примере 38 патента США № 7919094).
В этом примере полноразмерное антитело мыши против MASP-2, полученное из Fab2 #11, анализировали на модели инфекции мыши N. meningitidis.
Способы:
Полноразмерное антитело против MASP-2 изотипа IgG2a мыши, полученное из Fab2 #11, полученного, как описано выше, тестировали на модели инфекции мыши N. meningitidis следующим образом.
1. Введение моноклональных антител мыши против MASP-2 (MoAb) после инфицирования
Мышей C57/BL6 Charles River возрастом 9 недель обрабатывали ингибиторным антителом мыши против MASP-2 (1,0 мг/кг) (n=12) или контрольным изотипическим антителом (n=10) через 3 часа после i.p. инъекции высокой дозы (4×106 КОЕ) N. meningitidis серогруппы B штамма MC58.
Результаты:
Фигура 12 представляет собой график Каплана-Мейера, на котором показан процент выживаемости мышей после введения инфицирующей дозы 4×106 КОЕ N. meningitidis серогруппы B штамма MC58 с последующим введением ингибиторного антитела против MASP-2 (1,0 мг/кг) или контрольного изотипического антитела через 3 часа после инфицирования. Как показано на фигуре 12, 90% мышей, обработанных антителом против MASP-2, выживали на всем протяжении 72-часового периода после инфицирования. В отличие от этого, только 50% мышей, обработанных изотипическим контрольным антителом, выживали на всем протяжении 72-часового периода после инфицирования. Символом "*" указывают p=0,0301, определяемый при сравнении двух кривых выживаемости.
Эти результаты свидетельствуют о том, что введение антитела против MASP-2 является эффективным для лечения и улучшения выживаемости у индивидуумов, инфицированных N. meningitidis.
Как показано в настоящем описании, использование антитела против MASP-2 в лечении индивидуума, инфицированного N. meningitidis, является эффективным при введении в течение 3 часов после инфицирования, и ожидают, что оно будет эффективным в период от 24 часов до 48 часов после инфицирования. Менингококковое заболевание (менингококкемия или менингит) является неотложным состоянием, и, как правило, при подозрении на менингококковое заболевание терапию будут начинать незамедлительно (т.е. до положительной идентификации N. meningitidis в качестве этиологического фактора).
В свете результатов, полученных с использованием мышей MASP-2 KO, представленных в примере 1, предполагают, что введение антитела против MASP-2 до инфицирования N. meningitidis также будет эффективным в профилактике или облегчении тяжести инфекции.
ПРИМЕР 3
В этом примере показано, что комплемент-зависимое уничтожение N. meningitidis в сыворотках человека является MASP-3-зависимым.
Обоснование:
Пациенты со сниженными уровнями функционального MBL в сыворотке проявляют повышенную предрасположенность к рецидивирующим бактериальным и грибковым инфекциям (Kilpatrick et al., Biochim Biophys Acta 1572:401-413 (2002)). Известно, что N. meningitidis распознается MBL, и показано, что сыворотки при дефиците MBL не лизируют N. meningitidis.
С учетом результатов, описанных в примерах 1 и 2, осуществляли серию экспериментов для определения эффективности введения антитела против MASP-2 для лечения инфекции N. meningitidis в сыворотках при дефиците комплемента и контрольных сыворотках человека. Осуществляли эксперименты с высокой концентрацией сыворотки (20%) для сохранения пути комплемента.
Способы:
1. Бактерицидная активность сыворотки в различных сыворотках человека при дефиците комплемента и в сыворотках человека, обработанных антителом против MASP-2 человека
В этом эксперименте использовали следующие сыворотки человека при дефиците комплемента и контрольные сыворотки человека:
Тестируемые образцы сыворотки человека (как представлено на фигуре 13)
Рекомбинантное антитело против MASP-2 человека выделяли из комбинаторной библиотеки антител (Knappik, A., et al., J. Mol. Biol. 296:51-86 (2000)) с использованием рекомбинантного MASP-2A человека в качестве антигена (Chen, C.B. and Wallis, J. Biol. Chem. 276:25894-25902 (2001)). Идентифицировали scFv-фрагмент против человека, потенциально ингибирующий опосредованную лектиновым путем активацию C4 и C3 в плазме человека (IC50 ~20 нМ), и преобразовывали его в полноразмерное антитело IgG4 человека.
N. meningitidis серогруппы B-MC58 инкубировали с различными сыворотками, приведенными в таблице 5, каждая в 20% концентрации сыворотки, с добавлением ингибиторного антитела против MASP-2 человека (3 мкг в 100 мкл общего объема) или без него при 37°C со встряхиванием. Образцы получали в следующие моменты времени: через 0-, 30-, 60- и 90-минутные интервалы, выделяли, а затем определяли количество жизнеспособных микроорганизмов. Термически инактивированную сыворотку человека использовали в качестве отрицательного контроля.
Результаты:
На фигуре 13 графически показан log КОЕ/мл количества жизнеспособных микроорганизмов N. meningitidis серогруппы B-MC58, выделенных в разные моменты времени в образцах сывороток человека, приведенных в таблице 5. В таблице 6 представлены результаты t-теста Стьюдента для данных, представленных на фигуре 13.
Результаты t-теста Стьюдента для данных, представленных на фигуре 13 (момент времени через 60 минут)
Как показано на фигуре 13 и в таблице 6, комплемент-зависимое уничтожение N. meningitidis в 20% сыворотке человека значительно повышалось при добавлении ингибиторного антитела против MASP-2 человека.
2. Бактерицидная активность различных сывороток при дефиците комплемента
В этом эксперименте использовали следующие сыворотки человека при дефиците комплемента и контрольные сыворотки человека:
Тестируемые образцы сыворотки человека (как показано на фигуре 14)
N. meningitidis серогруппы B-MC58 инкубировали с различными сыворотками человека с дефицитом комплемента, каждая из которых находится в концентрации 20%, при 37°C со встряхиванием. Образцы забирали в следующие моменты времени: через 0-, 15-, 30-, 45-, 60-, 90- и 120-минутные интервалы, выделяли, а затем определяли количество жизнеспособных микроорганизмов. Термически инактивированную сыворотку человека использовали в качестве отрицательного контроля.
Результаты:
На фигуре 14 графически представлен log КОЕ/мл количества жизнеспособных микроорганизмов N. meningitidis серогруппы B-MC58, выделенных в разные моменты времени в образцах сыворотки человека, приведенных в таблице 7. Как показано на фигуре 14, сыворотка WT (NHS) имела наибольший уровень бактерицидной активности в отношении N. meningitidis. В отличие от этого, сыворотки человека MBL-/- и MASP-3-/- (где достаточно MASP-1) не имели какой-либо бактерицидной активности. Эти результаты свидетельствуют о том, что комплемент-зависимое уничтожение N. meningitidis в 20% (об./об.) сыворотке человека является MASP-3- и MBL-зависимым. В таблице 8 представлены результаты t-теста Стьюдента для данных, представленных на фигуре 14.
Результаты t-теста Стьюдента для данных, представленных на фигуре 14
В целом, результаты, представленные на фигуре 14 и в таблице 8, показывают, что комплемент-зависимое уничтожение N. meningitidis в 20% сыворотке человека является MASP-3- и MBL-зависимым.
3. Комплемент-зависимое уничтожение N. meningitidis в 20% (об./об.) сыворотках мыши с дефицитом MASP-2, MASP-1/3 или MBL A/C
В этом эксперименте использовали следующие сыворотки мыши с дефицитом комплемента и контрольные сыворотки мыши:
Тестируемые образцы сыворотки мыши (как показано на фигуре 15)
N. meningitidis серогруппы B-MC58 инкубировали с различными сыворотками мыши с дефицитом комплемента, каждая из которых находилась в концентрации 20%, при 37°C со встряхиванием. Образцы забирали в следующие моменты времени: через 0-, 15-, 30-, 60-, 90- и 120-минутные интервалы, выделяли, а затем определяли количество жизнеспособных микроорганизмов. Термически инактивированную сыворотку человека использовали в качестве отрицательного контроля.
Результаты:
На фигуре 15 графически представлен log КОЕ/мл количества жизнеспособных микроорганизмов N. meningitidis серогруппы B-MC58, выделенных в разные моменты времени, в образцах сыворотки мыши, приведенных в таблице 9. Как показано на фигуре 15, сыворотки мыши MASP-2-/- имели более высокий уровень бактерицидной активности в отношении N. meningitidis, чем сыворотки мыши WT. В отличие от этого, сыворотки мыши MASP-1/3-/- не имели какой-либо бактерицидной активности. Символом "**" указывают p=0,0058, символом "***" указывают p=0,001. В таблице 10 представлены результаты t-теста Стьюдента для данных, представленных на фигуре 15.
Результаты t-теста Стьюдента для данных, представленных на фигуре 15
В целом, результаты, представленные в этом примере, свидетельствуют о том, что сыворотка MASP-2-/- имела более высокий уровень бактерицидной активности в отношении N. meningitidis, чем сыворотка WT, и что комплемент-зависимое уничтожение N. meningitidis в 20% сыворотке является MASP-3- и MBL-зависимым.
ПРИМЕР 4
В этом примере описывают серию экспериментов, осуществленных для определения механизма MASP-3-зависимой резистентности к инфекции N. meningitidis, наблюдаемой у мышей MASP-2 KO, описанных в примерах 1-3.
Обоснование:
Для определения механизма MASP-3-зависимой резистентности к инфекции N. meningitidis, наблюдаемой у мышей MASP-2 KO (описанных выше в примерах 1-3), осуществляли серию экспериментов следующим образом.
1. У мышей с дефицитом MASP-1/3 не наблюдают дефицит функциональной активности лектинового пути (также обозначаемого как "LEA-2")
Способы:
Для определения того, имеется ли у мышей с дефицитом MASP-1/3 дефицит функциональной активности лектинового пути (также обозначаемого как LEA-2), осуществляли анализ для измерения кинетики активности конвертазы C3 в плазме различных линий мышей с дефицитом комплемента, тестируемых в специфичных для активации лектинового пути условиях анализа (1% плазма), как описано в Schwaeble W. et al, PNAS vol 108(18):7523-7528 (2011), таким образом, включенной в настоящее описание в качестве ссылки.
Плазму мышей WT, C4-/-, MASP-1/3-/-; фактор B-/- и MASP-2-/- тестировали следующим образом.
Для измерения активации C3, планшеты для микротитрования покрывали маннозой (1 мкг/лунку), зимозаном (1 мкг/лунку) в буфере для сенсибилизации (15 мМ Na2CO3, 35 мМ NaHCO3) или иммунными комплексами, полученными in situ посредством покрывания 1% сывороточным альбумином человека (HSA) в буфере для сенсибилизации, а затем добавления сыворотки овцы против HAS (2 мкг/мл) в TBS (10 мМ Tris, 140 мМ NaCl, pH 7,4) с 0,05% Tween 20 и 5 мМ Ca++. Планшеты блокировали 0,1% HSA в TBS и три раза промывали TBS/Tween20/Ca++. Образцы плазмы разводили в 4 мМ барбитале, 145 мМ NaCl, 2 мМ CaCl2, 1 мМ MgCl2, pH 7,4, добавляли на планшеты и инкубировали в течение 1,5 часов при 37°C. После промывания связанный C3b определяли с использованием антител кролика против C3c человека (Dako), а затем конъюгированных с щелочной фосфатазой антител козла против IgG кролика и p-нитрофенилфосфата.
Результаты:
Кинетика активации C3 (измеряемого по накоплению C3b на покрытых маннозой планшетах с 1%> сывороткой) в специфичных для лектинового пути условиях представлена на фигуре 16. Не наблюдали расщепления C3 в плазме MASP-2-/-. В плазме фактор B-/-, C3 расщеплялся с половиной скорости, наблюдаемой для плазмы WT, вероятно, в результате утраты петли амплификации. Значительное замедление зависящей от лектинового пути конвертации C3 в C3b наблюдали в плазме C4-/- (T1/2=33 мин), а также в плазме при дефиците MASP-1/3-/- (T1/2=49 мин). Показано, что это замедление активации C3 в плазме MASP-1/3-/- является скорее MASP-1-, чем MASP-3-зависимым. (См. Takahashi M. et al, J Immunol 180:6132-6138 (2008)). Эти результаты свидетельствуют о том, у мышей с дефицитом MASP-1/3 нет дефицита функциональной активности лектинового пути (также обозначаемого как "LEA-2").
2. Эффект наследственного дефицита MASP-3 на активацию альтернативного пути
Обоснование:
Определяли эффект наследственного дефицита MASP-3 на активацию альтернативного пути, тестируя сыворотку пациента с дефицитом MASP-3 с синдромом 3MC, вызываемым мутацией со сдвигом рамки считывания в экзоне, кодирующем домен сериновой протеазы MASP-3. Синдром 3MC представляет собой объединяющий термин для перекрывающихся синдромов Carneavale, Mingarelli, Malpuech и Michels. Эти редкие аутосомно рецессивные нарушения проявляют спектр черт развития, включая характерную лицевую дизморфию, заячью губу и/или волчью пасть, краниосиностоз, неспособность к обучению и аномалии гениталий, конечностей и пузырно-лоханочные аномалии. Rooryck et al, Nature Genetics 43: 197-203 (2011) исследовали 11 семей с синдромом 3MC и идентифицировали два мутантных гена, COLEC11 и MASP-1. Мутации гена MASP-1 делают экзон, кодирующий домен сериновой протеазы MASP-3, но не экзоны, кодирующие домен сериновой протеазы MASP-1, нефункциональным. Таким образом, пациенты с 3MC с мутациями в экзоне, кодирующем домен сериновой протеазы MASP-3, имеют дефицит MASP-3, но достаточную MASP-1.
Способы:
Сыворотку при дефиците MASP-3 получали от пациента с 3MC, матери и отца пациента с 3MC (оба гетерозиготны по аллелю, содержащему мутацию, делающую экзон, кодирующий домен сериновой протеазы MASP-3, нефункциональным), а также от пациента с дефицитом C4 (дефектного по обоим генам C4 человека) и индивидуума с дефицитом MBL. Анализ альтернативного пути осуществляли в традиционных AP-специфичных условиях (BBS/ Mg++/EGTA, без Ca++, где BBS = физиологический раствор с барбиталовым буфером, содержащий сахарозу), как описано в Bitter-Suermann et al., Eur. J. Immunol 1 1:291-295 (1981)), на покрытых зимозаном планшетах для микротитрования с концентрациями сыворотки в диапазоне от 0,5 до 25% и измеряли накопление C3b с течением времени.
Результаты:
На фигуре 17 графически представлен уровень запускаемого альтернативным путем накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных от индивидуумов с дефицитом MASP-3, дефицитом C4 и дефицитом MBL. Как показано на фигуре 17, сыворотка пациента с дефицитом MASP-3 имела остаточную активность альтернативного пути (AP) при высоких концентрациях сыворотки (концентрации сыворотки 25%, 12,5%, 6,25%), но значимо более высокое AP50 (т.е. для достижения 50% максимального накопления C3 необходимо 9,8% сыворотки).
На фигуре 18 графически представлен уровень запускаемого альтернативным путем накопления C3b на покрытых зимозаном планшетах для микротитрования в "традиционных" специфичных для альтернативного пути (AP-специфичных) условиях (т.е. BBS/EGTA/Mg++ без Ca++) как функция времени в образцах 10% сыворотки человека, полученных от индивидуумов с дефицитом MASP-3, с дефицитом C4 и с дефицитом MBL.
В таблице 11 ниже обобщены результаты в отношении AP50, показанные на фигуре 17, и время полужизни для накопления C3b, показанное на фигуре 18.
Обобщенные результаты, представленные на фигурах 17 и 18
В целом, в условиях этих анализов у пациента с 3MC альтернативный путь значительно нарушен.
3. Измерение накопления C3b на маннозе, зимозане и S. pneumoniae D39 в сыворотках мыши с дефицитом MASP-2 или MASP-1/3
Способы:
Измеряли накопление C3b на покрытых маннозой, зимозаном и S. pneumoniae D39 планшетах для микротитрования с использованием концентраций сывороток мышей в диапазоне от 0% до 20%, полученных из мышей MASP-2-/-, MASP-1/3-/- и WT. Анализы накопления C3b осуществляли в "традиционных" специфичных для альтернативного пути условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (т.е. BBS/Mg++/Ca++).
Результаты:
На фигуре 19A графически представлен уровень накопления C3b на покрытых маннозой планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных из мышей WT, мышей с дефицитом MASP-2 и мышей с дефицитом MASP-1/3 в традиционных специфичных для альтернативного пути условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++). На фигуре 19B графически представлен уровень накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации в образцах сыворотки мышей WT, мышей с дефицитом MASP-2 и мышей с дефицитом MASP-1/3 в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++). На фигуре 19C графически представлен уровень накопления C3b на покрытых S. pneumoniae D39 планшетах для микротитрования как функция концентрации в образцах сыворотки мышей WT, мышей с дефицитом MASP-2 и мышей с дефицитом MASP-1/3 в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++).
На фигуре 20A графически представлены результаты анализа накопления C3b в сильно разведенных сыворотках, проведенного на покрытых маннозой планшетах для микротитрования в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), с использованием концентраций сыворотки в диапазоне от 0% до 1,25%. На фигуре 20B графически представлены результаты анализа накопления C3b, проведенного на покрытых зимозаном планшетах для микротитрования в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/EGTA/Mg++/Ca++), с использованием концентраций сыворотки в диапазоне от 0% до 1,25%. На фигуре 20C графически представлены результаты анализа накопления C3b, проведенного на покрытых S. pneumoniae D39 планшетах для микротитрования в традиционных AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/EGTA/Mg++/Ca++), с использованием концентраций сыворотки в диапазоне от 0% до 1,25%.
Как показано на фигурах 20A-C, анализы накопления C3b также осуществляли в традиционных специфичных для альтернативного пути условиях (т.е. BBS/EGTA/Mg++ без Ca++) или в физиологических условиях, позволяющих функционировать и лектиновому пути, и альтернативному пути (BBS/Mg++/Ca++), с использованием более высоких разведений в диапазоне от 0% до 1,25% сыворотки на покрытых маннозой планшетах (фигура 20A); на покрытых зимозаном планшетах (фигура 20B) и покрытых S. pneumoniae D39 планшетах (фигура 20C). Альтернативный путь истощается в более разведенных сыворотках, таким образом, активность, наблюдаемая в сыворотке индивидуума с дефицитом MASP-1/3 в присутствие Ca++, является опосредованной MASP-2 активностью LP, и активность, наблюдаемая в сыворотке индивидуума с дефицитом MASP-2 в присутствие Ca++, является опосредованной MASP-1/3 остаточной активацией AP.
Обсуждение:
Результаты, описываемые в этом примере, свидетельствуют о том, что ингибитор MASP-2 (или MASP-2 KO) обеспечивает значительную защиту от инфекции N. meningitidis посредством стимуляции запускаемой MASP-3 активации альтернативного пути. Результаты анализа бактериолизиса в сыворотке мыши и анализов бактериолизиса в сыворотке человека при мониторинге бактерицидной активности сыворотки в отношении N. meningitidis дополнительно свидетельствуют о том, что бактерицидная активность в отношении N. meningitidis отсутствует при дефиците MBL (в сыворотках мыши с двойным дефицитом MBL A и MBL C и человека с дефицитом MBL).
На фигуре 1 представлено новое понимание лектинового пути и альтернативного пути с учетом результатов, представленных в настоящем описании. На фигуре 1 изображена роль LEA-2 в опсонизации и лизисе. Хотя MASP-2 является инициатором "нижележащего в каскаде" накопления C3b (и последующей опсонизации) во многих лектин-зависимых физиологических условиях (фигура 20A, 20B, 20C), он также играет роль в лизисе серологически типируемых бактерий. Как показано на фигуре 1, предлагаемый молекулярный механизм, ответственный за повышенную бактерицидную активность сыворотки/плазмы при дефиците MASP-2 или MASP-2-обедненной сыворотки/плазмы в отношении серологически типируемых патогенов, таких как N. meningitidis, состоит в том, что в случае лизиса бактерий распознающие комплексы лектинового пути, ассоциированные с MASP-1 и MASP-3, связываются в непосредственной близости друг с другом на поверхности бактерий, таким образом, позволяя MASP-1 расщеплять MASP-3. В отличие от MASP-1 и MASP-2, MASP-3 не является аутоактивирующимся ферментом, но во многих случаях для конвертации в свою ферментативно активную форму ей необходима активация/расщепление MASP-1.
Как дополнительно показано на фигуре 1, затем активированная MASP-3 может расщеплять связавшийся с C3b фактор B на поверхности патогена для инициации каскада активации альтернативного пути посредством образования ферментативно активных конвертаз C3 и C5 альтернативного пути C3bBb и C3bBb(C3b)n, соответственно. Несущие MASP-2 активационные комплексы лектинового пути не участвуют в активации MASP-3, и в отсутствие MASP-2 или после истощения MASP-2 все активационные комплексы лектинового пути будут нагружены MASP-1 или MASP-3. Таким образом, в отсутствие MASP-2 значительно повышается вероятность того, что на поверхности микроорганизма несущие MASP-1 и MASP-3 активационные комплексы лектинового пути будут располагаться в непосредственной близости друг с другом, что приводит к повышению активации MASP-3 и, таким образом, более высокой скорости опосредованного MASP-3 расщепления связавшегося с C3b фактора B для образования конвертаз C3 и C5 альтернативного пути C3bBb и C3bBb(C3b)n на поверхности микроорганизма. Это приводит к активации терминальных каскадов активации C5b-C9, образующих мембраноатакующий комплекс, состоящий из связанного с поверхностью C5b, связанного с C6, C5bC6, связанного с C7, C5bC6C7, связанного с C8, и C5bC6C7C8, приводящего к полимеризации C9, встраивающегося в структуры поверхности бактерии и образующего поры в бактериальной стенке, что приводит к осмолитическому комплемент-зависимому уничтожению бактерии.
Основополагающей идеей этой новой концепции является то, что данные, представленные в настоящем описании, четко демонстрируют то, что активационные комплексы лектинового пути запускают два следующих различных пути активации, как показано на фигуре 1.
ПРИМЕР 5
В этом примере показан ингибиторный эффект дефицита MASP-2 и/или дефицита MASP-3 на лизис эритроцитов из образцов крови, полученных из модели пароксизмальной ночной гемоглобинурии (PNH) мыши.
Уровень техники/Обоснование:
Пароксизмальная ночная гемоглобинурия (PNH), также обозначаемая как синдром Маркиафавы-Микели, является острым, потенциально угрожающим жизни заболеванием крови, отличающимся индуцируемой комплементом внутрисосудистой гемолитической анемией. Отличительным признаком PNH является хронический опосредованный комплементом внутрисосудистый гемолиз, являющийся следствием нерегулируемой активации альтернативного пути комплемента по причине отсутствия регуляторов комплемента CD55 и CD59 на эритроцитах при PNH с последующей гемоглобинурией и анемией (Lindorfer, M.A., et al., Blood 775(11) (2010), Risitano, A.M, Mini-Reviews in Medicinal Chemistry, 11:528-535 (2011)). Анемия при PNH является результатом деструкции эритроцитов в кровотоке. Симптомы PNH включают красную мочу по причине присутствия гемоглобина в моче, боль в позвоночнике, слабость, одышку и тромбоз. PNH может развиваться самостоятельно, в этом случае ее обозначают как "первичную PNH", или в связи с другими нарушениями костного мозга, такими как апластическая анемия, в этом случае ее обозначают как "вторичную PNH". Лечение PNH включает переливание крови от анемии, антикоагулянты от тромбоза и использование моноклонального антитела экулизумаба (Soliris®), защищающего клетки крови от иммунологической деструкции посредством ингибирования системы комплемента (Hillmen P. et al., N. Engl. J. Med. J50(6):552-9 (2004)). Экулизумаб (Soliris®) является гуманизированным моноклональным антителом против компонента комплемента C5, блокирующим его расщепление конвертазами C5, таким образом, предотвращая продукцию C5a и сборку MAC. Лечение пациентов с PNH экулизумабом приводит к снижению внутрисосудистого гемолиза, измеряемого по лактатдегидрогеназе (LDH), что приводит к стабилизации гемоглобина и независимости от переливаний крови приблизительно у половины пациентов (Hillmen P, et al., Mini-Reviews in Medicinal Chemistry, vol 11(6) (2011)). Хотя почти все пациенты, подвергаемые терапии экулизумабом, достигают нормальных или почти нормальных уровней LDH (в результате контроля внутрисосудистого гемолиза), только приблизительно треть пациентов достигает уровня гемоглобина приблизительно 11 г/дл, и оставшиеся пациенты, подвергаемые терапии экулизумабом, продолжают испытывать анемию от умеренной до тяжелой (т.е. зависимую от переливаний крови) в приблизительно равных пропорциях (Risitano A.M. et al, Blood 113:4094-100 (2009)). Как описано в Risitano et al, Mini-Reviews in Medicinal Chemistry 11:528-535 (2011), показано, что пациенты с PNH, подвергаемые лечению экулизумабом, имели фрагменты C3, связанные со значительной частью их эритроцитов при PNH (в то время как пациенты, не подвергнутые лечению, - нет), что приводит к заключению о том, что мембраносвязанные фрагменты C3 действуют как опсонины на эритроцитах при PNH, что приводит к их захвату ретикулоэндотелиальными клетками через специфичные рецепторы C3 и последующему внесосудистому гемолизу. Таким образом, для тех пациентов, у которых развивается опосредованный фрагментами C3 внесосудистый гемолиз, необходимы терапевтические стратегии в дополнение к применению экулизумаба, т.к. они продолжают испытывать потребность в переливаниях эритроцитов.
В этом примере описывают способы оценки эффекта сыворотки при дефиците MASP-2 и MASP-3 в отношении лизиса эритроцитов из образцов крови, полученных из модели PNH мыши, и демонстрируют эффективность ингибирования MASP-2 и/или ингибирования MASP-3 в лечении индивидуумов, страдающих PNH, а также подтверждают применимость ингибиторов MASP-2 и/или ингибиторов MASP-3 (включая двойные или биспецифические ингибиторы MASP-2/MASP-3) для облегчения эффектов опосредованного фрагментами C3 внесосудистого гемолиза у индивидуумов с PNH, подвергаемых терапии ингибитором C5, таким как экулизумаб.
Способы:
Модель PNH на животных:
Образцы крови получали из генно-модифицированных мышей с дефицитами Crry и C3 (Crry/C3-/-) и мышей с дефицитами CD55/CD59. У этих мышей отсутствуют соответствующие поверхностные регуляторы комплемента на эритроцитах, и, таким образом, эти эритроциты склонны к спонтанному опосредованному комплементом аутолизису, как и эритроциты человека с PNH.
Для большей сенсибилизации этих эритроцитов эти клетки покрывали или не покрывали маннозой, а затем тестировали на гемолиз в плазме WT C56/BL6, плазме без MBL, плазме MASP-2-/-, плазме MASP-1/3-/-, NHS человека, плазме человека MBL-/- и NHS, обработанной антителом против MASP-2 человека.
1. Анализ гемолиза эритроцитов мыши с двойным дефицитом Crry/C3 и CD55/CD59 в сыворотках при дефиците MASP-2/MASP-2-обедненных сыворотках и контролях
День 1. Получение RBC мыши (± покрывание маннозой).
Материалы включали: свежую кровь мыши, BBS/Mg++/Ca++ (4,4 мМ барбитуровая кислота, 1,8 мМ барбитал натрия, 145 мМ NaCl, pH 7,4, 5 мМ Mg++, 5 мМ Ca++), хлорид хрома CrCl3·6H2O (0,5 мг/мл в BBS/Mg++/Ca++) и маннозу, 100 мкг/мл в BBS/Mg++/Ca++.
Цельную кровь (2 мл) центрифугировали в течение 1-2 мин при 2000 g на центрифуге с охлаждением при 4°C. Плазму и лейкотромбоцитарный слой отсасывали. Затем образец промывали 3 раза, ресуспендируя депозит RBC в 2 мл холодного буфера BBS/желатин/Mg++/Ca++ и повторяя этап центрифугирования. После третьего промывания депозит ресуспендировали в 4 мл BBS/Mg++/Ca++. Аликвоту 2 мл RBC оставляли в качестве непокрытого контроля. К оставшимся 2 мл добавляли 2 мл CrCl3 и 2 мл маннозы и инкубировали образец с осторожным перемешиванием при RT в течение 5 мин. Реакцию останавливали добавлением 7,5 мл буфера BBS/желатин/Mg++/Ca++. Образец центрифугировали, как указано выше, ресуспендировали в 2 мл буфера BBS/желатин/Mg++/Ca++ и промывали дополнительные два раза, как указано выше, затем хранили при 4°C.
День 2. Анализ гемолиза
Материалы включали BBS/желатин/Mg++/Ca (как указано выше), тестовые сыворотки, 96-луночные круглодонные и плоскодонные планшеты и спектрофотометр, считывающий 96-луночные планшеты при 410-414 нм.
Сначала определяли концентрацию RBC, доводили клетки до 109/мл и хранили в этой концентрации. Перед использованием клетки разводили в аналитическом буфере до 108/мл, а затем использовали 100 мкл на лунку. Гемолиз измеряли при длине волны 410-414 нм (делающей возможной большую чувствительность, чем 541 нм). Получали разведения тестовых сывороток в холодном буфере BBS/желатин/Mg++/Ca++. 100 мкл каждого разведения сыворотки пипетировали в круглодонном планшете. Добавляли 100 мкл соответствующим образом разведенного препарата RBC (т.е. 108/мл), инкубировали при 37°C в течение приблизительно 1 часа и анализировали на предмет лизиса (в этот момент времени планшеты можно фотографировать). Затем планшет центрифугировали при максимальной скорости в течение 5 минут. Отсасывали 100 мкл жидкой фазы, переносили в плоскодонные планшеты и регистрировали OD при 410-414 нм. Сохраняли депозиты RBC (затем их можно лизировать водой для получения обратного результата).
Эксперимент №1
Получали свежую кровь мышей с двойным дефицитом CD55/CD59 и кровь мышей с двойным дефицитом Crry/C3 и получали эритроциты, как подробно описано выше. Клетки разделяли, и половину клеток покрывали маннозой, а другую половину оставляли необработанной, доводя конечную концентрацию до 108/мл, 100 мкл которой использовали в анализе гемолиза, осуществляемом, как описано выше.
Результаты эксперимента №1: Лектиновый путь участвует в лизисе эритроцитов в модели PNH на животных
В первоначальном эксперименте определяли, что непокрытые эритроциты мыши WT не лизировались в любой сыворотке мыши. Кроме того, определяли, что покрытые маннозой эритроциты мыши Crry-/- лизировались медленно (более 3 часов при 37°C) в сыворотке мыши WT, но не лизировались в сыворотке без MBL (данные не представлены).
Определяли, что покрытые маннозой эритроциты мыши Crry-/- быстро лизировались в сыворотке человека, но не в термически инактивированной NHS. Важно, что покрытые маннозой эритроциты мыши Crry-/- лизировались в NHS, разведенной до 1/640 (т.е. все из разведений 1/40, 1/80, 1/160, 1/320 и 1/640 приводили к лизису) (данные не представлены). В этом разведении альтернативный путь не действовал (функциональная активность AP значительно снижалось при концентрации сыворотки ниже 8%).
Выводы из эксперимента №1
Покрытые маннозой эритроциты мыши Crry-/- хорошо лизировались в сильно разведенной сыворотке человека с MBL, но не в отсутствие MBL. Эффективный лизис при каждой тестируемой концентрации сыворотки позволяет предполагать, что альтернативный путь не участвует в этом лизисе или не является необходимым для него. Неспособность сыворотки мыши и сыворотки человека с дефицитом MBL лизировать покрытые маннозой эритроциты мыши Crry-/- свидетельствует о том, что классический путь также не участвует в наблюдаемом лизисе. Поскольку необходимы распознающие молекулы лектинового пути (т.е. MBL), этот лизис опосредован лектиновым путем.
Эксперимент №2
Получали свежую кровь из мышей с двойным дефицитом Crry/C3 и CD55/CD59 и анализировали покрытые маннозой эритроциты мыши Crry-/- с помощью анализа гемолиза, как описано выше, в присутствие следующих сывороток человека: MASP-3-/-; без MBL; WT; NHS, предварительно обработанной антителом против MASP-2 человека; и термически инактивированной NHS в качестве контроля.
Результаты эксперимента №2: Ингибиторы MASP-2 и дефицит MASP-3 предотвращают лизис эритроцитов в модели PNH на животных
С покрытыми маннозой эритроцитами мыши Crry-/- инкубировали NHS в разведениях до 1/640 (т.е. 1/40, 1/80, 1/160, 1/320 и 1/640), сыворотку человека MBL-/-, сыворотку человека при дефиците MASP-3 (от пациента с 3MC), NHS, предварительно обработанную mAb против MASP-2 и термически инактивированную NHS в качестве контроля.
Центрифугировали планшет для микротитрования для ELISA, и нелизированные эритроциты собирали на дне лунок круглодонного планшета. Собирали супернатант из каждой лунки и измеряли количество гемоглобина, высвобождаемого лизированными эритроцитами, посредством считывания OD при 415 нм на спектрофотометре для ELISA.
Наблюдали, что сыворотка MASP-3-/- совсем не лизировала покрытые маннозой эритроциты мыши. Как и ожидали, в контрольной термически инактивированной NHS (отрицательный контроль) лизис не наблюдали. Сыворотка человека MBL-/- лизировала покрытые маннозой эритроциты мыши в разведениях 1/8 и 1/16. NHS, предварительно обработанная антителом против MASP-2, лизировала покрытые маннозой эритроциты мыши в разведениях 1/8 и 1/16, в то время как сыворотка человека WT лизировала покрытые маннозой эритроциты мыши вплоть до разведения 1/32.
На фигуре 21 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши (Crry/C3-/-) в супернатант) покрытых маннозой эритроцитов мыши сывороткой человека в диапазоне разведений сыворотки в сыворотке MASP-3-/-, термически инактивированной (HI) NHS, MBL-/-, NHS, предварительно обработанной антителом против MASP-2, и контрольной NHS.
На фигуре 22 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши (Crry/C3-/-) в супернатант) покрытых маннозой эритроцитов мыши сывороткой человека в диапазоне концентраций сыворотки в сыворотке MASP-3-/-, термически инактивированной (HI) NHS, MBL-/-, NHS, предварительно обработанной антителом против MASP-2, и контрольной NHS.
С учетом результатов, представленных на фигурах 21 и 22, показано, что ингибирование MASP-3 будет предотвращать любой опосредованный комплементом лизис сенсибилизированных эритроцитов с недостаточной защитой от аутологичной активации комплемента. Ингибирование MASP-2 антителом против MASP-2 значимо смещало CH50 и являлось в некоторой степени протективным, но ингибирование MASP-3 являлось более эффективным.
Эксперимент №3
Непокрытые эритроциты мыши Crry-/-, полученные из свежей крови мышей с двойным дефицитом Crry/C3 и CD55/CD59, исследовали с помощью анализа гемолиза, как описано выше, в присутствие следующих сывороток: MASP-3-/-; MBL-/-; WT; NHS, предварительно обработанной антителом против MASP-2 человека, и термически инактивированной NHS в качестве контроля.
Результаты:
На фигуре 23 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши WT в супернатант) непокрытых эритроцитов мыши в диапазоне концентраций сыворотки в сыворотках человека от пациента с 3MC (MASP-3-/-), термически инактивированной (HI) NHS, MBL-/-, NHS, предварительно обработанной антителом против MASP-2, и контрольной NHS. Как показано на фигуре 23 и обобщено в таблице 12, показано, что ингибирование MASP-3 ингибирует опосредованный комплементом лизис несенсибилизированных эритроцитов мыши WT.
На фигуре 24 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами мыши (CD55/59-/-) в супернатант) непокрытых эритроцитов мыши сывороткой человека в диапазоне концентраций сыворотки в сыворотках человека термически инактивированной (HI) NHS, MBL-/-, NHS, предварительно обработанной антителом против MASP-2, и контрольной NHS. Как показано на фигуре 24 и обобщено в таблице 12, показано, что ингибирование MASP-2 являлось в ограниченной степени протективным.
Значения CH50, выраженные как концентрации сыворотки
В целом, результаты, представленные в этом примере, свидетельствуют о том, что ингибирование MASP-3 предотвращает любой опосредованный комплементом лизис сенсибилизированных и несенсибилизированных эритроцитов с недостаточной защитой от аутологичной активации комплемента. Ингибирование MASP-2 также в некоторой степени являлось протективным. Таким образом, ингибиторы MASP-2 и MASP-3 в отдельности или в комбинации (т.е. совместно вводимые, вводимые последовательно) или биспецифические или двойные ингибиторы MASP-2/MASP-3 можно использовать для лечения индивидуумов, страдающих PNH, а также их можно использовать для облегчения (т.е. ингибирования, профилактики или снижения тяжести) внесосудистого гемолиза у пациентов с PNH, подвергаемых лечению ингибитором C5, таким как экулизумаб (Soliris®).
ПРИМЕР 6
В этом примере описывают анализ гемолиза, в котором покрытые маннозой эритроциты кролика тестировали на лизис в присутствие сыворотки мыши WT или MASP-1/3-/-.
Способы:
1. Анализ гемолиза RBC кролика (покрытых маннозой) в сыворотках мыши с дефицитом MASP-1/3 и контрольных сыворотках WT
День 1. Получение RBC кролика.
Материалы включали: свежую кровь кролика, BBS/Mg++/Ca++ (4,4 мМ барбитуровая кислота, 1,8 мМ барбитал натрия, 145 мМ NaCl, pH 7,4, 5 мМ Mg++, 5 мМ Ca++), BBS/ Mg++/Ca++ с 0,1% желатином, хлорид хрома, содержащийся в буфере; т.е. CrCl3·6H2O (0,5 мг/мл в BBS/Mg++/Ca++) и маннозу, 100 мкг/мл в BBS/Mg++/Ca++.
1. Цельную кровь кролика (2 мл) разделяли по двум пробиркам Eppendorf емкостью 1,5 мл и центрифугировали в течение 3 минут при 8000 об/мин (приблизительно 5,9 rcf) на центрифуге Eppendorf с охлаждением при 4°C. Депозит RBC промывали три раза после ресуспендирования в холодном буфере BBS/Mg++/Ca++. После третьего промывания депозит ресуспендировали в 4 мл буфере BBS/Mg++/Ca++. Два мл этой аликвоты добавляли в пробирку Falcon емкостью 15 мл для использования в качестве непокрытого контроля. Оставшиеся 2 мл аликвоты RBC разводили в 2 мл буфера CrCl3, добавляли 2 мл раствора маннозы и инкубировали суспензию при комнатной температуре в течение 5 минут с осторожным перемешиванием. Реакцию останавливали добавлением в смесь 7,5 мл буфера BBS/0,1% желатин/Mg++/Ca++. Осаждали эритроциты и дважды промывали RBC буфером BBS/0,1% желатин/Mg++/Ca++, как описано выше. Суспензию RBC хранили в буфере BBS/0,1% желатин/Mg++/Ca++ при 4°C.
2. 100 мкл суспендированных RBC разводили 1,4 мл воды, центрифугировали при 8000 об/мин (приблизительно 5,9 rcf) в течение 3 минут и доводили OD супернатанта до 0,7 при 541 нм (OD 0,7 при 541 нм соответствует приблизительно 109 эритроцитов/мл).
3. Ресуспендированные RBC разводили буфером BBS/0,1% желатин/Mg++/Ca++ до концентрации 108/мл.
4. Разведения тестовых сывороток получали в холодном буфере BBS/желатин/Mg++/Ca++ и 100 мкл каждого разведения сыворотки пипетировали в соответствующей лунке круглодонного планшета. 100 мкл соответствующим образом разведенных RBC (108/мл) добавляли в каждую лунку. В качестве контроля полного лизиса очищенную воду (100 мкл) смешивали с разведенными RBC (100 мкл) для вызывания 100% лизиса, в то время как BBS/0,1% желатин/Mg++/Ca++ без сыворотки (100 мкл) использовали в качестве отрицательного контроля. Затем планшет инкубировали в течение 1 часа при 37°C.
5. Круглодонный планшет центрифугировали при 3250 об/мин в течение 5 минут. Супернатант из каждой лунки (100 мкл) переносили в соответствующие лунки плоскодонного планшета и регистрировали OD с помощью спектрофотометра для ELISA при 415-490 нм. Результаты представлены в виде соотношения OD при 415 нм и OD при 490 нм.
Результаты:
На фигуре 25 графически представлен гемолиз (измеряемый с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами кролика в супернатант) покрытых маннозой эритроцитов кролика сывороткой мыши в диапазоне концентраций сыворотки в сыворотке MASP-1/3-/- и контроля WT. Как представлено на фигуре 25, показано, что ингибирование MASP-3 предотвращает опосредованный комплементом лизис покрытых маннозой эритроцитов кролика WT. Эти результаты дополнительно подтверждают применимость ингибиторов MASP-3 в лечении одного или нескольких проявлений PNH, как описано в примере 5.
ПРИМЕР 7
В этом примере показано, что альтернативный путь активируется в сыворотке при дефиците фактора D в присутствие Ca++.
Эксперимент №1: Анализ накопления C3b в специфичных для альтернативного пути условиях
Способы:
Анализ накопления C3b на покрытом зимозаном планшете для микротитрования осуществляли в специфичных для альтернативного пути условиях (BBS/EGTA/Mg++, без Ca++) с использованием возрастающих разведений следующих сывороток мыши: фактор D-/-; MASP-2-/- и WT.
Результаты:
На фигуре 26 графически представлен уровень накопления C3b (OD при 405 нм) как функция концентрации в образцах сыворотки мыши с фактором D-/-, MASP-2-/- и WT в анализе накопления C3, проведенном в специфичных для альтернативного пути условиях. Как показано на фигуре 26, в этих условиях сыворотка мыши с фактором D-/- совсем не активирует C3, и альтернативный путь не функционирует. В сыворотке MASP-2-/- наблюдали активацию альтернативного пути со скоростью, подобной таковой для сыворотки WT. Эти результаты подтверждают, что в отсутствие Ca++ для накопления C3b необходим фактор D. Это согласуется с доказательством того, что в этих условиях MASP-3 не может конвертироваться в свою ферментативно активную форму, т.к. взаимодействия MASP-1, активирующего MASP-3 фермента, и MASP-3 с соответствующими распознающими углеводы компонентами является Ca++-зависимым.
Эксперимент №2: Анализ накопления C3b в физиологических условиях
Способы:
Анализ накопления C3b осуществляли в физиологических условиях (BBS/Ca++/Mg++) (позволяющих функционировать LP и AP) с использованием возрастающих разведений следующих сывороток мыши: фактор D-/-; MASP-2-/- и WT.
Результаты:
На фигуре 27 графически представлен уровень накопления C3b (OD при 405 нм) как функция концентрации в сыворотке с использованием образцов сывороток мыши с фактором D-/-; MASP-2-/- и WT в анализе накопления C3b, проведенном в физиологических условиях (в присутствие Ca++). Как показано на фигуре 27, сыворотка мыши с фактором D-/- активировала C3 лектиновым и альтернативным путем без различий при сравнении с сывороткой WT во всех указанных разведений сыворотки. В сыворотке MASP- -/- наблюдали циклическую активацию C3 в более низких разведениях сыворотки исключительно с помощью альтернативного пути (т.е. запускаемую MASP-3 активацию альтернативного пути). Эти результаты свидетельствуют о том, что в присутствие Ca++ фактор D не является необходимым при условии, что MASP-3 может запускать активность альтернативного пути.
Эксперимент №3: Анализ накопления C3b с использованием сывороток мыши с дефицитом фактора B или фактора D в присутствие или отсутствие mAb против MASP-2
Способы:
Анализ накопления C3b осуществляли в физиологических условиях (BBS/Ca++/Mg++) на покрытых маннозой планшетах для микротитрования следующим образом:
1. Планшеты для микротитрования для ELISA покрывали маннозой (1 мкг/мл) в буфере для сенсибилизации (15 мМ Na2CO3, 35 мМ NaHCO3, 0,02% азид натрия, pH 9,6) в течение ночи при 4°C.
2. На следующий день оставшиеся участки связывания белка блокировали в течение 2 часов при комнатной температуре 250 мкл/лунку 0,1% HSA в BBS (4 мМ барбитал, 145 мМ NaCl, 2 мМ CaCl2, 1 мМ MgCl2, pH 7,4).
3. Планшеты промывали три раза промывочным буфером (TBS с 0,05% Tween 20 и 5 мМ CaCl2).
4. Разведенные 1:10 образцы сыворотки в BBS добавляли в лунки в конкретные моменты времени. Лунки, содержащие только буфер, использовали в качестве отрицательных контролей. Планшет инкубировали при 37°C в течение до 40 минут.
5. Затем планшеты 3 раза промывали промывочным буфером.
6. Затем в лунки добавляли 100 мкл антител кролика против C3c человека (Dako), разведенных 1:5000 в промывочном буфере, и инкубировали планшеты в течение 90 минут при 37°C.
7. После трехкратного промывания промывочным буфером в лунки добавляли 100 мкл конъюгированных с щелочной фосфатазой антител против кролика, разведенных 1:5000 в промывочном буфере, с последующей инкубацией в течение 90 минут при комнатной температуре.
8. После промывания щелочную фосфатазу определяли добавлением 100 мкл раствора субстрата.
9. После инкубации в течение 15 минут измеряли оптическую плотность OD при 405 нм.
Результаты:
На фигуре 28 графически представлен уровень накопления C3b (OD при 405 нм) как функция времени инкубации сыворотки (в минутах) в образцах сыворотки мыши, полученных из мышей с фактором D-/- или фактором B-/-, в присутствие или отсутствие mAb против MASP-2 в анализе накопления C3b, проведенном в физиологических условиях (в присутствие Ca++). Как показано на фигуре 28, не наблюдали различий в количестве накопленного C3b в сыворотке WT и с фактором D-/-, что представляет убедительное доказательство вывода о том, что MASP-3 может инициировать активацию альтернативного пути, даже в отсутствие фактора D. Считают, что наблюдаемый сигнал является результатом активации лектинового пути и альтернативного пути. Как дополнительно показано на фигуре 28, в случае сыворотки c фактором D-/- с mAb против MASP-2 наблюдают только опосредованную MASP-3 активацию альтернативного пути. В случае сыворотки с фактором B-/- с mAb против MASP-2 наблюдали только фоновый сигнал (данные не представлены). Термически инактивированную сыворотку использовали в качестве контрольного фонового значения, идентичного фактору D-/- и фактору B-/- с MASP-2 (данные не представлены).
В целом, результаты, представленные в этом примере, свидетельствуют о том, что фактор D является необходимым только в нефизиологических условиях (т.е. при тестировании на активацию альтернативного пути в BBS/EGTA/Mg++ в отсутствие Ca++). В отличие от этого, при тестировании на активацию альтернативного пути в физиологических условиях (в присутствие Ca++), позволяющих альтернативному пути активироваться через MASP-3, в сыворотке с дефицитом фактора D не наблюдают дефицита активности альтернативного пути по сравнению с контролем WT. Таким образом, в физиологических условиях фактор D не нужен, т.к. инициация активации альтернативного пути запускается MASP-3. Эти результаты подтверждают вывод о том, что лектиновый путь регулирует активацию AP посредством MASP-3-зависимой активации
ПРИМЕР 8
В этом примере описывают примеры способов получения моноклональных антител мыши против полипептидов MASP-1, MASP-2 или MASP-3 человека и получения двойных, биспецифических или панспецифических антител против MASP.
1. Способы получения антител против MASP
Самцам мышей A/J (Harlan, Houston, Tex.) возрастом от 8 до 12 недель подкожно инъецировали 100 мкг полноразмерных полипептидов человека: rMASP-1 (SEQ ID NO: 10), rMASP-2 (SEQ ID NO: 5) или rMASP-3 (SEQ ID NO: 8), или их антигенных фрагментов, например, приведенных в таблице 2, в полном адъюванте Фрейнда (Difco Laboratories, Detroit, Mich.) в 200 мкл фосфатно-солевого буфера (PBS), pH 7,4. Через две недели мышам подкожно инъецировали 50 мкг того же полипептида человека в неполном адъюванте Фрейнда. На шестой неделе мышам инъецировали 50 мкг того же полипептида человека в PBS и через 4 дня осуществляли слияние.
Для каждого слияния получали суспензии отдельных клеток из селезенки иммунизированной мыши и использовали их для слияния с миеломными клетками Sp2/0. 5×108 Sp2/0 и 5×108 клеток селезенки подвергали слиянию в среде, содержащей 50% полиэтиленгликоля (M.W. 1450) (Kodak, Rochester, N.Y.) и 5% диметилсульфоксида (Sigma Chemical Co., St. Louis, Mo.). Затем клетки доводили до концентрации 1,5×105 клеток селезенки на 200 мкл суспензии в среде Iscove (Gibco, Grand Island, N.Y.), дополненной 10% эмбриональной телячьей сывороткой, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина, 0,1 мМ гипоксантином, 0,4 мкМ аминоптерином и 16 мкМ тимидином. Двести микролитров клеточной суспензии добавляли в каждую лунку приблизительно двадцати 96-луночных планшетов для микрокультивирования. Приблизительно через десять дней супернатанты культур отбирали для скрининга на реактивность в отношении очищенного антигена-мишени (MASP-1, MASP-2 или MASP-3, или антигенных фрагментов из таблицы 2) с помощью анализа ELISA.
Анализ ELISA (описываемый в отношении MASP-2): Лунки планшетов для микроанализа Immulon 2 (Dynatech Laboratories, Chantilly, Va.) покрывали добавлением 50 мкл очищенной hMASP-2 в концентрации 50 нг/мл в течение ночи при комнатной температуре. Для покрывания использовали низкую концентрацию MASP-2, что позволяет осуществлять селекцию высокоаффинных антител. После покрывания раствор удаляли стряхиванием планшета, в каждую лунку добавляли 200 мкл BLOTTO (нежирного сухого молока) в PBS на один час для блокирования неспецифичных участков. Затем через час лунки промывали буфером PBST (PBS, содержащим 0,05% Tween 20). Супернатанты культур из каждой лунки для слияния (50 мкл) смешивали с 50 мкл BLOTTO, а затем добавляли в отдельные покрытые MASP-2 лунки планшетов для микроанализа. Через один час инкубации лунки промывали PBST и определяли антитела, связывающиеся с MASP-2, добавляя конъюгированные с пероксидазой хрена (HRP) антитела козла против IgG мыши (Fc-специфичные) (Jackson ImmunoResearch Laboratories, West Grove, Pa.). Конъюгированные с HRP антитела против IgG мыши соответствующим образом разводили в BLOTTO для получения соответствующего соотношения сигнала и шума и добавляли в каждую лунку, содержащую образец. После промывания, связавшееся HRP-конъюгированное антитело определяли с использованием раствора субстрата пероксидазы. Раствор субстрата пероксидазы, содержащий 0,1% 3,3,5,5-тетраметилбензидина (Sigma, St. Louis, Mo.) и 0,0003% пероксида водорода (Sigma), добавляли в лунки для осуществления цветной реакции в течение 30 минут. Реакцию останавливали добавлением 50 мкл 2M H2SO4 на лунку и измеряли оптическую плотность реакционной смеси при 450 нм с использованием BioTek ELISA Reader (BioTek Instruments, Winooski, Vt.).
Анализ связывания (описываемый в отношении MASP-2):
Супернатанты культур, положительные при тестировании в анализе MASP-2 с помощью ELISA, описываемом выше, можно тестировать в анализе связывания для определения аффинности связывания, которую имеют средства, ингибирующие MASP-2, в отношении MASP-2. Аналогичный анализ также можно использовать для определения того, связываются ли ингибирующие средства с другими антигенами системы комплемента.
Лунки полистиролового планшета для микротитрования (96-луночного планшета для связывания среды, Corning Costar, Cambridge, MA) покрывали MASP-2 (20 нг/100 мкл/лунку, Advanced Research Technology, San Diego, CA) в фосфатно-солевом буфере (PBS), pH 7,4, в течение ночи при 4°C. После отсасывания раствора MASP-2 лунки блокировали PBS, содержащим 1% бычьего сывороточного альбумина (BSA; Sigma Chemical), в течение 2 часов при комнатной температуре. Лунки без MASP-2 служили в качестве фоновых контролей. В лунки добавляли аликвоты супернатантов гибридом или очищенные MoAb против MASP-2 в различных концентрациях в блокирующем растворе BSA PBS. После двух часов инкубации при комнатной температуре лунки интенсивно промывали PBS. Связавшиеся с MASP-2 MoAb против MASP-2 определяли добавлением конъюгированных с пероксидазой антител козла против IgG мыши (Sigma Chemical) в блокирующем растворе, которые инкубировали в течение 1 часа при комнатной температуре. Планшет снова тщательно промывали PBS и добавляли 100 мкл субстрата 3,3',5,5'-тетраметилбензидина (TMB) (Kirkegaard and Perry Laboratories, Gaithersburg, MD). Реакцию TMB подавляли добавлением 100 мкл 1M фосфорной кислоты и анализировали планшет при 450 нм с использованием спектрофотометра для чтения планшетов (SPECTRA MAX 250, Molecular Devices, Sunnyvale, CA).
Затем супернатанты культур из положительных лунок тестировали на способность ингибировать активацию комплемента в функциональном анализе, таком как анализ расщепления C4, как представлено в настоящем описании (пример 9). Затем клетки в положительных лунках клонировали с помощью предельного разведения. MoAb снова тестировали на реактивность в отношении hMASP-2 в анализе ELISA, как описано выше. Выбранные гибридомы выращивали в роллерных колбах, и обедненный супернатант культуры собирали для очистки антитела с помощью аффинной хроматографии с протеином A.
Антитела против MASP-2 можно анализировать на предмет ингибиторной активности в отношении LEA-2 в анализе расщепления C4, например, как описано в примере 9.
Хотя представленные выше ELISA и анализ связывания описывают в отношении MASP-2, специалистам в данной области следует понимать, что те же ELISA и анализы связывания можно осуществлять с использованием полипептидов MASP-1 или MASP-3 и их антигенных фрагментов (например, как описано в таблице 2). Антитела против MASP-3 можно анализировать на предмет ингибирования расщепления сериновой протеазой MASP-3 субстрата MASP-3 и на предмет ингибиторной активности в отношении LEA-1 в анализе накопления C3b, например, как описано в примере 4, в анализе гемолиза, как описано в примере 5. Антитела против MASP-1 можно анализировать на предмет ингибирования расщепления сериновой протеазой MASP-1 субстрата MASP-1, на предмет ингибирования активации MASP-3 и ингибиторной активности в отношении LEA-1 в анализе накопления C3b, например, как описано в примере 4, и в анализе гемолиза, как описано в примере 5.
2. Способы получения антител против MASP с двойной специфичностью
Двойные ингибиторные антитела против MASP-2/3: Как показано на фигурах 4, 6 и 7C, в домене сериновой протеазы, кодируемом бета-цепью SEQ ID NO: 5 и SEQ ID NO: 8, существуют области, консервативные для MASP-2 и MASP-3. Таким образом, антитело против MASP-2/3 с двойной специфичностью можно получать с использованием антигена, содержащего или состоящего из домена сериновой протеазы MASP-2 (или MASP-3), такого как бета-цепь SEQ ID NO: 5 (или SEQ ID NO: 8), для получения моноклонального антитела, как описано выше, или, альтернативно, этот антиген(-ы) можно использовать для скрининга фаговой библиотеки на предмет клонов, специфически связывающихся с этим антигеном(-ами), с последующим скринингом на предмет двойного связывания с MASP-3 (или MASP-1). Затем антитела против MASP-2/3 с двойной специфичностью подвергали скринингу на ингибиторную активность в функциональном анализе, например, как описано в таблице 2.
Двойные ингибиторные антитела против MASP-1/3: Как показано на фигурах 3-5, MASP-1 и MASP-3 имеют идентичную консервативную область в домене CUBI-CCP2 (а/к 25-432 в SEQ ID NO: 10), который также является общим для MAp44. Как показано на фигуре 3, MAp44 не содержит домен CCP2. Таким образом, антитело против MASP-1/3 с двойной специфичностью, включая MAp44, получали с использованием антигена, содержащего или состоящего из домена CUBI-CCP-2 MASP-1 (или MASP-3), для получения моноклонального антитела, как описано выше, или, альтернативно, этот антиген использовали для скрининга фаговой библиотеки на предмет клонов, специфически связывающихся с эти антигеном, с последующим скринингом на предмет двойного связывания с MASP-3 (или MASP-1). Антитело MASP-1/3 с двойной специфичностью, исключая MAp44, получали аналогичным способом с использованием антигена, содержащего или состоящего из домена CCP2 MASP-1 (или MASP-3). Затем антитела против MASP-1/3 с двойной специфичностью подвергали скринингу на ингибиторную активность в функциональном анализе, например, как описано в таблице 2.
Двойные ингибиторные антитела против MASP-1/2: Как показано на фигурах 4, 6 и 7A, домен сериновой протеазы MASP-1 и MASP-2 содержит области, являющиеся консервативными. Таким образом, антитело против MASP-1/2 с двойной специфичностью получали с использованием антигена, содержащего или состоящего из домена сериновой протеазы MASP-1 (или MASP-2), для получения моноклонального антитела, как описано выше, или, альтернативно, этот антиген использовали для скрининга фаговой библиотеки на предмет клонов, специфически связывающихся с этим антигеном, с последующим скринингом на предмет двойного связывания с MASP-2 (или MASP-1). Затем антитела против MASP-1/2 с двойной специфичностью подвергали скринингу на ингибиторную активность в функциональном анализе, например, как описано в таблице 2.
3. Способы получения панспецифических антител против MASP:
Альфа-цепь: Наличие нескольких участков идентичности MASP-2 и MASP-1/3 позволяет предполагать, что можно получать моноклональные антитела, связывающиеся с MASP-1/3 и MASP-2. В частности, большинство участков идентичности находится в доменах CUB1-EGF-CUB2, как показано на фигуре 5. Различные домены, представленные на фигуре 5, идентифицировали согласно Yongqing, et al, Biochemica et Biophysica Acta 1824:253-262 (2012); Teillet et al, J. Biol. Chem. 283:25715-25724 (2008); и Marchler-Bauer et al, Nucleic acids Res. 39:D225-229 (2011).
Бета-цепь: Наличие нескольких участков идентичности MASP-2 и MASP-1/3, как показано на фигуре 6, позволяет получать панспецифический ингибитор MASP-1/2/3.
Способы:
Панспецифические ингибиторные антитела против MASP (т.е. антитела, ингибирующие активность MASP-1, 2 и 3) получали следующим образом:
1. Скрининг библиотеки на домены CUB1-EGF-CUB2 альфа-цепи MASP-1/3 и MASP-2 и выбор клонов, перекрестно реагирующих и с MASP-1/3, и с MASP-2.
2. Скрининг клонов на способность ингибировать функциональную активность, например, как описано в таблице 2.
3. Использование технологии анализа аффинности/созревания функциональности DTLacO (Yabuki et al., PLoS ONE, 7(4):e36032 (2012)) для оптимизации связывания со всеми тремя белками и ингибиторной функции.
4. Как описано в таблице 2, панспецифические ингибиторы MASP можно использовать для ингибирования опосредованной LEA-1 и LEA-2 активации комплемента.
4. Способы получения биспецифических антител против MASP-2/3
Биспецифические ингибиторные антитела против MASP-2/3 получали следующим образом:
1. Идентифицировали примеры специфических ингибиторных антител против MASP-2, связывающихся с доменом CCP1 и ингибирующих MASP-2-зависимую активацию комплемента, как описано в примерах 11-14.
2. Специфическое ингибиторное антитело против MASP-3 получали скринингом библиотеки на полипептид MASP-3 и идентификацией антител против MASP-3, как описано в примере 15, с последующим анализом антител на ингибиторную активность в отношении LEA-1 в функциональном анализе, например, как описано в таблице 2. Примеры антител против MASP-3 описывают в примере 15.
3. Антигенсвязывающую область, специфическую для MASP-2 и MASP-3, клонировали в каркас для получения биспецифического антитела. Описано несколько форматов биспецифического антитела, включая иммуноглобулин G-подобные форматы, а также различные конфигурации слитых белков и одноцепочечных вариабельных фрагментов (Holmes, Nature Reviews, Drug Discovery 10:798-800 (2011), Muller and Kontermann, Biodrugs 24:89-98 (2010)). В одном примере биспецифические антитела можно получать, подвергая слиянию две гибридомы, экспрессирующие антитела против двух различных антигенов, что приводит к образованию пар различных тяжелых и легких цепей, часть которых содержит тяжелую и легкую цепь, специфичные для одного антигена, спаренные с тяжелой и легкой цепью, специфичными для другого антигена (Milstein и Cuello, Nature 305:537-539 (1983)). Аналогичное биспецифическое антитело можно получать рекомбинантно посредством коэкспрессии двух пар тяжелой цепи/легкой цепи иммуноглобулина, где две тяжелые цепи имеют разные специфичности. Вариабельные домены антитела с желаемой специфичностью связывания (комбинированные участки антитело-антиген) (например, антитела против MASP-2, как описано в примерах 11-14, антитела против MASP-3, как описано в примере 15) можно подвергать слиянию с последовательностями константного домена иммуноглобулина. Предпочтительно, осуществляют слияние с константным доменом тяжелой цепи иммуноглобулина, включая по меньшей мере часть из шарнирной области, областей CH2 и CH3. ДНК, кодирующую продукты слияния тяжелой цепи иммуноглобулина и, при желании, легкой цепи иммуноглобулина, встраивают в отдельные экспрессирующие векторы и котрансфицируют в подходящего организма-хозяина.
В дополнение к спаренным тяжелым и легким цепям иммуноглобулина, в Kipriyanov et al, J. Mol. Biol. 293:41 (1999)) приводят пример соединения одноцепочечных вариабельных фрагментов, специфичных для двух различных мишеней. В этом примере, одну полинуклеотидную экспрессирующую конструкцию конструируют кодирующей две пары вариабельных областей тяжелой и легкой цепи, разделенных линкерными пептидами, где каждая пара обеспечивает специфичность к отдельному белку-мишени. После экспрессии полипептид собирается в конфигурацию, в которой пары тяжелых и легких цепей, специфичных к одной из мишеней, образуют одну антигенсвязывающую поверхность белка, а другая пара образует отдельную антигенсвязывающую поверхность, в результате получают молекулу, называемую одноцепочечным диателом. В зависимости от длины линкера между центральными вариабельными областями пары тяжелой и легкой цепи, полипептид также можно заставлять димеризоваться, что приводит к образованию тандемного диатела.
Например, ДНК, кодирующую следующие иммуноглобулиновые полипептиды, можно встраивать в один или несколько векторов и экспрессировать в подходящем организме-хозяине для получения следующих иллюстративных, неограничивающих примеров биспецифических антител.
Биспецифические антитела против MASP-2/3
Один из вариантов осуществления относится к биспецифическому антителу, связывающемуся с MASP-2 человека и MASP-3 человека и содержащему:
(I) MASP-2-специфичную область связывания, содержащую по меньшей мере одно или несколько из следующего: a) вариабельную область тяжелой цепи, содержащую: i) CDR1 тяжелой цепи, содержащую аминокислотную последовательность 31-35 из SEQ ID NO: 21; и ii) CDR2 тяжелой цепи, содержащую аминокислотную последовательность 50-65 из SEQ ID NO: 21; и iii) CDR3 тяжелой цепи, содержащую аминокислотную последовательность 95-102 из SEQ ID NO: 21; и/или по меньшей мере одно или несколько из следующего: b) вариабельную область легкой цепи, содержащую: i) CDR1 легкой цепи, содержащую аминокислотную последовательность 24-34 из SEQ ID NO: 25 или SEQ ID NO: 27; и ii) CDR2 легкой цепи, содержащую аминокислотную последовательность 50-56 из SEQ ID NO: 25 или SEQ ID NO: 27; и iii) CDR3 легкой цепи, содержащую аминокислотную последовательность 89-97 из SEQ ID NO: 25 или SEQ ID NO: 27; и
(II) MASP-3-специфичную область связывания, необязательно, MASP-3-специфичную область связывания, содержащую по меньшей мере одну из a) вариабельной области тяжелой цепи, содержащей: i) CDR1 тяжелой цепи, содержащую аминокислотную последовательность 31-35 из SEQ ID NO: 25 или SEQ ID NO: 26; и ii) CDR2 тяжелой цепи, содержащую аминокислотную последовательность 50-65 из SEQ ID NO: 25 или SEQ ID NO: 26; и iii) CDR3 тяжелой цепи, содержащую аминокислотную последовательность 95-102 из SEQ ID NO: 25 или SEQ ID NO: 26; и
b) вариабельной области легкой цепи, содержащей: i) CDR1 легкой цепи, содержащей аминокислотную последовательность 24-34 из SEQ ID NO: 28 или SEQ ID NO: 29; и ii) CDR2 легкой цепи, содержащей аминокислотную последовательность 50-56 из SEQ ID NO: 28 или SEQ ID NO: 29; и iii) CDR3 легкой цепи, содержащей аминокислотную последовательность 89-97 из SEQ ID NO: 28 или SEQ ID NO: 29.
Биспецифические антитела против MASP-1/2
Один из вариантов осуществления относится к биспецифическому антителу, связывающемуся с MASP-1 человека и MASP-2 человека и содержащему:
(I) MASP-2-специфическую область связывания, содержащую по меньшей мере одно или несколько из следующего: a) вариабельную область тяжелой цепи, содержащую: i) CDR1 тяжелой цепи, содержащую аминокислотную последовательность 31-35 из SEQ ID NO: 21; и ii) CDR2 тяжелой цепи, содержащую аминокислотную последовательность 50-65 из SEQ ID NO: 21; и iii) CDR3 тяжелой цепи, содержащую аминокислотную последовательность 95-102 из SEQ ID NO: 21; и/или по меньшей мере одно или несколько из следующего: b) вариабельную область легкой цепи, содержащую: i) CDR1 легкой цепи, содержащую аминокислотную последовательность 24-34 из SEQ ID NO: 25 или SEQ ID NO: 27; и ii) CDR2 легкой цепи, содержащую аминокислотную последовательность 50-56 из SEQ ID NO: 25 или SEQ ID NO: 27; и iii) CDR3 легкой цепи, содержащую аминокислотную последовательность 89-97 из SEQ ID NO: 25 или SEQ ID NO: 27; и
(II) MASP-1-специфичную область связывания.
4. Тестирование на функциональную ингибиторную активность в отношении MASP-2 и/или MASP-3 проводили, например, как описано в таблице 2 и как дополнительно представлено в настоящем описании.
ПРИМЕР 9
В этом примере описывают анализ расщепления C4 in vitro, используемый в качестве функционального скрининга для идентификации средств, ингибирующих MASP-2, способных блокировать MASP-2-зависимую активацию комплемента через L-фиколин/P35, H-фиколин, M-фиколин или маннозу.
Анализ расщепления C4: В Petersen, S.V., et al, J. Immunol. Methods 257:107, 2001 описывают анализ расщепления C4, в котором измеряют активацию лектинового пути, являющуюся результатом воздействия липотейхоевой кислоты (LTA) на S. aureus, связывающейся с L-фиколином.
Реагенты: Фиксированные формалином S. aureus (DSM20233) получали следующим образом: бактерии выращивали в течение ночи при 37°C в триптической соевой среде с кровью, три раза промывали PBS, затем фиксировали в течение 1 часа при комнатной температуре в PBS/0,5% формалине и промывали еще три раза PBS перед ресуспендированием в буфере для сенсибилизации (15 мМ Na2CO3, 35 мМ NaHCO3, pH 9,6).
Анализ: Лунки планшета для микротитрования Nunc MaxiSorb (Nalgene Nunc International, Rochester, NY) покрывали: 100 мкл фиксированных формалином S. aureus DSM20233 (OD550=0,5) в буфере для сенсибилизации с 1 мкг L-фиколина в буфере для сенсибилизации. После инкубации в течение ночи лунки блокировали 0,1% сывороточным альбумином человека (HSA) в TBS (10 мМ Tris-HCl, 140 мМ NaCl, pH 7,4), затем промывали TBS, содержащим 0,05% Tween 20 и 5 мМ CaCl2 (промывочным буфером). Образцы сыворотки человека разводили в 20 мМ Tris-HCl, 1 M NaCl, 10 мМ CaCl2, 0,05% Triton X-100, 0,1% HSA, pH 7,4, предотвращающем активацию эндогенного C4 и вызывающем диссоциацию комплекса C1 (состоящего из C1q, C1r и C1s). Средства, ингибирующие MASP-2, включая MoAb против MASP-2, добавляли в образцы сыворотки в различных концентрациях. Разведенные образцы добавляли на планшет и инкубировали в течение ночи при 4°C. Через 24 часа планшеты тщательно промывали промывочным буфером, затем в каждую лунку добавляли 0,1 мкг очищенного C4 человека (полученного, как описано в Dodds, A.W., Methods Enzymol. 223:46, 1993) в 100 мкл 4 мМ барбитала, 145 мМ NaCl, 2 мМ CaCl2, 1 мМ MgCl2, pH 7,4. Через 1,5 часа при 37°C планшеты снова промывали и определяли накопление C4b с использованием конъюгированных с щелочной фосфатазой антител курицы против C4c человека (полученных в Immunsystem, Uppsala, Sweden) и измеряли с использованием субстрата п-нитрофенилфосфата для колориметрического анализа.
Анализ C4 с использованием маннозы: Описываемый выше анализ адаптировали для измерения активации лектинового пути через MBL, покрывая планшет LSP и маннозой перед добавлением сыворотки, смешанной с различными средствами, ингибирующими MASP-2.
Анализ C4 с использованием H-фиколина (Hakata Ag): Описываемый выше анализ адаптировали для измерения активации лектинового пути через H-фиколин, покрывая планшет LPS и H-фиколином перед добавлением сыворотки, смешанной с различными средствами, ингибирующими MASP-2.
ПРИМЕР 10
Следующий анализ использовали для тестирования того, блокирует ли средство, ингибирующее MASP, классический путь, с помощью анализа эффекта средства, ингибирующего MASP, в условиях, в которых классический путь инициируется иммунными комплексами.
Способы: Для тестирования эффекта средства, ингибирующего MASP, в условиях активации комплемента, когда классический путь инициируется иммунными комплексами, образцы по 50 мкл в трех параллелях, содержащие 90% NHS, инкубировали при 37°C в присутствие 10 мкг/мл иммунного комплекса или PBS, а также при инкубации при 37°C включали другие образцы в трех параллелях (+/- иммунные комплексы), содержащие 200 нМ моноклонального антитела против пропердина. После двух часов инкубации при 37°C во все образцы добавляли 13 мМ ЭДТА для остановки дальнейшей активации комплемента, и образцы незамедлительно охлаждали до 5°C. Затем образцы хранили при -70°C до анализа на продукты активации комплемента (C3a и sC5b-9) с использованием наборов для ELISA (Quidel, кат. №№ A015 и A009) по инструкциям производителя.
ПРИМЕР 11
В этом примере описывают идентификацию высокоаффинных Fab2-фрагментов антител против MASP-2, блокирующих активность MASP-2.
Уровень техники и обоснование: MASP-2 является сложным белком с множеством отдельных функциональных доменов, включая: участок(-и) связывания MBL и фиколинов, каталитический участок сериновой протеазы, участок связывания протеолитического субстрата C2, участок связывания протеолитического субстрата C4, участок расщепления MASP-2 для аутоактивации зимогена MASP-2 и два Ca++-связывающих участка. Идентифицировали Fab2-фрагменты антител, связывающиеся с MASP-2 с высокой аффинностью, и идентифицированные Fab2-фрагменты тестировали в функциональном анализе для определения того, способны ли они блокировать функциональную активность MASP-2.
Для блокирования функциональной активности MASP-2 антитело или Fab2-фрагмент антитела должен связаться и противодействовать структурному эпитопу на MASP-2, необходимому для функциональной активности MASP-2. Таким образом, многие или все из Fab2, связывающихся MASP-2 с высокой аффинностью, могут не ингибировать функциональную активность MASP-2, если они не связываются со структурными эпитопами на MASP-2, напрямую вовлеченными в функциональную активность MASP-2.
Функциональный анализ, в котором измеряли ингибирование образования конвертазы C3 лектинового пути, использовали для оценки "блокирующей активности" Fab2 против MASP-2. Известно, что первичной физиологической ролью MASP-2 в лектиновом пути является образование следующего функционального компонента опосредованного лектинами пути комплемента, а именно конвертазы C3 лектинового пути. Конвертаза C3 лектинового пути является критическим ферментативным комплексом (C4bC2a), протеолитически расщепляющим C3 на C3a и C3b. MASP-2 не является структурным компонентом конвертазы C3 лектинового пути (C4bC2a); однако функциональная активность MASP-2 необходима для получения двух белковых компонентов (C4b, C2a), образующих конвертазу C3 лектинового пути. Кроме того, по-видимому, все из отдельных функциональных активностей MASP-2, указанных выше, необходимы MASP-2 для образования конвертазы C3 лектинового пути. По этим причинам считают, что предпочтительным анализом для использования в оценке "блокирующей активности" Fab2 против MASP-2 является функциональный анализ, в котором измеряют ингибирование образования конвертазы C3 лектинового пути.
Получение высокоаффинных Fab2: Для получения высокоаффинных Fab2 против белка MASP-2 крысы (SEQ ID NO: 13) использовали библиотеку фагового дисплея последовательностей вариабельных областей легкой и тяжелой цепи антитела человека и технологию автоматизированной селекции антител для идентификации Fab2, реагирующих с выбранными интересующими лигандами. Для скрининга антител использовали известное количество белка MASP-2 крысы (~1 мг, >85% чистый). Для селекции антител с лучшей аффинностью использовали три раунда амплификации. Приблизительно 250 различных совпадений экспрессируемых фрагментов антител отбирали для скрининга с помощью ELISA. Затем высокоаффинные совпадения секвенировали для определения уникальности различных антител.
Очищали пятьдесят уникальных антител против MASP-2 и 250 мкг каждого очищенного Fab2 антитела использовали для характеризации аффинности связывания с MASP-2 и функционального тестирования пути комплемента, как подробно описано ниже.
Анализы, используемые для оценки ингибиторной (блокирующей) активности Fab2 против MASP-2
1. Анализ для измерения ингибирования образования конвертазы C3 лектинового пути:
Уровень техники: Конвертаза C3 лектинового пути является ферментативным комплексом (C4bC2a), протеолитически расщепляющим C3 на два активных провоспалительных фрагмента, анафилотоксина C3a и опсонического C3b. По-видимому, образование конвертазы C3 является ключевым этапом лектинового пути в отношении опосредования воспаления. MASP-2 не является структурным компонентом конвертазы C3 лектинового пути (C4bC2a); таким образом, антитела против MASP-2 (или Fab2) не будут напрямую ингибировать активность уже существующей конвертазы C3. Однако, активность сериновой протеазы MASP-2 необходима для получения двух белковых компонентов (C4b, C2a), образующих конвертазу C3 лектинового пути. Таким образом, Fab2 против MASP-2, ингибирующие функциональную активность MASP-2 (т.е. Fab2, блокирующие MASP-2), будут ингибировать образование de novo конвертазы C3 лектинового пути. C3 содержит необычную и высоко реактивную тиоэфирную группу как часть своей структуры. После расщепления C3 конвертазой C3 в этом анализе тиоэфирная группа на C3b может образовывать ковалентную связь с гидроксильной группой или аминогруппой на макромолекулах, иммобилизированных на дне пластиковых лунок через сложноэфирную или амидную связь, таким образом, облегчая определение C3b в анализе ELISA.
Манноза дрожжей является известным активатором лектинового пути. В следующем способе измерения образования конвертазы C3 пластиковые лунки, покрытые маннозой, инкубировали в течение 30 минут при 37°C с разведенной сывороткой крысы для активации лектинового пути. Затем лунки промывали и анализировали на предмет C3b, иммобилизированного в лунках, с использованием общепринятых способов ELISA. Количество C3b, образованного в этом анализе, является прямым отражением образования de novo конвертазы C3 лектинового пути. В этом анализе тестировали Fab2 против MASP-2 в выбранных концентрациях на их способность ингибировать образование конвертазы C3 и последующее образование C3b.
Способы:
96-луночные планшеты Costar Medium Binding инкубировали в течение ночи при 5°C с маннозой, разведенной в 50 мМ карбонатном буфере, pH 9,5, в концентрации 1 мкг/50 мкл/лунку. После инкубации в течение ночи каждую лунку три раза промывали 200 мкл PBS. Затем лунки блокировали 100 мкл/лунку 1% бычьего сывороточного альбумина в PBS и инкубировали в течение одного часа при комнатной температуре с осторожным перемешиванием. Затем каждую лунку три раза промывали 200 мкл PBS. Образцы Fab2 против MASP-2 разводили до выбранных концентраций в буфере GVB, содержащем Ca++ и Mg++ (4,0 мМ барбитал, 141 мМ NaCl, 1,0 мМ MgCl2, 2,0 мМ CaCl2, 0,1% желатин, pH 7,4) при 5°C. К указанным выше образцам добавляли 0,5% сыворотку крысы при 5°C и в каждую лунку переносили 100 мкл. Планшеты закрывали и инкубировали в течение 30 минут на водяной бане при 37°C, позволяя комплементу активироваться. Реакцию останавливали переносом планшетов с водяной бани при 37°C в контейнер, содержащий водно-ледяную смесь. Каждую лунку пять раз промывали 200 мкл PBS-Tween 20 (0,05% Tween 20 в PBS), затем два раза промывали 200 мкл PBS. 100 мкл/лунку разведения 1:10000 первичного антитела (антитела кролика против C3c человека, DAKO A0062) добавляли в PBS, содержащий 2,0 мг/мл бычьего сывороточного альбумина, и инкубировали в течение 1 часа при комнатной температуре с осторожным перемешиванием. Каждую лунку 5 раз промывали 200 мкл PBS. 100 мкл/лунку разведения 1:10000 вторичного антитела (конъюгированного с пероксидазой антитела козла против IgG кролика, American Qualex A102PU) добавляли в PBS, содержащий 2,0 мг/мл бычьего сывороточного альбумина, и инкубировали в течение одного часа при комнатной температуре на шейкере с осторожным перемешиванием. Каждую лунку пять раз промывали 200 мкл PBS. Добавляли 100 мкл/лунку субстрата пероксидазы TMB (Kirkegaard & Perry Laboratories) и инкубировали при комнатной температуре в течение 10 минут. Реакцию пероксидазы останавливали добавлением 100 Tl/лунку 1,0 M H3PO4 и измеряли OD при 450 нм.
2. Анализ для измерения ингибирования MASP-2-зависимого расщепления C4
Уровень техники: Активность сериновой протеазы MASP-2 является высокоспецифичной, и для MASP-2 идентифицировали только два белковых субстрата, C2 и C4. При расщеплении C4 образуются C4a и C4b. Fab2 против MASP-2 могут связываться со структурными эпитопами MASP-2, напрямую участвующими в расщеплении C4 (например, участком связывания MASP-2 с C4; каталитическим участком сериновой протеазы MASP-2), и, таким образом, ингибировать функциональную активность MASP-2 в отношении расщепления C4.
Манноза дрожжей является известным активатором лектинового пути. В следующем способе измерения активности MASP-2 в отношении расщепления C4 пластиковые лунки, покрытые маннозой, инкубировали в течение 30 минут при 37°C с разведенной сывороткой крысы для активации лектинового пути. Поскольку первичное антитело, используемое в этом анализе ELISA, распознает только C4 человека, разведенную сыворотку крысы также дополняли C4 человека (1,0 мкг/мл). Затем лунки промывали и анализировали на C4b человека, иммобилизированный в лунках, с использованием стандартных способов ELISA. Количество C4b, образующегося в этом анализе, является мерой активности MASP-2-зависимого расщепления C4. В этом анализе Fab2 против MASP-2 в выбранных концентрациях тестировали на способность ингибировать расщепление C4.
Способы: 96-луночные планшеты Costar Medium Binding инкубировали в течение ночи при 5°C с маннозой, разведенной в 50 мМ карбонатном буфере, pH 9,5, при концентрации 1,0 Tg/50 мкл/лунку. Каждую лунку 3 раза промывали 200 мкл PBS. Затем лунки блокировали 100 мкл/лунку 1% бычьего сывороточного альбумина в PBS и инкубировали в течение одного часа при комнатной температуре с осторожным перемешиванием. Каждую лунку 3 раза промывали 200 мкл PBS. Образцы Fab2 против MASP-2 разводили до выбранных концентраций в содержащем Ca++ и Mg++ буфере GVB (4,0 мМ барбитал, 141 мМ NaCl, 1,0 мМ MgCl2, 2,0 мМ CaCl2, 0,1% желатин, pH 7,4) при 5°C. В эти образцы также включали 1,0 мкг/мл C4 человека (Quidel). В указанные выше образцы добавляли 0,5% сыворотки крысы при 5°C и в каждую лунку переносили 100 мкл. Планшеты закрывали и инкубировали в течение 30 минут на водяной бане при 37°C, чтобы позволить комплементу активироваться. Реакцию останавливали переносом планшетов из водяной бани с температурой 37°C в контейнер, содержащий водно-ледяную смесь. Каждую лунку 5 раз промывали 200 мкл PBS-Tween 20 (0,05% Tween 20 в PBS), затем каждую лунку 2 раза промывали 200 мкл PBS. В PBS, содержащий 2,0 мг/мл бычьего сывороточного альбумина (BSA), добавляли 100 мкл/лунку разведения 1:700 конъюгированного с биотином антитела курицы против C4c человека (Immunsystem AB, Uppsala, Sweden) и инкубировали в течение одного часа при комнатной температуре с осторожным перемешиванием. Каждую лунку 5 раз промывали 200 мкл PBS. В PBS, содержащий 2,0 мг/мл BSA, добавляли 100 мкл/лунку 0,1 мкг/мл конъюгированного с пероксидазой стрептавидина (Pierce Chemical #21126) и инкубировали в течение одного часа при комнатной температуре на шейкере с осторожным перемешиванием. Каждую лунку 5 раз промывали 200 мкл PBS. Добавляли 100 мкл/лунку субстрата пероксидазы TMB (Kirkegaard & Perry Laboratories) и инкубировали при комнатной температуре в течение 16 мин. Реакцию пероксидазы останавливали добавлением 100 мкл/лунку 1,0 M H3PO4 и измеряли OD при 450 нм.
3. Анализ связывания Fab2 против MASP-2 крысы с "нативной" MASP-2 крысы
Уровень техники: Как правило, MASP-2 присутствует в плазме в виде комплекса димера MASP-2, также включающего специфичные лектиновые молекулы (маннозо-связывающий белок (MBL) и фиколины). Таким образом, при исследовании связывания Fab2 против MASP-2 с соответствующей физиологической формой MASP-2 важно разрабатывать анализ связывания, в котором используют взаимодействие между Fab2 и "нативной" MASP-2 в плазме, а не очищенной рекомбинантной MASP-2. В этом анализе связывания "нативный" комплекс MASP-2-MBL из 10% сыворотки крысы сначала иммобилизируют на покрытых маннозой лунках. Затем с использованием стандартных способов ELISA исследуют аффинность связывания различных Fab2 против MASP-2 с иммобилизированной "нативной" MASP-2.
Способы: 96-луночные планшеты Costar High Binding инкубировали в течение ночи при 5°C с маннозой, разведенной в 50 мМ карбонатном буфере, pH 9,5, в концентрации 1 мкг/50 мкл/лунку. Каждую лунку 3 раза промывали 200 мкл PBS. Лунки блокировали 100 мкл/лунку 0,5% нежирного сухого молока в PBST (PBS с 0,05% Tween 20) и инкубировали в течение одного часа при комнатной температуре с осторожным перемешиванием. Каждую лунку 3 раза промывали 200 мкл промывочного буфера TBS/Tween/Ca++ (Tris-забуференным физиологическим раствором, 0,05% Tween 20, содержащим 5,0 мМ CaCl2, pH 7,4). Получали 10% сыворотку крысы в высокосолевом буфере для связывания (20 мМ Tris, 1,0 M NaCl, 10 мМ CaCl2, 0,05% Triton-X100, 0,1% (масс./об.) бычий сывороточный альбумин, pH 7,4) на льду. Добавляли 100 мкл/лунку и инкубировали в течение ночи при 5°C. Лунки 3 раза промывали 200 мкл промывочного буфера TBS/Tween/Ca++. Затем лунки 2 раза промывали 200 мкл PBS. Добавляли 100 мкл/лунку Fab2 против MASP-2 выбранной концентрации, разведенного в содержащем Ca++ и Mg++ буфере GVB (4,0 мМ барбитал, 141 мМ NaCl, 1,0 мМ MgCl2, 2,0 мМ CaCl2, 0,1 % желатин, pH 7,4), и инкубировали в течение одного часа при комнатной температуре с осторожным перемешиванием. Каждую лунку 5 раз промывали 200 мкл PBS. Добавляли 100 мкл/лунку HRP-конъюгированного антитела козла против Fab2 (Biogenesis, кат. № 0500-0099), разведенного 1:5000 в 2,0 мг/мл бычьего сывороточного альбумина в PBS, и инкубировали в течение одного часа при комнатной температуре с осторожным перемешиванием. Каждую лунку 5 раз промывали 200 мкл PBS. Добавляли 100 мкл/лунку субстрата пероксидазы TMB (Kirkegaard & Perry Laboratories) и инкубировали при комнатной температуре в течение 70 минут. Реакцию пероксидазы останавливали добавлением 100 мкл/лунку 1,0 M H3PO4 и измеряли OD450.
РЕЗУЛЬТАТЫ:
Для скрининга с помощью ELISA выбирали приблизительно 250 различных Fab2, реагирующих с высокой аффинностью с белком MASP-2 крысы. Эти высокоаффинные Fab2 секвенировали для определения уникальности различных антител, и для дальнейшего анализа очищали 50 уникальных антител против MASP-2. 250 мкг каждого очищенного антитела Fab2 использовали для определения характеристик аффинности связывания с MASP-2 и функционального тестирования пути комплемента. Результаты этого анализа представлены в таблице 13 ниже.
FAB2 ПРОТИВ MASP-2, БЛОКИРУЮЩИЕ АКТИВАЦИЮ ЛЕКТИНОВОГО ПУТИ КОМПЛЕМЕНТА
IC50 (нM)
(нМ)
IC50 (нМ)
Как показано в таблице 13, из 50 тестируемых Fab2 против MASP-2, 17 идентифицировали как Fab2, блокирующие MASP-2, потенциально ингибирующие образование конвертазы C3 с IC50, равной или меньшей 10 нМ Fab2 (коэффициент положительных попаданий 34%). Восемь из 17 идентифицированных Fab2 имели IC50 в субнаномолярном диапазона. Кроме того, все семнадцать из Fab2, блокирующих MASP-2, представленных в таблице 13, демонстрировали по существу полное ингибирование образования конвертазы C3 в анализе конвертазы C3 лектинового пути. Это важно, т.к. теоретически возможно, что "блокирующие" Fab2 могут только частично ингибировать функцию MASP-2, даже если каждая молекула MASP-2 связывается Fab2.
Хотя манноза является известным активатором лектинового пути, теоретически возможно, что наличие антител против маннозы в сыворотке крысы также может активировать классический путь и приводить к образованию C3b с помощью конвертазы C3 классического пути. Однако каждое из семнадцати Fab2, блокирующих MASP-2, указанных в этом примере, потенциально ингибирует образование C3b (>95%), таким образом, это свидетельствует о специфичности этого анализа в отношении конвертазы C3 лектинового пути.
Также осуществляли анализы связывания со всеми семнадцатью блокирующими Fab2 для вычисления кажущейся Kd для каждого антитела. Результаты анализов связывания Fab2 против MASP-2 крысы с нативной MASP-2 крысы для шести из блокирующих Fab2 также представлены в таблице 13. Аналогичные анализы связывания также осуществляли для других Fab2, результаты каждого из них представлены в таблице 13. В основном, кажущаяся Kd, получаемая для связывания каждого из шести Fab2 с "нативной" MASP-2, достаточно хорошо соответствует IC50 для Fab2 в функциональном анализе конвертазы C3. Существует доказательство того, что MASP-2 подвергается конформационному изменению из "неактивной" в "активную" форму после активации ее протеазной активности (Feinberg et al, EMBO J 22:2348-59 (2003); Gal et al, J. Biol. Chem. 250:33435-44 (2005)). В нормальной плазме крысы, используемой в анализе образования конвертазы C3, MASP-2 присутствует, главным образом, в конформации "неактивного" зимогена. В отличие от этого, в анализе связывания MASP-2 присутствует в виде части комплекса с MBL, связанного с иммобилизированной маннозой; таким образом, MASP-2 будет находиться в "активной" конформации (Petersen et al, J. Immunol Способы 257:107-16, 2001). Таким образом, необязательно, можно было бы ожидать точного соответствия между IC50 и Kd для каждого из семнадцати блокирующих Fab2, тестируемых в этих двух функциональных анализах, т.к. в каждом анализе Fab2 будут связываться с различными конформационными формами MASP-2. Как бы то ни было, за исключением Fab2 #88, в этом случае, по-видимому, существует по существу близкое соответствие между IC50 и кажущейся Kd для каждого из других шестнадцати Fab2, тестируемых в двух анализах (см. таблицу 13).
Несколько из блокирующих Fab2 оценивали на ингибирование опосредованного MASP-2 расщепления C4. Как показано в таблице 13, обнаруживали, что все из тестируемых Fab2 ингибировали расщепление C4 с IC50, аналогичной для получаемой в анализе конвертазы C3.
Хотя манноза является известным активатором лектинового пути, теоретически возможно, что наличие антител против маннозы в сыворотке крысы также может активировать классический путь и, таким образом, приводить к образованию C4b через опосредованное C1s расщепление C4. Однако идентифицировали несколько Fab2 против MASP-2, потенциально ингибирующих образование C4b (>95%), таким образом, это свидетельствует о специфичности этого анализа в отношении опосредованного MASP-2 расщепления C4. C4, подобно C3, содержит необычную и высоко реактивную тиоэфирную группу как часть своей структуры. После расщепления C4 MASP-2 в этом анализе, тиоэфирная группа C4b может образовывать ковалентную связь с гидроксильной группой или аминогруппой макромолекул, иммобилизированных на дне пластиковых лунок, посредством сложноэфирных или амидных связей, таким образом, облегчая определение C4b в анализе ELISA.
Эти исследования четко демонстрируют образование высокоаффинных Fab2 против белка MASP-2 крысы, функционально блокирующих активность конвертаз C4 и C3, таким образом, предотвращающих активацию лектинового пути.
ПРИМЕР 12
В этом примере описывают картирование эпитопов для нескольких из блокирующих антител Fab2 против MASP-2 крысы, получаемых, как описано в примере 11.
Способы:
Следующие белки, все с N-концевыми 6-гистидиновыми метками, экспрессировали в клетках CHO с использованием вектора pED4:
MASP-2A крысы, полноразмерный белок MASP-2, инактивированный посредством замены серина в активном центре на аланин (S613A);
MASP-2K крысы, полноразмерный белок MASP-2, измененный для снижения аутоактивации (R424K);
CUBI-II, N-концевой фрагмент MASP-2 крысы, содержащий только домен CUBI, EGF-подобный домен и домен CUBII; и
CUBI/EGF-подобный, N-концевой фрагмент MASP-2 крысы, содержащий только домен CUBI и EGF-подобный домен.
Эти белки выделяли из супернатантов культур с помощью никель-аффинной хроматографии, как описывали ранее (Chen et al, J. Biol. Chem. 276:25894-02 (2001)).
C-концевой полипептид (CCPII-SP), содержащий CCPII и домен сериновой протеазы MASP-2 крысы, экспрессировали в E. coli в виде слитого белка с тиоредоксином с использованием pTrxFus (Invitrogen). Белок выделяли из лизатов клеток с использованием аффинной смолы Thiobond. Партнер для слияния тиоредоксин экспрессировали из пустого pTrxFus в качестве отрицательного контроля.
Все рекомбинантные белки диализировали в буфер TBS и определяли их концентрации, измеряя OD при 280 нм.
Дот-блот анализ:
Серийные разведения пяти рекомбинантных полипептидов MASP-2, описываемых выше (и полипептида тиоредоксин в качестве отрицательного контроля для полипептида CCPII-сериновая протеаза) наносили пятнами на нитроцеллюлозную мембрану. Количество нанесенного белка находилось в диапазоне от 100 нг до 6,4 пг с пятикратным шагом. В последних экспериментах количество нанесенного белка находилось в диапазоне от 50 нг до 16 пг так же с пятикратным шагом. Мембраны блокировали 5% обезжиренным сухим молоком в TBS (блокирующем буфере), затем инкубировали с 1,0 мкг/мл Fab2 против MASP-2 в блокирующем буфере (содержащем 5,0 мМ Ca++). Связанные Fab2 определяли с использованием HRP-конъюгированного антитела против Fab человека (AbD/Serotec; разведенного 1/10000) и набора для определения ECL (Amersham). Одну мембрану инкубировали с поликлональным Ab кролика против MASP-2 человека (описываемым в Stover et al., J Immunol 7(55:6848-59 (1999)) в качестве положительного контроля. В этом случае связавшиеся Ab определяли с использованием HRP-конъюгированного антитела козла против IgG кролика (Dako; разведенного 1/2000).
Анализ связывания MASP-2:
Планшеты для ELISA покрывали 1,0 мкг/лунку рекомбинантной MASP-2A или полипептида CUBI-II в карбонатном буфере (pH 9,0) в течение ночи при 4°C. Лунки блокировали 1% BSA в TBS, затем добавляли серийные разведения Fab2 против MASP-2 в TBS, содержащем 5,0 мМ Ca++. Планшеты инкубировали в течение одного часа при RT. После трехкратного промывания TBS/Tween/Ca++, добавляли HRP-конъюгированные антитела против Fab человека (AbD/Serotec), разведенные 1/10000 в TBS/Ca++, и инкубировали планшеты в течение еще одного часа при комнатной температуре. Связавшееся антитело определяли с использованием набора субстрата пероксидазы TMB (Biorad).
Результаты:
Результаты дот-блот анализа, демонстрирующие реактивность Fab2 в отношении различных полипептидов MASP-2, представлены в таблице 14 ниже. Числовыми значениями, представленными в таблице 14, указывают количество нанесенного белка, необходимое для достижения приблизительно полумаксимальной силы сигнала. Как показано, все полипептиды (за исключением партнера по слиянию тиоредоксина в отдельности) распознавались Ab положительного контроля (поликлональными антителами против MASP-2 человека в сыворотках, индуцированных у кроликов).
РЕАКТИВНОСТЬ В ОТНОШЕНИИ РАЗЛИЧНЫХ РЕКОМБИНАНТНЫХ ПОЛИПЕПТИДОВ MASP-2 КРЫСЫ ПРИ ДОТ-БЛОТ АНАЛИЗЕ
Все из Fab2 реагировали с MASP-2A, а также MASP-2K (данные не представлены). Большинство Fab2 распознавали полипептид CCPII-SP, но не N-концевые фрагменты. Двумя исключениями являлись Fab2 #60 и Fab2 #57. Fab2 #60 распознавало MASP-2A и фрагмент CUBI-II, но не полипептид с CUBI/EGF-подобным доменом или полипептид CCPII-SP, что позволяет предполагать, что оно связывается с эпитопом CUBII, или распространяется на CUBII и EGF-подобный домен. Fab2 #57 распознавало MASP-2A, но не какой-либо из тестируемых фрагментов MASP-2, возможно, это свидетельствует о том, что это Fab2 распознает эпитоп CCP1. Fab2 #40 и #49 связывались только с полной MASP-2A. В анализе связывания ELISA Fab2 #60 также связывалось с полипептидом CUBI-II, хотя и с немного меньшей кажущейся аффинностью (данные не представлены).
Эти результаты свидетельствуют об идентификации уникальных блокирующих Fab2 ко многим областям белка MASP-2.
ПРИМЕР 13
В этом примере описывают фармакодинамический анализ типичных высокоаффинных антител Fab2 против MASP-2, идентифицированных, как описано в примере 11.
Уровень техники/Обоснование:
Как описано в примере 11, для идентификации высокоаффинных антител, блокирующих лектиновый путь крысы, для пэннинга библиотеки фагового дисплея использовали белок MASP-2 крысы. Эту библиотеку конструировали для получения высокого иммунологического разнообразия и с использованием полностью человеческих последовательностей генов иммуноглобулинов. Как показано в примере 11, идентифицировали приблизительно 250 отдельных фаговых клонов, связывающихся с высокой аффинностью с белком MASP-2 крысы при скрининге с помощью ELISA. При секвенировании этих клонов идентифицировали 50 уникальных антител против кодирующих MASP-2 фагов. Белок Fab2 экспрессировали из этих клонов, очищали и анализировали на аффинность связывания с MASP-2 и функциональное ингибирование лектинового пути комплемента.
Как показано в таблице 13 примера 11, в результате этого анализа идентифицировали 17 Fab2 против MASP-2 с функциональной блокирующей активностью (коэффициент попаданий для блокирующих антител 34%). Функциональное ингибирование лектинового пути комплемента Fab2 являлось очевидным на уровне накопления C4, что является непосредственной мерой расщепления C4 MASP-2. Важно, что ингибирование являлось в равной степени очевидным при оценке активности конвертазы C3, что свидетельствует о функциональной блокаде лектинового пути комплемента. 17 Fab2, блокирующих MASP-2, идентифицированных, как описано в примере 11, потенциально ингибируют образование конвертазы C3 со значениями IC50, равными или меньшими 10 нМ. Восемь из 17 идентифицированных Fab2 имели значения IC50 в субнаномолярном диапазоне. Кроме того, все 17 из Fab2, блокирующих MASP-2, осуществляли по существу полное ингибирование образования конвертазы C3 в анализе конвертазы C3 лектинового пути, как приведено в таблице 13 примера 11. Кроме того, каждое из 17 Fab2, блокирующих MASP-2, представленных в таблице 13, потенциально ингибируют образование C3b (>95%), таким образом, это свидетельствует о специфичности этого анализа в отношении конвертазы C3 лектинового пути.
Из Fab2 #11 получали изотипические варианты полноразмерного антитела IgG2c крысы и IgG2a мыши. В этом примере описывают характеризацию in vivo этих изотипов в отношении фармакодинамических параметров.
Способы:
Как описано в примере 11, белок MASP-2 крысы использовали для пэннинга библиотеки фагового дисплея Fab, из которой идентифицировали Fab2 #11. Из Fab2 #11 получали изотипические варианты полноразмерного антитела IgG2c крысы и IgG2a мыши. Изотипические варианты полноразмерного антитела IgG2c крысы и IgG2a мыши охарактеризовывали in vivo в отношении фармакодинамических параметров следующим образом.
Исследование in vivo на мышах:
Для изучения эффекта дозы антитела против MASP-2 в отношении активности лектинового пути в плазме in vivo осуществляли фармакодинамическое исследование на мышах. В этом исследовании измеряли накопление C4 ex vivo в анализе лектинового пути в различные моменты времени после подкожного (sc) и интраперитонеального (ip) введения 0,3 мг/кг или 1,0 мг/кг MoAb мыши против MASP-2 (изотипического варианта полноразмерного антитела IgG2a мыши, полученного из Fab2 #11).
На фигуре 29A графически представлено специфичное для лектинового пути накопление C4b на покрытом зимозаном планшете для микротитрования, измеряемое ex vivo в образцах неразведенной сыворотки, взятых из мыши (n=3 мышей/группу) в различные моменты времени после подкожного введения 0,3 мг/кг или 1,0 мг/кг MoAb мыши против MASP-2. Образцы сыворотки мышей, собранные до введения антитела, служили в качестве отрицательного контроля (100% активности), в то время как сыворотку, дополненную in vitro 100 нМ того же блокирующего антитела против MASP-2, использовали в качестве положительного контроля (0% активность).
Результаты, представленные на фигуре 29A, свидетельствуют о быстром и полном ингибировании накопления C4b после подкожного введения дозы 1,0 мг/кг MoAb мыши против MASP-2. Наблюдали частичное ингибирование накопление C4b после подкожного введения дозы 0,3 мг/кг MoAb мыши против MASP-2.
За динамикой восстановления лектинового пути следили в течение трех недель после однократного i.p.-введения мышам MoAb мыши против MASP-2 в дозе 0,6 мг/кг. Как показано на фигуре 29B, резкое падение активности лектинового пути происходило после введения антитела с последующим полным ингибированием лектинового пути, длившимся в течение приблизительно 7 дней после i.p.-введения. Медленное восстановление активности лектинового пути наблюдали в течение второй и третьей недель с полным восстановлением лектинового пути у мышей через 17 дней после введения MoAb против MASP-2.
Эти результаты свидетельствуют о том, что MoAb мыши против MASP-2, полученное из Fab2 #11, ингибирует лектиновый путь мышей дозозависимым образом при систематическом введении.
ПРИМЕР 14
В этом примере описывают идентификацию полностью человеческих антител scFv, связывающихся с MASP-2 и ингибирующих опосредованную лектинами активацию комплемента (LEA-2), в то же время оставляющих классический (C1q-зависимый) путь компонент иммунной системы интактным, с использованием фагового дисплея.
Обзор:
С помощью скрининга библиотеки фагового дисплея идентифицировали полностью человеческие высокоаффинные антитела против MASP-2. Вариабельные фрагменты легкой и тяжелой цепи антител выделяли в формате scFv и в формате полноразмерного IgG. Антитела против MASP-2 человека применимы для ингибирования повреждения клеток, ассоциированного с опосредованной лектиновым путем активацией альтернативного пути комплемента, в то же время оставляющего классический (C1q-зависимый) путь компонента иммунной системы интактным. В некоторых вариантах осуществления заявленные ингибиторные антитела против MASP-2 имеют следующие характеристики: (a) высокую аффинность в отношении MASP-2 человека (например, KD 10 нМ или менее) и (b) ингибирование MASP-2-зависимой активности комплемента в 90% сыворотке человека с IC50 30 нМ или менее.
Способы:
Экспрессия полноразмерной каталитически неактивной MASP-2:
Полноразмерную последовательность кДНК MASP-2 человека (SEQ ID NO: 4), кодирующую полипептид MASP-2 человека с лидерной последовательностью (SEQ ID NO: 5), субклонировали в экспрессирующийся в млекопитающих вектор pCI-Neo (Promega), запускающий эукариотическую экспрессию под контролем энхансерной/промоторной области CMV (описанной в Kaufman R.J. et al, Nucleic acids Research 7:4485-90, 1991; Kaufman, Methods in Enzymology, 185:531-66 (1991)).
Для получения каталитически неактивного белка MASP-2A человека осуществляли сайт-специфический мутагенез, как описано в US2007/0172483, таким образом, включенном в настоящее описание в качестве ссылки. Продукты ПЦР очищали после электрофореза в агарозном геле и получения полосы и получали единичные перекрывания аденозина с использованием стандартного способа присоединения. Затем MASP-2A с аденозиновым хвостом клонировали в вектор pGEM-T easy и трансформировали в E. coli. MASP-2A человека дополнительно субклонировали в экспрессирующиеся в млекопитающих векторы pED или pCI-Neo.
Экспрессирующую MASP-2A конструкцию, описываемую выше, трансфицировали в клетки DXB1 с использованием стандартного способа трансфекции с фосфатом кальция (Maniatis et al., 1989). MASP-2A получали в среде без сыворотки для обеспечения того, чтобы препараты не были контаминированы другими белками сыворотки. Среды собирали из конфлюэнтных клеток каждый второй день (всего четыре раза). Уровень рекомбинантной MASP-2A в среднем составлял приблизительно 1,5 мг/литр среды для культивирования. MASP-2A (Ser-Ala мутант, описываемый выше) очищали с помощью аффинной хроматографии на MBP-A-агарозной колонке.
ELISA MASP-2A на предмет клонов-кандидатов ScFv, идентифицированных с помощью пэннинга/конвертации scFv, и фильтрующий скрининг
Библиотеку фагового дисплея последовательностей вариабельных областей легкой и тяжелой цепи иммуноглобулина человека подвергали пэннингу на антиген с последующим автоматизированным скринингом антитела и селекцией для идентификации высокоаффинных антител scFv против белка MASP-2 человека. Осуществляли три раунда пэннинга фаговой библиотеки scFv с использованием MASP-2A с гистидиновой или биотиновой меткой. В третьем раунде пэннинга сначала проводили элюирование с использованием MBL, и затем TEA (щелочь). Для контроля специфичного обогащения фагов, экспонирующих фрагменты scFv против мишени MASP-2A, осуществляли ELISA поликлональных фагов с использованием иммобилизированной MASP-2A. Гены scFv, определенные в третьем раунде пэннинга, клонировали в экспрессирующий вектор pHOG и исследовали в маломасштабном фильтрующем скрининге для обнаружения специфичных клонов против MASP-2A.
Собирали бактериальные колонии, содержащие плазмиды, кодирующие фрагменты scFv из третьего раунда пэннинга, отмечали координаты на нитроцеллюлозных мембранах и выращивали в течение ночи на неиндуцирующей среде для получения контрольных планшетов. Всего из третьего раунда пэннинга выбирали и анализировали 18000 колоний, половину при конкурентном элюировании и половину из последующего элюирования с TEA. При пэннинге фагмидной библиотеки scFv против MASP-2A с последующей конвертацией scFv и фильтрующим скринингом получали 137 положительных клонов. 108/137 клонов являлись положительными при анализе ELISA на связывание с MASP-2 (данные не представлены), из которых 45 клонов дополнительно анализировали на способность блокировать активность MASP-2 в нормальной сыворотке человека.
Анализ для измерения ингибирования образования конвертазы C3 лектинового пути
Для оценки "блокирующей активности" клонов-кандидатов scFv против MASP-2 использовали функциональный анализ, в котором измеряли ингибирование образование конвертазы C3 лектинового пути. Активность сериновой протеазы MASP-2 необходима для образования двух белковых компонентов (C4b, C2a), содержащих конвертазу C3 лектинового пути. Таким образом, MASP-2-ингибирующая функциональная активность scFv против MASP-2 (т.е. scFv, блокирующего MASP-2) будет ингибировать образование de novo конвертазы C3 лектинового пути. C3 содержит необычную и высокореактивную тиоэфирную группу как часть его структуры. В этом анализе после расщепления C3 конвертазой C3 тиоэфирная группа C3b может образовывать ковалентную связь с гидроксильной или аминогруппой макромолекул, иммобилизированных на дне пластиковых лунок посредством сложноэфирной или амидной связи, таким образом, облегчая определение C3b в анализе ELISA.
Манноза дрожжей является известным активатором лектинового пути. В следующем способе измерения образования конвертазы C3 пластиковые лунки, покрытые маннозой, инкубировали с разведенной сывороткой человека для активации лектинового пути. Затем лунки промывали и анализировали на C3b, иммобилизированный в лунках, с использованием стандартных способов ELISA. Количество C3b, образовавшегося в этом анализе, является прямым отражением образования de novo конвертазы C3 лектинового пути. В этом анализе клоны scFv против MASP-2 в выбранных концентрациях тестировали на их способность ингибировать образование конвертазы C3 и последующее образование C3b.
Способы:
45 клонов-кандидатов, идентифицированных, как описано выше, экспрессировали, очищали и разводили до одинаковой стоковой концентрации, затем опять разводили содержащим Ca++ и Mg++ буфером GVB (4,0 мМ барбитал, 141 мМ NaCl, 1,0 мМ MgCl2, 2,0 мМ CaCl2, 0,1% желатин, pH 7,4) для обеспечения того, что растворы всех клонов содержали одинаковое количество буфера. Каждый из клонов scFv тестировали в трех параллелях в концентрации 2 мкг/мл. Положительным контролем являлось Fab2 OMS100, и его тестировали в концентрации 0,4 мкг/мл. Образование C3c контролировали в присутствие и отсутствие клонов scFv/IgG.
Маннозу разводили до концентрации 20 мкг/мл (1 мкг/лунку) в 50 мМ карбонатном буфере (15 мМ Na2CO3 + 35 мМ NaHCO3 + 1,5 мМ NaN3), pH 9,5, и покрывали ею планшет для ELISA в течение ночи при 4°C. На следующий день покрытые маннозой планшеты 3 раза промывали 200 мкл PBS. Затем в лунки добавляли 100 мкл блокирующего раствора 1% HSA и инкубировали в течение 1 часа при комнатной температуре. Планшеты 3 раза промывали 200 мкл PBS и хранили на льду с 200 мкл PBS до добавления образцов.
Нормальную сыворотку человека разводили до 0,5% в буфере CaMgGVB, и в этот буфер добавляли клоны scFv или Fab2 OMS100 положительного контроля в трех параллелях в концентрации 0,01 мкг/мл; 1 мкг/мл (только для контроля OMS100) и 10 мкг/мл и преинкубировали в течение 45 минут на льду до добавления на блокированный планшет для ELISA. Реакцию инициировали инкубацией в течение одного часа при 37°C и останавливали переносом планшетов на лед. Накопление C3b определяли с использованием антитела кролика против C3c α-мыши, а затем HRP-конъюгированного антитела козла против α-кролика. Отрицательным контролем являлся буфер без антитела (отсутствие антитела = максимальное накопление C3b), а положительным контролем являлся буфер с ЭДТА (без накопления C3b). Фоновое значение определяли, осуществляя тот же анализ, за исключением того, что лунки не содержали маннозу. Фоновый сигнал для планшетов без маннозы вычитали из сигналов для лунок, содержащих маннозу. Устанавливали пороговый критерий половины активности неродственного клона scFv (VZV) и буфера в отдельности.
Результаты: Учитывая пороговый критерий, обнаруживали всего 13 клонов, блокирующих активность MASP-2. Выбирали все 13 клона, вызывающих >50% супрессии пути, и секвенировали их, получая 10 уникальных клонов. Обнаруживали, что все десять клонов содержат один и тот же подкласс легкой цепи, λ3, но три различных подкласса тяжелой цепи: VH2, VH3 и VH6. В функциональном анализе пять из десяти клонов-кандидатов scFv имели наномолярные значения IC50 менее целевого критерия 25 нМ при использовании 0,5% сыворотки человека.
Для идентификации антител с улучшенной активностью три родительских клона scFv, идентифицированных, как описано выше, подвергали перестановке легких цепей. Этот способ включает получение комбинаторной библиотеки, состоящей из VH, каждая из которых происходит из родительских клонов, спаренной с библиотекой наивных, легких лямбда-цепей человека (VL), полученных из шести здоровых доноров. Затем эту библиотеку подвергали скринингу на клоны scFv с улучшенной аффинностью связывания и/или функциональностью.
Сравнение функциональной активности IC50 (нМ) лидерных дочерних клонов и соответствующих им родительских клонов (все в формате dcFv)
(IC50 нМ)
(IC50 nM)
Ниже представлены последовательности вариабельной области тяжелой цепи (VH) родительских клонов и дочерних клонов, приведенных в таблице 15 выше и таблицах 16A-F ниже.
CDR по Kabat (31-35 (H1), 50-65 (H2) и 95-102 (H3)) указаны жирным шрифтом; и CDR по Chothia (26-32 (H1), 52-56 (H2) и 95-101 (H3)) подчеркнуты.
Вариабельная область тяжелой цепи (VH) 17D20_35VH-21N11VL (SEQ ID NO: 15, кодируемая SEQ ID NO: 14)
QVTLKESGPVLVKPTETLTLTCTVSGFSLSRGKMGVSWIRQPPGKALEWLAHIFSSDEKSYRTSLKSRLTISKDTSKNQVVLTMTNMDPVDTATYYCARIRRGGIDYWGQGTLVTVSS
Вариабельная область тяжелой цепи (VH) d17N9 (SEQ ID NO: 16)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSTSА/КWNWIRQSPSRGLEWLGRTYYRSKWYNDYAVSVKSRITINPDTSKNQFSLQLNSVTPEDTAVYYCARDPFGVPFDIWGQGTMVTVSS
Тяжелая цепь (а/к 1-20)
(SEQ:15)
(SEQ:16)
Тяжелая цепь (а/к 21-40)
(SEQ:15)
(SEQ:16)
Тяжелая цепь (а/к 41-60)
(SEQ:15)
(SEQ:16)
Тяжелая цепь (а/к 61-80)
(SEQ:15)
(SEQ:16)
Тяжелая цепь (а/к 81-100)
(SEQ:15)
(SEQ:16)
тяжелая цепь (а/к 101-118)
(SEQ:15)
(SEQ:16)
Ниже представлены последовательности вариабельной области легкой цепи (VL) родительских клонов и дочерних клонов, приведенных ниже в таблицах 17A-F.
CDR по Kabat (24-34 (L1); 50-56 (L2) и 89-97 (L3)) указаны жирным шрифтом; и CDR по Chothia (24-34 (L1); 50-56 (L2) и 89-97 (L3) подчеркнуты. Эти области являются одинаковыми при нумерации по системам Kabat или Chothia.
Вариабельная область легкой цепи (VL) 17D20m_d3521N11 (SEQ ID NO: 17)
QPVLTQPPSLSVSPGQTASITCSGEKLGDKYAYWYQQKPGQSPVLVMYQDKQRPSGIPERFSGSNSGNTATLTISGTQAMDEADYYCQAWDSSTAVFGGGTKLTVL
Вариабельная область легкой цепи (VL) 17N16m_d17N9 (SEQ ID NO: 19, кодируемая SEQ ID NO: 18)
SYELIQPPSVSVAPGQTATITCAGDNLGKKRVHWYQQRPGQAPVLVIYDDSDRPSGI PDRFSASNSGNTATLTITRGEAGDEADYYCQVWDIATDHVVFGGGTKLTVLА/КAGSEQKLISE
Легкая цепь (а/к 1-20)
(SEQ:17)
(SEQ:19)
Легкая цепь (а/к 21-40)
(SEQ:17)
(SEQ:19)
Легкая цепь (а/к 41-60)
(SEQ:17)
(SEQ:19)
Легкая цепь (а/к 61-80)
(SEQ:17)
(SEQ:19)
Легкая цепь (а/к 81-100)
(SEQ:17)
(SEQ:19)
Легкая цепь (а/к 101-120)
(SEQ:17)
(SEQ:19)
Антитела против MASP-2 OMS100 и MoAb_d3521N11VL, которые, как показано, связываются с MASP-2 человека с высокой аффинностью и имеют способность блокировать функциональную активность комплемента, анализировали с помощью дот-блот анализа на предмет связывания с эпитопом. Результаты показали, что антитела d3521N11 и OMS100 являются высокоспецифичными в отношении MASP-2 и не связываются с MASP-1/3. Ни одно антитело не связывалось с MAp19 или фрагментами MASP-2, не содержащими домен CCP1 MASP-2, что приводит к выводу о том, что участки связывания включают CCP1.
Таким образом, в одном из вариантов осуществления средство, ингибирующее MASP-2, для применения в композициях и способах по описываемому в заявке изобретению содержит антитело человека, связывающееся с полипептидом, состоящим из MASP-2 человека (SEQ ID NO: 3), где антитело содержит:
I) a) вариабельную область тяжелой цепи, содержащую: i) CDR1 тяжелой цепи, содержащую аминокислотную последовательность 31-35 из SEQ ID NO: 21; и ii) CDR2 тяжелой цепи, содержащую аминокислотную последовательность 50-65 из SEQ ID NO: 21; и iii) CDR3 тяжелой цепи, содержащую аминокислотную последовательность 95-102 из SEQ ID NO: 21; и
b) вариабельную область легкой цепи, содержащую: i) CDR1 легкой цепи, содержащую аминокислотную последовательность 24-34 из SEQ ID NO: 25 или SEQ ID NO: 27; и ii) CDR2 легкой цепи, содержащую аминокислотную последовательность 50-56 из SEQ ID NO: 25 или SEQ ID NO: 27; и iii) CDR3 легкой цепи, содержащую аминокислотную последовательность 89-97 из SEQ ID NO: 25 или SEQ ID NO: 27; или II) их вариант, в ином случае идентичный указанным вариабельным доменам, за исключением всего до 6 замен аминокислот в указанных областях CDR указанной вариабельной области тяжелой цепи и всего до 6 замен аминокислот в указанных областях CDR указанной вариабельной области легкой цепи, где антитело или его вариант ингибирует MASP-2-зависимую активацию комплемента.
ПРИМЕР 15
В этом примере описывают получение моноклональных антител против MASP-1 и MASP-3 с использованием системы in vitro, содержащей модифицированную клеточную линию DT40, DTLacO.
Уровень техники/Обоснование:
Антитела против MASP-1 и MASP-3 человека получали с использованием системы in vitro, содержащей модифицированную клеточную линию DT40, DTLacO, делающую возможной обратную индукцию диверсификации конкретного полипептида, как дополнительно описывают в WO 2009029315 и US 2010093033. DT40 является B-клеточной линией курицы, о которой известно, что в культуре клеток гены тяжелой и легкой цепи иммуноглобулина (Ig) конститутивно мутируют. Как и у других B-клеток, этот конститутивный мутагенез направлен на мутации V-области генов Ig и, таким образом, CDR экспрессируемых молекул антител. Конститутивный мутагенез в клетках DT40 происходит посредством конверсии генов с использованием в качестве донорных последовательностей набора нефункциональных сегментов V-гена (V-псевдогенов; ψV), находящихся выше каждой функциональной V-области). Ранее показано, что делеция области вызывает переключение механизма диверсификации с конверсии генов на соматическую гипермутацию, механизм, как правило, наблюдаемый в B-клетках человека. Показано, что линия B-клеточной лимфомы курицы DT40 является многообещающей стартовой точкой для разработки антител ex vivo (Cumbers, S.J. et al. Nat 20 Biotechnol 1129-1134 (2002); Seo, H. et al. Nat Biotechnol 23, 731-735 (2005)). Клетки DT40 активно пролиферируют в культуре со временем удвоения 8-10 часов (по сравнению с 20-24 часами для линий B-клеток человека), и они поддерживают очень эффективное воздействие на гомологичные гены (Buerstedde, J.M. et al. Embo J 9, 921-927 (1990)). Клетки DT40 имеют огромное потенциальное разнообразие последовательностей V-области при условии, что им доступны два различных физиологических пути диверсификации, конверсия генов и соматическая гипермутация, приводящие к матричным и нематричным мутациям, соответственно (Maizels, N. Annu Rev Genet 39, 23-46 (2005)). Диверсифицированные тяжелые и легкие цепи иммуноглобулинов (Ig) экспрессируются в форме IgM, экспонированных на поверхности клеток. Поверхностные IgM имеют бивалентную форму, структурно аналогичную молекуле IgG. Клетки, экспонирующие IgM со специфичностью к конкретному антигену, можно выделять посредством связывания с иммобилизированным растворимым вариантом антигена или вариантом антигена, экспонированным на мембране. Однако применимость клеток DT40 для разработки антитела на практике ограничена т.к., как и в других трансформированных B-клеточных линиях, диверсификация происходит при скорости, составляющей менее 1% от физиологической.
В системе, используемой в этом примере, как описано в WO 2009029315 и US 2010093033, конструировали клетки DT40 для ускорения диверсификации генов Ig без утраты возможности дальнейшей генетической модификации или потенциала конверсии генов и соматической гипермутации для участия в мутагенезе. Осуществляли две ключевые модификации DT40 для повышения скорости диверсификации и, таким образом, комплексности специфичности связывания в полученной библиотеке клеток. Во-первых, диверсификацию генов Ig помещали под контроль мощной регуляторной сети лактозного оператора/репрессора E. coli. Мультимеры, состоящие из приблизительно 100 полимеризованных повторов мощного лактозного оператора E. coli (PolyLacO), встраивали выше перестраивающихся и экспрессирующихся генов Igλ и IgH посредством воздействия на гомологичные гены. Затем регуляторные факторы, слитые с лактозным репрессорным белком (LacI), можно соединять с регуляторными элементами LacO для регуляции диверсификации, используя преимущество высокой аффинности (kD=10-14 M) ДНК лактозного репрессора к оператору. Клетки DT40 PolyLacO-λR, в которых PolyLacO интегрируется только в Igλ, проявляют 5-кратное повышении скорости диверсификация генов Ig относительно родительских клеток DT40 до любого конструирования (Cummings, W.J. et al. PLoS Biol 5, e246 (2007)). Диверсификация также может повышаться в клетках, сконструированных несущими PolyLacO, направленный и на гены Igλ, и на гены IgH ("DTLacO"). Показано, что клетки DTLacO имеют скорости диверсификации в 2,5-9,2 раз выше относительно 2,8%, характерной для родительской линии DT40 PolyLacO-λR LacI-HP1. Таким образом, воздействие элементов PolyLacO на гены и тяжелой, и легкой цепи ускоряло диверсификацию в 21,7 раз относительно родительской клеточной линии DT40. Присоединение регуляторных факторов к локусам Ig не только повышает частоту мутагенеза, но также может изменять путь мутагенеза, приводя к образованию большей коллекции уникальных изменений последовательности (Cummings et al. 2007; Cummings et al. 2008). Во-вторых, получали разнообразную коллекцию стартовых точек последовательности для диверсификации генов Ig, ускоренной присоединением фактора. Эти разнообразные стартовые точки последовательности добавляли в DTLacO посредством воздействия на перестроенные вариабельные области тяжелой цепи Ig, выделенные из курицы возрастом два месяца, в локусе тяжелой цепи. Добавление этих вариабельных областей тяжелой цепи приводило к получению репертуара 107 новых стартовых точек диверсификации антитела. Создание эти новых стартовых точек в клеточной линии DTLacO делает возможной идентификацию клонов, связывающихся с конкретной мишенью, а затем осуществление быстрого созревания аффинности с помощью присоединенных факторов. После созревания аффинности полноразмерный рекомбинантный химерный IgG получают клонированием созревших, перестроенных вариабельных последовательностей тяжелой и легкой цепи (VH и Vλ; состоящих из каркасных областей и определяющих комплементарность областей или CDR курицы) в экспрессирующие векторы, содержащие константные области IgG1 и лямбда-цепи человека. Эти рекомбинантные mAb подходят для применения in vitro и in vivo, и они служат в качестве стартовой точки для гуманизации.
Способы:
Селекция по связыванию с антигенами MASP-1 и MASP-3
Исходную селекцию осуществляли по связыванию популяций DTLacO, диверсифицированных посредством воздействия на гены, с бусами, комплексированными с антигенами MASP-1 (SEQ ID NO: 10) и MASP-3 (SEQ ID NO: 8) человека; и последующей селекции с помощью FACS с использованием флуоресцентно меченного растворимого антигена (Cumbers, S.J. et al. Nat 20 Biotechnol 1129-1134 (2002); Seo, H. et al. Nat Biotechnol 23, 731-735 (2005). Из-за консервативной аминокислотной последовательности альфа-цепи, общей для MASP-1 и MASP-3 (показано на фигуре 5), и отличающихся последовательностей бета-цепи (показано на фигуре 6), осуществляли раздельный, параллельный скрининг на средства, связывающиеся с MASP-1 и MASP-3, для идентификации mAb, специфичных для MASP-1, mAb, специфичных для MASP-3, а также mAb, способных связываться с MASP-1 и MASP-3 (с двойной специфичностью). Для селекции и скрининга на связывающие средства использовали две формы антигена. Сначала, рекомбинантную MASP-1 или MASP-3, полноразмерную или в виде фрагмента, подвергнутую слиянию с Fc-доменом, связывали с бусами Dynal magnetic Protein G Beads или использовали в селекции с помощью FACS с использованием вторичного меченого PECy5 антитела IgG(Fc) человека. Альтернативно, рекомбинантные варианты белков MASP-1 или MASP-3 напрямую метили Dylight flours и использовали для селекции и скрининга.
Связывание и аффинность
Рекомбинантные антитела получали клонированием амплифицированных с помощью ПЦР V-областей в вектор, поддерживающий экспрессию IgG1 человека в клетках 293F (Yabuki et al, PLoS ONE, 7(4):e36032 (2012)). Кинетику насыщения связывания определяли посредством окрашивания клеток DTLacO, экспрессирующих антитело, связывающееся с MASP-1 или MASP-3, с использованием различных концентраций флуоресцентно меченого растворимого антигена. Функциональные анализы на MASP-3-специфичную активность, включая MASP-3-зависимое накопление C3b и MASP-3-зависимое расщепление фактора D, осуществляли, как описано в примерах 17 и 18, соответственно. Функциональный анализ на MASP-1-специфичную активность, а именно ингибирование MASP-1-зависимого накопления C3b, осуществляли, как описано ниже.
Результаты:
Используя способы, описываемые выше, получали множество антител, связывающихся с MASP-1 и MASP-3. Связывание, определенное с помощью анализа FACS, описывают для типичных клонов M3J5 и M3M1, выделенных при скрининге на средства, связывающиеся с MASP-3.
Фигура 30A является диаграммой FACS связывания антигена MASP-3/антитела для клона DTLacO M3J5. Фигура 30B является диаграммой FACS связывания антигена MASP-3/антитела для клона DTLacO M3M1. На Фигурах 30A и 30B серые заштрихованные кривые представляют собой окрашенный на IgG1 отрицательный контроль, и тонкие черные кривые представляют собой окрашивание на MASP-3.
На фигуре 31 графически представлена кривая насыщения связывания для клона M3J5 (клона 5) с антигеном MASP-3. Как показано на фигуре 31, кажущаяся аффинность связывания антитела M3J5 с MASP-3 составляет приблизительно 31 нМ.
Анализ последовательности идентифицированных клонов осуществляли с использованием стандартных способов. Все клоны сравнивали с общими (DT40) последовательностями VH и VL и друг с другом. Последовательности для двух указанных выше клонов, M3J5 и M3M1, представлены в виде выравнивания с двумя дополнительными типичными клонами, D14 и 1E10, идентифицированными при скрининге на фрагменты CCP1-CCP2-SP MASP-1 и MASP-3, соответственно. D14 и 1E10 связываются с областями, общими для MASP-1 и MASP-3.
Фигура 32A представляет собой выравнивание аминокислотной последовательности областей VH M3J5, M3M1, D14 и 1E10 с последовательностью VH DT40 курицы.
Фигура 32B представляет собой выравнивание аминокислотной последовательности областей VL M3J5, M3M1, D14 и 1E10 с последовательностью VL DT40 курицы.
Аминокислотная последовательность VH и VL каждого клона представлена ниже.
Последовательности вариабельной области тяжелой цепи (VH)
На фигуре 32A показано аминокислотное выравнивание последовательностей вариабельной области тяжелой цепи (VH) родительских DTLacO (SEQ ID NO: 24), связывающихся с MASP-3 клонов M3J5 (SEQ ID NO: 25) и M3M1 (SEQ ID NO: 26), и клонов D14 с двойным связыванием MASP-1/MASP-3 (SEQ ID NO: 30), и 1E10.
CDR по Kabat в последовательностях VH локализованы в положениях следующих аминокислот: H1: а/к 31-35; H2: а/к 50-62; и H3: а/к 95-102.
CDR по Chothia в последовательностях VH локализованы в положениях следующих аминокислот: H1: а/к 26-32; H2: а/к 52-56; и H3: а/к 95-101.
VH родительского DTLacO (SEQ ID NO:24)
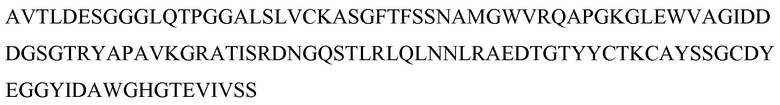
VH клона M3J5: (SEQ ID NO: 25)
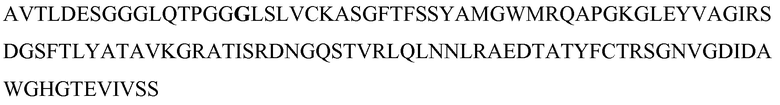
VH клона M3M1: (SEQ ID NO: 26)

VH клона D14: (SEQ ID NO: 30)

VH клона 1E10: (SEQ ID NO: 32)
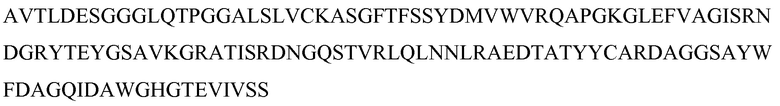
Последовательности вариабельной области легкой цепи (VL)
На фигуре 32B показано аминокислотное выравнивание последовательностей вариабельной области легкой цепи (VL) для родительского DTLacO (SEQ ID NO: 27) и связывающихся с MASP-3 клонов M3J5 (SEQ ID NO: 28), и M3M1 (SEQ ID NO: 29), и клонов D14 с двойным связыванием MASP-1/MASP-3 (SEQ ID NO: 31) и 1E10 (SEQ ID NO: 33).
VL родительского DTLacO (SEQ ID NO:27)
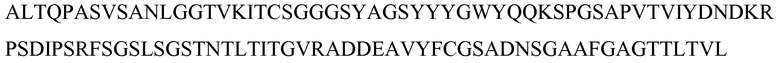
VL клона M3J5 (SEQ ID NO:28)
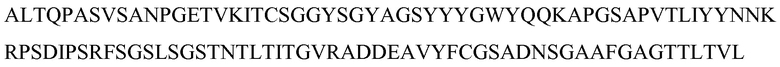
VL клона M3M1 (SEP ID NP:29)
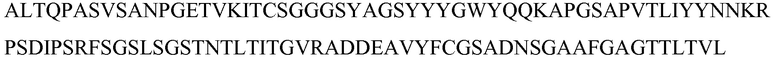
VL клона D14: (SEQ ID NP:31)
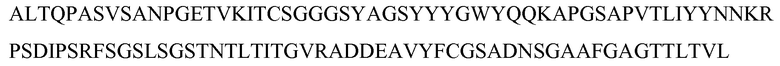
VL клона 1E10: (SEQ ID NP:33)
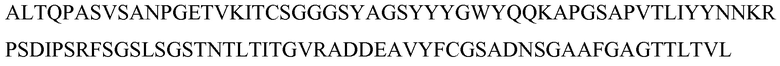
Функциональный анализ LEA-2 (MASP-2-зависимого)
MASP-1 участвует в LEA-2 благодаря своей способности активировать MASP-2 (см. Фигура 1). В анализе Wieslab® Complement System Screen MBL (Euro Diagnostica, Malmo, Sweden) измеряли накопление C5b-C9 в условиях, изолирующих LEA-2-зависимую активацию (т.е. активность традиционного лектинового пути). Анализ осуществляли по инструкциям производителя с использованием типичного клона 1E10, тестируемого в конечной концентрации 400 нМ.
Фигура 33 является столбчатой диаграммой, на которой показана ингибиторная активность mAb 1E10 по сравнению с положительной сывороткой, предоставленной с набором для анализа, а также изотипическим контрольным антителом. Как показано на фигуре 33, mAb 1E10 демонстрирует частичное ингибирование LEA-2-зависимой активации (посредством ингибирования MASP-1-зависимой активации MASP-2), в то время как изотипическое контрольное антитело - нет. Более сильного ингибирования должны достигать непрерывным созреванием аффинности этого антитела для связывания MASP-1 с использованием присоединенных факторов в системе DTLacO.
Функциональные анализы LEA-1 (MASP-3-зависимого) для типичных mAb представлены ниже в примерах 17 и 18.
Краткое изложение результатов:
Указанные выше результаты свидетельствовали о том, что платформа DTLacO делала возможной быструю разработку ex vivo моноклональных антител против MASP-1 и MASP-3 с ингибиторными свойствами в отношении LEA-1 (как показано ниже в примерах 17 и 18) и LEA-2 (как показано в этом примере).
ПРИМЕР 16
В этом примере описывают получение полипептидных ингибиторов MASP-1 и MASP-2.
Обоснование:
Получение специфичных ингибиторов MASP-1 и MASP-2, обозначенных как SGMI-1 и SGMI-2, соответственно, описывают в Heja et al, J Biol Chem 287:20290 (2012) и Heja et al., PNAS 109: 10498 (2012), каждая из которых, таким образом, включена в настоящее описание в качестве ссылки. Каждый из SGMI-1 и SGMI-2 является пептидом размером 36 аминокислот, выбранным из фаговой библиотеки вариантов ингибиторов протеазы 2 Schistocerca gregaria, в которых шесть из восьми положений петли связывания протеазы являются полностью случайными. Последующая разработка in vitro привела к получению моноспецифических ингибиторов с одноразрядными значениями нМ KI (Heja et al, J. Biol. Chem. 287:20290, 2012). Структурные исследования показали, что оптимизированная петля связывания протеазы образует первичный участок связывания, определяющий специфичность двух ингибиторов. Аминокислотные последовательности протяженной вторичной и внутренней областей связывания являются общими для двух ингибиторов и участвуют в образовании поверхности контакта (Heja et al., 2012. J. Biol. Chem. 287:20290). Механистически, и SGMI-1, и SGMI-2 блокируют лектиновый путь активации комплемента без влияния на классический или альтернативный путь (Heja et al., 2012. Proc. Natl. Acad. Sci. 109: 10498).
Аминокислотные последовательности ингибиторов SGMI-1 и SGMI-2 приведены ниже:
полноразмерный SGMI-1: LEVTCEPGTTFKDKCNTCRCGSDGKSAFCTRKLCYQ (SEQ ID NO: 34)
полноразмерный SGMI-2: LEVTCEPGTTFKDKCNTCRCGSDGKSAVCTKLWCNQ (SEQ ID NO: 35).
SGMI-1 и SGMI-2 являются высокоcпецифичными ингибиторами MASP-1 и MASP-2, соответственно. Однако, как пептиды они имеют ограниченный потенциал для применения в биологических исследованиях. Для разрешения этих ограничений авторы настоящего изобретения присоединяли аминокислотные последовательности этих биоактивных пептидов на амино-конец Fc-области IgG1 человека для получения Fc-слитого белка.
Способы:
Для экспрессии слитых белков SGMI-Fc IgG1 полинуклеотиды, кодирующие пептиды SGMI-1 (SEQ ID NO: 34) и SGMI-2 (SEQ ID NO: 35), синтезировали (DNA 2.0) и встраивали в экспрессирующий вектор pFUSE-hIgG1-Fc2 (InvivoGen) между нуклеотидными последовательностями, кодирующими сигнальную последовательность IL-2 и Fc-область IgG1 человека (SEQ ID NO: 36). Включали гибкий полипептидный линкер (например, SEQ ID NO: 37 или SEQ ID NO: 38) между пептидом SGMI и Fc-областью IgG1.
Последовательности гибкого полипептидного линкера:
GTGGGSGSSSRS (SEQ ID NO: 37)
GTGGGSGSSS (SEQ ID NO: 38)
Полученные конструкции описывают следующим образом:
Полинуклеотид, кодирующий слитый полипептид, содержащий сигнальную последовательность IL-2 человека, SGMI-1, линкер и Fc IgG1 человека (pFUSE-SGMI-lFc), приводят как SEQ ID NO: 39, кодирующую зрелый слитый полипептид, содержащий SGMI-1 (подчеркнуто), линкерную область (показано курсивом) и Fc IgG1 человека (вместе обозначаемый как "SGMI-1Fc"), приведенный как SEQ ID NO: 40.
SEQ ID NO:40

Полинуклеотид, кодирующий слитый полипептид, содержащий сигнальную последовательность IL-2 человека, SGMI-2, линкер и Fc IgG1 человека (pFUSE-SGMI-2Fc), приводят как SEQ ID NO: 41, кодирующую зрелый слитый полипептид, содержащий SGMI-2 (подчеркнуто), линкерную область (показано курсивом) и Fc IgG1 человека (вместе обозначаемый как "SGMI-2Fc"), приведенный как SEQ ID NO: 42:
SEQ ID NO:42

Получение рекомбинантных белков:
Клетки Freestyle 293-F или Expi293F (Invitrogen) транзиторно трансфицировали согласно рекомендациям производителя с использованием одной из двух экспрессирующих плазмид (pFUSE-SGMI-1Fc (SEQ ID NO: 39) и pFUSE-SGMI-2Fc (SEQ ID NO: 41). Через четыре дня инкубации при 37°C собирали среды для культивирования. Fc-слитые белки очищали с помощью аффинной хроматографии с протеином A.
Анализ измерения активации лектинового пути
Слитые белки SGMI-1Fc и SGMI-2Fc тестировали на способность ингибировать накопление C3b в 1% сыворотке на покрытом маннозой 96-луночном планшете, являющееся мерой активности лектинового пути. SGMI-1Fc и SGMI-2Fc преинкубировали с 1% нормальной сывороткой человека в течение одного часа на льду перед добавлением в лунки, покрытые маннозой (2 мкг/лунку). Накопление C3b измеряли с помощью ELISA, как описано в Schwaeble et al. PNAS 108:7523, 2011.
На фигуре 34 графически представлен уровень накопления C3b в 1% нормальной сыворотке человека с изотипическим контролем, SGMI-1Fc или SGMI-2Fc в диапазоне концентраций от 0,15 до 1000 нМ. Как показано на фигуре 34, SGMI-1Fc и SGMI-2Fc ингибировали накопление C3b в нормальной сыворотке в покрытых маннозой лунках для ELISA со значениями IC50 приблизительно 27 нМ и 300 нМ, соответственно.
Эти результаты свидетельствуют о том, что ингибиторные функции пептидов SGMI в отношении MASP-1 и MASP-2 сохраняются в слитых белках SGMI-1Fc и SGMI-2Fc.
ПРИМЕР 17
Анализ пути комплемента в сыворотке пациента с 3MC с использованием S. aureus
Уровень техники/Обоснование:
Определяли, что MASP-3 не активируется при подвергании воздействию неиммобилизированной маннозы, зимозана A или N-ацетилцистеина в жидкой фазе в присутствие или в отсутствие нормальной сыворотки человека. Однако определяли, что рекомбинантная и нативная MASP-3 активируется на поверхности термически инактивированных S. aureus в присутствие и в отсутствие нормальной сыворотки человека (NHS) или термически инактивированной сыворотки человека (HIS) (данные не представлены). Также определяли, что накопление C3b происходит на поверхности S. aureus в присутствие нормальной сыворотки человека, и что накопление можно определять с использованием проточного цитометра. Таким образом, ответ альтернативного пути (AP) на S. aureus измеряли, как описано в этом примере, как среднее при оценке участия MASP-3 в LEA-1.
Способы:
Рекомбинантная MASP-3: Полинуклеотидные последовательности, кодирующие полноразмерную рекомбинантную MASP-3 человека, укороченный активный вариант сериновой протеазы (SP) MASP-3 (CCP1-CCP2-SP) и SP-инактивированную форму MASP-3 (S679A), клонировали в экспрессирующийся в млекопитающих вектор pTriEx7 (Invivogen). Полученные экспрессирующие конструкции кодируют полноразмерную MASP-3 или фрагмент CCP1-CCP2-SP с амино-концевой меткой Strep-tag и карбокси-концевой 6-гистидиновой меткой. Экспрессирующие конструкции трансфицировали в клетки Freestyle 293-F или Expi293F (Invitrogen) по рекомендациям производителя. Через три-четыре дня культивирования в 5% CO2 при 37°C рекомбинантные белки очищали с помощью аффинной хроматографии со стрептактином.
Рекомбинантная MASP-1: полноразмерную или укороченную CCP1-CCP2-SP формы рекомбинантной MASP-1 со стабилизирующей мутацией R504Q (Dobo et al., J. Immunol 183: 1207, 2009) или SP инактивирующей (S646A) мутацией, или без них, и несущую амино-концевую метку Step-tag и карбокси-концевую 6-гистидиновую метку, получали, как описано для рекомбинантной MASP-3 выше.
1. Накопление C3b и расщепление фактора B на S. aureus в сыворотке пациента с 3MC (человека)
Исходный эксперимент осуществляли следующим образом для демонстрации того, что с помощью анализа проточной цитометрией можно определять наличие или отсутствие AP-запускаемого накопления C3b (AP-C3b). Пять процентов следующих сывороток: нормальной сыворотки человека, сыворотки человека с истощением фактора B, сыворотки человека с истощением фактора D и сыворотки человека с истощением пропердина (полученные из Complement Technology, Tyler, Texas, USA), смешивали с тестовым антителом в буфере Mg++/EGTA или ЭДТА при 4°C в течение ночи. Убитые нагреванием S. aureus (108/реакцию) добавляли к каждой смеси до конечного объема 100 мкл и вращали при 37°C в течение 40 минут. Бактерии промывали в промывочном буфере, бактериальный депозит ресуспендировали в промывочном буфере, и аликвоту 80 мкл каждого образца анализировали на предмет накопления C3b на поверхности бактерий, определяемого с помощью антитела против C3c человека (Dako, UK), с использованием проточной цитометрии.
Результаты определения накопления C3b с помощью проточной цитометрии показаны на фигуре 35A. Как показано на фигуре 35A, панель 1, в нормальной сыворотке человека в присутствие ЭДТА, которая, как известно, инактивирует AP, не наблюдали накопление C3b (отрицательный контроль). В нормальной сыворотке человека, обработанной Mg++/EGTA, мог функционировать только лектин-независимый путь комплемента. На панели 2, используют буфер Mg++/EGTA, таким образом, AP является активным, и наблюдают AP-запускаемое накопление C3b (положительный контроль). Как показано на панелях 3, 4 и 5, как и ожидали, в сыворотках с истощением фактора B, истощением фактора D и истощением пропердина, соответственно, не наблюдали запускаемого альтернативным путем накопления C3b. Эти результаты свидетельствуют о том, что с помощью этого анализа можно определять AP-зависимое накопление C3b.
Анализ накопления C3b на S. aureus осуществляли, как описано выше, для оценки способности рекомбинантной MASP-3 восстанавливать AP (LEA-1) в сыворотке человека с 3MC с дефицитом MASP-3 (Rooryck C, et al, Nat Genet. 43(3): 197-203 (2011)). Тестировали следующие комбинации реагентов.
1. 5% нормальная сыворотка человека + EDTA
2. 5% нормальная сыворотка человека + Mg++/EGTA
3. 5% сыворотка человека с 3MC (MASP-3-/-) + Mg++/EGTA
4. 5% сыворотка человека с 3MC (MASP-3-/-) + Mg++/EGTA + активная полноразмерная rMASP-3
5. 5% сыворотка человека с 3MC (MASP-3-/-) + Mg++/EGTA + укороченная активная rMASP-3 (CCP1/CCP2/SP)
6. 5% сыворотка человека с 3MC (MASP-3-/-) + Mg++/EGTA + неактивная rMASP-3 (S679A)
7. 5% сыворотка человека с 3MC (MASP-3-/-) + Mg++/EGTA + активная полноразмерная rMASP-1
Различные смеси 5% сыворотки и рекомбинантных белков (5 мкг каждого), как указано выше, инкубировали в конкретных буферных условиях (буфер Mg++/EGTA или ЭДТА) при 4°C в течение ночи. После инкубации в течение ночи в каждую смесь добавляли 108 убитых нагреванием S. aureus в общем объеме 100 мкл и вращали при 37°C в течение 40 минут. Бактерии промывали и ресуспендировали в промывочном буфере, и аликвоту 80 мкл каждого образца анализировали с помощью FACS на предмет накопления C3b. Оставшуюся аликвоту 20 мкл каждого образца использовали для измерения расщепления фактора B с помощью вестерн-блоттинга с использованием антитела против фактора B, как описано ниже.
Результаты определения C3b с помощью проточной цитометрии показаны на фигуре 35B. Номера панелей соответствуют номерам, присвоенным каждой из комбинаций реагентов, представленных выше. Как и ожидали, отрицательный контроль (панель 1) и положительный контроль (панель 2) демонстрировали отсутствие и наличие накопления C3b, соответственно. На панели 3 показано, что AP-запускаемое накопление C3b отсутствует в сыворотке пациента с 3MC. На панелях 4 и 5 показано, что активная полноразмерная rMASP-3 (панель 4) и активная rMASP-3 (CCP1-CCP2-SP) (панель 5) восстанавливали AP-запускаемое накопление C3b в сыворотке пациента с 3MC. На панели 6 показано, что неактивная rMASP-3 (S679A) не восстанавливает AP-запускаемое накопление C3b в сыворотке пациента с 3MC. На панели 7 показано, что rMASP-1 не восстанавливает AP-запускаемое накопление C3b в сыворотке пациента с 3MC.
В совокупности, эти результаты свидетельствуют о том, что MASP-3 необходима для AP-запускаемого накопления C3b на S. aureus в сыворотке человека.
2. MASP-3-зависимая активация фактора B
Для анализа MASP-3-зависимой активации фактора B различные смеси 5% сыворотки (нормальной сыворотки человека или сыворотки пациента с 3MC) и рекомбинантных белков, как указано выше, анализировали, как описано выше. Из каждой реакционной смеси отбирали 20 мкл и добавляли в буфер для внесения образцов белка. Образцы нагревали при 70°C в течение 10 минут и наносили на гель для электрофореза в ПААГ в присутствие SDS. Анализ вестерн-блоттинга осуществляли с использованием поликлонального антитела против фактора B (R&D Systems). Активацию фактора B наблюдали по образованию двух продуктов расщепления с меньшей молекулярной массой (Bb и Ba), полученных из белка про-фактора B с большей молекулярной массой.
На фигуре 36 представлены результаты анализа вестерн-блоттинга для определения расщепления фактора B в ответ на S. aureus в сыворотке пациента с 3MC в присутствие или в отсутствие rMASP-3. Как показано в линии 1, в нормальной сыворотке человека в присутствие ЭДТА (отрицательный контроль) наблюдали очень низкое расщепление фактора B относительно нормальной сыворотки человека в присутствие Mg++/EGTA, как показано в линии 2 (положительный контроль). Как показано в линии 3, в сыворотке пациента с 3MC наблюдали очень низкое расщепление фактора B в присутствие Mg++/EGTA. Однако, как показано в линии 4, расщепление фактора B восстанавливали добавлением полноразмерного рекомбинантного белка MASP-3 (5 мкг) в сыворотку пациента с 3MC и преинкубацией.
3. Анализ для определения эффекта rMASP-3 на про-фактор D в расщеплении фактора B/C3(H2O)
Для определения минимальной потребности в факторе B в MASP-3-зависимой активации/расщеплении осуществляли следующий анализ.
C3(H2O) (200 нг), очищенный фактор B плазмы (20 мкг), рекомбинантный про-фактор D (200 нг) и рекомбинантную MASP-3 человека (200 нг) смешивали в различных комбинациях (как показано на фигуре 37) в общем объеме 100 мкл в BBS/Ca++/Mg++ и инкубировали при 30°C в течение 30 минут. Реакцию останавливали добавлением 25 мкл красителя для нанесения с SDS, содержащего 5% 2-меркаптоэтанола. После кипячения при 95°C в течение 10 минут при встряхивании (300 об/мин) смесь центрифугировали при 1400 об/мин в течение 5 минут, и 20 мкл супернатанта наносили и разделяли в 10% геле с SDS. Гель окрашивали кумасси бриллиантовым синим.
Результаты:
На фигуре 37 показан окрашенный кумасси гель ПААГ после электрофореза в присутствие SDS, в котором анализировали расщепление фактора B. Как показано в линии 1, расщепление фактора B является наиболее оптимальным в присутствие C3, MASP-3 и про-фактора D. Как показано в линии 2, C3 является абсолютно необходимым; однако, как показано в линиях 4 и 5, MASP-3 или про-фактор D способны опосредовать расщепление фактора B при условии наличия C3.
4. Анализ способности mAb против MASP-3 ингибировать MASP-3-зависимое AP-запускаемое накопление C3b
Как описано в этом примере, показано, что MASP-3 необходима для AP-запускаемого накопления C3b на S. aureus в сыворотке человека. Таким образом, следующий анализ осуществляли для определения того, может ли типичное mAb против MASP-3, идентифицированное, как описано в примере 15, ингибировать активность MASP-3. Активный фрагмент рекомбинантного белка MASP-3 (CCP1-CCP2-SP) (250 нг) преинкубировали с изотипическим контрольным mAb, mAb1A5 (контролем, полученным с помощью платформы DTLacO, не связывающимся с MASP-3 или MASP-1), или mAbD14 (связывается с MASP-3) в трех различных концентрациях (0,5, 2 и 4 мкМ) в течение 1 часа на льду. Смесь фермент-mAb подвергали воздействию 5% сыворотки пациента с 3MC (с дефицитом MASP-3) и 5×107 убитых нагреванием S. aureus в конечном объеме реакционной смеси 50 мкл. Реакции проводили при 37°C в течение 30 минут, а затем окрашивали для определения накопления C3b. Окрашенные бактериальные клетки анализировали с помощью проточного цитометра.
На фигуре 38 графически представлены средние интенсивности флуоресценции (MFI) при окрашивании на C3b, получаемые от трех антител, построенные как функция концентрации mAb в сыворотке пациента с 3MC с наличием rMASP-3. Как показано на фигуре 38, в случае mAbD14 наблюдали ингибирование накопления C3b в зависимости от концентрации. В отличие от этого, ни одно из контрольных mAb не ингибировало накопление C3b. Эти результаты свидетельствуют о том, что mAbD14 способно ингибировать MASP-3-зависимое накопление C3b. Ожидают улучшенную ингибиторную активность mAbD14 после непрерывного созревания аффинности этого антитела для связывания MASP-3 с использованием присоединенных факторов в системе DTLacO.
Обобщенные результаты:
В целом, результаты, представленные в этом примере, свидетельствуют об очевидном дефекте AP в сыворотке при дефиците MASP-3. Таким образом, показано, что MASP-3 играет критическую роль в AP с использованием активации фактора B и накопления C3b в качестве функциональных конечных точек. Кроме того, добавление функциональной рекомбинантной MASP-3, включающей каталитически-активную C-концевую часть MASP-3, корректирует дефект активации фактора B и накопления C3b в сыворотке пациента с 3MC. В отличие от этого, как дополнительно показано в этом примере, добавление антитела против MASP-3 (например, mAbD14) в сыворотку пациента с 3MC с rMASP-3 ингибирует AP-запускаемое накопление C3b. Непосредственная роль MASP-3 в активации фактора B, и, таким образом, AP, показана при наблюдении того, что рекомбинантной MASP-3 вместе с C3 достаточно для активации рекомбинантного фактора B.
ПРИМЕР 18
В этом примере показано, что MASP-1 и MASP-3 активируют фактор D.
Способы:
Тестировали рекомбинантные MASP-1 и MASP-3 на их способность расщеплять два различных рекомбинантных варианта про-фактора D. В первом варианте (про-фактор D-His) отсутствует N-концевая метка, но присутствует C-концевая гистидиновая метка. Таким образом, этот вариант про-фактора D содержит пропептид размером 5 аминокислот, который удаляется при расщеплении при активации. Второй вариант (ST-про-фактор D-His) содержит последовательность Strep-TagII на N-конце, что, таким образом, удлиняет отщепляемый N-концевой фрагмент до 15 аминокислот. ST-про-фактор D также содержит 6-гистидиновую метку на C-конце. Увеличение длины пропептида ST-про-фактор D-His улучшает разрешение между расщепленной и нерасщепленной формами при электрофорезе в ПААГ в присутствие SDS по сравнению с разрешением, доступным при использовании формы про-фактор D-HIS.
Рекомбинантные белки MASP-1 или MASP-3 (2 мкг) добавляли к субстратам про-фактор D-His или ST-про-фактор D-His (100 нг) и инкубировали в течение 1 часа при 37°C. Продукты реакций подвергали электрофорезу 12% Bis-Tris геле для разделения про-фактора D и активного продукта расщепления фактора D. Разделенные белки переносили на мембрану PVDF и анализировали с помощью вестерн-блоттинга посредством определения биотинилированного антитела против фактора D (R&D Systems).
Результаты:
На фигуре 39 представлен анализ вестерн-блоттинга продуктов расщепления субстрата про-фактора D.
Описание дорожек для вестерн-блоттинга, представленного на фигуре 39
Как показано на фигуре 39, только полноразмерная MASP-3 (линия 2) и фрагмент MASP-1 CCP1-CCP2-SP (линия 5) расщепляли ST-про-фактор D-His6. Каталитически-неактивная полноразмерная MASP-3 (S679A; линия 3) и MASP-1 (S646A; линия 3) не могли расщеплять какой-либо субстрат. Идентичные результаты получали с использованием полипептида про-фактор D-His6 (данные не представлены). Сравнение молярного избытка MASP-1 (CCP1-CCP2-SP) относительно MASP-3 позволяет предполагать, что MASP-3 является более эффективным катализатором расщепления про-фактора D, чем MASP-1, по меньшей мере в условиях, представленных в настоящем описании.
Выводы: MASP-1 и MASP-3 способны расщеплять и активировать фактор D. Эта активность напрямую связывает LEA-1 с активацией AP. Более конкретно, активация фактора D MASP-1 или MASP-3 будет приводить к активации фактора B, накоплению C3b и, вероятно, опсонизации и/или лизису.
1. Анализ ингибирования MASP-3-зависимого расщепления про-фактора D антителами против MASP-3
Для определения ингибиторного эффекта типичных mAb против MASP-3 и MASP-1, идентифицированных, как описано в примере 15, на MASP-3-зависимое расщепление фактора D осуществляли анализ следующим образом. Активный рекомбинантный белок MASP-3 (80 нг) преинкубировали с 1 мкг типичных mAb D14, M3M1 и контрольного антитела (специфически связывающегося с MASP-1, но не MASP-3) при комнатной температуре в течение 15 минут. Добавляли про-фактор D с N-концевой меткой Strep-tag (ST-про-фактор D-His, 70 нг) и инкубировали смесь при 37°C в течение 75 минут. Затем продукты реакции подвергали электрофорезу, блоттингу и окрашивали антителом против фактора D, как описано выше.
На фигуре 40 представлен вестерн-блоттинг, на котором показана частичная ингибиторная активность mAb D14 и M3M1 по сравнению с контрольной реакционной смесью, содержащей только MASP-3 и ST-про-фактор D-His (без mAb; линия 1), а также контрольной реакционной смесью, содержащей mAb, полученное с помощью библиотеки DTLacO, связывающееся с MASP-1, но не MASP-3 (линия 4). Как показано на фигуре 40, в отсутствие ингибиторного антитела MASP-3 расщепляет приблизительно 50% про-фактора D до фактора D (линия 1). Контрольное специфичное антитело против MASP-1 (линия 4) не изменяло соотношение про-фактора D и фактора D. В отличие от этого, как показано в линиях 2 и 3, и mAb D14, и mAb M3M1 ингибировали MASP-3-зависимое расщепление про-фактора D до фактора D, что приводит к снижению образования фактора D.
Выводы: Эти результаты свидетельствуют о том, что mAb D14 и M3M1 против MASP-3 способны ингибировать MASP-3-зависимое расщепление фактора D. Ожидают улучшенную ингибиторную активность mAb D14 и mAb M3M1 после непрерывного созревания аффинности этих антител для связывания MASP-3 с использованием присоединенных факторов в системе DTLacO.
ПРИМЕР 19
В этом примере показано, что дефицит MASP-3 предотвращает опосредованный комплементом лизис покрытых маннозой эритроцитов кролика WT.
Уровень техники/Обоснование:
Как описано в примерах 5 и 6 в настоящем описании, эффект сыворотки при дефиците MASP-2 и MASP-3 в отношении лизиса эритроцитов из образцов крови, полученных из модели PNH мыши, показал эффективность ингибирования MASP-2 и/или ингибирования MASP-3 в лечении индивидуумов, страдающих PNH, а также подтверждает применимость ингибиторов MASP-2 и/или ингибиторов MASP-3 (включая двойные или биспецифические ингибиторы MASP-2/MASP-3) для снижения эффектов опосредованного фрагментами C3 внесосудистого гемолиза у индивидуумов с PNH, подвергаемых терапии ингибитором C5, таким как экулизумаб.
Как описано в этом примере, эксперименты по накоплению C3b и эксперименты по гемолизу осуществляли в сыворотке при дефиците MASP-3 от дополнительных пациентов с 3MC, что подтверждало результаты, полученные в примерах 5 и 6. Кроме того, осуществляли эксперименты, в которых показали, что добавление rMASP-3 в сыворотку пациента с 3MC способно восстанавливать накопление C3b и гемолитическую активность.
Способы:
От трех различных пациентов с 3MC получали сыворотки при дефиците MASP-3 следующим образом:
Пациент 1 с 3MC: имеет аллель, несущий мутацию, делающую экзон, кодирующий домен сериновой протеазы MASP-3, нефункциональным, добавлены мать и отец пациента с 3MC (оба гетерозиготны по аллелю, несущему мутацию, делающую экзон, кодирующий домен сериновой протеазы MASP-3, нефункциональным).
Пациент 2 с 3MC: Имеет мутацию C1489T (H497Y) в экзоне 12 MASP-1, кодирующем домен сериновой протеазы MASP-3, приводящую к нефункциональному белку MASP-3, но функциональному белку MASP-1.
Пациент 3 с 3MC: Имеет подтвержденный дефект гена MASP-1, приводящий к нефункциональным белкам MASP-3 и MASP-1.
Эксперимент №1: Анализ накопления C3b
Анализ AP осуществляли в традиционных AP-специфичных условиях (BBS/Mg++/EGTA, без Ca++, где BBS = забуференный барбиталом физиологический раствор, содержащий сахарозу), как описано в Bitter-Suermann et al., Eur. J. Immunol 1 1:291-295 (1981)), на покрытых зимозаном планшетах для микротитрования при концентрациях сыворотки в диапазоне от 0,5 до 25% и измеряли накопление C3b с течением времени.
Результаты:
На фигуре 41 графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации в образцах сыворотки, полученных от индивидуумов с дефицитом MASP-3 (3MC), дефицитом C4 и дефицитом MBL. Как показано на фигуре 41 и обобщено в таблице 18 ниже, сыворотки пациентов с дефицитом MASP-3 от пациента №2 и пациента №3 имели остаточную активность AP при высоких концентрациях (концентрации сыворотки 25%, 12,5%, 6,25%), но значимо более высокую AP50 (т.е. 8,2% и 12,3%) сыворотки, необходимую для достижения 50% максимального накопления C3).
На фигуре 42A графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования в "традиционных" AP-специфичных условиях (т.е. BBS/EGTA/Mg++ без Ca++) как функция времени в образцах 10% сыворотки человека, полученных от индивидуумов с дефицитом MASP-3, дефицитом C4 и дефицитом MBL.
В таблице 19 ниже обобщены результаты AP50, показанные на фигуре 41, и время полужизни для накопления C3b, показанное на фигуре 42A.
Общие результаты, представленные на фигурах 41 и 42A
Эксперимент №2: Анализ расщепления про-фактора D в сыворотках пациентов с 3MC с помощью вестерн-блоттинга
Способы: Получали сыворотку от пациента №2 с 3MC (MASP 3(-/-), MASP-1(+/+)) и пациента №3 с 3MC (MASP 3(-/-), MASP-1(-/-)). Сыворотки пациентов вместе с сыворотками нормальных доноров (W) подвергали разделению с помощью электрофореза в ПААГ в присутсвие SDS и разделенные белки подвергали блоттингу на мембране из поливинилиденфторида. Про-фактор D человека (25040 Да) и/или зрелый фактор D (24405 Да) определяли с использованием антитела против фактора D человека.
Результаты: Результаты вестерн-блоттинга представлены на фигуре 42B. Как показано на фигуре 42B, в сыворотках нормальных доноров (W) с помощью антитела против фактора D определяли белок, соответствующий зрелому фактору D (24405 Да). Как дополнительно показано на фигуре 42B, в сыворотках пациента №2 с 3MC (P2) и пациента №3 с 3MC (P3) с помощью антитела против фактора D определяли белок немного большего размера, соответствующий наличию про-фактора D (25040 Да) у этих пациентов с 3MC.
Эксперимент №3: Анализ комплемента Wieslab с использованием сывороток от пациентов с 3MC
Способы: Сыворотки от пациента №2 с 3MC (MASP 3(-/-), MASP-1 (+/+)) и пациента №3 с 3MC (MASP 3(-/-), MASP-1 (-/-)) также тестировали на активность классического, лектинового и альтернативного путей с использованием Wieslab Complement System Screen (Euro-Diagnostica, Malmo, Sweden) согласно инструкциям производителя. Параллельно в качестве контроля тестировали нормальную сыворотку человека.
Результаты: На фигуре 42C графически представлены результаты анализов классического, лектинового и альтернативного путей Wieslab с использованием плазмы, полученной от пациента №2 с 3MC, пациента №3 с 3MC и нормальной сыворотки человека. Как показано на фигуре 42C, в условиях анализа Wieslab в нормальной сыворотке человека все из классического, альтернативного и MBL (лектинового) путей являлись функциональными. В сыворотке пациента №2 с 3MC (MASP 3(-/-), MASP-1(+/+)) классический путь и лектиновый путь являлись функциональными, при этом не наблюдали детектируемой активности альтернативного пути. В сыворотке пациента №3 с 3MC (MASP 3(-/-), MASP-1(-/-)) классический путь являлся функциональным, при этом не наблюдали детектируемой активности лектинового пути и альтернативного пути.
Результаты, представленные на фигурах 42B и 42C, дополнительно подтверждают понимание авторами настоящего изобретения роли MASP-1 и MASP-3 в путях LEA-1 и LEA-2. В частности, отсутствие альтернативного пути при почти полностью функциональном лектиновом пути в сыворотке пациента № 2, у которого отсутствует только MASP-3, подтверждает то, что MASP-3 необходима для активации альтернативного пути. В сыворотке пациента № 3, у которого отсутствуют и MASP-1, и MASP-3, утратила способность активировать лектиновый путь, а также альтернативный путь. Этот результат подтверждает необходимость MASP-1 для функционального пути LEA-2, и это соответствует результатам в примерах 15 и 16 и данным из литературы, в которых показано, что MASP-1 активирует MASP-2. Очевидная неспособность обеих сывороток активировать про-фактор D также соответствует данным, описанным в примере 18, в котором показано, что MASP-3 расщепляет про-фактор D. Эти результаты сооответствуют путям LEA-1 и LEA-2, как они показаны на фигуре 1.
Эксперимент № 4: Анализ гемолиза, в котором покрытые маннозой эритроциты кролика тестируют на лизис в присутствие нормальной сыворотки человека или сыворотки пациента с 3MC (в отсутствие Ca++)
Способы:
Получение RBC кролика в отсутствие Ca++ (т.е. с использованием EGTA)
Цельную кровь кролика (2 мл) разделяли по двум пробиркам Eppendorf емкостью 1,5 мл и центрифугировали в течение 3 минут при 8000 об/мин (приблизительно 5,9 rcf) на центрифуге Eppendorf с охлаждением при 4°C. Депозит RBC три раза промывали после ресуспендирования в холодном буфере BBS/Mg++/Ca++ (4,4 мМ барбитуровая кислота, 1,8 мМ барбитал натрия, 145 мМ NaCl, pH 7,4, 5 мМ Mg++, 5 мМ Ca++). После третьего промывания депозит ресуспендировали в 4 мл буфера BBS/Mg++/Ca++. Эритроциты осаждали и промывали RBC буфером BBS/0,1% желатин/Mg++/Ca++, как описано выше. Суспензию RBC хранили в буфере BBS/0,1% желатин/Mg++/Ca++ при 4°C. Затем 100 мкл суспендированных RBC разводили 1,4 мл воды и центрифугировали при 8000 об/мин (приблизительно 5,9 rcf) в течение 3 минут и доводили OD супернатанта до 0,7 при 541 нм (OD 0,7 при 541 нм соответствует приблизительно 109 эритроцитам/мл). После этого 1 мл ресуспендированных RBC при OD 0,7 добавляли в 9 мл буфера BBS/Mg++/EGTA для достижения концентрации 108 эритроцитов/мл. Разведения тестовых сывороток или плазмы получали в холодном буфере BBS, Mg++, EGTA и 100 мкл каждого разведения сыворотки или плазмы пипетировали в соответствующую лунку круглодонного планшета. В каждую лунку добавляли 100 мкл соответствующим образом разведенных RBC (108 эритроцитов/мл). Воду, подвергнутую нанофильтрации, использовали для получения положительного контроля (100% лизис), в то время как разведение BBS/Mg++/EGTA без сыворотки или плазмы использовали в качестве отрицательного контроля. Затем планшет инкубировали в течение 1 часа при 37°C. Круглодонный планшет центрифугировали при 3750 об/мин в течение 5 минут. Затем 100 мкл супернатанта из каждой лунки переносили в соответствующие лунки плоскодонного планшета и регистрировали OD при 415-490 нм.
Результаты:
На фигуре 43 графически представлен процент гемолиза (измеряемого с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами кролика в супернатант) покрытых маннозой эритроцитов кролика в диапазоне концентраций сыворотки в сыворотке от нормальных индивидуумов и двух пациентов с 3MC (пациент №2 и пациент №3), измеряемого в отсутствие Ca++. Как представлено на фигуре 43, показано, что дефицит MASP-3 снижает процентную долю опосредованного комплементом лизиса покрытых маннозой эритроцитов по сравнению с нормальной сывороткой человека. Различия между двумя кривыми для нормальной сыворотки человека и двумя кривыми для пациентов с 3MC являются значимыми (p=0,013, критерий Фридмана).
В таблице 19 ниже обобщены результаты AP50, показанные на фигуре 43.
Общие результаты, показанные на фигуре 43
Необходимо отметить, что при объединении образцов сыворотки, представленных в таблице 20, значение AP50 для нормальной сыворотки человека = 7,9, и значение AP50 для сыворотки пациента с 3MC = 12,8 (p=0,031, знаковый ранговый тест Вилкоксона для парных данных).
Эксперимент №5: Восстановление сыворотки человека с 3MC с помощью рекомбинантной MASP-3 восстанавливает AP-запускаемое накопление C3b на покрытых зимозаном планшетах
Способы:
Анализ AP осуществляли в традиционных AP-специфичных условиях (BBS/Mg++/EGTA, без Ca++, где BBS = забуференный барбиталом физиологический раствор, содержащий сахарозу), как описано в Bitter-Suermann et al, Eur. J. Immunol 11:291-295 (1981)), на покрытых зимозаном планшетах для микротитрования в следующих образцах сыворотки: (1) 5% сыворотки человека от пациента №2 с 3MC с полноразмерной активной rMASP-3, добавленной в диапазоне концентраций от 0 до 20 мкг/мл; (2) 10% сыворотки человека от пациента №2 с 3MC с полноразмерной rMASP-3, добавленной в диапазоне концентраций от 0 до 20 мкг/мл; и (3) 5% сыворотки человека от пациента №2 с 3MC с неактивной rMASP-3A (S679A), добавленной в диапазоне концентраций от 0 до 20 мкг/мл.
Результаты:
На фигуре 44 графически представлен уровень AP-запускаемого накопления C3b на покрытых зимозаном планшетах для микротитрования как функция концентрации белка rMASP-3, добавляемого в образцы сыворотки, полученных от пациента №2 с 3MC (с дефицитом MASP-3). Как показано на фигуре 44, активный рекомбинантный белок MASP-3 восстанавливал AP-запускаемое накопление C3b на покрытых зимозаном планшетах в зависимости от концентрации. Как дополнительно показано на фигуре 44, не наблюдали накопления C3b в сыворотке пациента с 3MC, содержащей неактивную rMASP-3 (S679A).
Эксперимент №6: Восстановление сыворотки человека с 3MC с помощью рекомбинантной MASP-3 восстанавливает гемолитическую активность в сыворотке пациента с 3MC
Способы:
Гемолитический анализ осуществляли с использованием RBC кролика с использованием способов, описываемых выше в эксперименте №2, со следующими тестовыми сыворотками в диапазоне концентраций от 0 до 12% сыворотки: (1) нормальной сывороткой человека; (2) сывороткой пациента с 3MC; (3) сывороткой пациента с 3MC с активной полноразмерной rMASP-3 (20 мкг/мл); и (4) термически инактивированной сывороткой человека.
Результаты:
На фигуре 45 графически представлен процент гемолиза (измеряемого с помощью фотометрии по высвобождению гемоглобина лизированными эритроцитами кролика в супернатант) покрытых маннозой эритроцитов кролика в диапазоне концентраций сыворотки в (1) нормальной сыворотке человека; (2) сыворотке пациента с 3MC; (3) сыворотке пациента с 3MC с активной полноразмерной rMASP-3 (20 мкг/мл); и (4) термически инактивированной сыворотке человека, измеряемого в отсутствие Ca++. Как показано на фигуре 45, процент лизиса RBC кролика значимо повышен в сыворотке пациента с 3MC, включающей rMASP-3, по сравнению с процентом лизиса в сыворотке пациента с 3MC без rMASP-3 (p=0,0006).
На фигуре 46 графически представлен процент лизиса эритроцитов кролика в 7% сыворотке человека от пациента №2 с 3MC и пациента №3 с 3MC, содержащей активную rMASP-3 в диапазоне концентраций от 0 до 110 мкг/мл в BBS/Mg++/EGTA. Как показано на фигуре 46, процент лизиса RBC кролика восстанавливался с повышением количества rMASP-3 в зависимости от концентрации до 100% активности.
Эксперимент №7: Сыворотка пациента с дефицитом MASP-3 (CMC) содержит функциональную MASP-2 при наличии MBL
Способы:
Анализ накопления C3b осуществляли с использованием покрытых маннозой планшетов для ELISA для исследования того, присутствует ли в сыворотке пациента с 3MC дефицит LEA-2. Обработанную цитратом плазму разводили в буфере BBS в серийных разведениях (начиная с 1:80, 1:160, 1:320, 1:640, 1:1280, 1:2560) и наносили на покрытые маннозой планшеты. Накопление C3b определяли с использованием анализа антител курицы против C3b человека. Запускаемое LEA-2 накопление C3b (разведения плазмы являлись слишком сильными для функционирования AP и LEA-1) на покрытых маннозой планшетах для ELISA оценивали как функцию концентрации сыворотки человека в сыворотке от нормального человека (NHS), от двух пациентов с 3MC (пациента №2 и пациента №3), от родителей пациента №3 и от индивидуума с дефицитом MBL.
Результаты:
На фигуре 47 графически представлен уровень запускаемого LEA-2 (т.е. запускаемого MASP-2) накопления C3b на покрытых маннозой планшетах для ELISA как функция концентрации сыворотки человека, разведенной в буфере BBS, для сыворотки от нормального человека (NHS), от двух пациентов с 3MC (пациента №2 и пациента №3), от родителей пациента №3 и от индивидуума с дефицитом MBL. Эти данные свидетельствуют о том, что у пациента №2 достаточно MBL. Однако у пациента №3 и матери пациента №3 наблюдали дефицит MBL, и, таким образом, в их сыворотке на маннозе не накапливается C3b через LEA-2. Замещение MBL в этих сыворотках восстанавливало опосредованное LEA-2 накопление C3b в сыворотке пациента №3 (являющегося гомозиготным по SNP, приводящему к дефициту MASP-3) и его матери (являющейся гетерозиготной по мутантному аллелю MASP-3) (данные не представлены). Эти результаты свидетельствуют о том, что в сыворотке пациента с 3MC нет дефицита LEA-2, но, по-видимому, она содержит функциональную MASP-2.
Общее резюме и выводы:
Эти результаты свидетельствуют о том, что дефицит MASP-3 в сыворотке человека приводит к утрате активности AP, что проявляется в сниженном накоплении C3b на покрытых зимозаном лунках и сниженном лизисе эритроцитов кролика. AP можно восстанавливать в обоих анализах, дополняя сыворотки функциональной рекомбинантной MASP-3 человека.
ПРИМЕР 20
В этом примере описывают результаты анализа MASP-2-/- в модели дегенерации желтого пятна мыши.
Уровень техники/Обоснование: Возрастная дегенерация желтого пятна (AMD) является основной причиной слепоты после 55 лет в промышленно развитых странах. AMD развивается в двух основных формах: неоваскулярной (влажной) AMD и атрофической (сухой) AMD. На неоваскулярную (влажную) форму приходится 90% тяжелых случаев потери, зрения ассоциированной с AMD, хотя только у ~20% индивидуумов с AMD развивается влажная форма. Клинические признаки AMD включают многочисленные друзы, географическую атрофию и хороидальную неоваскуляризацию (CNV). В декабре 2004 года FDA одобрило макуген (пегаптаниб), новый класс офтальмологических лекарственных средств, конкретно направленных и блокирующих эффекты фактора роста эндотелия сосудов (VEGF), для лечения влажной (неоваскулярной) формы AMD (Ng et al., Nat Rev. Drug Discov 5: 123-32 (2006)). Хотя макуген представляет собой новый многообещающий вариант лечения подгруппы пациентов с AMD, сохраняется острая необходимость разработки дополнительных способов лечения этого комплексного заболевания. В многочисленных независимых исследованиях центральную роль в патогенезе AMD отводят активации комплемента. Патогенез хороидальной неоваскуляризации (CNV), наиболее тяжелой формы AMD, может включать активацию путей комплемента.
Более двадцати пяти лет назад Ryan описывал модель индуцируемого лазером повреждения CNV у животных (Ryan, S.J., Tr. Am. Opth. Soc. LXXVII: 707-745, 1979). Исходно разрабатывали модель с использованием макак-резусов, однако с тех пор эту же технологию используют для разработки аналогичных моделей CNV на множестве лабораторных животных, включая мышь (Tobe et aL, Am. J. Pathol. 755:1641-46, 1998). В этой модели лазерную фотокоагуляцию используют для разрушения мембраны Бруха, что приводит к образованию CNV-подобных мембран. Индуцированная лазером модель отражает многие из важных признаков нарушения у человека (недавний обзор см. в Ambati et al., Survey Ophthalmology 45:257-293, 2003). В настоящее время индуцированная лазером модель на мышах хорошо известна, и ее используют в качестве экспериментальной основы большого, и даже все возрастающего, количества исследовательских проектов. Как правило, общепринятым считается, что индуцированная лазером модель имеет достаточно биологического сходства с CNV у людей, чтобы преклинические исследования патогенеза и ингибирования лекарственными средствами с использованием этой модели соответствовали CNV у людей.
Способы:
Мышей MASP-2-/- получали, как описано в примере 1, и подвергали обратному скрещиванию с C57B1/6 в течение 10 поколений. В настоящем исследовании сравнивали результаты оценки самцов мышей MASP-2 (-/-) и MASP-2 (+/+) по течению индуцированной лазером CNV, ускоренной модели неоваскулярного AMD, в которой упор делают на объеме индуцированной лазером CNV, с помощью лазерной сканирующей конфокальной микроскопии в качестве меры повреждение ткани и определения уровней VEGF, мощного ангиогенного фактора, участвующего в CNV, в пигментном эпителии сетчатки (RPE)/хориоидеи посредством ELISA после повреждения лазером.
Индукция хороидальной неоваскуляризации (CNV): Лазерную фотокоагуляцию (532 нм, 200 мВ, 100 мс, 75 мкм; Oculight GL, Iridex, Mountain View, CA) на обоих глазах каждого животного в день 0 осуществлял один индивидуум, не знавший о распределении животных по исследуемым группам в отношении лекарственного средства. Лазерные пятна наносили стандартизированным образом вокруг зрительного нерва с использованием системы с щелевой лампой и покровного стекла в качестве контактной линзы. Морфологической конечной точкой повреждения лазером являлось появление кавитационного пузырька, признака, считающегося коррелирующим с разрушением мембраны Бруха. Подробности способов и оцениваемые конечные точки являлись следующими.
Флуоресцентная ангиография: Флуоресцентную ангиографию осуществляли с использованием камеры и системы визуализации (камера TRC 50 1A; система ImageNet 2.01; Topcon, Paramus, NJ) через 1 неделю после лазерной фотокоагуляции. Фотографии получали с использованием линзы 20-D, соприкасающейся с линзой фундус-камеры, после интраперитонеальной инъекции 0,1 мл 2,5% флуоресцеина натрия. Специалист-ретинолог, не участвовавший в лазерной фотокоагуляции или ангиографии, оценивал флуоресцентные ангиограммы за один сеанс слепым образом.
Объем хороидальной неоваскуляризации (CNV): Через одну неделю после повреждения лазером, глаза подвергали энуклеации и фиксировали 4% параформальдегидом в течение 30 мин при 4°C. Препараты глаза получали удалением передних сегментов и промывали три раза в PBS с последующей дегидратацией и регидратацией в серии разведений метанола. После двукратного блокирования буфером (PBS, содержащим 1% бычий сывороточный альбумин и 0,5% Triton X-100) в течение 30 минут при комнатной температуре, препараты глаза инкубировали в течение ночи при 4°C с 0,5% FITC-изолектином B4 (Vector laboratories, Burlingame, CA), разведенным в PBS, содержащем 0,2% BSA и 0,1% Triton X-100. FITC-изолектин B4 связывается с терминальными остатками β-D-гaлактозы на поверхности эндотелиальных клеток, и с помощью него избирательно метят сосудистую систему мыши. После двух промываний PBS, содержащим 0,1% Triton X-100, нейросенсорную часть сетчатки осторожно отделяли и отрезали от зрительного нерва. Делали четыре радиальных релаксирующих надреза и получали плоские препараты оставшегося комплекса RPE-хориоидеа-склера в среде, стабилизирующей флуорохромы (Immu-Mount Vectashield Mounting Medium; Vector Laboratories), и закрывали покровным стеклом.
Плоские препараты исследовали с использованием сканирующего лазерного конфокального микроскопа (TCS SP; Leica, Heidelberg, Germany). Сосуды визуализировали посредством возбуждения аргоновым лазером с длиной волны 488 нм и регистрации эмиссии между 515 и 545 нм. Для всех исследований по визуализации использовали масляно-иммерсионный объектив с увеличением 40X. Горизонтальные оптические срезы (шаг 1 мкм) получали с поверхности комплекса RPE-хориоидеа-склера. Самую глубокую фокусную плоскость, в которой можно было определить окружающую хороидальную сосудистую сеть, соединяющуюся с очагом повреждения, считали дном очага повреждения. Любой сосуд в поврежденной лазером области, являющийся внешним относительно референсной плоскости, считали CNV. Изображения каждого среза хранили в цифровом формате. Область связанной с CNV флуоресценции измеряли посредством компьютеризированного анализа изображений с помощью прилагающегося к микроскопу программного обеспечения (TCS SP; Leica). Сумму всей области флуоресценции в каждом горизонтальном срезе использовали в качестве индекса объема CNV. Визуализацию осуществлял оператор, не знающий о распределении исследуемых групп в отношении их обработки.
Из-за вероятности того, что на каждое повреждение лазером, в котором развивается CNV, влияет группа, к которой оно принадлежит (мышь, глаз и лазерное пятно), средние объемы повреждений сравнивали с использованием линейной смешанной модели с дизайном с расщепленными делянками с повторными измерениями. Фактором целой делянки являлась генетическая группа, к которой принадлежит животное, в то время как фактором расщепленной делянки являлся глаз. Статистическую значимость определяли на уровне 0,05. Апостериорные сравнения средних осуществляли с поправкой Бонферрони для множественных сравнений.
ELISA VEGF. Через три дня после повреждения 12 лазерными пятнами комплекс RPE-хориоидеа подвергали воздействию ультразвука в лизирующем буфере (20 мМ имидазол HCl, 10 мМ KCl, 1 мМ MgCl2, 10 мМ EGTA, 1% Triton X-100, 10 мМ NaF, 1 мМ молибдат Na и 1 мМ ЭДТА с ингибитором протеазы) на льду в течение 15 мин. Уровни белка VEGF в супернатанте определяли с помощью набора для ELISA (R&D Systems, Minneapolis, MN), который позволяет определять все варианты сплайсинга, при 450-570 нм (Emax; Molecular Devices, Sunnyvale, CA), и нормировали по общему белку. Повторные измерения слепым образом осуществлял оператор, не участвовавший в фотокоагуляции, визуализации или ангиографии. Количества VEGF представляли в виде среднего ± SEM по меньшей мере для трех независимых экспериментов и сравнивали с использованием U-теста Манна-Уитни. Нулевую гипотезу отвергали при P<0,05.
РЕЗУЛЬТАТЫ:
Оценка уровней VEGF
На фигуре 48A графически представлены уровни белка VEGF в комплексах RPE-хориоидеа, выделенных из мышей C57B16 дикого типа и мышей MASP-2(-/-) в день 0. Как показано на фигуре 48A, при оценке уровней VEGF наблюдали сниженные исходные уровни VEGF у мышей MASP-2(-/-) по сравнению с контрольными мышами C57bl/6 дикого типа. На фигуре 48B графически представлены уровни белка VEGF, измеряемые через три дня после индуцированного лазером повреждения. Как показано на фигуре 48B, через три дня после индуцированного лазером повреждения у мышей дикого типа (+/+) значимо повышались уровни VEGF, что соответствует данным опубликованных исследований (Nozaki et al, Proc. Natl. Acad. Sci. USA 103:2328-33 (2006)). Однако, у мышей MASP-2(-/-) неожиданно наблюдали очень низкие уровни VEGF.
Оценка хороидальной неоваскуляризации (CNV):
В дополнение к снижению уровней VEGF после индуцированной лазером дегенерации желтого пятна, определяли площадь CNV до и после повреждения лазером. На фигуре 49 графически представлен объем CNV, измеряемый у мышей C57bl/6 дикого типа и мышей MASP-2(-/-) через семь дней после индуцированного лазером повреждения. Как показано на фигуре 49, у мышей MASP-2 (-/-) через семь дней после индуцированного лазером повреждения наблюдали приблизительно 30%-ное снижение площади CNV по сравнению с контрольными мышами дикого типа.
Эти результаты свидетельствуют о снижении VEGF и CNV, наблюдаемом у мышей MASP(-/-) при сравнении с контролями дикого типа (+/+), и о том, что блокада MASP-2 с помощью ингибитора будет оказывать профилактический или терапевтический эффект при лечении дегенерации желтого пятна.
ПРИМЕР 21
В этом примере описывают анализ Moab мыши против MASP-2, полученного из Fab2 #11, на эффективность в модели возрастной дегенерации желтого пятна мыши.
Уровень техники/Обоснование:
Как описано в примерах 11 и 12, белок MASP-2 крысы использовали для пэннинга библиотеки фагового дисплея Fab, из которой Fab2#11 идентифицировали как функционально активное антитело. Из Fab2 #11 получали полноразмерные антитела изотипов IgG2c крысы и IgG2a мыши. Полноразмерное антитело против MASP-2 изотипа IgG2a мыши охарактеризовывали по фармакодинамическим показателям, как описано в примере 13. В этом примере, полноразмерное антитело мыши против MASP-2, полученное из Fab2 #11, анализировали в модели возрастной дегенерации желтого пятна мыши (AMD), описанной в Bora P.S. et al, J Immunol 174:491-497 (2005).
Способы:
Полноразмерное антитело против MASP-2 изотипа IgG2a мыши, полученное из Fab2 #11, как описано в примере 13, тестировали в модели возрастной дегенерации желтого пятна мыши (AMD), как описано в примере 20 со следующими модификациями.
Введение MoAb мыши против MASP-2
Две различные дозы (0,3 мг/кг и 1,0 мг/кг) MoAb мыши против MASP-2 вместе с изотипическим контрольным MoAb инъецировали i.p. мышам WT (+/+) (n=8 мышей на группу) за 16 до индукции CNV.
Индукция хороидальной неоваскуляризации (CNV)
Индукцию хороидальной неоваскуляризации (CNV) и измерение объема CNV осуществляли с использованием лазерной фотокоагуляции, как описано в примере 20.
Результаты:
На фигуре 50 графически представлена площадь CNV, измеряемая через семь дней после повреждения лазером у мышей, которым вводили изотипическое контрольное MoAb или MoAb мыши против MASP-2 (0,3 мг/кг и 1,0 мг/кг). Как показано на фигуре 50, у мышей, которым предварительно вводили 1,0 мг/кг MoAb против MASP-2, через семь дней после обработки лазером наблюдали статистически значимое (p<0,01) приблизительно 50% снижение CNV. Как дополнительно показано на фигуре 50, наблюдали, что доза 0,3 мг/кг MoAb против MASP-2 не являлась эффективной в снижении CNV. Необходимо отметить, что показано, что доза 0,3 мг/кг MoAb против MASP-2 вызывала частичное и временное ингибирование накопления C4b после подкожного введения, как описано в примере 13 и показано на фигуре 29A.
Результаты, описанные в этом примере, свидетельствуют о том, что блокада MASP-2 с помощью ингибитора, такого как MoAb против MASP-2, оказывает профилактический и/или терапевтический эффект в лечении дегенерации желтого пятна. Необходимо отметить, что эти результаты соответствуют результатам, полученным в исследовании, осуществленном на мышах MASP-2(-/-), описанном в примере 20, в котором через семь дней после обработки лазером у мышей MASP-2(-/-) наблюдали 30% снижение площади CNV по сравнению с контрольными мышами дикого типа. Кроме того, результаты в этом примере дополнительно свидетельствуют о том, что антитело против MASP-2, введенное системно, оказывает локальный благоприятный терапевтический эффект в глазу, что, таким образом, указывает на потенциал системного пути введения для лечения пациентов с AMD. В заключение, эти результаты представляют собой доказательство, подтверждающее применимость MoAb против MASP-2 в лечении AMD.
ПРИМЕР 22
В этом примере описывают анализ мышей MASP-2(-/-) в модели ишемии/реперфузии миокарда мыши.
Уровень техники/Обоснование:
Маннозо-связывающий лектин (MBL) является циркулирующей молекулой, инициирующей активацию комплемента независимо от иммунных комплексов в ответ на широкий диапазон углеводных структур. Эти структуры могут являться компонентами возбудителей инфекций или измененными эндогенными молекулами углеводов, в частности, внутри некротизированных, опухолевых или апоптотических клеток. Эти формы гибели клеток имеют место в подвергнутом реперфузии миокарде, где активация комплемента, по-видимому, увеличивает очаг повреждения за пределы границ, в которых он существует на момент, когда ишемию останавливают реперфузией. Хотя существует убедительное доказательство того, что активация комплемента усугубляет реперфузионное повреждение миокарда, механизм такой активации не вполне ясен, и ингибирование всех известных путей, вероятно, будет оказывать неприемлемые неблагоприятные воздействия. В недавнем исследовании подтвердили, что активация может включать MBL, а не классический путь или петлю амплификации альтернативного пути (как определено в настоящем изобретении), т.к. очаг инфаркта уменьшался у мышей MBL(A/C)-, но не у мышей C1q- и нулевых мышей (Walsh M.C. et al, Jour of Immunol. 775:541-546 (2005)). Однако, хотя эти результаты обнадеживают, у этих мышей все равно сохраняются циркулирующие компоненты, такие как фиколин A, способные активировать комплемент лектиновым путем.
В этом исследовании изучали мышей MASP-2(-/-) со сравнением с контролями дикого типа (+/+) для определения того, будут ли мыши MASP-2(-/-) менее чувствительными к повреждению миокарда при ишемии/реперфузии. Мышей MASP-2(-/-) подвергали локальной ишемии и сравнивали размер инфаркта с однопометными мышами дикого типа.
Способы: Следующий протокол основан на способе повреждения при ишемии/реперфузии, ранее описанном в Marber et al, J. Clin Invest. 95: 1446-1456 (1995)).
Получали мышей MASP-2(-/-), как описано в примере 1, и подвергали обратному скрещиванию с C57B1/6 в течение по меньшей мере 10 поколений. Семь мышей MASP-2 (-/-) и семь мышей дикого типа (+/+) подвергали анестезии с использованием кетамина/медетомидина (100 мг/кг и 0,2 мг/кг, соответственно) и помещали в положении лежа на спине на термостатически контролируемую грелку для поддержания ректальной температуры 37±0,3°C. Мышей интубировали под визуальным контролем и вентилировали комнатным воздухом при частоте дыхания 110/мин и дыхательном объеме 225 мкл/мин (вентилятор - Hugo Sachs Elektronic MiniVent Type 845, Germany).
Сбривали шерсть и делали переднелатеральный разрез кожи от левой подмышечной ямки до мечевидного отростка. Иссекали большую грудную мышцу, отрезали ее по стернальному краю и отводили в подмышечную ямку. Малую грудную мышцу отрезали по ее краниальному краю и отводили каудально. Позднее мышцу использовали в качестве мышечного лоскута, закрывающего сердце в течение окклюзии коронарной артерии. Через мышцы 5-го межреберья и париетальную плевру проникали с помощью пинцета в точке немного медиальнее края левого легкого, таким образом, избегая повреждения легкого или сердца. После проникновения через плевру пинцет осторожно направляли за плевру в сторону грудины, не трогая сердце, и плевру и межреберные мышцы иссекали с помощью питаемого от батареи каутера (Harvard Apparatus, UK). Особое внимание уделяли предотвращению любого кровотечения. Используя тот же способ, разрез при торакотомии увеличивали до средней подмышечной линии. После разрезания 4-го ребра по его грудинному краю межреберное пространство расширяли до получения доступа ко всему сердцу от основания до верхушки. Используя два небольших артериальных зажима, открывали перикард и карман перикарда приспосабливали для перемещения сердца немного вперед. Получали доступ к левой передней нисходящей коронарной артерии (LAD) и под LAD пропускали мононить 8-0 с хирургической круглой иглой. Участок наложения лигатуры на LAD располагается немного каудальнее верхушки левого предсердия, приблизительно на 1/4 вдоль линии от антривентрикулярного гребня до верхушки левого желудочка.
Все эксперименты осуществляли слепым образом, при этом исследователь не знал генотип каждого животного. После завершения инструментальных и хирургических процедур следовал период установления равновесия в течение 15 мин. Затем мышей подвергали окклюзии коронарной артерии в течение 30 мин и реперфузии в течение 120.
Модель окклюзии и реперфузии коронарной артерии
Окклюзию коронарной артерии осуществляли с использованием системы с подвешиванием грузов, как описано ранее (Eckle et al, Am J Physiol Heart Circ Physiol 2 7:H2533-H2540, 2006). Оба конца лигатуры мононити пропускали через фрагмент трубки из политена PE-10 длиной 2 мм и прикрепляли к отрезку шовного материала 5-0 с использованием цианоакрилатного клея. Затем шовный материал направляли поверх двух установленных горизонтально перемещаемых металлических прутков и к обоим концам шовного материала прикрепляли грузы по 1 г каждый. Поднимая прутки, подвешивали грузы и устанавливали контролируемое натяжение шовного материала для окклюзии LAD с определенным и постоянным давлением. Окклюзию LAD проверяли по побледнению области риска, превращения цвета перфузируемой LAD зоны из ярко-красного в фиолетовый, что свидетельствует о прекращении кровотока. Реперфузию осуществляли, опуская прутки до тех пор, пока грузы не опускались на операционную подушку и не ослаблялось натяжение лигатуры. Реперфузию проверяли по тем же трем критериям, используемым для проверки окклюзии. Мышей исключали из дальнейшего анализа при несоответствии всем трем критериям в момент начала окклюзии коронарной артерии или в течение 15 мин реперфузии, соответственно. В течение окклюзии коронарной артерии температуру и влажность поверхности сердца поддерживали, покрывая сердце мышечным лоскутом из малой грудной мышцы и закрывая торакотомический разрез влажной марлей, пропитанной 0,9% физиологическим раствором.
Измерение размера инфаркта миокарда:
Размер инфаркта (INF) и область риска (AAR) определяли с помощью планиметрии. После i.v.-инъекции 500 МЕ гепарина LAD подвергали повторной окклюзии и медленно инъецировали 300 мкл 5% (масс/об) красителя Эванса синего (Sigma-Aldrich, Poole, UK) в яремную вену для определения границ области риска (AAR). При этой стратегии краситель проникает в неишемизированную область левого желудочка и оставляет ишемизированную AAR неокрашенной. После умерщвления мышей с помощью смещения шейных позвонков быстро извлекали сердце. Сердце охлаждали на льду и заливали в блок 5% агарозы, а затем получали 8 поперечных срезов толщиной 800 мкм. Все срезы инкубировали при 37°C в течение 20 мин с 3% 2,3,5-трифенилтетразолия хлоридом (Sigma Aldrich, Poole, UK), растворенным в буфере 0,1 M Na2HPO4/NaH2PO4, доведенном до pH 7,4. Срезы фиксировали в течение ночи в 10% формальдегиде. Срезы помещали между двумя покровными стеклами и стороны каждого среза визуализировали в цифровом формате с использованием оптического сканера высокого разрешения. Затем цифровые изображения анализировали с использованием программного обеспечения SigmaScan (SPSS, US). Размер области инфаркта (бледной), области риска левого желудочка (LV) (красной) и нормально перфузируемой зоны LV (синей) определяли на каждом срезе посредством идентификации их цвета и границ цвета. Исследователь количественно анализировал и усреднял области на обеих сторонах каждого среза. Размер инфаркта вычисляли как % зоны риска для каждого животного.
РЕЗУЛЬТАТЫ: На фигуре 51A представлена оценка семи мышей WT (+/+) и семи мышей MASP-2(-/-) для определения размера инфаркта после осуществления описываемого выше способа окклюзии и реперфузии коронарной артерии. Как показано на фигуре 51A, у мышей MASP-2(-/-) наблюдали статистически значимое снижение (p<0,05) размера инфаркта по сравнению с мышами WT (+/+), что свидетельствует о протективном эффекте в отношении миокарда в модели повреждения при ишемии/реперфузии. На фигуре 51B представлено распределение отдельных тестируемых животных, свидетельствующее об очевидном протективном эффекте у мышей MASP-2(-/-).
ПРИМЕР 23
В этом примере описывают анализ мышей MASP-2(-/-) в модели ишемии/реперфузии миокарда мыши.
Уровень техники/Обоснование:
Для оценки участия MASP-2 в воспалительном реперфузионном повреждении после ишемического повреждения в результате окклюзии коронарной артерии мышей MASP-2(-/-) и MASP-2(+/+) сравнивали в мышиной модели ишемии/реперфузии (MIRP), как описано в Marber et al, J. Clin Invest. 95: 1446-1456 (1995), и в модели изолированного сердца мыши по Лангендорфу.
Способы:
Мышей MASP-2(-/-), используемых в этом исследовании, получали, как описано в примере 1. Ишемическое повреждение левого желудочка осуществляли на восьми мышах WT (MASP-2(+/+)) и одиннадцати мышах MASP-2(-/-) с использованием способов, описываемых в примере 22. Размер инфаркта (INF) и область риска (AAR) определяли с помощью планиметрии, как описано в примере 22.
Модель изолированного сердца мыши по Лангендорфу: Способ получения сердец мышей для модели изолированного сердца мыши по Лангендорфу осуществляли, как описано в F.J. Sutherland et al, Pharmacol Res 41: 613 (2000). См. также A.M. Kabir et al,. Am J Physiol Heart Circ Physiol 291: H1893 (2006); Y. Nishino et al, Circ Res 103:301 (2008) и I.G. Webb et al., Cardiovasc Res (2010)).
В кратком изложении, мышей WT (+/+) и MASP-2 (-/-) подвергали анестезии посредством интраперитонеального введения пентобарбитала (300 мг/кг) и гепарина (150 МЕ). Сердца быстро извлекали и помещали в ледяной модифицированный буфер Кребса-Хенселейта (KH, 118,5 ммоль/1 NaCl, 25,0 ммоль/1 NaHCO3, 4,75 ммоль KCl, KH2PO4 1,18, MgSO4 1,19, D-глюкоза 11,0 и CaCl2 1,41). Извлеченные сердца помещали в аппарат Лангендорфа с водяной рубашкой и ретроградно перфузировали при постоянном давлении 80 мм рт.ст. буфером KH, уравновешенным при 95% O2 и 5% CO2. Температуру перфузата поддерживали при 37°C. С помощью наполненного жидкостью баллона, введенного в левый желудочек, контролировали сократительную функцию. Баллон наполняли постепенно до достижения конечного диастолического давления от 1 до 7 мм рт.ст. Стимуляцию предсердий осуществляли при 580 ударах в минуту с использованием серебряной проволоки длиной 0,075 мм (Advent). Коронарный кровоток измеряли с помощью регулируемого по времени сбора перфузата.
Оценка инфаркта in vitro
После начала ретроградной перфузии сердца стабилизировали в течение 30 мин. Для включения в исследование все сердца должны были соответствовать следующим критериям: коронарный кровоток от 1,5 до 4,5 мл/мин, частота сердечных сокращений >300 ударов в минуту (без стимуляции), давление в левом желудочке >55 мм рт.ст., время от торакотомии до канюлирования аорты <3 мин и отсутствие стойкой аритмии при стабилизации. Затем осуществляли глобальную ишемию и реперфузию в отсутствие сыворотки. Затем все сердца подвергали глобальной ишемии в течение 30 мин посредством зажатия аортальных впускных трубок с последующей реперфузией в течение 2 часов.
Электростимуляцию прекращали при остановке сокращений в течение ишемии и начинали через 30 мин реперфузии. Через 2 часа реперфузии, сердца перфузировали в течение 1 мин 5 мл 1% трифенилтетразолия хлорида (TTC) в KH, а затем помещали в идентичный раствор при 37°C на 10 мин. Затем предсердия удаляли, и сердца промокали досуха, взвешивали и хранили при -20°C в течение периода времени до 1 недели.
Затем сердца размораживали, помещали в 2,5% глутаральдегид на 1 минуту, а затем в 5% агарозу. Получали срезы агарозных блоков сердца от верхушки до основания толщиной 0,7 мм с использованием вибратома (Agar Scientific). После получения срезы хранили в течение ночи в 10% формальдегиде при комнатной температуре перед переносом в PBS еще на один день при 4°C. Затем срезы зажимали между пластинами Perspex (на расстоянии 0,57 мм) и визуализировали с использованием сканера (Epson, модель G850A). После увеличения осуществляли планиметрию с использованием программного обеспечения для анализа изображений (SigmaScan Pro 5.0, SPSS), и площадь поверхности всего TTC-отрицательного миокарда левого желудочка переводили в объем, умножая на толщину ткани. Для каждого сердца после суммирования отдельных срезов объем TTC-отрицательного инфаркта выражали как процентную долю, или изображали в виде зависимости от, объема левого желудочка.
Результаты:
Размер области инфаркта (бледной), области риска левого желудочка (LV) (красной) и нормально перфузируемой зоны LV (синей) определяли на каждом срезе посредством идентификации их цвета и границ цвета. Исследователь количественно анализировал и усреднял области на обеих сторонах каждого среза. Объем инфаркта вычисляли как % зоны риска (% RZ) для каждого животного.
На фигуре 52A представлена оценка восьми мышей WT (+/+) и одиннадцати мышей MASP-2(-/-) для определения размера инфаркта после осуществления описываемого выше способа окклюзии и реперфузии коронарной артерии. На фигуре 52A графически представлена средняя площадь области риска (AAR, мера площади области, поврежденной при ишемии) и объем инфаркта (INF, мера повреждения миокарда) как процентная доля всего объема миокарда. Как показано на фигуре 52A, хотя и не наблюдали значимых различий AAR между двумя группами, объемы INF являлись значимо меньшими у мышей MASP-2(-/-) по сравнению с однопометными WT, что, таким образом, свидетельствует о протективном эффекте при повреждении миокарда в этой модели MIRP в отсутствие MASP-2.
На фигуре 52B графически представлено отношение INF, отложенного в виде зависимости от AAR, как % объема миокарда левого желудочка (LV). Как показано на фигуре 52B, в случае любой указанной AAR у животных MASP-2(-/-) наблюдали высоко значимое снижение размера инфаркта по сравнению с однопометными WT.
На фигурах 52C и 52D представлены результаты анализа инфаркта миокарда в перфузируемых буфером сердцах мышей WT (+/+) и MASP-2(-/-), полученных в соответствии с моделью изолированного сердца мыши по Лангендорфу, в которых глобальную ишемию и реперфузию осуществляли в отсутствие сыворотки. Как показано на фигурах 52C и 52D, не наблюдали значимых различий объема инфаркта (INF) между сердцами мышей MASP-2(-/-) и WT (+/+), что позволяет предполагать, что различия в размере инфаркта, представленные на фигурах 52A и 52B, вызваны факторами плазмы, а не более низкой восприимчивостью ткани миокарда мышей MASP-2(-/-) к ишемическому повреждению.
В совокупности, эти результаты свидетельствуют о том, что дефицит MASP-2 значимо снижает повреждение миокарда после реперфузии ишемизированного сердца в модели ишемии/реперфузии миокарда мыши, и подтверждают применимость ингибиторов MASP-2 в лечении и профилактике повреждения при ишемии/реперфузии.
ПРИМЕР 24
В этом примере описывают открытие новой, опосредованной лектиновым путем и MASP-2-зависимой активации компонента комплемента C3 в обход C4.
Обоснование:
Важнейший благоприятный терапевтический эффект применения ингибиторов активации комплемента для ограничения повреждения миокарда при ишемии/реперфузии (MIRI) был убедительно продемонстрирован на экспериментальной модели инфаркта миокарда крысы двумя десятилетиями ранее: Рекомбинантный sCR1, растворимое укороченное производное поверхностного клеточного рецептора комплемента типа-1 (CR1), вводили внутривенно и оценивали его эффект на модели MIRI крысы in vivo. Введение sCR1 снижало объем инфаркта более чем на 40% (Weisman, H.F., et al., Science 249: 146-151 (1990)). Терапевтический потенциал этого рекомбинантного ингибитора впоследствии продемонстрировали в клиническом испытании, показавшем, что введение sCR1 пациентам с MI предотвращало потерю сократимости в постишемическом сердце (Shandelya, S., et al., Circulation 87:536-546 (1993)). Однако, основной механизм, приводящий к активации комплемента в ишемизированной ткани, в конечном итоге, не установили, в основном, по причине отсутствия подходящих экспериментальных моделей, ограниченного понимания молекулярных процессов, приводящих к активации комплемента на лишенных кислорода клетках, и взаимного влияния и синергизма между различными путями активации комплемента.
Как основополагающий компонент иммунного ответа, система комплемента обеспечивает защиту от проникающих микроорганизмов посредством антитело-зависимого и -независимого механизмов. Она контролирует многие клеточные и гуморальные взаимодействия в рамках иммунного ответа, включая хемотаксис, фагоцитоз, адгезию клеток и B-клеточную дифференцировку. Каскад комплемента инициируется тремя различными путями: классическим путем, альтернативным путем и лектиновым путем. Распознающий субкомпонент C1q классического пути связывается со множеством мишеней, важнее всего - с иммунными комплексами, для инициации поэтапной активации ассоциированных сериновых протеаз C1r и C1s, обеспечивая основной механизм клиренса патогена и иммунных комплексов после вовлечения адаптивной иммунной системой. Связывание C1q с иммунными комплексами приводит к конвертации димера зимогена C1r в его активную форму для расщепления и, таким образом, активации C1s. C1s трансформирует связывание C1q в активацию комплемента двумя этапами расщепления: Сначала он конвертирует C4 в C4a и C4b, а затем расщепляет C4b-связанный C2 для образования конвертазы C3 C4b2a. Этот комплекс конвертирует избыточный плазматический компонент C3 в C3a и C3b. Накопление C3b в непосредственной близости от комплекса C4b2a сдвигает субстратную специфичность C3 к C5 для образования конвертазы C5 C4b2a(C3b)n. Комплексы конвертаз C3 и C5, образовавшиеся при активации классического пути, идентичны образующимся при активации лектинового пути. В альтернативном пути спонтанный низкоуровневый гидролиз компонента C3 приводит к накоплению фрагментов белка на поверхности клеток, запуская активацию комплемента на чужеродных клетках, в то время как ассоциированные с клетками регуляторные белки в тканях хозяина предотвращают активацию, и таким образом, самоповреждение. Как и альтернативный путь, лектиновый путь может активироваться в отсутствие иммунных комплексов. Активация инициируется связыванием мультимолекулярного комплекса активации лектинового пути с патоген-ассоциированными молекулярными паттернами (PAMP), в основном, углеводными структурами, присутствующими на бактериальных, грибковых или вирусных патогенах, или аномальными паттернами гликозилирования на апоптотических, некротизированных, злокачественных или лишенных кислорода клетках (Collard, CD., et al, Am. J. Pathol. 756: 1549-1556 (2000); Walport, M.J., N. Engl. J. Med. 544: 1058-1066 (2001); Schwaeble, W., et al, Immunobiology 205:455-466 (2002); и Fujita, T., Nat. Rev. Immunol. 2:346-353 (2002)).
Маннозо-связывающий лектин (MBL) являлся первым распознающим углеводы субкомпонентом, для которого показано образование комплексов с группой новых сериновых протеаз, названных MBL-ассоциированными сериновыми протеазами (MASP) и пронумерованными согласно последовательности их открытия (т.е. MASP-1, MASP-2 и MASP-3). У человека комплексы активации лектинового пути могут образовываться с четырьмя альтернативными распознающими углеводы субкомпонентами с различно специфичностью связывания углеводов, т.е. MBL2 и тремя различными членами семейства фиколинов, а именно L-фиколином, H-фиколином и M-фиколином, и MASP. Две формы MBL, MBL A и MBL C, и фиколин-A образуют комплексы активации лектинового пути с MASP в плазме мыши и крысы. Ранее авторы настоящего изобретения клонировали и охарактеризовали MASP-2 и дополнительный укороченный продукт гена MASP-2 размером 19 кДа, названный MAp19 или sMAP, у человека, мыши и крысы (Thiel, S., et al, Nature 556:506-510 (1997);. Stover, CM., et al, J. Immunol. 762:3481-3490 (1999); Takahashi, M., et al, Int. Immunol. 77:859-863 (1999); и Stover, CM., et al, J. Immunol. 765:6848-6859 (1999)). MAp19/sMAP не имеет протеазной активности, но может регулировать активацию лектинового пути, конкурируя с MASP за связывание с распознающими углеводы комплекса (Iwaki, D. et al, J. Immunol. 777:8626-8632 (2006)).
Существует убедительное доказательство того, что из трех MASP только MASP-2 необходима для преобразования связывания распознающих комплексов лектинового пути в активацию комплемента (Thiel, S., et al. (1997); Vorup-Jensen, T., et al, J. Immunol. 765:2093-2100 (2000); Thiel, S., et al, J. Immunol. 765:878-887 (2000); Rossi, V., et al, J. Biol. Chem. 27(5:40880-40887 (2001)). Этот вывод подтвержден фенотипом большинства недавно описанных линий мышей с дефицитом MASP-1 и MASP-3. За исключением задержки начала опосредованной лектиновым путем активации комплемента in vitro, мыши с дефицитом MASP-1/3 сохраняют функциональную активность лектинового пути. Восстановление сыворотки с дефицитом MASP-1- и MASP-3 с помощью рекомбинантного MASP-1 позволяет преодолеть эту задержку активации лектинового пути, свидетельствуя о том, что MASP-1 может способствовать активации MASP-2 (Takahashi, M., et al, J. Immunol. 750:6132-6138 (2008)). В недавнем исследовании показано, что MASP-1 (и, возможно, также MASP-3) необходима для конвертации фермента активации альтернативного пути фактора D из его зимогена в ферментативно активную форму (Takahashi, M., et al, J. Exp. Med. 207:29-37 (2010)). Физиологическую значимость этого процесса подчеркивает отсутствие функциональной активности альтернативного пути в плазме мышей с дефицитом MASP-1/3.
У недавно полученных линий мышей с целенаправленными комбинированными дефицитами распознающих углеводы субкомпонентов лектинового пути MBL A и MBL C все равно может происходить инициация активации лектинового пути через оставшийся распознающий субкомпонент лектинового пути мыши фиколин A (Takahashi, K., et al, Microbes Infect. 4:773-784 (2002)). Отсутствие какой-либо остаточной функциональной активности лектинового пути у мышей с дефицитом MASP-2 обеспечивает получение доказательной модели для исследования роли этого эффекторного плеча врожденного гуморального иммунитета в норме и при патологии.
Доступность линий мышей с дефицитом C4 и MASP-2 позволяет авторам настоящего изобретения определять новый специфичный для лектинового пути, но MASP-2-зависимый путь активации компонента комплемента C3 в обход C4. Необходимость участия этого нового опосредованного лектиновым путем способа активации в обход C4 по отношению к постишемической потери ткани подтверждается выраженным протективным фенотипом мышей с дефицитом MASP-2 при MIRI, в то время как у мышей с дефицитом C4, тестируемых в той же модели, не обнаруживали протективного эффекта.
В этом примере авторы настоящего изобретения описывают новый опосредованный лектиновым путем и MASP-2-зависимый путь активации компонента комплемента C3 в обход C4. Физиологическую значимость этого нового пути активации определяли по протективному фенотипу животных с дефицитом MASP-2 в экспериментальной модели повреждения миокарда при ишемии/реперфузии (MIRI), в которой у животных с дефицитом C4 не обнаруживали протективного эффекта.
Способы:
У мышей с дефицитом MASP-2 не обнаруживали аномалий развития. Мышей с дефицитом MASP-2 получали, как описано в примере 1. Гетерозиготные (+/-) и гомозиготные (-/-) мыши с дефицитом MASP-2 являлись здоровыми и фертильными, и у них не обнаруживали аномалий развития. Продолжительность их жизни являлась схожей с однопометными WT (>18 месяцев). Перед исследованием фенотипа этих мышей в экспериментальных моделях заболеваний имеющуюся у авторов настоящего изобретения линию MASP-2(-/-) подвергали обратному скрещиванию в течение одиннадцати поколений на фоне C57BL/6. Полное отсутствие мРНК MASP-2 подтверждали с помощью "нозерн"-блоттинга выбранных поли-A+ препаратов РНК печени, в то время как мРНК размером 1,2 т.п.н., кодирующая MApl9 или sMAP (укороченный продукт альтернативного сплайсинга гена MASP2), экспрессировалась в избытке.
При анализе с помощью qRT-ПЦР с использованием пар праймеров, специфичных для кодирующей последовательности домена сериновой протеазы MASP-2 (B-цепь) или оставшейся части кодирующей последовательности для A-цепи, у мышей MASP-2(-/-) не обнаруживали мРНК, кодирующую B-цепь, в то время как количество транскрипта мРНК разрушенной A-цепи значимо повышалось. Аналогично, у мышей MASP-2(+/-) и MASP-2(-/-) повышалось количество мРНК, кодирующей MAp19/sMAP. Уровни MASP-2 в плазме, определяемые с помощью ELISA у пяти животных каждого генотипа, составляли 300 нг/мл для контролей WT (диапазон 260-330 нг/мл), 360 нг/мл для гетерозиготных мышей (диапазон 330-395 нг/мл) и являлись неопределяемыми у мышей MASP-2(-/-). Используя qRT-ПЦР, определяли профили экспрессии мРНК, свидетельствующие о том, что у мышей MASP-2(-/-) экспрессируются мРНК MBL A, MBL C, фиколина A, MASP-1, MASP-3, C1q, C1rA, C1sA, фактора B, фактора D, C4, и C3 в количестве, схожим с таковым у однопометных животных с достаточной MASP-2 (данные не представлены).
Уровни C3 в плазме мышей MASP-2(-/-) (n=8) и однопометных мышей MASP-2(+/+) (n=7) измеряли с использованием коммерчески доступного набора для ELISA C3 мыши (Kamiya, Biomedical, Seattle, WA). Уровни C3 у мышей с дефицитом MASP-2 (в среднем 0,84 мг/мл, ±0,34) являлись схожими с таковыми у контролей WT (в среднем 0,92, ±0,37).
Результаты:
MASP-2 необходима для функциональной активности лектинового пути
Как представлено в настоящем описании и US 7919094, при анализах in vitro плазмы MASP-2-/- наблюдали полное отсутствие функциональной активности лектинового пути на активирующих покрытых маннозой и зимозаном поверхностях в отношении активации C4 и C3. Аналогично, в плазме MASP-2-/- не определяли зависящее от лектинового пути расщепление C4 или C3 на поверхностях, покрытых N-ацетилглюкозамином, связывающимся и запускающим активацию через MBL A, MBL C и фиколин A (данные не представлены).
При анализах сывороток и плазмы мышей MASP-2(-/-) однозначно определяли, что MASP-2 необходима для активации комплемента лектиновым путем, и что ни MASP-1, ни MASP-3 не способны поддерживать или восстанавливать активность лектинового пути при дефиците MASP-2 (данные не представлены).
Однако полный дефицит функциональной активности лектинового пути оставляет другие пути активации комплемента интактными: плазма MASP-2-/- все равно может активировать комплемент классическим (фигура 53A) и альтернативным путем (фигура 53B). На фигурах 53A и 53B символом "*" указывают сыворотку WT (MASP-2(+/+)); символом "•" указывают сыворотку WT (с истощением C1q); символом "□" указывают сыворотку MASP-2(-/-); и символом "Δ" указывают сыворотку MASP-2(-/-) (с истощением C1q).
На фигуре 53A графически представлено, что мыши MASP-2(-/-) сохраняют функциональный классический путь: накопление C3b анализировали на планшетах для микротитрования, покрытых иммунными комплексами (полученными in situ покрыванием BSA, а затем добавлением IgG козла против BSA). На фигуре 53B графически представлено, что мыши с дефицитом MASP-2 сохраняют функциональный альтернативный путь: накопление C3b анализировали на покрытых зимозаном планшетах для микротитрования в условиях, делающих возможной активацию только альтернативного пути (буфер, содержащий Mg2+ и EGTA). Результаты, представленные на фигуре 53 A и на фигуре 53B, являются средними значениями для двух повторений и характерными для трех независимых экспериментов. Одинаковые символы для обозначения источников сыворотки использовали на всем протяжении описания. Эти результаты показывают, что у мышей с дефицитом MASP-2 присутствует функциональный альтернативный путь, что подтверждается результатами, представленными на фигуре 53B, полученными в экспериментальных условиях, предназначенных для прямого запуска альтернативного пути, при инактивации классического пути и лектинового пути.
Лектиновый путь активации комплемента критически важен для воспалительной потери ткани при повреждении миокарда при ишемии/реперфузии (MIRI)
Как описано в примере 23, для исследования участия функциональной активности лектинового пути в MIRI, авторы настоящего изобретения сравнивали мышей MASP-2(-/-) и однопометные контроли WT в модели MIRI после временного наложения лигатуры и реперфузии левой передней нисходящей ветви коронарной артерии (LAD). Результаты, описанные в примере 23, четко свидетельствуют о том, что животные с дефицитом MASP-2 демонстрируют значимую степень защиты со значимо сниженными размерами инфаркта (p<0,01) по сравнению с однопометными животными с достаточным лектиновым путем.
Наличие или отсутствие компонента комплемента C4 не оказывает влияния на степень ишемической потери ткани при MIRI. Используя способ, описанный в пример 23, авторы настоящего изобретения оценивали влияние дефицита C4 на размер инфаркта после экспериментального MIRI. Как показано на фигуре 54A и на фигуре 54B, наблюдали почти идентичные размеры инфаркта у мышей с дефицитом C4 и однопометных мышей WT. На фигуре 54A графически представлена индуцированная MIRI потеря ткани после наложения лигатуры на LAD и реперфузии у мышей C4 (-/-) (n=6) и совпадающих однопометных контролей WT (n=7). Области риска (AAR) и размер инфаркта (INF) определяли, как описано для фигуры 52. На фигуре 54B графически представлен INF как функция AAR, четко свидетельствующий о том, что мыши C4 (-/-) так же восприимчивы к MIRI, как и контроли WT (пунктирная линия).
Эти результаты свидетельствуют о том, что мыши с дефицитом C4 не защищены от MIRI. Этот результат являлся неожиданным, т.к. он противоречит широко распространенной точке зрения о том, что основной фрагмент активации C4, C4b, является необходимым компонентом конвертазы C3 классического и лектинового пути C4b2a. Таким образом, авторы настоящего изобретения оценивали, можно ли определять остаточную специфическую активацию компонента комплемента C3 лектиновым путем в плазме мыши и человека с дефицитом C4.
Лектиновый путь может активировать компонент комплемента C3 в отсутствие C4 через новый MASP-2-зависимый путь активации в обход C4
Обнадеженные литературными данными о существовании пути активации в обход C4 в сыворотке морских свинок с дефицитом C4 (May, J.E., and M. Frank, J. Immunol. 777: 1671-1677 (1973)), авторы настоящего изобретения анализировали, могут ли мыши с дефицитом C4 иметь остаточную функциональную активность классического или лектинового пути, и контролировали активацию C3 в специфичных для пути условиях анализа, исключающих участие альтернативного пути.
Накопление C3b анализировали на покрытых маннозой планшетах для микротитрования с использованием рекальцифицированной плазмы при концентрациях плазмы, препятствующих активации альтернативного пути (1,25% и ниже). Хотя не определяли расщепление C3 в плазме с дефицитом C4, тестируемой на активацию классического пути (данные не представлены), наблюдали выраженную остаточную активность расщепления C3 в плазме мышей с дефицитом C4 при инициации активации комплемента через лектиновый путь. Зависимость от лектинового пути наблюдали при конкурентном ингибировании расщепления C3 после преинкубации разведений плазмы с дефицитом C4 с растворимой маннозой (см. фигуру 55A). Как показано на фигурах 55A-D, MASP-2-зависимую активацию C3 наблюдали в отсутствие C4. На фигуре 55A графически представлено накопление C3b в плазме мыши C4 (+/+) (кресты) и C4 (-/-) (незакрашенные круги). Преинкубация плазмы C4 (-/-) с избытком маннозы (1 мкг/мл) в жидкой фазе перед анализом полностью ингибирует накопление C3 (закрашенные круги). Результаты являются характерными для 3 независимых экспериментов. На фигуре 55B графически представлены результаты эксперимента, в котором плазму (1%) мышей WT (кресты), с дефицитом MASP-2 (незакрашенные квадраты) и C4 (-/-) (незакрашенные круги) смешивали с различными концентрациями mAbM11 крысы против MASP-2 (абсцисса), и анализа накопления C3b на планшетах, покрытых маннозой. Результаты представляют собой средние значения (±SD) для 4 анализов (два повторения 2 анализов для каждого типа плазмы).
На фигуре 55C графически представлены результаты эксперимента, в котором нормальную плазму человека: объединенную NHS (кресты), плазму C4 (-/-) (незакрашенные круги) и плазму C4 (-/-), преинкубированную с 1 мкг/мл маннозы (закрашенные круги), инкубировали в покрытых маннозой лунках и измеряли накопление C3b. Результаты являются характерными для трех независимых экспериментов.
На фигуре 55D графически представлено ингибирование накопления C3b в плазме (1%) человека с достаточным C4 и дефицитом C4 с помощью mAbH3 человека против MASP-2 (средние ± SD для трех повторений).
Как показано на фигуре 55B, в параллельно анализируемой плазме MASP-2(-/-) не определяли зависящую от лектинового пути активацию C3, что свидетельствует о том, что этот путь активации C3 в обход C4 является MASP-2-зависимым.
Для дополнительного подтверждения этих результатов авторы настоящего изобретения получали серию рекомбинантных ингибиторных mAb, выделенных из фаговых библиотек антител посредством скрининга на аффинность против рекомбинантной MASP-2A человека и крысы (где остаток серина в активном протеазном домене заменяли остатком аланина с помощью сайт-специфического мутагенеза для предотвращения аутолитической деградации антигена). Рекомбинантные антитела против MASP-2 (AbH3 и AbM11) выделяли из комбинаторных библиотек антител (Knappik, A., et al, J. Mol. Biol. 296:51-86 (2000)), с использованием рекомбинантных MASP-2A человека и крысы в качестве антигенов (Chen, C.B. and Wallis, J. Biol. Chem. 276:25894-25902 (2001)). Fab2-фрагмент против крысы, сильно ингибирующий опосредованную лектиновым путем активацию C4 и C3 в плазме мыши (IC50~1 нМ), преобразовывали в полноразмерное антитело IgG2a. Из крыс получали поликлональную антисыворотку против MASP-2A мыши. Эти инструменты позволяли авторам настоящего изобретения подтвердить зависимость этого нового специфичного для лектинового пути способа активации C3 в обход C4 от MASP-2, как описано ниже.
Как показано на фигуре 55B, M211, ингибиторное моноклональное антитело, селективно связывающееся с MASP-2 мыши и крысы, ингибировало активацию C3 в обход C4 в плазме мышей с дефицитом C4, а также активацию C3 в плазме мышей WT через лектиновый путь в зависимости от концентрации со схожими значениями IC50. Все анализы осуществляли с использованием сильных разведений плазмы, делающих альтернативный путь активации нефункциональным (при этом наибольшая концентрация плазмы составляла 1,25%).
Для исследования наличия аналогичной специфичной для лектинового пути активации C3 в обход C4 у людей, авторы настоящего изобретения анализировали плазму донора с наследственным дефицитом обоих генов C4 человека (т.е. C4A и C4B), приводящим к полному отсутствию C4 (Yang, Y., et al, J. Immunol. 775:2803-2814 (2004)). На фигуре 55C показана, что плазма этого пациента эффективно активировала C3 в сильных разведениях плазмы (делающих альтернативный путь активации нефункциональным). Специфичный для лектинового пути способ активации C3 на планшетах, покрытых маннозой, наблюдали в плазме мыши с дефицитом C4 (фигура 55A) и плазме человека с дефицитом C4 (фигура 55C) при добавлении избыточных концентраций маннозы в жидкой фазе. Зависимость этого механизма активации C3 MASP-2 от в плазме человека с дефицитом C4 оценивали с использованием AbH3, моноклонального антитела, специфически связывающегося с MASP-2 человека и нарушающего функциональную активность MASP-2. Как показано на фигуре 55D, AbH3 ингибировало накопление C3b (и C3dg) в плазме человека с достаточным C4 и дефицитом C4 со сравнимой эффективностью.
Для оценки возможной роли других компонентов комплемента в активации C3 в обход C4 авторы настоящего изобретения тестировали плазму мышей MASP-1/3(-/-) и Bf/C2(-/-) вместе с плазмой MASP-2(-/-), C4(-/-) и C1q (-/-) (в качестве контролей) в условиях анализа, специфичных для лектинового пути и классического пути. Относительную величину расщепления C3 откладывали в зависимости от количества накопленного C3 при использовании плазмы WT.
На фигуре 56A графически представлен сравнительный анализ активности конвертазы C3 в плазме линий мышей с различными дефицитами комплемента, тестируемых в условиях анализа, специфичных для лектинового пути активации или классического пути активации. Разбавленные образцы плазмы (1%) мышей WT (n=6), мышей MASP-2(-/-) (n=4), мышей MASP-1/3(-/-) (n=2), мышей C4(-/-) (n=8), мышей C4/MASP-1/3(-/-) (n=8), мышей Bf/C2(-/-) (n=2) и мышей C1q(-/-) (n=2) тестировали параллельно. Восстановление плазмы Bf/C2(-/-) с использованием 2 мкг/мл рекомбинантного C2 крысы (Bf/C2(-/-) + C2) восстанавливало накопление C3b. Результаты представляют собой средние значения (±SD). **p<0,01 (по сравнению с плазмой WT). Как показано на фигуре 56A, значительное накопление C3 наблюдали в плазме C4(-/-), тестируемой в специфичных для лектинового пути условиях анализа, но не в условиях, специфичных для классического пути. Кроме того, не наблюдали накопление C3 в плазме с дефицитом MASP-2 при активации лектиновым путем, при этом в той же плазме накапливался C3 при активации классическим путем. В плазме MASP-1/3(-/-) накопление C3 происходило в условиях анализа, специфичных и для лектинового, и для классического пути. Не наблюдали накопление C3 в плазме с комбинированным дефицитом C4 и MASP-1/3 в условиях анализа, специфичных и для лектинового, и для классического пути. Не определяли накопление C3 в плазме Bf/C2(-/-) через лектиновый путь или через классический путь. Однако, восстановление плазмы мыши C2/Bf-/- с использованием рекомбинантного C2 восстанавливало опосредованное и лектиновым путем, и классическим путем расщепление C3. Условия анализа проверяли с использованием плазмы C1q(-/-). На фигуре 56B графически представлена временная кинетика активности конвертазы C3 в плазме мышей различных линий с дефицитом комплемента, плазме WT, fB(-/-), C4(-/-), MASP-1/3(-/-) и MASP-2(-/-), тестируемой в условиях анализа, специфичных для лектинового пути активации (1% плазма, результаты являются характерными для трех независимых экспериментов). Как показано на фигуре 56B, хотя не наблюдали расщепление C3 в плазме MASP-2(-/-), плазма fB(-/-) расщепляла C3 с кинетикой, аналогичной таковой для плазмы WT. Значимую задержку зависящей от лектинового пути конвертации C3 в C3b (и C3dg) наблюдали в плазме C4(-/-), а также в плазме с дефицитом MASP-1/3. Недавно показано, что эта задержка активации C3 в плазме MASP-1/3(-/-) является MASP-1-, а не MASP-3-зависимой (Takahashi, M., et al., J. Immunol. 750:6132-6138 (2008)).
Обсуждение:
Результаты, описанные в этом примере, убедительно подтверждают, что функциональная активность MASP-2 необходима для активации C3 лектиновым путем при наличии и отсутствии C4. Кроме того, C2 и MASP-1 необходимы для работы этого нового специфичного для лектинового пути способа активации C3 в обход C4. Сравнительный анализ функциональной активности лектинового пути в плазме MASP-2 (-/-), а также плазме C4 (-/-) показал существование ранее неизвестного C4-независимого, но MASP-2-зависимого пути активации компонента комплемента C3, а также то, что C3 может активироваться зависящим от лектинового пути способом при полном отсутствии C4. Хотя подробная молекулярная композиция и последовательность события активации этого нового MASP-2-зависимого пути активации конвертазы C3 остается предметом изучения, полученные авторами настоящего изобретения результаты свидетельствуют о том, что для этого нового пути активации в обход C4 дополнительно необходимо наличие компонента комплемента C2, а также MASP-1. Утрату активности опосредованного лектиновым путем расщепления C3 в плазма мышей с комбинированным дефицитом C4 и MASP-1/3 можно объяснить недавно описанной ролью MASP-1 в усилении MASP-2-зависимой активации комплемента посредством прямого расщепления и активации MASP-2 (Takahashi, M., et al, J. Immunol. 750:6132-6138 (2008)). Аналогично, MASP-1 может способствовать функциональной активности MASP-2 благодаря своей способности расщеплять C2 (Moller-Kristensen, et al., Int. Immunol. 19:141-149 (2007)). Обе активности могут служить объяснением сниженной скорости расщепления C3 через лектиновый путь активации плазмой с дефицитом MASP-1/3 и того, почему MASP-1 может являться необходимой для поддержания конвертации C3 через путь активации в обход C4.
Показано, что неспособность плазмы C2/fB (-/-) активировать C3 через лектиновый путь является C2-зависимой, т.к. добавление рекомбинантного C2 крысы в плазму C2/fB (-/-) восстанавливало способность восстановленной плазмы активировать C3 на планшетах, покрытых маннозой.
Данные о том, что дефицит C4, в частности, нарушает классический путь активации комплемента, в то время как лектиновый путь сохраняет физиологически критический уровень активности конвертазы C3 с помощью MASP-2-зависимого пути активации в обход C4, требует переоценки роли лектинового пути в различных моделях заболеваний, включая экспериментальную инфекцию S. pneumoniae (Brown, J. S., et al, Proc. Natl. Acad. Sci. U. S. A. 99: 16969-1691 (2002)); экспериментальный аллергический энцефаломиелит (Boos, L.A., et al, Glia 49: 158-160 (2005)); и модели C3-зависимой регенерации печени мыши (Clark, A., et al, Mol. Immunol. 45:3125-3132 (2008)). Последняя группа показала, что у мышей с дефицитом C4 C3 может активировать независимо от альтернативного пути, т.к. ингибирование альтернативного пути in vivo посредством антитело-опосредованного истощения функциональной активности фактора B не влияло на зависящую от расщепления C3 регенерацию печени у мышей C4 (-/-) (Clark, A., et al. (2008)). Этот опосредованный лектиновым путем способ активации C3 в обход C4 также может являться объяснением отсутствия протективного фенотипа при дефиците C4 в используемой авторами настоящего изобретения модели MIRI, а также в описанной ранее модели отторжения аллотрансплантата почки (Lin, T., et al., Am. J. Pathol. 168: 1241-1248 (2006)). В отличие от этого, результаты, недавно полученные авторами настоящего изобретения, независимо показали значимый протективный фенотип у мышей MASP-2(-/-) в моделях трансплантации почки (Farrar, C.A., et al., Mol. Immunol. 46:2832 (2009)).
В заключение, результаты, представленные в этом примере, подтверждают точку зрения о том, что MASP-2-зависимая активация C3 в обход C4 является физиологически значимым механизмом, который может быть важен в условиях, когда доступность C4 ограничивает активацию C3.
ПРИМЕР 25
В этом примере показано, что отсутствие функциональной активности MASP-2 приводит к значимой степени защиты от желудочно-кишечного повреждения при ишемии/реперфузии (GIRI).
Обоснование:
Авторы настоящего изобретения исследовали роль MASP-2 в GIRI с использованием известной мышиной модели (Zhang, M. et al. Proc. Natl. Acad. Sci. U. S. A. 101, 3886-3891 (2004); Zhang, M. et al. J. Exp. Med. 203, 141-152 (2006)).
Способы:
Мышей с дефицитом MASP-2 получали, как описано в примере 1. Мышей MASP-2 (-/-) и однопометных контролей WT подвергали острой ишемии кишечника посредством хирургического наложения зажима на верхнюю брыжеечную артерию в течение 40 минут с последующей реперфузией в течение трех часов. Хирургический протокол GIRI осуществляли, как описано ранее (Zhang, M., et al, Proc. Natl. Acad. Sci. U.S.A. 707:3886-3891 (2004)). После анестезии осуществляли лапаротомию и устанавливали хирургический микрозажим на верхнюю брыжеечную артерию (SMA). Через 40 минут ишемии микрозажим удаляли, и ишемизированной ткани позволяли реперфузироваться в течение трех часов. Ложнооперированных контролей подвергали лапаротомии без наложения зажима на SMA. После реперфузии животных умерщвляли и собирали соответствующие сегменты дистальных отделов тонкого кишечника.
Повреждение кишечника оценивали с помощью полуколичественной шкалы оценки патологии на 200-400 ворсинках в определенной области тонкого кишечника, 4 см на тканевой срез. Криостатные срезы окрашивали гематоксилином и эозином, кодировали слепым образом и исследовали с помощью световой микроскопии. Результаты по шкале оценки патологии оценивали, как описано (Zhang, et al, 2004, выше). В первой серии экспериментов оценивали GIRI у самок MASP-2 (-/-) возрастом 8 недель и однопометных контролей MASP-2 (+/+). Во второй серии экспериментов, исследовали шесть групп самок мышей WT C57BL/6 возрастом 8 недель: ложнооперированные мыши и I/R-оперированные мыши, которым предварительно вводили физиологический раствор; или изотипическое контрольное антитело; или антитело mAbM11 против MASP-2. Антитела (каждое в дозе 1 мг/кг) или физиологический раствор инъецировали i.p. за 18 часов до хирургической операции.
Результаты:
На фигуре 57A графически показано, что у мышей MASP-2(-/-) наблюдали значимую степень защиты от тяжелого GIRI-повреждения после временной (40 мин) окклюзии брыжеечной артерии и реперфузии (3 часа) ишемизированной ткани кишечника. (*p<0,05, как определяли с помощью t-критерия Стьюдента). Как показано на фигуре 57A, у мышей MASP-2(-/-) наблюдали значимое снижение I/R-повреждения ткани по сравнению с однопометными животными WT (баллы по шкале оценки патологии I/R-группы MASP-2(-/-): 4±1, n=6; баллы по шкале оценки патологии I/R-группы MASP-2(+/+): 11±3, n=7; P<0,05).
Для оценки того, можно ли достигать временного ингибирования функциональной активности MASP-2 с использованием селективных ингибиторов MASP-2 на основе антител in vivo, авторы настоящего изобретения оценивали степень и длительность активности ингибирования лектинового пути мышиным ингибитором MASP-2 mAbM11 после i.p.-инъекции в дозе 0,6 мг/кг масса тела. После болюсной инъекции кровь собирали посредством сердечной пункции в моменты времени 0 часов, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа и 7 дней, 10 дней, 14 дней и 17 дней, и анализировали плазму на опосредованную лектиновым путем активацию C4 способами, описываемыми в Petersen, et al, J. Immunol. Methods 257:107-116 (2001), включенном в настоящее описание в качестве ссылки.
На фигуре 57B проиллюстрированы результаты, полученные за время абляции функциональной активности лектинового пути in vivo, осуществляемой с помощью однократной болюсной интраперитонеальной инъекции рекомбинантного антитела mAbM11 против MASP-2 мыши (0,6 мг/кг массы тела). В указанные моменты времени группы мышей (n=3) умерщвляли, сыворотки получали и анализировали на LP-зависимую активацию C4. Относительную функциональную активность LP нормировали по активности LP в объединенных сыворотках наивных мышей, измеряемой в отсутствие (100%) или в присутствие 100 нМ блокирующего антитела (0%). Результаты представляют собой средние значения (±SEM) для образцов плазмы от трех различных мышей в каждый момент времени.
Результаты, представленные на фигуре 57B, отражают относительную абляцию зависящей от лектинового пути активации C4 в виде относительной процентной доли опосредованной лектиновым путем активации C4 до введения антитела. Результаты свидетельствуют о том, что введение антитела приводит к полной абляции функциональной активности лектинового пути в течение шести часов после введения антитела. Функциональная активность лектинового пути полностью отсутствовала в пределах до 48 часов после введения и не восстанавливалась значимо (менее чем 10% уровней активности до введения антитела) в пределах до семи дней.
Для исследования того, может ли терапевтическое истощение функциональной активности MASP-2 защищать животных от GIRI, мышам WT (самцам C57BL/6J возрастом 8-10 недель) инъецировали mAbM11 (i.p., 1 мг/кг массы тела), или идентичную дозу неродственного изотипического контрольного антитела (i.p., 1 мг/кг массы тела) или физиологический раствор за 18 часов до кишечной I/R или ложной операции.
На фигуре 57C графически представлен протективный эффект введения mAb против MASP-2 в отношении тяжести патологии при GIRI. Мышам вводили 1 мг/кг mAbM11 (n=10) или неродственное изотипическое контрольное антитело (n=10) или инъецировали только физиологический раствор (n=10) за 24 часа до GI-ишемии в течение 40 мин с последующей реперфузией в течение трех часов. (*p<0,05 при сравнении животных, которым вводили антитело, ингибирующее MASP-2, с мышами, которым вводили неродственное изотипическое контрольное антитело или физиологический раствор). Ложнооперированных животных (n=5 на группу) обрабатывали идентичным образом, за исключением того, что на брыжеечную артерию не устанавливали зажим.
На фигуре 57D показано гистологическое представление GIRI-опосредованной патологии тонкого кишечника у мышей WT C57BL/6, которым предварительно делали однократную интраперитонеальную инъекцию изотонического физиологического раствора, изотипического контрольного антитела (1 мг/кг массы тела) или рекомбинантного антитела mAbM1l против MASP-2 мыши (1 мг/кг массы тела) за 12 часов до индукции GIRI, и соответствующих ложнооперированных контролей. Стрелками указаны субэпителиальные пространства люминальной части ворсинок (отличающиеся отсутствием клеточного содержимого под непрерывным эпителиальным слоем) как типичные черты патологии GIRI (увеличение ×100).
Как показано на фигурах 57C и 57D, когда мышей, которым вводили физиологический раствор, подвергали операции по кишечной I/R, у них развивалось значимое повреждение ткани по сравнению с ложнооперированными контролями (25±7, n=10; по сравнению с 1±0, n=5, P<0,01). Предварительное введение изотипического контрольного антитела не защищало от I/R-повреждения по сравнению с контролями, которым вводили физиологический раствор (17±2 по сравнению с 25±7, n=10/на группу, p>0,05). В отличие от этого, предварительное введение mAbM11 значимо снижало I/R-повреждение ткани более чем в 2 раза по сравнению с мышами, которым вводили изотипическое контрольное антитело (8±2 по сравнению с 17±2, n=10/на группу, p<0,01). Ишемическое повреждение кишечника в GIRI-группе, которой вводили mAb против MASP-2, не снижалось до исходных уровней, наблюдаемых в контрольной группе ложнооперированных животных (8±2, n=10, по сравнению с 2±1, n=5, p<0,01), но значимое снижение повреждения ткани наблюдали у животных MASP-2(-/-) и животных, которым вводили mAb против MASP-2. Результаты, полученные с использованием mAb против MASP-2, дополнительно подтверждали отрицательную роль, которую лектиновый путь играет в повреждении при ишемии/реперфузии.
Обсуждение:
Многие недавние исследования нацелены на определение механизма(-ов) и пути(-ей), приводящих к активации комплемента на лишенных кислорода клетках. Хорошо известно участие антител IgM в комплемент-зависимом GIRI (Zhang, M., et al, Proc. Natl. Acad. Sci. U.S.A. 70713886-3891 (2004); Zhang, M., et al, J. Exp. Med. 205: 141-152 (2006)). При том, что IgM является мощным активатором классического пути, считали, что мыши с дефицитом классического пути (такие как мыши C1qa (-/-)) будут защищены от комплемент-зависимого GIRI и MIRI (описываемого в примере 24). Неожиданно, в двух недавних исследованиях показали, что мыши C1qa (-/-) не защищены от GIRI или MIRI, в то время как у мышей с дефицитом распознающих молекул лектинового пути MBL A и MBL C наблюдали значимое снижение и GIRI, и MIRI (Hart, M., et al, J. Immunol. 774:6373-6380 (2005); Walsh, M.C. et al. J. Immunol. 775:541-546 (2005)). Эти результаты подтверждали в двух последующих исследованиях GIRI, в которых определяли, что критическое провоспалительное действие IgM-зависимой активации комплемента имело место в отсутствие активности классического пути посредством активации лектинового пути через прямые взаимодействия между аутореактивным IgM и MBL (Zhang, M., et al., J. Immunol. 777:4727-4734 (2006); McMullen, M.E., et al, Immunobiology 277:759-766 (2006)). В отличие от этого, ту же MBL-нулевую линию (т.е. MBL-нулевых мышей, сохраняющих остаточную функциональную активность лектинового пути посредством фиколина A) тестировали в модели IRI почки и показали только умеренную степень защиты от повреждения ткани (Moller-Kristensen, M., et al, Scand. J. Immunol. (57:426-434 (2005)).
В совокупности, эти исследования подтверждают, что защита у MBL-нулевых мышей может варьироваться между различными экспериментальными моделями IRI, т.к. роль оставшейся распознающей молекулы лектинового пути фиколина A в опосредовании IRI пока не понятна. Недавно авторы настоящего изобретения показали, что у людей MBL плазмы быстро расходуется в фазу реперфузии после хирургически-индуцируемой ишемии при операции при реконструкции аневризмы брюшной аорты (Norwood, M.G., et al, Eur. J. Vase. Endovasc. Surg. 57:239-243 (2006)). У людей ситуация может быть даже более сложной, т.к., в дополнение к MBL, три различных фиколина могут служить в качестве распознающих субкомпонентов лектинового пути.
Используя мышей MASP-2(-/-) в модели MIRI, авторы настоящего изобретения показали, что функциональная активность лектинового пути является необходимым компонентом воспалительного процесса, приводящего к значительной потери ткани миокарда. У мышей MASP-2(-/-) комплемент все равно может активироваться классическим или альтернативным путем, но лишен какой-либо остаточной функциональной активности лектинового пути при наличии всех трех распознающих паттерны молекул лектинового пути мыши, MBL A, MBL C и фиколина A, присутствующих в плазме. Кроме того, показано, что функциональная активность MASP-2 является необходимым компонентом в запуске постишемической воспалительной патологии в модели GIRI, контролируемой посредством оценки GIRI-опосредованного повреждения ткани у животных MASP-2(-/-) и MASP-2(+/+). Результаты, полученные авторами настоящего изобретения, недвусмысленно свидетельствуют о том, что ни классического, ни альтернативного пути активации комплемента не достаточно для инициации воспалительной патологии при постишемическом повреждении ткани в отсутствие функциональной активности лектинового пути. Несмотря на это, возможно, альтернативный путь может вторично вносить свой вклад на фоне усиления активации комплемента в других тканях. Это бы объясняло, почему дефицит фактора B может снижать постишемическую воспалительную потерю ткани в модели ишемической острой почечной недостаточности (Thurman, J.M., et al., J. Immunol. 770: 1517-1523 (2003)).
В конечном итоге, принимая во внимание фенотип дефицита MASP-2 и последствий терапевтического вмешательства, результаты, полученные авторами настоящего изобретения, свидетельствуют о том, что временной и длительной блокады MASP-2 и функциональной активности лектинового пути можно достигать in vivo посредством системного введения ингибиторных MASP-2-специфичных моноклональных антител. Высокая эффективность в ингибировании функциональной активности MASP-2 с использованием относительно низких доз ингибиторных антител in vivo может иметь терапевтическую значимость по причине относительно низкого количества MASP-2 в плазме (в диапазоне от 260 до 330 нг/мл в плазме мыши (см. результаты) и от 170 до 1196 нг/мл в плазме человека (Moller-Kristensen, M., et al., J. Immunol. Methods 282: 159-167 (2003)) и полного отсутствия какого-либо внепеченочного биосинтеза MASP-2 (Stover, CM., et al, J. Immunol. 7(55:6848-6859 (1999); Endo, Y., et al, Int. Immunol. 74: 1193-1201 (2002)). Таким образом, полагают, что ингибирование MASP-2 посредством введения ингибиторных моноклональных антител против MASP-2 будет эффективным в лечении индуцированных ишемией воспалительных патологий.
ПРИМЕР 26
В этом примере показано, что отсутствие функциональной активности MASP-2 в модели мыши MASP-2 (-/-)приводит к значимой степени защиты от повреждения при ишемии/реперфузии головного мозга (инсульте).
Способы:
Операция для осуществления трехсосудистой окклюзии (3VO):
Транзиторной ишемии достигали с помощью трехсосудистой окклюзионной (3VO) модели инсульта, как описано в Yanamoto et al, Exp Neurology 7S2(2):261-274 (2003). В кратком изложении, самкам мышей C57/B16 возрастом 8-18 недель перед операцией вводили Vetergesic (анальгетик) для минимизации послеоперационной боли. Животных подвергали анестезии с использованием 3-4% изофлурана с O2/N2O с последующим снижением изофлурана до 0,5-1,5% для поддержания анестезии. Получали доступ к двум общим сонным артериям (CCA) посредством разреза по вентральной срединной линии шеи, с последующим наложением зажима для аневризмы на левую CCA. Это снижает кровотечение в течение процедуры для каутеризации ипсилатеральной средней мозговой артерии (MCA). После наложения зажима на левую CCA удаляли левую скуловую дугу для получения доступа к черепу и средней мозговой артерии. Открывали трепанационное отверстие размером 1 мм для получения доступа к MCA с последующей необратимой каутеризацией с использованием биполярного коагулятора (Aura, Kirwan Surgical Products). После окклюзии MCA индуцировали ишемию в течение 30 минут посредством наложения зажима на правую CCA. На период ишемии отверстие на голове закрывали. После прекращения ишемии оба зажима снимали, делая возможной реперфузию в течение 24 часов, и затем животных умерщвляли с помощью смещения шейных позвонков.
Определение размеров инфаркта
После 24 часов реперфузии мышей умерщвляли с помощью смещения шейных позвонков, их головной мозг извлекали и получали срезы толщиной 1 мм с использованием предварительно охлажденной матрицы для ткани головного мозга. Объем инфаркта после ишемии определяли надежным способом с использованием 2,3,5-трифенилтетразолия хлорида (TTC), являющегося метаболическим клеточным индикатором митохондриальной активности, как описано в Bederson, J.B. et al, Stroke 77:1304-1308 (1986) и Lin T.N. et al, Stroke 24: 117-121 (1993). В этом анализе красное окрашивание (показанное в виде темных областей на черно-белых фотографиях) срезов головного мозга указывает на нормальную, не подвергнутую инфаркту ткань, в то время как неокрашенные, белые области указывают на подвергнутую инфаркту ткань (Bederson et al, 1986). После получения срезов головного мозга их окрашивали с использованием 2% TTC в физиологическом растворе при комнатной температуре в течение 30 минут в темноте. Затем срезы фиксировали в 10% формалине и хранили в темноте при 4°C. Цифровые изображения получали и анализировали с помощью программного обеспечения Scion Image для вычисления объема инфаркта. Для избежания завышенной оценки площади инфаркта в результате отека объем инфаркта вычисляли следующим образом:
Объем инфаркта = Площадь инфаркта/(ипсилатеральная область/контралатеральная область)×1 мм (толщина среза)
Результаты
На фигуре 58 графически представлен объем инфаркта головного мозга у мышей WT и MASP-2(-/-) после 30 минут ишемии и 24 часов реперфузии. Как показано на фигуре 58, объем инфаркта после 3-VO являлся значимо сниженным у мышей MASP-2(-/-) по сравнению с WT (мышами MASP-2(+/+) (p=0,0001)).
На фигуре 59A представлена серия срезов головного мозга мыши WT (MASP-2 +/+) после 30 минут ишемии и 24 часов реперфузии. На панелях 1-8 фигуры 59A показаны различные области срезов мозга, соответствующие точке Брегма 1-8, соответственно, в отношении выхода слухового нерва (точка Брегма 0).
На фигуре 59B представлена серия срезов головного мозга мыши MASP-2(-/-) после 30 минут ишемии и 24 часов реперфузии. На панелях 1-8 фигуры 59B показаны различные области срезов мозга, соответствующие точке Брегма 1-8, соответственно, в отношении выхода слухового нерва (точка Брегма 0).
Объемы инфарктов, измеряемые для срезов головного мозга, представленных на фигурах 59A и 59B, приведены в таблице 21 ниже.
Измерения объема инфаркта для срезов головного мозга (представленных на фигурах 59A и 59B) мышей, которым проводили окклюзию MCA в течение 30 минут с последующей реперфузией в течение 24 часов
Как представлено на фигурах 59A, 59B и в таблице 21, дефицит MASP-2 ограничивает потерю ткани после транзиторной ишемии головного мозга (MCAO в течение 30 минут) с последующей реперфузией в течение 24 часов. Эти результаты свидетельствуют о том, что отсутствие функциональной активности MASP-2 в модели мыши MASP-2(-/-) приводит к значимой степени защиты от повреждения при ишемии/реперфузии головного мозга (инсульте).
ПРИМЕР 27
В этом примере описывают результаты анализа MASP-2(-/-) в модели ревматоидного артрита мыши, индуцированного моноклональными антителами.
Уровень техники/Обоснование: Наиболее общеупотребительной моделью ревматоидного артрита (RA) на животных является коллаген-индуцированный артрит (CIA) (недавний обзор см. в Linton and Morgan, Mol. Immunol. 36:905-14, 1999). Коллаген типа II (CII) является одним из основных компонентов суставных белков клеточного матрикса, и иммунизация нативным CII в адъюванте индуцирует аутоиммунный полиартрит посредством перекрестно-реактивного аутоиммунного ответа на CII в суставном хряще. Как и при RA, предрасположенность к CIA сцеплена с экспрессией конкретных аллелей MHC класса II. Некоторые линии мышей, включая линию C57B1/6, устойчивы к классическому CIA в результате отсутствия у них соответствующего гаплотипа MHC и, таким образом, они не продуцируют высокие титры антител против CII. Однако обнаруживали, что соответствующий артрит можно индуцировать у всех линий мышей посредством i.v.- или i.p.-введения мышам смеси четырех специфичных моноклональных антител против коллагена типа II (MoAb против Col2). Эти артритогенные моноклональные антитела являются коммерчески доступными (Chondrex, Inc., Redmond, WA). Эту модель CIA с пассивным переносом успешно используют в ряде недавно опубликованных исследований с использованием мышей линии C57B1/6 (Kagari et al, J. Immunol. 169: 1459-66, 2002; Kato et al, J. Rheumatol. 50:247-55, 2003; Banda et al, J. Immunol. 777: 1904-12, 2006). В следующем исследовании сравнивали чувствительность мышей WT (+/+) и MASP-2 (-/-), имеющих генетический фон C57B1/6, к развитию артрита с использованием модели CIA с пассивным переносом.
Способы:
Животные: Получали мышей MASP-2(-/-), как описано в примере 1, и подвергали их обратному скрещиванию с C57B1/6 в течение 10 поколений. В этом исследовании использовали четырнадцать самцов и самок мышей C57BL/6 дикого типа возрастом от семи до восьми недель на момент инъекции антител и десять самцов и самок мышей MASP-2(-/-) и WT (+/+) C57B1/6 от семи до восьми недель на момент инъекции антител. Двадцати мышам инъецировали смесь моноклональных антител для получения 20 надежных респондеров (две группы по десять). Животных (десять/группу) содержали по пять животных/клетку и позволяли им акклиматизироваться в течение от пяти до семь дней перед началом исследования.
Мышам внутривенно инъецировали смесь моноклональных антител (Chondrex, Redmond WA) (5 мг) в день 0 и день 1. Тестовым средством являлось моноклональное антитело (MoAb против Col2) + LPS от Chondrex. В день 2 мышам i.p. вводили LPS. Мышей взвешивали в дни 0, 2, 4, 6, 8, 10, 12 и перед окончанием в день 14. В день 14 мышей подвергали анестезии изофлураном и полностью обескровливали для получения сыворотки. После забора крови мышей умерщвляли с удалением передних и задних конечностей с коленными суставами, которые помещали в формалин для дальнейшей обработки.
Исследуемые группы:
Группа 1 (контрольная): 4 мыши линии C57/BL/6 WT (+/+);
Группа 2 (тестовая): 10 мышей линии C57/BL/6 WT (+/+) (вводили MoAb против Col2 и LPS); и
Группа 3 (тестовая): 10 мышей линии C57/BL/MASP-2 KO/6Ai (-/-) (вводили MoAb против Col2 и LPS)
Баллы по клинической шкале артрита оценивали ежедневно с использованием следующей системы: 0 = норма; 1 = поврежден сустав 1 задней или передней конечности; 2 = повреждено 2 сустава передних или задних конечностей; 3 = повреждено 3 сустава передних или задних конечностей; 4 = умеренное (эритема и умеренный отек, или повреждены суставы 4 пальцев); 5 = тяжелое (диффузная эритема и тяжелый отек всей конечности, не может сгибать пальцы).
Результаты:
На фигуре 60 представлены сгруппированные данные, отложенные в зависимости от баллов при ежедневной оценке по клинической шкале артрита в течение периода до двух недель. В контрольной группе, которой не вводили MoAb против CoL2, не наблюдали повреждений по клинической шкале артрита. У мышей MASP (-/-) были более низкие баллы по клинической шкале артрита в дни 9-14. Общие баллы по клинической шкале артрита с анализом площади под кривой (AUC) свидетельствовали о 21% снижении в группе мышей MASP-2(-/-) по сравнению с мышами WT (+/+). Однако, как описано выше, генетический фон у мышей C57B16 не обеспечивает надежную общую оценку по клинической шкале артрита. По причине низкой частоты заболеваемости и размера групп, несмотря на положительную тенденцию, данные демонстрировали лишь тенденцию (p=0,1) и не являлись статистически значимыми при уровне p<0,05. Для достижения статистической значимости необходимы дополнительные животные в исследуемых группах. По причине низкой частоты заболеваемости артритом, баллы для поврежденных конечностей оценивали по тяжести. Не наблюдали ни одного случая получения баллов по клинической шкале артрита выше 3 у мышей MASP-2(-/-), которые наблюдали у 30% мышей WT (+/+), что дополнительно подтверждает то, что (1) тяжесть артрита может быть связана с путем активации комплемента, и (2) что блокада MASP-2 может оказывать положительное воздействие при артрите.
ПРИМЕР 28
В этом примере демонстрируют использование чистого аллергена клеща домашней пыли в качестве мощного активатора опосредованной лектиновым путем активации C3 в качестве модели астмы.
Обоснование:
Разрабатывали хорошо охарактеризованную модель индуцированной клещом домашней пыли (HDM) аллергической астмы мыши. См. X. Zhang et al, J. of Immunol. 182:5123-5130 (2009), таким образом, включенную в настоящее описание в качестве ссылки. Как описано в Zhang et al. (2009), модель включает подвергание мышей интратрахеальному воздействию HDM раз в неделю в течение трех недель. Интратрахеальное введение HDM значимо повышало чувствительность дыхательных путей, общее количество клеток и количество эозинофилов в жидкости BAL, а также уровни общего IgE и аллерген-специфичного IgE в сыворотке мышей WT BALB/c. Эту модель можно использовать для оценки применимости mAb против MASP-2 в качестве терапевтического средства при астме.
Способы:
Анализы накопления C3 осуществляли с использованием образцов сыворотки, полученных из мышей WT. Для измерения активации C3 планшеты для микротитрования покрывали маннозой (1 мкг/лунку), затем сывороткой овцы против HSA (2 мкг/мл) в TBS/Tween/Ca2+. Планшеты блокировали 0,1% HSA в TBS и промывали, как указано выше. Образцы плазмы разбавляли в 4 мМ барбитале, 145 мМ NaCl, 2 мМ CaCl2, 1 мМ MgCl2, pH 7,4, добавляли на планшеты и инкубировали в течение 1,5 часов при 37°C. После промывания определяли связавшийся C3b с использованием антител кролика против C3c человека (Dako), затем конъюгированных с щелочной фосфатазой антител козла против IgG кролик и pNPP.
Результаты:
На фигуре 61 графически представлены результаты анализа накопления C3 в образцах сыворотки, полученных из мышей WT, в присутствие клеща домашней пыли или зимозана. Как показано на фигуре 61, аллерген клеща домашней пыли является мощным активатором опосредованной лектиновым путем активации C3, активируя C3 практически с тем же уровнем, что и зимозан. Эти результаты свидетельствуют о том, что аллерген клеща домашней пыли способен стимулировать лектиновый путь. В свете того, что показано, что антитела против MASP-2 блокируют активацию альтернативного пути комплемента, ожидают, что антитела против MASP-2 будут эффективными в качестве терапевтических средств при лечении астмы у сенсибилизированных аллергеном клеща домашней пыли индивидуумов.
ПРИМЕР 29
В этом примере показано, что активация тромбина может происходить после активации лектинового пути в физиологических условиях, а также показана степень участия MASP-2. В нормальной сыворотке крыс активация лектинового пути приводит к активации тромбина (оцениваемой по накоплению тромбина), конкурирующей с активацией комплемента (оцениваемой по накоплению C4). Как можно видеть на фигурах 62A и 62B, активацию тромбина в этой системе ингибировали с помощью антитела, блокирующего MASP-2, H1 (Fab2-формат), демонстрирующего кривую ингибирования концентрация-ответ (на фигуре 62B), параллельную кривой активации комплемента (на фигуре 62A). Эти данные позволяют предполагать, что активация лектинового пути, как это происходит при травме, будет приводить к активации систем комплемента и свертывания в процессе, полностью зависящем от MASP-2. Подразумевают, что антитела, блокирующие MASP-2, могут оказаться эффективными в облегчении случаев избыточного системного свертывания, например, диссеминированного внутрисосудистого свертывания, являющегося одним из признаков, приводящих к гибели в случаях обширных травм.
ПРИМЕР 30
В этом примере представлены результаты, полученные с использованием модели локализованного феномена Санарелли-Шварцмана для диссеминированного внутрисосудистого свертывания ("DIC") у мышей MASP-2(-/-) и WT (+/+) для оценки роли лектинового пути при DIC.
Уровень техники/Обоснование:
Как описано выше, блокада MASP-2 ингибирует активацию лектинового пути и снижает образование обоих анафилотоксинов C3a и C5a. Можно показать, что анафилотоксины C3a являются мощными агрегантами тромбоцитов in vitro, но их участие in vivo определено хуже, и высвобождение тромбоцитарных веществ и плазмина при заживлении раны может включать компонент комплемента C3 лишь вторично. В этом примере анализировали роль лектинового пути у мышей MASP-2(-/-) и WT (+/+) для определения того, необходимо ли длительное повышение активации C3 для развития диссеминированного внутрисосудистого свертывания.
Способы:
Мышей MASP-2(-/-), используемых в этом исследовании, получали, как описано в примере 1. В этом эксперименте использовали модель локализованного феномена Санарелли-Шварцмана (LSR). LSR является индуцированным липополисахаридом (LPS) ответом с хорошо охарактеризованным участием клеточных и гуморальных элементов врожденной иммунной системы. хорошо известна зависимость LSR от комплемента (Polak, L., et al, Nature 225:738-739 (1969); Fong J.S. et al, J Exp Med 134:642-655 (1971)). В модели LSR мышей примировали в течение 4 часов с использованием TNF альфа (500 нг, внутримошоночно), затем мышей подвергали анестезии и подготавливали для прижизненной микроскопии мышцы, поднимающей яичко. Для наблюдения выбирали сети посткапиллярных венул (диаметром 15-60 мкм) с хорошим кровотоком (1-4 мм/сек). Животным вводили флуоресцентные антитела для селективного мечения нейтрофилов или тромбоцитов. Сети сосудов последовательно сканировали, и изображения всех сосудов регистрировали цифровым образом для последующего анализа. После регистрации исходного состояния микроциркуляции мышам делали однократную внутривенную инъекцию LPS (100 мкг) в отдельности или со средствами, указанными ниже. Затем ту же сеть сосудов сканировали каждые 10 минут в течение 1 часа. Специфическое накопление флуорофоров определяли, вычитая фоновую флуоресценцию, и увеличивали с помощью задания порога яркости изображения. Значение реакций измеряли по зарегистрированным изображениям. Первичной мерой LSR являлись сводные данные.
В исследованиях сравнивали мышей WT (+/+), подвергнутых воздействию известного ингибитора пути комплемента, фактора яда кобры (CVF) или ингибитора терминального пути (антагониста C5aR). Результаты (фигура 63 A) свидетельствуют о том, что CVF, а также антагонист C5aR, предотвращали появление агрегатов в сосудистой системе. Кроме того, у мышей MASP-2(-/-) (фигура 63B) также наблюдали полное ингибирование локализованного феномена Санарелли-Шварцмана, подтверждающее участие лектинового пути. Эти результаты четко демонстрируют роль MASP-2 в возникновении DIC и подтверждают применимость ингибиторов MASP-2 для лечения и профилактики DIC.
ПРИМЕР 31
В этом примере описывают активацию C3 субстратами тромбина и накопление C3 на маннозе у мышей WT (+/+), MASP-2(-/-), F11(-/-), F11/C4(-/-) и C4(-/-).
Обоснование:
Как описано в примере 29, определяли, что активация тромбина может происходить после активации лектинового пути в физиологических условиях, и демонстрировали степень участия MASP-2. C3 играет центральную роль в активации системы комплемента. Активация C3 необходима для классического и альтернативного путей активации комплемента. Осуществляли эксперимент для определения того, могут ли субстраты тромбина активировать C3.
Способы:
Активация C3 субстратами тромбина
Активацию C3 измеряли в присутствие следующих активированных форм субстратов тромбина; FXIa человека, FVIIa человека, бычьего FXa, FXa человека, активированного протеина C человека и тромбина человека. C3 инкубировали с различными субстраты тромбина, затем разделяли в 10% SDS-полиакриламидных гелях в восстановительных условиях. После электрофоретического переноса с использованием целлюлозной мембраны, мембрану инкубировали с меченным биотином моноклональным антителом крысы против C3 мыши, детектируемого с использованием набора стрептавидин-HRP и окрашиваемого с использованием реагента ECL.
Результаты:
Активация C3 включает расщепление интактной a-цепи на укороченную a'-цепь и растворимый C3a. На фигуре 64 представлены результаты анализа вестерн-блоттинга активации C3 человека субстратами тромбина, где нерасщепленная альфа-цепь C3 и продукт активации a'-цепи показаны стрелками. Как показано на фигуре 64, инкубация C3 с активированными формами фактора свертывания XI и фактора свертывания X человека, а также активированным бычьим фактором свертывания X, может приводить к расщеплению C3 in vitro в отсутствие какой-либо протеазы комплемента.
Накопление C3 на маннозе
Анализы накопления C3 осуществляли в образцах сыворотки, полученной из WT, MASP-2(-/-), F11(-/-), F11(-/-)/C4(-/-) и C4(-/-). F11 является геном, кодирующим фактор свертывания XI. Для измерения активации C3, планшеты для микротитрования покрывали маннозой (1 мкг/лунку), затем сывороткой овцы против HSA (2 мкг/мл) в TBS/Tween/Ca2+. Планшеты блокировали 0,1% HSA в TBS и промывали, как указано выше. Образцы плазмы разбавляли в 4 мМ барбитале, 145 мМ NaCl, 2 мМ CaCl2, 1 мМ MgCl2, pH 7,4, добавляли в планшеты и инкубировали в течение 1,5 часов при 37°C. После промывания связавшийся C3b определяли с использованием антител кролика против C3c человека (Dako), затем конъюгированных с щелочной фосфатазой антител козла против IgG кролика и pNPP.
Результаты:
На фигуре 65 представлены результаты анализа накопления C3 в образцах сыворотки, полученных из WT, MASP-2(-/-), F11(-/-), F11(-/-)/C4(-/-) и C4(-/-). Как показано на фигуре 65, функциональный лектиновый путь существовал даже при полном отсутствии C4. Как дополнительно показано на фигуре 65, для этой новой зависящей от лектинового пути активации комплемента необходим фактор свертывания XI.
Обсуждение:
До получения результатов этого эксперимента в этой области считали, что для активности лектинового пути комплемента необходим C4. Таким образом, данные, полученные с помощью нокаутных по C4 мышей (и людей с дефицитом C4), интерпретировали, предполагая, что у таких организмов есть дефицит лектинового пути (в дополнение к дефициту классического пути). Настоящие результаты свидетельствуют о том, что это мнение неверно. Таким образом, выводы, сделанные в предыдущих исследованиях, о том, что лектиновый путь не важен в условиях конкретного заболевания, основанные на фенотипе животных с дефицитом C4, могут являться ложными. Как описано в примере 24, авторы настоящего изобретения показали это на модели инфаркта миокарда, в которой мыши, нокаутные по MASP-2, были защищены, в то время как мыши, нокаутные по C4, - нет.
Данные, описываемые в этом примере, также демонстрируют, что в физиологическом контексте всей сыворотки лектиновый путь может активировать компоненты каскада свертывания. Таким образом, это свидетельствует о том, что существует взаимосвязь комплемента и свертывания, включающая MASP-2.
ПРИМЕР 32
В этом исследовании изучали дефицит MASP-2 в модели LPS (липополисахарид)-индуцированного тромбоза мыши.
Обоснование:
Гемолитико-уремический синдром (HUS), вызываемый инфекцией E. coli, продуцирующими токсин Шиги, является основной причиной острой почечной недостаточности у детей. В этом примере осуществляли модель LPS-индуцированного тромбоза по Шварцману (микрососудистого свертывания) на мышах MASP-2(-/-) для определения того, является ли ингибирование MASP-2 эффективным в ингибировании или профилактике образования внутрисосудистых тромбов.
Способы:
Анализировали мышей MASP-2(-/-) (n=9) и WT (n=10) в модели LPS-индуцированного тромбоза по Шварцману (микрососудистого свертывания). Мышам вводили LPS Serratia и контролировали образование тромбов с течением времени. Осуществляли сравнение частоты возникновения микротромбов и LPS-индуцированного микрососудистого свертывания.
Результаты:
Примечательно, что у всех тестируемых мышей MASP-2-/- (9/9) не образовывались микрососудистые тромбы после введения LPS Serratia. В отличие от этого, микротромбы определяли у 7 из 10 параллельно тестируемых мышей WT (p=0,0031, точный критерий Фишера). Как показано на фигуре 66, у мышей MASP-2(-/-) и WT измеряли время до начала окклюзии микрососудов после введения LPS, указывая процентную долю мышей WT с образованием тромбов, измеряемым в течение 60 минут, при этом образование тромбов определяли уже через приблизительно 15 минут. Через 60 минут определяли образование тромбов у до 80% мышей WT. В отличие от этого, как показано на фигуре 66, ни у одной из мышей MASP-2(-/-) через 60 минут не определяли образование тромбов (логарифмический ранговый критерий: p=0,0005).
Эти результаты свидетельствуют о том, что ингибирование MASP-2 является протективным в отношении развития внутрисосудистого тромбоза в модели HUS.
ПРИМЕР 33
В этом примере описывают эффект антител против MASP-2 в модели HUS мыши с использованием совместной интраперитонеальной инъекции очищенного токсина Шиги 2 и LPS.
Уровень техники:
Получали модель HUS мыши с использованием совместной интраперитонеальной инъекции очищенного токсина Шиги 2 (STX2) и LPS. При биохимическом и микроматричном анализе почек мыши определяли, что введение STX2 и LPS отличается от эффектов любого из средств в отдельности. При анализе крови и сыворотки этих мышей определяли нейтрофилию, тромбоцитопению, гемолиз эритроцитов и повышенный сывороточный креатинин и азот мочевины крови. Кроме того, при гистологическом анализе и электронной микроскопии почек мышей определяли накопление фибрина в клубочках, застой эритроцитов, образование микротромбов и изменение ультраструктуры клубочков. Определяли, что в этой модели HUS у мышей C57BL/6 индуцированы все клинические симптомы патологии HUS человека, включая тромбоцитопению, гемолитическую анемию и почечную недостаточность, отличающие заболевание человека (J. Immunol 187(1): 172-80 (2011)).
Способы:
Самок мышей C57BL/6 массой от 18 до 20 г получали из Charles River Laboratories и разделяли на две группы (по пять мышей в каждой группе). Одной группе мышей предварительно делали интраперитонеальную (i.p.) инъекцию рекомбинантного антитела против MASP-2 mAbM11 (доза 100 мкг на мышь; соответствующая конечной концентрации 5 мг/кг массы тела), разведенного в суммарном объеме 150 мкл физиологического раствора. Контрольной группе вводили физиологический раствор без какого-либо антитела. Через шесть часов после i.p.-инъекции антитела против MASP-2 mAb11 всем мышам делали комбинированную i.p.-инъекцию сублетальной дозы (3 мкг/животное; соответствующей 150 мкг/кг массы тела) LPS Serratia marcescens (L6136; Sigma-Aldrich, St. Louis, MO) и дозу 4,5 нг/животное (соответствующую 225 нг/кг) STX2 (двукратная доза LD50) в суммарном объеме 150 мкл. Для контролей использовали инъекцию физиологического раствора.
Выживаемость мышей контролировали каждые 6 часов после введения. Мышей умерщвляли, как только они достигали летаргической стадии патологии HUS. Через 36 часов всех мышей умерщвляли и извлекали обе почки для иммуногистохимического анализа и сканирующей электронной микроскопии. Образцы крови получали в конце эксперимента с помощью сердечной пункции. Отделяли сыворотку и хранили ее замороженной при -80°C для измерения уровней BUN и сывороточного креатинина в тестовой и контрольной группах.
Иммуногистохимический анализ
Одну треть почки каждой мыши фиксировали в 4% параформальдегиде в течение 24 часов, обрабатывали и заключали в парафин. Получали срезы толщиной три микрометра и помещали на заряженные предметные стекла для последующего окрашивания красителем H & E.
Электронная микроскопия
Среднюю часть почек нарезали блоками приблизительно от 1 до 2 мм3 и фиксировали в течение ночи при 4°C в 2,5% глутаральдегиде в 1-кратном PBS. Затем фиксированную ткань обрабатывали в University of Leicester Electron Microscopy Facility.
Криостатные срезы
Одну треть почки нарезали блоками приблизительно от 1 до 2 мм3, моментально замораживали в жидком азоте и хранили при -80°C для анализа криостатных срезов и мРНК.
Результаты:
На фигуре 67 графически представлен процент выживаемости контрольных мышей, которым вводили физиологический раствор, (n=5) и мышей, которым вводили антитело против MASP-2, (n=5) в STX/LPS-индуцированной модели с течением времени (часы). Примечательно, что, как показано на фигуре 67, все контрольные мыши умирали к 42 часам. В отличие от этого, 100% мышей, которым вводили антитело против MASP-2, выживали в течение всего эксперимента. В соответствии с результатами, представленными на фигуре 67, наблюдали, что все мыши, которым не вводили антитело, умершие или умерщвленные с признаками тяжелого заболевания, имели значительные повреждения клубочков, в то время как клубочки всех мышей, которым вводили антитело против MASP-2, выглядели нормальными (данные не представлены). Эти результаты свидетельствуют о том, что ингибиторы MASP-2, такие как антитела против MASP-2, можно использовать для лечения индивидуумов, страдающих или имеющих риск развития тромботической микроангиопатии (TMA), такой как гемолитико-уремический синдром (HUS), атипичный HUS (aHUS) или тромботическая тромбоцитопеническая пурпура (TTP).
ПРИМЕР 34
В этом примере описывают эффект дефицита MASP-2 и ингибирования MASP-2 в модели тромбоза при индуцированном FITC-декстраном/светом повреждении клеток эндотелия мыши.
Уровень техники/Обоснование: Как показано в примерах 32 и 33, дефицит MASP-2 (MASP-2 KO) и ингибирование MASP-2 (посредством введения ингибиторного антитела против MASP-2) защищает мышей в модели типичного HUS, в то время как у всех контрольных мышей, подвергнутых воздействию STX и LPS, развивался тяжелый HUS, и в пределах 48 часов у них начиналась агония или они умирали. Например, как показано на фигуре 67, все мыши, которым вводили ингибиторное антитело против MASP-2, а затем подвергали воздействию STX и LPS, выживали (точный критерий Фишера p<0,01; N=5). Таким образом, анти-MASP-2 терапия защищала мышей в этой модели HUS.
Следующие эксперименты осуществляли для анализа эффекта дефицита MASP-2 и ингибирования MASP-2 в модели тромботической микроангиопатии (TMA) при индуцированном флуоресцеинизотиоцианат (FITC)-декстраном повреждении клеток эндотелия для дополнительной демонстрации преимущества ингибиторов MASP-2 для лечения HUS, aHUS, TTP и TMA с другой этиологией.
Способы:
Прижизненная микроскопия
Мышей для прижизненной микроскопии получали, как описано в Frommhold et al., BMC Immunology 12:56-68, 2011. В кратком изложении, мышей подвергали анестезии с помощью интраперитонеальной (i.p.) инъекции кетамина (125 мг/кг массы тела, Ketanest, Pfitzer GmbH, Karlsruhe, Germany) и ксилазина (12,5 мг/кг массы тела; Rompun, Bayer, Leverkusen, Germany) и помещали на грелку для поддержания температуры тела 37°C. Прижизненную микроскопию осуществляли с помощью прямого микроскопа (Leica, Wetzlar, Germany) с иммерсионным объективом с физиологическим раствором в качестве иммерсионной жидкости (SW 40/0,75 числовая апертура, Zeiss, Jena, Germany). Для облегчения дыхания мышей интубировали с использованием трубки PE90 (Becton Dickson and Company, Sparks, MD, USA). Левую сонную артерию канюлировали с использованием трубки PE10 (Becton Dickson and Company, Sparks, MD, USA) для сбора крови и системного введения моноклонального антитела (mAb).
Получение мышцы, поднимающей
Хирургическое получение мышцы, поднимающей яичко, для прижизненной микроскопии осуществляли, как описано в Sperandio et al, Blood, 97:3812-3819, 2001. В кратком изложении, вскрывали мошонку и обеспечивали подвижность мышцы, поднимающей яичко. После продольного разреза и распределения мышцы по покровному стеклу, придаток яичка и яичко отводили в сторону и закрепляли, получая полный доступ для микроскопии микрососудов мышцы, поднимающей яичко. Венулы мышцы, поднимающей яичко, регистрировали с помощью камеры CCD (CF8/1; Kappa, Gleichen, Germany) на S-VHS-регистрирующем устройстве Panasonic. Мышцу, поднимающую яичко, обливали термоконтролируемым (35°C) физиологическим раствором, забуференным бикарбонатом, как описано ранее в Frommhold et al, BMC Immunology 12:56-68, 20112011.
Модель повреждения при световом возбуждении FITC-декстрана
Контролируемое, зависящее от интенсивности света сосудистое повреждение эндотелия венул и артериол мышцы, поднимающей яичко, индуцировали с помощью светового возбуждения фототоксичного (FITC)-декстрана (кат. № FD150S, Sigma Aldrich, Poole, U.K.). Эта процедура вызывала локализованный тромбоз. В качестве фототоксичного реагента через левую сонную артерию инъецировали 60 мкл 10% масс/об раствора FITC-декстрана и позволяли однородно распределяться по всему кровотоку в течение 10 минут. После выбора хорошо перфузируемой венулы излучение галогеновой лампы с интенсивностью от низкой до средней (800-1500) фокусировали на интересующем сосуде для индукции флуоресценции FITC-декстрана и фототоксичности от слабой до умеренной по отношению к поверхности эндотелия для стимуляции тромбоза воспроизводимым, контролируемым образом. Необходимую фототоксичную интенсивность света для возбуждения FITC-декстрана получали с использованием галогеновой лампы (12 В, 100 Вт, Zeiss, Oberkochen, Germany). Для фототоксичности, являющейся результатом индуцируемого светом возбуждения флуорохрома, необходимо пороговое значение интенсивности света и/или длительность освещения, и ее вызывает прямое нагревание поверхности эндотелия или образование реактивных радикалов кислорода, как описано в Steinbauer et al, Langenbecks Arch Surg 385:290-298, 2000.
Измеряли интенсивность света, используемого для каждого сосуда, для коррекции с помощью диодного детектора для коррекции длины волны измерения малых мощностей (Labmaster LM-2, Coherent, Auburn, USA). Автономный анализ видеоизображений осуществляли с помощью компьютеризированной системы анализа микроциркуляции (CAMAS, Dr. Zeintl, Heidelberg) и измеряли скорость эритроцитов, как описано в Zeintl et al, Int J Microcirc Clin Exp, 8(3):293-302, 2000.
Введение моноклонального ингибиторного антитела против MASP-2 человека (mAbH6) и контрольного средства перед индуцированием тромбоза
Используя дизайн слепого исследования, однопометным самцам мышей WT C57BL/6 возрастом 9 недель делали i.p.-инъекции рекомбинантного моноклонального антитела против MASP-2 человека (mAbH6), ингибитора функциональной активности MASP-2 (вводимого в конечной концентрации 10 мг/кг массы тела), или того же количества изотипического контрольного антитела (без MASP-2-ингибиторной активности) за 16 часов до фототоксического индуцирования тромбоза в модели мышцы, поднимающей яичко, с прижизненной микроскопией. За один час до индуцирования тромбоза вводили вторую дозу mAbH6 или контрольного антитела. Также в этой модели оценивали мышей, нокаутных по MASP-2 (KO).
mAbH6 (полученное против рекомбинантной MASP-2 человека) является мощным ингибитором функциональной активности MASP-2 человека, перекрестно реагирующим, связывающимся и ингибирующим MASP-2 мыши, но с меньшей аффинностью по причине своей видоспецифичности (данные не представлены). Для компенсации меньшей аффинности mAbH6 к MASP-2 мыши, mAbH6 вводили в высокой концентрации (10 мг/кг массы тела) для преодоления отклонений по причине видоспецифичности и меньшей аффинности к MASP-2 мыши для достижения эффективной блокады функциональной активности MASP-2 мыши в условиях in vivo.
В этом слепом исследовании регистрировали время, необходимое каждой отдельной венуле (критериями отбора являлись сравнимые диаметры и скорость кровотока) для полной окклюзии.
Процентную долю мышей с окклюзией микрососудов, время начала и время до возникновения окклюзии оценивали в течение 60-минутного периода наблюдений с использованием видеозаписей прижизненной микроскопии.
Результаты:
На фигуре 68 в виде функции времени после начала индуцирования повреждения графически представлена процентная доля мышей с окклюзией микрососудов в модели FITC/декстран-УФ после введения изотипического контрольного антитела или антитела против MASP-2 человека mAbH6 (10 мг/кг), вводимого за 16 часов и 1 час до инъекции FITC/декстрана. Как показано на фигуре 68, у 85% мышей дикого типа, которым вводили изотипическое контрольное антитело, окклюзия развивалась в пределах 30 минут или менее, в то время как только у 19% мышей дикого типа, которым предварительно вводили антитело против MASP-2 человека (mAbH6), окклюзия развивалась в пределах того же периода времени, и у мышей из группы, которой вводили антитело против MASP-2 человека, у которых, в конечном итоге, развивалась окклюзия, возникновение окклюзия было отсрочено. Также необходимо отметить, что у трех из мышей, которым вводили mAbH6 против MASP-2, в течение 60-минутного периода наблюдения окклюзия не развивалась совсем (т.е. они были защищены от тромботической окклюзии).
На фигуре 69 графически представлено время окклюзии в минутах для мышей, которым вводили антитело против MASP-2 человека (mAbH6) и изотипическое контрольное антитело. Данные представлены в виде рассеянных точек со средними значениями (горизонтальные линии) и среднеквадратичными ошибками (вертикальные линии). На этой фигуре представлено время окклюзии у мышей, у которых наблюдали окклюзию. Таким образом, трех мышей, которым вводили антитело против MASP-2 и у которых не развивалась окклюзия в течение 60-минутного периода наблюдения, не включали в этот анализ (не было мышей, которым вводили контрольное антитело и у которых не развивалась бы окклюзия). Статистическим тестом, используемым для анализа, являлся двухвыборочный критерий Стьюдента для независимых выборок; где символом "*" указывают p=0,0129. Как показано на фигуре 69, у четырех мышей, которым вводили антитело против MASP-2 (mAbH6) и у которых развивалась окклюзия, введение антитела против MASP-2 значимо повышало время венозной окклюзии в модели тромбоза при индуцированном FITC-декстраном/светом повреждения клеток эндотелия с использованием низкой интенсивности света (800-1500) по сравнению с мышами, которым вводили изотипическое контрольное антитело. Среднее время полной окклюзии для группы, которой вводили изотипическое контрольное антитело, составляло 19,75 минуты, в то время как среднее время полной окклюзии для группы, которой вводили антитело против MASP-2, составляло 32,5 минуты.
На фигуре 70 графически представлено время до развития окклюзии в минутах для мышей дикого типа, мышей MASP-2 KO и мышей дикого типа, которым предварительно вводили i.p. антитело против MASP-2 человека (mAbH6) в дозе 10 мг/кг за 16 часов, а затем вводили снова i.v. за 1 час до индуцирования тромбоза в модели тромбоза при индуцированном FITC-декстраном/светом повреждения клеток эндотелия с использованием низкой интенсивности света (800-1500). На фигуре 70 представлены только животные, у которых развивалась окклюзия; n=2 для мышей дикого типа, которым вводили изотипическое контрольное антитело; n=2 для MASP-2 KO; и n=4 для мышей дикого типа, которым вводили антитело против MASP-2 человека (mAbH6). Символом "*" указывают p<0,01. Как показано на фигуре 70, дефицит MASP-2 и ингибирование MASP-2 (mAbH6 в дозе 10 мг/кг) повышали время венозной окклюзии в модели тромбоза при индуцированном FITC-декстраном/светом повреждении клеток эндотелия с использованием низкой интенсивности света (800-1500).
Выводы:
Результаты в этом примере дополнительно свидетельствуют о том, что средство, ингибирующее MASP-2, блокирующее лектиновый путь (например, антитела, блокирующие функционирование MASP-2), ингибирует микрососудистое свертывание и тромбоз, характерные признаки множества микроангиопатических нарушений, в модели TMA мыши. Таким образом, ожидают, что введение средства, ингибирующего MASP-2, такого как ингибиторное антитело против MASP-2, будет представлять собой эффективную терапию для пациентов, страдающих HUS, aHUS, TTP или другими микроангиопатическими нарушениями, и обеспечивать защиту от микрососудистого свертывания и тромбоза.
ПРИМЕР 35
В этом примере описывают исследование, демонстрирующее, что ингибиторное антитело против MASP-2 человека (mAbH6) не имеет эффекта в отношении функционирования тромбоцитов в богатой тромбоцитами плазме человека.
Уровень техники/Обоснование: Как описано в примере 34, показано, что ингибирование MASP-2 ингибиторным антителом против MASP-2 человека (mAbH6) повышало время венозной окклюзии в модели тромбоза при индуцированном FITC-декстраном/светом повреждении эндотелиальных клеток. Следующий эксперимент осуществляли для определения того, имеет ли ингибиторное антитело против MASP-2 (mAbH6) эффект в отношении функционирования тромбоцитов.
Способы: Эффект антитела mAbH6 против MASP-2 человека тестировали на АДФ-индуцированной агрегации тромбоцитов следующим образом. Добавляли mAbH6 против MASP-2 человека в концентрации 1 мкг/мл или 0,1 мкг/мл в 40 мкл раствора в 360 мкл свежеприготовленной богатой тромбоцитами плазме человека. В качестве отрицательного контроля использовали изотипическое контрольное антитело. После добавления антител в плазму индуцировали активацию тромбоцитов добавлением АДФ в конечной концентрации 2 мкМ. Начинали анализ, перемешивая растворы с использованием небольшого магнита в кювете емкостью 1 мл. Агрегацию тромбоцитов измеряли с помощью двухканального оптического агрегометра для тромбоцитов Chrono-log модели 700, оптического агрегометра Lumi для цельной крови.
Результаты:
Процент агрегации в растворах измеряли в течение пяти минут. Результаты представлены в таблице 22 ниже.
Агрегация тромбоцитов за период пяти минут
Как показано выше в таблице 22, не наблюдали значимых различий между агрегацией ADP-индуцированных тромбоцитов, обработанных контрольным антителом или антителом против MASP-2 mAbH6. Эти результаты свидетельствуют о том, что антитело против MASP-2 человек (mAbH6) не имеет эффекта в отношении функционирования тромбоцитов. Таким образом, результаты, описываемые в примере 34, свидетельствующие о том, что ингибирование MASP-2 ингибиторным антителом против MASP-2 человека (mAbH6) повышало время венозной окклюзии в модели тромбоза при индуцированном FITC-декстраном/светом повреждении эндотелиальных клеток, не являлись следствием эффекта mAbH6 в отношении функционирования тромбоцитов. Таким образом, ингибирование MASP-2 предотвращает тромбоз, не влияя напрямую на функционирование тромбоцитов, позволяя выявить терапевтический механизм, отличающийся от существующих антитромботических средств.
Хотя проиллюстрирован и описан предпочтительный вариант осуществления изобретения, следует понимать, что можно осуществлять различные изменения без отклонения от сущности и объема изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ MASP-1, И/ИЛИ MASP-2, И/ИЛИ MASP-3 ДЛЯ ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНОЙ НОЧНОЙ ГЕМОГЛОБИНУРИИ | 2013 |
|
RU2655299C2 |
| Способы лечения состояний, связанных с masp-2 зависимой активацией комплемента | 2012 |
|
RU2662563C2 |
| СПОСОБЫ ЛЕЧЕНИЯ СОСТОЯНИЙ, СВЯЗАННЫХ С MASP-2 ЗАВИСИМОЙ АКТИВАЦИЕЙ КОМПЛЕМЕНТА | 2012 |
|
RU2743409C2 |
| СПОСОБЫ ЛЕЧЕНИЯ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С MASP-2-ЗАВИСИМОЙ АКТИВАЦИЕЙ КОМПЛЕМЕНТА | 2014 |
|
RU2718850C2 |
| СПОСОБЫ ЛЕЧЕНИЯ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С MASP-2-ЗАВИСИМОЙ АКТИВАЦИЕЙ КОМПЛЕМЕНТА | 2014 |
|
RU2830289C2 |
| КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ MASP-2-ЗАВИСИМОЙ АКТИВАЦИИ КОМПЛЕМЕНТА | 2012 |
|
RU2636038C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ КРОВИ ПУТЕМ ИНГИБИРОВАНИЯ MASP-2 ЗАВИСИМОЙ АКТИВАЦИИ КОМПЛЕМЕНТА | 2010 |
|
RU2600876C2 |
| КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ MASP-2-ЗАВИСИМОЙ АКТИВАЦИИ КОМПЛЕМЕНТА | 2017 |
|
RU2725958C2 |
| АНТИТЕЛА ПРОТИВ ФАКТОРА D И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2799044C2 |
| АНАЛОГИ ФАКТОРА КОМПЛЕМЕНТА В И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2639521C2 |




































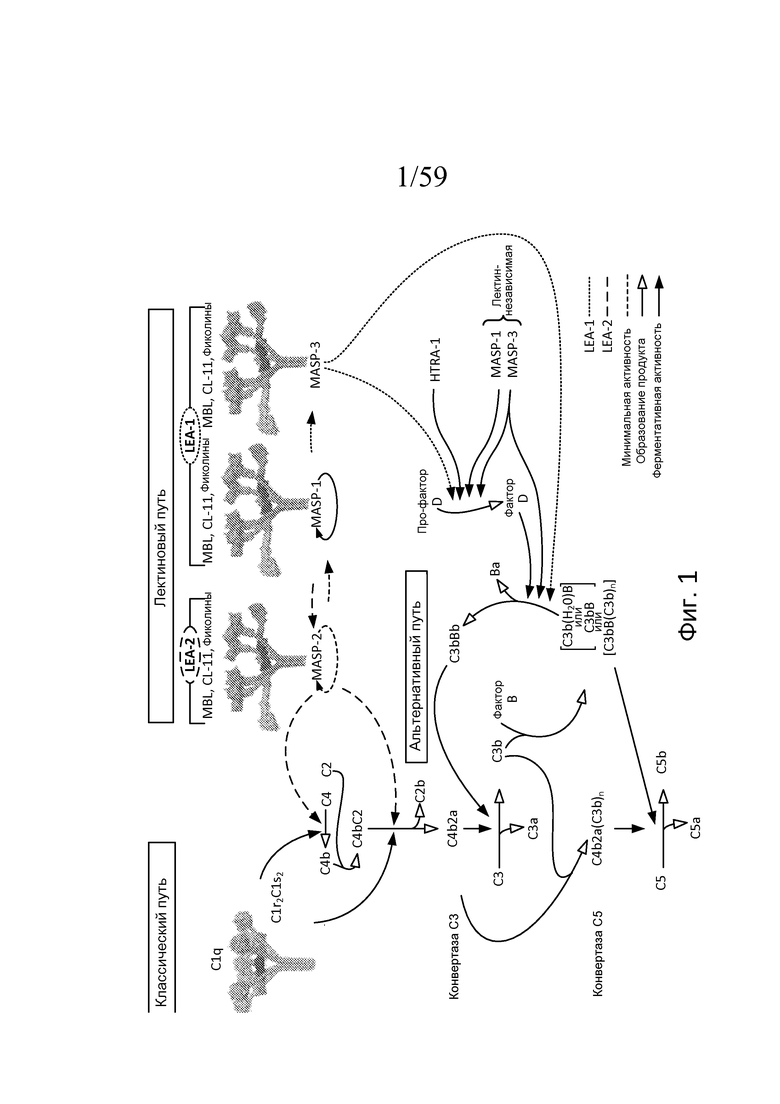
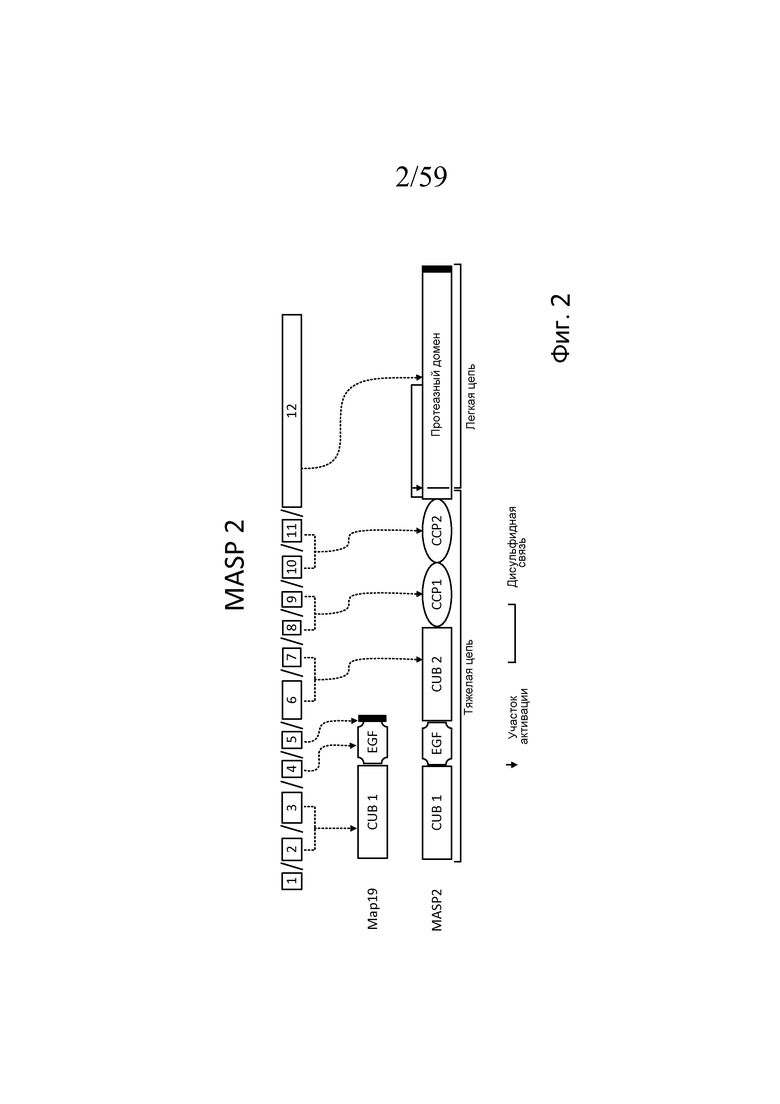
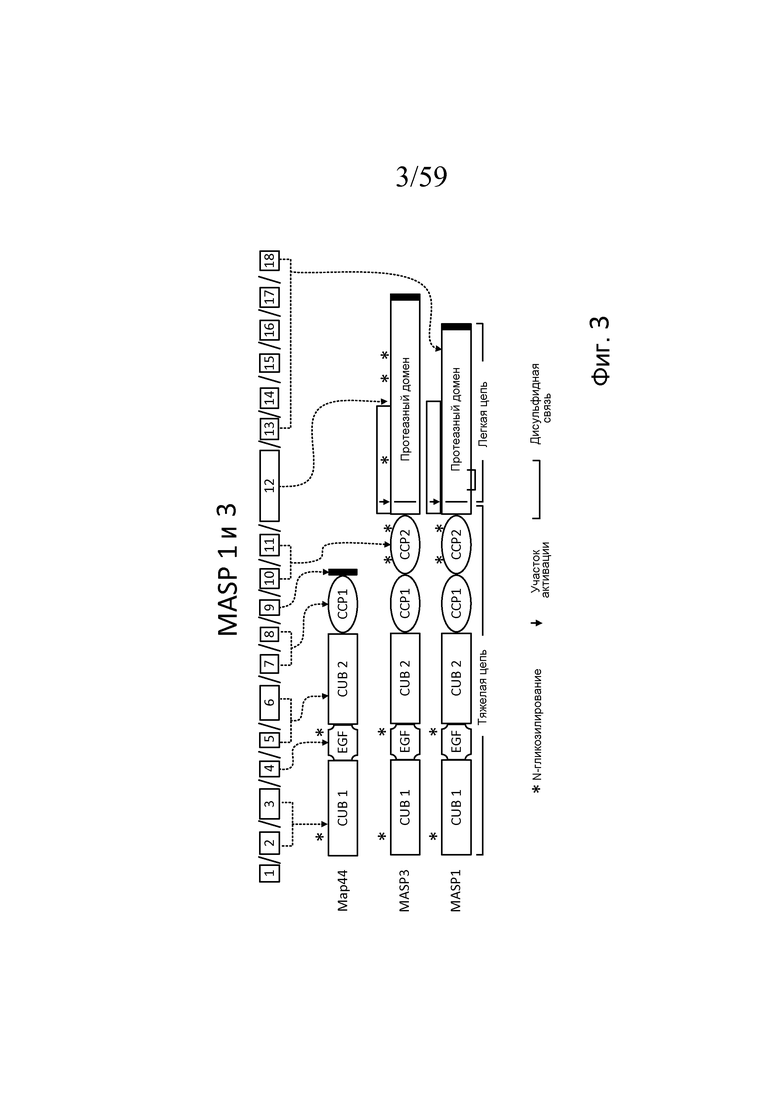
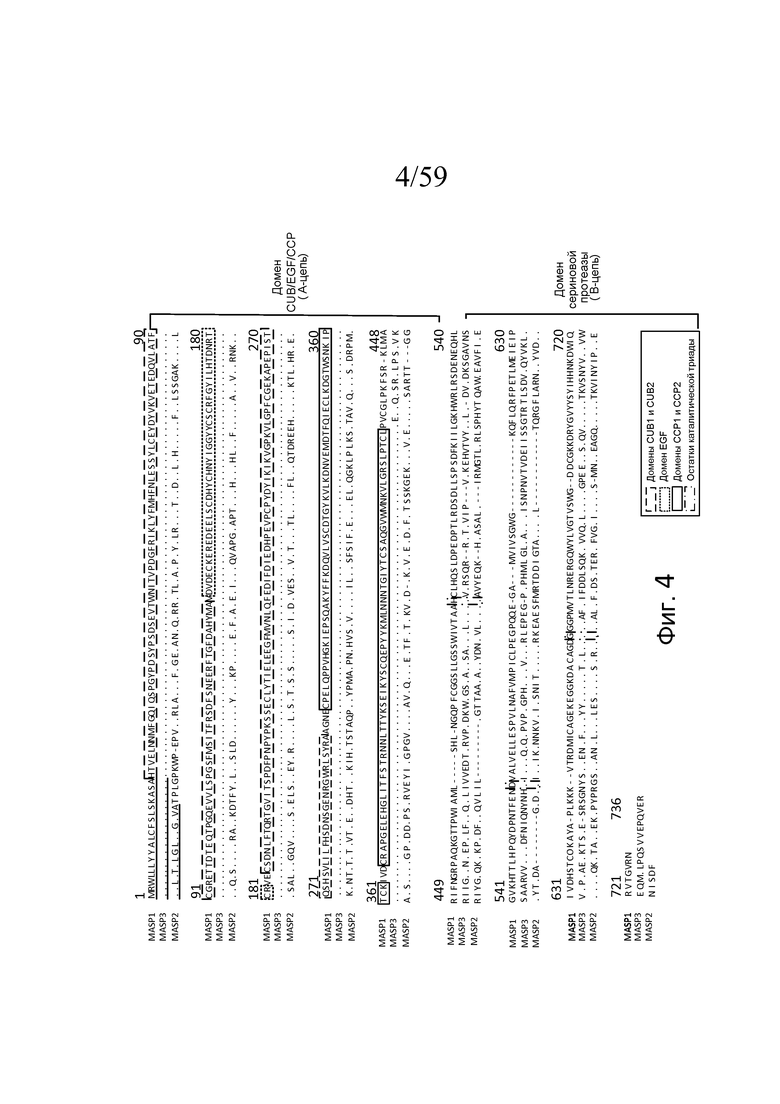





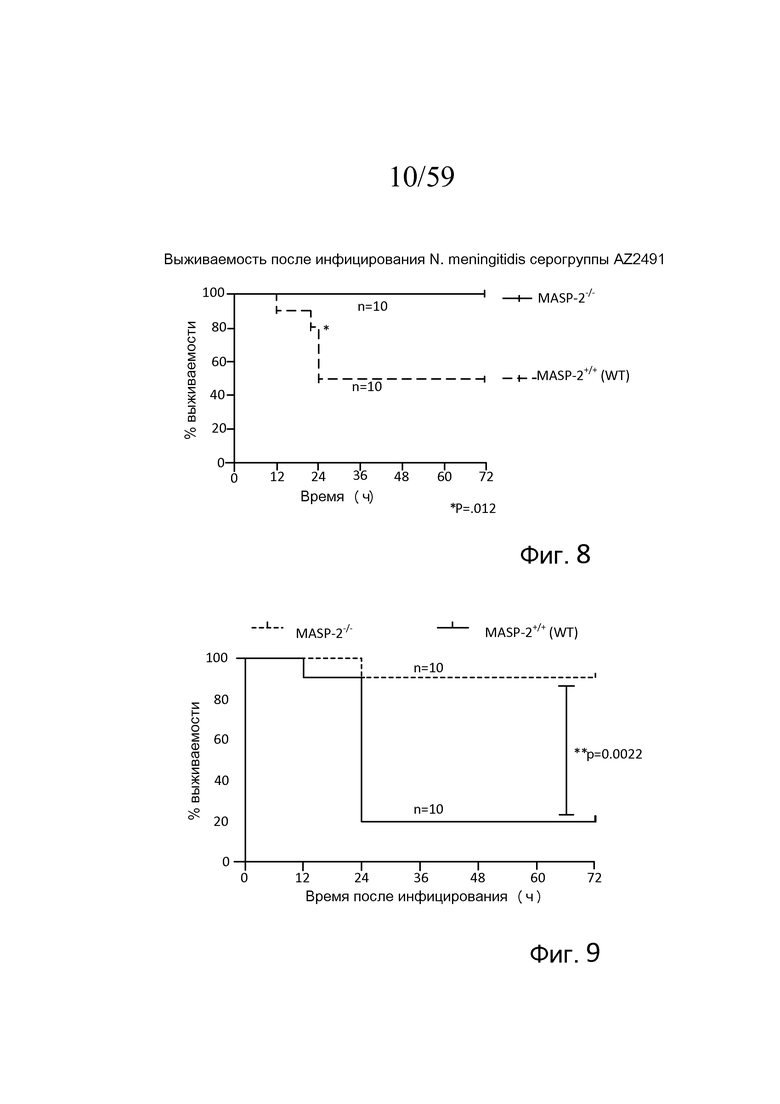
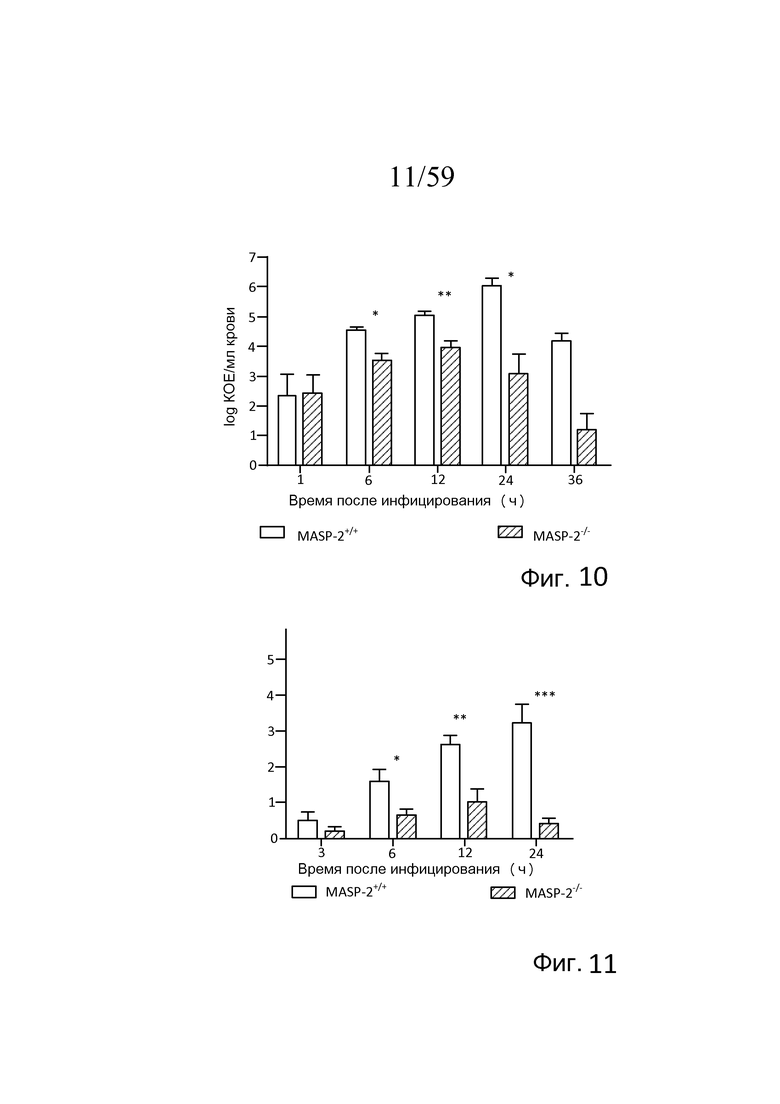
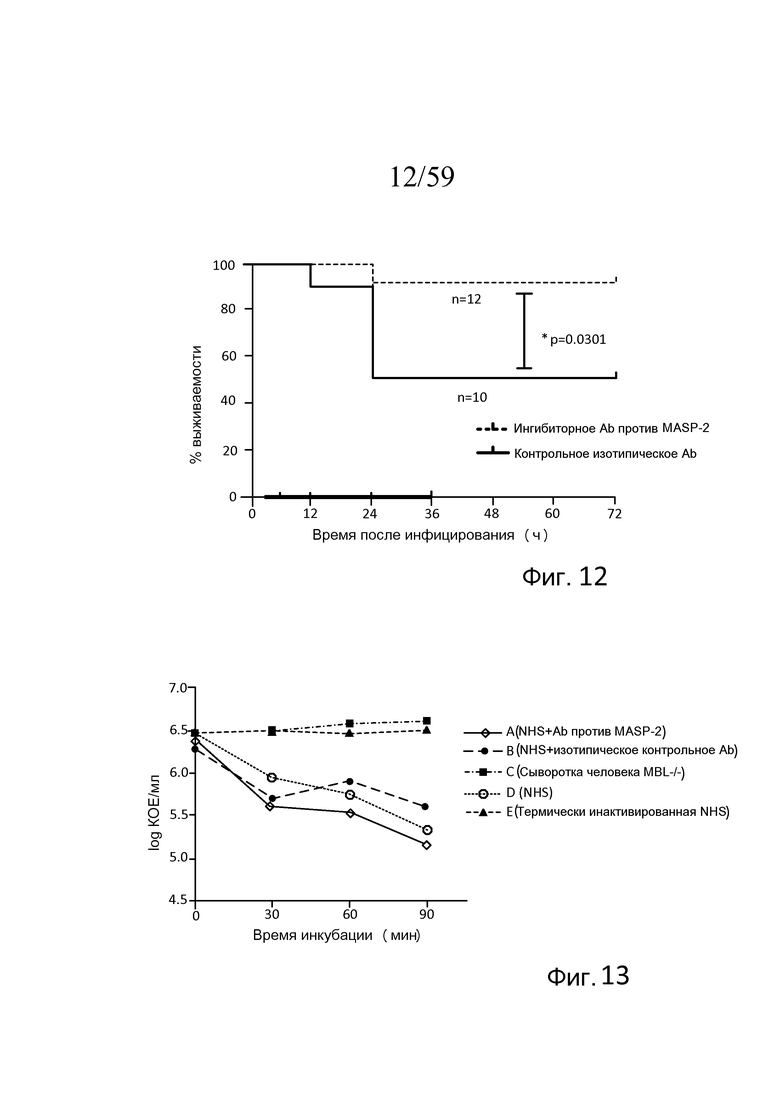
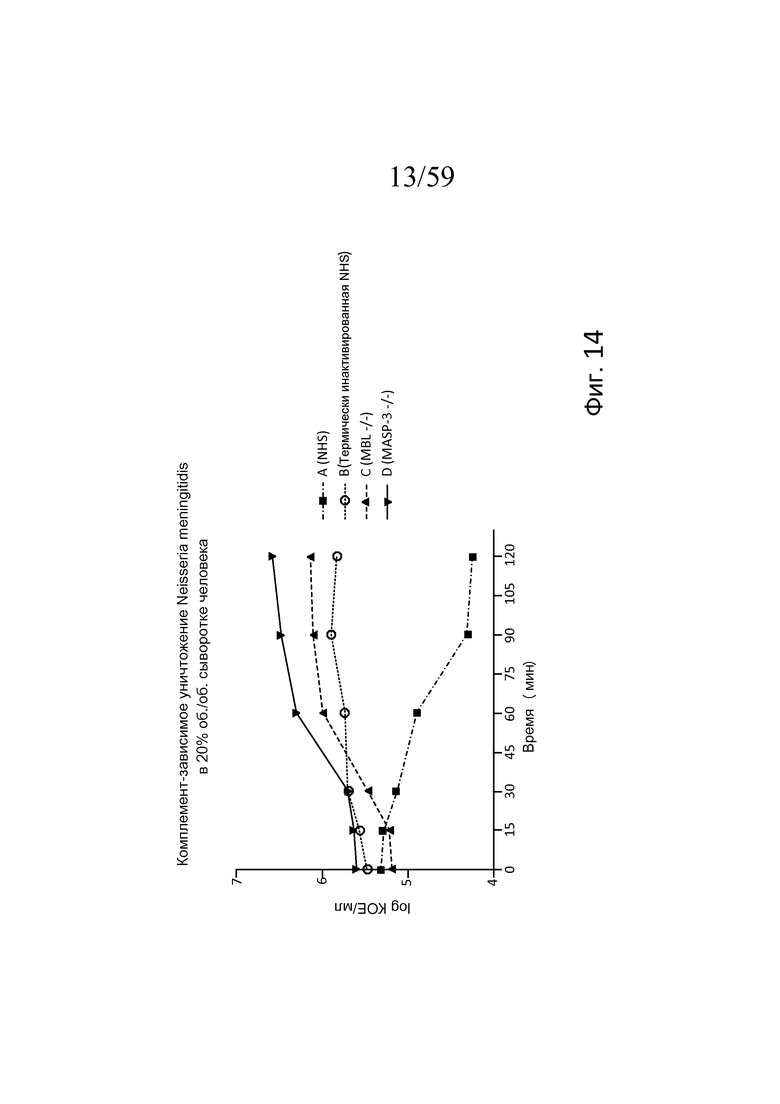
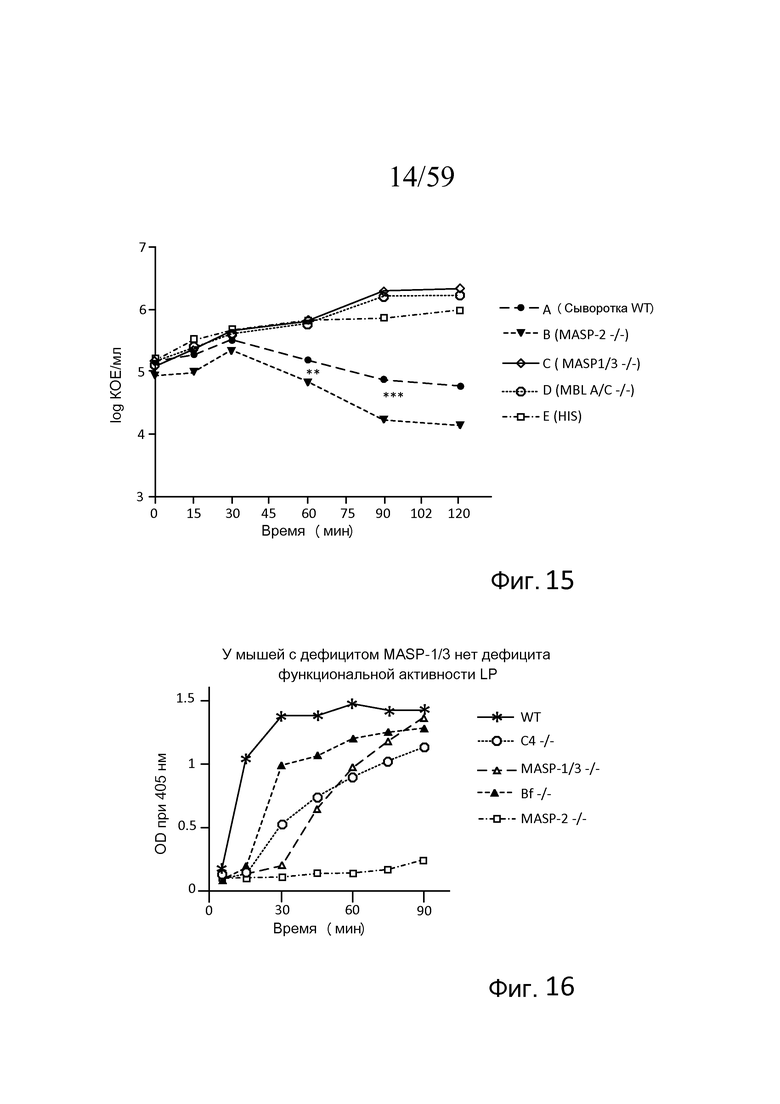
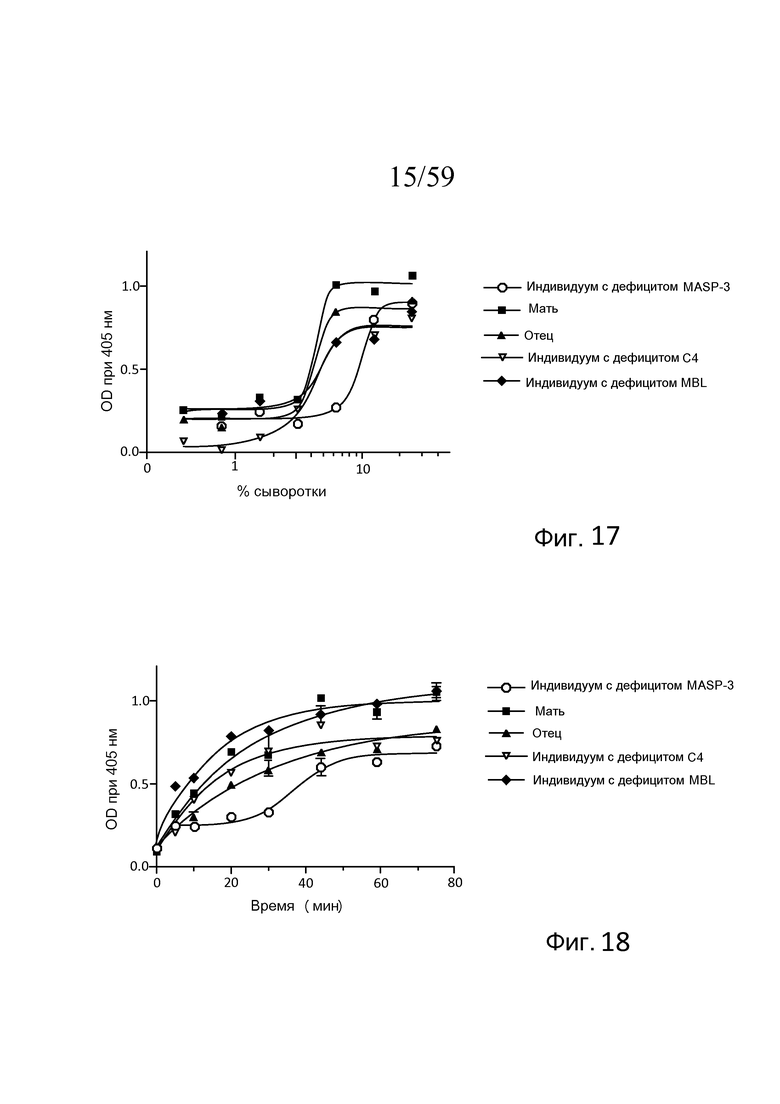
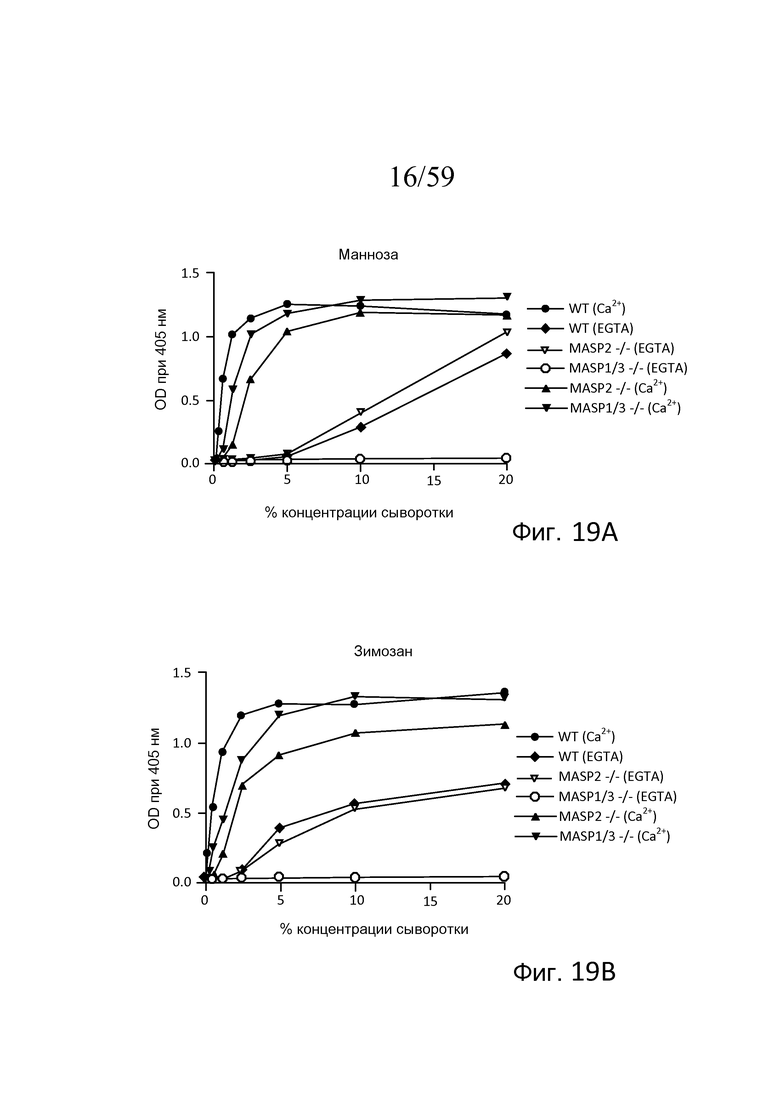
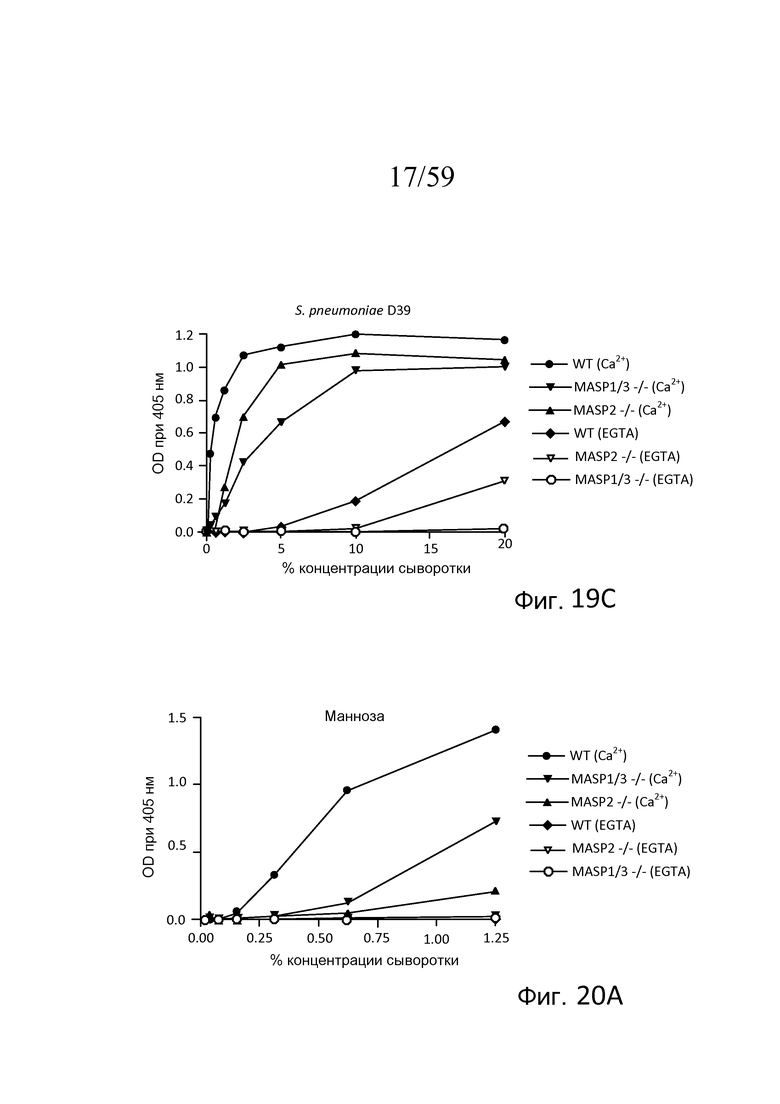
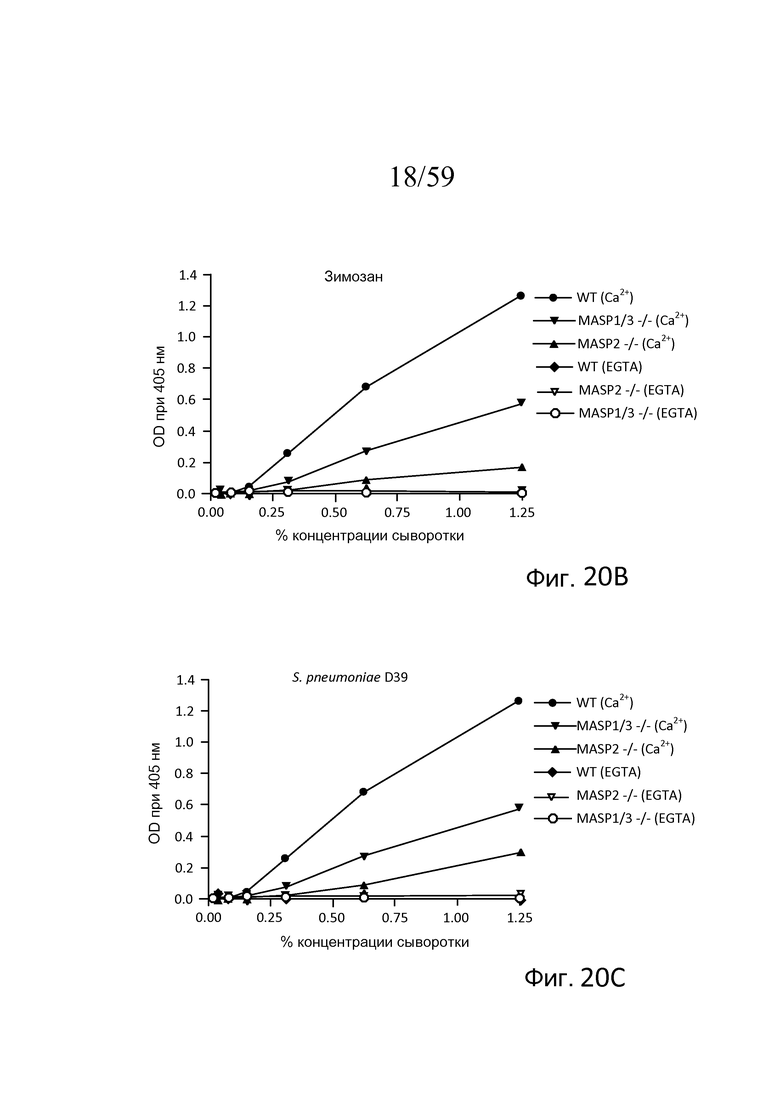
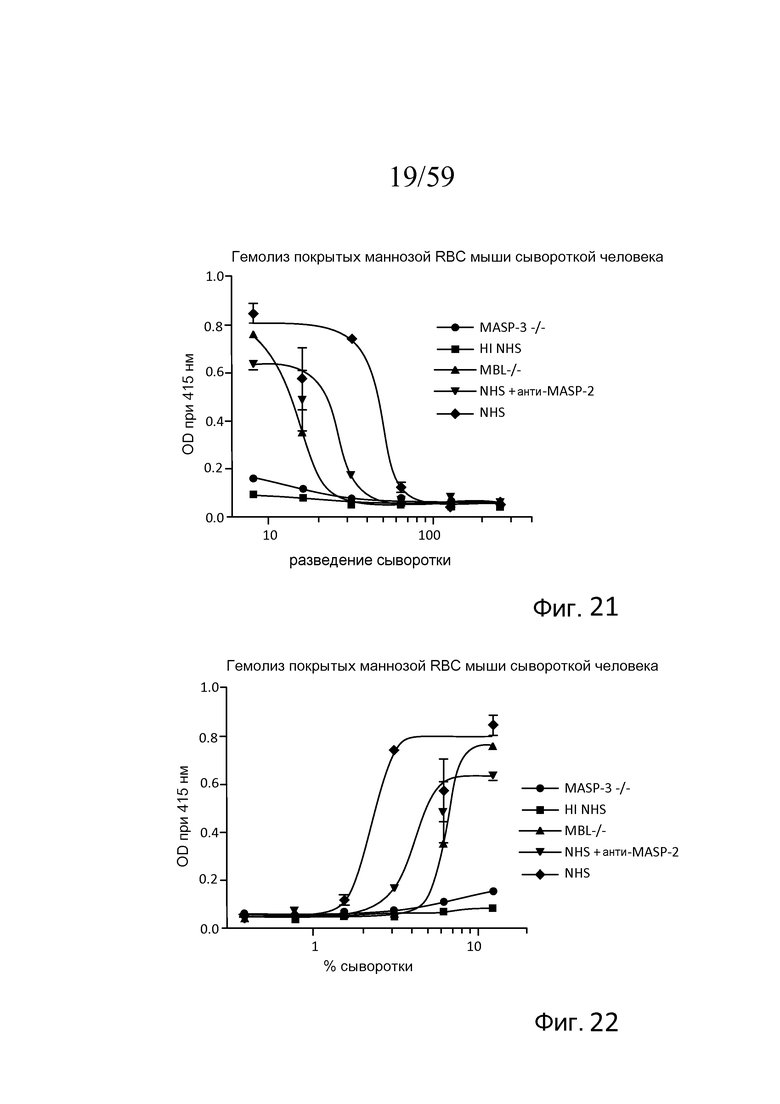
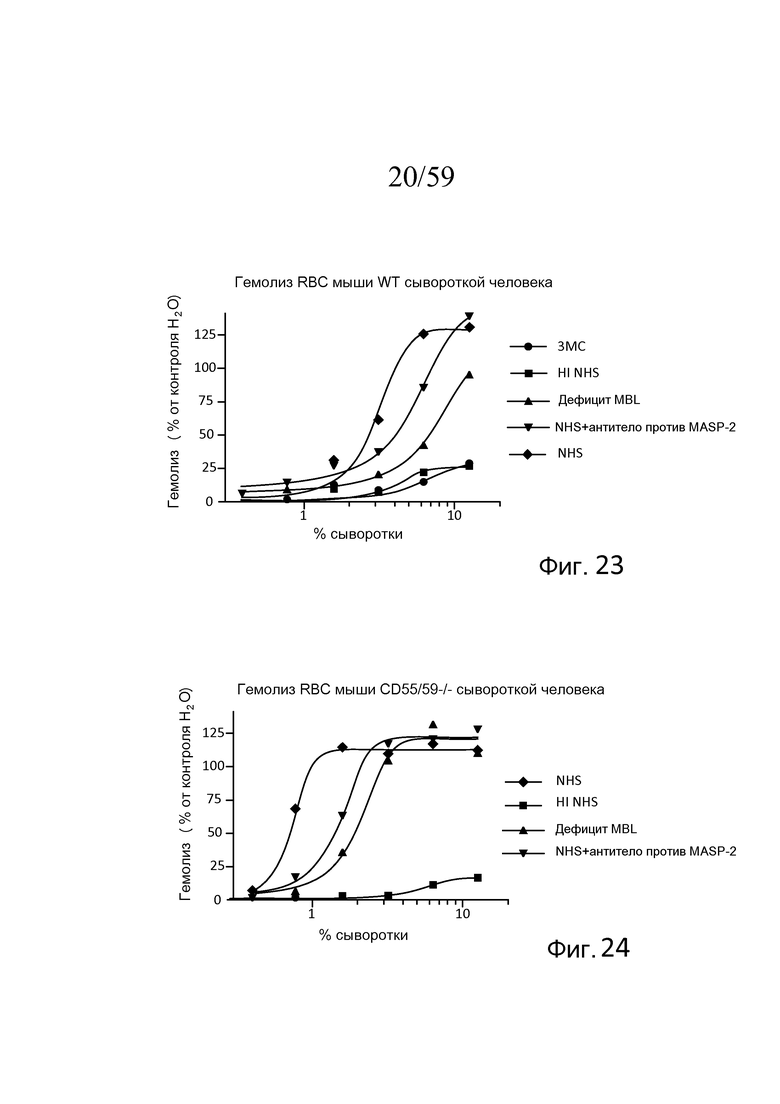

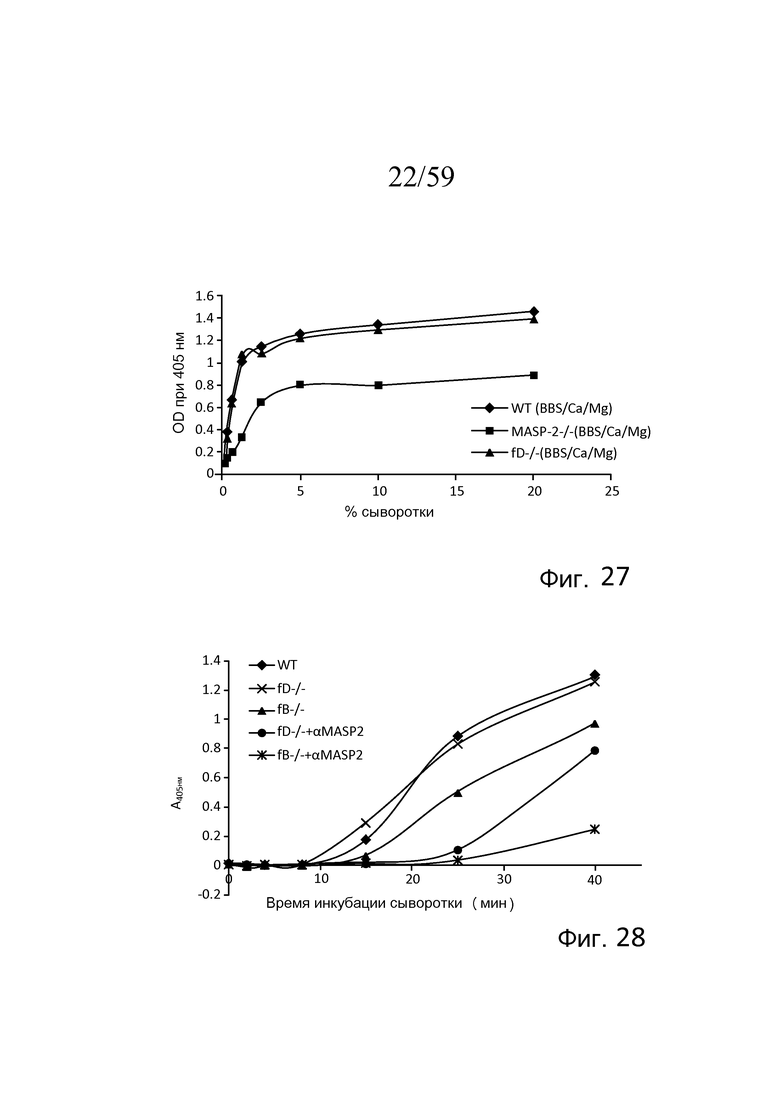
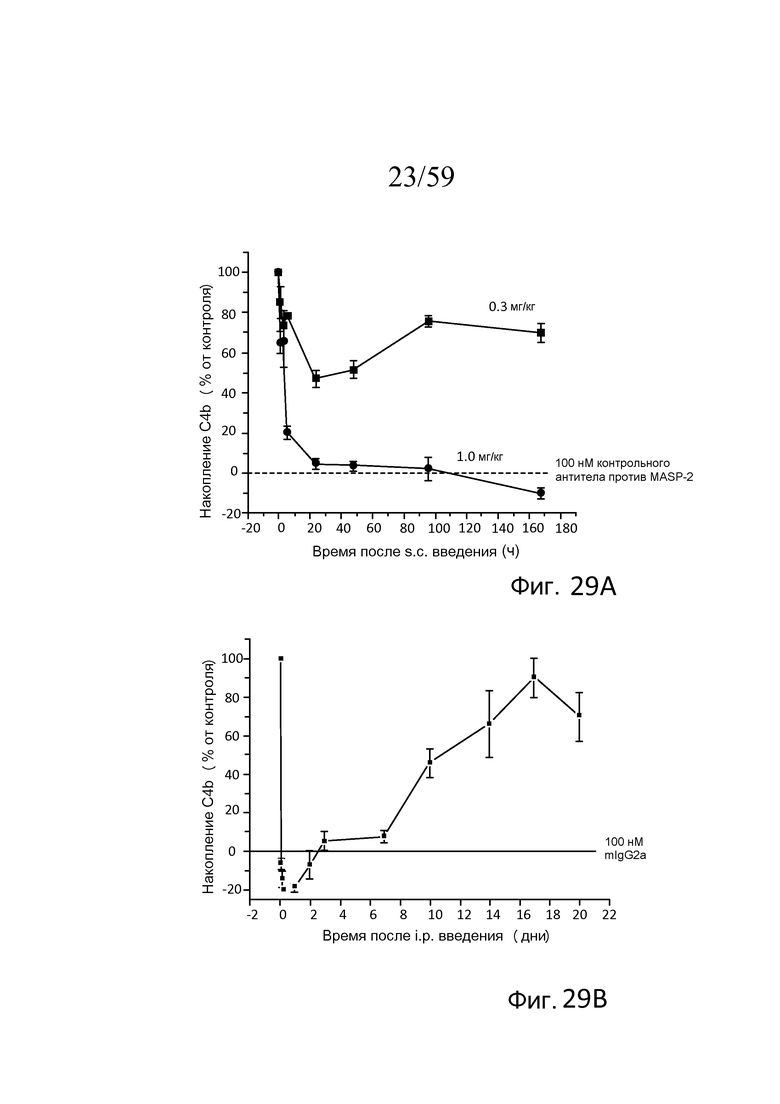
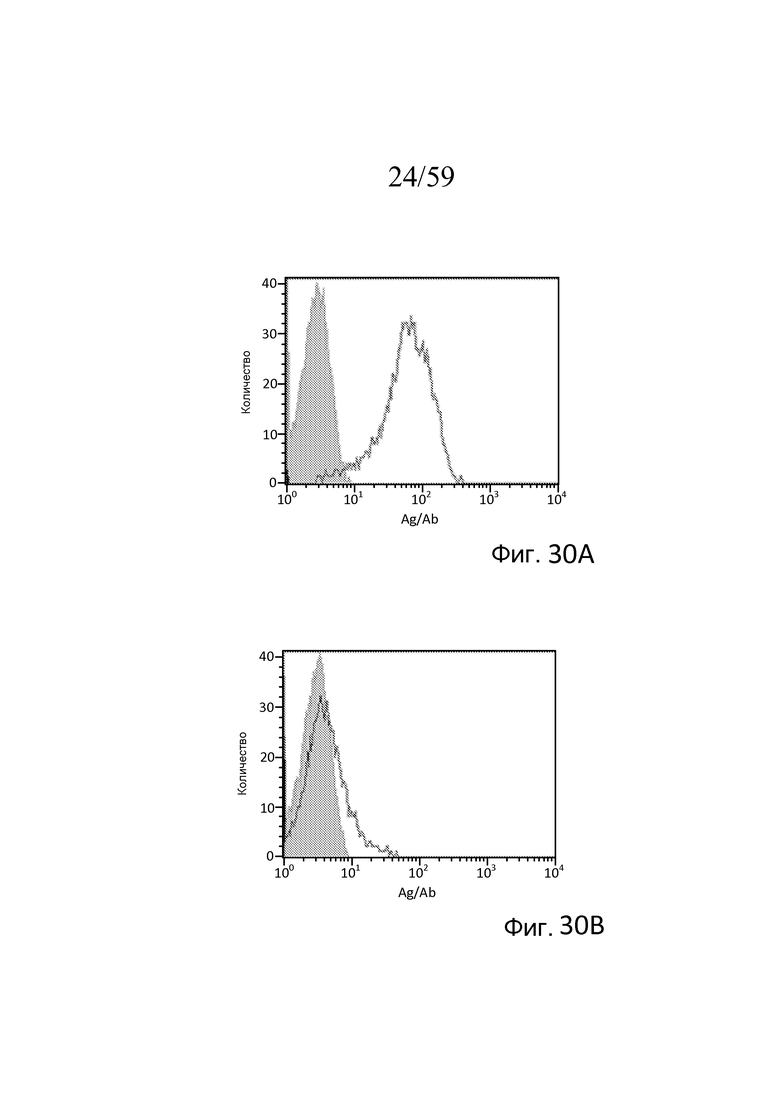
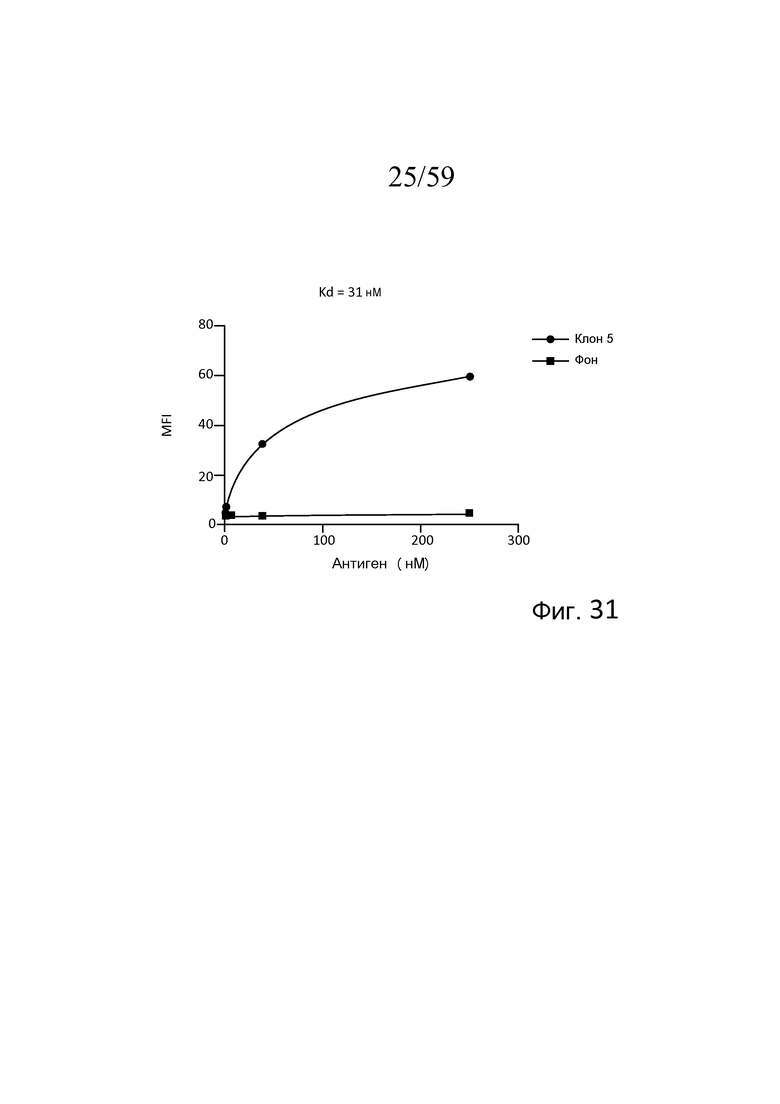
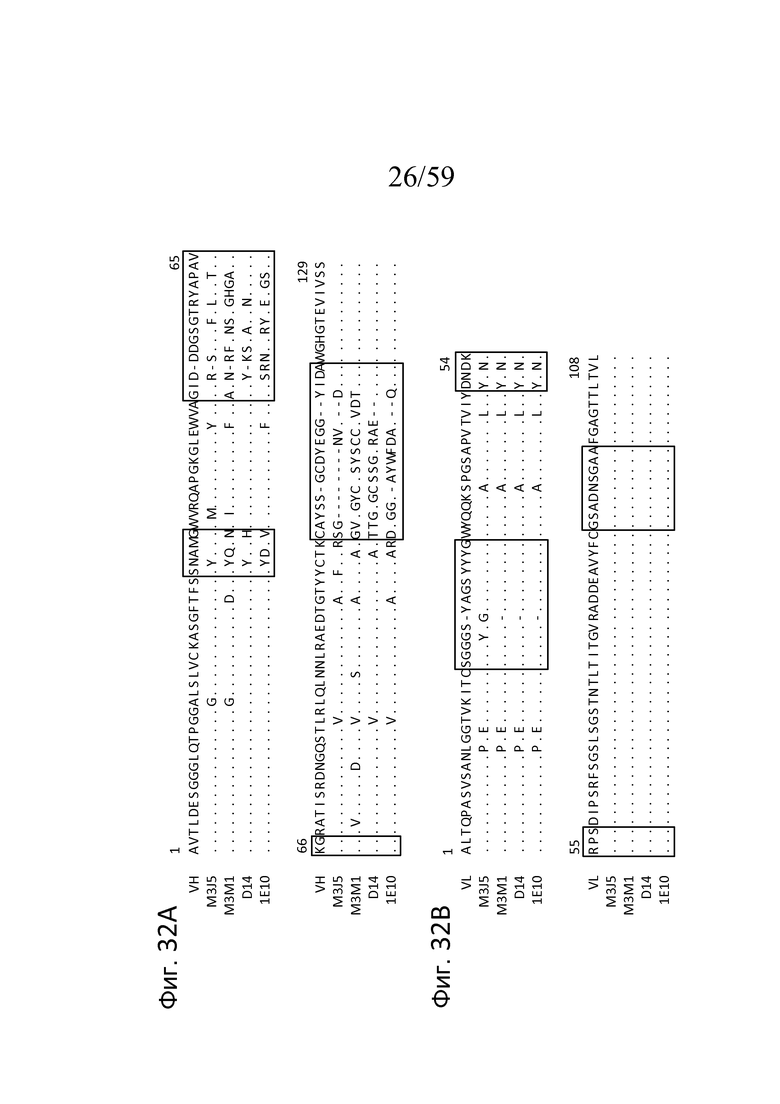
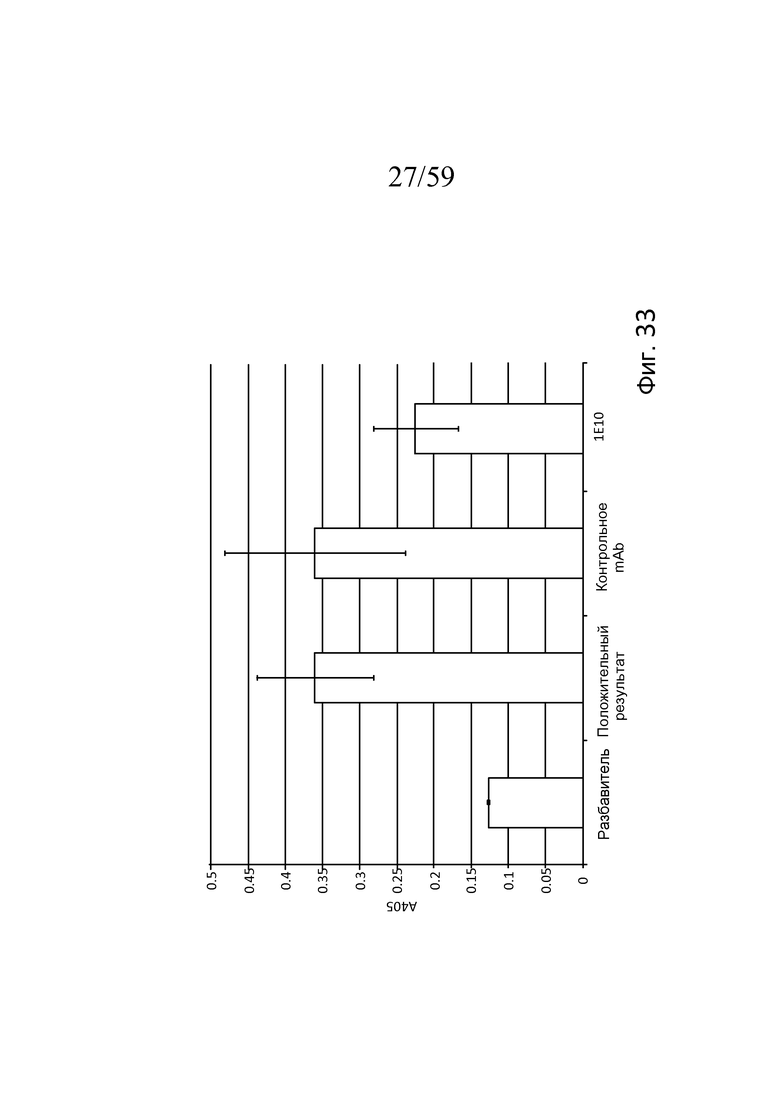
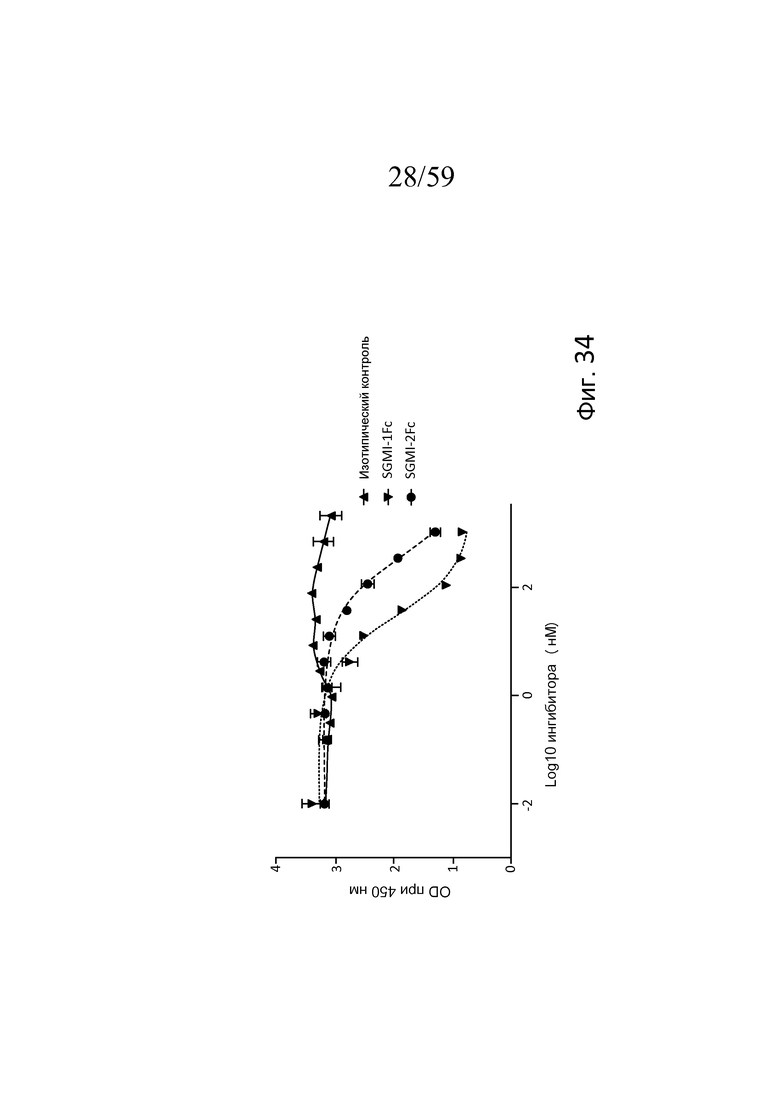
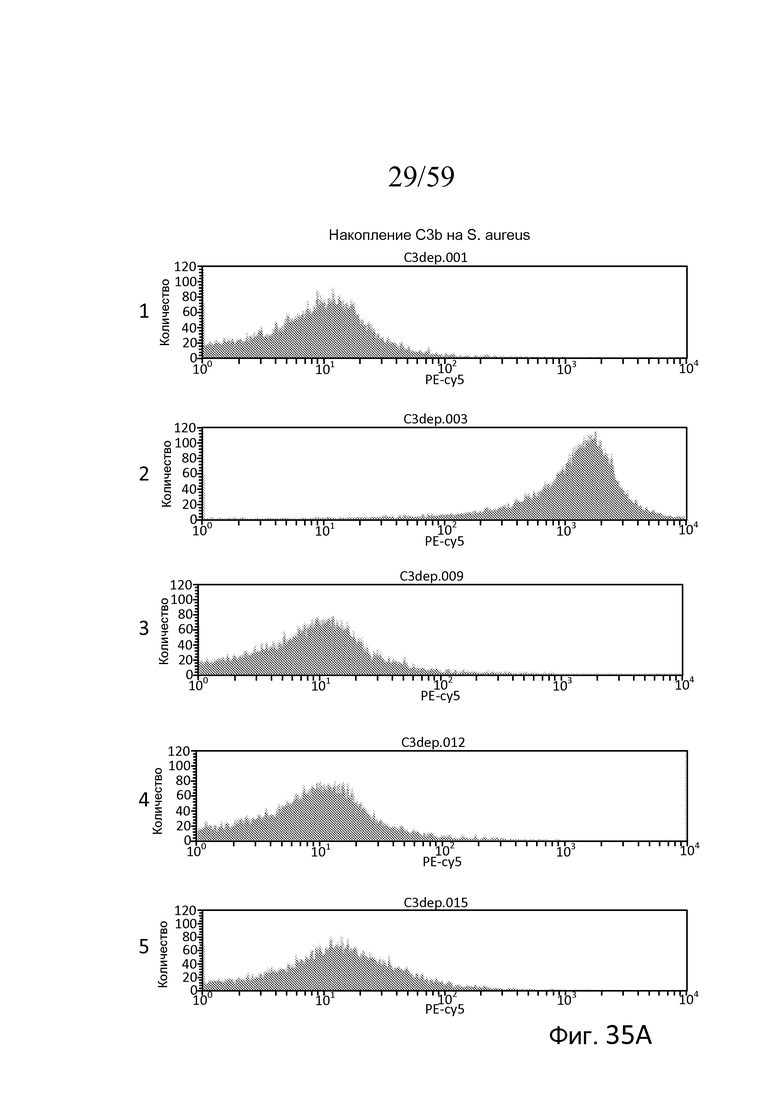
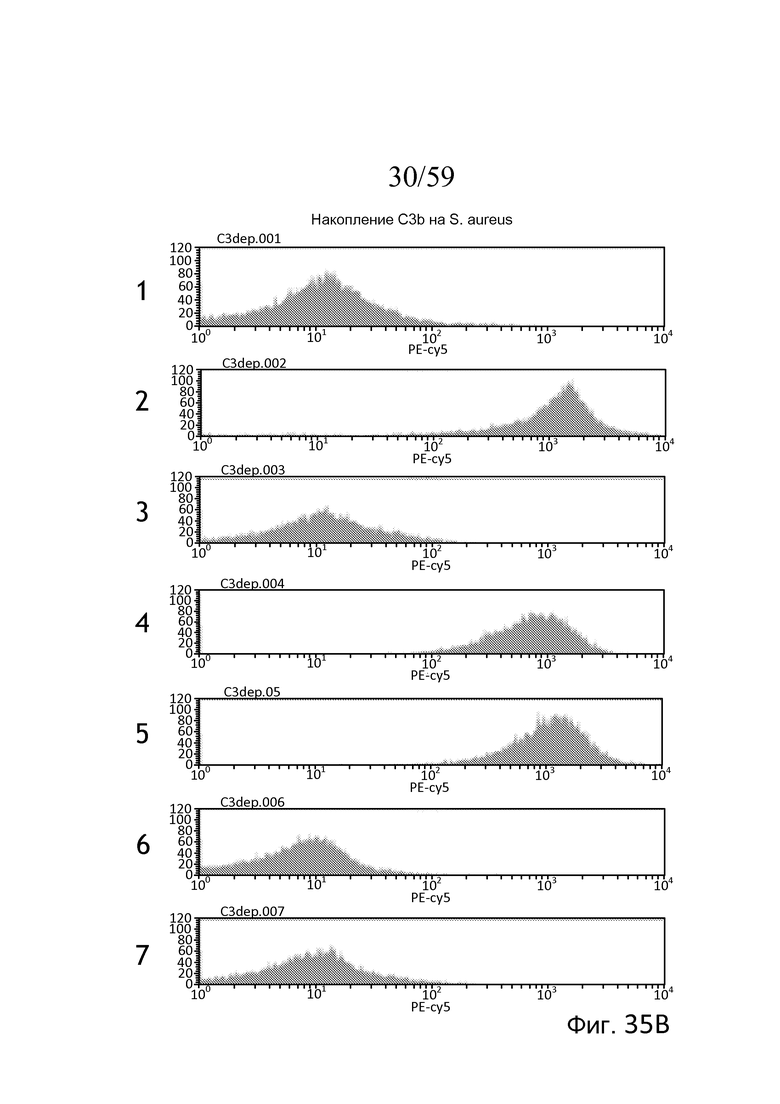
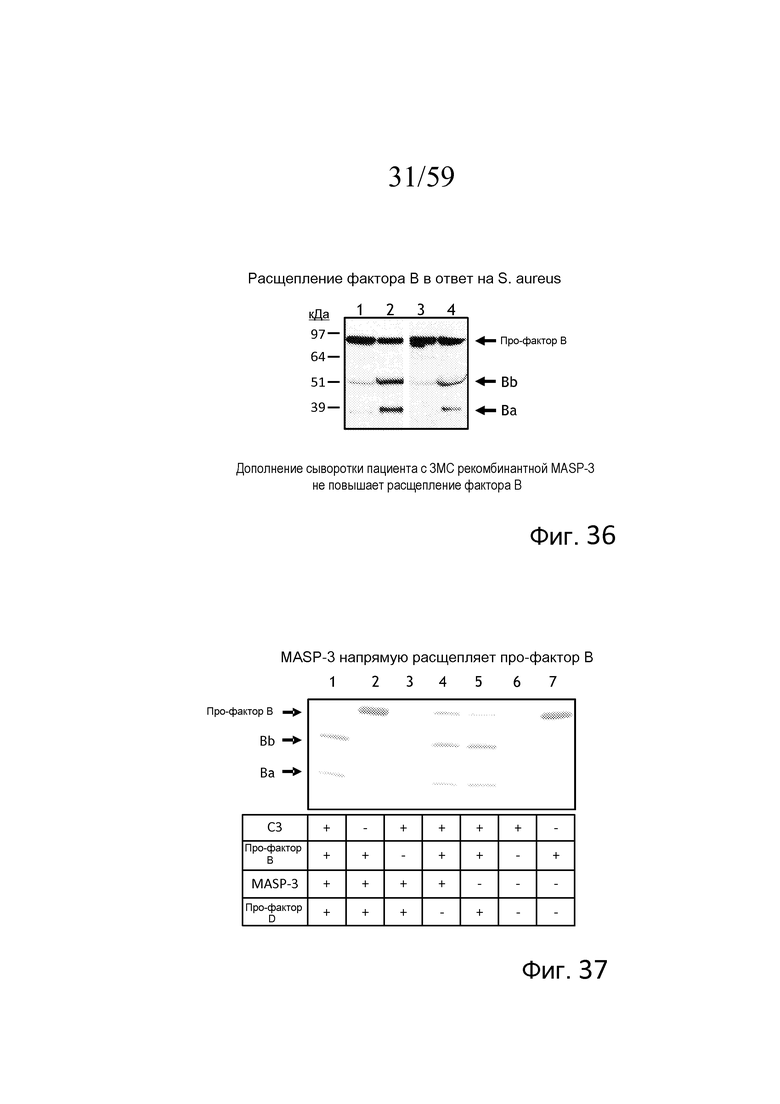
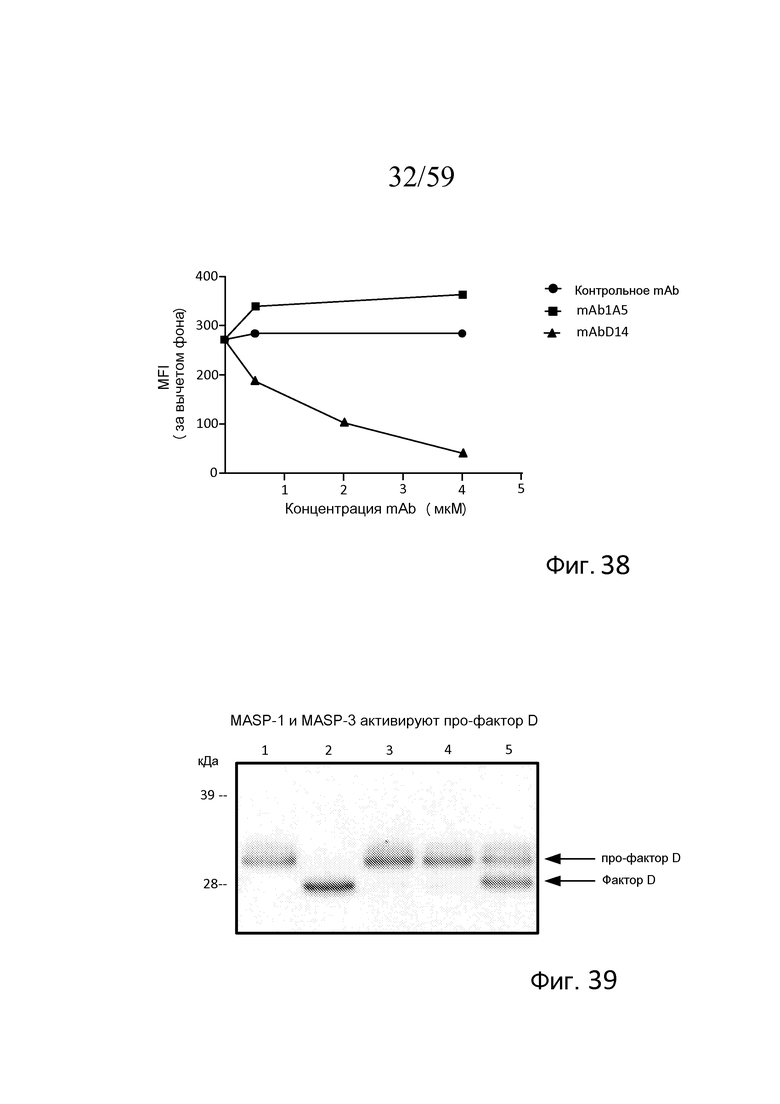
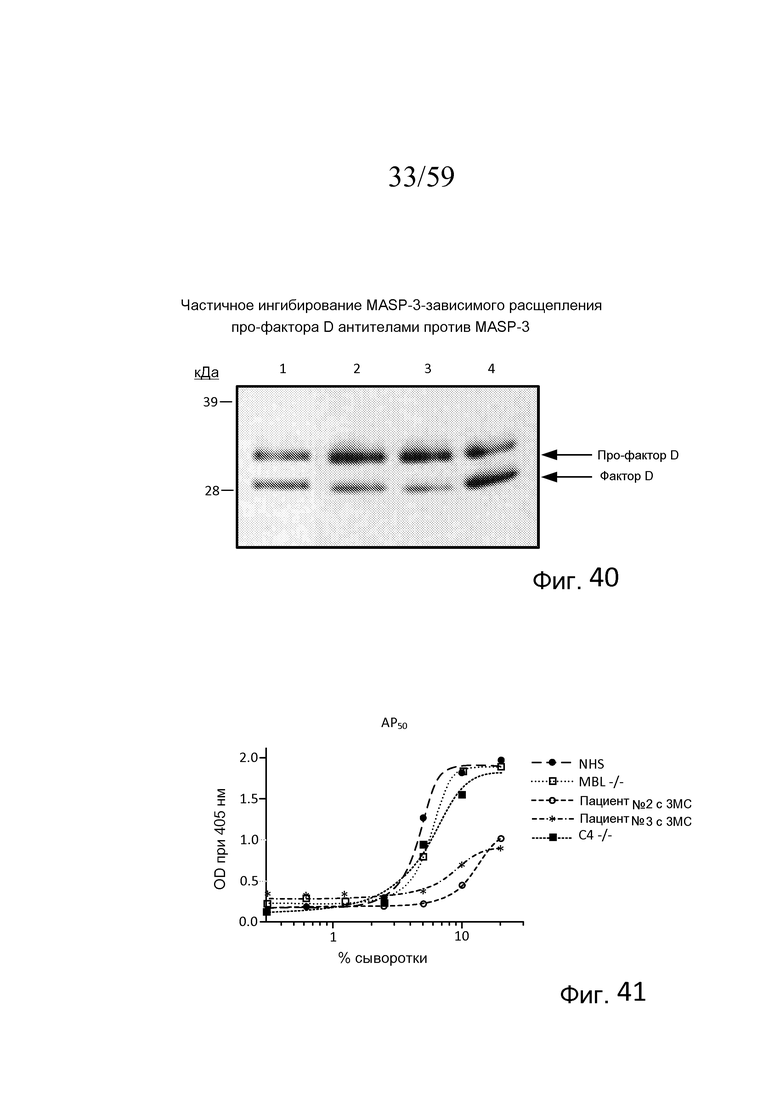
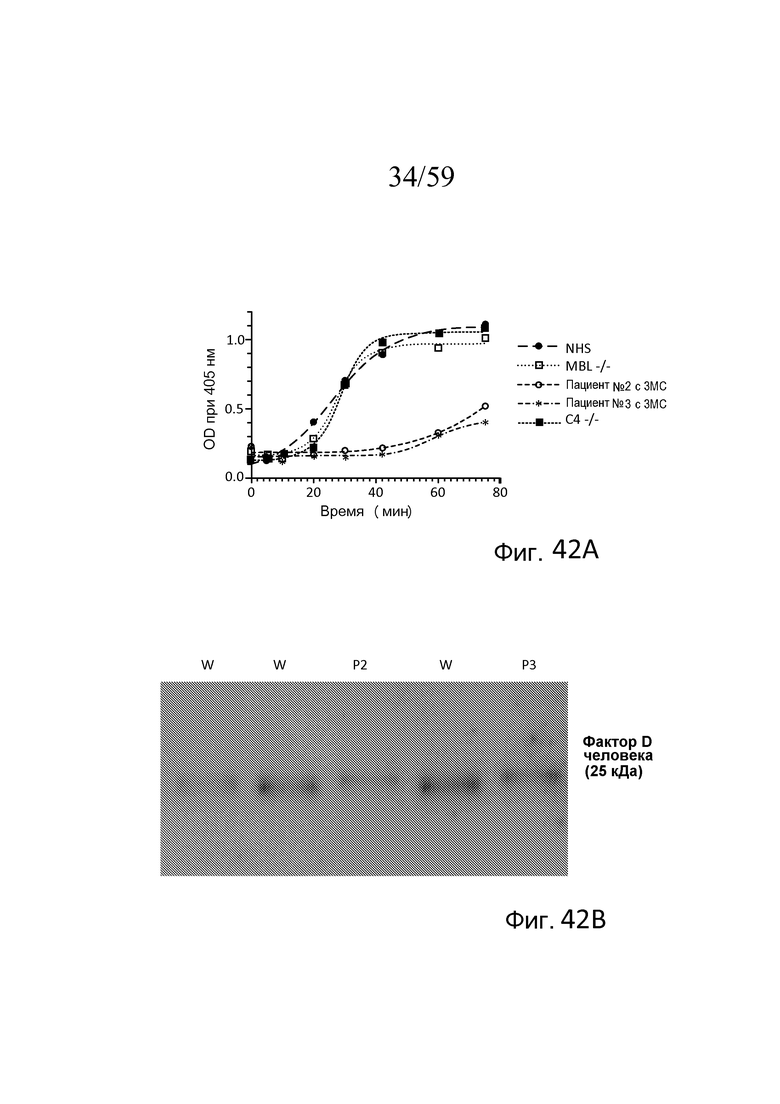
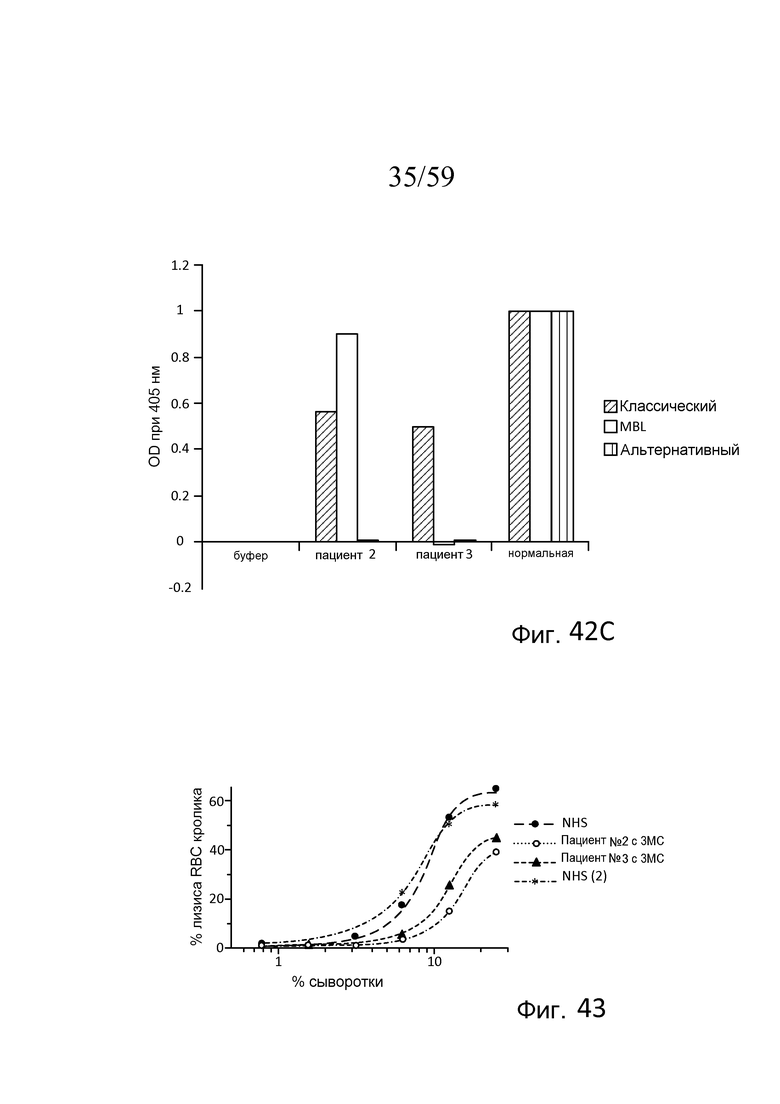
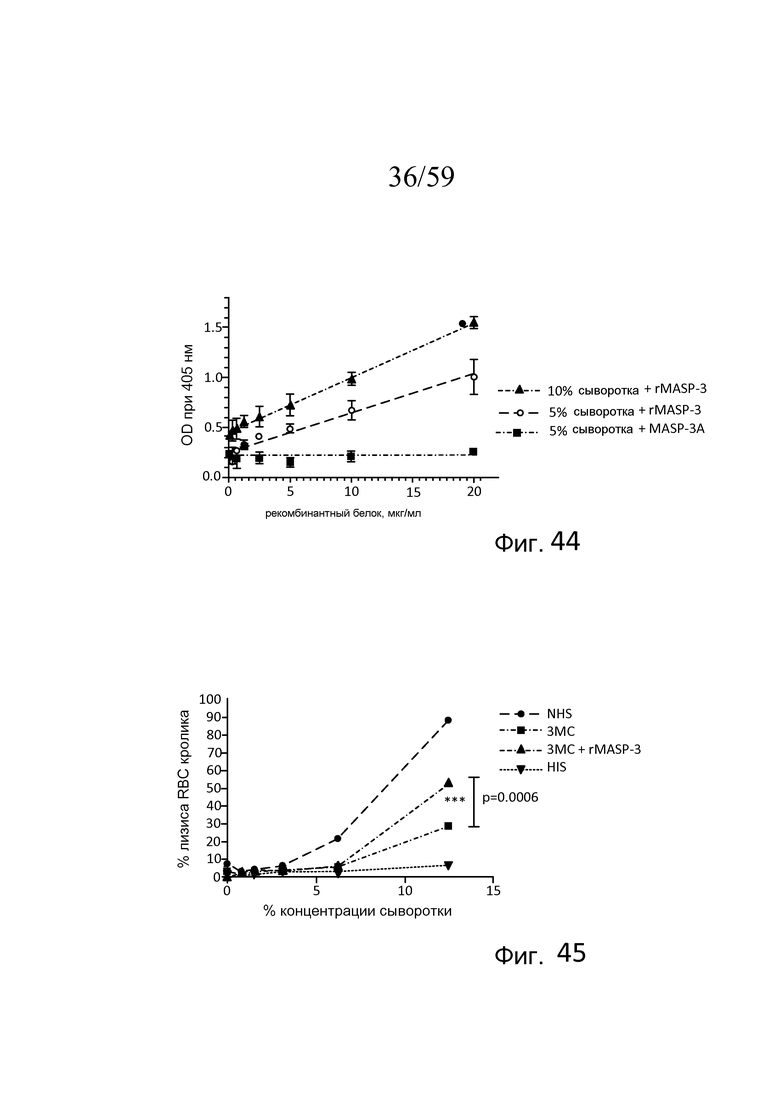
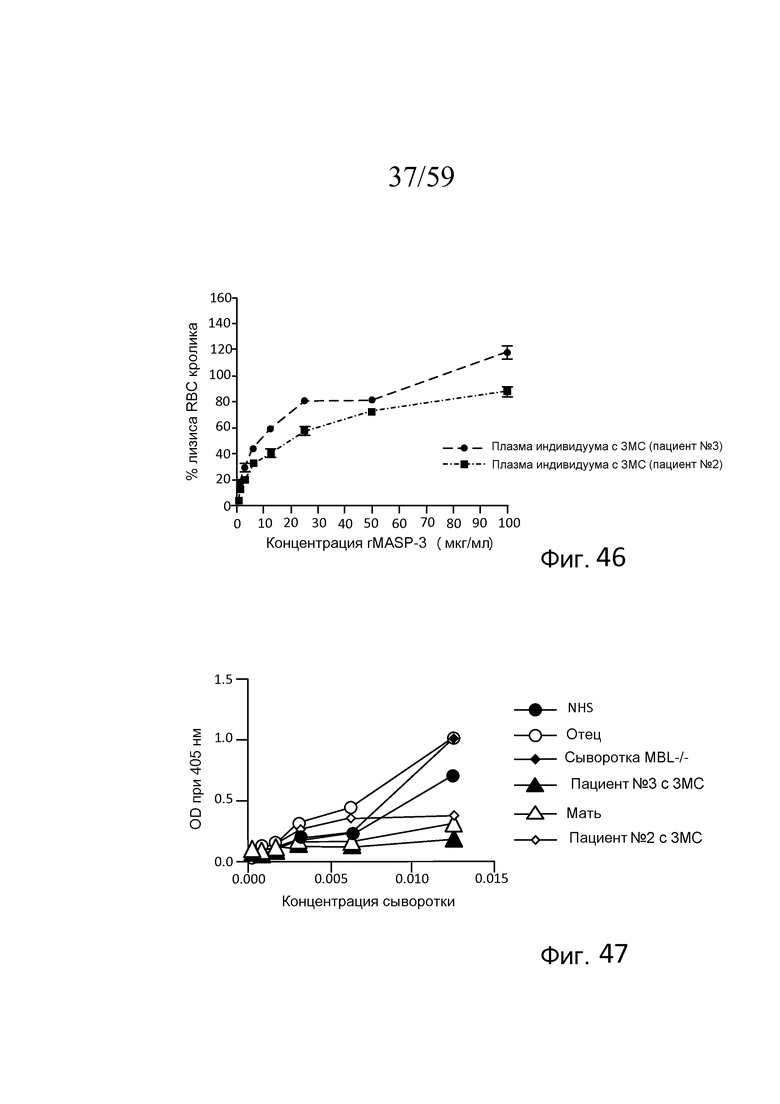
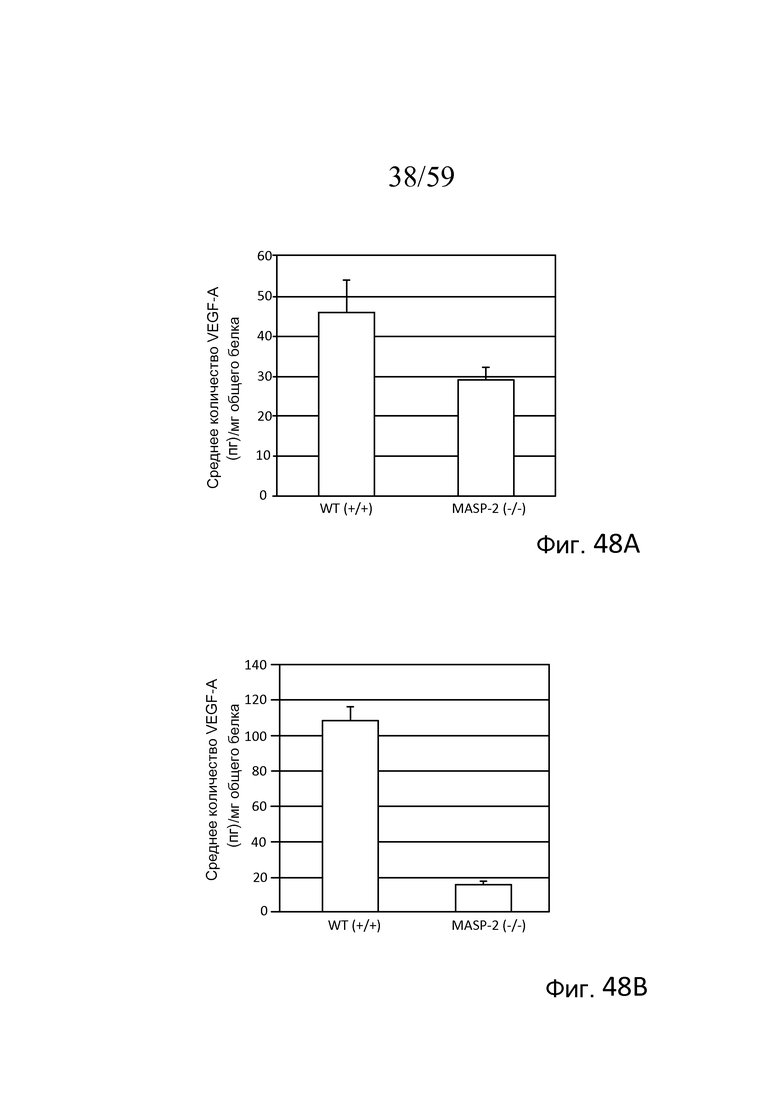
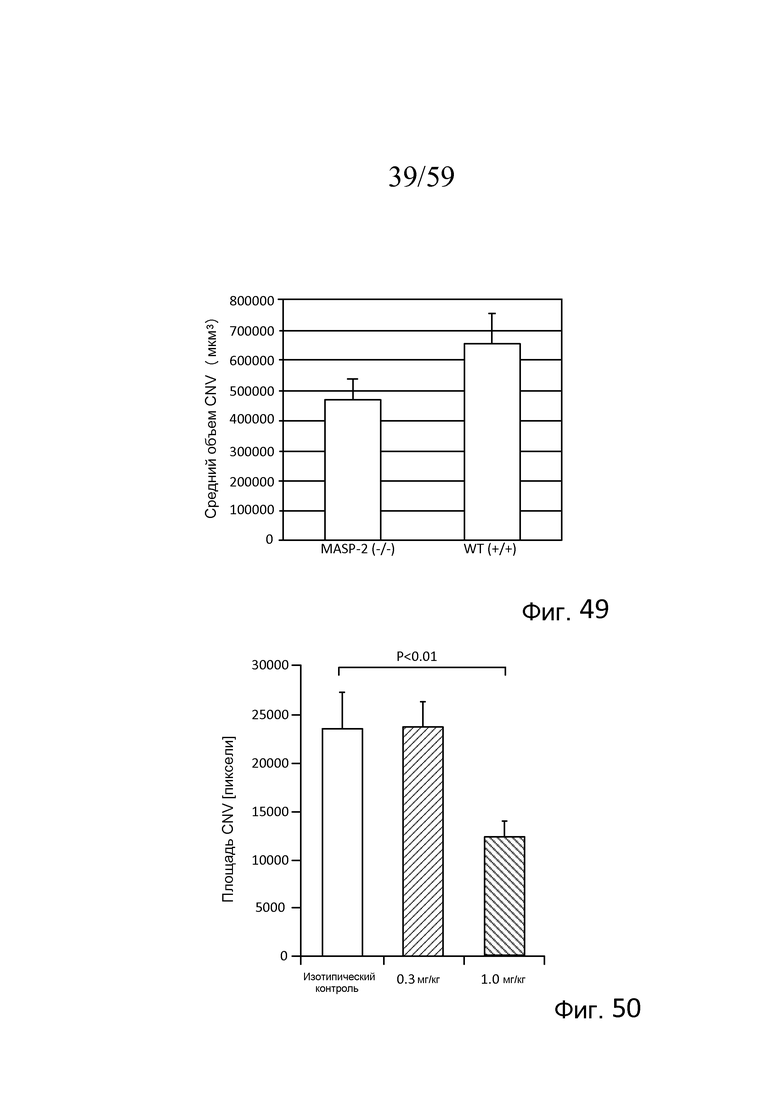
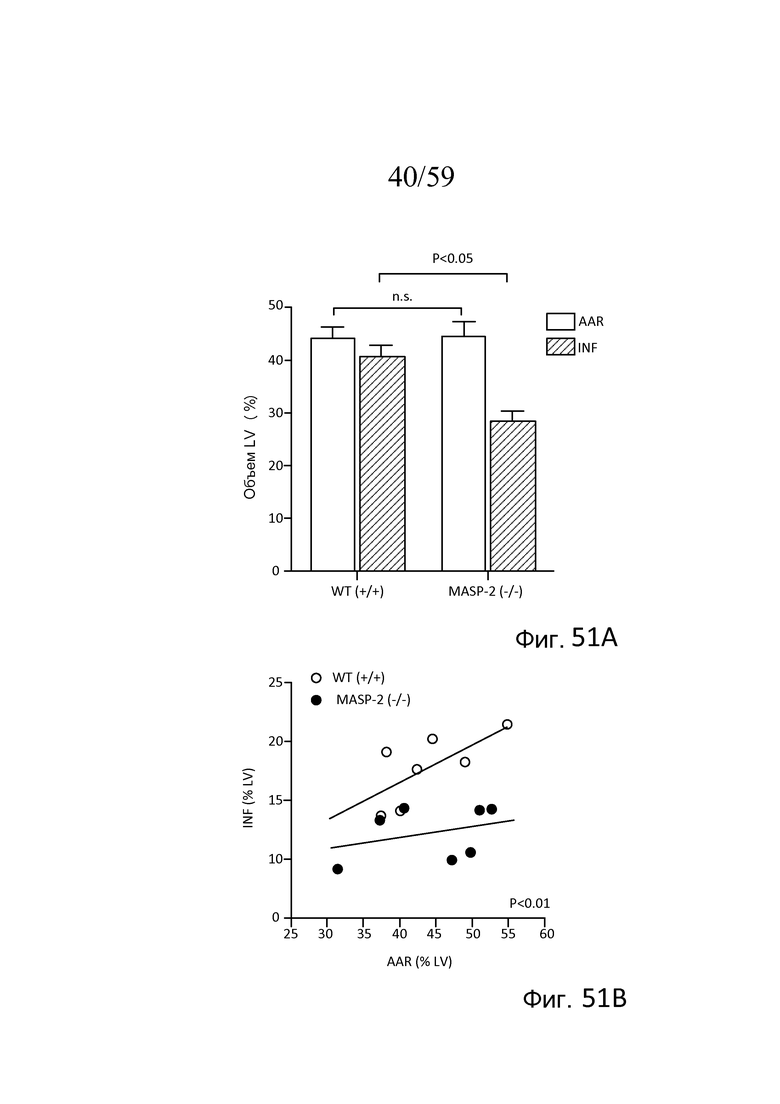
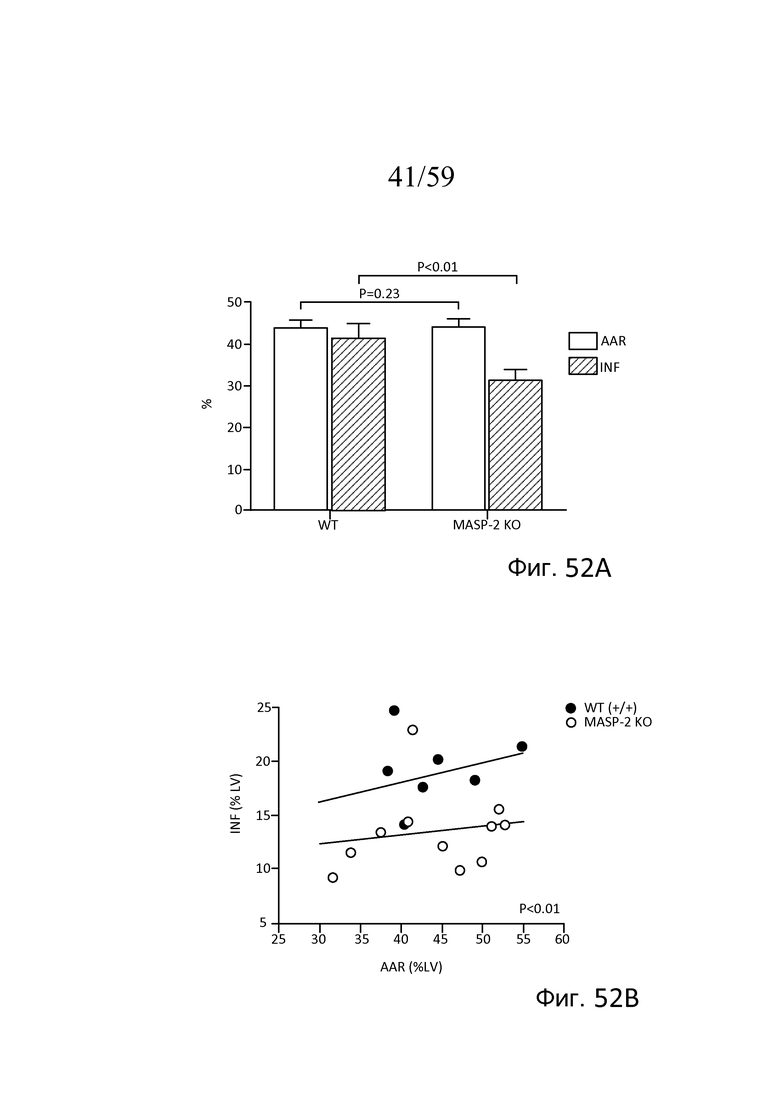
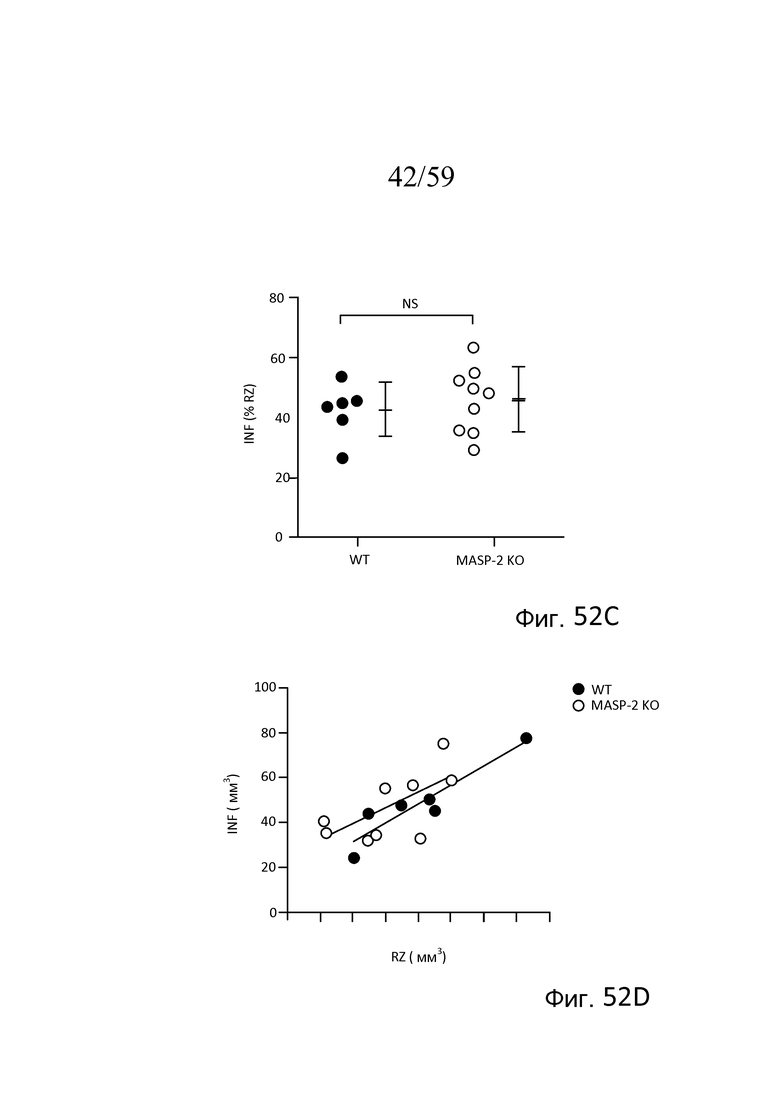
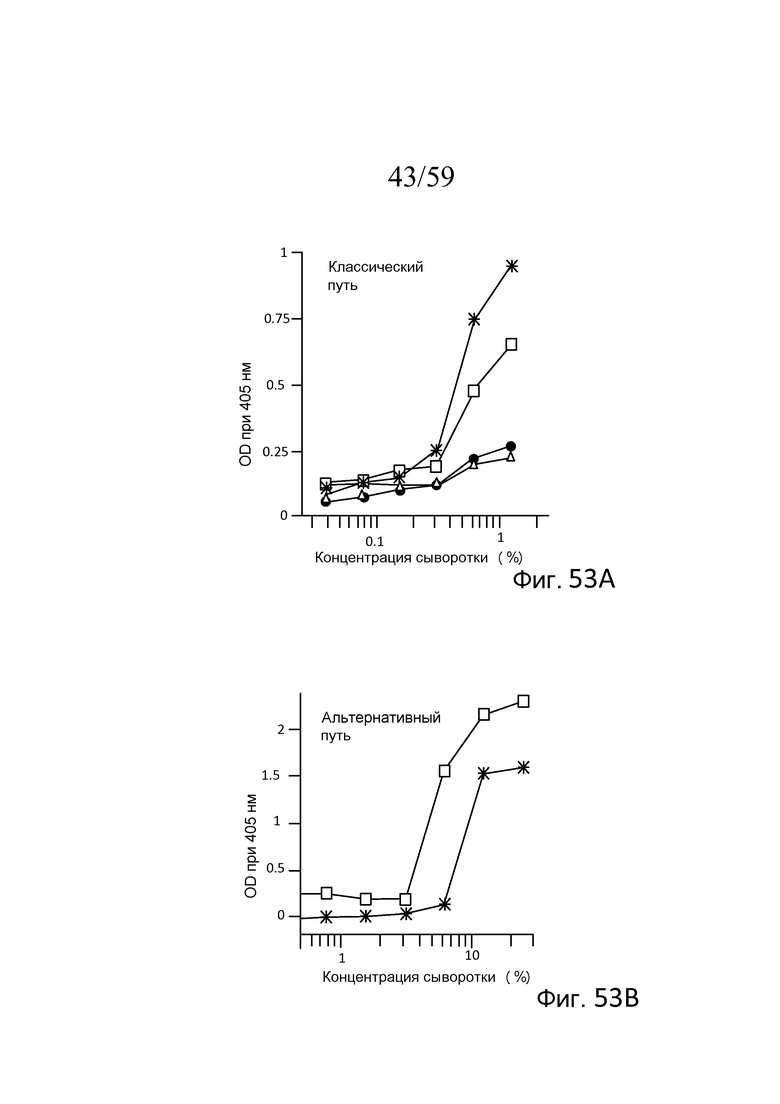
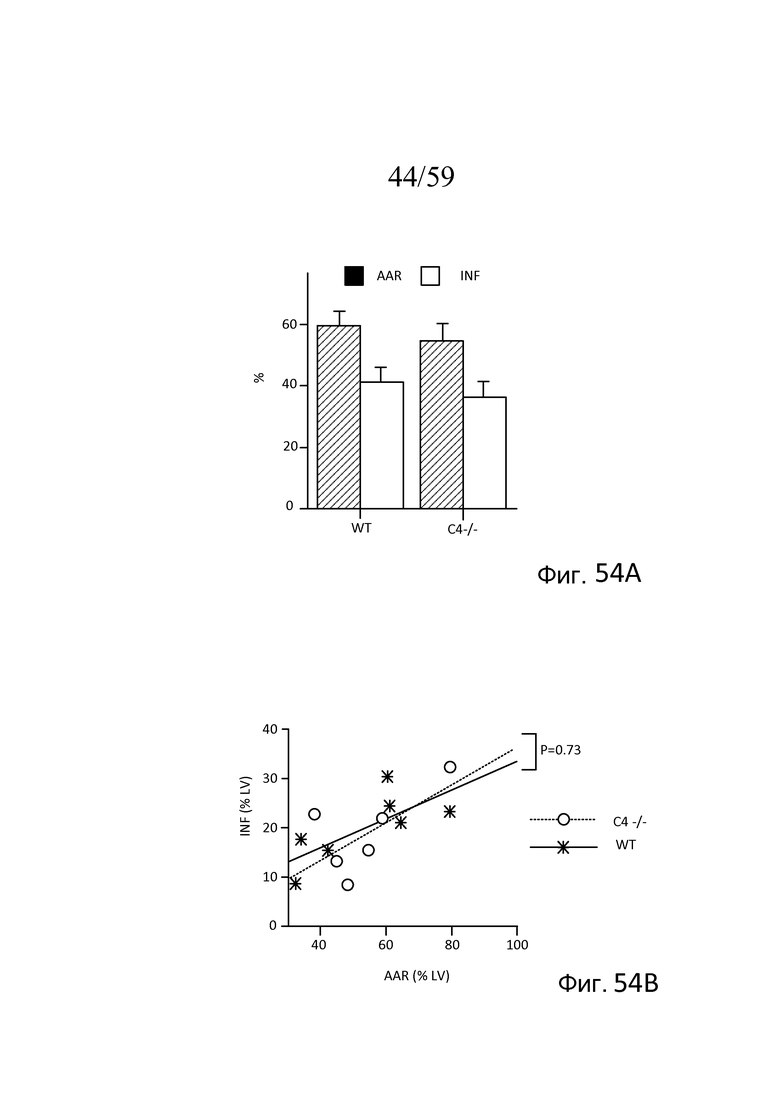
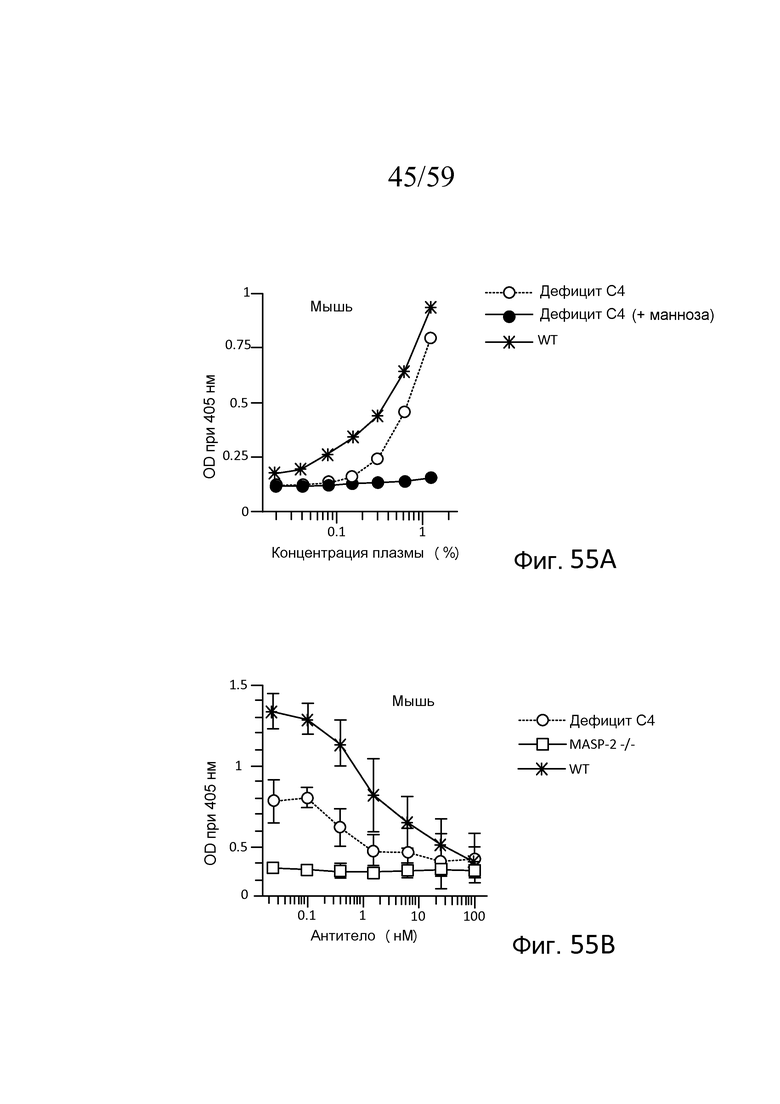

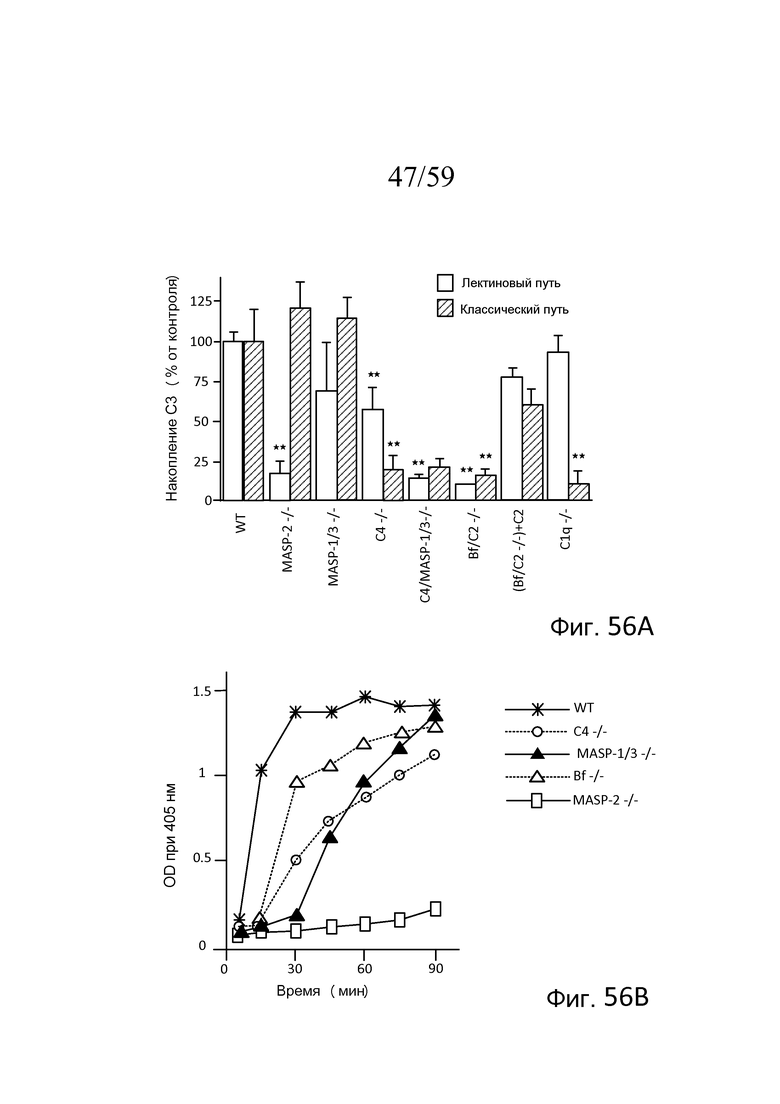
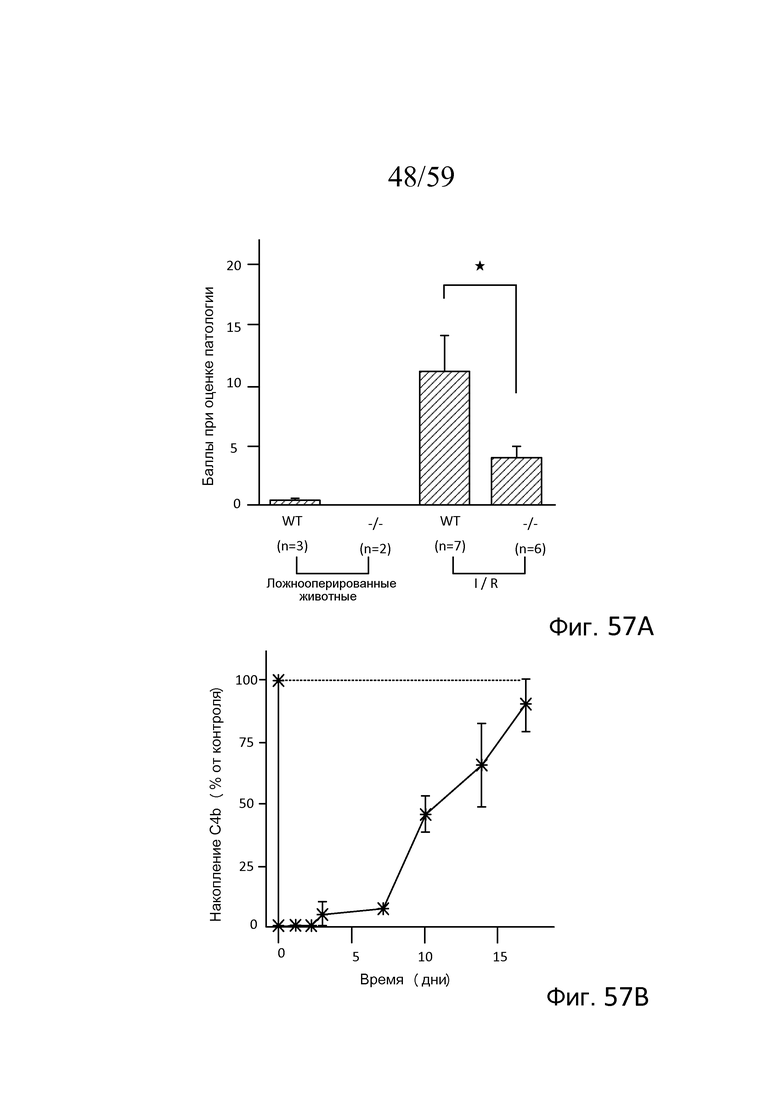
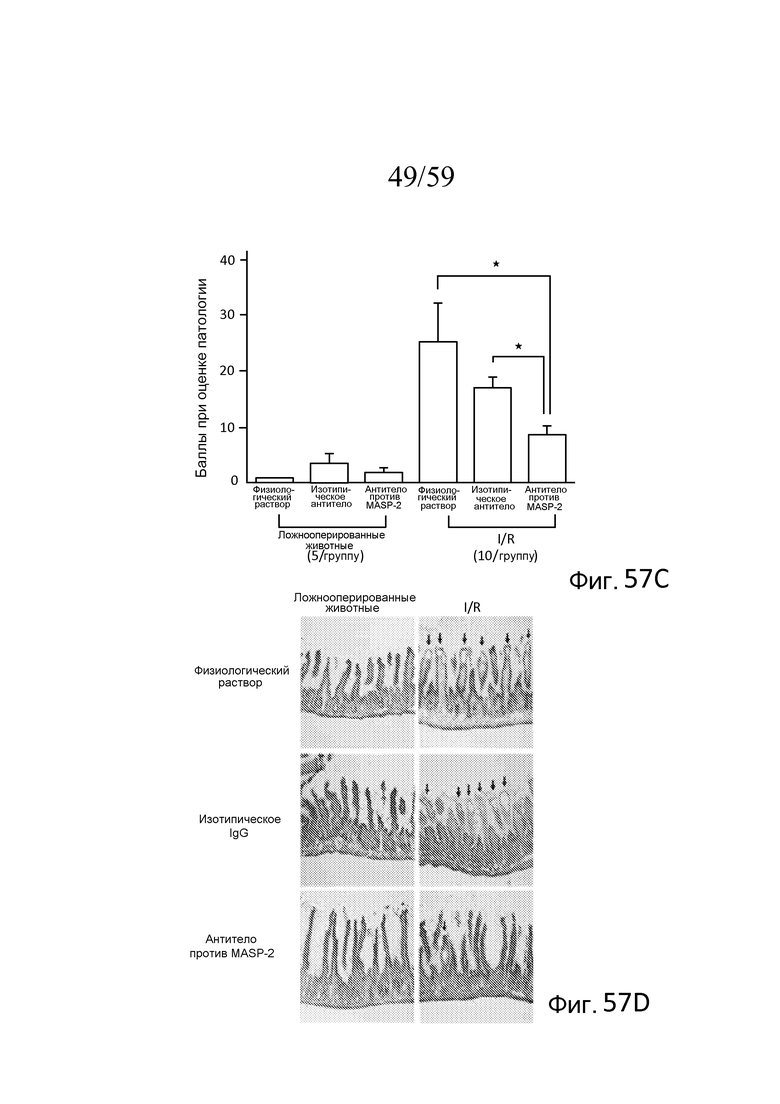
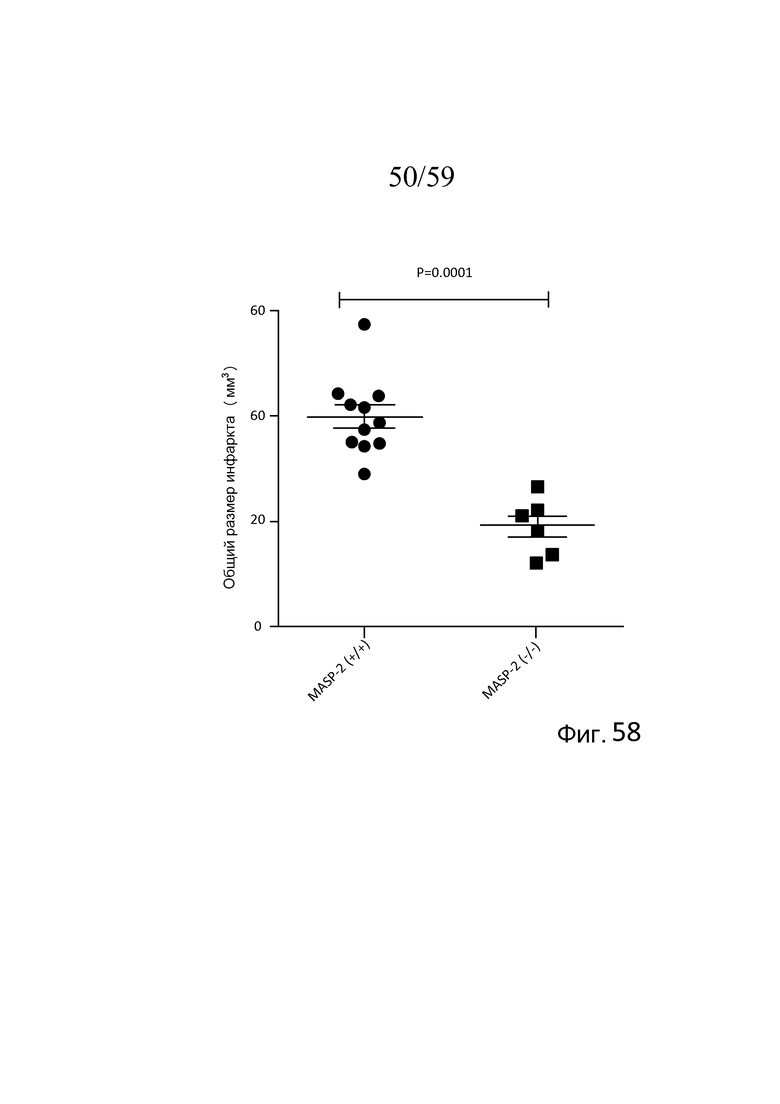
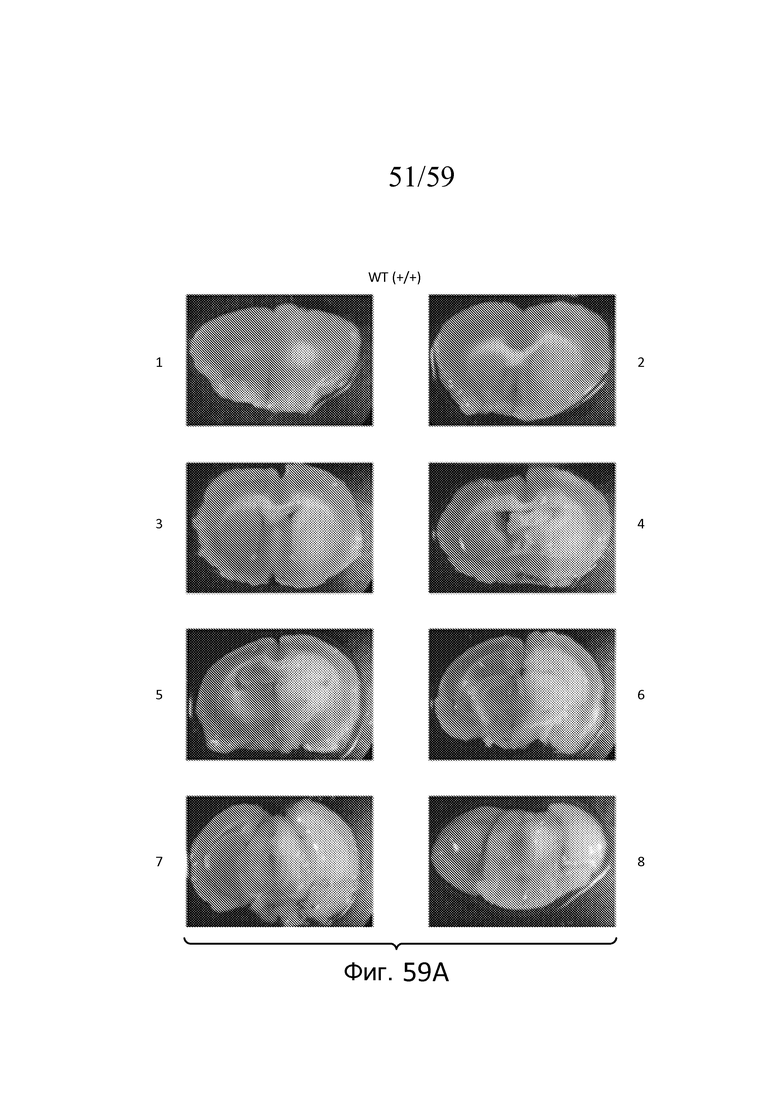
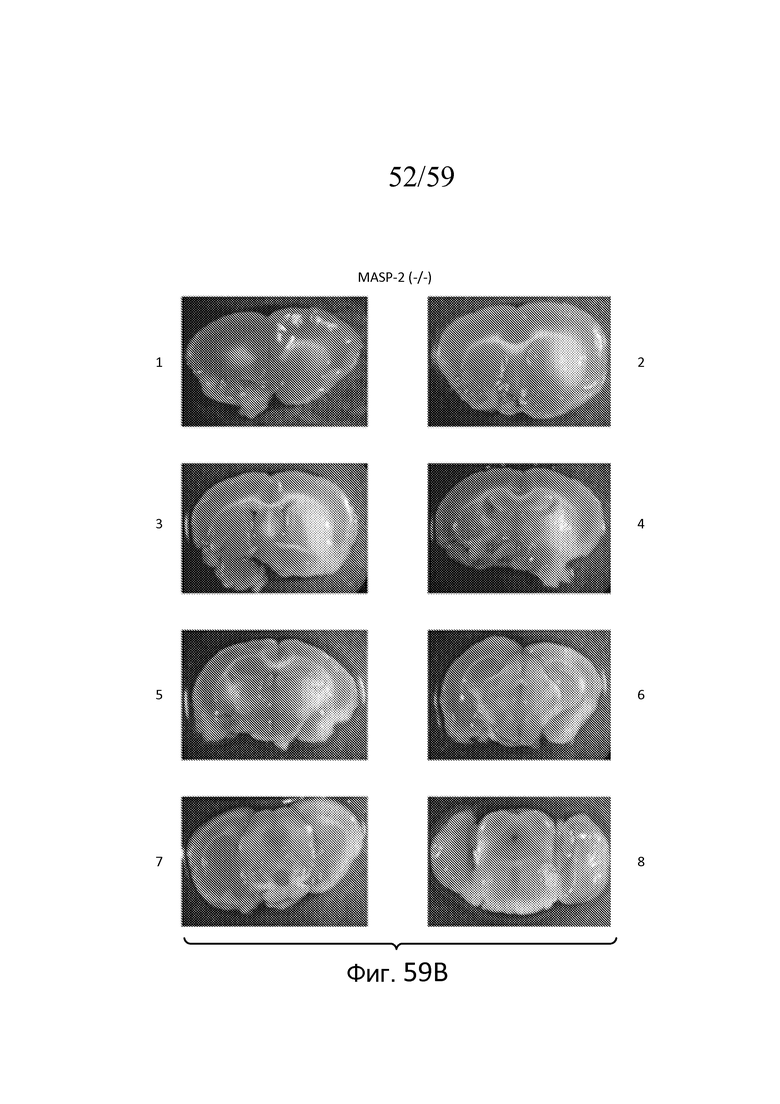
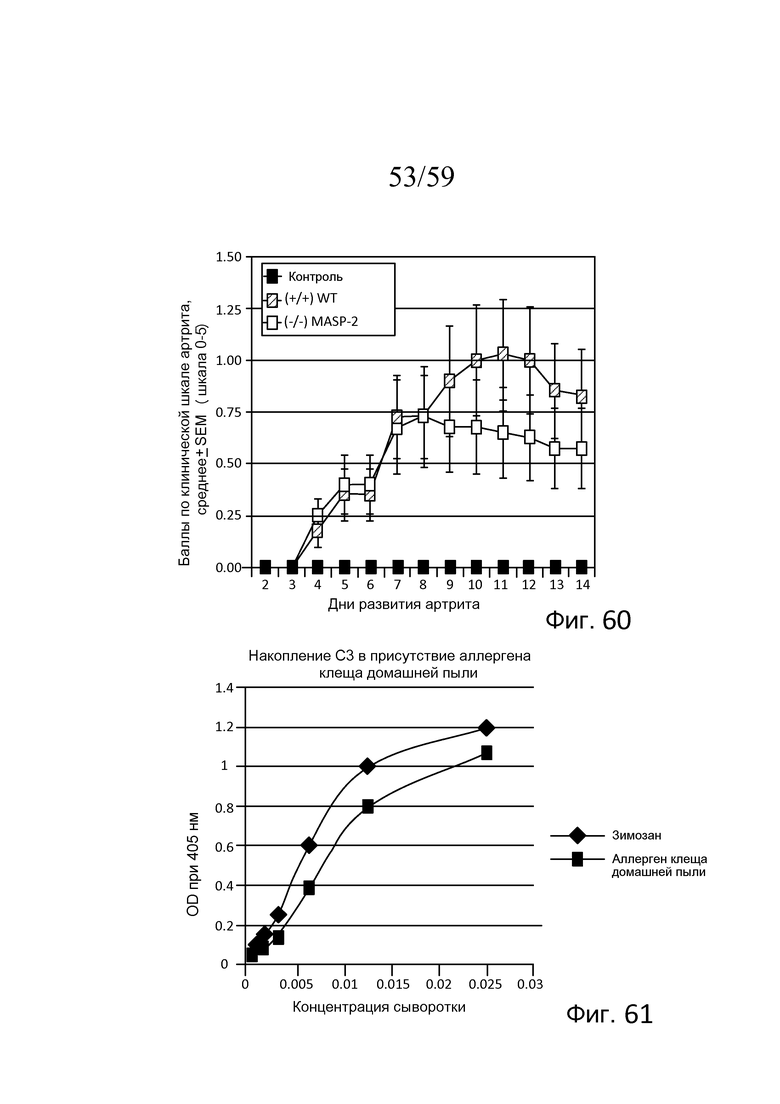
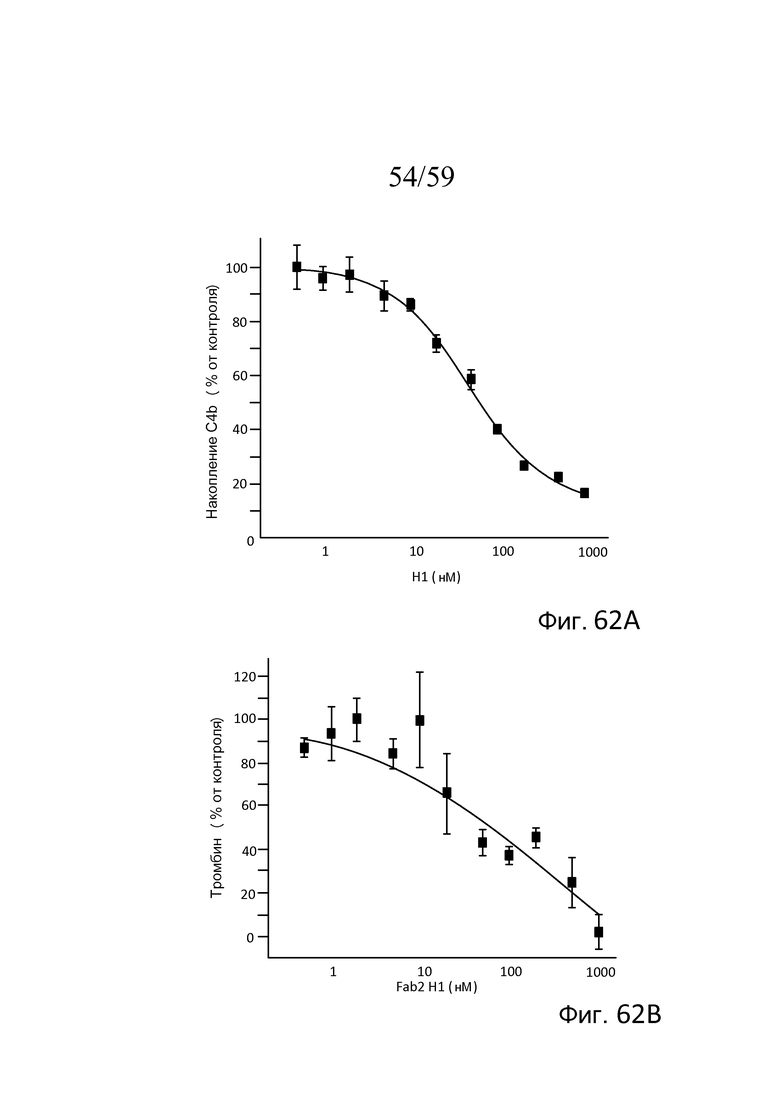
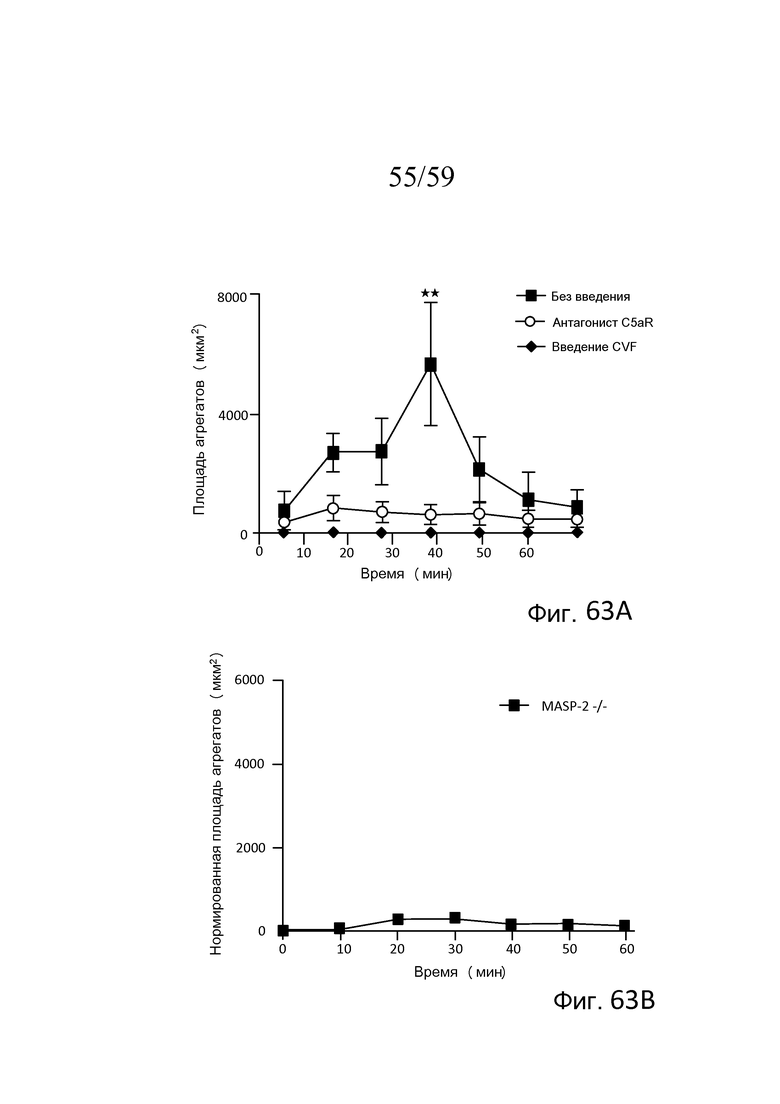
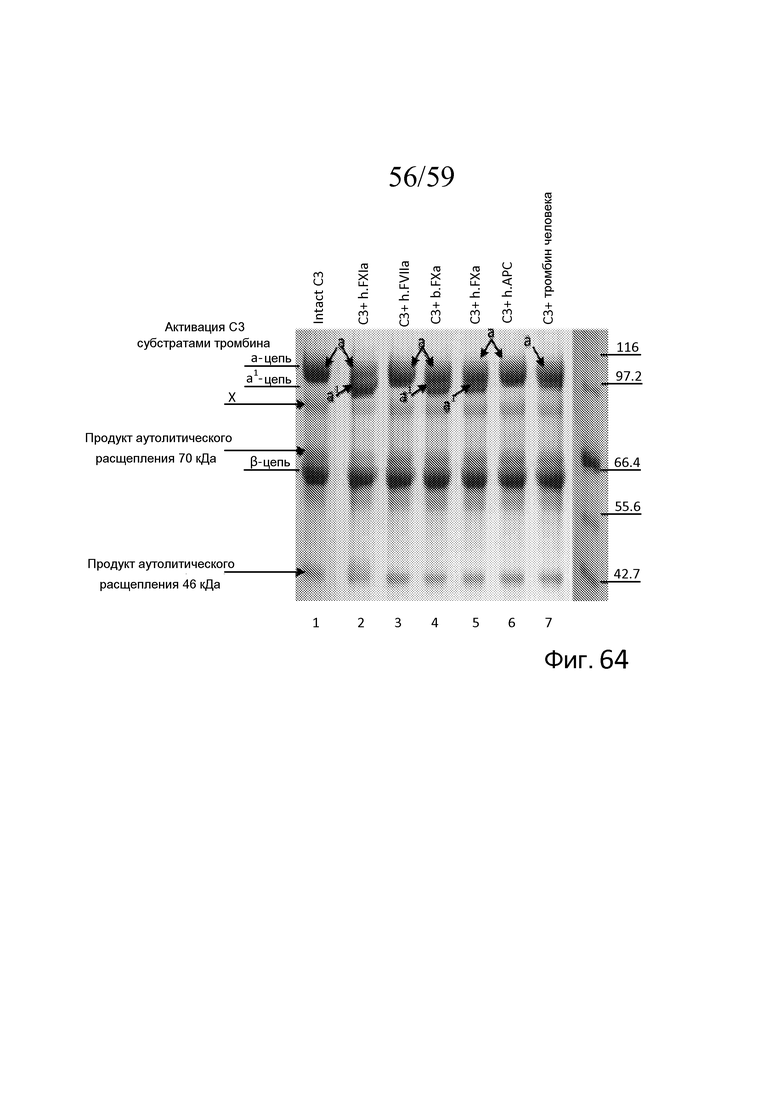
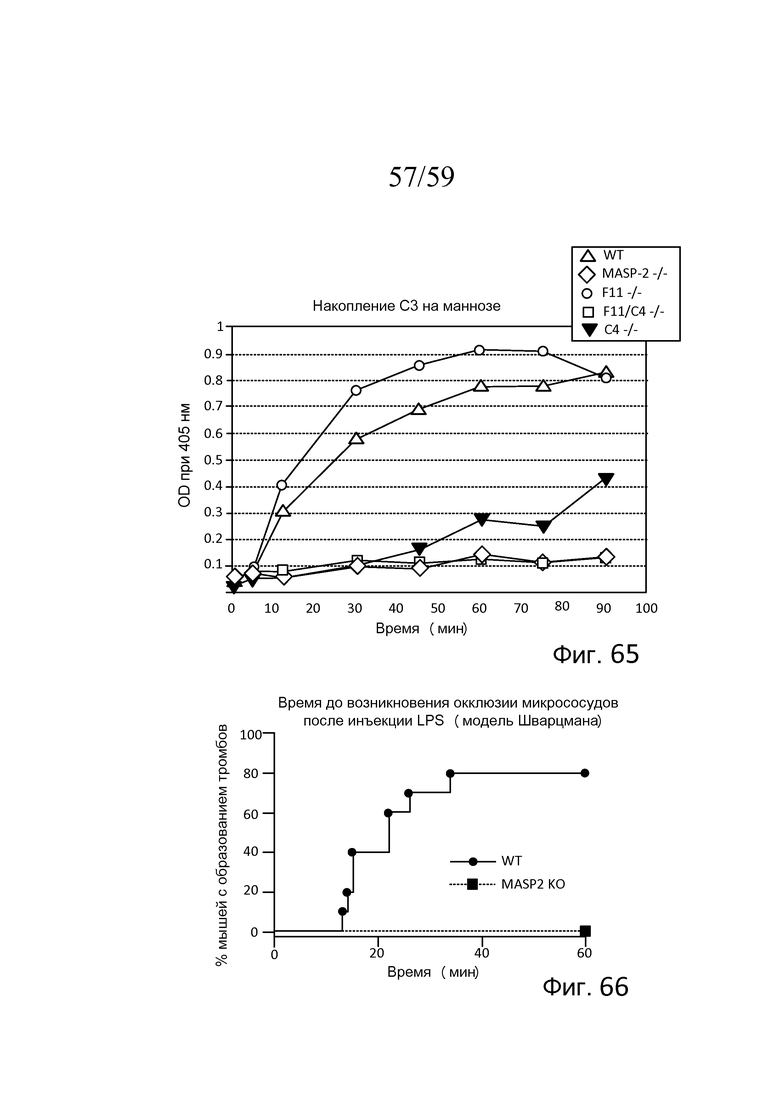
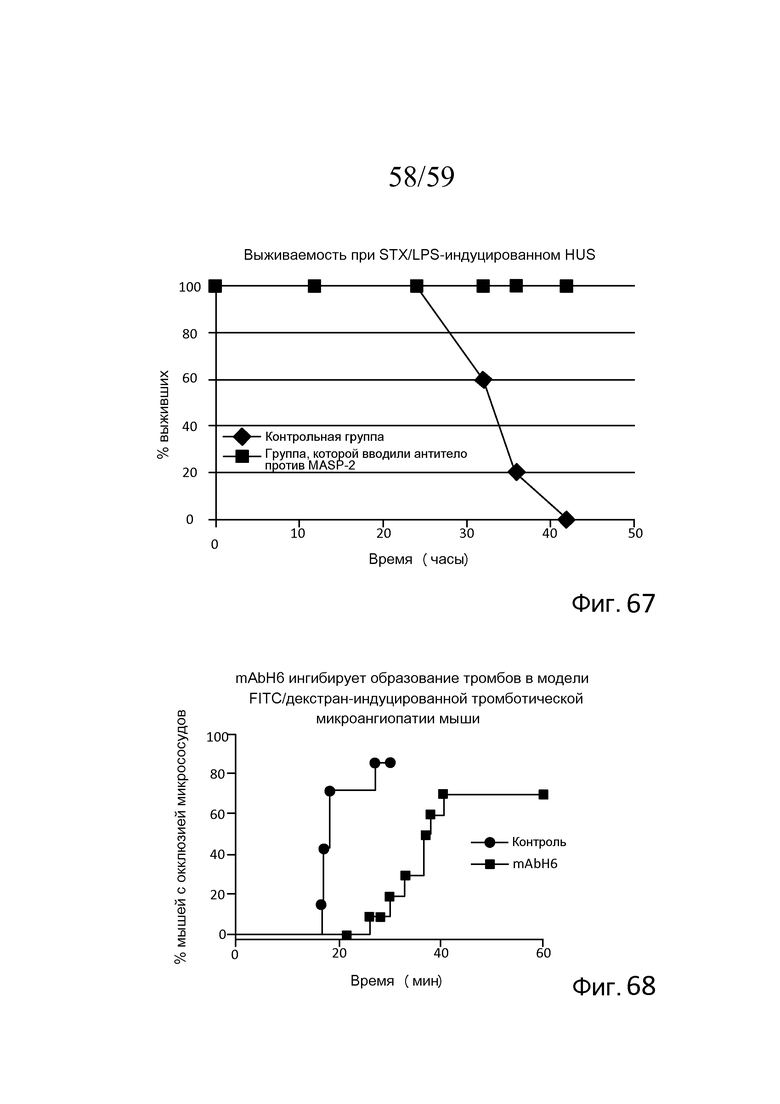
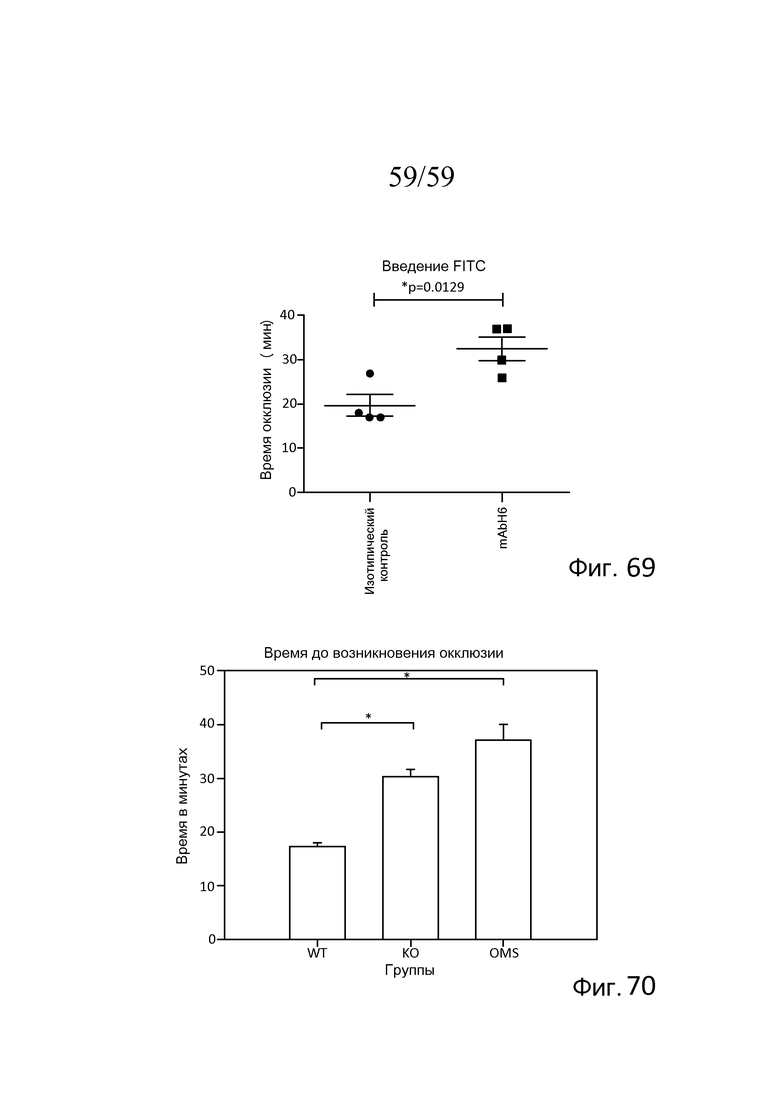
Изобретение относится к области биохимии, в частности к применению композиции, содержащей моноклональное антитело или его фрагмент против MASP-3, которое специфически связывается с частью MASP-3 человека и ингибирует созревание фактора D, для получения лекарственного средства для лечения субъекта. Изобретение позволяет эффективно осуществлять лечение заболевания или нарушения, выбранного из группы, состоящей из возрастной дегенерации желтого пятна, артрита, тромботической микроангиопатии, астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, нейромиелита зрительного нерва или болезни Бехчета. 25 з.п. ф-лы, 70 ил., 22 табл., 35 пр.
1. Применение композиции, содержащей количество средства, ингибирующего MASP-3, эффективное для ингибирования MASP-3-зависимой активации комплемента, для получения лекарственного средства для лечения субъекта, страдающего от заболевания или нарушения, выбранного из группы, состоящей из возрастной дегенерации желтого пятна, артрита, тромботической микроангиопатии, астмы, болезни плотного депозита, слабоиммунного некротизирующего гломерулонефрита с полулуниями, травматического повреждения головного мозга, аспирационной пневмонии, нейромиелита зрительного нерва или болезни Бехчета, где указанное средство, ингибирующее MASP-3, представляет собой моноклональное антитело против MASP-3 или его фрагмент, специфически связывающиеся с частью MASP-3 человека, как указано в SEQ ID NO: 8, и ингибирующее созревание фактора D.
2. Применение по п.1, где указанное лекарственное средство дополнительно содержит средство, ингибирующее MASP-1.
3. Применение по п.2, где средством, ингибирующим MASP-1, является моноклональное антитело против MASP-1 или его фрагмент, специфически связывающиеся с частью SEQ ID NO: 10.
4. Применение по п.1, где указанное лекарственное средство дополнительно содержит средство, ингибирующее MASP-2.
5. Применение по п.4, где средством, ингибирующим MASP-2, является моноклональное антитело против MASP-2 или его фрагмент, специфически связывающиеся с частью SEQ ID NO: 5.
6. Применение по п.1, где указанное лекарственное средство дополнительно содержит средство, ингибирующее MASP-1, и средство, ингибирующее MASP-2.
7. Применение по п.2, где средство, ингибирующее MASP-1, специфически связывается с частью MASP-1 с аффинностью по меньшей мере в 10 раз выше, чем при связывании с MASP-3, как указано в SEQ ID NO: 8.
8. Применение по п.2, где средство, ингибирующее MASP-1, специфически связывается с доменом сериновой протеазы MASP-1, как указано в а/к 449-694 в SEQ ID NO: 10.
9. Применение по п.1, где средство, ингибирующее MASP-3, связывается с частью MASP-3, как указано в SEQ ID NO: 8, и не ингибирует MASP-1 или MASP-2.
10. Применение по п.1, где средство, ингибирующее MASP-3, специфически связывается с частью MASP-3 с аффинностью по меньшей мере в 10 раз выше, чем при связывании с MASP-1, как указано в SEQ ID NO: 10.
11. Применение по п.1, где средство, ингибирующее MASP-3, специфически связывается с доменом сериновой протеазы MASP-3, как указано в а/к 450-711 в SEQ ID NO: 8.
12. Применение по п.6, где композиция содержит антитело против MASP-1 и антитело против MASP-2.
13. Применение по п.1, где композицию вводят системно.
14. Применение по п.13, где композицию вводят подкожно, внутримышечно, внутривенно, внутриартериально или в виде ингалянта.
15. Применение по п.1, где индивидуум страдает возрастной дегенерацией желтого пятна.
16. Применение по п.1, где индивидуум страдает артритом.
17. Применение по п.16, где артрит выбран из группы, состоящей из остеоартрита, ревматоидного артрита, ювенильного ревматоидного артрита и псориатического артрита.
18. Применение по п.1, где индивидуум страдает тромботической микроангиопатией.
19. Применение по п.18, где тромботическая микроангиопатия выбрана из группы, состоящей из гемолитико-уремического синдрома (HUS), атипичного гемолитико-уремического синдрома (aHUS) и тромботической тромбоцитопенической пурпуры (TTP).
20. Применение по п.1, где индивидуум страдает астмой.
21. Применение по п.1, где индивидуум страдает болезнью плотного депозита.
22. Применение по п.1, где индивидуум страдает слабоиммунным некротизирующим гломерулонефритом с полулуниями.
23. Применение по п.1, где индивидуум страдает травматическим повреждением головного мозга или имеет риск его развития.
24. Применение по п.1, где индивидуум страдает аспирационной пневмонией.
25. Применение по п.1, где индивидуум страдает нейромиелитом зрительного нерва.
26. Применение по п.1, где индивидуум страдает болезнью Бехчета.
| US20110311549 A1, 22.12.2011 | |||
| RU2008143559 A, 10.05.2010 | |||
| BRUCHIM Y., et al., Disseminated intravascular coagulation, Compend Contin Eud Vet, 2008, Vol.30, No.10, pp.E1-E10 | |||
| TAKAHASHI KAZUE et al., Mannose-binding lectin and its associated proteases (MASPs) mediate coagulation and its deficiency is a risk factor in developing complications from |
Авторы
Даты
2019-12-17—Публикация
2013-06-18—Подача