Изобретение относится к области медицинской химии и фармакологии, конкретно к новым соединениям (аддуктам) аскорбиновой кислоты с никотиновой или пиколиновой кислотами и способу их получения.
Ввиду особой биологической значимости апоптоза разработка препаратов, позволяющих направленно воздействовать на этот процесс, представляет большую важность для медицины и биологии. Индукторы апоптоза используются как в медицине в качестве лекарственных средств, обладающих апоптозиндуцирующей (противоопухолевой) активностью, так и в исследовательских целях при работе с клеточными культурами.
К настоящему времени известен ряд соединений, влияющих на апоптоз.
Известно средство, обладающее цитостатической и апоптозиндуцирующей активностью [1]. Изобретение используется в качестве лекарственного средства, обладающего цитостатической и апоптозиндуцирующей (противоопухолевой) активностью. Средство, обладающее цитостатической и апоптозиндуцирующей активностью, характеризующееся тем, что оно представляет собой β-аспарагин, полученный путем экстракции измельченных до определенных размеров частиц корней лопуха подогретой водой при определенном соотношении сырье : экстрагент, настаивания, отделения экстракта, концентрирования до сухого остатка в концентрате, фильтрования, двукратной перекристаллизации.
Известно изобретение, которое относится к биядерному катионному нитрозильному комплексу железа с природными алифатическими тиолилами общей формулы [Fe2(SR)2(NO)4]SO4, где R представляет собой алифатические лиганды природного происхождения [2]. Технический результат изобретения заключается в получении биядерного катионного нитрозильного комплекса железа, обладающего цитотоксической, апоптотической и NO-донорной активностью.
Известны хелатные комплексы ртути с цистеином и метионином, которые обладают противоопухолевым, противовирусным, противопаразитарным и иммуномодулирующим действием [3]. Изобретение обеспечивает получение новых хелатных комплексов ртути, обладающих противоопухолевым, противовирусным, противопаразитарным и иммуномодулирующим действием, а также упрощенный способ их получения, осуществляемый при более низких температурах.
Известно изобретение, которое относится к производному 1'-бромо-2',3',4'-триметоксибензо[5',6':4,5]-(aR,1S)-1-ацетамидо-6,7 дигидроциклогепта-[3,4-ƒ]- 1Н-индола [4]. Изобретение применяют в качестве активного компонента противоопухолевых лекарственных средств для лечения онкологических заболеваний. Соединения обладают высокой апоптозиндуцирующей активностью и активностью при ингибировании пролиферации опухолевых клеток.
Известно средство, обладающее апоптоз-индуцирующей активностью [5]. Средство представляет собой аскорбат лития общей формулы LiC6H7O6.2H2O. Изобретение расширяет арсенал средств, обладающих апоптоз-индуцирующей активностью.
Недостатком данных средств является их низкая эффективность, высокая токсичность, сложный процесс получения.
Близким аналогом заявляемого изобретения является аскорбат лития общей формулы LiC6H7O6 . 2H2O, проявляющий апопозиндуцирующую активность [5]. Изобретение относится к области медицины и биологии, а именно к веществам, обладающим апоптоз-индуцирующей активностью, и может быть использовано в онкологии, а также в качестве индуктора апоптоза при работе с клеточными культурами.
Апоптоз является генетически обусловленным механизмом клеточной гибели, играющий важную роль в регуляции дифференцировки клеток и поддержания гомеостаза организма. Процесс позволяет наиболее щадящим для организма путем ликвидировать клетки, имеющие генетические повреждения или метаболические нарушения, не совместимые с нормальной функцией. Апоптоз проявляется в уменьшении размера клетки, конденсации и фрагментации хроматина, уплотнении мембраны без выхода содержимого клетки наружу, и в конечном итоге, распаде клетки на апоптотические тельца, которые фагоцитируются макрофагами или соседними клетками без развития реакций воспаления и повреждения ткани. Однако, его апопозиндуцирующая активность невысока, кроме того аскорбат лития обладает нейрофизиологической активностью, которая способна оказать дополнительное воздействие на организм.
Никотиновая кислота (витамин B3 (PP) в основном применяется как специфическое средство для предупреждения и лечения пеллагры. Кроме того, ее используют при спазмах сосудов конечностей, головного мозга, при вяло заживающих ранах, язвах, невритах лицевого нерва, инфекционных заболеваниях, при желудочно-кишечных заболеваниях (гастритах с пониженной кислотностью, колитах), при заболеваниях печени [6].
Пиколиновая кислота в виде три пиколината хрома в комбинации с биотином применяется для лечения диабета II типа [7]. Изобретение относится к лечению инсулиннезависимого диабета взрослых (диабета II типа), в частности к лечению диабета II типа введением пиколината хрома и биотина. Способ лечения диабета II типа путем введения субъекту, страдающему этим заболеванием, комбинации трипиколината хрома с биотином. Оба эти соединения вводят орально или парентерально в таких суточных дозах, которые обеспечивают 50 - 1000 мкг хрома и 25 мкг - 200 мг биотина, причем такие количества хрома и биотина подобраны совместно, чтобы был обеспечен эффект, больший, чем аддитивный.
Известно также, что цитотоксическое действие некоторых противоопухолевых средств усиливается in vitro и in vivo в присутствии аскорбиновой кислоты [8].
Задачей заявленного изобретения является расширение арсенала высокоэффективных фармакологических апоптозиндуцирующих средств.
Поставленная задача решается получением новых соединений – аддуктов аскорбиновой С6Н8О6 (H2Asc) кислоты c пиколиновой С6Н5NО2 (HPic) либо никотиновой С6Н5NО2 (HNic) кислотой, обладающих апоптозиндуцирующим действием. Указанное соединение аскорбиновой и пиколиновой кислот и его свойства в литературе не описаны. Соединение аскорбиновой и никотиновой кислот известно [9], однако его свойства не изучались.
Апоптозиндуцирующие средства, представляют собой аддукты аскорбиновой кислоты с пиколиновой кислотой – аддукт (1) и никотиновой кислотой – аддукт (2) с общей формулой C6H5NO2 . C6H8O6, проявляющие апоптозиндуцирующую активность:
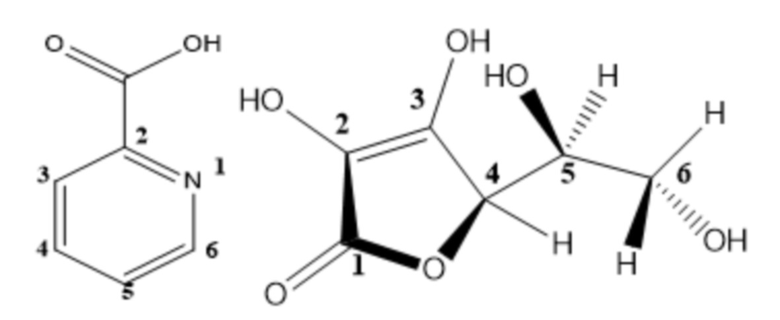 (1)
(1)
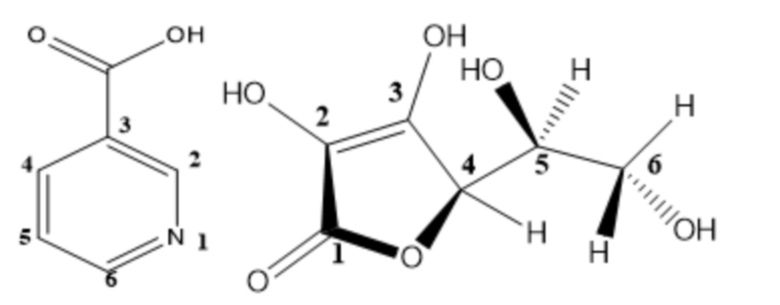 (2)
(2)
Способ получения аддуктов пиколиновой либо никотиновой кислоты с аскорбиновой кислотой характеризуется тем, что к водному раствору аскорбиновой кислоты добавляют пиколиновую кислоту либо никотиновую кислоту (последнюю предварительно обрабатывают микроволновым излучением) в мольном соотношении 1 : 2 (C6H5NO2 : C6H8O6) при постоянном перемешивании при комнатной температуре, а затем полученные осадки аддуктов промывают небольшими порциями растворителя и сушат на воздухе.
Факт применения аддуктов с достижением нового технического результата, заключающегося в апоптозиндуцирующем действии в отношении мононуклеарных клеток крови человека, для специалиста является не очевидным. Новые свойства не вытекают явным образом из уровня техники в данной области и не обнаружены в патентной и научно-технической литературе. Предлагаемое изобретение может быть использовано в медицине.
Исходя из вышеизложенного, следует считать заявляемое техническое решение соответствующим критериям: «Новизна», «Изобретательский уровень», «Промышленная применимость».
Синтез аддукта аскорбиновой кислоты с пиколиновой кислотой - аддукт (1) либо никотиновой кислотой – аддукт (2) осуществляется при комнатной температуре в водном растворе и мольном соотношении исходных компонентов 1 : 2 (С6Н5NО2 : С6Н8О6), причём никотиновая кислота предварительно подвергается воздействию микроволнового излучения. Выделенные осадки аддуктов промывают небольшими порциями растворителя и сушат на воздухе, состав получаемых соединений соответствует формуле С6Н5NО2 . С6Н8О6. Полученные соединения идентифицировали методами элементного анализа, ИК-спектроскопии (отнесение полос сделано на основании совпадения экспериментальных спектров и спектров, рассчитанных методом DFT (B3LYP 6-311+G(d,p)), ЭСП (электронный спектр поглощения в УФ-области), STA (синхронный термический анализ). Контроль состава синтезированных продуктов осуществляли определением содержания аскорбиновой кислоты в аддуктах перманганатометрическим методом (эмпирический титр рабочего раствора КМnO4 устанавливался по аскорбиновой кислоте в 2 N растворе H2SO4; точность определения ±1,5 %).
Токсичность соединений (1) и (2) в остром опыте определена на 24 мышах линии BALB/c при однократном введении водного раствора соединения в желудок в широком спектре доз (от 10 до 100 мг/кг веса). Наблюдения велись в течение 14 суток. При этом не обнаружено видимых признаков интоксикации и гибели подопытных животных. Согласно ГОСТ 12.1.007-76 соединения (1) и (2) при введении в желудок является малотоксичными соединениями.
Апоптозиндуцирующая активность соединений (1) и (2) определялась методом проточной цитофлуориметрии [10]. Метод заключается в определении фосфатидилсерина на поверхности клетки при связывании с меченным аннексином V и окраски ядерным красителем (йодидом пропидия), с последующей детекцией интенсивности флуоресценции. В качестве референтных препаратов для оценки апоптозиндуцирующей активности использовали пиколиновую и никотиновую кислоту по схеме, аналогичной соединениям (1) и (2).
Изобретение будет понятно из следующего описания и приложенной к нему фигуры.
Пример 1. Способ получения заявляемого соединения (1)
При комнатной температуре к водному раствору аскорбиновой кислоты (1,760 г H2Asc в 5 мл Н2О) добавляют навеску пиколиновой кислоты (0,615 г). После непродолжительного перемешивания образуется жёлтый осадок аддукта. Осадок оставляют на кристаллизацию (1 ч), затем фильтруют и промывают небольшими порциями воды. Выход продукта около 67 %, содержание аскорбиновой кислоты в его составе составляет 61,0 %, что немного превышает теоретическое значение - 58,86% (теор.), рассчитанное для С6Н5NО2 . С6Н8О6, tпл. = 174,4 оС (с разл.).
Для соединения С6Н5NО2 . С6Н8О6:
вычислено, %: С 48,12; Н 4,34; N 4,68
найдено, %: С 47,3; Н 4,4; N 5,4.
ИК спектр (эксп.), ν, см-1: 531(δ.С(2)-СООН); 688, 731,764, 1008 (δ. лактонового и пиридинового колец); 1109, 1136, 1296 (ɣ. аскорбиновой кислоты); 1233 (ɣ. пиколиновой кислоты); 1399, 1450 (δ.С(2)О-Н и OСО-Н); 1605, 1676, 1772 (v.C=О,С=С); 3345, 3452 (v.O-H).
ИК спектр (расчёт.), ν, см-1: 569 (δ.С(2)О-Н и С(4)-СООН); 691, 759, 773 (δ. лактонового и пиридинового колец); 870 (δ. С(4)-СООН); 1041, 1139, 1155, 1237 (ɣ. аскорбиновой и никотиновой кислот); 1375, 1449 (δ.С(2)О-Н и OСО-Н); 1723, 1750, 1806 (v.C=О,С=С); 3341, 3439 (v.O-H).
УФ-спектр HPic (тв.) λmax, нм: 236, 241, 283, 299.
УФ-спектр H2Asc (тв.) λmax, нм: 243, 256, 265.
УФ-спектр аддукта HPic . H2Asc (тв.) λ max, нм: 241, 245, 255, 279,299, 311, 318, 328, 336.
Пример 2. Способ получения заявляемого соединения (2)
При комнатной температуре к водному раствору аскорбиновой кислоты (0,880 г в 5 мл Н2О) добавляют навеску никотиновой кислоты (0,308 г), предварительно обработанную микроволновым излучением (2,45 ГГц мощностью 119 Вт в течение 1 мин). После непродолжительного перемешивания на магнитной мешалке образуется жёлтый осадок аддукта, который после часового созревания фильтруют, и сушат на воздухе. Выход аддукта около 94 % и содержание в его составе аскорбиновой кислоты составляет 60,0 %, tпл. = 187,2 оС (с разл.).
Для соединения С6Н5NО2 . С6Н8О6:
найдено, %: С 46,6; Н 4,2; N 4,9.
вычислено, %: С 48,12; Н 4,34; N 4,68.
ИК спектр, ν, см-1: 560 (δ.С(2)О-Н и С(3)-СООН ); 673, 695 (δ. лактонового и пиридинового колец); 749 (δ. О-С(1)-С(2)-О-Н и СООН); 1036, 1121, 1157 (ɣ. аскорбиновой и никотиновой кислот); 1389, 1458 (δ.С(2)О-Н и OСО-Н); 1624, 1685, 1758 (v.C=О,С=С); 3235, 3368 (v.O-H).
ИК спектр (расчёт.), ν, см-1: 569 (δ.С(2)О-Н и С(4)-СООН); 691, 759, 773 (δ. лактонового и пиридинового колец); 870 (δ. С(4)-СООН); 1041, 1139, 1155, 1237 (ɣ. аскорбиновой и никотиновой кислот); 1375, 1449 (δ.С(2)О-Н и OСО-Н); 1723, 1750, 1806 (v.C=О,С=С); 3341, 3439 (v.O-H).
УФ-спектр HNic (тв.), λmax, нм: 236, 265, 276, 308, 314.
УФ-спектр H2Asc (тв.), λmax, нм: 243, 256, 265.
УФ-спектр аддукта HNic . H2Asc (тв.), λ max, нм: 236, 252, 281, 297, 312, 318, 328.
Пример 3. Изучение острой токсичности соединения (1)
Острую токсичность соединения (1) исследовали на беспородных белых мышах с массой 19±2,0 г. Группе животных однократно в желудок через зонд вводили соединение (1) в дозах 5000, 7500 и 1000 мг/кг. Контрольные животные получали дистиллированную воду. Наблюдения за животными вели в течение двух недель. Отсутствие гибели животных свидетельствует о низкой токсичности соединения (1) в соответствии с ГОСТ 12.1.007-76. Дозы, вызывающие 50% гибель мышей, для пиколиновой кислоты и аскорбиновой кислоты больше 5000 мг/кг, малотоксичные соединениея (4-й класс опасности).
Пример 4. Изучение острой токсичности соединения (2)
Острую токсичность соединения (2) исследовали на беспородных белых мышах с массой 19±2,0 г. Группе животных однократно в желудок через зонд вводили соединение (2) в дозах 5000, 7500 и 1000 мг/кг. Контрольные животные получали дистиллированную воду. Наблюдения за животными вели в течение двух недель. Отсутствие гибели животных свидетельствует о низкой токсичности соединения (2) в соответствии с ГОСТ 12.1.007-76. Дозы, вызывающие 50% гибель мышей, для никотиновой кислоты и аскорбиновой кислоты больше 5000 мг/кг, малотоксичные соединения (4-й класс опасности).
Пример 5. Изучение апоптозиндуцирующей активности
Апоптозиндуцирующая активность соединений (1) и (2) определялась по следующей методике.
Мононуклеары периферической крови здоровых доноров, выделенные на градиенте фиколла, суспендировали в среде RPMI 1640 в концентрации 4 . 104 клеток/мл. Раствор аддукта аскорбиновой и пиколиновой (либо никотиновой) кислот (точная навеска 50 мг в 10 мл дистиллированной воды) добавляли в культуру мононуклеарных клеток крови из расчёта на требуемую конечную концентрацию аддукта – 0,05 мг/мл, 0,1 мг/мл. Затем планшет с клетками инкубировали в течение 24 часов (37 °С, 5 % СО2). Уровень апоптоза определяли методом проточной цитофлуориметрии по интенсивности сигнала красителей, конъюгированных c апоптотическими клетками.
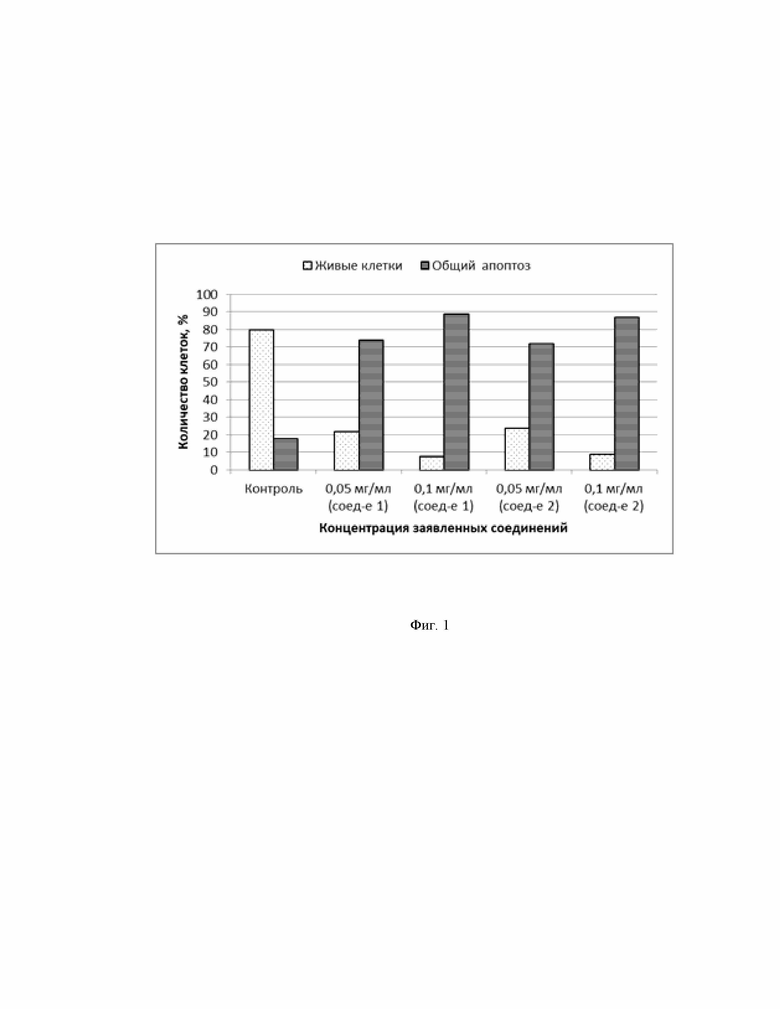
Результаты определения уровня апоптоза представлены в табл. 1 в процентах апоптотических клеток после 24 часов инкубации с заявленными соединениями и референтными веществами.
Результаты определения уровня апоптоза при воздействии различных концентраций заявляемых соединений представлены на Фиг. 1. Данные показаны в виде общего количества клеток в состоянии раннего и позднего (общего) апоптоза, выраженные в процентах.
Таблица 1. Сравнение уровня апоптоза при воздействии заявленных соединений и референтных веществ

Литература
1. Патент РФ 2296578, A61K36/28, A61K125/00, A61P35/00 опубл. 10.04.2007 г.
2. Патент РФ 2441873, C07F15/02, A61K31/295, A61P35/00, опубл. 10.02.2012 г.
3. Патент РФ 2456001, A61K33/28, A61K31/198, C01G13/00, A61P35/00, A61P31/12, A61P37/02, A61P33/00, опубл. 20.07.2012 г.
4. Патент РФ 2630303, C07D209/56, A61K31/404, A61P35/00, опубл. 08.09.2017 г.
5. Патент РФ 2654711, A61K31/375, A61P43/00, опубл. 22.05.2018 г.
6. Машковский М. Д. Лекарственные средства. – 16-е изд. – М.: Новая волна, 2012. – 1216 с.
7. Патент РФ 2223771, A61K33/24, A61P3/10, опубл. 20.02.2004 г.
8. Результаты фазы клинических испытаний каталитической системы «терафтал + аскорбиновая кислота». / Л.В. Манзюк [и др.] // Российский биотерапевтический журнал. 2005. №1. Т.4. С. 105-107
9. Wenner W. The reaction of L-ascorbic and D-isoascorbic acid with nicotinic acid and its amide / W. Wenner // J. Org. Chem. – 1949. – V.14. – P. 22–25.
10. Kaplan, A., Akalin Ciftci, G., Kutlu, H.M. Cytotoxic, anti-proliferative and apoptotic effects of silver nitrate against H-ras transformed 5RP7. Cytotechnology 2016, Volume 68(5):1727-1735.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, обладающее апоптозиндуцирующей активностью | 2018 |
|
RU2702656C1 |
| РАДИОСЕНСИБИЛИЗИРУЮЩЕЕ СРЕДСТВО | 2019 |
|
RU2720455C1 |
| РАДИОПРОТЕКТОРНОЕ СРЕДСТВО | 2020 |
|
RU2737898C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИЛИТИЕВОЙ СОЛИ ФОСФО-АСКОРБИНОВОЙ КИСЛОТЫ | 2020 |
|
RU2752829C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦИТОСТАТИЧЕСКОЙ И АПОПТОЗИНДУЦИРУЮЩЕЙ АКТИВНОСТЬЮ | 2005 |
|
RU2296578C2 |
| ГЕЛЕОБРАЗНАЯ КОМПОЗИЦИЯ ШИРОКОГО СПЕКТРА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ | 2013 |
|
RU2535141C1 |
| АПОПТОЗИНДУЦИРУЮЩАЯ И АНТИОКСИДАНТНАЯ КОМПОЗИЦИЯ | 2017 |
|
RU2682644C2 |
| Способ получения наночастиц селена | 2024 |
|
RU2840703C1 |
| СЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2021 |
|
RU2771237C1 |
| Способ применения ресвератрола для ускорения регенерации поврежденных нервов | 2021 |
|
RU2778199C1 |
Изобретение относится к способу получения аддуктов пиколиновой либо никотиновой кислоты с аскорбиновой кислотой, характеризующийся тем, что к водному раствору аскорбиновой кислоты добавляют пиколиновую кислоту либо никотиновую кислоту (предварительно обработанную микроволновым излучением) в мольном соотношении 1:2 (C6H5NO2:С6Н8О6) при постоянном перемешивании при комнатной температуре, после непродолжительного перемешивания образуется осадок аддукта пиколиновой либо никотиновой кислоты с аскорбиновой кислотой, который после часовой кристаллизации фильтруют, а затем полученный осадок аддукта промывают небольшими порциями растворителя и сушат на воздухе. 3 н.п. ф-лы, 1 ил., 1 табл., 5 пр.
1. Способ получения аддуктов пиколиновой либо никотиновой кислоты с аскорбиновой кислотой, характеризующийся тем, что к водному раствору аскорбиновой кислоты добавляют пиколиновую кислоту либо никотиновую кислоту (предварительно обработанную микроволновым излучением) в мольном соотношении 1:2 (C6H5NO2:С6Н8О6) при постоянном перемешивании при комнатной температуре, после непродолжительного перемешивания образуется осадок аддукта пиколиновой либо никотиновой кислоты с аскорбиновой кислотой, который после часовой кристаллизации фильтруют, а затем полученный осадок аддукта промывают небольшими порциями растворителя и сушат на воздухе.
2. Апоптозиндуцирующее средство, полученное способом по п. 1, представляющее собой аддукт аскорбиновой кислоты с пиколиновой кислотой с общей формулой C6H5NO2 ⋅ С6Н8О6 - аддукт (1), проявляющий апоптозиндуцирующую активность.
3. Применение аддукта аскорбиновой кислоты с никотиновой кислотой - аддукта (2) с общей формулой C6H5NO2 ⋅ С6Н8O6, полученного способом по п. 1, в качестве апоптозиндуцирующего средства.
| Partha Pratim Bag et al | |||
| "A kinetically controlled crystallization process for identifying new co-crystal forms: fast evaporation of solvent from solutions to dryness", The Royal Society of Chemistry, 2011, Vol | |||
| Насос | 1917 |
|
SU13A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| ГОРИЗОНТАЛЬНЫЙ ВЕТРО-ВОДЯНОЙ ДВИГАТЕЛЬ | 1926 |
|
SU5650A1 |
| Saul H | |||
| Lapidus et al | |||
| "A Comparison of Cocrystal Structure Solutions from Powder and Single Crystal | |||
Авторы
Даты
2019-12-18—Публикация
2018-12-25—Подача