Данная заявка имеет приоритет предварительной заявки на патент США №61/139679, поданной 22 декабря 2008 г., и предварительной заявки на патент США №61/164486, поданной 30 марта 2009 г., полностью включенных сюда посредством ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
В целом, настоящее изобретение относится к способу лечения и/или профилактики остеоартрита (OA). Согласно настоящему изобретению антагонист гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) может быть эффективным в лечении остеоартрита. Антагонист GM-CSF включает, без ограничения, антитело, специфичное в отношении GM-CSF или рецептора GM-CSF. Согласно настоящему изобретению также предложены трансгенные животные, такие как мышь-нокаут по GM-CSF, полезные для исследования антагонистов в определенных моделях заболеваний.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Остеоартрит, также известный как дегенеративный артрит, является заболеванием, наиболее распространенным у пожилых и тучных людей. OA представляет собой заболевание суставов, но в отличие от ревматоидного артрита (РА) заболевание не является системным, обычно поражая только один сустав или несколько суставов. Заболевание приводит к полной деструкции суставного хряща, склерозу нижележащих костей и образованию остеофитов, приводя к утрате подвижности и боли. Конечным результатом часто является необходимость полной замены сустава.
OA поражает приблизительно 21 миллион человек в США, составляет 25% всех случаев первичного обращения за медицинской помощью, и им обусловлено 50% всех случаев назначения НПВС (нестероидных противовоспалительных лекарственных средств). В настоящее время нет доступного лечения, замедляющего или останавливающего прогрессирование заболевания; современные лекарственные средства обеспечивают лишь симптоматическое лечение. Частота и тяжесть заболевания увеличиваются с возрастом. К возрасту 65 лет 80% американцев демонстрируют рентгенографические признаки OA, хотя только у 60% из них есть симптомы. 65% всех заболеваний суставов к возрасту 65 лет обусловлены OA. В 2006 году в США было 735000 связанных с OA госпитализаций.
Современные лекарственные средства от OA обеспечивают лишь симптоматическое лечение, а не лечение заболевания самого по себе. Лекарственные средства, обычно используемые для лечения OA, включают нестероидные противовоспалительные лекарственные средства (НПВС), такие как диацерин, вольтарен, мобик и артротек (международные непатентованные названия: диклофенак, мизопростол, мелоксикам). НПВС представляют собой соединения главным образом для перорального приема, которые действуют, ингибируя синтез простагландинов в центральной нервной системе (ЦНС). Другие часто используемые лекарственные средства включают ненаркотические анальгетики, такие как ультрам (трамадол), ингибиторы циклооксигеназы-2 (ЦОГ-2), такие как целебрекс и аркоксия (целекоксиб, эторикоксиб), наркотические анальгетики, такие как дурагезик (декстропропоксифенфентанил), гиалуроновые кислоты, такие как супартс (suparts), гиалган, ортовиск и синвиск (Hylan G-F20), и кортикостероиды, такие как преднизолон и метилпреднизолон. Современные способы лечения OA направлены на устранение необходимости хирургического лечения посредством тканевой инженерии, такого как трансплантация хондроцитов; тем не менее, эти способы лечения применимы лишь для лечения последней стадии OA. Другие рассматриваемые способы лечения OA включают пролотерапию, при которой в пораженный сустав вводят раздражитель, такой как декстроза, вызывая посредством этого острую воспалительную реакцию, но также приводя к усилению и возможно излечению тканей, связок, сухожилий и хряща. Таким образом, существует значительная неудовлетворенная медицинская потребность в лечении OA.
Известно, что некоторые цитокины связаны с остеоартритом (Blom et al., Current Drug Targets (2008) 8:283). Несколько цитокинов, таких как интерлейкин-1 (IL-1), «деструктивный» цитокин, и анаболический фактор роста трансформирующий фактор роста-В (TGFB), рассматривают как потенциальные мишени для лекарственных средств.
Гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) представляет собой цитокин, функционирующий как фактор роста лейкоцитов. GM-CSF стимулирует образование гранулоцитов (нейтрофилов, эозинофилов и базофилов) и моноцитов из стволовых клеток. Моноциты покидают кровообращение и мигрируют в ткань, где происходит их созревание с образованием макрофагов. Таким образом, он является частью природного иммунного/воспалительного каскада, посредством которого активация небольшого числа макрофагов может быстро приводить к увеличению их числа, что является критически важным процессом для борьбы с инфекцией. Активная форма GM-CSF обнаружена внеклеточно в виде гомодимера. В частности, было установлено, что GM-CSF является медиатором воспаления при аутоиммунных расстройствах, таких как ревматоидный артрит (РА), приводя к повышенному образованию провоспалительных цитокинов, хемокинов и протеаз, и посредством этого в конечном счете к деструкции сустава.
В WO 06/0234412 раскрыто множество биомаркеров остеоартрита, которые были установлены посредством белковых микроматриц. Одним из установленных биомаркеров является GM-CSF, о четырехкратной позитивной регуляции которого в ткани сообщено при OA. Тем не менее, не представлено указания или предложения о том, что GM-CSF может также быть точкой терапевтического воздействия, и всего лишь четырехкратная позитивная регуляция в ткани при OA, как установлено способом, раскрытым в WO 06/0234412, также не предполагает этого. В родственном источнике, Devalaraja et al (US 20020141994 A1), вскользь упоминают OA в длинном перечне потенциально подходящих показаний, подходящих для лечения антагонистами колониестимулирующих факторов. Перечень показаний включает атеросклероз, сепсис, астму, аутоиммунное заболевание, остеопороз и ревматоидный артрит. Помимо других колониестимулирующих факторов, таких как макрофагальный колониестимулирующий фактор (M-CSF) и гранулоцитарный колониестимулирующий фактор (G-CSF), GM-CSF является одним из колониестимулирующих факторов, упомянутых в Devalaraja et al. На самом деле, в Devalaraja et al. нет данных или другого понимания в отношении того, почему антагонизм в отношении GM-CSF будет подходящим для лечения субъекта, страдающего от OA.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении впервые продемонстрировано, что GM-CSF является эффективной мишенью для лечения OA. Это обнаружение является новым, и в предшествующем уровне техники отсутствуют идеи, предположения или предложения о каком-либо обосновании такой точки вмешательства при лечении OA. Соответственно, согласно изобретению предложен, например, способ лечения остеоартрита у субъекта, включающий стадию введения эффективного количества антагониста GM-CSF указанному субъекту.
В другом аспекте согласно настоящему изобретению предполагают способ профилактики остеоартрита у субъекта, включающий стадию введения эффективного количества антагониста GM-CSF указанному субъекту.
В другом аспекте настоящее изобретение направлено на композицию, содержащую антагонист GM-CSF, способный антагонизировать способность GM-CSF приводить к активации, пролиферации, индукции роста и/или выживания клеток у субъекта, страдающего от остеоартрита или предположительно страдающего от остеоартрита, дополнительно содержащую один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В другом аспекте настоящее изобретение направлено на композицию, содержащую антагонист GM-CSF, полезный в лечении остеоартрита, дополнительно содержащую один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В определенных аспектах настоящего изобретения антагонист GM-CSF представляет собой антитело, специфичное в отношении GM-CSF.
В альтернативных аспектах настоящего изобретения антагонист GM-CSF представляет собой антитело, специфичное в отношении рецептора GM-CSF.
В других аспектах настоящее изобретение направлено на применение антагониста GM-CSF в изготовлении лекарственного средства для лечения остеоартрита.
В других аспектах согласно настоящему изобретению предложены антагонисты GM-CSF для лечения остеоартрита.
В данном описании, если контекст не требует иного, слова «содержать», «иметь» и «включать» и их соответствующие варианты, такие как «содержит», «содержащий», «имеет», «имеющий», «включает» и «включающий», следует понимать как подразумевающие включение указанного элемента, или целого, или группы элементов или целых, но не исключение любого другого элемента, или целого, или группы элементов или целых.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
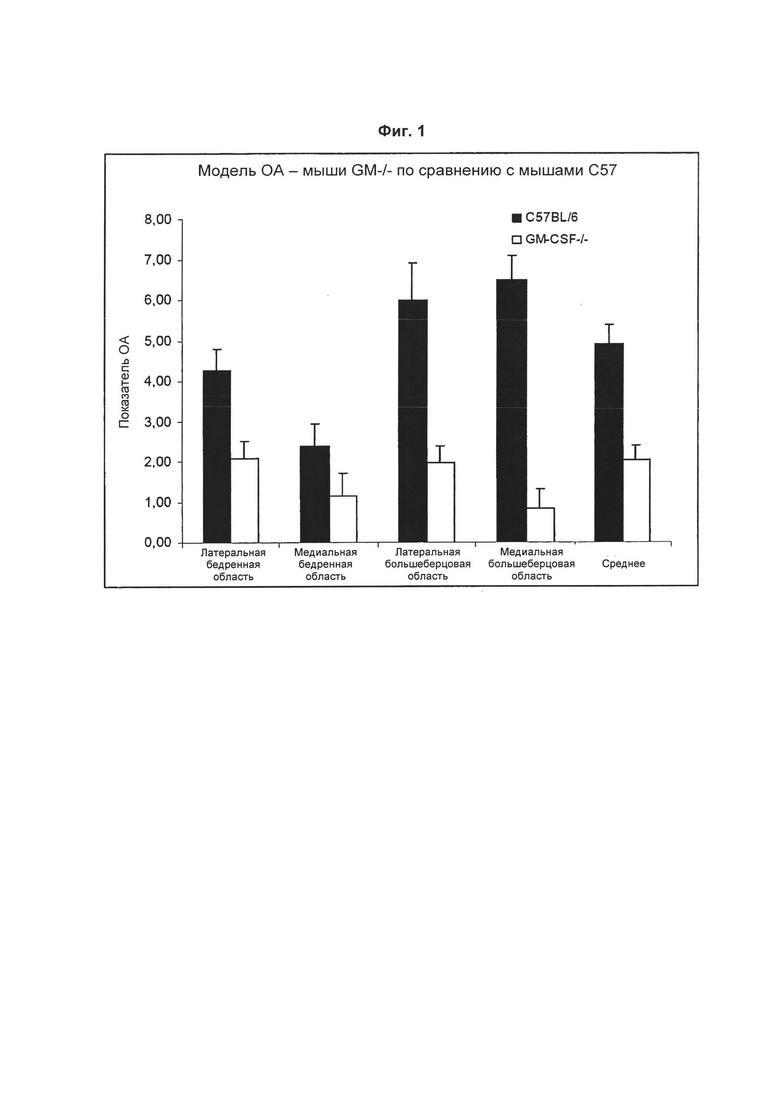
На Фиг. 1 показаны количественные данные о повреждении суставов в различных областях, оцениваемые по гистологическим показателям. Постановка эксперимента и система оценки описаны в Примере 2. «Lat.» означает латеральный. «Med.» означает медиальный. Статистический анализ проводили критерием Манна-Уитни. Данные статистически значимы для латеральной бедренной области (р=0,02), латеральной большеберцовой области (р=0,03), медиальной большеберцовой области (р=0,001) и всех областей вместе (среднее, р=0,002).
На Фиг. 2 показаны типичные гистологические срезы здоровых контрольных коленных суставов. Увеличение 100х. Нет видимого повреждения хряща, образования остеофитов, синовита или деформаций. S=синовиальная выстилка. С = хрящевой слой.
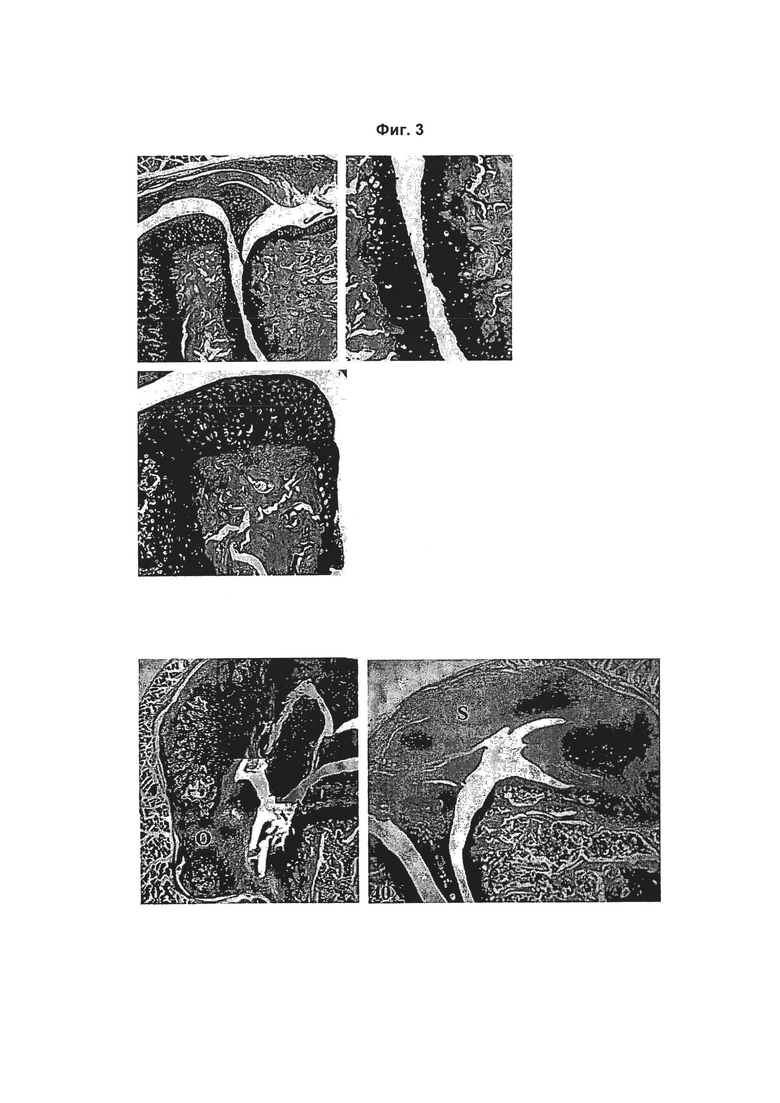
На Фиг. 3 показаны типичные гистологические срезы левых коленных суставов мышей C57/BL6 в модели коллаген-индуцированного OA. Увеличение отдельных срезов указано в графических материалах. В верхнем ряду изображений показано, что повреждение хряща, образование остеофитов и синовит очевидны. О = остеофит. S = синовиальная выстилка. В нижнем ряду изображений показано, что также присутствует деформация суставов.
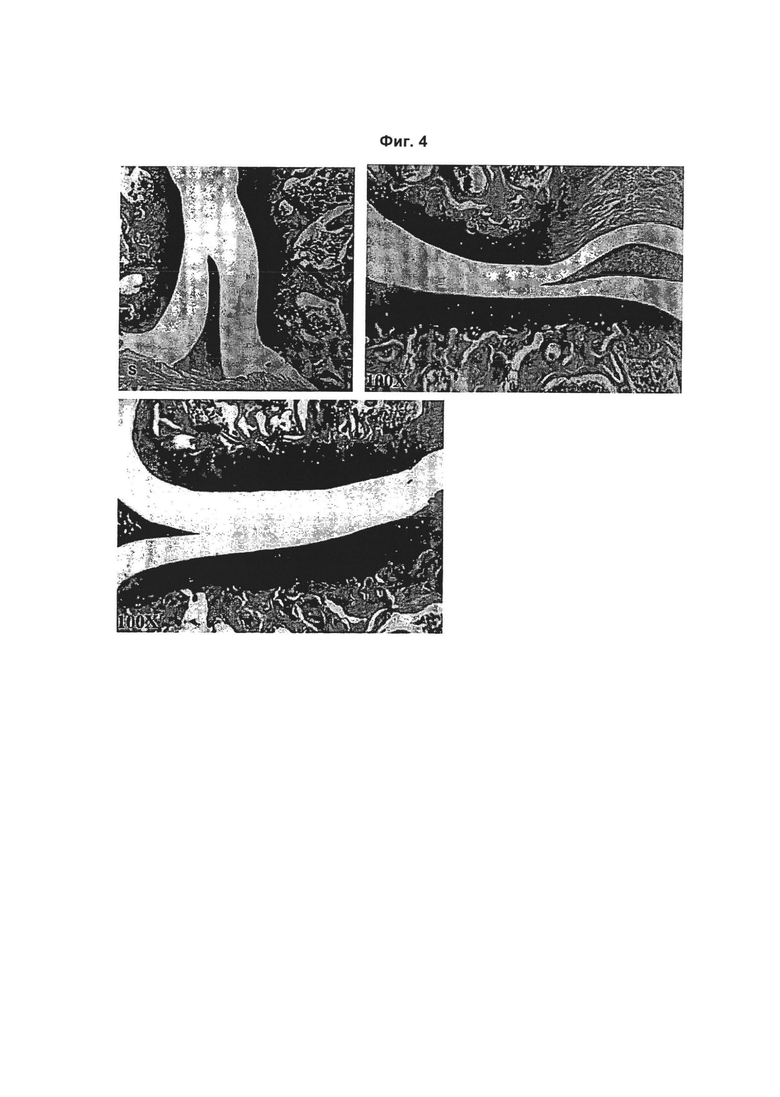
На Фиг. 4 показаны типичные гистологические срезы левых коленных суставов мышей GM-CSF-/- в модели коллаген-индуцированного OA. Увеличение отдельных срезов указано в графических материалах. Как можно видеть, тяжесть отклонений и/или повреждений значительно меньше по сравнению с мышами C57/BL6 (см. Фиг. 3), и они сопоставимы со здоровыми контрольными мышами (см. Фиг. 2). О = остеофит. S = синовиальная выстилка.
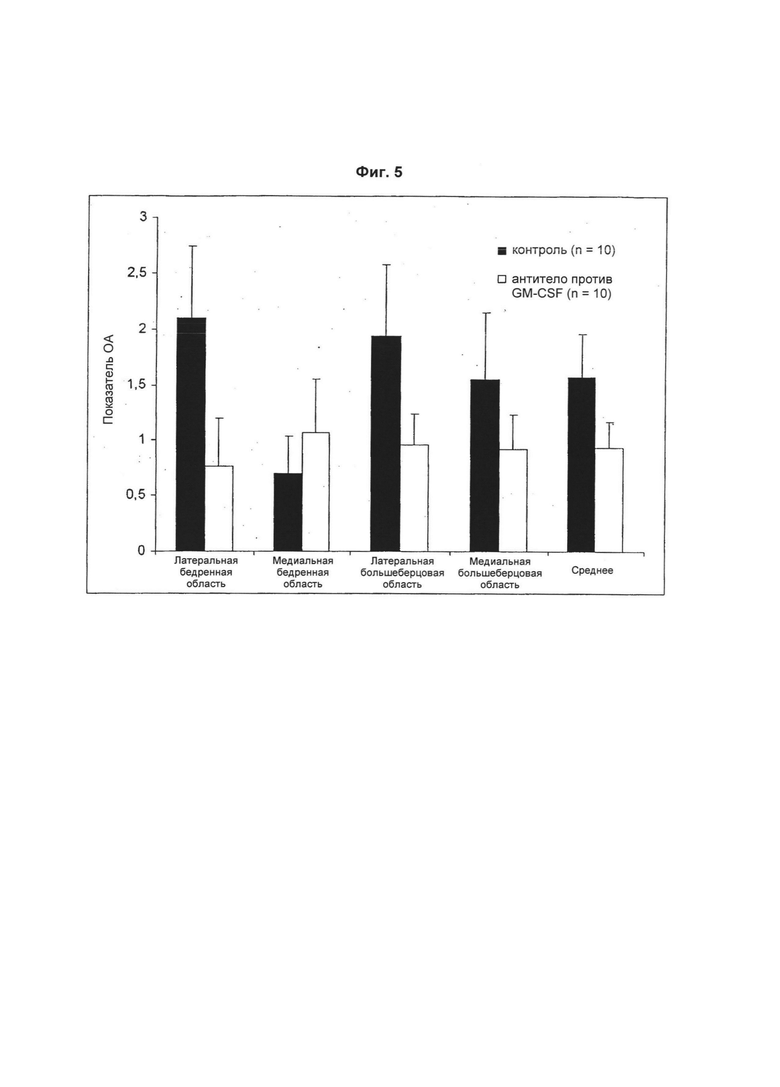
На Фиг. 5 показаны гистологические показатели коленных суставов при терапевтическом лечении антителом против GM-CSF в модели OA на мышах. Lat. = латеральный. Med. = медиальный. Результаты представлены как среднее ± стандартная ошибка среднего (SEM). Как можно видеть, мыши, получавшие лечение антителом против GM-CSF, демонстрируют менее тяжелое заболевание.
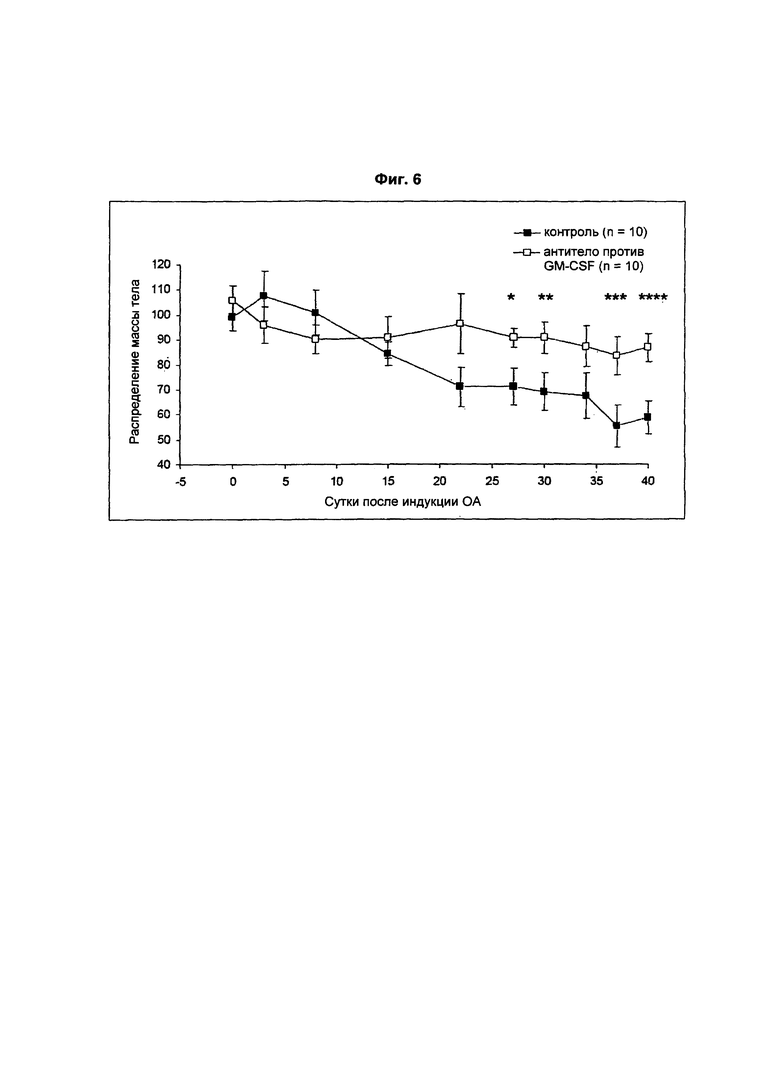
На Фиг. 6 показан результат эксперимента по оценке распределения массы тела по задним конечностям с использованием устройства для измерения нарушения функции. Данные значимы (непарный критерий Стьюдента), начиная с 27 суток после индукции OA, как показано на графике. Результаты представлены как среднее ± SEM. * р=0,04, ** р=0,04, *** р=0,02, **** р=0,005, непарный критерий Стьюдента.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении продемонстрировано, что GM-CSF является эффективной мишенью для лечения OA. В этом отношении в одном аспекте согласно изобретению предложены способы применения антагониста GM-CSF для обеспечения профилактической или терапевтической пользы в области OA.
Согласно настоящему изобретению предложены терапевтические способы, включающие введение терапевтически эффективного количества антагониста GM-CSF субъекту, нуждающемуся в таком лечении. «Терапевтически эффективное количество» или «эффективное количество» при использовании здесь относится к количеству антагониста GM-CSF, необходимому для обеспечения желаемого биологического ответа. Согласно данному изобретению терапевтически эффективное количество представляет собой количество антагониста GM-CSF, необходимое для лечения и/или предотвращения остеоартрита.
«Антагонисты GM-CSF» при использовании здесь включают антагонисты GM-CSF в наиболее широком смысле; включена любая молекула, ингибирующая активность или функцию GM-CSF или любым другим образом оказывающая терапевтический эффект на GM-CSF. Термин «антагонисты GM-CSF» включает, без ограничения, антитела, специфично связывающиеся с GM-CSF, ингибирующие нуклеиновые кислоты, специфичные в отношении GM-CSF, или малые органические молекулы, специфичные в отношении GM-CSF. Значение термина «антагонист GM-CSF» также включает антитела, специфично связывающиеся с рецептором GM-CSF, ингибирующие нуклеиновые кислоты, специфичные в отношении рецептора GM-CSF, или малые органические молекулы, специфичные в отношении рецептора GM-CSF.
Ингибирующие нуклеиновые кислоты включают, без ограничения, антисмысловую ДНК, триплекс-образующие олигонуклеотиды, внешние вспомогательные последовательности, малую интерферирующую РНК (миРНК) и микроРНК. Полезные ингибирующие нуклеиновые кислоты включают ингибирующие нуклеиновые кислоты, уменьшающие экспрессию РНК, кодирующей GM-CSF по меньшей мере на 20, 30, 40, 50, 60, 70, 80, 90 или 95 процентов по сравнению с контролями. Ингибирующие нуклеиновые кислоты и способы их получения хорошо известны в данной области техники. Доступно программное обеспечение для разработки миРНК.
Малые органические молекулы (SMOL), специфичные в отношении GM-CSF или рецептора GM-CSF, могут быть идентифицированы скринингом природных продуктов или скринингом химических библиотек. Типично молекулярная масса SMOL составляет менее 500 дальтон, более типично от 160 до 480 дальтон. Другими типичными свойствами SMOL являются одно или более из следующего:
- коэффициент распределения log Р в диапазоне от -0,4 до+5,6;
- молярная преломляющая способность от 40 до 130;
- число атомов от 20 до 70.
См. обзоры в Ghose et al, J Combin. Chem: 7:55-68, 1999 и Lipinski et al, Adv Drug Del Rev: 23:3-25, 1997.
Предпочтительно антагонист GM-CSF для использования в настоящем изобретении представляет собой антитело, специфичное в отношении GM-CSF или специфичное в отношении рецептора GM-CSF. Такое антитело может представлять собой антитело любого типа, такое как мышиное, крысиное, химерное, гуманизированное или человеческое антитело. «Человеческое» антитело или функциональный фрагмент человеческого антитела определено таким образом как антитело или функциональный фрагмент антитела, не являющиеся химерными (например, не являющиеся «гуманизированными») и не имеющие происхождение (либо полностью, либо частично) от вида, не являющегося человеком. Человеческое антитело или функциональный фрагмент антитела могут иметь происхождение от человека или могут представлять собой синтетическое человеческое антитело. «Синтетическое человеческое антитело» определено таким образом как антитело, имеющее последовательность, имеющую происхождение, полностью или частично, in silico от синтетических последовательностей, основанных на анализе известных последовательностей человеческих антител. Разработка последовательности человеческого антитела или его фрагмента in silico может быть осуществлена, например, анализом базы данных последовательностей человеческих антител или фрагментов антител и разработкой полипептидной последовательности с использованием полученных таким образом данных. Другим примером человеческого антитела или функционального фрагмента антитела являются антитело или функциональный фрагмент антитела, кодируемые нуклеиновой кислотой, выделенной из библиотеки последовательностей антител человеческого происхождения (то есть, библиотеки, основанной на антителах, полученных от природного источника, являющегося человеком).
«Гуманизированное антитело» или функциональный фрагмент гуманизированного антитела определено таким образом как (1) антитело или функциональный фрагмент антитела, имеющие происхождение от источника, не являющегося человеком (например, трансгенной мыши с гетерологичной иммунной системой), основанные на человеческой последовательности зародышевого типа; или (2) химерные антитело или функциональный фрагмент антитела, где вариабельный домен имеет происхождение от источника, не являющегося человеком, и константный домен имеет происхождение от источника, являющегося человеком, или (3) антитело или функциональный фрагмент антитела с перенесенными гипервариабельными участками (CDR), где CDR вариабельного домена имеют происхождение от источника, не являющегося человеком, в то время как одна или более чем одна каркасная область вариабельного домена имеет происхождение от источника, являющегося человеком, и константный домен (если он присутствует) имеет происхождение от источника, являющегося человеком.
Термин «химерное антитело» или функциональный фрагмент химерного антитела определены таким образом как молекула-антитело, имеющая константные области антитела, имеющие происхождение от последовательностей, обнаруженных у одного вида, или соответствующие последовательностям, обнаруженным у одного вида, и вариабельные области антитела, имеющие происхождение от другого вида. Предпочтительно константные области антитела имеют происхождение от последовательностей, обнаруженных у людей, например, в человеческой зародышевой линии или соматических клетках, или соответствуют этим последовательностям, и вариабельные области антитела (например, вариабельные области тяжелой цепи (VH), вариабельные области легкой цепи (VL), CDR или каркасные области (FR)) имеют происхождение от последовательностей, обнаруженных у животного, не являющегося человеком, например мыши, крысы, кролика или хомяка.
При использовании здесь антитело «связывается специфично с», «специфично связывается с», «специфично в отношении» или «специфично распознает» антиген (здесь, GM-CSF или альтернативно рецептор GM-CSF), если такое антитело способно различать такой антиген и один или более чем один контрольный антиген, поскольку специфичность связывания является не абсолютным, а относительным свойством. Контрольный антиген (антигены) может представлять собой один или более чем один близкородственный антиген (антигены), используемый в качестве контрольной точки, например, интерлейкин-3 (IL-3), интерлейкин-5 (IL-5), интерлейкин-4 (IL-4), интерлейкин-13 (IL-13) или макрофагальный колониестимулирующий фактор (M-CSF). В наиболее общей форме (и без упоминания определенной ссылки) «специфичное связывание» относится к способности антитела различать интересующий антиген и неродственный антиген, как определено, например, в соответствии с одним из следующих способов. Такие способы включают, без ограничения, вестерн-блоттинг, твердофазный иммуноферментный анализ (ELISA), радиоиммуноанализ (RIA), электрохемилюминесцентый анализ (ECL), иммунорадиометрический анализ (IRMA) и пептидные сканирования. Например, может быть проведен стандартный ELISA-анализ. Оценку можно проводить стандартным цветовым проявлением (например, вторичным антителом с пероксидазой хрена и тетраметилбензидином с перекисью водорода). Реакцию в определенных лунках оценивают по оптической плотности, например, при 450 нм. Обычный фон (= отрицательная реакция) может составлять 0,1 оптической плотности (OD), типичная положительная реакция может составлять 1 OD. Это означает, что разница положительный/отрицательный может составлять более 10 раз. Обычно определение специфичности связывания проводят с использованием не одного контрольного антигена, а набора из приблизительно трех-пяти неродственных антигенов, таких как сухое молоко, бычий сывороточный альбумин (BSA), трансферрин или тому подобное. В дополнение, «специфичное связывание» может относиться к способности антитела различать разные части его антигена-мишени, например, разные домены или области GM-CSF или рецептора GM-CSF, или один или более чем один ключевой аминокислотный остаток или группу аминокислотных остатков GM-CSF или рецептора GM-CSF.
Также при использовании здесь «иммуноглобулин» (lg) определен таким образом как белок, принадлежащий к классу IgG, IgM, IgE, IgA или IgD (или любому их подклассу), и данный термин включает все общеизвестные антитела и их функциональные фрагменты. «Функциональный фрагмент» антитела/иммуноглобулина определен таким образом как фрагмент антитела/иммуноглобулина (например, вариабельная область IgG), сохраняющий антиген-связывающую область. «Антиген-связывающую область» антитела обычно обнаруживают в одном или более чем одном гипервариабельном участке антитела, то есть, CDR1, CDR2 или CDR3; тем не менее, вариабельные «каркасные» области также могут играть важную роль в связывании с антигеном, как например, предоставляя каркас для CDR. Предпочтительно «антиген-связывающая область» включает по меньшей мере аминокислотные остатки 4-103 вариабельной области легкой цепи (VL) и 5-109 вариабельной области тяжелой цепи (VH), более предпочтительно аминокислотные остатки 3-107 VL и 4-111 VH, и особенно предпочтительны полноразмерные цепи VL и VH (аминокислотные положения 1-109 VL и 1-113 VH; нумерация согласно WO 97/08320). Предпочтительным классом иммуноглобулинов для использования в настоящем изобретении являются IgG. «Функциональные фрагменты» по изобретению включают домен F(ab')2-фрагмента, Fab-фрагмента, scFv или конструкции, содержащие полипептиды отдельных вариабельных доменов иммуноглобулинов или отдельных однодоменных антител, например, отдельных вариабельных доменов тяжелой цепи или отдельных вариабельных доменов легкой цепи. F(ab')2 или Fab могут быть сконструированы для минимизации или полного устранения межмолекулярных дисульфидных взаимодействий, происходящих между доменами СН1 и CL.
Антитело по изобретению может иметь происхождение от библиотеки рекомбинантных антител, основанной на аминокислотных последовательностях, разработанных in silico и кодируемых синтетически полученными нуклеиновыми кислотами. Разработка последовательности антитела in silico проводят, например, анализом базы данных человеческих последовательностей и разработкой полипептидной последовательности с использованием полученных таким образом данных. Способы разработки и получения in silico - получаемых последовательностей описаны, например, в Knappik et al, J. Mol. Biol. 296:57, 2000; Krebs et al, J. Immunol. Methods. 254:67, 2001, Rothe et al, J. Mol. Biol. 376:1182, 2008, и патенте США №6300064, выданном Knappik et al 2000 supra, полностью включенных сюда посредством ссылки.
В настоящем изобретении может быть использовано любое антитело, специфичное в отношении GM-CSF. Типичные антитела раскрыты в US 11/914599, полностью включенной сюда посредством ссылки. Другие типичные антитела включают антитела, содержащие аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 1, или аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 2. Другие типичные антитела включают антитела, имеющие происхождение от антител, содержащих вариабельную область тяжелой цепи, как показано в SEQ ID NO: 1, или аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 2. Другие типичные антитела включают антитела, имеющие такую же специфичность и/или связывающиеся с тем же эпитопом, что и антитела, содержащие вариабельную область тяжелой цепи, как показано в SEQ ID NO: 1, или аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 2. Другие типичные антитела включают антитела, содержащие вариабельную область тяжелой цепи, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичную последовательности, показанной в SEQ ID NO: 1. Другие типичные антитела включают антитела, содержащие вариабельную область легкой цепи, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичную последовательности, показанной в SEQ ID NO: 2.


Альтернативные типичные антитела, которые могут быть использованы в настоящем изобретении, представляют собой антитела, содержащие аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 3, или аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 4. Другие типичные антитела включают антитела, имеющие происхождение от антител, содержащих вариабельную область тяжелой цепи, как показано в SEQ ID NO: 3, или аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 4. Другие типичные антитела включают антитела, имеющие такую же специфичность и/или связывающиеся с тем же эпитопом, что и антитела, содержащие вариабельную область тяжелой цепи, как показано в SEQ ID NO: 3, или аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 4. Другие типичные антитела включают антитела, содержащие вариабельную область тяжелой цепи, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичную последовательности, показанной в SEQ ID NO: 3. Другие типичные антитела включают антитела, содержащие вариабельную область легкой цепи, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичную последовательности, показанной в SEQ ID NO: 4.

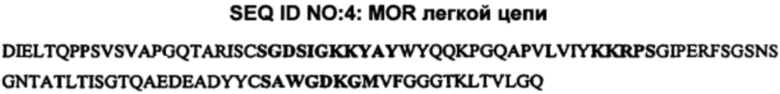
Альтернативные типичные антитела, которые могут быть использованы в настоящем изобретении, представляют собой антитела, содержащие последовательность CDR3 тяжелой цепи (H-CDR3), выбранную из:
 .
.
Предпочтительно антитела, содержащие последовательность H-CDR3, выбранную из любой из SEQ ID NO: 5-16, дополнительно содержат следующую последовательность CDR1 тяжелой цепи (H-CDR1):

и/или следующую последовательность CDR2 тяжелой цепи (H-CDR2):

и/или следующую последовательность CDR1 легкой цепи (L-CDR1):

и/или следующую последовательность CDR2 легкой цепи (L-CDR2):

и/или следующую последовательность CDR3 легкой цепи (L-CDR3):

Альтернативные типичные антитела, которые могут быть использованы в настоящем изобретении, представляют собой антитела, содержащие следующую последовательность L-CDR1:

и/или следующую последовательность L-CDR2:
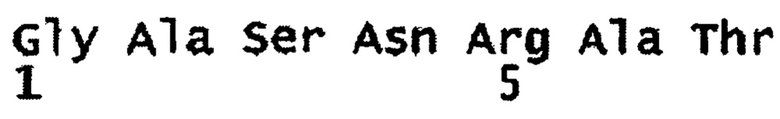

и/или следующую последовательность L-CDR3:

и/или следующую последовательность H-CDR1:

и/или следующую последовательность H-CDR2:

и/или следующую последовательность H-CDR3:

Предпочтительно указанное антитело содержит все CDR с SEQ ID NO: 22-27.
Рецептор GM-CSF является членом суперсемейства гемопоэтиновых рецепторов. Он является гетеродимерным и состоит из альфа- и бета-субъединицы. Альфа-субъединица высокоспецифична в отношении GM-CSF, в то время как бета-субъединица является общей с рецепторами других цитокинов, включая IL-3 и IL-5. Это отражено в более широком тканевом распределении бета-субъединицы рецептора. Альфа-субъединица, GM-CSFRα, экспрессирована главным образом на миелоидных клетках и негемопоэтических клетках, таких как нейтрофилы, макрофаги, эозинофилы, дендритные клетки, эндотелиальные клетки и клетки респираторного эпителия. Полноразмерная GM-CSFRα представляет собой мембранный гликопротеин I типа из 400 аминокислот, который принадлежит к семейству рецепторов цитокинов I типа и состоит из сигнального пептида из 22 аминокислот (положения 1-22), внеклеточного домена из 298 аминокислот (положения 23-320), трансмембранного домена с положения 321 до положения 345 и короткого внутриклеточного домена из 55 аминокислот.Происходит отщепление сигнального пептида с образованием зрелой формы GM-CSFRα в виде белка из 378 аминокислот. Доступны клоны комплементарной ДНК (кДНК-клоны) человеческой и мышиной GM-CSFRα, и идентичность субъединиц рецептора на уровне белков составляет 36%. GM-CSF способен связываться с относительно низкой аффинностью с α-субъединицей самой по себе (Kd 1-5 нМ), но не способен связываться с В-субъединицей самой по себе. Тем не менее, присутствие обеих α- и β-субъединиц приводит к образованию высокоаффинного комплекса лиганд-рецептор (Kd » 100 пМ). GM-CSF-сигнализация происходит через его начальное связывание с α-цепью GM-CSFR и затем перекрестное связывание с более крупной субъединицей общей β-цепи с установлением высокоаффинного взаимодействия, приводящего к фосфорилированию через метаболический путь JAK-STAT.
В настоящем изобретении может быть использовано любое антитело, специфичное в отношении рецептора GM-CSF. Типичные антитела включают антитела, содержащие аминокислотную последовательность последовательности H-CDR3, показанной в любой из SEQ ID NO: 28-46. Другие типичные антитела включают антитела, имеющие происхождение от антител, содержащих аминокислотную последовательность последовательности Н-CDR3, показанной в любой из SEQ ID NO: 28-46. Другие типичные антитела включают антитела, имеющие такую же специфичность и/или связывающиеся с тем же эпитопом, что и антитела, содержащие аминокислотную последовательность последовательности H-CDR3, показанной в любой из SEQ ID NO: 28-46. Другие типичные антитела включают антитела, содержащие последовательность H-CDR3, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% гомологичную последовательности H-CDR3, показанной в любой из SEQ ID NO: 28-46.



В определенных аспектах согласно настоящему изобретению предложены способы лечения остеоартрита у субъекта, включающие стадию введения антагониста GM-CSF указанному субъекту. «Субъект» при использовании в данном контексте относится к любому млекопитающему, включая грызунов, таких как мышь или крыса, и приматов, таких как яванский макак (Масаса fascicularis), макак-резус (Масаса mulatta) или люди (Homo sapiens). Предпочтительно субъект представляет собой примата, наиболее предпочтительно человека.
В определенном аспекте согласно настоящему изобретению предложена композиция, содержащая антагонист GM-CSF, способный антагонизировать способность GM-CSF приводить к активации, пролиферации, индукции роста и/или выживания клеток у субъекта, страдающего от остеоартрита или предположительно страдающего от остеоартрита, дополнительно содержащая один или более чем один фармацевтически приемлемый носитель и/или разбавитель. Антитела против GM-CSF по настоящему изобретению могут антагонизировать любую из функций GM-CSF при остеоартрите.
В другом аспекте согласно настоящему изобретению предложен способ профилактики остеоартрита у субъекта, включающий введение антагониста GM-CSF указанному субъекту. «Профилактика» при использовании в данном контексте относится к способам, направленным на предотвращение начала заболевания или приводящим к задержке начала заболевания.
В определенных аспектах согласно настоящему изобретению предложена композиция, содержащая антагонист GM-CSF, полезный в лечении остеоартрита, дополнительно содержащая один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
В других аспектах согласно настоящему изобретению предложено применение антагониста GM-CSF в изготовлении лекарственного средства для лечения остеоартрита.
В других аспектах согласно настоящему изобретению предложены антагонисты GM-CSF для лечения остеоартрита.
Композиции по настоящему изобретению предпочтительно представляют собой фармацевтические композиции, содержащие антагонист GM-CSF и фармацевтически приемлемый носитель, разбавитель или эксципиент, для лечения остеоартрита. Такие носители, разбавители и эксципиенты хорошо известны в данной области техники, и специалист в данной области техники найдет композицию и путь введения, наиболее подходящие для лечения субъекта антагонистами GM-CSF по настоящему изобретению.
В другом аспекте согласно настоящему изобретению предложено сконструированное с помощью генной инженерии млекопитающее, имеющее генотип GM-CSF -/-. В определенных аспектах указанное млекопитающее представляет собой мышь. Термины «мышь-нокаут» (или «млекопитающее- нокаут»), мышь (или млекопитающее) «с нарушением в» определенном гене и мышь (или млекопитающее) с «генотипом -/-» использованы в настоящем изобретении взаимозаменяемо и признаны в данной области техники. Соответствующие животные дефектны по соответствующему гену, здесь GM-CSF, в обоих аллелях хромосомы.
Пример 1:
Получение мыши GM-CSF-/-
Получение мышей GM-CSF-/- описано в Stanley et al (1994). Proc. Natl. Acad. Sci. USA 91:5592. Кратко, химерных мышей получали микроинъекцией клеток ES, имеющих происхождение от 129/OLA (Н-2b), с нарушением в гене GM-CSF в бластоцисты хозяина C57B L/6 (Н-2b). Переносчиков зародышевой линии с мутированным аллелем GM-CSF скрещивали с мышами C57BL/6 в 11 поколениях с получением мышей GM-CSF+/-, которых скрещивали между собой с получением мышей GM-CSF-/-, GM-CSF+/- и GM-CSF+/+, используемых для экспериментов. Состояние генотипа GM-CSF определяли анализом полимеразной цепной реакцией (ПЦР) хвостовой ДНК. Животных кормили стандартным кормом для грызунов и водой в свободном доступе и содержали с однопометными животными того же пола в клетках, выстланных опилками. Мышей обоих полов включали в эксперименты в возрасте от 8 до 15 недель.
Пример 2:
Подтверждение GM-CSF в качестве мишени при остеоартрите
Мышей GM-CSF-/- сравнивали с мышами C57/BL6 (см., например, Mills et al, J Immunol 764:6166-6173, 2000) в экспериментальной модели остеоартрита.
Метод. Мышам (п=10 на группу) проводили внутрисуставное введение коллагеназы в левый коленный сустав на -2 и 0 сутки (см. Blom et al. Arthritis Rheum 56:147-157, 2007). Ha 42 сутки мышей умерщвляли, коленные суставы собирали, фиксировали, декальцинировали, заключали в парафин и проводили приготовление срезов толщиной 7 мкм на микротоме. Микропрепараты затем окрашивали сафранином-О/быстрым зеленым и гематоксилином/эозином для демонстрации патологии суставов. Исследованная патология включает: повреждение хряща, синовит, образование остеофитов и деформацию суставов.
Система оценки, использованная для патологии хряща, представляла собой следующее. Степень
0 Норма
1 Неровный, но интактный
1,5 Неровный с шероховатой поверхностью
2 Поверхностное разволокнение
2,5 Поверхностное разволокнение с уменьшенным содержанием клеток в хрящевом слое
3 Вертикальные трещины
3,5 Разветвленные и/или горизонтальные трещины, краевые разрывы
4 Утрата хряща, не распространяющаяся до края
4,5 Утрата хряща, распространяющаяся до края
5 Утрата хряща, выходящая за край, но не распространяющаяся на кость
5,5 Утрата хряща, распространяющаяся на кость
6 Утрата/ремоделирование/деформация кости Стадия
1 Повреждение менее 10% площади
2 Повреждение 10-25% площади
3 Повреждение 25-50% площади
4 Повреждение 50-75% площади
Для получения показателя степень умножали на стадию.
Эта система оценки основана на признанном способе оценки гистопатологии OA при клиническом и экспериментальном OA. См. Pritzker et al. Osteoarthritis Cartilage 14:13-29, 2006. Степень определяют как глубину прогрессирования OA в хрящ. Стадию определяют как горизонтальную степень поражения хряща, то есть, насколько поражен хрящ. Степень умножают на стадию с получением показателя для получения общего показателя, чтобы представить комбинированную оценку тяжести и степени OA. Оценивают до шести срезов на мышь.
Результаты. Исследование этих суставов показало, что мыши GM-CSF-/-демонстрируют менее выраженную патологию коленных суставов, чем контрольные мыши, указывая на роль GM-CSF в обычной патологии и прогрессировании остеоартрита. Патология, наблюдаемая у мышей C57/BL6, включает тяжелое повреждение хрящевого слоя, образование остеофитов, деформацию суставов и синовит. Мыши GM-CSF-/- продемонстрировали отсутствие образования остеофитов или деформации суставов и значительно менее выраженное повреждение хряща и синовит.
Количественные данные о повреждении суставов в различных областях показаны на Фиг. 1. Типичная гистология показана на Фиг. 2 (здоровые контрольные коленные суставы), 3 (левые коленные суставы мышей C57/BL6) и 4 (левые коленные суставы мышей GM-CSF-/-). У мышей с недостаточностью гена GM-CSF при коллаген-индуцированном OA развивается менее выраженная патология по сравнению с мышами C57BL/6.
В завершение, мыши GM-CSF-/- продемонстрировали значительно менее выраженную патологию коленных суставов по сравнению с мышами C57/BL6 в экспериментальной модели остеоартрита, подтверждая, что GM-CSF является мишенью для лекарственных средств для терапевтического воздействия при остеоартрите.
Пример 3:
Терапевтическая эффективность антагонистов GM-CSF в лечении OA
В данном эксперименте авторы изобретения использовали моноклональное антитело, специфичное в отношении GM-CSF, для демонстрации того, что антагонист GM-CSF может быть эффективен для лечения остеоартрита.
Модель коллаген-индуцированного OA на мышах
Мышам C57BL/6 проводили внутрисуставное введение 1 единицы коллагеназы VII типа в правый коленный сустав на 0 и 2 сутки для индукции нестабильности сустава (см. Blom et al. (2004) Osteoarthritis Cartilage. 12; 627-35).
Лечение антителом против GM-CSF
20 мышей случайным образом разделяли на 2 группы (10 мышей на группу).
Группа 1 (n=10): антитело против GM-CSF (22Е9).
Группа 2 (n=10): контрольное антитело изотипа IgG2a.
Мышам проводили внутрибрюшинные введения три раза в неделю на протяжении 6 недель в дозе 250 мкг/мышь/введение антитела против GM-CSF (22Е9) или контрольного антитела изотипа IgG2a. Лечение начинали за 4 суток до индукции OA (профилактическое), то есть мышам проводили введения на -4 сутки, -2 сутки, 0 сутки (сутки первой инъекции коллагеназы), затем 3 раза в неделю до окончания эксперимента через 6 недель. На 2, 4 и 6 неделях у мышей проводили забор крови. Сыворотку проверяют в отношении содержания антитела и иммуногенности в отношении 22Е9. Проводили очистку как контрольного антитела, так и антитела против GM-CSF, чтобы они содержали менее 10 эндотоксиновых единиц на мл.
Антитело 22Е9 использовали в качестве типичного антитела против GM-CSF. 22Е9, изотипа IgG2a, представляет собой крысиное противомышиное антитело, специфичное в отношении GM-CSF. 22Е9 получали от AbD Serotec (Martinsried, Germany; номер по каталогу 1023501). Существуют альтернативные поставщики, например eBioscience (SanDiego, СА, USA, номер по каталогу 14-7331).
Гистологическое исследование
Через 6 недель после последних инъекций проводили гистологическое исследование коленных суставов мышей. Коленные суставы собирали, фиксировали, декальцинировали, заключали в парафин и проводили приготовление срезов толщиной 7 мкм на микротоме. Микропрепараты окрашивали сафранином-О/быстрым зеленым и гематоксилином/эозином для демонстрации патологии суставов. Исследованная патология включала повреждение хряща, синовит, образование остеофитов и деформацию суставов.
Для оценки патологии хряща использовали такую же систему оценки, как в Примере 2. Для получения показателя степень умножали на стадию.
Следующую систему оценки использовали для синовита (система оценки синовиального слоя).
0 Отсутствие изменений по сравнению с нормальными суставами
1 Утолщение синовиальной выстилки и некоторый приток воспалительных клеток
2 Утолщение синовиальной выстилки и умеренный приток воспалительных клеток
3 Сильное утолщение синовиальной выстилки и максимальный наблюдаемый приток воспалительных клеток
Измерения боли
Индикатором боли, используемым в моделях OA, является дифференциальное распределение массы тела, измеряемое с использованием устройства для измерения нарушения функции. Это устройство измеряет изменения в распределении массы тела между оперированной и противоположной неоперированной задней конечностью. Мышам дают привыкнуть к оборудованию три раза перед экспериментом. Массу тела, распределенную на каждую заднюю конечность, измеряли на протяжении пятисекундного периода. Затем усредняли три независимых измерения, проведенных у каждой мыши для каждой временной точки. Измерения проводили 2 раза в неделю на всем протяжении эксперимента. Результаты представлены как конечность с инъекцией коллагеназы/контрольная конечность ×100.
Результаты
Для всех проанализированных при гистологическом исследовании областей (за исключением медиальной бедренной), то есть латеральной бедренной, латеральной большеберцовой и медиальной большеберцовой, у мышей, получавших лечение антителом против GM-CSF, была отчетливая тенденция к менее выраженному заболеванию. Результаты показаны на Фиг. 5.
Оценка распределения массы тела в качестве критерия боли, связанной с артритом, продемонстрировала значительное смещение массы тела от колена с артритом, начиная с 27 суток в группе, получавшей лечение моноклональным антителом (mAb) против GM-CSF, по сравнению с группой, получавшей лечение контрольным mAb. Результаты показаны на Фиг. 6.
Мыши, получавшие лечение антагонистом GM-CSF, продемонстрировали менее выраженное заболевание по сравнению с мышами, получавшими лечение контрольным антителом. Мыши, получавшие лечение антагонистом GM-CSF, также продемонстрировали значительно менее выраженную боль на поздних стадиях заболевания по сравнению с мышами, получавшими лечение контрольным антителом. Мыши, получавшие лечение антителом контроля изотипа, продемонстрировали значительно более выраженные признаки остеоартрита по сравнению с мышами, получавшими антитело, специфичное в отношении GM-CSF. Это демонстрирует, что антагонисты GM-CSF эффективны в лечении OA.
Пример 4:
Терапевтическая эффективность антитела, специфичного в отношении GM-CSF, содержащего SEQ ID NO: 1 или 2
Повторяют Пример 3, где в качестве антагониста GM-CSF используют антитело, специфичное в отношении GM-CSF, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 1, или содержащее аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO:2. Может быть использован другой вид, не являющийся мышью, в частности, вид, в отношении которого антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно, видом животного, используемым в данном эксперименте, является крыса.
Животные, получавшие лечение контрольным антителом того же изотипа, демонстрируют значительно более выраженные признаки остеоартрита по сравнению с животными, получавшими антитело, специфичное в отношении GM-CSF, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 1, или содержащее аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO:2. Это демонстрирует эффективность антител в лечении OA.
Пример 5:
Терапевтическая эффективность антитела, специфичного в отношении GM-CSF, содержащего SEQ ID NO: 3 или 4
Повторяют Пример 3. В качестве антагониста GM-CSF используют антитело, специфичное в отношении GM-CSF, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 3, или содержащее аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 4. Может быть использован другой вид, не являющийся мышью, в частности, вид, в отношении которого антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно, видом животного, используемым в данном эксперименте, является крыса.
Животные, например крысы, получавшие лечение контрольным антителом того же изотипа, демонстрируют значительно более выраженные признаки остеоартрита по сравнению с животными, получавшими антитело, специфичное в отношении GM-CSF, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, как показано в SEQ ID NO: 3, или содержащее аминокислотную последовательность вариабельной области легкой цепи, как показано в SEQ ID NO: 4. Это демонстрирует эффективность антител в лечении OA.
Пример 6:
Терапевтическая эффективность антител, специфичных в отношении
GM-CSF, содержащих SEQ ID NO: 5-20
Повторяют Пример 3. В качестве антагониста GM-CSF используют антитело, специфичное в отношении GM-CSF, содержащее последовательность H-CDR3, выбранную из любой из SEQ ID NO: 5-16. Предпочтительно указанные антитела дополнительно содержат последовательность H-CDR1 с SEQ ID NO: 16, и/или последовательность Н-CDR2 с SEQ ID NO: 17, и/или последовательность L-CDR1 с SEQ ID NO:18, и/или последовательность L-CDR2 с SEQ ID NO: 19, и/или последовательность L-CDR3 с SEQ ID NO: 20. Может быть использован другой вид, не являющийся мышью, в частности, вид, в отношении которого антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно, видом животного, используемым в данном эксперименте, является крыса.
Животные, например крысы, получавшие лечение контрольным антителом того же изотипа, демонстрируют значительно более выраженные признаки остеоартрита по сравнению с животными, получавшими антитело, специфичное в отношении GM-CSF, использованное в данном примере. Это демонстрирует эффективность антител в лечении OA.
Пример 7:
Терапевтическая эффективность антител, специфичных в отношении GM-CSF, содержащих SEQ ID NO: 21-26
Повторяют Пример 3. В качестве антагониста GM-CSF используют антитело, специфичное в отношении GM-CSF, содержащее последовательность L-CDR1 с SEQ ID NO: 22, и/или последовательность L-CDR2 с SEQ ID NO:23, и/или последовательность L-CDR3 с SEQ ID NO: 24, и/или последовательность H-CDR1 с SEQ ID NO:25, и/или последовательность H-CDR2 с SEQ ID NO: 26, и/или последовательность H-CDR3 с SEQ ID NO: 27. Предпочтительно указанное антитело содержит все CDR с SEQ ID NO: 22-27. Может быть использован другой вид, не являющийся мышью, в частности, вид, в отношении которого антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно, видом животного, используемым в данном эксперименте, является крыса.
Животные, например крысы, получавшие лечение контрольным антителом того же изотипа, демонстрируют значительно более выраженные признаки остеоартрита по сравнению с животными, получавшими антитело, специфичное в отношении GM-CSF, использованное в данном примере. Это демонстрирует эффективность антител в лечении OA.
Пример 8:
Терапевтическая эффективность антител, специфичных в отношении рецептора GM-CSF
Повторяют Пример 3, с тем отличием, что вместо моноклонального антитела, специфичного в отношении GM-CSF, используют моноклональное антитело, специфичное в отношении рецептора GM-CSF.
В качестве антагониста GM-CSF используют антитело, специфичное в отношении рецептора GM-CSF, содержащее аминокислотную последовательность последовательности H-CDR3, показанной в любой из SEQ ID NO: 27-45. Может быть использован другой вид, не являющийся мышью, в частности, вид, в отношении которого антитело, используемое в данном эксперименте, является перекрестно реактивным. Предпочтительно, видом животного, используемым в данном эксперименте, является крыса.
Животные, например крысы, получавшие лечение контрольным антителом того же изотипа, демонстрируют значительно более выраженные признаки остеоартрита по сравнению с животными, получавшими антитело, специфичное в отношении рецептора GM-CSF, использованное в данном примере. Это демонстрирует эффективность антител в лечении OA.
Пример 9: Клиническое исследование
Проводят клиническое исследование на взрослых пациентах, страдающих от остеоартрита коленного сустава. Задачей рандомизированного двойного слепого плацебо-контролируемого клинического исследования является определение сравнительных эффективностей антагонистов GM-CSF по настоящему изобретению и плацебо в общем облегчении боли и улучшении качества жизни в общей выборке из 30 пациентов с диагностированным остеоартритом (OA) коленного сустава. Другой задачей является определение безопасности и переносимости антагонистов GM-CSF по настоящему изобретению, что определяют по нежелательным явлениям, физикальному осмотру и основным показателям состояния организма.
Методы
В исследование включают тридцать пациентов (приблизительно 15 взрослых мужчин и 15 взрослых женщин) в возрасте 40 лет или более с клиническим диагнозом остеоартрита коленного сустава (коленных суставов) и верифицированной болью в коленных суставах на протяжении по меньшей мере 15 суток в месяц перед исследованием. Пациенты получают терапевтически эффективное количество антагонистов GM-CSF или плацебо (например, один раз каждые две недели на протяжении приблизительно шести месяцев).
В исследовании применяют индекс WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index) (WOMAC; Bellamy et al, J Rheumatol 75(12): 1833-40, 1988) и способ балльной оценки качества жизни SF-36v2 (SF-36v2 Quality of Life instrument scales) (Quality Metric Health Outcomes Solutions, Lincoln, RI). WOMAC является болезнь-специфическим критерием состояния здоровья, определяемым самим пациентом. Он включает оценку клинически важных симптомов в области боли, тугоподвижности и функционального статуса у пациентов с остеоартритом тазобедренного сустава и/или коленного сустава. Индекс состоит из 24 вопросов (5 - боль, 2 - тугоподвижность и 17 - функциональный статус) и может быть определен менее чем за 5 минут.WOMAC является эффективным, надежным и чувствительным способом выявления клинически важных изменений состояния здоровья после различных вмешательств (фармакологических, диетологических, хирургических, физиотерапии и тому подобных). Анкета WOMAC эффективна для оценки эффектов вмешательства на остеоартрит тазобедренных суставов и/или коленных суставов. Способ балльной оценки качества жизни SF-36v2 является многоцелевым кратким исследованием состояния здоровья из 36 вопросов. Он позволяет получить 8-балльный профиль показателей функционального здоровья и самочувствия, а также основанные на психометрии суммарные критерии физического и психического здоровья и основанный на предпочтении индекс полезности для здоровья. Он является общим критерием, в отличие от критерия, направленного на определенный возраст, заболевание или группу лечения. Соответственно, SF-36v2 оказался полезным в исследованиях общей и специфических популяций по сравнению относительной тяжести заболеваний и в выявлении различий в полезных для здоровья эффектах, полученных широким спектром различных способов лечения. SF-36v2 позволяет получить информацию о следующих аспектах и подгруппах здоровья: физическое здоровье (состоит из функционального статуса, ролевого функционирования, обусловленного физическим состоянием, физической боли и общего состояния здоровья) и психическое здоровье (состоит из энергичности, социального функционирования, ролевого функционирования, обусловленного эмоциональным состоянием, и психического здоровья).
Результаты
Изменение физической боли. Улучшение показателя физической боли SF-36v2 статистически достоверно у пациентов, получавших антагонисты GM-CSF по настоящему изобретению, по сравнению с плацебо. Более высокий показатель лучше, поскольку это означает, что пациент чувствует меньшую боль после приема продукта. Присутствует статистически достоверное улучшение показателя физической боли в группе, получавшей антагонисты GM-CSF по настоящему изобретению, по сравнению с группой плацебо.
Изменение показателя ролевого функционирования, обусловленного физическим состоянием. Больший эффект антагонистов GM-CSF по настоящему изобретению по сравнению с плацебо статистически достоверен на 8 неделе, 12 неделе и 20 неделе в отношении ограничений ролевого функционирования, обусловленных физическим здоровьем (ролевого функционирования, обусловленного физическим состоянием). Более высокий показатель лучше, поскольку это означает, что пациент отмечает улучшение физического состояния и уменьшение ограничений в повседневной деятельности. Присутствует статистически достоверное улучшение показателя ролевого функционирования, обусловленного физическим состоянием, в группе, получавшей антагонисты GM-CSF по настоящему изобретению, по сравнению с группой плацебо.
Изменение общего показателя WOMAC. Общий показатель WOMAC в группе, получавшей лечение антагонистами GM-CSF по настоящему изобретению, статистически достоверно лучше общего показателя WOMAC группы плацебо (более низкий показатель лучше).
Изменение WOMAC ADL. Улучшение повседневной деятельности (измеренной как подпоказатель WOMAC ADL) в группе, получавшей лечение антагонистами GM-CSF по настоящему изобретению, больше, чем в группе плацебо. Присутствует статистически достоверное улучшение показателя WOMAC ADL в группе, получавшей лечение антагонистами GM-CSF по настоящему изобретению, по сравнению с группой плацебо (более низкий показатель лучше).
Выводы
Клиническое исследование демонстрирует эффективность антагонистов GM-CSF по настоящему изобретению в улучшении качества жизни пациентов с остеоартритом коленного сустава. Результаты клинического исследования также демонстрируют безопасность и переносимость продуктов, с учетом того, что серьезных нежелательных эффектов обнаружено не было.
Эффективность антагонистов GM-CSF по настоящему изобретению может также быть установлена исследованиями на других видах, в отношении которых антагонисты GM-CSF по настоящему изобретению являются перекрестно реактивными (например, на лошадях для оценки движения в суставах); и применением исследований in vitro для определения способности антагонистов GM-CSF по настоящему изобретению ингибировать индуцированную IL-1 деградацию агрекана, проводя исследование на культурах хондроцитов.
Специалистам в данной области техники будет ясно, что изобретение, описанное здесь, может быть изменено и модифицировано иным образом, чем конкретно описано здесь. Следует понимать, что изобретение включает все такие изменения и модификации. Изобретение также включает все стадии, признаки, композиции и соединения, упомянутые или указанные в данном описании, по отдельности или совместно, и все и любые комбинации любых двух или более из указанных стадий или признаков.
СПИСОК ЛИТЕРАТУРЫ
Bellamy et al, J Rheumatol 15(12): 1833-40, 1988.
Blom et al, Arthritis Rheum 56: 147-157, 2007.
Ghose et al, J Combin Chem: 7: 55-68, 1999.
Knappik et al, J. Mol. Biol. 296: 57, 2000.
Krebs et al, J. Immunol. Methods. 254: 67, 2001.
Lipinski et al, Adv Drug Del Rev: 23: 3-25, 1997.
Mills et al, J Immunol 164: 6166-6173, 2000.
Pritzker et al, Osteoarthritis Cartilage 14: 13-29, 2006
Rothe et al, J. Mol. Biol. 376: 1182, 2008.
| название | год | авторы | номер документа |
|---|---|---|---|
| Лечение боли | 2009 |
|
RU2712166C2 |
| Лечение боли | 2009 |
|
RU2630969C2 |
| ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА | 2010 |
|
RU2539034C2 |
| АНТИТЕЛА, НЕЙТРАЛИЗУЮЩИЕ GM-CSF, ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ РЕВМАТОИДНОГО АРТРИТА ИЛИ В КАЧЕСТВЕ АНАЛЬГЕТИКОВ | 2014 |
|
RU2714919C2 |
| ЛЕЧЕНИЕ ОСТЕОАРТРИТА И БОЛИ | 2012 |
|
RU2563830C2 |
| АНТИ-GM-CSF АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2447085C2 |
| СПОСОБЫ ЛЕЧЕНИЯ СОСТОЯНИЙ АНТИТЕЛАМИ, КОТОРЫЕ СВЯЗЫВАЮТ РЕЦЕПТОР КОЛОНИЕСТИМУЛИРУЮЩЕГО ФАКТОРА 1 (CSF1R) | 2012 |
|
RU2670743C9 |
| СПОСОБ ИНГИБИРОВАНИЯ GMCSFRa У ПАЦИЕНТА | 2012 |
|
RU2639546C2 |
| АНТИТЕЛА ПРОТИВ CSF-1R ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2617971C2 |
| АНТИТЕЛА ПРОТИВ NGF И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2019 |
|
RU2838175C2 |














Группа изобретений относится к медицине, а именно к способу лечения остеоартрита (OA). Для этого применяют антагонист гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) для уменьшения или предупреждения патологических признаков остеоартрита, включающих повреждение хряща, образование остеофитов и деформацию суставов, где антагонист представляет собой антитело, специфичное в отношении GM-CSF. Использование данной группы изобретений позволяет применять антагонист гранулоцитарно-макрофагального колониестимулирующего фактора лечения остеоартрита, в частности выраженных признаков остеартрита, которые обусловлены дегенеративными процессами в суставе и не имеют прямой взаимосвязи с воспалительным компонентом. 2 н. и 5 з.п. ф-лы, 6 ил., 9 пр.
1. Применение антагониста гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) для уменьшения или предупреждения патологических признаков остеоартрита, включающих повреждение хряща, образование остеофитов и деформацию суставов, где антагонист представляет собой антитело, специфичное в отношении GM-CSF.
2. Применение композиции, содержащей антагонист GM-CSF, для уменьшения или предупреждения патологических признаков остеоартрита, включающих повреждение хряща, образование остеофитов и деформацию суставов, где антагонист представляет собой антитело, специфичное в отношении GM-CSF и где указанная композиция дополнительно содержит один или более чем один фармацевтически приемлемый носитель и/или разбавитель.
3. Применение по п. 1 или 2, где антитело представляет собой химерное, гуманизированное или человеческое антитело.
4. Применение по п. 3, где антитело представляет собой гуманизированное антитело.
5. Применение по любому из пп. 1-4, где антитело содержит вариабельную область тяжелой цепи, по меньшей мере на 90% гомологичную аминокислотной последовательности SEQ ID NO: 3, или вариабельную область легкой цепи, по меньшей мере на 90% гомологичную аминокислотной последовательности SEQ ID NO: 4.
6. Применение по п. 5, где антитело содержит вариабельную область тяжелой цепи, по меньшей мере на 95% гомологичную аминокислотной последовательности SEQ ID NO: 3, или вариабельную область легкой цепи, по меньшей мере на 95% гомологичную аминокислотной последовательности SEQ ID NO: 4.
7. Применение по п. 5, где антитело содержит аминокислотную последовательность вариабельной области тяжелой цепи SEQ ID NO: 3 или аминокислотную последовательность вариабельной области легкой цепи SEQ ID NO: 4.
| WO 2007092939 A2, 16.08.2007 | |||
| WO 2006122797 A2, 23.11.2006 | |||
| US 2007243225 A1, 18.10.2007 | |||
| PLATER-ZYBERK C | |||
| et al | |||
| GM-CSF neutralisation suppresses inflammation and protects cartilage in acute streptococcal cell wall arthritis of mice // Ann Rheum Dis | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2020-01-28—Публикация
2009-12-21—Подача