Изобретение относится к области химико-фармацевтической промышленности и медицины и касается усовершенствованных способов получения лекарственных форм активных средств антиоксидантного и мембранопротекторного действия.
В последнее время пристальное внимание уделяется процессам свободно-радикального окисления в норме и патологии. Установлена их значительная роль в развитии множества заболеваний. В том числе, могут быть упомянуты: атеросклеротическое поражение сосудов сердца и мозга, гипертоническая болезнь, раковые образования, нейродегенеративные заболевания, судорожные состояния, стресс, невроз, болевые синдромы, остеоартрит, амилоидоз, холецистит, панкреатит, воспалительные процессы, заболевания крови, глаз (катаракта и др.), кожи, сахарный диабет, болезни почек, печени и легких, аллергические и иммунодефицитные состояния, старение организма.
Этим и были продиктованы исследования одного из наиболее перспективных направлений в поддержании адекватной деятельности эндогенной антиоксидантной системы - рациональной антиоксидантной терапии.
Создание синтетических антиоксидантов является несомненным достижением отечественной фармацевтической индустрии. Особое место среди подобных препаратов занимает этилметилгидроксипиридина сукцинат.
Этилметилгидроксипиридина сукцинат имеет широкий спектр фармакологической активности: является антигипоксическим, стресспротекторным, ноотропным, противосудорожным и анксиолитическим препаратом, ингибирующим свободнорадикальные процессы окисления липидов, повышает резистентность организма (и в частности мозга) к воздействию разных повреждающих факторов и к кислородзависимым патологическим состояниям (шок, гипоксия, ишемия, интоксикация алкоголем, антипсихотическими средствами и т.д.). В клинической практике препарат используют в форме раствора для инъекций, капсул и таблеток. Таблетки, содержащие в качестве активного начала Этилметилгидроксипиридина сукцинат, выпускаются производителями под различными торговыми наименованиями: Мексидол, Метостабил, Мексиприм, Мексифин, Армадин и др., в дозировке, как правило, составляющей 0,125 г на таблетку (https://www.rlsnet.rU/mnn_index_id_3049.htm#torgovye-nazvaniya). Однако пациенты с нарушениями эндогенной антиоксидантной системы, страдают рядом патологических нарушений, и для таких пациентов требуется повышенная дозировка активного вещества. В настоящее время разработаны таблетки «Мексидол® ФОРТЕ 250», имеющие двойную дозировку действующего вещества в одной таблетке, покрытой оболочкой (https://www.rlsnet.ru/tn_index_id_96306.htm#sostav).
Различные составы таблеток мексидола и способы их получения защищены рядом патентов.
Известен патент RU 2065299 С1, который раскрывает средство, выполненное в виде таблетки, состоящей из ядра, содержащего 16,7-41,6% вес. мексидола, и из полимерной оболочки. Ядро в качестве вспомогательных веществ содержит глину белую - 16,7-33,3% вес., крахмал картофельный - 16,7-33,7% вес., кальций стеариновокислый - 0,3-0,5% вес., кислоту стеариновую - 0,3-0,5% вес., тальк - 0,5-1,0% вес. и метилцеллюлозы 25,0-50% вес. с добавками твина 80 - 8,3-25,0% вес., и диоксида титана - 8,3-25,0% вес.
В качестве ближайшего аналога (прототипа) может быть указан патент RU 2428177 С1, который раскрывает средство в форме таблеток, содержащих мексидол, лактозы моногидрат, магния стеарат и натрий карбоксиметилцеллюлозу. Дополнительно фармацевтическое средство может содержать коллидон 30 (поливинилпирролидон). Таблетки покрывают оболочкой на основе пленкообразующей суспензии Опадрай II белого.
Известные формы не обеспечивают пролонгированный эффект действующего вещества. Кроме того, показатели выведения с мочой неизмененного препарата и метаболитов имеют значительную индивидуальную вариабельность концентраций, поэтому требуются формы замедленного действия с улучшенным фармакокинетическим профилем.
Задачей настоящего изобретения является разработка способа получения таблетированной формы, обеспечивающей модифицированное высвобождение при более высоком содержании действующего вещества в единичной дозированной форме.
Для выбора способа были протестированы различные пролонгирующие агенты и наполнители, замедляющие высвобождение мексидола, и оценено их влияние на вариабельность у пациентов.
Одним из известных замедляющих высвобождение наполнителей является гидроксипропилметилцеллюлоза (ГПМЦ), которая выпускается в виде субстанций с различными средними молекулярными массами и вязкостью.
Известно, что марки ГПМЦ с высокими значениями молекулярной массы предпочтительно используют для хорошо растворимых активных фармацевтических субстанций, поскольку высвобождение такого лекарственного средства регулируется, главным образом, диффузией через набухший слой геля. В то же время марки с низкими значениями молекулярной массы ГПМЦ предпочтительно используют для малорастворимых активных фармацевтических субстанций, так как для эффективного высвобождения такого лекарственного средства требуется эрозия матрицы.
Этилметилгидроксипиридина сукцинат относится к легко растворимым в воде субстанциям. Однако неожиданно нами было обнаружено, что наилучший эффект может быть обеспечен подбором двух разных по вязкости и молекулярной массе гидроксипропилметилцеллюлоз в сочетании с определенными вспомогательными веществами и оболочкой.
Задача изобретения была решена новым способом получения пролонгированной формы этилметилгидроксипиридина сукцината - препарата антиоксидантного действия, характеризующимся тем, что просеянную смесь этилметилгидроксипиридина сукцината и гидроксипропилметилцеллюлозы с вязкостью 2700-5040 мПа⋅с смешивают с предварительно полученным увлажняющим агентом, представляющим собой водный раствор гидроксипропилметилцеллюлозы с вязкостью 4,8-7,2 мПа⋅с, гранулируют смесь в кипящем (псевдоожиженном) слое, полученные гранулы опудривают стеаратом магния и кремния диоксидом коллоидным, подвергают повторной грануляции сухим методом с последующим прессованием в таблетку и нанесением пленочной оболочки.
Пленочное покрытие может быть выполнено на основе поливинилпирролидона, поливинилового спирта, производных целлюлозы, таких как гидроксиалкилцеллюлоза.
Пленочное покрытие предпочтительно представляет собой покрытие на основе гипромеллозы 2910 с номинальной вязкостью 3, 5, 6 или 15 мПа⋅с, например оболочку Opadry® белую или пигментированную. Такое покрытие может включать макрогол 6000, тальк, титана двуокись, необязательно краситель типа железа оксида желтого или красного.
Предпочтительно смесь прессуют в таблетки с содержанием действующего вещества не менее 300 мг на таблетку, например 300-400 мг.
Новый способ позволил получить таблетированную форму с улучшенными фармакокинетическими параметрами и механическими свойствами (технический результат).
Пример 1.
Способ производства таблеток с дозировкой 375 мг, покрытых оболочкой.
1. Приготовление увлажнителя.
Полученную склада ГПМЦ Е6 гранулировщик отвешивает на весах в емкость. В реактор отмеривают воду очищенную комнатной температуры. Включают мешалку, перемешивание продолжают до полного растворения ГПМЦ 6. Раствор должен быть бесцветным или со слегка желтоватым оттенком и прозрачным.
2. Просеивание сырья.
Этилметилгидроксипиридина сукцина (ЭМГПС), ГПМЦ К4М гранулировщик просеивает на вибросите с сеткой 0,5 мм (ГОСТ 214-83) в емкости. Просеивание порошков ведут раздельно, очищая сито после каждого вида сырья. Полученные просевы гранулировщик в закрытых и этикетированных приемных емкостях передает на стадию ТП 3 для получения гранулята.
Полученные со склада магния стеарат и кремния диоксид коллоидный гранулировщик просеивает на вибросите с сеткой №38 по ОСТ 17-46-82 Просеивание порошков ведут раздельно, очищая сито после каждого вида сырья. Полученные просевы в приемных емкостях передают на стадию ТП 3 для получения массы для таблетирования.
3. Гранулирование.
Гранулировщик на весах отвешивает полученный с операции. «Просев сырья» ЭМГПС и загружает его в емкость сушилки - гранулятор. Туда же загружает ГПМЦ К4М. Емкость устанавливают в сушилку-гранулятор LD 120. Заливают из емкости в дозатор сушилки-гранулятора раствор ГПМЦ Е6 полученный с операции 1. «Приготовление увлажнителя».
Контроль точности взвешивания, отмеривания и соответствие наименований ингредиентов осуществляет мастер (Кт ТП 3.1.).
Подсоединяют заземление к загрузочной емкости, открывают кран подачи пара и включают аппарат.
Влажность получаемого гранулята проверяет контролер ОКК или лаборант ОКК. Она должна составлять не более 2%.
4. Опудривание и калибровка гранулята.
Опудривание производится в LD-120 сразу после получения гранулята. Взвесить необходимое количество магния стеарата, кремния диоксида коллоидного.
Вручную совком в продуктовой емкости перемешать гранулят и опудривающие вещества.
Запустить процесс смешивания.
5. Сухое гранулирование.
В целях улучшения однородности таблетмассы гранулят, подвергают сухому гранулированию. Для этого гранулят из емкости сушилки - гранулятора Г-9 совком выгружают в гранулятор горизонтального типа с установленной сеткой с диаметром отверстий 1,5 мм. Полученный после сухого гранулирования гранулят собирают в емкости передают на операцию «Таблетирование»
5. Таблетирование.
Массу для таблетирования засыпают в бункер и приступают к пробному прессованию. После настройки массы таблетки проверяют по качественным показателям: внешний вид, средняя масса, отклонение от средней массы, прочность на излом, прочность на «Истирание» распадаемость, растворение.
Среднюю массу таблеток определяют взвешиванием 20 таблеток на электронных весах через каждые 60 минут. Средняя масса таблеток с дозой активного вещества 375 мг должна быть 780 мг плюс-минус 5%.
Таблетки имеют высокую прочность. Прочность на излом составляет не менее 5 кг, прочность на истирание не менее 99,6%.
Оценку внешнего вида производят на основании осмотра невооруженным глазом 50-100 таблеток. Таблетки должны иметь цельные края без выщербленных мест, правильную форму, поверхность должна быть гладкой и однородной.
6. Покрытие таблеток пленочной оболочкой.
Приготовление суспензии-пленкообразователя
В подготовленную ступку отвешивают на весах необходимые количества талька и титана двуокиси.
Перед началом покрытия в ступке пестиком растирают навески талька и двуокиси титана, в подготовленную тару отмеривают необходимое количество воды очищенной и постепенно добавляют воду в ступку, перемешивая пестиком, до получения однородной суспензии.
В емкость с мешалкой и дозирующим устройством через сито из нержавеющей стали процеживают предварительно приготовленные растворы Гипромеллозы и ПЭГ-6000 (макрогола), суспензию талька и двуокиси титана.
Включают мешалку, повернув кран емкости с мешалкой и дозирующим устройством, и устанавливают обороты мешалки до образования воронки. Перемешивание продолжают до получения однородной суспензии белого цвета. Далее подсоединяют шланг дозирующего устройства (перистальтического насоса) к верхнему штуцеру емкости. Получают однородную суспензию белого цвета.
Покрытия ядер таблеток оболочкой.
Для покрытия таблеток оболочкой на коутере СМ-80 устанавливают следующие параметры:
- Скорость вращения котла - 2 об/мин;
- Давление распыления - 0,2 МРа;
- Расход суспензии - 40 мл/мин;
- Отрицательное давление в котле -3 КРа;
- Время распыления 30 мин.
Затем наступает переходная фаза несения оболочки при следующих параметрах:
- Скорость вращения котла - 4 об/мин;
- Давление распыления - 0,3 МРа;
- Расход суспензии - 50 мл/мин;
- Отрицательное давление в котле -3 КРа;
- Время распыления 60 мин.
Приступая к конечной фазе нанесения оболочки, устанавливают следующие параметры:
- Скорость вращения котла - 6-8 об/мин;
- Расход суспензии - 60 мл/мин;
- время распыления - до полной выработки суспензии;
При завершении работы отключается распыление, отключается подача входящего воздуха и исходящий воздух, а так же нагрев входящего воздуха. Штатив с пистолетами выдвигают. Затем таблетки обкатывают (глянцуют) в течение 5 минут.
7. Упаковка.
Расфасовывают таблетки в контурную ячейковую упаковку из поливинилхлоридной пленки марки ЭП-73 или аналогичной и фольги алюминиевой печатной лакированной марки ФГПЛ А5Т с другой стороны.
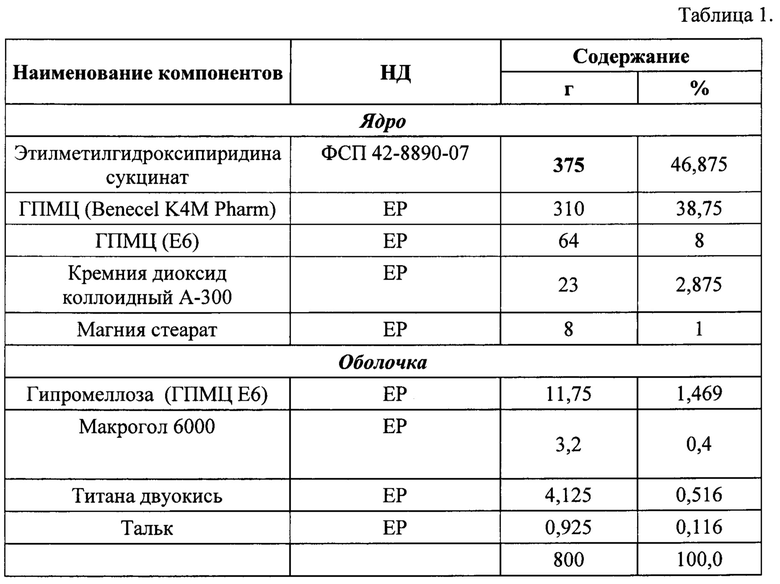
Состав полученных таблеток представлен в Таблице 1.
Пример 2.
Исследование фармакокинетики плазмы крови кроликов после однократного введения таблетированных форм мексидола (таблетки замедленного высвобождения, полученные по Примеру 1, и таблетка согласно прототипу).
Исследование проведено на двух группах по 10 кроликов-самцах массой 2,3±0,24 кг, содержащихся в стандартных условиях вивария. Животным однократно через зонд вводили 1 таблетку замедленного высвобождения согласно изобретению или 1 таблетку согласно прототипу. Образцы крови отбирали из краевой ушной вены через дискретные интервалы времени (0; 0,5; 1; 1,5; 2; 2,5; 3; 4; 6; 8; 12; 16; 24; 48 часа). Количественное определение действующего вещества в плазме крови кроликов проводили методом ВЭЖХ с пределом детектирования 20 нг/мл. Полученные экспериментальные данные предварительно были подвергнуты статистической обработки с помощью программы Statistica 6.0.
Сравнительный анализ основных фармакокинетических параметров показал, что среднее время удерживания препарата в плазме крови (MRT) для заявленных таблеток модифицированного высвобождения составило 6,50±0,40 ч, по прототипу - 3,48±1,05 ч. Время достижения максимальной концентрации сравнимо по показателям для кроликов одной группы. Период полувыведения для пролонгированных лекарственных форм согласно изобретению составил 2,75±0,45 ч, для таблеток по прототипу - 2,00±1,14 ч.
Таким образом, исследования показывают, что фармакокинетические параметры новой таблетки обеспечивает пролонгированный эффект действия без значительного разброса в концентрациях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АНТИОКСИДАНТНОГО ДЕЙСТВИЯ В ФОРМЕ ТАБЛЕТКИ | 2020 |
|
RU2749718C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭТИЛМЕТИЛГИДРОКСИПИРИДИНА СУКЦИНАТ | 2021 |
|
RU2798106C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ ТАБЛЕТКИ, ПОКРЫТОЙ ОБОЛОЧКОЙ | 2022 |
|
RU2786073C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОЙ ФОРМЫ ТРИМЕТАЗИДИНА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 2012 |
|
RU2530558C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНА СУКЦИНАТА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2444359C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, ОБЛАДАЮЩЕЙ НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ ПРИ ХРОНИЧЕСКОЙ ИШЕМИИ ГОЛОВНОГО МОЗГА | 2023 |
|
RU2816359C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ ИННЕРВАЦИЙ (ВАРИАНТЫ) | 2013 |
|
RU2536269C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ МЕМАНТИН И ЦИТИКОЛИН, А ТАКЖЕ ЛЕКАРСТВЕННАЯ ФОРМА НА ОСНОВЕ УКАЗАННОЙ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, ВКЛЮЧАЮЩЕЙ МЕМАНТИН И ЦИТИКОЛИН, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ЛЕКАРСТВЕННОЙ ФОРМЫ НА ОСНОВЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, ВКЛЮЧАЮЩЕЙ МЕМАНТИН И ЦИТИКОЛИН | 2020 |
|
RU2810575C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ТЕТРАМЕТИЛТЕТРААЗОБИЦИКЛООКТАНДИОНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2611194C2 |
| Система доставки 2-этил-6-метил-3-гидроксипиридина сукцината для перорального применения в форме гастроретентивной таблетки | 2019 |
|
RU2734970C1 |
Изобретение относится к области химико-фармацевтической промышленности и медицине. Раскрыт способ получения препарата антиоксидантного действия в форме пролонгированного высвобождения, характеризующийся тем, что просеянную смесь этилметилгидроксипиридина сукцината и гидроксипропилметилцеллюлозы с вязкостью 2700-5040 мПа⋅с смешивают с предварительно полученным увлажняющим агентом, представляющим собой водный раствор гидроксипропилметилцеллюлозы с вязкостью 4,8-7,2 мПа⋅с, гранулируют смесь в кипящем (псевдоожиженном) слое, полученные гранулы опудривают стеаратом магния и кремния диоксидом коллоидным, подвергают сухой грануляции с последующим прессованием в таблетки и нанесением пленочной оболочки. Таблетки имеют улучшенный фармакологический профиль высвобождения. 3 з.п. ф-лы, 1 табл., 2 пр.
1. Способ получения препарата антиоксидантного действия в форме пролонгированного высвобождения, характеризующийся тем, что просеянную смесь этилметилгидроксипиридина сукцината и гидроксипропилметилцеллюлозы с вязкостью 2700-5040 мПа⋅с смешивают с предварительно полученным увлажняющим агентом, представляющим собой водный раствор гидроксипропилметилцеллюлозы с вязкостью 4,8-7,2 мПа⋅с, гранулируют смесь в кипящем (псевдоожиженном) слое, полученные гранулы опудривают стеаратом магния и кремния диоксидом коллоидным, подвергают сухой грануляции с последующим прессованием в таблетки и нанесением пленочной оболочки.
2. Способ по п. 1, характеризующийся тем, что пленочное покрытие представляет собой покрытие на основе гипромеллозы 2910 с вязкостью 3, 5, 6 или 15 мПа⋅с.
3. Способ по п. 2, характеризующийся тем, что пленочное покрытие представляет собой покрытие, состоящее из гипромеллозы 2910 с номинальной вязкостью 6 мПа⋅с, макрогол 6000, тальк и титана двуокись.
4. Способ по любому из предшествующих пунктов, характеризующийся тем, что смесь прессуют в таблетку с содержанием действующего вещества, по крайней мере, 300 мг.
| ЛЕКАРСТВЕННАЯ ФОРМА С МОДИФИЦИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ 6-МЕТИЛ-2-ЭТИЛ-3-ГИДРОКСИПИРИДИНА СУКЦИНАТА | 2008 |
|
RU2411035C2 |
| ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО | 2010 |
|
RU2428177C1 |
| ГОМОДИННЫЙ РАДИОПРИЕМНИК | 2000 |
|
RU2241310C2 |
| Машковский М.Д | |||
| Лекарственные средства/ изд | |||
| Насос | 1917 |
|
SU13A1 |
| - М.: Медицина, 1997, ч.2, стр.197. | |||
Авторы
Даты
2020-01-29—Публикация
2019-06-04—Подача