Настоящее изобретение относится к основанному на применении микровезикул способу обнаружения некротического энтерита птиц, а также к новым маркерам, которые идентифицированы в качестве приемлемых для обнаружения некротического энтерита птиц и/или заражения птиц Clostridium perfringens.
Clostridium perfringens является основным возбудителем некротического энтерита птиц (NE), энтеральной болезни домашней птицы, впервые описанной в 1961 г. NE у кур проявляется в виде острой или хронической энтеротоксемии. Острая форма заболевания приводит к высокому уровню смертности из-за развития некротических повреждений в стенке кишечника, а хроническая форма заболевания приводит к значительному снижению продуктивности и материальным убыткам. Было установлено, что болезнь наносит ущерб птицеводству, исчисляемый несколькими миллиардами долларов США в год.
С.perfringens, как правило, присутствует в желудочно-кишечном тракте домашней птицы, однако некротический энтерит возникает лишь в единичных случаях. С.perfringens представляет собой грамположительную имеющую форму палочки спорообразующую толерантную к кислороду анаэробную бактерию. Штаммы С.perfringes классифицируют на пять продуцирующих токсины типов (А, В, С, D и Е) на основе производстве четырех возможных основных токсинов (альфа, бета, эпсилон и йота). В то время как тип А систематически выделяют из кишечника кур, другие типы встречаются реже.
Проведенные ранее исследования NE позволили предположить, что основной вирулентный фактор заболевания секретировался бактерией, это привело к предположению, что фермент фосфолипаза С, называемая альфа-токсином, представляла собой основной токсин, участвующий в патогенезе. Однако в современных исследованиях установлено, что альфа-токсин, по-видимому, не является имеющим решающее значение вирулентным фактором, поскольку штаммы с мутантным альфа-токсином обладали способностью вызывать NE, что ставит под сомнение роль альфа-токсина в возникновениизаболевания в целом. В более современных исследованиях было высказано предположение о том, что основную роль в развитии этого заболевания играет новый образующий поры токсин, netB.
Помимо просто ассоциации факторов вирулентности per se с заболеваемостью NE, все еще существует очень большая необходимость продемонстрировать механистическую связь между этими факторами и возникновением заболевания у птиц или сельскохозяйственных животных. Кроме того, связь доклинической NE-инфекции с любым из этих факторов вирулентности очень трудно установить, поскольку для птиц отсутствуют признаки надежной оценки до их убоя. Таким образом, существует насущная необходимость в способе раннего обнаружения NE, и, что является наиболее важным, доклинических форм NE.
Традиционно открытие и валидация биомеркеров болезни требует применения ткани, либо свежезамороженной, либо, что является более частым, фиксированной в формалине, залитой в парафин. Это относится, прежде всего, в биомаркерам на основе мРНК, поскольку расщепление РНКазой свободной РНК делает весьма проблематичным трансляцию тканевых биомаркеров в биологических жидкостях, таких как кровь и/или образцы фекалий/цекального помета. Однако, для изучения большого количества образцов, например, сельскохозяйственных животных, указанный мониторинг тканевых биомаркеров из-за его инвазивной природы является трудоемким и непрактичным.
Для обнаружения болезней у птиц описаны неинвазивные методы, такие как измерение параметров крови (Chuku и др., 2012; Aade и др., 2012; Saleem, 2012). В публикации Gulbeena Saleem (2012) высказано предложение, в качестве альтернативного подхода для определения доклинического NE измерять уровни белков острой фазы, таких как церуплазмин, PIT54 и овотрансферрин в ответ на контрольное заражение С.perfringes в сыворотке крови кур. Установлено, что только церуплазмин, вероятно, является приемлемым белком острой фазы, коррелирующим с встречаемостью доклинического NE. Тем на менее, это может быть проблематичным, поскольку церуплазмин не является специфическим маркером NE, но является также маркером заболеваний, вызываемых другими бактериальными патогенами (колибациллы у кур, Piercy, 1979; заражение сальмонеллой в промышленных масштабах, Garcia и др., 2009).
Однако в настоящее время обнаружено, что экзосомы и другие мембранные везикулы, обнаруженные в биоматериалах, содержат стабильную РНК из человеческих донорских клеток, включая мРНК, микроРНК (миРНК) и другую некодирующую РНК, с высокой специфичностью в отношении болезненных состояний (Skog и др., 2008; Nilsson и др., 2009; Li и др., 2009; Shao и др., 2012).
Так, при создании изобретения высказано неожиданное предположение о возможности применения мембранных везикул, выделенных из общей воды организма или экскрементов домашней птицы, для выявления у домашней птицы доклинического некротического энтерита. Это может иметь место, в частности, из-за накапливания специфических миРНК хозяев, для которых характерна корреляция с болезнью.
При создании изобретения неожиданно было установлено, что для микровезикул, выделенных из общей воды организма птиц или из экскрементов птиц, характерно изменение в составе поддающейся обнаружению РНК в зависимости от присутствия некротического энтерита. Помимо повышения уровня специфических для хозяина миРНК в микровезикулах в результате заражения С.perfringens, неожиданно было установлено, что во фракции микровезикул можно выявлять также последовательности мРНК С.perfringens, которые таким образом классифицируют как специфические для болезни факторы вирулентности и, следовательно, как приемлемые биомаркеры, которые служат признаком наличия некротического энтерита.
Наличие мРНК С.perfringens во фракции микровезикул можно объяснить тем фактом, что применяемая процедура выделения приводила не только к обогащению микровезикулами домашней птицы, но также и к обогащению микровезикулами инфекционной бактерии. Помимо известных предполагаемых факторов вирулентности типа netB при создании изобретения неожиданно удалось идентифицировать также последовательности РНК, коррелирующие с некротическим энтеритом, которые ранее не рассматривались в качестве таких факторов.
Таким образом, первым объектом настоящего изобретения является быстрый и надежный, предпочтительно неинвазивный способ обнаружения некротического энтерита птиц, в частности доклинического некротического энтерита птиц, предпочтительно домашней птицы, более предпочтительно кур, и/или идентификации особей птиц, страдающих некротическим энтеритом.
Следующим объектом настоящего изобретения является идентификация приемлемых маркеров, предпочтительно специфических для болезни маркеров, которые можно применять в указанном способе.
Таким образом, первым объектом настоящего изобретения является способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где способ включает выделение микровезикул из образца из организма птиц, в частности, из общей воды организма птиц или экскрементов птиц, и последующее определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком некротического энтерита, в этих микровезикулах, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита.
Маркер, который служит признаком некротического энтерита, согласно изобретению предпочтительно выбирают из следующих последовательностей Clostridium perfringens и их гомологов и фрагментов: SAM-область (SEQ ID NO: 1), область цинковых пальцев swim-типа (SEQ ID NO: 3), scPHK (SEQ ID NO: 4), cola-область (SEQ ID NO: 5), СРЕ0956-область (SEQ ID NO: 7), netB-область (SEQ ID NO: 8), virX-область (SEQ ID NO: 9) и TpeL-область (SEQ ID NO: 16); a также из следующих птичьих последовательностей и их гомологов и фрагментов: mir-16 (SEQ ID NO: 10), mir-24 (SEQ ID NO: 11), mir-155 (SEQ ID NO: 12), mir-206 (SEQ ID NO: 13).
Таким образом, предпочтительным объектом настоящего изобретения является способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где способ включает выделение микровезикул из образца из организма птиц, в частности, из общей воды организма птиц или экскрементов птиц, и последующее определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком некротического энтерита, в этих микровезикулах, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер выбирают из приведенной ниже группы («Перечень I»):
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 16;
и) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
к) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
л) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
м) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
н) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(м);
о) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (н);
п) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(о).
В указанном способе последовательности предпочтительно выбирают из приведенной ниже группы («Перечень II»):
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 630, предпочтительно от 460 до 560 SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 60 до 240, в частности, от 80 до 220, SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1300 до 1800, в частности от 1400 до 1700 (последовательности, представленной в), SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280, SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 240 до 540, в частности от 300 до 540, SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 12 до 418, в частности от 240 до 400, SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 673 до 5628 SEQ ID NO: 16;
и) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
к) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
л) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
м) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
н) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(м);
о) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (н);
п) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(о).
Более предпочтительно последовательности выбирают из приведенной ниже группы («Перечень III»):
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 460 до 560 SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 670 до 760 SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 80 до 220 SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1400 до 1700 SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 100 до 280 SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 300 до 540 SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 240 до 400 SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 673 до 5628 SEQ ID NO: 16;
и) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
к) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%), полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
л) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
м) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
н) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(м);
о) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (н);
п) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(о).
В предпочтительном варианте осуществления изобретения комбинации указанных полинуклеотидов/маркеров, предпочтительно комбинации по меньшей мере из 2, 3, 4, 5, 6 или 7 указанных маркеров применяют для обнаружения некротического энтерита.
Другим объектом настоящего изобретения является способ обнаружения инфекции, ассоциированной с Clostridium perfringens, в частности некротического энтерита, ассоциированного с Clostridium perfringens, где способ включает выделение микровезикул из образца из организма птиц и последующее определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком инфекции, ассоциированной с Clostridium perfringens, в частности некротического энтерита, ассоциированного с Clostridium perfringens, в этих микровезикулах, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком болезни, в частности, некротического энтерита. В этом способе по меньшей мере один маркер предпочтительно выбирают из полинуклеотидов, указанных в перечне I, (а)-(з), а также из полинуклеотидов (ДНК и РНК), комплементарных этим последовательностям. Более предпочтительно маркер выбирают из полинуклеотидов, указанных в перечне II, (а)-(з), а также из полинуклеотидов (ДНК и РНК), комплементарных этим последовательностям. Еще более предпочтительно маркер выбирают из полинуклеотидов, указанных в перечне III, (а)-(з), а также из полинуклеотидов (ДНК и РНК), комплементарных этим последовательностям.
Другим объектом настоящего изобретения является способ обнаружения инфекции, ассоциированной с миРНК, в частности некротического энтерита, ассоциированного с миРНК, где способ включает выделение микровезикул из образца из организма птиц и последующее определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком инфекции, ассоциированной с миРНК, в частности некротического энтерита, ассоциированного с миРНК, в этих микровезикулах, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком болезни, в частности, некротического энтерита. В этом способе по меньшей мере один маркер предпочтительно выбирают из полинуклеотидов, указанных в перечне I, (а)-(з), а также из полинуклеотидов (ДНК и РНК), комплементарных этим последовательностям. Более предпочтительно маркер выбирают из полинуклеотидов, указанных в перечне II, (а)-(з), а также из полинуклеотидов (ДНК и РНК), комплементарных этим последовательностям. Еще более предпочтительно маркер выбирают из полинуклеотидов, указанных в перечне III, (а)-(з), а также из полинуклеотидов (ДНК и РНК), комплементарных этим последовательностям.
Поскольку при создании изобретения неожиданно было установлено, что SAM-область (SEQ ID NO: 1), область цинковых пальцев swim-типа (SEQ ID NO: 3), scPHK (SEQ ID NO: 4), СРЕ0956-область (SEQ ID NO: 7) virX-область (SEQ ID NO: 9), а также mir-16 (SEQ ID NO: 10), mir-24 (SEQ ID NO: 11), mir-155 (SEQ ID NO: 12) и mir-206 (SEQ ID NO: 13) все можно применять в качестве маркеров для обнаружения некротического энтерита птиц, следующим объектом настоящего изобретения является способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, в котором обнаружение некротического энтерита осуществляют путем обнаружения присутствия и/или определения количества по меньшей мере одной из указанных ниже последовательностей («Перечень IV») в образце из организма птиц, предпочтительно в микровезикулах в образце из организма птиц, в частности в сравнении с контрольным образцом из незараженной птицы, в котором присутствие и/или повышенный уровень по меньшей мере одной из указанных последовательностей по сравнению с незараженным контролем служит признаком некротического энтерита:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
и) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(и);
л) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (к);
м) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(л).
В этом способе последовательности предпочтительно выбирают из приведенной ниже группы («Перечень V»):
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 560 SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 60 до 240, в частности от 80 до 220, SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280 SEQ ID NO: 7;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 12 до 418, в частности от 240 до 400 SEQ ID NO: 9;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
и) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(и);
л) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (к);
м) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(л).
Более предпочтительно последовательности выбирают из следующей группы («Перечень VI»):
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 460 до 560 SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 670 до 760 SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 80 до 220 SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 100 до 280 SEQ ID NO: 7;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 30 или 40, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 240 до 400 SEQ ID NO: 9;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
и) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(и);
л) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (к);
м) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(л).
В предпочтительном варианте осуществления изобретения комбинации указанных полинуклеотидов, предпочтительно комбинации по меньшей мере из 2, 3, 4, 5, 6 или 7 указанных полинуклеотидов применяют для обнаружения некротического энтерита.
Образец из организма птиц согласно изобретению может представлять собой образец ткани, предпочтительно образец кишечника, в частности, образец двенадцатиперстной или тощей кишки.
Предпочтительно образец из организма птиц выбирают из общей воды организма птиц и экскрементов птиц и их растворов и суспензий.
Общая вода организма птиц согласно изобретению предпочтительно представляет собой кровь, сыворотку крови или плазму крови.
Экскременты птиц согласно изобретению предпочтительно выбирают из таких экскрементов, как фекалии и цекальный помет.
Приемлемые объемы образцов составляют, например, 0,1-20 мл, в частности 0,2-10 мл, предпочтительно 0,5-5 мл. Приемлемая масса образцов составляет, например, 0,1-20 г, в частности 0,2-10 г, предпочтительно 0,5-5 г.
Птица согласно изобретению предпочтительно представляет собой домашнюю птицу.
Предпочтительной домашней птицей согласно изобретению являются куры, индюки, утки и гуси. Домашняя птица может быть оптимизирована для производства молодняка. Этот тип домашней птицы обозначают также как родительские особи. Таким образом, предпочтительными родительскими особями являются родительское поголовье бройлеров, родительское поголовье уток, родительское поголовье индюков и родительское поголовье гусей.
Домашнюю птицу согласно изобретению можно выбирать также из декоративных (выведенных для получения особых свойств) домашних птиц и диких птиц.
Предпочтительными декоративными домашними птицами или дикими птицами являются павлины, фазаны, серые куропатки, цесарки, перепела, глухари, шотландские куропатки, голуби и лебеди.
Другими предпочтительными домашними птицами согласно изобретению являются страусы и попугаи.
Наиболее предпочтительными домашними птицами согласно изобретению являются куры.
В контексте настоящего описания понятие «полинуклеотиды» или «нуклеиновые кислоты» относится к ДНК и РНК. Полинуклеотиды и нуклеиновые кислоты могут быть одноцепочечными или двухцепочечными.
Выделение микровезикул из экскрементов птиц и их последующее применение для обнаружения инфекции птиц, в частности бактериальной инфекции птиц, более конкретно некротического энтерита, ранее не было описано.
Таким образом, следующим объектом настоящего изобретения является способ обнаружения инфекции птиц, в частности доклинической инфекции птиц, предпочтительно бактериальной инфекции птиц, в частности доклинической бактериальной инфекции птиц, более предпочтительно некротического энтерита, в частности доклинического некротического энтерита, где способ включает обнаружение присутствия и/или определение количества по меньшей мере одного маркера, служащего признаком заболевания, в микровезикулах, выделенных из экскрементов птиц, в частности из таких экскрементов, как фекалии и цекальный помет, в котором присутствие и/или увеличение уровня указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком заболевания. В указанном способе по меньшей мере один маркер предпочтительно выбирают из любых полинуклеотидов, указанных в перечне I, предпочтительно указанных в перечне II, более предпочтительно указанных в перечне III.
Установлено, что встречаемость маркеров, которые служат признаком некротического энтерита, является специфической для образца, т.е. поддающееся обнаружению количество различных маркеров зависит от типа образца.
Так, было установлено, что в экскрементах в виде фекалий самым лучшим маркером является SAM-область, за ней следуют scPHK, netB-область, virX-область, cola-область, область цинковых пальцев swim-типа и СРЕ0956-область.
В противоположность этому, в экскрементах в виде цекального помета самым лучшим маркером также является SAM-область, но за ней следуют область цинковых пальцев swim-типа, scPHK, mir206, virX-область, netB-область, СРЕ0956-область и cola-область.
Кроме того, в образцах крови самым лучшим маркером является mirl6, за ним следуют mir155 и mir24.
Таким образом, предпочтительным вариантом осуществления настоящего изобретения является способ обнаружения некротического энтерита птиц, в частности доклинического некротического энтерита птиц, где способ включает обнаружение присутствия и/или определение уровня по меньшей мере одного маркера, служащего признаком заболевания, в экскрементах в виде фекалий, предпочтительно в микровезикулах, выделенных из экскрементов птиц в виде фекалий, в котором присутствие и/или увеличение уровня указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер предпочтительно выбирают из следующих последовательностей:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
з) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(ж);
и) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (з);
к) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(и).
В этом способе последовательности предпочтительно выбирают из следующей группы:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60 или 100, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 630, предпочтительно от 460 до 560, SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60 или 90, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100 или 140, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 60 до 240, в частности от 80 до 220, SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1300 до 1800, в частности от 1400 до 1700, SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150 или 180, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280 SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 240 до 540, в частности от 300 до 540 SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150 или 160, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 12 до 418, в частности от 240 до 400, SEQ ID NO: 9;
з) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(ж);
и) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (з);
к) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(и).
Таким образом, другим предпочтительным вариантом осуществления настоящего изобретения является способ обнаружения некротического энтерита птиц, в частности доклинического некротического энтерита птиц, где способ включает обнаружение присутствия и/или определение уровня по меньшей мере одного маркера, служащего признаком заболевания, в экскрементах птиц в виде цекального помета, в частности в микровезикулах, выделенных из экскрементов птиц в виде цекального помета, в котором присутствие и/или увеличение уровня указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер предпочтительно выбирают из следующих последовательностей:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
и) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(з);
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (и);
л) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(к).
В этом способе последовательности предпочтительно выбирают из следующей группы:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60 или 100, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 630, предпочтительно от 460 до 560, SEQ ID NO: 1,
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60 или 90, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3,
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100 или 140, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 60 до 240, в частности от 80 до 220, SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1300 до 1800, в частности 1400 до 1700, SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150 или 180, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280 SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 240 до 540, в частности от 300 до 540, SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150 или 160, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 12 до 418, в частности от 240 до 400, SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
и) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(з);
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (и);
л) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(к).
Таким образом, другим предпочтительным вариантом осуществления настоящего изобретения является способ обнаружения некротического энтерита птиц, в частности доклинического некротического энтерита птиц, где способ включает обнаружение присутствия и/или определение уровня по меньшей мере одного маркера, служащего признаком заболевания, в крови птиц, в частности в микровезикулах, выделенных из крови птиц, в котором присутствие и/или увеличение уровня указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер предпочтительно выбирают из следующих последовательностей:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
г) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(в);
д) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (г);
е) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(д).
В этом способе последовательности предпочтительно выбирают из следующей группы:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мерег 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
г) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(в);
д) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (г);
е) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(д).
Следующим объектом настоящего изобретения является способ лечения некротического энтерита, включающий осуществление описанного выше способа обнаружения некротического энтерита и последующее введение терапевтического агента для лечения некротического энтерита.
Дополнительным объектом настоящего изобретении является также массив нуклеотидов для обнаружения некротического энтерита, где массив нуклеотидов содержит по меньший один маркер, предпочтительно по меньшей мере 2, 3, 4 или 5 маркеров, выбранных из полинуклеотидов, указанных в перечне IV, предпочтительно указанных в перечне V, наиболее предпочтительно указанных в перечне VI.
Следующим объектом настоящего изобретении является также набор, содержащий комплект олигонуклеотидов для амплификации по меньшей мере одного полинуклеотида, ассоциированного с некротическим энтеритом, где по меньшей мере один полинуклеотид выбран из полинуклеотидов, указанных в перечне IV, предпочтительно указанных в перечне, наиболее предпочтительно указанных в перечне VI.
NetB и TpeL уже известны в качестве основных токсинов, участвующих в патогенезе некротического энтерита (Keyburn и др., 2010; WO 2008/148166; Shojadoost и др., 2012)
ColA обозначает коллагеназу А из Clostridium perfringens; этот ген может быть ассоциирован с патогенезом NE из-за его сходства с так называемым каппа-токсином, одним из предполагаемых основных токсинов этой бактерии (Obana и др., 2013).
Однако нельзя было ожидать присутствия, а также дерегуляции этих генов в микровезикулах.
Известно, что ген virX регулирует гены plx, cola и pfoA в С.perfringens (Ohtani и др., 2002), однако его участие в патогенезе NE ранее не было описано.
Для малой цитоплазматической РНК (scPHK), представителя семейства эволюционно консервативных распознающих сигнал напоминающих частицы РНК, участвующих в механизме спорообразования Clostridium perfringens (Nakamura et al., 1995), также ранее не была описана непосредственная ассоциация с NE у кур.
Кроме того, ранее не описана и не предполагалась возможность участия SAM-домена, домена цинковых пальцев swim-типа и СРЕ0956-области в патогенезе некротического энтерита, поскольку эти последовательности представляют собой последовательности с ранее неизвестными функциями.
Таким образом, следующим объектом настоящего изобретения являются полинуклеотиды, предпочтительно кодирующие полипептид, который обладает токсической активностью, и/или фактор вирулентности, принимающий участие в некротическом энтерите, которые выбраны из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
ж) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(е);
з) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(ж).
Наиболее предпочтительными являются полинуклеотиды, выбранные из группы, которая состоит из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 630, предпочтительно от 460 до 560, SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 630, предпочтительно от 460 до 560, SEQ ID NO: 1;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3;
д) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280, SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280, SEQ ID NO: 7;
ж) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(е);
з) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(ж).
Таким образом, следующим объектом настоящего изобретения являются также полипептиды, которые предпочтительно представляют собой токсины и/или факторы вирулентности, участвующие в некротическом энтерите, выбранные из группы, которая состоит из следующих полипептидов:
а) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60 или 70, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 2;
б) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 14;
в) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 190, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 15;
г) полипептиды, которые содержат полипептиды, указанные в подпунктах (а)-(в).
Наиболее предпочтительными являются полипептиды, выбранные из группы, которая состоит из следующих полипептидов:
а) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 2;
б) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 40, предпочтительно по меньшей мере 60 или 70, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 14;
в) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 190, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 15;
г) полипептиды, которые содержат полипептиды, указанные в подпунктах (а)-(в).
Таким образом, следующим объектом настоящего изобретения является также способ вызывания иммунного ответа у животного; где способ включает введение животному указанного выше полипептида, в частности, выбранного из группы, которая состоит из следующих полипептидов:
а) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 2;
б) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60 или 70, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 14;
в) полипептиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 190, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 15;
г) полипептиды, которые содержат полипептиды, указанные в подпунктах (а)-(в).
Полипептиды, предлагаемые в изобретении, предпочтительно обладают активностью токсина и их предпочтительно можно получать из Clostridium perfringens. Более предпочтительно полипептиды, предлагаемые в изобретении, представляют собой ассоциированные с NE факторы вирулентности.
Следующим объектом настоящего изобретения являются векторы, в частности, клонирующие и экспрессионные векторы, а также вирусные и плазмидные векторы, которые содержат полинуклеотид, предлагаемый в изобретении.
Следующим объектом настоящего изобретения являются также клетки, в частности бактериальные клетки, предпочтительно клетки Е. coli, которые содержат полинуклеотид, полипептид и/или вектор, предлагаемый в изобретении.
Следующим объектом настоящего изобретения является поликлональное или моноклональное антитело или его фрагмент, которое/который специфически связывается с предлагаемым в изобретении полипептидом, обладающим активностью токсина, в частности с факторами, ассоциированными с вирулентностью NE, предлагаемыми в изобретении.
Следующим объектом настоящего изобретения является композиция, которая содержит полинуклеотид, полипептид, вектор, клетку или антитело, предлагаемые в изобретении.
Следующим объектом настоящего изобретения является диагностический набор, который содержит полинуклеотид или антитело, предлагаемый/предлагаемое в изобретении. Набор может дополнительно содержать устройство с захватывающей поверхностью, которое можно применять для отделения микровезикул из биологического образца от нежелательных частиц, дебриса и малых молекул, что более подробно будет описано ниже. Набор может включать также инструкции по его применению, в частности по применению компонентов для оптимального выделения и лизиса микровезикул и последующего качественного или количественного определения присутствия по меньшей мере одного из маркеров, предлагаемых в изобретении.
Следующим объектом настоящего изобретения является иммуногенная композиция, которая содержит полипептид, предлагаемый в изобретении, и предпочтительно адъювант и/или фармацевтически приемлемый носитель.
Следующим объектом настоящего изобретения является вакцина, которая содержит полипептид, предлагаемый в изобретении, и адъювант и/или фармацевтически приемлемый носитель.
Микровезикулы, предлагаемые в изобретении, содержат мембранные везикулы из бактерий, в частности из Clostridium perfringens, а также из хозяина, в частности кур.
Эукариотическую версию мембранных везикул называют также экзосомами. Экзосомы, как правило, имеют диаметр 30-200 нм. Они выделяются во все биологические жидкости и несут большое количество интактных белков и олигонуклеотидов, поскольку они защищены от расщепления РНКазами (Koga и др., 2011).
Экзосомы изучены прежде всего в раковых и иммунных клетках.
Микровезикулы из бактерий называют также внеклеточными мембранными везикулами (MV) или везикулами наружной мембраны (OMV). Они имеют сферические бислойные структуры со средним диаметром 20-500 нм. Бактериальные микровезикулы впервые описаны для грамотрицательных бактерий, но позднее также и для грамположительных бактерий. В современном исследовании установлено, что микровезикулы продуцируются и высвобождают также штаммами С.perfringens типа А, запуская врожденный и адаптивный иммунные ответы. Далее в процессе указанного исследования установлено, что важные факторы вирулентности типа альфа-токсина и NetB, не присутствовали в мембранных везикулах, в то время как бета2-токсин обнаружен в мембранных везикулах (Jiang и др., (2014).
МикроРНК (миРНК) представляют собой малые некодирующие РНК, которые, как правило, состоят из 18-23 нуклеотидов и, как предполагается, играют решающую роль в регуляции экспрессии генов. В частности установлено, что гены, ассоциированные с иммунными ответами, являются основными мишенями миРНК. У кур экспрессия миРНК изучена в процессе развития эмбрионов, развитии зародышевых клеток, в органах иммунной системы и при болезнях.
В современных исследованиях изучен профиль миРНК в двух различных чистых куриных инбредных линиях белых Леггорнов, зараженных С.perfringens (Dinh и др., 2014; Hong и др., 2014). Анализ РНК осуществляли с использованием ткани из селезенки и слизистой кишечника. Результаты позволили предположить, что некоторые миРНК по-разному изменялись в ответ на заражение некротическим энтеритом, и что они модулировали экспрессию их генов-мишеней. В этих опытах не изучали микровезикулы.
Корреляция миРНК с некротическим энтеритом, установленная при создании настоящего изобретения, ранее была изучена Wang с соавторами в связи с анализом заражения бройлеров вирусом птичьего гриппа (Wang и др., 2012). Wang с соавторами установили, что уровень экспрессии миРНК miR-155, miR-16-1 и miR-24 был выше в легких инфицированных бройлеров, чем в легких неинфицированных бройлеров, но было установлено также, что для miR-206, наоборот, характерен более высокий уровень экспрессии в неинфицированных легких, чем в инфицированных. Таким образом, применение miR-206 в качестве маркера бактериальной инфекции в настоящем изобретении описано впервые. Кроме того, в отличие от результатов, полученных Wang с соавторами, в настоящем изобретении все миРНК обнаружены в микровезикулах, но не в ткани.
Таким образом, следующим объектом настоящего изобретения является способ обнаружения бактериальной инфекции птиц, в частности некротического энтерита птиц, где способ включает выделение микровезикул из образца из организма птиц и последующее определение уровня по меньшей мере одного маркера из организма птиц, служащего признаком инфекции, в котором повышенный уровень указанного по меньшей мере одного маркера из организма птиц по сравнению с незараженным контролем служит признаком инфекции и в котором по меньшей мере один маркер из организма птиц представляет собой птичью миРНК и предпочтительно его выбирают из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
д) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(г);
е) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (д);
ж) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(е).
В этом способе последовательности предпочтительно выбирают из следующей группы:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
б) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
в) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
г) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
д) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(г);
е) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (д);
ж) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(е).
Поскольку впервые удалось идентифицировать mir-206 в качестве маркера инфекции птиц, в целом, то дополнительным объектом настоящего изобретения является способ обнаружения инфекции птиц, предпочтительной бактериальной инфекции птиц, более предпочтительно некротического энтерита птиц, в котором повышенный уровень по меньшей мере одного маркера из организма птиц по сравнению с незараженным контролем служит признаком инфекции и в котором по меньшей мере один маркер из организма птиц выбирают из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60 последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13,
б) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (а);
в) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а) или (б).
В этом способе последовательности предпочтительно выбирают из следующей группы:
а) полинуклеотиды, которые имеют последовательность, идентичную по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100%, полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13,
б) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (а);
в) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а) или (б).
Вариантами применения способов, предлагаемых в изобретении, являются, например, (I) диагностирование и/или прогнозирование некротического энтерита птиц, (II) мониторинг развития или рецидива некротического энтерита птиц или (III) оценка эффективности лечения птиц, подвергающихся лечению или у которых предполагают лечить некротический энтерит; в которых определяют присутствие или отсутствие одного или нескольких указанных выше биомаркеров в экстракте нуклеиновых кислот, полученном согласно способу, и устанавливают ассоциацию одного или нескольких биомаркеров с диагнозом, развитием или рецидивом или эффективностью лечения соответственно некротического энтерита.
Варианты применения согласно изобретению позволяют, в частности, избегать снижения характеристик продуктивности птиц, таких как прирост массы и превращение (трансформация) корма.
Выделение микровезикул
Выделение микровезикул из биологического образца до экстракции нуклеиновых кислот является целесообразным, поскольку для содержащих нуклеиновые кислоты микровезикул характерны более высокие выходы видов нуклеиновых кислот с повышенной целостностью по сравнению с выходом/целостностью, получаемыми при экстракции нуклеиновых кислот непосредственно из жидкого образца или экскрементов без предварительного выделения микровезикул. Кроме того, можно также обнаруживать нуклеиновые кислоты, которые имеют низкие уровни экспрессии. Выделение микровезикул позволяет также исключать белки, липиды, клеточный дебрис, клетки и другие потенциально загрязняющие вещества и ингибиторы ПЦР, которые встречаются в естественных условиях с биологических образцах.
Выделение мембранных везикул из биологических образцов и последующую экстракцию нуклеиновых кислот можно осуществлять, например, с помощью ультрацентрифугирования, например, путем вращения при более чем 10000 g в течение 1-3 ч, с последующим удалением супернатанта, промывкой дебриса, лизисом дебриса и очисткой нуклеиновых кислот на колонке. Альтернативными методами являются ультрафильтрация, например, с использованием фильтров с верхней границей отсекаемой молекулярной массы 100 кДа, методы на основе осаждения полимером и/или фильтрации на основе размера.
Другими альтернативными методами являются дифференциальное центрифугирование, описанное у Raposo и др., 1996), Skog и др., 2008 и Nilsson и др., 2009; ионообменная и/или гель-проникающая хроматография, описанная в US №№6899863 и 6812023; электрофорез в градиентах плотности сахарозы или органелл, описанный в US №7198923; активируемая магнитным полем сортировка клеток (MACS), описанная у Taylor и Gercel-Taylor, 2008; ультрафильтрация через наномембраны, описанная у Cheruvanky и др., 2007; выделение в градиенте перколла, описанное у Miranda и др., 2010; и выделение с помощью микрофлюидного устройства, описанного у Chen и др., 2010.
Выделение микровезикул на основе применения захватывающей поверхности описано в WO 2014/107571.
В предпочтительном варианте осуществления изобретения микровезикулярная фракция связывается с захватывающей поверхностью, в частности с мембраной, фильтром или с гранулой с модифицированной поверхностью, как описано в WO 2014/107571.
Биологический образец предпочтительно растворяют в загрузочном буфере, который предпочтительно имеет рН 4-8, более предпочтительно 5-7. Таким образом, связывание с захватывающей поверхностью предпочтительно имеет место при рН 4-8, более предпочтительно 5-7. Предпочтительно после приведения в контакт биологического образца с захватывающей поверхностью осуществляют одну или несколько стадий промывки.
Загрузочные и промывочные буферы, которые можно применять согласно изобретению, могут иметь высокую или низкую ионную силу. Таким образом, концентрация соли, например, концентрация NaCl, может составлять от 0 до 2,4М. Предпочтительно буферы включают один или несколько из следующих компонентов: Трис, Бис-Трис, Бис-Трис-пропан, имидазол, цитррат, метилмолоновую кислоту, уксусную кислоту, этаноламин, диэтаноламин, триэтаноламин (ТЭА) и фосфат натрия.
Промывку предпочтительно осуществляют с использованием промывочного буфера, содержащего 250 мМ Бис-Трис-пропан и характеризующегося величиной рН 6,5-7,0.
Путем добавления детергентов к промывочному буферу подавляют неспецифическое связывание. Детергенты, пригодные для применения, включают (но, не ограничиваясь только ими) додецилсульфат натрия (ДСН), Твин-20, Твин-80, Тритон Х-100, Нонидет Р-40 (NP-40), Бридж-35, Бридж-58, октилглюкозид, октилтиоглюкозид, CHAPS или CHAPSO.
После промывки захватывающей поверхности нуклеиновую кислоту можно высвобождать путем лизиса фиксированных микровезикул. Для лизиса фиксированных микровезикул предпочтительно применяют лизирующий буфер на основе фенола, типа лизирующего реагента QIAzol® (фирма Qiagen, Германия). Затем можно осуществлять очистку нуклеиновой кислоты путем экстракции хлороформом с использованием PLG-пробирок с последующим кондиционированием этанолом. Затем нуклеиновую кислоту можно связывать с колонкой с силикагелем перед промывкой и элюцией.
Лизис микровезикул и экстракцию нуклеиновых кислот можно осуществлять также с использованием поступающего в продажу набора Qiagen R easy Plus, поступающего в продажу набора Qiagen miR или с использованием фенолхлороформа согласно стандартным процедурам и методикам, известным в данной области. В таких методах можно применять также связывающую нуклеиновую кислоту колонку для захвата содержащихся в микровезикулах нуклеиновых кислот. После связывания нуклеиновые кислоты затем можно элюировать, используя буфер или раствор, пригодный для нарушения взаимодействия между нуклеиновыми кислотами и связывающей колонкой.
Методы экстракции нуклеиновых кислот включают также применение дополнительных агентов типа ингибитора РНКазы, такого как Superase-In (поступает в продажу от фирмы Ambion Inc.) или RNaselNplus (поступает в продажу от Promega Corp.); протеазы (которая может функционировать также в качестве ингибитора РНКазы); ДНКазы; восстановителя; субстанции-ловушки, такой как синтетическая РНК и/или РНК-носитель; растворимого рецептора, который может связываться с РНКазой; малой интерферирующей РНК (siPHK); РНК-связывающей молекулы, такой как антитело к РНК, основного белка или белка-шаперона; денатурирующей РНКазу субстанции, такой как высокоосмолярный раствор, детергент или их комбинация.
Ингибиторы РНКазы, а также другие агенты можно добавлять в биологический образец и/или к выделенной фракции микровезикул перед экстракцией нуклеиновых кислот.
Указанные дополнительные агенты могут проявлять их функции различными путями, например, посредством ингибирования активности РНКазы (например, ингибиторы РНКазы), посредством повсеместного расщепления белков (например, протеазы) или посредством белка-шаперона (например, РНК-связывающего белка), который связывается и защищает РНК. Во всех случаях такая экстракция повышает удаление агентов или по меньшей мере уменьшает некоторые или все нежелательные факторы в биологическом образце или ассоциированные с выделенными частицами, которые в противном случае могут препятствовать или влиять на высококачественную экстракцию нуклеиновых кислот из выделенных частиц.
Для определения качества экстракции нуклеиновых кислот можно определять количество экстрагированных 18S и 28S рРНК.
Захватывающая поверхность может быть нейтральной, отрицательно заряженной или положительно заряженной. Это означает, что в принципе можно использовать любой вид захватывающей поверхности. В зависимости от материала мембраны размер пор мембраны может составлять от 20 нм до 5 мкм.
В частности, захватывающая поверхность может представлять собой поступающую в продажу мембрану типа ионообменной мембраны Mustang® фирмы PALL Corporation; Vivapure® Q, Vivapure® Q Maxi H; Sartobind® D, Sartobind (S), Sartobind® Q, Sartobind® IDA или Sartobind®-альдегид фирмы Sartorius AG; Whatman® DE81 фирмы Sigma; колонку для очистки вирусов Fast Trap фирмы EMD Millipore; или сильные катионо- и анионообменные вращающиеся колонки Thermo Scientific* Pierce.
Когда мембрану применяют для фиксации нуклеиновых кислот, то мембрана может быть изготовлена из различных приемлемых материалов, например, она может быть из полиэфирсульфона (ПЭС) (например, от фирмы Millipore или PALL Corp.) или из регенерированной целлюлозы (РЦ) (например, от фирмы Sartorius или Pierce).
Когда применяют отрицательно заряженную мембрану, то захватывающая поверхность предпочтительно представляет собой S-мембрану, которая представляет собой отрицательно заряженную мембрану и является катионообменником с группами сульфоновой кислоты. Предпочтительно S-мембрана функционализирована сульфоновой кислотой, R-CH2-SO3''. Альтернативно этому, отрицательно заряженная захватывающая поверхность представляет собой D-мембрану, которая представляет собой слабый основный анионообменник с диэтиламиновыми группами, R-CH2-NFT(C2H5)2. Альтернативно этому, захватывающая поверхность представляет собой металл-хелатную мембрану. Например, мембрана представляет собой IDA-мембрану, функционализированную иминодиуксусной кислотой -N(CH2COOH'')2. В некоторых вариантах осуществления изобретения захватывающая поверхность представляет собой микропористую мембрану, функционализированную альдегидными группами, -СНО. В других вариантах осуществления изобретения мембрана представляет собой слабый основный анионообменник с диэтиламиноэтил (ДЭАЭ)-целлюлозой.
Когда применяют нейтральную захватывающую поверхность, то захватывающая поверхность предпочтительно представляет собой фильтр, выбранный из группы, которая состоит из шприцевого фильтра с 20-нанометровым нейтральным ПЭС (фирма Tisch and Exomir), шприцевого фильтра с 30-нанометровым нейтральным ПЭС (фирма Sterlitech), шприцевого фильтра с 50-нанометровым нейтральным ПЭС (фирма Sterlitech), самодельной вращающейся фильтрационной колонки с 0,2-микрометровым нейтральным ПЭС (фирма Pall), самодельной вращающейся фильтрационной колонки с 0,8-микрометровым нейтральным ПЭС (фирма Pall). В вариантах осуществления изобретения, в которых захватывающая поверхность является нейтральной, предпочтительно нейтральная захватывающая поверхность не находится в шприцевом фильтре.
Заряженную поверхность предпочтительно выбирают из группы, которая состоит из 0,65-микрометровой положительно заряженной Q ПЭС-мембраны для вакуумной фильтрации из, 3-5-микрометровой положительно заряженной Q РЦ-мембраны для вращающейся фильтрационной колонки, 0,8-микрометровой положительно заряженной Q ПЭС-мембраны для самодельной вращающейся фильтрационной колонки, 0,8-микрометровой положительно заряженной Q ПЭС-мембраны для шприцевого фильтра, 0,8-микрометровой отрицательно заряженной S ПЭС-мембраны для самодельной вращающейся фильтрационной колонки, 0,8-микрометровой отрицательно заряженной S ПЭС-мембраны для шприцевого фильтра и 50-нанометровой отрицательно заряженного мембраны из нейлона для шприцевого фильтра.
В предпочтительном варианте осуществления изобретения, когда поверхность представляет собой положительно заряженную мембрану, можно использовать Q-мембрану, которая представляет собой положительно заряженную мембрану и является анионообменником с четвертичными аминами. В предпочтительном варианте осуществления изобретения Q-мембрана функционализирована четвертичным аммонием, R-СН2-N+(СН3)3.
В наиболее предпочтительном варианте осуществления изобретения положительно заряженная мембрана представляет собой регенерированную целлюлозу, мембрану, представляющую собой сильный основный анионообменник («РЦ/SBAE»), которая является анионообменником с четвертичными аминами. В предпочтительном варианте осуществления изобретения PU/SBAE-мембрана функционализирована четвертичным аммонием, R-СН2-N+(СН3)3. Размер пор мембраны предпочтительно составляет по меньшей мере 3 мкм.
Захватывающая поверхность, например мембрана, может находиться внутри устройства, применяемого для центрифугирования, например, во вращающихся колонках, или для вакуумного применения, например, в держателях вакуумного фильтра, или для фильтрации под давлением, например, в шприцевом фильтре.
В процессе очистки на основе вращающейся колонки предпочтительно параллельно в пробирке применяют более 1 мембраны, предпочтительно 2-5 мембран, при этом мембраны предпочтительно все находятся в непосредственной близости друг к другу на одном конце колонки. Пробирка для сбора может представлять собой поступающую в продажу пробирку, например, 50-миллилтровую фальконовскую пробирку. Колонку предпочтительно можно вращать, т.е. ее размер соответствует стандартной центрифуге и микроцентрифуге.
Вместо мембраны для захвата нуклеиновой кислоты можно применять также гранулу с такой же модификацией поверхности. Если применяют гранулу, то она может быть магнитной или немагнитной.
Если в качестве образца применяют кровь, то кровь можно собирать, например, в K2-ЭДТА-пробирки и хорошо смешивать путем полных переворачиваний. Затем пробирки центрифугируют при 1300×g в течение 10 мин для разделения клеток крови и плазмы. Затем плазму удаляют и фильтруют через 0,8-мкметровый фильтр для удаления клеточного дебриса и тромбоцитов. Затем все образцы плазмы разделяют на аликвоты, помещая их в 1-миллилитровые криофлаконы, и хранят при -80°С до использования.
Перед выделением РНК мембрану предпочтительно кондиционируют, пропуская уравновешивающий буфер. После оттаивания образцы плазмы разводят загрузочным буфером. Разведенный образец плазмы медленно пропускают через мембрану, которая адсорбирует микровезикулы. Затем мембрану промывают промывочным буфером для удаления любых слабо связанных компонентов плазмы. Затем лизирующий реагент пропускают через мембрану для лизиса микровезикул. РНК выделяют, используя набор miRNeasy (фирма Qiagen).
РНК можно оценивать в отношении качества и определять концентрацию с помощью биоанализатора 2100 (фирма Agilent), используя Pico-чип РНК 6000. Относительное количество экстрагированной РНК измеряют с помощью ОТ-qПЦР, используя выбранный анализ экспрессии человеческих генов фирмы Applied Biosystems (Taqman-анализ).
В предпочтительных вариантах осуществления изобретения, в частности, когда применяют солюбилизированные образцы фекалий или цекального помета, осуществляют предварительную стадию обработки до выделения, очистки или обогащения микровезикул для удаления крупных нежелательных частиц, клеток и/или клеточного дебриса и других загрязнителей, которые присутствуют в биологическом образце. Стадии предварительной обработки могут включать одну или несколько стадий центрифугирования (например, дифференциальное центрифугирование) или одну или несколько стадий фильтрации (например, ультрафильтрацию), или их комбинации. Когда осуществляют более одной стадии центрифугирования в качестве предварительной обработки, то биологический образец можно центрифугировать сначала при низкой скорости, а затем при более высокой скорости. При необходимости можно осуществлять дополнительные приемлемые стадии центрифугирования в качестве предварительной обработки. Альтернативно этому или в дополнение к одной или нескольким стадия центрифугирования в качестве предварительной обработки можно осуществлять фильтрацию биологического образца. Например, биологический образец можно сначала центрифугировать при низкой скорости примерно 100-500 g, предпочтительно 250-300 g, а затем при более высокой скорости от примерно 2000 g до примерно 200000 g, предпочтительно примерно 20000 g, в течение периода времени, составляющего от 10 мин до примерно 1 ч, предпочтительно при температуре 0-10°С, для удаления крупных нежелательных частиц; затем образец можно фильтровать, например, используя фильтр, исключающий частицы размером от 0,1 до 1,0 мкм.
Микровезикулы в дебрисе, полученном путем центрифугирования при высокой скорости, можно восстанавливать с использованием меньшего объема приемлемого буфера для осуществления последующих стадий процесса. Стадию концентрирования можно осуществлять также путем ультрафильтрации. Фактически указанная ультрафильтрация как концентрирует биологический образец, так и обеспечивает дополнительную очистку микровезирулярной фракции. В другом варианте осуществления изобретения фильтрация представляет собой ультрафильтрацию, предпочтительно тангенциальную ультрафильтрацию. Тангенциальная ультрафильтрация состоит в концентрировании и фракционировании раствора между двумя компартментами (фильтрат и ретентат), разделенными мембранами с определенными верхними границами отсекаемой молекулярной массы. Разделение осуществляют, используя поток в компартменте ретентата и трансмембранное давление между этим компартментом и компартментном фильтрата. Различные системы можно использовать для осуществления ультрафильтрации, такие как спиральные мембраны (фирмы Millipore, Amicon), плоские мембраны или полые волокна (фирмы Amicon, Millipore, Sartorius, Pall, GF, Sepracor). Согласно изобретению целесообразно применять мембраны с верхней границей отсекаемой молекулярной массы менее 1000 кДа, предпочтительно от 100 до 1000 кДа, еще более предпочтительно от 100 до 600 кДа.
В качестве дополнительных или альтернативных стадий процесса предварительной обработки можно осуществлять стадии гель-фильтрации, гель-проникающей хроматографии или аффинной хроматографии до или после приведения в контакт биологического образца с захватывающей поверхностью.
Для осуществления стадии гель-проникающей хроматографии предпочтительно используют подложку, выбранную из силикагеля, акриламида, агарозы, декстрана, сополимера этиленгликоля-метакрилата или их смесей, например, смесей агароза-декстран. Например, такие подложки включают (но, не ограничиваясь только ими): SUPERDEX® 200HR (фирма Pharmacia), TSK G6000 (фирма TosoHaas) или SEPHACRYL® S (фирма Pharmacia).
Аффинную хроматографию можно осуществлять, например, с использованием различных подложек, смол, гранул, антител, аптамеров, аналогов аптамеров, полимеров с молекулярными отпечатками или других молекул, известных в данной области, специфической мишенью которых являются требуемые поверхностные молекулы на микровезикулах.
Необязательно в образец до выделения микровезикул или экстракции нуклеиновых кислот можно добавлять контрольные частицы, которые служат внутренним контролем для оценки эффективности или качества очистки микровезикул и/или экстракции нуклеиновых кислот. Эти контрольные частицы включают бактериофаг Q-бета, вирусные частицы или любую другую частицу, которая содержит контрольные нуклеиновые кислоты (например, по меньшей мере один контрольный ген-мишень), которые могут представлять собой встречающиеся в естественных условиях или созданные методами рекомбинантной ДНК. Контрольный ген-мишень можно оценивать количественно с помощью ПЦР-анализа в реальном времени.
Предпочтительно контрольная частица представляет собой бактериофаг Q-бета, который в контексте настоящего описания обозначен как «частица Q-бета». Частица Q-бета может представлять собой встречающуюся в естественных условиях вирусную частицу или может представлять собой рекомбинантный или сконструированный вирус, в котором по меньшей мере один компонент вирусной частицы (например, часть генома или оболочечного белка) синтезирован с помощью рекомбинантной ДНК или методов молекулярной биологии, известных в данной области. Q-бета является представителем семейства Leviviridae, для которого характерен геном из линейной одноцепочечной РНК, который состоит из трех генов, кодирующих четыре вирусных белка: оболочечный белок, белок, участвующий в созревании, лизирующий белок и РНК-репликазу. Из-за их размера, сходного со средним размером микровезикул, Q-бета можно легко очищать из биологического образца с использованием таких же методов очистки, которые представлены в настоящем описании для выделения микровезикул. Кроме того, небольшая сложность структуры одноцепочечного гена вируса Q-бета является предпочтительной для его применения в качестве контроля в анализах, основанных на оценке амплификации нуклеиновых кислот. Частица Q-бета содержит контрольный ген-мишень или контрольную последовательность-мишень, предназначенную для обнаружения или измерения количества частиц Q-бета в образце. Например, контрольный ген-мишень представляет собой ген оболочечного белка Q-бета. После добавления частиц Q-бета в биологический образец нуклеиновые кислоты из частицы Q-бета экстрагируют наряду с нуклеиновыми кислотами из биологического образца с использованием методов экстракции и/или наборов, указанных в настоящем описании. Обнаружение контрольного гена-мишени Q-бета можно осуществлять с помощью ОТ-ПЦР-анализа, например, одновременно с представляющими интерес биомаркерами (т.е. BRAF). Для определения числа копий можно применять стандартную кривую, построенную с использованием по меньшей мере 2, 3 или 4 известных концентраций, полученных 10-кратным разведением контрольного гена-мишени.
Число обнаруженных копий и количество добавленных частиц Q-бета можно сравнивать для оценки качества процесса выделения и/или экстракции.
Так, в образец общей воды добавляют 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 1000 или 5000 копий частиц Q-бета. В предпочтительном варианте осуществления изобретения в образец общей воды добавляют 100 копий частиц Q-бета. Число копий частиц Q-бета можно рассчитывать на основе способности бактериофага Q-бета инфицировать клетки-мишени. Так, число копий частиц Q-бета коррелирует с колониеобразующими единицами бактериофага Q-бета.
Обнаружение нуклеиновых кислот-биомаркеров
Для обнаружения РНК предпочтительно осуществляют обратную транскрипцию РНК с образованием комплементарной ДНК (кДНК) перед дополнительной амплификацией. Указанную обратную транскрипцию можно осуществлять индивидуально или в сочетании со стадией амплификации. Одним из примеров метода, в котором объединены стадии обратной транскрипции и амплификации, является полимерная цепная реакция с обратной транскрипцией (ОТ-ПЦР), которую можно дополнительно модифицировать для того, чтобы она стала количественным методом, например, количественной ОТ-ПЦР, описанной в US №5639606. Другой пример метода включает две стадии: первая стадия обратной транскрипции для превращения РНК в кДНК, и вторая стадия определения количества кДНК с использованием количественной ПЦР.
ОТ-ПЦР анализ позволяет определять значение Ct (граничное значение порогового цикла) для каждой реакции. В ОТ-ПЦР положительную реакцию определяют по накапливанию флуоресцентного сигнала. Значение Ct определяют как количество циклов, требуемое для пересечения флуоресцентным сигналом порога (т.е., превышение фонового уровня). Уровни Ct обратно пропорциональны уровню нуклеиновой кислоты-мишени или контрольной нуклеиновой кислоты в образце (т.е. чем ниже уровень Ct, тем большее количество контрольной нуклеиновой кислоты присутствует в образце). Альтернативно этому, число копий контрольной нуклеиновой кислоты можно измерять, используя другие известные в данной области методики.
Анализ нуклеиновых кислот, присутствующих в выделенных частицах, является количественным и/или качественным. Для количественного анализа измеряют с помощью методов, известных в данной области, либо относительные, либо абсолютные количества (уровни экспрессии) конкретных представляющих интерес нуклеиновых кислот в выделенных частицах. Для качественного анализа виды конкретных представляющих интерес нуклеиновых кислот в выделенных микровезикулах идентифицируют с помощью методов, известных в данной области.
Рабочие примеры
Приготовления инокулята
Выделяли изолят Clostridium perfringens, позитивный по netB и tpeL, после хранения при -80°С и в асептических условиях наносили штрихами на планшеты с триптиказо-соевым агаром, содержащим 5% овечьей крови (TSA II). Планшеты инкубировали при 37°С в течение ночи в анаэробных условиях. За 15 часов до начала культивирования инокулята выделенной колонией из инкубированного в течение ночи планшета инокулировали 50 мл предварительно редуцированный BHI-бульон и инкубировали при 37°С в анаэробных условиях в течение примерно 15 ч. Затем 50 мкл культуры добавляли в 2×100 мл предварительно редуцированного BHI-бульона. Полученные культуральные бульоны распределяли так, чтобы высокая доза и низкая доза достигали их конечных концентраций одновременно (109 КОЕ /мл и 106 КОЕ/мл соответственно). В конце периода роста отбирали аликвоты каждой культуры и серийно высевали на TSA II агар +5% овечьей крови для верификации концентрации бактерий.
Эксперимент на животных
Семьсот двадцать (720) самцов бройлеров выращивании в 36 батарейных секциях в течение 30 дней. Птиц поровну и произвольным образом включали (по 9 секций) в одну из четырех групп обработки (отрицательный контроль, имитатор, принудительное оральное кормление низкой дозой и принудительное оральное кормление высокой дозой). Птицам давали стандартный кукурузный/соевый корм без антимикробных средств. На 13-ый день выращивания птиц с высоким или низким весом удаляли из всех секций и исключали из эксперимента. Затем птиц с весом в нормальных пределах подвергали контрольному заражению, вводя орально 1 мл штамма С.perfringens, несущего содержащую netB плазмиду и являющегося позитивным по гену Tpel, последовательно в дни 14,15 и 16. Группу-имитатор подвергали контрольному заражению 1 мл ЗФР, а группу, используемую в качестве отрицательного контроля, не подвергали никакому стрессу или контрольному заражению патогеном. Перед первой инокуляцией (день 14), произвольно отбирали по 3 птицы из каждой секции, умерщвляли для сбора образцов крови и содержимого желудка. Через 12 ч после второго контрольного заражения в день 15 вновь умерщвляли по 3 птицы из каждой секции для получения образцов крови и содержимого желудка. Содержимое пищеварительной системы всех умерщвленных птиц культивировали в течение ночи для определения соотношения спорулирующих С.perfringens и вегетативных клеток согласно описанному ранее методу (Heikinheimo и др., 2004). Для решения вопроса о том, являлось ли контрольное заражение успешным, осуществляли ПЦР для определения генов NetB и TpeL в содержимом пищеварительной системы. По меньшей мере 10 птиц оставляли в каждой секции до конца опыта. Собирали образцы экскретов с определенными интервалами вплоть до окончания опыта в день 20, когда всех птиц умерщвляли и из каждой группы получали по три пула образцов крови. В желудочно-кишечном тракте птиц (ЖКТ) оценивали типичные для NE признаки/повреждения и осуществляли аутопсии желудочно-кишечного тракта для получения образцов двенадцатиперстной и тощей кишки для гистопатологических анализов. Определяли показатели продуктивности бройлеров типа уровня смертности, потребления корма и групповые патологии (таблица 3).
Сбор образцов
1. Сбор образцов фекалий и цекальных экскретов
В секции помещали полоски бумаги для сбора объединенных образцов фекалий и объединенных образцов цекального помета через каждые 2 ч после первого контрольного заражения вплоть до 12 ч после второй инокуляции (день 15). Затем образцы собирали каждые 4 ч вплоть до дня 17. В конце опыта в день 20 также собирали образы фекалий и цекального помета. В процессе любого случая сбора на секцию получали по меньшей мере 1 г фекалий и цекального помета и образцы хранили при -80°С.
2. Сбор крови
Кровь собирали непосредственно из сердца, используя иглу 18 размера. Примерно 5-6 мл цельной крови получали из 3 произвольно обобранных птиц на секцию в пробирку для сбора, содержащую ЭДТА. Клетки удаляли из плазмы центрифугированием в течение 10 мин при 1000-2000×g, используя рефрижераторную центрифугу. После центрифугирования жидкий компонент (плазму) немедленно переносили в чистую полипропиленовую пробирку и хранили при -20°С.
3. Сбор содержимого пищеварительной системы
Содержимое пищеварительной системы получали из кишечника длиной примерно 20 см. Содержимое пищеварительной системы извлекали и измельчали в ЗФР + 20% глицерина и немедленно замораживали при -20°С. Затем образцы применяли для количественного определения вегетативных С.perfringens относительно спорулирующих С.perfringens и определения с помощью ПЦР netB и tpeL.
Гистология кишечника кур
1. Сбор и обработка ткани
У каждой птицы удаляли сегмент размером 5 см за петлей двенадцатиперстной кишки и помещали в 10% формалина и контейнер осторожно перемешивали для вытеснения корма, давая формалину проникнуть в кишку. После фиксации ткани хорошо промывали в нескольких сменах забуференного фосфатом физиологического раствора (ЗФР) и помещали в 70%-ный этанол для хранения. Для обработки тканей и заливки тканей парафином перед получением среза толщиной 5 мкм ткани обезвоживали путем 1-кратной промывки в течение 2 мин последовательно в 70% и 95% растворах этанола, а затем 2-кратной промывки в течение 2 мин в 100% растворе этанола. И, наконец, ткани промывали 2-кратно в течение 1 мин в ксилоле перед погружением в парафин. Затем обработанную ткань ориентировали в шаблоне, погруженном в парафиновый блок, и нарезали микротомом с получением срезов толщиной 5 мкм. Срезы ткани помещали на поверхность модифицированных поли-L-лизином (PLL) предметных стекол Срезы сушили и помещали в сушилку для «спекания» парафина.
2. Окрашивание срезов ткани гемотоксилином Гарриса и эозином
В целом, метод состоял в следующем: срезы повторно гидратировали путем последовательного снижения концентрации этанола: 2-кратно в течение 3 мин каждый раз в 100% этаноле, 2-кратно в течение 3 мин каждый раз в 95%-ном растворе этанола и 1-кратно в течение 3 мин в 70%-ном растворе этанола. Затем предметные стекла промывали в течение 5 мин в дистиллированной воде и затем окрашивали в течение 6 мин раствором гематоксилина (гематоксилин Гарриса, фирма Sigma, HHS-32). Предметные стекла промывали в проточной водопроводной воде в течение примерно 20 мин и обесцвечивали в кислом растворе спирта (95% этанола, 2578 мл dH2О, 950 мл НСl, 9 мл) в течение 1-3 с. Предметные стекла вновь промывали в проточной водопроводной воде в течение 5 мин и затем погружали в карбонат лития на 3 с и затем вновь промывали водопроводной водой в течение 5 мин. Ткани подвергали контрастному окрашиванию с использованием рабочего раствора эозина (100 мл маточного раствора эозина (1% водного эозина Y и 1% водного флоксина В), 10 мл маточного раствора флоксина В, 780 мл 95% этанола, 4 мл ледяной уксусной кислоты) в течение 15 с и повторно гидратировали путем последовательной инкубации в растворах этанола (2-кратно в течение 3 мин каждый раз в 95%-ном растворе этанола и 2-кратно в течение 3 мин каждый раз в 100%-ном растворе этанола). И, наконец, ткани инкубировали в растворе ксилола в течение 5 мин и затем монтировали в устройстве Cytoseal для анализа.
Обнаружение генов netB и tpeL Clostridium perfinzens с помощью ПЦР

1.Экстракция ДНК и определение концентрации ДНК
Экстракцию ДНК из штаммов С.perfringens, выделенных из содержимого кишечника, осуществляли с помощью поступающих в продажу наборов для экстракции ДНК фирмы Qiagen, Гильден, Германия согласно инструкции производителя.
2. Амплификация ДНК
ПЦР-амплификацию осуществляли в конечном объеме 25 мкл, содержащем 1 нг ДНК-матрицы, 0,2 мкМ каждый из праймеров подлежащего амплификации или обнаружению гена и 12 мкл 1 × ПЦР-мастер смеси, включающей 1,2 ед./25 мкл ДНК-полимеразы Taq. Амплификацию осуществляли в ПЦР-системе для амплификации генов в термоциклере 9600 (Мастер-циклер фирмы Эппендорф, Германия). Начальную денатурацию осуществляли при 95°С в течение 5 мин, после чего осуществляли 40 циклов при 95°С в течение 30 с, отжиг при 55°С в течение 30 с и удлинение при 72°С в течение 30 с, конечное удлинение при 72°С в течение 7 мин и выдерживали при 40°С.
Обработка образцов
В целом, обрабатывали 36 образцов плазмы, 96 образцов фекалий и 87 образцов цекального помета для выделения и экстракции из микровезикул всей РНК. Объемы плазмы варьировались от 0,5 до 3 мл для различных животных.
Получение плазмы
В целом, метод состоял в следующем: кровь собирали в К2-ЭДТА-пробирки и смешивали путем полных переворачиваний. Затем пробирки центрифугировали при 1300×g в течение 10 мин для разделения клеток крови и плазмы. Затем плазму удаляли и фильтровали через 0,8-мкметровый фильтр для удаления клеточного дебриса и тромбоцитов. Затем все образцы плазмы разделяли на аликвоты в 1-миллилитровые криофлаконы и хранили при -80°С до использования.
Выделение микровезикул и экстракция РНК
Известные из существующего уровня методы экстракции микровезикул и дополнительной очистки содержимого микровезикул (MV) из биоматериалов, таких как кровь, СМЖ, ткани и культуры клеток, описаны ранее в US 6899863 В1 (Dhellin и др., 2005), ЕР 2495 25 Al, WO 2014107571 А и 2014/0178885А1. Методы включают применение высокоскоростного ультрацентрифугирования или применение низкоскоростного центрифугирования для отделения клеточного дебриса, после чего осуществляли гель-фильтрацию или аффинное связывание со специфическими мембранами или фильтрацию (см. обзор Witwer и Colleagues, 2013). Описано также несколько иммунологических методов очистки микровезикул (Thery и др., 2016; Clayton и др., 2001; Wubbolts и др., 2003). Микровезикулы можно очищать с использованием матриксов, гранул или магнитных частиц, функционализированных антителами, которые связываются с поверхностными белками микровезикул, для положительной селекции требуемой популяции, или антителами, которые связываются с поверхностными белками других клеточной компонентов, для их истощения (Kim и др. и др., 2012 и Mathivanan и др., 2010). Быстрые методы выделения микровезикул, доступные для исследований, включают применение микрофлюидных устройств (Chen и др., 2010; ЕР 2740536 А2) и поступающих в продажу наборов (например, SeraMir™ (фирма System Biosciences), ExoSpin™ (фирма Cell Guidance), ExoMir™ (фирма Bioo Scientiflcs), miRCURY™ (фирма Exiqon), для которых требуется минимальное лабораторное оборудование или не требуется вообще.
При создании настоящего изобретения экстракцию микровезикул из образцов плазмы, фекалий и цекального помета осуществляли методами, описанными в WO 2014/107571 A1 (Enderle и др., 2014). Метод включает выделение микровезикул из биологической жидкости путем их захвата на поверхности Q-функционализированнного мембранного фильтра (Ехо50, фирма Exosome Diagnostics). Содержащуюся в захваченных микровезикулах РНК высвобождали путем лизиса реагентом Qiazol, а затем РНК очищали экстракцией хлороформом или с помощью поступающего в продажу набора RNAesay фирмы Qiagen. В целом, метод состоял в следующем: образцу плазмы давали медленно оттаивать на льду и разводили в соотношении 1:1 ЗФР или 0,9% NaOH; раствор плазмы центрифугировали при 300 g в течение 10 мин для удаления клеток и дебриса. Супернатант пропускали через 0,8-мкметровый фильтр и проточную фракцию центрифугировали при 20000 g при 4°С в течение 30 мин для удаления любого оставшегося клеточного дебриса. Колонку Ехо50 с аффинной мембраной, которая связывает микровезикулы, предварительно кондиционировали, путем пропускания через нее 5 мл загрузочного буфера (2×) 100 мМ фосфатный буфер, 370 мМ NaCl). Затем в содержащий микровезикулы супернатант, полученный после второй стадии центрифугирования, впрыскивали 1000 копий частиц Q-бета для оценки эффективности экстракции и выделения после загрузки на предварительно кондиционированную вращающуюся колонку. Колонку кратковременно вращали и проточную фракцию отбрасывали. Колонку промывали дважды 2 мл промывочного буфера (250 мМ Бис-Трис-пропан, рН 6,5-7 и (1×) 50 мМ фосфатный буфер, 185 мМ NaCl) и после второй стадии промывки колонку кратковременно вращали и проточную фракцию отбрасывали. Микровезикулы, связанные с мембраной, лизировали для высвобождения содержимого путем добавления 5 мл (2,25 мл) лизирующего буфера (реагент Qiazol) и вращали для сбора лизата. РНК экстрагировали из лизата с помощью набора Rneasy (фирма Qiagen) согласно инструкции производителя. РНК, элюированную с помощью свободной от РНКазы воды, объединяли для взятых с дублированием образцов с получением общего объема каждого образца 46 мкл. 1 мкл РНК анализировали с помощью набора Agilent RNA 6000 Nano для оценки качества и определения концентрации РНК, а оставшуюся РНК хранили при -80°С для дополнительного последующего применения (q-ПЦР или секвенирование). Эффективность экстракции и количество экстрагированной РНК определяли путем сравнения экспрессии контрольного гена-мишени Q-бета (ген оболочечного белка Q-бета) в экстрагированной РНК с помощью ОТ-ПЦР-анализа с экспрессией представляющих интерес генов-мишеней. Для определения числа копий использовали стандартную кривую, построенную для контрольного гена-мишени по меньшей мере по 2, 3 или 4 известным концентрациям, полученным 10-кратным разведением. Выявленное число копий и количество добавленных частиц Q-бета сравнивали для определения качества процесса выделения и/или экстракции.
Образцы фекалий и цекального помета
Поскольку образцы фекалий и цекального помета содержат большое количество грубых материалов, осуществляли дополнительные стадии предварительной обработки перед выделением микровезикул и экстракции РНК с использованием набора Ехо50 и соответствующих методов, которые описаны выше для образцов плазмы. Например, 200 мг образца фекалий давали медленно оттаивать; затем добавляли 1 мл холодного ЗФР или 0,9% стерильного NaOH для гомогенизации образца фекалий/цекального помета с последующим интенсивным перемешиванием в течение примерно 1 мин. Образовавшуюся суспензию разводили в соотношении 1:1 ЗФР и затем центрифугировали при 20000×g в течение 30 мин при 4°С для удаления крупных нежелательных частиц. Супернатант фильтровали, пропуская через 0,8-микрометровый фильтра из смешанных сложных эфиров целлюлозы (например, фильтр фирмы Millipore) и фильтрат хранили при 4°С для дальнейшего применения или обрабатывали согласно методу, описанному выше для образца плазмы.
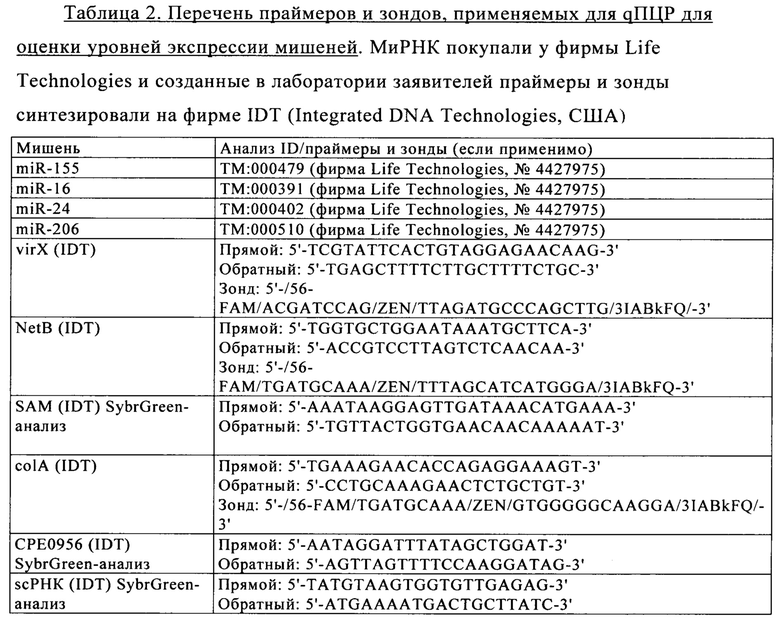
qOT-ПЦР РНК, полученной из фекалий/цекального помета Обратную транскрипцию РНК фекалий и цекального помета осуществляли с помощью набора для синтеза кДНК Superscript VILO согласно инструкциям производителя и со следующими модификациями: смесь для ОТ-реакции содержала 11 мкл (5× реакционная смесь VILO), 5,5 мкл (10× смесь ферментов SS), 5,5 мкл (свободная от нуклеазы Н2О) и 33 мкл (РНК). При этом профиль ОТ-цикла состоял из 4 последовательных циклов инкубации/выдерживания при 25° в течение 10 мин, 42° в течение 60 мин, 85° в течение 5 мин и конечной стадии выдерживания при 4°С.
qOT-ПЦР миРНК, полученной из плазмы и фекалий/цекального помета Обратную транскрипцию миРНК осуществляли в трех повторностях, используя набор для обратной транскрипции РНК TaqMan MicroRNA со следующим составом мастер-смеси для ОТ и профиля циклов: смесь для ОТ-реакции содержала 6 мкл (пул праймеров для ОТ), 0,3 мкл (дНТФ, 100 мМ), 1,5 мкл (10× ОТ-буфер), 0,2 мкл ингибитора РНКазы, 3,0 мкл ОТ MultiScribe и 4 мкл (4 мкл РНК образцов фекалий и цекального помета и 2 мкл РНК + 2 мкл ТЕ-буфера для образцов плазмы). При этом профиль ОТ-цикла состоял из 4 последовательных циклов инкубации/выдерживания при 16° в течение 30 мин, 42° в течение 30 мин, 85° в течение 5 мин и конечной стадии выдерживания при 4°С. Пул праймеров для ОТ получали путем объединения по 10 мкл каждого ОТ-праймера и разведения до 1 мл с помощью ТЕ-буфера, с получением конечной концентрации каждого ОТ-праймера 0,05 х. К соответствующему пулу ОТ-праймеров добавляли (5х) соответствующую миРНК для анализа (miR-16, miR-21, miR-24, miR-155 и miR-206).
qПЦР РНК фекалий/цекального помета
Осуществляли цПЦР в анализе на основе зондов генов РНК с использованием набора Qiagen Rotor -Gene Q согласно инструкции производителя. Температура отжига в анализах virX, colA и netB составляла 57°С, в то время как температура отжига в анализах 16s рРНК Clostridium perfringens составляла 60°С.Реакционные мастер-смеси для анализов состояли из 5,5 мкл (свободная от нуклеазы вода), 10 мкл (универсальной мастер-смеси для ПЦР TaqMan Fast без AmpErase UNG), 0,5 мкл прямого праймера (20 мкМ), 1,5 мкл обратного праймера (20 мкМ), 0,25 мкл зонда (20 мкМ), 0,25 мкл UNG (урацил-N-гликозилаза) и 2 мкл кДНК. Для амплификации 16s РНК применяли по 1 мкл и прямого, и обратного праймера.
Анализ с использованием набора для ПЦР Rotor-Gene SYBR Green осуществляли для малой некодирующей РНК VR-PHK, e45nt и scPHK. Реакционные мастер-смеси для анализов состояли из 5,75 мкл (свободная от нуклеазы вода), 10 мкл (Rotor Gene SYBR 2× мастер-смесь), 0,5 мкл прямого праймара (20 мкМ), 1,5 мкл обратного праймера (20 мкМ), 0,25 мкл зонда (20 мкМ), 0,25 мкл (урацил-N-гликозилаза) и 2 мкл кДНК. Амплификацию осуществляли в следующих условиях: первая стадия выдерживания при 50°С в течение 2 мин, затем другая стадия выдерживания при 95°С в течение 10, а затем 40 циклов, включающих 95°С в течение 2 с, 60°С в течение 15 с, 72°С в течение 20 с.
Статистический анализ
Все статистические расчеты проводили с использованием программного обеспечения для статистического анализа R. Вследствие стехиометрии анализа и общей эффективности протоколов анализа перед осуществлением стандартизации проводили замену отсутствующих величин (отсутствие сигнала) на 40, что представляет собой наиболее высокое значение СТ в цПЦР с 40 циклами амплификации. Осредненные статистические данные для парного сравнения групп обработки рассчитывали с использованием функции ImFit, имеющейся в пакете программ limma (limma: линейные модели для данных, полученных с использованием микромассивов (linear models for microarray data), Smyth G.K. B: Bioinformatics and Computational Biology Solutions using R and Bioconductor, изд-во Springer, New York, cc. 397-420, пакет программ R, версия 2.16.5), и рассчитанные величины р корректировали согласно методу Benjamini и Hochberg (1995) с получением величин q (ожидаемая доля ложный отклонений) Мультивариантный анализ (дисперсионный анализ, ANOVA) Зависимости между временем, обработкой и типом образца оценивали качественно. Формальную количественную оценку возможных ассоциаций осуществляли с помощью двустороннего дисперсионного анализа и непараметрических критериев Крускала-Уоллиса. Оба метода применяли независимо для обработки данных, касающихся миРНК и бактериальной РНК. Двусторонний дисперсионный анализ применяли для оценки двух основных факторов и их взаимодействия. Первый основной фактор представлял собой время после обработки (в часах), второй основной фактор представлял собой тип обработки (контроль, имитатор, высокая доза, низкая доза). Критерий Крускала-Уоллиса применяли отдельно к времени и типу обработки для оценки ассоциации этих факторов с экспрессией генов. С помощью этого метода не оценивали многовариантное взаимодействие. Три типа образцов (цекальный помет, экскрет и плазма) анализировали в отношении 4 миРНК (miR-16, miR-24, miR-155 и miR-206), и для этого анализа оказалось возможным использовать в целом 216 полученных с дублированием данных. Кроме того, анализировали шесть бактериальных генов-мишеней в двух типах образцов (цекальный помет и экскрет) и для этого анализа оказалось возможным использовать в целом 108 полученных с дублированием данных. Средние величины полученных с дублированием данных (средне значения Ct каждого образца) применяли для дополнительных статистических анализов. Анализ осуществляли как для необработанных данных, так и для стандартизованных данных. MiR-191 применяли в качестве нормализатора для анализа микроРНК, а значения Ct 16S рРНК С.perfringens применяли в качестве нормализатора для бактериальных мишеней. Линейная модель дисперсионного анализа (Anova (Im(экспрессия ~ время + обработка + время * обработка)) позволяла получать р-значения для трех факторов (время-действие, обработка-действие, взаимодействие) для стандартизованных и необработанных данныха, а 2 р-значения (время-действие и обработка-действие) получали с помощью критерия Крускала-Уоллиса для стандартизованных и необработанных данных.
Результаты:
Таблица 3. Количество мертвых птиц на группу после контрольного заражения С.perfringens. Одна птица погибла в каждой из групп:
: оральная обработка низкой дозой, группа-имитатор и группа, представляющая собой отрицательный контроль. 4 птицы погибли в группе, обработанной высокой дозой Clostridium perfringens.
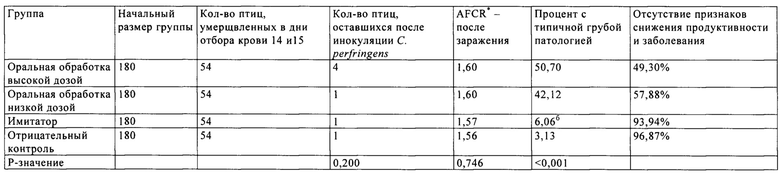
* AFCR (скорректированный коэффициент превращения корма), который определяли как количество потребленного корма, деленное на вес тела птиц, скорректированное с учетом смертности и удаления птиц из-за отклонения их веса птиц от веса птиц до контрольного заражения

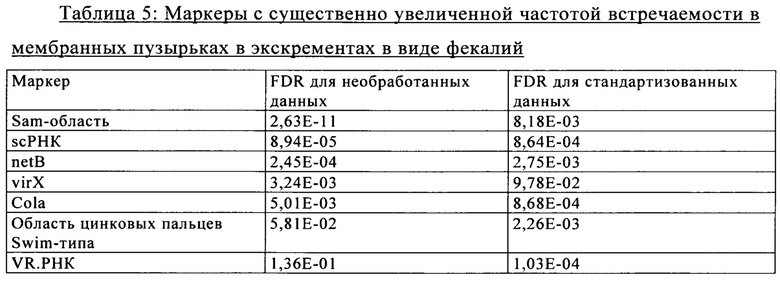

Перечень ссылок
1. Thery С, Amigorena S., Raposo G., Clayton A., Isolation and characterization of exosomes from cell culture supernatants and biological fluids. Curr Protoc Cell Biol., часть 3: unit 3.22, 2006.
2. Clayton A., Court J., Navabi H., Adams M., Mason M.D., Hobot J.А. и др., Analysis of antigen presenting cell derived exosomes, based on immuno-magnetic isolation and flow cytometry. J Immunol. Methods; 247, 2001, cc. 163-74.
3. Wubbolts R., Leckie R.S., Veenhuizen P.Т., Schwarzmann G., Mobius W., Hoernschemeyer J. и др., Proteomic and biochemical analyses of human В cell-derived exosomes. Potential implications for their function and multivesicular body formation. J Biol Chem., 278, 2003, cc. 10963-10972.
4. Kim G., Yoo C.E., Kim M., Kang H.J., Park D., Lee M. и др., Noble polymeric surface conjugated with zwitterionic moieties and antibodies for the isolation of exosomes from human serum. Bioconjug. Chem., 23, 2012, cc. 2114-2120.
5. Mathivanan S., Lim J.W., Tauro B.J., Ji H., Moritz R.L., Simpson R.J., Proteomics analysis of A33 immunoaffinity-purified exosomes released from the human colon tumor cell line LIM1215 reveals a tissue-specific protein signature. Mol. Cell. Proteomics, 9, 2010, cc. 197-208.
6. Smyth G.K., linear models for microarray data In: Bioinformatics and Computational Biology Solutions using R and Bioconductor, изд-во Springer, New York, 2004, cc. 397-420.
7. Hochberg и Roy, Controlling the false discovery rate: a practical and powerful approach to multiple testing. Journal of the Royal Statistical Soc. Ser В (Methodological), 57, 1995, cc. 289-300.
8. Heikinheimo А. и  M. и Korkeala H., Enumeration and Isolation of cpe-Positive Clostridium perfringens Spores from Feces. Journal of Clinical Microbiology, 42, 9, 2004, cc. 3992-3997.
M. и Korkeala H., Enumeration and Isolation of cpe-Positive Clostridium perfringens Spores from Feces. Journal of Clinical Microbiology, 42, 9, 2004, cc. 3992-3997.
9. Dinh H. и др., Modulation of microRNAs in two genetically disparate chicken lines showing different necrotic enteritis disease susceptibility. Vet. Immunol. Immunopathol., http://dx.doi.Org/10.1016/j.vetimm.2014.02.003.
10. Aade U.P., Wankhede H.J. и Kaldate K.D., Haematological parameters change in Gallus gallus domesticus infected with cestode parasite. International Multidisciplinary Research Journal, 2(4), 2012, cc. 13-15.
11. Chuku L.C. и др., A comparison of the haematological and biochemical indices of broiler and red jungle (hamburgh) fowl (gallus gallus domesticus), Discovery Nature, 2012, 1(1), 2012, cc. 15-18.
12. Wang и др., Integrated analysis of microRNA expression and mRNA transcriptome in lungs of avian influenza virus infected broilers BMC Genomics 2012, 13, 2012, c. 278.
13. Jiang и др., Membrane vesicles of Clostridium perfringens type A strains induceinnate and adaptive immunity. International Journal of Medical Microbiology 304, 2014, cc. 431-443.
14. Obana и др., Structural Requirement in Clostridium perfringens Collagenase mRNA 5'Leader Sequence for Translational Induction through Small RNA-mRNA Base Pairing Journal of Bacteriology, т.195, №12, 2013, cc. 2937-2946.
15. Ohtani и др., Identification of a novel locus that regulates expression of toxin genes in Clostridium perfringens FEMS Microbiology Letters, 209, 2002, cc. 113-118.
16. Nakamura и др., Small cytoplasmic RNA (scRNA) gene from Clostridium perfringens can replace the gene for the Bacillus subtilis scRNA in both growth and sporulation Microbiology, 141, 1995, cc. 2965-2975.
17. KEYBURN и др., Association between avian necrotic enteritis and Clostridium perfringens strains expressing NetB toxin Vet. Res. 41, 2010, c. 21.
18. Shojadoost и др., The successful experimental induction of necrotic enteritis in chickens by Clostridium perfringens: a critical review Veterinary Research, 43, 2012, c. 74.
19. Koga и др., Exosome can prevent RNase from degrading microRNA in feces. J Gastrointest Oncol; 2, 2011, cc. 215-222.
20. Saleem Gulbeena, Identification of biochemical markers for sub-clinical necrotic enteritis in broiler chickens (In Necrotic enteritis, disease induction, predisposing factors and novel biochemical markers in broilers chickens), глава 8, диссертация PhD, University of Glasgow, UK, 2013.
21. Garcia и др., Experimental infection of commercial layers using a Salmonella enterica serovar Gallinarum strain: Leukogram and serum acute-phase protein concentrations. Revista
Brasileira de  11, 2009, cc. 263-270.
11, 2009, cc. 263-270.
22. Piercy, Acute phase responses to experimental salmonellosis in calves and colibacillosis in chickens: serum iron and caeruloplasmin. Journal of Comparative Pathology 89, 1979, cc. 309-319.
23. Witwer и др., Standardization of sample collection, isolation and analysis methods in extracellular vesicle research Journal of Extracellular Vesicles, 2, 2013, c. 20360.
24. Nilsson и др., Prostate cancer-derived urine exosomes: a novel approach tobiomarkers for prostate cancer. Br J Cancer, 100, 2009, cc. 1603-160.
25. Li и др., Claudin-containing exosomes in the peripheral circulation of women with ovarian cancer. BMC Cancer, 9, 2009, c. 244.
26. Shao и др., Protein typing of circulating microvesicles allows real time monitoring of glioblastoma therapy. Nat Med., 18, 2012, cc. 1835-1840.
27. Taylor и Gercel-Taylor Taylor, MicroRNA signatures of tumor-derived exosomes as diagnostic biomarkers of ovarian cancer Gynecologic Oncology, 110, 2008, cc. 13-21.
28. Cheruvanky и др., Rapid isolation of urinary exosomal biomarkers using a nanomembrane concentrator. Am J Physiol Renal Physiol., 292, 2007, cc. 1657-1661.
29. Miranda и др., Nucleic acids within urinary exosomes/ microvesicles are potential biomarkers for renal disease. Kidney Int., 78, 2010, cc. 191-199.
30. Chen и др., Microfluidic isolation and transcriptome analysis of serum microvesicles. Lab Chip., 10, 2010, cc. 505-511.
31. Skog и др., Glioblastoma microvesicles transport RNA and proteins that promote tumour growth and provide diagnostic biomarkers. Nat Cell Biol., 10, 2008, cc. 1470-1476.
32. Moore и др., Clostridium toxin netB (WO 2008/148166), 2008.
33. Dhellin и др., Method for preparing membrane vesicles (US 6899863 B1), 2005.
34. Lamparski и др., Method of producing membrane vesicles (US 6812023 B1), 2004.
35. Abrignani и др., Method for the preparation of purified HCV RNA by exosome separation (US 7198923 B1), 2007.
36. Giorgio, Filter for the removal of micro-vesicles from biological fluids, methods anddevices using such a filter (EP 2495025 A1), 2012.
37. Enderle и др., methods for isolating microvesicles (WO 2014/107571), 2014.
38. Kyung-Hee и др., Composition and kit for diagnosing breast cancer including polynucleotide within vesicle, and method of diagnosing breast cancer using the same (US 2014/0178885 A1), 2014.
39. Min Soak и Jong-Myeon, Microfluidic apparatus and method of enriching target material in biological sample by using the same (EP 2740536 A2), 2014.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ ЗАБОЛЕВАНИЙ, ВЫЗЫВАЕМЫХ C. PERFRINGENS, У ЖИВОТНЫХ | 2018 |
|
RU2769503C2 |
| СПОСОБ РАННЕГО ВЫЯВЛЕНИЯ ВСПЫШКИ НЕКРОТИЧЕСКОГО ЭНТЕРИТА В ПОПУЛЯЦИИ ПТИЦ | 2019 |
|
RU2771793C1 |
| НИТРИЛГИДРАТАЗА ИЗ Rhodococcus | 2005 |
|
RU2385932C2 |
| КЛОСТРИДИАЛЬНЫЙ ТОКСИН NetB | 2008 |
|
RU2474587C2 |
| ВАКЦИНА ПРОТИВ НЕКРОТИЧЕСКОГО ЭНТЕРИТА У ДОМАШНЕЙ ПТИЦЫ | 2018 |
|
RU2788096C2 |
| ПЕПТИДЫ RUMC, ОБЛАДАЮЩИЕ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2464274C2 |
| РАСТЕНИЯ, УСТОЙЧИВЫЕ К НАСЕКОМЫМ-ВРЕДИТЕЛЯМ | 2012 |
|
RU2671143C2 |
| ПОДАВЛЕНИЕ ЭКСПРЕССИИ ГЕНОВ У НАСЕКОМЫХ-ВРЕДИТЕЛЕЙ | 2012 |
|
RU2665549C1 |
| ПОДАВЛЕНИЕ ЭКСПРЕССИИ ГЕНОВ У НАСЕКОМЫХ-ВРЕДИТЕЛЕЙ | 2012 |
|
RU2619219C2 |
| РАСТЕНИЯ, УСТОЙЧИВЫЕ К НАСЕКОМЫМ-ВРЕДИТЕЛЯМ | 2012 |
|
RU2691697C2 |
Изобретение относится к биотехнологии, в частности описан основанный на применении микровезикул способ обнаружения некротического энтерита птиц, а также новые маркеры, которые идентифицированы в качестве приемлемых для обнаружения некротического энтерита птиц и/или заражения птиц Clostridium perfringens. 9 н. и 3 з.п. ф-лы, 6 табл., 1 пр.
1. Способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где способ включает выделение микровезикул из образца из организма птиц и последующее определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком некротического энтерита, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором образец из организма птиц представляет собой общую воду организма, предпочтительно кровь, в частности плазму крови или сыворотку крови, или экскремент организма, предпочтительно экскремент в виде фекалий или цекального помета, и в котором маркер выбран из следующих последовательностей:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 16;
и) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
к) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
л) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
м) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
н) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(м);
о) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (н);
п) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(о).
2. Способ по п. 1, в котором обнаружение некротического энтерита осуществляют посредством обнаружения по меньшей мере одной из следующих последовательностей:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 630, в частности от 420 до 630, SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 600 до 1000, в частности от 670 до 760, SEQ ID NO: 3;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 60 до 240, в частности от 80 до 220, SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1300 до 1800, в частности от 1400 до 1700, SEQ ID-NO: 5;
д) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 1 до 591, в частности от 100 до 280, SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 240 до 540, в частности от 300 до 540, SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 12 до 418, в частности от 240 до 400, SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 673 до 5628 SEQ ID NO: 16;
и) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 14 до 25 SEQ ID NO: 10;
к) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 44 до 65 SEQ ID NO: 11;
л) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 3 до 24 SEQ ID NO: 12;
м) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18 или 20, последовательно расположенных нуклеотидов нуклеотидной последовательности, простирающейся от положения 45 до 66 SEQ ID NO: 13;
н) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(м);
о) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (н);
п) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(о).
3. Способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где обнаружение некротического энтерита осуществляют посредством обнаружения присутствия и/или определения количества по меньшей мере одной из следующих последовательностей в образце из организма птиц, в которых образец из организма птиц представляет собой общую воду организма, предпочтительно кровь, в частности плазму крови или сыворотку крови, или экскремент организма, предпочтительно экскремент в виде фекалий или цекального помета:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
д) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
е) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
ж) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
з) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
и) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(и);
л) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (к);
м) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(л).
4. Способ обнаружения бактериальной инфекции птиц, предпочтительно некротического энтерита птиц, в частности, доклинического некротического энтерита, где способ включает выделение микровезикул из образца из организма птиц и последующее определение присутствия и/или уровня по меньшей мере одного маркера из организма птиц, служащего признаком инфекции, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера из организма птиц по сравнению с незараженным контролем служит признаком инфекции, и в котором образец из организма птиц представляет собой общую воду организма, предпочтительно кровь, в частности плазму крови или сыворотку крови, или экскремент организма, предпочтительно экскремент в виде фекалий или цекального помета, и в котором по меньшей мере один маркер из организма птиц представляет собой птичью миРНК и его предпочтительно выбирают из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
д) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(г);
е) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (д);
ж) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(е).
5. Способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где способ включает определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком некротического энтерита птиц, в экскрементах птиц в виде фекалий, предпочтительно в микровезикулах, выделенных из экскрементов птиц в виде фекалий, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер предпочтительно выбирают из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
з) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(ж);
и) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (з);
к) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(и).
6. Способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где способ включает определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком некротического энтерита птиц, в экскрементах птиц в виде цекального помета, в частности, в микровезикулах, выделенных из экскрементов птиц в виде цекального помета, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер предпочтительно выбирают из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 4;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 5;
д) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 8;
ж) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 9;
з) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 13;
и) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(з);
к) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (и);
л) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(к).
7. Способ обнаружения некротического энтерита птиц, в частности, доклинического некротического энтерита птиц, где способ включает определение присутствия и/или уровня по меньшей мере одного маркера, служащего признаком некротического энтерита птиц, в крови птиц, предпочтительно в микровезикулах, выделенных из крови птиц, в котором присутствие и/или повышенный уровень указанного по меньшей мере одного маркера по сравнению с незараженным контролем служит признаком некротического энтерита, и в котором маркер предпочтительно выбирают из группы, состоящей из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40, 60 или 80, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 10;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 11;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 8 или 10, предпочтительно по меньшей мере 12, 14, 16, 18, 20, 25, 40 или 60, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 12;
г) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(в);
д) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпункте (г);
е) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(д).
8. Способ по одному из предыдущих пунктов, в котором образец из организма птиц представляет собой образец из организма домашней птицы, предпочтительно образец из организма кур, индюков, уток, гусей, павлинов, фазанов, серых куропаток, цесарок, перепелов, глухарей, шотландских куропаток, голубей, лебедей, страусов и попугаев, наиболее предпочтительно кур.
9. Способ лечения, включающий осуществление способа по одному из предыдущих пунктов и введение терапевтического агента, предназначенного для лечения заражения некротическим энтеритом.
10. Полинуклеотид, который представляет собой праймер ПЦР или биомаркер некротического энтерита птиц, выбран из группы, которая состоит из следующих полинуклеотидов:
а) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
б) полинуклеотиды, которые имеют последовательность, по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 1;
в) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
г) полинуклеотиды, которые имеют последовательность, по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 3;
д) полинуклеотиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 100, предпочтительно по меньшей мере 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
е) полинуклеотиды, которые имеют последовательность, по меньшей мере на 90%, предпочтительно по меньшей мере на 95, 98 или 99%, наиболее предпочтительно на 100% идентичную полинуклеотиду, который содержит по меньшей мере 20, предпочтительно по меньшей мере 25, 40, 60, 100, 150, 180 или 200, последовательно расположенных нуклеотидов нуклеотидной последовательности, которая представлена в SEQ ID NO: 7;
ж) полинуклеотиды (ДНК и РНК), которые комплементарны последовательностям, указанным в подпунктах (а)-(е);
з) полинуклеотиды, которые содержат полинуклеотиды, указанные в подпунктах (а)-(ж).
11. Вектор для экспрессии полипептида, который является фактором вирулентности, вовлеченным в некротический энтерит птиц, содержащий полинуклеотид по п. 10.
12. Полипептид, который представляет собой фактор вирулентности, вовлеченный в некротический энтерит птиц, выбран из группы, которая состоит из:
а) полипептиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 200, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 2;
б) полипептиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60 или 70, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 14;
в) полипептиды, которые имеют последовательность, по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90 или 95%, наиболее предпочтительно на 100% идентичную полипептиду, который содержит по меньшей мере 10, предпочтительно по меньшей мере 15, 20, 25, 40, 60, 100, 150, 180 или 190, в частности все, последовательно расположенные аминокислоты аминокислотной последовательности, которая представлена в SEQ ID NO: 15;
полипептиды, которые содержат полипептиды, указанные в подпунктах (а)-(в).
| M.T.McCourt ET AL, Sandwich ELISA detection of Clostridium perfringens cells and α-toxin from field cases of necrotic enteritis of poultry, Veterinary Microbiology, Volume 106, Issues 3-4, 10 April 2005, Pages 259-264 | |||
| HAN SANG YOO ET AL, Molecular Typing and Epidemiological Survey of Prevalence of Clostridium perfringens Types by Multiplex PCR, |
Авторы
Даты
2020-01-29—Публикация
2016-02-19—Подача