ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение раскрывает жидкий ферментный препарат и способ его получения, в частности, относится к жидкому препарату трансглутаминазы (EC2.3,2,13) и способу его получения, где жидкий препарат может храниться при комнатной температуре, являясь стабильным по свойствам, с ферментативной активностью, поддерживаемой на уровне выше 80%. Настоящее изобретение принадлежит к области ферментных препаратов и области пищевых добавок.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0002] Глутаминтрансаминаза (EC,2.3,2,13, полное название: Амин-γ-глутамил-трансфераза, сокращенно именуемая трансглутаминаза, с аббревиатурой ТГ) представляет собой сшивающий белковый фермент, который может катализировать образование изопептидной связи ε-(γ-глутамил)лизина в белковой молекуле или молекулах между белками посредством использования ε-аминогруппы лизина в пептидной цепи белка в качестве акцептора ацила, улучшать свойства белка, такие как эмульгируемость, реологические характеристики, растворимость и вспениваемость, придавать белокспецифичные характеристики строения и адгезивности и улучшать цвет, аромат и вкус продуктов, и имеет, таким образом, большое промышленное значение.
[0003] Трансглутаминаза была впервые выделена из печени морской свинки Clarke et al. В 1989 году Ando et al. из Amano Pharmaceutical Co., Ltd. (Япония) изобрел способ микробиологической ферментации для получения трансглутаминазы. В 1997 году Ajinomoto Co., Inc. (Япония) осуществила производство трансглутаминазы в промышленном масштабе. В 2001 году трансглутаминаза была официально одобрена в Китае для применения в качестве пищевой добавки. В настоящее время основным производителем ферментов в мире является Ajinomoto Co., Inc. (Япония), продукт трансглутаминазы которой имеет торговое наименование Acvita. Основными производителем в Китае являются Shanghai Kinry Food Ingredients Co., Ltd., Kinry Biotech (Жинань) Co., Ltd., Taixing Dongsheng Bio-Tech Co., Ltd., Taixing Yiming Biological Product Co. Ltd., Henan Yangshao Bio-products Co., Ltd. и т.д. Их продуктами являются ферментные препараты в форме твердого порошка, причем Shanghai Kinry Food Ingredients Co., Ltd. является первой компанией, применившей вакуумную упаковку. Ajinomoto Co., Inc. (Japan) в настоящее время использует упаковку с заполнением азотом для порошковых продуктов.
[0004] Несмотря на то, препараты трансглутаминазы в виде порошков производят в крупном масштабе и широко применяют в пищевой промышленности в настоящее время, еще существует множество проблем, связанных с их производством, транспортировкой, хранением и применением.
1) Себестоимость: во время призводства трансглутаминазы сначала получают жидкую ферментационную среду, которая требует нескольких стадий обработки во время ее очистки, таких как осаждение, сушка и измельчение; вследствие усложненных процессов себестоимость увеличивается.
2) Обеспечение безопасности: препараты трансглутаминазы в виде порошков легко диспергируются во время получения и применения, состояние окружающей среды в цехе ухудшается, и оборудование трудно чистить. Рабочее место наполнено пылью, с которой трудно бороться и от которой трудно защищаться. При вдыхании ферментного порошка в организм человека он вызывает сильную анафилактическую ответную реакцию и серьезно повреждает органы дыхательных путей операторов, у которых могут появляться такие симптомы, как высокая температура, пневмония и шок, и, следовательно, он является очень вредным для здоровья операторов. До настоящего времени случаи возникновения симптомов аллергии, вызываемых трансглутаминазой, таких как кашель и лихорадка, происходили на фабриках множество раз.
3) Проблемы упаковки: вакуумную упаковку применяют для порошковых ферментных препаратов трансглутаминазы. Однако порошок легко попадает в оборудование при вакуумировании, что приводит к значительным потерям. Если упаковка ферментного препарата неплотно герметизирована и происходит пропускание воздуха, препарат будет увлажняться, агломерироваться со снижением ферментативной активности. Если применяют упаковку с заполнением азотом, операция заполнения азотом является трудоемкой и приводит к возникновению пыли, и себестоимость значительно увеличивается.
4) В отношении применения: хорошо известно, что трансглутаминаза может работать только будучи растворенной в воде. Вследствие вторичного растворения порошкового препарата во время его получения и применения продолжительность работы фермента значительно снижается. Кроме того, неполное растворение часто возникает после добавления воды, в то время как непосредственное добавление порошка просто приводит к неравномерному распределению. Кроме того, когда применяют устройство для выполнения операции прокатки и разглаживания, порошок легко прилипает к устройству, снижая степень использования порошковых препаратов, и оказывает отрицательное воздействие на применение. Следовательно, количество порошкового препарата трансглутаминазы должно увеличиваться.
5) Направление развития ферментных препаратов: в области биологических ферментных препаратов и различных областях промышленности различные виды ферментных препаратов уже являются доступными в жидких дозированных формах, причем проблемы хранения, транспортировки и применения разрешены, и их производство и применение осуществляют экономно и экологически безопасно, например, жидкая целлюлаза (Патентная публикация №: CN103981168A, CN101381716), жидкая фитаза (Патентная публикация №: CN101617740), жидкая пектиназа (Патентная публикация №: CN104531653A), жидкая липаза (Патентная публикация № CN103525797A). Однако во всем мире жидкие препараты трансглутаминазы, которые могут храниться при комнатной температуре в течение долгого времени, еще не являются доступными для приобретения.
[0005] Патентная публикация № CN104024406A предоставляет способ получения жидкого ферментного препарата трансглутаминазы. Однако, поскольку способ позволяет достичь хранения только при низкой температуре в течение до 180 дней, а хранение и транспортировка продукта должны осуществляться в условиях замораживания, промышленное применение способа было ограниченным, и до сих пор конечные продукты способа отсутствуют. Разработка жидкого ферментного препарата трансглутаминазы, который является стабильным при комнатной температуре (25°C, также как далее), сейчас стало проблемой, которая в настоящее время нуждается в срочном решении в пищевой промышленности.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0006] Одной целью настоящего изобретения является предоставление жидкого препарата трансглутаминазы (EC2.3.2.13), который может храниться при комнатной температуре в течение 6 месяцев и поддерживает ферментативную активность свыше 80%.
[0007] Еще одной целью настоящего изобретения является предоставить способ получения жидкого препарата трансглутаминазы (EC2.3.2.13), где жидкий препарат трансглутаминазы, полученный посредством указанного способа, имеет хорошую стабильность, может храниться при комнатной температуре в течение 6 месяцев и поддерживает ферментативную активность свыше 80%.
[0008] Настоящее изобретение в первую очередь решает техническую проблему, касающуюся трудности хранения жидких препаратов трансглутаминазы при комнатной температуре, чтобы жидкие препараты трансглутаминазы могли соответствовать требованиям, предъявляемым при промышленном производстве и применении.
[0009] Чтобы достичь указанных выше целей, технические растворы настоящего изобретения сначала необходимо иллюстрировать экспериментально и теоретически, и затем подвести итоги. Подробности являются следующими:
Первоначально, при исследовании воздействий физико-химических факторов, таких как pH, водная активность и окислительно-восстановительный потенциал, на степень консервации ферментативной активности (стабильности) раствора трансглутаминазы при комнатной температуре, определяли оптимальный интервал рН, водную активность и интервал окислительно-восстановительного потенциала для стабильного хранения трансглутаминазы при комнатной температуре.
[0010] 1. Стабильность растворов трансглутаминазы при различных значениях рН
К концентрированным ферментным растворам добавляли хлористоводородную кислоту и гидроксид натрия для получения растворов трансглутаминазы при различных значениях рН. После стерилизующей фильтрации растворы трансглутаминазы содержали при комнатной температуре в течение 2 дней, чтобы оценить их ферментативную активность (стабильность). Результаты показаны в Таблице 1.
Таблица 1. Изменения ферментативных активностей очищенных концентрированных ферментных растворов при различных pH
активность через 2 дня, Ед/мл
Данные в Таблице 1 показывают, что, когда трансглутаминазу содержали при pH 5,0-9,0, очищенные ферментные растворы имели степень консервации ферментативной активности выше 80%, в то же время, когда трансглутаминазу содержали при pH выше 9,0 или ниже 4,0, ферментативная активность быстро снижалась. Следовательно, ферментный раствор может храниться при pH 5,0-9,0, а предпочтительный pH составляет 5,0-7,5.
[0011] 2. Стабильность растворов трансглутаминазы при различных водных активностях
Регулятор рН применяли для регуляции pH очищенного ферментного раствора сначала до рН 6,0, и ферментный раствор разбавляли регулирующим буфером до 1000 Ед/мл. К 10 мл разбавленного ферментного раствора добавляли глицерин в различных количествах (Таблица 2), и полученные в результате растворы разбавляли буфером до объема 100 мл. После стерилизующей фильтрации получали жидкие ферментные препараты с различными водными активностями. После содержания при комнатной температуре в течение 10 дней оценивали стабильность жидких ферментных препаратов, и результаты показаны в Таблице 2.
Таблица 2. Ферментативная активность (стабильность) очищенных концентрированных ферментных растворов при различных водных активностях
активность после регулирования, Ед/мл
активность через 10 дней, Ед/мл
Данные в Таблице 2 показывают, что добавление регулятора водной активности может увеличить стабильность жидкого препарата трансглутаминазы при комнатной температуре. Когда водная активность составляет ниже 0,89, степень консервации ферментативной активности достигает значения свыше 85% в день 10, а когда водная активность составляет ниже 0,85, степень консервации ферментативной активности достигает 92%. Однако дополнительное снижение водной активности имеет небольшое воздействие на степень консервации ферментативной активности. Следовательно, хорошая степень консервации может быть получена, когда водная активность будет ниже 0,89. Однако, с точки зрения затрат на сырье, предпочтительная водная активность находится в интервале 0,60-0,85.
[0012] 3. Стабильность растворов трансглутаминазы при комнатной температуре при различных условиях окислительно-восстановительного потенциала
Регулятор рН добавляли для регуляции pH очищенного концентрированного ферментного раствора до 6,0, а затем окислительно-восстановительные потенциалы ферментного раствора регулировали до различных значений с использованием регуляторов окислительно-восстановительного потенциала, боргидрида натрия и пероксида водорода. После стерилизующей фильтрации ферментный раствор содержали при комнатной температуре в течение 30, 60 и 90 дней и определяли ферментативные активности и степени консервации образцов ферментных растворов. Результаты показаны в Таблице 3.
Таблица 3. Ферментативные активности и степени консервации жидких препаратов трансглутаминазы при различных окислительно-восстановительных потенциалах
(Ед/мл)
активность
(Ед/мл)
консервации, %
активность
(Ед/мл)
консервации, %
активность
.
(Ед/мл)
консервации, %
Данные в Таблице 3 показывают, что окислительно-восстановительный потенциал обладает значительным воздействием на стабильность жидкого препарата трансглутаминазы. Когда окислительно-восстановительный потенциал находится в интервале от -400 мВ до 50 мВ, степень консервации через 30 дней составляет свыше 80% при комнатной температуре. Когда окислительно-восстановительный потенциал жидкого ферментного препарата составляет ниже 50 мВ, степень консервации ферментативной активности значительно увеличивается. Когда потенциал находится между -400 мВ и 0 мВ, степень консервации достигает свыше 80% через 90 дней. Предпочтительный потенциал для жидкого ферментного препарата находится между -400 мВ и 0 мВ.
[0013] Во-вторых, регуляторы рН, регуляторы водной активности и регуляторы окислительно-восстановительного потенциала оценивали с точки зрения их воздействий на стабильность жидкой трансглутаминазы, таким образом, выбирая подходящие регуляторы рН, регуляторы водной активности и регуляторы окислительно-восстановительного потенциала.
[0014] 4. Эффект различных регуляторов рН на стабильность растворов трансглутаминазы
Один регулятор из хлористоводородной кислоты, серной кислоты, уксусной кислоты, молочной кислоты, лимонной кислоты, яблочной кислоты, фитиновой кислоты, фосфорной кислоты, азотной кислоты, щавелевой кислоты, гидроксида натрия, гидроксида калия, карбоната натрия, бикарбоната натрия, карбоната калия, бикарбоната калия, цитрата тринатрия, цитрата трикалия, ацетата натрия, ацетата калия, лактата натрия, лактата калия, гидрофосфата динатрия, гидрофосфата дикалия, фосфата натрия, фосфата калия, водопроводной воды, очищенной воды и минеральной воды или буферной системы, состоящей из нескольких регуляторов рН, был выбран для регуляции pH очищенного раствора трансглутаминазы до интервала, приведенного в Таблице 1. Различные регуляторы рН и случайные комбинации различных регуляторов рН исследовали на предмет их воздействия на стабильность жидкой трансглутаминазы при комнатной температуре. Результаты показаны в Таблицах 4-1, 4-2 и 4-3.
Таблица 4-1. Действие различных щелочных регуляторов рН на стабильность жидкой трансглутаминазы
после регуляции
(Ед/мл)
через 2 дня
(Ед/мл)
консервации (%)
(1:1)
(0,1:0,9)
Таблица 4-2. Действие различных кислотных регуляторов рН на стабильность жидкой трансглутаминазы
после регуляции
(Ед/мл)
через 2 дня
(Ед/мл)
консервации (%)
Таблица 4-3. Действие различных комбинаций регуляторов рН на стабильность жидкой трансглутаминазы
после регуляции
(Ед/мл)
через 2 дня
(Ед/мл)
%
Данные в таблицах 4-1, 4-2 и 4-3 показывают, что отсутствуют значительные различия и изменения, касающиеся действия выбранных кислотных регуляторов рН, щелочных регуляторов рН и т.п. на хранение ферментного раствора при комнатной температуре. Следовательно, любой регулятор из хлористоводородной кислоты, серной кислоты, уксусной кислоты, молочной кислоты, лимонной кислоты, яблочной кислоты, фитиновой кислоты, фосфорной кислоты, азотной кислоты, щавелевой кислоты, гидроксида натрия, гидроксида калия, карбоната натрия, бикарбоната натрия, карбоната калия, бикарбоната калия, цитрата тринатрия, цитрата трикалия, ацетата натрия, ацетата калия, лактата натрия, лактата калия, гидрофосфата динатрия, гидрофосфата дикалия, фосфата натрия, фосфата калия, водопроводной воды, очищенной воды и минеральной воды или буферной системы, состоящей из нескольких регуляторов рН, указанных выше, может быть выбран в качестве регулятора рН для регуляции pH жидкой трансглутаминазы. С точки зрения безопасности при производственных операциях и действия временно экстремальных значений pH от сильной кислоты или сильного основания на активность трансглутаминазы во время операции регуляции, буфер, содержащий фосфорную кислоту, уксусную кислоту, молочную кислоту или лимонную кислоту или их соль, является предпочтительным.
5. Действие различных регуляторов водной активности и их количеств на стабильность жидкой трансглутаминазы при комнатной температуре
Действие различных регуляторов водной активности на стабильность растворов трансглутаминазы тестировали следующим образом: при комнатной температуре и стерильных условиях к раствору трансглутаминазы добавляли один или несколько регуляторов из сорбита, мальтита, пропиленгликоля, глицерина, ксилита, полиэтиленгликоля (ПЭГ) 400, ПЭГ 600, ПЭГ 800, ПЭГ 20000, глюкозы, трегалозы, сахарозы, мальтозы, изомальтозы, мальтодекстрина и ксилита, чтобы регулировать водную активность жидкого ферментного препарата до 0,75, и жидкий ферментный препарат содержали в стерильных условиях в течение 10 дней. Результаты показаны в Таблице 5-1.
Таблица 5-1. Действие различных регуляторов водной активности на ферментативную активность трансглутаминазы
активность (Ед/мл)
активность
ферментативной активности (%)
(9:1)
(9:1)
(7:3)
(9:1)
(9:1)
Глицерин:
Мальтит
(1:5:4)
Данные в Таблице 5-1 показывают, что, когда один или несколько регуляторов из сорбита, мальтита, пропиленгликоля, глицерина, ксилита, ПЭГ 400, ПЭГ 600, ПЭГ 800, ПЭГ 20000, трегалозы, сахарозы, мальтозы, изомальтозы, мальтодекстрина и ксилита применяют в качестве регулятора водной активности для регуляции водной активности жидкой трансглутаминазы до 0,75, они оказывают хороший защитный эффект на стабильность жидкого ферментного препарата при комнатной температуре. Как представлено в результатах, сорбит, мальтит, глицерин или любая их комбинация являются предпочтительными. Регулятор может применяться в количестве 30-80% (м/об), предпочтительно 30-70% (м/об).
Несколько регуляторов водной активности из Таблицы 5-1 тестировали на предмет взаимосвязи между применяемым количеством и степенью консервации ферментативной активности при комнатной температуре. Жидкий ферментный препарат содержали в стерильных условиях при pH 6,0, затем через 10 дней определяли степени консервации ферментативной активности (%) при комнатной температуре. Результаты показаны в Таблице 5-2.
[0015] Таблица 5-2. Действие различных регуляторов водной активности на ферментативную активность трансглутаминазы
(м/об)
(м/об)
(м/об)
(м/об)
(м/об)
(м/об)
(м/об)
Замечание: в Таблице 5-2 A представляет мальтит; B представляет глицерин; C представляет трегалозу; D представляет ПЭГ 600; E представляет глицерин: сорбит (9: 1); F представляет глицерин: мальтит (7:3); G представляет мальтит: сорбит (9:1); и H представляет пропиленгликоль: глицерин: мальтит (1: 5:4).
Данные в Таблице 5-2 показывают, что при оптимальном pH, когда регулятор водной активности применяют в количестве выше 30%, указанные регуляторы водной активности по отдельности или в комбинации приводят к степени консервации ферментативной активности свыше 80% при комнатной температуре через 10 дней для жидкого ферментного препарата. Когда регулятор водной активности применяют в количестве свыше 40%, степень консервации ферментативной активности составляет свыше 86%. При увеличении количества регулятора (регуляторов) водной активности, степень консервации ферментативной активности увеличивается, но не в большой степени. С позиций себестоимости количество регулятора (регуляторов) водной активности предпочтительно составляет между 30 и 70% (м/об).
[0016] 6. Действие различных регуляторов окислительно-восстановительного потенциала на стабильность жидкой трансглутаминазы при комнатной температуре
В пределах предпочтительного интервала окислительно-восстановительного потенциала авторы настоящего изобретения исследовали действие различных регуляторов окислительно-восстановительного потенциала на стабильность жидкой трансглутаминазы, используя регулятор окислительно-восстановительного потенциала, применяемый в максимальном количестве, как установлено стандартом GB2760-2014. В эксперименте для регуляции pH раствора трансглутаминазы до 6,0 применяют цитратный буфер (pH 6,0), а для регуляции водной активности до 0,73-0,75 добавляют глицерин.
[0017] Данные в Таблице 6 и Таблице 7 показывают, что, когда различные регуляторы окислительно-восстановительного потенциала применяют для регуляции окислительно-восстановительных потенциалов жидкой трансглутаминазы до между 50 мВ и -150 мВ, степень консервации ферментативной активности препарата при добавлении регуляторов окислительно-восстановительного потенциала достигает свыше 80% после хранения в течение 90 дней при комнатной температуре, указывая на то, что препарат имеет промышленное значение. За исключением нескольких регуляторов окислительно-восстановительного потенциала, таких как лактат натрия и лактат кальция, все другие формулы препарата, содержащие регуляторы окислительно-восстановительного потенциала имеют степень консервации ферментативной активности выше 80% после хранения в течение 180 дней при комнатной температуре.
[0018] Таблица 6. Действие различных регуляторов окислительно-восстановительного потенциала на стабильность жидких препаратов трансглутаминазы
потенциала
Кол-во(%)
Ед/мл
кислота
%
динатрия
кислота
натрия
Как показано в Таблице 7, когда применяют один или несколько регуляторов окислительно-восстановительного потенциала, жидкая трансглутаминаза имеет степень консервации ферментативной активности выше 80% после хранения при комнатной температуре в течение 180 дней, что полностью соответствует требованиям к промышленному производству и применению. С позиций себестоимости и желания людей потреблять экологически чистую пищу, регуляторы потенциала из природных источников, такие как L-аскорбиновая кислота и ее соли, L-серин и его соли, L-цистеин и его соли, восстановленный глутатион, полифенол чая, гидролизат соевого белка, гидролизат пшеничного белка, гидролизат казеина, гидролизат хитозана, антиоксидант листьев бамбука, экстракт розмарина и экстракт антиоксиданта лакрицы являются предпочтительными; или низкозатратные супероксиддисмутаза, глюкозооксидаза, бисульфит натрия, метабисульфит натрия, метабисульфит калия, сульфит натрия, гипосульфит натрия, фитиновая кислота и т.д. являются предпочтительными. Исходя из результатов в Таблице 6 и Таблице 7, определют, что регулятор окислительно-восстановительного потенциала подлежит добавлению в интервале 0,0075-1%.
[0019] Таблица 7. Действие регуляторов окислительно-восстановительного потенциала на стабильность жидких препаратов трансглутаминазы
кол-во (%)
кол-во (%)
кол-во (%)
Посредством добавления регулятора рН, регулятора водной активности и регулятора окислительно-восстановительного потенциала жидкую трансглутаминазу регулируют до интервала рН 5,0-9,0, водной активности, составляющей <0,89, и окислительно-восстановительного потенциала от -400 мВ до +50 мВ. Жидкий ферментный препарат достигает степени консервации выше 80% после хранения при комнатной температуре в стерильных условиях в течение 180 дней, что по существу соответствует требованиям к стабильному жидкому препарату трансглутаминазы, который имеет промышленную применимость.
[0020] Далее, согласно требованиям GB25594-2010, ферментный препарат для применения в пищевой промышленности должен соответствовать соответствующим стандартам гигиены, таким как индекс микроорганизмов.
[0021] Вот почему проводили дополнительные исследования действия водной активности, пищевого консерванта и способов получения, таких как стерилизующая фильтрация и заполнение, на общее число колоний и индекс болезнетворных микроорганизмов в жидком препарате трансглутаминазы.
[0022] 7. Действие различных концентраций регуляторов водной активности на общее число колоний в препарате жидкой трансглутаминазы, хранящемся при комнатной температуре
рН концентрированного раствора трансглутаминазы регулировали до 6,0 и добавляли 1% гидролизат пшеничного белка (м/об) для регуляции окислительно-восстановительного потенциала, глицерин добавляли в различных количествах % (м/об) и регулятор рН добавляли для достижения объема 100%, получая жидкий ферментный препарат с различными водными активностями. Жидкий ферментный препарат распределяли и упаковывали в открытых условиях, и исследовали изменения общего числа колоний в ферментном препарате во время хранения при комнатной температуре. Результаты показаны в Таблице 8.
Таблица 8. Действие различных концентраций регуляторов водной активности на общее число колоний в жидком ферментном препарате
Данные в Таблице 8 показывают, что когда водная активность превышает 0,85, глицерин присутствует в количестве ниже 40% и отсутствует консервант в жидком ферментном препарате трансглутаминазы, быстро размножаются микроорганизмы, и общее число колоний превышает максимальное значение, установленное соответствующими законами и нормами во время хранения в течение 180 дней при комнатной температуре. Когда регулятор водной активности присутствует в количестве выше 40%, рост и размножение микроорганизмов существенно подавляются вследствие самой низкой водной активности. С позиций требований к показателям гигиены ферментных препаратов для применения в пищевой промышленности формулы препаратов с регулятором водной активности выше 40%-80% являются предпочтительными.
[0023] 8. Действие различных пищевых консервантов на микроорганизмы в ферментном растворе
Раствор трансглутаминазы разбавляли 0,02 M натрийцитратным буфером (pH 6,0) до 1000 Ед/мл. К 100 мл разбавленного ферментного раствора добавляли 300 г глицерина и 10 г регулятора потенциала из гидролизата пшеничного белка и затем добавляли 0,02 M натрийцитратный буфер с pH 6,0 до конечного объема, равного 1000 мл. Добавляли пищевые консерванты, перечисленные в GB2760-2014, как показано в Таблице 9, контролями служили A: без консерванта, и B: без консерванта, но раствор фильтровали через мембрану 0,1-0,22 мкм и заполнение проводили в стерильных условиях. В открытых условиях ферментным раствором в виде экспериментального образца заполняли непрозрачные бутыли из ПЭТ и их хранили при комнатной температуре в течение 180 дней. Микробиологическое исследование было проведено согласно GB4789.2-2010 National Food Safety Standard ʺFood microbiological examination: Aerobic plate countʺ, GB 4789.3 National Food Safety Standard ʺFood microbiological examination: Enumeration of coliformsʺ, GB/T 4789.38 National Food Safety Standard ʺFood microbiological examination: Escherichia coli countʺ, и GB 4789.4-2010 National Food Safety Standard ʺFood microbiological examination: Salmonellaʺ. Результаты показаны в Таблице 9.
Таблица 9. Действие различных пищевых консервантов на микроорганизмы в жидких ферментных препаратов
Данные в Таблице 9 показывают, что когда регулятор водной активности имеет концентрацию всего лишь 30% (м/об), различные пищевые консерванты, добавленные в количествах, разрешенных законами и нормами, могут эффективно ингибировать пролиферацию микроорганизмов, таким образом обеспечивая гигиену и безопасность раствора трансглутаминазы. С учетом предпочтений пользователя и применяемого интервала различных пищевых консервантов, один пищевой консервант или комбинация из нескольких пищевых консервантов может применяться в производстве жидкой трансглутаминазы; предпочтительными являются природные пищевые консерванты, таки как ε-полилизин, натамицин, лизоцим и низин, или жидкость можно фильтровать через мембрану 0,1 мкм с последующим стерильным заполнением или альтернативно, с учетом затрат на применения, можно применять один или несколько консервантов из сорбиновой кислоты и сорбата калия, диацетата натрия, дегидроацетата натрия, метил-п-гидроксибензоата, метабисульфита калия и метабисульфита натрия; или в способе можно использовать фильтрацию через 0,1 мкм мембрану с последующим стерильным заполнением.
[0024] 9. Действие различных ферментативных активностей на стабильность жидких препаратов при комнатной температуре
К различным количествам очищенных концентрированных ферментных растворов добавляли 50% (м/об) глицерин и 0,1% (м/об) бисульфит натрия, и регулятор рН добавляли до конечного объема, равного 1000 мл. После стерилизующей фильтрации полученный раствор хранили при комнатной температуре в течение 180 дней, а затем определяли ферментативную активность и проводили сравнение степени консервации ферментативной активности (%).
[0025] Таблица 10. Действие различных ферментативных активностей ферментных растворов на стабильность жидкой трансглутаминазы
кол-во
ферм.
раствора % (об/об)
кол-во
ферм.
раствора (мл)
активность
после регуляции (Ед/мл)
активность
через 180 дней (Ед/мл)
Консервации ферм. активности %
Как показано в Таблице 10, действие различных ферментативных активностей ферментных растворов на стабильность жидкой трансглутаминазы не является значительным. Однако при практическом применении предпочтительно контролировать ферментативную активность жидкого препарата в пределах интервала 10-1000 Ед/мл.
[0026] При исследовании эффектов вышеуказанных физико-химических факторов на степень консервации ферментативной активности (стабильность) раствора трансглутаминазы при комнатной температуре авторы настоящего изобретения определили оптимальный интервал рН, виды регуляторов рН, интервал водной активности и количество регулятора водной активности, интервал окислительно-восстановительного потенциала и виды регуляторов окислительно-восстановительного потенциала, которые можно применять/использовать для поддержания жидкого препарата трансглутаминазы в стабильном состоянии при комнатной температуре.
[0027] Кроме того, было подтверждено, что посредством стерилизующей фильтрации и заполнения или добавления консерванта при производстве жидкий ферментный препарат может стабильно храниться при комнатной температуре.
[0028] На основании того принципа, что для увеличения стабильности фермента применяют несколько способов в комбинации, чтобы таким образом достичь цели синергетического увеличения стабильности фермента, настоящее изобретение успешно решает проблему хранения жидкого препарата трансглутаминазы при комнатной температуре посредством управления промежуточными показателями и параметрами во время производства и позволяет разработать жидкий препарат трансглутаминазы, который имеет хорошую стабильность при комнатной температуре, который можно хранить в течение длительного времени и можно производить в промышленном масштабе. Это имеет большое значение для снижения производственных затрат при получении трансглутаминазы, энергосбережения, защиты окружающей среды, безопасного для здоровья применения и продвижения на рынок.
[0029] В итоге технические растворы настоящего изобретения представляют собой следующее:
жидкий ферментный препарат, отличающийся тем, что жидкий ферментный препарат представляет собой жидкий ферментный препарат трансглутаминазы EC2.3.2.13, имеющий ферментативную активность 10-1000 Ед/мл;
жидкий ферментный препарат, отличающийся тем, что его компоненты и их количества являются следующими: жидкий препарат трансглутаминазы имеет ферментативную активность, равную 10-1000 Ед/мл, регулятор водной активности присутствует в количестве 30-80 мас./об.%, регулятор окислительно-восстановительного потенциала присутствует в количестве 0,0075-1 мас./об.%, пищевой консервант присутствует в количестве 0-0,1 мас./об.%, и регулятор рН добавляют до конечного объема, равного 100%.
[0030] Жидкий ферментный препарат имеет следующие физико-химические свойства:
1) имеет pH 5,0-9,0; предпочтительно pH 5,0-7,5;
2) имеет водную активность Aw ≤0,89; предпочтительно водную активность Aw 0,60-0,85; и
3) имеет окислительно-восстановительный потенциал от -400 мВ до +50 мВ; предпочтительно, окислительно-восстановительный потенциал от -400 мВ до 0 мВ.
регулятор рН представляет собой один регулятор из хлористоводородной кислоты, серной кислоты, уксусной кислоты, молочной кислоты, лимонной кислоты, яблочной кислоты, фитиновой кислоты, фосфорной кислоты, азотной кислоты, щавелевой кислоты, гидроксида натрия, гидроксида калия, карбоната натрия, бикарбоната натрия, карбоната калия, бикарбоната калия, цитрата тринатрия, цитрата трикалия, ацетата натрия, ацетата калия, лактата натрия, лактата калия, гидрофосфата динатрия, гидрофосфата дикалия, фосфата натрия, фосфата калия, водопроводной воды, очищенной воды и минеральной воды, или буферной системы, состоящей из нескольких регуляторов рН; предпочтительно, регулятор имеет буферную емкость pH, такой как буфер, содержащий один регулятор из фосфорной кислоты, уксусной кислоты, молочной кислоты или лимонной кислоты или их соли.
Регулятор водной активности выбирают из группы, содержащей сорбит, мальтит, пропиленгликоль, глицерин, ксилит, ПЭГ, трегалозу, сахарозу, мальтозу, изомальтозу, мальтодекстрин, ксилит и маннит, предпочтительно, содержащей сорбит, мальтит или глицерин или их комбинацию. Количество составляет 30-80% (м/об), предпочтительно 30-70% (м/об).
Регулятор окислительно-восстановительного потенциала содержит один или несколько регуляторов из L-аскорбиновой кислоты и ее соли, L-серина и его соли, L-цистеина и его соли, восстановленного глутатиона, полифенола чая, гидролизата соевого белка, гидролизата пшеничного белка, гидролизата казеина, гидролизата хитозана, антиоксиданта листьев бамбука, экстракта розмарина, экстракта антиоксиданта лакрицы, супероксиддисмутазы, глюкозооксидазы, бисульфита натрия, метабисульфита натрия, метабисульфита калия, сульфита натрия, гипосульфита натрия, фитиновой кислоты и т.д., и его применяют в количестве 0,0075%-1%.
Пищевой консервант выбирают из группы, содержащей ε-полилизин, натамицин, лизоцим, низин, сорбат калия, дегидроацетат натрия, диацетат натрия, метил-п-гидроксибензоат, этиллауроиларгинат HCl, метабисульфит калия и метабисульфит натрия и, как правило, добавляют в количестве 0%-0,1%.
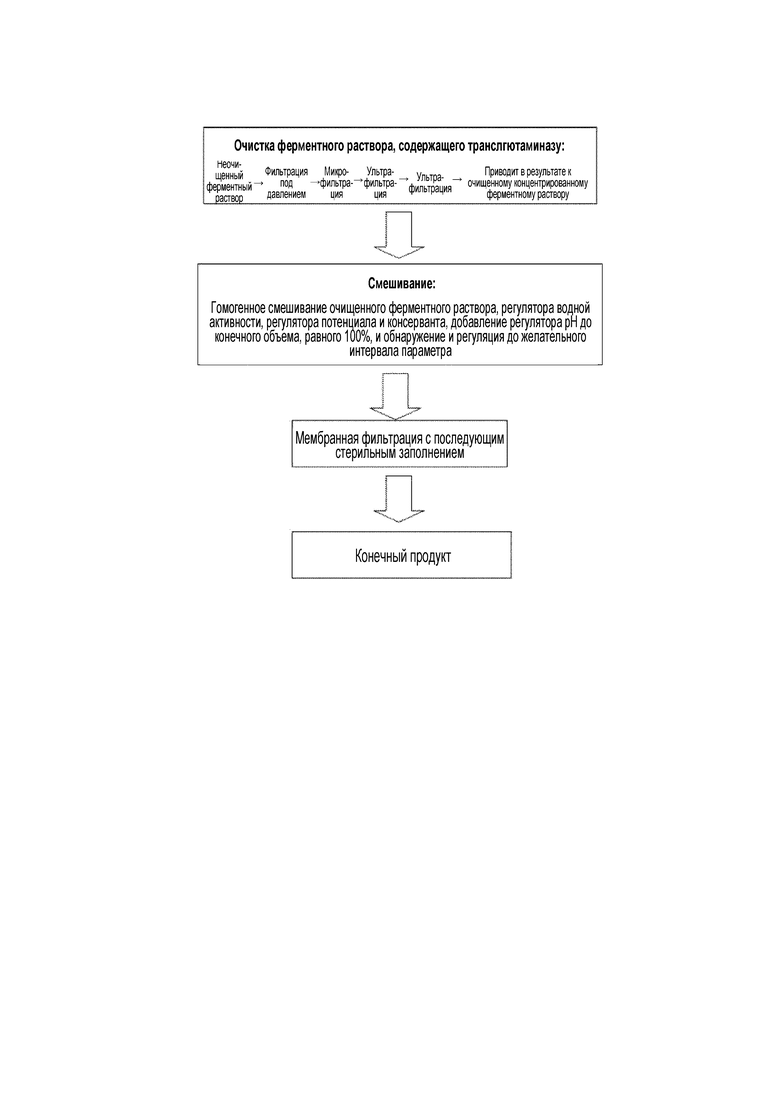
[0031] Способ получения жидкого ферментного препарата, характеризуется следующими стадиями:
1) очистка ферментного раствора: подвергание неочищенного ферментного раствора фильтрации под давлением, микрофильтрации и вторичной ультрафильтрации для получения очищенного концентрированного ферментного раствора;
2) смешивание: количественное определение массы очищенного концентрированного ферментного раствора, регулятора водной активности и регулятора окислительно-восстановительного потенциала, добавление пищевого консерванта, если он присутствует, и смешивание; добавление регулятора рН до конечного объема, равного 100%; после гомогенного смешивания тестирование и регулирование следующих параметров жидкого ферментного препарата: рН 5,0-9,0, водная активность Aw ≤0,89 и окислительно-восстановительный потенциал от -400 мВ до +50 мВ;
3) удаление бактерий: фильтрация полученной в результате смеси через мембрану 0,1-0,22 мкм для стерилизации с последующим стерильным заполнением;
4) упаковка: упаковка жидкого ферментного препарата посредством стерильного заполнения или другого соответствующего процесса упаковки жидких сред.
[0032] В настоящем изобретении впервые удалось получить жидкий препарат трансглутаминазы, который имеет ферментативную активность не менее 80% и является стабильным в форме раствора после хранения при комнатной температуре в течение 6 месяцев, соответствует требованиям промышленного внедрения на рынок, является удобным для производства, имеет хороший эффект применения и не нуждается в охлаждении или транспортировке в условиях холодной логистики.
[0033] Изобретательский уровень настоящего изобретения:
В настоящем изобретении впервые удалось получить жидкий препарат трансглутаминазы, который имеет степень консервации ферментативной активности выше 80% и является стабильным в форме раствора после хранения при комнатной температуре в течение 6 месяцев, соответствует требованиям промышленного внедрения на рынок, является удобным для производства, имеет хороший эффект применения и не нуждается в охлаждении или транспортировке в условиях холодной логистики. Настоящее изобретение имеет важное значение для продвижения с целью промышленного применения и разработки трансглутаминазы.
[0034] В настоящем изобретении впервые установлено, что окислительно-восстановительный потенциал в системе является наиболее важным фактором для поддержания стабильности жидкой трансглутаминазы при комнатной температуре. Когда окислительно-восстановительный потенциал жидкого ферментного препарата находится между (-400 мВ) и +50 мВ, стабильность раствора трансглутаминазы при комнатной температуре значительно увеличивается. Как макромолекулярный белок, трансглутаминаза имеет каталитическую активность, должна поддерживать стабильность своей трехмерной структуры в максимальной степени, чтобы поддерживать стабильность молекул фермента. Однако группы и фрагменты внутри макромолекулы имеют различные характеристики заряда вследствие различия их аминокислотных последовательностей. В жидкой системе это проявляется в виде типичного амфотерного электролитного характера. Поскольку трехмерная структура нуждается в поддержании посредством нековалентных связей, таким образом, как за счет сил Ван-дер-Ваальса между группами и фрагментами, на такое слабозарядное действие легко влияет окислительно-восстановительный потенциал жидкой системы, в которой присутствуют молекулы фермента. Когда окислительно-восстановительный потенциал жидкой системы является более высоким, чем устойчивый потенциал молекул фермента, молекулы трансглутаминазы, как восстановитель, окисляются в системе; когда окислительно-восстановительный потенциал жидкой системы является более низким, чем устойчивый потенциал молекул фермента, молекулы трансглутаминазы, как оксидант, восстанавливаются в системе, что приводит к потере трехмерной структуры и активности молекул фермента. В настоящем изобретении жидкий препарат трансглутаминазы, являющийся стабильным при комнатной температуре, получают посредством регуляции потенциала жидкого ферментного препарата, чтобы он находился в пределах указанного выше интервала потенциала, с использованием подходящего регулятора окислительно-восстановительного потенциала, где окислительно-восстановительный потенциал окружения, в котором присутствует трансглутаминаза, находился как раз в интервале, в котором молекула фермента является стабильной.
[0035] Следовательно, в формулу препарата настоящего изобретения впервые добавлен регулятор окислительно-восстановительного потенциала, такой как восстановленный глутатион, L-цистеин и его гидрохлорид, гидролизат пшеничного белка, гидролизат хитозана, антиоксидант листьев бамбука, экстракт розмарина, экстракт антиоксиданта лакрицы и сульфит, который по существу обеспечивает стабильность жидкого препарата трансглутаминазы при комнатной температуре и является основным в формуле препарата.
[0036] В формуле препарата настоящего изобретения также применяют регулятор водной активности и регулятор рН, где буфер может эффективно регулировать изменение pH жидкого ферментного препарата, вызванного добавлением различных добавок, и поддерживать pH жидкой трансглутаминазы в оптимальном интервале. Добавление регулятора водной активности может поддерживать жидкий ферментный препарат при более низкой водной активности Aw и также является благоприятным для подавления размножения микроорганизмов и увеличения стерической стабильности молекул фермента. Например, в настоящем изобретении применяют регуляторы водной активности, содержащие многочисленные гидроксильные блоки, такие как трегалоза, ПЭГ и сорбит, которые могут значительно стабилизировать пространственную структуру молекул трансглутаминазы. Применение регулятора водной активности, регулятора окислительно-восстановительного потенциала и регулятора рН в комбинации может синергетически поддерживать стабильность фермента и позволяет достичь наилучшего стабилизирующего эффекта.
[0037] В способе получения настоящего изобретения жидкий препарат трансглутаминазы получают посредством смешивания. Во-первых, очищают концентрированный раствор трансглутаминазы или порошок трансглутаминазы. Поскольку сама трансглутаминаза имеет молекулярную массу, приблизительно равную 38-45 кДа, сначала проводят фильтрацию под давлением и микрофильтрацию (с размером пор 0,1-1 мкм). На этой стадии можно удалить осадки, такие как бактериальные твердые вещества и частицы. Затем полученный в результате раствор подвергают ультрафильтрации (отсечение по молекулярной массе: 100-200 кДа), и на этой стадии можно удалить большую часть микроорганизмов, уменьшить порчу от микробов и уменьшить воздействие микроорганизмов на фермент. В завершение проводят ультрафильтрацию (отсечение по молекулярной массе: 10-30 кДа) для получения очищенного концентрированного ферментного раствора. Затем добавляют регулятор водной активности, регулятор окислительно-восстановительного потенциала и пищевой консервант согласно формуле препарата, для регуляции pH применяют регулятор рН. После гомогенного смешивания определяют соответствующие параметры. Небольшую регуляцию осуществляют добавлением регуляторов, чтобы таким образом обеспечить соответствие физико-химическим свойствам препарата. Смешанный раствор дополнительно подвергают мембранной фильтрации для удаления бактерий с последующим заполнением таким образом, чтобы весь раствор находился в стерильном окружении или окружении с небольшим количеством бактерий. В то же время необязательно можно применять пищевой консервант, чтобы предотвратить рост бактерий в жидком ферментном препарате во время хранения и транспортировки. Формула и способ получения препарата согласно настоящему изобретению могут значительно увеличить термическую стабильность трансглутаминазы и продлить срок хранения жидкого ферментного препарата.
[0038] Компоненты, применяемые в формуле препарата жидкого препарата трансглутаминазы согласно настоящему изобретению, являются дешевыми и могут быть легко получены, и их источники для применения в пищевой промышленности являются доступными. Формула жидкого препарата трансглутаминазы также соответствует национальным стандартам безопасности пищевых продуктов и пищевых добавок. Способ получения жидкого ферментного препарата является научным и обоснованным и имеет высокую эффективность при производстве. Он значительно упрощается с позиций проведения способа и затрат на производство в сравнении со способом получения порошкового ферментного препарата посредством лиофилизации. Потери ферментативной активности почти не существует, и производственная эффективность значительно увеличивается. Он соответствует принципам энергосбережения, защиты окружающей среды, безопасного для здоровья применения ферментов и экологически-ориентированной экономики, что поощряется в Китае.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0039] Фиг. 1 представляет собой схему методики получения жидкого ферментного препарата.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0040] Следующие примеры предоставлены для лучшего понимания настоящего изобретения, заявленный объем притязаний в настоящем изобретении включает, без ограничения, содержание следующих примеров, и любые модификации и улучшения, сделанные согласно общепринятому уровню знаний в данной области, будут находиться в пределах объема притязаний, заявленного в настоящем изобретении. Схема представлена на Фиг. 1.
[0041] Пример 1
Неочищенный раствор трансглутаминазы получают посредством микробиологической ферментации, которую может выполнять со ссылкой на патент (Патентная публикация №: EP0379606B1): Streptomyces mobaraensis применяют как исходный штамм, несколько бактериальных колоний в состоянии хорошего роста пикируют с помощью петли для инокуляции, засевают на скошенной культуральной среде и культивируют при постоянной температуре, равной 30°C в течение 7 дней. Активированные штаммы далее высевают в среду для посевной культуры, культивируемой при 30°C в течение 48 ч, добавляют в среду для ферментации в инокуляционном количестве, равном 10%, и культивируют при 30°C в течение 48-72 ч, получая, таким образом, неочищенный раствор трансглутаминазы. Неочищенный ферментный раствор очищают и концентрируют посредством следующих стадий:
1) фильтрация под давлением: при размере пор 1 мкм, рабочем давлении 0,20 мПа и температуре 20°C с получением фильтрата;
2) микрофильтрация: при размере пор 0,25 мкм, рабочем давлении 0,25 мПа и температуре 20°C с получением фильтрата;
3) ультрафильтрация: при отсечении по молекулярной массе, равном 100 кДа, рабочем давлении 0,30 мПa и температуре 20°C с получением фильтрата;
4) ультрафильтрация: при отсечении по молекулярной массе, равном 10 кДа, рабочем давлении 0,30 мПa и температуре 20°C, сохраняя ультраконцентрат (т.е очищенный концентрированный ферментный раствор).
[0042] Ферментативную активность определяют методом с гидроксамовой кислотой (Peng Can, Stabilization Study of Microbial Transglutaminasa [D]. East China Normal University, 2007), (также как далее) и получают очищенный концентрированный раствор трансглутаминазы, имеющий ферментативную активность, равную 2500 Ед/мл. По данным измерений он имеет рН 5,80, водную активность 0,95 и окислительно-восстановительный потенциал 60 мВ. Раствор сохраняют для более позднего применения.
[0043] Пример 2
Неочищенный раствор трансглутаминазы получают растворением порошка фермента. Определяют массу некоторого количества чистой воды и помещают в контейнер, оборудованный мешалкой. Медленно, при перемешивании, добавляют порошок трансглутаминазы с ферментативной активностью 5000-8000 Ед/мл (порошок фермента, производства Shanghai Kinry Food Ingredients Co., Ltd), чтобы получить ферментный раствор определенной концентрации. Бактерии удаляют микрофильтрацией с получением прозрачного раствора трансглутаминазы с ферментативной активностью 2500 Ед/мл, т.е. очищенного концентрированного раствора трансглутаминазы с ферментативной активностью 2500 Ед/мл. По данным измерения, он имеет pH 6,30, водную активность 0,95 и окислительно-восстановительный потенциал 58 мВ. Раствор сохраняют для более позднего применения.
[0044] Пример 3
Способ получения жидкой трансглутаминазы: жидкий фермент в полном объеме 1000 мл получают следующим образом, и массу исходных веществ определяют согласно Таблице 11.
Таблица 11. Получение жидкой трансглутаминазы
(Пример 1)
Натрийцитратный буфер
Массу исходных веществ определяют и их гомогенно смешивают, и после фильтрации через стерильную мембрану 0,1 мкм получают раствор светло-желтого цвета. По данным измерений, он имеет окислительно-восстановительный потенциал -100 мВ, водную активность 0,79, pH 6,0 и ферментативную активность 498,1 Ед/мл. Раствором заполняют десять непрозрачных бутылей из ПЭТ с объемом 100 мл, чтобы окончательно получить препарат трансглутаминазы в жидкой форме. После хранения при комнатной температуре в течение 180 дней ферментный препарат с этой формулой наблюдают, ферментативную активность измеряют, и рассчитывают степень консервации ферментативной активности посредством ссылки на GB4789.2-2010 National Food Safety Standard ʺFood microbiological examination: Aerobic plate countʺ, GB 4789.3 National Food Safety Standard ʺFood microbiological examination: Enumeration of coliformsʺ, GB/T 4789,38 National Food Safety Standard ʺFood microbiological examination: Escherichia coli countʺ и GB 4789.4-2010 National Food Safety Standard ʺFood microbiological examination: Salmonellaʺ, проводят микробиологическое исследование. Результаты показывают, что жидкий ферментный препарат не имеет значительного изменения внешнего вида, запаха и т.п. Он имеет степень консервации ферментативной активности 86%, и его индексы микроорганизмов соответствуют требованиям Стандарта GB25594-2010. Следовательно, он может применяться для промышленного внедрения.
[0045] Пример 4
Очищенный концентрированный раствор трансглутаминазы, полученный в Примере 2, применяют для получения жидкого препарата трансглутаминазы согласно формуле препарата в таблице 12. После гомогенного смешивания измеряют pH, водную активность, окислительно-восстановительный потенциал и начальную ферментативную активность согласно соответствующим методам в Примере 3. Жидкий препарат трансглутаминазы затем фильтруют через стерильную мембрану 0,1 мкм и его распределяют и упаковывают в бутыли из ПЭТ в стерильных условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого препарата трансглутаминазы и измеряют конечные ферментативную активность, индексы микроорганизмов и т.п. согласно соответствующим методам в Примере 3, и рассчитывают степень консервации ферментативной активности.
[0046] Таблица 12. Получение жидкой трансглутаминазы
(Пример 2)
Натрийцитратный буфер
Результаты показывают, что препарат трансглутаминазы, полученный посредством указанного способа, имеет хорошую стабильность, не имеет значительных и видимых изменений внешнего вида и имеет степень консервации ферментативной активности 82%. Индексы микроорганизмов соответствуют требованиям Стандарта GB25594-2010. Он может применяться для промышленного внедрения. Применение фильтрации через стерильную мембрану 0,1 мкм и стерильное заполнение могут обеспечить жидкий ферментный препарат, имеющий степень консервации ферментативной активности до 80% и могут контролировать индексы микроорганизмов в жидком ферментном препарате приведенной формулы с использованием 30% регулятора водной активности во время периода хранения.
[0047] Пример 5
Таблица 13. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 2)
Натрийцитратный буфер
После гомогенного смешивания указанных исходных веществ смесью непосредственно заполняют бутыли из ПЭТ в открытых условиях. После хранения при комнатной температуре в течение 180 дней препарат трансглутаминазы, полученный посредством указанного способа, имеет хорошую стабильность, не имеет значительных и видимых изменений внешнего вида и имеет степень консервации ферментативной активности 84%. Индексы микроорганизмов соответствуют требованиям Стандарта GB25594-2010, и его можно применять для промышленного внедрения.
[0048] Пример 6
Таблица 14. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
(об/об)
(м/об)
87%
(м/об)
(м/об)
соответствует стандарту
Натрийцитратный буфер
Компоненты, перечисленные в Таблице 14, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 87%, индексы микроорганизмов соответствуют требованиям, и, таким образом, получают стабильный жидкий препарат трансглутаминазы.
[0049] Пример 7
Таблица 15. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
89%
-32 мВ
соотв. стандарту
Компоненты, перечисленные в Таблице 15, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата, и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что в присутствии консерванта, после хранения при комнатной температуре в течение 180 дней, степень консервации ферментативной активности достигает 89%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы.
[0050] Пример 8
Компоненты, перечисленные в Таблице 16, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 88%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы, где регуляторы потенциала и регуляторы водной активности являются комбинированными компонентами, и добавляют консервант.
[0051] Таблица 16. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
(об/об)
Сорбит 30%
89%
-38 мВ
соответствуют стандарту
[0052] Пример 9
Таблица 17. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
88%
(м/об)
-42 мВ
соотвует стандарту
Компоненты, перечисленные в Таблице 17, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 88%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 1000 Ед/мл.
[0053] Пример 10
Компоненты, перечисленные в Таблице 18, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 81,5%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 10 Ед/мл и pH 5,5.
Таблица 18. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
81,5%
-60 мВ
соотв. стандарту
Очищенная вода
[0054] Пример 11
Компоненты, перечисленные в Таблице 19, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 81%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 99,8 Ед/мл и pH 8,0.
Таблица 19. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
80,5%
(м/об)
-32 мВ
соотв. стандарту
Очищенная вода
[0055] Пример 12
Компоненты, перечисленные в Таблице 20, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 81%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 100 Ед/мл, pH 6,0 и окислительно-восстановительным потенциалом -400 мВ. Поскольку боргидрид натрия в препарате не соответствует требованиям Правил пищевой гигиены, жидкий ферментный препарат с этой формулой можно применять только с целью проведения научных исследований или получения непищевых добавок.
[0056] Таблица 20. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
80,1%
(м/об)
-400 мВ
соотв. стандарту
Очищенная вода
[0057] Пример 13
Компоненты, перечисленные в Таблице 21, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 82%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 50 Ед/мл, pH 6,0 и окислительно-восстановительным потенциалом 50 мВ.
Таблица 21. Получение жидкой трансглутаминазы
Без видимого изменения
(Пример 1)
82%
L-цистеин HCl
0,01% (м/об)
50 мВ
соотв. стандарту
Фосфатный буфер
[0058] Пример 14
Таблица 22. Получение жидкой трансглутаминазы
L-цистеин HCl
0,03% (м/об)
0 мВ
соответствует стандартам
Компоненты, перечисленные в Таблице 22, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 84%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 100 Ед/мл, pH 6,0 и окислительно-восстановительным потенциалом 0 мВ.
[0059] Пример 15
Компоненты, перечисленные в Таблице 23, гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 89%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 50 Ед/мл, водной активностью 0,61 и окислительно-восстановительным потенциалом -140 мВ. В формулу препарата не включен консервант.
[0060] Таблица 23. Получение жидкой трансглутаминазы
-140 мВ
соответствует станд.
[0061] Пример 16
Компоненты в формуле препарата из Примера 15 гомогенно смешивают для получения жидкого препарата трансглутаминазы и измеряют соответствующие параметры. Жидким препаратом трансглутаминазы заполняют непрозрачные бутыли из ПЭТ объемом 1 л в открытых условиях. После хранения при комнатной температуре в течение 180 дней наблюдают внешний вид жидкого ферментного препарата, и измеряют ферментативную активность и индексы микроорганизмов. Результаты показывают, что после хранения при комнатной температуре в течение 180 дней степень консервации ферментативной активности достигает 88%, и индексы микроорганизмов соответствуют требованиям, таким образом, получают стабильный жидкий препарат трансглутаминазы с ферментативной активностью 101 Ед/мл, водной активностью 0,85 и окислительно-восстановительным потенциалом -38 мВ. Упаковкой для ферментного препарата служит непрозрачный материал, и он не оказывает значительного эффекта на стабильность фермента.
[0062] Пример 17
После хранения при комнатной температуре в течение 180 дней измеренная ферментативная активность жидкого препарата трансглутаминазы, полученного в Примере 7, составляет 98,79 Ед/мл. Его применяют в производстве колбасы. Конкретная формула препарата и способ представлены в Таблице 24-1. Доступный для приобретения препарат трансглутаминазы в форме порошка (от Kinry Biotech (Jinan) Co., Ltd.) применяют в качестве контроля. Его измеренная ферментативная активность составляет 100 Ед/г перед применением.
[0063] Таблица 24-1. Применение жидкой, порошковой трансглутаминазы в производстве колбасы
После изготовления колбасы конечный продукт тестировали для определения показателей качества, таких как прочность геля, эластичность и органолептическая оценка. Результаты экспериментов показаны в Таблице 24-2.
[0064] Таблица 24-2. Действие препарата трансглутаминазы в жидкой форме и форме порошка на показатели колбасы
Результаты экспериментального теста показывают, что жидкий препарат трансглутаминазы имеет хороший эффект применения в производстве колбасы и имеет значительно улучшенные показатели качества колбасных продуктов, такие как сила геля и эластичность, в сравнении с порошковым препаратом трансглутаминазы при такой же дозе. Потери при готовке в некоторой степени, но не существенно улучшены, а органолептическая оценка значительно улучшенв.
[0065] Пример 18
Продукт жидкой трансглутаминазы, полученный в Примере 5 (99,5 Ед/мл), применяют в производстве тофу (соевого творога) Чиба. Доступные для приобретения порошковые ферментные препараты, продукт A (трансглутаминаза, производитель: Taixing Dongsheng Bio-Tech Co., Ltd., тип TG-TI, партия № B20150926, номинальная ферментативная активность: 116 Ед/г, действительная ферментативная активность, измеренная в лаборатории авторов изобретения: 108 Ед/г), и продукт B (трансглутаминаза, производитель: Taixing Yiming Biological Co. Ltd., тип TG-B, партия № 20150824, номинальная ферментативная активность: 110 Ед/г, действительная ферментативная активность, измеренная в лаборатории авторов изобретения: 100Ед/г) применяют в качестве контролей. Производителем изолятов соевого белка являлся Shandong Yuwang Group; денатурированный крахмал из маниоки получали от Rose Brand; соевое масло предоставлено COFCO Corporation; I+G и соль подливки были куплены в супермаркете METRO; и контроль C представлял собой порошок ферментного препарата Biobond TG-I производства Kinry Biotech (Jinan) Co., Ltd., действительная измеренная ферментативная активность: 110 Ед/мл. Тофу Чиба получают согласно формуле и способу, представленному в Таблице 25-1.
[0066] Таблица 25-1. Применение жидкой и порошковой трансглутаминазы в производстве тофу Чиба
Тофу Чиба, полученный с использованием различных препаратов трансглутаминазы, тестировали на прочность геля, эластичность, цвет и блеск, вкусовое внечатление и т.д. Результаты показаны в Таблице 25-2.
Таблица 25-2. Оценка качества тофу Чиба, полученного с жидкой и порошковой трансглутаминазой
и аппетитный
Результаты экспериментального теста показывают, что жидкий препарат трансглутаминазы сравним с порошковыми препаратами трансглутаминазы для применения в производстве тофу Чиба, и порошковый препарат может быть полностью заменен жидким препаратом во время производства тофу Чиба. Тофу Чиба, полученный таким образом, имеет в некоторой степени улучшенное качество. Жидкий препарат трансглутаминазы имеет промышленное значение.
[0067] Приведенные выше примеры представляют собой лишь некоторые предпочтительные варианты осуществления и примеры применения настоящего изобретения, и настоящее изобретение ими не ограничивается. Специалист в области техники, к которой относится настоящее изобретение, легко может осуществить различные изменения и модификации настоящего изобретения. Любое изменение, эквивалентные замены, усовершенствование способов и т.п. в объеме идеи и замысла настоящего изобретения включены в объем притязаний настоящего изобретения.
Изобретение относится к биотехнологии. Представлены жидкий ферментный препарат трансглутаминазы и способ его получения. Жидкий ферментный препарат представляет собой жидкий препарат трансглутаминазы EC2.3.2.13, а его компоненты и количества являются следующими: жидкий препарат трансглутаминазы имеет ферментативную активность, равную 10-1000 Ед/мл, регулятор водной активности присутствует в количестве 30-80 мас./об.%, регулятор окислительно-восстановительного потенциала присутствует в количестве 0,0075-1 мас./об.%. Его способ получения включает очистку ферментного раствора, смешивание, стерилизацию, заполнение и получение конечного продукта. Изобретение позволяет получить стабильный при комнатной температуре активный препарат. 2 н. и 5 з.п. ф-лы, 1 ил., 25 табл., 18 пр.
1. Жидкий препарат трансглутаминазы EC2.3.2.13, способный храниться при комнатной температуре в течение 6 месяцев, поддерживая свою ферментативную активность свыше 80%, где жидкий препарат содержит:
трансглутаминазу EC2.3.2.13, имеющую ферментативную активность 10-1000 Ед/мл,
регулятор окислительно-восстановительного потенциала, который
представляет собой по меньшей мере один, выбранный из группы, состоящей из L-аскорбиновой кислоты и ее соли, L-серина и его соли, L-цистеина и его соли, восстановленного глутатиона, полифенола чая, гидролизата соевого белка, гидролизата пшеничного белка, гидролизата казеина, гидролизата хитозана, антиоксиданта листьев бамбука, экстракта розмарина, экстракта антиоксиданта лакрицы, супероксиддисмутазы, глюкозооксидазы, бисульфита натрия, метабисульфита натрия, метабисульфита калия, сульфита натрия, гипосульфита натрия и фитиновой кислоты, и
присутствует в количестве 0,0075-1 мас./об.%, и
регулятор водной активности, который
представляет собой по меньшей мере один, выбранный из группы, содержащей сорбит, мальтит, пропиленгликоль, глицерин, ксилит, полиэтиленгликоль, трегалозу, сахарозу, мальтозу, изомальтозу, мальтодекстрин, ксилит и маннит, и
присутствует в количестве 30-80 мас./об.%,
где жидкий препарат имеет
окислительно-восстановительный потенциал от -400 мВ до +50 мВ,
водную активность Aw ≤ 0,89, и
pH 5,0-9,0.
2. Жидкий препарат по п. 1, отличающийся тем, что его компоненты и их количества являются следующими:
жидкий препарат трансглутаминазы имеет ферментативную активность, равную 10-1000 Ед/мл,
пищевой консервант присутствует в количестве 0-0,1 мас./об.% и регулятор рН добавляют до конечного объема, равного 100%.
3. Жидкий препарат по п. 1, отличающийся тем, что жидкий ферментный препарат предпочтительно имеет следующие физико-химические свойства:
1) имеет pH 5,0-7,5;
2) имеет водную активность Aw 0,6-0,85 и
3) имеет окислительно-восстановительный потенциал от -400 мВ до 0 мВ.
4. Жидкий препарат по п. 2, отличающийся тем, что пищевой консервант выбирают из группы, содержащей ε-полилизин, натамицин, лизоцим, низин, сорбат калия, дегидроацетат натрия, диацетат натрия, метил-п-гидроксибензоат, этиллауроиларгинат HCl, метабисульфит калия и метабисульфит натрия.
5. Жидкий препарат по п. 2, отличающийся тем, что регулятор рН представляет собой один регулятор из хлористо-водородной кислоты, серной кислоты, уксусной кислоты, молочной кислоты, лимонной кислоты, яблочной кислоты, фитиновой кислоты, фосфорной кислоты, азотной кислоты, щавелевой кислоты, гидроксида натрия, гидроксида калия, карбоната натрия, бикарбоната натрия, карбоната калия, бикарбоната калия, цитрата тринатрия, цитрата трикалия, ацетата натрия, ацетата калия, лактата натрия, лактата калия, гидрофосфата динатрия, гидрофосфата дикалия, фосфата натрия, фосфата калия, водопроводной воды, очищенной воды и минеральной воды или буферной системы, состоящей из нескольких регуляторов рН.
6. Жидкий препарат по п. 1, отличающийся тем, что регулятор водной активности содержит один или несколько из сорбита, мальтита и глицерина; и регулятор рН представляет собой буфер, содержащий фосфорную кислоту, уксусную кислоту, молочную кислоту или лимонную кислоту или их соль.
7. Способ получения жидкого препарата по любому одному из пп. 1-6, характеризуемый следующими стадиями:
1) очистка ферментного раствора: подвергание неочищенного раствора трансглутаминазы EC2.3.2.13, полученного ферментацией Streptomyces mobaraensis, фильтрации под давлением, микрофильтрации и вторичной ультрафильтрации для получения очищенного концентрированного ферментного раствора;
2) смешивание: количественное определение массы очищенного концентрированного ферментного раствора, регулятора водной активности и регулятора окислительно-восстановительного потенциала, добавление пищевого консерванта, если он присутствует, и смешивание; добавление регулятора рН до конечного объема, равного 100%; после гомогенного смешивания тестирование и регуляция жидкого ферментного препарата для получения следующих параметров: pH 5,0-9,0, водная активность Aw ≤0,89 и окислительно-восстановительный потенциал от -400 мВ до 50 мВ;
3) удаление бактерий: фильтрация полученной в результате смеси через мембрану 0,1-0,22 мкм для стерилизации с последующим стерильным заполнением;
4) упаковка: упаковка жидкого ферментного препарата посредством стерильного заполнения или другого соответствующего процесса упаковки жидкостей,
где
регулятор окислительно-восстановительного потенциала
представляет собой по меньшей мере один, выбранный из группы, состоящей из L-аскорбиновой кислоты и ее соли, L-серина и его соли, L-цистеина и его соли, восстановленного глутатиона, полифенола чая, гидролизата соевого белка, гидролизата пшеничного белка, гидролизата казеина, гидролизата хитозана, антиоксиданта листьев бамбука, экстракта розмарина, экстракта антиоксиданта лакрицы, супероксиддисмутазы, глюкозооксидазы, бисульфита натрия, метабисульфита натрия, метабисульфита калия, сульфита натрия, гипосульфита натрия и фитиновой кислоты, и
присутствует в количестве 0,0075-1 мас./об.%, и
регулятор водной активности
представляет собой по меньшей мере один, выбранный из группы, содержащей сорбит, мальтит, пропиленгликоль, глицерин, ксилит, полиэтиленгликоль, трегалозу, сахарозу, мальтозу, изомальтозу, мальтодекстрин, ксилит и маннит, и
присутствует в количестве 30-80 мас./об.%.
| RU 2009134725 A, 27.03.2011 | |||
| RU 2010145064 A, 27.05.2012 | |||
| WO 2013064736 A1, 10.05.2013. |
Авторы
Даты
2020-01-29—Публикация
2016-05-16—Подача