Изобретение относится к микробиологии и биотехнологии и касается получения трансформантов дрожжей Pichia pastoris, способных продуцировать ксиланазу.
Ксилан является основным структурным полисахаридом растительных клеткок и вторым после целлюлозы наиболее распространенным полисахаридом в природе [Biotech. Genet Eng. Rev. 1995, 13, 100-131]. Это комплексный полисахарид, основная цепь которого состоит из β-(1-4) связанного ксилозного скелета с небольшим количеством β-(1-3) ответвлений [Macromol Rapid Commun., 2000, 21(9), 542-556. doi: 10.1002/1521-3927(20000601)21:9<542::AID-MARC542>3.0.CO;2-7].
Полная деградация ксилана требует комплекса ксиланолитических ферментов, включающих эндо-ксиланазу, ксилозидазу, глюкуронидазу, ацетилэстеразу и арабинофуранозидазу [Crit Rev Biotechnol., 2002, 22, 33-64, doi:10.1080/07388550290789450].
Основную роль в разрушении ксилана играет эндо-ксиланаза (эндо-1,4-β-ксиланаза, ЕС 3.2.1.8), которая катализирует случайный гидролиз ксилана до ксилололигосахаридов.
Ксиланазы широко используются в различных отраслях промышленности.
Так при кормопроизводстве введение ксиланаз уменьшает содержание некрахмальных полисахаридов, тем самым снижая вязкость корма в кишечнике животных и улучшая усвояемость и питательную ценность плохо разлагаемых кормов. [J. Anim. Sci., 2002, 80, 2773-2779; Br. Poult. Sci., 2003, 44, 60-66; Br. Poult. Sci., 2003, 44, 291-298]
Природными источниками ксиланаз являются различные микроорганизмы: бактерии, грибы, дрожжи и актиномицеты [FEMS Microbiology Reviews, 2005, 29 (1), 3-23].
Традиционно ферментные препараты, в состав которых входят ксиланазы, получают на основе нерекомбинантных или рекомбинантных штаммов грибов рода Trichoderma, Aspergillus или Penicillium. Однако грибные штаммы, помимо ксиланазы, продуцируют ряд других ферментов, относящихся к карбогидразам, а именно: целлюлазу, глюканазу, пектиназу и маннаназу, что не позволяет использовать их при производстве моноферментных препаратов.
Наиболее перспективным является создание продуцентов ферментов на основе рекомбинантных штаммов метилотрофных дрожжей Pichia pastoris. При использовании несбраживаемых источников углерода (глицерина, метанола и т.п.) дрожжи Pichia pastoris способны к росту с образованием биомассы высокой плотности, что позволяет получать значительные количества гетерологичного белка [Appl. Microbiol. Biotechnol, 2000, 54(6), 741-750]. При этом процесс культивирования метилотрофных дрожжей достаточно прост, поскольку их рост не блокируется продуктами метаболизма [FEMS Microbiol.Rev., 2000, 24:45-66, doi: 10.1111/j.l574-6976.2000.tb00532.x].
Известны примеры создания продуцентов ксиланазы на основе дрожжей Pichia pastoris.
Показано [Protein Expression and Purification 57 (2008), 101-107], что ген reBlxA из Bacillus licheniformis, кодирующий ксиланазу А, эффективно экспрессируется в клетках дрожжей Pichia pastoris, при этом активность рекомбинантной ксиланазы в культуральной жидкости составляет 122.9 U/mg.
Известны также рекомбинантные штаммы Pichia pastoris, продуцирующие ксиланазу из Streptomyces sp.FA1 [CN107142225A] и ксиланазу из Neocallimastix frontalis [CN104130951A].
В работе [Биотехнология, 2018, 34(6), в печати] описан ген xyl из Paenibacillus brasilensis кодирующий фермент эндо-1,4-β-ксиланазу (ЕС 3.2.1.8).
Поскольку гены ксиланаз различного происхождения экспрессируются в дрожжах Pichia pastoris с различной эффективностью [Биотехнология, 2018, 34(4), 26-36] важной задачей для конструирования эффективных продуцентов является выбор генов, кодирующих ксиланазу и эффективно работающих в дрожжах Pichia pastoris.
Задачей заявляемого изобретения является расширение арсенала рекомбинантных микроорганизмов, продуцирующих ксиланазу.
Задача решена путем получения трансформанта дрожжей Pichia pastoris, продуцирующего ксиланазу, содержащего ген xyl, кодирующий эндо-1,4-β-ксиланазу из Paenibacillus brasilensis или фермент, аминокислотная последовательность которого гомологична ей не менее, чем на 93%
К ферментам, аминокислотная последовательность которых гомологична эндо-1,4-β-ксиланазе из Paenibacillus brasilensis [NCBI: MK014302] не менее, чем на 93% относятся, например, эндо-1,4-β-ксиланаза из Paenibacillus polymyxa [NCBI: WP_061831741.1], или эндо-1,4-β-ксиланаза из Paenibacillus terrae [NCBI: WP_014280040.1], или эндо-1,4-β-ксиланаза из Paenibacillus peoriae [NCBI: WP_104496610.1], или эндо-1,4-β-ксиланаза из Paenibacillus jamilae [NCBI: WP_063212880.1.
Получение заявленных трансформантов включает введение гена xyl из Paenibacillus brasilensis в клетки дрожжей Pichia pastoris с помощью экспрессионной кассеты, включающей в свой состав ген xyl, промотор, работающий в дрожжах Pichia pastoris, сигнальный пептид для осуществления секреции фермента в культуральную жидкость, терминатор, маркерный ген и, предпочтительно, сайт для гомологичной интеграции в хромосому. Интеграция может быть осуществлена путем как гомологичной, так и негомологичной рекомбинации. Трансформацию экспрессионной кассеты в клетки дрожжей Pichia pastoris осуществляют любым подходящим методом, например, методом электоропорации [http://tools.thermofisher.com/content/sfs/manuals/pich_man.pdf) или методом с использованием полиэтиленгликоля или протопластов [http://www.thermofisher.com/order/catalog/product/K173001].
Конструирование экспрессионных кассет осуществляют стандартными методами генетической инженерии [Рыбчин В.Н. Основы генетической инженерии. - СПб.: СПбГТУ, 1999; Sambrook J., Maniatis Т., Fritsch Е. Molecular cloning: a laboratory manual. - N.Y.: Cold Spring Harbor Laboratory, 1989.] с использованием генетических элементов, подходящих для работы с, дрожжами Pichia pastoris. В качестве промоторов используют АОХ1, DAS, FLD1, ICL1, PHO89, THI11, ADH1, ENO1, GUT1, GAP, TEF1, PGK1, GCW14, G1, G6 или другие [Appl Microbiol Biotechnol, 2014, 98, 5301-5317]. В качестве сигнальных пептидов используют α-фактор, PHO1, SUC2, PHA-E, KILM1, pGKL, CLY, CLY-L8, K28 pre-pro-toxin или другие [Appl Microbiol Biotechnol., 2014, 98, 5301-5317]. В качестве селективных маркеров используют любые подходящие маркеры, например, гены резистентности к антибиотикам зеоцину, генетицину (G418) или бластицидину С, а также гены комплементирующие ауксотрофные мутации в геноме Pichia pastoris, например, HIS4, МЕТ2, ADE1, ARG4, URA3, URA5, GUT1 [Yeast 2005; 22, 249-270]. В качестве плечей для гомологичной интеграции используют последовательности генов АОХ1, HIS4 (http://www.thermofisher.com/order/catalog/product/V17520] или другие последовательности, гомологичные участкам хромосомы дрожжей Pichia pastoris.
Изобретение проиллюстрировано следующими фигурами.
Фиг. 1 Экспрессионная кассета 1
Фиг. 2 Электрофорез гена xyl Paenibacillus brasilensis.
Фиг. 3 Фингерпринт штамма Pichia pastoris ВКПМ Y-4393
Изобретение подтверждено следующими примерами.
Пример 1. Получение трансформанта дрожжей Pichia pastoris, несущего ген xyl из Paenibacillus brasilensis
При конструировании интегративной экспрессионной кассеты используют метод "фьюжн-пцр" [Gene., 1989, 15, 77(1), 61-68.]. В качестве источника гена xyl используют тотальную геномную ДНК Paenibacillus brasilensis X1 ВКПМ В-13092 [Биотехнология, 2018, 34(6) в печати]. Синтезируют ДНК гена xyl методом ПЦР с использованием праймеров XylP-f и XylP-r

Полученную последовательность ДНК встраивают в состав экспрессионной кассеты 1 (фиг. 1), в состав которой входят следующие генетические элементы:
1. Ген xyl Paenibacillus brasilensis, встроенный в единую рамку считывания с нуклеотидной последовательностью сигнального пептида α-фактороа, под контролем АОХ1 промотора;
2. Терминатор транскрипции ТТАОХ1;
3. Дрожжевой селективный маркер kan, фланкированный сайтами lox 66 и lox 71, под контролем дрожжевого TEF промотора и обуславливающий у дрожжей Pichia pastoris устойчивость к антибиотику генетицину (G418);
4. Область интеграции - нуклеотидная последовательность гена АОХ2.
Указанную интегративную экспрессионную кассету трансформируют в штамм Pichia pastoris ВКПМ Y-4392, полученный на основе штамма Pichia pastoris DSMZ 70877 интеграцией в хромосому кассеты Pcup-cre, состоящей из гена cre, кодирующего рекомбиназу бактериофага Р1 под контролем Pcup промотора из Saccharomyces cerevisiae.
Штамм Pichia pastoris ВКПМ Y-4392 предварительно выращивают в жидкой питательной среде YPD (мас. %: дрожжевой экстракт - 1, пептон - 2, вода - остальное) до концентрации 1×108 клеток на 1 мл. Клетки центрифугируют, промывают в ледяной стерильной воде, а затем в ледяном растворе 1М сорбитола. Затем клетки инкубируют в 25 мМ растворе дитиотрейтола в течение 15 минут и промывают в ледяном растворе 1М сорбитола. Обработанные таким образом клетки ресуспендируют в ледяном растворе 1 М сорбитола в концентрации 1-5×109 клеток на 1 мл. Аликвоту, объемом 40 мкл клеточной суспензии, переносят в охлажденный эппендорф, добавляют 400 нг ДНК экспрессионной интеграционной кассеты, и инкубируют во льду 5 минут. Смесь клеток и ДНК переносят в предварительно охлажденную кювету для электропорации. Электропорацию проводят при следующих условиях: 1,5 кВ, 400 Ом, 25uF. После порации добавляют 1 мл ледяного раствора 1М сорбитола.
Селекцию трансформантов ведут на агаризованной среде среде YPD (мас. %: дрожжевой экстракт - 1, пептон - 2, агар - 2, вода - остальное) с добавлением глюкозы (2 мас. %) в течение 5 суток при температуре 30°С. В качестве селективного агента добавляют антибиотик G418 в количестве 500 мкг/мл.
Для отбора наиболее продуктивных трансформантов проводят их культивирование в жидкой ферментационной питательной среде YP (мас. %: дрожжевой экстракт - 1, пептон - 2, агар - 2, вода - остальное) с добавлением метанола (3 мас. %) в 96-луночных планшетах при 30°С в течение 72 ч на качалке (250 об/мин). В качестве контроля используют штамм Pichia pastoris Y-4392.
Определение активности ксиланазы в культуральной жидкости проводят с использованием ДНС метода [Anal Chem., 1959, 31 (3), 426-428] в 96-луночном планшете следующим образом: в каждой лунке смешивают 25 мкл 1% раствора субстрата ксилана березы в 0,5 М ацетатном буфере (рН 6) и 25 мкл культуральной жидкости. Инкубацию проводят при 50°С 10 минут, после чего добавляют в лунку 50 мкл раствора ДНС. Планшет прогревают при 99°С 10 минут и измеряют оптическую плотность окрашенного раствора при длине волны 546 нм. В качестве стандарта используют раствор глюкозы.
По результатам ферментации отбирают наиболее продуктивный трансформант №378, который при культивировании в планшете синтезирует ксиланазу в количестве 212 ед/мл культуральной жидкости.
Для выщепления маркерного гена kanMX из экспрессионной кассеты, интегрированной в хромосому трансформанта №378, проводят индукцию гена cre, кодирующего рекомбиназу бактериофага Р1, встроенного в хромосому штамма Pichia pastoris Y-4392 (Mut+, INS Pcup-cre) и находящегося под контролем промотора Pcup. Индукция происходит в присутствии ионов меди. Для этого клетки трансформанта №378 выращивают в жидкой питательной среде YPD (мас. %: дрожжевой экстракт - 1, пептон - 2, вода - остальное) до концентрации 1×108 клеток на 1 мл, после чего добавляют раствор сульфата меди до концентрации 0,3 М, инкубируют в течении 3 часов, после чего клетки высевают на агаризованную питательную среду YPD (мас. %: дрожжевой экстракт - 1, пептон - 2, агар - 2, вода - остальное) с добавлением глюкозы (2 мас. %). Отбирают колонии, не способные к росту в присутствии антибиотика G418.
Таким образом отобран трансформант №378 kanMX- с выщепленным маркерным геном kanMX, способный к синтезу фермента эндо-1,4-β-ксиланазы Paenibacillus brasilensis который депонирован во Всероссийской Коллекции Промышленных Микроорганизмов (ВКПМ) как Pichia pastoris ВКПМ Y-4393.
Наличие в хромосоме штамма вставки гена xyl Paenibacillus brasilensis подтверждают методом полимеразной цепной реакции (ПЦР), для чего используют хромосомальную ДНК, выделенную из клеток штамма Pichia pastoris ВКПМ Y-4393 и специфические праймеры XylP-f и XylP-r

Режим реакции ПЦР:
95°С - 3 мин - 1 цикл
30 циклов:
95°С - 30 сек.
60°С - 30 сек.
72°С - 60 сек.
72°С - 5 мин. - 1 цикл
Для контроля величины амплифицированного фрагмента ДНК при электрофорезе использован молекулярный маркер GeneRuler 1 kb DNA Ladder (Fermentas) (линия 2, фиг. 2, размер фрагментов снизу вверх 10000, 8000, 6000, 5000, 4000, 3500, 3000, 2500, 2000, 1500, 1000, 750, 500, 250 п.н.). Наработка фрагмента ДНК размером 552 п.н. (линия 1 фиг. 2) свидетельствует о присутствии в хромосоме штамма вставки гена xyl Paenibacillus brasilensis
Результаты ПЦР-фингерпринта [Applied and Environmental Microbiology, Oct, 1999, 4351-4356] штамма Pichia pastoris ВКПМ Y-4393 представлены на фиг 3.
Фингерпринт проведен с использованием полимеразной цепной реакции (PCR) с использованием неспецифических праймеров М13 (линия 1 фиг. 3) и 1254 (линия 2 фиг. 3).
Праймер М13 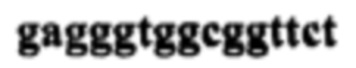
режим реакции:
1 цикл
95°С - 3 мин.
39 циклов
95°С - 30 сек.
45°С - 30 сек.
72°С - 2 мин.
1 цикл
72°С - 5 мин
Праймер 1254 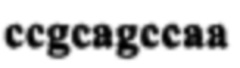
режим реакции:
1 цикл
95°С - 3 мин.
39 циклов
95°С - 30 сек.
48°С - 30 сек.
72°С - 1 мин.
1 цикл
72°С - 5 мин
Для контроля величины фрагментов ДНК при электрофорезе использован молекулярный маркер 1kb DNA GeneRuler (Fermentas) (линия 3, фиг. 3 размер фрагментов снизу вверх 10000, 8000, 6000, 5000, 4000, 3500, 3000, 2500,2000, 1500, 1000, 750, 500, 250 п.н.).
Пример 2. Продукция ксиланазы штаммом Pichia pastoris ВКПМ Y-4393
Посевную культуру выращивают в пробирках (50 мл) с 10 мл жидкой питательной среды YPD с добавлением глюкозы (2 мас. %) при 30°С в течение 24 ч на качалке с 250 об/мин. Посев ферментационной среды осуществляют в соотношении 1/10.
Ферментацию проводят при 30°С на качалке (250 об/мин) в питательной среде состава (мас. %): дрожжевой экстракт - 0,5, пептон - 1, вода - остальное с добавлением глюкозы (1 мас. %) в пробирках (50 мл) с рабочим объемом 5 мл. Через 18 часов добавляют метанол (1 мас. %) Ферментацию продолжают в течение 72 часов, добавляя метанол (1 мас. %) через каждые 24 часа. После окончания ферментации определяют количество фермента ксиланазы в культуральной жидкости с использованием ДНС метода [Anal. Chem., 1959, 31 (3), 426-428].
Через 72 часа ферментации количество фермента составило 1114 ед/мл культуральной жидкости.
Пример 3. Получение трансформантов дрожжей Pichia pastoris. несущих ген xyl из Paenibacillus polymyxa
При конструировании интегративной экспрессионной кассеты используют метод "фьюжн-пцр". В качестве источника гена xyl используют тотальную геномную ДНК Paenibacillus polymyxa ВКПМ В-3015 [Биотехнология, 2018, 34(4), 26-36]. Синтезируют ДНК гена xyl методом ПЦР с использованием праймеров XylPol-f и XylPol-r
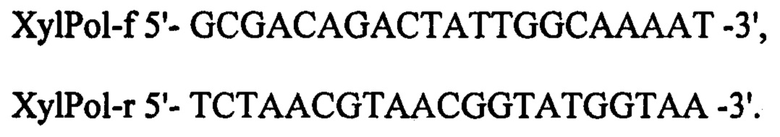
Полученную последовательность ДНК встраивают в состав экспрессионной кассеты, в состав которой входят следующие генетические элементы:
1. Ген xyl Paenibacillus polymyxa, встроенный в единую рамку считывания с нуклеотидной последовательностью сигнального пептида α-фактороа, под контролем АОХ1 промотора;
2. Терминатор транскрипции ТТАОХ1»
3. Дрожжевой селективный маркер - последовательность гена HIS4 под контролем дрожжевого TEF;
4. Область интеграции - нуклеотидная последовательность гена АОХ1.
Полученную интегративную экспрессионную кассету трансформируют в штамм Pichia pastoris GS115 (his4) так, как описано в примере 1.
Селекцию трансформантов ведут на агаризованной среде среде YNB (HiMedia Laboratories Pvt. Limited, Индия) с добавлением глюкозы (2 мас. %) в течение 5 суток при температуре 30°С.
Отбор наиболее продуктивных трансформантов и определение активности ксиланазы в культуральной жидкости проводят как описано в примере 1.
По результатам ферментации отобран наиболее продуктивный трансформант №56, который при культивировании в планшете синтезирует ксиланазу в количестве 113 ед/мл культуральной жидкости.
Пример 4. Получение трансформантов дрожжей Pichia pastoris, несущих ген xyl из Paenibacillus jamilae
При конструировании интегративной экспрессионной кассеты используют метод "фьюжн-пцр". В качестве источника гена xyl используют тотальную геномную ДНК Paenibacillus jamilae ВКПМ В-4226. Синтезируют ДНК гена xyl методом ПЦР с использованием праймеров Xyljam-f и Xyljam-r
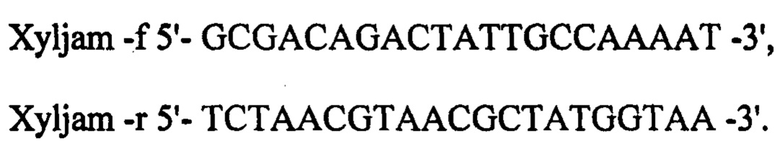
Полученную последовательность ДНК встраивают в состав экспрессионной кассеты, которая содержит следующие генетические элементы:
1. Ген xyl Paenibacillus jamilae, встроенный в единую рамку считывания с нуклеотидной последовательностью сигнального пептида α-фактороа, под контролем АОХ1 промотора;
2. Терминатор транскрипции ТТАОХ1;
3. Дрожжевой селективный маркер - последовательность гена HIS4 под контролем дрожжевого TEF;
4. Область интеграции - нуклеотидная последовательность гена АОХ1.
Трансформацию указанной интегративной экспрессионной кассеты в дрожжи Pichia pastoris GS115 (his4), отбор наиболее активных трансформантов и определение активности ксиланазы в культуральной жидкости проводят как описано в примере 3.
По результатам ферментации отобран наиболее продуктивный трансформант №118, который при культивировании в планшете синтезирует ксиланазу в количестве 89 ед/мл культуральной жидкости.
| название | год | авторы | номер документа |
|---|---|---|---|
| Трансформант дрожжей Pichia pastoris, продуцирующий эндо-1,4-β-ксиланазу из Paenibacillus brasilensis | 2019 |
|
RU2728033C1 |
| Штамм дрожжей Pichia pastoris, продуцирующий ксиланазу из Paenibacillus brasilensis | 2019 |
|
RU2728243C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris - продуцент ксиланазы | 2018 |
|
RU2701308C1 |
| Штамм дрожжей Pichia pastoris - продуцент ксиланазы | 2018 |
|
RU2701642C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris - продуцент ксиланазы из Pyromyces finnis | 2019 |
|
RU2725475C1 |
| Трансформант дрожжей Pichia pastoris, продуцирующий бета-глюканазу | 2019 |
|
RU2720914C1 |
| Дрожжи Komagataella kurtzmanii - рекомбинантный продуцент бета-глюканазы | 2019 |
|
RU2736440C1 |
| Рекомбинантный штамм дрожжей Komagataella kurtzmanii - продуцент бета-глюканазы из Paenibacillus jamilae | 2019 |
|
RU2730577C1 |
| Трансформант дрожжей Komagataella kurtzmanii, продуцирующий бета-глюканазу | 2019 |
|
RU2722563C1 |
| Штамм Komagataella phaffii T07/pPZL-4x-OA-xyl-AsOr, обладающий способностью продуцировать ксиланазу из грибов вида Aspergillus oryzae | 2022 |
|
RU2796447C1 |


Изобретение относится к микробиологии и биотехнологии, в частности к трансформанту дрожжей Pichia pastoris, продуцирующему ксиланазу и содержащему ген xyl, кодирующий эндо-1,4-β-ксиланазу из Paenibacillus brasilensis или фермент, аминокислотная последовательность которого гомологична ей не менее чем на 93%. 1 з.п. ф-лы, 3 ил., 4 пр.
1. Трансформант дрожжей Pichia pastoris, продуцирующий ксиланазу, содержащий ген xyl, кодирующий эндо-1,4-β-ксиланазу из Paenibacillus brasilensis или фермент, аминокислотная последовательность которого гомологична ей не менее чем на 93%.
2. Трансформант по п. 1, в котором в качестве фермента, аминокислотная последовательность которого гомологична эндо-1,4-β-ксиланазе из Paenibacillus brasilensis не менее чем на 93%, используют эндо-1,4-β-ксиланазу из Paenibacillus polymyxa, или эндо-1,4-β-ксиланазу из Paenibacillus terrae, или эндо-1,4-β-ксиланазу из Paenibacillus peoriae, или эндо-1,4-β-ксиланазу из Paenibacillus jamilae.
| CN 107142225 A, 2017-09-08 | |||
| МУЗАЕВ Д | |||
| М | |||
| и др., Новые штаммы дрожжей Pichia pastoris - продуценты гетерологичных белков, Экологическая генетика, 2015, т.13, н.1, стр.10-15 | |||
| Рекомбинантный штамм дрожжей Pichia pastoris - продуцент ксиланазы | 2018 |
|
RU2701308C1 |
| КАЛИНИНА А.Н | |||
| и др., Сравнение ксиланаз различного происхождения в экспрессионной системе Pichia pastoris: экспрессия, биохимическая характеристика | |||
Авторы
Даты
2020-02-11—Публикация
2019-03-15—Подача