Область техники, к которой относится изобретение
Настоящее изобретение касается рекомбинантных вирусов MDV1 и их применения. В частности, изобретение касается новых рекомбинантных вирусов болезни Марека серотипа 1 и их применения для экспрессии или доставки представляющих интерес полипептидов животным, в особенности домашним птицам. Изобретение особенно подходит для вакцинации домашней птицы от птичьих патогенов.
Уровень техники
Мясо и яйца птицы являются важными источниками пищи, потребление которых постоянно возрастает из-за роста численности населения и их высокого соотношения цена-качество. Недавняя эпидемия птичьего гриппа обратила внимание общественности на здоровье домашней птицы, а также на их безопасность и безопасность пищевых продуктов. Всемирной проблемой стала технология вакцин для домашней птицы.
В качестве вакцины для птиц против целевых патогенов обычно применяются рекомбинантные вирусы, экспрессирующие белки патогенов. Вакцины, содержащие такие вирусы, индуцируют экспрессию чужеродных патогенных белков или их фрагментов в инфицированных клетках, которые впоследствии могут индуцировать специфический и защитный гуморальный иммунитет, а также и клеточный иммунитет.
Как известно, различные вирусы могут выживать в организме инфицированного животного в состоянии латентной или постоянной инфекции. Поэтому были разработаны такие вирусы, в которые встроены чужеродные гены, происходящие из патогена, для применения в качестве вирусно-векторных вакцин, увеличивающих продолжительность иммунитета у иммунизированных животных. Как правило, такие вирусные векторы (или рекомбинантные вирусы) получают на основе авипоксвирусов типа птичьих поксвирусов (EP-A-0,517,292), вирусов герпеса, в особенности HVT (напр., WO-A-87/04463, 5,980,906, 5,853,733), вируса болезни Ньюкасл (NDV) или птичьих аденовирусов. Эти рекомбинантные птичьи вирусы проявляют различные уровни защиты. В частности, поскольку поксвирусы, NDV и аденовирусы не сохраняются у кур, то длительного иммунитета не ожидается. Рекомбинантный HVT, экспрессирующий VP2 IBDV, проявил преимущества перед классическими вакцинами против IBD (Vectormune® IBD). Другие представляющие интерес HVT-векторы экспрессируют антигены NDV (Vectormune® ND) или ILTV (Vectormune® LT).
Одной из практических проблем с рекомбинантными вирусами на основе HVT является их интерференция при использовании нескольких вирусов в комбинации для придания иммуногенности против разных патогенов. Так, при смешивании двух разных rHVT, экспрессирующих различные антигены, снижается степень защиты по крайней мере против одного из заболеваний (напр., см. Slacum G. et al., 2009, The compatibility of HVT recombinants with other Marek’s disease vaccines, 58th Western Poultry Disease Conference, Sacramento, CA, USA, March 23-25, p 84).
Были разработаны мультивалентные HVT-векторы, которые могут экспрессировать два различных антигенных пептида (см. PCT/EP2013/056839) и потенциально преодолеть ограничения предшествующего уровня техники. Кроме того, изучаются новые вирусные серотипы с целью поиска альтернативных совместимых вирусных векторов. В этом отношении в экспериментах использовался MDV1, но полученные до сих пор рекомбинанты пока не дали удовлетворительных результатов.
Соответственно, по-прежнему существует потребность в новых альтернативных подходах к улучшению вакцинации у животных, особенно у домашней птицы, позволяющих стабильную экспрессию белка и, предпочтительно, одновременную защиту от нескольких заболеваний.
Cущность изобретения
В настоящем изобретении раскрыты новые рекомбинантные вирусы, подходящие для индуцирования сильной иммунной защиты у животных, которые, кроме того, могут применяться в сочетании с другими вирусными вакцинами для обеспечения широкого иммунитета. В частности, настоящее изобретение касается новых рекомбинантных вирусов болезни Марека серотипа 1 (“rMDV1”). В изобретении раскрыты новые генетические участки в геноме MDV1, которые обеспечивают эффективное клонирование и стабильную экспрессию чужеродных генов.
Итак, предметом изобретения являются рекомбинантные вирусы болезни Марека серотипа 1 (rMDV1), содержащие в своем геноме чужеродные гены, причем такие чужеродные гены располагаются в нетранслируемых генетических участках генома. Более предпочтительно нетранслируемые генетические участки располагаются в вирусном геноме между MDV010 и MDV016, между MDV033 и MDV034, между MDV071 и MDV072 или между MDV096 и MDV097.6.
Как изложено в экспериментальном разделе, такие конструкции позволяют значительно улучшить экспрессию и индуцировать сильный защитный иммунитет. Кроме того, вирусы по изобретению могут применяться в комбинации с другими вирусами типа HVT без перекрестной интерференции, вызывая при этом широкий иммунитет.
Другим предметом изобретения являются молекулы нуклеиновых кислот, содержащие геном rMDV1, как определено выше.
Изобретение также касается плазмид, содержащих молекулы нуклеиновых кислот, как определено выше.
Другим предметом изобретения являются клетки хозяина или культуры таких клеток, содержащие молекулы нуклеиновых кислот либо плазмиды или вирусы, как определено выше.
Следующим предметом изобретения является способ получения или воспроизведения rMDV1, включающий инфицирование компетентных клеток молекулами нуклеиновой кислоты или rMDV1, как определено выше, и извлечение rMDV1.
Следующим предметом изобретения является способ получения rMDV1, экспрессирующих чужеродные гены, причем способ включает введение чужеродного гена в нетранслируемый генетический участок генома, предпочтительно расположенный между MDV010 и MDV016, между MDV033 и MDV034, между MDV071 и MDV072 или между MDV096 и MDV097.6.
Другим предметом изобретения являются композиции, содержащие rMDV1 или нуклеиновые кислоты, как определено выше, и фармацевтически либо ветеринарно приемлемые эксципиенты или носители.
Следующим предметом изобретения являются вакцинные композиции, содержащие rMDV1 или нуклеиновые кислоты, как определено выше, фармацевтически или ветеринарно приемлемые эксципиенты или носители, а также необязательно подходящий адъювант. Такие вакцины могут применяться, к примеру, для иммунизации птиц типа домашней птицы.
Другим предметом изобретения являются rMDV1 либо композиции или вакцины, как определено выше, для применения при вакцинации птиц, предпочтительно кур.
Следующим предметом изобретения являются rMDV1 либо композиции или вакцины, как определено выше, для индукции или стимуляции иммунного ответа у птиц, предпочтительно кур.
Еще одним предметом изобретения являются рекомбинантные MDV1, как определено выше, для применения в комбинации с другим рекомбинантным герпесвирусом другого серотипа и экспрессирующим другой антиген для вакцинации птиц, предпочтительно кур, путем одновременного, раздельного последовательного или поочередного введения.
В другом аспекте изобретения предусмотрен способ вакцинации животных, включающий введение данным животным композиции, вакцины или вируса, как определено выше.
В следующем аспекте изобретения предусмотрен способ индуцирования иммуногенного или защитного ответа у животных против одного или нескольких патогенов птиц, включающий введение данным животным композиции, вакцины или вируса, как определено выше.
Изобретением также предусмотрены наборы для иммунизации птиц, которые содержат эффективное количество вакцины по изобретению и средство для введения данной вакцины данным птицам.
Изобретение может применяться для экспрессии полипептидов у любых животных, предпочтительно для вакцинации птиц, причем оно подходит для экспрессии одного или нескольких полипептидов или пептидов, в особенности иммуногенных пептидов патогенов птиц. Рекомбинантные вирусы MDV1 по изобретению предпочтительно представлены штаммом Rispens.
Краткое описание фигур
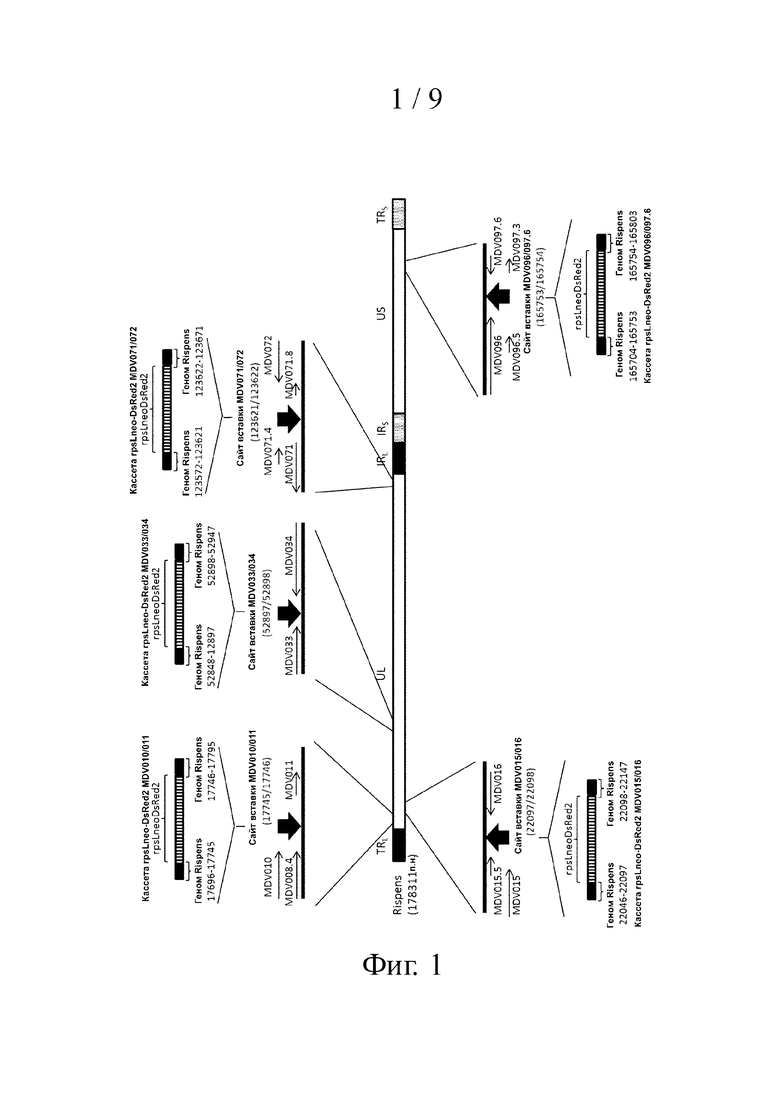
На фиг. 1 представлена схема генома вируса Rispens и расположение клонируемого участка рекомбинантного Rispens/rpsLneo-DsRed2, включая место вставки.
На фиг. 2 представлена схема генома рекомбинантного Rispens/rpsLneo-DsRed2 с указанием расположения Junction 1, Junction 2 и Junction 3, подвергаемых амплификации при реакциях ПЦР для подтверждения структуры генома вирусов.
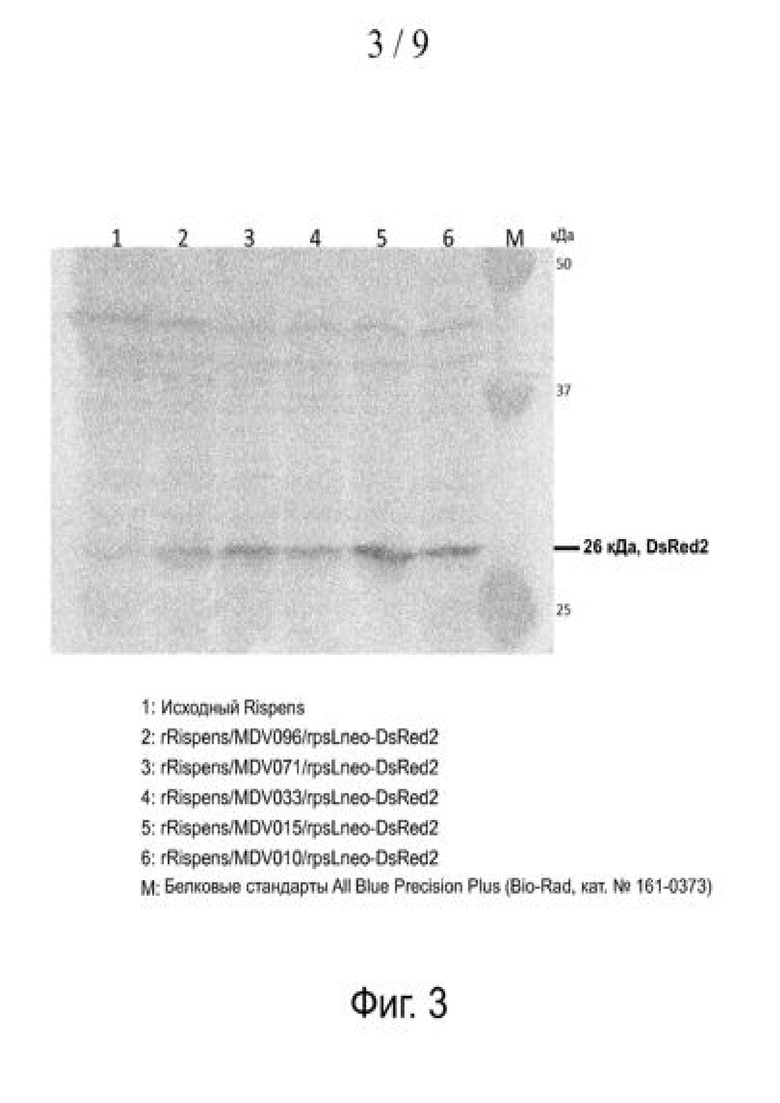
На фиг. 3 представлен вестерн-блот, показывающий экспрессию белка DsRed2 рекомбинантными вирусами Rispens/rpsLneo-DsRed2.
На фиг. 4 представлена кинетика роста рекомбинантных вирусов Rispens/rpsLneo-DsRed2 или исходного Rispens.
На фиг. 5 представлен средний размер бляшек у рекомбинантных вирусов Rispens/DsRed2 или исходного Rispens.
На фиг. 6 представлена схема генома вируса Rispens и расположение клонируемого участка рекомбинантного Rispens/IBD, включая место вставки.
На фиг. 7 представлена схема генома рекомбинантного Rispens/IBD с указанием расположения Junction 4 и Junction 5, подвергаемых амплификации при реакциях ПЦР для подтверждения структуры генома вирусов.
На фиг. 8 представлен вестерн-блот, показывающий экспрессию белка VP2 IBDV рекомбинантными вирусами Rispens/IBD.
На фиг. 9 представлены титры IBDV по ELISA у коммерческих белых кур леггорн, вакцинированных рекомбинантными вирусами Rispens/IBD, с помощью коммерческого набора IBD ELISA.
Раскрытие сущности изобретения
Настоящее изобретение в общем касается вирусов rMDV1, содержащих последовательности чужеродных генов, расположенные в геноме в определенных местах вставки. Настоящее изобретение также касается композиций, содержащих такие rMDV1, а также их применения для вакцинации животных, в особенности домашней птицы.
Настоящее описание будет легче понять с привлечением следующих определений.
Определения
Термином “вирус” обозначаются, в частности, вирусные частицы, содержащие молекулы нуклеиновой кислоты (напр., генома), инкапсулированные в капсиде или капсуле. Термином “вирус” также обозначаются вирусные векторы или выделенный вирусный геном.
Термином “рекомбинантные” обозначаются молекулы, которые были созданы, разработаны или модифицированы с использованием генетических технологий. В отношении вирусов термином “рекомбинантные” более конкретно обозначаются вирусы, геном которых (или геном их предков) был модифицирован путем введения по меньшей мере одной чужеродной нуклеиновой кислоты, то есть такой нуклеиновой кислоты (напр., ДНК), которая не встречается естественным образом в геноме вируса или же которая встречается естественным образом в данном геноме, но в другой форме или в другом положении.
В настоящем описании термином “нуклеиновая кислота” или “нуклеиновые кислоты” обозначаются любые молекулы нуклеиновой кислоты типа дезоксирибонуклеотидов (ДНК) или рибонуклеотидов (РНК), которые могут быть, к примеру, одно- или двухцепочечными. Нуклеиновые кислоты могут содержать или не содержать ORF. Молекулы нуклеиновой кислоты могут быть получены способами, известными per se в данной области, такими как искусственный синтез, рекомбинантные технологии, энзиматические технологии, воспроизведение в клетках хозяина либо их комбинации.
“Ген” означает молекулу или последовательность нуклеиновой кислоты, которая содержит открытую рамку считывания (ORF), кодирующую продукт типа полипептида (напр., пептид, белок и т.д.) или РНК.
Термин “нетранслируемый генетический участок” в настоящем изобретении относится к таким участкам в последовательности или молекуле нуклеиновой кислоты, которые не является частью кодирующей последовательности. Таким образом, термин “нетранслируемый генетический участок” в настоящем изобретении охватывает некодирующие участки вирусного генома, но не охватывает участки ORF.
Термин “птица” служит для обозначения всяческих птиц типа птиц из класса Aves, то есть позвоночных животных, которые являются пернатыми, крылатыми, двуногими, эндотермическими и яйцекладущими. В контексте изобретения птицы или виды птиц относятся, в частности, к птицам, представляющим экономический и/или агрономический интерес, таким как домашние птицы (как-то куры и индюки), водоплавающие птицы (как-то утки и гуси) и декоративные птицы (как-то лебеди и попугаи).
Термином “вакцина” в настоящем изобретении обозначаются вещества, которые могут использоваться для выработки, стимуляции или усиления иммунного ответа в организме.
“Иммунный ответ” означает развитие в организме клеточного и/или антительного иммунного ответа на представляющую интерес композицию или вакцину. Обычно “иммунный ответ” включает в себя вырабатывание антител, B-клеток, хелперных T-клеток и/или цитотоксических T-клеток, направленных специфически на антиген или антигены, входящие в данную композицию или вакцину. Предпочтительно иммунный ответ является защитным в том, что повышается устойчивость к новой инфекции и/или уменьшается клиническая тяжесть заболевания.
Вирусы болезни Марека серотипа 1
Вирусы болезни Марека серотипа 1 - это птичьи герпесвирусы. Они относятся к большой группе вирусов болезни Марека, которые включают серотип 2 и серотип 3, вирусы HVT. Хотя вирусы HVT широко изучены, MDV1 изучены меньше. В частности, этот вирус использовался гораздо меньше и имеется немного сообщений о подходящих рекомбинантах. В этом отношении предыдущие попытки использовать этот вирус по сути пытались клонировать чужую последовательность внутри гена (например, UL43) или в пределах регуляторного домена (напр., длинного IR) в геноме. Однако оказалось, что такие рекомбинанты не дают стабильной или сильной экспрессии. В результате MDV1 привлек меньше внимания, чем другие вирусы, такие, к примеру, как HVT.
Авторы настоящего изобретения провели дальнейшие исследования по MDV1 и смогли получить стабильные рекомбинанты. В частности, изобретатели обнаружили, что устойчивые рекомбинанты получаются при клонировании чужеродных последовательностей в нетранслируемые генетические участки генома. С такими рекомбинантами достигается сильная экспрессия чужеродных генов in vitro и возникает очень сильный защитный иммунный ответ (защита вплоть до 100%) in vivo. Таким образом, эти новые рекомбинанты представляют собой очень ценные векторы для переноса и экспрессии генов in vivo, особенно у домашней птицы, наиболее предпочтительно в целях вакцинации.
Итак, настоящее изобретение касается рекомбинантных вирусов MDV1, содержащих чужеродную нуклеиновую кислоту, клонированную в нетранслируемый генетический участок.
rMDV1 по изобретению могут быть получены из любых MDV1, предпочтительно таких серотипов или штаммов, которые не патогенны для данного вида животных (напр., птиц). Отмечено несколько штаммов MDV1, которые доступны из общественных коллекций, как-то штамм CVI988/Rispens, штамм C2 и штамм R2/23.
В предпочтительном воплощении rMDV1 представляет собой MDV1 штамма Rispens, более предпочтительно штамма CVI988 (см. полный геном, GenBank: DQ530348.1; Spatz et al., Journal of General Virology (2007), 88, 1080-1096), или такой MDV1, который по последовательности по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, на 96%, на 97%, на 98% или на 99% идентичен штамму CVI988.
Чужеродные нуклеиновые кислоты можно клонировать в любой нетранслируемый генетический участок генома MDV1. Однако наиболее предпочтительно нуклеиновые кислоты клонируют в нетранслируемые генетические участки, расположенные в геноме между MDV010 и MDV016, между MDV033 и MDV034, между MDV071 и MDV072 или между MDV096 и MDV097.6. В самом деле, изобретение показало, что именно эти нетранслируемые участки являются важными сайтами для вставки нуклеиновых кислот, не препятствуя эффективной репликации вируса и инфекции, и позволяют эффективно экспрессировать нужные продукты in vivo.
В более предпочтительном воплощении чужеродные нуклеиновые кислоты вводятся в нетранслируемые генетические участки генома, расположенные между MDV010 и MDV011, между MDV015.5 и MDV016, между MDV033 и MDV034, между MDV071 и MDV072 или между MDV096 и MDV097.6.
Еще более предпочтительно чужеродные нуклеиновые кислоты вводятся в нетранслируемые генетические участки, расположенные между MDV010 и MDV011, между MDV015.5 и MDV016 или между MDV071 и MDV072.
Нетранслируемый генетический участок, расположенный между MDV010 и MDV011, обычно соответствует нт. 17324-17878 генома MDV1. Клонирование может проводиться в любом положении в пределах данного участка, более предпочтительно между нт. 17500 и 17850, еще более предпочтительно между нт. 17700 и 17800. В конкретном воплощении клонирование проводится между нт. 17745 и 17746 (напр., RR043 и rRispens/MDV010/rpsLneo-DsRed2).
Нетранслируемый генетический участок, расположенный между MDV015.5 и MDV016, обычно соответствует нт. 21940-22256 генома MDV1. Клонирование может проводиться в любом положении в пределах данного участка, более предпочтительно между нт. 22000 и 22200, еще более предпочтительно между нт. 22050 и 22150. В конкретном воплощении клонирование проводится между нт. 22097 и 22098 (напр., RR044 и rRispens/MDV015/rpsLneo-DsRed2).
Нетранслируемый генетический участок, расположенный между MDV033 и MDV034, обычно соответствует нт. 52797-52942 генома MDV1. Клонирование может проводиться в любом положении в пределах данного участка, более предпочтительно между нт. 52800 и 52950, еще более предпочтительно между нт. 52850 и 52950. В конкретном воплощении клонирование проводится между нт. 52897 и 52898 (напр., RR045 и rRispens/MDV033/rpsLneo-DsRed2).
Нетранслируемый генетический участок, расположенный между MDV071 и MDV072, обычно соответствует нт. 123273-123904 генома MDV1. Клонирование может проводиться в любом положении в пределах данного участка, более предпочтительно между нт. 123400 и 123800, еще более предпочтительно между нт. 123500 и 123700. В конкретном воплощении клонирование проводится между нт. 123621 и 123622 (напр., RR046 и rRispens/MDV071/rpsLneo-DsRed2).
Нетранслируемый генетический участок, расположенный между MDV096 и MDV097.6, обычно соответствует нт. 165464-166202 генома MDV1. Клонирование может проводиться в любом положении в пределах данного участка, более предпочтительно между нт. 165500 и 166000, еще более предпочтительно между нт. 165700 и 165800. В конкретном воплощении клонирование проводится между нт. 165753 и 165754 (напр., RR047 и rRispens/MDV096/rpsLneo-DsRed2).
Следует отметить, что специалисты могут идентифицировать соответствующие положения сайта клонирования из любого штамма MDV1 просто путем совмещения последовательностей.
Чужеродные нуклеиновые кислоты можно клонировать в MDV1 с заменой всего или части (напр., от 1 до 500 нт.) нетранслируемого генетического участка или без удаления данного нетранслируемого генетического участка.
Кроме того, rMDV1 по изобретению могут содержать и несколько чужеродных генов.
Чужеродные гены в rMDV1 по изобретению обычно находятся под контролем транскрипционного промотора. Предпочтительно промотор клонируют вместе с чужеродным геном. Промотором может быть любой природный или синтетический промотор, происходящий из клеточных или вирусных генов. Примеры подходящих промоторов включают, к примеру, промотор куриного β-актина (Bac) или его производные типа Coa5, промотор Pec, самый ранний промотор ie1 цитомегаловируса мыши (Mcmv), промотор цитомегаловируса человека (Hcmv), промотор вируса SV40 обезьян и промотор вируса саркомы Рауса (RSV) или же любые их фрагменты, сохраняющие активность промотора.
Конструирование и клонирование вирусов может осуществляться методами, известными per se в данной области техники. Клонирование генов и конструирование плазмид хорошо известно рядовым специалистам и может в основном проводиться стандартными методами молекулярной биологии (Molecular Cloning: A Laboratory Manual. 4th Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, USA, 2012). Как правило, рекомбинантные вирусы получают посредством гомологической рекомбинации между вирусным геномом и конструкцией (напр., гомологичной плазмидой), содержащей вставляемую нуклеиновую кислоту, фланкированную нуклеотидами из сайта вставки, обеспечивающими рекомбинацию. Клонирование может проводиться с удалением эндогенных последовательностей или без него. В предпочтительном воплощении рекомбинантная последовательность клонируется с заменой по крайней мере части последовательности генома типа по меньшей мере 50 нуклеотидов или больше. Такое удаление повышает клонирующую способность вируса.
Для конструирования обычно сначала клонируют последовательность, содержащую целевой участок вставки, в подходящий вектор, получая гомологический вектор. Примеры векторов включают плазмиды типа pBR322, pBR325, pBR327, pBR328, pUC18, pUC19, pUC7, pUC8 или pUC9; фаги типа фага лямбда и фага M13; или космиды типа pHC79. Последовательность целевого участка встраивают в вектор стандартными методами клонирования. Используемая последовательность целевого участка предпочтительно имеет достаточную длину с тем, чтобы обеспечить последующую гомологическую рекомбинацию in vivo с вирусным геномом. Предпочтительно клонируемая последовательность целевого участка должна иметь длину по меньшей мере в 100 нуклеотидов, обычно больше 300, как-то от 500 до 2000 нуклеотидов. Затем в целевой участок, клонированный в вектор, вставляют чужеродную нуклеиновую кислоту (которая обычно содержит ген и промотор). Вставка предпочтительно должна проводиться таким образом, чтобы на каждой стороне клонированной вставки оставалась часть последовательности целевого участка достаточной длины для обеспечения гомологической рекомбинации (напр., по меньшей мере 50 нуклеотидов, предпочтительно по меньшей мере 100 нуклеотидов). Чужеродную нуклеиновую кислоту можно вводить в клонированный целевой участок классическими методами типа использования рестрикционных ферментов и лигирования. При необходимости в определенное место целевого участка можно ввести мутации для создания нового сайта расщепления для рестрикционного фермента. Для этого можно использовать стандартные методы мутагенеза, хорошо известные специалистам в данной области, такие, к примеру, как мутагенез in vitro или ПЦР. Затем гомологичные векторы, у которых в целевой участок была вставлена чужеродная нуклеиновая кислота, можно вводить в клетки, инфицированные MDV1 или трансфицированные геномом MDV1, используя известные методы, такие как электропорация, методы на основе фосфата кальция, липофектина и т.п. При этом получаются рекомбинантные вирусы при рекомбинации между вирусом и вектором в данных клетках. Полученные рекомбинантные вирусы можно подвергнуть отбору по генотипу или по фенотипу, используя известные методы, напр., посредством гибридизации, секвенирования, ПЦР или функционального анализа для выявления любого продукта, кодируемого чужеродной нуклеиновой кислотой. Отобранные рекомбинантные вирусы можно культивировать в крупном масштабе в культуре клеток, после чего можно выделять рекомбинантные вирусы.
Чужеродные гены
rMDV1 по изобретению могут содержать любую чужеродную нуклеиновую кислоту, предпочтительно любой чужеродный ген. Чужеродный ген может кодировать любой представляющий интерес продукт, как-то РНК или биологически активные и/или иммуногенные (напр., антигенные) белки, полипептиды или пептиды. В предпочтительном воплощении чужеродный ген кодирует антиген, еще более предпочтительно пептид или полипептид, полученный из антигена патогенного организма, способного вызвать инфекцию у животных, в особенности у птиц. Примеры возбудителей, вызывающих инфекции у птиц, включают вирусы, бактерии, грибы, простейшие и т.д. Иммуногенный (поли)пептид предпочтительно может представлять собой поверхностный белок, секретируемый белок или структурный белок данного патогена либо происходить из него или их фрагментов. Полипептид может происходить из любого источника, напр., вирусного, прокариотического, эукариотического или синтетического.
В предпочтительном воплощении чужеродный ген кодирует антигенный пептид возбудителя заболевания птиц.
Конкретные примеры возбудителей заболеваний включают, без ограничения, вирус птичьего гриппа, птичий парамиксовирус типа 1, также называемый вирусом болезни Ньюкасл (NDV), птичий метапневмовирус, вирус болезни Марека, вирус болезни Гумборо, также называемый вирусом инфекционного бурсита (IBDV), вирус инфекционного ларинготрахеита (ILVT), вирус инфекционного бронхита (IBV), Escherichia coli, Salmonella sp., Pasteurella multocida, Riemerella anatipestifer, Ornithobacterium rhinotracheale, Mycoplasma gallisepticum, Mycoplasma synoviae, микроорганизмы Mycoplasma, инфицирующие различные виды птиц, или кокцидии.
Предпочтительно чужеродный ген кодирует антиген, выбранный из белка F NDV, белка HN NDV, белка VP2 IBDV, белка gB ILTV, белка 40K Mycoplasma galisepticum или поверхностного белка гемагглютинина (HA) вируса птичьего гриппа либо их иммуногенных фрагментов. В контексте изобретения термином “фрагмент” белка предпочтительно обозначаются фрагменты, содержащие по меньшей мере 5 последовательных аминокислотных остатков данного белка, еще более предпочтительно от 5 до 100. В предпочтительном воплощении такой фрагмент содержит по меньшей мере один эпитоп и/или является иммуногенным in vivo, то есть может вызывать образование антител, связывающих полноразмерный белок.
Конкретные примеры иммуногенных пептидов включают, к примеру, пептиды, содержащие аминокислотные остатки 1-453 полного VP2.
Предпочтительные rMDV1s
Один предпочтительный rMDV1 по изобретению содержит по меньшей мере
один чужеродный ген, кодирующий птичий антиген, клонированный в нетранслируемый генетический участок, расположенный между MDV010 и MDV011. Предпочтительно птичий антиген представляет собой белок VP2, HN или F либо его иммуногенный фрагмент.
Другой предпочтительный rMDV1 по изобретению содержит по меньшей мере один чужеродный ген, кодирующий птичий антиген, клонированный в нетранслируемый генетический участок, расположенный между MDV015.5 и MDV016. Предпочтительно птичий антиген представляет собой белок VP2, HN или F либо его иммуногенный фрагмент.
Еще один предпочтительный rMDV1 по изобретению содержит по меньшей мере один чужеродный ген, кодирующий птичий антиген, клонированный в нетранслируемый генетический участок, расположенный между MDV033 и MDV034. Предпочтительно птичий антиген представляет собой белок VP2, HN или F либо его иммуногенный фрагмент.
Еще один предпочтительный rMDV1 по изобретению содержит по меньшей мере один чужеродный ген, кодирующий птичий антиген, клонированный в нетранслируемый генетический участок, расположенный между MDV071 и MDV072. Предпочтительно птичий антиген представляет собой белок VP2, HN или F либо его иммуногенный фрагмент.
Еще один предпочтительный rMDV1 по изобретению содержит по меньшей мере один чужеродный ген, кодирующий птичий антиген, клонированный в нетранслируемый генетический участок, расположенный между MDV096 и MDV097.6. Предпочтительно птичий антиген представляет собой белок VP2, HN или F либо его иммуногенный фрагмент.
Культуры клеток
Рекомбинантные вирусы настоящего изобретения можно размножить в культурах любых компетентных клеток. После достижения необходимого роста вирусов клетки можно отделить от лунок с помощью скребка или трипсина, а инфицированные клетки отделить от супернатанта посредством центрифугирования.
Примеры компетентных клеток включают CEF, содержащие эмбрионы яйца, почечные клетки кур и др. Клетки или вирусы можно культивировать в культуральной среде типа MEM Игла, культуральной среде Leibowitz-L-15/McCoy 5A (1:1) примерно при 37°C в течение 3-6 дней. Инфицированные клетки обычно суспендируют в культуральной среде, содержащей 10% диметилсульфоксида (ДМСО), и хранят в замороженном виде под жидким азотом.
Композиции и вакцины
Изобретение также касается композиций типа вакцин, содержащих один или несколько рекомбинантных MDV1 по изобретению.
Композиции по изобретению могут содержать rMDV1 в фармацевтически или ветеринарно приемлемом носителе или эксципиенте. Композиции могут содержать и подходящие адъюванты.
rMDV1s по изобретению можно использовать в живом виде (напр., для получения живых вакцин) или же в инактивированном, ослабленном или убитом виде. Получение таких форм известно в данной области.
Вакцины по настоящему изобретению также могут содержать подходящий растворитель, такой, к примеру, как водный буфер или фосфатный буфер. Предпочтительно вакцины также содержат добавки. Добавки по настоящему изобретению могут быть получены из самых разных источников, включая различные белки и пептиды, полученные из животных (напр., гормоны, цитокины, костимулирующие факторы), и новые нуклеиновые кислоты, происходящие из вирусов и других источников (напр., двухцепочечная РНК, CpG) и пр., которые вводятся вместе с вакциной в количестве, достаточном для усиления иммунного ответа. Кроме того, различные комбинации вышеупомянутых веществ могут давать иммунопотенциирующие эффекты и поэтому могут составлять иммуностимуляторы по настоящему изобретению.
Вакцины по настоящему изобретению также могут быть составлены с одной или несколькими дополнительными добавками для поддержания изотоничности, физиологического рН и стабильности, например, с буфером типа физиологического раствора (0,85%), фосфатно-солевого буфера (PBS), цитратного буфера, трис(гидроксиметиламинометана (TRIS), трис-солевого буфера и др., или с антибиотиком, к примеру, неомицином или стрептомицином и пр.
Способом введения может быть любой способ, включая пероральное, глазное (напр., глазные капли), глазоносовое введение с помощью аэрозоля, интраназальное, клоакальное с кормом, с водой или при помощи спрея, in ovo, топически или посредством инъекции (напр., внутривенной, подкожной, внутримышечной, внутриглазничной, внутриглазной, интрадермальной и/или внутрибрюшинной) при вакцинации. Специалисты смогут легко адаптировать состав вакцинной композиции для каждого способа введения.
Каждая доза вакцины может содержать подходящую дозу, достаточную для получения защитного иммунитета у птиц. Оптимизация таких доз хорошо известна в данной области. Количество антигена на 1 дозу можно определить известными способами с использованием реакции антиген/антитело, например, методом ELISA.
Вакцины по изобретению можно вводить в виде однократных доз или в виде многократных доз в зависимости от протокола вакцинации.
Вакцины по настоящему изобретению имеют дополнительное преимущество в том, что они обеспечивают птицам защиту почти на 80% от целевых патогенов птиц.
Настоящее изобретение также касается применения вакцин, как описано выше, для иммунизации птиц типа домашней птицы, и способа иммунизации птиц путем введения иммунологически эффективного количества вакцины по изобретению. Вакцина преимущественно вводится интрадермально, подкожно, внутримышечно, перорально, in ovo, через слизистую или посредством глазоносового введения.
Настоящее изобретение также касается вакцинационных наборов для иммунизации птиц, которые содержат эффективное количество поливалентной вакцины, как описано выше, и средство для введения данных компонентов данному виду. Например, такой набор включает в себя устройство для инъекции, заполненное вакциной по изобретению, и инструкции для внутрикожного, подкожного, внутримышечного или введения in ovo. В качестве альтернативы набор содержит устройство для распыления/аэрозоля или глазных капель, заполненное вакциной по изобретению, и инструкции для глазоносового введения, перорального или введения через слизистую оболочку.
Другие аспекты и преимущества изобретения будут изложены в следующем экспериментальном разделе, который иллюстрирует заявленное изобретение.
Примеры
Пример 1. Конструирование экспрессирующей кассеты rpsLneo-DsRed2
Конструировали фрагмент ДНК в 2,8 т.о. для кассеты rpsLneo-DsRed2 при помощи реакций ПЦР (фиг. 1). Вкратце, проводили три реакции ПЦР. Первую реакцию ПЦР проводили с помощью пары праймеров SEQ ID NO: 1 (5′-GGCCTGGTGATGATGGCGG′) и SEQ ID NO: 2 (5′-CCATGGTGCTGCGCTCAGAA GAACTCGTCA-3′) с матрицей из синтезированного фрагмента rpsLneo (SEQ ID NO: 3). Вторую реакцию ПЦР проводили с помощью пары праймеров SEQ ID NO: 4 (5′-ACGAGTTCTTCTGAGGGCC-3′) и SEQ ID NO: 5 (5′-TCGGAGGAGGCCATCCTTAAGAGCTG′) с матрицей из плазмиды pSI Mammalian Expression Vector (Promega, кат. № E1721). Третью реакцию ПЦР проводили с помощью пары праймеров SEQ ID NO: 6 (5′-TACAGCTCTTAAGGATGGCCTCCTCCGAGA-3′) и SEQ ID NO: 7 (5′-GCAGTGAAAAAA′) с матрицей из плазмиды pIRES2-DsRed2 (Clontech, кат. № 632420). Проводили еще одну реакцию ПЦР, используя в качестве матрицы смесь ПЦР-продуктов из первой и второй реакций ПЦР и в качестве праймеров - SEQ ID NO: 1 и SEQ ID NO: 5. Этот ПЦР-продукт смешивали с ПЦР-продуктом из третьей реакции ПЦР и использовали для последней реакции ПЦР с парой праймеров SEQ NO: 1 и SEQ NO: 7, получая кассету rpsLneo-DsRed2.
Пример 2. Конструирование кассет со вставками
Конструировали 5 фрагментов ДНК для кассет rpsLneo-DsRed2 с добавленными к ним с 5′- и 3′-стороны гомологичными последовательностями (по 50 п.о.) межгенных участков MDV010/011, MDV015.5/016, MDV033/034, MDV071/072 или MDV096/097.6 Rispens при помощи реакций ПЦР (фиг. 1). Проводили 5 реакций ПЦР, используя в качестве матрицы кассету rpsLneo-DsRed2. Использовали следующие пары праймеров:
SEQ ID NO: 8 (5′-CATCTTCGTATTCGTCACTTGCGAAATGGCCTGGTAATTATAACAT TGGGGGCCTGGTGATGATGGCGGG-3′) и SEQ ID NO: 9 (5′-CACAATCTCTCACTCCT CAAATTGCATTTTCAGTGCTGTTAAATACATTCGCAGTGAAAAAAATGCTTTA-3′) для сайта вставки MDV010/011, SEQ ID NO: 10 (5′-ATGAATAAAGTGAGACTTATAATA CTTATTGCATAGATGTGTTTTATTACGGCCTGGTGATGATGGCGGG-3′) и SEQ ID NO: 11 (5′-TATTATAACATACTTGTAGGTAATAAACAAACTACCCCTGTAAAAGGCAAGCA GTGAAAAAAATGCTTTA-3′) для сайта вставки MDV015/016, SEQ ID NO: 12 (5′-T ACCTGAAATGTGATCGGACTTGGGAAAAATCTTCACGCGAAATAAATTCGGCCTGG TGATGATGGCGGG-3′) и SEQ ID NO: 13 (5′-TTTAATGCAAAAATAAATAAAGAACCT TTGGGAATAACAAGCTATGTATAGCAGTGAAAAAAATGCTTTA-3′) для сайта вставки MDV033/034, SEQ ID NO: 14 (5′-AAAAGTTATTAGTCATGCAAGCATCTGTCAAATA GCAATCACATAATGGAGGCCTGGTGATGATGGCGGG-3′) и SEQ ID NO: 15 (5′-TTT CAATGAGGAGAAGGTTCCCCTCATTATGCAGCTTTGAGGCCTTTGATGCAGTGAAAAAAATGCTTTA-3′) для сайта вставки MDV071/072 или SEQ ID NO: 16 (5′-GATC CGAAAATATATCATGCAAATAAGCATGTTCTAGCACCACTGCAACAGGCCTGGTGA TGATGGCGGG-3′) и SEQ ID NO: 17 (5′-TGCTCGGAGGCAATGGTTCAACTATTCT TTCCGGAAATCGATAAACCACAGCAGTGAAAAAAATGCTTTA-3′) для сайта вставки MDV096/097.6. Полученные ПЦР-фрагменты подвергали электрофорезу и очищали.
Пример 3. Конструирование рекомбинантных Rispens, несущих ген rpsLneo-DsRed2
Конструирование рекомбинантных Rispens, несущих ген rpsLneo-DsRed2, проводили путем гомологической рекомбинации в E. coli. Штамм DH10B E. coli, несущий геном Rispens в виде бактериальных искусственных хромосом (BAC), подвергали трансфекции 0,1 мкг одной из вставочных кассет. Трансфекцию проводили методом электропорации с помощью Gene Pulser Xcell (Bio-Rad Laboratories) при 1,75 кВ, 25 мкФ и 200 Ом. После трансфекции высеивали E. coli на чашки с агаром Luria-Bertani (LB) и инкубировали в течение ночи при 30°C. Клоны E. coli, несущие соответствующие вставки, содержащие ген rpsLneo-DsRed2, идентифицировали методом ПЦР, используя пары праймеров, амплифицирующие участки между геном rpsLneo-DsRed2 и каждым сайтом вставки участка генома Rispens (фиг. 2). Использовали праймеры SEQ ID NO: 6 и SEQ ID NO: 18 (5′-GTGCGAGATTATTCCTTTTAAGGAATACTC-3′) для сайта вставки MDV010/011, SEQ ID NO: 19 (5′-GGACAAATTTCCTCATATAAGTGGAGAAG-3′) для сайта вставки MDV015/016, SEQ ID NO: 20 (5′-CGAGAACTGATTGCAGGAGGGAATTCATCC-3′) для сайта вставки MDV033/034, SEQ ID NO: 21 (5′-CATGTAGACATAGACACACAGAA TATATCC-3′) для сайта вставки MDV071/072 или SEQ ID NO: 22 (5′-CATCATAG TTGTATGTTCGACGAATTAAGC-3′) для сайта вставки MDV096/097.6, соответственно. Из клонов E. coli с соответствующими вставками экстрагировали ДНК модифицированных BAC Rispens и трансфицировали ею клетки CEF с помощью Nucleofector II (Lonza, Basel, Switzerland). Трансфицированные клетки вносили в смесь среды Leibovitz’s L-15 (Life Technologies Corp., кат. № 41300-39) и среды McCoy’s 5A (Life Technologies Corp., кат. № 21500-061) (1:1) с 4% телячьей сыворотки [среда LM (+)] и высеивали в 96-луночные планшеты для тканевых культур, а затем инкубировали при 37°C в 4-5% CO2 в течение 5-7 дней до появления видимых бляшек Rispens.
Пример 4. Проверка структуры генома
Структуру генома у рекомбинантных Rispens/rpsLneo-DsRed2 проверяли путем ПЦР-амплификации трех стыковочных участков (Junction 1, Junction 2 и Junction 3, фиг. 2) на каждом конце вставленных генов. Пары праймеров при реакциях ПЦР для Junction 1 описаны в эксперименте 3. При реакциях ПЦР для Junction 2 использовали следующие пары праймеров: SEQ ID NO: 23 (5′-TCAGAAGAACTCGTCAAGAAGGC-3′) и SEQ ID NO: 24 (5′-AAATCAGATCGGTTGTCTACTTCGAGTATG-3′) для rRispens/MDV010/DsRed2, SEQ ID NO: 25 (5′-AGACTATATGCTTTTCTTGAATACGACTAG-3′)
для rRispens/MDV015/rpsLneo-DsRed2, SEQ ID NO: 26 (5′-TAAAGACATTGATCCCAT AGACGTCGCG-3′) для rRispens/MDV033/rpsLneo-DsRed2, SEQ ID NO: 27 (5′-AGACA TGTAAAATGGTTGTACTGAAATTCG-3′) для rRispens/MDV071/rpsLneo-DsRed2 или SEQ ID NO: 28 (5′-ACTGATATGTACATATTTAAACTTAATGGG-3′) для rRispens/MDV096/DsRed2, соответственно. Для Junction 3 использовали SEQ ID NO: 18 и SEQ ID NO: 24 (rRispens/MDV010/rpsLneo-DsRed2), SEQ ID NO: 19 и SEQ ID NO: 25 (rRispens//rpsLneo-DsRed2), SEQ ID NO: 20 и SEQ ID NO: 26 (rRispens/MDV033/rpsLneo-DsRed2), SEQ ID NO: 21 и SEQ ID NO: 27 (rRispens/MDV071/rpsLneo-DsRed2) или SEQ ID NO: 22 и SEQ ID NO: 28 (rRispens/MDV096/rpsLneo-DsRed2), соответственно. У всех рекомбинантных Rispens/rpsLneo-DsRed2 наблюдались ожидаемые размеры продуктов ПЦР, подтверждая, что эти рекомбинантные Rispens/rpsLneo-DsRed2 имеют ожидаемые структуры генома.
Пример 5. Экспрессия DsRed2 у рекомбинантных Rispens/rpsLneo-DsRed2
Экспрессию белка DsRed2 у рекомбинантных Rispens/rpsLneo-DsRed2 проверяли по флуоресценции DsRed2 или методом вестерн-блоттинга. Флуоресценцию DsRed2 проверяли на клетках CEF, инфицированных рекомбинантными Rispens. Вкратце, клетки CEF в 6-луночных планшетах инфицировали одним из рекомбинантных вирусов или исходным штаммом Rispens при множественности заражения примерно 0,001. Через 5 дней после инокуляции клетки возбуждали при 563 нм. Красная флуоресценция наблюдалась только в бляшках рекомбинантных Rispens/rpsLneo-DsRed2. Эти клетки, инфицированные исходным Rispens или одним из рекомбинантных вирусов, также использовали для анализа методом вестерн-блот. Вкратце, клетки обрабатывали трипсином и центрифугировали при 913×g в течение 5 мин. Осадок промывали PBS и ресуспендировали в 50 мкл PBS. После добавления такого же объема буфера для образцов 2×SDS (130 мМ трис-Cl, pH 6,8, 6% SDS, 20% глицерина, 10% 2-меркаптоэтанола и 0,01% бромфенолового синего) суспензию клеток кипятили в течение 5 мин. Образцы разделяли методом SDS-PAGE в 12% полиакриламидном геле и переносили на мембрану PVDF (Immobilon-P, Millipore). Мембрану полностью высушивали, а затем инкубировали с моноклональным антителом против DsRed (антитело Living Colors® DsRed, TaKaRa). После отмывки от моноклонального антитела против DsRed мембрану инкубировали с биотинилированным антителом против IgG мыши (Vector Laboratories, кат. № BA-9200), а затем с набором VECTASTAIN ABC-AP (Vector Laboratories, кат. № AK-5000). Белок, связавшийся с моноклональным антителом против DsRed, визуализировали добавлением раствора NBT/BCIP (Roche Applied Science, кат. № 1681451).
Как видно из фиг. 3, полосы белка в 26 килодальтон (кДа), то есть ожидаемого размера для белка DsRed2, наблюдались только на дорожках с клетками, инфицированными рекомбинантными вирусами.
Пример 6. Кинетика роста и морфология бляшек у рекомбинантных Rispens/rpsLneo-DsRed2
Сравнивали кинетику роста и морфологию бляшек у рекомбинантных вирусов Rispens/rpsLneo-DsRed2 и исходного Rispens. Вкратце, в 6-луночные планшеты высеивали 9,5×105 клеток CEF и 950 бляшкообразующих единиц одного из рекомбинантных вирусов Rispens/rpsLneo-DsRed2 или исходного штамма Rispens. Клетки собирали через 0, 24, 48, 72, 96, 120 или 144 часа. Клетки трипсинизировали и ресуспендировали в 1 мл среды LM и сразу же титровали методом бляшкообразования. Для анализа бляшкообразования клетки CEF инфицировали серийными 10-кратными разведениями трипсинизированных клеток. Через 4 дня визуализировали бляшки методом черных бляшек. Вкратце, клетки фиксировали смесью метанол:ацетон (1:2) и инкубировали с моноклональным антителом 2BN90 против Rispens (Avian Diseases 37: 561-567, 1993). Затем инкубировали с биотинилированным антителом против IgG мыши, а затем с набором VECTASTAIN ABC-AP, и окрашивали бляшки Rispens добавлением раствора NBT/BCIP. Количество бляшек подсчитывали макроскопически и рассчитывали средний размер 50 бляшек с помощью программы CellSens Standard (OLYMPUS) для морфологии бляшек.
Как видно из фиг. 4 и 5, все рекомбинантные вирусы Rispens/rpsLneo-DsRed2 по изобретению росли сравнимо с исходным Rispens.
Пример 7. Анализ стабильности рекомбинантных Rispens/rpsLneo-DsRed2 in vitro
Анализировали стабильность рекомбинантных Rispens/rpsLneo-DsRed2 in vitro на клетках CEF. Вкратце, клетки CEF в 6-луночных планшетах инфицировали одним из рекомбинантных вирусов Rispens/rpsLneo-DsRed2 при множественности заражения примерно 0,001. Через 3-4 дня после заражения инфицированные клетки трипсинизировали и переносили в новые 6-луночные планшеты с клетками CEF. Инфицированные клетки пересеивали по 15 раз, причем через каждые 5 пассажей проверяли структуру генома и экспрессию DsRed2. Структуру генома анализировали путем ПЦР-амплификации стыковочных участков (Junction 1, Junction 2 и Junction 3; фиг. 2). Используемые пары праймеров представлены в примере 4. У всех рекомбинантных Rispens/rpsLneo-DsRed2 наблюдались ожидаемые размеры продуктов ПЦР при всех пассажах. В соответствии с этим результатом, экспрессия DsRed2 во всех бляшках рекомбинантных Rispens/rpsLneo-DsRed2 на всех пассажах подтверждалась при флуоресцентной микроскопии.
Пример 8. Конструирование рекомбинантного MDV1 RR043
RR043 - это рекомбинантный вирус MDV1 по изобретению, в который клонирован антиген VP2 под контролем синтетического промотора Coa5 между MDV010 и MDV011 (RR043: Rispens/MDV010/Coa5-VP2stc).
Для конструирования вируса сначала конструировали гомологический вектор, который затем использовали для получения вируса при гомологической рекомбинации. Конструирование плазмид и манипуляции с ДНК в основном проводились в соответствии со стандартными методами молекулярной биологии (Molecular Cloning: A Laboratory Manual. 4th Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, USA, 2012).
Конструирование pUC18-MDV010-SfiI
Клонировали фрагмент ДНК в 1,2 т.п.н. из генома Rispens, фланкирующий заданный сайт вставки (межгенный участок MDV010/011, содержащий участки MDV010 и MDV011), при помощи реакций ПЦР, добавляя сайт распознавания SfiI на сайт вставки (фиг. 6). Вкратце, используя в качестве матрицы ДНК, экстрагированную из Rispens, проводили две реакции ПЦР. Использовали следующие пары праймеров: SEQ ID NO: 29 (5′-GCGCATGCGCACGCATATAGATCGAAC-3′) и SEQ ID NO: 30 (5′-CGGCCAATAA GGCCCCCAATGTTATAATTA-3′), SEQ ID NO: 31 (5′-GCGAATTCATAACAGAATGTCA CGATAAAG-3′) и SEQ ID NO: 32 (5′-GGGCCTTATTGGCCGAATGTATTTAACAGC-3′). Проводили еще одну реакцию ПЦР, используя в качестве матрицы смесь ПЦР-продуктов из двух предыдущих реакций ПЦР и в качестве праймеров SEQ ID NO: 29 и SEQ ID NO: 31. Полученный ПЦР-фрагмент клонировали в вектор pUC18 (GenBank Acc. No. L09136) после расщепления EcoRI и SphI, получая pUC18-MDV010-SfiI.
Конструирование гомологического вектора
Используя плазмиду pUC18-MDV010-SfiI, конструировали гомологический вектор, содержащий промотор и ген VP2 IBDV из стандартного провоцирующего штамма (VP2-STC). В этом эксперименте конструировали гомологическую плазмиду, содержащую частичную последовательность (SEQ ID NO: 33) ядра промотора Bac (промотора Coa5). Сначала расщепляли pUC18-MDV010-SfiI с помощью SfiI и дефосфорилировали с помощью щелочной фосфатазы из рекомбинанта S1B1 Shewanella sp. (PAP) (Funakoshi # DE110). Промотор Coa5 получали из плазмиды pGICOA (U.S. Pat. No. 6,866,852) путем расщепления BglI и XbaI и лигировали с фрагментом XbaI-EcoRI (6,3 т.н.) и фрагментом EcoRI-BglI (0,1 т.н.) из p45/46bacVP2-STC#11 (U.S. Pat. No. 6,764,684), получая p45/46VP2-STC#11. Затем вырезали кассету промотор Coa5-VP2-STC из p45/46COA5VP2-STC#11 путем расщепления BglI и лигировали с расщепленной SfiI pUC18-MDV010-SfiI, получая pUC18-MDV010-Coa5VP2stc. Эту плазмиду использовали для конструирования RR043.
Конструирование рекомбинантного RR043
Конструирование RR043 проводили путем гомологической рекомбинации. В первом продукционном эксперименте получали ДНК вируса Rispens дикого типа, как описано в Morgan et al. (Avian Diseases, 34: 345-351, 1990). Примерно 2 мкг ДНК Rispens и 1 мкг гомологической плазмиды трансфицировали примерно в 107 клеток CEF путем электропорации с помощью Nucleofector II (Lonza, Basel, Switzerland). Трансфицированные клетки вносили в среду LM (+), высеивали в 96-луночные планшеты для тканевых культур, а затем инкубировали при 37°C в 4-5% CO2 в течение 5-7 дней до появления видимых бляшек Rispens. Затем клетки отделяли от планшетов путем трипсинизации, переносили поровну в два 96-луночных планшета с CEF и инкубировали 4-6 дней до появления бляшек. Проводили скрининг методом черных бляшек с окрашиванием только бляшек, экспрессирующих белок VP2IBDV. Вкратце, один из двух планшетов фиксировали смесью метанол:ацетон (1:2) и инкубировали с моноклональным антителом R63 против VP2 IBDV (№ по ATCC: HB-9490). Затем инкубировали с биотинилированным антителом против IgG мыши (Vector Laboratories, кат. № BA-9200), а затем с набором VECTASTAIN ABC-AP (Vector Laboratories, кат. № AK-5000), причем бляшки, экспрессирующие белок VP2, окрашивали добавлением NBT/BCIP (Roche Applied Science, кат. № 1681451). Идентифицировали лунки, содержащие окрашенные рекомбинантные бляшки, и трипсинизировали клетки из соответствующих лунок в другом 96-луночном планшете. Затем клетки разбавляли свежими вторичными клетками CEF и переносили в 96-луночные планшеты для завершения первого раунда очистки. Процедуру очистки повторяли до тех пор, пока все бляшки не давали положительной окраски при анализе методом черных бляшек.
В другом продукционном эксперименте штамм DH10B E.coli, несущий геном Rispens в виде BAC, подвергали трансфекции с помощью 1 мкг гомологического вектора. Трансфекцию проводили методом электропорации с помощью Gene Pulser Xcell при 1,75 кВ, 25 мкФ и 200 Ом. После трансфекции высеивали E. coli на чашки с агаром LB и инкубировали в течение ночи при 37°C. Клоны E. coli, несущие соответствующие вставки, содержащие ген VP2, идентифицировали методом ПЦР, используя пары праймеров, амплифицирующие участок между геном VP2 и сайтом вставки участка генома Rispens. Использовали праймеры SEQ ID NO: 34 (5′-GAGCAACTTCGAGCTGATCC-3′) и SEQ ID NO: 24. Из клонов, содержащих вставку, экстрагировали ДНК BAC Rispens и трансфицировали ею клетки CEF с помощью Nucleofector II. Трансфицированные клетки CEF высеивали в 96-луночные планшеты и инкубировали при 37°C в 4-5% CO2 в течение 5-7 дней до появления видимых бляшек Rispens. Бляшки, экспрессирующие белок VP2, подвергали очистке, как описано выше.
Пример 9. Конструирование рекомбинантного MDV1 RR044
RR044 - это рекомбинантный вирус MDV1 по изобретению, в который клонирован антиген VP2 под контролем синтетического промотора Coa5 между MDV015 и MDV016 (RR044: Rispens/MDV015/Coa5-VP2stc).
Для конструирования вируса сначала конструировали гомологический вектор, который затем использовали для получения вируса при гомологической рекомбинации. Конструирование плазмид и манипуляции с ДНК в основном проводились в соответствии со стандартными методами молекулярной биологии (Molecular Cloning: A Laboratory Manual. 4th Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, USA, 2012).
Конструирование pUC18-MDV015-SfiI
Клонировали фрагмент ДНК в 1,2 т.п.н. из генома Rispens, фланкирующий заданный сайт вставки (межгенный участок MDV015/016, содержащий участки MDV015 и MDV016), при помощи реакций ПЦР, добавляя сайт распознавания SfiI на сайт вставки (фиг. 6). Вкратце, используя в качестве матрицы ДНК, экстрагированную из Rispens, проводили две реакции ПЦР. Использовали следующие пары праймеров: SEQ ID NO: 35 (5′-GCGGTACCGCCCTAGAACTCAGCCGAGT-3′) и SEQ ID NO: 36 (5′-AGGCCAATAA GGCCGTAATAAAACACATCT-3′), SEQ ID NO: 37 (5′-GCGAGCTCCGTCTTAACTATTA TGTGGATG-3′) и SEQ ID NO: 38 (5′-CGGCCTTATTGGCCTTGCCTTTTACAGGGG-3′). Проводили еще одну реакцию ПЦР, используя в качестве матрицы смесь ПЦР-продуктов из двух предыдущих реакций ПЦР и в качестве праймеров SEQ ID NO: 35 и SEQ ID NO: 37. Полученный ПЦР-фрагмент клонировали в вектор pUC18 (GenBank Acc. No. L09136) после расщепления KpnI и SacI, получая pUC18-MDV015-SfiI.
Конструирование гомологического вектора
Используя плазмиду pUC18-MDV015-SfiI, конструировали гомологический вектор, содержащий промотор и ген VP2 IBDV из стандартного провоцирующего штамма (VP2-STC). В этом эксперименте конструировали гомологическую плазмиду, содержащую частичную последовательность (SEQ ID NO: 33) ядра промотора Bac (промотора Coa5). Сначала расщепляли pUC18-MDV015-SfiI с помощью SfiI и дефосфорилировали с помощью щелочной фосфатазы из рекомбинанта S1B1 Shewanella sp. (PAP) (Funakoshi # DE110). Затем вырезали кассету промотор Coa5-VP2-STC из p45/46COA5VP2-STC#11 путем расщепления BglI и лигировали с расщепленной SfiI pUC18-MDV015-SfiI, получая pUC18-MDV015-Coa5VP2stc. Эту плазмиду использовали для конструирования RR044.
Конструирование рекомбинантного RR044
Конструирование рекомбинантного RR044 проводили путем гомологической рекомбинации, как описано в Примере 8. Клоны RR044, несущие соответствующую вставку, содержащую ген VP2, можно идентифицировать методом ПЦР, используя пару праймеров, амплифицирующую участок между геном VP2 и сайтом вставки участка генома Rispens, напр., SEQ ID NO: 34 и SEQ ID NO: 25.
Пример 10. Конструирование рекомбинантного MDV1 RR045
RR045 - это рекомбинантный вирус MDV1 по изобретению, в который клонирован антиген VP2 под контролем синтетического промотора Coa5 между MDV033 и MDV034 (RR045: Rispens/MDV033/Coa5-VP2stc).
Для конструирования вируса сначала конструировали гомологический вектор, который затем использовали для получения вируса при гомологической рекомбинации. Конструирование плазмид и манипуляции с ДНК в основном проводились в соответствии со стандартными методами молекулярной биологии (Molecular Cloning: A Laboratory Manual. 4th Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, USA, 2012).
Конструирование pUC18-MDV033-SfiI
Клонировали фрагмент ДНК в 1,2 т.п.н. из генома Rispens, фланкирующий заданный сайт вставки (межгенный участок MDV033/034, содержащий участки MDV033 и MDV034), при помощи реакций ПЦР, добавляя сайт распознавания SfiI на сайт вставки (фиг. 6). Вкратце, используя в качестве матрицы ДНК, экстрагированную из Rispens, проводили две реакции ПЦР. Использовали следующие пары праймеров: SEQ ID NO: 39 (5′-GCGGTACCTTCGCGAGTTGTGCGATCATC-3′) и SEQ ID NO: 40 (5′-AGGCCAATA AGGCCGAATTTATTTCGCGTG-3′), SEQ ID NO: 41 (5′-GCGAGCTCTTTGCCCATTTCT GGACTAGG-3′) и SEQ ID NO: 42 (5′-CGGCCTTATTGGCCTATACATAGCTTGTTA-3′). Проводили еще одну реакцию ПЦР, используя в качестве матрицы смесь ПЦР-продуктов из двух предыдущих реакций ПЦР и в качестве праймеров SEQ ID NO: 39 и SEQ ID NO: 41. Полученный ПЦР-фрагмент клонировали в вектор pUC18 (GenBank Acc. No. L09136) после расщепления KpnI и SacI, получая pUC18-MDV033-SfiI.
Конструирование гомологического вектора
Используя плазмиду pUC18-MDV033-SfiI, конструировали гомологический вектор, содержащий промотор и ген VP2 IBDV из стандартного провоцирующего штамма (VP2-STC). В этом эксперименте конструировали гомологическую плазмиду, содержащую частичную последовательность (SEQ ID NO: 33) ядра промотора Bac (промотора Coa5). Сначала расщепляли pUC18-MDV033-SfiI с помощью SfiI и дефосфорилировали с помощью щелочной фосфатазы из рекомбинанта S1B1 Shewanella sp. (PAP) (Funakoshi # DE110). Затем вырезали кассету промотор Coa5-VP2-STC из p45/46COA5VP2-STC#11 путем расщепления BglI и лигировали с расщепленной SfiI pUC18-MDV033-SfiI, получая pUC18-MDV033-Coa5VP2stc. Эту плазмиду использовали для конструирования RR045.
Конструирование рекомбинантного RR045
Конструирование рекомбинантного RR045 проводили путем гомологической рекомбинации, как описано в примере 8. Клоны RR045, несущие соответствующую вставку, содержащую ген VP2, можно идентифицировать методом ПЦР, используя пару праймеров, амплифицирующую участок между геном VP2 и сайтом вставки участка генома Rispens, напр., SEQ ID NO: 34 и SEQ ID NO: 26.
Пример 11. Конструирование рекомбинантного MDV1 RR046
RR046 - это рекомбинантный вирус MDV1 по изобретению, в который клонирован антиген VP2 под контролем синтетического промотора Coa5 между MDV071 и MDV072 (RR046: Rispens/MDV071/Coa5-VP2stc).
Для конструирования вируса сначала конструировали гомологический вектор, который затем использовали для получения вируса при гомологической рекомбинации. Конструирование плазмид и манипуляции с ДНК в основном проводились в соответствии со стандартными методами молекулярной биологии (Molecular Cloning: A Laboratory Manual. 4th Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, USA, 2012).
Конструирование pUC18-MDV071-SfiI
Клонировали фрагмент ДНК в 1,2 т.п.н. из генома Rispens, фланкирующий заданный сайт вставки (межгенный участок MDV071/072, содержащий участки MDV071 и MDV072), при помощи реакций ПЦР, добавляя сайт распознавания SfiI на сайт вставки (фиг. 6). Вкратце, используя в качестве матрицы ДНК, экстрагированную из Rispens, проводили две реакции ПЦР. Использовали следующие пары праймеров: SEQ ID NO: 43 (5′-GCGGTACCTCCATATATGTTTCCGTCCTG-3′) и SEQ ID NO: 44 (5′-TGGCCAATAA GGCCTCCATTATGTGATTGC-3′), SEQ ID NO: 45 (5′-GCGAGCTCATAACTGCAGAAA CCAAACG-3′) и SEQ ID NO: 46 (5′-AGGCCTTATTGGCCATCAAAGGCCTCAAAG-3′). Проводили еще одну реакцию ПЦР, используя в качестве матрицы смесь ПЦР-продуктов из двух предыдущих реакций ПЦР и в качестве праймеров SEQ ID NO: 43 и SEQ ID NO: 45. Полученный ПЦР-фрагмент клонировали в вектор pUC18 (GenBank Acc. No. L09136) после расщепления KpnI и SacI, получая pUC18-MDV071-SfiI.
Конструирование гомологического вектора
Используя плазмиду pUC18-MDV071-SfiI, конструировали гомологический вектор, содержащий промотор и ген VP2 IBDV из стандартного провоцирующего штамма (VP2-STC). В этом эксперименте конструировали гомологическую плазмиду, содержащую частичную последовательность (SEQ ID NO: 33) ядра промотора Bac (промотора Coa5). Сначала расщепляли pUC18-MDV071-SfiI с помощью SfiI и дефосфорилировали с помощью щелочной фосфатазы из рекомбинанта S1B1 Shewanella sp. (PAP) (Funakoshi # DE110). Затем вырезали кассету промотор Coa5-VP2-STC из p45/46COA5VP2-STC#11 путем расщепления BglI и лигировали с расщепленной SfiI pUC18-MDV071-SfiI, получая pUC18-MDV071-Coa5VP2stc. Эту плазмиду использовали для конструирования RR046.
Конструирование рекомбинантного RR046
Конструирование рекомбинантного RR046 проводили путем гомологической рекомбинации, как описано в Примере 8. Клоны RR046, несущие соответствующую вставку, содержащую ген VP2, можно идентифицировать методом ПЦР, используя пару праймеров, амплифицирующую участок между геном VP2 и сайтом вставки участка генома Rispens, напр., SEQ ID NO: 34 и SEQ ID NO: 27.
Пример 12. Конструирование рекомбинантного MDV1 RR047
RR047 - это рекомбинантный вирус MDV1 по изобретению, в который клонирован антиген VP2 под контролем синтетического промотора Coa5 между MDV096 и MDV097.6 (RR047: Rispens/MDV096/Coa5-VP2stc).
Для конструирования вируса сначала конструировали гомологический вектор, который затем использовали для получения вируса при гомологической рекомбинации. Конструирование плазмид и манипуляции с ДНК в основном проводились в соответствии со стандартными методами молекулярной биологии (Molecular Cloning: A Laboratory Manual. 4th Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, USA, 2012).
Конструирование pUC18-MDV071-SfiI
Клонировали фрагмент ДНК в 1,1 т.п.н. из генома Rispens, фланкирующий заданный сайт вставки (межгенный участок MDV096/097.6, содержащий участки MDV096 и MDV097.6), при помощи реакций ПЦР, добавляя сайт распознавания SfiI на сайт вставки (фиг. 6). Вкратце, используя в качестве матрицы ДНК, экстрагированную из Rispens, проводили две реакции ПЦР. Использовали следующие пары праймеров: SEQ ID NO: 47 (5′-GCGGTACCTTTTACTCACATCGCTATC-3′) и SEQ ID NO: 48 (5′-AGGCCAATAA GGCCTGTTGCAGTGGTGCTA-3′), SEQ ID NO: 49 (5′-GCGAGCTCGCTGCATATTGCA TCACTATA-3′) и SEQ ID NO: 50 (5′-AGGCCTTATTGGCCTGTGGTTTATCGATTT-3′). Проводили еще одну реакцию ПЦР, используя в качестве матрицы смесь ПЦР-продуктов из двух предыдущих реакций ПЦР и в качестве праймеров SEQ ID NO: 47 и SEQ ID NO: 49. Полученный ПЦР-фрагмент клонировали в вектор pUC18 (GenBank Acc. No. L09136) после расщепления KpnI и SacI, получая pUC18-MDV096-SfiI.
Конструирование гомологического вектора
Используя плазмиду pUC18-MDV096-SfiI, конструировали гомологический вектор, содержащий промотор и ген VP2 IBDV из стандартного провоцирующего штамма (VP2-STC). В этом эксперименте конструировали гомологическую плазмиду, содержащую частичную последовательность (SEQ ID NO: 33) ядра промотора Bac (промотора Coa5). Сначала расщепляли pUC18-MDV096-SfiI с помощью SfiI и дефосфорилировали с помощью щелочной фосфатазы из рекомбинанта S1B1 Shewanella sp. (PAP) (Funakoshi # DE110). Затем вырезали кассету промотор Coa5-VP2-STC из p45/46COA5VP2-STC#11 путем расщепления BglI и лигировали с расщепленной SfiI pUC18-MDV096-SfiI, получая pUC18-MDV096-Coa5VP2stc. Эту плазмиду использовали для конструирования RR047.
Конструирование рекомбинантного RR047
Конструирование рекомбинантного RR047 проводили путем гомологической рекомбинации, как описано в Примере 8. Клоны RR047, несущие соответствующую вставку, содержащую ген VP2, можно идентифицировать методом ПЦР, используя пару праймеров, амплифицирующую участок между геном VP2 и сайтом вставки участка генома Rispens, напр., SEQ ID NO: 34 и SEQ ID NO: 28.
Пример 13. Проверка структуры генома
Структуру генома у рекомбинантных Rispens/IBD проверяли по реакциям ПЦР-амплификации двух стыковочных участков (Junction 4 и Junction 5) на каждом конце вставленных генов. Расположение Junction 4 и Junction 5 в геноме рекомбинантных вирусов показано на фиг. 7. При реакциях ПЦР для Junction 4 использовали следующие пары праймеров: SEQ ID NO: 34 и SEQ ID NO: 24 для RR043, SEQ ID NO: 25 для RR044, SEQ ID NO: 26 для RR045, SEQ ID NO: 27 для RR046 или SEQ ID NO: 28 для RR047, соответственно. Для Junction 5 использовали SEQ ID NO: 51 (5′-GCCAGGGAATCCAGGG AAAAAGAC-3′) и SEQ ID NO: 18 для RR043, SEQ ID NO: 19 для RR044, SEQ ID NO: 20 для RR045, SEQ ID NO: 21 для RR046 или SEQ ID NO: 22 для RR047, соответственно. У всех рекомбинантных Rispens наблюдались ожидаемые размеры продуктов ПЦР, подтверждая, что эти рекомбинантные Rispens имеют ожидаемые структуры генома.
Пример 14. Экспрессия вставленного антигена у рекомбинантных Rispens
Экспрессию белка VP2 у RR043, RR044, RR046 и RR047 проверяли методом черных бляшек и методом вестерн-блоттинга. Процедуры для метода черных бляшек описаны в Примере 8. Вестерн-блоттинг проводили, используя клетки CEF, инфицированные рекомбинантными вирусами, и моноклональное антитело R63 против VP2 вируса IBDV. Вкратце, клетки CEF в 6-луночных планшетах инфицировали одним из рекомбинантных вирусов или исходным штаммом Rispens при множественности заражения примерно 0,1. Через три дня после инокуляции клетки обрабатывали трипсином и центрифугировали при 913×g в течение 5 мин. Осадок промывали PBS и ресуспендировали в 100 мкл PBS. После добавления такого же объема буфера для образцов 2×SDS суспензию клеток кипятили в течение 5 мин. Образцы разделяли методом SDS-PAGE в 12% полиакриламидном геле и переносили на мембрану PVDF (Immobilon-P, Millipore). Мембрану полностью высушивали, а затем инкубировали с моноклональным антителом R63. После отмывки от антитела R63 мембрану инкубировали с биотинилированным антителом против IgG мыши (Vector Laboratories, кат. № BA-9200), а затем с набором VECTASTAIN ABC-AP (Vector Laboratories, кат. № AK-5000). Белок, связавшийся с моноклональным антителом R63, визуализировали добавлением раствора NBT/BCIP (Roche Applied Science, кат. № 1681451).
Результаты представлены на фиг. 8. Они показывают, что полосы белка в 40 килодальтон (кДа), то есть ожидаемого размера для белка VP2, наблюдались на всех дорожках с зараженными рекомбинантными вирусами клетками. Экспрессия белка VP2 с рекомбинантами RR043 и RR044 была особенно сильной, о чем свидетельствуют очень заметные полосы.
Пример 15. Эффективность рекомбинантных Rispens in vivo на цыплятах
Оценивали эффективность рекомбинантных вирусов Rispens по изобретению, экспрессирующих ген VP2 IBDV, против заражения вирулентным IBDV. В этом исследовании использовались три рекомбинантных вируса Rispens/IBD (RR043, RR044 и RR046). Цыплят от коммерческих несушек (белый леггорн) с материнскими антителами в 1-дневном возрасте разделяли на пять групп и цыплят в группах 3-5 вакцинировали подкожно примерно по 3000 бляшкообразующих единиц (pfu)/0,2 мл одним из рекомбинантных Rispens (группа 3: RR043, группа 4: RR044, группа 5: RR046). Цыплят в группе 1 (неиммунизированный, незараженный отрицательный контроль) и цыплят в группе 2 (неиммунизированный, зараженный положительный контроль) не вакцинировали. У цыплят брали кровь каждую неделю в возрасте от 1 до 6 недель для оценки гуморального иммунитета против IBDV. Антитела против IBDV определяли с помощью коммерческого набора IBDV ELISA (Idexx Laboratories, FlockChek IBD). В 5-недельном возрасте все цыплята, за исключением группы 1, получали 103 средних яичных инфицирующих доз (EID50) стандартного провоцирующего штамма (STC) вирулентного IBDV перорально. Цыплят наблюдали ежедневно на такие клинические признаки, связанные с IBD, как депрессия и смерть. Через 7 дней после заражения цыплят подвергали аутопсии и проверяли на наличие макроскопических повреждений бурсы типа отека, изменения окраски, атрофии, кровоизлияния и желтых или студенистых экссудатов. При вскрытии также измеряли вес тела и бурсы для вычисления индекса B/B, то есть соотношения между весом бурсы и весом тела у зараженных птиц, деленного на такое же отношение у незараженных птиц.
Результаты приведены в табл. 1. У всех цыплят в группе 2 (зараженный положительный контроль) развивались макроскопические повреждения бурсы, типичные для IBD, тогда как все цыплята в группе 1 (незараженный отрицательный контроль) оставались свободными от таких повреждений. У цыплят во всех вакцинированных группах проявлялся очень сильный защитный иммунитет, предотвращающий возникновение заболевания. Поразительно, но степень защиты под действием RR043 (группа 3) составляла 100% (22/22), что очень замечательно. RR044 и RR046 также проявляли очень высокую степень защиты в 90% (группа 4) и 95% (группа 5), соответственно. Более того, индекс B/B у этих групп составлял 1,03 (RR043), 1,10 (RR044) и 1,01 (RR046), соответственно, свидетельствуя об отсутствии значительной атрофии в бурсе.
В заключение, rMDV1 по изобретению обеспечивают очень сильный гуморальный и защитный иммунитет.
Таблица 1. Защита рекомбинантными Rispens от заражения вирулентным IBDV у цыплят SPF (испытание на эффективность)
NINC = неиммунизированный, незараженный отрицательный контроль
NICC = неиммунизированный, зараженный положительный контроль




Изобретение относится к области биотехнологии и молекулярной биологии. Предложены рекомбинантный вирус болезни Марека серотипа 1 (rMDV1) для лечения птиц, содержащий в своем геноме чужеродный ген, в котором данный чужеродный ген располагается в нетранслируемом генетическом участке генома, и причем данный нетранслируемый генетический участок расположен в геноме между MDV010 и MDV011, между MDV015.5 и MDV016, между MDV033 и MDV034, между MDV071 и MDV072 или между MDV096 и MDV097.6, а также молекула нуклеиновой кислоты, клетка-хозяин, способ получения или воспроизведения rMDV1, композиция, вакцина, применение rMDV1 и набор для вакцинации. Изобретение может быть использовано для вакцинации домашней птицы от птичьих патогенов. 8 н. и 11 з.п. ф-лы, 9 ил., 1 табл., 15 пр.
1. Рекомбинантный вирус болезни Марека серотипа 1 (rMDV1) для лечения птиц, содержащий в своем геноме чужеродный ген, в котором данный чужеродный ген располагается в нетранслируемом генетическом участке генома, и причем данный нетранслируемый генетический участок расположен в геноме между MDV010 и MDV011, между MDV015.5 и MDV016, между MDV033 и MDV034, между MDV071 и MDV072 или между MDV096 и MDV097.6.
2. rMDV1 по п. 1, в котором чужеродный ген располагается в нетранслируемом генетическом участке генома, расположенном между MDV010 и MDV011, между MDV015.5 и MDV016 или между MDV071 и MDV072.
3. rMDV1 по п. 1 или 2, в котором последовательность чужеродного гена вставлена с заменой всего или части нетранслируемого генетического участка.
4. rMDV1 по п. 1 или 2, в котором последовательность чужеродного гена вставлена в нетранслируемый генетический участок без удаления данного нетранслируемого генетического участка.
5. rMDV1 по любому из предыдущих пунктов, в котором данный MDV1 представляет собой MDV1 штамма Rispens.
6. rMDV1 по любому из предыдущих пунктов, в котором данный чужеродный ген кодирует антиген, предпочтительно антиген патогена птиц, более предпочтительно выбранного из вирусного патогена, бактериального патогена, грибкового патогена и протозойного патогена.
7. rMDV1 по п. 6, в котором данный патоген выбран из вируса болезни Ньюкасл (NDV), вируса болезни Гумборо (вируса инфекционного бурсита, IBDV), вируса инфекционного ларинготрахеита (ILVT), вируса инфекционного бронхита (IBV), микоплазмы (MG) или кокцидий.
8. rMDV1 по п. 7, в котором чужеродный ген кодирует антиген VP2 IBDV, антиген HN NDV, антиген F NDV либо их иммуногенные фрагменты.
9. rMDV1 по любому из предыдущих пунктов, в котором чужеродный ген в данном геноме находится под контролем транскрипционного промотора.
10. rMDV1 по п. 9, в котором промотор выбран из промотора куриного β-актина (Bac) или его производного типа Coa5, промотора Pec, самого раннего промотора ie1 цитомегаловируса мыши (Mcmv), промотора цитомегаловируса человека (Hcmv), промотора вируса SV40 обезьян и промотора вируса саркомы Рауса (RSV) или же любых их фрагментов, сохраняющих активность промотора.
11. rMDV1 по п. 1, в котором данный rMDV1 содержит чужеродный ген, кодирующий VP2 IBDV, который располагается в нетранслируемом участке, расположенном в геноме между MDV010 и MDV011, MDV015.5 и MDV016, MDV033 и MDV034, MDV071 и MDV072 или MDV096 и MDV097.6.
12. rMDV1 по п. 1, в котором данный rMDV1 содержит чужеродный ген, кодирующий HN и/или F NDV, который располагается в нетранслируемом участке, расположенном в геноме между MDV010 и MDV011, MDV015.5 и MDV016, MDV033 и MDV034, MDV071 и MDV072 или MDV096 и MDV097.6.
13. Молекула нуклеиновой кислоты для продукции и воспроизведения rMDV1, содержащая геном rMDV1 по любому из предыдущих пунктов.
14. Клетка-хозяин для продукции и воспроизведения rMDV1, содержащая rMDV1 по любому из пп. 1-12 или молекулу нуклеиновой кислоты по п. 13.
15. Способ получения или воспроизведения rMDV1 по любому из пп. 1-12, включающий инфицирование компетентных клеток молекулой нуклеиновой кислоты по п. 13 или rMDV1 по п. 1 и извлечение rMDV1.
16. Композиция для лечения птиц, включающая эффективное количество rMDV1 по любому из пп. 1-12 и наполнитель.
17. Вакцина, подходящая для иммунизации птиц против патогена, включающая эффективное количество rMDV1 по любому из пп. 6-12, наполнитель и необязательно адъювант.
18. Применение rMDV1 по любому из пп. 6-12 для производства медикамента для иммунизации птиц против патогена.
19. Набор для вакцинации, предназначенный для иммунизации птиц, который содержит следующие компоненты:
a) эффективное количество вакцины по п. 17 и
b) средство для введения данной вакцины данным птицам.
| ZHANG ZHENJIE | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| SAKAGUCHI M | |||
| Protection of chickens with or without maternal antibodies against both Marek's and Newcastle diseases by one-time vaccination with recombinant | |||
Авторы
Даты
2020-02-14—Публикация
2016-01-29—Подача