Предлагаемое изобретение относится к области аналитической химии, а именно к методам определения концентрации компонентов электролитов для тепловых химических источников тока (ТХИТ) и может быть использовано для определения галогенидов щелочных металлов при их совместном присутствии в твердых литиевых электролитах.
Актуальность решаемой проблемы основана на необходимости определения индивидуальных концентраций галогенидов лития при разработке и исследовании составов литиевых электролитов для ТХИТ в электролитных массах, в которых присутствуют одновременно хлориды, бромиды, фториды лития и загустители на основе сложных солей алюминия. Трудности такого определения состоят в том, что указанные элементы являются представителями одной группы элементов - группы галогенов и обладают сходными химическими свойствами. Традиционными аналитическими методами определение примесных концентраций галогенов, как при совместном присутствии, так и по отдельности, было реализовано при сочетании физико-химических методов: нейтроноактивационного, рентгеноспектрального, или масс-спектрометрического методов анализа, атомно-эмиссионной спектрометрии с индукционно-связанной плазмой. Такие методы сложны и достаточно продолжительны во времени (трудозатратны), и не всегда доступны для реализации.
Анализ отобранной патентной информации показал, что проблема избирательного определения содержания отдельных компонентов сложных смесей решается сочетанием многосложных этапов экстракции, потенциометрического титрования с применением сочетания индикаторного ионоселективного и сравнительного электродов.
Из предшествующего уровня техники известен способ раздельного определения анионных, катионных и неионогенных поверхностноактивных веществ (ПАВ) методом потенциометрического титрирования анализируемых проб с использованием индикаторного ионоселективного твердоконтактного электрода и сравнительного хлоридсеребряного электрода и применением различных титрантов соответственно для анионных, катионных и неионогенных соединений (патент РФ №2141110, МПК G01N 27/42, публ. 10.11.99 г.)
Известен способ определения концентрации фторид-ионов в воде (патент РФ №2331873, МПК G01N 27/42, публ. 20.08.08 г.) с использованием для измерений фонового электролита, в качестве которого был выбран водный раствор химически активной азотной кислоты, фторидселективного электрода.
Известен в качестве прототипа заявляемого способ раздельного определения хлоридсодержащих соединений при их совместном присутствии (патент РФ №2210767, МПК G01N 31/16, публ. 20.08.03 г.), согласно которому проводят концентрирование хлоридсодержащих соединений жидкостной экстракцией с использованием в качестве дифференцирующего растворителя диметилформамида в различных объемных соотношениях к экстракту с последующим потенциометрическим титрованием экстракта раствором КОН в этиловом спирте.
К недостаткам аналогов относится отсутствие возможности раздельного определения близких по химическим свойствам галогенидов лития при их совместном присутствии в твердых пробах литиевого электролита для ТХИТ, содержащих дополнительно соединения алюминия.
Задачей авторов изобретения является разработка способа избирательного определения галогенидов лития в твердом электролите при их совместном присутствии и в присутствии соединений алюминия.
Технический результат, обеспечиваемый при использовании предлагаемого изобретения, заключается в обеспечении возможности определения индивидуальных концентраций галогенидов щелочных металлов и солей алюминия при их совместном присутствии в твердом литиевом электролите, повышения точности их определения, в сокращении продолжительности процесса и упрощении.
Технический результат достигается тем, что, в отличие от известного способа определения галогенсодержащих соединений, включающего подготовку пробы, проведение определения индивидуальных концентраций галоген - ионов, согласно изобретению, проводят предварительное измельчение перетиранием твердого образца электролита, затем отобранные и измельченные пробы твердого литиевого электролита направляют на раздельные этапы последовательного определения фторидов, бромидов и хлоридов, на каждом из которых проводят циклы специфических операций:
- для определения массовой доли фторидов в электролите используют гравиметрический метод после сплавления измельченной перетиранием пробы твердого литиевого электролита совместно с комплексным реактивом из кварцевого песка и углекислых солей калия и натрия, выщелачивания плава горячей дистиллированной водой, нейтрализациии раствора минеральными кислотами последовательно соляной, затем азотной кислотой, нагрева раствора до не более 40°С, отделения гидроксидов алюминия фильтрованием, осаждения фторидов контактированием с раствором уксуснокислого свинца и промывки осадка фторхлорида свинца при рН в диапазоне 3,5-4,6, сутки полученного осадка и окончательного определения массовой доли фторидов по математической формуле (1)

где CF - массовая доля фторидов, %;
mF - масса полученного осадка фторхлорида свинца, г;
mн F - масса навески пробы электролита, взятая при анализе на содержание фторидов, г;
0,0726 - коэффициент пересчета массы фторхлорида свинца на массу фторида;
200 - вместимость мерной колбы с раствором электролита, см3;
100 - объем аликвоты раствора электролита, см3.
В отсутствии алюминия для определения фторидов используют метод потенциометрического титрования с фторид- селективным электродом, для этого навеску измельченной пробы твердого литиевого электролита растворяют в разбавленном растворе соляной кислоты, в раствор помещают фторид- селективный и вспомогательный электроды и при постоянном перемешивании на магнитной мешалке проводят титрование фторидов из стеклянной бюретки раствором лантана азотнокислого с индикацией точки эквивалентности по рН- метру-иономеру.
Вычисление массовой доли фторидов проводят по формуле (2)

где CF - массовая доля фторидов, %;
VLa- объем раствора лантана азотнокислого, израсходованный на титрование, см3;
mн F - масса навески пробы электролита, взятая при анализе на содержание фторидов в отсутствии алюминия, г;
TLa-F - массовая концентрация раствора лантана азотнокислого по фториду, мг/см3;
- для определения массовой доли бромидов в электролите - из измельченной пробы твердого литиевого электролита готовят водный раствор с добавлением концентрированной серной кислоты с последующим контактированием нейтрализованного раствора с раствором калия йодноватокислого (с предварительно установленным коэффициентом объемного отношения между растворами калия йодноватокислого и натрия серноватистокислого), кипячением на плитке в течение 2 ч для удаления образовавшегося брома, охлаждением, перенесением в колбу, добавкой калиия йодистого, выстаиванием в темном месте для образования йода и титрованием раствором натрия серноватистокислого до перехода бурого окрашивания раствора в соломенно-желтое, с добавлением раствора крахмала и продолжением титрования до полного обесцвечивания раствора. Вычисление массовой доли бромидов в электролите проводили по математической формуле (3)
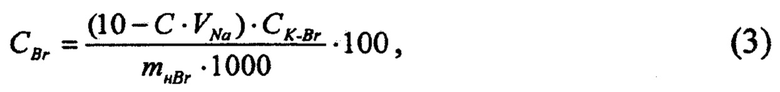
где CBr) - массовая доля бромидов в электролите, %;
10 - объем добавленного в избытке раствора калия йодноватокислого, см3;
mн Br - масса навески пробы электролита, взятая при анализе на содержание бромидов, г;
CK-Br - массовая концентрация раствора калия йодноватокислого по бромиду, мг/см3;
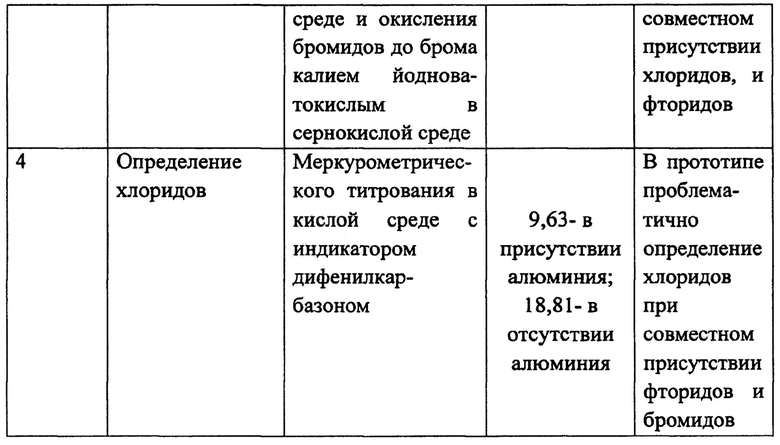
- для определения массовой доли хлоридов в электролите определяют разницу между суммарной величиной массовых долей бромидов и хлоридов, определенных методом меркурометрического титрования в кислой среде с индикатором дифенилкарбазоном, и предварительно установленной массовой долей бромидов в пробе, определяют израсходованный объем раствора реагента титрования - ртути (I) азотнокислой на титрование суммы хлоридов и бромидов, определяют израсходованный объем ртути (I) азотнокислой на титрование бромидов, после чего по разности объемов рассчитывают израсходованный объем ртути (I) азотнокислой на титрование хлоридов, и определяют соответствующую этому значению массовую долю хлоридов в литиевом электролите по формуле (4)
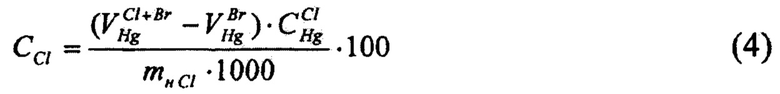
где CCl - массовая доля хлоридов в электролите, %;
 - объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
- объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
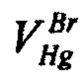 - объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
- объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
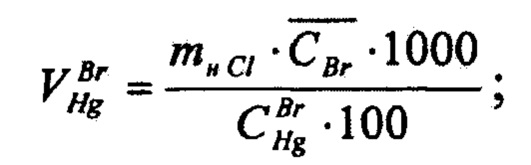
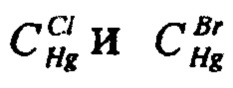 - массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
- массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
 - массовая доля бромидов в электролите, %;
- массовая доля бромидов в электролите, %;
mн Cl - навеска электролита, взятая при определении хлоридов, г.
Заявляемый способ определения галогенидов лития в литиевом электролите для тепловых химических источников тока поясняется следующим образом.
Первоначально проводят подготовку пробы анализируемого твердого литиевого электролита для ТХИТ, для чего измельчают перетиранием твердого образца электролита до порошкообразного состояния, т.е. осуществляют так называемое «усреднение пробы». Затем отобранные и измельченные пробы твердого литиевого электролита, в котором присутствуют одновременно и бромиды, и фториды и хлориды лития, а также вещество загустителя на основе солей алюминия, направляют на раздельные этапы последовательного определения фторидов, бромидов и хлоридов. Затем проводят определение массовой доли фторидов гравиметрическим методом (в присутствии алюминия).
Для определения массовой доли фторидов в электролите используют гравиметрический метод после предварительного сплавления измельченной пробы твердого литиевого электролита совместно с комплексным реактивом из кварцевого песка и углекислых солей калия и натрия, выщелачивания плава горячей дистиллированной водой, нейтрализациии раствора минеральными кислотами последовательно соляной, затем азотной кислотой, нагрева раствора до не более 40°С, отделения гидроксидов алюминия фильтрованием, осаждения фторидов контактированием с раствором уксуснокислого свинца и промывки осадка фторхлорида свинца при рН в диапазоне 3,5-4,6, и окончательного определения массовой доли фторидов по математической формуле (1)

где CF - массовая доля фторидов, %;
mF - масса полученного осадка фторхлорида свинца, г;
mн F - масса навески пробы электролита, взятая при анализе на содержание фторидов, г;
0,0726 - коэффициент пересчета массы фторхлорида свинца на массу фторида;
200 - вместимость мерной колбы с раствором электролита, см3;
100 - объем аликвоты раствора электролита, см3.
Таким образом, при реализации указанных выше операций из среды реакционного объема выводятся соединения алюминия, в присутствии которого определение фторидов невозможно. Избирательность предлагаемого способа основана на том, что проводят дробный последовательный анализ по каждому из составляющих литиевого электролита. Такой порядок операций предусмотрен в заявляемом способе в качестве оптимального для исключения конкурирующего взаимодействия выбранных реагентов с алюминием, бромидами и хлоридами. В отсутствии соединений алюминия определение фторидов проводят методом потенциометрического титрования с фторидным ионселективным электродом раствором лантана азотнокислого.
Для определения массовой доли бромидов в электролите - из измельченной пробы твердого литиевого электролита готовят водный раствор с добавлением концентрированной серной кислоты с последующим контактированием нейтрализованного раствора с раствором калия йодноватокислого (с предварительно установленным коэффициентом объемного отношения между растворами калия йодноватокислого и натрия серноватистокислого), кипячением на плитке в течение 2 ч для удаления образовавшегося брома, охлаждением, перенесением в колбу, добавкой калиия йодистого, выстаиванием в темном месте для образования йода и титрованием раствором натрия серноватистокислого до перехода бурого окрашивания раствора в соломенно-желтое, с добавлением раствора крахмала и продолжением титрования до полного обесцвечивания раствора. Вычисление массовой доли бромидов в электролите проводили по формуле (3)
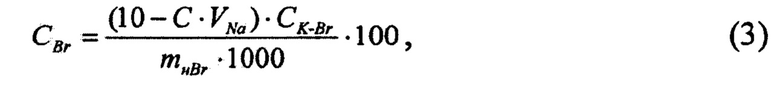
где СBr) - массовая доля бромидов в электролите, %;
10 - объем добавленного в избытке раствора калия йодноватокислого, см3;
mн Br - масса навески пробы электролита, взятая при анализе на содержание бромидов, г;
CK-Br - массовая концентрация раствора калия йодноватокислого по бромиду, мг/см3.
Для определения массовой доли хлоридов в электролите определяют разницу между суммарной величиной массовых долей бромидов и хлоридов, определенных методом меркурометрического титрования в кислой среде с индикатором дифенилкарбазоном, и предварительно установленной массовой доли бромидов в пробе, определяют израсходованный объем раствора реагента титрования - ртути (I) азотнокислой на титрование суммы хлоридов и бромидов, определяют израсходованный объем ртути (I) азотнокислой на титрование бромидов, после чего по разности объемов рассчитывают израсходованный объем ртути (I) азотнокислой на титрование хлоридов, и определяют соответствующую этому значению массовую долю хлоридов в литиевом электролите по формуле (4)
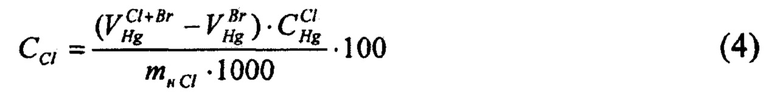
где CCl - массовая доля хлоридов в электролите, %;
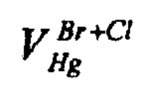 - объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
- объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
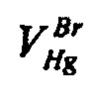 - объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
- объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
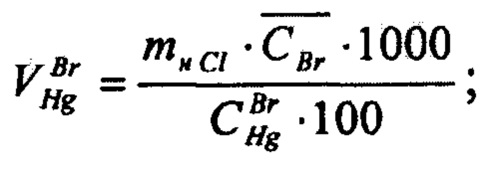
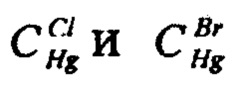 - массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
- массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
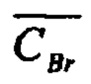 - массовая доля бромидов в электролите, %;
- массовая доля бромидов в электролите, %;
mн Cl - навеска электролита, взятая при определении хлоридов, г.
Экспериментально вся предлагаемая последовательность операций для раздельного определения содержания бромидов, фторидов и хлоридов лития была опробована в указанной выше последовательности, что обеспечило возможность их раздельного определения с приемлемой точностью определения.
В способе прототипа присутствует этап экстракции для концентрирования галогена, что является продолжительным применительно к анализу смесей, содержащих бромиды, хлориды и фториды при совместном их присутствии в анализируемой смеси, что усложнило бы в конечном итоге весь способ.
Таким образом, как это показали эксперименты, при использовании предлагаемого способа избирательного определения галогенидов лития в электролите, обеспечивается новый, более высокий, по сравнению с прототипом, результат, а именно возможность определения индивидуальных концентраций галогенидов щелочных металлов при их совместном присутствии в литиевом электролите, повышение точности их определения, сокращение продолжительности процесса и упрощение процесса определения.
Возможность промышленной реализации предлагаемого способа подтверждается следующими примерами.
Пример 1. В лабораторных условиях был опробован предлагаемый способ на примере анализа твердого литиевого электролита, содержащего галогениды лития и вещество загустителя на основе алюмината лития. Для этого брали твердый образец электролита, перетирали его в агатовой ступке с применением пестика.
Определение фторидов. Для переведения в раствор навеску пробы массой примерно 0,500 г сплавляли с 6 г реактива калий углекислый -натрий углекислый в присутствии кварцевого песка в муфельной печи при температуре 850°С в течение 10 мин. Полученный плав выщелачивали горячей дистиллированной водой с дополнительным нагреванием. Раствор количественно переносили в мерную колбу вместимостью 200 см3, объем раствора доводили до метки дистиллированной водой. Для отделения осадка соединений алюминия и кремния полученный раствор фильтровали через обеззоленный фильтр «синяя лента». В фильтрате проводили определение фторидов. Аликвоту фильтрата объемом 100 см3 помещали в стакан прибавляли 1,1 см3 раствора соляной кислоты концентрации 4 моль/дм3, 3 капли раствора индикатора метилового оранжевого, нейтрализовали раствор пробы раствором азотной кислоты концентрации 4 моль/дм3 до появления оранжево-розовой окраски, затем добавляли избыток этой кислоты объемом 1 см3. Добавляли 0,5 см3 концентрированной уксусной кислоты, стакан с раствором нагревали до 40°С. Осаждение фторидов проводили раствором свинца уксуснокислого, добавляя его при перемешивании до изменения окраски из розовой в оранжевую. Через несколько минут выпадал белый осадок фторхлорида свинца, который выдерживали при комнатной температуре не менее 10 ч. Затем осадок отфильтровывали, промывали насыщенным раствором фторхлорида свинца, дистиллированной водой и сушили при 120°С до постоянной массы. Рассчитывали результат определения массовой доли фторидов (CF) в образце в процентах по формуле

где CF - массовая доля фторидов, %;
mF - масса полученного осадка фторхлорида свинца, г;
mн F - масса навески пробы электролита, взятая при анализе на содержание фторидов, г;
0,0726 - коэффициент пересчета массы фторхлорида свинца на массу фторида;
200 - вместимость мерной колбы с раствором электролита, см3;
100 - объем аликвоты раствора электролита, см3.
Полученные значения mн F, mF и результаты единичных определений приведены в таблице 1.
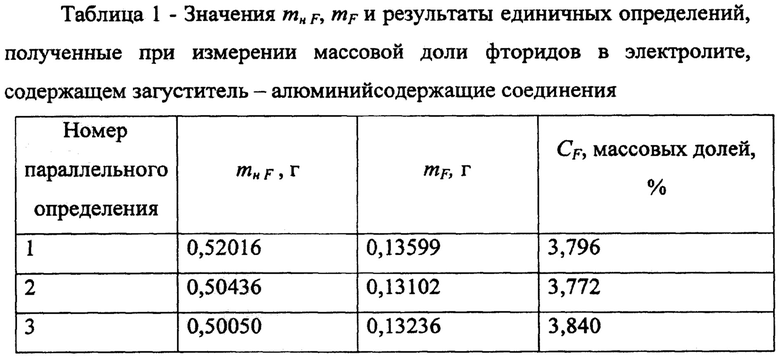
Массовая доля фторидов в электролите, определенная как среднее значение из трех результатов параллельных определений составила 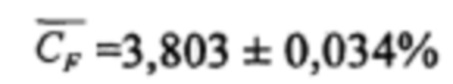 .
.
Определение массовой доли бромидов. Для переведения в раствор навеску электролита массой от 0,040 до 0,080 г помещали в стакан и растворяли в 40 см3 дистиллированной воды с добавлением 1 см3 концентрированной серной кислоты. Затем добавляли 10 см3 раствора калия йодноватокислого молярной концентрации 0,0166 моль/дм3 с предварительно установленным коэффициентом объемного отношения между растворами калия йодноватокислого и натрия серноватистокислого (С). Раствор в стакане кипятили на плитке в течение 2 ч для удаления образовавшегося брома. После охлаждения раствор переносили в колбу для титрования, добавляли 2 г калия йодистого, закрывали колбу пробкой и помещали в темное место для образования йода. Через пять минут йод в колбе титровали раствором натрия серноватистокислого до перехода бурого окрашивания раствора в соломенно-желтое, затем прибавляли 1 см3 раствора крахмала и продолжали титрование до полного обесцвечивания раствора. Фиксировали объем раствора натрия серноватистокислого, израсходованный на титрование избытка калия йодноватокислого, VNa, см3. Вычисление результатов определения массовой доли бромидов в электролите (CBr), %, проводили по формуле
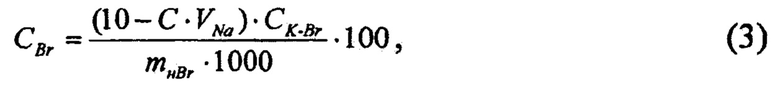
где 10 - объем добавленного в избытке раствора калия йодноватокислого, см3;
mн Br - масса навески пробы электролита, взятая при анализе на содержание бромидов, г;
CK-Br - предварительно установленная массовая концентрация раствора калия йодноватокислого по бромиду, мг/см3.
Полученные значения mн Br, VNa, CK-Br и и результаты единичных определений CBr приведены в таблице 2.
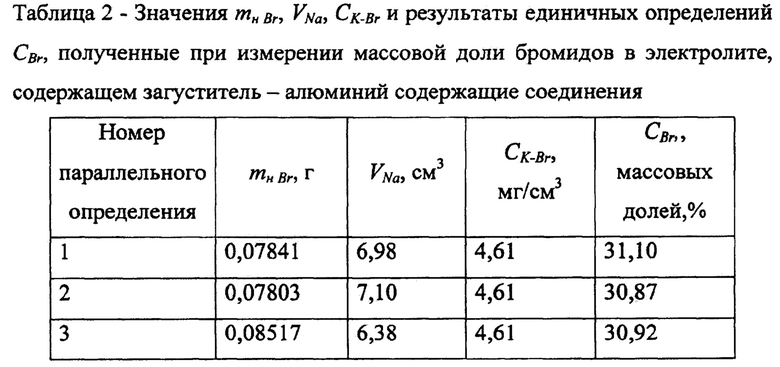
Массовая доля бромида в электролите, определенная как среднее значение из трех параллельных определений составила 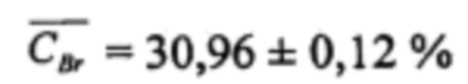 .
.
Определение массовой доли хлоридов. Предварительно определяли массовые концентрации раствора ртути азотнокислой в мг/см3 по хлориду- 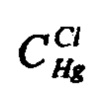 и по бромиду -
и по бромиду - 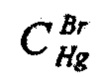 . Затем устанавливали объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов,
. Затем устанавливали объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, 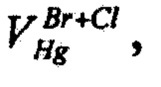 см3. Для этого навеску массой от 0,120 до 0,160 г помещали в стакан, растворяли в 45 см3 дистиллированной воды с добавлением 5 см3 раствора азотной кислоты с массовой долей 25%, не содержащей оксидов азота и титровали раствором ртути (I) азотнокислой молярной концентрации 0,05 моль/дм3 в присутствии раствора дифенилкарбазона в качестве индикатора до перехода окраски из голубоватой в сине-фиолетовую. Фиксировали объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов,
см3. Для этого навеску массой от 0,120 до 0,160 г помещали в стакан, растворяли в 45 см3 дистиллированной воды с добавлением 5 см3 раствора азотной кислоты с массовой долей 25%, не содержащей оксидов азота и титровали раствором ртути (I) азотнокислой молярной концентрации 0,05 моль/дм3 в присутствии раствора дифенилкарбазона в качестве индикатора до перехода окраски из голубоватой в сине-фиолетовую. Фиксировали объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, 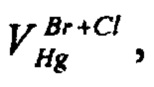 см3. Используя определенное значение массовой доли бромидов в электролите
см3. Используя определенное значение массовой доли бромидов в электролите  вычисляли объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов,
вычисляли объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, 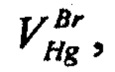 см3:
см3:

где mн Cl - навеска электролита, взятая при определении хлоридов, г.
Массовую долю хлоридов с электролите (CCl, %) определяли расчетным путем по разности после определения массовой доли суммы хлоридов и бромидов и массовой доли бромидов:
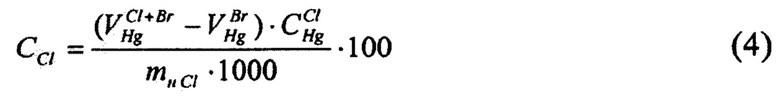
Полученные значения 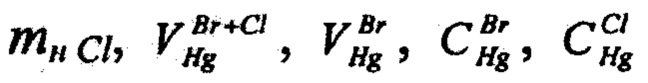 и результаты единичных определений CCl приведены в таблице 3.
и результаты единичных определений CCl приведены в таблице 3.
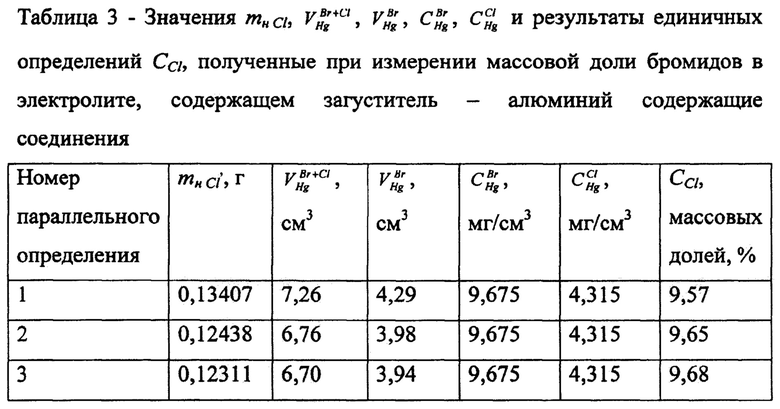
Массовая доля хлорида в электролите, определенная как среднее значение из трех параллельных определений составила 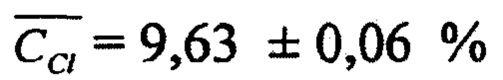
Таким образом, применение разработанного способа для анализа образца литиевого электролита в присутствии загустителя - алюминий содержащиго соединения, позволило установить массовые доли хлоридов - 9,63%, бромидов - 30,96% и фторидов - 3,803%, при их совместном присутствии.
Пример 2 - определение хлоридов, бромидов и фторидов в литиевом электролите, не содержащем загустителя - алюминий содержащих соединений.
Определение фторидов. Для переведения в раствор к навеске пробы массой примерно 0,070-0,080 г добавляли 20 см3 дистиллированной воды, 4 капли концентрированной соляной кислоты. Затем по рН-метру-иономеру доводили рН раствора до значения рН 6,5-7,0, добавляя раствор гидроксида натрия. Помещали в раствор фторидселективный и вспомогательный электроды и титровали из бюретки раствором лантана азотнокислого до потенциала конечной точки титрования, который был определен заранее. Фиксировали объем раствора лантана азотнокислого, израсходованного на титрование. Вычисление результатов измерений массовой доли фторидов (CF), %, проводили по формуле

где VLa - объем раствора лантана азотнокислого, израсходованный на титрование, см3;
mн F - масса навески электролита, г;
TLa-F - массовая концентрация раствора лантана азотнокислого по фториду, мг/см3.
Полученные значения mн F, VLa, TLa-F и результатов единичных определений приведены в таблице 4.
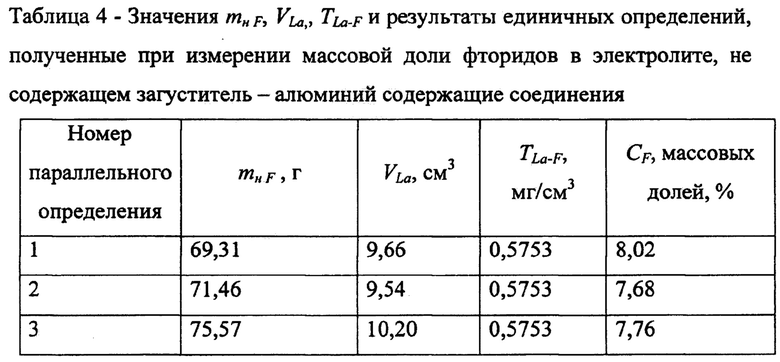
Массовая доля фторидов в электролите, не содержащем загуститель-алюминий содержащие соединения, определенная как среднее значение из трех параллельных определений составила 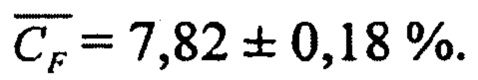
Определение массовой доли бромидов. Определение бромидов в электролите, не содержащем загуститель - алюминий содержащие соединения, проводили в соответствии с процедурами, приведенными в примере 1 при определении бромидов.
Полученные значения mн Br, VNa, CK-Br и результаты единичных определений CBr приведены в таблице 5.
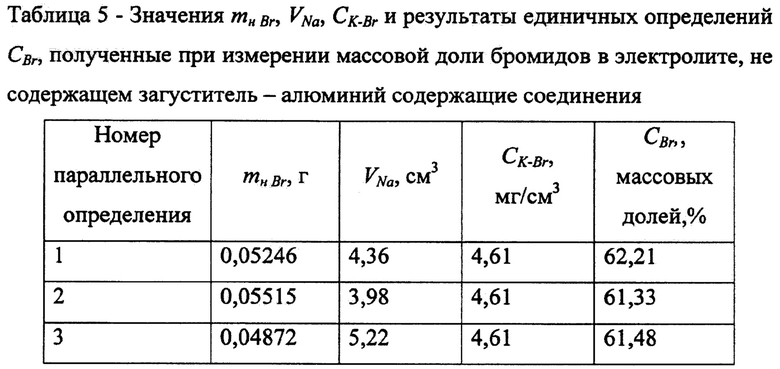
Массовая доля бромида в электролите, не содержащем загуститель - алюминийсодержащие соединения, определенная как среднее значение из трех параллельных определений составила 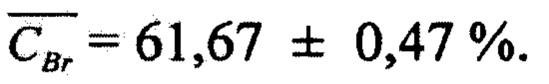
Определение массовой доли хлоридов. Определение хлоридов в электролите, не содержащем загуститель - алюминий содержащие соединения, проводили в соответствии с процедурами, приведенными в примере 1 при определении бромидов.
Полученные значения  и результаты единичных определений CCl приведены в таблице 6.
и результаты единичных определений CCl приведены в таблице 6.

Массовая доля хлорида в электролите, определенная как среднее значение из трех параллельных определений составила 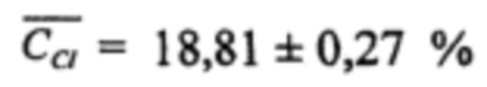
Таким образом, применение разработанного способа для анализа образца литиевого электролита, не содержащего загуститель - алюминий содержащие соединения, позволило установить массовые доли хлоридов - 18,81%, бромидов - 61,67% и фторидов - 7,82%,
Результаты контрольных испытаний сведены в таблицу 7.
Как это показали примеры реализации предлагаемого способа, подтверждена возможность достижения технического результата, состоящего в возможности определения индивидуальных концентраций галогенидов щелочных металлов и солей алюминия при их совместном присутствии в литиевом электролите, достижение требуемой точности их определения, необходимой для аттестации качества электролита, сокращение общей продолжительности процесса и упрощение процесса определения. 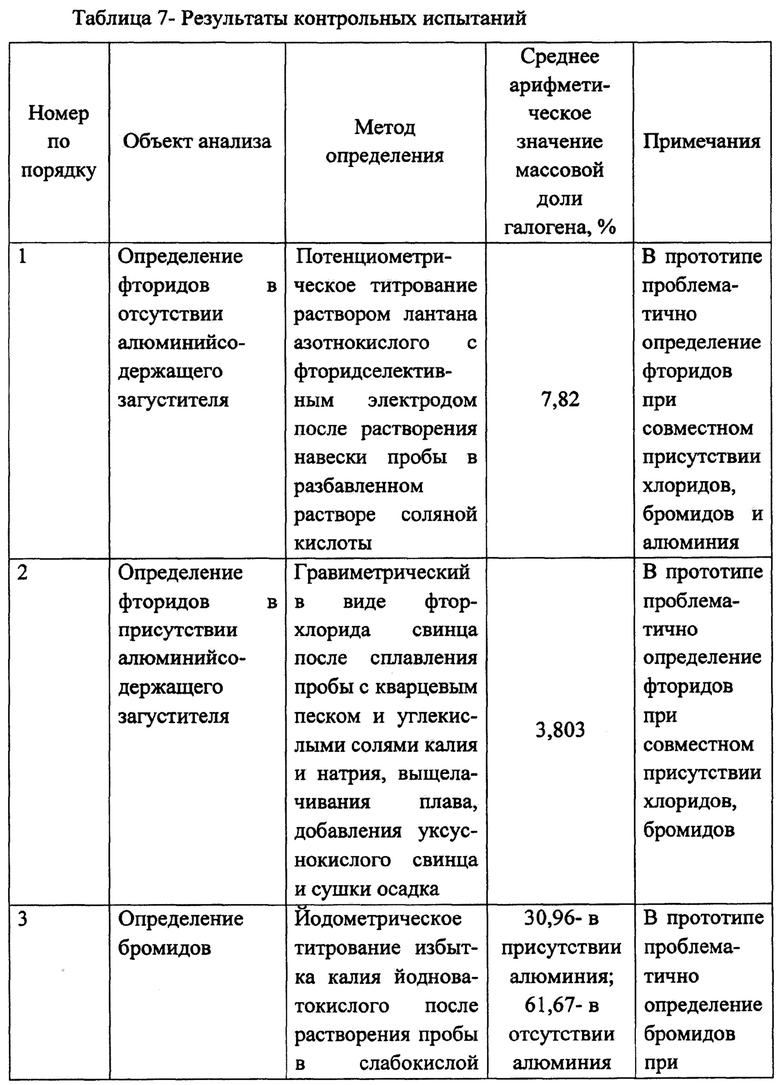
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ комплексного анализа материальных образцов | 1991 |
|
SU1786428A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ФОРМИАТОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ В ПРОТИВОГОЛОЛЕДНЫХ РЕАГЕНТАХ | 2012 |
|
RU2478203C1 |
| Способ определения массовой доли урана (III) и урана (IV) при их совместном присутствии в урансодержащих хлоридных расплавах щелочных металлов | 2023 |
|
RU2802629C1 |
| Способ определения 2-(2,4-динитрофенилтио)-бензтиазола | 1988 |
|
SU1642378A1 |
| ТИТРИМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА В ГОСУДАРСТВЕННОМ СТАНДАРТНОМ ОБРАЗЦЕ СОСТАВА 2-ХЛОРВИНИЛАРСИНОКСИД | 2008 |
|
RU2360243C1 |
| СПОСОБ РАЗДЕЛЬНОГО ОПРЕДЕЛЕНИЯ 0-2-ЭТИЛГЕКСИЛМЕТИЛФОСФОНАТОВ ЦИНКА И КАЛЬЦИЯ В ПРЕПАРАТЕ "СТАБФОН" | 1991 |
|
RU2011197C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АЛЮМИНАТА, ГИДРОКСИДА И КАРБОНАТА НАТРИЯ В РАСТВОРАХ АЛЮМИНАТА НАТРИЯ | 1992 |
|
RU2043627C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЙОДА МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2011 |
|
RU2459199C1 |
| СПОСОБ ТИТРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА В СТАНДАРТНОМ ОБРАЗЦЕ СОСТАВА β,β'-ДИГИДРООКСИДИЭТИЛСУЛЬФИДА | 2011 |
|
RU2453838C1 |
| Способ комплексонометрического определе-Ния МЕди(п) | 1979 |
|
SU833526A1 |
Изобретение относится к аналитической химии, а именно к методам определения концентрации компонентов электролитов для тепловых химических источников тока (ТХИТ), и может быть использовано для определения галогенидов щелочных металлов при их совместном присутствии в твердых литиевых электролитах. Для этого проводят предварительное измельчение перетиранием твердого образца электролита, затем отобранные и измельченные пробы твердого литиевого электролита направляют на раздельные этапы последовательного определения фторидов, бромидов и хлоридов. Для определения массовой доли фторидов используют гравиметрический метод после предварительного сплавления измельченной пробы с комплексным реактивом из углекислых солей калия и натрия и последующим выщелачиванием смеси горячей дистиллированной водой. Осадок примесных соединений алюминия и кремния отделяют и нейтрализуют соляной (HCl), затем азотной кислотами (HNO3) при температуре не более 40°С. Фториды концентрируют осаждением раствором уксуснокислого свинца, осадок фторхлорида свинца промывают при рН 3,5 - 4,6, а затем сушат и определяют массовую долю фторидов по формуле:
 ,
,
где CF - массовая доля фторидов, %; mF - масса полученного осадка фторхлорида свинца, г; mнF - масса навески пробы электролита, взятая при анализе на содержание фторидов, г; 0,0726 - коэффициент пересчета массы фторхлорида свинца на массу фторида; 200 - вместимость мерной колбы с раствором электролита, см3; 100 - объем аликвоты раствора электролита, см3. При отсутствии алюминийсодержащего загустителя в электролите массовую долю фторидов определяют методом потенциометрического титрования с фторидселективным электродом. Для этого навеску измельченной пробы растворяют в разбавленном растворе HCl, в который помещают фторид-селективный и вспомогательный электроды и при постоянном перемешивании на магнитной мешалке проводят титрование фторидов из стеклянной бюретки раствором лантана азотнокислого до точки эквивалентности по рН-метру-иономеру; вычисление массовой доли фторидов проводят по формуле:

где CF - массовая доля фторидов, %; VLa - объем раствора лантана азотнокислого, израсходованный на титрование, см3; mнF - масса навески пробы электролита, взятая при анализе на содержание фторидов в отсутствие алюминия, г; TLa-F - массовая концентрация раствора лантана азотнокислого по фториду, мг/см3. Для определения массовой доли бромидов в электролите готовят водный раствор измельченной пробы твердого литиевого электролита с добавлением концентрированной серной кислоты (Н2SO4) с последующим добавлением раствора со смесью калия йодноватокислого и натрия серноватистокислого. Взаимодействие бромида лития с йодистым калием приводит к получению брома, его удалению кипячением и титрованием избытка йодистого калия для определения массовой доли бромидов йодометрическим методом по формуле:
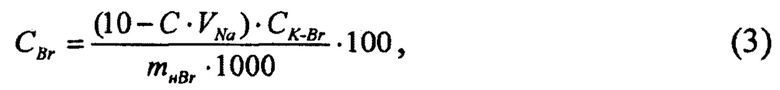
где СBr - массовая доля бромидов в электролите, %; 10 - объем добавленного в избытке раствора калия йодноватокислого, см3; mнBr - масса навески пробы электролита, взятая при анализе на содержание бромидов, г; СK-Br - массовая концентрация раствора калия йодноватокислого по бромиду, мг/см3. Для определения массовой доли хлоридов в электролите определяют разницу между суммарной величиной массовых долей бромидов и хлоридов, определенных методом меркурометрического титрования в кислой среде с индикатором дифенилкарбазоном, и предварительно установленной массовой долей бромидов в пробе, установленной при титровании растровом ртути (I) азотнокислой. Затем по разности объемов рассчитывают израсходованный объем ртути (I) азотнокислой на титрование хлоридов и определяют соответствующую этому значению массовую долю хлоридов в литиевом электролите по формуле:
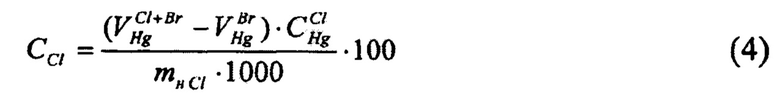 ,
,
где CCl - массовая доля хлоридов в электролите, %;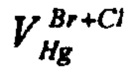 - объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
- объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3; 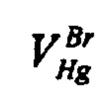 - объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
- объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
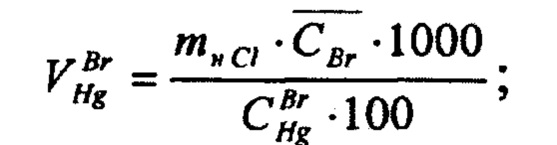
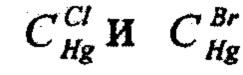 - массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
- массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3; 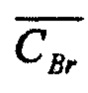 - массовая доля бромидов в электролите, %; mнCl - навеска электролита, взятая при определении хлоридов, г. Изобретение обеспечивает повышение точности определения индивидуальных концентраций галогенидов лития в присутствии солей алюминия в твердом литиевом электролите. 7 табл., 2 пр.
- массовая доля бромидов в электролите, %; mнCl - навеска электролита, взятая при определении хлоридов, г. Изобретение обеспечивает повышение точности определения индивидуальных концентраций галогенидов лития в присутствии солей алюминия в твердом литиевом электролите. 7 табл., 2 пр.
Способ определения галогенидов лития в литиевом электролите для тепловых химических источников тока, включающий подготовку пробы, проведение определения индивидуальных концентраций галогенид-ионов, отличающийся тем, что, с целью обеспечения возможности определения индивидуальных концентраций галогенидов щелочных металлов и солей алюминия при их совместном присутствии в литиевом электролите, повышения точности их определения, проводят предварительное измельчение перетиранием твердого образца электролита, затем отобранные и измельченные пробы твердого литиевого электролита направляют на раздельные этапы последовательного определения фторидов, бромидов и хлоридов, на каждом из которых проводят циклы специфических операций:
- для определения массовой доли фторидов в электролите - гравиметрическим методом после предварительного сплавления измельченной пробы твердого литиевого электролита совместно с комплексным реактивом из углекислых солей калия и натрия с последующим выщелачиванием плава горячей дистиллированной водой, отделением осадка примесных соединений алюминия и кремния, нейтрализацией раствора минеральными кислотами последовательно соляной, затем азотной кислотой, нагревом раствора до не более 40°С, осаждением фторидов контактированием с раствором уксуснокислого свинца и промывкой осадка фторхлорида свинца при рН в диапазоне 3,5-4,6, сушкой полученного осадка и окончательным определением массовой доли фторидов весовым методом по математической формуле:

где CF - массовая доля фторидов, %;
mF - масса полученного осадка фторхлорида свинца, г;
mн F - масса навески пробы электролита, взятая при анализе на содержание фторидов, г;
0,0726 - коэффициент пересчета массы фторхлорида свинца на массу фторида;
200 - вместимость мерной колбы с раствором электролита, см3;
100 - объем аликвоты раствора электролита, см3;
- для определения массовой доли фторидов в электролите в отсутствие алюминийсодержащего загустителя используют метод потенциометрического титрования с фторидселективным электродом, для этого навеску измельченной пробы твердого литиевого электролита растворяют в разбавленном растворе соляной кислоты, в раствор помещают фторид-селективный и вспомогательный электроды и при постоянном перемешивании на магнитной мешалке проводят титрование фторидов из стеклянной бюретки раствором лантана азотнокислого с индикацией точки эквивалентности по рН-метру-иономеру, вычисление массовой доли фторидов проводят по формуле (2)

где CF - массовая доля фторидов, %;
VLa - объем раствора лантана азотнокислого, израсходованный на титрование, см3;
mн F - масса навески пробы электролита, взятая при анализе на содержание фторидов в отсутствие алюминия, г;
TLa-F - массовая концентрация раствора лантана азотнокислого по фториду, мг/см3;
- для определения массовой доли бромидов в электролите - из измельченной пробы твердого литиевого электролита готовят водный раствор с добавлением концентрированной серной кислоты с последующим контактированием нейтрализованного раствора с раствором калия йодноватокислого (с предварительно установленным коэффициентом объемного отношения между растворами калия йодноватокислого и натрия серноватистокислого), кипячением на плитке в течение 2 ч для удаления образовавшегося брома, охлаждением, перенесением в колбу, добавкой калия йодистого, выстаиванием в темном месте для образования йода и титрованием раствором натрия серноватистокислого до перехода бурого окрашивания раствора в соломенно-желтое, с добавлением раствора крахмала и продолжением титрования до полного обесцвечивания раствора, вычисление массовой доли бромидов в электролите проводили по формуле (3)
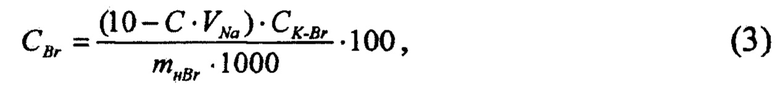
где CBr - массовая доля бромидов в электролите, %;
10 - объем добавленного в избытке раствора калия йодноватокислого, см3;
mн Br - масса навески пробы электролита, взятая при анализе на содержание бромидов, г;
CK-Br - массовая концентрация раствора калия йодноватокислого по бромиду, мг/см3;
- для определения массовой доли хлоридов в электролите определяют разницу между суммарной величиной массовых долей бромидов и хлоридов, определенных методом меркурометрического титрования в кислой среде с индикатором дифенилкарбазоном, и предварительно установленной массовой долей бромидов в пробе, определяют израсходованный объем раствора реагента титрования - ртути (I) азотнокислой на титрование суммы хлоридов и бромидов, определяют израсходованный объем ртути (I) азотнокислой на титрование бромидов, после чего по разности объемов рассчитывают израсходованный объем ртути (I) азотнокислой на титрование хлоридов, и определяют соответствующую этому значению массовую долю хлоридов в литиевом электролите по формуле (4)
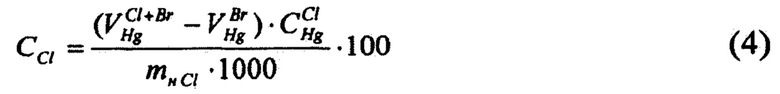
где CCl - массовая доля хлоридов в электролите, %;
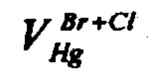 - объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
- объем раствора ртути (I) азотнокислой, израсходованный на титрование суммы хлоридов и бромидов, см3;
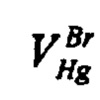 - объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
- объем раствора ртути (I) азотнокислой, израсходованный на титрование бромидов, см3:
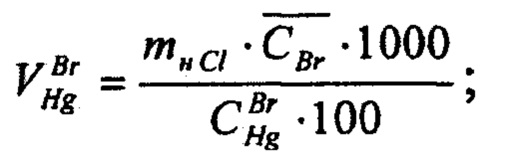
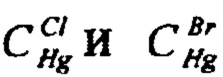 - массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
- массовые концентрации раствора ртути азотнокислой по хлориду и по бромиду, мг/см3;
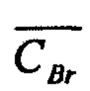 - массовая доля бромидов в электролите, %;
- массовая доля бромидов в электролите, %;
mн Cl - навеска электролита, взятая при определении хлоридов, г.
| ЭЛИКТРОЛИТНАЯ СМЕСЬ ДЛЯ ТЕПЛОВОГО ХИМИЧЕСКОГО ИСТОЧНИКА ТОКА | 2015 |
|
RU2607471C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ХИМИЧЕСКОГО ИСТОЧНИКА ТОКА | 2011 |
|
RU2489776C1 |
| WILKEN A | |||
| et al, A fluoride-selective electrode (Fse) for the quantification of fluoride in lithium-ion battery (Lib) electrolytes, Analytical Methods, 2016, 8, 38, pp | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ ПОДЪЕМА ЩИТОВ ПРИ УСТРОЙСТВЕ НАБИВНЫХ СТЕН | 1927 |
|
SU6932A1 |
Авторы
Даты
2020-02-26—Публикация
2019-09-16—Подача