Изобретение относится к медицинской вирусологии и микробиологии, а именно к штамму бактериофага Pseudomonas aeruginosa, используемого при производстве медицинских биологических антибактериальных лекарственных средств - препаратов бактериофагов, предназначенных для профилактики и лечения гнойно-воспалительных и энтеральных заболеваний, вызванных бактериями Pseudomonas aeruginosa.
Бактерии синегнойной палочки (лат.Pseudomonas aeruginosa) (далее - P. aeruginosa) отличаются высокой как естественной, так и приобретенной резистентностью (50-100%) к большинству антибиотиков и обладают способностью поражать все органы и ткани макроорганизма больного [1, 2, 3]. Бактерии P. aeruginosa являются одним из основных возбудителей нозокомиальных пневмоний, инфекций дыхательных путей, легких и плевры и вызывают тяжелейшие заболевания в виде муковисцидоза - от 20% до 61% всех внутрибольничных инфекций [2, 4]; от 11% до 30% нагноений ожоговых ран [4]; более 30% всех гнойно-воспалительных гинекологических и урологических инфекционных заболеваний; являются причиной 20-25% гнойных хирургических инфекций и генерализованных септических заболеваний - сепсиса, летальность при которых составляет 18% - 61% [4, 5].
На сегодняшний день в Российской Федерации известны моно- и поливалентные лечебно-профилактические препараты бактериофагов, содержащие штаммы бактериофагов P. aeruginosa: «Бактериофаг синегнойной палочки», «Пиобактериофаг поливалентный очищенный», «Интести-бактериофаг», которые наряду с антибиотиками применяются для лечения и профилактики синегнойных инфекций.
В соответствии с российскими требованиями Общей фармакопейной статьи «Бактериофаги. ОФС.1.7.1.0002.15 [6] («Государственная фармакопея Российской Федерации. XIII издание. Том II»), введенной в действие Приказом Минздрава России от 29.10.2015 №771 с 01.01.2016 и международными требованиями, установленными Решением Совета Евразийской экономической комиссии от 03.11.2016 №89 «Об утверждении Правил проведения исследований биологических лекарственных средств Евразийского экономического союза» [7], Директивой №2001/83/ЕС Европейского парламента и Совета Европейского Союза «О Кодексе Сообщества о лекарственных средствах для использования человеком» (Принята в г. Брюсселе 06.11.2001) [8] для гарантий клинической эффективности, широкого спектра антибактериальной активности и генетической безопасности их терапевтического применения лечебно-профилактические препараты бактериофагов P. aeruginosa должны иметь в своем составе бактериофаги биологически, морфологически и генетически охарактеризованные с широким спектром антибактериальной активности, принадлежащие к генетическим литическим группам, не содержащие гены лекарственной устойчивости, лизогенности и токсигенности, обладающих способностью передавать лекарственную устойчивость и токсигенность другим бактериям в организме больного.
Недостатком известных лечебно-профилактических препаратов бактериофагов Р. aeruginosa является отсутствие вышеперечисленных характеристик биологических свойств бактериофагов в составе препаратов по причине пассирования на бактериальных штаммах P. aeruginosa фагов, выделенных из образцов почвы, сточных вод, отделяемого ран.
Критерием активности отобранных «пассажных» фагов при этом является степень и стабильность их литической активности в тесте по Аппельману в отношении производственных штаммов бактерий P. aeruginosa.
Пассажи бактериофагов проводят постоянно для поддержания необходимой активности и возможности их дальнейшего использования в качестве рабочего посевного материала при получении маточных фагов и получении собственно препаратов бактериофагов.
Отдельные штаммы бактериофагов P. aeruginosa не выделяются и не изучаются, а постоянное пассирование бактериофагов на бактериальных клетках достаточно часто, из-за неконтролируемых рекомбинаций бактериофагов при их совместном размножении, приводит к «вырождению» пассажей и потере ими литической активности.
Указанный способ создания антибактериальной основы препаратов бактериофагов на практике приводит к попаданию в состав «пассажных фагов» и в состав препаратов умеренных фагов и литических фагов, содержащих гены лекарственной устойчивости, лизогенности и токсигенности, которые обладают способностью передавать лекарственную устойчивость и токсигенность другим бактериям в организме больного.
Задача, решаемая изобретением, состоит в получении штамма литического бактериофага P. aeruginosa, не содержащего гены лекарственной устойчивости, лизогенности и токсигенности, обладающего широким спектром антибактериальной активности в отношении эпидемиологически значимых выделенных от больных клинических и госпитальных штаммов бактерий P. aeruginosa.
Техническим результатом предлагаемого изобретения является селекция высокоактивного штамма бактериофага P. aeruginosa, предназначенного для приготовления моно- и поливалентных лечебно-профилактических препаратов бактериофагов P. aeruginosa, относящегося к генетической литической группе (роду), не содержащего гены лекарственной устойчивости, лизогенности и токсигенности, обладающего широким спектром антибактериальной активности в отношении эпидемиологически значимых выделенных от больных клинических и госпитальных штаммов бактерий P. aeruginosa и отвечающего российским и международным требованиям, предъявляемым к бактериофагам в составе лечебно-профилактических препаратов.
Выделенный штамм бактериофага P. aeruginosa депонирован в Государственной коллекции патогенных микроорганизмов (ГКПМ) Федерального государственного бюджетного учреждения «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) под регистрационным номером №328 (500322) и обладает широким спектром антибактериальной активности в отношении лекарственно-устойчивых клинических и госпитальных штаммов бактерий P. aeruginosa, относящийся по морфологии вирионов и генетическим свойствам к литическим бактериофагам порядка Caudovirales, семейства Myoviridae, рода Phikzlikevirus, не содержащий гены лизогении, токсигенности и лекарственной устойчивости.
Область применения штамма бактериофага №328 (500322) - производство лечебно-профилактических препаратов бактериофагов, предназначенных для лечения гнойно-септических и энтеральных заболеваний, вызванных бактериями P. aeruginosa,: «Пиобактериофага поливалентного очищенного», «Интести-бактериофага», «Бактериофага синегнойной палочки».
Известен Патент RU 2455355, 2011 г. [9], в котором предлагается использовать штамм бактериофага P. aeruginosa ph57, выделенный из экскрементов животных вивария, в качестве основы ветеринарного антисептического средства для лечения гнойно-септических заболеваний животных, вызванных бактериями P. aeruginosa.
Недостатками изобретения являются:
- отсутствие генетических характеристик предлагаемого бактериофага ph57, определен только тип его нуклеиновой кислоты - ДНК;
- не определена его принадлежность к умеренным или литическим генетическим родам бактериофагов;
- не установлено наличие или отсутствие генов лекарственной устойчивости, токсигенности и лизогенности, что не гарантирует генетическую безопасность его клинического применения даже в ветеринарии и противоречит российским и международным требованиям [7, 8, 9].
- отсутствуют данные о широте спектра антибактериальной активности предлагаемого штамма бактериофага в отношении эпидемиологически значимых госпитальных и клинических - выделенных от больных с различной патологией штаммов бактерий P. aeruginosa, поскольку метод определения активности не описан, а спектр антибактериальной активности штамма фага - 100%, определенный на 78 штаммах, заявленный в патенте, не подтвержден данными примеров, которые показывают, что оценка спектра активности проведена авторами не на 78, а только на 10 штаммах бактерий P. aeruginosa.
Известен патент WO 2015059298, 2015 г. [10], предлагающий 13 штаммов бактериофагов P. aeruginosa, для использования в качестве активных агентов фармацевтических или ветеринарных препаратов в различных композициях в количестве от 2 до 13 бактериофагов.
Недостатками изобретения являются:
- отсутствие убедительных данных, подтверждающих (90%) широту спектра антибактериальной активности предлагаемых 13 штаммов бактериофагов Pseudomonas aeruginosa и их сочетаний (композиций), поскольку при изучении их спектра и степени антибактериальной активности не использованы эпидемиологически значимые госпитальные и клинические выделенных от больных с различной патологией штаммы бактерий P. aeruginosa, а использованы всего 20 коллекционных эталонных лабораторных штаммов бактерий P. aeruginosa из международной коллекции LMG (ВССМ LMG / бактерий Collection);
- отсутствие сведений о литической природе предлагаемых 13 фагов - не установлено наличие или отсутствие у них генов лекарственной устойчивости, токсигенности и лизогенности, что не гарантирует генетическую безопасность их клинического применения и противоречит российским и международным требованиям [6,7,8].
Известен патент ЕР 2248890, 2010 г. [11], предлагающий использование 6 штаммов бактериофагов P. aeruginosa семейства Myoviridae литических родов РАК и СНА, для создания композиций фагов, предназначенных для профилактики или лечения муковисцидоза - легочных инфекционных заболеваний у млекопитающих и человека, вызванных бактериями P. aeruginosa штаммами РАК и СНА.
Недостатками изобретения являются:
- отсутствие сведений о наличии у запатентованных штаммов бактериофагов генов лекарственной устойчивости, токсигенности и лизогенности, достаточно узкий спектр (всего 30-40%) антибактериальной активности предлагаемых бактериофагов и их комбинаций и активность только в отношении штаммов бактерий P. aeruginosa РАК и СНА, вызывающих муковисцидоз;
- отсутствие данных о широте спектра антибактериальной активности в отношении эпидемиологически значимых госпитальных и клиническиих выделенных от больных с различной патологией штаммов бактерий P. aeruginosa, а также малое количество тестированных штаммов бактерий P. aeruginosa при определении широты спектра антибактериальной активности (всего 40 штаммов бактерий P. aeruginosa РАК и СНА) и отсутствие данных о спектре антибактериальной активности предлагаемых бактериофагов в отношении представителей других генетических видов бактерий P. aeruginosa.
Известен патент PL 007472, 2006 г. [12], в котором предложены 20 штаммов бактериофагов P. aeruginosa, активных в отношении лекарственно-устойчивых бактериальных штаммов гомологичных видов, и предназначенных для лечения муковисцидоза.
Недостатками изобретения являются:
- недостаточная генетическая характеристика генома запатентованных фагов -определена только принадлежность к семейству, не установлена принадлежность к генетическому роду, не охарактеризована принадлежности к литическим или умеренным фагам;
- отсутствие сведений о наличии у запатентованных штаммов бактериофагов генов лекарственной устойчивости, токсигенности и лизогенности, и достаточно узкий спектр антибактериальной активности большинства штаммов в отношении бактерий гомологичного вида - лишь 2 штамма фагов P. aeruginosa были активны в отношении 43% и 64% бактерий P. aeruginosa.
Известен патент RU 2186574, 2001 г. [13], в котором предложен препарат бактериофагов Combiphage, предназначенный для лечения инфекций, вызванных бактериями P. aeruginosa, представляющий собой суспензию в пептонной воде смеси 4 штаммов бактериофагов P. aeruginosa (№№05, 03, 06 и 07), дополнительно содержащий компоненты питательной среды и вспомогательные добавки.
Недостатками изобретения являются:
- отсутствие генетических характеристик предлагаемых штаммов бактериофагов Р. aeruginosa (№№05, 03, 06 и 07), определяющих их принадлежность к умеренным или литическим генетическим видам бактериофагов, принадлежность к семейству, роду, группе;
- отсутствие сведений о наличие у запатентованных штаммов бактериофагов генов лекарственной устойчивости, токсигенности и лизогенности, что приводит к отсутствию гарантий генетической безопасности клинического применения препарата Combiphage.
Известен патент RU 2112800, 1996 г. [15], в котором предлагается использовать пилеспецифичный бактериофаг P. aeruginosa - фаг №03, обладающий антибактериальной активностью в отношении пилесодержащих клинических штаммов бактерий P. aeruginosa, для включения его в состав лечебного препарата для лечения синегнойных инфекций. Между тем пили (фимбрии) бактерий P. aeruginosa являются одним, но не единственным, из факторов патогенности клинических штаммов бактерий P. aeruginosa.
При этом авторами показано, что у большинства фагорезистентных форм Р. aeruginosa пили отсутствуют, предлагаемый фаг №03 был не активен в отношении бактерии P. aeruginosa, не содержащих пили, к которым по данным авторов относится большинство фагорезистентных форм P. aeruginosa.
Недостатками изобретения являются:
- отсутствие обязательных полных генетических характеристик предлагаемого бактериофага P. aeruginosa №03;
Установлено, что в тестах с Митомицином-С, фаг P. aeruginosa №03 не лизогенизирует клетки бактерий P. aeruginosa, на основании чего сделан вывод о том, что это вирулентный (литический) фаг;
- не определена принадлежность фага P. aeruginosa №03 к определенному генетическому порядку, семейству и роду, отсутствуют данные о наличии или отсутствии у фага генов лекарственной устойчивости, токсигенности и лизогенности, что не гарантирует генетическую безопасность его клинического применения и противоречит российским и международным требованиям [6, 7, 8].
Известен патент RU 2113476, 1996 г. [15], в котором предлагается штамм бактериофага P. aeruginosa №02, для включения в состав поливалентного лечебного препарата, предназначенного для лечения инфекционных заболеваний, вызванных бактериями P. aeruginosa.
Недостатками изобретения являются:
- отсутствие обязательных полных генетических характеристик предлагаемого штамма бактериофага P. aeruginosa №02, указан только тип нуклеиновой кислоты - ДНК;
- отсутствие сведений о литической природе штамма фага №02, не определена его принадлежность к умеренным или литическим бактериофагам, принадлежность к порядку, семейству, роду, не установлено наличие или отсутствие у штамма фага Р. aeruginosa №02 генов лекарственной устойчивости, токсигенности и лизогенности, что не гарантирует генетическую безопасность клинического применения штамма и противоречит российским и международным требованиям [6, 7, 8].
Известен патент №2366437, 2007 г. [16], в котором для обеспечения стабильной вирулентности бактериофагов в композиции и их адаптации к циркулирующим возбудителям инфекций за счет получения бактериофагов путем последовательных многократных пассажей фагов препаратов бактериофагов через тест-штаммы и свежевыделенные изоляты нелизогенных бактерий с добавлением в питательную среду индуцирующего агента, например, митомицина С.
Недостатками изобретения являются:
- использование для получения поливалентного препарата бактериофагов «пассажных» фагов - смесей фагов P. aeruginosa, а не отдельных штаммов бактериофагов P. aeruginosa с изученными биологическими и генетическими свойствами;
- отсутствие гарантий получения стабильной индуцированной вирулентности у умеренных бактериофагов при использовании мутагена Митомицина С и гарантий, что препарат не будет содержать умеренных фагов. В патенте не содержится сведений о наличии в «пассажных» фагах, обработанных митомицином С, литических фагов, не имеющих нежелательные гены лекарственной устойчивости, токсигенности, лизогенности;
- отсутствие полной информации о биологических свойствах бактериофагов в составе препарата - морфологии фаговых вирионов, их принадлежности к порядку, семейству, роду, нет информации о нуклеотидной последовательности ДНК фагов в составе препарата с убедительным доказательством отсутствия у них нежелательных генов лекарственной устойчивости, токсигенности, лизогенности, что противоречит российским и международным требованиям и не обеспечивает генетическую безопасность терапевтического использования препарата бактериофагов.
Проведенный анализ изобретений свидетельствует о том, что ни один из приведенных аналогов не может быть выбран в качестве прототипа. При этом большинство аналогов не содержат информации, доказывающей широкий спектр антибактериальной активности запатентованных бактериофагов в отношении эпидемиологически значимых госпитальных и выделенных от больных клинических штаммов бактерий P. aeruginosa.
Приведенные аналоги не содержат предусмотренных российскими и международными требованиями полных сведений о генетических свойствах запатентованных бактериофагов; принадлежности к умеренным или литическим группам фагов; принадлежности к определенному генетическому порядку, семейству, роду; наличии или отсутствии у запатентованных фагов генов лекарственной устойчивости, лизогенности и токсигенности, в связи с чем их присутствие в лечебно-профилактических препаратах бактериофагов не обеспечивает эффективность и генетическую безопасность терапевтического использования препаратов.
В отличие от большинства аналогов у штамма бактериофага P. aeruginosa №328 (500322), предлагаемого для включения в состав моно- и поливалентных лечебно-профилактических препаратов бактериофагов, существенными отличительными признаками являются:
1. наличие характеристик биологических свойств - литический характер взаимодействия с бактериальными клетками, высокая степень (91%) и скорости адсорбции (7-10 мин), длительность латентного периода (30 мин), урожайность (10 фаговых вирионов/бакт.кл), морфологии негативных колоний;
2. наличие характеристик морфологии бактериофаговых вирионов штамма фага №328 (500322), полученных путем электронной микроскопии;
3. наличие характеристик генетических свойств ДНК штамма фага №328 (500322), полученных путем высокопроизводительного полногеномного секвенирования его ДНК с последующим биоинформационным анализом, при котором установлена принадлежность штамма фага к литическим бактериофагам порядка Caudovirales, семейства Myoviridae, рода Phikzlikevirus и установлено отсутствие у штамма фага №328 (500322) генов лизогении, токсигенности и лекарственной устойчивости;
4. наличие данных, полученные указанным в Государственной фармакопее РФ ГФXIII методом Аппельмана [6] о широком спектре антибактериальной активности штамма фага №328 (500322) (58,79%) в отношении 917 эпидемиологически значимых госпитальных и выделенных от больных клинических штаммов патогенных бактерий P. aeruginosa в 100% резистентных к одному или более антибиотикам, полученных из санитарно-эпидемиологических служб и стационаров с максимальным расширением географии регионов выделения - из 30 территориально удаленных регионов России и стран СНГ.
Предлагаемая совокупность существенных признаков изобретения является новой, а влияние отличительных от аналогов существенных признаков на достижение технического результата не следует из известного уровня техники.
Для приготовления поливалентных лечебно-профилактических препаратов бактериофагов предлагается штамм бактериофага P. aeruginosa, депонированный в Государственной коллекции патогенных микроорганизмов (ГКПМ) Федерального государственного бюджетного учреждения «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) под регистрационным номером №328 (500322), всесторонне биологически, морфологически и генетически изученный, относящийся к литическим бактериофагам порядка Caudovirales, семейства Myoviridae, рода Phikzlikevirus, не содержащий гены лизогении, токсигенности и лекарственной устойчивости, обладающий широким спектром антибактериальной активности (58,79%) в отношении 917 эпидемиологически значимых госпитальных и выделенных от больных с различной патологией клинических штаммов патогенных бактерий P. aeruginosa в 100% резистентных к одному или более антибиотикам, полученных с максимальным расширением географии регионов выделения из санитарно-эпидемиологических служб и стационаров 30 территориально удаленных регионов России и стран СНГ.
Штамм бактериофага P. aeruginosa №328 (500322) обеспечивает присутствие в лечебно-профилактических препаратах бактериофагов биологически, морфологически и генетически изученного литического бактериофага, а также обеспечивает широкий спектр и стабильность антибактериальной активности лечебно-профилактического препарата на его основе в отношении лекарственно устойчивых клинических и госпитальных штаммов бактерий P. aeruginosa, безвредность, эффективность, и генетическую безопасность его терапевтического применения.
Штамм бактериофага P. aeruginosa №328 (500322) характеризуется следующими свойствами.
1. Штамм бактериофага P. aeruginosa депонирован в Государственной коллекции патогенных микроорганизмов (ГКПМ) Федерального государственного бюджетного учреждения «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) под регистрационным номером №328 (500322).
Авторское обозначение штамма, с которым штамм бактериофага P. aeruginosa поступил на депонирование - бактериофаг P. aeruginosa PaUfa№P15.
Дата депонирования в ГКПМ ФГБУ «НЦЭСМП» Минздрава России - 01.11.2018.
Место нахождения ГКПМ ФГБУ «НЦЭСМП» Минздрава России: 127051, г. Москва, Петровский бульвар, д. 8, стр. 2.
Штамм бактериофага P. aeruginosa №328 (500322) найден в 2016 году в естественных условиях в озерной воде г. Владивосток, изучен и охарактеризован депозитором в филиале АО «НПО «Микроген» в г. Уфа «Иммунопрепарат».
Тест-штамм бактерии P. aeruginosa, который используют для размножения штамма бактериофага P. aeruginosa №328 (500322), выделен из клинического материала и депонирован в Государственной коллекции патогенных микроорганизмов (ГКПМ) Федерального государственного бюджетного учреждения «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) под номером №321 (500315).
Тест-штамм бактерии P. aeruginosa №321 (500315) выделен от больного из клинического материала в 2009 году, типичен по своим культуральным, морфологическим, тинкториальным и биохимическим свойствам, изучен и охарактеризован депозитором в филиале АО «НПО «Микроген» в г. Уфа «Иммунопрепарат».
Авторское обозначение тест-штамма, поступившего на депонирование - штамм бактерии P. aeruginosa №376.
Дата депонирования в ГКПМ ФГБУ «НЦЭСМП» Минздрава России - 01.11.2018.
Место нахождения ГКПМ ФГБУ «НЦЭСМП» Минздрава России: 127051, Москва, Петровский бульвар, д. 8, стр. 2.
2. Способ выделения штамма бактериофага №328 (500322).
Штамм фага выделен методом клонирования уколом из негативной колонии, полученной по рассеве пробы озерной воды и тест-штамма бактерии P. aeruginosa №321 (500315) двухслойным методом Грациа на 0,7% - 1,5% агаровой среде [17].
3. Условия размножения штамма бактериофага №328 (500322).
Для размножения штамма бактериофага P. aeruginosa №328 (500322) используют 18-24 часовую бульонную культуру тест-штамма бактерии P. aeruginosa №321 (500315), жидкие (бульоны) и агаровые (0,7%, 1,5%) питательные среды на основе панкреатических мясных или казеиновых гидролизатов или мясо-пептонного бульона, рН 7,0-7,7.
Штамм бактерии P. aeruginosa №321 (500315) и штамм бактериофага P. aeruginosa №328 (500322) одномоментно вносят в стерильный бульон в соотношении (фаг/бактерия) 1/10, инкубирование проводят при температуре 37°С в течение 18-24 часов в условиях периодического статического культивирования. Об окончании процесса культивирования штамма фага свидетельствует визуальное просветление культуральной жидкости (фаголизата).
Штамм бактериофага №328 (500322) не чувствителен к хлороформу, поэтому фаголизат, содержащий штамм фага, консервируют добавлением хлороформа в конечной концентрации от объема - 5-10%. Концентрация фагов в фаголизате после окончания культивирования определяется методом Грациа [17] и составляет (0,5-5,0)×109 фаговых вирионов в 1 мл.
4. Хранение штамма бактериофага №328 (500322).
Штамм бактериофага устойчив к хлороформу, сохраняет антибактериальную литическую активность в течение 5 лет при хранении в виде фаголизата в мясо-пептонном бульоне (МПБ), содержащего 5-10% хлороформа, при температуре от +2°С до +8°С.
При хранении лиофильно высушенного штамма бактериофага P. aeruginosa №328 (500322) в сахарозо-желатиновой среде при температуре от +2°С до +8°С штамм бактериофага сохраняет антибактериальную литическую активность в течение 15 лет.
5. Морфология негативных колоний штамма бактериофага №328 (500322).
При высеве штамма фага двухслойным методом Грациа на газоне тест-штамма бактерии P. aeruginosa №321 (500315) образуются негативные колонии диаметром (1,0±0,5) мм и шириной зоны неполного лизиса (0,3-0,7) мм.
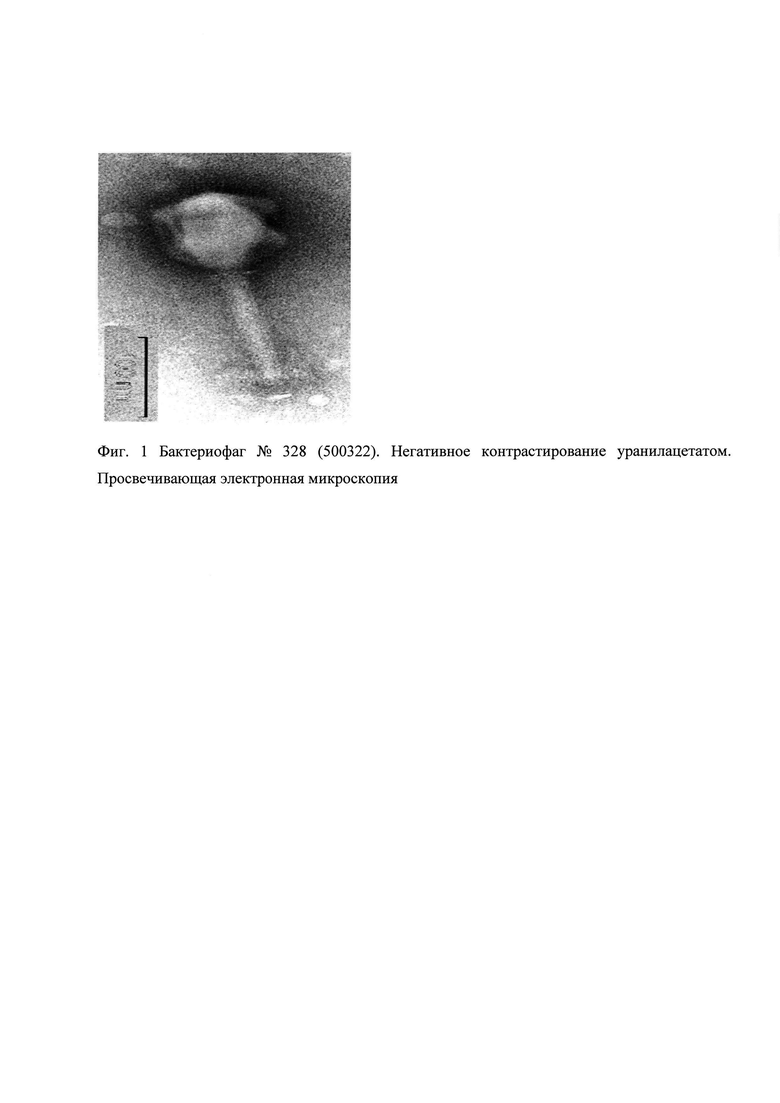
6. Морфология фаговых вирионов штамма бактериофага №328 (500322).
По данным электронной микроскопии штамм бактериофага №328 (500322) принадлежит к семейству Myoviridae, имеет капсид диаметром 115 нм, длина отростка составляет 150 нм. (фиг. 1).
7. Особенности фаз взаимодействия штамма бактериофага с бактериальными клетками, изученные в одиночном цикле размножения [17] в модификации [18] с использованием тест-штамма бактерий P. aeruginosa №321 (500315) свидетельствуют, что штамм бактериофага №328 (500322) обладает литическим циклом взаимодействия с бактериальными клетками гомологичного вида бактерий - внутриклеточно размножается, лизирует бактериальные клетки и характеризуется следующими параметрами взаимодействия с ними:
- степень максимальной адсорбции на бактериальных клетках Pseudomonas aeruginosa - 91%, время максимальной адсорбции - 7-10 мин.;
- длительность внутриклеточного цикла размножения - 30 мин.;
- величина выхода фага из одной инфицированной бактериальной клетки (урожайность) - 10 фаг.вирионов/ бакт.кл.
8. Спектр антибактериальной активности штамма бактериофага P. aeruginosa №328 (500322).
Широта спектра антибактериальной активности штамма бактериофага P. aeruginosa №328 (500322), определенная в тесте Аппельмана, составляет 58,79% в отношении 917 выделенных от больных с различной патологией и госпитальных штаммов P. aeruginosa эпидемиологически значимых, типичных по своим культуральным, морфологическим, тинкториальным и биохимическим свойствам, в 100% резистентных к одному или более антибиотикам, полученных из стационаров и санитарно-эпидемиологических служб 30 городов различных территориально удаленных регионов России и стран СНГ.
9. Генетические свойства штамма бактериофага P. aeruginosa №328 (500322).
Характеристика генома штамма бактериофага P. aeruginosa №328 (500322) - размер генома 278 771 п.н., ДНК двухцепочечная, содержание ГЦ - 36,8%.
По данным высокопроизводительного полногеномного секвенирования и последующего биоинформационного анализа штамм фага №328 (500322) относится к литическим бактериофагам порядка Caudovirales, близок по строению генома к группе литических фагов семейства Myoviridae, рода Phikzlikevirus.
В геноме штамма бактериофага отсутствуют гены лизогении, токсигенности, лекарственной устойчивости.
Полная нуклеотидная последовательность ДНК штамма бактериофага P. aeruginosa №328 (500322) определена высокопроизводительным полногеномным секвенированием на платформе Illumina Miseq со сборкой de novo.
Пример 1. Условия выделения, размножения и хранения штамма бактериофага P. aeruginosa №328 (500322).
Штамм бактериофага №328 (500322) выделен методом клонирования [17] уколом из негативной колонии, полученной по рассеве двухслойным методом Грациа на 0,7% - 1,5% агаровой среде пробы полученной по рассеве двухслойным методом Грациа на 0,7% - 1,5% агаровой среде пробы озерной воды (г.Владивосток) и тест-штамма бактерии P. aeruginosa №321 (500315) и тест-штамма бактерии P. aeruginosa №321 (500315).
Для размножения штамма фага используют питательные среды - стерильный мясо-пептонный бульон или бульоны с основами роста в виде панкреатических гидролизатов мяса или казеина.
Для размножения штамма фага штамм бактерии P. aeruginosa №321 (500315) (18-24 часовую культуру) вносят в стерильный бульон в исходной концентрации бактерий (4,0-5,0)×107 бакт.кл\мл и одномоментно вносят бактериофаг №328 (500322) в соотношении фаг/бактерия 1/10.
Инкубирование проводят в течение 18-24 часов при температуре 37°С в условиях периодического статического культивирования.
Об окончании процесса размножения фага свидетельствует визуальное просветление культуральной жидкости (фаголизата).
Штамм фага №328 (500322) не чувствителен к хлороформу, поэтому фаголизат консервируют добавлением хлороформа (5-10)%. Концентрация фагов в фаголизате после окончания культивирования определяется методом Грациа и составляет (0,5-5,0)×109 фаговых вирионов в 1 мл.
Штамм фага №328 (500322) сохраняет литическую активность при хранении в виде фаголизата, содержащего 5-10% хлороформа, при температуре от +2°С до +8°С в МПБ в течение 5 лет.
При хранении лиофильно высушенного штамма бактериофага P. aeruginosa №328 (500322) в сахарозо-желатиновой среде при температуре от +2°С до +8°С штамм бактериофага сохраняет антибактериальную литическую активность в течение 15 лет.
Пример 2. Характеристика биологических свойств штамма бактериофага Р. aeruginosa №326 (500320).
Морфология негативных колоний штамма бактериофага №328 (500322).
Штамм фага при высеве разведений фага двухслойном методом Грациа в 1,5% - 0,7% агаровой среде [17] образует негативные колонии диаметром (1,0±0,5) мм, ширина зоны неполного лизиса (0,3-0,7) мм.
Особенности фаз взаимодействия штамма бактериофага P. aeruginosa №328 (500322) с бактериальными клетками изучают в одиночном цикле размножения [17] в модификации [18] использованием тест-штамма бактерий P. aeruginosa 321 (500315).
Результаты свидетельствуют, что штамм бактериофага обладает литическим циклом взаимодействия с бактериальными клетками гомологичного вида бактерий - внутриклеточно размножается и лизирует бактериальные клетки и характеризуется следующими параметрами взаимодействия с ними:
- степень максимальной адсорбции на бактериальных клетках P. aeruginosa - 91%, время максимальной адсорбции - 7-10 мин.;
- длительность внутриклеточного цикла размножения на бактериальных клетках - 30 мин.;
- величина выхода фага из одной инфицированной бактериальной клетки (урожайность) - 10 фаг.вирионов/ бакт.кл.
Пример 3. Морфология вирионов штамма фага P. aeruginosa №328 (500322).
Изучение морфологии вирионов штамма бактериофага проводят методом электронной микроскопии. Суспензии бактериофаговых вирионов для электронной микроскопии очищали от бактериальных примесей методом ультрацентрифугирования в градиенте хлористого цезия [19].
Таксономическую принадлежность изучали с использованием электронного микроскопа JEM-1400 (Jeol, Япония), оснащенного цифровой камерой бокового ввода Veleta (SIS, Германия).
Размеры и морфология вирионных частиц штамма бактериофага по данным электронной микроскопии - семейству Myoviridae, имеет капсид диаметром 115 нм, длина отростка составляет 150 нм. (фиг. 1).
Пример 4. Спектр антибактериальной активности штамма бактериофага Р. aeruginosa №328 (500322).
Для определения широты спектра антибактериальной активности штамма бактериофага используют тест Аппельмана в разведении 10-1 [6] и эпидемиологически значимые штаммы бактерий P. aeruginosa (917 шт.), выделенные от больных с различной патологией и госпитальные, типичные по своим культуральным, тинкториальным, морфологическим и биохимическим свойствам, в 100% резистентные к одному или нескольким антибиотикам, полученные из санитарно-эпидемиологических служб и стационаров 30 городов различных территориально удаленных регионов России и стран СНГ.
Для оценки антибиотикочувствительности 917 клинических и госпитальных бактериальных штаммов P. aeruginosa, используют 1,5% МПА, метод антибиотических дисков, в том числе и набор дисков антибиотиков №9, рекомендованных для бактерий Р. aeruginosa (Федеральное бюджетное учреждение науки «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера»).
Тестирование антибиотикочувствительности клинических и госпитальных штаммов бактерий P. aeruginosa показывает, что бактерии P. aeruginosa (917 штаммов) в 100% резистентны к одному или более антибиотикам, в том числе к антибиотикам цефтазидиму (35,7%), гентамицину (41,0%), амикацину (43,5%), к аминогликозидам (60-85%), фторхинолам (77,0%), цефалоспоринам (60,0% - 76,0% - 85,0%), ципрофлоксацину (47,0%) и тикарциллину (53,5%), карбопенемам - меропинем, ипинем (70,0%).
100% штаммов бактерий P. aeruginosa были резистентны к антибиотикам пенициллинового и тетрациклинового рядов.
Параллельное тестирование антибактериальной активности штамма бактериофага P. aeruginosa №328 (500322) в тесте по Аппельману в разведении 10-1 на 917 клинических и госпитальных штаммах бактерий P. aeruginosa, 100% резистентных к одному или нескольким антибиотикам свидетельствует о широком спектре и стабильности антибактериальной активности штамма бактериофага P. aeruginosa №328 (500322) - активность 58,79% в отношении бактерий P. aeruginosa.
Пример 5. Изучение генетических свойств штамма бактериофага P. aeruginosa №328 (500322).
Для изучения генетических свойств штамма бактериофага P. aeruginosa использовали метод высокопроизводительного полногеномного секвенирования с последующим биоинформационным анализом.
Для проведения анализов геномов штаммов бактериофагов P. aeruginosa выделяли ДНК штаммов бактериофагов методом экстракции фенол-хлороформом с предварительной ферментативной обработкой РНКазой А, ДНКазой I и Протеиназой К (Thermo Fisher Scientific, США) [20].
Секвенирование библиотек ДНК проводили на платформе Illumina Miseq.
Сборка нуклеотидных последовательностей de novo была выполнена с помощью пакета ABYSS.
Поиск открытых рамок трансляции (ОРТ), таксономическая и функциональная идентификация этих ОРТ была проведена с помощью программного обеспечения MG-RAST с использованием последовательностей ДНК, находящихся в базах данных GenBank и др.
Характеристика генома штамма бактериофага P. aeruginosa - размер генома 278 771 н.п., ДНК двухцепочечная, содержание ГЦ - 36,8%.
По данным высокопроизводительного полногеномного секвенирования и последующего биоинформационного анализа установлено, что штамм бактериофага №328 (500322) относится к литическим бактериофагам порядка Caudovirales, близок по строению генома к группе (роду) литических фагов семейства Myoviridae, рода Phikzlikevirus.
Установлено, что в геноме штамма бактериофага отсутствуют гены лизогении, токсигенности, лекарственной устойчивости.
Полная нуклеотидная последовательность ДНК штамма бактериофага P. aeruginosa №328 (500322) определена высокопроизводительным полногеномным секвенированием на платформе Illumina Miseq со сборкой de novo.
Источники информации
1. Тикунова Н.В., Ворошилова Н.Н., Полыгач О.А., Морозова В.В., Тикунов А.Ю., Курильщиков A.M., Власов В.В.. Генетическая характеристика и спектр антибактериальной активности бактериофагов, входящих в состав промышленных серий лекарственного препарата Пиобактериофаг поливалентный очищенный. Эпидемиология и Вакцинопрофилактика. 2016; 2 (87): 93-100.
2. Антибиотикорезистентность нозокомиальных штаммов Pseudomonas aeruginosa в стационарах России: результаты многоцентрового эпидемиологического исследования «МАРАФОН» в 2011-2012 гг. Сухорукова М.В., Эйделынтейн М.В., Склеенова Е.Ю., Иванчик Н.В., Тимохова А.В., Шек Е.А., Дехнич А.В., Козлов Р.С. и исследовательская группа «МАРАФОН». Клиническая микробиология и антимикробная химиотерапия, 2014; 16(4): 273-279.
3. Антибиотикорезистентность нозокомиальных штаммов Pseudomonas aeruginosa в стационарах России: результаты многоцентрового эпидемиологического исследования «МАРАФОН» 2013-2014. Эйдельштейн М.В., Сухорукова М.В., Склеенова Е.Ю., Иванчик Н.В., Микотина А.В., Шек Е.А., Дехнич А.В., Азизов И.С., Козлов Р.С. и исследовательская группа «МАРАФОН». Клиническая микробиология и антимикробная химиотерапия. 2017; 19(1): 37-41.
4. Кузнецова М.В. Распространенность возбудителя и разнообразие нозоологических форм синегнойной инфекции. Здоровье семьи - 21 век. 2014; 2: 84-112.
5. Лазарева А.В., Чеботарь И.В., Крыжановская О.А., Чеботарь В.И., Маянский Н.А. Pseudomonas aeruginosa: патогенность, патогенез и патология. Клиническая микробиология и антимикробная химиотерапия. 2015; том 17 (3): 170-187.
6. Общая фармакопейная статья Бактериофаги. ОФС.1.7.1.0002.15. Государственная фармакопея Российской Федерации. XIII издание. Том И.
7. Правила проведения исследований биологических лекарственных средств Евразийского экономического союза от 06.05.17 г, решение №89 от 03.11.2016 (доступно на: https://docs.eaeunion.org/docs/ru-ru/01411954/cncd_21112016_89).
8. Gilbert Verbeken, Jean-Paul Pirnay, Rob Lavigne, Serge Jennes, Daniel De Vos, Minne Casteels, and Isabelle Huys. Call for a Dedicated European Legal Framework for Bacteriophage Therapy. Archivum Immunologiae Et Therapiae Experimentalis. Feb 6, 2014; 62(2): 117-129.
9. Патент RU №2455355, опубл. 10.07.2012. Козлова Ю.Н., Репин B.E., Анищенко В.В., Власов В.В., Ганичев Д.А., Семенов С.А., Пугачев В.Г., Тарасов О.С. Штамм бактериофага Pseudomonas aeruginosa, используемый в качестве основы для приготовления асептического средства против синегнойной палочки.
10. Патент WO 2015059298. Phage therapy of Pseudomonas infections. Pouillot Flavie, Blois Helene [FR], 30.04.2015.
11. Патент EP 2248890. Bacteriophages specific to РАК and СНА strains of Pseudomonas aeruginosa and their applications. Debarbieux Laurent [FR]; Morello Eric [FR]. 10.11.2010.
12. Патент PL №007472, опубл. 27.10.2006. Вебер-Дабровска Б., Мульчик М., Гурски А., Боратыньски Я, Лусяк-Шелаховска М., Сыпер Д. Поливалентные штаммы бактериофага, способы их получения и использования и содержащее указанные штаммы лекарственное средство.
13. Патент RU №2186574, опубл. 10.08.2002. Яфаев Р.Х., Асланов Б.И., Зуева Л.П. Препарат поливалентного бактериофага против синегнойной палочки, штаммы бактериофага Bacteriophagum Pseudomonas aeruginosa СПБГМА им. И.И. Мечникова №05, №03, №06 и №07, используемые при приготовлении поливалентного препарата против синегнойной палочки.
14. Патент RU №2112800 от 29.03.1996. Жиленков Е.Л., Степанов А.В., Дианов Е.Е., Негрий В.Ф., Гаевская Г.Б. Штамм пилеспецифического бактериофага Pseudomonas aeruginosa ГНЦПМ №03, используемый для приготовления лечебного препарата против синегнойной палочки.
15. Патент RU №2113476 опубл. 20.06.1998. Жиленков Е.Л.; Благодатских А.Я.; Степанов А.В.; Негрий В.Ф.; Ковалева З.А. Штамм бактериофага Pseudomonas aeruginosa SA ГНЦ ПМ №02, используемый при изготовлении поливалентного лечебного препарата против синегнойной палочки.
16. Патент RU №2366437 опубл. 10.09.2009. Алешкин А.В., Алешкин В.А., Амерханова A.M., Афанасьев Д.С., Афанасьев С.С., Гаврин А.Г., Голикова В.М., Давыдкин В.Ю., Давыдкин И.Ю., Киселева И.А., Логунов О.В., Пугачева Т.Г., Рубальский Е.О., Рубальский О.В. Композиция на основе бактериофага (варианты).
18. Авторское свидетельство №1158578 «Способ определения выхода бактериофага S3 шигелл Зонне», 1985 г.
19. Каттер Э., Сулаквелидзе А. Бактериофаги: биология и практическое применение. Пер. с англ. Москва: Научный мир; 2012.
20. Bacteriophage and its vectors. Ed.: Sambrook J., Russell D. Molecular Cloning. Cold Spring Harbour Laboratory Press. 2001.































































































Изобретение относится к области биотехнологии. Изобретение относится к штамму бактериофага Pseudomonas aeruginosa, используемого при производстве медицинских биологических антибактериальных лекарственных средств - препаратов бактериофагов, предназначенных для профилактики и лечения гнойно-воспалительных и энтеральных заболеваний, вызванных бактериями Pseudomonas aeruginosa. Штамм обладает литической активностью в отношении бактерий синегнойной палочки Pseudomonas aeruginosa. Штамм депонирован в Государственной коллекции патогенных микроорганизмов (ГКПМ) Федерального государственного бюджетного учреждения «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) под регистрационным номером №328 (500322). Штамм обладает широким спектром антибактериальной активности в отношении эпидемиологически значимых госпитальных и выделенных от больных с различной патологией клинических штаммов патогенных бактерий P. aeruginosa, в 100% резистентных к одному или более антибиотикам, полученных с максимальным расширением географии регионов выделения. 4 пр., 1 ил.
Штамм бактериофага Pseudomonas aeruginosa, депонированный в Государственной коллекции патогенных микроорганизмов (ГКПМ) Федерального государственного бюджетного учреждения «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) под регистрационным номером N328 (500322), обладающий антибактериальной активностью в отношении лекарственно устойчивых клинических и госпитальных штаммов бактерий P. aeruginosa, предназначенный для приготовления моно- и поливалентных препаратов бактериофагов, использующихся для лечения и профилактики инфекционных заболеваний, вызванных бактериями Pseudomonas aeruginosa.
| ШТАММ БАКТЕРИОФАГА Pseudomonas aeruginosa, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ОСНОВЫ ДЛЯ ПРИГОТОВЛЕНИЯ АСЕПТИЧЕСКОГО СРЕДСТВА ПРОТИВ СИНЕГНОЙНОЙ ПАЛОЧКИ | 2011 |
|
RU2455355C1 |
| БАКТЕРИОФАГ, ОБЛАДАЩИЙ АКТИВНОСТЬЮ ПРОТИВ PSEUDOMONAS AERUGINOSA, БЕЛКИ БАКТЕРИОФАГА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2580248C9 |
| БАКТЕРИОФАГИ, ФАГОВЫЕ ПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2614114C2 |
| ШТАММ ПИЛЕСПЕЦИФИЧЕСКОГО БАКТЕРИОФАГА PSEUDOMONAS AERUGINOSA ГНЦПМ N 03, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ЛЕЧЕБНОГО ПРЕПАРАТА ПРОТИВ СИНЕГНОЙНОЙ ПАЛОЧКИ | 1996 |
|
RU2112800C1 |
| ШТАММ БАКТЕРИОФАГА PSEUDOMONAS AERUGINOSA ГНЦ ПМ N 02, ИСПОЛЬЗУЕМЫЙ ПРИ ИЗГОТОВЛЕНИИ ПОЛИВАЛЕНТНОГО ЛЕЧЕБНОГО ПРЕПАРАТА ПРОТИВ СИНЕГНОЙНОЙ ПАЛОЧКИ | 1996 |
|
RU2113476C1 |
| Штамм бактериофага РSеUDомоNаS aeRUGINoSa, используемый для идентификации и индикации микробов РSеUDомоNаS aeRUGINoSa | 1987 |
|
SU1472500A1 |
| Видоизменение приспособления для подведения пенообразующих реактивов в резервуары с огнеопасными жидкостями, охарактеризованного в пат. № 18673 | 1929 |
|
SU20968A1 |
Авторы
Даты
2020-03-17—Публикация
2019-06-28—Подача