Изобретение относится к области органической химии, а именно к способу получения замещенных α-бромарилацетальдегидов* соответствующих структурной формуле 1.
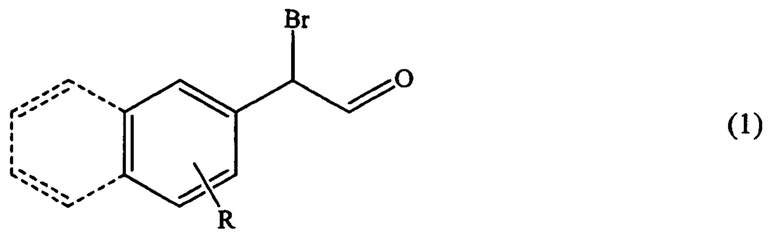
Где R - может быть 2-Hal**; 3-Hal**; 4-Hal**; 2,3-Ди-Hal**; 2,4-ди-Hal**; 2,6-ди-Hal**; 2-алкил***; 3-алкил***; 4-алкил***; 2,3-диалкил***; 2,4-диалкил***; 2,6-диалкил***;
* - арил = фенил, нафтил;
**-Hal = F, Cl, Br;
*** - алкильные радикалы содержат от 1 до 3 атомов углерода,
α-бромарилацетальдегиды могут быть использованы в качестве прекурсоров для синтеза различных классов органических соединений.
Известно несколько способов селективного бромирования арилацетальдегидов в α-положение относительно карбонильной группы.
В работах [1]-[6] описывается получение α-бромфенилацетальдегида взаимодействием фенилацетальдегида с молекулярным бромом в среде различных растворителей при температурах от минус 10°С до 0°С. Однако, данный способ не эффективен для бромирования фенилацетальдегидов с заместителями в ароматическом кольце, ввиду низких выходов конечных продуктов (10-35%), а также необходимостью работы с бромом, который является высокотоксичным и летучим веществом, что усложняет аппаратурное оформление и требования по технике безопасности.
L.J. Gun и др. в работе [7] описывают бромирование фенилацетальдегида системой бромата натрия с триметилсилилбромидом в присутствии катализатора межфазного переноса бензилтриэтиламмонийхлорида в четыреххлористом углероде. Недостатками реакции являются высокая стоимость используемых реагентов, а также необходимость тщательной подготовки растворителя.
В доступной литературе [8]-[16] имеются данные о бромировании альдегидов в α-положение относительно карбонильной группы. В качестве бромирующих агентов используют N-бромсукцинимид, комплекс бром-диоксан, 5,5-дибромбарбитуровую кислоту, 4,4-дибромциклогекса-2,5-диенон и др., однако данные сведения не распространяются на способы получения замещенных α-бромфенилацетальдегидов.
Наиболее близким к способу, предлагаемому в настоящем изобретении, является способ, описанный в патенте [17]. В нем авторами предложен способ получения α-бром-α-метилфенилацетальдегида, который заключается в последовательном воздействии на исходный α-метилфенилацетальдегид изопропенилацетатом и последующей обработкой образовавшегося ацилированного енола двумя эквивалентами бромида меди (II) в ацетонитрильной среде при температуре кипения растворителя в течение 30 минут (процесс бромирования). Выход продукта бромирования не превышает 60%, к тому же, велика вероятность гидролиза целевого продукта при выделении, что отмечено авторами.
Задачей данного изобретения является упрощение процесса получения α-бромарилацетальдегидов и увеличение выхода целевых соединений.
Предлагаемый способ ранее не описан в доступной литературе для синтеза данного класса соединений и заключается в том, что соответствующие арилацетальдегиды бромируют бромидом меди (II) в смеси растворителей хлороформ/этилацетат (1 к 1 по объему) при кипячении.
Отличием предлагаемого способа от ранее известного является то, что исходные арилацетальдегиды бромируются напрямую, без предварительного ацилирования. В этом случае выделение продукта из реакционной смеси происходит фильтрацией, отгонкой растворителя при пониженном давлении и перегонкой при пониженном давлении или разделением при помощи колоночной хроматографии, что исключает возможность гидролиза целевых соединений.
Экспериментальная часть
Описываемый способ иллюстрируется следующими примерами.
Пример 1.
Синтез α-бром-2,3-дифторфенилацетальдегида
В круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником с хлоркальциевой защитой, помещают 2,0 г (8,9 ммоль) бромида меди (II) в 30 мл смеси хлороформ/этилацетат (50/50). К нему при перемешивании и комнатной температуре прикапывают 0,7 г (4,5 ммоль) 2,3-дифторфенилацетальдегида в 20 мл смеси хлороформ/этилацетат (50/50). Реакционную массу перемешивают при комнатной температуре 1 час, а затем кипятят до полного превращения черного бромида меди (II) в белый бромид меди (I), 20…24 часа. Полученный раствор фильтруют через силикагель, растворитель упаривают. Остаток перегоняют в вакууме (110°С/4 мм рт. ст.). Получают 0,75 г (3,2 ммоль) α-бром-2,3-дифтор-фенилацетальдегида в виде светло-желтой жидкости. Выход продукта составил 71%. Найдено, %: С, 40.91; Н,2.18; Br, 33.94; F, 16.12; О, 6.85. C8H5BrF2O. Вычислено, %: С, 40.88; Н, 2.14; Br, 34.00; F, 16.17; О, 6.81.
Пример 2.
Синтез α-бром-2,6-дихлорфенилацетальдегида
В круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником с хлоркальциевой защитой, помещают 4,7 г (21,2 ммоль) бромида меди (II) в 50 мл смеси хлороформ/этилацетат (50/50). К нему при перемешивании и комнатной температуре прикапывают 1,0 г (5,3 ммоль) 2,6-дихлорфенилацетальдегида в 30 мл смеси хлороформ/этилацетат (50/50). Реакционную массу перемешивают при комнатной температуре 1 час, а затем кипятят в течение 24 часов. Полученный раствор фильтруют через силикагель, растворитель упаривают, а-бром-2,6-дихлорфенилацетальдегид отделяют на флэш-хроматографе с использованием нормальнофазной колонки, элюент - дихлорметан. Получают 1,1 г (4,1 ммоль) α-бром-2,6-дихлорфенилацетальдегида в виде желтой маслянистой жидкости. Выход составил 75%. Найдено, %: С, 35.80; Н, 1.93; Br, 29.86; Cl, 26.37; О, 6.03. C8H5BrCl2O. Вычислено, %: С, 35,86; Н, 1.88; Br, 29.82; Cl, 26.46; О, 5.97.
Пример 3.
Синтез α-бром-2,3-диметилфенилацетальдегида
В круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником с хлоркальциевой защитой, помещают 3,0 г (13,4 ммоль) бромида меди (II) в 50 мл смеси хлороформ/этилацетат (50/50). К нему при перемешивании и комнатной температуре прикапывают 1,0 г (6,7 ммоль) 2,3-диметилфенилацетальдегида в 40 мл смеси хлороформ/этилацетат (50/50). Реакционную массу перемешивают при комнатной температуре 1 час, а затем кипятят до полного превращения черного бромида меди (II) в белый бромид меди (I), 15…18 часов. Полученный раствор фильтруют через силикагель, растворитель упаривают. Остаток перегоняют в вакууме (135°С/5 мм рт. ст.). Получают 1,0 г (4,3 ммоль) q-бром-2,3-диметилфенилацетальдегида в виде светло-желтой жидкости. Выход составил 63%. Найдено, %: С, 52.90; Н, 4.92; Br, 35.13; О, 7.05. C10H11BrO. Вычислено, %: С, 52.89; Н, 4.88; Br, 35.18; О, 7.04.
Таким образом, предлагаемый способ селективного бромирования замещенных арилацетальдегидов бромидом меди (II) позволяет получать замещенные α-бромарилацетальдегиды с выходом до 80%. Данный способ отличается простотой и хорошей воспроизводимостью результатов, а также исключает использование дорогостоящих и опасных реактивов.
Литература
1. US 20130184284 Diaminocyclohexane compounds as NPY Y4 receptor modulator and their preparation / E.R. William, Y. Zhu, C. Sun, Y. Huang, M.S. Karatholuvhu. - опубл. 18.07.2013 г.
2. WO 2008144767 (A1) Heterocyclic kinase modulators / P.-Y. Bounaud, C.R. Smith, E.A. Jefferson, J. HEndle, P.S. Lee, A.M. Thayer, G.C. Hirst. - опубл. 27.11.2008 г.
3. WO 2009062676 (A2) Imidazo[1,2-A]pyribine derivatives and their use as positive allosteric modulators of mglur2 receptors / A.A. Tabanco-Suarez, G.J. Tresadern, J.A. Vega Ramiro. - опубл. 22.05.2009 г.
4. Eckhardt M. Product class 4:2-heteroatom-substituted aldehydes and sugar aldehydes. - Science of Synthesis. - №25. - 2007. - P. 463-506.
5. WO 2010144550 (A1) Preparation of triazine derivatives as protein kinases modulators for treating diseases characterized by undersired cellular proliferation or hyperproliferation / T. Chunlin, Q. Wang, L. Nallan, T. Polat. - опубл. 16.12.2010 г.
6. WO 2017025416 (A1) Preparation of imidazo[1,2-b][1,2,4]triazine and imidazo[1,2-α]pyrimidine derivatives for treatment or prevention of parasitic diseases / B. Stephen, P.G. Dodd, E.J. Ko, M.M. Martin, T.J. Miles. - опубл. 16.02.2017 г.
7. Lee J.G. and others, Benzylic bromination of alkylbenzenes with sodium bromate-bromotrimethylsilane. - Bulletin of the Korean Chemical Society, 16(4), 1995, P. 371-374.
8. Eckhard M. 2-heteroatom-substituted aldehydes and sugar aldehydes. - J. Science of Synthesis. - №25 - Vol. 4 - P. 463-506.
9. Erlenmeyer H., Jung J.P. Helv. Chim. Acta. - 1949. - №32. - P. 35.
10. Stevens C.L., Gillis B.T. J. Am. Chem. Soc. - 1957. - №79. - P. 3448.
11. Kanao M., Watanabe Y. / M.Kanao, Y. Watanabe, Y. Kimura, J. Seagusa, K. Yamamoto, H. Kanno, N. Kanaya, H. Kubo, S.-i.Ashida, F. Ishikawa. - J. Med. Chem. - 1986. - №21 - P. 461.
12. Dubief R., Robbe Y. / R. Dubief, Y. Robbe, J.-P. Fernandes, G. Subra, A. Terol, J.-P. Chapat, H. Sentenac-Roumanou, M. Fatome. - J. Med. Chem. - 1986. - №21. - P. 1326
13. Minami I., Yuhara M. / I. Minami, M. Yuhara, H. Watanabe, J. Tsuji. - J. Organomet. Chem. - 1987. - №334. - P. 225.
14. Kanao M., Watanabe Y. / M.Kanao, Y. Watanabe, Y. Kimura, H. Kanno, H. Kubo, S. -i.Ashida. - Chem. Pharm. Bull. - 1988. - №36 - P. 2968.
15. Meakins G.D., Musk S.R.R. / G.D. Meakins, S.R.R. Musk, C.A. Robertson, L.S. Woodhouse. - J. Chem. Soc, Perkin Trans. 1. - 1989. - P. 643.
16. Eriks J.C., van der Goot H. / J.C. Eriks, H. van der Goot, G.J. Sterk, H. Timmerman. - J. Med. Chem. - 1992. - №35. - P. 3239.
17. US 20170174607 (A1) Methods of preparing α,β-unsaturated or a-halo ketones and aldehydes / I.R. Baxendale, J.S. Sharley, A.F. Miranda, A.M.C. Perez. - опубл. 22.06.2017 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛЗАМЕЩЕННОГО ГЕТЕРОЦИКЛИЧЕСКОГО ПРОИЗВОДНОГО ПОСРЕДСТВОМ СОЧЕТАНИЯ С ИСПОЛЬЗОВАНИЕМ ПЕРЕХОДНОГО МЕТАЛЛА В КАЧЕСТВЕ КАТАЛИЗАТОРА | 2010 |
|
RU2510393C9 |
| СПОСОБ ПОЛУЧЕНИЯ ОНИЕВЫХ СОЛЕЙ С ТЕТРАФТОРБОРАТНЫМ АНИОНОМ, ИМЕЮЩИХ НИЗКОЕ СОДЕРЖАНИЕ ГАЛОГЕНИДОВ | 2005 |
|
RU2415843C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АЛКОКСИ-3-ГИДРОКСИПИКОЛИНОВЫХ КИСЛОТ | 2017 |
|
RU2744834C2 |
| Способ получения спинохрома D | 2016 |
|
RU2612265C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ (ЦИКЛОПЕНТИЛ[d]ПИРИМИДИН-4-ИЛ)ПИПЕРАЗИНОВЫХ СОЕДИНЕНИЙ | 2015 |
|
RU2732404C2 |
| ПОЛИМЕРЫ БЕНЗОДИТИОФЕНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ОРГАНИЧЕСКИХ ПОЛУПРОВОДНИКОВ | 2011 |
|
RU2575852C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛЗАМЕЩЕННОГО ГЕТЕРОЦИКЛИЧЕСКОГО ПРОИЗВОДНОГО ПОСРЕДСТВОМ СПОСОБА СОЧЕТАНИЯ С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЯ ПАЛЛАДИЯ | 2011 |
|
RU2563459C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ (ЦИКЛОПЕНТИЛ[D]ПИРИМИДИН-4-ИЛ)ПИПЕРАЗИНОВЫХ СОЕДИНЕНИЙ | 2015 |
|
RU2712224C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-БРОМАДАМАНТАНА | 2009 |
|
RU2428408C2 |
| СПОСОБ ПОЛУЧЕНИЯ (3R,7R)-ГЕКСАГИДРОФАРНЕЗИЛБРОМИДА | 2007 |
|
RU2359952C2 |
Изобретение относится к области органической химии. Изобретение касается способа получения замещенных α-бромарилацетальдегидов* согласно схеме 1:
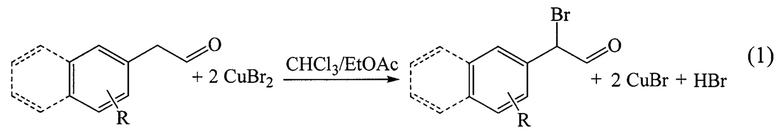
Где R - может быть 2-Hal**; 3-Hal**; 4-Hal**; 2,3-Ди-Hal**; 2,4-ди-Hal**; 2,6-ди-Hal**; 2-алкил***; 3-алкил***; 4-алкил***; 2,3-диалкил***; 2,4-диалкил***; 2,6-диалкил***; * - арил = фенил, нафтил; **-Hal = F, Cl, Вr; *** - алкильные радикалы содержат от 1 до 3 атомов углерода, отличающийся тем, что бромирование арилацетальдегидов производится в системе хлороформ/этилацет, а в качестве бромирующего агента выступает бромид меди (II). Техническом результатом данного изобретения является упрощение процесса получения α-бромарилацетальдегидов и увеличение выхода целевых соединений. 3 пр.
Новый способ получения замещенных α-бромарилацетальдегидов* согласно схеме 1:
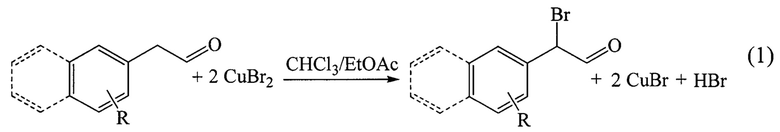
Где R - может быть 2-Hal**; 3-Hal**; 4-Hal**; 2,3-Ди-Hal**; 2,4-ди-Hal**; 2,6-ди-Hal**; 2-алкил***; 3-алкил***; 4-алкил***; 2,3-диалкил***; 2,4-диалкил***; 2,6-диалкил***;
* - арил = фенил, нафтил;
**-Hal = F, Cl, Вr;
*** - алкильные радикалы содержат от 1 до 3 атомов углерода,
отличающийся тем, что бромирование арилацетальдегидов производится в системе хлороформ/этилацет, а в качестве бромирующего агента выступает бромид меди (II).
| US 20170174607 A1, 22.06.2017 | |||
| WO 2017025416 A1, 16.02.2017 | |||
| 6,7-ДИФЕНИЛ-2,3-ДИЦИАНОНАФТАЛИН И СПОСОБ ПОЛУЧЕНИЯ 6,7-ДИФЕНИЛ-2,3-ДИЦИАНОНАФТАЛИНА | 2010 |
|
RU2426725C1 |
| WO 2010144550 A1, 16.12.2010. | |||
Авторы
Даты
2020-03-27—Публикация
2019-08-05—Подача