Область техники, к которой относится изобретение
Изобретение относится к области переработки отработавшего ядерного топлива.
Более конкретно, изобретение относится к применению альдоксимов, содержащих по меньшей мере пять атомов углерода, в качестве агентов противоазотистого действия в операциях восстановительной реэкстракции плутония.
Изобретение может найти применение в любых способах переработки отработанного ядерного топлива, включающих одну или нескольку операций восстановительной реэкстракции плутония.
Такие операции имеются, в частности, в процессе PUREX в том виде, как он применяется на современных заводах по переработке отработанного ядерного топлива (т.е. на заводах UP3 UP2-800 на Аге (La Hague), Франция, и на заводе Роккашо (Rokkasho), Япония), во-первых, для осуществления этапа разделения урана и плутония при первом цикле дезактивации этого процесса, а в-вторых, для улучшения дезактивации плутония в продуктах деления во время цикла очистки плутония, обычно называемого «вторым циклом плутония» и следующего за первым циклом дезактивации.
Эти операции присутствуют также в некоторых способах, которые являются производными способа PUREX, например в способе, описанном в международной заявке PCT WO 2006/072729 [1], известном под названием СОЕХ, или же в способе, описанном в международной заявке PCT WO 2011/000844 [2].
Уровень техники
Операции восстановительной реэкстракции плутония, применяемые в названных выше способах переработки отработанного ядерного топлива, заключаются в переводе плутония из органической фазы (или фазы растворителя), в которой он находится при степени окисления (IV), в водную фазу посредством восстановления плутония до степени окисления (III), при которой его сродство к органической фазе очень низко.
Восстановление плутония (IV) в плутоний (III) происходит под действием восстановителя, добавляемого в водную фазу, используемую для реэкстракции, и стабилизируемого агентом противоазотистого действия.
Например, при первом цикле дезактивации процесса PUREX в том виде, как он применяется на современных заводах по переработке отработанного ядерного топлива (упрощенно называемого ниже «процессом PUREX»), восстановителем, применяемым для реэкстракции плутония на этапе разделения урана и плутония, выступает уран (IV) (или нитрат четырёхвалентного урана), в то время как агентом противоазотистого действия является нитрат гидразина, называемый также гидразином.
Основными рассматриваемыми химическими реакциями являются:
- восстановление плутония (IV) в плутоний (III) ураном (IV) (рабочая реакция):
U4+ + 2Pu4+ + 2H2O → UO22+ + 2Pu3+ + 4H+,
- повторное окисление плутония (III) в плутоний (IV) (побочная реакция):
Pu3+ + HNO3 + 1,5H+ + 0,5NO3- → Pu4+ + 0,5H2O + 1,5HNO2 ,
- окисление урана (IV) в уран (VI) азотистой кислотой (побочная реакция):
U4+ + 2HNO2 → UO2+ + 2NO + 2H+,
- разложение азотистой кислоты с образованием азотистоводородной кислоты посредством гидразина (полезная реакция):
N2H5NO3 + HNO2 → N3H + HNO3 + 2H2O.
Две первых реакции протекают в водной и органической фазах, в то время как реакция разложения азотистой кислоты гидразином происходит только в водной фазе вследствие неэкстрагируемости гидразина органической фазой, где последняя состоит из фосфата три-н-бутила (или ТВР) при 30% (в объёмном отношении) в гидрогенированном тетрапропилене (или ТРН).
Присутствие плутония (III) в органической фазе, даже в малом количестве, катализирует окисление урана (IV) при обеих первых реакциях и поэтому образуется азотистая кислота.
В ходе экспериментальных исследований, проведённых в лабораторных центробежных экстракторах, удалось установить, что даже при кратком времени пребывания в экстракторе (порядка нескольких секунд) расход урана (IV) вследствие окисления очень значителен. Такое окисление урана (IV) происходит преимущественно в органической фазе, при этом гидразин присутствует только в водной фазе. Поэтому схемами по применению операций восстановительной реэкстракции плутония предусмотрен большой избыток восстановителя.
В свою очередь азотистоводородная кислота, образующаяся вследствие реакции разложения азотистой кислоты гидразином, вступает с азотистой кислотой в следующую реакцию:
HN3 + HNO2 → N2 + N2O + H2O.
Однако кинетика такой реакции намного более медленная, чем кинетика реакции разложения азотистой кислоты гидразином, вследствие чего азотистоводородная кислота находится в водной и органической фазах, выделяющихся на этапе разделения урана и плутония.
Следовательно, тот факт, что гидразин не способен экстрагироваться органической фазой и поэтому действует только в водной фазе, ведёт к значительному расходу реактивов и к образованию химических веществ, осложняющих промышленное применение такого способа.
Для решения этой проблемы в международной заявке PCT WO 2008/148863 [3] было предложено применять двухфазную систему противоазотистого действия, включающую в себя оксим бутаналя, называемый также оксимом бутиралдегида или бутиралдоксимом, с гидразином, при этом оксим бутаналя позволяет стабилизировать органическую фазу, в то время как гидразин стабилизирует водную фазу.
Хотя применение оксима бутаналя в ассоциации с гидразином обеспечивает определённые преимущества, в частности, оно позволяет существенно снизить количество нитрата четырёхвалентного урана и гидразина, необходимое для проведения восстановительной реэкстракции плутония и, следовательно, уменьшает недостатки, вызванные не-экстракцией гидразина органической фазой, такое применение не является, тем не менее, полностью удовлетворительным по следующим причинам:
- экстракция оксима бутаналя органической фазой относительно слаба, что приводит к необходимости вводить этот оксим в большом количестве в экстрактор, в котором протекает восстановительная реэкстракция плутония, если при этом требуется получить эффективную концентрацию оксима бутаналя в органической фазе; в частности, на этапе разделения урана и плутония экстракция оксима бутаналя органической фазой существенно снижается вследствие насыщения этой фазы актинидами, что в конечном итоге делает мало пригодным применение такого оксима для проведения этапа разделения;
- продолжающееся применение гидразина в водной фазе; действительно, несмотря на то, что гидразин является одним из наиболее эффективных агентов противоазотистого действия в водной фазе, его применение является вынужденной мерой не только вследствие приведённых выше проблем, связанных с образованием азотистоводородной кислоты, но также с его токсичностью; в самом деле, гидразин числится в списке веществ, являющихся канцерогенными, мутагенными и токсичными при воспроизведении, т.е. веществ, которые рассматриваются в Положении (СЕ) 1907/2006 о регистрации, оценке, и выдаче разрешений и ограничениях химических веществ (Положение REACH) как потенциально или доказано канцерогенные, мутагенные и/или токсичные вещества в отношении воспроизводства и которые рано или поздно могут быть внесены в перечень веществ, для которых согласно приложению XIV этого Положения требуется разрешение, и в таком случае его доступность на рынке и промышленное применение будут запрещены, за исключением специальных отступлений со стороны Европейского агентства по химическим продуктам (ECHA).
Кроме того, отмечалась реакция между оксимом бутаналя и гидразином с образованием гидразина. Такая реакция снижает рабочие характеристики оксима бутаналя и ведёт к перерасходу обоих реактивов.
Учитывая сказанное выше, авторы изобретения поставили перед собой целью обнаружение соединений, обладающих значительным противоазотистым действием, но применение которых не сопровождается недостатками, присущими гидразину в том виде, как он в настоящее время применяется в способе PUREX или при использовании двухфазной системы «оксим бутаналя/гидразин», такой, как предложенная в документе [3].
Более конкретно, авторы изобретения поставили перед собой цель обеспечить большую, чем у оксима бутаналя, способность к экстракции органической фазой для этих соединений, в частности такого типа фазы, которая применяется в процессе PUREX (при той же температуре и давлении), включая даже случаи, когда эта органическая фаза насыщена актинидами, с тем, чтобы можно было (1) уменьшить количество таких соединений, необходимое для проведении восстановительной реэкстракции плутония и (2) применять их при реэкстракции плутония на этапе разделения урана и плутония при первом цикле дезактивации процесса PUREX, а также при реэкстракции плутония при втором цикле данного процесса.
Кроме того, авторы поставили целью обеспечить возможность полного отказа от применения гидразина.
Раскрытие изобретения
Названные цели, а также и другие, достигаются посредством настоящего изобретения, в котором предложено применять по меньшей мере альдоксим, содержащий по меньшей мере пять атомов углерода, т.е. оксим формулы R-CH=N-OH, где R означает углеводородную цепь, содержащую по меньшей мере 4 атома углерода, в качестве агента противоазотистого действия, при проведении операции восстановительной реэкстракции плутония.
Предпочтительно альдоксим отвечает приведённой выше формуле, в которой R содержит не более 12 атомов углерода, предпочтительно не более 8 атомов углерода.
Более предпочтительно, чтобы альдоксим отвечал приведённой выше формуле, в которой R означает линейную алкильную цепь с 4-8 атомами углерода.
Такими альдоксимами являются оксим пенталя, называемый также валериановым альдегидом или валериановым оксимом, формулы n-C4H9-CH=N-OH, оксим гексаналя формулы: n-C5H11-CH=N-OH, оксим гептаналя формулы: n-C6H13-CH=N-OH, оксим октаналя формулы: n-C7H15-CH=N-OH и оксим нонаналя формулы: n-C8H17-CU=N-OH.
Из этих альдоксимов наиболее предпочтительны оксим пентаналя и оксим гексаналя.
Согласно изобретению операция восстановительной реэкстракции плутония предпочтительно включает в себя:
- приведение в контакт органической не смешивающейся с водой фазы, содержащей экстрагент и плутоний в степени окисления IV в органическом растворителе, с водной фазой, содержащей восстановитель, способный восстанавливать плутоний (IV) в плутоний (III), и азотную кислоту, при этом альдоксим присутствует либо в органической фазе, либо в водной фазе в соответствии со своей растворимостью в воде, и
- разделение указанных органической и водной фаз, находящихся в контакте.
Таким образом оксим пенталя, частично растворимый в воде и частично растворимый в органических растворителях, пригодных для применения в операциях восстановительной реэкстракции плутония (в условиях температуры и давления, обычно применяемых при таких операциях), может быть добавлен как в водную фазу, так и в органическую, в то время как альдоксимы с 6 атомами углерода и более, которые нерастворимы или практически нерастворимы в воде (в указанных выше условиях), добавляют в органическую фазу.
Согласно изобретению присутствующий в водной фазе восстановитель предпочтительно выбирается из урана (IV), нитрата гидроксиламмония, называемого также нитратом гидроксиламина, алкилированных производных гидроксиламина, сульфамата двухвалентного железа и сульфаминовой кислоты.
Из этих восстановителей особо предпочтительны уран (IV) и нитрат гидроксиламмония, являющиеся двумя агентами, применяемыми при восстановлении плутония (IV) в плутоний (III) в способе PUREX, первый - на этапе разделения урана и плутония во время первого цикла дезактивации, второй - во время второго цикла, касающегося плутония.
В частности экстрагентом предпочтительно является фосфат три-н-алкила, более предпочтительно фосфат три-н-бутила (TBP), а органическим растворителем предпочтительно является линейный или разветвлённый додекан, такой как н-додекан или гидрированный тетрапропилен (TPH), изопарафиновый растворитель, такой как Isane IP185, Isane IP165 или Isopar L или керосин, в таком случае экстрагент предпочтительно присутствует в данном органическом растворителе в количестве 30% (в объёмном отношении).
В любом случае альдоксим применяется при концентрации, предпочтительно лежащей в диапазоне от 0,01 до 3 моль/литр, более предпочтительно от 0,05 до 0,5 моль/л органической или водной фазы, в то время как восстановитель предпочтительно применяется при концентрации от 0,2 до 0,6 моль/л, более предпочтительно от 0,2 до 0,4 моль/л водной фазы.
Что касается азотной кислоты, то её концентрация в водной фазе предпочтительно составляет от 0,05 до 2 моль/л.
Согласно изобретению альдоксим может использоваться в качестве единственного агента противоазотистого действия в операции восстановительной реэкстракции плутония в том случае, когда он сбалансированно распределяется между органической и водной фазами, находящимися в контакте между собой. Однако в том случае, когда это не происходит из-за очень выраженной способности альдоксима к экстракции органической фазой (при температуре и давлении, обычно применяемых при операциях восстановительной реэкстракции плутония), что обычно происходит с альдоксимами, имеющими 6 атомов углерода или более, такими как оксим гексаналя, оксим гептаналя или оксим октаналя, то этот альдоксим предпочтительно применяется в ассоциации со вторым агентом противоазотистого действия, которым является оксим, не экстрагируемый данной органической фазой (при тех же температуре и давлении).
В таком случае этот неэкстрагируемый оксим, присутствующий в водной фазе, предпочтительно является формальдоксимом, называемым также оксимом формальдегида, формулы CH2=N-OH, или ацеталдоксимом, называемым также оксимом ацеталдегида, формулы CH3-CН=N-OH, предпочтительно применяемым при концентрации от 0,01 до 1 моль/л, более предпочтительно от 0,05 до 0,2 моль/л водной фазы.
Согласно особо предпочтительному варианту выполнения изобретения операция восстановительной реэкстракции плутония является одной из операций по реэкстракции плутония в способе PUREX или способе СОЕХ.
Изобретению присуще множество преимуществ. Действительно, оно предлагает целый набор агентов противоазотистого действия, которые способны, одни при индивидуальном использовании, другие - при использовании в комбинации с неэкстрагируемым органической фазой оксимом, очень эффективно блокировать повторное окисление плутония (III) в плутоний (IV) одновременно и в органической, и водной фазах.
Поэтому, помимо того, что изобретение позволяет осуществлять операции восстановительной реэкстракции плутония без применения гидразина и операции, будь то в ходе операции, применяемой на этапе разделения урана и плутония в способе PUREX, или же в ходе операции, применяемой во время второго плутониевого цикла в том же способе, изобретение, кроме того, позволяет очень существенно снизить количество восстановителя и агента противоазотистого действия, необходимых для проведения этих операций, по сравнению с их количеством в том случае, когда агентом противоазотистого действия выступает гидразин.
Следовательно, настоящее изобретение позволяет ожидать снижения количества точек, необходимых для введения этих агентов противоазотистого действия в аппараты, предназначенные для операций восстановительной реэкстракции плутония, и, следовательно, позволяет упростить эти аппараты.
Кроме того, поскольку реэкстракция плутония оказывается более эффективной и в результате позволяет получить в конце операции реэкстракции водную фазу с большей концентрацией плутония, чем концентрация при использовании гидразина в качестве агента противоазотистого действия, настоящее изобретение позволяет также ожидать уменьшения размеров применяемых в настоящее время аппаратов для осуществления операций восстановительной реэкстракции плутония.
Другие признаки и преимущества изобретения станут более понятны из приводимых ниже примеров.
Разумеется, эти примеры приведены только для иллюстрации предмета изобретения и ни в какой степени не ограничивают его.
Краткое описание фигур
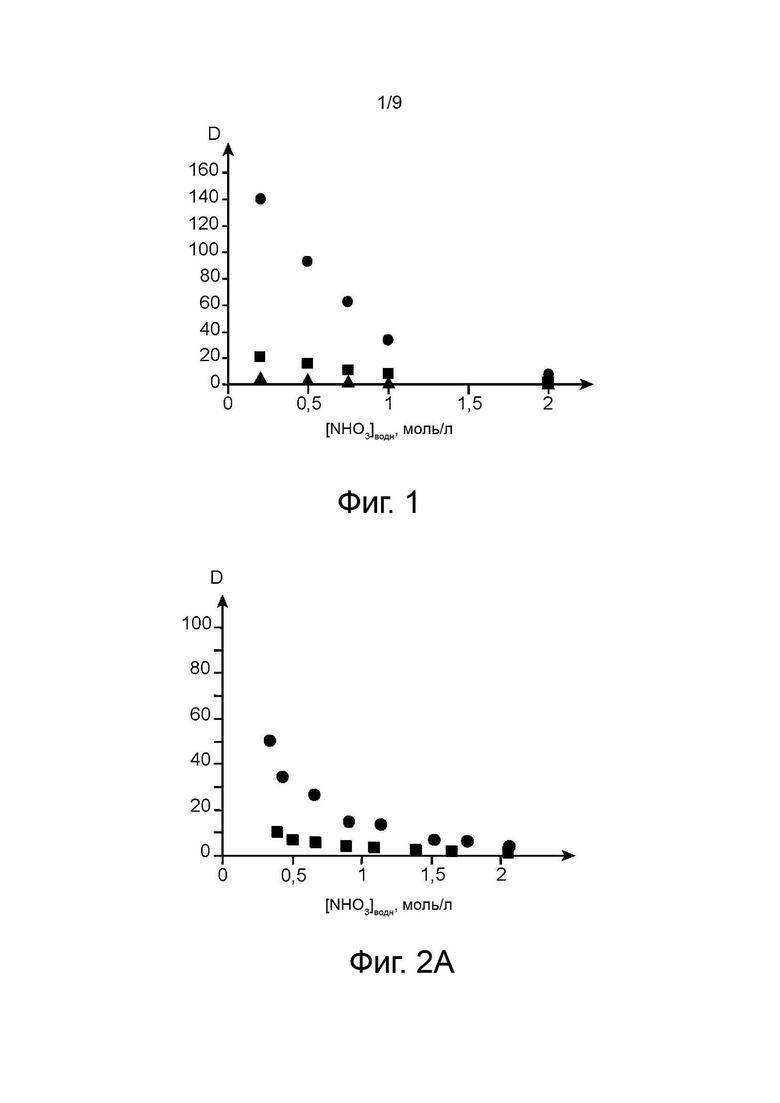
На фиг. 1 приведены коэффициенты распределения оксима пентаналя (символ ■) и оксима гексаналя (символ ●) между органическими фазами, содержащими TBP в н-додекане, и водными фазами, содержащими азотную кислоту в разных концентрациях; для сравнения на этой фигуре также показаны коэффициенты распределения, полученные при тех же условиях для оксима бутаналя (символ ▲).
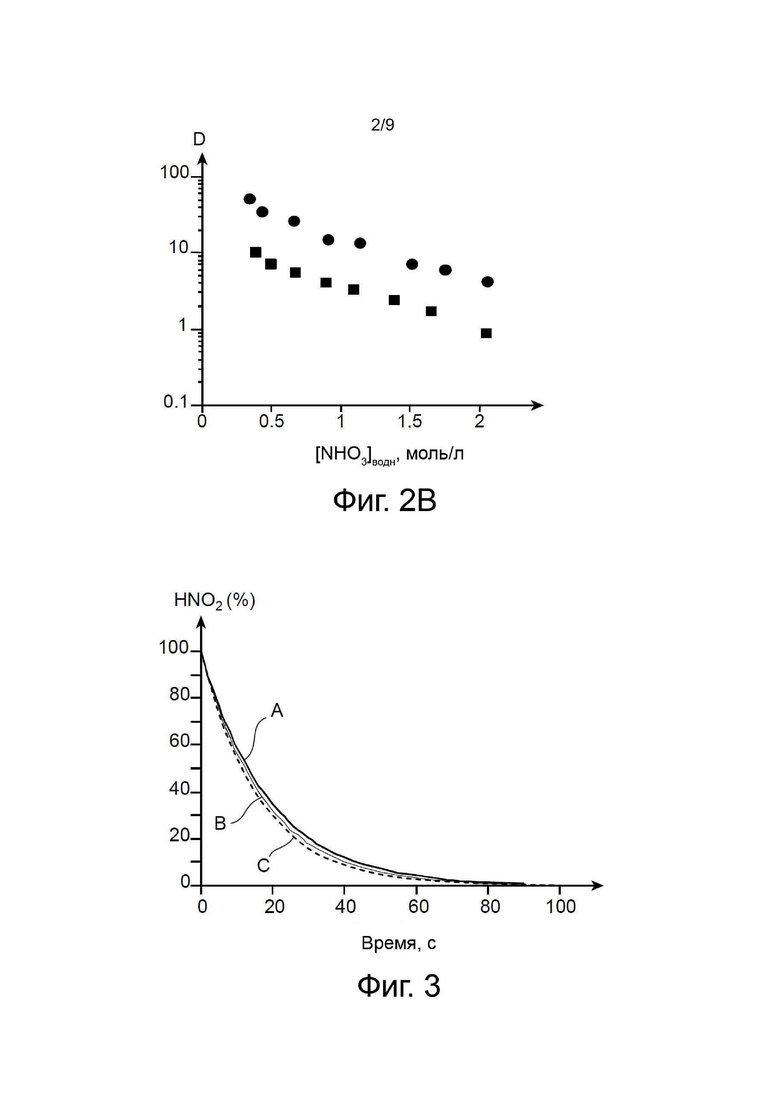
На фиг. 2А и 2В приведены коэффициенты распределения оксима пенталя (символ ■) и оксима гексаналя (символ ●) между органическими и водными фазами, моделирующими, с точки зрения концентрации урана (VI) и концентрации азотной кислоты, органические фазы и водные фазы, полученные на этапе разделения урана и плутония в способе PUREX.
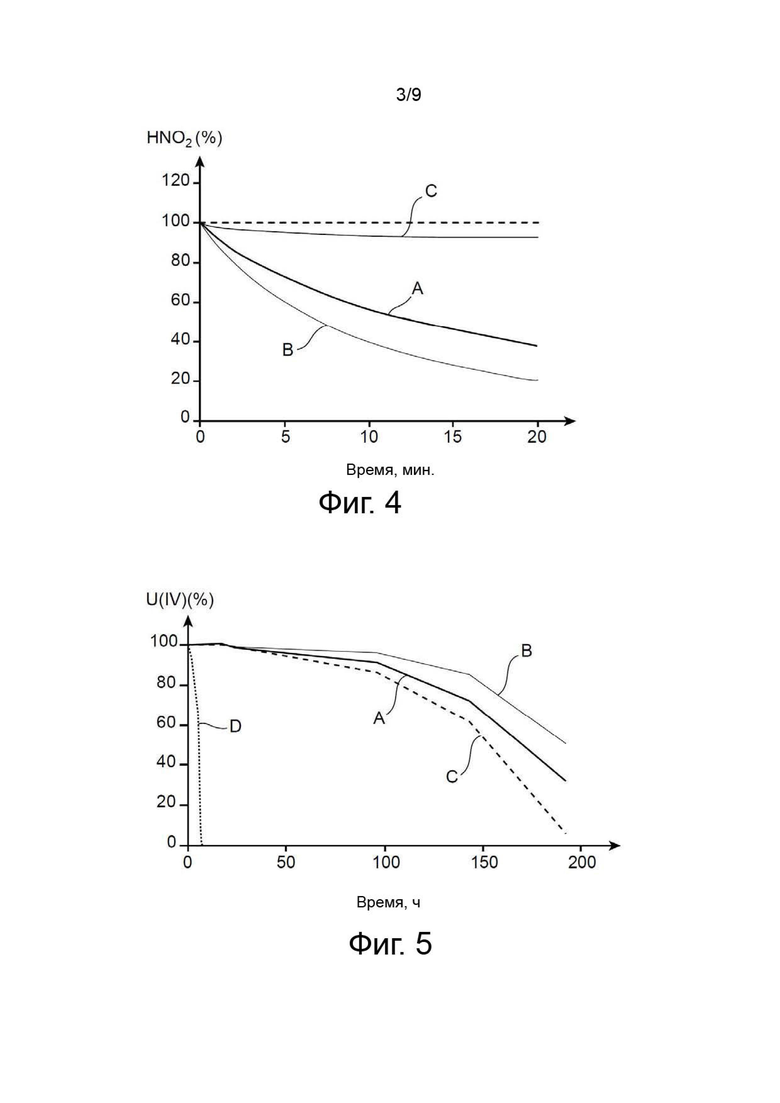
На фиг. 3 проиллюстрирована кинетика разложения азотистой кислоты оксимом пентаналя (кривая А) в азотной водной фазе; для сравнения на этой фигуре представлены также показатели кинетики разложения азотистой кислоты оксимом бутаналя (кривая В) и ацеталдоксимом (кривая С), полученные в тех же условиях.
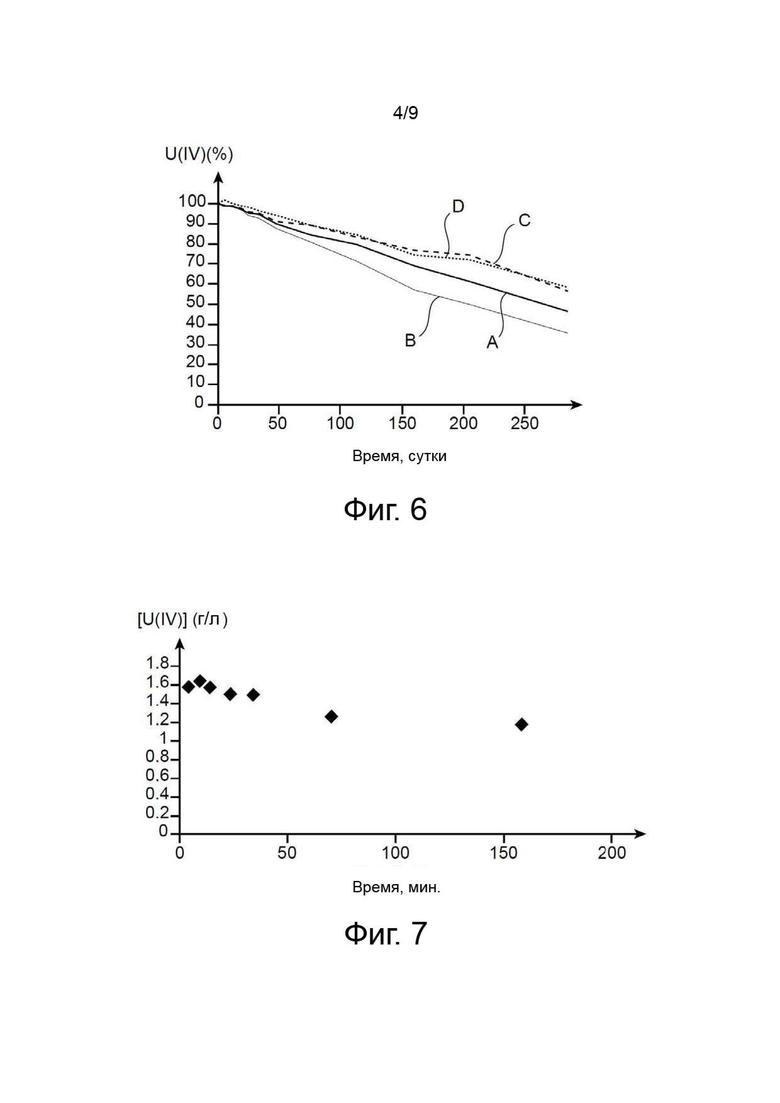
На фиг. 4 приведены показатели кинетики разложения азотистой кислоты оксимом пентаналя (кривая А) и оксимом гексаналя (кривая В) в органических фазах, содержащих TBP в н-додекане; для сравнения на этой фигуре представлена также кинетика разложения азотистой кислоты оксимом бутаналя (кривая С), полученная в тех же условиях.
На фиг. 5 проиллюстрированы показатели кинетики окисления урана (IV), полученные в присутствии оксима пентаналя (кривая А) и оксима гексаналя (кривая В) в органических фазах, содержащих TBP в н-додекане после контакта этих органических фаз с азотной водной фазой и последующего разделения этих фаз; для сравнения на этой фигуре представлены также показатели кинетики окисления урана (IV), полученные в тех же условиях в присутствии оксима бутаналя (кривая С) и в отсутствие какого-либо оксима (кривая D).
На фиг. 6 проиллюстрирована кинетика окисления урана (IV), полученная в присутствии оксима пентаналя (кривая А) в азотной водной фазе; для сравнения на этой фигуре приведены также показатели кинетики окисления урана (IV), полученные в тех же условиях, в присутствии оксима бутаналя (кривая В), ацеталдоксима (кривая С) и гидразина (кривая D).
На фиг. 7 проиллюстрирована кинетика окисления урана (IV) в органической фазе (TBP/ТPH) после опыта по восстановительной реэкстракции плутония, при котором оксим гексаналя применялся в качестве агента противоазотистого действия.
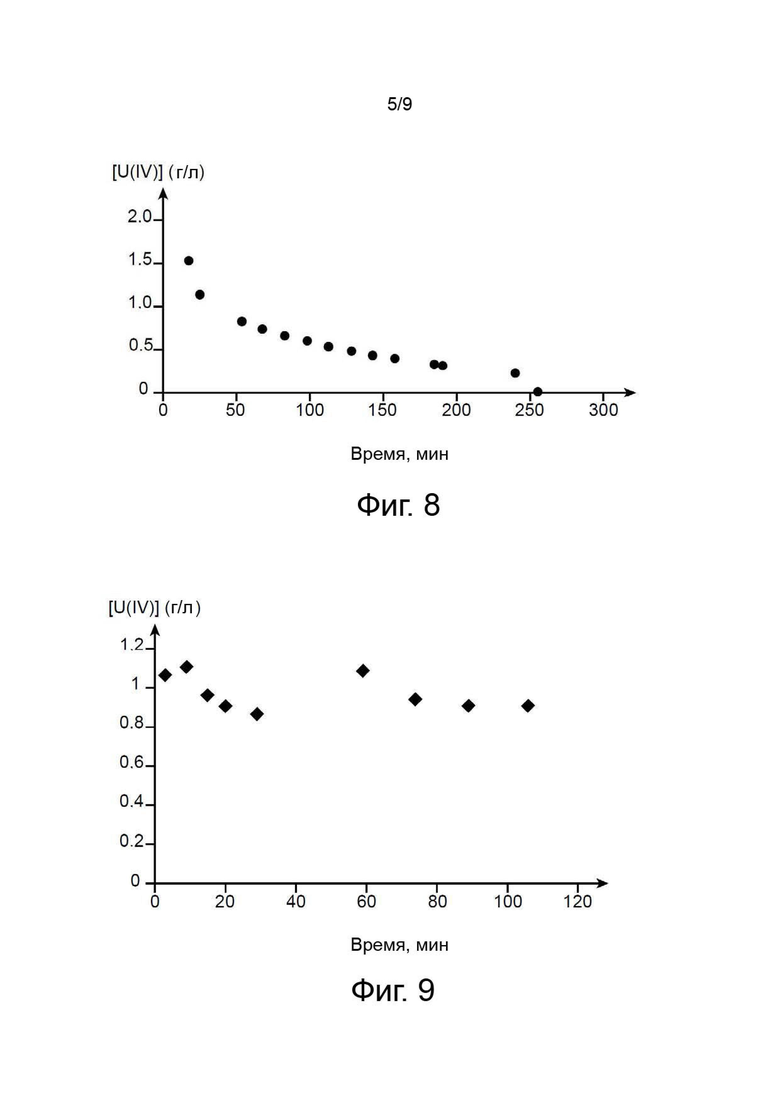
На фиг. 8 проиллюстрирована кинетика окисления урана (IV) в органической фазе (TBP/TPH) после опыта по восстановительной реэкстракции плутония, при котором оксим гексаналя применялся в качестве агента противоазотистого действия и при котором технеций подвергался реэкстракции вместе с плутонием.
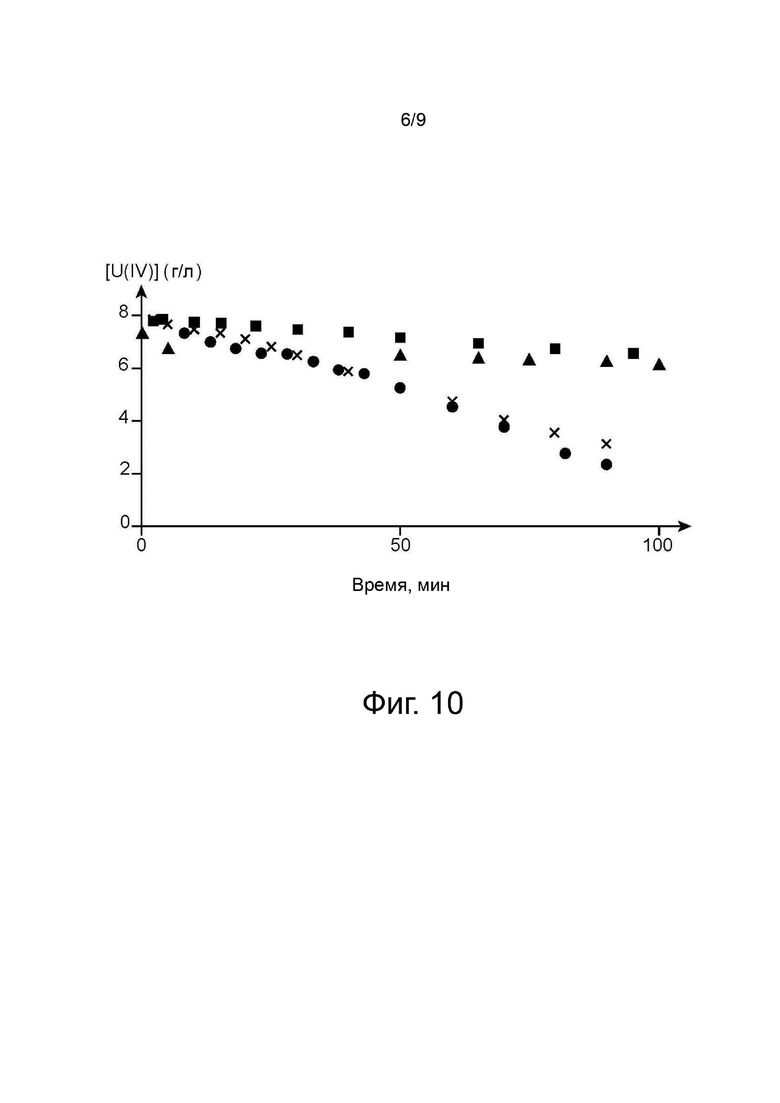
На фиг. 9 проиллюстрирована кинетика окисления урана (IV) в органической фазе (TBP/TPH) после опыта по восстановительной реэкстракции плутония, при котором оксим пенталя применялся в качестве агента противоазотистого действия.
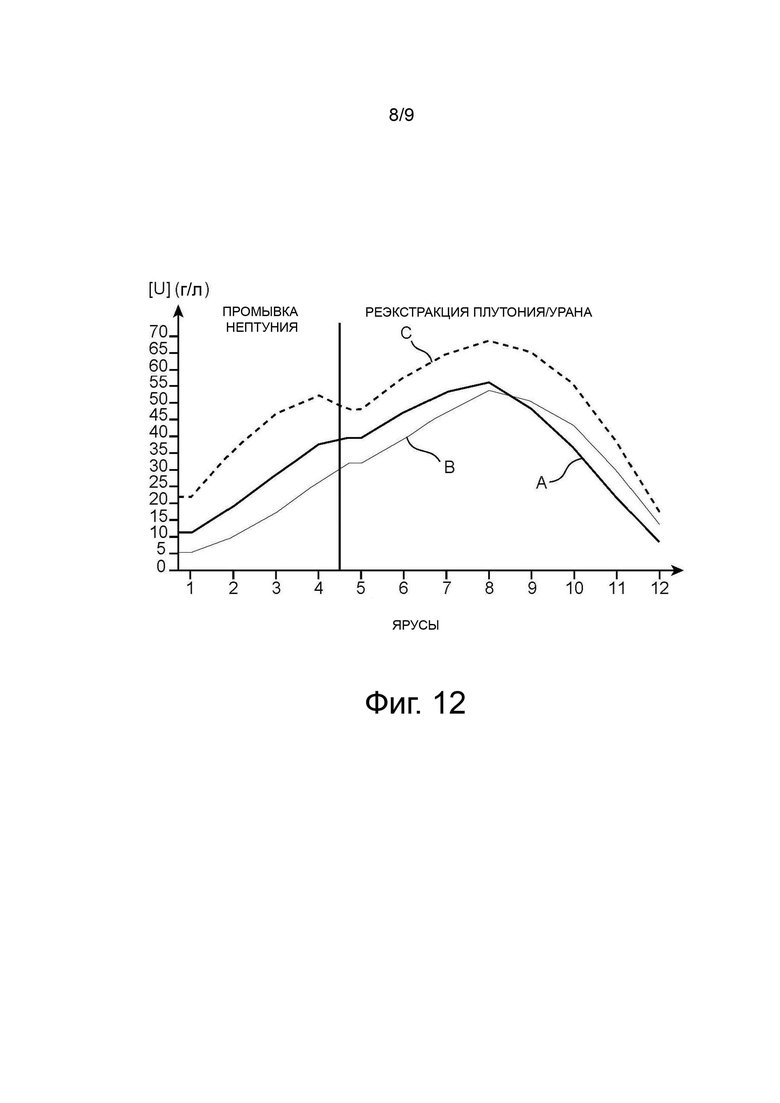
На фиг. 10 проиллюстрирована кинетика окисления урана (IV) в присутствии ацеталдоксима в азотных водных фазах с содержанием 100 мг/л (символ ■) или 200 мг/л (символ х) технеция; для сравнения на этой фигуре показаны также параметры кинетики окисления урана (IV), полученные в тех же условиях в присутствии гидразина и 100 мг/л (символ ▲) или 200 мг/л (символ ●) технеция.
На фиг. 11 проиллюстрирована схема переработки жидкого раствора из отработанного ядерного топлива, включающая этап разделения урана и плутония, на котором в качестве системы противоазотистого действия используется комбинация из оксима гексаналя и ацеталдоксима; на этой фигуре прямоугольные пометки 1-7 означают многоярусные экстракторы, такие как традиционно применяемые при переработке отработанного ядерного топлива (смесители-отстойники, пульсационные колонны, центробежные экстракторы); в частности, органические фазы, поступающие в экстракторы и выходящие из них, показаны символически сплошной линией, а водные фазы, входящие в эти экстракторы и выходящие из них - пунктирной линией.
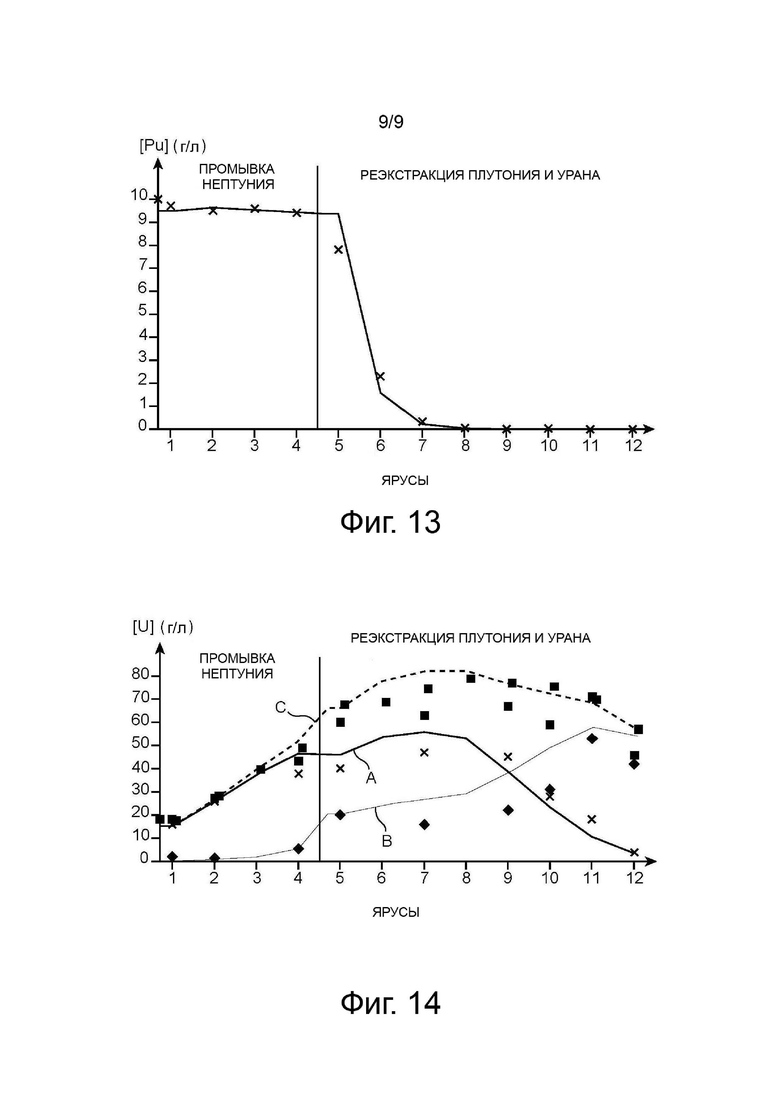
На фиг. 12 проиллюстрирован профиль концентрации урана (IV) в водных фазах, циркулирующих в экстракторах 5 и 6 схемы на фиг. 11, такой как полученный расчётным способом (кривая А); для сравнения представлен также профиль концентраций урана (IV), который был бы получен, если бы оксим гектораля и ацеталдоксим были заменены в этой схеме гидразином (кривая В), а также профиль концентраций урана (IV), который был бы получен, если бы реакции повторного окисления плутония (III) были полностью нейтрализованы (кривая С).
На фиг. 13 проиллюстрированы профили концентраций плутония в водных фазах, циркулирующих в экстракторах 5 и 6 схемы на фиг. 11, которые получают экспериментально (символ х) и расчётным путём (кривая ―);
На фиг. 14 проиллюстрирован профиль концентрации урана (IV), урана (VI) и всего урана в водных фазах, циркулирующих в экстракторах 5 и 6 схемы на фиг. 11, такой как полученный экспериментально и расчетным способом; на этой фигуре символами х, ♦ и ■ обозначены соответственно профили концентраций урана (VI), урана (IV) и всего урана, полученные экспериментально, а кривые А, В и С соответствуют профилям концентраций урана (VI) , урана (IV) и общего урана, полученным расчётами.
Подробное описание частных вариантов выполнения
Пример 1. Свойства оксима пентаналя и оксима гексаналя
1.1 Коэффициенты распределения
Коэффициенты распределения оксима пентаналя и оксима гексаналя, обозначенные буквой D, определяли в двух сериях опытов, а именно:
- первая серия состояла в определении этих коэффициентов распределения между органическими фазами, содержащими 30% (в объёмном отношении) TBP в н-додекане, и водными фазами с содержанием азотной кислоты 0,2-2 моль/л; и
- вторая серия состояла в определении этих коэффициентов распределения между органическими фазами и водными фазами, моделирующими, с точки зрения концентрации урана (VI) и концентрации азотной кислоты, органические фазы и водные фазы, полученные на этапе разделения урана и плутония в способе PUREX, причём эту серию опытов осуществляли в восьмиярусной батарее смесителей-отстойников ВХ1-ВХ8.
Для этого в ходе двух серий опытов каждую органическую фазу приводили в контакт (в объёмном отношении) в течение 15 минут при комнатной температуре (20-25°С) при перемешивании с азотной водной фазой. При этом оксим пентаналя добавляли в водную фазу, а оксим гексаналя - в органическую фазу, концентрация каждого составляла 0,1 моль/л фазы.
Затем находящиеся в контакте между собой органические и водные фазы разделяли центрифугированием, и концентрации альдоксима в этих фазах замеряли посредством жидкой хроматографии высокого разрешения для водных фаз и газовой хроматографии для органических фаз.
Коэффициенты распределения, полученные в первой серии опытов, представлены в таблице 1 ниже. Они приведены также на фиг. 1, на которой показаны значения, приведенные в этой таблице, и на которой коэффициенты распределения оксима пентаналя обозначены символом ■, в то время как коэффициенты распределения оксима гексаналя обозначены символом ●. Для сравнения на фиг. 1 показаны также коэффициенты распределения, полученные в тех же условиях для оксима бутаналя (▲).
Таблица 1
Полученные во время второй серии опытов коэффициенты распределения приведены в таблице 2 ниже. Они приведены и на фиг. 2А и 2В, на которые перенесены их значения (ось ординат) и кислотность водных фаз (ось абсцисс) и на которых коэффициенты распределения оксима пентаналя обозначены символом ■, в то время как коэффициенты распределения оксима гексаналя обозначены символом ●. Ординаты приведены в десятичной шкале на фиг. 2А и в логарифмической - на фиг. 2В.
Таблица 2
моль/л
г/л.
г/л
моль/л
г/л
г/л
Как показано в таблице 1 и на фиг. 1, оксим пентаналя и оксим гексаналя характеризуются коэффициентами распределения, которые значительно превосходят аналогичные коэффициенты оксима бутаналя, что свидетельствует о том, что они обладают намного большей способностью к экстракции в органической фазе, чем оксим бутаналя.
В том случае, когда водная фаза содержит актиниды (таблица 2 и фиг. 2А, 2В), коэффициенты распределения оксима пентаналя и оксима гексаналя оказываются ниже, чем в случае, когда актиниды отсутствуют; вместе с тем, они остаются достаточно высокими для того, чтобы оксим пентаналя и оксим гексаналя в значительной степени подвергались экстракции. Коэффициенты распределения оксима бутаналя в тех же условиях составляют менее 1.
Коэффициенты распределения оксима пентаналя и оксима гексаналя обеспечивают:
- для оксима пентаналя: уравновешенное распределение органической и водной фаз, что даёт возможность применять схемы восстановительной реэкстракции плутония, в которых оксим пенталя применяется самостоятельно для стабилизации одновременно органической и водной фаз, в то время как
- для оксима гексаналя: квазиколичественную экстракцию в органической фазе, что позволяет применять схемы восстановительной реэкстракции плутония, при которых оксим гексаналя может использоваться в очень малых количествах для стабилизации органической фазы, при этом водная фаза может быть стабилизирована гидрофильным оксимом, таким как ацеталдоксим,
- для этих обоих альдоксимов: возможность их применения на этапе разделения урана и плутония.
1.2. Противоазотистое действие
Способность оксима пентаналя и оксима гексаналя разлагать азотистую кислоту (HNO2) была исследована в двух сериях опытов, а именно:
- первая серия, предназначенная для определения кинетики разложения азотистой кислоты оксимом пентаналя и, в целях сравнения, для определения кинетики разложения азотистой кислоты оксимом бутаналя в водных фазах, содержащих 0,1 моль/л азотной кислоты,
- вторая серия опытов, предназначенная для определения кинетики разложения азотистой кислоты оксимом пентаналя и оксимом гексаналя и, для сравнения, для определения кинетики разложения азотистой кислоты оксимом бутаналя в органических фазах, содержащих 30% (в объёмном отношении) TBP в н-додекане.
В первой серии опытов показатели начальной концентрации азотистой кислоты и оксима пентаналя или оксима бутаналя в азотных водных фазах составляли соответственно 0,005 моль/л и 0,025 моль/л фазы. Изменение по времени концентрации азотистой кислоты в водных фазах прослеживалось посредством спектрофотометрии (непрерывное измерение пика при λ = 370 нм, соответствующего HNO2).
Во второй серии опытов первую группу органических фаз, которые были предварительно уравновешены азотной кислотой 1М, сначала приводили в контакт (объем к объему) с водной фазой, содержащей 1 моль/л азотной кислоты и 0,002 моль/л азотистой кислоты, в течение 10 минут при комнатной температуре (20-25°С) при перемешивании, а затем эту группу фаз отделяли от указанной водной фазы центрифугированием. Азотистая кислота квазиколичественно экстрагировалась в органических фазах.
Затем вторую группу органических фаз, предварительно уравновешенных азотной кислотой 1М и в которые были добавлены оксим пенталя, оксим гексаналя или оксим бутаналя при концентрации 0,15 моль/л органической фазы, приводили в контакт (объем к объему) с водной фазой, содержащей 1 моль/л азотной кислоты, в течение 10 минут при комнатной температуре (20-25°С) при перемешивании, и затем эту группу фаз отделяли от указанной водной фазы центрифугированием. Оксимы распределялись между органическими фазами и водной фазой.
После этого быстро смешивали 1 мл органических фаз, взятых от первой группы (содержавшей, следовательно, азотистую кислоту), и 8 мл органических фаз, взятых от второй группы. Изменение концентрации азотистой кислоты в этих смесях отслеживали спектрофотометрией (λ = 370 нм). Результаты этих опытов приведены на фиг. 3 и 4 в виде кривых процентного содержания остаточной азотистой кислоты в зависимости от времени (в секундах на фиг. 3 и в минутах на фиг. 4).
На фиг. 3, которая относится к первой серии опытов, кривая А соответствует результатам, полученным для оксима пентаналя, в то время как кривая В соответствует результатам, полученным для оксима бутаналя. Также на этой фигуре показана кинетика разложения азотистой кислоты ацеталдоксимом (кривая С), при этом данная кинетика была определена путем моделирования на основе экспериментально измеренной константы скорости.
На фиг. 4, относящейся ко второй серии опытов, кривая А соответствует результатам, полученным для оксима пентаналя; кривая В соответствует результатам, полученным для оксима гексаналя, а кривая С соответствует результатам, полученным для оксима бутаналя.
Из этих фигур следует, что:
- в водной однофазной системе оксим пенталя, хотя он и содержит больше атомов углерода, чем оксим бутаналя и ацеталдоксим, обладает противоазотистым действием, эквивалентным действию оксима бутаналя и ацеталдоксима (фиг. 3), в то время как
- в органической однофазной системе, в которой органическая фаза, содержащая оксим пентаналя, оксим гексаналя и оксим бутаналя предварительно приведена в контакт с водной фазой (что привело к разделению этих оксимов между органической и водной фазами, из-за чего произошло уменьшение их концентрации в органической фазе), было отмечено, что при одной и той же концентрации оксима, первоначально введённого в органическую фазу, разложение азотистой кислоты в органической фазе резко ускорялось в присутствии оксима пентаналя или оксима гексаналя по сравнению со случаем, когда присутствовал оксим бутаналя (фиг. 4).
Пример 2. Стабилизация актинидов посредством оксима пентаналя и оксима гексаналя
Способность оксима пентаналя и оксима гексаналя стабилизировать актиниды в водной или органической фазе была оценена в ходе двух серий опытов, а именно:
- первая серия, предназначенная для определения кинетики окисления урана (IV) в присутствии оксима пентаналя, оксима гексаналя и, для сравнения, оксима бутаналя, а также в отсутствие какого-либо оксима в органических фазах, содержащих 30% (в объёмном отношении) TBP в н-додекане после приведения в контакт этих органических фаз с водными фазами, содержащими 1,8 моль/л азотной кислоты и последующего разделения этих фаз,
- вторая серия опытов, предназначенная для определения кинетики окисления урана (IV) в присутствии оксима пентаналя и, для сравнения, оксима бутаналя, ацеталдоксима и гидразина в водных фазах, содержащих 1,3 моль/л азотной кислоты.
При первой серии опытов каждую органическую фазу, предварительно уравновешенную азотной кислотой 1,8М и в которую при необходимости вводили оксим в концентрации 0,1 моль/л, приводили в контакт с азотной водной фазой, содержащей 6 г/л урана (IV) при объёмном отношении О/А = 2 в течение 10 минут при комнатной температуре (20-25°С) и при перемешивании. Затем контактирующие органические и водные фазы разделяли между собой центрифугированием и отслеживали изменение концентрации урана (IV) в органических фазах посредством спектрофотометрии (λ = 653 нм) при временных интервалах в течение 200 часов.
При второй серии опытов начальные концентрации урана (IV) и агента противоазотистого действия (оксима или гидразина) в азотных водных фазах составили 66 г/л и 0,2 моль/л соответственно. Изменение концентрации урана (IV) по времени в водных фазах отслеживали посредством спектрофотометрии (λ = 653 нм) при временных интервалах в течение 300 дней.
Результаты этих опытов приведены на фиг. 5 и 6 в виде кривых, выражающих остаточное процентное содержание урана (IV) в зависимости от времени (в часах на фиг. 5 и в сутках на фиг. 6).
На фиг. 5, относящейся к первой серии опытов, кривая А соответствует результатам, полученным для оксима пентаналя; кривая В соответствует результатам, полученным для оксима гексаналя; кривая С соответствует результатам, полученным для оксима бутаналя, а кривая D соответствует результатам, полученным в отсутствие оксима.
На фиг. 6, относящейся ко второй серии опытов, кривая А соответствует результатам, полученным для оксима пентаналя; кривая В соответствует результатам, полученным для оксима бутаналя; кривая С соответствует результатам, полученным для ацеталдоксима, а кривая D соответствует результатам, полученным для гидразина.
Как показано на фиг. 5, уран (IV) имеет превосходную стабильность в органической фазе в течение по меньшей мере 15 часов в присутствии оксима, в то время как его полное окисление происходит менее, чем за 8 часов в отсутствие какого-либо оксима. Кроме того, способность оксима пентаналя и оксима гексаналя стабилизировать уран (IV) в органической фазе превосходит такую способность оксима бутаналя, поскольку в присутствии оксима пентаналя и оксима гексаналя за 100 часов окисляется менее 10% урана (IV), чего не удается достичь в присутствии оксима бутаналя.
В водной фазе способность оксима пентаналя стабилизировать уран (IV) превышает такую способность оксима бутаналя. Однако эта способность выражена слабее, чем у ацеталдоксима и гидразина, которые сопоставимы между собой (фиг. 6).
Все эти периоды, выраженные в сутках, тем не менее значительно превосходят периоды присутствия органических и водных фаз во время промышленных операций по реэкстракции плутония.
Данные результаты свидетельствуют о возможности стабилизировать азотные водные фазы с высокой концентрацией урана (IV) либо посредством оксима пентаналя в случае применения схемы с одним оксимом, либо посредством ацеталдоксима в случае применения схемы с двумя оксимами, например с применением оксима гексаналя в органической фазе, и таким образом позволят избавиться от использования гидразина.
Пример 3. Противоазотистая способность оксима пентаналя и оксима гексаналя в химических условиях, характерных для операции реэкстракции плутония
Противоазотистые свойства оксима пентаналя и оксима гексаналя оценивались в ходе серии опытов, обозначенных ниже как ВХ1-ВХ10, представляющих собой химические условия, в которых осуществляется операция восстановительной реэкстракции плутония в способе PUREX, при этом применялось:
- восстановление ураном (IV) плутония (IV) в плутоний (III) и повторное окисление азотистой кислотой плутония (III) с получением плутония (IV);
- разложение азотистой кислоты с помощью одного из приведённых выше оксимов;
- распределение интересующих веществ между водной и органической фазами.
С этой целью были использованы:
- в качестве водных фаз: растворы 1 моль/л или 2 моль/л азотной кислоты, содержавшие уран (VI), уран (IV) (в качестве восстановителя плутония (IV)), и, при необходимости, гидразин и технеций в концентрациях согласно таблицам 3 и 4 ниже;
- в качестве органических фаз: 30% раствор TBP (в объёмном отношении) в ТРН, содержащий оксим, уран (VI) и плутоний (IV) в концентрациях согласно таблицам 3 и 4 ниже.
Оксимы вводили в органические фазы в твёрдом виде (количество введённого оксима контролировалось взвешиванием).
Органические фазы приводили в контакт с водными фазами в течение 15 минут (за исключением испытания ВХ3, для которого длительность контакта составила лишь 5 минут) при комнатной температуре (20-25°С) при перемешивании, при объёмном отношении О/А, равном 2, затем эти фазы отделяли друг от друга.
После такого разделения концентрацию урана (VI), урана (IV) и плутония (III) измеряли в каждой фазе посредством ультрафиолетовой спектрофотометрии, а совокупное количество плутония - посредством альфа-спектрометрии. Концентрацию урана (VI) и урана (IV) в органических фазах измеряли ультрафиолетовой спектрофотометрией, а концентрацию всего плутония - альфа-спектрометрией.
На основе этих результатов измерений для каждого опыта определяли отношение между количествами израсходованного урана (IV) и реэкстрагированного плутония, обозначенное как U(IV)изр./Puреэкс., а также коэффициент отделения плутония, обозначенный как FDPu.
Результаты этих опытов приведены в таблицах 3 и 4 ниже. В таблице 3 - результаты, полученные для опытов, проводившихся с использованием оксима гексаналя (ВХ1-ВХ5, ВХ8, ВХ10), в таблице 4 - результаты, полученные для опытов, проводившихся с использованием оксима пентаналя (ВХ6, ВХ7).
Таблица 3
моль/л
моль/л
моль/л
моль/л
моль/л
моль/л
моль/л
моль/л
моль/л
Таблица 4
Как показано в таблицах:
- для обеспечения концентрации оксима гексаналя 0,1 моль/л в органической фазе и для получения начального отношения по массе (U(IV)/Pu) от 0,8 до 1,5 количество израсходованного урана (IV), отнесенное к количеству реэкстрагированного плутония (отношение U(IV)изр./Puреэкс.), cоставляет от 0,5 до 0,6; следовательно посторонние явления повторного окисления плутония очень слабо выражены или даже отсутствуют; эти результаты наблюдались для водных фаз, содержавших азотную кислоту при концентрации 1 моль/л или 2 моль/л (опыты ВХ1-ВХ5);
- снижение концентрации оксима гексаналя в органической фазе наполовину (0,05 моль/л по сравнению с 0,1 моль/л) и присутствие технеция в водной фазе приводит к более значительному расходу урана (IV) (отношение U(IV)изр./Puреэкс.=1), который однако остается умеренным (опыты ВХ8, ВХ10);
- оксим пенталя позволяет также ограничить окислительно-восстановительные явления, приводящие к дополнительному расходу урана (IV), однако с незначительным снижением эффективности по сравнению со значениями, достигаемыми с оксимом гексаналя, так как отношение U(IV)изр. /Puреэкс., достигаемое при использовании оксима пентаналя, составляет от 0,6 до 0,8 (опыты ВХ8, ВХ10).
Вместе с тем, изменение концентрации урана (IV) в органических фазах, таких как полученные в опытах ВХ5, ВХ10 и ВХ6, отслеживалось методом спектрофотометрии (λ = 653 нм) при временных интервалах в течение нескольких часов.
Результаты такого отслеживания приведены на фиг. 7, 8 и 9, которые соответствуют органическим фазам ВХ5, ВХ10, ВХ6.
Эти фигуры подтверждают способность оксима пентаналя и оксима гексаналя к стабилизации урана (IV) в органической фазе. Такая стабилизация снижается в присутствии технеция, однако кинетика окисления урана (IV) остаётся относительно слабой, так как за 50 минут наблюдалось уменьшение концентрации урана (IV) наполовину.
Пример 4. Разработка схемы переработки раствора из отработанного ядерного топлива, включающей этап разделения урана и плутония без использования гидразина
Была разработана схема переработки раствора из отработанного ядерного топлива, включающая этап разделения урана и плутония без использования гидразина, но с использованием комбинации из оксима гексаналя и ацеталдоксима в качестве системы противоазотистого действия, при этом оксим гексаналя использовался в органической фазе, а ацеталдоксим - в водной фазе.
Предварительно при разработке этой схемы авторы убедились:
- с одной стороны, что ацеталдоксим действительно способен заменить гидразин в качестве водного агента противоазотистого действия в водной фазе в присутствии технеция и,
- с другой стороны, что оксим гексаналя способен также стабилизировать уран (IV) в органической фазе, служащей для проведения операции “промывка Np”, которая в процессах PUREX и COEX служит для удаления из водной фазы, образуемой при операции восстановительной реэкстракции плутония, нептуния, который был реэкстрагирован при этой операции.
4.1. Противоазотистая активность ацеталдоксима в водной фазе в присутствии технеция
Были проведены опыты для сравнения противоазотистой активности ацеталдоксима в водной фазе и аналогичной активности гидразина в присутствии технеция.
Для этого использовали следующий методический протокол:
- готовили водные растворы с содержанием 9 г/л урана (IV) и 2 моль/г азотной кислоты, а также 2 моль/г ацеталдоксима или гидразина, эти растворы термостатировали при 35°С;
- в эти растворы добавляли водный раствор с содержанием 8,88 г/л технеция (VII) (т.е. 0,09 моль/л) для получения конечной концентрации технеция 100 мг/л или 200 мг/л; после встряхивания:
- контролировали кинетику окисления урана (IV) в этих водных растворах путём спектрофотометрических замеров (λ = 653 нм) в течение 100 минут.
Результаты этих опытов приведены на фиг. 10, на которой полученные результаты по ацеталдоксиму в присутствии 100 мг/л и 200 мг/л технеция обозначены символами ■ и х, в то время как результаты, полученные для гидразина в присутствии 100 мг/л и 200 мг/л, обозначены символами ▲ и ●, соответственно. Как можно видеть на этой фигуре, противоазотистая активность оксима ацеталдегида в водной фазе в присутствии 100 мг или 200 мг технеция сопоставима с аналогичной активностью гидразина.
Следовательно, можно заменить гидразин, являющийся агентом противоазотистого действия в водной фазе, ацеталдоксимом.
4.2. Стабилизация урана (IV) при операции «промывка нептуния»
Было проведено два опыта, обозначенных ниже как BS16 и ВS17, при этом использовали:
- в качестве органических фаз: 30% растворы ТВР (в объёмном отношении) в ТРН, содержащие 0,1 моль/л оксима гексаналя или без него,
- в качестве водных фаз: водные растворы с 1,3 моль/л азотной кислоты с содержанием урана (IV), ацеталдоксима, плутония (III) и технеция согласно таблице 5; технеций добавляли в водные фазы как раз перед их контактом с органическими фазами в виде концентрированного раствора технеция (VII) при 8,88 г/л.
Органические и водные фазы приводили в контакт (объем к объему)в течение 15 минут при комнатной температуре (20-25°С) при перемешивании, затем эти фазы отделяли друг от друга.
Измеряли концентрацию урана (IV) в водных и органических растворах и определяли процентное количество урана (IV), израсходованного при каждом из этих опытов, обозначенное как U(IV)изр..
Результаты представлены в таблице 5 ниже.
Из этой таблицы следует, что присутствие оксима гексаналя в органической фазе (опыт BS16) позволяет снизить расход урана (IV) на 50% по сравнению с расходом в отсутствие этого оксима (опыт BS17).
Таблица 5
%
4.3 Схема переработки
Разработанная схема переработки раствора отработанного ядерного топлива показана на фиг. 11.
В этой схеме присутствуют два значимых этапа первого цикла очистки способа COEX, а именно:
(1) этап очистки урана и плутония от актинидов (III) (америция и кюрия) и некоторого количества продуктов деления, включающий:
* операцию, именуемую «соэкстракцией урана/плутония» на фиг. 11, предназначенную для совместной экстракции урана, плутония и нептуния, причём первый из них - в степени окисления VI, второй - в степени окисления IV и третий - в степени окисления VI, из растворённого топлива посредством органической фазы, содержащей 30% TBP ( в объёмном отношении) в ТРН;
* операцию, именуемую «промывка продуктов деления» на фиг. 11, предназначенную для извлечения продуктов деления из органической фазы, образовавшейся при операции «соэкстракция урана и плутония», в частности во время «соэкстракции урана и плутония» экстрагируются рутений и цирконий;
* операцию, именуемую «промывка технеция» на фиг. 11, предназначенную для извлечения из органической фазы, образовавшейся при «промывке продуктов деления», технеция, экстрагированного во время «соэкстракции урана и плутония», посредством водной фазы, и
* операцию, именуемую «дополнительной соэкстракцией урана и плутония» на фиг. 11, предназначенную для возврата в органическую фазу фракций урана (VI), плутония (IV) и нептуния, последовавших за технецием в водную фазу во время «промывки технеция», и
(2) этап разделения урана и плутония на два водных потока, из которых один поток содержит уран, второй поток - плутоний и уран (при массовом отношении U/Pu порядка от 20/80 до 30/70), который включает:
* операцию, именуемую «реэкстракция плутония и урана» на фиг. 11, предназначенную для реэкстракции плутония из органической фазы, образовавшейся при «промывке технеция», и части урана, присутствующего в этой органической фазе, при этом операция проводилась с использованием водной фазы, содержащей уран (IV) в качестве восстановителя, способного перевести плутоний в состояние окисления III;
* операцию, именуемую «промывкой нептуния» на фиг. 11, предназначенную для извлечения из водной фазы, образовавшейся при «реэкстракции плутония и урана», избыточного урана по сравнению с массовым отношением U/Pu от 20/80 до 30/70 и фракции нептуния, последовавшего за плутонием в водную фазу во время «реэкстракции урана и плутония», и
* операцию, именуемую «реэкстракцией урана», предназначенную для реэкстракции из органической фазы, образовавшейся при «реэкстракции урана и плутония», урана и нептуния с использованием водной фазы.
Однако в схеме на фиг. 11 гидразин, являющийся агентом противоазотистого действия в способе COEX, заменён комбинацией из оксима гексаналя и ацеталдоксима.
Как показано на фиг. 11, оксим гексаналя (обозначенный на фиг. 11 как HexOx) вводится, с учётом его сильно выраженного липофильного характера, в органическую фазу, поступающую в экстрактор 5, в котором происходит «промывка нептуния», а также в органическую фазу, образовавшуюся при «промывке технеция», как раз перед тем, как эта фаза поступает в экстрактор 6.
Ацеталдоксим (обозначенный как АсОх на фиг. 11) вводится, с учётом его гидрофильного свойства, в водную фазу, циркулирующую в экстракторе 6, это введение происходит на трёх разных ярусах данного экстрактора: на ярусе 8, на уровне которого он впрыскивается в водную фазу, предназначенную для реэкстракции, и на ярусах 1 и 4, на уровне которых ацеталдоксим впрыскивается в водные потоки, питающие водную фазу с ураном (IV).
Элементарные закупки оксимов для обеих фаз, водной и органической, были использованы для создания первых моделей для моделирования их распределения между используемыми в способе водной и органической фазами и определения их кинетики реакции с азотистой кислотой. Эти модели были использованы в программном коде PAREX, который является программным обеспечением для моделирования распределения интересующих веществ в операциях, таких как разделение урана и плутония на два водных потока. Именно посредством такого моделирования определяли операционные параметры, с помощью которых экспериментально тестировали схему на фиг. 11.
На фиг. 12 сравниваются профили концентрации урана (IV) в водных фазах, циркулирующих в экстракторах 5 и 6, рассчитанные, с одной стороны, для схемы на фиг. 11 (кривая А) и, с другой стороны, для равнозначной схемы с использованием гидразина (кривая В). Там же показан и идеальный профиль (кривая С), полученный в результате нейтрализации (согласно коду PAREX) реакций повторного окисления плутония (III).
Как следует из этой фигуры, использование комбинации из оксима гексаналя и ацеталдоксима позволяет получить профиль более высокой концентрации урана (IV), в случае использования гидразина, что подтверждает снижение расхода урана (IV) в присутствии этих оксимов.
Схема на фиг. 11 была успешно применена в экранированной ячейке способа ATALANTE на реальном растворе из отработанного ядерного топлива. Эта схема позволила получить поток плутония с концентрацией 10 г/л при соответствующей концентрации урана (IV) (16 г/л), при этом уран (IV) не вводился на операции «промывка нептуния», в то время как такая добавка необходима в аналогичной схеме, использующей гидразин. Расход урана (IV) также был менее значительным, чем в схеме с применением гидразина.
На фиг. 13 показаны профили концентрации плутония в водных фазах, циркулирующих в экстракторах 5 и 6, полученные экспериментально (символ х) и рассчитанные с применением кода PAREX (кривая ―), в то время как на фиг. 14 приведены профили концентрации урана (IV), урана (VI) и всего урана в водных фазах, циркулирующих в тех же экстракторах, полученные экспериментально и путём расчётов; на этой фигуре символами х, ♦ и ■ обозначены профили концентрации урана (IV), урана (VI) и всего урана, соответственно, полученные экспериментально, в то время как кривые А, В и С соответствуют профилям концентрации урана (IV), урана (VI) и всего урана, полученным расчётным способом.
Вместе с тем, в приводимой ниже таблице 6 представлены концентрация урана в водной фазе, полученной из экстрактора 5 (обозначенная как [U(IV)]flux de production Pu), концентрация плутония в водной фазе, полученной из экстрактора 5 (обозначенная как [Pu]flux de production Pu), отношение между потоком урана (IV), введённым в экстрактор 6, и потоком плутония, введённым в тот же экстрактор (обозначенное как U(IV)/Puввед.) , процентное содержание израсходованного урана (IV) (обозначенное как U(IV)изр.), а также отношение между потоком израсходованного урана (IV) и потоком введённого плутония (обозначенное как U(IV)изб./Pu), которые были получены экспериментально для схемы на фиг. 11.
Для сравнения в этой таблице также приведены те же концентрации, отношения и процентное содержание, но только полученные экспериментально в равнозначной схеме, использующей гидразин.
Таблица 6
Использованные отсылки
[1] WO-A-2006/072729
[2] WO-A-2011/000844
[3] WO-A-2008/148863
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ ГИДРОКСИИМИНОАЛКАНОВЫХ КИСЛОТ В КАЧЕСТВЕ АГЕНТОВ ПРОТИВОАЗОТИСТОГО ДЕЙСТВИЯ ПРИ ОПЕРАЦИЯХ ВОССТАНОВИТЕЛЬНОЙ РЕЭКСТРАКЦИИ ПЛУТОНИЯ | 2016 |
|
RU2713495C2 |
| СПОСОБ ОБРАБОТКИ ВОДНОГО АЗОТНОКИСЛОГО РАСТВОРА, ПОЛУЧЕННОГО ПРИ РАСТВОРЕНИИ ОТРАБОТАВШЕГО ЯДЕРНОГО ТОПЛИВА, ВЫПОЛНЯЕМЫЙ В ОДНОМ ЦИКЛЕ И НЕ ТРЕБУЮЩИЙ КАКОЙ-ЛИБО ОПЕРАЦИИ, ВКЛЮЧАЮЩЕЙ ВОССТАНОВИТЕЛЬНУЮ РЕЭКСТРАКЦИЮ ПЛУТОНИЯ | 2016 |
|
RU2706954C2 |
| НОВЫЕ АСИММЕТРИЧНЫЕ N,N-ДИАЛКИЛАМИДЫ, ИХ СИНТЕЗ И ПРИМЕНЕНИЕ | 2016 |
|
RU2702739C2 |
| СПОСОБ ПЕРЕРАБОТКИ ОТРАБОТАННОГО ЯДЕРНОГО ТОПЛИВА, НЕ ТРЕБУЮЩИЙ ВОССТАНОВИТЕЛЬНОЙ РЕЭКСТРАКЦИИ ПЛУТОНИЯ | 2011 |
|
RU2558332C9 |
| СПОСОБ ПЕРЕРАБОТКИ ОТРАБОТАННОГО ЯДЕРНОГО ТОПЛИВА, ВКЛЮЧАЮЩИЙ СТАДИЮ ОЧИСТКИ УРАНА (VI) ОТ ПО МЕНЬШЕЙ МЕРЕ ОДНОГО АКТИНИДА (IV) ПУТЕМ ПОЛУЧЕНИЯ КОМПЛЕКСА ДАННОГО АКТИНИДА (IV) | 2014 |
|
RU2663882C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ОТРАБОТАННОГО ЯДЕРНОГО ТОПЛИВА И ПОЛУЧЕНИЯ СМЕШАННОГО УРАН-ПЛУТОНИЕВОГО ОКСИДА | 2007 |
|
RU2431896C2 |
| СПОСОБ ПЕРЕРАБОТКИ ОБЛУЧЕННОГО ЯДЕРНОГО ТОПЛИВА (ОЯТ) АЭС | 1997 |
|
RU2132578C1 |
| СПОСОБ ПЕРЕРАБОТКИ ОТРАБОТАННОГО ЯДЕРНОГО ТОПЛИВА (ВАРИАНТЫ), ВОССТАНОВИТЕЛЬ NP(VI) | 1998 |
|
RU2229178C2 |
| СПОСОБ ПЕРЕРАБОТКИ ОБЛУЧЕННОГО ТОПЛИВА АЭС | 2013 |
|
RU2535332C2 |
| НЕСИММЕТРИЧНЫЕ N,N-ДИАЛКИЛАМИДЫ, В ЧАСТНОСТИ ИСПОЛЬЗУЕМЫЕ ДЛЯ ОТДЕЛЕНИЯ УРАНА(VI) ОТ ПЛУТОНИЯ(IV), ИХ СИНТЕЗ И ПРИМЕНЕНИЕ | 2018 |
|
RU2762634C2 |

Изобретение относится к применению альдоксимов в качестве агентов противоазотистого действия при операциях восстановительной реэкстракции плутония. Изобретение может найти применение в любых способах переработки отработанного ядерного топлива. В качестве агента противоазотистого действия в операции восстановительной реэкстракции плутония применяют по меньшей мере один альдоксим формулы R-CH=N-OH, где R означает линейную или разветвлённую углеводородную цепь с по меньшей мере 4 атомами углерода. Изобретение позволяет получить водную фазу с большей концентрацией плутония, а также уменьшить размеры применяемых аппаратов для осуществления восстановительной реэкстракции плутония. 13 з.п. ф-лы, 14 ил., 6 табл., 4 пр.
1. Применение альдоксима формулы R-CH=N-OH, где R означает линейную или разветвлённую углеводородную цепь с по меньшей мере 4 атомами углерода, в качестве агента противоазотистого действия в операции восстановительной реэкстракции плутония.
2. Применение по п. 1, в котором R означает линейную или разветвлённую углеводородную цепь с 4-12 атомами углерода.
3. Применение по п. 2, в котором R означает линейную или разветвлённую углеводородную цепь с 4-8 атомами углерода.
4. Применение по п. 3, в котором R означает линейную алкильную цепь с 4-8 атомами углерода.
5. Применение по п. 4, в котором альдоксимом является оксим пенталя или оксим гексаналя.
6. Применение по любому из пп. 1-5, в котором операция восстановительной реэкстракции плутония включает:
- приведение в контакт органической не смешивающейся с водой фазы, содержащей экстрагент и плутоний в степени окисления IV в органическом растворителе, с водной фазой, содержащей восстановитель для восстановления плутония (IV) в плутоний (III) и азотную кислоту, при этом одна из органической и водной фаз дополнительно содержит альдоксим, и
- разделение контактирующих таким образом органической и водной фаз.
7. Применение по п. 6, в котором восстановитель выбран из урана (IV), нитрата гидроксиламмония, алкильных производных гидроксиламина, сульфамата двухвалентного железа и сульфаминовой кислоты.
8. Применение по п. 7, в котором восстановителем является уран (IV) или нитрат гидроксиламмония.
9. Применение по п. 6, в котором экстрагентом является фосфат три-н-алкила.
10. Применение по п. 9, в котором экстрагентом является фосфат три-н-бутила.
11. Применение по п. 6, в котором альдоксим используется при концентрации от 0,01 до 3 моль/л органической или водной фазы.
12. Применение по п. 6, в котором водная фаза дополнительно содержит оксим, не экстрагируемый органической фазой.
13. Применение по п. 12, в котором не экстрагируемым органической фазой оксимом является ацеталдоксим.
14. Применение по п. 6, в котором операцией восстановительной реэкстракции плутония является одна из операций по реэкстракции плутония в способе PUREX или способе COЕX.
| WO 2008148863 A1, 11.12.2008 | |||
| WO 2007118904 A1, 25.04.2008 | |||
| СПОСОБ ОТДЕЛЕНИЯ УРАНА ( VI ) ОТ АКТИНОИДОВ ( IV ) И/ИЛИ ( VI ) И ЕГО ИСПОЛЬЗОВАНИЕ | 2004 |
|
RU2352006C2 |
| Центробежный водоподъемный аппарат | 1927 |
|
SU13187A1 |
Авторы
Даты
2020-04-06—Публикация
2016-10-18—Подача