ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет на основании предварительной заявки США № 62/050116, поданной 13 сентября 2014, предварительной заявки США № 62/059788, поданной 3 октября 2014, предварительной заявки США № 62/119060, поданной 20 февраля 2015, и предварительной заявки США № 62/199030, поданной 30 июля 2015 г, причем содержание упомянутых выше заявок включено в данное описание посредством ссылки во всей полноте.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, представленный в электронном виде в формате ASCII, и включенный сюда в качестве ссылки во всей своей полноте. Указанная копия ASCII, созданная 11 сентября 2015 года, называется C2160-7013WO_SL.txt и имеет размер 14750 байт.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Способность Т-клеток опосредовать иммунный ответ против антигена обуславливается двумя разными сигнальными взаимодействиями (Viglietta, V. et al. (2007) Neurotherapeutics 4: 666-675; Korman, A. J. et al. (2007) Adv. Immunol. 90: 297-339). Вначале антиген, расположенный на поверхности антиген-презентирующих клеток (АРС), представляется антиген-специфичным наивным Т-клеткам CD4+. Такое представление генерирует сигнал через Т-клеточный рецептор (TCR), который направляет Т-клетки к инициации иммунного ответа, специфического для презентированного антигена. Затем разные костимуляторные и ингибиторные сигналы, опосредованные взаимодействием APC и разных поверхностных молекул Т-клеток, вызывают активацию и пролиферацию Т-клеток и, в конечном счете, их ингибирование.
Иммунная система жестко регулируется сетью костимуляторных и коингибиторных лигандов и рецепторов. Эти молекулы обеспечивают генерирование второго сигнала для активации Т-клеток и представляют собой сбалансированную сеть положительных и отрицательных сигналов, которая обуславливает максимальное усиление иммунного ответа против инфекции, ограничивая при этом иммунитет к собственному организму (Wang, L. et al. (Epub Mar. 7, 2011) J. Exp. Med. 208(3):577-92; Lepenies, B. et al. (2008) Endocrine, Metabolic & Immune Disorders-Drug Targets 8:279-288). Примеры костимуляторных сигналов включают в себя связывание лигандов B7.1 (CD80) и В7.2 (CD86) APC с рецепторами CD28 и CTLA-4 Т-лимфоцитов CD4+ (Sharpe, A. H. et al. (2002) Nature Rev. Immunol. 2:116-126; Lindley, P. S. et al. (2009) Immunol. Rev. 229:307-321). Связывание B7.1 или B7.2 с CD28 стимулирует активацию Т-клеток, тогда как связывание B7.1 или B7.2 с CTLA-4 ингибирует такую активацию (Dong, C. et al. (2003) Immunolog. Res. 28(1):39-48; Greenwald, R. J. et al. (2005) Ann. Rev. Immunol. 23:515-548). CD28 конститутивно экспрессируется на поверхности Т-клеток (Gross, J., et al. (1992) J. Immunol. 149:380-388), тогда как экспрессия CTLA4 быстро повышается после активации Т-клеток (Linsley, P. et al. (1996) Immunity 4:535-543).
Другие лиганды рецептора CD28 включают в себя группу молекул, родственных В7, также известную как "суперсемейство B7" (Coyle, A. J. et al. (2001) Nature Immunol. 2(3):203-209; Sharpe, A. H. et al. (2002) Nature Rev. Immunol. 2:116-126; Collins, M. et al. (2005) Genome Biol. 6:223.1-223.7; Korman, A. J. et al. (2007) Adv. Immunol. 90:297-339). Известно несколько членов суперсемейства B7, в том числе B7.1 (CD80), В7.2 (CD86), индуцируемый костимуляторный лиганд (ICOS-L), лиганд программируемой гибели 1 (PD-L1; B7-H1), лиганд программируемой гибели 2 (PD-L2;. В7-DC), В7-Н3, В7-Н4 и В7-Н6 (Collins, M. et al. (2005) Genome Biol. 6:223.1-223.7).
Белок программируемой гибели 1 (PD-1) является ингибиторным членом расширенного семейства Т-клеточных регуляторов CD28/CTLA4 (Okazaki et al. (2002) Curr Opin Immunol 14: 391779-82; Bennett et al. (2003) J. Immunol. 170:711-8). Другие члены семейства CD28 включают в себя CD28, CTLA-4, ICOS и BTLA. Полагают, что PD-1 существует в виде мономера, утратившего непарный остаток цистеина, характерный для других членов семейства CD28. PD-1 экспрессируется на активированных В-клетепх, Т-клетках и моноцитах.
Ген PD-1 кодирует трансмембранный белок типа I размером 55 кДа (Agata et al. (1996) Int Immunol. 8:765-72). Несмотря на структурное подобие CTLA-4, PD-1 не содержит мотив MYPPY (SEQ ID NO: 1), имеющий важное значение для связывания В7-1 и В7-2. Идентифицированы два лиганда PD-1, PD-L1 (B7-H1) и PD-L2 (B7-DC), которые, как показано, подавляют активацию Т-клеток после связывания с PD-1 (Freeman et al. (2000) J. Exp. Med. 192:1027-34; Carter et al. (2002) Eur. J. Immunol. 32:634-43). Как PD-L1, так и PD-L2, являются гомологами B7, которые связываются с PD-1, но не связываются с другими членами семейства CD28. PD-L1 в большом количестве присутствует в разных раковых опухолях человека (Dong et al. (2002) Nat. Med. 8:787-9).
PD-1 известен как иммуноингибиторный белок, который подавляет сигналы TCR (Ishida, Y. et al. (1992) EMBO J. 11:3887-3895; Blank, C. et al. (Epub 2006 Dec. 29) Immunol. Immunother. 56(5):739-745). Взаимодействие между PD-1 и PD-L1 может действовать как контрольная точка иммунного ответа, которая может приводить, например, к уменьшению лимфоцитов, инфильтрующих опухоль, уменьшению пролиферации, опосредованной Т-клеточным рецептором, и/или уклонения раковых клеток от иммунного надзора (Dong et al. (2003) J. Mol. Med. 81:281-7; Blank et al. (2005) Cancer Immunol. Immunother. 54:307-314; Konishi et al. (2004) Clin. Cancer Res. 10:5094-100). Подавление иммунитета можно отменить путем ингибирования локального взаимодействия PD-1 с PD-L1 или PD-L2; эффект является аддитивным, есл при этом также блокируется взаимодействие PD-1 с PD-L2 (Iwai et al. (2002) Proc. Nat'l. Acad. Sci. USA 99:12293-7; Brown et al. (2003) J. Immunol. 170:1257-66).
Поскольку пути контрольных точек иммунного ответа играют важную роль в регуляции иммунного ответа, существует необходимость в разработке новых сочетанных способов лечения, активирующих иммунную систему.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает, по меньшей мере, в числе прочего, способы и композиции, содержащие иммуномодулятор (например, один или несколько, выбранных из активатора костимуляторной молекулы или ингибитора молекулы иммунной контрольной точки) в сочетании со вторым терапевтическим средством LDK378. В одном варианте осуществления ингибитор молекулы иммунной контрольной точки (например, один или несколько ингибиторов PD-1, PD-L1, LAG-3, TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5) или CTLA4) можно использовать в сочетании с LDK378. Описанные здесь сочетания могут оказывать благоприятное действие, например, при лечении рака, такое как усиление противоракового эффекта, снижение токсичности и/или уменьшение побочных эффектов. Например, иммуномодуляторное средство, второе терапевтическое средство, или и то, и другое, можно вводить в более низких дозах, чем дозы, требующиеся для достижения такого же терапевтического эффекта при монотерапии. Таким образом, в данном документе раскрываются композиции и способы, которые можно использовать для лечения гиперпролиферативных расстройств, таких как рак, включающие в себя применение вышеуказанной сочетанной терапии.
Соответственно, в одном аспекте изобретение предлагает способ лечения (например, ингибирования, уменьшения, ослабления или предотвращения) у индивидуума гиперпролиферативных состояний или расстройств (таких как рак). Способ включает введение индивидууму иммуномодулятора (например, одного или нескольких, выбранных из: активатора костимуляторной молекулы или ингибитора молекулы иммунной контрольной точки) и второго терапевтического средства LDK378 с целью лечения гиперпролиферативного состояния или расстройства (такого как рак). В некоторых вариантах осуществления иммуномодулятор представляет собой ингибитор молекулы иммунной контрольной точки (например, ингибитор PD-1, PD-L1, LAG-3, TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5) или CTLA4, или любое их сочетание). Сочетание иммуномодулятора и второго средства можно вводить вместе в составе одной композиции, или по отдельности в составе двух или более разных композиций, например, композиций или лекарственных форм, как описано в данном документе. Введение иммуномодулятора и второго средства можно осуществлять в любом порядке. Например, иммуномодулятор можно вводить одновременно со вторым средством, до него, или после.
В другом аспекте изобретение относится к способу снижения активности (например, роста, выживаемости или жизнеспособности, или всех типов активности), гиперпролиферативной (например, раковой) клетки. Способ включает приведение клетки в контакт с иммуномодулятором (например, с одним или несколькими, выбранными из: активатора костимуляторной молекулы или ингибитора молекулы иммунной контрольной точки) и LDK378, обуславливающее уменьшение активности в клетке. В некоторых вариантах осуществления иммуномодулятор представляет собой ингибитор молекулы иммунной контрольной точки (например, ингибитор PD-1, PD-L1, LAG-3, TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5) или CTLA4, или любое их сочетание). Описанные здесь способы можно использовать in vitro или in vivo, например, для лечения животного, или как часть терапевтической схемы лечения. Приведение клетки в контакт с иммуномодулятором и вторым средством можно осуществлять в любом порядке. В некоторых вариантах осуществления клетку приводят в контакт с иммуномодулятором и со вторым средством одновременно, либо контакт с иммуномодулятором осуществляют до или после контакта со вторым средством.
В другом аспекте изобретение предлагает композицию (например, одну или несколько композиций или лекарственных форм), содержащую иммуномодулятор (например, один или несколько, выбранных из: активатора костимуляторной молекулы или ингибитора молекулы иммунной контрольной точки) и второе терапевтическое средство LDK378. В некоторых вариантах осуществления иммуномодулятор представляет собой ингибитор молекулы иммунной контрольной точки (например, ингибитор PD-1, PD-L1, LAG-3, TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5) или CTLA4, или любое их сочетание). В одном варианте осуществления композиция содержит фармацевтически приемлемый носитель. Иммуномодулятор и второе средство могут присутствовать в составе одной композиции, или в составе двух или более разных композиций. Иммуномодулятор и второе средство можно вводить с помощью одного и того же способа, или с помощью разных способов введения.
В другом аспекте настоящее изобретение предлагает фармацевтическую комбинацию, содержащую (i) LDK378, или его фармацевтически приемлемую соль, и (ii) ниволумаб, или его фармацевтически приемлемую соль.
Кроме того, в данном описании раскрываются композиции, например, дозированные композиции, а также наборы, например, терапевтические наборы, которые содержат иммуномодулятор (например, один или несколько, выбранных из: активатора костимуляторной молекулы или ингибитора молекулы иммунной контрольной точки), второе терапевтическое средство LDK378 и инструкции по применению.
Ниже приведены пункты, в которых описаны другие предпочтительные варианты осуществления, по отдельности или в сочетании:
1. Фармацевтическая комбинация, содержащая (i) LDK378, или его фармацевтически приемлемую соль, и (ii) ниволумаб, или его фармацевтически приемлемую соль.
2. Фармацевтическая комбинация согласно абзацу 1, содержащая компоненты (i) и (ii), по отдельности или вместе.
3. Фармацевтическая комбинация по абзацам 1 или 2 для применения в качестве лекарственного средства, где LDK378 и ниволумаб вводят независимо друг от друга, в одно и то же время, или по отдельности с определенными интервалами времени.
4. Фармацевтическая комбинация согласно абзацу 3, где интервалы времени обеспечивают совместную активность партнеров в комбинации.
5. Фармацевтическая комбинация по любому из абзацев 1-4, содержащее количество, которое в сочетании является терапевтически эффективным для лечения ALK-опосредованного заболевания.
6. Фармацевтическая комбинация согласно абзацу 5, где ALK-опосредованное заболевание представляет собой рак.
7. Фармацевтическая комбинация согласно абзацу 6, где ALK-опосредованное заболевание представляет собой NSCLC или лимфому.
8. Фармацевтическая комбинация согласно абзацу 6, где АЛК-опосредованное заболевание представляет собой NSCLC.
9. Фармацевтическая комбинация по любому из абзацев 1-8 для применения в качестве лекарственного средства.
10. Фармацевтическая комбинация по любому из абзацев 1-8 для применения в лечении рака.
11. Фармацевтическая комбинация согласно абзацу 10, где рак представляет собой немелкоклеточный рак легкого.
12. Применение LDK378 в сочетании с ниволумабом в производстве лекарственного средства против ALK-опосредованного заболевания.
13. Применение LDK378 в сочетании с ниволумабом в производстве лекарственного средства согласно абзацу 12, где заболевание представляет собой рак.
14. Применение LDK378 в сочетании с ниволумабом в производстве лекарственного средства согласно абзацу 13, где рак представляет собой немелкоклеточный рак легкого.
15. Фармацевтическая композиция, содержащая LDK378, или его фармацевтически приемлемую соль, и ниволумаб, или его фармацевтически приемлемую соль, для одновременного или раздельного введения с целью лечения рака.
16. Фармацевтическая композиция согласно абзацу 15, где рак представляет собой немелкоклеточный рак легкого.
17. Фармацевтическая композиция по абзацу 22 или 23, где композиция содержит эффективное количество LDK378 и ниволумаба.
18. Фармацевтическая композиция по любому из абзацев 15-18, где композиция дополнительно содержит фармацевтически приемлемый носитель.
19. LDK378 для применения в качестве лекарственного средства, где LDK378, или его фармацевтически приемлемую соль, следует вводить в сочетании с ниволумабом, или его фармацевтически приемлемой солью.
20. LDK378 для применения в качестве лекарственного средства согласно абзацу 19 для лечения рака.
21. LDK378 для применения в качестве лекарственного средства согласно абзацу 20, где рак представляет собой немелкоклеточный рак легкого.
22. Фармацевтическая комбинация по любому из абзацев 1-11 в виде набора компонентов для сочетанного введения.
23. Фармацевтическая комбинация согласно абзацу 22, где LDK378, или его фармацевтически приемлемую соль, и ниволумаб, или его фармацевтически приемлемую соль, вводят совместно или независимо друг от друга, одновременно или по отдельности с определенными интервалами времени.
24. Способ лечения рака у индивидуума, нуждающегося в этом, включающий введение указанному индивидууму терапевтически эффективного количества i) LDK378, или его фармацевтически приемлемой соли, и (ii) ниволумаба, или его фармацевтически приемлемой соли.
25. Фармацевтическая комбинация по любому из абзацев 3-11, 22 или 23, применение по любому из абзацев 12-14, способ лечения рака согласно абзацу 24, фармацевтическая композиция по любому из абзацев 15-18, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21, где LDK378 и ниволумаб вводят ALK-наивному пациенту.
26. Фармацевтическая комбинация по любому из абзацев 3-11, 22 или 23, применение по любому из абзацев 12-14, способ лечения рака согласно абзацу 24, фармацевтическая композиция по любому из абзацев 15-18, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21, где LDK378 и ниволумаб вводят пациенту, который ранее получал ингибитор ALK.
27. Фармацевтическая комбинация по любому из абзацев 3-11, 22 или 23, применение по любому из абзацев 12-14, способ лечения рака согласно абзацу 24, фармацевтическая композиция по любому из абзацев 15-18, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21, где LDK378 и ниволумаб вводят пациенту, который ранее получал LDK378.
28. Фармацевтическая комбинация по любому из абзацев 3-11, 22, 23 или 25-27, применение по любому из абзацев 12-14 или 25-27, способ лечения рака по любому из абзацев 24-27, фармацевтическая композиция по любому из абзацев 15-18 или 25-27, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21 или 25-27, где рак характеризуется наличием транслокации или перегруппировки ALK.
29. Фармацевтическая комбинация по любому из абзацев 3-11, 22, 23 или 25-27, применение по любому из абзацев 12-14 или 25-27, способ лечения рака по любому из абзацев 24-27, фармацевтическая композиция по любому из абзацев 15-18, или 25-27, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21 или 25-27, где рак характеризуется наличием гибридизации EML4-ALK.
30. Фармацевтическая комбинация по любому из абзацев 3-11, 22, 23 или 25-27, применение по любому из абзацев 12-14 или 25-27, способ лечения рака по любому из абзацев 24-27, фармацевтическая композиция по любому из абзацев 15-18 или 25-27, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21 или 25-27, где рак характеризуется наличием гибридизации ALK-ROS1.
31. Фармацевтическая комбинация по любому из абзацев 1-11, 22, 23 или 25-30, применение по любому из абзацев 12-14 или 25-30, способ лечения рака по любому из абзацев 24-30, фармацевтическая композиция по любому из абзацев 15-18 или 25-30, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21 или 25-30, где доза серитиниба составляет 450 мг, а доза ниволумаба составляет 3 мг/кг.
32. Фармацевтическая комбинация по любому из абзацев 1-11, 22, 23 или 25-30, применение по любому из абзацев 12-14 или 25-30, способ лечения рака по любому из абзацев 24-30, фармацевтическая композиция по любому из абзацев 15-18 или 25-30, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21 или 25-30, где доза серитиниба составляет 600 мг, а доза ниволумаба составляет 3 мг/кг.
33. Фармацевтическая комбинация по любому из абзацев 1-11, 22, 23 или 25-32, применение по любому из абзацев 12-14 или 25-32, способ лечения рака по любому из абзацев 24-32, фармацевтическая композиция по любому из абзацев 15-18 или 25-32, или LDK378 для применения в качестве лекарственного средства по любому из абзацев 19-21 или 25-32, где серитиниб вводят с едой с низким содержанием жира.
Другие признаки или варианты осуществления раскрытых здесь способов, композиций, дозированных лекарственных форм и наборов включают в себя один или несколько из описанных ниже:
В некоторых вариантах осуществления иммуномодулятор представляет собой активатор костимуляторной молекулы. В одном варианте осуществления изобретения агонист костимуляторной молекулы может быть выбран из агониста (например, агонистического антитела или его антиген-связывающего фрагмента или растворимого гибрида) OX40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3 или лиганда CD83.
В некоторых вариантах осуществления иммуномодулятор представляет собой ингибитор молекулы иммунной контрольной точки. В одном варианте осуществления иммуномодулятор представляет собой ингибитор PD-1, PD-L1, PD-L2, CTLA4, TIM3, LAG3, CEACAM (например, CEACAM-1, -3 и/или -5), VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и/или TGFR-бета. В одном варианте осуществления ингибитор молекулы иммунной контрольной точки ингибирует PD-1, PD-L1, LAG-3, TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5) или CTLA4, или любое их сочетание. Термин "ингибирование" или "ингибитор" относится к уменьшению определенного параметра, например, активности, конкретной молекулы, например, ингибитора иммунной контрольной точки. Например, данный термин включает в себя ингибирование активности, например, активности PD-1 или PD-L1, по меньшей мере, на 5%, 10%, 20%, 30%, 40% или более. Но ингибирование не должно достигать 100%.
Ингибирование ингибиторной молекулы можно проводить на уровне ДНК, РНК или белка. В некоторых вариантах осуществления для ингибирования экспрессии ингибиторной молекулы можно использовать ингибиторную нуклеиновую кислоту (например, дцРНК, миРНК или кшРНК). В других вариантах осуществления ингибитор ингибиторного сигнала представляет собой полипептид, например, растворимый лиганд (например, PD-1-Ig или CTLA-4 Ig), или антитело или его антиген-связывающий фрагмент, которые связываются с ингибиторной молекулой; например, антитело или его фрагмент (также называемые здесь "молекула антитела"), которые связываются с PD-1, PD-L1, PD-L2, CTLA4, TIM3, LAG3, CEACAM (например, CEACAM-1, -3 и/или -5), VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и/или TGFR-бета, или их сочетания.
В одном варианте осуществления молекула антитела представляет собой полноразмкерное антитело или его фрагмент (например, Fab, F(аb')2, Fv, или одноцепочечный Fv-фрагмент (scFv)). В других вариантах осуществления молекула антитела содержит константный участок тяжелой цепи (Fc), выбранный, например, из константных участков тяжелой цепи IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE; предпочтительно выбранный, например, из константных участков тяжелой цепи IgG1, IgG2, IgG3 и IgG4, более предпочтительно, из константных участков тяжелой цепи IgG1 или IgG4 (например, человеческого IgG1 или IgG4). В одном варианте осуществления константный участок тяжелой цепи получен из человеческого IgG1 или человеческого IgG4. В одном варианте осуществления константный участок модифицируют, например, путем введения мутаций, чтобы изменить свойства молекулы антитела (например, чтобы повысить или понизить один или несколько из следующих параметров: связывание с рецептором Fc; гликозилирование антитела, количество остатков цистеина, активность в отношении эффекторных клеток или активность в отношении комплемента).
В некоторых вариантах осуществления молекула антитела представляет собой биспецифическую или мультиспецифическую молекулу антитела. В одном варианте осуществления молекула биспецифического антитела может обладать первой специфичностью к PD-1 или PD-L1 и второй специфичностью, например, второй специфичностью связывания, к TIM-3, LAG-3 или PD-L2. В одном варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1 и TIM-3. В другом варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1 и LAG-3. В другом варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1 и CEACAM (например, CEACAM-1, -3 и/или -5). В другом варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1 и CEACAM-1. В следующем варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1 и CEACAM-3. В следующем варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1 и CEACAM-5. В другом варианте осуществления биспецифическая молекула антитела связывается с PD-1 или PD-L1. В следующем варианте осуществления биспецифическая молекула антитела связывается с PD-1 и PD-L2. В другом варианте осуществления биспецифическая молекула антитела связывается с TIM-3 и LAG-3. В другом варианте осуществления биспецифическая молекула антитела связывается с CEACAM (например, CEACAM-1, -3 и/или -5) и LAG-3. В другом варианте осуществления биспецифическая молекула антитела связывается с CEACAM (например, CEACAM-1, -3 и/или -5) и TIM-3. Любое сочетание вышеуказанных молекул может присутствовать в мультиспецифической молекуле антитела, например, триспецифической молекуле антитела, которая обладает первой специфичностью в отношении PD-1 или PD-1, и второй и третьей специфичностями в отношении двух или более из следующих молекул: TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5), LAG-3 или PD-L2. В некоторых вариантах осуществления иммуномодулятор представляет собой ингибитор PD-1, например, человеческого PD-1. В другом варианте осуществления иммуномодулятор представляет собой ингибитор PD-L1, например, человеческого PD-L1. В одном варианте осуществления ингибитор PD-1 или PD-L1 представляет собой молекулу антитела против PD-1 или PD-L1. Ингибитор PD-1 или PD-L1 можно вводить отдельно или в сочетании с другими иммуномодуляторами, например, в сочетании с ингибитором LAG-3, TIM-3, CEACAM (например, CEACAM-1, -3 и/или -5) или CTLA4. В иллюстративном варианте осуществления ингибитор PD-1 или PD-L1, такой как молекула антитела против PD-1 или PD-L1, вводят в сочетании с ингибитором LAG-3, таким как молекула антитела против LAG-3. В другом варианте осуществления ингибитор PD-1 или PD-L1, такой как молекула антитела против PD-1 или PD-L1, вводят в сочетании с ингибитором TIM-3, таким как молекула антитела против TIM-3. В других вариантах осуществления ингибитор PD-1 или PD-L1, такой как молекула антитела против PD-1, вводят в сочетании с ингибитором LAG-3, таким как молекула антитела против LAG-3, и ингибитором TIM-3, таким как молекула антитела против TIM-3. В другом варианте осуществления ингибитор PD-1 или PD-L1, такой как молекула антитела против PD-1 или PD-L1, вводят в сочетании с ингибитором CEACAM (например, ингибитором CEACAM-1, -3 и/или -5), таким как молекула антитела против CEACAM. В другом варианте осуществления ингибитор PD-1 или PD-L1, такой как молекула антитела против PD-1 или PD-L1, вводят в сочетании с ингибитором CEACAM-1, таким как молекула антитела против CEACAM-1. В другом варианте осуществления ингибитор PD-1 или PD-L1, такой как молекула антитела против PD-1 или PD-L1, вводят в сочетании с ингибитором CEACAM-5, таким как молекула антитела против CEACAM-5. Другие сочетания иммуномодуляторов с ингибитором PD-1 (например, одного или нескольких из PD-L2, CTLA4, TIM3, CEACAM (например, CEACAM-1, -3 и/или -5) LAG3, VISTA, BTLA, TIGIT, LAIRI, CD160, 2В4 и/или TGFR) также входят в объем настоящего изобретения. В вышеуказанных сочетаниях ингибиторов молекул контрольных точек можно использовать любые молекулы антител, известные в данной области или описанные в настоящем документе.
Примеры ингибиторов молекул иммунных контрольных точек
В одном варианте осуществления ингибитор PD-1 представляет собой антитело против PD-1, выбранное из ниволумаба, пембролизумаба или пидилизумаба. Предпочтительно ингибитор PD-1 представляет собой ниволумаб.
В некоторых вариантах осуществления антитело против PD-1 представляет собой ниволумаб. Альтернативные названия ниволумаба включают в себя MDX-1106, MDX-1106-04, ONO-4538, или BMS-936558. В некоторых вариантах осуществления антитело против PD-1 представляет собой ниволумаб (регистрационный номер CAS: 946414-94-4). Ниволумаб представляет собой полноразмерное моноклональное человеческое антитело IgG4, способное специфически блокировать PD1. Ниволумаб (клон 5C4) и другие человеческие моноклональные антитела, способные специфически связываться с PD1, описаны в патенте США 8008449 и WO2006/121168. Ниволумаб является предпочтительным ингибитором PD-1.
В других вариантах осуществления антитело против PD-1 представляет собой пембролизумаб. Пембролизумаб (торговое название KEYTRUDA, ранее называемый лабролизумаб и также известный как Merck 3745, МК-3475 или SCH-900475) представляет собой гуманизированное моноклональное антитело IgG4, способное связываться с PD1. Пембролизумаб описан, например, в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, WO2009/114335 и US 8354509.
В некоторых вариантах осуществления антитело против PD-1 представляет собой пидилизумаб. Пидилизумаб (CT-011; Cure Tech) представляет собой гуманизированное моноклональное антитело IgG1k, способное связываться с PD1. Пидилизумаб и другие гуманизированные моноклональные антитела против PD-1 описаны в WO2009/101611. Другие антитела против PD1 раскрыты в патенте США 8609089, US 2010028330, и/или US 20120114649. Другие антитела против PD1 включают в себя AMP 514 (Amplimmune).
В некоторых вариантах осуществления ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, содержащий внеклеточный или PD-1-связывающий домен PD-L1 или PD-L2, гибридизованный с константным участком (таким как Fc-участок последовательности иммуноглобулина). В некоторых вариантах осуществления настоящего изобретения ингибитор PD-1 представляет собой АМР-224.
В некоторых вариантах осуществления ингибитор PD-L1 представляет собой антитело против PD-L1. В некоторых вариантах осуществления ингибитор PD-L1 может быть выбран из YW243.55.S70, MPDL3280A, MEDI-4736, MSB-0010718C или MDX-1105.
В одном варианте осуществления изобретения ингибитор PD-L1 представляет собой MDX-1105. MDX-1105, также известный как BMS-936559, представляет собой антитело против PD-L1, описанное в WO2007/005874.
В одном варианте осуществления ингибитор PD-L1 представляет собой YW243.55.S70. Антитело YW243.55.S70 представляет собой антитело против PD-L1, раскрытое в WO 2010/077634 (последовательности вариабельных участков тяжелой и легкой цепи описаны в SEQ ID No. 20 и 21, соответственно).
В одном варианте осуществления ингибитор PD-L1 представляет собой MDPL3280A (Genentech/Roche). MDPL3280A представляет собой человеческое Fc-оптимизированное моноклональное антитело IgG1, способное связываться с PD-L1. MDPL3280A и другие человеческие моноклональные антитела против PD-L1 раскрыты в патенте США № 7943743 и публикации США № 20120039906.
В других вариантах осуществления ингибитор PD-L2 представляет собой АМР-224. AMP-224 представляет собой растворимый рецепторный гибридный белок PD-L2-Fc, способный блокировать взаимодействие между PD1 и B7-H1 (B7-DCIg; Amplimmune, например, раскрытый в WO2010/027827 и WO2011/066342).
В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела против LAG-3. В одном варианте осуществления ингибитор LAG-3 представляет собой BMS-986016, более подробно описанный ниже.
Один или несколько из перечисленных выше ингибиторов молекул иммунных контрольных точек можно использовать в сочетании с LDK378, что ниже иллюстрируется более подробно.
Примеры сочетанных способов лечения
В одном варианте осуществления ингибитор PD-1 представляет собой ниволумаб (также называемый здесь MDX-1106, ONO-4538, BMS0936558, регистрационный номер CAS: 946414-94-4), раскрытый, например, в US 8008449, и имеющий последовательность, описанную в настоящем документе (или последовательность по существу идентичную или подобную описанной последовательности, например, последовательность, по меньшей мере, на 85%, 90%, 95% или более идентичную описанной последовательности).
В другом варианте осуществления ингибитор PD-1 пембролизумаб (также называемый здесь ламбролизумаб, МК-3475, MK03475 или KEYTRUDA), раскрытый, например, в US 8354509 и WO 2009/114335, и имеющий последовательность, описанную в настоящем документе (или последовательность по существу идентичную или подобную описанной последовательности, например, последовательность, по меньшей мере, на 85%, 90%, 95% или более идентичную описанной последовательности).
В другом варианте осуществления ингибитор PD-L1 представляет собой MSB0010718C (также упоминаемый как A09-246-2), раскрытый, например, в WO 2013/0179174, и имеющий последовательность, описанную в настоящем документе (или последовательность по существу идентичную или подобную описанной последовательности, например, последовательность, по меньшей мере, на 85%, 90%, 95% или более идентичную описанной последовательности).
В некоторых вариантах осуществления настоящего изобретения ингибитор PD-1, такой как антитело против PD-1 (например, ниволумаб), используют в описанных здесь способах или композициях. Например, ингибитор PD-1, такой как антитело против PD-1 (например, ниволумаб или пембролизумаб); или ингибитор PD-L1, такой как антитело против PD-L1 (например, MSB0010718C) (отдельно или в сочетании с другими иммуномодуляторами), используют в сочетания с ингибитором ALK LDK378. В одном варианте осуществления одно или несколько из перечисленных выше сочетаний используют для лечения расстройства, например, описанного здесь расстройства (такого как расстройство, описанное в таблице 1). В одном варианте осуществления одно или несколько из перечисленных выше сочетаний используют для лечения рака, например, описанного здесь рака (такого как рак, описанный в таблице 1). Каждое из указанных сочетаний ниже описано более подробно.
В соответствии с настоящим изобретением, ингибитор PD-1, такой как антитело против PD-1 (например, ниволумаб или пембролизумаб); или ингибитор PD-L1, такой как антитело против PD-L1 (например, MSB0010718C) (по отдельности или в сочетания с другими иммуномодуляторами), используют в сочетании с ингибитором Alk LDK378 для лечения рака, например, описанного здесь рака (такого как рак, описанный в таблице 1, например, немелкоклеточный рак легких). Ингибитор Alk LDK378 описан в таблице 1, или в публикации, указанной в таблице 1. В одном варианте осуществления ингибитор Alk LDK378 имеет структуру (структуру соединения или общую структуру), приведенную в таблице 1, или описанную в публикации, указанной в таблице 1. В одном варианте осуществления один из ниволумаба, пембролизумаба или MSB0010718C используют в сочетании с LDK378 для лечения рака, описанного в таблице 1, такого как солидная опухоль, например, рак легкого (например, немелкоклеточный рак легкого (NSCLC)), лимфома (например, анапластическая крупноклеточная лимфома или неходжкинская лимфома), воспалительная миофибробластическая опухоль (IMT), или нейробластома. В некоторых вариантах осуществления NSCLC представляет собой NSCLC на стадии IIIB или IV, или рецидивирующий местнораспространенный или метастатический NSCLC. В некоторых вариантах осуществления рак (такой как рак легкого, лимфома, воспалительная миофибробластическая опухоль или нейробластома) характеризуется наличием, или идентифицирован как характеризующийся наличием перегруппировки или транслокации ALK, например, гибридизацией ALK. В одном варианте осуществления гибрид ALK представляет собой гибрид EML4-ALK, например, описанный здесь гибрид EML4-ALK. В некоторых вариантах осуществления рак прогрессирует в присутствии другого ингибитора ALK или ингибитора ROS1, или является устойчивым или толерантным к другому ингибитору ALK или ингибитору ROS1. В некоторых вариантах осуществления рак прогрессирует в присутствии кризотиниба, или является устойчивым или толерантным к кризотинибу.
LDK378 имеет следующую структуру:
 .
.
Особенно предпочтительным сочетанием настоящего изобретения является фармацевтическая комбинация, содержащее (i) LDK378, или его фармацевтически приемлемую соль, и (ii) ниволумаб, или его фармацевтически приемлемую соль.
LDK378 (серитиниб) представляет собой ингибитор киназы анапластической лимфомы (ALK). Он имеет химическое название 5-хлор-N2-(2-изопропокси-5-метил-4-(пиперидин-4-ил)фенил)-N4-[2-(пропан-2-сульфонил)фенил]пиримидин-2,4-диамин. Способ получения LDK378 описан в WO2008/073687. Соединение утверждено FDA США как Zykadia® для лечения пациентов с киназа анапластической лимфомы (ALK)-положительным метастатическим немелкоклеточным раком легкого (NSCLC), который прогрессирует в присутствии кризотиниба, или устойчив к кризотинибу. Утвержденная в настоящее время суточная доза для применения LDK378 (отдельно) при NSCLC составляет 750 мг перорально на пустой желудок (то есть, его не следует вводить в течение 2 часов до или после приема пищи).
В клиническом исследовании LDK378 демонстрирует высокую частоту быстрых и длительных ответов у 246 ALK-положительных пациентов с NSCLC из группы, получающей дозу 750 мг (RD). У этих пациентов общая частота ответа (ORR) составляет 58,5%. Среди 144 ALK-положительных пациентов с NSCLC с подтвержденным полным ответом (CR) или частичным ответом (PR) у 86,1% пациентов ответ развивается в течение 12 недель, с медианным значением времени до ответа 6,1 недель. Медианное значение длительности ответа (DOR), определенное на основании оценки исследователя, составляет 9,69 месяцев. Медианное значение выживаемости при отсутствии прогрессирования (PFS) составляет 8,21 месяцев, причем оценке подвергались 53,3% пациентов. Важно отметить, что серитиниб демонстрирует указанный уровень высокой противораковой активности независимо от предшествующего статуса ингибитора ALK (т.е., независимо от того, получал пациент ранее лечение ингибитором ALK, или нет). Высокая ORR 54,6% и 66,3% наблюдалась у пациентов, получавших ранее лечение ингибитором ALK, и у ингибитор ALK-наивных пациентов, соответственно.
Однако метастатический ALK-положительный NSCLC остается неизлечимой болезнью. Использование возможностей иммунной системы для лечения пациентов с NSCLC представляет собой новую стратегию лечения, в которой ниволумаб можно безопасно использовать в сочетании с LDK378. Сочетанная терапия, включающая в себя применение целевого средства LDK378 и иммунотерапии (ниволумаб), может повышать выживаемость при отсутствии прогрессирования заболевания и, в конечном счете, общую выживаемость пациентов с NSCLC.
Предположительно механизм действия серитиниба не препятствует иммунному ответу. Кроме того, в испытаниях серитиниба редко встречаются неблагоприятные иммунные явления. Потенциальное перекрывание токсичности серитиниба и ниволумаба включает в себя диарею, тошноту, повышение AST и ALT, пневмонию и гипергликемию. Механизмы указанных проявлений токсичности предположительно не являются одинаковыми, причем механизмы действия двух соединений, и, следовательно, профиль безопасности можно регулировать.
LDK378 в сочетании с ниволумабом также можно использовать в способе промышленного получения лекарственного средства против ALK-опосредованного заболевания. Фармацевтическая композиция может содержать эффективные количества LDK378, или его фармацевтически приемлемой соли, и ниволумаба, или его фармацевтически приемлемой соли, которые можно вводить одновременно или отдельно с целью лечения рака. Аналогичным образом, LDK378 можно использовать в качестве лекарственного средства, где LDK378, или его фармацевтически приемлемая соль, предназначается для введения в сочетании с ниволумабом, или его фармацевтически приемлемой солью.
Фармацевтически приемлемые соли могут представлять собой, например, кислотно-аддитивные соли, предпочтительно соли, образованные органическими или неорганическими кислотами. Подходящие неорганические кислоты включают в себя, например, галоген-содержащие кислоты, такие как хлористоводородная кислота. Подходящие органические кислоты включают в себя, например, карбоновые кислоты или сульфоновые кислоты, такие как фумаровая кислота или метансульфоновая кислота. В целях выделения или очистки также можно использовать фармацевтически неприемлемые соли, такие как пикраты или перхлораты. Для терапевтического применения используют только фармацевтически приемлемые соли или свободные соединения (если это применимо, в виде фармацевтических препаратов), и, следовательно, они являются предпочтительными. С учетом тесной взаимосвязи между новыми соединениями в свободном виде и в виде солей, включающих в себя соли, которые можно использовать в качестве промежуточных соединений, например, для очистки или идентификации новых соединений, любую ссылку на свободные соединения, приведенную выше или ниже в данном описании, следует рассматривать как ссылку на соответствующие соли, в зависимости от обстоятельств и целесообразности. Соли соединений формулы (I) предпочтительно представляют собой фармацевтически приемлемые соли; подходящие противоионы, образующие фармацевтически приемлемые соли, известны в данной области.
Настоящее изобретение, в соответствии с указанным выше первым вариантом осуществления, относится к фармацевтическому сочетанию, особенно, к фармацевтическому сочетанному продукту, содержащему указанные компоненты сочетания.
В соответствии с настоящим изобретением, компоненты фармацевтического сочетания, соединения (i) LDK378, или его фармацевтически приемлемую соль, и (ii) ниволумаб, или его фармацевтически приемлемую соль, можно вводить по отдельности или вместе.
Фармацевтическая комбинация, в соответствии с настоящим изобретением предназначенное для применения в качестве лекарственного средства, содержит LDK378 и ниволумаб, которые можно вводить независимо друг от друга, в одно и то же время, или по отдельности через промежутки времени, где промежутки времени позволяют партнерам в комбинации проявлять совместную активность.
Термин "фармацевтическая комбинация" в данном описании относится к продукту, полученному путем смешивания или объединения в нефиксированном сочетании активных ингредиентов, например, (i) LDK378, или его фармацевтически приемлемой соли, и (ii) ниволумаба, или его фармацевтически приемлемой соли, по отдельности или вместе.
Термин "сочетание" относится к композициям, содержащим отдельные партнеры и, необязательно, инструкции по применению сочетания или по сочетанным продуктам. Объединяемые соединения могут быть изготовлены и/или получены одним производителем, или разными производителями. Таким образом, партнеры в комбинации могут представлять собой полностью раздельные фармацевтические лекарственные формы, или фармацевтические композиции, которые также продаются независимо друг от друга, и предоставляются только инструкции по их совместному применению: (i) перед разрешением к использованию для врачей (например, в случае "набора компонентов", содержащего соединение настоящего изобретения и другое терапевтическое средство); (ii) самим врачом (или под руководством врача) непосредственно перед введением; (iii) самому пациенту врачом или медицинским персоналом.
Термин "нефиксированное сочетание" означает, что активные ингредиенты, например, LDK378 и ниволумаб, вводят по отдельности или вместе, независимо друг от друга в одно и то же время, или по отдельности с определенными интервалами времени, причем такое введение обеспечивает терапевтически эффективный уровень активного ингредиента в организме индивидуума, нуждающегося в этом. Последнее также относится к коктейльной терапии, включающей в себя, например, введение трех или более активных ингредиентов. Данный термин, в особенности, относится к "набору компонентов", в том смысле, что партнеры в комбинации, например (i) LDK378 и (ii) ниволумаб (а также одно или несколько других средств, в случае их совместного использования), как указано в данном документе, можно вводить независимо друг от друга.
Термин "оказывающий совокупный терапевтический эффект" означает, что соединения оказывают синергическое действие при введении по отдельности или вместе, независимо друг от друга в одно и то же время, или по отдельности с определенными интервалами времени, с целью лечения индивидуума, нуждающегося в этом, такого как теплокровное животное, в частности, человек.
Было показано, что сочетание настоящего изобретения обладает полезными терапевтическими свойствами, например, его компоненты могут оказывать синергическое действие, проявляя высокую противоопухолевую активность in vivo и in vitro, и, следовательно, указанное сочетание можно использовать в качестве лекарственного средства. Его характеристики делают его особенно полезным при лечении рака.
Подходящие виды рака, которые можно лечить с помощью сочетания настоящего изобретения, включают в себя, без ограничения, анапластическую крупноклеточную лимфому (ALCL), нейробластому, рак легкого, немелкоклеточный рак легкого (NSCLC). В предпочтительном варианте осуществления рак представляет собой NSCLC.
Сочетание настоящего изобретения, помимо или в дополнение к вышесказанному, можно использовать, особенно при лечении рака, наряду с химиотерапией, лучевой терапией, иммунотерапией, хирургическим вмешательством, или их сочетанием. Длительную терапию в равной степени можно использовать в качестве вспомогательной терапии в контексте других стратегий лечения, как описано выше. Другие возможные способы лечения включают в себя терапию с целью поддержания состояния пациента после регрессии опухоли, или даже профилактическую химиотерапию, например, для пациентов с повышенным риском.
Термины "лечить" или "лечение", используемые в применении к любому заболеванию или расстройству, относятся к облегчению заболевания или расстройства (например, к замедлению, прекращению или ослаблению развития заболевания или, по меньшей мере, одного из его клинических симптомов), с целью предотвращения или задержки появления, или развития, или прогрессирования заболевания или расстройства. Кроме того указанные термины относятся к облегчению или улучшению, по меньшей мере, одного физического параметра, включающего в себя параметры, которые могут не ощущаться пациентом, а также параметры, которые могут модулировать заболевание или расстройство, либо физическому (например, стабилизация ощущаемого симптома), либо физиологическому (например, стабилизация физического параметра), либо тому и другому.
Термин "лечение" включает в себя, например, терапевтическое введение партнеров в комбинации теплокровному животному, в частности, человеку, нуждающемуся в таком лечении, с целью излечения заболевания, или достижения регрессии заболевания, или задержки развития заболевания.
Сочетание LDK378 и ниволумаба можно использовать для промышленного получения лекарственного средства против ALK-опосредованного заболевания, описанного выше. Подобным образом, сочетание можно использовать в способе лечения ALK, как описано выше, где указанный способ включает в себя введение эффективного количества сочетания (i) LDK378, или его фармацевтически приемлемой соли, и (ii) ниволумаба, или его фармацевтически приемлемой соли, по отдельности или вместе, индивидууму, нуждающемуся в таком введении, в соответствии с настоящим изобретением.
Например, термин "(терапевтически) активный при совместном ведении" может означать, что указанные соединения можно вводить раздельно или последовательно (с постоянными интервалами, предпочтительно, в последовательной манере) через определенные промежутки времени, которые предпочтительно обеспечивают у теплокровного животного, особенно человека, подлежащего лечению, (предпочтительно синергическую) активность (совместное терапевтическое действие). Совместный терапевтический эффект можно отслеживать, в частности, путем определения уровней в крови, демонстрирующих, что оба соединения присутствуют в крови человека, подлежащего лечению, по меньшей мере в течение определенных интервалов времени, однако это не исключает того случая, когда соединения оказывают совместную активность, хотя и не присутствуют в крови одновременно.
Настоящее изобретение также описывает способ лечения ALK-опосредованного заболевания, в котором сочетание (i) LDK378, или его фармацевтически приемлемой соли, и (ii) ниволумаба, или его фармацевтически приемлемой соли, вводят по отдельности или вместе.
Настоящее изобретение предлагает фармацевтическую композицию, содержащую эффективное количество (i) LDK378, или его фармацевтически приемлемой соли, и (ii) ниволумаба, или его фармацевтически приемлемой соли. Фармацевтическая композиция может содержать фармацевтически приемлемый носитель, который может представлять собой, например, любое подходящее фармацевтическое вспомогательное вещество. Носитель включает в себя любые и все связующие средства, наполнители, растворители, диспергирующие среды, покрывающие вещества, поверхностно-активные вещества, антиоксиданты, консерванты (например, противобактериальные средства, противогрибковые средства), средства, обеспечивающие изотоничность, средства, замедляющие абсорбцию, соли, стабилизаторы лекарственных средств, разрыхлители, смазывающие средства, подслащивающие средства, ароматизирующие средства, красители и т.п., а также их сочетания, известные специалистам в данной области (см., например, Remington's Pharmaceutical Sciences, 18th Ed. Mack Printing Company, 1990, pp. 1289- 1329; Remington: The Science and Practice of Pharmacy, 21st Ed. Pharmaceutical Press 2011; а также его последующие версии). Для получения терапевтических или фармацевтических композиций можно использовать любой обычный носитель, за исключением тех случаев, когда носитель является несовместимым с активным ингредиентом. Для получения фармацевтических композиций также можно использовать способы и ингредиенты, отличные от описанных в данном документе.
В соответствии с настоящим изобретением партнеры в комбинации можно вводить независимо друг от друга в одно и то же время, или раздельно с определенными интервалами времени в отдельных стандартных лекарственных формах. Два терапевтических партнера можно получить с помощью известного способа, подходящего для энтерального, такого как пероральное или ректальное, местного и парентерального введения нуждающемуся в указанном введении индивидууму, такому как теплокровное животное, в частности, человек. Подходящие фармацевтические композиции содержат, например, примерно от 0,1% до 99,9% активного ингредиента.
Фармацевтическую композицию можно подвергнуть обработке с целью получения конечной лекарственной формы - таблетки или капсулы. Это можно осуществить путем прессования конечной смеси сочетания, необязательно вместе с одним или несколькими наполнителями. Прессование можно проводить, например, с помощью роторного таблеточного пресса. Можно получить таблетки, имеющие разные формы (круглые, овальные или другие подходящие формы). Таблетка необязательно может иметь покрытие, которое наносят с помощью известных методов, чтобы замедлить дезинтеграцию и абсорбцию в желудочно-кишечном тракте и тем самым обеспечить пролонгированное действие в течение более длительного периода времени. Если не указано иначе, таблетки получают с помощью известного способа, включающего в себя, например, процессы смешивания, грануляции и нанесения сахарного покрытия. Композицию для перорального применения можно получить в виде твердых желатиновых капсул, которые содержат активный ингредиент в смеси с инертным твердым разбавителем, таким как карбонат кальция, фосфат кальция или наполнитель на основе целлюлозы, или в виде мягких желатиновых капсул, которые содержат активный ингредиент в смеси с водой или масляной средой, такой как оливковое масло, жидкий парафин или арахисовое масло.
Термин "фармацевтически приемлемый" относится к соединениям, веществам, композициям и/или лекарственным формам, которые подходят для применения в контакте с тканями человека и животных, не вызывая чрезмерных токсичности, раздражения, аллергической реакции или других проблем или осложнений, и характеризуются разумным соотношением польза/риск.
В другом аспекте изобретение предлагает LDK378 для применения в качестве лекарственного средства, причем при лечении ALK-опосредованного заболевания, такого как рак, LDK378, или его фармацевтически приемлемую соль, нужно вводить в сочетании с ниволумабом, или его фармацевтически приемлемой солью.
Раковые опухоли и индивидуумы
Термин "ALK-опосредованное заболевание" относится к заболеванию, при котором активность данной киназы приводит к аномальной активности регуляторных путей, в том числе, к сверхэкспрессии, мутации или относительному снижению активности других регуляторных путей в клетке, вызывая чрезмерную пролиферацию клеток, например, рак. ALK-опосредованное заболевание может представлять собой немелкоклеточный рак легкого (NSCLC), который характеризуется транслокацией ассоциированный с микротрубочками белок иглокожих 4 (EML4) - киназа анапластической лимфомы (ALK). ALK представляет собой рецепторную тирозинкиназу суперсемейства рецепторов инсулина, которая играет важную роль в развитии и функционировании нервной системы. При некоторых типах опухолей наблюдается транслокация, мутация или амплификация ALK и, следовательно, ALK-опосредованное заболевание включает в себя, помимо NSCLC, нейробластому и анапластическую крупноклеточную лимфому (ALCL). Изменения в ALK играют ключевую роль в патогенезе указанных опухолей. Другие партнеры ALK по гибридизации, помимо EML4, которые могут участвовать в развитии ALK-опосредованного заболевания, включают в себя KIF5B, TFG, KLC1 и PTPN3, но, предположительно, они менее распространены, чем EML4. Доклинические эксперименты демонстрируют, что разные партнеры ALK по гибридизации опосредуют лиганд-независимую димеризацию/олигомеризацию ALK, приводящую к конститутивной активности киназы и высокой онкогенной активности in vitro и in vivo и, таким образом, после транслокации ALK контролирует, т.е. опосредует развитие заболевания.
В некоторых вариантах осуществления описанных здесь композиций и способов гиперпролиферативные расстройства или состояния, такие как рак, включают в себя, без ограничения, солидную опухоль, опухоль мягких тканей (такую как гематологический рак, лейкоз, лимфома или миелома) и метастатическое поражение, обусловленное одним из указанных выше видов рака. В одном из вариантов осуществления рак представляет собой солидную опухоль. Примеры солидных опухолей включают в себя злокачественные опухоли, такие как саркомы, аденокарциномы и карциномы, поражающие разные системы органов, включающие в себя легкие, молочную железу, яичники, лимфоидную систему, желудочно-кишечный тракт (например, толстую кишку), анальный канал, половые органы и мочеполовой тракт (например, почки, уротелий, клетки мочевого пузыря, простату), глотку, ЦНС (например, головной мозг, нервные или глиальные клетки), голову и шею, кожу (например, меланома) и поджелудочную железу, а также аденокарциномы, которые включают в себя такие злокачественные опухоли, как рак толстой кишки, рак прямой кишки, почечно-клеточная карцинома, рак печени, немелкоклеточный рак легкого, рак тонкой кишки и рак пищевода. Рак может находиться на ранней, промежуточной или поздней стадии, или он может представлять собой метастатический рак.
В одном из вариантов осуществления рак выбран из раковых заболеваний, описанных в таблице 1. Например, рак может быть выбран из солидных опухолей, таких как рак легкого (например, немелкоклеточный рак легкого (NSCLC) (например, NSCLC с плоскоклеточной и/или неплоскоклеточной гистологией)), колоректальный рак, меланома (например, запущенная меланома), рак головы и шеи (например, плоскоклеточный рак головы и шеи (HNSCC), рак пищеварительного/желудочно-кишечного тракта, рак желудка, рак нервной системы, глиобластома (например, мультиформная глиобластома), рак яичника, рак почки, рак печени, рак поджелудочной железы, рак предстательной железы, рак печени, рак молочной железы, рак анального канала, рак желудка и пищевода, рак щитовидной железы, рак шейки матки, воспалительная миофибробластическая опухоль (IMT), нейробластома; или гематологических раковых заболеваний (таких как лимфома Ходжкина, неходжкинская лимфома, анапластическая крупноклеточная лимфома, лимфоцитарный лейкоз или миелоидный лейкоз).
В одном из вариантов осуществления рак представляет собой немелкоклеточный рак легкого (NSCLC), например, ALK+ NSCLC. Используемый в настоящем описании термин "ALK+ немелкоклеточный рак легкого" или "ALK+ NSCLC" относится к NSCLC, который характеризуется повышенной (например, конститутивно повышенной) активностью киназы анапластической лимфомы, или перестройкой или транслокацией гена киназы анапластической лимфомы (ALK). Как правило, по сравнению с общей популяцией пациентов с NSCLC, пациенты с ALK+ NSCLC, как правило, моложе, имеют легкий (например, <10 пачек/год) анамнез курения, или не имеют анамнеза курения, имеют более низкий общесоматический статус в соответствии с определением Восточной объединенной онкологической группы, или они могут иметь более агрессивное заболевание и, следовательно, могут ощущать заболевание на более ранней стадии развития (Shaw et al. J Clin Oncol. 2009; 27(26):4247-4253; Sasaki et al. Eur J Cancer. 2010; 46(10):1773-1780; Shaw et al. N Engl J Med. 2013;368(25):2385-2394; Socinski et al. J Clin Oncol. 2012; 30(17):2055-2062 ; Yang et al. J Thorac Oncol. 2012;7(1):90-97).
В одном из вариантов осуществления рак, например, NSCLC, характеризуется перегруппировкой или транслокацией гена ALK. В одном варианте осуществления перегруппировка или транслокация гена ALK приводит к гибридизации (например, к гибридизации выше участка промотора ALK). В некоторых вариантах осуществления гибридизация приводит к конститутивной активации киназы.
В одном варианте осуществления гибрид представляет собой гибрид EML4-ALK. Примеры гибридных белков EML4-ALK включают в себя, без ограничения, E13;A20 (V1), E20;A20 (V2), E6a/b;A20 (V3a/b), E14;A20 (V4), E2a/b;A20 (V5a/b), E13b;A20 (V6), E14;A20(V7), E15;A20("V4") или E18;A20 (V5) (Choi et al. Cancer Res. 2008; 68(13): 4971-6; Horn et al. J Clin Oncol. 2009; 27(26): 4232-5; Koivunen et al. Clin Cancer Res. 2008; 14(13): 4275-83; Soda et al. Nature. 2007; 448(7153): 561-6; Takeuchi et al. Clin Cancer Res. 2008; 14(20): 6618-24; Takeuchi et al. Clin Cancer Res. 2009; 15(9): 3143-9; Wong et al. Cancer. 2009 Apr 15;115(8): 1723-33).
В некоторых вариантах осуществления ген ALK гибридизуется с партнером, отличным от EML4. В одном варианте осуществления гибрид представляет собой гибрид KIF5B-ALK. В другом варианте осуществления изобретения гибрид представляет собой гибрид TFG-ALK. Примеры гибридов KIF5B-ALK и TFG-ALK описаны, например, в Takeuchi et al. Clin Cancer Res. 2009; 15(9): 3143-9, Rikova et al. Cell. 2007; 131(6): 1190-203.
Перегруппировки или транслокации гена ALK, или раковые клетки, несущие перегруппировку или транслокацию гена ALK, можно детектировать, например, методом флуоресцентной гибридизации in situ (FISH), например, с отщеплением ALK от зонда.
Раскрытые здесь способы и композиции можно использовать для лечения метастатических поражений, связанных с упомянутыми выше видами рака.
Термин "нуждающийся в этом индивидуум" относится к теплокровному животному, в частности, к человеку, у которого лечение может вызвать биологическое улучшение, медицинское улучшение, или улучшение качества жизни. Индивидуум или пациент, которому можно вводить сочетание, включает в себя млекопитающих и отличных от млекопитающих животных. Примерами млекопитающих являются, без ограничения, люди, шимпанзе, приматы, мартышки, крупный рогатый скот, лошади, овцы, козы, свиньи; кролики, собаки, кошки, крысы, мыши, морские свинки и т.п. Примерами отличных от млекопитающих животных являются, без ограничения, птицы, рыбы и т.п. В наиболее предпочтительном варианте осуществления индивидуум или пациент представляет собой человека. Он может представлять собой человека, который в соответствии с поставленным диагнозом нуждается в лечении описанного здесь заболевания или расстройства.
В других вариантах осуществления индивидуум представляет собой млекопитающее, такое как примат, предпочтительно высший примат, например, человек (например, пациент, страдающий от описанного здесь расстройства, или пациент, имеющий риск развития описанного здесь расстройства). В одном варианте осуществления индивидуум нуждается в усиления иммунного ответа. В одном варианте осуществления индивидуум страдает от описанного здесь расстройства, или имеет риск развития описанного здесь расстройства, такого как рак, описанный в настоящем документе. В некоторых вариантах осуществления индивидуум страдает от иммунодефицита, или имеет риск развития иммунодефицита. Например, индивидуум, который получает, или получал химиотерапевтическое лечение и/или лучевую терапию. Альтернативно, или в добавление к вышесказанному индивидуум страдает от иммунодефицита, или имеет риск развития иммунодефицита в результате инфекции.
В одном варианте осуществления индивидуум (например, индивидуум, имеющий рак легкого (такой как немелкоклеточный рака легкого), лимфому (такую как анапластическая крупноклеточная лимфома или неходжкинская лимфома), воспалительную миофибробластическую опухоль или нейробластому) получает лечение, или получал лечение другим ингибитором ALK, и/или ингибитором ROS1, таким как кризотиниб. Например, серитиниб можно вводить в суточной пероральной дозе 750 мг или ниже, например, 600 мг или ниже, например, 450 мг или ниже.
В другом варианте осуществления присутствующее у индивидуума раковое заболевание (например, рак легкого (такой как немелкоклеточный рак легкого), лимфома (такая как анапластическая крупноклеточная лимфома или неходжкинская лимфома), воспалительная миофибробластическая опухоль, или нейробластома) прогрессирует на фоне другого ингибитора ALK и/или ингибитора ROS1, такого как кризотиниб, или является устойчивым или толерантным к такому ингибитору.
В следующем варианте осуществления присутствующее у индивидуума раковое заболевание (например, рак легкого (такой как немелкоклеточный рак легкого), лимфома (такая как анапластическая крупноклеточная лимфома или неходжкинская лимфома), воспалительная миофибробластическая опухоль или нейробластома) характеризуется риском прогрессирования на фоне другого ингибитора ALK и/или ингибитора ROS1, такого как кризотиниб, или риском развуития устойчивости или толерантности к такому ингибитору.
В других вариантах осуществления присутствующее у индивидуума раковое заболевание является устойчивым или толерантным, или характеризуется риском развития устойчивости или толерантности к ингибитору тирозинкиназы (TKI), например, к ингибитору тирозинкиназы EGFR.
В некоторых вариантах осуществления присутствующее у индивидуума раковое заболевание не связано с мутацией EGFR, мутацией KRAS, или обоими мутациями.
Дозы и введение
Дозы и схемы введения описанных здесь средств может определить специалист в данной области. Термин "эффективное количество" относится к количеству рассматриваемого соединения, которое вызывает биологический или медицинский ответ в клетке, ткани, органе, системе, организме животного или человека, где указанный ответ определяет исследователь, ветеринар, врач или другой клиницист. Эффективная доза каждого средства, входящего в состав сочетания настоящего изобретения, может варьировать в зависимости от конкретного используемого соединения, или конкретной используемой фармацевтической композиции, способа введения, состояния, подлежащего лечению, тяжести состояния, подлежащего лечению. Врач, клиницист или ветеринар обычной квалификации может легко определить и назначить эффективное количество лекарственного средства, необходимое для предотвращения или прекращения развития состояния, или противодействия развитию состояния. Конкретную оптимальную величину концентрации лекарственного средства в эффективном диапазоне определяют по схеме, учитывающей кинетику доступности входящих в состав сочетания лекарственных средств в целевых участках. Кроме того, учитывают распределение, равновесное состояние и выведение лекарственного средства.
Настоящее изобретение также описывает фармацевтическая комбинация в виде "набора компонентов" для совместного введения. Сочетание может находиться либо в виде фиксированного сочетания в составе одной стандартной лекарственной формы, либо в виде набора компонентов для совместного введения, где (i) LDK378, или его фармацевтически приемлемую соль, и (ii) ниволумаб, или его фармацевтически приемлемую соль, можно вводить независимо друг от друга, в одно и то же время, или по отдельности с определенными интервалами времени, предпочтительно так, чтобы указанные интервалы времени обеспечивали объединенный (=совместный) эффект партнеров в комбинации. Затем независимые ингредиенты или компоненты препарата, продукта или композиции, можно, например, вводить одновременно или с чередованием в хронологическом порядке, то есть в разные моменты времени, или с одинаковыми или разными для всех компонентов набора интервалами времени. В сочетанных способах лечения настоящего изобретения можно использовать соединения, произведенные и/или полученные одним производителем, или разными производителями. Кроме того, партнеры в комбинации могут быть объединены в сочетанной терапии: (i) перед разрешением к использованию сочетанного продукта для врачей (например, в случае набора, содержащего LDK378 и ниволумаб); (ii) самим врачом (или под руководством врача) непосредственно перед введением; (iii) самими пациентами, например, в процессе последовательного введения соединения настоящего изобретения и другого терапевтического средства. В одном варианте осуществления сочетание оказывает синергическое действие.
Терапевтически эффективную дозу сочетания настоящего изобретения или фармацевтической композиции, которая зависит от вида индивидуума, массы тела, возраста и индивидуального состояния, расстройства или заболевания, подлежащего лечению, или его тяжести, можно определить с помощью стандартных клинических методов. Кроме того, для определения оптимальных диапазонов доз можно использовать анализы in vitro или in vivo. Конкретная точная доза также может зависеть от способа введения и тяжести состояния, подлежащего лечению, и может быть назначена по усмотрению лечащего врача, в зависимости от состояния каждого индивидуума с учетом, например, опубликованных клинических исследований. Как правило, удовлетворительных результатов можно достичь при системном введении суточной дозы LDK378 от 150 мг до 750 мг перорально. В большинстве случаев суточная доза LDK378 может находиться в диапазоне от 300 мг до 750 мг.
LDK378 обычно вводят перорально в дозе, составляющей примерно от 100 до 1000 мг, например, примерно от 150 мг до 900 мг, примерно от 200 мг до 800 мг, примерно от 300 мг до 700 мг, или примерно от 400 мг до 600 мг, например, в дозе, составляющей примерно 150 мг, 300 мг, 450 мг, 600 мг или 750 мг. В конкретном варианте осуществления LDK378 вводят перорально в дозе, составляющей примерно 750 мг или ниже, например, примерно 600 мг или меньше, например, примерно 450 мг или ниже. В некоторых вариантах осуществления LDK378 вводят с пищей. В других вариантах осуществления настоящего изобретения дозу вводят натощак. Режим дозирования может варьировать и включает в себя, например, введение от одного раза в два дня до одного, двух или трех раз в день. В одном варианте осуществления LDK378 вводят ежедневно. В одном варианте осуществления LDK378 вводят перорально в дозе примерно от 150 мг до 750 мг в сутки, либо во время еды, либо натощак. В одном варианте осуществления LDK378 вводят перорально в дозе примерно 750 мг в день натощак. В одном варианте осуществления LDK378 вводят перорально в дозе примерно 750 мг в день в виде капсулы или таблетки. В другом варианте осуществления LDK378 вводят перорально в дозе примерно 600 мг в день в виде капсулы или таблетки. В одном варианте осуществления LDK378 вводят перорально в дозе примерно 450 мг в день в виде капсулы или таблетки.
В сочетании с ниволумабом LDK378 можно вводить в дозе 450 мг, если доза ниволумаба составляет 3 мг/кг, 600 мг, если доза ниволумаба составляет 3 мг/кг, или 300 мг, если доза ниволумаба составляет 3 мг/кг. Наиболее предпочтительные дозы обоих соединений, используемых для сочетанной терапии, составляют 600 мг LDK378 и 3 мг/кг ниволумаба. В частности, 600 мг LDK378 и 3 мг/кг ниволумаба составляют наиболее предпочтительный режим дозирования для лечения ALK-положительного (например, EML4-ALK) NSCLC. Ниволумаб можно вводить в виде инфузии с фиксированной дозой каждые две недели. Серитиниб следует принимать вместе с пищей пониженной жирности. Допустимо принимать серитиниб в течение 30 минут после употребления пищи пониженной жирности. Пациент должен воздержаться от приема пищи в течение, по меньшей мере, одного часа после приема серитиниба и пищи пониженной жирности. Предполагается, что прием серитиниба с ежедневным приемом пищи может уменьшить частоту и/или тяжесть желудочно-кишечных явлений. Согласно оценкам, оказываемое в равновесном состоянии воздействие серитиниба, вводмого в дозе 450 мг и 600 мг во время ежедневного приема пищи пониженной жирности, находится в пределах 20% от величины воздействия серитиниба при его введении натощак в дозе, рекомендуемой фазой II и составляющей 750 мг, что предсказано на основе моделирования клинического исследования с использованием популяционной фармакокинетической модели, разработанной для пациентов с ALK-положительным раком в одном клиническом исследовании, и параметров абсорбции, определенных в другом клиническом исследовании.
Термин "пища пониженной жирности" в данном описании относится к пище, которая содержит примерно от 1,5 до 15 граммов жира и всего примерно от 100 до 500 калорий.
В некоторых вариантах осуществления молекулу антитела против PD-1 вводят путем инъекции (например, подкожно или внутривенно) в дозе, составляющей примерно от 1 до 30 мг/кг, например, примерно от 5 до 25 мг/кг, примерно от 10 до 20 мг/кг, примерно от 1 до 5 мг/кг, или в дозе, составляющей примерно 3 мг/кг. Режим дозирования может варьировать, например, от одного раза в неделю до одного раза в 2, 3 или 4 недели. В одном варианте осуществления молекулу антитела против PD-1 вводят в дозе, составляющей примерно от 10 до 20 мг/кг, каждые две недели.
В одном из вариантов осуществления молекулу антитела против PD-1, например, ниволумаб, вводят внутривенно в дозе, составляющей примерно от 1 мг/кг до 3 мг/кг, например, примерно 1 мг/кг, 2 мг/кг или 3 мг/кг, каждые две недели. В одном варианте осуществления молекулу антитела против PD-1, например, ниволумаб, вводят внутривенно в дозе примерно 2 мг/кг с интервалами в 3 недели.
Описанные здесь сочетанные терапевтические средства можно вводить индивидууму системно (например, перорально, парентерально, подкожно, внутривенно, ректально, внутримышечно, внутрибрюшинно, интраназально, трансдермально или путем ингаляции или внутриполостной инсталляции), местно или путем нанесения на слизистую оболочку, например, на слизистую оболочку носа, горла и бронхов.
Описанные здесь способы и композиции можно использовать в сочетании с другими средствами или терапевтическими препаратами. Сочетанные терапевтические средства можно вводить одновременно или последовательно в любом порядке. Можно использовать любое сочетание молекул антител против PD-1 или PD-L1 и других терапевтических средств, процедур или препаратов (например, описанных в данном документе) в любой последовательности. Сочетанные терапевтические средства можно вводить в периоды активного развития расстройства, или в периоды ремиссии или менее активного течения заболевания. Сочетанные терапевтические средства можно вводить до проведения другого способа лечения, одновременно с ним, или после него, или во время ремиссии заболевания.
В некоторых вариантах осуществления описанные здесь способы и композиции используют в сочетании с одним или несколькими способами лечения, включающими в себя введение других молекул антител, химиотерапию, другую противораковую терапию (такую как направленная противораковая терапия, генная терапия, вирусная терапия, трансплантация костного мозга с РНК-терапией, нанотерапия или применение онколитических средств), применение цитотоксических средств, иммунную терапию (например, применение цитокинов или клеточной иммунной терапии), хирургическое вмешательство (такое как люмпэктомия или мастэктомия) или облучение, или сочетание любых вышеперечисленных способов. Дополнительная терапия может представлять собой адъювантную или неоадъювантную терапию. В некоторых вариантах осуществления другая терапия включает в себя применение ингибитора фермента (например, низкомолекулярного ингибитора фермента), или ингибитора метастазирования. Примеры цитотоксических средств, которые можно вводить в сочетании, включают в себя ингибиторы образования микротрубочек, ингибиторы топоизомеразы, антиметаболиты, ингибиторы митоза, алкилирующие средства, антрациклины, алкалоиды барвинка, интеркалирующие средства, средства, способные препятствовать передаче сигнала, средства, инициирующие апоптоз, ингибиторы протеосом и облучение (например, локальное или полное облучение организма (например, гамма-облучение)). В других вариантах осуществления другая терапия представляет собой хирургическое вмешательство или облучение, или их сочетание. В других вариантах осуществления другая терапия представляет собой терапию, направленную на путь mTOR, применение ингибитора HSP90 или ингибитора тубулина.
Альтернативно, или наряду с вышеуказанными сочетаниями, описанные здесь способы и композиции можно использовать в сочетании с одним или несколькими из следующих способов лечения: терапия, проводимая с использованием вакцин, например, терапевтических вакцин против рака; другие виды клеточной иммунотерапии.
В другом варианте осуществления сочетанную терапию используют в сочетания с одним, двумя или всеми средствами, выбранными из оксалиплатина, лейковорина или 5-FU (например, совместное введение FOLFOX). Альтернативно, или кроме того, сочетание дополнительно включает в себя ингибитор VEGF (например, описанный здесь ингибитор VEGF). В некоторых вариантах осуществления рак, который можно лечить сочетанием, выбран из таких заболеваний, как меланома, колоректальный рак, немелкоклеточный рак легкого, рак яичника, рак молочной железы, рак простаты, рак поджелудочной железы, гематологическая злокачественная опухоль или почечноклеточный рак. Рак может находиться на ранней, средней или поздней стадии.
В других вариантах осуществления для лечения почечноклеточной карциномы и других солидных опухолей сочетанную терапию вводят наряду с ингибитором тирозинкиназы (таким как акситиниб).
В других вариантах осуществления сочетанную терапию вводят наряду со средством, направленным на рецептор 4-1BB (таким как антитело, которое стимулирует передачу сигнала через 4-1ВВ (CD-137), например, PF-2566). В одном из вариантов осуществления сочетанную терапию вводят наряду с ингибитором тирозинкиназы (таким как акситиниб) и средством, направленным на рецептор 4-1BB.
Все упомянутые здесь публикации, заявки на патенты, патенты и другие ссылки включены в данное описание в качестве ссылки во всей их полноте.
Другие признаки, цели и преимущества настоящего изобретения будут очевидны из описания и чертежей, а также из формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1 показано графическое изображение экспрессии мРНК PD-L1 в клетках H3122 in vitro в присутствии и в отсутствии LDK378. Клетки H3122 представляют собой клетки немелкоклеточного рака легкого (НМРЛ) с транслокацией ALK.
КРАТКОЕ ОПИСАНИЕ ТАБЛИЦЫ 1
В таблице 1 приведены характеристики терапевтического средства LDK378, которое можно вводить в сочетании с иммуномодуляторами (например, в сочетании с одним или несколькими из: активатора костимуляторной молекулы и/или ингибитора молекулы иммунной контрольной точки), описанными в настоящем документе. В таблице 1 приведены слева направо после LDK378: название и/или обозначение второго терапевтического средства, структура соединения, патентная публикация, в которой раскрывается соединение, избранные показания и общая структура.
ние струк
туры
дия
US 8039479 - семейство в пункте 1; виды в пункте 5
Подсемейство формулы 2
R1 обозначает галоген;
R2 обозначает H;
R3 обозначает SO2R12, а R12 обозначает C1-6 алкил;
R4 обозначает H (n=1);
R6 обозначает изопропокси;
Один из R8 и R9 обозначает (CR2)qY, где q=0, Y обозначает пиперидинил, а другой обозначает C1-6 алкил
точного рака легкого
Терапия солидных опухолей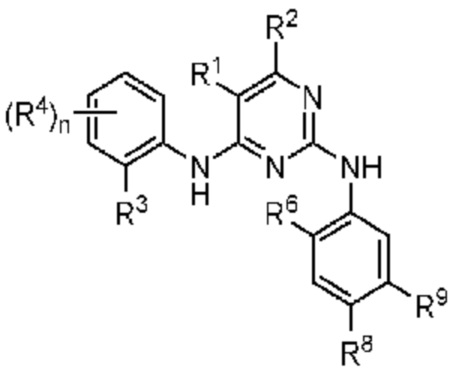
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретние предлагает способы и композиции, которые содержат иммуномодулятор (например, один или несколько из: активатора костимуляторной молекулы и/или ингибитора молекулы иммунной контрольной точки) в сочетания со вторым терапевтическим средством LDK378. В одном варианте осуществления ингибитор молекулы иммунной контрольной точки (например, один или несколько ингибиторов PD-1, PD-L1, LAG-3, TIM-3 или CTLA4) можно объединить со вторым терапевтическим средством LDK378. Описанные здесь сочетания могут оказывать благоприятный эффект, например, при лечении рака, такой как усиленный противораковый эффект, и могут обладать пониженной токсичностью и/или вызывать меньше побочных эффектов. Например, иммуномодулятор, второе терапевтическое средство, или тот и другой, можно вводить в более низкой дозе, чем доза, требуемая для достижения такого же терапевтического эффекта при монотерапии.
Термин "белок программируемой гибели 1", или "PD-1", включает в себя изоформы млекопитающих, например, человеческий PD-1, видовые гомологи человеческого PD-1 и их аналоги, содержащие, по меньшей мере, один общий эпитоп с PD-1. Аминокислотная последовательность PD-1, например, человеческого PD-1, известна в данной области и описана, например, в Shinohara T et al. (1994) Genomics 23(3):704-6; Finger LR, et al. Gene (1997) 197(1-2):177-87.
Термин "лиганд PD-1" или "PD-L1" включает в себя изоформы млекопитающих, например, человеческий PD-L1, видовые гомологи человеческого PD-L1 и их аналоги, содержащие, по меньшей мере, один общий эпитоп с PD-L1. Аминокислотная последовательность PD-L1, например, человеческого PD-L1, известна в данной области.
Термин "ген активации лимфоцитов 3" или "LAG-3" включает в себя изоформы млекопитающих, например, человеческий LAG-3, видовые гомологи человеческого LAG-3 и их аналоги, содержащие, по меньшей мере, один общий эпитоп с LAG-3. Аминокислотная и нуклеотидная последовательности LAG-3, например, человеческого LAG-3, известны в данной области и описаны, например, в Triebel et al. (1990) J. Exp. Med. 171: 1393-1405.
В данном описании термин "TIM-3" относится к трансмембранному рецепторному белку, который экспрессируется на клетках Th1 (Т-хелперы 1). TIM-3 участвует в регуляции иммунитета и толерантности in vivo (см. Hastings et al., Eur J Immunol. 2009 Sep;39(9):2492-501).
Термин "молекула клеточной адгезии, связанная с карциноэмбриональным антигеном", или "CEACAM", включает в себя всех членов семейства (например, CEACAM-1, CEACAM-3 или CEACAM-5), изоформы млекопитающих, например, человеческий CEACAM, видовые гомологи человеческого CEACAM и их аналоги, содержащие, по меньшей мере, один общий эпитоп с CEACAM. Аминокислотная последовательность CEACAM, например, человеческого CEACAM, известна в данной области и описана, например, в Hinoda et al. (1988) Proc. Natl. Acad. Sci. U.S.A. 85 (18), 6959-6963; Zimmermann W. et al. (1987) Proc. Natl. Acad. Sci. U.S.A. 84 (9), 2960-2964; Thompson J. et al. (1989) Biochem. Biophys. Res. Commun. 158 (3), 996-1004.
Другие термины определены ниже, а также по всему описанию заявки.
В данном описании грамматические объекты, используемые в единственном числе, также включают в себя применение указанных объектов во множественном числе.
Если контекст однозначно не указывает иное, термин "или" используют здесь для обозначения или вместо термина "и/или".
Термины "примерно" и "приблизительно", как правило, относятся к приемлемой степени погрешности измеряемой величины с учетом характера или точности измерений. Примерные степени погрешности находятся в пределах 20 процентов (%), как правило, в пределах 10%, чаще в пределах 5% от заданного значения или диапазона значений.
В композициях и способах настоящего изобретения используют полипептиды и нуклеиновые кислоты, имеющие указанные последовательности, или последовательности, по существу идентичные или подобные указанным последовательностям, например, последовательности, по меньшей мере, на 85%, 90%, 95% или более идентичные указанной последовательности. В контексте аминокислотной последовательности термин "по существу идентичный" используют здесь для обозначения первой аминокислотной последовательности, которая содержит достаточное или минимальное число аминокислотных остатков, которые в результате выравнивая последовательностей идентифицируют как i) идентичные аминокислотным остаткам второй аминокислотной последовательности, или ii) представляющие собой консервативные замены соответствующих аминокислотных остатков, то есть, где первая и вторая аминокислотные последовательности имеют общий структурный домен, и/или общую функциональную активность. Например, аминокислотные последовательности, которые содержат общий структурный домен, по меньшей мере, примерно на 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичны исходной последовательности, например, последовательности, описанной в данном документе.
В контексте нуклеотидной последовательности, термин "по существу идентичные" используется здесь для обозначения первой нуклеотидной последовательности, которая содержит достаточное или минимальное число нуклеотидов, которые в результате выравнивая последовательностей идентифицируют как идентичные соответствующим нуклеотидам второй нуклеотидной последовательности, то есть, где первая и вторая нуклеотидные последовательности кодируют полипептиды, обладающие общей функциональной активностью, или кодируют полипептиды, содержащие общий структурный домен, или обладающие общей функциональной полипептидной активностью. Например, данный термин может относится к нуклеотидным последовательностям, по меньшей мере, примерно на 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичным исходной последовательности, например, описанной здесь последовательности.
Термин "функциональный вариант" относится к полипептидам, которые являются по существу идентичными природной аминокислотной последовательности, или кодируются по существу идентичной нуклеотидной последовательностью, и которые обладают одной или несколькими активностями природной последовательности.
Расчеты гомологии или идентичности последовательностей (данные термины используются здесь как взаимозаменяемые) проводят следующим образом.
Чтобы определить процент идентичности двух аминокислотных последовательностей или двух нуклеотидных последовательностей, последовательности выравнивают с целью оптимального сравнения (например, можно ввести пробелы в одну или обе из первой и второй аминокислотных или нуклеотидных последовательностей с целью оптимального выравнивания, а негомологичными последовательностями можно пренебречь в целях сравнения). В предпочтительном варианте осуществления длина исследуемой последовательности, выравниваемой с целью сравнения, составляет, по меньшей мере 30%, предпочтительно, по меньшей мере 40%, более предпочтительно, по меньшей мере 50%, 60%, и еще более предпочтительно, по меньшей мере 70%, 80%, 90%, 100% от длины стандартной последовательности. Затем сравнивают аминокислотные остатки или нуклеотиды в соответствующих аминокислотных или нуклеотидных положениях. Если положение в первой последовательности занято тем же аминокислотным остатком или нуклеотидом, что и соответствующее положение во второй последовательности, то молекулы являются идентичными по данному положению (в данном описании термин "идентичность", используемый в применении к аминокислотным или нуклеотидным последовательностям, эквивалентен термину "гомологичность").
Процент идентичности двух последовательностей является функцией от числа идентичных положений в последовательностях и определяется с учетом числа пробелов и длины каждого пробела, который необходимо ввести для оптимального выравнивания двух последовательностей.
Сравнение последовательностей и определение процента идентичности двух последовательностей можно проводить с использованием математического алгоритма. В предпочтительном варианте осуществления процент идентичности двух аминокислотных последовательностей определяют с помощью алгоритма, описанного Needleman and Wunsch ((1970) J. Mol. Biol. 48:444-453), который включен в программу GAP пакета программного обеспечения GCG (который можно приобрести на http://www.gcg.com), используя матрицу Blossum 62 или матрицу РАМ250, штраф за открытие гэпа 16, 14, 12, 10, 8, 6 или 4, и штраф за продолжение гэпа 1, 2, 3, 4, 5 или 6. В следующем предпочтительном варианте осуществления процент идентичности двух нуклеотидных последовательностей определяют с помощью программы GAP, входящей в пакет программного обеспечения GCG (который можно приобрести на http://www.gcg.com), используя матрицу NWSgapdna.CMP, штраф за открытие гэпа 40, 50, 60, 70 или 80, и штраф за продолжение гэпа 1, 2, 3, 4, 5 или 6. Особенно предпочтительный набор параметров (который следует использовать, если не указано иначе) вклчает в себя матрицу замен Blossum 62, штраф за открытие гэпа 12, штраф за продолжение гэпа 4, и штраф за гэп со сдвигом рамки считывания 5.
Процент идентичности двух аминокислотных или нуклеотидных последовательностей можно определить с помощью алгоритма E. Meyers and W. Miller ((1989) CABIOS, 4:11-17), который включен в программу ALIGN (версия 2.0), используя таблицу весов замен остатков РАМ120, штраф за продление гэпа 12 и штраф за пропуск в последовательности 4.
Описанные здесь нуклеотидные и белковые последовательности можно использовать в качестве "запрашиваемой последовательности" для проведения поиска в общедоступных базах данных, например, с целью идентификации других членов семейства или родственных последовательностей. Такой поиск можно проводить с помощью программы NBLAST и XBLAST (версия 2.0), Altschul, et al. (1990) J. Mol. Biol. 215:403-10. Чтобы получить нуклеотидные последовательности, гомологичные молекулам нуклеиновых кислот данного изобретения, можно провести нуклеотидный поиск BLAST с использованием программы NBLAST, оценки=100, длины слова=12. Белковый поиск BLAST можно проводить с использованием программы XBLAST, оценки=50, длины слова=3, с получением аминокислотных последовательностей, гомологичных белковым молекулам настоящего изобретения. Для проведения выравнивания с введением гэпов в целях сравнения можно использовать Gapped BLAST, как описано в Altschul et al., (1997) Nucleic Acids Res. 25:3389-3402. При использовании программ BLAST и Gapped BLAST можно использовать параметры по умолчанию соответствующих программ (например, XBLAST и NBLAST). См. http://www.ncbi.nlm.nih.gov.
В данном описании термин "гибридизуется в условиях низкой жесткости, средней жесткости, высокой жесткости, или очень высокой жесткости" описывает условия гибридизации и промывания. Руководство по проведению реакций гибридизации можно найти в Current Protocols in Molecular Biology, John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6, включенном в настоящее описание в качестве ссылки. В данной ссылке описаны водные и неводные способы, любой из которых можно использовать. Конкретные условия гибридизации, в соответствии с данным описанием, включают в себя: 1) условия низкой жесткости, с использованием 6× хлорида натрия/цитрата натрия (SSC) примерно при 45°С, с последующими двумя промываниями 0,2×SSC, 0,1% SDS, по меньшей мере, при 50°C (температура промывания может быть увеличена до 55°C при использовании условий низкой жесткости); 2) условия средней жесткости, с использованием 6× SSC примерно при 45°С, с последующими одним или несколькими промываниями 0,2×SSC, 0,1% SDS при 60°С; 3) условия высокой жесткости, с использованием 6× SSC примерно при 45°С, с последующими одним или несколькими промываниями 0,2×SSC, 0,1% SDS, при 65°С; и, предпочтительно, 4) условия очень высокой жесткости, с использованием 0,5М фосфата натрия, 7% SDS, при 65°С, с последующими одним или несколькими промываниями 0,2×SSC, 0,1% SDS, при 65°С. Условия очень высокой жесткости (4) являются предпочтительными условиями, которые следует использовать, если не указано иначе.
Следует понимать, что молекулы настоящего изобретения могут содержать дополнительные консервативные замены, или замены на неэссенциальные аминокислоты, которые не оказывают существенного влияния на их функции.
Термин "аминокислота" охватывает все молекулы, как природные, так и синтетические, которые содержат одновременно функциональную аминогруппу и функциональную кислотную группу и могут входить в состав полимера из природных аминокислот. Примеры аминокислот включают в себя природные аминокислоты; аналоги, производные и родственные соединения; аналоги аминокислот, содержащие разные боковые цепи; а также все стереоизомеры вышеперечисленных соединений. В данном описании термин "аминокислота" включает в себя как D-, так и L-оптические изомеры и пептидомиметики.
Термин "консервативная аминокислотная замена" относится к замене аминокислотного остатка на аминокислотный остаток, имеющий сходную боковую цепь. В данной области аминокислотные остатки подразделяют на семейства, имеющие подобные боковые цепи. Указанные семейства включают в себя аминокислоты, содержащие основные боковые цепи (такие как лизин, аргинин, гистидин), кислотные боковые цепи (такие как аспарагиновая кислота, глутаминовая кислота), незаряженные полярные боковые цепи (такие как глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), неполярные боковые цепи (такие как аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленные боковые цепи (такие как треонин, валин, изолейцин) и ароматические боковые цепи (такие как тирозин, фенилаланин, триптофан, гистидин).
Термины "полипептид", "пептид" и "белок" (одноцепочечный) используются здесь как взаимозаменяемые и обозначают полимеры из аминокислот любой длины. Полимер может быть линейным или разветвленным, он может содержать модифицированные аминокислоты и вставки, отличные от аминокислот. Данные термины также охватывают модифицированные полимеры из аминокислот; модификации полимеров могут включать в себя, например, образование дисульфидной связи, гликозилирование, липидирование, ацетилирование, фосфорилирование, или любые другие манипуляции, такие как конъюгация с меченным компонентом. Полипептид можно выделить из природных источников, получить с помощью рекомбинантных методов в организме эукариотического или прокариотического хозяина, или его можно получить синтетическим путем.
Термины "нуклеиновая кислота", "последовательность нуклеиновой кислоты", "нуклеотидная последовательность" или "полинуклеотидная последовательность" и "полинуклеотид" используются как взаимозаменяемые. Они относятся к полимерной форме любой длины, состоящей из нуклеотидов, либо из дезоксирибонуклеотидов, либо из рибонуклеотидов, или из их аналогов. Полинуклеотид может быть одно- или двухцепочечным, и, если он является одноцепочечным, он может представлять собой кодирующую или некодирующую (антисмысловую) цепь. Полинуклеотид может содержать модифицированные нуклеотиды, такие как метилированные нуклеотиды, и аналоги нуклеотидов. Последовательность нуклеотидов может содержать вставки компонентов, отличных от нуклеотидов. Полинуклеотид можно дополнительно модифицировать после полимеризации, например, путем конъюгации с меченным компонентом. Нуклеиновая кислота может представлять собой рекомбинантный полинуклеотид, или полинуклеотид геномного происхождения, кДНК, полусинтетический или синтетический полинуклеотид, который либо не встречается в природе, либо связан с другим полинуклеотидом, с которым он не связан в естественных условиях.
Термин "выделенный" в данном описании относится к веществу, удаленному из исходного или природного окружения (например, из природной среды, если вещество является природным). Например, встречающийся в природе полинуклеотид или полипептид, присутствующий в организме живого животного, не является выделенным, но тот же самый полинуклеотид или полипептид, отделенный в результате вмешательства человека от некоторых или всех веществ, присутствующих вместе с ним в природной системе, является выделенным. Такие полинуклеотиды могут быть частью вектора, и/или такие полинуклеотиды или полипептиды могут быть частью композиции, и при этом они могут являться выделенными, поскольку такой вектор или такая композиция не являются частью среды, в которой полинуклеотиды или полипептиды присутствуют в природе.
Разные аспекты изобретения ниже описаны более подробно. Дополнительные определения приведены в тексте описания.
Молекулы антител
В одном варианте осуществления молекула антитела способна связываться с молекулой контрольной точки млекопитающего, например, человека, такой как PD-1, PD-L1, LAG-3 или TIM-3. Например, молекула антитела способна специфически связываться с эпитопом, например, с линейным или конформационным эпитопом (таким как описанный здесь эпитоп) на PD-1, PD-L1, LAG-3 или TIM-3.
В данном описании термин "молекула антитела" относится к белку, содержащему, по меньшей мере, одну последовательность вариабельного домена иммуноглобулина. Например, термин "молекула антитела" охватывает полноразмерные зрелые антитела и антиген-связывающие фрагменты антител. Например, молекула антитела может содержать последовательность вариабельного домена тяжелой (H) цепи (сокращенно обозначаемую здесь VH) и последовательность вариабельного домена легкой (L) цепи (сокращенно обозначаемую здесь VL). В другом примере молекула антитела содержит две последовательности вариабельного домена тяжелой (Н) цепи и две последовательности вариабельного домена легкой (L) цепи, образуя два антигенсвязывающих участка, и включает в себя Fab, Fab', F(аb')2, Fc, Fd, Fd', Fv, одноцепочечные антитела (например, ScFv), антитела, содержащие один переменный домен, диатела (Dab) (двухвалентные и биспецифические) и химерные (например, гуманизированные) антитела, которые можно получить путем модификации полноразмерного антитела, или синтезировать de novo с использованием технологий рекомбинантных ДНК. Указанные функциональные фрагменты антител сохраняют способность селективно связываться с соответствующим антигеном или рецептором. Антитела и фрагменты антител могут относится к любому классу антител, включающему в себя, без ограничения, IgG, IgA, IgM, IgD и IgE, и к любому подклассу (например, IgG1, IgG2, IgG3 и IgG4) антител. Антитела настоящего изобретения могут быть моноклональными или поликлональными. Антитело также может представлять собой человеческое, гуманизированное, CDR-привитое или полученное in vitro антитело. Антитело может содержать константный домен тяжелой цепи, выбранный, например, из константных доменов IgG1, IgG2, IgG3 или IgG4. Антитело может также содержать легкую цепь, выбранную, например, из легких цепей каппа или лямбда.
Примеры антигенсвязывающих фрагментов включают в себя: (i) фрагмент Fab, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) фрагмент F(аb')2, бивалентный фрагмент, содержащий два фрагмента Fab, связанных дисульфидным мостиком в шарнирном участке; (iii) фрагмент Fd, состоящий из доменов VH и CH1; (iv) фрагмент Fv, состоящий из доменов VL и VH одного плеча антитела, (v) фрагмент диатела (dAb), который состоит из домена VH; (vi) верблюжий или камелизированный вариабельный домен; (vii) одноцепочечный Fv (ScFv), см., например, Bird et al. (1988) Science 242:423-426; and Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883); (viii) однодоменное антитело. Указанные фрагменты антител можно получить с помощью традиционных методов, известных специалистам в данной области, и затем подвергнуть скринингу на полезные характеристики таким же способом, как и интактные антитела.
Термин "антитело" включает в себя интактные молекулы, а также их функциональные фрагменты. Константные домены антител можно модифицировать, например, путем введения мутации, с целью изменения свойств антитела (например, с целью увеличения или уменьшения одной или нескольких из следующих характеристик: способность связываться с рецептором Fc, гликозилирование антитела, число остатков цистеина, активность в отношении эффекторных клеток или активность в отношении комплемента).
Молекулы антитела также могут представлять собой однодоменные антитела. Однодоменные антитела могут включать в себя антитела, гипервариабельные участки которых являются частью однодоменного полипептида. Примеры включают в себя, без ограничения, антитела, состоящие только из тяжелых цепей, антитела, естественным образом лишенные легких цепей, однодоменные антитела, полученные из обычных 4-цепочечных антител, рекомбинантные антитела и однодоменные каркасы, отличные от каркасов, полученных из антител. Однодоменные антитела могут представлять собой любые однодоменные антитела, известные в данной области, или любые однодоменные антитела, которые могут быть получены в будущем. Однодоменные антитела можно получить из любых видов, включающих в себя, без ограничения, мышь, человека, верблюда, ламу, рыбу, акулу, козу, кролика и крупный рогатый скот. В соответствии с другим аспектом изобретения однодоменное антитело представляет собой природное однодоменное антитело, известное как антитело из тяжелых цепей, лишенное легких цепей. Такие однодоменные антитела описаны, например, в WO 9404678. Для ясности, указанный вариабельный домен, полученный из тяжелоцепочечного антитела, естественным образом лишенного легких цепей, называют здесь VHH или нанотело, в отличие от традиционного VH четырехцепочечного иммуноглобулина. Такую молекулу VHH можно получить из антител, образовавшихся в организме видов Camelidae, таких как верблюд, лама, одногорбый верблюд, альпака и гуанако. Тяжелоцепочечные антитела, естественным образом лишенные легких цепей, могут продуцировать и другие виды, помимо Camelidae; такие VHH входят в объем настоящего изобретения.
Домены VH и VL содержат участки гипервариабельности, называемые "участки, определяющие комплементарность" (CDR), которые чередуются с более консервативными участками, называемыми "каркасные участки" (FR или FW).
Границы каркасных участков и CDR точно определены с помощью ряда методов (см. Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242; Chothia, C. et al. (1987) J. Mol. Biol. 196:901-917; и определение AbM, используемое в программном обеспечении Oxford Molecular's AbM antibody modeling. Общую информацию можно найти, например, в Protein Sequence and Structure Analysis of Antibody Variable Domains. In: Antibody Engineering Lab Manual (Ed.: Duebel, S. and Kontermann, R., Springer-Verlag, Heidelberg).
Термины "участок, определяющий комплементарность" и "CDR" в данном описании относятся к последовательностям аминокислот в вариабельных участках антитела, которые отвечают за антигенную специфичность и аффинность связывания. Как правило, каждый вариабельный домен тяжелой цепи содержит три CDR (HCDR1, HCDR2, HCDR3) и каждый вариабельный домен легкой цепи содержит три CDR (LCDR1, LCDR2, LCDR3).
Точные границы аминокислотной последовательности конкретного CDR можно определить с помощью одной из ряда хорошо известных систем, включающих в себя системы, описанные Kabat et al. (1991), "Sequences of Proteins of Immunological Interest," 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (система нумерации "Kabat"), Al-Lazikani et al., (1997) JMB 273,927-948 (система нумерации "Chothia"). В данном описании CDR, определенные по системе нумерации "Chothia" также иногда называют "гипервариабельные петли".
Например, в соответствии с системой Kabat аминокислотные остатки CDR вариабельного домена тяжелой цепи (VH) нумеруют как 31-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3); а аминокислотные остатки CDR вариабельного домена легкой цепи (VL) нумеруют как 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3). В соответствии с системой Chothia аминокислоты CDR в ВХ нумеруют как 26-32 (HCDR1), 52-56 (HCDR2) и 95-102 (HCDR3); а аминокислотные остатки в VL нумеруют как 26-32 (LCDRl), 50-52 (LCDR2) и 91-96 (LCDR3). В соответствии с объединенным определением Kabat и Chothia CDR включают в себя аминокислотные остатки 26-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3) человеческого VH и аминокислотные остатки 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3) человеческого VL.
В настоящем описании термин "последовательность вариабельного домена иммуноглобулина" относится к аминокислотной последовательности, которая может образовывать структуру вариабельного домена иммуноглобулина. Например, последовательность может содержать всю аминокислотную последовательность природного вариабельного домена, или ее часть. Например, последовательность может содержать или не содержать одну, две или более N- или С-концевых аминокислот, или она может содержать другие изменения, совместимые с образованием структуры белка.
Термин "антиген-связывающий участок" относится к части молекулы антитела, которая содержит детерминанты, образующие поверхность, способную связываться с полипептидом PD-1, или его эпитопом. Что касается белков (или белковых миметиков), антиген-связывающий участок, как правило, содержит одну или несколько петель (состоящих, по меньшей мере, из четырех аминокислот или миметиков аминокислот), которые образуют поверхность, способную связываться с полипептидом PD-1. Как правило, антиген-связывающий участок молекулы антитела содержит, по меньшей мере, один или два CDR, и/или одну или дву гипервариабельные петли, или, чаще, по меньшей мере, три, четыре, пять или шесть CDR и/или гипервариабельных петель.
Термины "моноклональное антитело" или "композиция моноклонального антитела" в контексте настоящего описания относятся к препарату молекул антител, содержащему молекулы одного вида. Композиция моноклонального антитела обладает одной специфичностью связывания и сродством к конкретному эпитопу. Моноклональное антитело можно получить с использованием гибридомной технологии, или с помощью методов, в которых не используется гибридомная технология (например, с помощью рекомбинантных методов).
"Эффективно человеческий" белок представляет собой белок, который не вызывает ответ, опосредованный нейтрализующими антителами, например, ответ, опосредованный человеческими антителами против мышиных антител (HAMA). HAMA может представлять собой проблему в ряде случаев, например, если молекулу антитела вводят многократно, например, при лечении хронического или рецидивирующего болезненного состояния. Ответ HAMA может сделать повторное введение антитела потенциально неэффективным вследствие повышенного выведения антител из сыворотки (см., например, Saleh et al., Cancer Immunol. Immunother., 32:180-190 (1990)), а также вследствие возможных аллергических реакций (см., например, LoBuglio et al., Hybridoma, 5: 5117-5123 (1986)).
Молекула антитела может представлять собой поликлональное или моноклональное антитело. В других вариантах осуществления изобретения антитело может быть получено рекомбинантным способом, например, с использованием фагового дисплея или с помощью комбинаторных методов.
Способы получения антител с использованием фаговых дисплеев и с помощью комбинаторных методов известны в данной области (и описаны, например, в Ladner et al., патент США N 5223409; Kang et al. международная публикация № WO 92/18619; Dower et al. международная публикация № WO 91/17271; Winter et al. международная публикация WO 92/20791; Markland et al. международная публикация № WO 92/15679; Breitling et al. международная публикация WO 93/01288; McCafferty et al. международная публикация WO 92/01047; Garrard et al. международная публикация № WO 92/09690; Ladner et al. международная публикация № WO 90/02809; Fuchs et al. (1991) Bio/Technology 9:1370-1372; Hay et al. (1992) Hum Antibod Hybridomas 3:81-85; Huse et al. (1989) Science 246:1275-1281; Griffths et al. (1993) EMBO J 12:725-734; Hawkins et al. (1992) J Mol Biol 226:889-896; Clackson et al. (1991) Nature 352:624-628; Gram et al. (1992) PNAS 89:3576-3580; Garrad et al. (1991) Bio/Technology 9:1373-1377; Hoogenboom et al. (1991) Nuc Acid Res 19:4133-4137; and Barbas et al. (1991) PNAS 88:7978-7982, содержание которых включено в настоящее описание в качестве ссылки).
В одном варианте осуществления изобретения антитело представляет собой полностью человеческое антитело (например, антитело, полученное в организме рекомбинантной мыши, продуцирующей антитело с последовательностью человеческого иммуноглобулина), или нечеловеческое антитело, например, антитело грызуна (мыши или крысы), козы, примата (например, обезьяны), верблюда. Предпочтительно нечеловеческое антитело представляет собой антитело грызуа (мышиное или крысиное антитело). Способы получения антител грызунов известны в данной области.
Человеческие моноклональные антитела можно получить с использованием трансгенных мышей, несущих гены человеческих иммуноглобулинов вместо мышиных. Спленоциты указанных трансгенных мышей, иммунизированных представляющим интерес антигеном, используют для получения гибридом, секретирующих человеческие mAb, обладающие специфическим сродством к эпитопам человеческого белка (см., например, Wood et al. международная заявка WO 91/00906, Kucherlapati et al. публикация РСТ WO 91/10741; Lonberg et al. международная заявка WO 92/03918; Kay et al. международная заявка 92/03917; Lonberg, N. et al. 1994 Nature 368: 856-859; Green, L.L. et al. 1994 Nature Genet. 7:13-21; Morrison, S.L. et al. 1994 Proc. Natl. Acad. Sci. USA 81:6851-6855; Bruggeman et al. 1993 Year Immunol 7:33-40; Tuaillon et al. 1993 PNAS 90:3720-3724; Bruggeman et al. 1991 Eur J Immunol 21:1323-1326).
Антитело может представлять собой антитело, вариабельный участок которого, или его фрагмент, например, CDR, получен в организме отличного от человека животного, такого как крыса или мышь. Химерные, CDR-привитые и гуманизированные антитела входят в объем настоящего изобретения. Антитела, полученные в организме отличного от человека животного, такого как крыса или мышь, и затем модифицированные, например, по каркасному участку вариабельного домена, или по константному домену, с целью уменьшения антигенности в организме человека, входят в объем настоящего изобретения.
Химерные антитела можно получить с помощью методов рекомбинантных ДНК, известных в данной области (см. Robinson et al., международная патентная публикация PCT/US86/02269; Akira, et al., европейская патентная заявка 184187; Taniguchi, M., европейская патентная заявка 171496; Morrison et al., европейская патентная заявка 173494; Neuberger et al., международная заявка WO 86/01533; Cabilly et al. патент США № 4816567; Cabilly et al., европейская патентная заявка 125023; Better et al. (1988 Science 240:1041-1043); Liu et al. (1987) PNAS 84:3439-3443; Liu et al., 1987, J. Immunol. 139:3521-3526; Sun et al. (1987) PNAS 84:214-218; Nishimura et al., 1987, Canc. Res. 47:999-1005; Wood et al. (1985) Nature 314:446-449; and Shaw et al., 1988, J. Natl Cancer Inst. 80:1553-1559).
В гуманизированном или CDR-привитом антителе, по меньшей мере, один или два, но чаще все три реципиентые CDR, (тяжелой и/или легкой цепей иммуноглобулина) заменены на донорные CDR. CDR антитела могут быть заменены, по меньшей мере, частично, на нечеловеческие CDR, или только некоторые из CDR могут быть заменены нечеловеческими CDR. Нужно заменить такое число CDR, которое необходимо для связывания гуманизированного антитела с PD-1. Предпочтительно донорное антитело представляет собой антитело грызуна, например, антитело крысы или мыши, а реципиентом является человеческий каркасный участок, или консенсусный человеческий каркасный участок. Как правило, иммуноглобулин, предоставляющий CDR, называют "донор", а иммуноглобулин, предоставляющий каркасный участок, называют "акцептор". В одном варианте осуществления донорный иммуноглобулин представляет собой нечеловеческий иммуноглобулин (например, иммуноглобулин грызуна). Акцепторный каркасный участок представляет собой природный (например, человеческий) каркасный участок, или консенсусный каркасный участок, или последовательность, идентичную ему примерно на 85% или более, предпочтительно на 90%, 95%, 99% или более.
Используемый в данном описании термин "консенсусная последовательность" относится к последовательности, образованной из аминокислот (или нуклеотидов), наиболее часто встречающихся в семействе родственных последовательностей (см., например, Winnaker, From Genes to Clones (Verlagsgesellschaft, Weinheim, Germany 1987). Каждое положение консенсусной последовательности занимает аминокислота, встречающаяся наиболее часто в этом положении в семействе белков. Если две аминокислоты встречаются одинаково часто, в консенсусную последовательность может быть включена любая из них. Термин "консенсусный каркасный участок" относится к каркасному участку консенсусной последовательности иммуноглобулина.
Антитело можно гуманизировать с помощью способов, известных в данной области (см., например, Morrison, S. L., 1985, Science 229:1202-1207, Oi et al., 1986, BioTechniques 4:214, и Queen et al. US 5585089, US 5693761 и US 5693762, содержание которых включено в данное описание в качестве ссылки).
Гуманизированные или CDR-привитые антитела можно получить путем CDR-прививания или замещения CDR, при этом могут быть заменены один, два или все CDR цепи иммуноглобулина. См., например, патент США 5225539; Jones et al. 1986 Nature 321:552-525; Verhoeyan et al. 1988 Science 239:1534; Beidler et al. 1988 J. Immunol. 141:4053-4060; Winter US 5225539, содержание которых специально включено в данное описание в качестве ссылки. Winter описывает метод CDR-прививания, который можно использовать для получения гуманизированных антител настоящего изобретения (патентная заявка Великобритании GB 2188638A, поданная 26 марта 1987; Winter US 5225539), содержание которых включено в данное описание в качестве ссылки.
Настоящее изобретение также охватывает гуманизированные антитела, полученные путем замещения, удаления или добавления конкретных аминокислот. Критерии выбора аминокислот из донорного антитела описаны в US 5585089, например, в разделах 12-16 US 5585089, содержание которого включено в данное описание в качестве ссылки. Другие методы гуманизации антител описаны в Padlan et al. EP 519596 A1, опубликованном 23 декабря 1992 года.
Молекула антитела может представлять собой одноцепочечное антитело. Одноцепочечное антитело (ScFv) можно получить рекомбинантными методами (см., например, Colcher, D. et al. (1999) Ann N Y Acad Sci 880:263-80; и Reiter, Y. (1996) Clin Cancer Res 2:245-52). Одноцепочечное антитело можно подвергнуть димеризации или мультимеризации с получением поливалентных антител, обладающих специфичностью в отношении разных эпитопов одного и того же белка-мишени.
В следующих вариантах осуществления молекула антитела содержит константный участок тяжелой цепи, выбранный, например, из константных участков тяжелых цепей IgG1, IgG2, IgG3, IgG4, IgM, Iga1, IgA2, IgD и IgE; предпочтительно, из константных участков тяжелых цепей (например, человеческих) IgGl, IgG2, IgG3 и IgG4. В другом варианте осуществления молекула антитела содержит константный участок легкой цепи, выбранный, например, из константных участков легкой цепи каппа или лямбда (например, человеческих). Константный участок можно изменить, например, в него можно вести мутацию, с целью изменения свойств антитела (например, с целью увеличения или уменьшения одной или нескольких из следующих характеристик: способность связываться с рецептором Fc, гликозилирование антитела, число остатков цистеина, активность в отношении эффекторных клеток, и/или активность в отношении комплемента). В одном варианте осуществления антитело обладает: эффекторной функцией; и способностью фиксировать комплемент. В других вариантах осуществления антитело не обладает способностью мобилизовать эффекторные клетки; или фиксировать комплемент. В другом варианте осуществления антитело обладает пониженной способностью к связыванию с рецептором Fc, или не обладает такой способностью. Например, антитело может представлять собой антитело определенного изотипа или подтипа, фрагмент или другой мутант, который не сохраняет способность связываться с рецептором Fc, например, в результате мутации или делеции участка, связывающего рецептор Fc.
Способы изменения константного участка антитела известны в данной области. Антитела с измененной функцией, например, с измененным сродством к эффекторному лиганду, такому как FcR на поверхности клетки или компонент C1 комплемента, можно получить путем замены, по меньшей мере, одного аминокислотного остатка в константном участке антитела на другой остаток (см., например, EP 388151 A1, патент США № 5624821 и патент США № 5648260, содержание которых включено в данное описание в качестве ссылки). Можно описать изменения подобного типа, которые у мышиных иммуноглобулинов, или у иммуноглобулинов других видов приводят к уменьшению или устранению способности выполнять эффекторные функции.
Молекулу антитела можно дериватизировать или присоединить к другой функциональной молекуле (такой как другой пептид или белок). В данном описании термин "дериватизированная" молекула антитела относится к модифицированной молекуле антитела. Методы дериватизации включают в себя, без ограничения, присоединение флуоресцентного фрагмента, радионуклеотида, токсина, фермента или аффинного лиганда, такого как биотин. Соответственно, предполагается, что молекулы антител настоящего изобретения включают в себя дериватизированные и иным образом модифицированные формы антител, описанных в настоящем документе, в том числе молекулы иммуноадгезии. Например, молекула антитела может быть функционально связана (путем химического присоединения, генетической гибридизации, нековалентной ассоциации или иным образом) с одним или несколькими другими молекулярными объектами, такими как другое антитело (например, биспецифическое антитело или диатело), детектируемое средство, цитотоксическое средство, фармацевтическое средство, и/или белок или пептид, который может опосредовать связь антитела или фрагмента антитела с другой молекулой (такой как активный центр стрептавидина или полигистидиновый маркер).
Один тип дериватизированной молекулы антитела получают путем сшивания двух или более антител (одного и того же типа, или разных типов, например, с получением биспецифических антител). Подходящие сшивающие средства включают в себя гетеробифункциональные средства, содержащие две разные реакционноспособные группы, разделенные подходящим спейсером (такие как м-малеимидобензоил-N-гидроксисукцинимид), или гомобифункциональные средства (такие как дисукцинимидилсуберат). Такие линкеры можно приобрести у Pierce Chemical Company, Rockford, Ill.
Молекулы антител можно конъюгировать с другим молекулярным объектом, обычно представляющим собой метку или терапевтическое (например, цитотоксическое или цитостатическое) средство, или его фрагмент. Радиоактивные изотопы можно использовать в диагностических или терапевтических целях. Радиоактивные изотопы, которые можно присоединить к антителам против PSMA, включают в себя, без ограничения, α-, β- или γ-излучатели, или β- и γ-излучатели. Такие радиоактивные изотопы включают в себя, без ограничения, иод (131I или 125I), иттрий (90Y), лютеций (177Lu), актиний (225Ac), празеодим, астат (211At), рений (186Re), висмут (212Bi или 213Bi), индий (111In), технеций (99mTc), фосфор (32P), родий (188Rh), серу (35S), углерод (14C), тритий (3Н), хром (51Cr), хлор (36С1), кобальт (57Co или 58Co), железо (59Fe), селен (75Se) или галлий (67Ga). Радиоизотопы, используемые в качестве терапевтических средств, включают в себя иттрий (90Y), лютеций (177Lu), актиний (225Ac), празеодим, астат (211At), рений (186Re), висмут (212Bi или 213Bi) и родий (188Rh). Радиоизотопы, используемые в качестве меток, например, для применения в диагностике, включают в себя иод (131I или 125I), индий (111In), технеций (99mTc), фосфор (32P), углерод (14С) и тритий (3Н), или один или несколько из перечисленных выше терапевтических изотопов.
Изобретение предлагает радиоактивно меченные молекулы антител и способы их мечения. В одном варианте осуществления изобретение предлагает способ мечения молекулы антитела. Способ включает в себя приведение молекулы антитела в контакт с хелатирующим средством с получением конъюгированного антитела. Конъюгированное антитело метят радиоактивным изотопом, таким как 111индий, 90иттрий и 177лютеций, с получением меченой молекулы антитела.
Как указано выше, молекула антитела может быть конъюгирована с терапевтическим средством. Терапевтически активные радиоизотопы описаны выше. Примеры других терапевтических средств включают в себя таксол, цитохалазин, грамицидин D, бромид этидия, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаина, лидокаин, пропранолол, пуромицин, мейтансиноиды, такие как майтанзинол (см. патент США 5208020), CC-1065 (см. патенты США №№ 5475092, 5585499, 5846545), а также их аналоги или гомологи. Терапевтические средства включают в себя, без ограничения, антиметаболиты (такие как метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацилдекарбазин), алкилирующие средства (такие как мехлорэтамин, тиотепа хлорамбуцил, CC-1065, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклотосфамид, бусульфан, дибромманнит, стрептозотоцинов, митомицин С и цис- дихлордиамин платина(II) (DDP), цисплатин), антрациклины (такие как даунорубицин (ранее называемый дауномицин) и доксорубицин), антибиотики (такие как дактиномицин (ранее называемый актиномицин), блеомицин, митрамицин и антрамицин (АМС)), и антимитотические средства (такие как винкристин, винбластин, таксол и майтансиноиды).
Фармацевтические композиции и наборы
В другом аспекте настоящее изобретение предлагает композиции, например, фармацевтически приемлемые композиции, которые содержат описанную здесь молекулу антитела в сочетании с фармацевтически приемлемым носителем. В данном описании термин "фармацевтически приемлемый носитель" включает в себя любой и все физиологически совместимые растворители, диспергирующие среды, изотонические средства, средства, замедляющие абсорбцию, и т.п. Носитель может быть подходящим для внутривенного, внутримышечного, подкожного, парентерального, ректального, спинального или эпидермального введения (например, путем инъекции или инфузии).
Композиции настоящего изобретения могут находиться в виде разных форм. Указанные формы включают в себя, например, жидкие, полутвердые и твердые лекарственные формы, такие как жидкие растворы (например, растворы для инъекций и инфузий), дисперсии или суспензии, липосомы и суппозитории. Предпочтительная форма зависит от предполагаемого способа введения и терапевтического применения. Примерами предпочтительных композиций являются растворы для инъекций или инфузий. Предпочтительным способом введения является парентеральное (например, внутривенное, подкожное, внутрибрюшинное, внутримышечное) введение. В предпочтительном варианте осуществления антитело вводят путем внутривенной инфузии или инъекции. В другом предпочтительном варианте осуществления антитело вводят путем внутримышечной или подкожной инъекции.
Фразы "парентеральное введение" и "вводят парентерально", в соответствии с данным описанием, относятся к способам введения, обычно путем инъекции, отличным от энтерального и местного введения, и включают в себя, без ограничения, внутривенные, внутримышечные, внутриартериальные, интратекальные, интракапсулярные, интраорбитальные, внутрисердечные, внутрикожные, внутрибрюшинные, транстрахеальные, подкожные, подэпидермисные, внутрисуставные, субкапсулярные, субарахноидальные, интраспинальные, эпидуральные и внутригрудинные инъекции и инфузии.
Как правило, терапевтические композиции должны быть стерильными и стабильными в условиях производства и хранения. Композиция может находиться в виде раствора, микроэмульсии, дисперсии, липосомы или другой упорядоченной структуры, подходящей для введения антителв в высокой концентрации. Стерильные растворы для инъекций можно получить путем введения активного соединения (такого как антитело или фрагмент антитела) в требуемом количестве в соответствующий растворитель в сочетании с одним или несколькими из перечисленных выше ингредиентов, по необходимости, с последующей стерилизацией фильтрованием. Дисперсии обычно получают путем введения активного соединения в стерильный носитель, который содержит основную диспергирующую среду и другие необходимые ингредиенты из перечисленных выше. Предпочтительные способы получения стерильных порошков для приготовления стерильных растворов для инъекций включают в себя вакуумную сушку и сушку из замороженного состояния, которые позволяют получить порошок активного ингредиента в сочетании с любым другим желательным ингредиентом из раствора, предварительно стерилизованного фильтрованием. Подходящую текучесть раствора можно поддерживать, например, путем применения покрытия, такого как лецитин, частиц требуемого размера в случае дисперсии и поверхностно-активных веществ. Пролонгированную абсорбцию инъекционных композиций можно достичь путем включения в композицию средств, замедляющих абсорбцию, таких как моностеараты и желатин.
Молекулы антител можно вводить разными способами, известными в данной области, хотя для многих терапевтических применений, предпочтительным путем/способом введения является внутривенная инъекция или инфузия. Например, молекулы антитела можно вводить путем внутривенной инфузии со скоростью менее 10 мг/мин; предпочтительно со скоростью, меньшей или равной 5 мг/мин, до достижения дозы примерно от 1 до 100 мг/м2, предпочтительно примерно от 5 до 50 мг/м2, примерно от 7 до 25 мг/м2, и более предпочтительно примерно от 10 мг/м2. Для специалиста в данной области должно быть очевидно, что путь и/или способ введения может варьировать в зависимости от желаемых результатов. В некоторых вариантах осуществления активное соединение может находиться в сочетании с носителем, защищающим соединение от быстрого высвобождения, например, в составе композиции с контролируемым высвобождением, включающей в себя имплантаты, трансдермальные пластыри и микроинкапсулированные системы доставки. Можно использовать биоразрушаемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие способы получения таких композиций запатентованы или хорошо известны специалистам в данной области техники. См., например, Sustained and Controlled Release Drug Delivery Systems, J. R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
В некоторых вариантах осуществления молекулу антитела можно вводить перорально, например, с использованием инертного разбавителя или усваиваемого пищевого носителя. Соединение (и другие ингредиенты, по необходимости) также можно заключить в капсулу с твердой или мягкой желатиновой оболочкой, прессовать в таблетки, или включить непосредственно в пищу индивидуума. Соединения, предназначенные для перорального терапевтического введения, наряду со вспомогательными веществами, могут находиться в виде таблеток для приема внутрь, щечных таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, вафель и т.п. Для введения соединения настоящего изобретения способом, отличным от парентерального введения, может потребоваться нанесение покрыния на соединение, или совместное введение соединения с веществом, предотвращающим его инактивацию. Терапевтические композиции также можно вводить с помощью медицинских устройств, известных в данной области техники.
Режимы введения лекарственных средств корректируют, чтобы достичь оптимальный желательный ответ (например, терапевтический ответ). Например, можно ввести один болюс, можно ввести несколько разделенных доз в течение определенного периода времени, или дозу можно пропорционально уменьшить или увеличить, в зависимости от терапевтической ситуации. Особенно предпочтительные парентеральные композиции получают в виде стандартных лекарственных форм, обеспечивающих простоту введения и однородность дозирования. Термин "стандартная лекарственная форма" в данном описании относится к физически дискретным единицам, подходящим для введения в качестве единичных доз индивидуумам, подлежащим лечению; причем каждая единица содержит предварительно определенное количество активного соединения, рассчитанное для достижения желательного терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем. Характеристики стандартных лекарственных форм настоящего изобретения определяются и непосредственно зависит от (a) уникальных характеристик активного соединения и конкретного терапевтического эффекта, который предполагается достичь, и (b) ограничений, существующих в области компаундирования таких активных соединений для лечения чувствительности у индивидуумов.
Термин "терапевтически эффективное количество" относится к количеству, эффективному в необходимых дозах и в течение необходимых периодов времени для достижения желательного терапевтического результата. Терапевтически эффективное количество модифицированного антитела или фрагмента антитела может варьировать в зависимости от таких факторов, как состояние болезни, возраст, пол и масса индивидуума, а также способность антитела или фрагмента антитела вызывать желательный ответ у индивидуума. Терапевтически эффективное количество также представляет собой количество, при котором терапевтически благоприятные эффекты преобладают над токсическими или вредными эффектами модифицированного антитела или фрагмента антитела. "Терапевтически эффективная доза" предпочтительно ингибирует измеримый параметр, например, скорость роста опухоли, по меньшей мере, примерно на 20%, более предпочтительно, по меньшей мере, примерно на 40%, еще более предпочтительно, по меньшей мере, примерно на 60%, и еще более предпочтительно, по меньшей мере, примерно на 80% по сравнению с индивидуумами, не получающими лекарственное средство. Способность соединения ингибировать измеряемый параметр, например, рак, можно оценить на животной модели, позволяющей прогнозировать эффективность в отношении опухолей человека. Альтернативно данное свойство композиции можно оценить путем определения способности соединения к ингибированию in vitro с помощью анализов, известных специалистам в данной области.
Термин "профилактически эффективное количество" относится к количеству, эффективному в необходимых дозах и в течение необходимых периодов времени для достижения желательного профилактического результата. Поскольку профилактическую дозу используют у индивидуумов до появления заболевания, или на ранней стадии заболевания, профилактически эффективное количество, как правило, является меньше, чем терапевтически эффективное количество.
Способы введения молекул антител известны в данной области и описаны ниже. Подходящие используемые дозы молекул зависят от возраста и массы индивидуума и конкретного используемого лекарственного средства. Дозы и режимы введения молекул антител против PD-1 может определить специалист в данной области. В некоторых вариантах осуществления молекулу антитела против PD-1 вводят путем инъекции (например, подкожно или внутривенно) в дозе примерно от 1 до 30 мг/кг, например, примерно от 5 до 25 мг/кг, примерно от 10 до 20 мг/кг, примерно от 1 до 5 мг/кг, или примерно 3 мг/кг. Режим дозирования может варьировать, например, от одного раза в неделю до одного раза в 2, 3 или 4 недели. В одном варианте осуществления молекулу антитела против PD-1 вводят в дозе примерно от 10 до 20 мг/кг каждые две недели.
Иллюстративный, не ограничивающий диапазон терапевтически или профилактически эффективного количества молекулы антитела составляет 0,1-30 мг/кг, более предпочтительно 1-25 мг/кг. Дозы и режимы введения молекулы антитела против PD-1 может определить специалист в данной области. В некоторых вариантах осуществления молекулу антитела против PD-1 вводят путем инъекции (например, подкожно или внутривенно) в дозе примерно от 1 до 30 мг/кг, например, примерно от 5 до 25 мг/кг, примерно от 10 до 20 мг/кг, примерно от 1 до 5 мг/кг, от 1 до 10 мг/кг, от 5 до 15 мг/кг, от 10 до 20 мг/кг, от 15 до 25 мг/кг, или примерно 3 мг/кг. Режим дозирования может варьировать, например, от одного раза в неделю до одного раза в 2, 3 или 4 недели. В одном варианте осуществления молекулу антитела против PD-1 вводят в дозе примерно от 10 до 20 мг/кг каждые две недели. Молекулу антитела можно вводить путем внутривенной инфузии со скоростью менее 10 мг/мин, предпочтительно со скоростью, меньшей или равной 5 мг/мин, с достижением дозы, составляющей примерно от 1 до 100 мг/м2, предпочтительно примерно от 5 до 50 мг/м2, примерно от 7 до 25 мг/м2, и более предпочтительно, примерно 10 мг/м2. Следует отметить, что величина дозы может варьировать в зависимости от типа и тяжести состояния, подлежащего лечению. Следует также понимать, что для любого конкретного индивидуума режим введения лекарственного средства нужно корректировать с течением времени в соответствии с индивидуальными требованиями и профессиональной оценкой лица, назначающего введение, или наблюдающего за введением композиций, и что диапазоны доз, указанные в данном описании, являются только иллюстративными и не предназначены для ограничения объема или применения заявленной композиции.
Молекулы антител можно использовать отдельно или в сочетании со вторым средством, таким как цитотоксическое лекарственное средство, радиоизотоп, или белок, например, белковый токсин, или вирусный белок. Данный способ включает в себя: введение молекулы антитела, самой по себе, или конъюгированной с цитотоксическим средством, индивидууму, нуждающемуся в таком лечении. Молекулы антител можно использовать для доставки разных терапевтических средств, таких как цитотоксический фрагмент, например, терапевтическое средство, радиоактивный изотоп, молекулы растительного, грибкового или бактериального происхождения, или биологические белки (такие как белковые токсины) или частицы (например, рекомбинантные вирусные частицы, например, с белком вирусной оболочки), или их смеси.
Кроме того, в объем изобретения входит набор, содержащий описанное здесь сочетание терапевтических средств. Набор может содержать один или несколько других элементов, включающих в себя: инструкции по применению; другие реагенты, такие как метка, терапевтическое средство или средство, используемое для хелатирования или присоединения иным способом антитела к метке, или терапевтическому средству, или радиопротекторной композиции; устройства или другие вещества для получения антитела, предназначенного для введения; фармацевтически приемлемые носители; а также устройства или другие вещества для введения индивидууму.
Применение сочетанных способов лечения
Описанные здесь сочетанные способы лечения можно использовать в терапевтических и профилактических целях in vitro и in vivo. Например, указанные молекулы можно вводить в культивируемые клетки in vitro или ex vivo, или в организм индивидуума, например, человека, с целью лечения, профилактики и/или диагностики разных заболеваний, таких как рак.
Соответственно, в одном аспекте изобретение предлагает способ модификации иммунного ответа у индивидуума, включающий в себя введение индивидууму описанной здесь молекулы антитела, приводящее к изменению иммунного ответа у индивидуума. В одном варианте осуществления иммунный ответ усиливается, стимулируется или подвергается повышающей регуляции. В одном варианте осуществления молекулы антитела усиливают иммунный ответа у индивидуума путем блокады ингибитора контрольной точки (такой как PD-1, PD-L1, LAG-3 или TIM-3).
В данном описании термин "индивидуум" включает в себя человека и отличных от человека животных. В одном варианте осуществления индивидуум представляет собой человека, например, человека-пациента, страдающего от расстройства или состояния, характеризующегося аномальным функционированием иммунной системы. Термин "отличные от человека животные" включает в себя млекопитающих и не млекопитающих, например, отличных от человека приматов. В одном из вариантов осуществления индивидуум представляет собой человека. В одном варианте осуществления индивидуум представляет собой человека-пациента, нуждающегося в усилении иммунного ответа. В одном варианте осуществления индивидуум имеет ослабленную иммунную систему, например, индивидуум подвергается, или подвергался химиотерапии или лучевой терапии. Альтернативно, или в добавление к вышесказанному, индивидуум страдает от ослабления иммунной системы, или подвергается риску ослабления иммунной системы в результате инфекции. Описанные здесь способы и композиции можно использовать для лечения пациентов-людей, страдающих от расстройства, которое можно лечить путем усиления иммунного ответа, опосредованного Т-клетками. Например, описанные здесь способы и композиции могут способствовать повышению активности ряда иммунных компонентов. В одном варианте осуществления у индивидуума повышается число или активность проникающих в опухоль Т-лимфоцитов (TIL). В другом варианте осуществления у индивидуума повышается экспрессия или активность интерферона-гамма (IFN-γ). В следующем варианте осуществления у индивидуума наблюдается пониженная экспрессия или активность PD-L1.
Рак
Блокада ингибиторов контрольной точки, например, PD-1, может приводить к усилению иммунного ответа на раковые клетки у индивидуума. PD-L1, лиганд PD-1, не экспрессируется в нормальных клетках человека, но в изобилии присутствует в ряде раковых опухолей человека (Dong et al. (2002) Nat Med 8:787-9). Взаимодействие между PD-1 и PD-L1 может привести к уменьшению лимфоцитов, проникающих в опухоль, снижению опосредованной рецептором пролиферации Т-клеток, и/или к развитию у раковых клеток механизма ускользания от иммуннологического надзора (Dong et al. (2003) J Mol Med 81:281-7; Blank et al. (2005) Cancer Immunol. Immunother. 54:307-314; Konishi et al. (2004) Clin. Cancer Res. 10:5094-100).
В одном аспекте настоящее изобретение относится к лечению индивидуума in vivo с использованием молекулы антитела против PD-1 или против PD-L1, приводящему к подавлению или уменьшению роста раковых опухолей. Антитело против PD-1 или против PD-L1 можно использовать отдельно для ингибирования роста раковых опухолей. Альтернативно антитело против PD-1 или против PD-L1 можно использовать в сочетании с одним или несколькими из следующих средств: средство, описанное в таблице 1, традиционно используемое в медицине (например, для лечения рака), другое антитело или его антиген-связывающий фрагмент, другой иммуномодулятор (например, активатор костимуляторной молекулы или ингибитор ингибиторной молекулы); вакцина, например, терапевтическая противораковая вакцина; или другие формы клеточной иммунотерапии, как описано ниже.
Соответственно, в одном варианте осуществления изобретение предлагает способ ингибирования роста опухолевых клеток у индивидуума, включающий в себя введение индивидууму терапевтически эффективного количества описанного здесь сочетания терапквтических средств. В одном варианте осуществления указанные способы можно использовать для лечения рака in vivo. Если антитела против PD-1 вводят в сочетании с одним или несколькими средствами, компоненты сочетания можно вводить в любом порядке или одновременно.
В другом аспекте изобретение предлагает способ лечения индивидуума, например, обеспечивающий улучшение или облегчение гиперпролиферативного состояния или расстройства (включающего в себя рак), такого как солидная опухоль, опухоль мягких тканей, или метастатическое поражение. Способ включает в себя введение индивидууму одной или нескольких описанных здесь молекул антител против PD-1 или PD-L1, отдельно или в сочетании с другими средствами или терапевтическими препаратами.
В соответствии с данным описанием термин "рак" охватывает все виды раковых опухолей или онкогенных процессов, метастатических тканей или претерпевших злокачественную трансформацию клеток, тканей или органов, независимо от гистологического типа или стадии инвазии. Примеры раковых заболеваний включают в себя, без ограничения, солидные опухоли, опухоли мягких тканей и метастатические поражения. Примеры солидных опухолей включают в себя злокачественные опухоли, такие как саркомы, аденокарциномы и карциномы, разных органов и систем, например, поражающие печень, легкие, молочную железу, лимфатическую систему, желудочно-кишечный тракт (например, толстую кишку), мочеполовой тракт (например, почки, уротелиальные клетки), предстательную железу и глотку. Аденокарциномы представляют собой злокачественные опухоли, включающие в себя большинство видов рака толстой кишки, рак прямой кишки, почечноклеточный рак, рак печени, немелкоклеточный рак легкого, рак тонкой кишки и рак пищевода. В одном из вариантов осуществления рак представляет собой меланому, например, меланому на запущенной стадии. Метастатические поражения, обусловленные вышеуказанными видами рака, также можно лечить или предотвращать с помощью способов и композиций настоящего изобретения.
Примеры раковых опухолей, рост которых можно ингибировать с помощью описанных здесь молекул антител, включают в себя раковые заболевания, обычно отвечающие на иммунотерапию. Не ограничивающие примеры раковых заболеваний, предпочтительно подлежащих лечению с помощью описанных здесь способов, включают в себя меланому (такую как метастатическая злокачественная меланома), рак почек (такой как светлоклеточный рак), рак предстательной железы (такой как гормонорезистентная аденокарцинома предстательной железы), рак молочной железы, рак толстой кишки и рак легких (такой как немелкоклеточный рак легкого). Кроме того, с помощью описанных здесь молекул антител можно лечить резистентные или рецидивирующие злокачественные опухоли.
Примеры других раковых заболеваний, которые можно лечить с помощью описанных здесь способов, включают в себя рак кости, рак поджелудочной железы, рак кожи, рак головы или шеи, злокачественную меланому кожи или интраокулярную меланому, рак матки, рак яичников, рак прямой кишки, рак анального канала, гастроэзофагеальный рак, рак желудка, рак яичка, рак матки, карциному фаллопиевых труб, карциному эндометрия, карциному шейки матки, карциному влагалища, карциному вульвы, болезнь Ходжкина, неходжкинскую лимфому, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягких тканей, рак уретры, рак полового члена, хронический или острый лейкоз, в том числе острый миелолейкоз, хронический миелолейкоз, острый лимфолейкоз, хронический лимфолейкоз, солидные опухоли детского возраста, лимфоцитарную лимфому, рак мочевого пузыря, рак почки или мочеточника, карциному почечной лоханки, новообразования центральной нервной системы (ЦНС), первичную лимфому ЦНС, ангиогенез опухоли, опухоли позвоночника, глиому ствола мозга, аденому гипофиза, саркому Капоши, эпидермоидный рак, плоскоклеточный рак, Т-клеточную лимфому, индуцированные факторами окружающей среды раковые заболевания, такие как индуцированный асбестом рак, а также сочетания указанных видов рака.
Лечение метастатических раковых заболеваний, например, метастатических раковых заболеваний, при которых наблюдается экспрессия PD-L1 (Iwai et al. (2005) Int. Immunol. 17:133-144), можно проводить с использованием молекул антител, описанных в данном документе. В одном варианте осуществления рак характеризуется повышенным уровнем PD-L1, IFNγ и/или CD8.
Гематологические раковые состояния включают в себя такие раковые заболевания, как лейкоз и злокачественные лимфопролиферативные состояния, поражающие кровь, костный мозг и лимфатическую систему. Лейкоз можно классифицировать как острый лейкоз и хронический лейкоз. Острый лейкоз можно дополнительно классифицировать как острый миелолейкоз (AML) и острый лимфолейкоз (ALL). Хронический лейкоз включает в себя хронический миелолейкоз (CML) и хронический лимфолейкоз (CLL). Другие подходящие состояния включают в себя миелодиспластические синдромы (MDS, ранее известные как "прелейкозы"), которые представляют собой разнородную совокупность гематологических состояний, характеризующихся неэффективной продукцией (или дисплазией) миелоидных клеток крови и риском трансформации в AML.
В других вариантах осуществления рак представляет собой гематологическое злокачественное заболевание, или гематологический рак, включающий в себя, без ограничения, лейкозы или лимфомы. Например, сочетанную терапию можно использовать для лечения раковых заболеваний и злокачественных опухолей, таких как, например, острый лейкоз, включающий в себя, без ограничения, В-клеточный острый лимфолейкоз ("BALL"), Т-клеточный острый лимфолейкоз ("TALL"), острый лимфолейкоз (ALL); один или несколько хронических лейкозов, включающих в себя, без ограничения, хронический миелолейкоз (CML), хронический лимфолейкоз (CLL); другие гематологические раковые заболевания или гематологические состояния, включающие в себя, без ограничения, например, В-клеточный пролимфоцитарный лейкоз, опухоль бластных плазмацитоидных дендритных клеток, лимфому Беркитта, диффузную крупноклеточную В-клеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную или крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, лимфому MALT, мантийноклеточную лимфому, лимфому маргинальной зоны, множественную миелому, миелодисплазию и миелодиспластический синдром, неходжкинскую лимфому, плазмобластную лимфому, опухоль плазмоцитоидных дендритных клеток, макроглобулинемию Вальденстрема и "предлейкоз", которые представляют собой разнородную совокупность гематологических условий, объединяемых неэффективной продукцией (или дисплазией) миелоидных клеток крови и т.п. В некоторых вариантах осуществления лимфома (например, анапластическая крупноклеточная лимфома или неходжкинская лимфома) ассоциирована, либо идентифицирована как ассоциированная с транслокацией ALK, например, с гибридизацией EML4-ALK.
В одном из вариантов осуществления рак выбран из таких заболеваний, как рак легкого (например, немелкоклеточный рак легкого (NSCLC) (такой как NSCLC с плоскоклеточной и/или неплоскоклеточной гистологией)), меланома (например, запущенная меланома), рак почки (например, почечноклеточный рак, такой как светлоклеточная почечноклеточная карцинома), рак печени, миелома (например, множественная миелома), рак предстательной железы, рак молочной железы (например, рак молочной железы, при котором отсутствует экспрессия одного, двух или всех из рецептора эстрогена, рецептора прогестерона или Her2/neu, такой как трижды негативный рак молочной железы), колоректальный рак, рак поджелудочной железы, рак головы и шеи (например, плоскоклеточный рак головы и шеи (HNSCC), рак анального канала, гастроэзофагеальный рак, рак щитовидной железы, рак шейки матки, лимфопролиферативное заболевание (например, посттрансплантационное лимфопролиферативное заболевание) или гематологический рак, Т-клеточная лимфома, неходжкинская лимфома или лейкоз (например, миелолейкоз).
В другом варианте осуществления рак выбран из карциномы (такой как запущенная или метастатическая карцинома), меланомы или рака легких, такого как немелкоклеточный рак легкого.
В одном варианте осуществления рак представляет собой рак легкого, например, немелкоклеточный рак легкого. В некоторых вариантах осуществления рак легкого, такой как немелкоклеточный рак легкого, ассоциирован, либо идентифицирован как ассоциированный с перестройкой или транслокацией ALK, например, с гибридизацией ALK, такой как гибридизация EML4-ALK.
В другом варианте осуществления рак представляет собой гепатокарциному, например, запущенную гепатокарциному, необязательно сопровождающуюся вирусной инфекцией, такой как хронический вирусный гепатит.
В другом варианте осуществления рак представляет собой рак предстательной железы, такой как запущенный рак простаты. В следующем варианте осуществления рак представляет собой миелому, такую как множественная миелома.
В следующем варианте осуществления рак представляет собой рак почки, такой как почечноклеточная карцинома (RCC) (например, метастатическая RCC или светлоклеточная почечноклеточная карцинома).
В одном варианте осуществления рак представляет собой меланому, например, запущенную меланому. В одном варианте осуществления рак представляет собой запущенную или неоперабельную меланому, которая не отвечает на другие виды терапии. В других вариантах осуществления рак представляет собой меланому с мутацией BRAF (такой как мутация гена BRAF V600). В следующих вариантах осуществления молекулу антитела против PD-1 или PD-L1 вводят после антитела против CTLA4 (такого как ипилимумаб) в присутствии или в отсутствии ингибитора BRAF (такого как вемурафениб или дабрафениб).
В другом варианте осуществления рак представляет собой воспалительную миофибробластическую опухоль (IMT). В некоторых вариантах осуществления воспалительная миофибробластическая опухоль ассоциирована, либо идентифицирована как ассоциированная с перестройкой или транслокацией ALK, например, с гибридизацией ALK, такой как гибридизация EML4-ALK.
В следующем варианте осуществления рак представляет собой нейробластому. В некоторых вариантах осуществления нейробластома ассоциирована, либо идентифицирована как ассоциированная с перестройкой или транслокацией ALK, например, с гибридизацией ALK, такой как гибридизация EML4-ALK. Раскрытые здесь способы и композиции можно использовать для лечения метастатических поражений, вызванных упомянутыми выше раковыми заболеваниями.
Сочетанные способы лечения
Описанные здесь способы и композиции можно использовать в сочетании с одним или несколькими из следующих средств: иммуномодулятор (такой как активатор костимуляторной молекулы или ингибитор ингибиторной молекулы); вакцина, такая как терапевтическая вакцина против рака; или другие средства клеточной иммунотерапии.
Термин "в сочетании с" не означает, что терапию, или терапевтические средства, нужно вводить одновременно и/или в составе одной композиции для совместной доставки, хотя указанные способы доставки входят в объем настоящего изобретения. Иммуномодулятор и второе терапевтическое средство можно вводить одновременно, до или после применения одного или нескольких других способов лечения или других терапевтических средств. Входящие в состав сочетания средства можно вводить в любом порядке. Как правило, каждое средство вводят в дозе и/или в режиме, которые определены для данного средства. Кроме того, следует учитывать, что другое терапевтическое средство, используемое в данном сочетании, можно вводить вместе в составе одной композиции, или отдельно в составе другой композиции. Предполагается, что другие терапевтические средства, являющиеся компонентами сочетания, можно использовать на уровне, который не превышает уровня, на котором их используют по отдельности. В некоторых вариантах осуществления уровни терапевтических средств, используемых в сочетании, ниже, чем уровни терапевтических средств, используемых по отдельности.
В одном варианте осуществления описанные здесь сочетанные способы лечения включают в себя применение ингибитора молекулы, ингибирующей иммунную контрольную точку. Термин "иммунные контрольные точки" относится к группе молекул, присутствующих на поверхности Т-клеток CD4 и CD8. Указанные молекулы могут эффективно функционировать в качестве "тормозной системы", осуществляющей понижающую регуляцию иммунного ответа против опухоли, или подавляющей иммунный ответ против опухоли. Молекулы иммунной контрольной точки включают в себя, без ограничения, белок программируемой гибели 1 (PD-1), цитотоксический Т-лимфоцитарный антиген 4 (CTLA-4), B7H1, B7H4, ОХ-40, CD137, CD40 и LAG3, которые непосредственно ингибируют иммунные клетки, иммунотерапевтические средства, которые могут функционировать как ингибиторы иммунной контрольной точки, и могут использоваться в способах настоящего изобретения, включают в себя, без ограничения, ингибиторы PD-L1, PD-L2, CTLA4, TIM3, LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и/или TGFR бета. Ингибирование ингибиторной молекулы можно осуществлять на уровне ДНК, РНК или белка. В некоторых вариантах осуществления для подавления экспрессии ингибиторной молекулы можно использовать ингибиторную нуклеиновую кислоту (например, дцРНК, миРНК или кшРНК). В других вариантах осуществления ингибитор ингибиторного сигнала представляет собой полипептид, такой как растворимый лиганд, или антитело, или его антиген-связывающий фрагмент, способный связываться с ингибиторной молекулой.
В некоторых вариантах осуществления описанные здесь молекулы против PD-1 вводят в сочетании с одним или несколькими другими ингибиторами PD-1, PD-L1 и/или PD-L2, известными в данной области. Антагонист может представлять собой антитело, его антиген-связывающий фрагмент, иммуноадгезин, гибридный белок или олигопептид.
В некоторых вариантах осуществления другое антитело против PD-1 выбрано из MDX-1106, Merck 3475 или CT-011.
В некоторых вариантах осуществления ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, содержащий внеклеточный или PD-1-связывающий фрагмент PD-L1 или PD-L2, гибридизованный с константным доменом (например, Fc-участком последовательности иммуноглобулина).
В некоторых вариантах осуществления ингибитор PD-1 представляет собой АМР-224. В некоторых вариантах осуществления ингибитор PD-L1 представляет собой антитело против PD-L1.
В некоторых вариантах осуществления антагонист, способный связываться с PD-L1, выбран из YW243.55.S70, MPDL3280A, MEDI-4736, MSB-0010718C или MDX-1105. MDX-1105, также известный как BMS-936559, представляет собой антитело против PD-L1, описанное в WO2007/005874. Антитело YW243.55.S70 (последовательности вариабельных участков тяжелой и легкой цепи описаны в SEQ ID No. 20 и 21, соответственно) представляет собой антитело против PD-L1, описанное в WO 2010/077634.
В некоторых вариантах осуществления антитело против PD-1 представляет собой ниволумаб. Альтернативные названия ниволумаба включают в себя MDX-1106, MDX-1106-04, ONO-4538 или BMS-936558. В некоторых вариантах осуществления антитело против PD-1 представляет собой ниволумаб (регистрационный номер CAS: 946414-94-4). Ниволумаб (также упоминается как BMS-936558 или MDX1106, Bristol-Myers Squibb) представляет собой полностью человеческое моноклональное антитело IgG4, которое специфически блокирует PD-1. Ниволумаб (клон 5C4) и другие человеческие моноклональные антитела, способные специфически связываться с PD-1, описаны в US 8008449, EP2161336 и WO2006/121168. Ниволумаб содержит следующие аминокислотные последовательности тяжелой и легкой цепей:
Тяжелая цепь (SEQ ID NO: 2)
QVQLVESGGGVVQPGRSLRLDCKASGITFSNSGMHWVRQAPGKGLEWVAVIWYDGSKRYYADSVKGRFTISRDNSKNTLFLQMNSLRAEDTAVYYCATNDDYWGQGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
Легкая цепь (SEQ ID NO: 3)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSSNWPRTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Ниволумаб является предпочтительным партнером в комбинации.
В некоторых вариантах осуществления антитело против PD-1 представляет собой пембролизумаб. Пембролизумаб (также называемый ламбролизумаб, МК-3475, MK03475, SCH-900475 или KEYTRUDA®; Merck) представляет собой гуманизированное моноклональное антитело IgG4, которое связывается с PD-1. Пембролизумаб и другие гуманизированные антитела против PD-1 описаны в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, US 8,354,509 and WO2009/114335. Пембролизумаб содержит следующие аминокислотные последовательности тяжелой и легкой цепей:
Тяжелая цепь (SEQ ID NO: 4)

Легкая цепь (SEQ ID NO: 5)

Пидилизумаб (CT-011; Cure Tech) представляет собой гуманизированное моноклональное антитело IgG1k, способное связываться с PD1. Пидилизумаб и другие гуманизированные моноклональные антитела против PD-1 описаны в WO2009/101611.
Другие антитела против PDL включают в себя AMP 514 (амплимун), в числе других, таких как антитела против PD1, описанные в US 8609089, US 2010028330 и/или US 20120114649.
В некоторых вариантах осуществления антитело против PD-L1 представляет собой MSB0010718C. MSB0010718C (также называемое A09-246-2, Merck Serono) представляет собой моноклональное антитело, способное связываться с PD-L1. Пембролизумаб и другие гуманизированные антитела против PD-L1 описаны в WO2013/079174. MSB0010718C содержит, по меньшей мере, следующие аминокислотные последовательности тяжелой и легкой цепей:
Тяжелая цепь (SEQ ID NO: 24, описана в WO2013/079174) (SEQ ID NO: 6)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYIMMWVRQAPGKGLEWVSSIYPSGGITFYADKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARIKLGTVTTVDYWGQGTLVTVSS
Легкая цепь (SEQ ID NO: 25, описана в WO2013/079174) (SEQ ID NO: 7)
QSALTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSN RPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTRVFGTGTKVTVL
MDPL3280A (Genentech/Roche) представляет собой человеческое Fc-оптимизированное моноклональное антитело IgG1, способное связываться с PD-L1. MDPL3280A и другие человеческие моноклональные антитела против PD-L1 описаны в патенте США № 7943743 и публикации США № 20120039906. Другие средства, способные связываться с PD-L1, включают в себя YW243.55.S70 (вариабельные участки тяжелой и легкой цепей описаны в SEQ ID NO: 20 и 21, WO2010/077634) и MDX-1105 (также известный как BMS-936559, а также, например, средства, способные связываться с PD-L1, описанные в WO2007/005874).
AMP-224 (В7-DCIg; амплимун, описан, например, в WO2010/027827 и WO2011/066342) представляет собой Fc-гибридный растворимый рецептор PD-L2, который блокирует взаимодействие PD1 и B7-H1.
В некоторых вариантах осуществления антитело против LAG-3 представляет собой BMS-986016. BMS-986016 (также обозначаемое BMS986016; Bristol-Myers Squibb) представляет собой моноклональное антитело, способное связываться с LAG-3. BMS-986016 и другие гуманизированные антитела против LAG-3 описаны в US 2011/0150892, WO2010/019570 и WO2014/008218.
В некоторых вариантах осуществления описанное здесь сочетание терапевтических средств содержит модулятор костимуляторной молекулы или ингибиторной молекулы, например, коингибиторный лиганд или рецептор.
В одном варианте осуществления костимуляторный модулятор, например, агонист костимуляторной молекулы выбран из агониста (такого как агонистическое антитело или его антиген-связывающий фрагмент, или растворимый гибрид) OX40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3 или лиганда CD83.
В другом варианте осуществления описанное здесь сочетание терапевтических средств содержит костимуляторную молекулу, такую как агонист, связанный с положительным сигналом, который содержит костимуляторный домен CD28, CD27, ICOS и GITR.
Примеры агонистов GITR включают в себя, например, GITR-гибридные белки и антитела против GITR (например, двухвалентные антитела против GITR), такие как гибридный белок GITR, описанный в патенте США № 6111090, европейском патенте № 090505B1, патенте США № 8586023, публикациях РСТ №№ WO 2010/003118 и 2011/090754, или антитело против GITR, описанное, например, в патенте США № 7025962, европейском патенте № 1947183B1, патенте США № 7812135, патенте США № 8388967, патенте США № 8591886, европейском патенте № EP 1866339, публикации РСТ № WO 2011/028683, публикации РСТ № WO 2013/039954, публикации РСТ № WO2005/007190, публикации РСТ № WO 2007/133822, публикации РСТ № WO2005/055808, публикации РСТ № WO 99/40196, публикации РСТ № WO 2001/03720, публикации РСТ № WO99/20758, публикации РСТ № WO2006/083289, публикации РСТ № WO 2005/115451, патенте США № 7618632 и публикации РСТ № WO 2011/051726.
В одном варианте осуществления ингибитор представляет собой растворимый лиганд (например, CTLA-4-Ig), или антитело или фрагмент антитела, способные связываться с PD-L1, PD-L2 или CTLA4. Например, молекулу антитела против PD-1 можно вводить в сочетании с антителом против CTLA-4, таким как ипилимумаб, например, для лечения рака (такого как: меланома, например, метастатическая меланома, рак легкого, например, немелкоклеточный рак легкого, или рак предстательной железы). Примеры антител против CTLA4 включают в себя тремелимумаб (моноклональное антитело IgG2, которое можно приобрести в Pfizer, ранее известное как тицилимумаб, CP-675206); и ипилимумаб (антитело против CTLA-4, также известное как MDX-010, CAS № 477202-00-9).
В одном варианте осуществления молекулу антитела против PD-1 вводят после лечения, например, после лечения меланомы, с антителом против CTLA4 (таким как ипилимумаб) в присутствии или в отсутствии ингибитора BRAF (такого как вемурафениб или дабрафениб). Примеры подходящих для использования доз включают в себя дозу молекулы антитела против PD-1, составляющую примерно от 1 до 10 мг/кг, например, 3 мг/кг, и дозу антитела против CTLA-4, такого как ипилимумаб, составляющую примерно 3 мг/кг.
В другом варианте осуществления молекулу антитела против PD-1 или PD-L1 вводят в сочетании с антителом против LAG-3, или его антиген-связывающим фрагментом. В другом варианте осуществления молекулу антитела против PD-1 или PD-L1 вводят в сочетании с антителом против TIM-3, или его антиген-связывающим фрагментом. В других вариантах осуществления молекулу антитела против PD-1 или PD-L1 вводят в сочетании с антителом против LAG-3 и антителом против TIM-3, или их антиген-связывающими фрагментами. Антитела, входящие в описанное здесь сочетание, можно вводить по отдельности, например, в виде отдельных антител, или они могут быть связаны между собой, например, они могут находиться в виде молекулы биспецифического или триспецифичного антитела. В одном варианте осуществления вводят биспецифическое антитело, которое содержит молекулу антитела против PD-1 или PD-L1 и антитело против TIM-3 или против LAG-3, или его антиген-связывающий фрагмент. В некоторых вариантах осуществления описанное здесь сочетание антител используют для лечения рака, такого как рак, описанный в настоящем документе (например, солидная опухоль). Эффективность вышеуказанных сочетаний можно тестировать на животных моделях, известных в данной области. Например, животные модели для тестирования синергетического действия антитела против PD-1 и антитела против LAG-3 описаны в Woo et al. (2012) Cancer Res. 72(4):917-27.
В другом варианте осуществления молекулу антитела против PD-1 или PD-L1 вводят в сочетании с ингибитором CEACAM (например, CEACAM-1, -3 и/или -5). В одном варианте осуществления ингибитор CEACAM (например, CEACAM-1, -3 и/или -5) представляет собой молекулу антитела против CEACAM. Не желая быть связанными с теорией, авторы полагают, что молекула клеточной адгезии, связанная с карциноэмбриональным антигеном (CEACAM), такая как CEACAM-1 и CEACAM-5, опосредует, по меньшей мере частично, ингибирование иммунного ответа против опухоли (см., например, Markel et al. J Immunol. 2002 Mar 15;168(6):2803-10; Markel et al. J Immunol. 2006 Nov 1;177(9):6062-71; Markel et al. Immunology. 2009 Feb;126(2):186-200; Markel et al. Cancer Immunol Immunother. 2010 Feb;59(2):215-30; Ortenberg et al. Mol Cancer Ther. 2012 Jun;11(6):1300-10; Stern et al. J Immunol. 2005 Jun 1;174(11):6692-701; Zheng et al. PLoS One. 2010 Sep 2;5(9). pii: e12529). Например, CEACAM-1 описан как гетерофильный лиганд TIM-3, участвующий в TIM-3-опосредованном развитии толерантности и истощения Т-клеток (см., например, WO 2014/022332; Huang, et al. (2014) Nature doi:10.1038/nature13848). В некоторых вариантах осуществления показано, что совместная блокада CEACAM-1 и TIM-3 усиливает иммунный ответ против опухоли у моделей с ксенотрансплантатами колоректального рака (см., например, WO 2014/022332; Huang, et al. (2014), выше). В других вариантах осуществления совместная блокада CEACAM-1 и PD-1 снижает толерантность Т-клеток, как описано, например, в WO 2014/059251. Таким образом, ингибиторы CEACAM можно использовать в сочетании с другими иммуномодуляторами, описанными в данном документе (такими как ингибиторы PD-1 и/или TIM-3) для усиления иммунного ответа против рака, такого как меланома, рак легких (например, NSCLC), рак мочевого пузыря, рак ободочной кишки, рак яичника, и другие описанный здесь раковые опухоли.
Соответственно, в некоторых вариантах осуществления молекулу антитела против PD-1 вводят в сочетании с ингибитором CEACAM (таким как ингибитор CEACAM-1, CEACAM-3 и/или CEACAM-5). В одном варианте осуществления ингибитор CEACAM представляет собой молекулу антитела против CEACAM. В одном варианте осуществления молекулу антитела против PD-1 вводят в сочетании с ингибитором CEACAM-1, таким как молекула антитела против CEACAM-1. В другом варианте осуществления молекулу антитела против PD-1 вводят в сочетании с ингибитором CEACAM-3, таким как молекула антитела против CEACAM-3. В другом варианте осуществления изобретения молекулу антитела против PD-1 вводят в сочетании с ингибитором CEACAM-5, таким как молекула антитела против CEACAM-5. Примеры антител против CEACAM-1, описанные в WO 2010/125571, WO 2013/082366 и WO 2014/022332, включают в себя моноклональные антитела 34B1, 26H7 и 5F4; или их рекомбинантные формы, описанные, например, в US 2004/0047858, US 7132255 и WO 99/052552. В других вариантах осуществления антитело против CEACAM связывается с CEACAM-5, как описано, например, в Zheng et al. PLoS One. 2010 Sep 2;5(9). pii: e12529 (DOI:10:1371/journal.pone.0021146), или перекрестно взаимодействует с CEACAM-1 и CEACAM-5, как описано, например, в WO 2013/054331 и US 2014/0271618.
В другом варианте осуществления сочетание терапевтических средств включает в себя применение модифицированных Т-клеток, например, в сочетании с адоптивной Т-клеточной иммунотерапией с использованием Т-клеток, несущих химерный антигенный рецептор (CAR) (например, как описано John LB, et al. (2013) Clin. Cancer Res. 19(20): 5636-46).
В других вариантах осуществления описанное здесь сочетание терапевтических средств также может включать в себя цитокины, такие как интерлейкин-21 или интерлейкин-2. В некоторых вариантах осуществления описанное здесь сочетание используют для лечения рака, такого как описанный здесь рак (например, солидная опухоль или меланома).
Примеры иммуномодуляторов, которые можно использовать в сочетанных способах лечения, включают в себя, без ограничения, например, афутузумаб (поставляемый Roche®); пегфилграстим (Neulasta®); леналидомид (CC-5013, Revlimid®); талидомид (Thalomid®), актимид (CC4047); а также цитокины, такие как IL-21 или IRX-2 (смесь человеческих цитокинов, содержащая интерлейкин 1, интерлейкин 2 и интерферон γ, CAS 951209-71-5, поставляется IRX Therapeutics).
В других вариантах осуществления сочетание терапевтических средств можно вводить индивидууму наряду (например, до, одновременно или после) с применением одного или нескольких из следующих способов лечения: трансплантация костного мозга, Т-клеточная абляционная терапия с использованием химиотерапевтических средств, таких как флударабин, наружная дистанционная лучевая терапия (XRT), циклофосфамид и/или антитела, такие как OKT3 или САМРАТН. В одном варианте осуществления молекулу антитела против PD-1 или PD-L1 вводят после В-клеточной абляционной терапии, такой как средства, взаимодействующие с CD20, например, ритуксан. Например, в одном варианте осуществления индивидуумы могут получать стандартное лечение высокой дозой химиотерапевтического средства с последующей трансплантацией стволовых клеток периферической крови. В некоторых вариантах осуществления после трансплантации индивидуумы получают молекулы антител против PD-1 или PD-L1. В другом варианте осуществления молекулы антитела против PD-1 или PD-L1 вводят до или после операции.
Другой пример дополнительной сочетанной терапии включает в себя применение декарбазина для лечения меланомы. Не желая быть связанными с теорией, авторы полагают, что совместное применение блокады PD-1 и химиотерапии оказывает благоприятный эффект благодаря гибели клеток вследствие цитотоксического действия большинства химиотерапевтических соединений, которое может приводить к повышению уровня опухолевого антигена в пути презентации антигена. Другие сочетанные способы лечения, которые могут обеспечивать синергический эффект с блокадой PD-1 посредством гибели клеток, включают в себя облучение, хирургическое вмешательство и выключение эндокринной функции. Каждая из указанных схем лечения создает источник опухолевого антигена в организме хозяина. Ингибиторы ангиогенеза также можно объединять с блокадой PD-1. Ингибирование ангиогенеза приводит к гибели опухолевых клеток, которые могут питать опухолевый антиген в путях презентации антигена в организме хозяина.
Сочетанные способы лечения также можно использовать наряду с применением биспецифических антител. Биспецифические антитела можно использовать для нацеливания на два разных антигена. Например, биспецифические антитела против рецептора Fc/опухолевого антигена (такого как Her-2/neu) используют для нацеливания макрофагов на участки опухоли. Такое нацеливание может обеспечить более эффективную активацию опухоль-специфичных ответов. T-клеточная ветвь этих ответов дополняется в результате применения блокады PD-1. Альтернативно антиген можно доставлять непосредственно к DC с помощью биспецифических антител, способных связываться с опухолевым антигеном и со специфическим маркером клеточной поверхности дендритных клеток.
Опухоли уклоняются от иммунного надзора организма-хозяина посредством широкого ряда механизмов. Многие из таких механизмов можно блокировать путем инактивации белков, которые экспрессируются опухолями и обладают иммуносупрессорной активностью. К ним относятся, в числе прочих, TGF-бета (Kehrl, J. et al. (1986) J. Exp. Med. 163: 1037-1050), IL-10 (Howard, M. & O'Garra, A. (1992) Immunology Today 13: 198-200) и лиганд Fas (Hahne, M. et al. (1996) Science 274: 1363-1365). Антитела или их антигенсвязывающие фрагменты, специфичные к каждому из указанных соединений, можно использовать в сочетании с антителом против PD-1, чтобы препятствовать проявлению иммуносупрессивной активности и способствовать развитию у хозяина иммунного ответа на опухоль.
Наряду с описанной здесь сочетанной терапией можно использовать и другие антитела, способствующие активации иммунного ответа. Они включают в себя молекулы на поверхности дендритных клеток, которые активируют функцию DC и презентацию антигена. Антитела против CD40, способные эффективно заменять активность хелперных Т-клеток (Ridge, J. et al. (1998) Nature 393: 474-478), можно использовать в сочетании с антителами против PD-1 (Ito, N. et al. (2000) Immunobiology 201 (5) 527-40). Антитела против костимуляторных молекул Т-клеток, таких как CTLA-4 (например, патент США № 5811097), OX-40 (Weinberg, A. et al. (2000) Immunol 164: 2160-2169), 4-1BB (Melero, I. et al. (1997) Nature Medicine 3: 682-685 (1997) и ICOS (Hutloff, A. et al. (1999) Nature 397: 262-266), также могут привести к повышению уровня активации Т-клеток.
Во всех описанных здесь способах блокаду PD-1 можно сочетать с другими формами иммунотерапии, такими как лечение цитокином (таким как интерферон, GM-CSF, G-CSF, IL-2, IL-21), или лечение биспецифическим антителом, которые увеличивают презентацию опухолевых антигенов (см., например, Holliger (1993) Proc. Natl. Acad. Sci. USA 90:6444-6448; Poljak (1994) Structure 2:1121-1123).
Описанные здесь сочетанные способы лечения также можно объединить с иммуногенным средством, таким как раковые клетки, очищенные опухолевые антигены (включающие в себя рекомбинантные молекулы белков, пептидов и углеводов), клетки и клетки, трансфицированные генами, кодирующими иммуностимулирующие цитокины (He et al. (2004) J. Immunol. 173:4919-28). Неограничивающие примеры подходящих опухолевых вакцин включают в себя пептиды, полученные из антигенов меланомы, такие как пептиды gp100, антигенов MAGE, Trp-2, MARTI и/или тирозиназы, или опухолевые клетки, трансфицированных с целью экспрессии цитокина GM-CSF.
Блокаду PD-1 можно использовать в сочетании с вакцинацией. Разработано много экспериментальных стратегий вакцинации против опухолей (см. Rosenberg, S., 2000, Development of Cancer Vaccines, ASCO Educational Book Spring: 60-62; Logothetis, C., 2000, ASCO Educational Book Spring: 300-302; Khayat, D. 2000, ASCO Educational Book Spring: 414-428; Foon, K. 2000, ASCO Educational Book Spring: 730-738; см. также Restifo, N. and Sznol, M., Cancer Vaccines, Ch. 61, pp. 3023-3043 in DeVita, V. et al. (eds.), 1997, Cancer: Principles and Practice of Oncology. Fifth Edition). В соответствии с одной из указанных стратегий, вакцины получают с использованием аутологичных или аллогенных опухолевых клеток. Показано, что такие клеточные вакцины являются наиболее эффективными, если используют трансдуцированные опухолевые клетки, экспрессирующие GM-CSF. Показано, что GM-CSF является мощным активатором презентации антигена, используемого для противоопухолевой вакцинации (Dranoff et al. (1993) Proc. Natl. Acad. Sci. U.S.A. 90: 3539-43).
Блокаду PD-1 можно использовать в сочетании с рядом рекомбинантных белков и/или пептидов, экспрессируемых в опухоли, с целью получения иммунного ответа на эти белки. Обычно иммунная система принимает такие белки за собственные антигены и, следовательно, является толерантной к ним. Опухолевый антиген может также включать в себя белковую теломеразу, которая необходима для синтеза теломеров хромосом и которая экспрессируется в более чем в 85% раковых опухолей человека и лишь в ограниченном количестве соматических тканей (Kim, N et al. (1994) Science 266: 2011-2013). (Указанные соматические ткани можно защитить от иммунной атаки разными способами). Опухолевый антиген также может включать в себя "неоантигены", экспресирующиеся в раковых клетках вследствие соматических мутаций, которые могут приводить к изменению последовательности белка или образованию гибридных белков из двух неродственных последовательностей (например, bcr-abl в хромосоме Philadelphia), или идиотипа из В-клеточных опухолей.
Другие противоопухолевые вакцины могут включать в себя белки вирусов, участвующих в развитии человеческих раковых опухолей, таких как вирусы папилломы человека (HPV), вирусы гепатита (HBV и HCV) и вирус герпеса, связанный с саркомой Капоши (KHSV). Другой вид опухоль-специфических антигенов, подходящих для применения в сочетании с блокадой PD-1, включает в себя очищенные белки теплового шока (HSP), выделенные непосредственно из опухолевой ткани. Указанные белки теплового шока содержат фрагменты белков опухолевых клеток и могут обеспечивать высокоэффективную доставку к антиген-презентирующим клеткам, индуцируя противоопухолевый иммунитет (Suot, R & Srivastava, P (1995) Science 269:1585-1588; Tamura, Y. et al. (1997) Science 278:117-120).
Дендритные клетки (DC) представляют собой активные антиген-презентирующие клетки, которые можно использовать для инициации антиген-специфических ответов. DC можно получить ex vivo и нагрузить разными белковыми и пептидными антигенами, а также экстрактами опухолевых клеток (Nestle, F. et al. (1998) Nature Medicine 4: 328-332). DC также можно трансдуцировать генетическими методами с получением клеток, экспрессирующих указанные опухолевые антигены. DC также можно гибридизовать непосредственно с опухолевыми клетками и затем использовать для иммунизации (Kugler, A. et al. (2000) Nature Medicine 6:332-336). Иммунизацию DC, как способ вакцинации, можно эффективно сочетать с блокадой PD-1, что позволяет индуцировать более интенсивные противоопухолевые ответы.
Другие сочетанные способы лечения
Описанные здесь сочетанные терапевтические средства могут дополнительно содержать одно или несколько других терапевтических средств, и/или их можно вводить совместно с одним или несколькими другими терапевтическими средствами, включающими в себя противораковые средства, цитотоксические или цитостатические средства, гормональные средства, вакцины и/или другие иммунотерапевтические средства. В других вариантах осуществления молекулы антитела вводят в сочетании с другими способами лечения, такими как хирургия, радиация, криохирургия и/или термотерапия. В таких сочетанных способах лечения преимущественно вводят более низкие дозы терапевтических средств, что позволяет избежать возможных проявлений токсичности или осложнений, связанных с разными видами монотерапии.
Например, описанные здесь сочетанные способы лечения также можно сочетать со стандартными способами лечения рака. Например, блокаду PD-1 можно эффективно сочетать с введением химиотерапевтических средств. При этом дозу вводимого химиотерапевтического средства ((Mokyr, M. et al. (1998) Cancer Research 58: 5301-5304) можно уменьшить. В некоторых вариантах осуществления описанные здесь способы и композиции используют в сочетании с одним или несколькими из средств, включающих в себя молекулы других антител, химиотерапевтические средства, другие противораковые терапевтические способы лечения (такие как направленная противораковая терапия или применение онколитических средств), цитотоксические средства, иммунологические терапевтические средства (такие как цитокины), хирургическое вмешательство и/или облучение. Примеры цитотоксических средств, которые можно вводить в сочетании с описанными здесь средствами, включают в себя ингибиторы образования микротрубочек, ингибиторы топоизомеразы, антиметаболиты, ингибиторы митоза, алкилирующие средства, антрациклины, алкалоиды барвинка, интеркалирующие средства, средства, препятствующие передаче сигнала, средства, инициирующие апоптоз, ингибиторы протеосом и облучение (например, локальное облучение или полное облучение всего организма).
Примеры сочетаний со стандартными средствами лечения рака включают в себя, по меньшей мере, следующие средства.
В некоторых вариантах осуществления сочетанную терапию используют в сочетании со стандартным противораковым химиотерапевтическим средством, включающим в себя, без ограничения, анастрозол (Arimidex®), бикалутамид (Casodex®), блеомицина сульфат (Blenoxane®), бусульфан (Myleran®), бусульфан инъекционный (Busulfex®), капецитабин (Xeloda®), Н4-пентоксикарбонил-5-дезокси-5-фтороцитидин, карбоплатин (Paraplatin®), кармустин (BiCNU®), хлорамбуцил (Leukeran®), цисплатин (Platinol®), кладрибин (Leustatin®), циклофосфамид (Cytoxan® или Neosar®), цитарабин, цитозинарабинозид (цитозара-U®), инъекции цитарабин липосомами (DepoCyt®), Дакарбазин (DTIC-Dome®), дактиномицин (Актиномицин D, Cosmegan), даунорубицина гидрохлорид (Cerubidine®), инъекционный липосомальный препарат, содержащий даунорубицина цитрат (DaunoXome®), дексаметазон, доцетаксел (Taxotere®), доксорубицина гидрохлорид (Adriamycin®, Rubex®), этопозид (Vepesid®), флударабина фосфат (Fludara®), 5-фторурацил (Adrucil®, Efudex®), флутамид (Eulexin®), тезацитибин, гемцитабин (дифтордезоксицитидин), гидроксимочевину (Hydrea®), идаруцибин (Idamycin®), ифосфамид (IFEX®), иринотекан (Camptosar®), L-аспарагиназу (ELSPAR®), лейковорин кальция, мелфалан (Alkeran®), 6-меркаптопурин (Purinethol®), метотрексат (Folex®), митоксантрон (Novantrone®), милотарг, паклитаксел (Taxol®), nab-паклитаксел (Abraxane®), феникс (иттрий90/MX-DTPA), пентостатин, полифупросан 20 с кармустин-содержащим имплантатом (Gliadel®), тамоксифена цитрат (Nolvadex®), тенипозил (Vumon®), 6-тиогуанин, тиотепа, тирапазамин (Tirazone®), топотекана гидрохлорид для инъекций (Hycamptin®), винбластин (Velban®), винкристин (Oncovin®) и винорелбин (Navelbine®).
Примеры алкилирующих средств включаютв себя, без ограничения, азотистые иприты, производные этиленимина, алкилсульфонаты, нитрозомочевины и триазены): урамустин (Aminouracil Mustard®, Chlorethaminacil®, Demethyldopan®, Desmethyldopan®, Haemanthamine®, Nordopan®, Uracil nitrogen mustard®, Uracillost®, Uracilmostaza®, Uramustin®, Uramustine®), хлорметин (Mustargen®), циклофосфамид (Cytoxan®, Neosar®, Clafen®, Endoxan®, Procytox®, Revimmune™), ифосфамид (Mitoxana®), мелфалан (Alkeran®), хлорамбуцил (Leukeran®), пипоброман (Amedel®, Vercyte®), триэтиленмеламин (Hemel®, Hexalen®, Hexastat®), триэтилентиофосфорамин, темозоламид (Temodar®), тиотепа (Thioplex®), бусульфан (Busilvex®, Myleran®), кармустин (BiCNU®), ломустин (CeeNU®), стрептозоцин (Zanosar®) и дакарбазин (DTIC-Dome®). Другие примеры алкилирующих средств включают в себя, без ограничения, оксалиплатин (Eloxatin®); темозоламид (Temodar® и Temodal®); дактиномицин (также известный как актиномицин-D, Cosmegen®); мелфалан (также известный как L-РАМ, L-сарколизин и фенилаланин-иприт, Alkeran®); алтретамин (также известный как гексаметилмеламин (СММ), Hexalen®); кармустин (BiCNU®); бендамустин (Treanda®); бусульфан (Busulfex® и Myleran®); карбоплатин (Paraplatin®); ломустин (также известный как CCNU, CeeNU®); цисплатин (также известный как CDDP, Platinol® и Platinol®-AQ); хлорамбуцил (Leukeran®); циклофосфамид (Cytoxan® и Neosar®); дакарбазин (также известный как DTIC, DIC и имидазола карбоксамид, DTIC-Dome®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); ифосфамид (Ifex®); преднумустин; прокарбазин (Matulane®); мехлорэтамин (также известный как азотистый иприт, мустин и мехлорэтамина гидрохлорид, Mustargen®); стрептозоцин (Zanosar®); тиотепа (также известный как тиофосфамид, TESPA и TSPA, Thioplex®); циклофосфамид (Endoxan®, Cytoxan®, Neosar®, Procytox®, Revimmune®); и бендамустина HCl (Treanda®).
Примеры антрациклинов включают в себя, например, доксорубицин (Adriamycin® и Rubex®); блеомицин (lenoxane®); даунорубицин (даунорубицина гидрохлорид, дауномицин и рубидомицина гидрохлорид, Cerubidine®); даунорубицин липосомальный (липосомальный препарат, содержащий даунорубицина цитрат, DaunoXome®); митоксантрон (DHAD, Novantrone®); эпирубицин (Ellence™); идаруцибин (Idamycin®, Idamycin PFS®); митомицин C (Mutamycin®); гелданамицин; гербимицин; равидомицин; и деацетилравидомицин.
Примеры алкалоидов барвинка, подходящих для совместного применения с описанным здесь сочетанным терапевтическим средством (таким как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), и соединение, описанное в таблице 1), включают в себя, без ограничения, винорелбина тартрат (Navelbine®), винкристин (Oncovin®) и виндезин (Eldisine®)); винбластин (также известный как винбластина сульфат, винкалейкобластин и VLB, Alkaban-AQ® и Velban®); и винорелбин (Navelbine®).
Примеры ингибиторов протеосом, подходящих для совместного применения с описанным здесь сочетанным терапевтическим средством (таким как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), и LDK378), включают в себя, без ограничения, бортезомиб (Velcade®); карфилзомиб (PX-171-007, (S)-4-метил-N-((S)-1-(((S)-4-метил-1-((R)-2-метилоксиран-2-ил)-1-оксопентан-2-ил)амино)-1-оксо-3-фенилпропан-2-ил)-2-((S)-2-(2-морфолиноацетамидо)-4-фенилбутанамидо)пентанамид); маризомиб (НПИ-0052); иксазомиба цитрат (MLN-9708); деланзомиб (СЕР-18770); O-метил-N-[(2-метил-5-тиазолил)карбонил]-L-серил-O-метил-N-[(1S)-2-[(2R)-2-метил-2-оксиранил]-2-оксо-1-(фенилметил)этил]-L-серинамид (ONX-0912); данопревир (RG7227, CAS 850876-88-9); иксазомиб (MLN2238, CAS 1072833-77-2); и (S)-N-[(фенилметокси)карбонил]-L-лейцил-N-(1-формил-3-метилбутил)-L-лейцинамид (MG-132, CAS 133407-82-6).
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и LDK378 используют вместе с ингибитором тирозинкиназы (таким как ингибитор рецепторной тирозинкиназы (RTK)). Примеры ингибиторов тирозинкиназ включают в себя, без ограничения, ингибитор пути эпидермального фактора роста (EGF) (такой как ингибитор рецептора эпидермального фактора роста (EGFR)), ингибитор пути фактора роста эндотелия сосудов (VEGF) (такой как ингибитор рецептора фактора роста эндотелия сосудов (VEGFR) (например, ингибитор VEGFR-1, ингибитор VEGFR-2, ингибитор VEGFR-3)), ингибитор пути фактора роста тромбоцитов (PDGF) (такой как ингибитор рецептора фактора роста тромбоцитов (PDGFR) (например, ингибитор PDGFR-β)), ингибитор RAF-1, ингибитор KIT и ингибитор RET. В некоторых вариантах осуществления настоящего изобретения противораковое средство используется в сочетании с ингибитором hedgehog, выбранным из группы, включающей в себя: акситиниб (AG013736), босутиниб (SKI-606), седираниб (RECENTIN™, AZD2171), дазатиниб (SPRYCEL®, BMS-354825), эрлотиниб (TARCEVA®), гефитиниб (IRESSA®), иматиниб (Gleevec®, CGP57148B, STI-571), лапатиниб (TYKERB®, TYVERB®), лестауртиниб (CEP-701), нератиниб (HKI-272), нилотиниб (TASIGNA®), семаксаниб (семаксаниб, SU5416), сунитиниб (SUTENT®, SU11248), тоцераниб (PALLADIA®), вандетаниб (ZACTIMA®, ZD6474), ваталаниб (PTK787, PTK/ZK), трастузумаб (HERCEPTIN®), бевацизумаб (Avastin®), ритуксимаб (RITUXAN®), цетуксимаб (ERBITUX®), панитумумаб (VECTIBIX®), ранибизумаб (Lucentis®), нилотиниб (TASIGNA®), сорафениб (Nexavar®), алемтузумаб (Campath®), гемтузумаб озогамицина (Mylotarg®), ENMD-2076, PCI-32765, AC220, довитиниба лактат (TKI258, CHIR-258), BIBW 2992 (TOVOK™), SGX523, PF-04217903, PF-02341066, PF-299804, BMS-777607, ABT-869, MP470, BIBF 1120 (VARGATEF®), AP24534, JNJ-26483327, MGCD265, DCC-2036, BMS-690154, СЕР-11981, тивозаниб (AV-951), OSI-930, ММ-121, XL-184, XL-647, XL228, AEE788, AG-490, АСТ-6, BMS-599626, CUDC-101, PD153035, пелитиниб (EKB-569), вандетаниб (зактима), WZ3146, WZ4002, WZ8040, ABT-869 (линифаниб), AEE788, AP24534 (понатиниб), AV-951 (тивозаниб), акситиниб, BAY 73-4506 (регорафениб), бриваниба аланинат (BMS-582664), бриваниб (BMS-540215), цедираниб (AZD2171), CHIR-258 (довитиниб), CP 673451, CYC116, E7080, Ki8751, маситиниб (AB1010), MGCD-265, мотесаниба дифосфат (AMG-706), MP-470, OSI-930, пазопаниба гидрохлорид, PD173074, сорафениба тозилат (Bay 43-9006), SU 5402, TSU-68 (SU6668), ваталаниб, XL880 (GSK1363089, EXEL-2880). Другие примеры ингибиторов hedgehog включают в себя, без ограничения, висмодегиб (2-хлор-N-[4-хлор-3-(2-пиридинил)фенил]-4-(метилсульфонил)бензамид, GDC-0449, описанный в публикации РСТ WO 06/028958); 1-(4-хлор-3-(трифторметил)фенил)-3-((3-(4-фторфенил)-3,4-дигидро-4-оксо-2-хиназолинил)метил)мочевина (CAS 330796-24-2); N-[(2S,3R,3'R,3aS,4'aR,6S,6'aR,6'bS,7aR,12'aS,12'bS)-2',3',3a,4,4',4'a,5,5',6,6',6'a,6'b,7,7',7a,8',10',12',12'a,12'b-эйкозагидро-3,6,11',12'b-тетраметилспиро[фуро[3,2-b]пиридин-2(3H),9'(1'H)-нафт[2,1-a]азулен]-3'-ил]метансульфонамид (IPI926, CAS 1037210-93-7); и 4-фтор-N-метил-N-[1-[4-(1-метил-1H-пиразол-5-ил)-1-фталазинила]-4-пиперидинил]-2-(трифторметил)бензамид (LY2940680, CAS 1258861-20-9); и эрисмодегиб (LDE225). Отдельные ингибиторы тирозинкиназ включают в себя гефитиниб; гидрохлорид эрлотиниба (Tarceva®); линифаниб (N-[4-(3-амино-1H-индазол-4-ил)фенил]-N'-(2-фтор-5-метилфенил)мочевина, также известный как ABT 869, доступный от Genentech); сунитиниба малат (Sutent®); босутиниб (4-[(2,4-дихлор-5-метоксифенил)амино]-6-метокси-7-[3-(4-метилпиперазин-1-ил)пропокси]хинолин-3-карбонитрил, известный также как SKI-606, описанный в патенте США № 6780996); дазатиниб (Sprycel®); пазопаниб (Votrient®); сорафениб (Nexavar®); зактима (ZD6474); и иматиниб или иматиниба мезилат (Gilvec® и Gleevec®).
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и соединение, описанное в таблице 1, LDK378) используют в сочетании с ингибиторами рецепторов фактор роста эндотелия сосудов (VEGF), включающими в себя, без ограничения, бевацизумаб (Avastin®), акситиниб (Inlyta®); бриваниба аланинат (BMS-582664, (S)-((R)-1-(4-(4-фтор-2-метил-1H-индол-5-илокси)-5-метилпирроло[2,1-f][1,2,4]триазин-6-илокси)пропан-2-ил)-2-аминопропаноат); сорафениб (Nexavar®); пазопаниб (Votrient®); сунитиниба малат (Sutent®); седираниб (AZD2171, CAS 288383-20-1); варгатеф (BIBF1120, CAS 928326-83-4); форетиниб (GSK1363089); телатиниб (BAY57-9352, CAS 332012-40-5); апатиниб (YN968D1, CAS 811803-05-1); иматиниб (Gleevec®); панатиниб (AP24534, CAS 943319-70-8); тивозаниб (AV951, CAS 475108-18-0); регорафениб (BAY73-4506, CAS 755037-03-7); ваталаниба дигидрохлорид (PTK787, CAS 212141-51-0); бриваниб (BMS-540215, CAS 649735-46-6); вандетаниб (Caprelsa® или AZD6474); мотесаниба дифосфат (AMG706, CAS 857876-30-3, N-(2,3-дигидро-3,3-диметил-1H-индол-6-ил)-2-[(4-пиридинилметил)амино]-3-пиридинкарбоксамид, описанный в публикации РСТ WO 02/066470); довитиниба дилактат (TKI258, CAS 852433-84-2); линфаниб (ABT869, CAS 796967-16-3); карбозантиниб (XL184, CAS 849217-68-1); лестауртиниб (CAS 111358-88-4); N-[5-[[[5-(1,1-диметилэтил)-2-оксазолил]метил]тио]-2-тиазолил]-4-пиперидинкарбоксамид (BMS38703, CAS 345627-80-7); (3R,4R)-4-амино-1-((4-((3-метоксифенил)амино)пирроло[2,1-f][1,2,4]триазин-5-ил)метил)пиперидин-3-ол (BMS690514); N-(3,4-дихлор-2-фторфенил)-6-метокси-7-[[(3aα,5β,6aα)-октагидро-2-метилциклопента[с]пиррол-5-ил]метокси]-4-хиназолинамин (XL647, CAS 781613-23-8); 4-метил-3-[[1-метил-6-(3-пиридинил)-1H-пиразоло[3,4-d]пиримидин-4-ил]амино]-N-[3-(трифторметил)фенил]бензамид (BHG712, CAS 940310-85-0); и афлиберцепт (Eylea®).
Примеры антител против VEGF включают в себя, без ограничения, моноклональное антитело, которое связывается с тем же эпитопом, что и моноклональное антитело против VEGF A4.6.1, продуцируемое гибридомой АТСС НВ 10709; рекомбинантное гуманизированное моноклональное антитело против VEGF, полученное по способу, описанному Presta et al. (1997) Cancer Res. 57:4593-4599. В одном варианте осуществления антитело против VEGF представляет собой бевацизумаб (BV), также известный как rhuMAb VEGF или AVASTIN®. Оно содержит мутантные фрагменты каркасного участка человеческого IgG1 и антигенсвязывающие гипервариабельные участки мышиного моноклонального антитела против hVEGF А.4.6.1, способные блокировать связывание человеческого VEGF с его рецепторами. Бевацизумаб и другие гуманизированные антитела против VEGF дополнительно описаны в патенте США № 6884879, выданном 26 февраля 2005. Другие антитела включают в себя антитела серии G6 или B20 (такие как G6-31, B20-4.1), описанные в публикации РСТ WO2005/012359, публикации РСТ WO2005/044853, где содержание указанных патентных заявок специально включено в настоящий документ в качестве ссылки. Описание других антител можно найти в патентах США №№ 7060269, 6582959, 6703020, 6054297, W098/45332, WO 96/30046, WO-94/10202, ЕР 0666868B1, публикациях патентных заявок США №№ 2006009360, 20050186208, 20030206899, 20030190317, 20030203409 и 20050112126; а также в Popkov et al, Journal of Immunological Methods 288: 149-164 (2004). Другие антитела включают в себя антитела, способные связываться с функциональным эпитопом человеческого VEGF, содержащим остатки F17, M18, D19, Y21, Y25, Q89, I91, K101, E103 и C104, или, альтернативыно, содержащим остатки F17, Y21, Q22, Y25, D63, I83 и Q89.
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и соединение, описанное в таблице 1, LDK378) используют в сочетании с ингибитором PI3K. В одном варианте осуществления изобретения ингибитор PI3K представляет собой ингибитор дельта- и гамма-изоформ PI3K. Примеры ингибиторов PI3K, подходящих для применения в сочетании, описаны, например, в WO 2010/036380, WO 2010/006086, WO 09/114870, WO 05/113556, и включают в себя GSK 2126458, GDC-0980, GDC-0941, Sanofi XL147, XL756, XL147, PF-46915032, BKM 120, CAL-101, CAL 263, SF1126, PX-886, а также двойные ингибиторы PI3K (такие как Novartis BEZ235). Другие примеры ингибиторов PI3K включают в себя, без ограничения, 4-[2-(1H-индазол-4-ил)-6-[[4-(метилсульфонил)пиперазин-1-ил]метил]тиено[3,2-d]пиримидин-4-ил]морфолин (также известный как GDC 0941, описанный в публикациях РСТ №№ WO 09/036082 и WO 09/055730); 2-метил-2-[4-[3-метил-2-оксо-8-(хинолин-3-ил)-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил]пропионитрил (также известный как BEZ235 или NVP-BEZ235, описанный в публикации РСТ WO 06/122806); 4-(трифторметил)-5-(2,6-диморфолинопиримидин-4-ил)пиридин-2-амин (также известный как BKM120 или NVP-BKM120, описанный в публикации РСТ WO2007/084786); тозасертиб (VX680 или MK-0457, CAS 639089-54-6); (5Z)-5-[[4-(4-пиридинил)-6-хинолинил]метилен]-2,4-тиазолидиндион (GSK1059615, CAS 958852-01-2); (1E,4S,4aR,5R,6aS,9aR)-5-(ацетилокси)-1-[(ди-2-пропениламино)метилен]-4,4a,5,6,6a,8,9,9a-октагидро-11-гидрокси-4-(метоксиметил)-4a,6a-диметилциклопента[5,6]нафто[1,2-с]пиран-2,7,10(1H)-трион (PX866, CAS-502632-66-8); 8-фенил-2-(морфолин-4-ил)хромен-4-он (LY294002, CAS 154447-36-6); 2-амино-8-этил-4-метил-6-(пиразол-5-ил)-пиридо[2,3-d]пиримидин-7(8Н)-он (SAR 245409 или XL 765); 1,3-дигидро-8-(6-метокси-3-пиридинил)-3-метил-1-[4-(1-пиперазинил)-3-(трифторметил)фенил]-2H-имидазо[4,5-с]хинолин-2-он, (2Z)-2-бутендиоат (1:1) (BGT 226); 5-фтор-3-фенил-2-[(1S)-1-(9Н-пурин-6-иламино)этил]-4(3H)-хиназолинон (CAL101); 2-вмино-N-[3-[N-[3-[(2-хлор-5-метоксифенил)амино]хиноксалин-2-ил]сульфамоил]фенил]-2-метилпропанамид (SAR 245408 или XL 147); и (S)-пирролидин-1,2-дикарбоновой кислоты 2-амид 1-({4-метил-5-[2-(2,2,2-трифтор-1,1-диметилэтил)пиридин-4-ил]тиазол-2-ил}амид) (ВYL719).
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и соединение, описанное в таблице 1, LDK378) используют в сочетании с ингибитором mTOR, например, с одним или несколькими ингибиторами mTOR, выбранными из группы, включающей в себя рапамицин, темсиролимус (TORISEL®), AZD8055, BEZ235, BGT226, XL765, PF-4691502, GDC0980, SF1126, OSI-027, GSK1059615, KU-0063794, WYE-354, Palomid 529 (P529), PF-04691502 или PKI-587; ридафоролимус (формально известный как деферолимус, (1R,2R,4S)-4-[(2R)-2-[(1R,9S,12S,15R,16E,18R,19R,21R,23S,24E,26E,28Z,30S,32S,35R)-1,18-дигидрокси-19,30-диметокси-15,17,21,23,29,35-гексаметил-2,3,10,14,20-пентаоксо-11,36-диокса-4-азатрицикло[30.3.1.04,9]гексатриаконта-16,24,26,28-тетраен-12-ил]пропил]-2-метоксициклогексила диметилфосфинат, также известный как АР23573 и MK8669, и описанный в публикации РСТ WO 03/064383); эверолимус (Afinitor® или RAD001); рапамицин (AY22989, Sirolimus®); симапимод (CAS 164301-51-3); эмсиролимус, (5-{2,4-бис[(3S)-3-метилморфолин-4-ил]пиридо[2,3-d]пиримидин-7-ил}-2-метоксифенил)метанол (AZD8055); 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8Н)-он (PF04691502, CAS 1013101-36-4); и N2-[1,4-диоксо-4-[[4-(4-оксо-8-фенил-4H-1 бензопиран-2-ил)морфолиний-4-ил]метокси]бутил]-L-аргинилглицил-L-α-аспартил-серин-, внутренняя соль (SF1126, CAS 936487-67-1) (1r,4r)-4-(4-амино-5-(7-метокси-1H-индол-2-ил)имидазо[1,5-f][1,2,4]триазин-7-ил)циклогексанкарбоновой кислоты (ВОС-027); и XL765.
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и соединение, описанное в таблице 1, LDK378) используют в сочетании с ингибитором BRAF, таким как GSK2118436, RG7204, PLX4032, GDC-0879, PLX4720 и сорафениба тозилат (Bay 43-9006). В других вариантах осуществления ингибитор BRAF включает в себя, без ограничения, регорафениб (BAY73-4506, CAS 755037-03-7); тувизаниб (AV951, CAS 475108-18-0); вемурафениб (Zelboraf®, PLX-4032, CAS 918504-65-1); энкорафениб (также известный как LGX818); 1-метил-5-[[2-[5-(трифторметил)-1H-имидазол-2-ил]-4-пиридинил]окси]-N-[4-(трифторметил)фенил-1H-бензимидазол-2-амин (RAF265, CAS 927880-90-8); 5-[1-(2-гидроксиэтил)-3-(пиридин-4-ил)-1H-пиразол-4-ил]-2,3-дигидроинден-1-она оксим (GDC-0879, CAS-905281-76-7); 5-[2-[4-[2-(диметиламино)этокси]фенил]-5-(4-пиридинил)-1H-имидазол-4-ил]-2,3-дигидро-1H-инден-1-она оксим (GSK2118436 или SB590885); (+/-)-метил (5-(2-(5-хлор-2-метилфенил)-1-гидрокси-3-оксо-2,3-дигидро-1H-изоиндол-1-ил)-1H-бензимидазол-2-ил)карбамат (также известный как XL-281 и BMS908662) и N-(3-(5-хлор-1H-пирроло[2,3-b]пиридин-3-карбонил)-2,4-дифторфенил)пропан-1-сульфонамид (также известный как PLX4720).
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и соединение, описанное в таблице 1, LDK378) используют в сочетании с ингибитором МЕК. В некоторых вариантах осуществления сочетание антитела против PD-1 и ингибитора МЕК используют для лечения рака (например, описанного здесь рака). В некоторых вариантах осуществления рак, подлежащий лечению сочетанием, включает в себя меланому, колоректальный рак, немелкоклеточный рак легкого, рак яичника, рак молочной железы, рак простаты, рак поджелудочной железы, гематологическую злокачественную опухоль или почечноклеточную карциному. В некоторых вариантах осуществления рак характеризуется наличием мутации BRAF (такой как мутация гена BRAF V600E), BRAF дикого типа, KRAS дикого типа или KRAS-активирующей мутации. Рак может находиться на ранней, средней или поздней стадии. В сочетании можно использовать любой ингибитор МЕК, включающий в себя, без ограничения, селуметиниб (5-[(4-бром-2-хлорфенил)амино]-4-фтор-N-(2-гидроксиэтокси)-1-метил-1H-бензимидазол-6-карбоксамид, известный также как AZD6244 или ARRY 142886, описанный в публикации РСТ WO2003077914); траметиниба диметилсульфоксид (GSK-1120212, CAS 1204531-25-80); RDEA436; N-[3,4-дифтор-2-[(2-фтор-4-иодфенил)амино]-6-метоксифенил]-1-[(2R)-2,3-дигидроксипропил]-циклопропансульфонамид (также известный как RDEA119 или BAY869766, описанный в публикации РСТ WO2007014011); AS703026; BIX 02188; BIX 02189; 2-[(2-хлор-4-иодфенил)амино]-N-(циклопропилметокси)-3,4-дифторбензамид (также известный как CI-1040 или PD184352, описанный в публикации РСТ WO2000035436); N-[(2R)-2,3-дигидроксипропокси]-3,4-дифтор-2-[(2-фтор-4-иодфенил)амино]бензамид (также известный как PD0325901, описанный в публикации РСТ WO2002006213); 2'-амино-3'-метоксифлавон (также известный как PD98059, поставляемый Biaffin GmbH & Co., KG, Germany); 2,3-бис[амино[(2-аминофенил)тио]метилен]бутандинитрил (также известный как U0126, описанный в патенте США № 2779780); XL-518 (также известный как GDC-0973, Cas № 1029872-29-4, поставляемый ACC Corp.); G-38963; и G02443714 (также известный как AS703206), или его фармацевтически приемлемые соли или сольваты. Другие примеры ингибиторов МЕК раскрыты в WO 2013/019906, WO 03/077914, WO 2005/121142, WO 2007/04415, WO 2008/024725 и WO 2009/085983, содержание которых включено в настоящее описание в качестве ссылки. Другие примеры ингибиторов MEK включают в себя, без ограничения, бениметиниб (6-(4-бром-2-фторфениламино)-7-фтор-3-метил-3Н-бензоимидазол-5-карбоновой кислоты (2-гидроксиэтилокси)амид, также известный как MEK162, CAS 1073666-70-2, описанный в публикации РСТ № WO2003077914); 2,3-бис[амино[(2-аминофенил)тио]метилен]бутандинитрил (также известный как U0126 и описанный в патенте США № 2779780); (3S,4R,5Z,8S,9S,11E)-14-(этиламино)-8,9,16-тригидрокси-3,4-диметил-3,4,9,19-тетрагидро-1H-2-бензоксациклотетрадецин-1,7(8H)-дион] (также известный как E6201, описанный в публикации РСТ WO2003076424); вемурафениб (PLX-4032, CAS 918504-65-1); (R)-3-(2,3-дигидроксипропил)-6-фтор-5-(2-фтор-4-иодфениламино)-8-метилпиридо[2,3-d]пиримидин-4,7(3H,8Н)дион (TAK-733, CAS 1035555-63-5); пимасертиб (AS-703026, CAS 1204531-26-9); 2-(2-фтор-4-иодфениламино)-N-(2-гидроксиэтокси)-1,5-диметил-6-оксо-1,6-дигидропиридин-3-карбоксамид (AZD 8330); и 3,4-дифтор-2-[(2-фтор-4-иодфенил)амино]-N-(2-гидроксиэтокси)-5-[(3-оксо-[1,2]оксазинан-2-ил)метил]бензамид (CH 4987655 или Ro 4987655).
В некоторых вариантах осуществления описанное здесь сочетанное терапевтическое средство (такое как молекула антитела против PD-1 или PD-L1, используемая отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3) и соединение, описанное в таблице 1, LDK378) используют в сочетании с ингибитором JAK2, таким как CEP-701, INCB18424, CP-690550 (тасоситиниб). Примеры ингибиторов JAK включают в себя, без ограничения, руксолитиниб (Jakafi®); тофаситиниб (CP690550); акситиниб (AG013736, CAS 319460-85-0); 5-хлор-N-2-[((1S)-1-(5-фтор-2-пиримидинил)этил]-N4-(5-метил-1H-пиразол-3-ил)-12,4-пиримидиндиамин (AZD1480, Cas 935666-88-9); (9E)-15-[2-(1-пирролидинил)этокси]-7,12,26-триокса-19,21,24-триазатетрацикло[18.3.1.12,5.114,18]-гексакоза-1(24),2,4,9,14,16,18(25),20,22-нонаен (SB-1578, CAS 937273-04-6); момелотиниб (CYT 387); бариситиниб (INCB-028050 или LY-3009104); пакритиниб (SB1518); (16Е)-14-метил-20-окса-5,7,14,27-тетраазатетрацикло[19.3.1.12,6.18,12]гептакоза-1(25),2,4,6(27),8,10,12(26),16,21,23-декаен (SB 1317); гандотиниб (LY 2784544); и N,N-циклопропил-4-[(1,5-диметил-1H-пиразол-3-ил)амино]-6-этил-1,6-дигидро-1-метилимидазо[4,5-d]пирроло[2,3-b]пиридин-7-карбоксамид (BMS 911543).
В некоторых вариантах осуществления описанные здесь сочетанные терапевтические средства содержат паклитаксел или паклитаксел-содержащее средство, например, TAXOL®, связанный с белком паклитаксел (например, ABRAXANE®). Примеры паклитаксел-содержащих средств включают в себя, без ограничения, паклитаксел, связанный с наночастицами альбумина (ABRAXANE, поставляемый Abraxis Bioscience), паклитаксел, связанный с докозагексаеновой кислотой (DHA-паклитаксел, таксопрексин, поставляемый Protarga), полиглутамат-связанный паклитаксел (PG-паклитаксел, паклитаксел полиглумекс, CT-2103, XYOTAX, поставляемый Cell Therapeutic), опухоль-активируемое пролекарство (ТАР), ANG105 (Angiopep-2, связанный с тремя молекулами паклитаксела, поставляемый ImmunoGen), паклитаксел-EC-1 (паклитаксел, связанный с erbB2-распознающим пептидом EC-1; см. Li et al., Biopolymers (2007) 87:225-230), и глюкозо-конъюгированный паклитаксел (например, 2'-паклитакселметил-2-глюкопиранозилсукцинат, см. Liu et al., Bioorganic & Medicinal Chemistry Letters (2007) 17:617-620).
В некоторых вариантах осуществления молекулу антитела против PD-1 или PD-L1, используемую отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), вводят в сочетании с антителом против иммуноглобулиноподобного рецептора клетки-киллера (также называемым здесь "антитело против KIR"). В некоторых вариантах осуществления описанное здесь сочетание молекулы антитела против PD-1 и антитела против KIR используют для лечения рака, такого как рак, описанный в настоящем документе (например, солидная опухоль, такая как запущенная солидная опухоль).
В одном варианте осуществления молекулу антитела против PD-1 или PD-L1, используемую отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), вводят в сочетании с клеточным иммунотерапевтическим средством (таким как провендж (например, Sipuleucel)) и, необязательно, в сочетании с циклофосфамидом. В некоторых вариантах осуществления сочетание, содержащее молекулу антитела против PD-1, провендж и/или циклофосфамид, используют для лечения рака, такого как описанный здесь рак (например, рак предстательной железы, такой как запущенный рак простаты).
В другом варианте осуществления молекулу антитела против PD-1 или PD-L1, используемую отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), вводят в сочетании с вакциной, такой как вакцина из дендритных клеток против карциномы почки (DC-RCC). В некоторых вариантах осуществления настоящего изобретения сочетание молекулы антитела против PD-1 и вакцины DC-АС используют для лечения рака, например, описанного здесь рака (такого как рак почки, например, метастатический почечноклеточный рак (RCC) или светлоклеточная почечноклеточная карцинома (CCRCC).
В следующем варианте осуществления молекулу антитела против PD-1 или PD-L1, используемую отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), вводят в сочетании с химиотерапевтическим и/или иммунотерапевтическим средством. Например, молекулу антитела против PD-1 или PD-L1 можно использовать для лечения миеломы отдельно или в сочетании с одним или несколькими из следующих средств: химиотерапевтические или другие противораковые средства (такие как аналоги талидомида, например, леналидомид), антитело против TIM3, дендритные клетки, сенсибилизированные опухолевым антигеном, гибриды (например, полученные путем электрослияния) опухолевых клеток и дендритных клеток, или вакцинация идиотипом иммуноглобулина продуцируемым злокачественными плазматическими клетками. В одном варианте осуществления молекулу антитела против PD-1 или PD-L1 используют в сочетании с антителом против TIM-3 для лечения миеломы, например, множественной миеломы.
В одном из вариантов осуществления молекулу антитела против PD-1 или PD-L1, отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), используют в сочетании с химиотерапией для лечения рака легкого, такого как немелкоклеточный рак легкого. В одном варианте осуществления молекулу антитела против PD-1 или PD-L1 используют для лечения рака легких в сочетании с платиновой дублетной терапией.
В следующем варианте осуществления молекулу антитела против PD-1 или PD-L1, отдельно или в сочетании с другим иммуномодулятором (таким как молекула антитела против LAG-3 или против TIM-3), используют для лечения рака почки, такого как почечноклеточная карцинома (RCC) (например, светлоклеточная почечноклеточная карцинома (CCRCC) или метастатическая RCC. Молекулу антитела против PD-1 или PD-L1 можно вводить в сочетания с одним или несколькими из следующих средств: средство для проведения иммунной стратегии (такое как интерлейкин-2 или интерферон-α), направленное средство (например, ингибитор VEGF, такой как моноклональное антитело против VEGF); ингибитор тирозинкиназы VEGF, такой как сунитиниб, сорафениб, акситиниб и пазопаниб; ингибитор РНК-интерференции, или ингибитор нижестоящего медиатора сигнального пути VEGF, например, ингибитор мишени рапамицина млекопитающих (mTOR), такой как эверолимус и темсиролимус.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения рака поджелудочной железы, включают в себя, без ограничения, химиотерапевтическое средство, такое как паклитаксел или паклитаксел-содержащее средство (например, композиция паклитаксела, такая как таксол, композиция нанодисперсного паклитаксела, стабилизированного альбумином (такая как ABRAXANE), или липосомальная композиция паклитаксела); гемцитабин (например, один или в сочетании с AXP107-11); другие химиотерапевтические средства, такие как оксалиплатин, 5-фторурацил, капецитабин, рубитекан, эпирубицин гидрохлорид, NC-6004, цисплатин, доцетаксел (например, TAXOTERE), митомицин C, ифосфамид; интерферон; ингибитор тирозинкиназы (например, ингибитор EGFR (такой как эрлотиниб, панитумумаб, цетуксимаб, нимотузумаб); ингибитор рецептора HER2/neu (такой как трастузумаб); двойной ингибитор киназы (такой как босутиниб, саракатиниб, лапатиниб, вандетаниб); мультикиназный ингибитор (такой как сорафениб, сунитиниб, XL184, пазопаниб); ингибитор VEGF (такой как бевацизумаб, AV-951, бриваниб); радиоиммунотерапевтическое средство (такое как XR303); противораковая вакцина (такая как GVAX, пептид сурвивин); ингибитор СОХ-2 (например, целекоксиб); ингибитор рецептора IGF-1 (такой как AMG 479, MK-0646); ингибитор mTOR (такой как эверолимус, темсиролимус); ингибитор IL-6 (такой как CNTO 328); ингибитор циклин-зависимой киназы (такой как P276-00, UCN-01); соединение, направленное на измененный энергетический метаболизм (AEMD) (такое как CPI-613); ингибитор HDAC (например, вориностат); рецептор TRAIL 2 (TR-2) агонисты (такие как конатумумаб); ингибитор MEK (такой как AS703026, селуметиниб, GSK1120212); двойной ингибитор киназ Raf/MEK (такой как R05126766); ингибитор сигнального пути Notch (такой как MK0752); гибридный белок моноклональное антитело-антитело (такой как L19IL2); куркумин; ингибитор HSP90 (такой как танеспимицин, STA-9090); RIL-2;, денилейкин-дифтитокс; ингибитор топоизомеразы 1 (такой как иринотекан, PEP02); статин (такой как симвастатин); ингибитор фактора VIIa (такой как PCI-27483); ингибитор AKT (такой как RX-0201); гипоксия-активируемое пролекарство (такое как TH-302); гидрохлорид метформина, ингибитор гамма-секретазы (такой как RO4929097); ингибитор рибонуклеотидредуктазы (такой как 3-АР); иммунотоксин (такой как HuC242-DM4); ингибитор PARP (такой как KU-0059436, велипариб); ингибитор CTLA-4 (такой как CP-675206, ипилимумаб); терапия AdV-tk; ингибитор протеасом (такой как бортезомиб (велкад), NPI-0052); тиазолидиндион (такой как пиоглитазон); NPC-1C; ингибитор киназы Aurora (такой как R763/AS703569), ингибитор CTGF (такой как FG-3019); siG12D LODER; а также лучевая терапия (такая как томотерапия, стереотаксическая лучевая терапия, протонная терапия), хирургическое вмешательство, и их сочетание. В некоторых вариантах осуществления сочетание паклитаксела или паклитаксел-содержащего средства и гемцитабина можно использовать вместе с описанными здесь молекулами антител против PD-1.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения мелкоклеточного рака легких, включают в себя, без ограничения, химиотерапевтическое средство, такое как этопозид, карбоплатин, цисплатин, иринотекан, топотекан, гемцитабин, липосомальный SN-38, бендамустин, темозоломид, белотекан, NK012, FR901228, флавопиридол; ингибитор тирозинкиназы (например, ингибитор EGFR (такой как эрлотиниб, гефитиниб, цетуксимаб, панитумумаб); мультикиназный ингибитор (такой как сорафениб, сунитиниб); ингибитор VEGF (такой как бевацизумаб, вандетаниб); противораковую вакцину (такую как GVAX); ингибитор Bcl-2 (такой как облимерсен натрия, ABT-263); ингибитор протеасом (такой как бортезомиб (велкад), NPI- 0052), паклитаксел или паклитаксел-содержащее средство; доцетаксел; ингибитор рецептора IGF-1 (такой как AMG 479); ингибитор HGF/SF (такой как AMG 102, МК-0646); хлорохин; ингибитор киназы Aurora (такой как MLN8237); радиоиммунотерапевтическое средство (такое как TF2); ингибитор HSP90 (такой как танеспимицин, STA-9090); ингибитор mTOR (такой как эверолимус); биспецифическое антитело против Ep-CAM/CD3 (такое как MT110); ингибитор CK-2 (такой как CX-4945); ингибитор HDAC (такой как белиностат); антагонист SMO (такой как BMS 833923); пептидная противораковая вакцина, а также лучевая терапия (такая как лучевая терапия с модулированной интенсивностью (IMRT), лучевая терапия с гипофракционированием, гипоксия-наведенная лучевая терапия), хирургическое вмешательство и их сочетания.
Примерв терапевтических средств, подходящих для применения в сочетании с целью лечения немелкоклеточного рака легких, включают в себя, без ограничения, химиотерапевтическое средство, такое как винорелбин, цисплатин, доцетаксел, пеметрексед динатрия, этопозид, гемцитабин, карбоплатин, липосомальный SN-38, TLK286, темозоломид, топотекан, пеметрексед динатрия, азацитидин, иринотекан, тегафур-гимерацил-отерацил калия, сапацитабин; ингибитор тирозинкиназы (такой как ингибитор EGFR (например, эрлотиниб, гефитиниб, цетуксимаб, панитумумаб, нецитумумаб, PF-00299804, нимотузумаб, RO5083945), ингибитор MET (например, PF-02341066, ARQ 197), ингибитор киназы PI3K (например, XL147, GDC-0941), двойной ингибитор киназ Raf/MEK (например, R05126766), двойной ингибитор киназы PI3K/mTOR (например, XL765), ингибитор SRC (например, дазатиниб), двойной ингибитор (например, BIBW 2992, GSK1363089, ZD6474, AZD0530, AG-013736, лапатиниб, MEHD7945A, линифаниб), мультикиназный ингибитор (например, сорафениб, сунитиниб, пазопаниб, AMG 706, XL184, MGCD265, BMS-690514, R935788), ингибитор VEGF (например, эндостар, эндостатин, бевацизумаб, седираниб, BIBF 1120, акситиниб, тивозаниб, AZD2171), противораковая вакцина (например, липосомная вакцина BLP25, GVAX, рекомбинантная ДНК и аденовирус, экспрессирующие белок L523S), ингибитор Bcl-2 (например, облимерсен натрия), ингибитор протеасом (например, бортезомиб, карфилзомиб, NPI-0052, MLN9708), паклитаксел или паклитаксел-содержащее средство, доцетаксел, ингибитор рецептора IGF-1 (например, циксутумумаб, MK-0646, OSI 906, CP-751871, BIIB022), гидроксихлорохин, ингибитор HSP90 (например, танеспимицин, STA-9090, AUY922, XL888), ингибитор mTOR (например, эверолимус, темсиролимус, ридафоролимус), Ep-CAM-/CD3-биспецифическое антитело (например, MT110), ингибитор CK-2 (например, CX-4945), ингибитор HDAC (например, MS 275, LBH589, вориностат, вальпроевая кислота, FR901228), ингибитор DHFR (например, пралатрексат), ретиноид (например, бексаротен, третиноин), конъюгат антитело-лекарственное средство (например, SGN-15), бисфосфонат (например, золедроновая кислота), противораковая вакцина (например, белагенпуматуцел-L), низкомолекулярный гепарин (LMWH) (например, тинзапарин, эноксапарин), GSK1572932A, мелатонин, талактоферрин, димесна, ингибитор топоизомеразы (например, амрубицин, этопозид, каренитецин), нелфинавир, силенгитид, ингибитор ErbB3 (например, ММ-121, U3-1287), ингибитор сурвивина (например, YM155, LY2181308), эрибулина мезилат, ингибитор COX-2 (например, целекоксиб), пегфилграстим, ингибитор Polo-подобной киназы 1 (например, BI 6727), агонисты рецептора TRAIL 2 (TR-2) (например, CS-1008), конъюгат пептид CNGRC-TNF альфа, дихлорацетат (DCA), ингибитор HGF (например, SCH 900105), SAR240550, агонист PPAR-гамма (например, CS-7017), ингибитор гамма-секретазы (например, RO4929097), эпигенетическое терапевтическое средство (например, 5-азацитидин), нитроглицерин, ингибитор MEK (например, AZD6244), ингибитор циклин-зависимой киназы (например, UCN-01), холестерин-Fus1, антитубулиновое средство (например, E7389), ингибитор фарнезил-ОН-трансферазы (например, лонафарниб), иммунотоксин (например, BB-10901, SS1 (dsFv) PE38), фондапаринукс, сосудоразрушающее средство (например, AVE8062), ингибитор PD-L1 (например, MDX-1105, MDX-1106), бета-глюкан, NGR-hTNF, EMD 521873, ингибитор MEK (например, GSK1120212), аналог эпотилона (например, иксабепилон), ингибитор кинезина-веретена (например, 4SC-205), теломера-специфичное средство (например, KML-001), ингибитор пути Р70 (например, LY2584702), ингибитор AKT (например, МК-2206), ингибитор ангиогенеза (например, леналидомид), ингибитор сигнального пути Notch (например, OMP-21M18), лучевая терапия, хирургическое вмешательство, а также их сочетания.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения рака яичников, включают в себя, без ограничения, химиотерапевтическое средство (например, паклитаксел или паклитаксел-содержащее средство; доцетаксел; карбоплатин; гемцитабин; доксорубицин; топотекан; цисплатин; иринотекан, TLK286, ифосфамид, олапариб, оксалиплатин, мелфалан, пеметрексед динатрия, SJG-136, циклофосфамид, этопозид, децитабин; антагонист грелина (например, AEZS-130), иммунотерапевтическое средство (например, APC8024, ореговомаб, OPT-821), ингибитор тирозинкиназы (например, ингибитор EGFR (например, эрлотиниб), двойной ингибитор (например, E7080), мультикиназный ингибитор (например, AZD0530, СО-101, сорафениб, сунитиниб, пазопаниб), ON 01910.Na), ингибитор VEGF (например, бевацизумаб, BIBF 1120, седираниб, AZD2171), ингибитор PDGFR (например, IMC-3G3), паклитаксел, ингибитор топоизомеразы (например, каренитецин, иринотекан), ингибитор HDAC (например, вальпроат, вориностат), ингибитор рецептора фолиевой кислоты (например, фарлетузумаб), ингибитор ангиопоэтина (например, AMG 386), аналог эпотилона (например, иксабепилон), ингибитор протеасом (например, карфилзомиб), ингибитор рецептора IGF-1 (например, OSI 906, AMG 479), ингибитор PARP (например, велипариб, AG014699, инипариб, MK-4827), ингибитор киназы Aurora (например, MLN8237, ENMD-2076), ингибитор ангиогенеза (например, леналидомид), ингибитор DHFR (например, пралатрексат), радиоиммунотерапевтическое средство (например, Hu3S193), статин (например, ловастатин), ингибитор топоизомеразы 1 (например, NKTR-102), противораковая вакцина (например, р53 синтетическая вакцина из длинных пептидов, аутологичная вакцина OC-DC), ингибитор mTOR (например, темсиролимус, эверолимус), ингибитор BCR/ABL (например, иматиниб), антагонист рецепторов ET-A (например, ZD4054), агонист рецептора TRAIL 2 (TR-2) (например, CS-1008), ингибитор HGF/SF (например, AMG 102), EGEN-001, ингибитор Polo-подобной киназы 1 (например, BI 6727), ингибитор гамма-секретазы (например, RO4929097), ингибитор Wee-1 (например, MK-1775), антитубулиновое средство (например, винорелбин, E7389), иммунотоксин (например, денилейкин-дифтитокс), SB-485232, сосудоразрушающее средство (например, AVE8062), ингибитор интегрина (например, EMD 525797), ингибитор кинезина-веретена (например, 4SC-205), REVLIMID, ингибитор HER2 (например, MGAH22), ингибитор ErrB3 (например, ММ-121), лучевая терапия; и их сочетания.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения миеломы, отдельно или вместе с одним или несколькими из следующих средств: химиотерапевтические или другие противораковые средства (например, аналоги талидомида, такие как леналидомид), HSCT (Cook, R. (2008) J Manag Care Pharm. 14(7 Suppl):19-25), антитело против TIM3 (Hallett, WHD et al. (2011) J of American Society for Blood and Marrow Transplantation 17(8):1133-145), дендритные клетки, сенсибилизированные опухолевым антигеном, гибриды (например, полученные путем электрослияния) опухолевых клеток и дендритных клеток, или вакцинация идиотипом иммуноглобулина продуцируемым злокачественными плазматическими клетками (обзор можно найти в Yi, Q. (2009) Cancer J. 15(6):502-10).
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения рака почки, такого как почечноклеточный рак (RCC) или метастатический RCC. Молекулу антитела против PD-1 можно вводить в сочетании с одним или несколькими из ледующих средств: средство для проведения иммунной стратегии (такое как интерлейкин-2 или интерферон-α), направленное средство (например, ингибитор VEGF, такой как моноклональное антитело против VEGF, например, бевацизумаб (Rini, B.I. et al. (2010) J. Clin. Oncol. 28(13):2137-2143)); ингибитор тирозинкиназы VEGF, такой как сунитиниб, сорафениб, акситиниб и пазопаниб (обзор можно найти в Pal. S.K. et al. (2014) Clin. Advances in Hematology & Oncology 12(2):90-99)); ингибитор РНК-и); или ингибитор нижестоящего медиатора сигнального пути VEGF, например, ингибитор мишени рапамицина млекопитающих (mTOR), такой как эверолимус и темсиролимус (Hudes, G. et al. (2007) N. Engl. J. Med. 356(22):2271-2281, Motzer, R.J. et al. (2008) Lancet 372: 449-456).
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения хронического миелолейкоза (AML), в соответствии с изобретением включают в себя, без ограничения, химиотерапевтическое средство (такое как цитарабин, гидроксимочевина, клофарабин, мелфалан, тиотепа, флударабин, бусульфан, этопозид, кордицепин, пентостатин, капецитабин, азацитидин, циклофосфамид, кладрибин, топотекан), ингибитор тирозинкиназы (такой как ингибитор BCR/ABL (например, иматиниб, нилотиниб), ON 01910.Na, двойной ингибитор (такой как дазатиниб, босутиниб), мультикиназный ингибитор (такой как DCC-2036, понатиниб, сорафениб, сунитиниб, RGB-286638)), интерферон-альфа, стероиды, апоптическое средство (такое как омасетаксина мепесукцинат), иммунотерапевтическое средство (например, аллогенные CD4+ Th1 клетки памяти-подобные Т-клетки/связанные с микрочастицами антитела против CD3/CD28, аутологичные цитокин-индуцированные клетки-киллеры (CIK), AHN-12), CD52-специфичное средство (такое как алемтузумаб), ингибитор HSP90 (такой как танеспимицин, STA-9090, AUY922, XL888), ингибитор mTOR (такой как эверолимус), антагонист SMO (такой как BMS 833923), ингибитор рибонуклеотидредуктазы (такой как 3-AP), ингибитор JAK-2 (такой как INCB018424), гидрокссихлорохин, ретиноид (такой как фенретиниб), ингибитор циклин-зависимой киназы (такой как UCN-01), ингибитор HDAC (такой как белиностат, вориностат, JNJ-26481585), ингибитор PARP (такой как велипариб), антагонист MDM2 (такой как RO5045337), ингибитор киназы Aurora B (такой как TAK-901), радиоиммунотерапевтическое средство (такое как актиний-225-меченное антитело против CD33 HuM195), ингибитор Hedgehog (такой как PF-04449913), ингибитор STAT3 (такой как OPB-31121), KB004, противораковая вакцина (например, AG858), трансплантация костного мозга, трансплантация стволовых клеток, лучевая терапия и их сочетания.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения хронического лимфолейкоза (CLL) включают в себя, без ограничения, химиотерапевтическое средство (такое как флударабин, циклофосфамид, доксорубицин, винкристин, хлорамбуцил, бендамустин, хлорамбуцил, бусульфан, гемцитабин, мелфалан, пентостатин, митоксантрон, 5-азацитидин, пеметрексед динатрия), ингибитор тирозинкиназы (такой как ингибитор EGFR (например, эрлотиниб), ингибитор BTK (такой как PCI-32765), мультикиназный ингибитор (такой как MGCD265, RGB-286638), CD-20-специфическое средство (такое как ритуксимаб, офатумумаб, RO5072759, LFB-R603), CD52-специфическое средство (такое как алемтузумаб), преднизолон, дарбэпоэтин альфа, леналидомид, ингибитор Bcl-2 (такой как ABT-263), иммунотерапевтическое средство (например, аллогенные CD4+ Th1 клетки памяти-подобные Т-клетки/связанные с микрочастицами антитела против CD3/CD28, аутологичные цитокин-индуцированные клетки-киллеры (CIK)), ингибитор HDAC (такой как вориностат, вальпроевая кислота, LBH589, JNJ-26481585, AR-42), ингибитор XIAP (такой как AEG35156), CD-74-специфическое средство (такое как милатузумаб), ингибитор mTOR (такой как эверолимус), AT-101, иммунотоксин (такой как CAT-8015, антитело против Тас(Fv)-PE38 (LMB-2)), CD37-специфическое средство (такое как TRU-016), радиоиммунотерапевтическое срдство (такое как 131-тозитумомаб), гидроксихлорохин, перифосин, ингибитор SRC (такой как дазатиниб), талидомид, ингибитор PI3K дельта (такой как CAL-101), ретиноид (например, фенретинид), антагонист MDM2 (такой как RO5045337), плериксафор, ингибитор киназы Aurora (такой как MLN8237, TAK-901), ингибитор протеасом (такой как бортезомибом), CD-19-специфическое средство (такое как MEDI-551, MOR208), ингибитор MEK (такой как ABT-348), ингибитор JAK-2 (такой как INCB018424), гипоксия-активируемое пролекарство (такое как TH-302), паклитаксел или паклитаксел-содержащее средство, ингибитор HSP90, ингибитор AKT (такой как MK2206), ингибитор HMG-CoA (такой как симвастатин), GNKG186, лучевая терапия, трансплантация костного мозга, трансплантация стволовых клеток, а также их сочетания.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения острого лимфолейкоза (ALL), включают в себя, без ограничения, химиотерапевтическое средство (такое как преднизолон, дексаметазон, винкристин, аспарагиназа, даунорубицин, циклофосфамид, цитарабин, этопозид, тиогуанин, меркаптопурин, клофарабин, липосомальный аннамицин, бусульфан, этопозид, капецитабин, децитабин, азацитидин, топотекан, темозоломид), ингибитор тирозинкиназы (такой как ингибитор BCR/ABL (например, иматиниб, нилотиниб), ON 01910.Na, мультикиназный ингибитор (такой как сорафениб)), CD-20-специфическое средство (такое как ритуксимаб), CD52-специфическое средство (такое как алемтузумаб), ингибитор HSP90 (такой как STA-9090), ингибитор mTOR (такой как эверолимус, рапамицин), ингибитор JAK-2 (такой как INCB018424), ингибитор рецептора HER2/neu (такой как трастузумаб), ингибитор протеасом (такой как бортезомибом), метотрексат, аспарагиназа, CD-22-специфическое средство (такое как эпратузумаб, инотузумаб), иммунотерапевтическое средство (такое как аутологичные цитокин-индуцированные клетки-киллеры (CIK), AHN-12), блинатумомаб, ингибитор циклин-зависимой киназы (такой как UCN-01), CD45-специфическое средство (такое как BC8), антагонист MDM2 (такой как RO5045337), иммунотоксин (такой как CAT-8015, DT2219ARL), ингибитор HDAC (такой как JNJ-26481585), JVRS-100, паклитаксел или паклитаксел-содержащее средство, ингибитор STAT3 (такой как OPB-31121), ингибитор PARP (такой как велипариб), EZN-2285, лучевая терапия, стероидная терапия, пересадка костного мозга, трансплантации стволовых клеток, или их сочетание.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения острого миелолейкоза (AML), включают в себя, без ограничения, химиотерапевтическое средство (такое как цитарабин, даунорубицин, идарубицин, клофарабин, децитабин, восароксин, азацитидин, клофарабин, рибавирин, CPX-351, треосульфан, элацитарабин, азацитидин), ингибитор тирозинкиназы (такой как ингибитор BCR/ABL (например, иматиниб, нилотиниб), ON 01910.Na, мультикиназный ингибитор (например, мидостаурин, SU 11248, хизартиниб, сорафиниб)), иммунотоксин (такой как гемтузумаба озогамицин), гибридный белок DT388IL3, ингибитор HDAC (такой как вориностат, LBH589), плериксафор, ингибитор mTOR (такой как эверолимус), ингибитор SRC (такой как дазатиниб), ингибитор HSP90 (такой как STA-9090), ретиноид (такой как бексаротен, ингибитор киназы Aurora (такой как BI 811283), ингибитор JAK-2 (такой как INCB018424), ингибитор Polo-подобной киназы (такой как BI 6727), сенерсен, CD45-специфическое средство (такое как BC8), ингибитор циклин-зависимой киназы (такой как UCN-01), антагонист MDM2 (такой как RO5045337), ингибитор mTOR (такой как эверолимус), LY573636-натрий, ZRx-101, MLN4924, леналидомид, иммунотерапевтическое средство (такое как AHN-12), дигидрохлорид гистамина, лучевая терапия, трансплантация костного мозга, трансплантация стволовых клеток, а также их сочетания.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения множественной миеломы (ММ), включают в себя, без ограничения, химиотерапевтическое средство (такое как мелфалан, амифостин, циклофосфамид, доксорубицин, клофарабин, бендамустин, флударабин, адриамицин, SyB L-0501), талидомид, леналидомид, дексаметазон, преднизолон, помалидомид, ингибитор протеасом (такой как бортезомибом, карфилзомиб, MLN9708), противораковая вакцина (такая как GVAX), CD-40-специфическое средство (например, SGN-40, CHIR-12.12), перифосин, золедроновая кислота, иммунотерапевтическое средство (такое как MAGE-A3, NY-ESO-1, HuMax-CD38), ингибитор HDAC (такой как вориностат, LBH589, AR-42), аплидин, ингибитор циклин-зависимой киназы (такой как PD-0332991, динациклиб), триоксид мышьяка, CB3304, ингибитор HSP90 (такой как KW-2478), ингибитор тирозинкиназы (такой как ингибитор EGFR (например, цетуксимаб), мультикиназный ингибитор (такой как AT9283)), ингибитор VEGF (такой как бевацизумаб), плериксафор, ингибитор MEK (такой как AZD6244), IPH2101, аторвастатин, иммунотоксин (такой как BB-10901), NPI-0052, радиоиммунотерапевтическое средство (такое как иттрий Y90 ибритумомаба тиуксетан), ингибитор STAT3 (такой как OPB-31121), MLN4924, ингибитор киназы Aurora (такой как ENMD-2076), IMGN901, АСЕ-041, ингибитор CK-2 (такой как CX-4945), лучевая терапия, трансплантации костного мозга, трансплантации стволовых клеток, а также их сочетания.
Примеры терапевтических средств, подходящих для применения в сочетании с целью лечения рака предстательной железы, включают в себя, без ограничения, химиотерапевтическое средство (такое как доцетаксел, карбоплатин, флударабин), абиратерон, гормональное терапевтическое средство (такое как флутамид, бикалутамид, нилютамид, ципротерона ацетат, кетоконазол, аминоглютетимид, абареликс, дегареликс, лейпролид, гозерелин, трипторелин, бусерелин), ингибитор тирозинкиназы (такой как двойной ингибитор киназы (например, лапатаниб), мультикиназный ингибитор (например, сорафениб, сунитиниб)), ингибитор VEGF (такой как бевацизумаб), TAK-700, противораковая вакцина (такая как BPX-101, PEP223), леналидомид, TOK-001, ингибитор рецептора IGF-1 (такой как циксутумумаб), TRC105, ингибитор киназы Aurora (такой как MLN8237), ингибитор протеасом (такой как бортезомиб), OGX-011, радиоиммунотерапевтическое средство (такое как HuJ591-GS), ингибитор HDAC (такой как вальпроевая кислота, SB939, LBH589), гидроксихлорохин, ингибитор mTOR (такой как эверолимус), довитиниба лактат, дииндолилметан, эфавиренц, OGX-427, генистеин, IMC-3G3, бафетиниб, СР-675206, лучевая терапия, хирургическое вмешательство, или их сочетание.
Сочетанные терапевтические средства можно использовать наряду с одним или несколькими из существующих способов лечения раковых заболеваний, включающих в себя, без ограничения: хирургическое вмешательство; лучевую терапию (такую как наружная дистанционная лучевая терапия, которая включает в себя трехмерную конформную лучевую терапию, в которой создают модель области излучения, локальное облучение (например, облучение, направленное на заранее выбранную мишень или орган), или сфокусированное облучение). Сфокусированное облучение может быть выбрано из группы, включающей в себя стереотаксическую радиохирургию, фракционированную стереотаксическую радиохирургию, и лучевую терапию с модулированной интенсивностью. Для сфокусированного облучения можно использовать источник облучения, выбранный из группы, включающей в себя пучок частиц (протоны), кобальт-60 (фотоны) и линейный ускоритель (рентгенография), например, описанные в WO 2012/177624.
Лучевую терапию можно вводить с помощью одного из нескольких способов, или сочетания способов, включающих в себя, без ограничения, дистанционную лучевую терапию, внутреннюю лучевую терапию, лучевую терапию с использованием имплантатов, стереотаксическую радиохирургию, системную лучевую терапию и постоянную или временную интерстициальную брахитерапию. Термин "брахитерапия" относится к лучевой терапии, которую осуществляют посредством пространственно ограниченного радиоактивного вещества, помещенного в организм непосредственно в участок опухоли или другого пролиферативного заболевания ткани, или вблизи такого участка. Предполагается, что данный термин включает в себя, без ограничения, применение радиоактивных изотопов (таких как At-211, I-131, I-125, Y-90, Re-186, Re-188, Sm-153, Bi-212, P-32 и радиоактивные изотопы Lu). Источники излучения, подходящие для применения в качестве клеточного кондиционирующего средства настоящего изобретения, могут находиться как в твердом, так и в жидком виде. В качестве не ограничивающего примера, источник излучения может представлять собой радионуклид, такой как I-125, I-131, Yb-169, Ir-192, присутствующий в твердом виде, I-125 в твердом виде, или другие радионуклиды, испускающие фотоны, бета-частицы, гамма-излучение или другие терапевтические лучи. Радиоактивное вещество также может находиться в виде жидкости, представляющей собой раствор радионуклида (радионуклидов), например, раствор I-125 или I-131, или в виде жидкости, представляющей собой суспензию содержую мелкие частицы твердых радионуклидов, таких как Au-198, Y-90. Кроме того, радионуклид (радионуклиды) можно включить в гель или радиоактивные микросферы.
Нуклеиновые кислоты
Изобретение также описывает нуклеиновые кислоты, содержащие нуклеотидные последовательности, которые кодируют вариабельные участки тяжелой и легкой цепей, а также CDR или гипервариабельные петли описанных здесь молекул антител. Нуклеиновая кислота может содержать нуклеотидную последовательность, описанную в данном документе, или последовательность, по существу идентичную ей (например, последовательность, идентичную ей, по меньшей мере, примерно на 85%, 90%, 95%, 99% или более, или последовательность, которая отличается не более чем на 3, 6, 15, 30 или 45 нуклеотидов от последовательностей, описанных в приведенных здесь таблицах.
Векторы
Настоящее изобретение также предлагает векторы, содержащие нуклеотидные последовательности, кодирующие описанные здесь молекулы антител. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие описанную здесь молекулу антитела. В одном варианте осуществления векторы содержат описанные здесь нуклеотидные последовательности. Векторы включают в себя, без ограничения, вирусы, плазмиды, космиды, фаги лямбда или искусственные дрожжевые хромосомы (YAC).
Можно использовать разные векторные системы. Например, один класс векторов содержит элементы ДНК, полученные из вирусов животных, таких, как, например, вирус бычьей папилломы, вирус полиомы, аденовирус, вирус коровьей оспы, бакуловирус, ретровирусы (вируса саркомы Рауса, MMTV или MOMLV) или вирус SV40. Другой класс векторов содержит элементы РНК, полученные из РНК-вирусов, таких как вирус леса Семлики, вирус восточного лошадиного энцефалита и флавивирусы.
Кроме того, клетки, которые содержат ДНК, стабильно интегрированную в их хромосомы, можно выбрать путем введения одного или нескольких маркеров, способствующих отбору трансфицированных клеток-хозяев. Например, маркер может обеспечивать прототропию к ауксотрофному хозяину, устойчивость к биоцидам (таким как антибиотики), или устойчивость к тяжелым металлам, таким как медь, и т.п. Селектируемый маркерный ген может быть непосредственно связан с экспрессируемыми последовательностями ДНК, или он может быть введен в ту же клетку путем совместной трансформации. Для оптимального синтеза мРНК могут потребоваться дополнительные элементы. Такие элементы могут включать в себя сигналы сплайсинга, а также промоторы и энхансеры транскрипции и сигналы терминации.
После получения вектора экспрессии или последовательности ДНК, содержащей конструкции, с целью осуществления их экспрессии, векторы экспрессии можно трансфицировать или ввести в соответствующую клетку-хозяина. Трансфекцию можно проводить с помощью разных способов, включающих в себя, например, слияние протопластов, осаждение фосфатом кальция, электропорацию, трансдукцию ретровирусом, вирусную трансфекцию, метод генной пушки, липидную трансфекцию или другие традиционные методы. В случае слияния протопластов клетки выращивают в среде и подвергают скринингу на соответствующую активность.
Способы и условия, используемые для культивирования полученных трансфицированных клеток, а также для извлечения продуцируемых молекул антител, известные специалистам в данной области, можно изменить или оптимизировать в зависимости от конкретного вектора экспрессии и используемой клетки-хозяина млекопитающего, в соответствии с настоящим описанием.
Клетки
Настоящее изобретение также предлагает клетки-хозяева, содержащие нуклеиновую кислоту, кодирующую описанную здесь молекулу антитела.
В одном варианте осуществления клетки-хозяева получают методом генной инженерии с введением в них нуклеиновых кислот, кодирующих молекулы антител.
В одном варианте осуществления клетки-хозяева получают методом генной инженерии с использованием кассеты экспрессии. Фраза "кассета экспрессии" относится к нуклеотидным последовательностям, которые способны влиять на экспрессию гена в организме хозяине, совместимого с такими последовательностями. Такие кассеты могут содержать промотор, открытую рамку считывания с интронами, или без интронов, и сигнал терминации. Также можно использовать и другие факторы, необходимые для осуществления экспрессии, или способствующие экспрессии, такие как, например, индуцируемый промотор.
Настоящее изобретение также предлагает клетки-хозяева, содержащие векторы, описанные в настоящем документе.
Клетка может представлять собой, без ограничения, эукариотическую клетку, бактериальную клетку, клетку насекомого или клетку человека. Подходящие эукариотические клетки включают в себя, без ограничения, клетки Vero, клетки HeLa, клетки COS, клетки СНО, клетки НЕК293, клетки BHK и клетки MDCKII. Подходящие клетки насекомых включают в себя, без ограничения, клетки Sf9.
ПРИМЕРЫ
Пример 1: Влияние средств направленного действия на модуляцию PD-L1
В данном примере оценивают способность выбранного терапевтического средства LDK378 модулировать PD-L1 (CD274). Влияние LDK378 на уровень PD-L1 определяют методами ПЦР в режиме реального времени и проточной цитометрии. Наблюдают значительное ингибирование PD-L1 в опухолевых клетках под действием LDK378.
LDK378 уменьшает уровень мРНК PD-L1
Разработаны анализы ОТ-ПЦР TaqMan для детекции изменения уровня экспрессии PD-L1 (CD274) в клеточных линиях и ксенотрансплантатах опухолей. мРНК выделяют из замороженных клеточных осадков или фрагментов опухоли с помощью набора Qiagen RNeasy Mini. Выделенную РНК замораживают при -80°С. Проверяют качественный состав РНК и затем проводят количественное определение РНК с помощью 2100 Agilent Bioanalyzer, в соответствии с инструкциями для набора Agilent RNA 6000 Nano. кДНК получают с использованием набора для синтеза кДНК на РНК-матрице с высокой пропускной способностью (Applied Biosystems).
Реакции ПЦР в режиме реального времени проводят в общем объеме 20 мкл, содержащем 10 мкл универсального мастер-микса для ПЦР (Applied Biosystems), 1 мкл набора зонд/праймер человеческого PD-L1 (CD274) (Applied Biosystems) и 8 мкл кДНК. Каждый образец используют с тройными повторами. В каждой реакции ПЦР используют количество кДНК, полученное из 25-50 нг РНК в результате обратной транскрипции. Вследствие разницы в уровнях мРНК PD-L1 и GAPDH две реакции ПЦР в режиме реального времени проводят в отдельных пробирках, используя одинаковое количество кДНК. Реакции ПЦР в режиме реального времени проводят на C1000 Thermal Cycle (BioRad), используя следующую циклическую программу: инкубация при 95°С в течение 10 минут, затем 40 циклов при 95°С в течение 15 секунд и при 60°С в течение 1 минуты. После завершения реакции среднее значение Ct PD-L1 нормализуют по каждому значению Ct стандартной реакции получением GAPDH. Затем каждое нормализованное логарифмическое значение преобразуют в линейное значение.
Ингибирование мРНК PD-L1 под действием LDK378 наблюдают в H3122 (клетки немелкоклеточного рака легких (NSCLC) с транслокацией ALK) in vitro (фигура 1).
Результаты, приведенные в настоящем документе, демонстрируют участие LDK378 в регуляции молекул иммунной контрольной точки при раке. Наблюдаемое ингибирование экспрессии PD-L1 под действием LDK378 позволяет предположить, что данное средство с направленным действием может обладать способностью модулировать иммунный ответ, помимо его влияния на передачу сигнала при раке. Таким образом, представленные здесь результаты демонстрируют, что введение направленного средства LDK378 вместе с ингибитором иммунной контрольной точки, такой как PD1, PD-L1, LAG3 и/или TIM3, позволяет достичь более эффективного обратного развития подавления иммунитета, опосредованного иммунной контрольной точкой.
Пример 2: Клиническое исследование, проводимое для оценки эффективности и безопасности сочетания серитиниба и ниволумаба
Эффективность и безопасность сочетания серитиниба и ниволумаба можно оценить в открытом, многоцентровом исследовании с увеличением дозы и расширением ее применения, в котором помимо безопасности и эффективности также можно исследовать переносимость и PK/PD сочетания серитиниба и ниволумаба, используемого для лечения пациентов с метастатическим, ALK-положительным NSCLC. Исследование можно начинать с периода скрининга, который может продолжаться вплоть до 28 дней включительно перед введением первой дозы исследуемых средств, с целью оценки приемлемости. Период лечения может начинаться в первый день первого цикла. Продолжительность цикла составляет 28 дней.
Лечение серитинибом и ниволумабом может продолжаться, например, до тех пор, пока пациент не начнет испытывать неприемлемую токсичность, исключающую возможность дальнейшего лечения, и/или до тех пор, пока не будет установлено прогрессирование заболевания.
В случаях обособленного прогрессирования в мозге, или другого локального прогрессирования, пациенты могут дополнительно получать паллиативную лучевую терапию.
Исследование может включать в себя фазу повышения дозы и фазу расширения применения дозы.
1. Фаза повышения дозы
Фаза исследования с повышением дозы позволяет определить максимально переносимую дозу (MTD)/рекомендуемую для расширенного исследования дозу (RDE) сочетания, включающего в себя серитиниб, вводимый перорально и ежедневно с пищей пониженной жирности, и ниволумаб, вводимый внутривенно каждые 2 недели (Q2W), на основании значений дозо-лимитирующей токсичности (DLT), полученных с использованием байесовской модели логистической регрессии (BLRM). Например, в данной фазе исследования могут участвовать 12 пациентов. Исходный уровень дозы серитиниба может составлять 450 мг в сутки при введении ниволумаба в дозе 3 мг/кг Q2W. Используют следующие предварительные уровни доз:
- [-1 экспериментальная группа] серитиниб 300 мг+ниволумаб (3 мг/кг)
- [1ая экспериментальная группа] серитиниб 450 мг+ниволумаб (3 мг/кг)
- [2ая экспериментальная группа] серитиниб 600 мг+ниволумаб (3 мг/кг)
MTD представляет собой самую высокую дозу лекарственного средства при применении обоих средств, которая не вызывает DLT более чем у 35% пациентов в течение первых 6 недель лечения. Окончательную рекомендованную MTD/RDE для сочетания серитиниба и ниволумаба определяют на основании рекомендаций BLRM, а также на основании общей оценки безопасности с учетом значений переносимости и фармакокинетических данных, полученных в последующих циклах с использованием тестируемых доз. Если MTD для сочетания серитиниба и ниволумаба невозможно установить после анализа всех запланированных уровней доз, включающих в себя целевые дозы серитиниба (600 мг с пищей низкой жирности) и ниволумаба (3 мг/кг), то RDE определяют путем анализа всех доступных значений безопасности, PK и эффективности.
2. Фаза расширенного применения
После определения MTD для сочетания и/или RDE проводят фазу расширенного исследования, в которой используют дополнительных пациентов, получающих сочетание в дозе, соответствующей RDE. Например, в фазе расширенного исследования могут участвовать 60 пациентов. Фазу расширенного исследования, которая позволяет определить безопасность и предварительное значение эффективности сочетания серитиниба и ниволумаба при RDE, проводят в 2 группах (примерно по 30 пациентов в каждой группе):
- Группа 1: пациенты, получавшие ингибитор ALK (допускается предшествующее лечение любым ингибитором ALK, кроме серитиниба).
- Группа 2: пациенты, не получавшие ингибитор ALK
Сбор данных для отчета о первичном клиническом исследовании можно прекращать после того, как все пациенты, участвующие в фазе расширения, завершают, по меньшей мере, 6 циклов (24 недели) лечения, или ранее прекращают участие в исследовании.
Пример 3: Клинические эффекты сочетания LDK378 и ниволумаба
Восемь пациентов входят в первую экспериментальную группу исследования, описанную в примере 2, и ниже приведены данные, полученные для единственного пациента с имеющейся достоверной оценкой опухоли. У данного пациента наблюдается частичный ответ. Для подтверждения ответа необходима вторая оценка.
Оцениваемым пациентом является 64-летний кавказец мужского пола с диагностированным NSCLC IV стадии. Пораженные болезнью участки включают в себя легкие, надпочечники и абдоминальные лимфатические узлы. У пациента после одного предварительного курса химиотерапии цисплатином и пеметрекседом наблюдается частичная ремиссия. Другие медицинские состояния включают в себя недостаточность надпочечников, пролапс митрального клапана, гиперхолестеринемию и мочекаменную болезнь.
Участвующий в исследовании пациент начинает лечение, включающее в себя введение 450 мг LDK378 QD (перорально) с пищей низкой жирности в сочетании с ниволумабом 3 мг/кг каждые 2 недели (внутривенно). Через 29 дней после введения первой дозы исследуемого препарата (сочетание LDK378+ниволумаб) у пациента наблюдается лихорадка, боль в животе, тошнота и рвота. Ультразвуковое исследование брюшной полости имеет отрицательный результат, однако компьютерная томография (CT) брюшной полости демонстрирует наличие острого панкреатита. Кроме того, наблюдается повышение уровней липазы, амилазы, ALT, AST, билирубина, ALP и GGT. Пациента госпитализируют и лечение исследуемым препаратом LDK378 временно прекращают. Проводят лечение путем внутривенного вливания парацетамола, контрамола (трамадола гидрохлорид) и литикана (ализаприд). В последующие дни результаты лабораторных анализов и состояние пациента улучшаются; пациент больше не жалуется на боль, лихорадку, тошноту и рвоту. Введение всех поддерживающих лекарственных средств останавливают и пациента выписывают из больницы.
При последующем обследовании в клинике жалобы не выявлены (лихорадка, тошнота, рвота или боль в животе отсутствуют). После выписки из больницы пациент не получает обезболивающие или противорвотные средства. Биохимический анализ крови демонстрирует:
липаза и амилаза в пределах нормы, Gr1:билирубин, AST и ALT Gr2:щелочная фосфатазы 3 степени:GGT
Через 1 день после обследования в клинике возобновляют введение LDK378 в пониженной дозе 300 мг в день. Лечение ниволумабом возобновляют примерно через неделю.
Пациента один раз вырвало в отсутствии тошноты или боли в животе. Пациент нетемпературящий, хотя один раз температура повышалась до 38 градусов. Жалобы на физическое состояние у пациента отсутствуют.
Результаты лабораторных анализов после возобновления введения ниволумаба: AST: 120 ед/л, ALT: 139 ед/л, билирубин общий 33 мкмоль/л, щелочная фосфатаза 551 ед/л. Амилаза и липаза в норме.
Введение LDK378 прекращают и возобновляют в дозе 300 мг.
Оценка опухоли:
Результаты CT при первой оценке опухоли демонстрируют снижение общих целевых поражений на 62,9% в правом надпочечнике и брюшных лимфатических узлах по сравнению с исходными данными CT. Также существуют данные, свидетельствующие о наличии нецелевых поражений левой нижней доли легкого.
ВКЛЮЧЕНИЕ ПУТЕМ СЫЛКИ
Все упомянутые здесь публикации, патенты и номера доступа включены в настоящее описание в качестве ссылки во всей их полноте, как если бы каждая отдельная публикация или патент были конкретно и индивидуально указаны как включенные в качестве ссылки.
ЭКВИВАЛЕНТЫ
Хотя здесь описаны конкретные варианты осуществления настоящего изобретения, приведенное выше описание является иллюстративным, но не ограничивающим. Многие изменения настоящего изобретения будут очевидны для специалистов в данной области после рассмотрения настоящего описания и приведенной ниже формулы изобретения. Полный объем изобретения должен определяться формулой изобретения, наряду с полным объемом эквивалентов, и описанием, наряду с указанными изменениями.
--->
SEQUENCE LISTING
<110> NOVARTIS AG
<120> СОЧЕТАННЫЕ СПОСОБЫ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ ИНГИБИТОРОВ ALK
<130> C2160-7013WO
<140>
<141>
<150> 62/199,030
<151> 2015-07-30
<150> 62/119,060
<151> 2015-02-20
<150> 62/059,788
<151> 2014-10-03
<150> 62/050,116
<151> 2014-09-13
<160> 7
<170> PatentIn version 3.5
<210> 1
<211> 5
<212> Белок
<213> Неизвестный
<220>
<221> source
<223> /note="Описание неизвестного белка:
пептидный мотив PD-1"
<400> 1
Met Tyr Pro Pro Tyr
1 5
<210> 2
<211> 440
<212> Белок
<213> Искусственная последовательность
<220>
<221> source
<223> /note="Описание искусственной последовательности: синтетический
полипептид"
<400> 2
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser
115 120 125
Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys
180 185 190
Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
210 215 220
Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
225 230 235 240
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
245 250 255
Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
260 265 270
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
275 280 285
Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
290 295 300
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
305 310 315 320
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
325 330 335
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr
340 345 350
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
355 360 365
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
370 375 380
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
385 390 395 400
Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe
405 410 415
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
420 425 430
Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 3
<211> 214
<212> Белок
<213> Искусственная последовательность
<220>
<221> source
<223> /note="Описание искусственной последовательности: синтетический
полипептид"
<400> 3
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 4
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<221> source
<223> /note="Описание искусственной последовательности: синтетический
полипептид"
<400> 4
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 5
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<221> source
<223> /note="Описание искусственной последовательности: синтетический
полипептид"
<400> 5
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 6
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> source
<223> /note="Описание искусственной последовательности: синтетический
полипептид"
<400> 6
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ile Met Met Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Pro Ser Gly Gly Ile Thr Phe Tyr Ala Asp Lys Gly
50 55 60
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
65 70 75 80
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
85 90 95
Ile Lys Leu Gly Thr Val Thr Thr Val Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 7
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> source
<223> /note="Описание искусственной последовательности: синтетический
полипептид"
<400> 7
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОЛЕКУЛЫ АНТИТЕЛ К PD-1 И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2788092C2 |
| РЕЖИМЫ ДОЗИРОВАНИЯ АНТИТЕЛ АНТИ-LAG-3 И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2801208C2 |
| ИНГИБИТОРЫ FGFR2 ОТДЕЛЬНО ИЛИ В КОМБИНАЦИИ С ИММУНОСТИМУЛИРУЮЩИМИ АГЕНТАМИ В ЛЕЧЕНИИ РАКА | 2016 |
|
RU2834309C2 |
| АНТИТЕЛА ПРОТИВ PD-1 И КОМПОЗИЦИИ | 2016 |
|
RU2750675C1 |
| ИНГИБИТОРЫ FGFR2 ОТДЕЛЬНО ИЛИ В КОМБИНАЦИИ С ИММУНОСТИМУЛИРУЮЩИМИ АГЕНТАМИ В ЛЕЧЕНИИ РАКА | 2016 |
|
RU2745707C2 |
| АНТИТЕЛА К PD-1(CD279) | 2017 |
|
RU2752562C2 |
| ЛЕЧЕНИЕ РАКА КОМБИНАЦИЕЙ АНТАГОНИСТА PD-1 И ДИНАЦИКЛИБА | 2014 |
|
RU2705795C2 |
| КОМБИНАЦИЯ АНТАГОНИСТА PD-1, ИНГИБИТОРА ТИРОЗИНКИНАЗЫ VEGFR/FGFR/RET И ИНГИБИТОРА CBP/БЕТА-КАТЕНИНА ДЛЯ ЛЕЧЕНИЯ РАКА | 2020 |
|
RU2838452C1 |
| НОВАЯ КОМБИНАЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ | 2016 |
|
RU2742494C2 |
| БЕЛКИ НА ОСНОВЕ АНТИТЕЛ С ПРИВИТЫМ ЦИТОКИНОМ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ РАКА | 2018 |
|
RU2815389C2 |
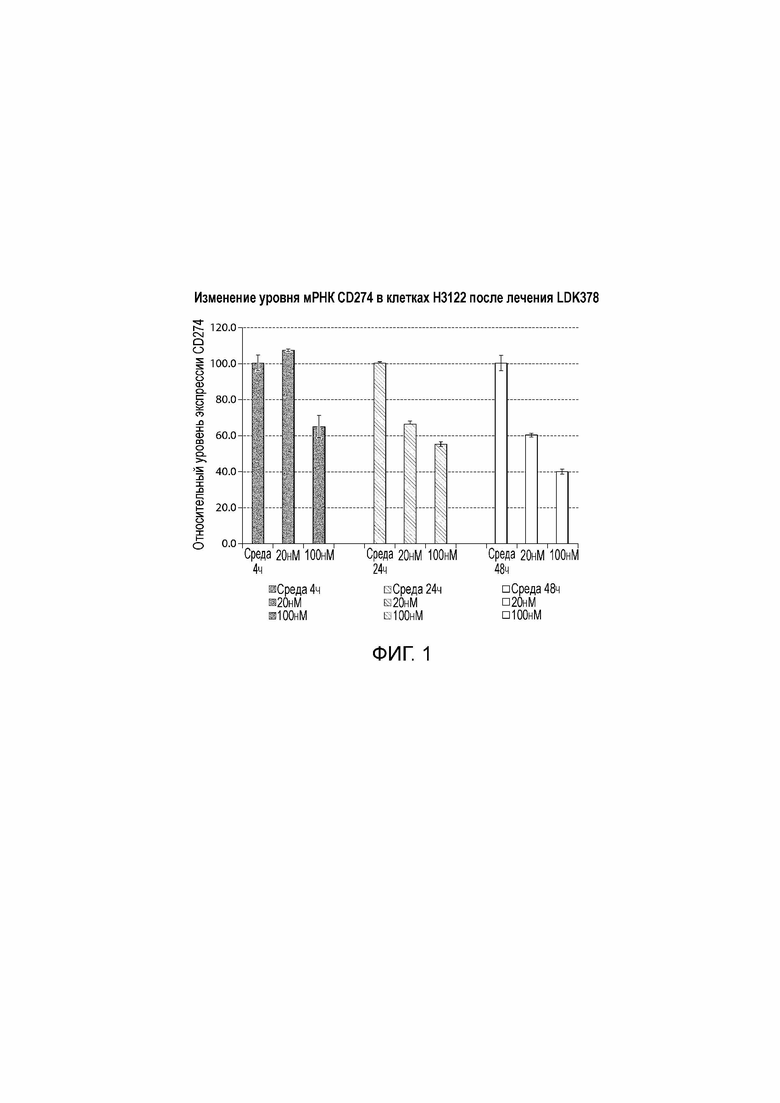
Изобретение относится к медицине и касается способа лечения пациента, имеющего немелкоклеточный рак лёгкого с транслокацией ALK, включающего введение указанному пациенту терапевтически эффективного количества серитиниба в комбинации с ниволумабом. Изобретение обеспечивает модулирование иммунного ответа. 1 з.п. ф-лы, 1 ил., 2 табл., 3 пр.
1. Способ лечения пациента, имеющего немелкоклеточный рак лёгкого с транслокацией ALK, включающий введение указанному пациенту терапевтически эффективного количества серитиниба в комбинации с ниволумабом.
2. Способ по п.1, где указанная транслокация ALK представляет собой гибрид EML4-ALK.
| WO 2013059740 A1, 25.04.2013 | |||
| US 20140099254 A1, 10.04.2014 | |||
| FISHER TS | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| CAMIDGE DR | |||
| et al | |||
| Activity and safety of crizotinib in patients with ALK-positive | |||
Авторы
Даты
2020-04-15—Публикация
2015-09-11—Подача