Изобретение относится к области органической химии, а именно к структуре и биологической активности новых индивидуальных соединений класса хиноксалинилиденбутанамидов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и обладающих анальгетической активностью, что позволяет предположить их использование в медицине в качестве лекарственных средств с анальгетическими свойствами.
Аналогом по структуре заявляемому ряду соединений являются (Z)-4-арил-2,4-диоксо-3-(2-оксо-1,2,3,4-тетрагидро-3-хиноксалнилиден)бутановые кислоты [А.Н. Масливец, И.В. Машевская, Ю.С. Андрейчиков. Пятичленные 2,3-диоксогетероциклы. XL*. Взаимодействие 3-ароил-1,2-дигидро-4H-пирроло[5,1-с][1,4]бензоксазин-1,2,4-трионов с о-фенилендиамином // ЖОрХ. 1995. Т. 31. №4. с. 616-619] формулы:
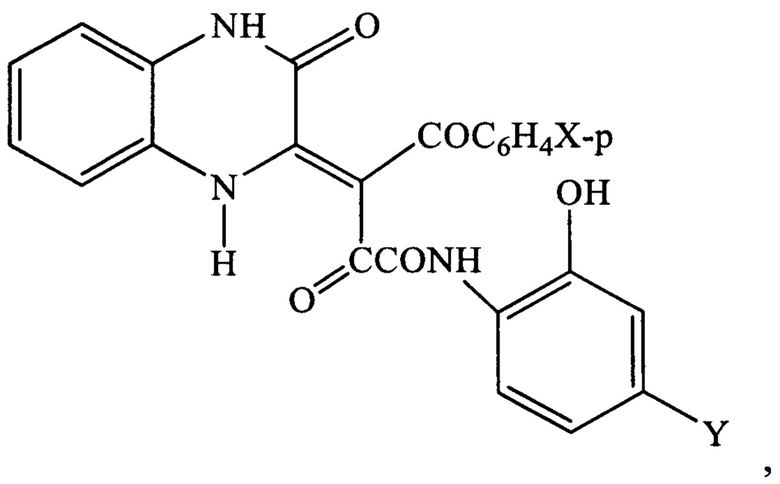
где X=Y=Н; X=СН3, Y=Н; X=Y=СН3
В качестве эталона сравнения по фармакологическому действию выбран известный практической медицине анальгетический препарат, метамизол натрия (анальгин).
Задачей изобретения является поиск в ряду производных хиноксалинилиденбутанамидов веществ с выраженным анальгетическим действием и низкой токсичностью, расширение арсенала средств воздействия на живой организм.
Поставленная задача достигается синтезированием ряда (Z)-4-арил-N-[2-(2-гидроксиметил)фенил]-2,4-диоксо-3-[3-оксо-3,4-дигидрохиноксалин-2(1H)-илиден]бутанамидов формулы:
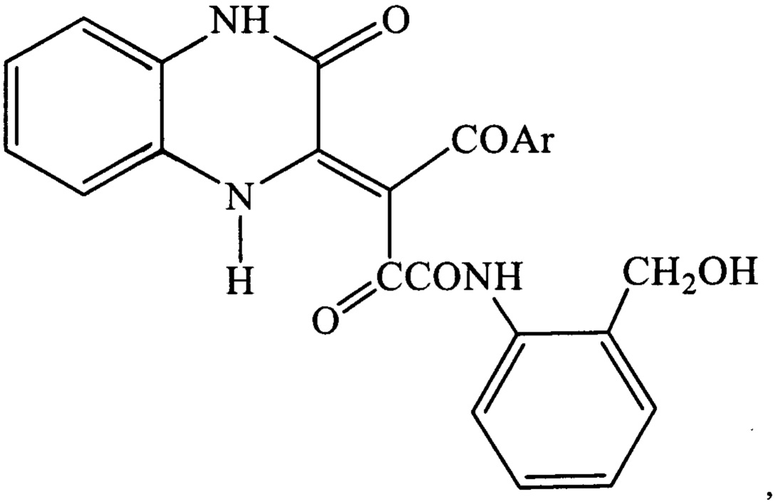
где Ar = 4-ClC6H4, 4-СН3С6Н4, 4-СН3ОС6Н4.
Полученные соединения проявляют анальгетическую активность.
Заявляемые соединения синтезируют взаимодействием 3-ароилпирроло[1,2-с][4,1]бензоксазепин-1,2,4-трионов с о-фенилендиамином в кипящем безводном хлороформе в течение 4-5 мин по следующей схеме:
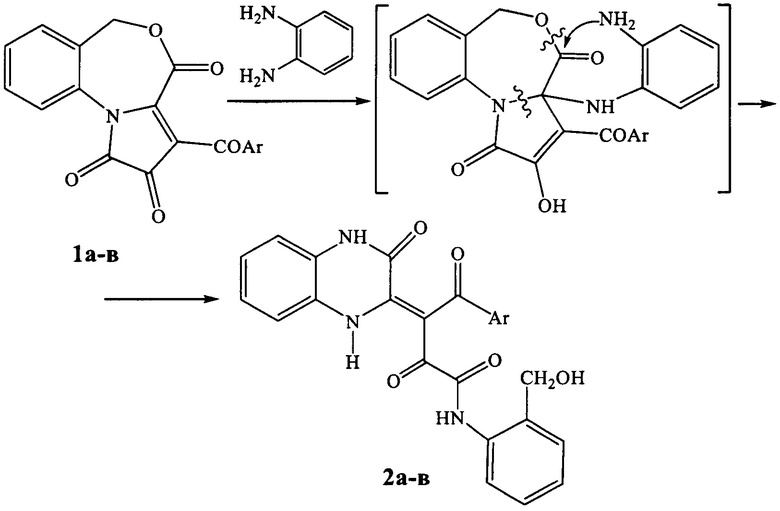
где Ar = 4-ClC6H4 (а), 4-СН3С6Н4 (б), 4-СН3ОС6Н4 (в).
Изобретение иллюстрируется следующими примерами.
Пример 1. (Z)-N-[2-(2-гидроксиметил)фенил]-2,4-диоксо-3-[3-оксо-3,4-дигидрохиноксалин-2(1H)-илиден]-4-(4-хлорфенил)бутанамид (2а). Раствор 1.0 ммоль соединения 3-(4-хлорфенил)пирроло[1,2-с][4,1]бензоксазепин-1,2,4-триона (1а) и 1.0 ммоль о-фенилендиамина в 40 мл безводного хлороформа кипятили 5 мин (до исчезновения ярко-красной окраски исходного соединения), охлаждали, образовавшийся осадок отфильтровывали. Выход 97,5%, т.пл. 216-217°С (разл., хлороформ). Соединение (2а) C25H18ClN3O5
Найдено, %: С 63.13; Н 3.88; Cl 7.39; N 8.77.
Вычислено, %: С 63.10; Н 3.81; Cl 7.45; N 8.83.
Соединение (2а) - желто-оранжевое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в менее полярных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (2а), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний, ν, см-1: 3308 (ОН), 3162, 3109 (NH), 1687, 1644 (С3=Охинокс., С4=O, С1=O), 1582 ш (С2=O).
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 4.59 с (2Н, СН2), 5.68 с (1Н, ОН), 7.10-7.83 гр.с (12Н, 3С6Н4), 10.52 с (1Н, C1ONH), 12.22 с (1Н, N4'H), 14.68 с (1Н, N1'H).
Пример 2. (Z)-N-[2-(2-гидроксиметил)фенил]-4-(4-метилфенил)-2,4-диоксо-3-[3-оксо-3,4-дигидрохиноксалин-2(1H)-илиден]бутанамид (26). Раствор 1.0 ммоль соединения 3-(метилфенил)пирроло[1,2-с][4,1]бензоксазепин-1,2,4-триона (1б) и 1.0 ммоль о-фенилендиамина в 40 мл безводного хлороформа кипятили 5 мин (до исчезновения ярко-красной окраски исходного соединения), охлаждали, образовавшийся осадок отфильтровывали. Выход 95%, т.пл. 215-216°С (разл., хлороформ). Соединение (2б) C26H21N3O5
Найдено, %: С 68.50; Н 4.69; N 9.20.
Вычислено, %: С 68.56; Н 4.65; N 9.23.
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 2.33 с (3Н, СН3), 4.58 с (2Н, СН2), 5.65 с (1Н, ОН), 7.09-7.77 гр.с (12Н, 3С6Н4), 10.44 с (1Н, C1ONH), 12.17 с (1Н, N4'H), 14.63 с (1Н, N1'H).
ИК спектр, ν, см-1: 3303 (ОН), 3160 (NH), 1689 ш, 1643 (С3=Охинокс., С4=O, С1=O), 1579 (С2=O).
Пример 3. (Z)-N-[2-(2-гидроксиметил)фенил]-4-(4-метоксифенил)-2,4-диоксо-3-[3-оксо-3,4-дигидрохиноксалин-2(1H)-илиден]бутанамид (2в). Раствор 1.0 ммоль соединения 3-(4-метоксифенил)пирроло[1,2-с][4,1]бензоксазепин-1,2,4-триона (1в) и 1.0 ммоль о-фенилендиамина в 40 мл безводного хлороформа кипятили 5 мин (до исчезновения ярко-красной окраски исходного соединения), охлаждали, образовавшийся осадок отфильтровывали. Выход 91,5%, т.пл. 217-218°С (разл., хлороформ). Соединение (2в) C26H21N3O6
Найдено, %: С 66.19; Н 4.54; N 8.96.
Вычислено, %: С 66.24; Н 4.49; N 8.91.
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 3.27 с (3Н, ОСН3), 4.58 с (2Н, СН2), 5.64 с (1H, ОН), 6.94-7.76 гр.с (12Н, 3C6H4), 10.43 с (1Н, C1ONH), 12.15 с (1Н, N4'H), 14.65 с (1Н, N1'H).
ИК спектр, ν, см-1: 3313 (ОН), 3182 (NH), 1687 ш, 1635 (С3=Охинокс., С4=O, С1=O), 1575 (С2=O).
Пример 4. Фармакологическое исследование соединений 2а-в на наличие анальгетической активности.
Оценку анальгетических свойств соединений изучали на беспородных мышах массой 18-22 грамм методом термического раздражения «горячая пластинка» по Эдди и Леймбах (Eddy N.B., Leimbarh D.J. - Pharmacol and Exper. Gher., 1953, 385-393).
Исследуемое соединение вводили внутрибрюшинно в виде 2% крахмальной слизи в дозе 50 мг/кг за 0,5 ч до помещения животных на нагретую до 53,5°С металлическую пластинку. У интактных животных латентный период оборонительного рефлекса не превышает 10 сек. Показателем болевой чувствительности служила длительность пребывания животного на горячей пластинке до момента облизывания задних лапок, измеряемая в секундах. В качестве препарата сравнения использовали метамизол натрия (М.Д. Машковский, «Лекарственные средства», т. 1, стр. 184, М., Медицина, 1978).
Проведенные исследования показали (см. табл.), что соединения обладают анальгетической активностью. Данные о фармакологической активности структурных аналогов заявляемых соединений в доступной литературе отсутствуют.
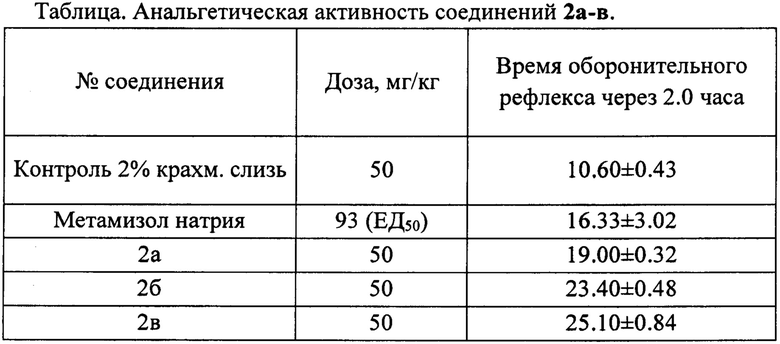
Как видно из данных таблицы, заявляемые соединения достоверно увеличивает время оборонительного рефлекса до 25.10±0.84 с (2в), что выше, чем у препарата сравнения метамизола натрия (16,33±3,02 с). При этом следует учесть, что испытуемая доза метамизола натрия (93 мг/кг) почти в 2 раза превосходит дозу исследуемых соединений (50 мг/кг).
Изобретение относится к (Z)-4-арил-N-[2-(2-гидроксиметил)фенил]-2,4-диоксо-3-[3-оксо-3,4-дигидрохиноксалин-2(1H)-илиден]бутанамидам общей формулы, представленной ниже, где Ar = 4-ClC6H4, 4-CH3C6H4, 4-СН3ОС6Н4. Технический результат – получены новые соединения, которые могут найти применение в медицине в качестве лекарственных средств с анальгетическими свойствами. 4 пр., 1 табл.
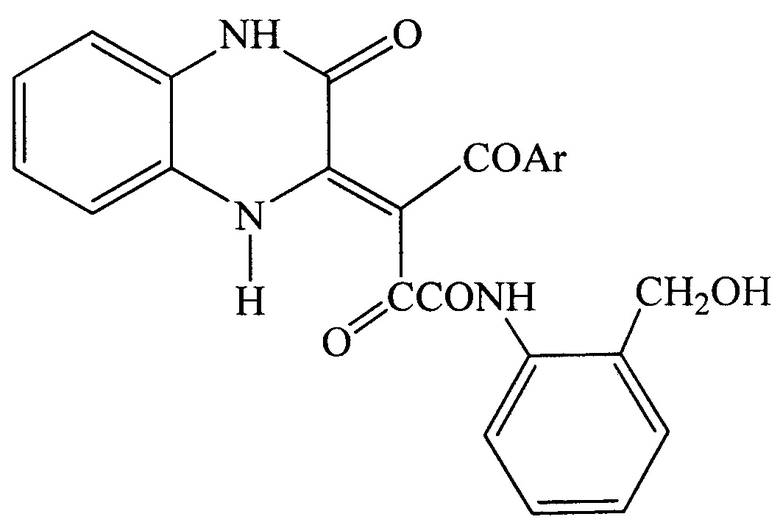
(Z)-4-арил-N-[2-(2-гидроксиметил)фенил]-2,4-диоксо-3-[3-оксо-3,4-дигидрохиноксалин-2(1H)-илиден]бутанамиды общей формулы
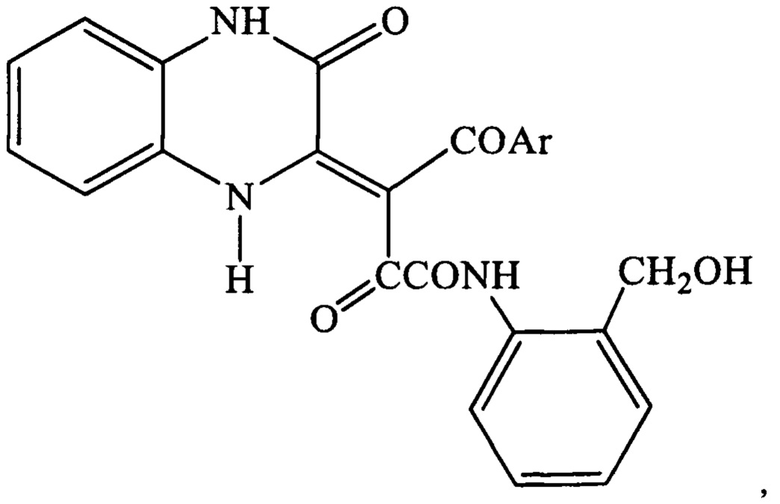
где Ar = 4-ClC6H4, 4-CH3C6H4, 4-СН3ОС6Н4,
обладающие анальгетической активностью.
Авторы
Даты
2020-05-28—Публикация
2019-09-06—Подача