Изобретение относится к области медицины, а именно сердечно-сосудистой хирургии, и может использоваться для профилактики тромбоэмболических осложнений в отдаленные сроки после коронарного шунтирования, включающего резекцию ушка левого предсердия без искусственного кровообращения у больных с фибрилляцией предсердий (ФП).
Ушко левого предсердия (ЛП) при фибрилляции предсердий является основным источником тромбоэмболий артерий большого круга кровообращения, наиболее часто в сосуды головного мозга [1]. Эмболия сосудов головного мозга приводит к развитию ишемического инсульта, нередко фатального; эмболии висцеральных артерий также являются жизнеугрожающими осложнениями, а при эмболиях магистральных артерий конечностей происходит внезапное прекращение кровоснабжения конечности с развитием острой ишемии и возможной гангрены [2]. Поиск эффективных мер профилактики эмболии, в том числе хирургических способов, у больных с ФП продолжается [3, 4].
В настоящее время существует 2 вида хирургических способов «выключения» ушка ЛП у больных с ФП: эндокардиальные и эпикардиальные. Эндокардиальные способы заключаются в эндоваскулярной имплантации окклюдеров ушка ЛП. Авторитетные исследования PROTECT и PREVAIL AF, показали высокую эффективность этих методов в профилактике эмболии у больных с ФП в отдаленные сроки после операции [5]. Эти способы применяются изолированно при отсутствии необходимости открытых операций на сердце.
При необходимости выполнения открытых операций на сердце, в частности, коронарного шунтирования у больных ишемической болезнью сердца и ФП, применяются эпикардиальные способы удаления ушка ЛП. Наиболее известные способы: перевязка ушка простой лигатурой или кисетным швом [6], прошивание ушка степплером [7], наложение на ушко специальной эпикардиальной клипсы AtriClip [8], инвагинация ушка в просвет левого предсердия [9], ампутация ушка с последующим шовным закрытием культи в условиях искусственного кровообращения [4]. Такое многообразие методик свидетельствует, что окончательного решения рассматриваемой проблемы пока не найдено [10].
У каждого из вышеперечисленных способов наряду с достоинствами имеются и недостатки. Перевязка ушка лигатурой или кисетным швом - наиболее простая процедура и наименее надежная в отдаленном периоде. К недостаткам этих методик относят высокую вероятность неполного закрытия просвета ушка и высокую частоту реканализации ушка ЛП в отдаленные сроки [11]. Неполное закрытие просвета и/или реканализация ушка способно привести даже к увеличению риска тромбоэмболических осложнений в отдаленные сроки после операции [6] и не может сравниться по надежности с полной резекцией ушка [12].
Прошивание основания ушка ЛП степплером с последующей резекцией или наложение эпикардиальной клипсы AtriClip требует наличия специального дорогостоящего оборудования и расходного материала. Широкого применения в кардиохирургической практике эти методики, несмотря на их высокую эффективность, из-за высокой стоимости не нашли.
Ручное ушивание культи ЛП после удаления ушка проводится в условиях искусственного кровообращения (ИК). Это наиболее часто используемая методика эпикардиальной резекции ушка.
Следует отметить, что расположение ушка ЛП в ране имеет свои особенности. Ушко ЛП располагается относительно «неудобно» для хирурга при типичном доступе из стернотомии - латерально позади легочной артерии у основания сердца. Из раны ушко ЛП не визуализируется, а доступ к нему обычно затруднен. Подключение аппарата ИК необходимо для снятия давления со стенок сердца, что позволяет безопасно вывернуть сердце и получить доступ к ушку ЛП. Это минимизирует вероятность развития хирургических осложнений и создает возможность лечения интраоперационных осложнений в случае их развития. Известно, что удаление ушка ЛП может сопровождаться хирургическими интраоперационными осложнениями, такими как неконтролируемое кровотечение из левого предсердия и повреждение близлежащих структур - верхней левой легочной вены, митрального клапана, огибающей артерии сердца [13]. Лечение таких осложнений без аппарата ИК часто невозможно.
В современных условиях существует большая категория пациентов (так называемые «пациенты высокого хирургического риска»), в первую очередь больные пожилого и старческого возраста, больные с тяжелой сопутствующей патологией, которым подключение аппарата ИК в ходе кардиохирургического вмешательства крайне нежелательно из-за высокого риска послеоперационных осложнений, связанных с искусственным кровообращением. По данным отдельных авторов, подключение аппарата ИК может в 3,6 раз увеличить 30-дневную летальность у больных пожилого и старческого возраста при выполнении открытых операций на сердце [14]. Таким пациентам коронарное шунтирование безопаснее выполнять на работающем сердце без искусственного кровообращения [15].
Таким образом, у значительной группы пациентов с ИБС и ФП существует необходимость выполнения коронарного шунтирования с одновременной резекцией ушка ЛП на работающем сердце, избегая использования аппарата искусственного кровообращения.
Эффективных и безопасных способов шовной пластики культи ЛП после удаления ушка на работающем сердце, исключая использование аппарата искусственного кровообращения, к настоящему времени не предложено.
По наиболее близкой технической сущности в качестве прототипа нами выбран способ удаления ушка левого предсердия при выполнении изолированного коронарного шунтирования у больных с фибрилляцией предсердий при открытых операциях на сердце с использованием аппарата ИК [4].
К недостаткам способа, выбранного нами в качестве прототипа, можно отнести недостаточную эффективность способа, проявляющуюся в риске развития в ближайшем послеоперационном периоде, ввиду использования аппарата ИК, побочных эффектов в виде системной воспалительной реакции, высокой вероятности развития полиорганной (сердечной, дыхательной, печеночно-почечной) недостаточности, особенно у пожилых пациентов и больных с распространенной сопутствующей патологией, высокой потребности в гемотрансфузиях, что в совокупности увеличивает время проведения искусственной вентиляции легких (ИВЛ) после операции и продолжительность лечения пациента в отделении реанимации.
Задачей изобретения является:
• снижение риска осложнений в ближайшем послеоперационном периоде, в виде системной воспалительной реакции, высокой вероятности развития полиорганной (сердечной, дыхательной, печеночно-почечной) недостаточности, особенно у пожилых пациентов и больных с распространенной сопутствующей патологией;
• уменьшение потребности в проведении гемотрансфузий в периоперационном периоде;
• снижение длительности ИВЛ после операции;
• сокращение послеоперационного койко-дня в отделении реанимации.
Техническим результатом изобретения является обеспечение возможности выполнения способа удаления ушка левого предсердия при выполнении изолированного коронарного шунтирования у больных с фибрилляцией предсердий при открытых операциях на сердце без использования аппарата ИК.
Технический результат изобретения достигается тем, что способ резекции ушка ЛП при коронарном шунтировании у больных с фибрилляцией предсердий при открытых операциях на сердце заключается в выполнении полной срединной стернотомии, вскрытии перикарда, выделении сосудистых аутотрансплантатов, формировании дистальных анастомозов аутотрансплантатов с целевыми коронарными артериями, вертикализации сердца, перед выполнением которой накладывают глубокие тракционные швы на перикард позади левого предсердия. После чего прижимают боковую стенку сердца под основанием ушка ЛП вакуумным стабилизатором миокарда. Затем накладывают изогнутый атравматический зажим с прямыми браншами на основание ушка ЛП. После чего под браншами накладывают непрерывный горизонтальный матрасный шов атравматичной мононитью 4/0. Эпикардиальную резекцию ушка ЛП осуществляют над браншами закрытого зажима, причем при невскрытой полости левого предсердия с последующим снятием зажима и наложением обратного обвивного шва той же нитью с захватом предыдущего шва и основания ушка левого предсердия до первого конца нити. Причем резекцию ушка ЛП и шовное закрытие его культи выполняют на работающем сердце, исключая подключение аппарата искусственного кровообращения
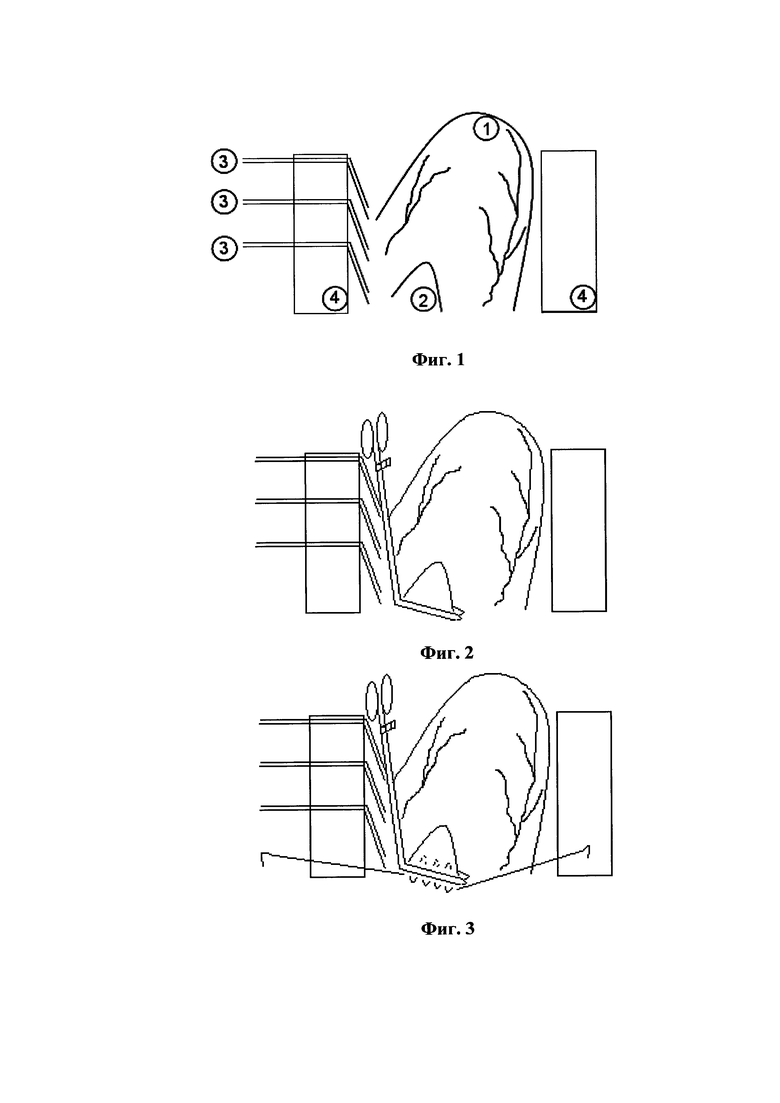
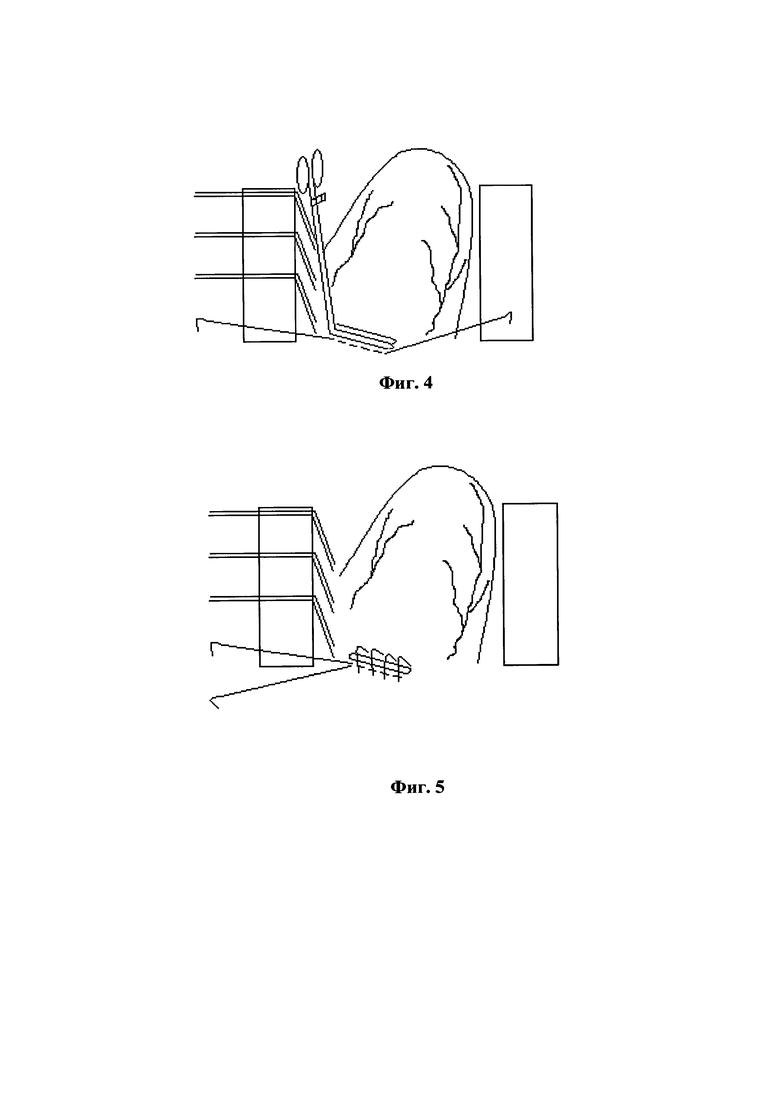
Способ осуществляется следующим образом: Операцию выполняют на фоне системной антикоагуляции. В дооперационном периоде пациенту назначают подкожное введение низкомолекулярных гепаринов в терапевтических дозировках (фрагмин или клексан). Последнее введение низкомолекулярных гепаринов выполняют за 24 часа до начала операции. Под наркозом выполняют полную продольную срединную стернотомию. Выделяют необходимые для формирования шунтов сосудистые аутотрансплантаты. Внутривенно вводят расчетную дозу гепарина из расчета 0,05 мл (100 ME) гепарина на 1 кг массы тела пациента. Достижение требуемой гипокоагуляции контролируют аппаратом для измерения активированного времени свертывания крови (не менее 300 секунд). Вскрывают перикард. С использованием вакуумного стабилизатора миокарда по общепринятой методике на работающем сердце без подключения аппарата ИК формируют дистальные анастомозы сосудистых аутотрансплантатов с целевыми коронарными артериями. Далее проводят вертикализацию сердца, перед выполнением которой накладывают 3 глубоких тракционных шва на перикард позади левого предсердия, лигатуры выводят из операционной раны и натягивают. Одновременно с натяжением лигатур оператор рукой вертикализирует сердце, чтобы получить доступ к тупому краю сердца и ушку левого предсердия. Фиг. 1 иллюстрирует вертикализацию сердца (выведение сердца в рану, которая представлена со стороны головы пациента), где 1 - верхушка левого желудочка, 2 - ушко левого предсердия, 3 - глубокие швы на перикард, наложенные позади левого предсердия, выведенные из раны и натянутые, 4 - пластины ранорасширителя. При наличии гемодинамической нестабильности при вертикализации сердца (например, при кардиомегалии) широко вскрывают правую плевральную полость. Прижимают вакуумным стабилизатором миокарда боковую стенку сердца под основанием ушка левого предсердия, чтобы обеспечить хорошую визуализацию основания ушка. Накладывают изогнутый атравматический зажим с прямыми браншами на основание ушка левого предсердия (Фиг. 2). В качестве зажима возможно использование любой модификации изогнутого атравматического зажима Де-Беки. После наложения зажима под его браншами на основание ушка ЛП накладывают непрерывный горизонтальный матрасный шов атравматичной мононитью 4/0 (Фиг. 3), эпикардиальную резекцию ушка ЛП осуществляют над браншами закрытого зажима, причем при невскрытой полости левого предсердия (Фиг. 4), ассистент натягивает оба конца нити, и зажим снимают. Этой же нитью выполняют обратный непрерывный обвивной шов с захватом предыдущего шва и основания ушка левого предсердия (Фиг. 5) до первого конца нити без вскрытия полости левого предсердия, после чего концы обеих нитей связывают и отсекают. Глубокие швы, наложенные на перикард, и ваккумный стабилизатор миокарда удаляют, сердце возвращают в горизонтальную позицию. Далее формируют проксимальные анастомозы сосудистых аутотрансплантатов с восходящей аортой и/или левой внутренней грудной артерией.
После выполнения всех процедур выполняют чрезпищеводную эхокардиография для оценки радикальности удаления ушка ЛП (длина остаточной культи ушка ЛП должна быть не более 1 см) [11]. В случае превышения этого значения на культю накладывают дополнительные швы. Вводят протамин-сульфат для нейтрализации гепарина. После пробуждения пациента ему назначаются непрямые антикоагулянты - ривароксабан 20 мг 1 раз в день пожизненно (возможна замена на апиксабан или дабигатрана этексилат).
Существенные отличительные признаки заявляемого способа и причинно-следственная связь между ними и достигаемым техническим результатом:
• Перед выполнением вертикализации сердца накладывают глубокие тракционные швы на перикард позади левого предсердия. Тракционные швы на перикард позади левого предсердия необходимы для последующей гемодинамически безопасной вертикализации сердца.
• Прижимают боковую стенку сердца под основанием ушка ЛП вакуумным стабилизатором миокарда.
Прижатие боковой стенки сердца вакуумным стабилизатором под основанием ушка левого предсердия необходимо для хорошей визуализации основания ушка и прилежащих анатомических структур, в частности огибающей артерии для исключения их повреждения при прошивании культи ушка.
• Накладывают изогнутый атравматический зажим с прямыми браншами на основание ушка ЛП.
Атравматический зажим на основание ушка необходим для последующего формирования первого ряда швов на основание ушка ЛП на работающем сердце без вскрытия полости левого предсердия.
• Под браншами накладывают непрерывный горизонтальный матрасный шов атравматичной мононитью 4/0 и эпикардиальную резекцию ушка ЛП осуществляют над браншами закрытого зажима, причем при невскрытой полости левого предсердия с последующим снятием зажима и наложением обратного обвивного шва той же нитью с захватом предыдущего шва и основания ушка левого предсердия до первого конца нити.
Выполнение такой последовательности позволяет безопасно и радикально удалить ушко ЛП над браншами зажима при невскрытой полости левого предсердия и обеспечить при этом надежный гемостаз.
• Резекцию ушка ЛП и шовное закрытие его культи выполняют на работающем сердце, исключая подключение аппарата искусственного кровообращения.
Выполнение резекции ушка ЛП без подключения аппарата ИК позволяет снизить частоту возможных осложнений в раннем послеоперационном периоде, связанных с использованием аппарата искусственного кровообращения, а также уменьшить потребность в проведении гемотрансфузий в периоперационном периоде, снизить длительность послеоперационной ИВЛ и сократить время нахождения пациента в отделении реанимации.
В качестве иллюстрации эффективности и безопасности заявляемого способа приводим клинический пример.
Пример 1. Пациентка З., 81 года, доставлена бригадой «Скорой помощи» в клинику кардиохирургии с хирургическим лечением сложных нарушений ритма сердца и электрокардиостимуляции кафедры общей хирургии Северо-Западного государственного медицинского университета имени И.И. Мечникова 22/04/2018 с жалобами на боли за грудиной при минимальной физической нагрузке и в покое, которые купируются при прекращении нагрузки или при приеме нитратов, перебои в работе сердца. Боли за грудиной беспокоили в течение последних нескольких лет, последний месяц боли стали более продолжительными и интенсивными. За несколько часов до госпитализации боли приняли нестерпимый характер, возник приступ удушья. Пациентка вызвала бригаду «Скорой помощи». Перебои в работе сердца в виде постоянной формы фибрилляции предсердий беспокоят около 8 лет. В анамнезе острый Q-инфаркт миокарда неизвестной давности.
При госпитализации диагностирован острый непроникающий инфаркт передне-перегодочной области левого желудочка от 22/04/2018, начато консервативное лечение. На фоне проводимого лечения состояние оставалось тяжелым, обусловленным ежедневными приступами стенокардии с острой левожелудочковой недостаточностью. При эхокардиографии диагностирована сниженная сократительная способность миокарда (фракция выброса 40%). При коронарографии - гемодинамически значимое сужение ствола левой коронарной артерии и хроническая окклюзия начального отдела правой коронарной артерии. Возможности эндоваскулярного лечения (стентирования) коронарных артерий вследствие особенностей поражения коронарных артерий признаны ограниченными, в связи с чем было рекомендовано аорто-коронарное шунтирование по жизненным показаниям с высоким риском развития периоперационных интракардиальных и экстракардиальных осложнений с одновременной резекцией ушка левого предсердия, учитывая длительно существующую постоянную форму фибрилляции предсердий. Обращало на себя внимание наличие распространенной тяжелой сопутствующей патологии. На основании данных обследования был поставлен следующий диагноз и определены показания к аорто-коронарному шунтированию. Основной: ИБС. Острый инфаркт миокарда непроникающий 2 типа передне-перегородочной области от 22.04.2018 г. Нестабильная (ранняя постинфарктная) стенокардия. Постинфарктный кардиосклероз (ОИМ неизвестной давности). Гипертоническая болезнь III ст. Риск ССО 4. Осложнения основного: острая левожелудочковая недостаточность от 22.04.2018 г, купирована. Хроническая сердечная недостаточность III ф. кл. по NYHA. Сопутствующий: Сахарный диабет 2 типа, инсулинотерапия.
Гигантоклеточный артериит (болезнь Хортона). Церебро-васкулярная болезнь, дисциркуляторная энцефалопатия 2 ст. Язвенная болезнь желудка, ремиссия.
ЖКБ. Холецистэктомия в 2000 г. Хронический вирусный гепатит C с исходом в цирроз, неактивная фаза. Диффузный эутиреоидный зоб, эутиреоз на заместительной гормональной терапии. Синдром обструктивного апноэ сна.
Состояние после эндопротезирования правого коленного (2010 г) и правого т/б (2011 г) суставов. Диабетическая полинейропатия.
03/05/2018 выполнена операция - коронарное шунтирование (4), резекция ушка левого предсердия на работающем сердце. Резекция ушка выполнялась по заявляемому способу. Послеоперационное течение гладкое, в переливаниях донорских компонентов крови не нуждалась, отделяемое по дренажам составило 180 мл, длительность послеоперационной ИВЛ составила 2 ч, на следующий день переведена из отделения реанимации в профильное отделение. Осложнений в ближайшем послеоперационном периоде в виде системной воспалительной реакции, развития полиорганной (сердечной, дыхательной, печеночно-почечной) недостаточности не наблюдалось. Отсутствовала потребность в проведении гемотрансфузий в периоперационном периоде. Швы сняты на 12 сутки после операции, раны зажили первичным натяжением. Переведена для дальнейшего лечения в отделение реабилитации. При контрольном осмотре через 1 год после операции - пациентка приступов стенокардии не отмечает, толерантность к физической нагрузке выше среднего, занимается работой на приусадебном участке, эмболических событий в магистральные артерии головного мозга и/или нижних конечностей за прошедшее после операции время не было.
Группы исследования.
Апробация заявляемого способа успешно проведена в клинике кардиохирургии с хирургическим лечением сложных нарушений ритма сердца и электрокардиостимуляции кафедры общей хирургии Северо-Западного государственного медицинского университета имени И.И. Мечникова в 2016-2019 гг.
Резекция ушка ЛП при изолированном коронарном шунтировании выполнена у 23 пациентов. В контрольную группу (n=10) включены пациенты, которым коронарное шунтирование и резекция ушка ЛП выполнялась в условиях ИК. В исследуемой группе (n=13) коронарное шунтирование и резекция ушка проводилась на работающем сердце без использования аппарата ИК. Краткая клиническая характеристика изучаемых групп пациентов приведена в таблице 1.
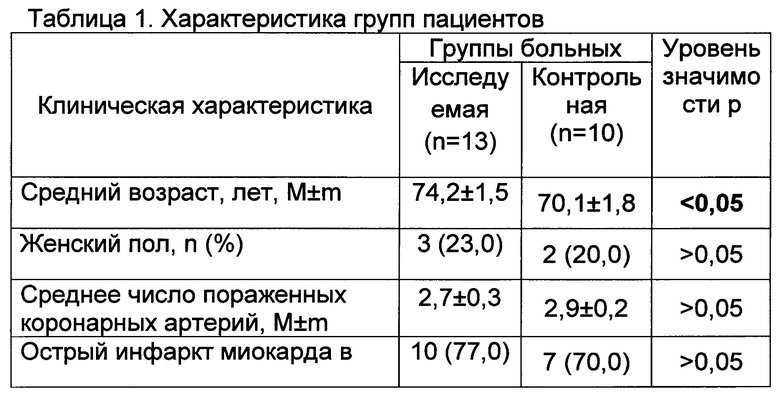
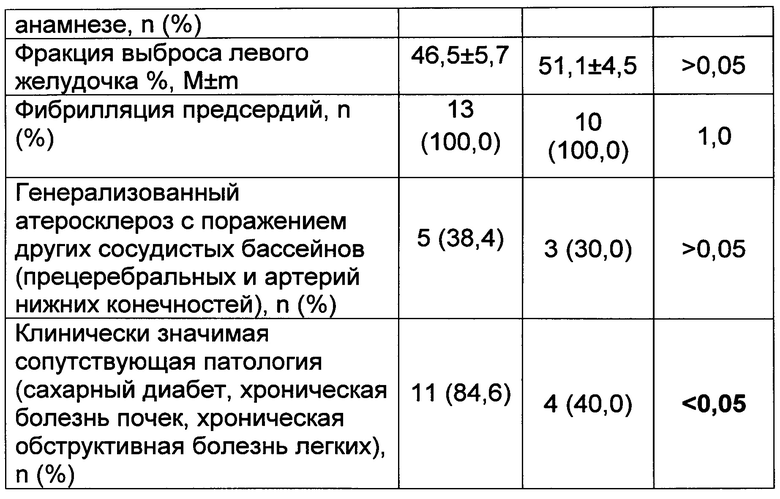
Как видно из таблицы 1, сравниваемые группы были сопоставимы по основным клиническим характеристикам. Более того, пациенты исследуемой группы были старше по возрасту и у них чаще встречались хронические сопутствующие заболевания.
Резекция ушка ЛП в контрольной группе выполнялась в условиях ИК на остановленном сердце со вскрытием полости левого предсердия. Ушивание культи проводилась по общепринятым методикам. В исследуемой группе резекция ушка выполнялась по заявляемому способу. Основные характеристики выполненных операций и особенности течения послеоперационного периода приведены в таблице 2.

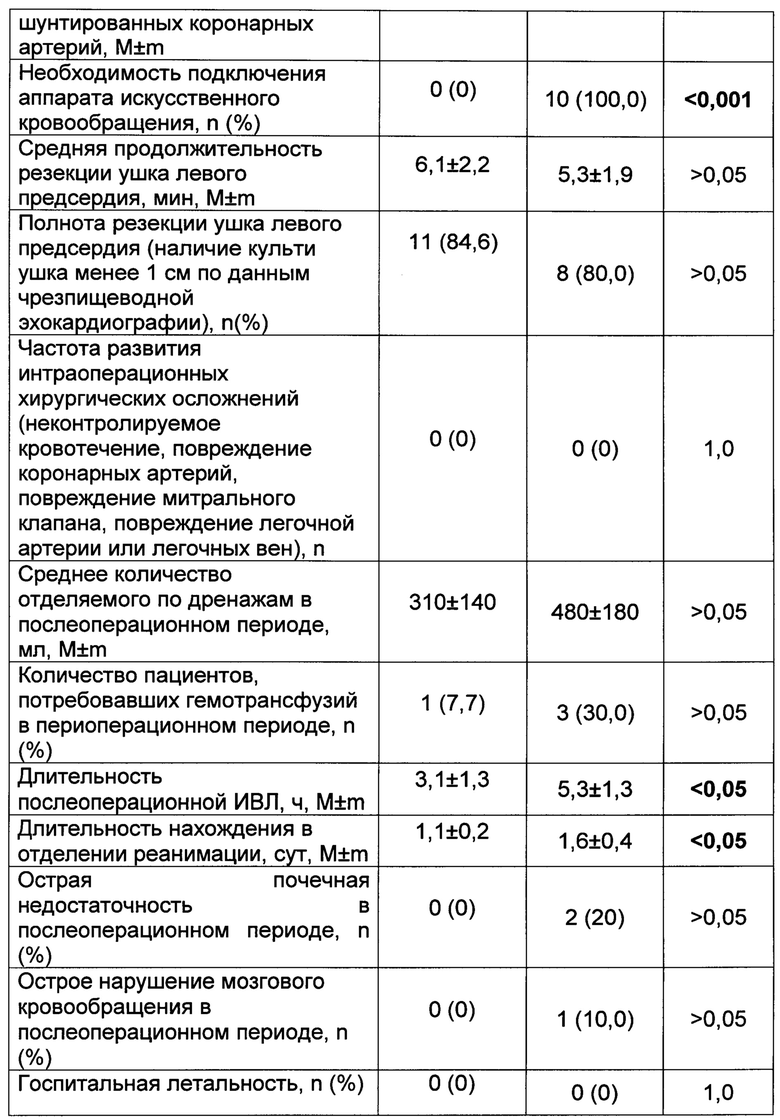
Из таблицы 2 следует, что заявляемый способ резекции ушка левого предсердия без подключения аппарата ИК не менее эффективен, по сравнению с прототипом, по таким критериям, как полнота удаления ушка ЛП, развитие интраоперационных угрожающих жизни осложнений, потребность в переливании донорских компонентов крови, госпитальная летальность.
Заявляемый способ, по сравнению с прототипом, уменьшает продолжительность проведения послеоперационной ИВЛ и продолжительность нахождения пациентов в отделении реанимации в полтора раза. Снижает потребность в проведении гемотрансфузий в периоперационном периоде на 22,3%.
Таким образом, заявляемый способ обеспечивает возможность выполнения способа удаления ушка левого предсердия при выполнении изолированного коронарного шунтирования у больных с фибрилляцией предсердий без использования аппарата искусственного кровообращения, что позволяет:
• снизить риск осложнений в ближайшем послеоперационном периоде, в виде системной воспалительной реакции, высокой вероятности развития полиорганной (сердечной, дыхательной, печеночно-почечной) недостаточности, особенно у пожилых пациентов и больных с распространенной сопутствующей патологией;
• уменьшить потребность в проведении гемотрансфузий в периоперационном периоде;
• снизить длительность ИВЛ после операции;
• сократить послеоперационный койко-день в отделении реанимации.
Список литературы:
1. Ramlawi В., Saleh W.K., Edgerton J. The left atrial appendage: target for stroke reduction in atrial fibrillation // Methodist Debakey Cardiovasc J. - 2015. - Vol. 11, №2. - P. 100-103.
2. Wasilewska M, Gosk-Bierska I. Thromboembolism associated with atrial fibrillation as a cause of limb and organ ischemia // Adv Clin Exp Med. - 2013. - Vol. 22, №6. - P. 865-873.
3. Сотников А.В., Мельников M.В., Маринин В.А. с соавт. Предупреждение эмболий у больных с фибрилляцией предсердий после резекции ушка левого предсердия при открытых операциях на сердце (пилотное исследование) // Вестник СЗГМУ им. И.И. Мечникова. - 2018. - Т. 10, №2. - с. 52-57.
4. Whitlock R., Healey J., Vincent J. Rationale and design of the Left Atrial Appendage Occlusion Study (LAAOS) III // Ann Cardiothorac Surg. - 2014. - Vol. 3, №1. - P. 45-54.
5. Reddy V.Y., Doshi S.K., Sievert H., et al. Percutaneous left atrial appendage closure for stroke prophylaxis in patients with atrial fibrillation: 2.3-year follow-up of the PROTECT AF (Watchman Left Atrial Appendage System the special contribution of the European Heart Rhythm Association // Eur Heart J. - 2012. - Vol. 33, №21. - P. 2719-2747.
6. Aryana A., Singh S.K., Singh S.M., et al. Association between incomplete surgical ligation of left atrial appendage and stroke and systemic embolization // Heart Rhythm. - 2015. - Vol. 12, №7. - P. 1431-1437.
7. Gillinov A.M., Pettersson G., Cosgrove D.M. Stapled excision of the left atrial appendage // J Thorac Cardiovasc Surg. - 2005. - Vol. 129, №3. - P. 679-80.
8. Caliskan E, Sahin A, Yilmaz M, Seifert В et al. Epicardial left atrial appendage AtriClip occlusion reduces the incidence of stroke in patients with atrial fibrillation undergoing cardiac surgery // Europace. - 2018. - Vol 20, №7. - e105-e114.
9. Hernandez-Estefania R., Levy Praschker В., Bastarrika G., Rabago G. Left atrial appendage occlusion by invagination and double suture technique // Eur J Cardiothorac Surg. - 2012. - Vol. 41, №1. - P. 134-136.
10. Mirow N., Vogt S., Irqsusi M., Moosdorf R. et al. Epicardial left atrial appendage closure-comparison of surgical techniques in an ex vivo model // J Thorac Dis. - 2017. - Vol. 9, №3. - P. 757-761.
11. Kanderian A.S., Gillinov A.M., Pettersson G.B., Blackstone E. et al. Success of surgical left atrial appendage closure: assessment by transesophageal echocardiography // J Am Coll Cardiol. - 2008. - Vol. 52, №11. - P. 924-929.
12. Sievers H.H. Excision or exclusion of left atrial appendage? // Eur J Cardiothorac Surg. - 2012. - Vol. 41, №1. - P. 136-137.
13. Su P., McCarthy K.P., Ho S.Y. Occluding the left atrial appendage: anatomical considerations // Heart. - 2008. - Vol. 94, №9. - P. 1166-1170.
14. Шихвердиев H.H., Ушаков Д.И., Пелешок А.С. с соавт. Биологический возраст и его роль в стратификации кардиохирургического риска // Вестник хирургии им. Грекова. - 2019. - Т. 178, №1. - с. 17-20.
15. Marui A., Okabayashi Н., Komiya Т. et al. Benefits of off-pump coronary artery bypass grafting in high-risk patients // Circulation. - 2012. - Vol. 126, №11, Suppl 1. - P. 151-157.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОЙ ОККЛЮЗИИ УШКА ЛЕВОГО ПРЕДСЕРДИЯ | 2022 |
|
RU2782147C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ ОБЛИТЕРАЦИИ УШКА ЛЕВОГО ПРЕДСЕРДИЯ У ПАЦИЕНТОВ С ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ ПРИ ОПЕРАЦИИ НА МИТРАЛЬНОМ КЛАПАНЕ ИЛИ НА МИТРАЛЬНОМ КЛАПАНЕ И ОПЕРАЦИИ "ЛАБИРИНТ" В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2019 |
|
RU2691437C1 |
| СПОСОБ АМПУТАЦИИ УШКА ЛЕВОГО ПРЕДСЕРДИЯ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАЦИЕНТОВ С ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ | 2024 |
|
RU2833936C1 |
| СПОСОБ ВЫБОРА ХИРУРГИЧЕСКОЙ ТАКТИКИ КОРРЕКЦИИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ ПРИ НАЛИЧИИ ОБРАЗОВАНИЯ В УШКЕ ЛЕВОГО ПРЕДСЕРДИЯ | 2024 |
|
RU2828574C1 |
| СПОСОБ БИАТРЕАЛЬНОЙ КРИОАБЛАЦИИ С ХИРУРГИЧЕСКОЙ ОККЛЮЗИЕЙ УШКА ЛЕВОГО ПРЕДСЕРДИЯ ПОЛНОСТЬЮ ТОРАКОСКОПИЧЕСКИМ МЕТОДОМ ПРИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2024 |
|
RU2826346C1 |
| СПОСОБ БИПОЛЯРНОЙ РАДИОЧАСТОТНОЙ АБЛЯЦИИ В ЛЕВОМ ПРЕДСЕРДИИ ВО ВРЕМЯ ОПЕРАЦИЙ НА ОТКРЫТОМ СЕРДЦЕ | 2009 |
|
RU2414176C1 |
| Способ окклюзии ушка левого предсердия во время коронарного шунтирования у пациентов с ишемической болезнью сердца | 2016 |
|
RU2621954C1 |
| СПОСОБ ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ ВО ВРЕМЯ ОПЕРАЦИЙ С ИСКУССТВЕННЫМ КРОВООБРАЩЕНИЕМ БЕЗ ВСКРЫТИЯ ЛЕВЫХ ОТДЕЛОВ СЕРДЦА | 2005 |
|
RU2294155C2 |
| Способ выполнения изоляции задней стенки левого предсердия через устье отсечённого ушка левого предсердия | 2017 |
|
RU2664958C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2024 |
|
RU2833935C1 |
Изобретение относится к области медицины, а именно сердечно-сосудистой хирургии. Перед выполнением вертикализации сердца накладывают глубокие тракционные швы на перикард позади левое предсердие (ЛП). Прижимают боковую стенку сердца под основанием ушка ЛП вакуумным стабилизатором миокарда. Накладывают изогнутый атравматический зажим с прямыми браншами на основание ушка ЛП. Под браншами накладывают непрерывный горизонтальный матрасный шов. Эпикардиальную резекцию ушка ЛП осуществляют над браншами закрытого зажима при невскрытой полости ЛП. Снимают зажим и накладывают обратный обвивной шов той же нитью. Резекцию ушка ЛП и шовное закрытие его культи выполняют на работающем сердце, исключая подключение аппарата искусственного кровообращения (ИК). Способ позволяет снизить риск осложнений в послеоперационном периоде, таких как: системная воспалительная реакция, полиорганная недостаточность, уменьшить потребность в проведении гемотрансфузий в периоперационном периоде; а также позволяет снизить длительности ИВЛ после операции; сократить послеоперационное количество койко-дней в отделении реанимации. 2 табл., 1 пр., 5 ил.
Способ резекции ушка левого предсердия (ЛП) при коронарном шунтировании у больных с фибрилляцией предсердий, заключающийся в выполнении полной срединной стернотомии, вскрытии перикарда, выделении сосудистых аутотрансплантатов, формировании дистальных анастомозов аутотрансплантатов с целевыми коронарными артериями, вертикализации сердца с последующей эпикардиальной резекцией ушка левого предсердия и шовным закрытием культи ушка, отличающийся тем, что перед выполнением вертикализации сердца накладывают глубокие тракционные швы на перикард позади левого предсердия, после чего прижимают боковую стенку сердца под основанием ушка ЛП вакуумным стабилизатором миокарда, затем накладывают изогнутый атравматический зажим с прямыми браншами на основание ушка ЛП, после чего под браншами накладывают непрерывный горизонтальный матрасный шов атравматичной мононитью 4/0 и эпикардиальную резекцию ушка ЛП осуществляют над браншами закрытого зажима, причем при невскрытой полости левого предсердия с последующим снятием зажима и наложением обратного обвивного шва той же нитью, с захватом предыдущего шва и основания ушка левого предсердия до первого конца нити без вскрытия полости левого предсердия, причем резекцию ушка ЛП и шовное закрытие его культи выполняют на работающем сердце, исключая подключение аппарата искусственного кровообращения.
| Whitlock R., Healey J., Vincent J | |||
| Rationale and design of the Left Atrial Appendage Occlusion Study (LAAOS) III, Ann Cardiothorac Surg, 2014, Vol | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ ОБЛИТЕРАЦИИ УШКА ЛЕВОГО ПРЕДСЕРДИЯ У ПАЦИЕНТОВ С ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ ПРИ ОПЕРАЦИИ НА МИТРАЛЬНОМ КЛАПАНЕ ИЛИ НА МИТРАЛЬНОМ КЛАПАНЕ И ОПЕРАЦИИ "ЛАБИРИНТ" В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2019 |
|
RU2691437C1 |
| Многоходовой переключательный клапан | 1930 |
|
SU20424A1 |
| БОКЕРИЯ О.Л | |||
| и др., ХИРУРГИЧЕСКАЯ ПРОФИЛАКТИКА ТРОМБОЭМБОЛИЙ ПРИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | |||
| ПЕРСПЕКТИВА ОТЕЧЕСТВЕННЫХ СИСТЕМ ДЛЯ | |||
Авторы
Даты
2020-06-04—Публикация
2019-07-26—Подача