Изобретение относится к металлургии тугоплавких соединений, в частности к синтезу порошков боридов титана и может быть использовано в получении огнеупоров из индивидуальных и композиционных соединений для высокотемпературных агрегатов химической, цветной и черной металлургии.
Промышленные способы получения порошков диборида титана TiB2 основываются преимущественно на высокотемпературном карботермическом и карбидоборным восстановлении смеси рутила и борного ангидрида при температурах выше 1800°С:
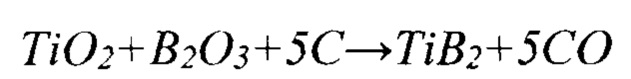
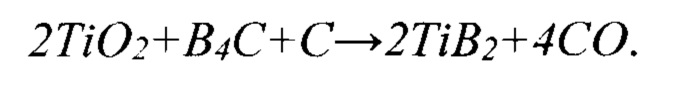
Подробно эти способы представлены Г.В. Самсоновым с сотрудниками [1] и позволяют получать конгломераты конечного продукта из относительно крупных зерен (50-100 мкм). Но высокие температуры процессов, т.е. большая энергоемкость, необходимость создания высокого вакуума и низкая производительность сложного оборудования определяют, с одной стороны, высокую стоимость продукта. А с другой - генерируют попытки совершенствования процесса и уменьшения энергоемкости карботермического синтеза диборида титана.
В патенте (патент US №5087592, С04В 35/58, 1992 г. [2]), для проведения карботермического восстановления оксида титана при температурах 1550÷1800°С предлагается вести процесс TiO2+B2O3+5С-÷TiB2+5СО в инертной атмосфере и присутствии в реакционной смеси до 30 мас. % оксидов щелочного металла, таких как оксид натрия или оксид калия. Предполагается, что эти оксиды взаимодействуют с оксидом бора до образования метабората натрия Na2O+B2O3 → 2NaBO2, который будет растворять оксид титана с последующими реакциями образования диборида титана:
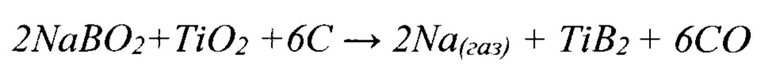
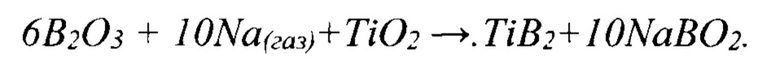
Основным недостатком известного способа остается необходимость применения дорогостоящего оборудования, высокая температура и энергоемкость синтеза. Кроме того, метод подразумевает высокий расход оксида бора на невосполнимые потери с метаборатом натрия. Эти недостатки определяют высокую стоимость конечного продукта - диборида титана.
Известен способ получения порошка диборида титана (патент RU №2498880, B22F, 2013 г., [3]), в котором снижение температуры синтеза целевого продукта достигаютувеличением контактной поверхности исходной реакционной смеси. По сути, осуществляют диспергирование субмикронных порошков оксида титана (пигмента) и сажи в растворе борной кислоты в расчетных стехиометрических или не стехиометрических количествах карботермической реакции: TiO2+2Н3ВО3+5С→TiB2+3H2O+5СО. После сушки водной дисперсии и удаления связанной воды при 150÷200оС процесс синтеза диборида титана осуществляют в инертной атмосфере при температурах 1200÷1500°С в течение 3-4 часов. Сообщается о высоком выходе целевого продукта 93-95% (остальное TiC/TiO) с частицами порошка размером до 5-15 мкм в не агрегированной форме.
Известен способ синтеза диборида титана (патент US №8216536, С01В 35/04, 2012 г., [4]), в котором, после предварительного приготовления водной дисперсионной смеси оксида титана, оксида бора (или борной кислоты) и углерода и последующей распылительной сушки суспензии, карботермический процесс получения диборида титана ведут в соответствии с основными процессами синтеза:
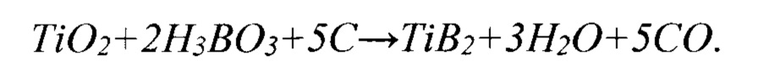
Получение порошка диборида титана целевого размера и морфологии достигается выбором типа углерода с известным содержанием серы от 0,1 до 4,0 мас. %, проведением карботермического процесса при температурах 1300÷1700°С в течение 0,5÷4 часов и с регулировкой потока аргона в реакционной зоне в пределах от 0,25 до 3 л/мин.
Известные способы требуют длительного времени и сложного оборудования на предварительную подготовку реакционной смеси (сушку распылением и агломерацию) и измельчение готового продукта. Кроме того, несмотря на тщательную подготовку смеси, температура синтеза высокая, что является существенным недостатком методов, снижающим технологические и экономические параметры процесса получения целевого продукта.
Наиболее близким техническим решением, выбранным в качестве прототипа, является способ синтеза порошков диборида титана (патент RU №2603407, B22F, 2016 г., [5]), в соответствии с которым подготовку реакционной смеси TiO2-В2О3-С осуществляют растворным методом, в качестве титансодержащих компонентов применяют диоксид титана в форме анатаза или его прекурсоры, осуществляют их гидролиз и модифицирование фторид-анионом. В качестве восстановителя используются активные формы углерода в виде сажи, или содержащиеся в патоке, сахарозе, лимонной кислоте. Нагрев и синтез диборида титана ведут в атмосфере динамического вакуума при температурах от 1000 до 1050°С в период трансформации анатаза в рутил. По окончании стадии синтеза атмосфера динамического вакуума заменяется на атмосферу аргона.
Недостатком является то, что в способе синтеза порошков диборида титана нагрев и выдержка не дифференцированы по составу атмосферы и осуществляются при 1000÷1050°С в режиме динамического вакуума, который при нагреве и выдержке интенсифицирует процесс трансформации анатаза в рутил, что ограничивает цикл восстановления TiO2 до активных промежуточных форм монооксида и оксикарбида титана. Кроме того, на активной стадии синтеза TiB2 разряженная атмосфера интенсифицирует высокие потери В2О3. Таким образом, выход годного продукта (диборида титана) значительно снижается.
Задачей предлагаемого технического решения является обеспечение синтеза диборида титана в низкотемпературных условиях производства огнеупорных изделий.
Техническим результатом является получение технически чистого диборида титана с выходом конечного продукта 98-99,8% при температурах не выше 1060°С.
Технический результат достигается тем, что в способе низкотемпературного синтеза диборида титана, включающем приготовление реакционной смеси TiO2-В2О3-С, содержащей диоксид титана в форме анатаза, модифицированного фтор-анионом, в виде агломерированного композита, нагрев и выдержку реакционной смеси осуществляют сначала при температуре 940÷980°С в кислородсодержащей атмосфере в течение 30÷60 минут, а затем при 1030÷1060°С в бескислородной среде в течение 120÷180 минут. Причем бескислородная среда может быть обеспечена применением инертной газовой среды аргона и гелия.
Сравнение предлагаемого технического решения с ближайшим аналогом показывает следующее. Оба решения характеризуются общими признаками:
• Объект защиты - технология карботермического синтеза диборида титана, пригодного для использования в производстве огнеупоров из индивидуальных и композиционных соединений для высокотемпературных агрегатов химической, цветной и черной металлургии;
• Предварительная стадия - приготовление исходной реакционной смеси оксидов титана и бора;
• В качестве титансодержащих компонентов применяют диоксид титана в форме анатаза или его прекурсоров;
• Осуществляют модифицирование и гидролиз анатаза и прекурсоров диоксида титана с получением осадка аморфного геля;
• Для модифицирования применяют фтор-анион, в наибольшей степени стабилизирующий анатазную форму диоксида титана;
• Нагрев до температуры синтеза в присутствии углеродных восстановителей и борсодержащих соединений.
Предлагаемое решение характеризуется также признаками, отличающимися от признаков ближайшего аналога:
• Нагрев до температуры синтеза дифференцирован в последовательности:
- на первом этапе нагрев и выдержку при температуре 940÷980°С осуществляют в кислородсодержащей атмосфере в течение 30÷60 минут;
- на втором этапе последующий нагрев и синтез при температурах 1030÷1060°С в течение 120÷180 минут производят в условиях бескислородной атмосферы в инертных газах.
• Синтез диборида титана на втором этапе производят в результате взаимодействия нестехиометрических оксидов и оксикарбидов титана с газообразным оксидом бора.
Наличие в предлагаемом техническом решении признаков, отличных от признаков, характеризующих ближайший аналог, позволяет сделать вывод о соответствии предлагаемого решения условию патентоспособности изобретения «новизна».
В процессе поиска и сравнительного анализа не выявлено технических решений, характеризующихся совокупностью признаков аналогичной с совокупностью признаков предлагаемого технического решения и дающих при использовании аналогичные результаты, что позволяет сделать вывод о соответствии предлагаемого решения условию патентоспособности «изобретательский уровень».
Техническая сущность предлагаемого решения заключается в следующем.
Известная процедура допирования аморфного оксида титана фторид-ионами по схеме 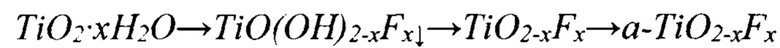 и сдвиг анатаз-рутил трансформации (ART) из температурного интервала 600÷700°С в область 900÷1100°С продлевает период перестройки кристаллической решетки в процессе а-TiO2-х → r-TiO3. Это обеспечивает продление активного состояния оксида титана и при 860÷980°С создает условия для его последовательного восстановления по схеме:
и сдвиг анатаз-рутил трансформации (ART) из температурного интервала 600÷700°С в область 900÷1100°С продлевает период перестройки кристаллической решетки в процессе а-TiO2-х → r-TiO3. Это обеспечивает продление активного состояния оксида титана и при 860÷980°С создает условия для его последовательного восстановления по схеме:

Активное нестехиометрическое состояние оксикарбида титана является необходимым условием для перехода системы TiO2-В2О3-С к следующим этапам фазообразования при температурах до 1100°С с участием оксида бора:
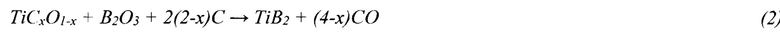

Тем не менее, выполнение условия достаточности требует обеспечения специальных режимов разогрева и выдержки реакционной смеси TiO2-В2О3-С в определенных температурных и временных интервалах, в которых последовательно происходят восстановление оксида титана до его нестехиометрических оксикарбидных форм, газификация оксида бора и последующее их взаимодействие между собой.
Теоретически и практически, процессы (2) и (3) с участием оксида бора в конденсированном состоянии маловероятны:

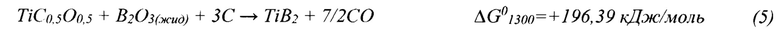
и развиваются с участием оксида бора в газообразном состоянии до образования диборида титана:


и бората титана
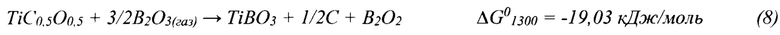
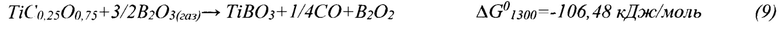
В соответствии с уравнениями(6)÷(9) образование бората титана TiBO3, относительно диборида титана TiB2, имеет незначительную, но 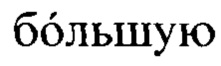 вероятность при наличии исходного реагента TiCxO1-x одинакового состава. Диборид титана образуется только при х<0.5 по реакции (7), то есть с меньшим содержанием углерода в составе промежуточной оксикарбидной фазы. Это может означает, что оксикарбид титана TiCxO1-x, обедненный по углероду, имеет наиболее высокую реакционную активность. Свежеобразованные и активные центры этих оксикарбидов при дальнейшем нагреве и выдержке при 1030-1060°С термодинамически являются лучшими стартовыми фазами для взаимодействия с углерод- и борсодержащим и компонентами в системе TiO2-В2О3-С с последующим образованием диборида титана TiB2.
вероятность при наличии исходного реагента TiCxO1-x одинакового состава. Диборид титана образуется только при х<0.5 по реакции (7), то есть с меньшим содержанием углерода в составе промежуточной оксикарбидной фазы. Это может означает, что оксикарбид титана TiCxO1-x, обедненный по углероду, имеет наиболее высокую реакционную активность. Свежеобразованные и активные центры этих оксикарбидов при дальнейшем нагреве и выдержке при 1030-1060°С термодинамически являются лучшими стартовыми фазами для взаимодействия с углерод- и борсодержащим и компонентами в системе TiO2-В2О3-С с последующим образованием диборида титана TiB2.
Наоборот, TiCxO1-x с составом приближенным к карбиду титана TiC (0.5<х≤1) малоактивен, а точнее, способен к взаимодействию с оксидом бора только до бората титана. Заметим также, что наличие остаточного углерода (см. реакцию (8)) будет тормозить начальное образование TiBO3, но это же означает присутствие значительных количеств примесей углерода в продуктах синтеза.
Таким образом, существенными условиями низкотемпературного синтеза диборида титана являются:
1) Предварительное допирование аморфного оксида титана фтором TiO2-xFx для стабилизации анатазной модификации оксида титана и переноса анатаз-рутил трансформации (ART) из интервала 600-700°С в высокотемпературную зону 900-1000°С. Предварительными исследованиями установлено, что ART допированного фтором оксида титана происходит в интервале 860÷980°С [6] и является периодом наибольшей реакционной активности оксида титана при его карботермическом восстановлении.
2) Формирование активной промежуточной фазы оксикарбида титана TiCxO1-x с дефицитным составом по углероду х<0,5 в атмосфере воздуха при нагреве до 960°С с максимальным развитием процесса при 890°С:
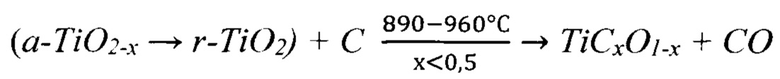
Таким условием может быть баланс между температурой и продолжительностью фазовых превращений 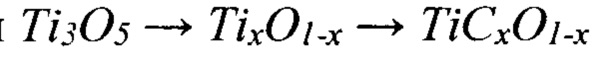 в течение выдержки системы.
в течение выдержки системы.
Это условие необходимо для ограничения или исключения «паразитной» реакции образования бората титана TiBO3, увеличивающей расход оксида бора и загрязняющей конечный целевой продукт TiB2. Оксикарбид TiCxO1-x с составом приближенным к карбиду титана TiC малоактивен, но способен для реакции
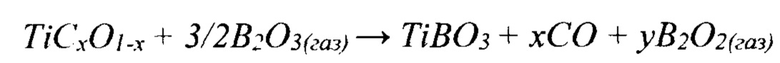
вследствие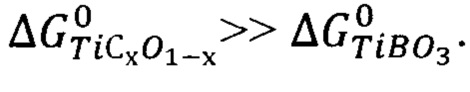
3) Синтез диборида титана TiB2 при температуре 1030÷1060°С в течение 2-3 часов с участием оксида бора B2O3(газ) в реакциях фазообразования в газообразном виде:
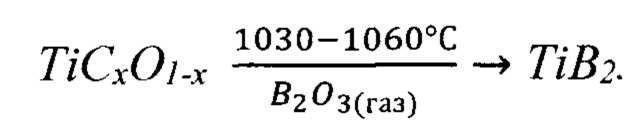
Это условие определяет возможность низкотемпературного синтеза и выход целевого продукта, который тем выше, чем дольше период контакта В2О3↑ с активными промежуточными продуктами в объеме реакционного тела. Процесс газификации B2O3(жидк.)→B2O3↑ является общепризнанным эффектом и интенсифицируется с увеличением температуры выше 1000°С. Поэтому период реакционного контакта Тконт.=ƒ(Тсинтеза, Ратм) зависит от температуры и давления атмосферы в системе. Вакуум и высокая температура будут способствовать быстрому удалению В2О3↑ из зоны реакции и существенно ограничивать полноту реакции синтеза TiB2. Наоборот, бескислородная атмосфера с повышенным Ратм. и минимизация Тсинтеза в системе будут способствовать наибольшей полноте протекания целевой реакции.
При соблюдении перечисленных условий конечным продуктом является технически чистый диборид титана TiB2.
Способ синтеза диборида титана осуществляется следующим образом.
Реализация процесса на стадии подготовки реакционной смеси требует модифицирования (допирования) оксида титана с использованием гидролиза минеральных солей титана или диоксида титана в гидратированной форме, который протекает с образованием метатитановой кислоты. Формирование комплекса метатитановой кислоты в присутствии фтористоводородной кислоты (источник фтор-иона) и гидроксида аммония (активатор гидролиза и регулятор рН) протекает следующим образом:
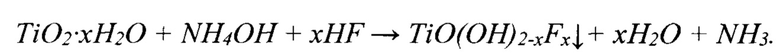
Затем в гелеобразный раствор TiO(OH)2-xFx последовательно при постоянном перемешивании добавляются остальные компоненты реакционной смеси: борная кислота и углерод в виде сажи или сахарозы. Готовая смесь сушится на воздухе, затем при 80-90°С в сушильном шкафу. Полученный агломерированный композит нагревается и выдерживается в герметичной ячейке при 940÷980°С в кислородсодержащей атмосфере в течение 30÷60 минут для восстановления оксида титана a-TiO2-x углеродом до нестехиометрического оксикарбида титана TiCxO1-x. Далее в системе создается бескислородная атмосфера (аргон, гелий) и производится нагрев смеси до 1030÷1060°С с выдержкой в течение 120÷180 минут. В этих условиях происходит газификация оксида бора 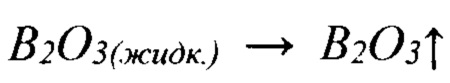 и продолжение процесса синтеза диборида титана:
и продолжение процесса синтеза диборида титана:
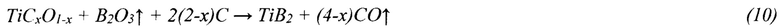
Температура синтеза в интервале 1030÷1060°С обеспечивает наибольшие преференции основной реакции синтеза диборида титана (10). При этих температурах газообразный B2O3↑ имеет меньшее парциальное давление и более длительный период контактирует с промежуточными продуктами карботермического восстановления оксида титана. Кроме того, при пониженных температурах в меньшей степени развивается процесс насыщения монооксида титана углеродом, что поддерживает нестабильность оксикарбида титана и соответственно его реакционную активность. В результате образуется технически чистый диборид титана TiB2.
Таким образом, способ низкотемпературного синтеза диборида титана в системе TiO2-В2О3-С требует поэтапного осуществления процессов (1) и (2). На первом этапе выбор температурного интервала выдержки 940÷980°С установлен предварительными исследованиями [6]. Ограничение периода выдержки 30÷60 минутами в кислородсодержащей атмосфере обусловлен необходимостью доведения процесса восстановления допированного оксида титана до оксикабида TiCxO1-x в наиболее активной его форме с содержанием углерода менеех <0,5. Вне указанных температурного и временного интервалов процесс завершается на стадии образования неактивных форм оксида титана для продолжения процесса синтеза диборида титана. При осуществлении первого этапа при температурах ниже указанного предела (до 940°С или до 30 минут) процесс ограничен недостатком энергии для восстановления до оксикарбида титана и завершается на стадии формирования низших оксидов титана TiO2→TinO2n-1. Выдержка реакционной смеси выше 980°С или более 60 минут вызывает потери активной анатазной формы оксида титана на образование стабильной (неактивной) рутильной или формирование оксикарбида титана, приближенного по составу к карбиду титана с х>0,5. В обоих случаях дальнейший синтез чистого диборида титана невозможен или выход целевого продукта TiB2 резко снижается с содержанием в своем составе примесей оксидов, оксикарбидов, боратов титана и углерода.
Проведение синтеза диборида титана на втором этапе вне указанных температурного и временного интервалов не обеспечивает завершение и достижение максимального выхода процесса (2). При температуре ниже 1030°С или с выдержкой менее 120 минут процесс синтеза не развивается из-за недостатка энергии. При температуре выше 1060°С скорость газификации и эвакуации оксида бора повышенная, время контакта TiCxO1-x - B2O3↑ в объеме реакционной смеси резко уменьшается. Соответственно, уменьшается выход диборида титана при любом периоде выдержки. Выдержка реакционной смеси более 180 минут чрезмерна и не оказывает влияние на количество и чистоту конечного продукта, но увеличивает непроизводительный перерасход электроэнергии.
Таким образом, при корректном составлении исходной реакционной смеси, учитывающей стехиометрию карботермической реакции и потери компонентов на всех стадиях процесса, выполнение режимов разогрева и выдержки системы, продуктом синтеза будет технически чистый порошок диборида титана TiB2.
Отработку и реализацию предлагаемого решения проводили в лабораторных условиях. Способ низкотемпературного синтеза диборида титана поясняется следующими фигурами:
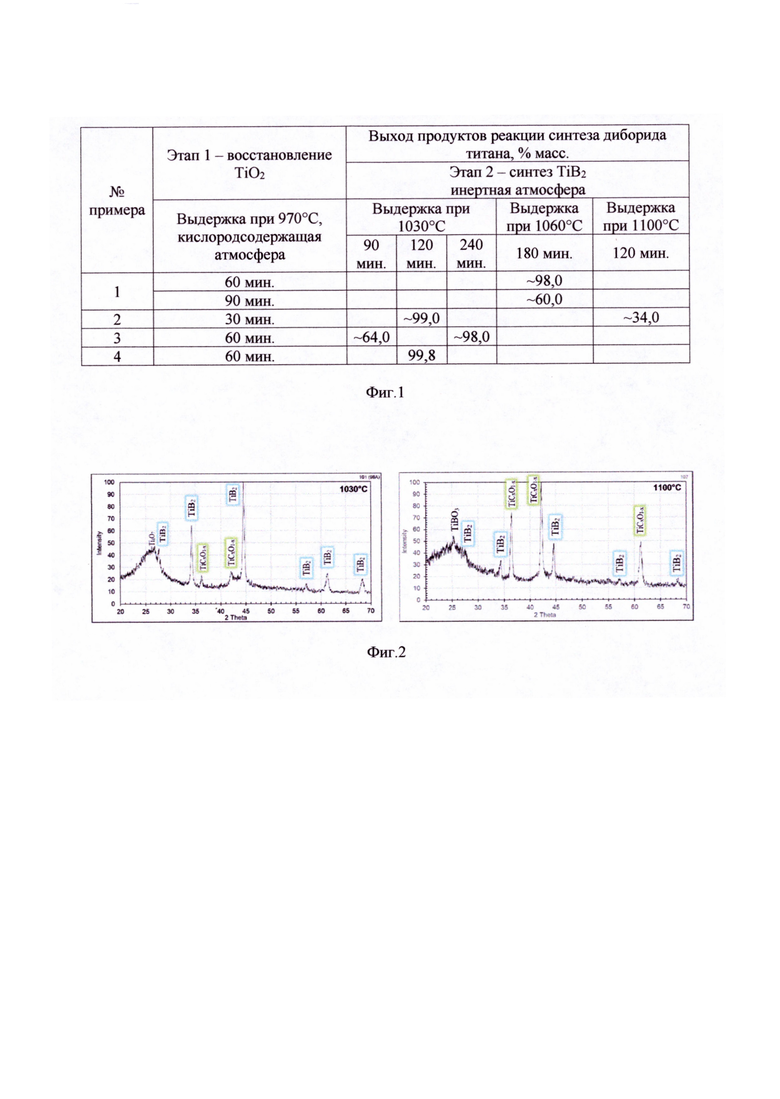
Фиг. 1 - Результаты РФА продуктов реакции синтеза диборида титана.
Фиг. 2 - Рентгенограммы продуктов синтеза 1TiO2-7B2O3-13C при 1030°С и 1100°С.
Пример 1. В 50 мл дистиллированной воды при перемешивании вводили фторид-ионы в виде HF в количестве F/TiO2=1,2 (массовая доля) и осуществляли регулировку кислотности раствора добавкой гидроксида аммония NH4OH до рН=2÷2,5. После охлаждения до 20°С в раствор в виде порошка вводили метатитановую кислоту H2TiO3 в количестве 2,0 моль/л (в пересчете на TiO2), раствор белого цвета перемешивают в течение 0,5 часа. Изменение рН раствора до 7÷7,5 свидетельствовал об образовании гелеобразного осадка модифицированной фтором метатитановой кислоты TiO(ОН)2-xFx. Далее последовательно при постоянном перемешивании добавлялись борная кислота и сахароза в количествах, обеспечивающих мольное соотношение TiO2:В2О3:С=1:7:13. Готовая смесь сушилась на воздухе, затем при 80-90°С в сушильном шкафу. Полученный агломерированный композит разделялся на две части. Каждая из них нагревалась в ячейке в кислородсодержащей атмосфере до 970°С, но с выдержкой при этой температуре раздельно в течение 60 и 90 минут. Далее в ячейках производили замену кислородсодержащей атмосферы на бескислородную (аргон) и нагревали систему до температуры синтеза 1060°С. После выдержки в течение 180 минут печь отключали и охлаждали ячейки до комнатной температуры. Полученный порошок темно-серого цвета направлялся на РФА для определения фазового состава (см. Фиг. 1).
Пример 2. По примеру 1 готовилась исходная реакционная смесь TiO2 - В2О3 - С и разделялась на две части. Каждая из них нагревалась в ячейке в кислородсодержащей атмосфере до 970°С с выдержкой при этой температуре в течение 30 минут, после чего в ячейках производили замену кислородсодержащей атмосферы на бескислородную (аргон) и нагревали систему до температур синтеза диборида титана 1030 и 1100°С. После выдержки при этих температурах в течение 120 минут печь отключали и охлаждали ячейки до комнатной температуры. Полученный порошок направлялся на РФА для определения фазового состава. Результаты анализа представлены на Фиг. 1 и Фиг. 2.
Пример 3. По примеру 1 готовилась исходная реакционная смесь TiO2 - В2О3 - С. Полученный агломерированный композит разделялся на две части. Каждая из них нагревалась в ячейке в кислородсодержащей атмосфере до 970°С с выдержкой при этой температуре в течение 60 минут, после чего в ячейках производили замену кислородсодержащей атмосферы на бескислородную (аргон) и нагревали систему до температур синтеза диборида титана 1030°С. После выдержки при этих температурах в течение 90 и 240 минут печь отключали и охлаждали ячейки до комнатной температуры. Полученный порошок направлялся на РФА для определения фазового состава (см. Фиг. 1).
Результаты осуществления способа низкотемпературного синтеза диборида титана по условиям примеров 1÷3 свидетельствуют о наиболее приемлемых и эффективных интервалах температур на первом 940÷980°С и втором 1030÷1060°С этапах с соответствующими выдержками 30÷60 минут и 120÷180 минут. В этих условиях процесс получения TiB2 проходит с 98÷99,8% выходом конечного продукта. При отклонении от установленных предлагаемым способом параметров технологический процесс заканчивается низким выходом целевого продукта с высоким остаточным содержанием примесей. Основной примесью является оксикарбид титана (TiCxO1-x). Температура синтеза 1100°С является чрезмерной и ведет к неоправданному перерасходу электроэнергии на обеспечение процесса.
Расчетная себестоимость порошков диборида титана, полученных в лабораторных условиях (Примеры 1÷3) по технологии низкотемпературного синтеза, составляет 40÷44 USD за 1 кг TiO2. С учетом рыночной цены на исходные материалы и накладных расходов, стоимость материала будет находиться в пределах 40÷50 USD/кг TiB2.
Использование предлагаемой технологии на доступном стандартном оборудовании позволяет осуществлять производство диборида титана как самостоятельного продукта в виде порошка, так и проводить синтез в составе любых композитных огнеупорных изделий, в том числе бескислородных, оксидных и углеграфитовых, проходящих стадию технологического обжига выше 1030°С. Особенности предлагаемой технологии получения диборида титана открывают возможности расширения коммерческого применения конечного продукта в виде компактных индивидуальных или композитных изделий, для развития новых технологий в металлургии, химической и электродной промышленности. Технология позволяет приступить к проектированию электролизеров нового поколения с дренированным катодом и вертикальным расположением электродов для коммерческого использования в производстве алюминия и других металлов.
ИНФОРМАЦИЯ
1. Самсонов Г.В., Серебрякова Т.И., Неронов В.А. Бориды. М.: Атомиздат, 1975, 376 с.
2. Патент US №5087592, С04В 35/58, 1992 г.
3. Патент RU №2498880, B22F 9/18, 2013 г.
4. Патент US №8216536, С01В 35/04, 2012 г.
5. Патент RU №2603407, B22F, 2016 г.
6. Горланов, Е.С. К вопросу о низкотемпературном синтезе диборида титана /Е.С. Горланов, В.Л. Уголков // Научный журнал «Вестник ИРГТУ». Металлургия и материаловедение. - 2018. - №2. - С. 153-165.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИБОРИДА ТИТАНА | 2015 |
|
RU2603407C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИБОРИДА ТИТАНА | 2018 |
|
RU2684381C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИТНЫХ МАТЕРИАЛОВ НА ОСНОВЕ УГЛЕРОДА | 2023 |
|
RU2814568C1 |
| СПОСОБ ЭЛЕКТРОЛИЗА КРИОЛИТОГЛИНОЗЕМНЫХ РАСПЛАВОВ С ПРИМЕНЕНИЕМ ТВЕРДЫХ КАТОДОВ | 2019 |
|
RU2716569C1 |
| Способ получения смесей высокодисперсных гетерофазных порошков на основе карбида бора | 2018 |
|
RU2683107C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИБОРИДА ТИТАНА ДЛЯ МАТЕРИАЛА СМАЧИВАЕМОГО КАТОДА АЛЮМИНИЕВОГО ЭЛЕКТРОЛИЗЕРА | 2012 |
|
RU2498880C1 |
| СПОСОБЫ ИЗГОТОВЛЕНИЯ ПОРОШКОВ ДИБОРИДА ТИТАНА | 2010 |
|
RU2513398C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИТНОГО УГЛЕРОДСОДЕРЖАЩЕГО МАТЕРИАЛА | 2022 |
|
RU2793027C1 |
| РЕАКТОР ДЛЯ КАРБОТЕРМИЧЕСКОГО ПОЛУЧЕНИЯ ДИБОРИДА ТИТАНА | 2010 |
|
RU2572425C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО МАТЕРИАЛА НА ОСНОВЕ ДИБОРИДА ТИТАНА | 1992 |
|
RU2063391C1 |
Изобретение относится к низкотемпературному синтезу диборида титана. Способ включает приготовление реакционной смеси TiO2-В2О3-С, содержащей диоксид титана в форме анатаза, модифицированного фтор-анионом, в виде агломерированного композита, нагрев с обеспечением карботермического синтеза диборида титана и выдержку при температуре синтеза. Нагрев и выдержку реакционной смеси осуществляют сначала при температуре 940÷980°С в кислородсодержащей атмосфере в течение 30÷60 минут, а затем при 1030÷1060°С в бескислородной среде в течение 120÷180 минут. В качестве бескислородной среды может быть использован аргон или гелий. Обеспечивается получение технически чистого диборида титана с выходом конечного продукта 98-99,8%. 1 з.п. ф-лы, 2 ил., 3 пр.
1. Способ низкотемпературного синтеза диборида титана, включающий приготовление реакционной смеси TiO2-В2О3-С, содержащей диоксид титана в форме анатаза, модифицированного фтор-анионом, в виде агломерированного композита, нагрев с обеспечением карботермического синтеза диборида титана и выдержку при температуре синтеза, отличающийся тем, что нагрев и выдержку реакционной смеси осуществляют сначала при температуре 940÷980°С в кислородсодержащей атмосфере в течение 30÷60 минут, а затем при 1030÷1060°С в бескислородной среде в течение 120÷180 минут.
2. Способ по п. 1, отличающийся тем, что в качестве бескислородной среды используют аргон или гелий.
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИБОРИДА ТИТАНА | 2015 |
|
RU2603407C1 |
| Дымоочиститель | 1928 |
|
SU11640A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИБОРИДА ТИТАНА | 2013 |
|
RU2559482C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИБОРИДА ТИТАНА | 2018 |
|
RU2684381C1 |
| US 8216536 B2, 10.07.2012 | |||
| US 4503021 A1, 05.03.1985 | |||
| CN 109574029 A, 05.04.2019. | |||
Авторы
Даты
2020-06-17—Публикация
2019-09-13—Подача