Изобретение относится к медицине, а именно к медицинской генетике и оториноларингологии, в частности, предназначено для выявления мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103.
В литературе описан только один случай аутосомно-рецессивной глухоты-103 (DFNB103; OMIM#607293), в одной турецкой семье с двумя сибсами с прогрессирующей тугоухостью (от легкой до тяжелой степени тяжести) (www.ncbi.nlm.nih.gov/pubmed/24781754). В этой семье, путем картирования хромосомы 6p21.1-q15 была обнаружена нонсенс-мутация с.96Т>А (p.Cys32*) в гене CLIC5 (С32Х; 607923.0001).
Наиболее близким прототипом изобретения является способ идентификации нонсенс-мутации с.96Т>А (p.Cys32*) в гене CLIC5 описанный в исследовании Seco в соавторстве (см. Progressive hearing loss and vestibular dysfunction caused by a homozygous nonsense mutation in CLIC5 / C.Z. Seco, A.M. Oonk, M. Dominguez-Ruiz et al // Eur J Hum Genet. - 2015. - Vol. 23(2). - P. 189-194. doi: 10.1038/ejhg.2014.83).
Мутация c.96T>A (p.Cys32*) была обнаружена путем картирования в семье, где потомки от близкородственного брака (двоюродные сибсы) имели аутосомно-рецессивную потерю слуха ранее неизвестной этиологии. В результате, у двух пробандов (брат и сестра) на хромосоме 6p21.1-q15 был выявлен гомозиготный участок 47,4 Мб, содержащий 247 генов, из которых наиболее вероятным геном-кандидатам являлся ген CLIC5, мутации в котором, предположительно, являлись причиной потери слуха в данной семье. Дальнейший мутационный анализ гена CLIC5 был проведен с помощью секвенирования по Сэнгеру. Амплификация, включающая экзоны и экзон-интронные области гена CLIC5 (CLIC5A - NM_016929.4, CLIC5B NM_001114086.1), была проведена с помощью ПЦР, с использованием олигонуклеотидных праймеров, разработанных с помощью ExonPrimer (http://www.ihg.gsf.de/ihg/ExonPrimer.html). Амплификацию ПЦР проводили в присутствии стандартных ионных буферов и термостабильного фермента Taq-полимеразы. Амплифицированные фрагменты очищали от компонентов ПЦР на ПЦР-планшетах NucleoFast 96 и/или ExoI/FastAP в соответствии с протоколом изготовителя. Секвенирование проводили с помощью набора ABI PRISM BigDye Terminator Cycle Sequencing V2.0 Ready Reaction и анализировали с помощью генетического анализатора ABI PRISM 3730 (Applied Biosystems Foster City, CA, USA). На наличие трансверсии c.96T>A гена CLIC5 в контрольной выборке лиц (n=111), проводился ПДРФ-анализ с использованием эндонуклеазы рестрикции HpyCH4III, результаты которого анализировали в 1-1,5% агарозном геле, где наличие мутации с.96Т>А в гене CLIC5 приводила к потере сайта рестрикции HpyCH4III.
Известное техническое решение является результатом поискового научного исследования и не предназначено для практического применения в рутинной ДНК-диагностике аутосомно-рецессивной глухоты-103 (DFNB103). Показано, что мутация с.96Т>А (p.Cys32*) в гене CLIC5, ассоциированная с данной формой глухоты, была выявлена только в одной инбредной турецкой семье и не была обнаружена у 213 пациентов с аутосомно-рецессивной тугоухостью, преимущественно, голландского и испанского происхождения. Исходя из этого, использование способа выявления мутации с.96Т>А (p.Cys32*) в гене CLIC5 для ДНК-диагностики аутосомно-рецессивной глухоты-103 не целесообразно.
Ген CLIC5 (chloride intracellular channel 5) является одним из новых «генов глухоты», мутации в котором могут быть ассоциированы с несиндромальной аутосомно-рецессивной потерей слуха (Hereditary Hearing Loss Homepage https://hereditaryhearingloss.org/recessive-genes). CLIC5 является членом семейства белков внутриклеточного канала, которые участвуют в транспорте иона хлорида в различных субклеточных компартментах. Seco в соавторстве (см. Progressive hearing loss and vestibular dysfunction caused by a homozygous nonsense mutation in CLIC5 / C.Z. Seco, A.M. Oonk, M. Dominguez-Ruiz et al // Eur J Hum Genet. - 2015. - Vol. 23(2). - P. 189-194. doi: 10.1038/ejhg.2014.83) обнаружили, что белок CLIC5 широко экспрессируется в тканях как плода, так и взрослого человека. Было показано, что экспрессия CLIC5 во внутреннем ухе плода в 26 раз выше, чем в печени, которая имела самый низкий уровень экспрессии. На модельных животных было обнаружено, что мутированный ортологичный ген clic5 у мыши (jbg), создающий трансляционный сдвиг рамки и преждевременный стоп-кодон, приводит к тремору и прогрессирующему нарушению слуха, а также вестибулярной дисфункции. В последующем, результаты иммуногистохимии подтвердили предсказанное отсутствие белка clic5 в тканях мышей-мутантов линии jbg/jbg (гомозиготное состояние).
Ранее, молекулярно-генетические исследования причин несиндромальной нейросенсорной тугоухости у населения Якутии (n=393) были направлены на поиск мутаций в генах GJB2 (Сх26), GJB6 (Сх30) и GJB3 (Сх31), ответственных за аутосомно-рецессивную глухоту 1А типа (АРГ 1А; DFNB1A - OMIM#220290) (см. Анализ спектра и частоты GJB2-мутаций у пациентов с врожденными нарушениями слуха в Республике Саха (Якутия) / В.Г. Пшенникова, Н.А. Барашков, Ф.М. Терютин и др. // Мед. генетика. - 2015. - Т. 14. - №6 (156). - С. 10-2327; Spectrum and Frequency of the GJB2 Gene Pathogenic Variants in a Large Cohort of Patients with Hearing Impairment Living in a Subarctic Region of Russia (the Sakha Republic) / N.A. Barashkov, V.G. Pshennikova, O.L. Posukh et al // PLoS One. - 2016. - Vol. 11(5):e0156300. doi: 10.1371/journal.pone.0156300; Поиск мутаций в генах GJB6 (Сх30) и GJB3 (Сх31) у глухих пациентов с моноаллельными мутациями гена GJB2 (Сх26) в Якутии / В.Г. Пшенникова, Н.А. Барашков, А.В. Соловьев и др. // Генетика. - 2017. - Т. 53. - №3. - С. 705-715. doi: 10.7868/S0016675817030109). Показано, что основной вклад в нарушение слуха у пациентов из Якутии приходится на биаллельные мутации гена GJB2, который составил 49%. Связь изученных двух других генов GJB6 и GJB3 с наследственными нарушениями слуха в Якутии не была подтверждена. Учитывая выявленные особенности спектра и частоты мутаций гена GJB2, был разработан регионально-адаптированный подход к рутинной ДНК-диагностике АРГ 1А типа в Якутии (см. RU №2688180, кл. G01N 33/50, C12Q 1/68, опубл. 21.05.2019). Тем не менее, у 51% GJB2-негативных пациентов причина потери слуха осталась не установленной. Высоко вероятно, что потеря слуха у части GJB2-негативных пациентов может быть обусловлена мутациями в других генах, ассоциированных с несиндромальными нарушениями слуха, которых в настоящее время идентифицировано около 100 (Hereditary Hearing loss Homepage - http://hereditaryhearingloss.org).
Детальное клинико-генеалогическое изучение выборки GJB2-негативных пациентов из Якутии позволило выявить двух пораженных сибсов (родители имели нормальный слух), эвенов по этнической принадлежности, у которых причина потери слуха не была установлена. У данных сибсов отмечался поздний дебют потери слуха (у пробанда в 7 лет, у сибса в 4 года) с прогрессирующим течением со II-III до IV степени тяжести. С целью поиска причин потери слуха в этой семье у одного из сибсов был проведен полноэкзомный анализ ДНК (Illumina NextSeq 500). В результате проведенного полноэкзомного анализа в 6 экзоне гена CLIC5 была выявлена ранее неизвестная (не сведений в базах данных: 1000 Genomes Project, Exome Aggregation Consortium, OMIM, HGMD и ClinVar) гомозиготная мутация C.1121G>A (chr6: 45870937C>T), приводящая к образованию преждевременного стоп-кодона р.Trp374* (NM_001114086.1), терминирующего трансляцию белка CLIC5 (chloride intracellular channel 5 (CLIC5), transcript variant 1, mRNA). Поскольку мутация нарушает синтез полноразмерного белка CLIC5, то она может быть отнесена к вероятно патогенным вариантам. В дальнейшем, прямое секвенирование по Сэнгеру фрагмента 6-го экзона гена CLIC5 подтвердило полученные результаты. Дальнейший скрининг данной мутации среди 241 GJB2-негативного пациента (n=177 ранее исследованные, n=64 из Всероссийского общества глухих, г. Якутск), выявил мутацию c.H21G>A (р.Trp374*) гена CLIC5 еще у 36 пациентов, из них: у 26 человек в гомозиготном состоянии, а у 10 человек - в гетерозиготном. Таким образом, вклад мутации гена CLIC5 в этиологию нарушений у GJB2-негативных пациентов из Якутии составил 11% (только гомозиготы по найденной мутации), что может являться основой для разработки эффективных способов ДНК-диагностики наследственных нарушений слуха.
Задача, на решение которой направлено заявленное изобретение, является создание способа ДНК-диагностики аутосомно-рецессивной глухоты-103 (DFNB103).
Технический результат, получаемый при решении поставленной задачи, выражается в ДНК-диагностике аутосомно-рецессивной глухоты-103 (DFNB103) с высокой точностью.
Для решения поставленной задачи, был разработан способ ДНК-диагностики аутосомно-рецессивной глухоты-103 (DFNB103), включающий детекцию нонсенс-мутации c.1121G>A (р.Trp374*) гена CLIC5, отличается тем, что для проведения амплификации значимого района 6-го экзона гена CLIC5, используются следующие оригинальные праймеры: (F) - 5'-CGTCATCTCAGCCGGGATATCATAGTTGCG-3', (R) - 5'-TGCTGGTATCATGGGAACTCCA-3', с последующим проведением анализа полиморфизма длин рестрикционных фрагментов с использованием эндонуклеазы Bsc4I. При наличии фрагмента длиной 293 пн диагностируется носительство патогенного аллеля в гомозиготном состоянии (DFNB103 - подтверждается), при наличии фрагментов 293 пн и 258 пн диагностируется гетерозиготное носительство патогенного аллеля (DFNB103 - не подтверждается) и при фрагменте 258 пн диагностируется отсутствие патогенного аллеля (DFNB103 - не подтверждается).
Сопоставительный анализ признаков заявленного решения с признаками аналога свидетельствует о соответствии заявленного решения критерию «новизна».
Совокупность признаков изобретения обеспечивает решение заявленной технической задачи, а именно, получение молекулярно-генетического способа ДНК-диагностики аутосомно-рецессивной глухоты-103.
Преимуществом предлагаемого способа перед существующим аналогом является то, что он позволяет быстро и с высокой точностью подтвердить аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293), обусловленную нонсенс-мутацией c.1121G>A (р.Trp374*) гена CLIC5, который разработан на основе полученных результатов многолетних молекулярно-генетических исследований нейросенсорных нарушений слуха в Якутии.
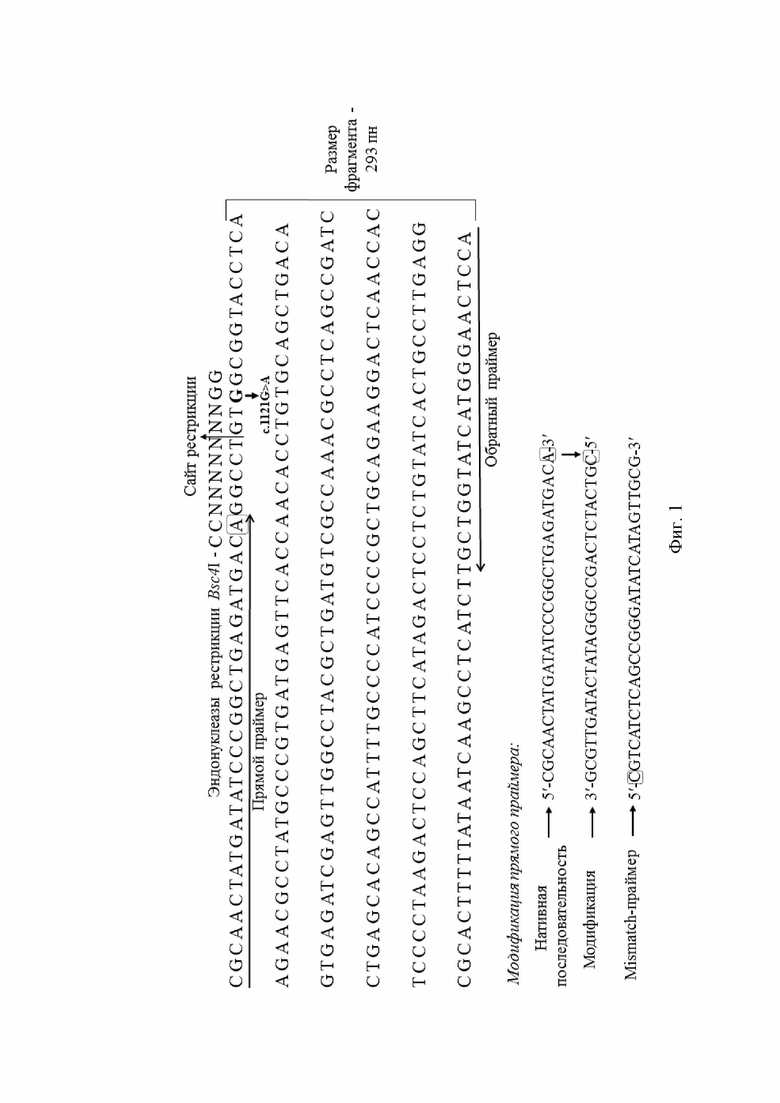
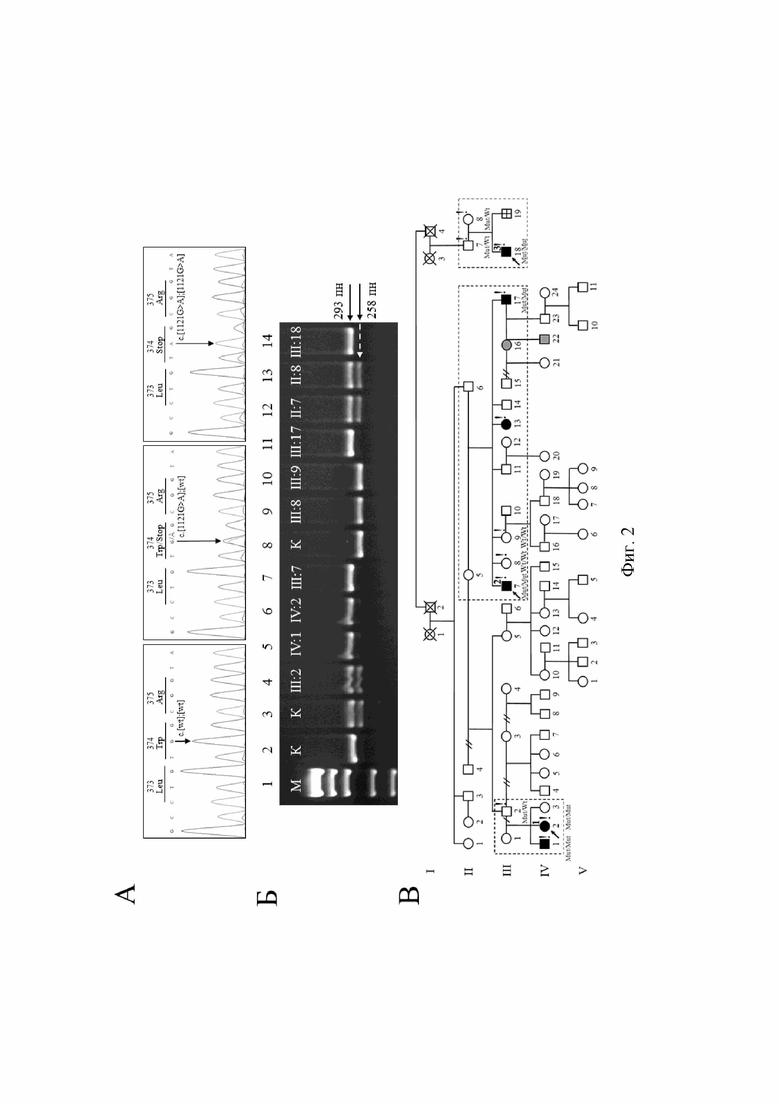
Заявляемое техническое решение иллюстрируется чертежами, где на фигуре 1, представлена область перекрывания оригинальной последовательности олигонуклеотидных праймеров для детекции нонсенс-мутации c.1121G>A (р.Trp374*) в 6-ом экзоне гена CLIC5 (размер области составляет 293 пн). Горизонтальными стрелками отмечены прямой и обратный олигодезоксинуклеотидные праймеры. Внизу показана модификация прямого праймера, где пунктирной рамкой выделен нуклеотид - аденин в 1113 положении, заменяемый на цитозин для создания искусственного палиндромного участка сайта рестрикции эндонуклеазой Bsc4I. На фигуре 2, представлена идентификация мутации c.1121G>A (р.Trp374*) в 6-ом зкзоне гена CLIC5: А - фрагменты результатов прямого секвенирования по Сэнгеру: первый фрагмент - норма (с.[wt]; [wt]), второй - моноаллельный (гетерозиготный) (с.[1121G>A]; [wt]), третий - биаллельный (гомозиготный) (с.[1121G>A]; [1121G>A]); Б - электрофореграмма ПЦР-ПДРФ анализа для детекции мутации c.1121G>A в трех ядерных семьях (4% агарозный гель). При наличии биаллельной мутации сайт рестрикции отсутствует - 293 пн; при наличии моноаллельной мутации присутствует наличие двух бэндов - 293 пн и 258 пн; при отсутствии мутации визуализируется один бэнд - 258 пн. Дорожки: 1 - маркер молекулярного веса pUC19 DNA/MspI; 2, 3 и 8 - контроль биаллельной, моноаллельной и без мутации, соответственно; 4 (III;2) - отец пробанда 1; 5 (IV;1) - сибс пробанда 1; 6 (IV;2) - пробанд 1; 7 (III;7) - пробанд 2; 9 (III;8), 10 (III;9) и 11 (III;17) - сибсы пробанда 2; 12 (III;18) - пробанд 3; 13 (II;7) - отец пробанда 3; 14 (II;8) - мать пробанда 3; В - родословная трех ядерных семей (состоящих в родстве) с выявленными генотипами по мутации c.1121G>A (р.Trp374*) гена CLIC5. Условные обозначения: черным цветом обозначены члены семьи с признаками наследственной/постлингвальной формы глухоты, серым - члены семьи с АРГ 1А (DFNB1A; OMIM#220290), плюсом - член семьи, имеющий признак наследственной/постлингвальной формы потери слуха со слов близких родственников, восклицательным знаком - обследованные лично, пунктиром выделены ядерные семьи, стрелкой и нумерацией сверху обозначены пробанды в ядерных семьях, Mut (Mutation) - c.1121G>A (p.Trp374*), Wt (Wild type) - норма.
Заявленный способ ДНК-диагностики аутосомно-рецессивной глухоты-103 осуществляется следующим образом.
1) С информированного согласия на обследование (у детей - после информированного согласия родителей или опекунов) осуществляется забор венозной крови из локтевой вены для выделения образцов геномной ДНК.
2) Геномная ДНК выделяется с помощью фенол-хлороформной экстракции, описанный в работе С. Метью (см. Mathew С.С. The isolation of high molecular weight eucariotic DNA / C.C. Mathew // Methods in Molecular Biology / Ed. Walker J.M.Y.L.: Human Press. - 1984. - Vol. 2. - P. 31-34).
3) В дальнейшем, полученную ДНК без посторонних примесей (со значениями ΔA260/ΔA280=1/8-2,0), используют в качестве матрицы для полимеразной цепной реакции для амплификации значимого района гена CLIC5. Для амплификации участка экзона 6, возможно содержащий вариант c.1121G>A (р.Trp374*), используются оригинальные последовательности олигонуклеотидов, дизайн которых представлен на фигуре 1: (F) - 5'-CGTCATCTCAGCCGGGATATCATAGTTGCG-3', (R) - 5'-TGCTGGTATCATGGGAACTCCA-3'.
Способ осуществляется с применением стандартного состава реакционной смеси: 2,0 мкл геномной ДНК, соответствующее количество каждого олигонуклеотида, 125 мкМ дезоксинуклеозидтрифосфата (Promega, USA) помещают в буфер для ПЦР следующего компонента: Буфер (х10) - 0,8 мкл (67 mM Tris-HCl, рН 8,6-8,8 при 20°С, 6,7 тМ MgCl2, 16,6 mM (NH4)2SO4, 0,01% Tween 20); Дезоксинуклеотидтрифосфаты (dNTP) - 0,5 мкл; Праймеры: F - 0.24 мкл и R - 0,142 мкл; термостабильная Taq-полимераза - 0,2 мкл; Деионизированная вода - 5,56 мкл; Бетаин - 5,56 мкл, ДНК (100 нг/мл) - 2,0 мкл. Суммарный объем - 15 мкл. При этом применяют следующий режим амплификации: 1) предварительная денатурация в течение 5 мин при t 95°С, далее 28 циклов со следующими параметрами - 95°С - 45 с, 60°С - 45 с, 72°С - 45 с. После 28-го цикла проводят инкубацию при 72°С в течение 10 мин.
4) После проведения амплификации необходимых фрагментов, для детекции мутации c.1121G>A (p.Trp374*) гена CLIC5 проводится ПДРФ-анализ с использованием эндонуклеазы Bsc4I (см. фиг. 1). Реакция проводится согласно протоколу фирмы производителя указанной эндонуклеазы. Результаты ПДРФ-анализа оцениваются методом электрофореза на горизонтальном (15×15) в 4% агарозном геле. Перед нанесением на электрофорез пробы в соотношении 1:5 с краской, содержащей 0,25% бромфенолового синего, 0,25% ксиленцианола и 15% фикола.
5) Детекцию результатов проводят путем окрашивания гелей бромистым этидием с последующей визуализацией в УФ-свете на трансиллюминаторе. На фигуре 2-Б показана электрофореграмма ПЦР-ПДРФ анализа для детекции мутации c.1121G>A (р.Trp374*) гена CLIC5, где при наличии фрагмента длиной 293 пн диагностируется носительство патогенного аллеля в гомозиготном состоянии (DFNB103 - подтверждается), при наличии фрагментов 293 пн и 258 пн диагностируется гетерозиготное носительство патогенного аллеля (DFNB103 - не подтверждается) и при фрагменте 258 пн диагностируется отсутствие патогенного аллеля (DFNB103 - не подтверждается).
Время исследования (от выделения ДНК исследуемого до детекции мутации) составляет 4 дня.
Результативность предлагаемого способа ДНК-диагностики аутосомно-рецессивной глухоты-103 была проверена на образцах ДНК 241 GJB2-негативного пациента из Якутии, обнаруженных в результате прямого секвенирования по Сэнгеру значимого района 6-го экзона гена CLIC5, содержащую мутацию c.1121G>A (р.Trp374*). В результате проведенной проверки предлагаемого способа на образцах ДНК GJB2-негативных пациентов все генотипы полностью соответствовали результатам ранее полученных с помощью прямого секвенирования по Сэнгеру гена CLIC5: мутация в гомозиготном состоянии у 26 (11%) пациентов, в геторозиготном - у 10 (4,14%), у остальных 205 (85%) мутация не была обнаружена. Таким образом, предлагаемый способ в применении оказался точным и информативным и может быть применим при рутинной ДНК-диагностике аутосомно-рецессивной глухоты-103.
Ниже приведены примеры проведенного способа ДНК-диагностики DFNB103.
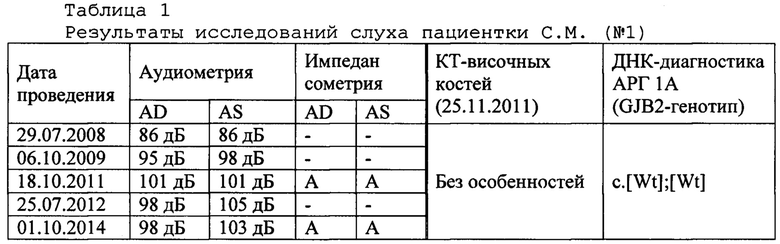
Пример 1. Пациентка С.М. (проба ДНК - АБ1037) - пробанд 1 (см. фиг. 2В - IV;2), эвенка, 1998 года рождения, с. Батагай-Алыта Эвено-Бытантайского национального улуса, Республика Саха (Якутия). Статус по слуху: двусторонняя глухота, с детства; инвалид по слуху. Наследственность по глухоте отягощена (старший брат (IV;1) с двусторонней тугоухостью, с дебютом потери слуха в 4 года). Обучалась в ГКОУ Республиканской специальной (коррекционной) общеобразовательной школе-интернате II вида для слабослышащих детей (г. Якутск). Нарушение слуха было замечено в 7 лет. Состояла на диспансерном учете (1 раз в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 - Национального центра медицины с 2008 по 2014 гг. Клинический диагноз от 02.10.2014 г. (основное заболевание / сопутствующие заболевания): двусторонняя глухота (МКБ: Н90.3) / системное недоразвитие речи. В настоящее время, пациентка носит слуховой аппарат. Результаты исследований слуха пациентки С.М. (№1) представлены в таблице 1.
Предлагаемый способ ДНК-диагностики АРГ-103 был проведен у 10 членов семьи данного пробанда 1 (см. фиг. 2). В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293) предложенным способом ДНК-диагностики DFNB103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации), мутация c.1121G>A (р.Trp374*) гена CLIC5 в гомозиготном состоянии (аллель 293 пн) была обнаружена у 5 пораженных членов семьи: у пробанда 1 (IV;2), сибса пробанда 1 (IV;1), пробанда 2 (III;7), сибса пробанда 2 (III;17) и пробанда 3 (III;18), что подтверждает диагноз - аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Гетерозиготное носительство мутантной аллели (аллели 293 пн и 258 пн) было обнаружено у отца пробанда 1 (III;2) и родителей пробанда 3 (II;7 и II;8). У здоровых сибсов пробанда 2 (III;8 и III;9) мутация не была обнаружена (аллель 258 пн). Идентификация мутации c.1121G>A (р.Trp374*) в 6-ом экзоне гена CLIC5 в случае данного примера приведена в описании фигуры 2.
Продолжительность ДНК-исследования 10 членов семьи пациентки С.М. составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
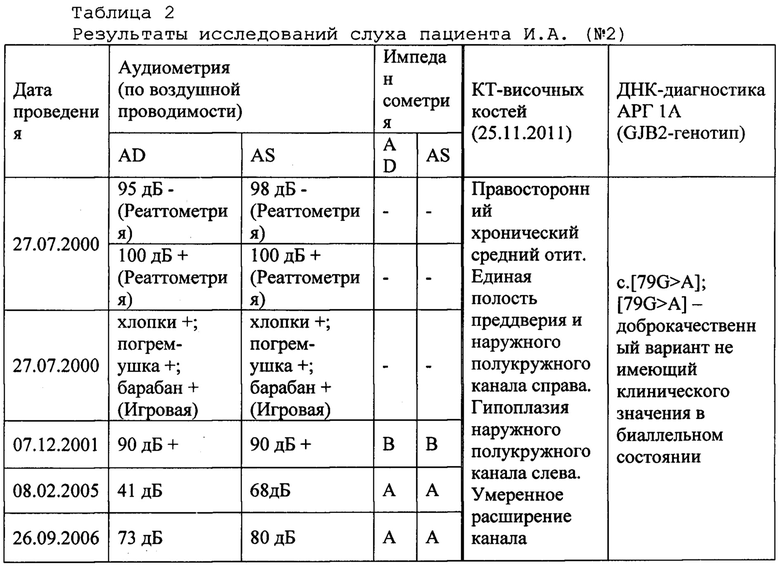
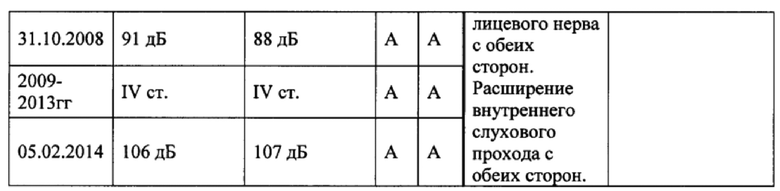
Пример 2. Пациент И.А. (проба ДНК - АБ1050), эвенк, 1995 года рождения, с. Оленек Оленекского эвенкийского национального улуса, Республика Саха (Якутия). Статус по слуху: двусторонняя глухота, с детства; инвалид по слуху. Нарушение слуха было замечено в 4 года. Наследственность по глухоте не отягощена. Обучался в ГКОУ Республиканской специальной (коррекционной) общеобразовательной школе-интернате II вида для слабослышащих детей (г. Якутск). Состоял на диспансерном учете (2 раза в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 - Национального центра медицины с 2000 по 2014 гг. Клинический диагноз от 07.10.2014 г. (основное заболевание / сопутствующие заболевания): двусторонняя глухота (МКБ: Н90.3) / резидуальная энцефалопатия, компенсированная форма. Системное недоразвитие речи. Ношение слухового аппарата / слухопротезирование с 2006 года. Результаты исследований слуха пациента И.А. (№2) представлены в таблице 2.
В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293) предложенным способом ДНК-диагностики АРГ-103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации) искомая мутация c.1121G>A (р.Trp374*), у пациента И.А. была обнаружена в гомозиготном состоянии (аллель 293 пн), что подтверждает диагноз аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Продолжительность ДНК-исследования предлагаемым способом составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
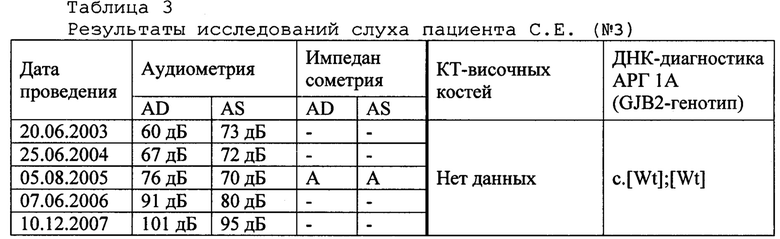
Пример 3. Пациент С.Е. (проба ДНК: АА6283), эвенк, 1993 года рождения, пгт. Тикси, Булунский улус, Республика Саха (Якутия). Статус по слуху: двусторонняя глухота, с детства; инвалид по слуху. Нарушение слуха было замечено в 7-8 лет. Наследственность по глухоте не отягощена. Обучался в массовой общеобразовательной школе (пгт. Тикси). Состоял на диспансерном учете (1 раз в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 - Национального центра медицины с 2003 по 2009 гг. Клинический диагноз от 29.06.2009 г. (основное заболевание / сопутствующие заболевания): двусторонняя сенсоневральная тугоухость III ст. справа, IV ст. слева / резидуальная энцефалопатия, церебрастенический синдром. Ношение слухового аппарата / слухопротезирование с 2006 года. Результаты исследований слуха пациента С.Е. (№3) представлены в таблице 3.
В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293) предложенным способом ДНК-диагностики DFNB103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации) искомая мутация c.1121G>A (р.Trp374*), у пациента С.Е. была обнаружена в гомозиготном состоянии (аллель 293 пн), что подтверждает диагноз аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Продолжительность ДНК-исследования предлагаемым способом составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
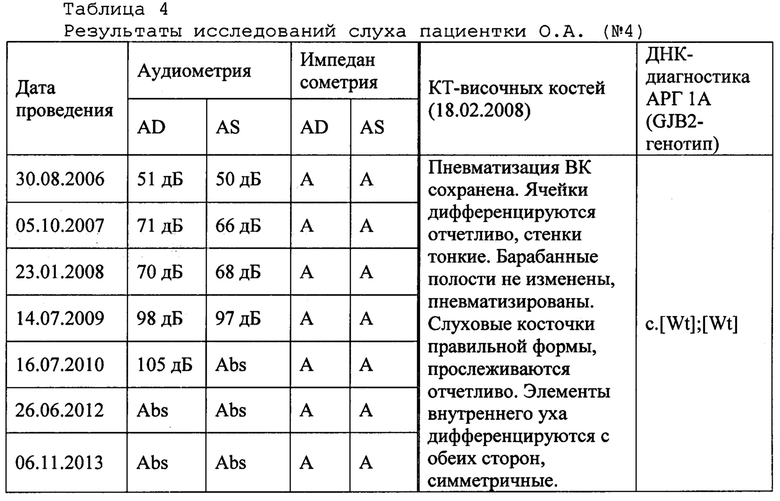
Пример 4. Пациентка О.А. (проба ДНК: АА7602), якутка, 2000 года рождения, с. Тулагино, Городской округ г. Якутск, Республика Саха (Якутия). Статус по слуху: двусторонняя глухота, с детства; инвалид по слуху. Наследственность по глухоте не отягощена. Нарушение слуха было замечено в 4 года. Обучалась в специализированной коррекционной общеобразовательной школе-интернате для слабослышащих детей (г. Москва, г. Якутск). С 13 лет обучалась в массовой общеобразовательной школе (с. Тулагино). Состояла на диспансерном учете (1 раз в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 - Национального центра медицины с 2005 по 2013 гг. Клинический диагноз от 09.09.2013 г. (основное заболевание / сопутствующие заболевания): двусторонняя глухота (МКБ: Н90.3) / резидуальная энцефалопатия с общим недоразвитием речи. 09.12.2011 г. проведена кохлеарная имплантации на оба уха (Клиническая больница №122 им. Л.Г. Соколова, г. Санкт-Петербург). Результаты исследований слуха пациентки О.А. (№4) представлены в таблице 4.
В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293) предложенным способом ДНК-диагностики DFNB103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации), искомая мутация c.1121G>A у пациентки О.А. была обнаружена в гомозиготном состоянии (аллель 293 пн), что подтверждает диагноз аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Продолжительность ДНК-исследования предлагаемым способом составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
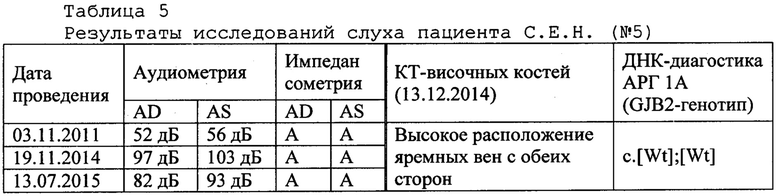
Пример 5. Пациент С.Е.Н. (проба ДНК - АБ3182), якут, 2005 года рождения, г. Нюрба, Нюрбинский улус, Республика Саха (Якутия). Статус по слуху: с детства тугоухость справа, глухота слева; инвалид по слуху. Наследственность по глухоте отягощена по отцу. Нарушение слуха было замечено в 3 года. В настоящее время обучается в ГКОУ Республиканской специальной (коррекционной) общеобразовательной школе-интернате II вида для слабослышащих детей (г. Якутск). С 2011 г. состоит на диспансерном учете (1 раз в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 - Национального центра медицины. Клинический диагноз от 22.06.2015 г. (основное заболевание / сопутствующие заболевания): сенсоневральная тугоухость IV ст.справа. Глухота слева (МКБ: Н90.3) / задержка речевого развития. Резидуальная энцефалопатия с синдромом дефицита внимания и гиперактивности. 06.07.2015 г. проведена кохлеарная имплантации на левое ухо (Клиническая больница №122 им. Л.Г. Соколова, г. Санкт-Петербург). Результаты исследований слуха пациента С.Е.Н. (№5) представлены в таблице 5.
В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103 - OMIM#616042) предложенным способом ДНК-диагностики АРГ-103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации) искомая мутация c.1121G>A (р.Trp374*), у пациента С.Е.Н. была обнаружена в гомозиготном состоянии (аллель 293 пн), что подтверждает диагноз аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Продолжительность ДНК-исследования предлагаемым способом составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
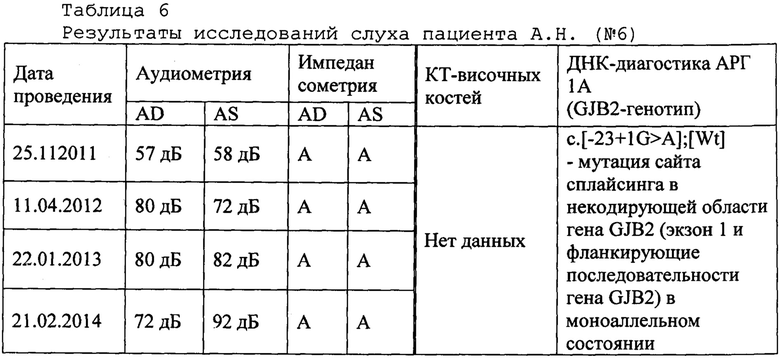
Пример 6. Пациент А.Н. (проба ДНК - АБ2181), якут, 2004 года рождения, г. Якутск, Республика Саха (Якутия). Статус по слуху: двусторонняя тугоухость с детства; инвалид по слуху. Наследственность по глухоте не отягощена. Обучается в массовой общеобразовательной школе (г. Якутск). С 2011 г. состоит на диспансерном учете (1 раз в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 - Национального центра медицины. Клинический диагноз от 21.02.2014 г. (основное заболевание / сопутствующие заболевания): двусторонняя сенсоневральная тугоухость IV ст. - Грань глухоты (МКБ: Н90.3) / резидуальная энцефалопатия. 02.10.2014 г. проведена кохлеарная имплантации на левое ухо (Клиническая больница №122 им. Л.Г. Соколова, г. Санкт-Петербург). Результаты исследований слуха пациента А.Н. (№6) представлены в таблице 6.
В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293) предложенным способом ДНК-диагностики DFNB103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации), искомая мутация c.1121G>A (р.Trp374*) у пациента А.Н. была обнаружена в гомозиготном состоянии (аллель 293 пн), что подтверждает диагноз аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Продолжительность ДНК-исследования предлагаемым способом составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
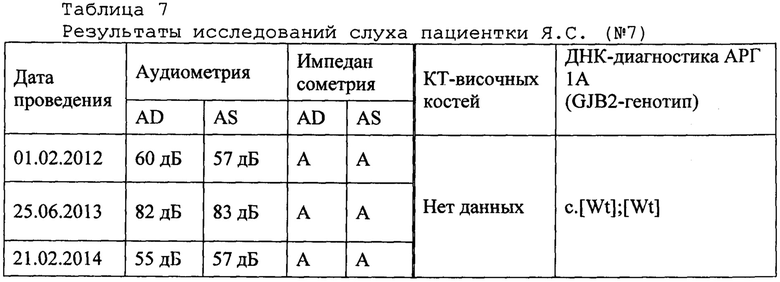
Пример 7. Пациентка Я.С. (проба ДНК - АБ3477), якутка, 2003 года рождения, г. Якутск, Республика Саха (Якутия). Статус по слуху: двусторонняя тугоухость с детства; инвалид по слуху. Наследственность по глухоте не отягощена. Обучается в массовой общеобразовательной школе (г. Якутск). С 2012 г. состоит на диспансерном учете (1 раз в год) в Сурдологопедическом центре ГАУ Республики Саха (Якутия) Республиканская больница №1 Национального центра медицины. Клинический диагноз от 27.03.2014 г. (основное заболевание / сопутствующие заболевания): двусторонняя сенсоневральная тугоухость II-IV ст. (МКБ: Н90.3) / ВСД с церебрастенией. Дизартрия. Результаты исследований слуха пациентки Я.С. (№7) представлены в таблице 7.
В результате молекулярно-генетического исследования на наличие мутации c.1121G>A (р.Trp374*) гена CLIC5, обуславливающей аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293) предложенным способом ДНК-диагностики DFNB103 (ПЦР-ПДРФ анализ с использованием оригинальной последовательности олигонуклеотидных праймеров и эндонуклеазы рестрикции Bsc4I с последующим электрофоретическим разделением продуктов гидролиза в 4%-ном агарозном геле и визуализацией с помощью системы гель-видеодокументации), искомая мутация c.1121G>А (р.Trp374*) у пациента Я.С. была обнаружена в гомозиготном состоянии (аллель 293 пн), что подтверждает диагноз аутосомно-рецессивная глухота-103 (DFNB103; OMIM#607293). Продолжительность ДНК-исследования предлагаемым способом составила 4 дня. Полученный результат верифицирован с помощью прямого секвенирования по Сэнгеру фрагмента 6-го экзона гена CLIC5. Рекомендуется: ДНК-тестирование близких родственников (супруг/супруга, родители/дети, братья/сестры и др.) и консультация врача-генетика при планировании семьи.
Таким образом, использование молекулярно-генетического способа ДНК-диагностики аутосомно-рецессивной глухоты-103 позволяет быстро и с высокой точностью подтвердить аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293), обусловленной нонсенс-мутацией C.1121G>A (р.Trp374*) гена CLIC5. Техническое решение разработано на основе результатов многолетних молекулярно-генетических исследований нейросенсорных нарушений слуха в Якутии.
--->
Перечень последовательностей
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing SYSTEM "ST26SequenceListing_V1_2.dtd" PUBLIC "-//WIPO//DTD Sequence Listing 1.2//EN">
-<ST26SequenceListing productionDate="2020-01-30" softwareVersion="1.0.0-beta1" softwareName="WIPO Sequence" fileName="Способ ДНК-диагностики АРГ-103" dtdVersion="V1_2">
-<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2019141020/20(080142)</ApplicationNumberText>
<FilingDate/>
</ApplicationIdentification>
<ApplicantName languageCode="ru">ФГБНУ "Якутский научный центр комплексных медицинских проблем", ФГАОУ ВО "Северо-Восточный федеральный универститет имени М.К.Аммосова" </ApplicantName>
<ApplicantNameLatin>FBSO "Yakut Science Centre of complex medical problems", FSAIHE "M.K. Ammosov North-Eastern Federal University" </ApplicantNameLatin>
<InventorName languageCode="ru">Барашков Н.А.</InventorName>
<InventorNameLatin>Barashkov N.A.</InventorNameLatin>
<InventionTitle languageCode="ru">Способ ДНК-диагностики аутсомно-рецессивной глухоты-103</InventionTitle>
<SequenceTotalQuantity>2</SequenceTotalQuantity>
-<SequenceData sequenceIDNumber="1">
-<INSDSeq>
<INSDSeq_length>30</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
-<INSDSeq_feature-table>
-<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..30</INSDFeature_location>
-<INSDFeature_quals>
-<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>genomic DNA</INSDQualifier_value>
</INSDQualifier>
-<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cgtcatctcagccgggatatcatagttgcg</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
-<SequenceData sequenceIDNumber="2">
-<INSDSeq>
<INSDSeq_length>22</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
-<INSDSeq_feature-table>
-<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..22</INSDFeature_location>
-<INSDFeature_quals>
-<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>genomic DNA</INSDQualifier_value>
</INSDQualifier>
-<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>tgctggtatcatgggaactcca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListin
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выявления мутаций гена GJB2, обуславливающих аутосомно-рецессивную глухоту 1А типа | 2017 |
|
RU2688180C1 |
| СПОСОБ ДЕТЕКЦИИ 17 МУТАЦИЙ ГЕНОВ GJB2 И GJB6 ПРИ НАСЛЕДСТВЕННОЙ НЕСИНДРОМАЛЬНОЙ ГЛУХОТЕ | 2010 |
|
RU2448163C2 |
| Способ ДНК-диагностики врожденной формы катаракты (CTRCT18) | 2017 |
|
RU2648464C1 |
| Способ одновременной диагностики наследственных заболеваний | 2015 |
|
RU2627115C2 |
| СПОСОБ ВЫЯВЛЕНИЯ МУТАЦИЙ В ГЕНЕ GJB2, СОПРОВОЖДАЮЩИХСЯ РАЗВИТИЕМ НЕСИНДРОМАЛЬНОЙ АУТОСОМНО-РЕЦЕССИВНОЙ ГЛУХОТЫ | 2006 |
|
RU2317547C1 |
| Способ диагностики мутации c.-23+1G>A (rs80338940) гена GJB2 | 2020 |
|
RU2746055C1 |
| Способ диагностики мутации 167delT (rs80338942) гена GJB2 | 2020 |
|
RU2739943C1 |
| Способ диагностики мутации 35delG (rs80338939) гена GJB2 | 2020 |
|
RU2739889C1 |
| СПОСОБ ДИАГНОСТИКИ 3-М СИНДРОМА В ЯКУТСКОЙ ПОПУЛЯЦИИ | 2006 |
|
RU2315310C1 |
| СПОСОБ ВЫЯВЛЕНИЯ МУТАЦИИ с.-53-2А>G В ГЕНЕ ПРЕСТИНА (SLC26A5), ВЫЗЫВАЮЩЕЙ РАЗВИТИЕ НЕСИНДРОМАЛЬНОЙ АУТОСОМНО-РЕЦЕССИВНОЙ ГЛУХОТЫ | 2012 |
|
RU2505608C1 |
Изобретение относится к области биотехнологии. Изобретение предназначено для выявления мутации c.1121G>А (p.Trp374*) гена СLIC5, обуславливающей аутосомно-рецессивную глухоту-103. Способ ДНК-диагностики аутосомно-рецессивной глухоты-103 (DFNB103), включающий детекцию нонсенс-мутации c.1121G>A(p.Trp374*) гена CLIC5, для чего, выделяют геномную ДНК, проводят ПЦР-ПДРФ-анализ с использованием следующих оригинальных праймеров: (F) - 5'-CGCAACTATGATATCCCGGCTGAGATGACA-3', (R) - 5'-ТGCTGGTATCATGGGAACTCCA-3' и эндонуклеазой рестрикции Bsc4I. В результате наличия на электрофореграмме фрагмента длиной 293 пн диагностируют носительство патогенного аллеля в гомозиготном состоянии, что соответствует результатам положительной ДНК-диагностике на DFNB103. Предлагаемый способ разработан на основе полученных результатов многолетних молекулярно-генетических исследований нейросенсорных нарушений слуха в Якутии и позволяет быстро и с высокой точностью подтвердить аутосомно-рецессивную глухоту-103 (DFNB103; OMIM#607293), обусловленную нонсенс-мутацией c.1121G>A (p.Trp374*) гена CLIC5. 2 ил., 7 табл., 7 пр.
Способ ДНК-диагностики аутосомно-рецессивной глухоты-103 (DFNB103), включающий детекцию нонсенс-мутации c.1121G>A (p.Trp374*) гена CLIC5, отличающийся тем, что для проведения амплификации значимого района 6-го экзона гена CLIC5 используют следующие оригинальные праймеры: (F) - 5'-CGTCATCTCAGCCGGGATATCATAGTTGCG-3', (R) - 5'-ТGCTGGTATCATGGGAACTCCA-3', с последующим проведением анализа полиморфизма длин рестрикционных фрагментов с использованием эндонуклеазы Bsc4I, и при наличии фрагмента длиной 293 пн диагностируют носительство патогенного аллеля в гомозиготном состоянии, при котором DFNB103 подтверждается, при наличии фрагментов 293 пн и 258 пн диагностируют гетерозиготное носительство патогенного аллеля, при котором DFNB103 не подтверждается, при наличии фрагмента 258 пн диагностируют отсутствие патогенного аллеля, при котором DFNB103 не подтверждается.
Авторы
Даты
2020-07-22—Публикация
2019-12-12—Подача